Lampiran 2. Bagan kerja penelitian
Herba kurmak mbelin disortir dicuci
ditiriskan lalu ditimbang dikeringkan Simplisia pemeriksaan makroskopik dihaluskan Serbuk simplisia Skrining Fitokimia: - Alkaloida - Flavonoida - Saponin - Tanin - Glikosida - Antrakuinon - Steroida/triterpenoi Karakterisasi:
- Pemeriksaan makroskopik - Penetapan kadar:
- air
- sari yang larut dalam etanol
- sari yang larut dalam air - abu total
- abu yang tidak larut dalam asam Pembuatan ekstrak ekstraksi dengan etanol Esktrak etanol
dipartisi dengan n-heksana
Ekstrak n-heksana penentuan fase gerak secara KLT diisolasi secara kromatografi kolom dan preparatif dan hasilnya dipantau dengan KLT
Isolat
dilakukan uji kemurnian dengan KLT 2 arah
Isolat murni
Lampiran 3. Bagan pembuatan ekstrak n-heksana herba kurmak mbelin
direndam selama 3 jam
dimasukkan ke dalam alat perkolator
dituangkan cairan penyari etanol secukupnya sampai semua simplisia terendam
mulut perkolator ditutup dengan alumunium foil
perkolator didiamkan selama 24 jam keran perkolator dibuka dan perkolat diatur menetes dengan kecepatan 20 tetes/menit sampai pada saat beberapa tetes perkolat tidak bereaksi ketika ditambahkan pereaksi Liebermann-Burchard
diuapkan dengan rotary evaporator pada suhu 50o C
ditambahkan 40 ml etanol ditambahkan 100 ml air panas, dihomogenkan
dimasukkan ke dalam corong pisah dipartisi dengan 100 ml n-heksana sebanyak 3 kali
400 g serbuk simplisia
Ampas Perkolat
Ekstrak etanol
Lampiran 4. Gambar makroskopik dari tumbuhan kurmak mbelin (Enydra fluctuans Lour.)
Gambar tumbuhan kurmak mbelin
Lampiran 4. (Lanjutan)
Gambar simplisia herba kurmak mbelin
Lampiran 5. Gambar mikroskopik dari tumbuhan segar dan serbuk simplisia herba kurmak mbelin (Enydra fluctuans Lour.)
Penampang melintang daun segar kurmak mbelin (perbesaran 10 x 40) Keterangan:
1. Kutikula
2. Rambut penutup 3. Epidermis atas 4. Jaringan pagar 5. Rongga udara 6. Stomata
7. Jaringan bunga karang 8. Floem
9. Xilem
10. Epidermis bawah
1 2 3 4 5
6 7 8
Lampiran 5. (lanjutan)
Penampang melintang batang tumbuhan segar kurmak mbelin (perbesaran 10 x 40)
Keterangan: 1. Epidermis 2. Rongga udara 3. Floem
4. Korteks 5. Xilem 6. Parenkim 7. Kambium
1
2
3
4
5
Lampiran 5. (lanjutan)
Mikroskopik serbuk simplisia herba kurmak mbelin (perbesaran 10 x 40) Keterangan:
1. Fragmen mesofil
2. Stomata tipe anomositik 3. Jaringan pagar
4. Rambut penutup
5. Xilem dengan penebalan spiral
1
2
4 3
Lampiran 6. Perhitungan hasil penetapan kadar a. Perhitungan hasil penetapan kadar air
Kadar air = volume air (ml)
berat sampel (g)
x 100%
1. Sampel 1
Berat sampel = 5,078 g Volume air = 0,3 ml
Kadar air = 0,3
5,078 x100%
= 5,9 % v�b 2. Sampel 2
Berat sampel = 5,103 g Volume air = 0,3 ml
Kadar air = 0,3
5,103
x
100%= 5,8 % v�b 3. Sampel 3
Berat sampel = 5,121 g Volume air = 0,2 ml
Kadar air = 0,2
5,121 x100%
= 3,9 % v�b
Kadar air rata – rata = 5,9%
+ 5,8% + 3,9%
3
Lampiran 6. (lanjutan)
b. Perhitungan hasil penetapan kadar sari yang larut dalam air
Kadar sari yang larut dalam air = berat sari
berat simplisia
x
100
20
x
100% 1. Kadar sari yang larut dalam air IBerat cawan = 45,184 g
Berat cawan + berat sari = 45,382 g
Berat sampel = 5,078 g
Berat sari = 0,198 g
Kadar sari yang larut dalam air = 0,198
5,078
x
10020
x
100% = 19,49 %2. Kadar sari yang larut dalam air II
Berat cawan = 44,200 g
Berat cawan + berat sari = 44,403 g
Berat sampel = 5,074 g
Berat sari = 0,203 g
Kadar sari yang larut dalam air = 0,203
5,074
x
10020
x
100% = 20,01 %3. Kadar sari larut dalam air III
Berat cawan = 44,214 g
Berat cawan + berat sari = 44,441 g
Berat sampel = 5,070 g
Berat sari = 0,227 g
Kadar sari yang larut dalam air = 0,227
5,070
x
100Lampiran 6. (lanjutan)
Kadar sari yang larut dalam air rata – rata = 19,49%+20,01%+22,38%
3
= 20,63 %
c. Perhitungan hasil penetapan kadar sari yang larut dalam etanol
1. Kadar sari yang larut dalam etanol I
Berat Cawan = 46,792 g
Berat Cawan + Berat Sari = 46,977 g
Berat Sampel = 5,051 g
Berat sari = 0,185 g Kadar sari yang larut dalam etanol = 0,185
5,051
x
10020
x
100%= 18,31% 2. Kadar sari yang larut dalam etanol II
Berat Cawan = 45,113g
Berat Cawan + Berat Sari = 45,287g
Berat Sampel = 5,046 g
Berat sari = 0,174 g Kadar sari yang larut dalam etanol = 0.174
5,046
x
100
20
x
100%= 17,24% 3. Kadar sari yang larut dalam etanol III
Berat Cawan = 45,284g
Berat Cawan + Berat Sari = 45,447g
Berat Sampel = 5,040 g
Berat sari = 0.163 g Kadar sari yang larut dalam etanol
=
berat sariberat simplisia
x
10020
Lampiran 6. (lanjutan)
Kadar sari yang larut dalam etanol = 0,163
5,040
x
100
20
x
100% = 16,17%Kadar sari yang larut dalam etanol rata-rata = 18,31%+17,24%+16,17%
3
= 17,24 % d. Perhitungan hasil penetapan kadar abu total
1. Sampel I
Berat simplisia = 2,028 g
Berat abu = 0,311g
Kadar abu total = 0,311
2,028
x
100% = 15,33 % 2. Sampel IIBerat simplisia = 2,022 g
Berat abu = 0,268g
Kadar abu total = 0,268
2,022
x
100%= 13,25% 3.Sampel III
Berat simplisia = 2,020 g
Berat abu = 0,288g
Kadar abu total
=
0,2882,020
x
100% = 14,26 % Kadar abu total=
berat abuLampiran 6. (lanjutan)
Kadar abu total rata-rata = 15,33%+13,25%+14,26%
3
= 14,28%
e. Perhitungan Hasil Penetapan Kadar Abu Tidak Larut Dalam Asam
1. Sampel I
Berat simplisia = 2,028 g
Berat abu = 0,013g
Kadar abu tidak larut asam = 0,013
2,028
x
100% = 0,64% 2. Sampel IIBerat simplisia = 2,022 g
Berat abu = 0,009g
Kadar abu tidak larut asam = 0,009
2,022
x
100%= 0,44% 3.Sampel III
Berat simplisia = 2,020 g
Berat abu = 0,011g
Kadar abu tidak larut asam = 0,011
2,020
x
100% = 0,54%Kadar abu tidak larut asam rata-rata = 0,64%+0.44%+0,54%
3
= 0,54%
Kadar abu tidak larut dalam asam
=
berat abudicuci dengan metanol dingin
spektrofotometri UV dan IR Lampiran 7. Bagan kromatografi kolom
Eluat (68 vial) Fraksi n-heksana
dikromatografi kolom:
fase gerak: n-heksana:etilasetat (landaian) fase diam: silika gel 60 H
dikromatografi lapis tipis:
fase gerak: n-heksana:etilasetat (70:30) fase diam: silika gel F254
dikerok
diuapkan
KLT 2 arah Isolat
(Rf = 0,57)
Tiga noda Noda 1 (biru hijau) Noda 2 (kuning) Noda 3 (hijau)
Residu Filtrat
Isolat
Spektrum Isolat murni
(satu noda) Fraksi 1
(1 - 17)
Fraksi 2 (18 - 21)
Fraksi 3 (22 - 26)
Fraksi 4 (27 - 34)
Fraksi 5 (35 - 57)
Fraksi 6 (58 - 61)
Fraksi 7 (62 - 64)
Lampiran 8. Kromatogram dan harga Rf dari fraksi n-heksana herba kurmak belin
100:0 90:10 80:20 70:30 60:40 50:50
Keterangan: fase diam: silika gel F254, fase gerak: n-heksana-etilasetat,
penampak bercak: Liebermann-Burchard, tp:titik penotolan, bp:batas pengembangan.
bp
Lampiran 8. (lanjutan)
No. Perbandingan fase gerak Rf Warna noda
1. 100:0 0,01
0,11 0,21
hijau biru merah ungu
2. 90:10 0,08
0,24 0,53
hijau biru merah ungu
3. 80:20 0,19
0,38 0,44 0,89 hijau biru merah ungu merah ungu
4. 70:30 0,50
0,59 0,69 0,83 0,99 hijau hijau biru merah ungu merah ungu
5. 60:30 0,55
0,65 0,99
hijau biru merah ungu
6. 50:50 0,75
0,83 0,99
Lampiran 9. Kromatogram KLT hasil kromatografi kolom dari ekstrak n-heksana herba kurmak mbelin
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17
Lampiran 9. (lanjutan)
35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51
Lampiran 9. (lanjutan)
No. Eluat Rf Warna noda
1. Fraksi 1 (vial 1 - 17) 0,90 merah pucat
2. Fraksi 2 (vial 18 - 21) 0,80 hijau
3. Fraksi 3 (vial 22 - 26) 0,69 0,80
merah muda hijau 4. Fraksi 4 (vial 27 - 34) 0,56
0,69 0,80
biru merah muda
hijau 5. Fraksi 5 (vial 35 - 57) 0,41
0,53 0,78
biru hijau
biru 6. Fraksi 6 (vial 58 - 61) 0,28
0,41 0,53 0,78 biru muda biru hijau biru 7. Fraksi 7 (vial 62 - 64) 0,28
0,41 0,53
biru muda biru hijau 8. Fraksi 8 (vial 65 - 68) 0,28
0,41
Lampiran 10. Kromatogram hasil KLT preparatif dari F4
Keterangan: F4 (vial 27 - 34), fase diam: silika gel F254, fase gerak: n-heksana
: etilasetat (70 : 30), penampak bercak: Liebermann-Burchard, tp:titik penotolan, bp:batas pengembangan.
bp
Lampiran 11. Kromatogram hasil KLT dua arah dari isolat murni
Keterangan: Fase diam: silika gel F254, penampak bercak: Liebermann–Burchard,
tp:titik pentotolan, A1:arah pengembangan pertama, A2:arah pengembangan kedua.
Harga Rf KLT dua arah isolat
No. Fase Gerak Harga Rf
1. n-heksana-etilasetat (70:30) 0,57
2. Toluen-etilasetat (90:10) 0,30
A1
Lampiran 13. Spektrum IR isolat murni dari herba kurmak mbelin
DAFTAR PUSTAKA
Ali, M, R., Mustahsan, B., Syed, M,M., dan Al, E. (2013). Enydra fluctuans Lour: A Review. Research J.Pharm and Tech. 6(9): 927-929.
Anonim. (2010). Enydra fluctuans Loureiro. [Diakses Juni 2014], Diambil dari: http://www.globinmed.com/enydra-fluctuans-loureiro.html.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Padang: Andalas University Press. Halaman 3-5, 21.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Direktorat Jenderal Pengawas Obat dan Makanan. Halaman 299-305, 321-327, 333-337.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman 1-11.
Farnsworth, N.R. (1966). Biological and Phytochemical Screening of Plant. Journal of Pharmaceutical Sciences. 55(3): 262-263.
Gandjar, I.G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 323, 353-361.
Gandjar, I.G., dan Rohman, A. (2012). Analisis Obat Secara Spektrofotometri dan Kromatografi. Yogyakarta: Pustaka Pelajar. Halaman 156-157, 333.
Gritter, R.J., Bobbit, J., dan Schwarting, A.E. (1991). Pengantar Kromatografi. Penerjemah: Kokasih Padmawinata. Edisi 2. Bandung: ITB. Halaman 107-146.
Grover, V.K., Ramesh, B., dan Bedi, S. (2007). Steroid Therapy – Current Indications in Practice. Indian Journal of Anaesthesia. 51(5): 389-393. Handa, S., Suman, P.S.K., Gennaro, L., Dev, D.R.. (2008). Extraction
Technologies For Medicinal And Aromatic Plants. Italy: International Centre For Science and High Technology. Halaman 22.
Harborne, J.B. (1987). Metode Fitokimia. Penuntun Cara Modern Menganalisis Tumbuhan. Penerjemah: Kokasih Padmawinata, dan Iwang Sooediro. Edisi 2. Bandung: ITB. Halaman 102-103, 147-149, 234.
Hostettmann, K., dan Marston. (1995). Saponins. New York: Cambridge University Press. Halaman 2.
Kumar, S., Patro, V.J., Dinda, S., dan Nayak, D.P. (2012). Hepatoprotective Activity of Enydra fluctuans Lour. Parts Against CCl4 Induced
Hepatotoxicity in Rats. International Journal of Research in Ayurveda & Pharmacy. 3(6): 893.
Kuri, S., Mustahsan, B., Masud, R., dan Zannatul, N. (2014). Phytochemical and In Vitro Biological Investigations of Methanolic Extracts of Enhydra fluctuans Lour. Asian Pasific Journal of Tropical Biomedicine. 4(4): 299-305.
Lenny, S. (2006). Senyawa Terpenoid dan Steroid. Skripsi. Medan: Fakultas MIPA Universitas Sumatera Utara.
Lestari, P. (2010). Karakterisasi Simplisia dan Isolasi Senyawa Triterpenoida/Steroida dari Herba Suruhan (Peperomiae pellucidae herba). Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara.
Nigam, A. dan Archana, A. (2008). Lab Manual in Biochemistry, Immunology and Biotechnology. New Delhi: McGraw-Hill. Halaman 166.
Nurhidayah., Minarti., Anugrah, P., Imran. (2013). Uji Aktivitas Senyawa Turunan Terpenoid, Steroid dan Fenolik dari Ekstrak Jaringan Kayu Batang Tumbuhan Ndokulo (Kleinhovia hospita L.) terhadap Pertumbuhan Sel Kanker (Leukimia P-388). Kendari: Fakultas MIPA Universitas Halu Oleo. Halaman 1.
Pasaribu, E.M. (2011). Isolasi Senyawa Flavonoida dari Kulit Batang Tumbuhan Mangga (Mangivera indica L). Skripsi. Medan: Fakultas MIPA Universitas Sumatera Utara.
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Penerjemah: Kokasih Padmawinata. Bandung: ITB. Halaman 123-157, 191.
Rohman, A. (2009). Kromatografi Untuk Analisis Obat. Yogyakarta: Graha Ilmu. Halaman 51.
Saleh, C. (2008). Isolasi dan Penentuan Struktur Senyawa Steroid dari Akar Tumbuhan Cendana (Santalum album Linn). Disertasi. Medan: Fakultas MIPA Universitas Sumatera Utara.
Sastrohamidjojo, H. (1985). Kromatografi. Yogyakarta: Liberty. Halaman 1-28, 160-162.
Stahl, E. (1985). Analisis Obat Secara Kromatografi dan Mikroskopik. Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Bandung: ITB. Hal. 3-18.
Uddin, S.B. (2013). Bangladesh Ethnobotany Online Database. [Diakses Juni 2014], Diambil dari: http://www.ebbd.info/enhydra-fluctuans.html.
BAB III
METODE PENELITIAN
Metode yang digunakan adalah metode eksploratif meliputi pengumpulan bahan tumbuhan, identifikasi tumbuhan, pembuatan simplisia, pemeriksaan karakterisasi simplisia, skrining fitokimia simplisia, pembuatan ekstrak etanol, fraksinasi ekstrak etanol, kromatografi lapis tipis (KLT), kromatografi kolom, KLT preparatif, KLT dua arah dan karakterisasi isolat secara spektrofotometri UV dan spektrofotometri IR. Penelitian dilakukan di Laboratorium Farmakognosi dan Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara.
3.1 Alat-alat yang Digunakan
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas laboratorium, blender (Panasonic), eksikator, mikroskop (Olympus), seperangkat alat destilasi, seperangkat alat penetapan kadar air, seperangkat alat kromatografi kolom, oven listrik (Stork), hair dryer (Maspion), neraca analitik (Vibra AJ), neraca kasar (Saherand), penangas air (Yenaco), seperangkat alat kromatografi lapis tipis, lemari pengering, spektrofotometer UV (Shimadzu) dan spektrofometer IR (IR - Prestige 21).
3.2 Bahan-bahan yang Digunakan
pekat, kalium bromida, plat pra lapis silika gel F254, silika gel 60 H, metanol,
n-heksana hasil destilasi dan air suling.
3.3 Pembuatan Pereaksi 3.3.1 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida P dilarutkan dalam air secukupnya, lalu ditambahkan 2 g iodium P kemudian ditambahkan air hingga 100 ml (Depkes, 1995).
3.3.2 Pereaksi Mayer
Larutan raksa (II) klorida P 2,266% b/v sebanyak 60 ml dicampur dengan 10 ml larutan kalium iodida P 50% b/v, kemudian ditambahkan air secukupnya hingga 100 ml (Depkes, 1995).
3.3.3 Larutan asam sulfat 2 N
Larutan asam sulfat pekat sebanyak 9,8 ml diencerkan dengan air suling sampai volume 100 ml (Depkes, 1995).
3.3.4 Larutan asam nitrat 0,5 N
Sebanyak 3,4 ml asam nitrat pekat diencerkan dengan air suling hingga volume 100 ml (Depkes, 1995).
3.3.5 Pereaksi Dragendorff
3.3.6 Pereaksi Molish
Sebanyak 3 g α-naftol P, dilarutkan dalam asam nitrat 0,5 N hingga
diperoleh larutan 100 ml (Depkes, 1995). 3.3.7 Larutan asam klorida 2 N
Larutan asam klorida pekat sebanyak 17 ml ditambahkan air suling sampai 100 ml (Depkes, 1995).
3.3.8 Larutan timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat P dilarutkan dalam air bebas karbon dioksida hingga 100 ml (Depkes, 1995).
3.3.9 Larutan besi (III) klorida 1% b/v
Sebanyak 1 g besi (II) klorida dilarutkan dalam air secukupnya hingga 100 ml (Depkes, 1995).
3.3.10 Larutan pereaksi kloralhidrat
Sebanyak 70 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 30 ml air suling (Depkes, 1995).
3.3.11 Larutan pereaksi Liebermann-Burchard
Asam sulfat pekat sebanyak 5 ml dicampurkan dalam 50 ml etanol 96%, lalu ditambahkan 5 ml asam asetat anhidrida ke dalam campuran tersebut.
3.3.12 Larutan pereaksi Floroglusin
3.4 Pengumpulan dan Pengolahan Tumbuhan 3.4.1 Pengumpulan bahan tumbuhan
Pengambilan bahan dilakukan secara purposif yaitu bahan tumbuhan diambil dari satu tempat saja tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Sampel yang digunakan adalah herba kurmak mbelin (Enydra fluctuans Lour.) yang diperoleh dari Desa Singa, Kabanjahe, Kabupaten Karo,
Provinsi Sumatera Utara. 3.4.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi - LIPI Bogor.
3.4.3 Pengolahan tumbuhan
Pengolahan herba kurmak mbelin dilakukan terhadap tumbuhan segar, yaitu herba dibersihkan dari kotoran - kotoran, dicuci dengan air sampai bersih, ditiriskan, ditimbang (5 kg ), lalu dikeringkan di lemari pengering pada suhu 40 -50 oC sampai menjadi simplisia, dihaluskan dan ditimbang (430 g).
3.5 Pemeriksaan Mikroskopik Herba Kurmak Mbelin Segar
Pemeriksaan mikroskopik dilakukan terhadap penampang melintang dari daun dan batang kurmak mbelin yang segar untuk melihat anatomi dari daun dan batang.
Caranya:
floroglusin diteteskan di atas objek, dan ditutup kembali dengan kaca penutup, diamati di bawah mikroskop.
3.6 Pemeriksaan Karakteristik Simplisia Herba Kurmak Mbelin 3.6.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, ukuran, warna, karakteristik permukaan dan tekstur dari simplisia.
3.6.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia herba kurmak mbelin.
Caranya:
Sedikit serbuk simplisia ditaburkan di atas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan ditutup dengan kaca penutup, kemudian diamati di bawah mikroskop.
3.6.3 Penetapan kadar air
Penetapan kadar air dilakukan menurut metode Azeotropi (destilasi toluena). Alat terdiri dari labu alas bulat 500 ml, pendingin, tabung penyambung, tabung penerima 5 ml berskala 0,05 ml, alat penampung dan pemanas listrik. Cara kerja:
kecepatan tetesan diatur 2 tetes untuk tiap detik sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Saat semua air terdestilasi, setelah itu dibilas bagian dalam pendingin dengan toluen. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada suhu kamar, setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 2011).
3.6.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk yang telah dikeringkan di udara, dimaserasi selama 24 jam dalam 100 ml air - kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18 jam, kemudian disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan di udara (Depkes, 1995).
3.6.5 Penetapan kadar sari larut dalam etanol
sari yang larut dalam etanol 95% dihitung terhadap bahan yang telah dikeringkan di udara (Depkes, 1995).
3.6.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan - lahan sampai arang habis, pemijaran dilakukan pada suhu 600oC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan di udara (Depkes, 1995).
3.6.7 Penetapan kadar abu tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring, dipijarkan sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang dikeringkan di udara (Depkes, 1995).
3.7 Skrining Fitokimia
Skrining fitokimia serbuk simplisia herba kurmak mbelin meliputi: pemeriksaan senyawa alkaloid, glikosida, saponin, flavonoid, antrakinon, tannin dan steroid/triterpenoid.
3.7.1 Pemeriksaan alkaloid
Diambil 3 tabung reaksi, lalu ke dalam masing-masing tabung reaksi dimasukkan 0,5 ml filtrat. Pada tabung :
a. Ditambahkan 2 tetes pereaksi Bouchardat b. Ditambahkan 2 tetes pereaksi Dragendorff c. Ditambahkan 2 tetes pereaksi Mayer
Alkaloid disebut positif jika terjadi endapan atau kekeruhan pada paling sedikit 2 tabung reaksi dari percobaan diatas (Depkes, 1995).
3.7.2 Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g kemudian disari dengan 30 ml campuran 7 bagian volume etanol 96% dan 3 bagian volum air suling ditambah dengan 10 ml asam klorida 2 N. Direfluks selama 30 menit, didinginkan dan disaring. Diambil 20 ml filtrat ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, lalu dikocok selama 5 menit dan disaring. Filtrat disari dengan 20 ml campuran 3 bagian kloroform dan 2 isopropanol dilakukan berulang sebanyak tiga kali. Kumpulan sari air diuapkan pada temperatur tidak lebih dari 500C. Sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut, yaitu 0,1 ml larutan percobaan dimasukkan ke dalam tabung reaksi, diuapkan di penangas air. Sisa dilarutkan dalam 2 ml air suling dan 5 tetes pereaksi Molish. Secara perlahan ditambahkan 2 ml asam sulfat pekat. Glikosida positif jika terbentuk cincin berwarna ungu (Depkes, 1995).
3.7.3 Pemeriksaaan saponin
1-10 cm. Ditambahkan 1 tetes larutan asam klorida 2 N, bila buih tidak hilang menunjukkan adanya saponin (Depkes, 1995).
3.7.4 Pemeriksaan flavonoid
Sebanyak 10 g serbuk simplisia kemudian ditambahkan 100 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, filtrat yang diperoleh kemudian diambil 5 ml lalu di tambahkan 0,1 g serbuk Mg dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok, dan dibiarkan memisah. Flavonoid positif jika terjadi warna merah, kuning, jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.7.5 Pemeriksaan glikosida antrakinon
Sebanyak 0,2 g serbuk simplisia ditambahkan 5 ml asam sulfat 2 N, dididihkan 5 menit, dinginkan. Tambahkan 10 ml benzena, kocok, diamkan. Pisahkan lapisan benzen, saring; filtrat berwarna kuning, menunjukkan adanya antrakinon. Lapisan benzena dikocok dengan 1 - 2 ml natrium hidroksida 2 N, diamkan; lapisan air berwarna merah dan lapisan benzena tidak berwarna menunjukkan adanya glikosida antrakinon (Depkes, 1995).
3.7.6 Pemeriksaan tanin
Sebanyak 0,5 g sampel disari dengan 10 ml air suling, disaring lalu filtratnya diencerkan dengan air suling sampai tidak berwarna. 2 ml larutan ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida. Terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.7.7 Pemeriksaan steroid/triterpenoid
asam asetat anhidrida dan 1 tetes asam sulfat pekat. Timbul warna biru atau hijau menunjukkan adanya steroid jika timbul warna merah, pink atau ungu menunjukkan adanya triterpenoid (Farnsworth, 1966).
3.8 Pembuatan Ekstrak
Pembuatan ekstrak dilakukan secara perkolasi menggunakan pelarut etanol. Cara kerja :
Sebanyak 400 g serbuk simplisia herba kurmak mbelin dibasahi dengan penyari dan dibiarkan selama 3 jam, kemudian dimasukkan ke dalam alat perkolator. Lalu larutan penyari etanol dituang secukupnya sampai semua simplisia terendam dan terdapat selapis cairan penyari di atasnya, mulut tabung perkolator ditutup dengan alumunium foil dan dibiarkan selama 24 jam, kemudian kran dibuka dan perkolat dibiarkan menetes dengan kecepatan 20 tetes/menit. Perkolasi dihentikan pada saat beberapa tetes perkolat tidak bereaksi ketika ditambahkan pereaksi Liebermann - Burchard. Pelarut yang digunakan yaitu sebanyak 11 liter. Perkolat yang diperoleh kemudian dipekatkan dengan alat penguap vakum putar pada temperatur yang tidak lebih dari 50oC sampai diperoleh ekstrak kental.
3.9 Fraksinasi Ekstrak Etanol
Cara kerja:
Ekstrak etanol ditambahkan 40 ml etanol, lalu dilarutkan dengan air panas sebanyak 100 ml, lalu dimasukkan ke dalam corong pisah, difraksinasi/partisi dengan n - heksana sebanyak 100 ml, dilakukan 3 kali, sehingga diperoleh fraksi n-heksana dan fraksi air. Fraksi n-heksana dipekatkan (Rohman, 2009).
3.10 Kromatografi Lapis Tipis dari Ekstrak n–Heksana Herba Kurmak Mbelin
Kromatografi lapis tipis (KLT) digunakan untuk mendapatkan fase gerak yang terbaik untuk dipakai pada KLT hasil kromatografi kolom. Terhadap fraksi n - heksana dilakukan analisis secara KLT menggunakan fase diam silika gel F254 dan fase gerak campuran n-heksana : etilasetat dengan perbandingan
(100 : 0), (90 : 10), (80 : 20), (70 : 30), dan (60 : 40), sebagai penampak bercak digunakan pereaksi Liebermann-Burchard.
Cara kerja:
Ekstrak dilarutkan dalam n-heksana, ditotolkan pada plat lapis tipis, kemudian dimasukan ke dalam chamber yang telah jenuh dengan uap fase gerak. Pengembangan selesai, lalu plat dikeluarkan dan dikeringkan, plat disemprot dengan penampak bercak Liebermann-Burchard dan dipanaskan di oven pada suhu 110℃ selama 10 menit. Amati warna yang terbentuk dan dihitung harga Rf pada semua bercak. Fase gerak yang menghasilkan noda (bercak) paling banyak adalah fase gerak yang terbaik (Stahl, 1985).
dengan perbandingan (100 : 0), (90 : 10), (80 : 20), (70 : 30), (60 : 40), (50 : 50), (40 : 60), (30 : 70), (20 : 80), (10 : 90), (0 : 100) dan metanol.
Cara kerja:
Seperangkat alat kromatografi kolom dipasang sedemikian rupa dan pada dasar kolom dimasukkan kapas bebas lemak, kemudian dimasukkan fase gerak. Silika gel 60 H dibuat bubur dengan larutan fase gerak sampai bebas gelembung udara, kran dibuka kemudian bubur silika dimasukkan ke dalam kromatografi kolom secara perlahan-lahan sambil dinding kolom diketuk-ketuk dan fase gerak tetap dialiri sampai silika gel turun, lalu didiamkan sampai kolom kompak, selanjutnya fase gerak diturunkan sampai setinggi lebih kurang 1 cm di atas fase diam, kran ditutup. Bagian atas silika gel dilapisi dengan kertas saring kemudian ekstrak n-heksana yang sebelumnya telah dicampur dengan silika gel 60 H dimasukkan ke dalam bejana kromatografi kolom sambil fase gerak ditambah sedikit demi sedikit, setelah sampel turun kran dibuka perlahan sambil fase gerak terus ditambah. Eluat yang keluar ditampung dalam vial, masing-masing sebanyak 5 ml. Hal ini dilakukan sampai eluat memberikan hasil negatif terhadap pereaksi Liebermann-Burchard. Hasil elusi dipantau dengan kromatografi lapis tipis menggunakan fase gerak n-heksana : etilasetat (70 : 30), penampang bercak Liebermann-Burchard. Untuk eluat yang mempunyai pola kromatogram yang sama digabung menjadi satu fraksi (Sastrohamidjojo, 1985).
3.12 Isolasi Senyawa Steroid/Triterpenoid Hasil Kromatografi Kolom dengan KLT Preparatif
pereaksi LiebermanBurchard dan sebagai fase gerak digunakan n-heksana:etilasetat (70 : 30) dan fase diam silika gel F254.
Cara kerja:
Fraksi ditotolkan berupa pita pada jarak 2 cm dari tepi bawah plat KLT berukuran 20 x 20 cm yang telah diaktifkan, setelah kering plat KLT dimasukkan ke dalam bejana yang telah jenuh dengan uap fase gerak, pengembang dibiarkan naik membawa komponen yang ada, setelah mencapai batas pengembangan plat dikeluarkan dari bejana lalu dikeringkan. Bagian tengah plat ditutup dengan kaca yang bersih sedangkan pada sisi kanan dan kiri plat disemprot dengan penampak bercak Liebermann-Burchard. Bagian tengah plat yang sejajar dengan bercak berwarna biru-hijau dikerok dan dikumpulkan, direndam dengan metanol satu malam lalu disaring kemudian pelarutnya diuapkan, kemudian dilakukan uji kemurnian dengan KLT terhadap isolat yang diperoleh (Hostettmann, 1995).
3.13 Uji Kemurnian Terhadap Kristal Hasil Isolasi
Terhadap isolat hasil isolasi dilakukan KLT 2 arah menggunakan fase gerak n-heksana : etilasetat (70 : 30) dan toluen:etilasetat (90 : 10).
Cara kerja:
Isolat ditotolkan pada plat pra lapis silika gel F254 ukuran 20 x 20 lalu
dikembangkan memakai fase gerak I yaitu n-heksana : etilasetat (70 : 30) hingga mencapai batas pengembangan, kemudian plat dikeluarkan dari dalam bejana dan dikeringkan, setelah plat kering dikembangkan kembali dengan arah yang berbeda 90o
pada suhu 110℃ selama 10 menit lalu ditandai bercak yang terbentuk (Gandjar dan Rohman, 2012).
3.14 Karakterisasi Isolat
3.14.1 Karakterisasi isolat secara spektrofotometri UV Cara kerja:
Isolat dilarutkan dalam pelarut metanol, kemudian dimasukkan ke dalam kuvet yang telah dibilas dengan larutan sampel, selanjutnya absorbansi larutan sampel diukur pada panjang gelombang 200 - 400 nm (Dachriyanus, 2004). 3.14.2 Karakterisasi isolat secara spektrofotometri IR
Cara kerja:
Karakterisasi isolat secara spektrofotometri IR dilakukan dengan cara mencampurkan 1 mg isolat dengan 150 mg kalium bromida menggunakan alat mixture vibrator, kemudian dicetak menjadi pelet pada tekanan 11,5 ton dan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi-LIPI Bogor menunjukkan bahwa tumbuhan yang diteliti termasuk suku Asteraceae spesies Enydra fluctuans Lour. Hasil identifikasi tumbuhan dapat dilihat pada Lampiran 1, halaman 45.
4.2 Hasil Karakterisasi Bahan Tumbuhan dan Serbuk Simplisia
Hasil pemeriksaan makroskopik dari simplisia menunjukkan simplisia berupa daun kering menggulung tidak beraturan dan keriput, memiliki warna hijau tua dengan bau aromatik, ukuran panjang 4 - 6 cm dan lebar 1 - 1,5 cm; batang menyusut dan keriput berwarna hijau kecoklatan. Hasil pengamatan makroskopik dapat dilihat pada Lampiran 4, halaman 48.
Hasil pemeriksaan mikroskopik serbuk simplisia terdapat stomata dengan tipe anomositik, rambut penutup, fragmen mesofil, jaringan pagar dan xilem dengan penebalan dinding berbentuk spiral. Hasil pengamatan mikroskopik serbuk simplisia dapat dilihat pada Lampiran 5, halaman 52.
[image:42.595.117.513.263.384.2]Hasil pemeriksaan karakterisasi simplisia herba kurmak mbelin dapat dilihat pada Tabel 4.1 di bawah ini.
Tabel 4.1. Hasil karakterisasi simplisia dari herba kurmak mbelin
No Karakterisasi Simplisia Hasil
(%)
1 Kadar air 5,20
2 Kadar sari yang larut dalam air 20,63
3 Kadar sari yang larut dalam etanol 17,24
4 Kadar abu total 14,28
5 Kadar abu yang tidak larut dalam asam 0,54
Hasil skrining fitokimia terhadap herba kurmak mbelin dapat diketahui bahwa herba kurmak mbelin mengandung senyawa-senyawa kimia seperti yang terlihat pada Tabel 4.2 di bawah ini.
Tabel 4.2. Hasil skrining fitokimia dari simplisia herba kurmak mbelin
No Nama Senyawa Hasil
1. Alkaloid -
2. Flavonoid +
3. Steroid/Triterpenoid +
4. Tanin +
5. Glikosida +
6. Saponin +
Keterangan : (+) positif : mengandung golongan senyawa (-) negatif : tidak mengandung golongan senyawa
[image:42.595.115.511.490.623.2]kecoklatan, dengan pereaksi Bouchardat tidak memberikan endapan warna kuning kecoklatan dan dengan pereaksi Mayer tidak terbentuk endapan putih dan kekeruhan, ini menunjukkan tidak adanya alkaloid. Alkaloid dianggap positif jika terjadi endapan pada paling sedikit dua atau tiga dari pereaksi yang ditambahkan (Depkes, 1995).
Flavonoid dengan penambahan serbuk Mg, HCl 2 N dan amil alkohol memberikan warna jingga pada lapisan amil alkohol. Ini dianggap bahwa flavonoid positif pada herba kurmak mbelin (Farnsworth, 1966). Penambahan Liebermann-Burchard memberikan warna hijau menunjukkan adanya senyawa triterpen/steroid (Harborne, 1987). Skrining pada tanin dengan penambahan FeCl3
memberikan warna biru kehitaman yang menunjukan adanya tanin (Farnsworth, 1966).
Hasil skrining glikosida positif yaitu ditunjukkan dengan penambahan pereaksi Molish dan asam sulfat pekat dimana terbentuk cincin ungu. Pereaksi Molish merupakan pereaksi umum yang digunakan untuk identifikasi karbohidrat, dalam hal ini adalah gula (Depkes, 1995). Skrining saponin positif karena menghasilkan busa yang stabil dengan tinggi busa 3 cm dan tidak hilang dengan penambahan HCl 2 N (Depkes, 1995).
4.3 Hasil Isolasi Senyawa Steroid/Triterpenoid
Ekstraksi dilakukan dengan cara perkolasi menggunakan pelarut etanol, dari hasil perkolasi 400 g serbuk simplisia diperoleh ekstrak kental
(70 : 30) karena menghasilkan pemisahan noda steroid/ triterpenoid yang paling baik. Hasil analisis KLT ekstrak n-heksana dapat dilihat pada Lampiran 8, halaman 59.
Selanjutnya terhadap ekstrak n-heksana dilakukan isolasi secara kromatografi kolom dengan pelarut landaian n-heksana : etilasetat dengan perbandingan 100 : 0, 90 : 10, 80 : 20, 70 : 30, 60 : 40, 50 : 50, 40 : 60, 30 : 70, 20 : 80, 10 : 90, 0 : 100 dan methanol, diperoleh eluat sebanyak 68 vial. Masing-masing eluat dikromatografi lapis tipis dengan fase gerak n-heksana-etilasetat (70:30) dengan penampak bercak Lieberman-Burchard. Eluat yang mempunyai pola kromatogram yang sama di gabung menjadi satu fraksi yaitu F1 (vial 1 - 17), F2 (vial 18 - 21), F3 (vial 22 - 26), F4 (vial 27 - 34), F5 (vial 35 - 57), F6 (vial 58 - 61), F7 (vial 62 - 64) dan F8 (vial 65 - 68). Kristal terbanyak dan noda berwarna biru hijau pada kromatogram terdapat pada Fraksi 4 (vial 27 - 34. Hasil kromatografi kolom dapat dilihat pada Lampiran 9, halaman 61.
Salah satu F4 diisolasi secara kromatografi lapis tipis preparatif dengan fase gerak n-heksana : etilasetat (70 : 30). Hasil kromatografi lapis tipis preparatif untuk F4 terdapat 3 noda yaitu noda biru hijau, kuning dan hijau. Noda berwarna biru hijau dikerok dan dicuci dengan metanol dingin. Hasil KLT preparatif dapat dilihat pada Lampiran 10, halaman 64.
Berdasarkan data di atas, diduga isolat merupakan steroid, hal ini diperkuat dengan timbulnya noda berwarna biru dengan pereaksi Liebermann Burchard yang menunjukkan adanya steroid (Nigam, 2008).
Isolat secara spektrofotometri ultraviolet (UV) dan spektrofotometri inframerah (IR). Hasil pengukuran secara spektrofotometri UV memberikan panjang gelombang absorpsi maksimum sebesar 212, 2 nm, hal ini menunjukkan adanya gugus kromofor (Dachriyanus, 2004). Hasil karakterisasi isolat secara Spektrofotometri UV dapat dilihat pada Lampiran 12, halaman 66.
Hasil spektrofotometri inframerah (IR) menunjukkan pada bilangan gelombang 3433,29 cm-1 terdapat gugus -OH alkohol, namun masih perlu dilakukan identifikasi untuk mengetahui apakah gugus -OH ini berasal dari isolat atau berasal dari pelarut, karena pelarut yang digunakan adalah metanol. Gugus -OH tersebut dikuatkan oleh serapan C-O pada bilangan gelombang 1056,99 cm-1, pada bilangan gelombang 2939,52 cm-1 menunjukkan adanya gugus CH alifatis, yang diperkuat oleh puncak pada bilangan gelombang 1450,47 cm-1 menunjukkan adanya gugus metilen (CH2) dan puncak pada bilangan gelombang 1365,6 cm-1
menunjukkan adanya gugus metil (CH3). Pada bilangan gelombang 1643,35 cm-1
menunjukkan adanya gugus C=C (Dachriyanus, 2004). Hasil karakterisasi isolat secara Spektrofotometri IR dapat dilihat pada Lampiran 13, halaman 67.
Tabel 4.3 Hasil Analisis Spektrum Inframerah
No. Bilangan gelombang (cm-1) Gugus fungsi
1 1056,99 C-O
2 1365,6 -CH3
3 1450,47 -CH2
4 1643,35 C=C
5 2939,52 C-H alifatis
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
a. Hasil karakterisasi simplisia herba kurmak mbelin (Enydra fluctuans Lour.) diperoleh kadar air 5,20%, kadar sari yang larut dalam air 20,63%, kadar sari yang larut dalam etanol 17,24%, kadar abu total 14,28% dan kadar abu yang tidak larut asam 0,54%.
b. Golongan senyawa kimia simplisia herba kurmak mbelin (Enydra fluctuans Lour.) adalah flavonoid, steroid/triterpenoid, tanin, saponin dan
glikosida.
c. Isolat diperoleh dan dikarakterisasi secara spektrofotometri UV memberikan panjang gelombang absorbsi maksimum 212,2 nm. Hasil pengukuran spektrum dengan spektrofotometri inframerah menunjukkan adanya gugus C-O, -CH3, -CH2, C=C, C-H alifatis dan -OH.
5.2Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi habitat, nama daerah, nama asing, morfologi tumbuhan, sistematika tumbuhan, kandungan kimia dan kegunaan dari tumbuhan. 2.1.1 Daerah Tumbuh
Kurmak mbelin adalah tumbuhan yang berasal dari wilayah Indo-China, yang tumbuh di daerah tropis di Asia dan Afrika. Tumbuhan ini umum ditemukan di Asia Tenggara dan beberapa negara di Asia Selatan (Kuri, et al., 2014).
Tumbuhan kurmak mbelin terdapat pada daerah yang beriklim subtropis dan tropis. Tumbuhan ini tumbuh di dataran tinggi dengan ketinggian 1800 m dari permukaan laut. Tumbuhan ini biasanya terdapat di selokan atau aliran sungai kecil, tepi kolam ikan, rawa dan sawah (Anonim, 2010).
2.1.2Nama Daerah
Nama daerah kurmak mbelin menurut Anonim (2010) adalah sebagai berikut:
Sumatera : Ambur
Jawa Barat : Kokoha, Godobos 2.1.3 Nama Asing
Nama asing kurmak mbelin menurut Ali, et., al (2013) dan Uddin (2013) adalah sebagai berikut:
Bangladesh : Helencha, Harhack, Hinchashak Filipina : Kangkong kelabaw
Indonesia : Kokoha, Godobos, Ambur Kamboja : Kanting ring
Inggris : Buffalo spinach, Water cress, Marsh herb Malaysia : Chengkeru, Kangkong kerbau
Thailand : Phakbum-ruang, Phakpaeng 2.1.4 Sistematika Tumbuhan
Sistematika tumbuhan kurmak mbelin menurut Ali, et al., (2013) adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledoneae Ordo : Asterales Famili : Asteraceae Genus : Enydra
Spesies : Enydra fluctuans Lour. 2.1.5Morfologi Tumbuhan
2.1.6 Kandungan kimia
Tumbuhan kurmak mbelin kaya akan protein dan merupakan penghasil β -carotene yang baik (3,7 - 4,2 mg/100 g berat tumbuhan segar). Tumbuhan ini
mengandung saponin, tanin, steroid, glikosida, kaurol, giberelin A9 dan A13, seskiterpen laktonnya yaitu germakranolida, enhydrin, fluctuanin dan fluctuandin (Ali, et al., 2013).
2.1.7 Kegunaan
Semua bagian kurmak mbelin yang berwarna hijau terutama pucuk muda, digunakan sebagai sayur di Asia Tenggara, baik mentah maupun direbus. Di Kolkata, daun tumbuhan ini dibuat menjadi jus dan digunakan sebagai tonik yang diberikan pada penderita neuralgia dan penyakit saraf lainnya. Di Filipina, daunnya ditumbuk dan digunakan untuk mengobati kulit yang melepuh pada penderita penyakit herpes. Daunnya sedikit pahit, digunakan sebagai antiinflamasi, pencahar, pengobatan penyakit kulit dan cacar. Berdasarkan hasil penelitian, telah dilaporkan bahwa tumbuhan ini memiliki aktivitas antioksidan, antimikroba, antihelmintik dan hipotensif (Ali, et al., 2013; Kumar, et al., 2012).
2.2 Uraian Kandungan Kimia Tumbuhan 2.2.1 Alkaloida
Contoh:
Gambar 2.1 Koniina 2.2.2 Flavonoida
Golongan flavonoid dapat digambarkan sebagai deretan senyawa C6-C3
-C6. Yang berarti, kerangka karbonnya terdiri atas dua gugus C6 (cincin benzena
tersubstitusi) disambungkan oleh rantai alifatik tiga karbon (Robinson, 1995). Flavonoid mencakup banyak pigmen yang paling umum dan terdapat pada seluruh dunia tumbuhan mulai dari fungi sampai angiospermae. Beberapa fungsi flavonoid untuk tumbuhan ialah sebagai pengatur tumbuh, pengatur fotosintesis, antimikroba dan antivirus (Robinson, 1995).
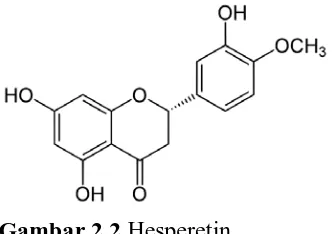
Contoh:
Gambar 2.2 Hesperetin 2.2.3 Saponin
[image:50.595.114.281.473.590.2]sangat encer saponin sangat beracun untuk ikan, dan tumbuhan yang mengandung saponin telah digunakan sebagai racun ikan selama beratus-ratus tahun. Beberapa saponin bekerja sebagai antimikroba (Robinson, 1995).
Molekul saponin terdiri dari dua bagian yaitu, aglikon dan glikon. Bagian aglikon atau non-sakarida dari molekul molekul saponin disebut genin atau sapogenin. Berdasarkan aglikonnya, Hostettman dan Marston (1995) membagi saponin menjadi 3 kelas utama yaitu:
1. Glikosida triterpenoid 2. Glikosida steroid
3. Glikosida steroid alkaloid Contoh:
[image:51.595.111.286.289.473.2]
Gambar 2.3 Diosgenin 2.2.4 Tanin
Tanin terdapat luas dalam tumbuhan berpembuluh, dalam angiospermae terdapat khusus dalam jaringan kayu. Pada kenyataanya, sebagian besar tumbuhan yang banyak tanin dihindari oleh hewan pemakan tumbuhan karena rasanya yang sepat (Harborne, 1987).
Contoh:
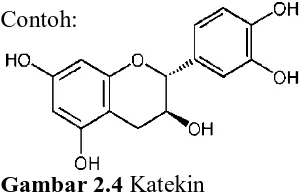
[image:51.595.113.264.634.731.2]2.2.5 Glikosida
Glikosida adalah suatu golongan senyawa bila dihidrolisis akan terurai menjadi gula (glikon) dan senyawa lain (aglikon atau genin). Umumnya glikosida mudah terhidrolisis oleh asam mineral atau enzim. Hidrolisis oleh asam memerlukan panas, sedangkan hidrolisis oleh enzim tidak memerlukan panas (Sirait, 2007).
Berdasarkan ikatan antara glikon dan aglikon, glikosida dapat dibedakan menjadi (Sirait, 2007):
a. Tipe O-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan O.
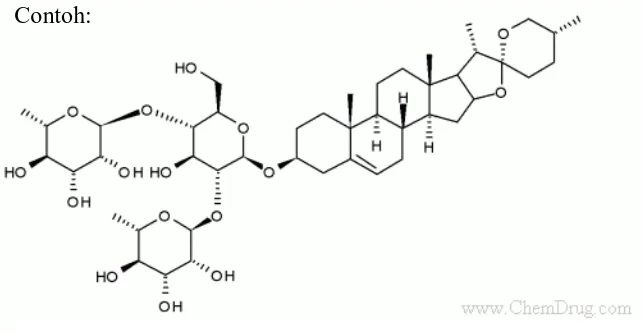
Contoh:
Gambar 2.5 Dioscin
b. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan S.
Contoh:
[image:52.595.124.445.360.527.2]
c. Tipe N-glikosida, ikatan antara bagian dari glikon dengan aglikon melalui jembatan N.
Contoh:
Gambar 2.7 Nikleosidin
d. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan C.
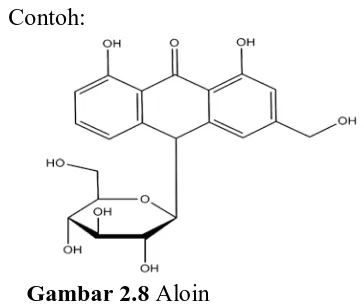
[image:53.595.127.309.359.511.2]Contoh:
Gambar 2.8 Aloin 2.2.6 Glikosida antrakuinon
Golongan kuinon alam terbesar terdiri dari antrakuinon. Beberapa antrakuinon merupakan zat warna penting dan yang lainnya sebagai pencahar. Keluarga tumbuhan yang kaya akan senyawa jenis ini ialah Rubiaceae, Rhamnaceae, Polygonaceae (Robinson, 1995). Contoh: Aloin.
2.2.7 Steroid/triterpenoid
dari hidrokarbon C30 asiklik, yaitu skualena. Triterpenoid berupa senyawa tanpa warna, berbentuk kristal, sering kali bertitik leleh tinggi dan aktif optik. Uji yang banyak digunakan ialah reaksi Liebermann-Burchard yang dengan kebanyakan triterpena dan sterol memberikan warna hijau-biru (Harborne, 1987).
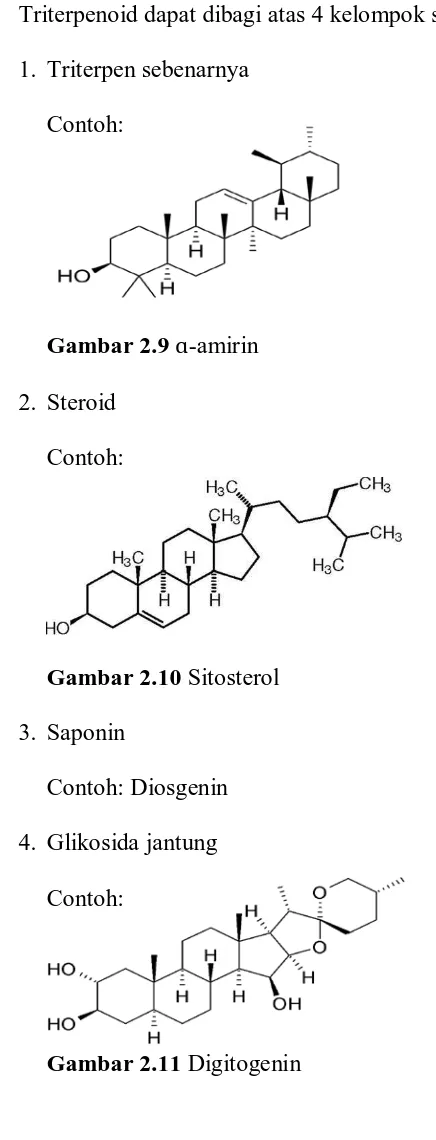
Triterpenoid dapat dibagi atas 4 kelompok senyawa yaitu: 1. Triterpen sebenarnya
[image:54.595.104.322.195.765.2]Contoh:
Gambar 2.9 ɑ-amirin 2. Steroid
Contoh:
Gambar 2.10 Sitosterol 3. Saponin
Contoh: Diosgenin 4. Glikosida jantung
Contoh:
Senyawa triterpenoid merupakan komponen aktif dalam tumbuhan obat yang telah digunakan untuk penyakit termasuk diabetes, gangguan menstruasi, patukan ular, gangguan kulit, kerusakan hati, dan malaria (Harborne, 1987; Robinson, 1995).
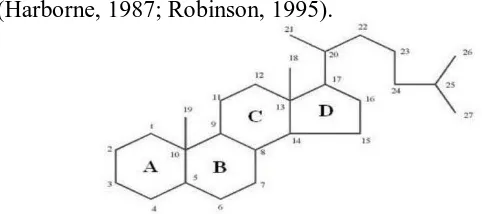
[image:55.595.115.356.308.415.2]Sterol adalah triterpen yang kerangka dasarnya sistem cincin siklopentana perhidrofenantren. Dahulu steroid dianggap sebagai senyawa satwa (digunakan sebagai hormon kelamin, asam empedu) tetapi pada tahun-tahun terakhir ini makin banyak senyawa steroid yang ditemukan dalam jaringan tumbuhan (Harborne, 1987; Robinson, 1995).
Gambar 2.12 Struktur dasar steroida dan sistem penomorannya Menurut asalnya senyawa steroid dibagi atas:
a. Zoosterol, yaitu steroid yang berasal dari hewan. Contoh:
Gambar 2.13 Kolesterol
b. Fitosterol, yaitu steroid yang berasal dari tumbuhan. Contoh:
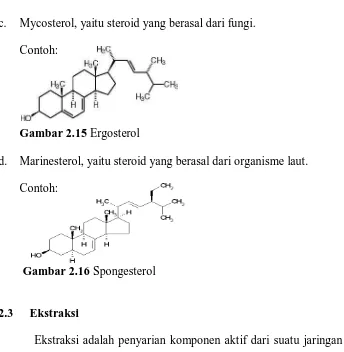
c. Mycosterol, yaitu steroid yang berasal dari fungi. Contoh:
Gambar 2.15 Ergosterol
d. Marinesterol, yaitu steroid yang berasal dari organisme laut. Contoh:
Gambar 2.16 Spongesterol
2.3 Ekstraksi
Ekstraksi adalah penyarian komponen aktif dari suatu jaringan tumbuhan atau hewan dengan menggunakan pelarut yang cocok (Handa, 2008).
Beberapa metode ekstraksi dengan menggunakan pelarut yaitu: A. Cara dingin
1. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur kamar. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus – menerus). Remaserasi berarti dilakukan penyaringan maserat pertama, dan seterusnya (Depkes, 2000).
2. Perkolasi
Proses perkolasi terdiri dari tahap pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1 - 5 kali bahan (Depkes, 2000).
B. Cara panas 1. Refluks
Refluks adalah ekstraksi dengan menggunakan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40 - 50oC.
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut yang relatif konstan dengan adanya pendingin balik.
4. Infundasi
5. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama (≥30 menit) dan temperatur sampai titik didih air (Depkes, 2000).
2.4 Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan perpindahan dari komponen-komponen senyawa di antara dua fase yaitu fase diam (dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau zat cair). Jika fase diam berupa zat padat maka cara tersebut dikenal sebagai kromatografi serapan, jika zat cair dikenal sebagai kromatografi partisi (Depkes, 1995; Sastrohamidjojo, 1985).
Pemisahan dan pemurnian kandungan kimia tumbuhan terutama dilakukan dengan menggunakan salah satu dari lima teknik kromatografi atau gabungan teknik tersebut. Kelima teknik kromatografi itu adalah: kromatografi kolom (KK), kromatografi kertas (KKt), kromatografi lapis tipis (KLT), kromatografi gas cair (KGC), dan kromatografi cair kinerja tinggi (KCKT). Pemilihan teknik kromatografi sebagian bergantung pada sifat kelarutan dan keatsirian senyawa yang akan dipisah (Harborne, 1987).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis merupakan metode pemisahan campuran analit dengan mengelusi analit melalui suatu lempeng kromatografi lalu melihat komponen/analit yang terpisah dengan penyemprotan atau pewarnaan (Gandjar dan Abdul, 2012).
Campuran yang akan dipisah, berupa larutan ditotolkan berupa bercak ataupun pita, setelah plat atau lapisan dimasukkan ke dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak), pemisahan terjadi selama pengembangan, selanjutnya senyawa yang tidak berwarna harus ditampakkan (Stahl, 1985).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa cara. Untuk senyawa tak berwarna cara yang paling sederhana adalah dilakukan pengamatan dengan sinar ultraviolet. Beberapa senyawa organik bersinar atau berfluorosensi jika disinari dengan sinar ultraviolet gelombang pendek (254 nm) atau gelombang panjang (366 nm), jika dengan cara itu senyawa tidak dapat dideteksi maka harus disemprot dengan pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu dengan pemanasan (Gritter, et al., 1991; Stahl, 1985).
a. Fase diam (lapisan penyerap)
Fase diam berupa lapisan tipis yang terdiri atas bahan padat yang dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca, plastik atau logam. Lapisan fase diam melekat pada permukaan dengan bantuan bahan pengikat, biasanya kalsium sulfat atau amilum (Gritter, et al., 1991).
b. Fase gerak (pelarut pengembang)
Fase gerak ialah medium angkut yang terdiri atas satu atau campuran beberapa pelarut, jika diperlukan sistem pelarut multi komponen, harus berupa suatu campuran sesederhana mungkin yang terdiri atas maksimum tiga komponen (Stahl, 1985).
Pemisahan pada KLT dikendalikan oleh rasio distribusi komponen dalam sistem fase diam/penyerap dan fase gerak tertentu. Profil pemisahan pada KLT dapat dimodifikasi dengan mengubah rasio distribusi dengan mengubah komposisi fase gerak dengan memperhatikan polaritas (Gandjar dan Abdul, 2012). c. Harga Rf
Mengidentifikasi noda-noda dalam kromatogram KLT sangat lazim menggunakan harga Rf (Retardation Factor) yang didefinisikan sebagai:
Rf= Jarak titik pusat bercak dari titik awal Jarak garis depan pelarut dari titik awal
Faktor-faktor yang mempengaruhi harga Rf: a. struktur kimia dari senyawa yang sedang dipisahkan, b. Sifat penyerap, c. tebal dan kerataan lapisan penyerap, d. pelarut dan derajat kemurniannya, e. derajat kejenuhan uap pengembang dalam bejana, f. teknik percobaan, g. jumlah cuplikan yang digunakan, h. Suhu dan i. kesetimbangan (Sastrohamidjojo, 1985).
2.4.2 Kromatografi kolom
Kromatografi kolom biasanya dikembangkan dengan campuran pelarut yang terus-menerus berubah dengan cara landaian. Eluat yang keluar dari dasar kolom harus dipantau untuk mengetahui dimana linarut itu berada. Ini dapat dilakukan secara terus-menerus dengan memakai detektor yang cocok atau dengan membagi eluat menjadi sejumlah cuplikan yang berurutan dan menganalisisnya dengan KLT (Gritter, et al., 1991).
2.4.3 Kromatografi lapis tipis preparatif
Kromatografi lapis tipis (KLT) preparatif merupakan salah satu metode pemisahan yang memerlukan pembiayaan paling murah dan menggunakan peralatan sederhana. Ketebalan penyerap yang sering dipakai adalah 0,5 - 2 mm, ukuran plat kromatografi biasanya 20 x 20 cm. Pembatasan ketebalan lapisan dan ukuran plat sudah tentu mengurangi jumlah bahan yang dapat dipisahkan dengan KLT preparatif. Penyerap yang paling umum digunakan adalah silika gel (Hostettmann, et al., 1995).
Penotolan cuplikan dilakukan dengan melarutkan cuplikan dalam sedikit pelarut. Cuplikan ditotolkan berupa pita dengan lebar pita sesempit mungkin karena pemisahan tergantung pada lebar pita. Penotolan dapat dilakukan dengan pipet tetapi lebih baik dengan penotol otomatis. Pengembangan plat KLT preparatif dilakukan dalam bejana kaca yang dapat menampung beberapa plat. Bejana dijaga tetap jenuh dengan pelarut pengembang dengan bantuan kertas saring yang tercelup ke dalam pengembang (Hostettmann, et al., 1995).
yaitu dengan cara menutup plat dengan sepotong kaca lalu menyemprot kedua sisi dengan penyemprot (Hostettmann, et al., 1995).
2.4.4 Kromatografi lapis tipis dua arah (two-dimensional TLC)
KLT dua arah atau KLT dua dimensi ini bertujuan untuk meningkatkan resolusi sampel ketika komponen-komponen solut mempunyai karakteristik kimia yang hampir sama, karena nilai Rf juga hampir sama. Selain itu, dua sistem fase gerak yang sangat berbeda dapat digunakan secara berurutan pada suatu campuran tertentu sehingga memungkinkan untuk melakukan pemisahan analit yang mempunyai tingkat polaritas yang hampir sama. Dengan demikian maka KLT dua dimensi dapat dipakai untuk memeriksa kemurnian isolat (Rohman, 2009).
KLT dua dimensi dilakukan dengan melakukan penotolan sampel disalah satu sudut lapisan lempeng tipis dan mengembangkannya sebagaimana biasa dengan fase gerak pertama. Lempeng kromatografi selanjutnya dipindahkan dari chamber pengembang dan eluen dibiarkan menguap dari lempeng. Lempeng
dimasukkan ke dalam chamber yang menggunakan eluen kedua sehingga pengembangan dapat terjadi pada arah kedua yang tegak lurus dengan arah pengembangan yang pertama. Suksesnya pemisahan tergantung pada kemampuan untuk memodifikasi selektifitas eluen kedua dibandingkan dengan selektifitas eluen pertama (Rohman, 2009).
2.5 Spektrofotometri
2.5.1 Spektrofotometri sinar ultraviolet
nm. Serapan cahaya oleh molekul dalam daerah spektrum ultra violet tergantung pada struktur elektronik dari molekul yang bersangkutan (Sastrohamidjojo, 1985).
Suatu atom atau molekul menyerap sinar UV dan energi tersebut akan menyebabkan tereksitasinya elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Tipe eksitasi tergantung panjang gelombang cahaya yang diserap. Gugus yang dapat mengabsorpsi cahaya disebut dengan gugus kromofor (Dachriyanus, 2004).
Pelarut yang banyak digunakan untuk spektrofotometri sinar UV adalah etanol 95% karena kebanyakan golongan senyawa larut dalam pelarut tersebut dan etanol tidak menyerap sinar UV. Alkohol mutlak niaga harus dihindari karena mengandung benzena yang dapat menyerap di daerah sinar UV pendek. Pelarut yang sering digunakan ialah air, etanol, metanol, n-heksana, eter minyak bumi dan eter. Konsentrasi dari analit di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang gelombang tertentu dengan menggunakan hukum Lambert-Beer (Gandjar dan Rohman, 2007; Harborne, 1987).
2.5.2 Spektrofotometri sinar inframerah
BAB I PENDAHULUAN
1.1 Latar Belakang
Indonesia merupakan salah satu negara yang memiliki hutan tropis yang sangat luas dan merupakan negara kedua yang kaya akan keanekaragaman hayati sesudah Brazil. Tanahnya banyak ditumbuhi tumbuh-tumbuhan yang dapat digunakan untuk obat-obat tradisional. Hutan tropis yang kaya dengan berbagai jenis tumbuhan merupakan sumber daya hayati dan sekaligus gudang senyawa kimia baik berupa senyawa kimia hasil metabolisme primer yang disebut juga sebagai metabolit primer seperti protein, karbohidrat, lemak yang digunakan sendiri oleh tumbuhan tersebut untuk pertumbuhannya, maupun sebagai sumber senyawa metabolit sekunder seperti steroid/triterpenoid, flavonoid dan alkaloid (Saleh, 2008; Lenny, 2006).
Senyawa metabolit sekunder yang terdapat dalam tumbuhan merupakan zat bioaktif yang berkaitan dengan kandungan kimia dalam tumbuhan, sehingga sebagian tumbuhan dapat digunakan sebagai bahan obat. Upaya pencarian tumbuhan berkhasiat obat telah lama dilakukan, baik untuk mencari senyawa baru ataupun menambah keanekaragaman senyawa yang telah ada. Hasil pencarian dan penelitian tersebut kemudian dilanjutkan dengan upaya pengisolasian senyawa murni dan turunannya sebagai bahan dasar obat (Lestari, 2010; Pasaribu, 2011).
anti-emetik, mengatasi edema serebral dan kerusakan saraf tulang belakang (Grover, et al., 2007).
Tumbuhan berkhasiat secara tradisional telah banyak digunakan oleh masyarakat ketika penyembuhan medis susah dijangkau secara ekonomi ataupun pengobatan secara medis tidak lagi memberikan harapan penyembuhan. Untuk itu, pemanfaatan tumbuhan berkhasiat dalam penyembuhan penyakit sangat potensial dan perlu dikaji secara ilmiah melalui penelitian (Nurhidayah, dkk., 2013).
Kurmak mbelin (Enydra fluctuans Lour.) termasuk suku Asteraceae, tumbuhan ini terdapat di beberapa tempat di benua Asia, khususnya Asia tenggara dan Asia Selatan. Di Filipina, daunnya yang ditumbuk dilaporkan digunakan untuk mengobati lepuh kulit pada penyakit herpes. Di Bangladesh, tumbuhan ini digunakan untuk mengobati masyarakat yang terkena patokan ular dan penyakit edema. Tumbuhan ini merupakan salah satu sayuran yang ada di Kabupaten Karo, Provinsi Sumatera Utara, Indonesia. Tumbuhan ini mudah diperoleh dengan harga relatif murah, serta menjadi sangat bermanfaat sebagai obat jika dikaitkan dengan salah satu kandungan kimianya yaitu steroid.
Berdasarkan hal di atas, penulis merasa tertarik untuk melakukan penelitian tentang karakterisasi simplisia, skrining fitokimia dan isolasi steroid/ triterpenoid ekstrak n-heksana herba kurmak mbelin (Enydra fluctuans Lour.) sehingga masyarakat mengenal dan mengetahui manfaat herba kurmak mbelin.
1.2 Perumusan Masalah
2. Apakah golongan senyawa kimia dari simplisia herba kurmak mbelin dapat ditentukan?
3. Apakah senyawa steroid/triterpenoid dari herba kurmak mbelin dapat diisolasi dari ekstrak n-heksana dan isolatnya dapat diidentifikasi secara spektrofotometri UV dan spektrofotometri IR?
1.3 Hipotesis
1. Karakterisasi simplisia herba kumak mbelin dapat dilakukan dengan menggunakan prosedur karakterisasi simplisia pada Materia Medika Indonesia dan World Health Organization.
2. Golongan senyawa kimia dari herba kurmak mbelin dapat ditentukan dengan menggunakan prosedur skrining fitokimia pada Materia Medika Indonesia (1995) dan Farnsworth (1966).
3. Senyawa steroid/triterpenoid dari herba kurmak mbelin dapat diisolasi dari ekstrak n-heksana dan isolatnya dapat diidentifikasi secara spektrofotometri UV dan spektrofotometri IR.
1.4Tujuan Penelitian
1. Untuk mengetahui karakterisasi simplisia herba kurmak mbelin.
2. Untuk mengetahui golongan senyawa kimia yang terdapat pada herba kurmak mbelin.
1.5Manfaat Penelitian
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA ISOLASI STEROID/TRITERPENOID DARI EKSTRAK n-HEKSANA HERBA KURMAK MBELIN
(Enydra fluctuans Lour.)
ABSTRAK
Salah satu tumbuhan suku Asteraceae yang digunakan sebagai sayuran oleh masyarakat Kabupaten Karo yaitu kurmak mbelin (Enydra fluctuans Lour.), dapat digunakan sebagai pencahar dan untuk mengobati penyakit herpes. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, skrining fitokimia untuk golongan senyawa yang terkandung di dalam herba kurmak mbelin dan mengisolasi senyawa steroid/triterpenoid.
Penelitian ini meliputi karakterisasi simplisia, skrining fitokimia, ekstraksi dilakukan secara perkolasi dengan pelarut etanol, kemudian ekstrak yang diperoleh difraksinasi dengan n-heksana, penentuan perbandingan fase gerak dengan mengunakan kromatografi lapi tipis (KLT), kemudian ekstrak n-heksana difraksinasi dengan kromatografi kolom (KK) dan KLT preparatif. Kemurnian isolat ditentukan dengan kromatografi lapis tipis (KLT) dua arah dan isolat murni yang diperoleh dikarakterisasi secara spektrofotometri sinar ultraviolet (UV) dan sperktrofotometri sinar inframerah (IR).
Hasil karakterisasi simplisia herba kurmak mbelin diperoleh kadar air 5,20%, kadar sari yang larut dalam air 20,63%, kadar sari yang larut dalam etanol 17,24%, kadar abu total 14,28% dan kadar abu yang tidak larut asam 0,54%. Hasil skrining fitokimia diperoleh adanya senyawa flavonoid, steroid/triterpenoid, tanin, saponin dan glikosida. Hasil analisis isolat menunjukkan bahwa isolat yang diperoleh adalah senyawa golongan steroid/triterpenoid dengan penampak bercak Liebermann-Burchard berwarna biru dengan nilai Rf 0,57 dan isolat yang diperoleh dianalisis secara spektrofotometri sinar UV memberikan absorbansi maksimum pada panjang gelombang 212,2 nm menunjukkan adanya gugus kromofor dan hasil spektrofotometri sinar IR menunjukkan adanya gugus C-O,-CH3,-CH2, C=C, C-H alifatis dan -OH.
SIMPLEX CHARACTERIZATION AND PHYTOCHEMICAL SCREENING AND ISOLATION OF STEROID/TRITERPENOID OF
n-HEXANE EXTRACT OF KURMAK MBELIN HERB (Enydra fluctuans Lour.)
ABSTRACT
One of the Asteraceae plants that is consumed as a vegetable in Karo is kurmak mbelin (Enydra fluctuans Lour.). This plant has traditionally been used as a laxative and to treat herpes. The purpose of this study was to perform simplex characterization, the phytochemical screening of compounds contained in kurmak mbelin herb and the isolation of the steroid/triterpenoid compound.
This research included simplex characterization, phytochemical screening, extraction was accomplished by percolation with ethanol as solvent, then the ethanol extract was fractionated with n-hexane as solvent, determination of the ratio of mobile phase by Thin Layer Chromatography, then the n-hexane extract was fractionated with Column Chromatography and followed by preparativeThin Layer Chromatography. The purity of isolate was confirmed by two-dimensional Thin Layer Cromatography and the pure isolate was characterized with ultraviolet and infrared spectrophotometric methods.
The result of simplex characterization, the water content 5.20%, water-soluble extract 20.63%, ethanol-water-soluble extract 17.24%, total ash 14.28%, acid-insoluble ash 0.54%. The result of phytochemical screening showed the presence of flavonoid, steroid/triterpenoid, tanin, saponin and glycosides. The result of isolate analysis indicated that the isolate was steroid/triterpenoid which gave blue colour with Rf value 0.57 with Liebermann-Burchard reagent, and the resulting isolat was then characterized by UV spectrophotometry that gave maximum absorption at wavelength 212.2 nm indicating the presence of chromophore and the result of IR spectrophotometry indicated the presence of C-O, -CH3, CH2, C=C, aliphatic C-H and –OH functional groups.
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA ISOLASI STEROID/TRITERPENOID DARI
EKSTRAK n-HEKSANA HERBA KURMAK MBELIN
(Enydra fluctuans Lour.)
SKRIPSI
Diajukan untuk mUniversitas Sumatera Uta
OLEH:
YEMIMA KASIH ORIZA S.
NIM 101501099
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA ISOLASI STEROID/TRITERPENOID DARI
EKSTRAK n-HEKSANA HERBA KURMAK MBELIN
(Enydra fluctuans Lour.)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
iajukan untuk mUniversitas Sumatera Uta
OLEH:
YEMIMA KASIH ORIZA S.
NIM 101501099
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA ISOLASI STEROID/TRITERPENOID DARI
EKSTRAK n-HEKSANA HERBA KURMAK MBELIN
(Enydra fluctuans Lour.)
OLEH:
YEMIMA KASIH ORIZA S.
NIM 101501099
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 16 Agustus 2014 Pembimbing I, Panitia Penguji,
Dra. Herawaty Ginting, M.Si., Apt. Dr. Marline Nainggolan, M.S., Apt. NIP 195108161980031002 NIP 195709091985112001
Dra. Herawaty Ginting, M.Si., Apt.
Pembimbing II, NIP 195108161980031002
Dr. M. Pandapotan Nasution, MPS., Apt Dra. Erly Sitompul, M.Si., Apt. NIP 194908111976031001 NIP 195006121980032001
Drs. Panal Sitorus, M.Si., Apt. NIP 19510301980031002
Medan, 6 Oktober 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat dan kasihnya, sehingga penulis dapat menyelesaikan skripsi ini yang berjudul “Karakterisasi Simplisia dan Skrining Fitokimia serta Isolasi Steroid/ Triterpenoid dari Ekstrak n-Heksana Herba Kurmak Mbelin (Enydra fluctuans Lour.)”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
dengan tulus ikhlas bagi kesuksesan penulis, juga kepada abang dan adikku tersayang, Dea Reo Prasadena Silalahi dan Ias Zilena Cacia Silalahi yang selalu memberi doa, dorongan dan semangat.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, 6 Oktober 2014
Penulis,
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA ISOLASI STEROID/TRITERPENOID DARI EKSTRAK n-HEKSANA HERBA KURMAK MBELIN
(Enydra fluctuans Lour.)
ABSTRAK
Salah satu tumbuhan suku Asteraceae yang digunakan sebagai sayuran oleh masyarakat Kabupaten Karo yaitu kurmak mbelin (Enydra fluctuans Lour.), dapat digunakan sebagai pencahar dan untuk mengobati penyakit herpes. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, skrining fitokimia untuk golongan senyawa yang terkandung di dalam herba kurmak mbelin dan mengisolasi senyawa steroid/triterpenoid.
Penelitian ini meliputi karakterisasi simplisia, skrining fitokimia, ekstraksi dilakukan secara perkolasi dengan pelarut etanol, kemudian ekstrak yang diperoleh difraksinasi dengan n-heksana, penentuan perbandingan fase gerak dengan mengunakan kromatografi lapi tipis (KLT), kemudian ekstrak n-heksana difraksinasi dengan kromatografi kolom (KK) dan KLT preparatif. Kemurnian isolat ditentukan dengan kromatografi lapis tipis (KLT) dua arah dan isolat murni yang diperoleh dikarakterisasi secara spektrofotometri sinar ultraviolet (UV) dan sperktrofotometri sinar inframerah (IR).
Hasil karakterisasi simplisia herba kurmak mbelin diperoleh kadar air 5,20%, kadar sari yang larut dalam air 20,63%, kadar sari yang larut dalam etanol 17,24%, kadar abu total 14,28% dan kadar abu yang tidak larut asam 0,54%. Hasil skrining fitokimia diperoleh adanya senyawa flavonoid, steroid/triterpenoid, tanin, saponin dan glikosida. Hasil analisis isolat menunjukkan bahwa isolat yang diperoleh adalah senyawa golongan steroid/triterpenoid dengan penampak bercak Liebermann-Burchard berwarna biru dengan nilai Rf 0,57 dan isolat yang diperoleh dianalis