KARYA TULIS ILMIAH
PERBANDINGAN EFEKTIVITAS ANTARA ASPIRIN DENGAN MADU DAN PROPOLIS SEBAGAI ANTIPLATELET BERDASARKAN
WAKTU PERDARAHAN PADA EKOR MENCIT
Oleh:
LOGASELVI A/P RAMAR 120100521
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
PERBANDINGAN EFEKTIVITAS ANTARA ASPIRIN DENGAN MADU DAN PROPOLIS SEBAGAI ANTIPLATELET BERDASARKAN WAKTU
PERDARAHAN PADA EKOR MENCIT
Oleh :
LOGASELVI A/P RAMAR 120100521
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
PERBANDINGAN EFEKTIVITAS ANTARA ASPIRIN DENGAN MADU DAN PROPOLIS SEBAGAI ANTIPLATELET BERDASARKAN WAKTU
PERDARAHAN PADA EKOR MENCIT
KARYA TULIS ILMIAH
“Karya Tulis Ilmiah Ini Diajukan Sebagai Salah Satu Syarat Untuk
Memperoleh Kelulusan Sarjana Kedokteran”
Oleh:
LOGASELVI A/P RAMAR 120100521
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
ABSTRAK
Prevalensi penyakit kardiovaskular (CVD) dan mortalitasnya terus meningkat. Berbagai penelitian telah membuktikan bahwa aspirin dapat mengurangi mortalitas yang disebabkan oleh CVD namun ternyata aspirin memiliki efek samping yang merugikan. Penelitian untuk meneliti perbandingan efektivitas aspirin dengan madu dan propolis belum ada padahal madu dan propolis memiliki efek antiplatelet.
Penelitian ini bertujuan untuk membuktikan adanya efek antiplatelet pada madu dan propolis serta mengetahui perbandingan efektivitas antara aspirin dengan madu dan propolis sebagai antiplatelet berdasarkan pengukuran waktu perdarahan pada ekor mencit.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan
post test only control group yang dilakukan pada 32 ekor mencit jantan (mus musculus), galur Double Ditsch Webster, berumur ± 3 bulan, berat badan 20-30 g, dibagi secara acak menjadi 4 kelompok. Terdiri dari kelompok kontrol negatif (plasebo), aspirin, madu dan propolis. Pemberian suspensi dilakukan peroral melalui sonde lambung selama 12 hari. Penelitian dilaksanakan di Laboratorium Farmakologi Departemen Farmakologi dan Terapetik Fakultas Kedokteran Universitas Sumatera Utara pada bulan September hingga Desember 2015. Data yang dikumpulkan adalah lamanya waktu perdarahan pada ekor mencit. Data dianalisis dengan uji Shapiro Wilk, kemudian dilanjutkan uji Kruskal Wallis dan Mann Whitney.
Rerata waktu perdarahan pada ekor mencit untuk masing-masing kelompok adalah plasebo (102,88 detik), aspirin (369,38 detik), propolis (385,88 detik) dan madu (304,63 detik). Uji Mann Whitney menunjukkan hasil yang signifikan pada kelompok aspirin, madu dan propolis terhadap kelompok kontrol (plasebo) dengan p=0,001. Tidak didapatkan perbedaan bermakna pada kelompok aspirin terhadap propolis (p=0,834) dan madu (p=0,172) dan antara kelompok propolis terhadap madu (p=0,294).
Madu dan propolis dapat menimbulkan efek antiplatelet pada mencit. Rerata waktu perdarahan pada ekor mencit dengan pemberian propolis dan madu lebih panjang atau mendekati dengan rerata waktu perdarahan dengan pemberian aspirin. Hasil penelitian ini dapat dijadikan dasar penelitian lebih lanjut untuk mengetahui penggunaannya pada manusia dalam menangani penyakit jantung dan pembuluh darah.
ABSTRACT
The prevalence of cardiovascular disease (CVD) and its mortality continues to increase. Various studies have shown that aspirin can reduce CVD mortality but it has adverse side effects. Research to examine the comparative effectiveness of aspirin with honey and propolis has not been done even though both have antiplatelet effects.
This study aimed to prove the antiplatelet effects on honey and propolis and to compare the antiplatelet effects of aspirin with honey and propolis based on the bleeding time in mice.
This study is a true experimental design with post test only control group that performed on 32 male mice, Double Ditsch Webster, ± 3 months old, weight of 20-30 g, were randomly divided into 4 groups. Consisting of a negative control group (placebo), aspirin, honey and propolis. The suspension were given orally for 12 days using sonde. Research was conducted at the Laboratory of Pharmacology Department of Pharmacology and Therapeutics Faculty of Medicine, University of North Sumatra in September until December 2015. The data collected was the bleeding time in mice. Data were analyzed by Shapiro Wilk test, followed by Kruskal Wallis and Mann Whitney.
The mean bleeding time in mice was placebo (102.88 seconds), aspirin (369.38 seconds), propolis (385.88 seconds) and honey (304.63 seconds). Mann Whitney test showed a significant results in the aspirin, honey and propolis groups against the control group (placebo) with p=0.001. There were no significant differences in the aspirin group against propolis (p=0.834) and honey (p=0.172) and between propolis group and honey (p=0.294).
Honey and propolis have an antiplatelet effects in mice. The mean bleeding time in mice given honey and propolis are longer or closer to the mean bleeding time in aspirin group. The results could be used as a basis for further research to determine its use in humans with cardiovascular disease.
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan, atas berkat dan rahmatnya,
sehingga penulis dapat menyelesaikan penelitian dan penulisan karya tulis ilmiah ini
dengan judul “Perbandingan Efektivitas antara Aspirin dengan Madu dan
Propolis Sebagai Antiplatelet Berdasarkan Waktu Perdarahan pada Ekor
Mencit”.
Penulis mendapatkan banyak bantuan dari berbagai pihak dalam
melaksanakan penelitian ini. Untuk itu, penulis ingin menyampaikan ucapan terima
kasih dan penghargaan yang setinggi-tingginya kepada:
1. Prof. dr. Gontar Alamsyah Siregar, Sp. PD-KGEH, selaku Dekan Fakultas
Kedokteran Universitas Sumatera Utara.
2. dr. Sake Juli Martina, Sp.FK selaku Dosen Pembimbing, yang telah banyak
memberikan bimbingan dan arahan kepada penulis, sehingga karya tulis
ilmiah ini dapat diselesaikan dengan baik.
3. dr. Wulan Fadine, M.Ked(An), Sp.An selaku Dosen Penguji 1 (Seminar
Proposal), dr. Jelita Siregar, M.Ked(Clin-Path), Sp.PK selaku Dosen Penguji
1 (Seminar Hasil) dan dr. Ronald Sitohang, Sp.B selaku Dosen Penguji 2,
yang telah banyak memberikan komentar dan saran-saran yang bermanfaat,
sehingga karya tulis ilmiah ini dapat diselesaikan dengan lebih lengkap.
4. Pihak Departemen Farmakologi dan Terapetik yang telah memberikan izin
penelitian kepada penulis untuk melakukan penelitian di Laboratorium
Farmakologi.
5. Kedua orang tua penulis, yang senantiasa mendoakan serta memberikan
6. Teman sekelompok saya yaitu Michael R I Silaban dan Muhammad Luthfi
yang selalu memberikan masukan dan bantuan dalam pengambilan data untuk
menyempurnakan karya tulis ilmiah ini.
7. Semua pihak baik langsung maupun tidak langsung yang telah memberikan
bantuan dalam penulisan karya tulis ilmiah ini.
Penulis menyadari bahwa karya tulis ilmiah ini masih jauh dari sempurna,
untuk itu penulis mengharapkan karya ini dapat bermanfaat bagi semua. Akhir kata
saya ucapkan banyak terima kasih.
Medan, 1 Desember 2015,
Peneliti,
Logaselvi A/P Ramar
DAFTAR ISI
Halaman
LEMBAR PENGESAHAN ………... i
ABSTRAK ……….. ii
ABSTRACT ……… iii
KATA PENGANTAR ……… iv
DAFTAR ISI ……….... vi
DAFTAR TABEL ………... ix
DAFTAR GAMBAR ……….. x
DAFTAR SINGKATAN ……… xi
DAFTAR LAMPIRAN ……….. xiii
BAB 1 PENDAHULUAN ………... 1
1.1. Latar Belakang ………... 1
1.2. Rumusan Masalah ……….. 4
1.3. Tujuan Penelitian ………... 4
1.4. Manfaat Penelitian ………. 5
BAB 2 TINJAUAN PUSTAKA ………. 6
2.1. Hemostasis ………. 6
2.1.1. Pengertian ………. 6
2.1.2. Spasme Pembuluh Darah ………. 6
2.1.3. Pembentukan Sumbat Trombosit ………. 7
2.1.4. Pembekuan Darah ……… 10
2.1.5. Sistem Fibrinolisis ……… 12
2.2. Trombosis ………... 12
2.3. Aspirin ……… 13
2.3.1. Definisi ………. 13
2.3.3. Farmakokinetik ……… 13
2.3.4. Efek Samping ………... 14
2.4. Propolis ……….. 16
2.4.1. Definisi ………. 16
2.4.2. Karakteristik Propolis ……….. 16
2.4.3. Kandungan Propolis ………. 16
2.4.4. Pengaruh Propolis terhadap Agregasi Trombosit …………. 17
2.5. Madu ……….. 17
2.5.1. Definisi ………. 17
2.5.2. Jenis-jenis Madu ………... 17
2.5.3. Karakteristik Madu ………... 18
2.5.4. Kandungan Madu ………. 18
2.5.5. Pengaruh Madu terhadap Agregasi Trombosit ………. 19
BAB 3 KERANGKA KONSEP DAN DEFINISI OPERASIONAL …….. 20
3.1. Kerangka Konsep Penelitian ……….. 20
3.2. Definisi Operasional ……….. 20
3.3. Hipotesis ……… 22
BAB 4 METODE PENELITIAN ………... 23
4.1. Jenis Penelitian ………... 23
4.2. Waktu dan Tempat Penelitian ………. 24
4.3. Populasi dan Sampel Penelitian ………. 24
4.4. Kriteria Inklusi, Eksklusi, dan Drop Out ………... 25
4.5. Cara Kerja dan Alur Penelitian ……….. 26
4.6. Data yang dikumpul ………... 29
BAB 5 HASIL PENELITIAN DAN PEMBAHASAN ……… 30
5.1. Hasil Penelitian ……….. 30
5.1.1. Deskripsi Lokasi Penelitian ………. 30
5.1.2. Deskripsi Sampel Penelitian ……… 30
5.1.3. Hasil Analisis Data ……….. 30
5.1.4. Uji Normalitas Data ………. 31
5.1.5. Uji Homogenitas Data ……….. 32
5.1.6. Uji Komparabilitas ………... 32
5.1.7. Uji Lanjutan (Post Hoc Test) ……… 33
5.2. Pembahasan ……… 33
BAB 6 KESIMPULAN DAN SARAN ……….. 36
6.1. Kesimpulan ……… 36
6.2. Saran ……….. 36
DAFTAR TABEL
Nomor Judul Halaman
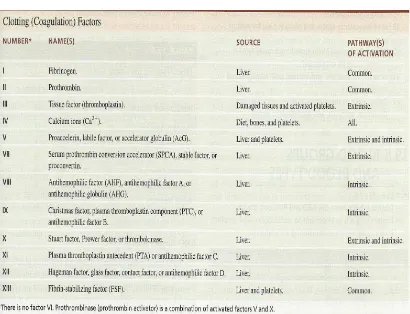
Tabel 2.1. Faktor Koagulasi 10
Tabel 4.1. Tabel Konversi Perhitungan Dosis secara per oral 28
Tabel 5.1. Waktu Perdarahan Mencit (detik) 30
Tabel 5.2. Hasil Uji Normalitas Waktu Perdarahan 32
Tabel 5.3. Uji Homogenitas Waktu Perdarahan antar Kelompok 32
DAFTAR GAMBAR
Nomor Judul Halaman
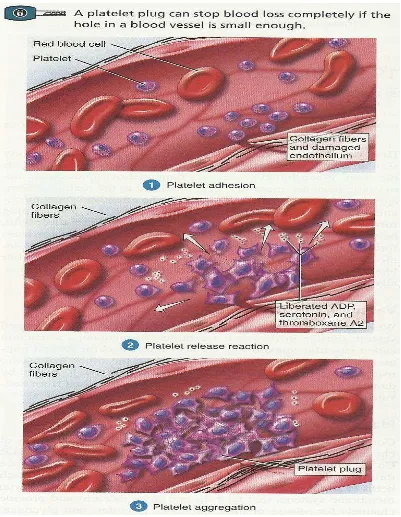
Gambar 2.1. Pembentukan Sumbat Trombosit 9
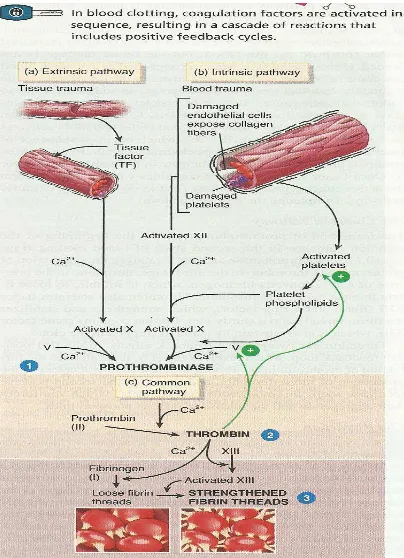
Gambar 2.2. Kaskade Pembekuan Darah 11
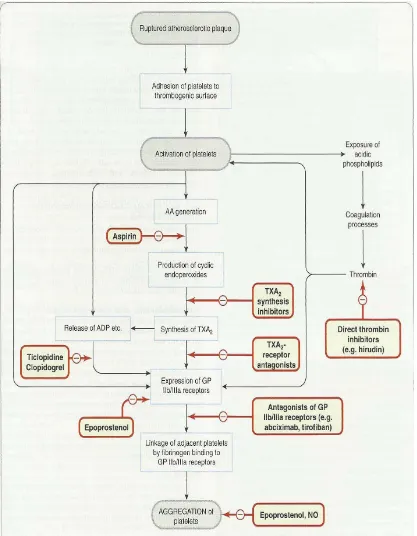
Gambar 2.3. Tempat Aksi Obat Antiplatelet 15
Gambar 3.1. Kerangka Konsep 20
DAFTAR SINGKATAN
ADP Adenosine diphosphate
ANOVA Analysis of variance
ASA Acetylsalicylic acid
cAMP Cyclic adenosine monophosphate
CAPE Caffeic Acid Phenethyl Ester
cGMP Cyclic guanosine monophosphate
COX-1 Cyclooxygenase-1
CVD Cardiovascular disease
DDW Double Ditsch Webster
LDL Low-density lipoprotein
NCD Noncommunicable diseases
OECD Organization for Economic Co-operation and Development
PGI2 Prostacyclin
PKC Protein kinase C
SPSS Statistical Package for Social Sciences
TIA Transient ischemic attacks
TXA2 Thromboxane A2
VASP Ser157 Vasodilator-stimulated phosphoprotein Serine 157
DAFTAR LAMPIRAN
Lampiran 1 Daftar Riwayat Hidup Lampiran 2 Ethical Clearance
ABSTRAK
Prevalensi penyakit kardiovaskular (CVD) dan mortalitasnya terus meningkat. Berbagai penelitian telah membuktikan bahwa aspirin dapat mengurangi mortalitas yang disebabkan oleh CVD namun ternyata aspirin memiliki efek samping yang merugikan. Penelitian untuk meneliti perbandingan efektivitas aspirin dengan madu dan propolis belum ada padahal madu dan propolis memiliki efek antiplatelet.
Penelitian ini bertujuan untuk membuktikan adanya efek antiplatelet pada madu dan propolis serta mengetahui perbandingan efektivitas antara aspirin dengan madu dan propolis sebagai antiplatelet berdasarkan pengukuran waktu perdarahan pada ekor mencit.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan
post test only control group yang dilakukan pada 32 ekor mencit jantan (mus musculus), galur Double Ditsch Webster, berumur ± 3 bulan, berat badan 20-30 g, dibagi secara acak menjadi 4 kelompok. Terdiri dari kelompok kontrol negatif (plasebo), aspirin, madu dan propolis. Pemberian suspensi dilakukan peroral melalui sonde lambung selama 12 hari. Penelitian dilaksanakan di Laboratorium Farmakologi Departemen Farmakologi dan Terapetik Fakultas Kedokteran Universitas Sumatera Utara pada bulan September hingga Desember 2015. Data yang dikumpulkan adalah lamanya waktu perdarahan pada ekor mencit. Data dianalisis dengan uji Shapiro Wilk, kemudian dilanjutkan uji Kruskal Wallis dan Mann Whitney.
Rerata waktu perdarahan pada ekor mencit untuk masing-masing kelompok adalah plasebo (102,88 detik), aspirin (369,38 detik), propolis (385,88 detik) dan madu (304,63 detik). Uji Mann Whitney menunjukkan hasil yang signifikan pada kelompok aspirin, madu dan propolis terhadap kelompok kontrol (plasebo) dengan p=0,001. Tidak didapatkan perbedaan bermakna pada kelompok aspirin terhadap propolis (p=0,834) dan madu (p=0,172) dan antara kelompok propolis terhadap madu (p=0,294).
Madu dan propolis dapat menimbulkan efek antiplatelet pada mencit. Rerata waktu perdarahan pada ekor mencit dengan pemberian propolis dan madu lebih panjang atau mendekati dengan rerata waktu perdarahan dengan pemberian aspirin. Hasil penelitian ini dapat dijadikan dasar penelitian lebih lanjut untuk mengetahui penggunaannya pada manusia dalam menangani penyakit jantung dan pembuluh darah.
ABSTRACT
The prevalence of cardiovascular disease (CVD) and its mortality continues to increase. Various studies have shown that aspirin can reduce CVD mortality but it has adverse side effects. Research to examine the comparative effectiveness of aspirin with honey and propolis has not been done even though both have antiplatelet effects.
This study aimed to prove the antiplatelet effects on honey and propolis and to compare the antiplatelet effects of aspirin with honey and propolis based on the bleeding time in mice.
This study is a true experimental design with post test only control group that performed on 32 male mice, Double Ditsch Webster, ± 3 months old, weight of 20-30 g, were randomly divided into 4 groups. Consisting of a negative control group (placebo), aspirin, honey and propolis. The suspension were given orally for 12 days using sonde. Research was conducted at the Laboratory of Pharmacology Department of Pharmacology and Therapeutics Faculty of Medicine, University of North Sumatra in September until December 2015. The data collected was the bleeding time in mice. Data were analyzed by Shapiro Wilk test, followed by Kruskal Wallis and Mann Whitney.
The mean bleeding time in mice was placebo (102.88 seconds), aspirin (369.38 seconds), propolis (385.88 seconds) and honey (304.63 seconds). Mann Whitney test showed a significant results in the aspirin, honey and propolis groups against the control group (placebo) with p=0.001. There were no significant differences in the aspirin group against propolis (p=0.834) and honey (p=0.172) and between propolis group and honey (p=0.294).
Honey and propolis have an antiplatelet effects in mice. The mean bleeding time in mice given honey and propolis are longer or closer to the mean bleeding time in aspirin group. The results could be used as a basis for further research to determine its use in humans with cardiovascular disease.
BAB 1 PENDAHULUAN 1.1. Latar Belakang
Hemostasis adalah suatu reaksi tubuh yang terjadi secara berurutan untuk
menghentikan perdarahan. Bila pembuluh darah rusak atau pecah, maka proses
hemostasis harus terjadi dengan cepat pada daerah yang telah terjadi kerusakan dan
dikendalikan dengan hati-hati agar efektif. Tiga mekanisme utama yang terjadi untuk
mengurangi kehilangan darah adalah vascular spasm (spasme pembuluh darah),
platelet plug formation (pembentukan sumbat trombosit), dan koagulasi (pembekuan
darah) (Tortora dan Derrickson, 2011).
Proses hemostasis dapat terjadi tanpa adanya cedera tambahan pada pembuluh
darah pasien yang mempunyai riwayat penyakit jantung dan kelainan pada pembuluh
darah (Tortora dan Derrickson, 2011). Dengan kata lain, trombosis merupakan
pembentukan sumbat hemostatik yang patologis dalam pembuluh darah yang tidak
terjadi perdarahan (Rang et al., 2012). Misalnya, pada pasien dengan transient
ischemic attacks (TIA), cerebrovascular disease (stroke), myocardial infarction, atau
penyumbatan pada arteri perifer yang digolongkan sebagai cardiovascular disease
(CVD) (OECD/WHO, 2014).
Penyakit kardiovaskular (CVD) adalah penyebab utama kecacatan dan
kematian prematur di seluruh dunia. Proses patologi yang mendasari CVD adalah
aterosklerosis (WHO, 2007). Menurut World Health Organization (WHO) pada
tahun 2012, kematian yang disebabkan oleh noncommunicable diseases (NCD)
adalah sebanyak 38 juta dari 56 juta kematian global, yaitu sekitar 68%. Penyebab
utama kematian NCD pada tahun 2012 adalah penyakit kardiovaskular (CVD) yaitu
Di wilayah Asia/Pasifik, ternyata penyebab kematian utama adalah CVD yaitu
diperkirakan sebanyak 9,3 juta kematian dan menyumbang sekitar sepertiga daripada
seluruh kematian yang terjadi pada tahun 2012 (OECD/WHO, 2014).
Menurut WHO-Noncommunicable Diseases (NCD) Country Profiles pada
tahun 2014, penyakit kardiovaskular (CVD) telah menjadi penyebab utama kematian
di Indonesia yaitu sekitar 37% dari seluruh kematian (1,551,000) di negara tersebut.
Pemberian obat antiplatelet misalnya aspirin dapat mengurangi angka
kematian yang disebabkan oleh CVD. Terapi antiplatelet ini dikatakan efektif dalam
menangani penyakit vaskular yang berat dengan pemberian secara jangka pendek
maupun jangka panjang (Antithrombotic Trialists’ Collaboration, 2002). Aspirin
(Acetylsalicylic acid-ASA) ternyata bekerja dengan menghambat sintesis tromboksan
A2 (TXA2) di dalam trombosit dan prostasiklin (PGI2) di pembuluh darah dengan
menghambat secara ireversibel enzim siklo-oksigenase (Rosmiati dan Gan, 1995).
Namun, dosis aspirin yang digunakan sebagai obat antiplatelet dalam uji klinis tidak
setara (Patrono et al., 2004). Pemberian aspirin dosis tunggal yang berlebihan serta
secara jangka panjang dapat menyebabkan risiko terjadinya keracunan (Litovitz et al.,
2001). Tingkat keparahan komplikasi yang terjadi dengan pemberian aspirin
tergantung pada dosis dan lama pengobatannya. Komplikasinya bisa berupa
perdarahan dan perforasi pada sistem gastrointestinal (Farrugia, 1999). Ternyata
setiap terapi farmakologis memiliki efek samping yang merugikan baik secara
langsung maupun tidak langsung. Maka bahan alami yang aman diperlukan sebagai
terapi farmakologis yang alternatif atau sebagai suplemen (Ndagu et al., 2013).
Madu adalah suatu cairan manis dan kental dengan rasa yang unik yang
dihasilkan oleh lebah madu (Farooqui, 2009). Madu sangat berkhasiat dalam terapi
medis karena adanya berbagai komponen phenolic yang mempunyai banyak aktivitas
biologis, termasuk antioksidan dan anti-inflamasi (Farooqui et al., 2014). Penelitian
antiagregasi platelet. Madu mengandung flavonoid, termasuk hesperetin yang
berfungsi sebagai antiagregasi platelet (Jin, 2007).
Propolis adalah produk lebah resin yang mempunyai penampilan fisik yang
bervariasi, tergantung pada banyak faktor (Salatino et al., 2005). Caffeic acid
phenethyl ester (CAPE) merupakan komponen aktif propolis yang diperoleh dari
sarang lebah madu. CAPE terbukti memiliki aktivitas antiplatelet, yaitu dengan
menghambat agregasi platelet (Chen et al., 2007).
Dengan adanya efek antiplatelet pada madu dan propolis, maka peneliti
tertarik untuk melakukan penelitian tentang perbandingan efektivitas aspirin dengan
madu dan propolis sebagai antiplatelet berdasarkan pengukuran waktu perdarahan
pada ekor mencit. Penelitian ini diharapkan dapat berguna dalam pencegahan CVD
1.2. Rumusan Masalah
Prevalensi penyakit kardiovaskular (CVD) dan mortalitas yang berkaitan dengannya terus meningkat. Berbagai penelitian telah membuktikan bahwa aspirin
dapat mengurangi mortalitas yang disebabkan oleh CVD namun ternyata aspirin
memiliki efek samping yang merugikan. Penelitian untuk meneliti perbandingan
efektivitas aspirin dengan madu dan propolis belum ada padahal madu dan propolis
terbukti mempunyai efek antiplatelet. Dengan demikian, masalah penelitian ini
adalah bagaimana perbandingan efektivitas aspirin dengan madu dan propolis sebagai
antiplatelet dinilai berdasarkan lama waktu perdarahan pada ekor mencit.
1.3. Tujuan Penelitian 1.3.1. Tujuan Umum
Dibuktikan adanya efek antiplatelet pada madu dan propolis serta
diketahuinya perbandingan efektivitas antara aspirin dengan madu dan
propolis sebagai antiplatelet berdasarkan pengukuran lama waktu perdarahan
pada ekor mencit.
1.3.2. Tujuan Khusus
Yang menjadi tujuan khusus dalam penelitian ini adalah:
1. Dibuktikan adanya pemanjangan waktu perdarahan pada ekor mencit
setelah pemberian propolis.
2. Dibuktikan adanya pemanjangan waktu perdarahan pada ekor mencit
setelah pemberian madu.
3. Diketahui perbandingan rerata waktu perdarahan pada ekor mencit dengan
pemberian aspirin dan propolis.
4. Diketahui perbandingan rerata waktu perdarahan pada ekor mencit dengan
1.4. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan manfaat sebagai berikut:
1. Bagi peneliti
Dapat memberikan pengetahuan dan informasi tentang efektivitas madu dan
propolis sebagai antiplatelet dan menjadi suatu pengalaman dalam
mengembangkan kemampuan peneliti di bidang penelitian kesehatan.
2. Bagi masyarakat
Bila terbukti pemakaian madu dan propolis dapat memanjangkan waktu
perdarahan, maka pemakaiannya dapat dipertimbangkan sebagai terapi
antiplatelet yang alternatif atau sebagai suplemen dalam menangani penyakit
jantung dan pembuluh darah.
3. Bagi ilmu pengetahuan
Sebagai bahan acuan atau dasar perkembangan informasi bagi peneliti lain
BAB 2
TINJAUAN PUSTAKA 2.1. Hemostasis
2.1.1. Pengertian
Hemostasis berasal dari kata haima (darah) dan stasis (berhenti), merupakan
proses yang amat kompleks, berlangsung secara terus menerus dalam mencegah
kehilangan darah secara spontan, serta menghentikan perdarahan akibat kerusakan
sistem pembuluh darah. Proses yang terjadi secara lokal berfungsi untuk menutup
kebocoran pembuluh darah, membatasi kehilangan darah yang berlebihan, dan
memberi kesempatan untuk perbaikan pembuluh darah (Suharti, 2009).
Hemostasis merupakan proses pembentukan bekuan pada dinding pembuluh
darah yang rusak dan mencegah kehilangan darah disamping mempertahankan darah
dalam keadaan cair dalam sistem vaskular (Barrett et al., 2012). Mekanisme yang
terjadi dalam upaya mengurangi kehilangan darah adalah spasme pembuluh darah
(vascular spasm), pembentukan sumbat trombosit (platelet plug formation), dan
pembekuan darah atau koagulasi (Tortora dan Derrickson, 2011).
2.1.2. Spasme Pembuluh Darah
Otot polos sirkuler yang tersusun pada dinding pembuluh darah akan
berkontraksi dengan segera setelah terjadi kerusakan pada pembuluh darah arteri,
yang disebut vascular spasm. Mekanisme ini akan mengurangi kehilangan darah
selama beberapa menit sampai jam sehingga mekanisme hemostatik lain terjadi.
Spasme ini terjadi mungkin karena kerusakan pada otot polos, disebabkan oleh zat
atau substansi yang dilepaskan dari trombosit teraktivasi (activated platelets) dan
2.1.3. Pembentukan Sumbat (plug) Trombosit 2.1.3.1. Platelet/ Trombosit
Trombosit adalah suatu sel berbentuk cakram (disc-shaped), sangat kecil
(diameternya 1-5µm), yang beredar dalam darah pada konsentrasi
200,000-400,000/µ L, dengan umur rata-rata 7-10 hari. Trombosit berasal dari megakariosit,
polyploidal hematopoietic cells yang terdapat di sumsum tulang. Pengatur utama
dalam pembentukan trombosit adalah hormon thrombopoietin (TPO) yang diproduksi
oleh hepar dan ginjal (Longo et al., 2012). Trombosit mengandung butiran berisi
bahan kimia yang sekali dilepaskan akan memicu terjadi pembekuan darah (Tortora
dan Derrickson, 2011). Secara ultrastruktur, trombosit terdiri atas zona perifer, zona
sol-gel dan zona organela (Suharti, 2009).
2.1.3.2. Adhesi Trombosit
Bila terjadi kerusakan pada sel endotel, trombosit akan menempel dan hampir
menutupi kolagen pada subendotel yang terpapar. Hal ini memicu terjadinya reaksi
kimia yang mengaktifkan trombosit (Howland dan Mycek, 2006).
2.1.3.3. Aktivasi Trombosit
Reseptor pada permukaan trombosit yang terlekat diaktifkan oleh kolagen dari
jaringan ikat yang mendasari. Hal ini menyebabkan terjadi perubahan morfologi di
dalam trombosit, dan terjadi pelepasan mediator kimia dari vesikel trombosit
(Howland dan Mycek, 2006). Fase ini disebut reaksi pelepasan dari trombosit. ADP
yang dilepaskan dan tromboksan A2 memainkan peran utama dengan mengaktifkan
trombosit yang terdekat. Serotonin dan tromboksan A2 berfungsi sebagai
vasokonstriktor, menyebabkan dan mempertahankan kontraksi otot polos pembuluh
darah, yang menurunkan aliran darah pada bagian pembuluh yang rusak (Tortora dan
2.1.3.4. Agregasi Trombosit
Pelepasan ADP menyebabkan trombosit lain di sekitarnya lengket, dan sifat
lengket pada trombosit yang baru diaktifkan ini menyebabkan terjadinya penempelan
pada trombosit yang telah aktif sebelumnya. Pertemuan trombosit ini disebut sebagai
agregasi trombosit. Akhirnya, akumulasi dan perlengketan sejumlah besar trombosit
akan membentuk suatu massa yang disebut platelet plug. Sumbat trombosit sangat
efektif dalam mencegah kehilangan darah dalam pembuluh darah yang kecil. Sumbat
trombosit akan menjadi sangat ketat ketika diperkuat oleh fibrin yang terbentuk
2.1.4. Pembekuan Darah (Koagulasi)
Pembekuan adalah kaskade kompleks dari reaksi enzimatik di mana setiap
faktor pembekuan mengaktifkan molekul dalam urutan tetap. Pada akhirnya,
sejumlah besar produk yaitu fibrin terbentuk. Dua jalur, disebut jalur ekstrinsik dan
jalur intrinsik akan memicu terjadi pembentukan enzim protrombinase. Enzim ini
akan mengubah protrombin menjadi trombin di common pathway. Akhirnya, enzim
trombin akan mengubah fibrinogen menjadi fibrin yang membentuk bekuan (Tortora
dan Derrickson, 2011).
Tabel 2.1. Faktor Koagulasi
2.1.5. Sistem Fibrinolisis
Sistem fibrinolisis berfungsi menghancurkan bekuan fibrin (Suharti, 2009).
Plasminogen diubah menjadi plasmin oleh activator plasminogen di jaringan. Plasmin
membatasi perkembangan bekuan dan melarutkan jaringan fibrin untuk penyembuhan
luka (Howland dan Mycek, 2006). Pada umumnya proses penyembuhan berlangsung
dalam waktu 14 hari (Tambunan, 2009).
2.2. Trombosis
Trombosis adalah proses pembentukan trombus atau adanya trombus dalam
pembuluh darah atau ruang jantung (Tambunan, 2009). Trombosis merupakan
pembentukan sumbat hemostatik yang patologis dalam pembuluh darah yang tidak
terjadi perdarahan (Rang et al., 2012). Trombosis dapat terjadi pada arteri dan vena.
Trombosis pada arteri disebut trombus putih karena komposisinya selain fibrin
didominasi oleh trombosit (Tambunan, 2009). Trombus tersebut biasanya
berhubungan dengan aterosklerosis dan dapat mengganggu aliran darah sehingga
menyebabkan iskemia atau kematian jaringan (Rang et al., 2012). Trombus pada vena
disebut trombus merah karena komposisinya selain fibrin didominasi oleh sel darah
merah (Tambunan, 2009).
Trombosis terjadi bila ada gangguan keseimbangan antara yang merangsang
trombosis dan yang mencegah trombosis. Faktor merangsang atau faktor risiko
trombosis pada arteri adalah endotel pembuluh darah yang tidak utuh, trombosit yang
teraktivasi, defisiensi antipembekuan, klirens faktor pembekuan aktif berkurang,
sistem fibrinolisis berkurang, dan stagnasi. Trombosis pada arteri serebral akan
mengakibatkan Transient ischemic attack (TIA) atau strok iskemik. Trombosis pada
arteri koroner mengakibatkan angina pektoris atau infark miokard. Trombosis pada
arteri perifer akan menyebabkan klaudikasio intermiten atau nekrosis/gangren
Trombus vena biasanya dimulai di vena betis yang kemudian meluas sampai
vena proksimal. Trombus biasanya dibentuk pada daerah aliran darah yang lambat
atau yang terganggu. Stasis merupakan predisposisi trombosis karena mencegah
faktor koagulasi aktif dilarutkan oleh darah yang tidak aktif, mencegah klirens faktor
koagulasi aktif, dan mencegah bercampurnya faktor koagulasi aktif dengan
penghambatnya (Tambunan, 2009).
2.3. Aspirin 2.3.1. Definisi
Acetylsalicylic acid, atau dikenal sebagai aspirin merupakan obat golongan
antitrombosit yang dapat menghambat agregasi trombosit sehingga menyebabkan
terhambatnya pembentukan trombus yang terutama sering ditemukan pada sistem
arteri (Rosmiati dan Gan, 1995).
2.3.2. Mekanisme Kerja
Aspirin menghambat sintesis tromboksan A2 (TXA2) di dalam trombosit dan
prostasiklin (PGI2) di pembuluh darah dengan menghambat secara ireversibel enzim
siklo-oksigenase (akan tetapi siklo-oksigenase dapat dibentuk kembali oleh sel
endotel). Sebagai akibatnya terjadi pengurangan agregasi trombosit (Rosmiati dan
Gan, 1995). Trombosit tidak dapat mensintesis protein karena tidak mempunyai inti
sel, sehingga setelah pemberian aspirin, sintesis TXA2 tidak terjadi sampai trombosit
yang berkenaan diganti dalam tujuh hingga sepuluh hari (Rang et al., 2012).
2.3.3. Farmakokinetik
Aspirin diserap dari lambung dan usus kecil. Aspirin memiliki sifat kelarutan
air yang rendah yang merupakan faktor pembatas dalam penyerapan. Aspirin dapat
deasetilasi dengan cepat di dinding usus, hati, plasma, dan jaringan lain untuk
plasma sekitar 80% dan memiliki volume distribusi sebesar 0.17 L/kg. Aspirin secara
perlahan memasuki otak, tetapi bebas melintasi plasenta. Kedua aspirin dan asam
salisilat terkonjugasi dalam hati dengan membentuk salicyluric acid dan glucuronic
acid. Beberapa metabolit kecil lainnya juga diproduksi. Metabolit tersebut diekskresi
melalui filtrasi glomerulus serta sekresi tubular. Biasanya, hanya 1/10 diekskresikan
sebagai asam salisilat bebas, tapi dapat ditingkatkan dengan alkalinisasi. Waktu paruh
aspirin adalah 15-20 menit. Namun, proses metabolisme menjadi jenuh selama
rentang terapeutik; waktu paruh obat dengan dosis antiinflamasi mugkin sekitar
delapan sampai dua belas jam sedangkan selama keracunan mungkin sampai 30 jam.
Dengan demikian, proses eliminasi tergantung pada dosisnya (Tripathi, 2008).
2.3.4. Efek Samping
Efek samping aspirin misalnya rasa tidak enak di perut, mual, dan perdarahan
saluran cerna biasanya dapat dihindarkan bila dosis per hari tidak lebih dari 325 mg.
Penggunaan bersama antasid atau antagonist H2 dapat mengurangi efek tersebut. Obat
ini dapat mengganggu hemostasis pada tindakan operasi dan bila diberikan bersama
heparin atau antikoagulan oral dapat meningkatkan risiko perdarahan (Rosmiati dan
Gan, 1995). Efek samping aspirin, terutama pada saluran pencernaan, yang
bagaimanapun, jelas berhubungan dengan dosis, sehingga dosis rendah (sering 75 mg
sekali sehari) biasanya dianjurkan untuk tromboprofilaksis. Thromboprophylaxis
disediakan untuk orang yang berisiko tinggi menderita penyakit kardiovaskular (Rang
2.4. Propolis 2.4.1. Definisi
Propolis adalah hasil campuran dari lilin lebah dan resin yang dikumpulkan
oleh lebah madu dari tanaman, khususnya dari bunga dan kuncup daun. Air liur dan
sekresi lain dari lebah dicampur berserta dengan lilin dalam proses pengumpulan dan
pemodelan resin. Resin ini digunakan oleh lebah untuk melapisi bagian dalam rongga
sarang. Komposisi propolis tergantung pada jenis tanaman yang didatangi oleh lebah
(Krell, 1996).
2.4.2. Karakteristik Propolis
Propolis merupakan hasil produk lebah resin dengan penampilan fisik yang
bervariasi, tergantung pada beberapa faktor. Warna propolis bervariasi dari kuning,
hijau, sampai coklat gelap (Salatino et al., 2005). Propolis bersifat lembut, lentur, dan
sangat lengket pada suhu 250-450 C. Propolis akan menjadi keras dan rapuh di bawah
suhu 150 C. Sementara di atas suhu 450 C propolis semakin lengket dan akan menjadi
cair pada suhu 600 sampai 700 C. Pelarut yang paling umum digunakan untuk
ekstraksi komersial adalah etanol, glikol dan air (Krell, 1996).
2.4.3. Kandungan Propolis
Komposisi propolis sangat kompleks dan lebih dari 300 senyawa telah
diidentifikasi. Komposisinya bervariasi dan tergantung pada musim dan vegetasi di
daerah di mana propolis dikumpulkan (Castro, 2001). Propolis terdiri dari resin
(50%), lilin (30%), minyak esensial (10%), pollen (5%), dan senyawa organik lain
(5%) (Gomez-Caravaca et al., 2006). Polyphenols, termasuk flavonoid, phenolic
acids dan ester merupakan molekul aktif yang utama dalam propolis (Havsteen,
2002). Caffeic Acid Phenethyl Ester (CAPE) adalah komponen aktif propolis yang
2.4.4. Pengaruh Propolis terhadap Agregasi Trombosit
Agregasi trombosit merupakan penyumbang utama pada proses aterosklerosis.
Komponen propolis telah menunjukkan efek yang penting pada agregasi trombosit.
CAPE (15 dan 25 µM) ternyata menghambat agregasi trombosit yang dirangsang
oleh kolagen. CAPE yang terlibat dalam beberapa jalur penghambatan agregasi
trombosit menjadi kontributor penting untuk aktivitas antiplatelet dalam propolis
(Chen et al., 2007). Penelitian yang telah dilakukan oleh Ivashchenko et al. pada
tahun 2014 juga telah membuktikan bahwa propolis efektif dalam mengurangi fungsi
agregasi trombosit.
2.5. Madu 2.5.1. Definisi
Madu adalah bahan manis alami yang dihasilkan oleh lebah madu, Apis
melifera yang berasal dari nektar bunga atau sekresi dari tanaman. Lebah madu
mengumpulkan nektar atau sekresi, mengubahnya dengan kombinasi dari zat-zat
lebah sendiri, dan menyimpannya dalam sarang lebah untuk menjadi matang (Codex
Stan 12-1981).
2.5.2. Jenis-jenis Madu
Madu dapat diklasifikasikan dalam beberapa kategori berdasarkan asal nektar.
Pertama, blossom honey (madu flora) yang diperoleh dari nektar bunga. Kedua,
honeydew honey (madu embun) yang dihasilkan oleh lebah setelah mengumpulkan “honeydew”(cairan hasil sekresi serangga dari genus Rhynchota). Ketiga, madu monofloral yang berasal dari satu jenis nektar atau didominasi oleh satu nektar.
Keempat, madu multifloral yang berasal dari beberapa jenis tanaman (Alvarez-Suarez
2.5.3. Karakteristik Madu
Madu merupakan cairan yang kental. Viskositas madu tergantung pada jenis
dan komposisi zat terutamanya kadar air yang terkandung dalam madu.
Higroskopisitas adalah salah satu sifat madu yang menggambarkan kemampuan
madu untuk menyerap dan menahan kelembaban dari lingkungan. Madu dengan
kadar air sebanyak 18,8% atau kurang akan menyerap kelembaban dari udara pada
kelembaban relatif di atas 60%. Warna madu bervariasi dari yang tidak berwarna ke
kuning gelap atau hitam tergantung pada jumlah partikel seperti serbuk sari (Olaitan
et al., 2007). Madu memiliki tegangan permukaan rendah sehingga menjadi pelembab
yang sangat baik dalam produk kosmetik. Tegangan permukaan bervariasi dengan
asal madu dan mungkin karena zat koloidnya. Viskositas yang tinggi dan tegangan
permukaan yang rendah bertanggung jawab untuk karakteristik berbusa pada madu.
Madu memiliki kapasitas menyerap panas yang bervariasi dari 0,56-0,73 kal/g/0C
sesuai dengan komposisi dan keadaan kristalisasi (Krell, 1996).
2.5.4. Kandungan Madu
Madu alami mengandung lebih kurang 200 zat termasuk asam amino, vitamin,
mineral, dan enzim (saccharase, amylase, catalase, glucose oxidase), tetapi gula dan
air adalah kandungan utamanya (Eteraf-Oskouei dan Najafi, 2013). Madu terdiri dari
95-99% gula, termasuk fruktosa dan glukosa yang mewakili sebanyak 85-95% dari
totalnya. Madu juga mengandung disakarida (sukrosa dan maltosa) dan beberapa
trisakarida serta oligosakarida dalam jumlah yang kecil. Komponen kedua yang
paling penting dalam madu adalah air (Krell, 1996). Madu mengandung beberapa
enzim, termasuk amylase, α-Glucosidase, glucose oxidase, dan catalase. Kandungan
minor pada madu adalah asam amino, mineral, vitamin, dan polyphenols (Apigenin,
2.5.5. Pengaruh Madu terhadap Agregasi Trombosit
Madu ternyata mempunyai efek kardioprotektif, termasuk antitrombotik,
vasodilator, mempertahankan peran homeostasis pembuluh darah, menghambat
oksidasi LDL dan sebagainya. Oleh karena itu, madu berperan penting dalam
mengobati penyakit jantung (Farooqui et al., 2014).
Madu mengandung flavonoid, termasuk hesperetin yang berfungsi sebagai
antiagregasi platelet. Hesperetin bekerja dengan menghambat fosforilasi fosfolipase γ2 dan mengganggu aktivitas COX-1 (Jin, 2007). Dalam studi lain, peneliti telah menganalisis aktivitas antiagregasi terhadap 30 jenis flavonoid. Flavonoid yang
paling berpotensi dalam aktivitas antiagregasi adalah 3,6-dihydroxyflavone
(0.119µM) dan syringetin (O-methylated flavonol) (Bojic et al., 2011). Penelitian
yang dilakukan oleh Ahmed et al. pada tahun 2011 terbukti madu mempunyai efek
BAB 3
KERANGKA KONSEP DAN DEFINISI OPERASIONAL 3.1. Kerangka Konsep Penelitian
Berdasarkan tujuan penelitian di atas maka kerangka konsep dalam penelitian ini
adalah:
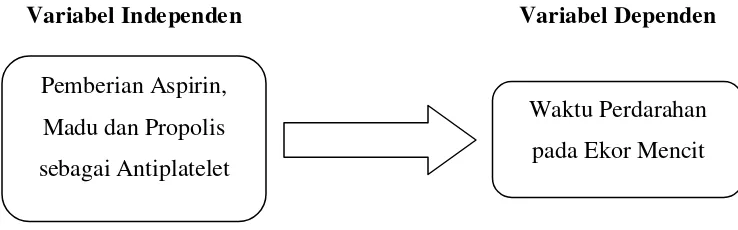
[image:38.612.134.503.257.372.2]Variabel Independen Variabel Dependen
Gambar 3.1. Kerangka konsep
3.2. Definisi Operasional 3.2.1. Definisi
1. Madu adalah suatu cairan manis dan kental dengan rasa yang unik yang
diproduksi oleh lebah Apis mellifera yang berasal dari nektar tumbuhan dan
dikumpulkan dalam sarang lebah.
2. Propolis adalah suatu bahan resin yang berasal dari kulit kayu dan
pucuk-pucuk tanaman yang dikumpulkan oleh lebah dari berbagai macam jenis
tumbuhan dan dicampurkan dengan lilin dan air liur lebah untuk melindungi
serta memperbaiki sarang lebah.
3. Aspirin adalah obat kelompok salisilat dan digunakan sebagai antiplatelet
(80-325 mg per hari). Pemberian Aspirin,
Madu dan Propolis
sebagai Antiplatelet
Waktu Perdarahan
4. Antiplatelet adalah obat yang dapat menghambat pembentukan trombus yang
sering ditemukan pada pembuluh darah arteri dengan menghambat agregasi
trombosit.
5. Waktu perdarahan adalah waktu mulai perdarahan pada ekor mencit yang
dipotong sampai darah berhenti keluar yaitu ketika sudah tidak ada darah pada
kertas serap untuk mengetahui efektivitas dari hasil pemberian obat yang akan
diteliti.
3.2.2. Cara Ukur
Metode Duke-Tail Bleeding
3.2.3. Alat Ukur 1. Pisau bedah
2. Kapas alkohol
3. Stopwatch
4. Kertas saring
3.2.4. Hasil Ukur
1. Dinyatakan Normal bila hasil interpretasi menunjukkan waktu perdarahan
normal antara 1-3 menit (60-180 detik)
2. Dinyatakan Memendek bila hasil interpretasi menunjukkan waktu perdarahan
kurang dari satu menit (< 60 detik).
3. Dinyatakan Memanjang bila hasil interpretasi menunjukkan waktu perdarahan
lebih dari tiga menit (> 180 detik).
3.3. Hipotesis
Tidak ada perbedaan waktu perdarahan antara aspirin dengan madu dan propolis.
BAB 4
METODE PENELITIAN 4.1. Jenis Penelitian
Penelitian ini merupakan penelitian true experimental design karena
melakukan randomisasi (simple random sampling), kontrol, dan perlakuan.
Rancangan penelitian adalah posttest only control group design.
K1
P R K2
K3
K4
P = Populasi (Mencit)
R = Randomisasi
K1 = Kel. Plasebo Kontrol (-) tanpa perlakuan
K2 = Kel. Plasebo Kontrol (+) dengan pemberian Aspirin tanpa perlakuan
K3 = Kel. Perlakuan dengan pemberian Propolis per oral selama 12 hari
Pengambilan sampel acak sederhana (simple random sampling)
1. Dibuat label nomor pada setiap hewan coba yang memenuhi kriteria inklusi.
2. Kemudian dipilih sebanyak 32 ekor mencit dari mereka untuk dijadikan
sampel dan dibagi menjadi 4 kelompok secara random.
Pemberian intervensi pada hewan coba (mencit) dilakukan secara single blind.
4.2. Waktu dan Tempat Penelitian
Penelitian ini telah dilakukan di Laboratorium Farmakologi Departemen
Farmakologi dan Terapetik Fakultas Kedokteran Universitas Sumatera Utara.
Penelitian ini telah dilaksanakan pada bulan September hingga Desember 2015.
Penelitian telah dilakukan setelah mendapat persetujuan dari Ethical Clearance dari
Komisi Etik Fakultas Kedokteran Universitas Sumatera Utara.
4.3. Populasi dan Sampel Penelitian
Pada penelitian ini telah digunakan mencit jantan (mus musculus), galur
Double Ditsch Webster umur : ± 3 bulan (dewasa), berat badan 20-30 gram, sehat,
belum pernah digunakan untuk penelitian lain. Mencit diperoleh dari Laboratorium
FMIPA Biologi Universitas Sumatera Utara Medan. Jumlah hewan coba
perkelompok ditentukan dengan rumus menurut Federer (1963), sebagai berikut:
(t-1)(n-1) ≥ 15 Keterangan :
n = besar sampel
Maka besar sampel yang dibutuhkan adalah :
(t-1)( n-1) ≥ 15
(4-1)(n-1) ≥ 15 (n-1) ≥ 5 n ≥ 6
Dibutuhkan sampel sebanyak enam ekor hewan coba untuk masing-masing
kelompok berdasarkan rumus Federer. Ditambahkan dengan perkiraan drop out 10%,
maka besar sampel minimal yang diperlukan untuk tiap kelompok adalah tujuh ekor
hewan coba.
Berdasarkan jumlah sampel minimal yang diperbolehkan secara statistik dan
tidak melanggar prinsip 3 R (Reduction, Replacement, Refinement) dalam penelitian
hewan coba, maka jumlah sampel yang diambil menjadi delapan ekor untuk tiap-tiap
kelompok. Jadi jumlah seluruh hewan coba yang digunakan sebanyak 32 ekor.
4.4. Kriteria Inklusi, Eksklusi dan Drop Out 4.4.1. Kriteria Inklusi :
1. Mencit (mus musculus) galur Double Ditsch Webster, jantan, umur: 2-3 bulan,
berat badan: 20-30 gram
2. Mencit sehat, bergerak aktif dan berasal dari kelompok yang sama
4.4.2. Kriteria Eksklusi :
4.4.3. Kriteria Drop Out :
1. Mencit mati dalam periode penelitian
4.5. Cara Kerja dan Alur Penelitian 4.5.1. Bahan
Pada penelitian ini bahan-bahan yang digunakan adalah :
1. Madu High Desert® 75 mg
2. Propolis High Desert® 500 mg
3. Aspirin 80 mg
4.5.2. Persiapan dan Pemeliharaan Hewan Coba
Sebelum penelitian dilakukan, adaptasi hewan di lokasi dengan cahaya 12 jam
siklus jadwal gelap, diet yang standard yaitu makan dan minum ad libitum. Makanan
yang dikonsumsi berasal dari Charoen Pokhpand. Hewan coba dipelihara dalam suhu
25 ± 10 ºC, kelembaban relatif 60%. Mencit dipelihara selama masa penelitian, berat
badan ditimbang sebelum dan sesudah percobaan.
4.5.3. Cara Kerja
Mencit jantan (mus musculus), galur DDW, sehat, berat badan : 20-30 gram,
dibagi menjadi 4 kelompok :
1. Mencit normal sebagai kontrol (-)
2. Mencit dengan pemberian Aspirin namun tidak diberi intervensi (kontrol
positif)
3. Mencit dengan pemberian propolis per oral selama 12 hari
Telah dilakukan pemberian pada mencit mulai hari pertama penelitian, selama 12 hari
dengan dosis menurut Tabel Dosis Konversi.
Perhitungan Dosis Konversi :
1. Aspirin: 80 mg x 0,0026 x 1000 : 20 = 10,40 mg/kgBB
2. Propolis: 500 mg x 0,0026 x 1000 : 20 = 65 mg/kgBB
3. Madu: 75 mg x 0,0026 x 1000 : 20 = 9,75 mg/kgBB
Setelah pemberian intervensi selama 12 hari, seluruh hewan coba mencit telah
dilakukan pengukuran waktu perdarahan dengan menggunakan metode Duke-Tail
bleeding sebagai berikut :
1. Daerah yang dilakukan pemeriksaan (ekor mencit) telah dibersihkan dengan
kapas alkohol.
2. Pertama, ekor mencit dipotong (dibuat luka) pada diameter 1mm
menggunakan pisau bedah dan biarkan darah keluar dengan bebas, saat darah
mulai keluar stopwatch dijalankan.
3. Darah yang keluar diisap dengan kertas saring setiap 30 detik sampai darah
berhenti mengalir (jangan sampai kertas saring menyentuh luka), stopwatch
dihentikan pada saat darah tidak dapat dihisap lagi menggunakan kertas
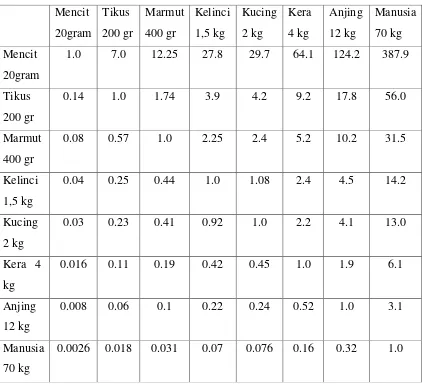
Tabel 4.1. Tabel Konversi Perhitungan Dosis (Laurence & Bacharach, 1964) secara per oral Mencit 20gram Tikus 200 gr Marmut 400 gr Kelinci 1,5 kg Kucing 2 kg Kera 4 kg Anjing 12 kg Manusia 70 kg Mencit 20gram
1.0 7.0 12.25 27.8 29.7 64.1 124.2 387.9
Tikus
200 gr
0.14 1.0 1.74 3.9 4.2 9.2 17.8 56.0
Marmut
400 gr
0.08 0.57 1.0 2.25 2.4 5.2 10.2 31.5
Kelinci
1,5 kg
0.04 0.25 0.44 1.0 1.08 2.4 4.5 14.2
Kucing
2 kg
0.03 0.23 0.41 0.92 1.0 2.2 4.1 13.0
Kera 4
kg
0.016 0.11 0.19 0.42 0.45 1.0 1.9 6.1
Anjing
12 kg
0.008 0.06 0.1 0.22 0.24 0.52 1.0 3.1
Manusia
70 kg
4.6. Data yang dikumpul
Data yang telah dikumpulkan dalam penelitian ini adalah data primer yang
didapat dari pengukuran waktu perdarahan pada ekor mencit setelah pemberian
intervensi selama 12 hari.
4.7. Analisis Data
Data yang didapat telah dianalisis dengan menggunakan program komputer.
Data tersebut telah dilakukan uji normalitas dengan menggunakan uji Shapiro-Wilk
karena jumlah sampel sedikit. Dilanjutkan dengan uji homogenitas menggunakan
Levene test. Kemudian dilakukan uji statistik non parametrik Kruskal-Wallis karena
distribusi data normal tetapi varian data tidak sama (tidak homogen), lalu dilanjutkan
dengan analisis post hoc menggunakan uji Mann Whitney. Suatu perbedaan
BAB 5
HASIL PENELITIAN DAN PEMBAHASAN 5.1. Hasil Penelitian
5.1.1. Deskripsi Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Farmakologi Departemen
Farmakologi dan Terapetik Fakultas Kedokteran Universitas Sumatera Utara. Lokasi
tersebut berada di Jalan Dr. T. Mansur, No.5, Medan, Sumatera Utara.
5.1.2. Deskripsi Sampel Penelitian
Dalam penelitian ini digunakan sebanyak 32 ekor mencit jantan (mus
musculus), galur Double Ditsch Webster umur : ± 3 bulan (dewasa), sehat, berat
badan 20-30 gram sebagai sampel, yang terbagi menjadi 4 kelompok masing-masing
berjumlah 8 ekor mencit, yaitu kelompok kontrol (plasebo), kelompok aspirin,
kelompok propolis, dan kelompok madu.
5.1.3. Hasil Analisis Data
Efek antiplatelet pada mencit yang dihitung dari waktu perdarahan dianalisa
dengan menggunakan program komputer. Dari penelitian didapatkan data sebagai
[image:48.612.105.535.580.665.2]berikut:
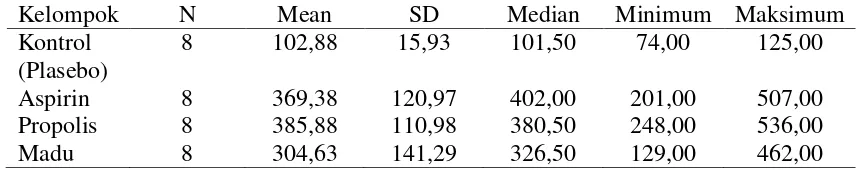
Tabel 5.1. Waktu Perdarahan Mencit (detik)
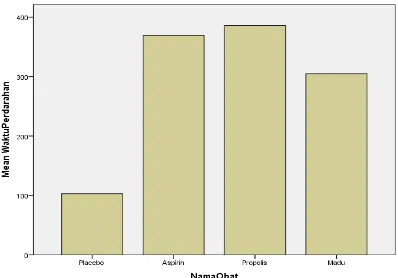
Gambar 5.1. Rerata Waktu Perdarahan Mencit (detik)
Data pada Tabel 5.1. dan Gambar 5.1. menunjukkan rerata waktu perdarahan
pada ekor mencit yang tertinggi adalah pada kelompok mencit dengan pemberian
propolis (mean=385,88 detik), kemudian diikuti kelompok mencit dengan pemberian
aspirin (mean=369,38 detik), kelompok mencit dengan pemberian madu
(mean=304,63 detik), dan terendah adalah kelompok kontrol (plasebo) yaitu dengan
nilai mean sebanyak 102,88 detik.
5.1.4. Uji Normalitas Data
Data waktu perdarahan pada masing-masing kelompok diuji normalitasnya dengan menggunakan uji Shapiro-Wilk. Hasilnya menunjukkan bahwa data
Tabel 5.2. Hasil Uji Normalitas Waktu Perdarahan
Kelompok N p Keterangan
Kontrol (Plasebo) Aspirin Propolis Madu 8 8 8 8 0,847 0,188 0,398 0,133 Normal Normal Normal Normal
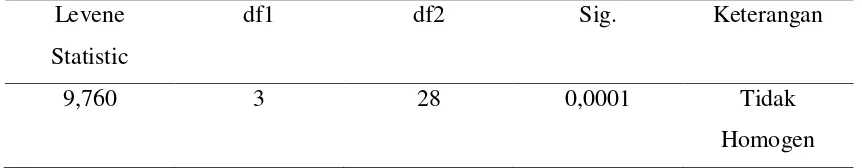
5.1.5. Uji Homogenitas Data
Data waktu perdarahan pada ekor mencit diuji homogenitasnya dengan
menggunakan uji Levene’s test. Hasilnya menunjukkan varian data tidak homogen
(p<0,05), disajikan pada Tabel 5.3.
Tabel 5.3. Uji Homogenitas Waktu Perdarahan antar Kelompok
Levene
Statistic
df1 df2 Sig. Keterangan
9,760 3 28 0,0001 Tidak
Homogen
5.1.6. Uji Komparabilitas
Uji komparabilitas bertujuan untuk membandingkan rerata waktu perdarahan
pada kelompok plasebo, aspirin, propolis dan madu. Berdasarkan hasil uji normalitas
dan homogenitas, data pada penelitian ini terdistribusi normal tetapi tidak memiliki
varian yang sama (tidak homogen), maka analisis komparatif yang digunakan adalah
uji non parametrik yaitu Kruskal-Wallis. Uji statistik non parametrik Kruskal-Wallis
menunjukkan terdapat perbedaan bermakna pada paling tidak dua kelompok
perlakuan (p=0,0001), sehingga dilanjutkan dengan analisis post hoc dengan uji
[image:50.612.106.537.398.482.2]5.1.7. Uji Lanjutan (Post Hoc Test)
Uji lanjutan ini bertujuan untuk melihat kelompok mana yang mempunyai perbedaan yang signifikan. Dalam penelitian ini, uji lanjutan yang digunakan adalah
[image:51.612.108.534.270.373.2]uji Mann Whitney. Hasil analisis uji tersebut disajikan pada Tabel 5.4.
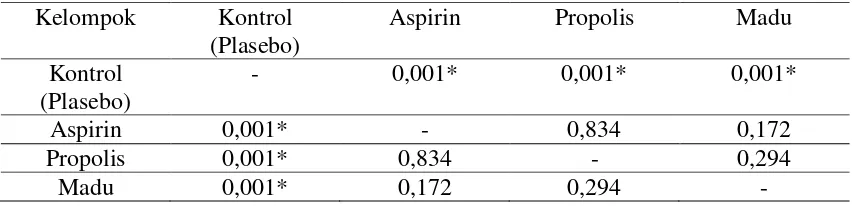
Tabel 5.4. Analisis Data dengan Uji Mann Whitney
Kelompok Kontrol (Plasebo)
Aspirin Propolis Madu
Kontrol (Plasebo)
- 0,001* 0,001* 0,001*
Aspirin 0,001* - 0,834 0,172 Propolis 0,001* 0,834 - 0,294
Madu 0,001* 0,172 0,294 -
*p<0,05 : terdapat perbedaan yang bermakna
Data pada Tabel 5.4. menunjukkan terdapat perbedaan yang bermakna antara
kelompok aspirin, propolis dan madu terhadap kelompok kontrol (plasebo) yaitu
p=0,001. Tidak terdapat perbedaan yang bermakna antara kelompok aspirin terhadap
kelompok propolis (p=0,834) dan madu (p=0,172) serta tidak ada perbedaan
bermakna antara kelompok propolis terhadap kelompok madu (p=0,294).
5.2. Pembahasan
Penelitian ini merupakan penelitian true experimental design dengan tujuan
untuk membuktikan adanya efek antiplatelet pada madu dan propolis serta
mengetahui perbandingan efektivitas antara aspirin dengan madu dan propolis
sebagai antiplatelet berdasarkan pengukuran lama waktu perdarahan pada ekor
Waktu perdarahan adalah waktu mulai perdarahan pada ekor mencit yang
dipotong sampai darah berhenti keluar. Adanya efek antiplatelet yang ditunjukkan
oleh madu dan propolis ditandai dengan semakin panjangnya waktu perdarahan
setelah dilakukan perlakuan pemberian luka pada ekor mencit.
Rata-rata waktu perdarahan pada kelompok perlakuan yang diberi madu dan
propolis lebih panjang dari kelompok kontrol (plasebo) dan hampir mendekati
rata-rata waktu perdarahan kelompok kontrol positif (aspirin). Hal ini demikian karena
flavonoid, salah satu kandungan dari madu dan propolis mempunyai aktivitas
antiplatelet yang dapat dikaitkan dengan terjadinya peningkatan produksi prostasiklin
oleh sel endotel. Prostasiklin tersebut menghambat proses agregasi melalui sintesis
cAMP yang akan menyebabkan terhambatnya ekspresi reseptor platelet GPIIb/IIIa
(Akhlaghi dan Bandy, 2009). Penghambatan proses agregasi tersebut menyebabkan
rata-rata waktu perdarahan pada ekor mencit dengan pemberian madu dan propolis
memanjang.
Dari uji statistik didapatkan perbedaan bermakna waktu perdarahan pada
kelompok kontrol (plasebo) terhadap kelompok perlakuan yang diberi madu dan
propolis.
Pada kelompok perlakuan yang diberi madu dan propolis tidak menunjukkan
perbedaan bermakna terhadap kelompok kontrol positif (aspirin). Hal ini
membuktikan bahwa madu dan propolis memiliki efek antiplatelet pada mencit,
seperti halnya aspirin.
Mekanisme penghambatan agregasi platelet oleh madu tergantung pada
beberapa faktor. Suatu penelitian telah menunjukkan bahwa paparan terhadap
hidrogen peroksida (salah satu kandungan madu) dapat menyebabkan penghambatan
aktivitas platelet yaitu agregasi platelet (Ferroni et al., 2004). Selain itu, madu juga
dapat mempengaruhi fungsi platelet dengan menghambat oksidasi LDL yang secara
karena penelitian telah membuktikan bahwa platelet yang teraktivasi setelah proses
agregasi akan memproduksi beberapa sitokin yang akan mengaktivasi fagosit
sehingga terjadi peningkatan produksi radikal bebas oksigen yang pada akhirnya akan
menyebabkan terjadinya proses oksidasi LDL (Ferroni et al., 2004).
Komponen aktif propolis, CAPE telah terbukti mempunyai efek antiplatelet
berdasarkan mekanisme berikut yaitu dengan meningkatkan pembentukan cGMP
yang akan mengaktifkan fosforilasi cyclic GMP-dependent VASP Ser157 dan
kemudian menghambat aktivitas PKC (protein kinase C). Pada akhirnya terjadi
penghambatan fosforilasi P47 dan memicu terjadi penghambatan agregasi platelet
(Chen et al., 2007).
Dari hasil penelitian ini ternyata rerata waktu perdarahan pada ekor mencit
dengan pemberian madu dan propolis lebih panjang atau mendekati dengan kelompok
kontrol positif (aspirin). Maka dapat dipertimbangkan pemakaiannya sebagai terapi
antiplatelet yang alternatif maupun sebagai suplemen dalam upaya pencegahan
penyakit jantung dan pembuluh darah. Oleh karena itu, penelitian yang lebih lanjut
perlu dilakukan pada manusia untuk hasil yang lebih efektif serta dilakukan
BAB 6
KESIMPULAN DAN SARAN
6.1. Kesimpulan
Berdasarkan analisis data yang diperoleh pada penelitian ini, disimpulkan
sebagai berikut:
1. Penelitian ini membuktikan bahwa madu dan propolis dapat memberikan efek
antiplatelet pada mencit dengan terjadinya pemanjangan waktu perdarahan
pada ekornya.
2. Rerata waktu perdarahan pada ekor mencit dengan pemberian propolis
(385,88 detik) lebih panjang daripada rerata waktu perdarahan dengan
pemberian aspirin (369,38 detik) sehingga propolis dapat dipertimbangkan
sebagai terapi antiplatelet yang alternatif dalam menangani penyakit jantung
dan pembuluh darah.
3. Rerata waktu perdarahan pada ekor mencit dengan pemberian madu (304,63
detik) hampir mendekati dengan rerata waktu perdarahan dengan pemberian
aspirin (369,38 detik) sehingga madu dapat dipertimbangkan sebagai
suplemen dalam menangani penyakit jantung dan pembuluh darah.
6.2. Saran
1. Perlu dilakukan penelitian serupa dengan jumlah sampel yang lebih banyak
agar diperoleh hasil yang lebih representatif.
2. Perlu dilakukan penelitian lebih lanjut pada manusia untuk mendapatkan data
3. Hasil penelitian ini diharapkan dapat menjadi acuan bagi pihak tenaga medis,
baik dokter maupun perawat dalam rangka untuk menangani penyakit jantung
dan pembuluh darah, sehingga dapat meningkatkan kualitas hidup penderita
DAFTAR PUSTAKA
Ahmed, A., et al., 2011. Effect of Natural Honey on Human Platelets and Blood
Coagulation Proteins. Pak. J. Pharm. Sci., 24 (3): 389-397.
Akhlaghi, M., Bandy, B., 2009. Mechanisms of flavonoid protection against
myocardial ischemia-reperfusion injury. Journal of Molecular and Cellular
Cardiology, 46: 309-317.
Alvarez-Suarez, J.M., Gasparrini, M., Forbes-Hernández, T.Y., Mazzoni, L.,
Giampieri, F., 2014. Review: The Composition and Biological Activity of
Honey: A Focus on Manuka Honey. Foods, 3: 420-432.
Antithrombotic Trialists’ Collaboration, 2002. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial
infarction, and stroke in high risk patients. British Medical Journal, 324: 71-86.
Barrett, K.E., Barman, S.M., Boitano, S., Brooks, H.L., 2012. Blood as a Circulatory
Fluids & the Dynamics of Blood & Lymph Flow. Dalam: Ganong’s Review of
Medical Physiology. 24th ed. USA: McGraw-Hill, 565.
Bogdanov, S., Jurendic, T., Sieber, R., Gallmann, P., 2008. Honey for nutrition and
health: A review. J. Am. Coll. Nutr., 27: 677-689.
Bojic, M., Debeljak, Z., Tomicic, M., Medic-Saric, M., Tomic, S., 2011. Evaluation
of antiaggregatory activity of flavonoid aglycone series. Nutrition Journal,
10: 73.
Castro, S.L., 2001. Propolis: Biological and Pharmacological Activities. Therapeutic
Chen, T., et al., 2007. Antiplatelet Activity of Caffeic Acid Phenethyl Ester Is
Mediated through a Cyclic GMP-Dependent Pathway in Human Platelets.
Chinese Journal of Physiology, 50 (3): 121-126.
Codex Stan 12-1981. Revised Codex Standard for Honey. Codex Stan 12-1981,
Rev. 1 (1987), Rev. 2 (2001). Diunduh dari:
www.codexalimentarius.org/input/download/standards/310/cxs_012e.pdf.
[Diakses pada 5 April 2015].
Eteraf-Oskouei, T., Najafi, M., 2013. Traditional and Modern Uses of Natural Honey
In Human Diseases: A Review. Iran J Basic Med Sci, 16: 731-742.
Farooqui, T., 2009. Honey: An Anti-Aging Remedy to Keep you Healthy in a Natural
Way. Diunduh dari:
http://www.scienceboard.net/community/perspectives.228.html.
[Diakses pada 23 May 2015].
Farooqui, T., Farooqui, A.A., 2014. Honey for Cardiovascular Disease. Dalam:
Boukraa, L., 2014. Honey in Traditional and Modern Medicine. USA: Taylor &
Francis Group, 187-216.
Farrugia, C.A., 1999. The Antiplatelet Activity of Aspirin. The chronic ill, 3: 14-18.
Federer, W.Y., 1963. Experimental Design, Theory and Application. New York:
Mac. Millan: 544.
Ferroni, P., Basili, S., Falco, A., Davi, G., 2004. Oxidant stress and platelet activation
in hypercholesterolemia. Antioxid. Redox. Signal, 6 (4): 747-756.
Gomez-Caravaca, A.M., Gomez-Romero, M., Arraez-Roman, D., Segura-Carretero,
A., Fernandez-Gutierrez, A., 2006. Advances in the analysis of phenolic
compounds in products derived from bees. Journal of Pharmaceutical and
Havsteen, B.H., 2002. The biochemistry and medical significance of the flavonoids.
Pharmacol. Ther., 96: 67-202.
Hegazi, A.G., El-Hady, F.K.A., 2009. Influence of Honey on the Suppression of
Human Low Density Lipoprotein (LDL) Peroxidation (In vitro). eCAM, 6 (1):
113-121.
Howland, R.D., Mycek, M.J., 2006. Drugs Affecting The Blood. Dalam: Lippincott’s
Illustrated Reviews: Pharmacology. 3rd ed. USA: Williams & Wilkins, 227-244.
Ivashchenko, M.N., Samodelkin, A.G., 2014. Effect of Propolis on Platelet
Aggregation. Biological Sciences. Fundamental Research, 12: 2146-2149.
Jin, Y., 2007. Antiplatelet activity of hesperetin, a bioflavonoid, is mainly mediated
by inhibition of PLC-γ2 phosphorylation and cyclooxygenase-1 activity.
Atherosclerosis, 194: 144-152.
Krell, R., 1996. Honey. Value Added Products From Beekeeping. FAO Agricultural
Services Bulletin. Food and Agriculture Organization of the United Nation. 124:
16-23.
Krell, R., 1996. Propolis. Value Added Products From Beekeeping. FAO Agricultural
Services Bulletin. Food and Agriculture Organization of the United Nation. 124:
153-157.
Laurence, D.R., Bacharach, A.L., 1964. Evaluation of drug activities:
Pharmacometrics. New York: Academic Press, 1: 196.
Litovitz, T.L., et al., 2001. Annual Report of the American Association of Poison
Control Centers Toxic Exposure Surveillance System. American Journal of
Longo, D.L., et al., 2012. Arterial and Venous Thrombosis. Dalam: Harrison’s
Principles of Internal Medicine. 18th ed. USA: McGraw-Hill, 117.
Ndagu, L.F., Arjana, A.A., Berata, I.K., 2013. Madu Berefek Protektif Terhadap
Infiltrasi Sel Radang dan Perdarahan Ginjal Akibat Induksi Aspirin. Indonesia
Medicus Veterinus, 2 (1): 102-114.
OECD/WHO, 2014. Mortality from cardiovascular disease. In: Health at a Glance:
Asia/Pacific 2014: Measuring Progress towards Universal Health Coverage,
OECD Publishing: 22-23.
Olaitan, P.B., Adeleke, O.E., Ola, I.O., 2007. Honey: a reservoir for microorganisms
and an inhibitory agent for microbes. African Health Sciences, 7 (3): 159-165.
Patrono, C., et al., 2004. Platelet-Active Drugs: The Relationships Among Dose,
Effectiveness, and Side Effects. The Seventh ACCP Conference on
Antithrombotic and Thrombolytic Therapy. CHEST, 126 (3): 234S-264S.
Rang, H.P., Dale, M.M., Ritter, J.M., Flower, R.J., Henderson, G., 2012. Haemostasis
and thrombosis. Dalam: Rang & Dale’s Pharmacology. 7th ed. Spain: 294-308.
Rosmiati, H., Gan, V.H.S., 1995. Antikoagulan, Antitrombosit, Trombolitik dan
Hemostatik. Dalam: Ganiswara, S.G., Setiabudy, R., Suyatna, F.D.,
Purwantyastuti, 1995. Farmakologi dan Terapi, edisi ke-4. Jakarta: Gaya Baru,
747-761.
Salatino, A., Teixeira, E.W., Negri, G., Message, D., 2005. Review: Origin and
Chemical Variation of Brazilian Propolis. eCAM, 2 (1): 33-38.
Suharti, C., 2009. Dasar-dasar Hemostasis. Dalam: Sudoyo, A.W., Setiyohadi, B.,
Alwi, I., Simadibrata, M., Setiati, S., 2009. Ilmu Penyakit Dalam, edisi ke-5,
Tambunan, K.L., 2009. Patogenesis Trombosis. Dalam: Sudoyo, A.W.,
Setiyohadi, B., Alwi, I., Simadibrata, M., Setiati, S., 2009. Ilmu Penyakit Dalam,
edisi ke-5, Jilid II. Jakarta: 1301-1306.
Tortora, G.J., Derrickson, B., 2011. The Cardiovascular System: The Blood. Dalam:
Principles of Anatomy & Physiology: Maintenance and Continuity of the Human
Body. 13th ed. Volume 2. Asia: John Wiley & Sons, Inc., 728-756.
Tripathi, K.D., 2008. Nonsteroidal Antiinflammatory Drugs and Antipyretic-
Analgesics. Dalam: Essentials of Medical Pharmacology. 6th ed. New Delhi:
Jaypee Brothers Medical Publishers, 187-189.
WHO, 2007. Prevention of Cardiovascular Disease: Pocket Guidelines for
Assessment and Management of Cardiovascular Risk: WHO/ISH Cardiovascular
Risk Prediction Charts for the African Region. Diunduh dari:
http://www.who.int/cardiovascular_diseases/guidelines/PocketGL.ENGLISH.
AFR-D-E.rev1.pdf. [Diakses pada 23 April 2015].
WHO, 2012. NCD mortality and morbidity. WHO. Diunduh dari:
http://www.who.int/gho/ncd/mortality_morbidity/en/. [Diakses pada 14
April 2015].
WHO-Noncommunicable