KAJIAN PENGAWETAN NIRA MENGGUNAKAN
ASAP CAIR TEMPURUNG KELAPA
TUBAGUS BAHTIAR RUSBANA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Kajian Pengawetan Nira Menggunakan Asap Cair Tempurung Kelapa adalah karya saya dengan arahan komisi pembimibing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Agustus 2009
ABSTRACT
TUBAGUS BAHTIAR RUSBANA. Study of Palm Juice Preservation using Coconut Shell Liquid Smoke. Under direction of SLAMET BUDIJANTO and HARSI DEWANTARI KUSUMANINGRUM.
Smoke is used traditionally as an alternative indirect way to preserve the palm juice. Preservation of palm juice using liquid smoke directly have never been conducted before. The aim of this study is to investigate the effects of redistilated liquid smoke to preserve the palm juice. The plam juice of Arenga pinnata was chose. Antimicrobial effect of crude liquid smoke was determinated. Concentration of crude liquid smoke at 0,50% until 3,00% gave the inhibitory effect of microbial growth in the palm juice, but it caused the colour of palm sugar getting dark. Redistilation was done to make the crude liquid smoke clearer. It also caused the change of total fenol. The method to measure the number of total fenol was AOAC 1995. Antimicrobial activity of redistilated liquid smoke was tested by suspension methode to determine the MIC. This test used concentrations 0,22% - 0,30%(v/v) for P.aeruginosa, 0,20% - 0,40%(v/v) for S.aureus, and 3,00% - 30,00%(v/v) for isolated lactic acid bacteria (LAB) from palm juice. When the redistilation liquid smoke applied in the nira, it used concentrations 0,50% - 3,00%(v/v). Total amount of microorganism and pH value were measured in this step. In conclusion, redistilation caused total fenol decrease 0,7%. The MIC value of P.aeruginosa S.aureus, and LAB isolate are 0,22%, 0,20% and 3,00% consecutively. The most preferable concentration of redestilated liquid smoke for application is 1,00 %. It is the smallest concentration that could prevent the decrease of pH by inhibit the microorganism growth until 12 hours.
RINGKASAN
TUBAGUS BAHTIAR RUSBANA. Kajian Pengawetan Nira menggunakan Asap Cair Tempurung Kelapa. Dibawah bimbingan SLAMET BUDIJANTO dan HARSI DEWANTARI KUSUMANINGRUM.
Gula merah merupakan gula hasil pengolahan nira tanaman palma banyak digunakan sebagai ingredient pada industri pangan. Keunggulan dari gula merah adalah memiliki nilai indeks glisemik (IG) rendah serta komposisi asam-asam organik dan komponen volatil yang terdapt didalamnya dapat memberikan rasa khas yang disukai secara sensori yang tidak dapat digantikan oleh gula putih (tebu). Akan tetapi, nira sebagai bahan baku pembuatan gula merah merupakan bahan yang mudah mengalami perubahan fermentatif akibat aktivitas mikroorganisme yang mengkontaminasinya selama penyadapan. Teknik pengawetan nira secara tradisional yang selama ini dilakukan belum dapat mengatasi masalah tersebut. Penerapan hasil penelitian pengawetan menggunakan natrium bisulfit, natrium metabisulfit dan natrium benzoat, serta zat aditif berupa penambahan kapur di satu sisi dapat mengawetkan nira tetapi disisi lain dapat menurunkan kualitas gula merah. Oleh karena itu perlu dilakukan upaya pengawetan lain yang lebih efektif dan lebih terjamin dari segi keamanan pangan.
Penggunaan asap sebagai pengawet nira secara tidak langsung telah lama dilakukan oleh penderes dengan mengasapi wadah penampung (lodong). Penggunaan asap cair sebagai pengawet nira secara langsung belum pernah dilakukan. Penelitian ini mengkaji potensi asap cair tempurung kelapa sebagai pengawet nira. Asap cair tempurung kelapa diperoleh dari CV Wulung Prima, Desa Cihideung Udik – Ciampea, Bogor. Nira aren segar diambil dari penderes di Desa Cibogo, Kecamatan Cigombong, Kabupaten Bogor. Uji aktivitas mikroba dilakukan dengan menentukan nilai MIC (Minimum Inhibitory Concentration) asap cair hasil destilasi ulang terhadap bakteri uji dengan metode kontak (suspension test). Kultur murni yang digunakan adalah Staphylococcus aureus, Pseudomonas aeruginosa, serta bakteri asam laktat (BAL) yang diisolasi dari nira. Uji aplikasi asap cair dilakukan dengan simulasi di laboratorium untuk menentukan konsentrasi berapa yang akan diujikan pada tahap simulasi penyadapan dengan melihat perubahan nilai pH, total mikroba, serta aplikasi langsung dalam pembuatan gula merah setelah penyadapan. Pengujian terakhir berupa uji organoleptik dan perubahan warna gula.
Hasil penelitian awal menunjukkan bahwa penggunaan asap cair hasil pengendapan tanpa destilasi ulang (asap cair kasar) berpotensi untuk digunkan sebagai pengawet nira, tetapi penggunaan asap cair tersebut mempengaruhi karakteristik gula terutama warna. Gula merah yang dihasilkan berwarna hitam sehingga asap cair yang digunakan untuk tahap selanjutnya adalah asap cair hasil destilasi ulang (redestilasi).
Uji aplikasi asap cair redestilasi pada konsentrasi 0,50%, 1,00%, 1,50%, 2,00%, dan 3,00% menunjukkan bahwa konsentrasi 1,00% dapat digunakan untuk pengawetan nira. Nira yang disadap selama 12 jam dengan penambahan asap cair redestilasi pada konsentrasi 1,00% memiliki pH lebih dari enam. Gula merah yang dihasilkan dari nira tersebut memiliki warna coklat cerah dengan rasa yang disukai panelis pada tingkat kesukaan 5 (suka).
© Hak Cipta milik IPB, tahun 2009 Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
KAJIAN PENGAWETAN NIRA MENGGUNAKAN
ASAP CAIR TEMPURUNG KELAPA
TUBAGUS BAHTIAR RUSBANA
Tesis
sebagai syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Kajian Pengawetan Nira menggunakan Asap Cair Tempurung
Kelapa
Nama : Tubagus Bahtiar Rusbana NRP : F251070021
Disetujui, Komisi Pembimbing
Dr. Ir. Slamet Budijanto, M.Agr Ketua
Dr.Ir. Harsi Dewantari Kusumaningrum Anggota
Diketahui, Ketua Program Studi
Myor Ilmu Pangan
Dr. Ir. Ratih Dewanti Hariyadi, M.Sc
Dekan Sekolah Pascasarjana
Prof. Dr. Ir. Khairil A. Notodiputro, M.S
PRAKATA
Alhamdulillahi rabbil ’aalamiin, sepenuh hati penulis ungkapkan rasa syukur atas selesainya penelitian bertema ”Kajian Pengawetan Nira menggunakan Asap Cair Tempurung Kelapa” yang diakhiri dengan penulisan tesis ini. Berangkat dari keprihatinan terhadap potensi besar yang dimiliki komoditi gula merah yang tersisihkan karena penggunaan pengawet yang tidak tepat dan proses pengolahan yang kurang baik, maka kajian ini dilakukan dengan harapan agar gula merah dari Indonesia dapat dikenal dan menjadi komoditi bernilai tinggi.
Penyelesaian tesis ini tidak dilakukan oleh penulis sendiri melainkan dengan bantuan beberapa pihak yang dengan penuh perhatian mendukung, mengarahkan, serta berjuang bersama penulis dalam rangka penyempurnaan kajian ini. Oleh karena itu dalam kesempatan ini penulis menyampaikan rasa terima kasih dan penghormatan yang setinggi-tingginya kepada :
1. Dr. Ir. Slamet Budijanto, M.Agr yang telah memberi rekomendasi untuk kelanjutan studi S2 sekaligus menjadi pembimbing utama. Tidak ada penghargaan yang bisa saya berikan selain ucapan terima kasih yang sedalam-dalamnya atas jasanya selama ini.
2. Dr.Ir. Harsi Dewantari Kusumaningrum selaku anggota pembimbing yang senantiasa memberikan keluangan waktu dan curahan pemikiran ditengah kesibukan tugasnya.
3. Dr.Ir. Yadi hariyadi, M.Sc sebagai Dosen Penguji. Terima kasih atas waktu dan semua saran yang diberikan.
4. Ratri Hanindha Majid, S.P. Istri tercinta yang menjadi sumber motivasi, ilmuwan yang senantiasa memberikan solusi cerdas dalam setiap kesempitan, pendamping dengan segala curahan kasih sayang yang tidak ternilai tingginya bagi penulis, aca.
5. Ananda Tubagus Alifian Akhyar, kehadirannya memberi semangat dan ketenangan dalam kesibukan setiap hari.
6. Keluarga Semarang dan Keluarga Pandeglang yang memberikan doa dan dukungan baik moril maupun materil.
7. Rekan-rekan IPN 2007 terutama untuk Reski dan Zaim, serta Mbak Dwi dan keluarga.
8. Rekan-rekan satu laboratorium, Mbak Ari, Pak Taufik, Mbak Mar, Ibu Sofi, dan Ibu Sari; serta
9. Semua pihak yang tidak bisa saya sebutkan satu per satu dalam kesempatan ini.
Semoga apa yang kita lakukan senantiasa bermanfaat dan diberi balasan oleh Allah SWT sebagai tabungan amal kebajikan.
”Tak ada gading yang tak retak” merupakan pepatah yang tepat untuk karya ini sehingga penulis sangat mengharapkan saran dan kritik agar karya ini menjadi lebih baik. Semoga karya ini dapat memberi manfaat bagi yang membacanya.
RIWAYAT HIDUP
DAFTAR ISI
Halaman
DAFTAR ISI ... i
DAFTAR TABEL ... iii
DAFTAR GAMBAR ... iv
DAFTAR LAMPIRAN ... v
1. PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 2
1.3. Tujuan Penelitian ... 3
1.4. Manfaat Penelitian ... 4
2. TINJAUAN PUSTAKA ... 5
2.1. Gula Merah ... 5
2.2. Nira ... 9
2.3. Penyadapan Nira dan Sumber-Sumber Kontaminasi Nira... 10
2.4. Mikrobiologi Nira ... 14
2.5 Bakteri Asam Laktat dan Fermentasi Nira ... 17
2.6. Derajat Keasaman (pH) Nira dalam Pembuatan Gula Merah ... 19
2.7. Upaya-Upaya Pengawetan Nira ... 20
2.8. Aspek Keamanan Pangan dalam Penggunaan Zat Aditif ... 22
2.9. Asap Cair ... 23
2.10 Aktivitas Antimikroba Asap Cair... 24
2.11. Asap Cair Tempurung Kelapa... 25
2.12. Redestilasi Asap Cair ... 28
3. METODOLOGI ... 30
3.1. Waktu dan Tempat Penelitian ... 30
3.2. Bahan dan Alat ... 30
3.3. Tahapan Penelitian dan Prosedur Pengujian ... 30
3.3.1. Penelitian Pendahuluan ... 33
3.3.3. Uji Aktivitas Antimikroba Asap Cair Redestilasi ... 34
3.3.4. Aplikasi Asap Cair Redestilasi untuk Pengawetan Nira ... 36
3.3.5. Pembuatan Gula Merah dengan Menggunakan Konsentrasi Asap Cair Redestilasi Terpilih ... 38
3.3.6. Analisis Statistik ... 39
4. HASIL DAN PEMBAHASAN ... 40
4.1. Potensi Penggunaan Asap Cair Tempurung Kelapa sebagai Pengawet Nira... 40
4.2. Kadar Fenol Asap Cair Redestilasi ... 43
4.3. Aktivitas Antimikroba Asap Cair Redestilasi ... 50
4.3.1. Uji Aktivitas Antibakteri Asap Cair Tempurung Kelapa Redestilasi 46 4.3.2. Uji Aktivitas Antibakteri Asap cair Tempurung Kelapa Redestilasi terhadap Isolat Bakteri Asal Nira ... 49
4.4. Aplikasi Asap Cair Redestilasi sebagai Pengawet Nira ... 51
4.4.1. Perubahan pH selama 12 Jam Penyimpanan ... 51
4.4.2. Perubahan Jumlah Mikroba selama 12 Jam Penyimpanan ... 53
4.4.3.. Aplikasi Penyadapan Selama 12 Jam ... 55
4.4.4. Simulasi Perubahan pH selama Penyadapan ... 56
4.5. Uji Organoleptik ... 57
4.6. Pengujian Warna ... 58
5. SIMPULAN DAN SARAN ... 61
5.1.Simpulan ... 61
5.2. Saran ... 61
DAFTAR PUSTAKA ... 62
DAFTAR TABEL
Halaman
Tabel 1 Populasi Industri Gula Merah di Indonesia Tahun 2001 ... 5
Tabel 2 Komposisi Asam Organik yang terdapat pada Kecap (mg/100g) .... 6
Tabel 3 Jenis dan Persentase Area Komponen Volatil Kecap Manis dan Gula Merah ... 7
Tabel 4 Kategori Pangan Berdasarkan Indeks Glisemik ... 8
Tabel 5 Syarat Mutu Gula Palma berdasarkan SNI 01-3743-1995 ... 9
Tabel 6 Komposisi Nira dari Berbagai Tanaman Palmae ... 10
Tabel 7 Isolat Mikroorganisme dari Nira Lontar pada Berbagai Waktu Fermentasi ... 16
Tabel 8 Komponen-Komponen yang Teridentifikasi dari Fraksi terlarut Asap Cair Tempurung Kelapa dalam dichloromethane... 27
Tabel 9 Jumlah Mikroba setelah Dikontakkan selama 24 Jam dengan Asap Cair Kasar pada berbagai Konsentrasi ... 41
DAFTAR GAMBAR
Halaman
Gambar 1 Proses Pengasapan Lodong menggunakan Pemuput ... 12
Gambar 2 Proses Penyadapan Nira : (A) Penyayatan Ujung Mayang dan (B) Pemasangan Penampung Nira dan Penutupnya ... 13
Gambar 3 Alat Destilasi Asap Cair ... 29
Gambar 4 Skema Alur Penelitian Kajian Pengawetan Nira Menggunakan Asap Cair Tempurung Kelapa... 32
Gambar 5 Deskripsi Nilai L, a, dan b pada Pembacaan Chromameter ... 38
Gambar 6 Asap Cair Kasar Tempurung Kelapa Hasil Pengendapan... 41
Gambar 7 Perubahan pH Nira setelah Diberi Perlakuan Penambahan Asap Cair (AC) pada Berbagai Konsentrasi selama 12 Jam ... 42
Gambar 8 Gula Merah dari Nira yang Mengandung Asap Cair 0,50% ... 43
Gambar 9 Total fenol Asap Cair Sebelum (A) dan Sesudah Destilasi (B) ... 44
Gambar 10 Asap Cair Sebelum (A) dan Sesudah Destilasi (B) ... 45
Gambar 11 Jumlah S.aureus setelah Diuji Kontak dengan Asap Cair (AC) pada Berbagai Konsentrasi selama 24 Jam ... 46
Gambar 12 Jumlah P.aeruginosa setelah Diuji Kontak dengan Asap Cair (AC) pada Berbagai Konsentrasi selama 24 Jam ... 47
Gambar 13 Isolat Bakteri Asam Laktat Asal Nira Hasil Pewarnaan Gram .... 50
Gambar 14 JumlahBakteriAsam Laktat setelah Diuji Kontak dengan Asap Cair (AC) pada Berbagai Konsentrasi selama 24 Jam ... 51
Gambar 15 Grafik Perubahan pH Nira yang Diberi Asap Cair (AC) pada Berbagai Konsentrasi selama 12 Jam Penyimpanan ... 52
Gambar 16 Jumlah Total Mikroba pada Nira yang Diberi Asap Cair (AC) Redestilasi 1,00% selama 12 Jam Penyimpanan ... 53
Gambar 17 Jumlah Total BAL pada Nira yang Diberi Asap Cair Redestilasi 1,00% selama 12 Jam Penyimpanan ... 54
Gambar 18 Jumlah Total Khamir pada Nira yang Diberi Asap Cair Redestilasi 1% selama 12 Jam Penyimpanan ... 54
Gambar 19 Hubungan pH dan Jumlah Bakteri Asam Laktat pada Fermentasi Nira selama 12 Jam Penyimanan ... 55
Gambar 20 Perubahan pH selama Simulasi Penyadapan selama 12 Jam Menggunakan Asap Cair pada Konsentrasi 1,00% dan 3,00% .... 56
Gambar 21 Penilaian Panelis terhadap Kenormalan Rasa Gula Merah dengan Nira yang Mengandung Asap Cair 1,00% dan 3,00%... 58
DAFTAR LAMPIRAN
Halaman Lampiran 1. Data Pengukuran Total Fenol Pada Asap Cair
Tempurung Kelapa ... 69
Lampiran 2. Hasil ANOVA Kadar Fenol Asap Cair Redestilasi ... 70
Lampiran 3. Uji Lanjut Duncan untuk Pengaruh Destilasi ... 71
Lampiran 4. Penentuan MIC Asap Cair Redestilasi Terhadap P.aeruginosa . 72 Lampiran 5. Hasil ANOVA Nilai MIC P.aeruginosa... 73
Lampiran 6. Uji Lanjut Duncan untuk Nilai MIC P.aeruginosa... 75
Lampiran 7. Data Penentuan MIC S.aureus... 76
Lampiran 8. Hasil ANOVA Nilai MIC S.aureus ... 77
Lampiran 9. Uji Lanjut Duncan untuk Nilai MIC S.aureus... 79
Lampiran 10. Data Penentuan MIC Isolat BAL ... 80
Lampiran 11. Hasil ANOVA Nilai MIC Isolat BAL ... 81
Lampiran 12. Uji Lanjut Duncan untuk Nilai MIC Isolat BAL ... 82
Lampiran 13. Perubahan pH Nira Selama 12 Jam Penyimpanan ... 83
Lampiran 14. Hasil ANOVA Perubahan pH Nira Selama 12 Jam Penyimpanan ... 84
Lampiran 15. Uji Lanjut Duncan untuk Konsentrasi ... 86
Lampiran 16. Uji Lanjut Duncan untuk Waktu ... 87
Lampiran 17. Data Simulasi Penyadapan Nira ... 89
Lampiran 18. Hasil ANOVA Perubahan pH Simulasi Penyadapan Nira ... 90
Lampiran 19. Uji Lanjut Duncan untuk Konsentrasi ... 92
Lampiran 20. Uji Lanjut Duncan untuk Waktu ... 93
Lampiran 21. Hasil Uji Organoleptik ... 95
Lampiran 22. Hasil ANOVA Uji Organoleptik ... 96
Lampiran 23. Uji Lanjut Duncan untuk Kesukaan ... 97
I PENDAHULUAN
1.1. Latar Belakang
Gula merah merupakan gula yang diperoleh dari pengolahan nira tanaman palma seperti aren, kelapa, dan lontar (nipah). Di Indonesia, produksi gula aren tersebar hampir diseluruh pulau. Daerah yang paling banyak memproduksi gula merah adalah: Sumatera Utara, Bengkulu, Jawa Barat, Banten, Jawa Tengah, Kalimantan Tengah, Kalimantan Selatan, Bali, Nusa Tenggara Barat, Sulawesi Utara, dan Sulawesi Barat (Sulaeman, 2002).
Hasil penelusuran media massa menunjukkan bahwa pengembangan industri gula aren, salah satu jenis gula merah, mulai dilakukan pada tahun 2006 terutama di Sulawesi Utara, Sumatera Utara, Jawa Barat, Jawa Timur, Sulawesi Tenggara, Kalimantan Barat, dan Kalimantan Timur. Pada tanggal 14 Januari 2007 dilakukan ekspor perdana gula aren sebanyak 12,5 ton dari Tomohon, Sulawesi Utara, ke Rotterdam, Belanda. Hal ini menunjukkan bahwa gula merah memiliki pasar yang luas, tidak hanya dalam negeri tetapi juga luar negeri (ekspor).
Keunggulan yang dimiliki gula merah diantaranya adalah memiliki flavor dengan komposisi tertentu asam-asam organik dan komponen volatil yang dapat memberikan rasa dan aroma khas sehingga penggunaannya sebagai ingredient pada industri pangan seperti kecap manis dan makanan tradisional tidak dapat digantikan oleh gula putih. Keunggulan lain dari gula merah adalah memiliki nilai indeks glisemik (IG) sebesar 35 yang menggolongkannya sebagai bahan pangan dengan IG rendah sehingga lebih aman untuk dikonsumsi bagi para penderita diabetes karena tidak menyebabkan kadar gula darah meningkat tajam.
penyadapan. Nira yang asam akibat proses fermentasi tidak dapat diolah menjadi gula cetak karena sukar mengeras.
Antispasi terhadap kerusakan nira dilakukan dengan pengawetan baik secara tradisional maupun dengan penambahan zat aditif. Teknik pengawetan nira secara tradisional yang selama ini dilakukan oleh para penderes adalah dengan melakukan pembersihan lodong (wadah penampung nira) dan melakukan pemuputan atau pengasapan lodong sebelum digunakan untuk menyadap. Ketika proses pemasakan nira menjadi gula merah dengan bahan bakar kayu berlangsung, lodong yang telah dibersihkan diletakkan di atas perapian. Dengan demikian lodong mengalami proses pengasapan dan mendapat efek antimikroba. Upaya lain yang dilakukan adalah menambahkan pengawet alami seperti kulit pohon manggis, kulit buah manggis muda, daun manggis, akar kawao, kulit kayu ralu, dan sebagainya.
Pengetahuan mengenai pengawet kimia (zat aditif) mendorong petani untuk menambahkan pengawet kimia seperti natrium bisulfit, natrium metabisulfit, serta natrium benzoat ketika penyadapan dan pengolahan nira. Penggunaan zat aditif seperti ini di satu sisi dapat mengawetkan nira tetapi disisi lain mendatangkan masalah baru dimana para penderes menggunakan zat aditif tersebut secara berlebihan sehingga dapat menurunkan kualitas gula merah. Efek yang paling umum terjadi akibat penggunaan pengawet secara berlebihan adalah timbulnya rasa (after taste) yang tidak enak. Efek lain penggunaan zat aditif seperti sulfit yang berasal dari zat aditif makanan dapat mengakibatkan serangan asma, rasa panas dan gangguan pada daerah abdomen (perut). Hal ini tentu akan menjadi hambatan dalam pemasaran gula merah sebagai komoditi ekspor.
1.2. Perumusan Masalah
penyadapan. Penurunan pH nira akibat fermentasi akan menghambat proses pengkristalan sukrosa sehingga gula yang dihasilkan tidak padat. Nira yang disadap tanpa disertai upaya pengawetan memiliki pH dibawah 5. Proses pengkristalan sukrosa agar menghasilkan gula yang padat harus dilakukan pada pH diatas 5,5. Penambahan pengawet sintetis seperti asam dan garam benzoat serta senyawa golongan sulfit yang biasa digunakan penderes mengakibatkan gula yang dihasilkan ditolak oleh konsumen khususnya konsumen luar negeri. Penambahan kapur untuk menetralkan keasaman nira yang sudah terlanjur asam mengakibatkan perubahan rasa pada gula yang dihasilkan. Oleh karena itu perlu dilakukan suatu langkah pengawetan guna mencegah penurunan pH dengan menghambat pertumbuhan mikroorganisme yang mengkontaminasi nira selama penyadapan menggunaan pengawet yang lebih efektif dan aman.
Pengasapan merupakan metode tradisional yang digunakan oleh petani penderes untuk membantu membunuh mikroorganisme pada peralatan penyadapan nira (lodong). Pengasapan tradisional ini belum dapat mengatasi masalah fermentasi nira karena prosesnya tidak terkontrol dan efek antimikroba yang didapatkan tidak seragam. Penggunaan asap cair secara langsung belum pernah dilakukan. Asap cair merupakan hasil kondensasi asap yang tidak mengandung zat karsinogenik dan memiliki aktivitas antimikroba, serta terbukti sebagai ingredient yang aman. Penggunaan asap cair diharapkan dapat menjadi pengawet alternatif nira yang aman dan lebih terkontrol proses penggunaannya.
1.3. Tujuan
nira, dan (3) Menentukan konsentrasi asap cair untuk aplikasi dalam penyadapan nira yang mampu mempertahankan kesegaran nira (pH = 6 – 7) selama penyadapan (12 jam).
1.4. Manfaat penelitian
II TINJAUAN PUSTAKA
2.1. Gula Merah
Gula merah atau gula palma merupakan produk olahan yang diperoleh
dari pengolahan nira segar tumbuhan palma. Agroindustri usaha gula merah
umumnya terdapat di pedesaan pada skala rumah tangga dengan tingkat
permodalan yang kecil tetapi berkontribusi besar dalam memberikan
tambahan pendapatan bagi rumah tangga pengrajin. Gula merah diproduksi
dalam skala rumah tangga dengan jumlah unit produksi sebanyak 147.362 unit
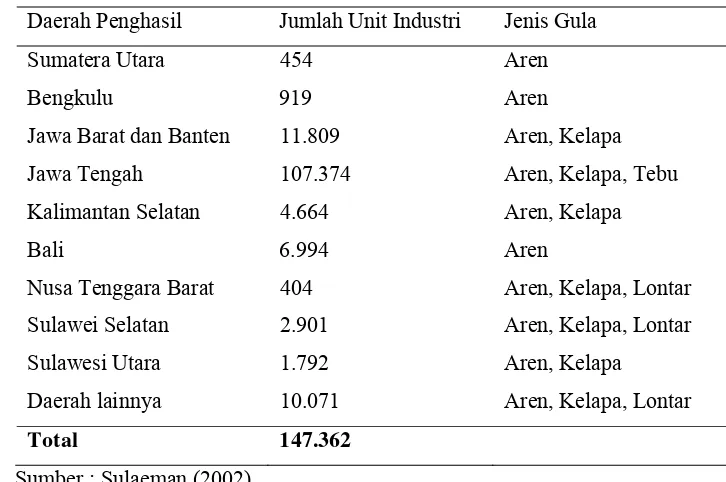
(Sulaeman, 2002). Populasi industri gula merah di Indonesia dapat dilihat
pada Tabel 1.
Tabel 1 Populai Industri Gula Merah di Indonesia Tahun 2001
Daerah Penghasil Jumlah Unit Industri Jenis Gula
Sumatera Utara 454 Aren
Bengkulu 919 Aren
Jawa Barat dan Banten 11.809 Aren, Kelapa
Jawa Tengah 107.374 Aren, Kelapa, Tebu
Kalimantan Selatan 4.664 Aren, Kelapa
Bali 6.994 Aren
Nusa Tenggara Barat 404 Aren, Kelapa, Lontar
Sulawei Selatan 2.901 Aren, Kelapa, Lontar
Sulawesi Utara 1.792 Aren, Kelapa
Daerah lainnya 10.071 Aren, Kelapa, Lontar
Total 147.362
Sumber : Sulaeman (2002)
Hasil penelusuran mengenai perkembangan industri gula merah dari
media massa menunjukkan bahwa pengembangan industri gula aren mulai
dilakukan lagi pada tahun 2006 terutama di Sulawesi Utara, Sumatera Utara,
Jawa Barat, Jawa Timur, Pulau Muna di Sulawesi Tenggara, Kalimantan
Barat, dan Kalimantan Timur (Tempointeraktif, 2006). Pada tanggal 14
Januari 2007 dilakukan ekspor perdana gula aren sebanyak 12,5 ton dari
Korbidkesra, 2007). Hal ini menunjukkan bahwa gula merah memiliki pasar
yang luas, tidak hanya dalam negeri tetapi juga luar negeri (ekspor).
Gula merah memiliki perbedaan sifat fungsional dengan gula putih
(tebu) terutama pada rasa manis, warna, aroma, dan keempukan. Karena
kekhasan yang dimilikinya, gula merah banyak digunakan sebagai ingredient
(bahan tambahan pangan) dalam berbagai jenis makanan dan minuman
tradisional. Gula merah dibedakan berdasarkan asal niranya. Gula kelapa, gula
aren, dan gula nipah masing-masing secara berturut-turut berasal dari nira
kelapa, nira aren, dan nira nipah. Soekarto et al. (1991) menjelaskan bahwa penggunaan gula merah di industri pangan (kecap, dodol, dan tauco) lebih
banyak menggunakan gula kelapa dan gula aren.
Penelitian sensoris yang dilakukan oleh Apriyantono dan Wiratma
(1997) memberi kesimpulan bahwa penggunaan gula merah (gula kelapa dan
gula aren) sebagai ingredient pada kecap manis lebih disukai dari pada gula putih. Hal ini disebabkan karena gula merah memiliki kandungan flavor khas
dengan komposisi tertentu asam-asam organik yang dapat memberikan rasa
disukai secara sensori.
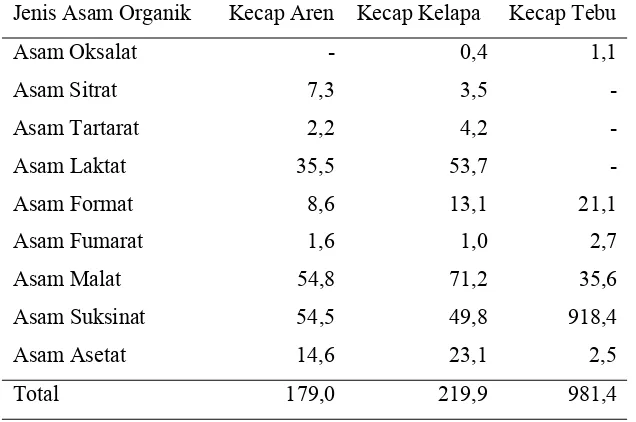
Tabel 2 Komposisi Asam Organik yang terdapat pada Kecap (mg/100g)
Jenis Asam Organik Kecap Aren Kecap Kelapa Kecap Tebu
Asam Oksalat - 0,4 1,1
Asam Suksinat 54,5 49,8 918,4
Asam Asetat 14,6 23,1 2,5
Total 179,0 219,9 981,4
Sumber : Apriyantono dan Wiratma (1997)
diperkuat oleh hasil penelitian Nurhayati (1996) yang menyimpulkan bahwa
hampir semua komponen volatil yang terdeteksi pada gula merah juga
terdeteksi pada kecap manis yang ingredientnya adalah gula merah (Tabel 3).
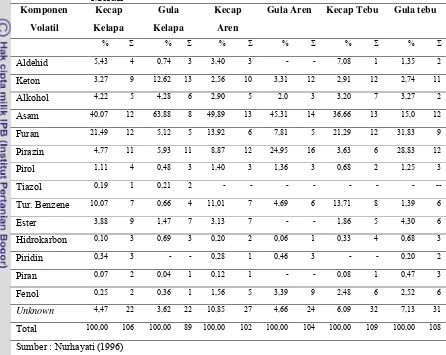
Tabel 3. Jenis dan Persentase Area Komponen Volatile Kecap Manis dan Gula Merah
Total 100,00 106 100,00 89 100,00 102 100,00 104 100,00 109 100,00 108
Sumber : Nurhayati (1996)
Keunggulan lain yang dimiliki gula merah ditunjukkan dengan hasil
penelitian yang dilakukan oleh Philippine Food and Nutrition Research Institute (PFNRI) (2009) mengenai indeks glisemik gula merah. Indeks glisemik (IG) merupakan angka yang menunjukkan tingkatan pangan
berdasarkan besarnya efek (immediate effect) pengaruh konsumsi suatu jenis makanan terhadap kadar gula darah. Dengan mengetahui nilai IG suatu
makanan, penderita diabetes khususnya dapat melakukan pemilihan makanan
sendiri sehingga kadar gula darah dapat dikontrol. Makanan dengan nilai IG
didalamnya dapat dengan cepat diubah menjadi gula sederhana (glukosa) yang
menyebabkan kenaikan gula darah secara cepat. Kategori bahan pangan
berdasarkan nilai IG dapat dilihat pada Tabel 4.
Tabel 4 Kategori Pangan Berdasarkan Indeks Glisemik
Kategori Pangan Rentang Indeks Glisemik*
IG Rendah < 55
IG Sedang (intermediate) 56 – 69
IG Tinggi >70
*Pangan acuan yang digunakan adalah glukosa
Sumber : Miller et al. (1996)
Miller (1996) diacu dalam Rimbawan dan Siagian (2004)
menjelaskan bahwa gula pasir (sukrosa) memiliki IG sedang yaitu 65.
Fruktosa murni memiliki IG sebesar 23 (rendah) karena untuk menjadi gula
darah harus diubah dahulu dalam hati menjadi glukosa sehingga respon
kenaikan gula darah pasca konsumsi fruktosa terjadi lebih lambat. Bahan
pangan yang mengandung sukrosa tinggi ternyata memiliki IG mendekati nilai
60, lebih rendah dari IG sukrosa sendiri. Begitupun dengan madu yang terdiri
dari beragam jenis gula, memiliki IG 58. Namun beberapa jenis madu yang
telah dicampur sirup glukosa memiliki IG sangat tinggi yaitu 87. Hal ini
menunjukkan bahwa pengaruh komposisi gula (yang secara alami terdapat
didalam pangan seperti laktosa, sukrosa, glukosa, dan fruktosa dalam berbagai
proporsi) terhadap respon gula darah sangat sulit diprediksi.
Hasil penelitian PNFRI (2009) menunjukkan bahwa gula merah dari
nira kelapa (gula kelapa) memiliki indeks glisemik (IG) sebesar 35 sehingga
gula merah ini digolongkan sebagai bahan pangan dengan IG rendah.
Makanan dengan IG rendah dinilai lebih aman untuk dikonsumsi karena tidak
menyebabkan kadar gula darah meningkat tajam setelah dikonsumsi terutama
bagi para penderita diabetes.
Gula merah yang berkualitas diperoleh dari nira yang masih terjaga
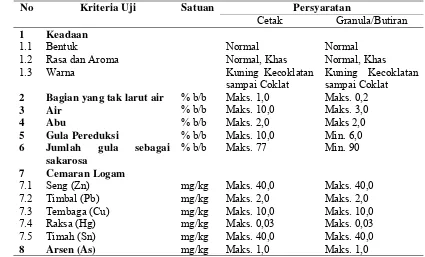
kesegarannya. Kualitas gula merah menurut Standar Nasional Indonesia
Tabel 5 Syarat Mutu Gula Palma berdasarkan SNI 01-3743-1995
Persyaratan
No Kriteria Uji Satuan
Cetak Granula/Butiran 1 Keadaan
1.1 Bentuk Normal Normal 1.2 Rasa dan Aroma Normal, Khas Normal, Khas 1.3 Warna Kuning Kecoklatan
sampai Coklat 6 Jumlah gula sebagai
sakarosa
Sumber : Dewan Standardisasi Nasional (1995)
2.2. Nira
Nira adalah cairan mengandung gula yang diperoleh dari tanaman
tertentu seperti tebu dan tanaman palma. Nira tebu diperoleh dengan
melakukan pemerasan batang tebu, sedangkan nira dari tanaman palma
diperoleh dengan melakukan penyadapan. Tanaman palma yang umum
disadap niranya adalah kelapa, aren, dan lontar. Cairan yang mengandung gula
ini mempunyai pH netral sekitar 7 pada saat keluar dari mayang dengan kadar
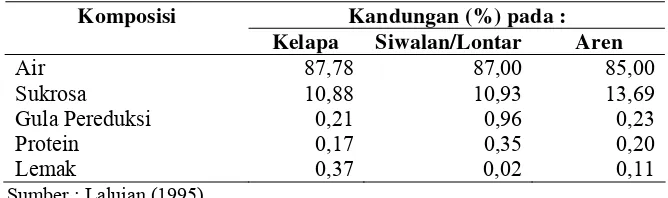
air sekitar 80-85% (Lalujan, 1995). Komposisi nira dari berbagai jenis
tanaman palma disajikan pada Tabel 6.
Komposisi nira pada berbagai jenis tanaman palma tidak begitu
berbeda jauh. Semua komponen tersebut merupakan faktor-faktor yang
menentukan karakter dari produk olahan yang dihasilkan. Walaupun
demikian, perbedaan kandungan komponen organik mikro seperti asam
organik, gula perduksi, jumlah protein, serta kondisi nira ketika akan diolah
dan penggunaan zat aditif pada akhirnya akan membedakan karakteristik gula
Tabel 6 Komposisi Nira dari Berbagai Tanaman Palma
Gula Pereduksi 0,21 0,96 0,23
Protein 0,17 0,35 0,20
Lemak 0,37 0,02 0,11
Sumber : Lalujan (1995)
Putra (1990) dan Apriyantono et al. (2003) menyatakan bahwa komponen pada nira yang menjadi reaktan proses pencoklatan pada
pembuatan gula merah adalah gula dan protein. Komponen gula yang
berpengaruh pada pembentukan warna coklat dalam pembuatan gula merah
adalah glukosa dan fruktosa (sebagai gula perduksi) dan reaksi Maillard
memegang peranan penting dalam pembentukan warna coklat dari gula merah.
Kemampuan nira untuk mengeras (mengkristal) ditentukan oleh kandungan
sukrosa dan keasaman nira. Penggunaan kapur untuk menetralkan nira yang
telah sedikit asam akan menyebabkan warna gula menjadi lebih gelap,
sebaliknya penggunaan senyawa sulfit sebagai pengawet akan meningkatkan
kecerahan warna gula merah karena sulfit menghambat terjadinya reaksi
pencoklatan.
2.3. Penyadapan Nira dan Sumber-Sumber Kontaminasi Nira
Penyadapan nira dilakukan dua kali sehari, yaitu pada pagi hari dan
sore hari. Nira hasil penyadapan yang dimulai pada pagi hari dikumpulkan
pada sore harinya, sedangkan yang disadap pada sore hari dikumpulkan pada
pagi hari berikutnya. Proses penyadapan nira diawali dengan mempersiapkan
lodong (wadah penmpung nira). Pembersihan lodong yang biasa dilakukan
yaitu dengan membasuh lodong menggunakan air dingin, kemudian dibasuh
dengan air panas sesaat sebelum lodong dibawa menuju tempat penyadapan.
Pembersihan lodong juga dilakukan dengan pengasapan selama sepuluh menit
menggunakan suatu alat khusus (pemuput). Penggunaan lodong saat ini mulai
digantikan dengan ember plastik karena lebih praktis.
Lodong merupakan salah satu sumber kontaminasi silang terhadap
lodong dengan menggunakan air panas dan pengasapan pada bumbung yang
masih baru tidak berbeda nyata pengaruhnya terhadap pH, kadar sukrosa, dan
kadar gula pereduksi dari nira aren. Lodong yang telah digunakan
berulang-ulang tidak cukup hanya dibasuh dengan air karena bumbung yang telah lama
biasanya memiliki retakan-retakan yang sangat mungkin untuk ditumbuhi
berbagai jenis mikroorganisme perusak nira dan tidak terbersihkan sewaktu
dilakukan pencucian. Oleh karena itu bumbung sering juga disucihamakan
dengan menggunakan kaporit atau dengan asap belerang (BBIHP, 1984; diacu
dalam Iskandar, 1991).
Bakteri asam laktat, khamir, serta mikroorganisme lainnya dapat
mengkontaminasi nira jika lodong yang digunakan dalam penyadapan nira
tidak bersih. BAL diduga kuat merupakan mikroba awal yang menyebabkan
kerusakan nira. Bakteri asam laktat adalah kelompok bakteri yang dicirikan
dengan hasil metabolisme terhadap karbohidrat yang membentuk asam laktat
(sebagai produk utama) yang berdampak pada penurunan pH nira. BAL
merupakan bakteri pembusuk berbentuk basil golongan gram positif
sedangkan P.aeruginosa merupakan bakteri pembusuk berbentuk basil, termasuk dalam golongan bakteri gram negatif yang sering menimbulkan
kerusakan pada berbagai jenis makanan (Fardiaz, 1992). .
Pengasapan yang dilakukan oleh petani penderes dilakukan dengan
dua cara. Cara pertama dengan memanfaatkan asap pada saat pembuatan gula.
Ketika proses pembuatan gula dilakukan, lodong diletakkan diatas perapian
sehingga asap pembakaran melingkupinya. Proses pengasapan lainnya adalah
dengan menggunakan alat khusus yang disebut pemuput atau alat untuk
memuput (mengasapi). Proses pemuputan dilakukan kurang lebih sepuluh
menit.
Gambar 1 menunjukkan proses pengasapan yang sedang dilakukan
oleh penderes sebelum lodong digunakan untuk menyadap. Asap yang
digunakan pada proses pengasapan berasal dari pembakaran berbagai macam
kayu. Dengan demikian, proses pengasapan yang dilakukan secara tradisional
ini tidak terkontrol dan setiap kali proses ini dilakukan efek antimikroba yang
LODONG
PEMUPUT
Gambar 1 Proses Pengasapan Lodong menggunakan Pemuput.
Setelah proses pembersihan dan pengasapan lodong selesai,
selanjutnya dilakukan penyadapan. Petani menggunakan sigay, sejenis tangga dari sebatang bambu, untuk mencapai posisi tandan yang terdapat dibagian
atas pohon aren. Panjang sigay mencapai 15 sampai 20 meter. Penyadapan pertama kali dilakukan dengan memotong tandan bunga atau mayang. Untuk
mengawali proses penyadapan berikutnya dilakukan dengan menyayat
permukaan mayang yang telah dipotong. Penyayatan yang dilakukan setiap
kali akan menyadap mengakibatkan panjang mayang mengalami pengurangan
sampai akhirnya tidak dapat disadap lagi.
Purnomo (1997) menjelaskan bahwa pemotongan atau pengirisan
ujung mayang dilakukan untuk mempermudah proses keluarnya nira. Jika
tidak dilakukan pengirisan, ujung mayang akan mengalami kebusukan dan
pori-pori mayang tetutup sehingga nira yang dihasilkan jumlahnya sedikit dan
terkontaminasi mikroba yang sudah tumbuh lama pada ujung mayang.
Purnomo (1997) juga menjelaskan bahwa pada penyadapan nira kelapa yang
baik, pengirisan batang mayang dilakukan ketika ujung mayang yang telah
dipotong sebelumnya mengalami kebusukan. Tebal irisan tidak boleh terlalu
tipis dan juga tidak boleh terlalu tebal. Pengirisan yang baik adalah pada
permukaan mayang yang layu saja. Jika terlalu tebal akan merugikan petani
menyisakan bagian mayang yang layu dan telah terkontaminasi
mikroorganisme.
Gambar 2 memperlihatkan proses penyadapan nira oleh penderes.
Pada penyayatan mayang aren, pemotongan dan penyayatan mayang
dilakukan dengan menggunakan golok yang tajam. Penyayatan mayang
dilakukan dengan teknik khusus sehingga tetesan nira tepat masuk kedalam
wadah penampung. Setelah penyayatan dilakukan, wadah penampung yang
telah disiapkan dipasang dengan cara dikaitkan pada mayang sedemikian rupa
sehingga tetesan nira dapat tertampung. Setelah wadah penampung dipasang,
dilakukan penutupan dengan menggunakan penutup yang dibuat dari kulit
pohon, kain atau plastik.
A B
Gambar 2 Proses Penyadapan Nira : (A) Penyayatan Ujung Mayang dan (B) Pemasangan Penampung Nira dan Penutupnya.
Pisau atau golok yang digunakan sebagai alat pengiris biasanya
diasah menggunakan batu asah dan air terlebih dahulu. Golok dengan kondisi
tidak bersih ini merupakan sumber kontaminasi terhadap nira yang disadap.
Kondisi penampung yang terbuka merupakan sumber kontaminasi yang lain
dimana dari udara bebas akan masuk kontaminan. Penutupan wadah
penampung bertujuan untuk melindungi nira agar tidak terkena panas matahari
langsung dan tidak terkena air hujan. Tetapi penutupan yang dilakukan tidak
dapat menghindarkan nira dari jangkauan serangga seperti lebah, lalat, dan
semut. Serangga-serangga ini merupakan agen sumber kontaminasi karena
pada permukaan tubuhnya membawa mikroorganisme yang bisa
Nira segar yang keluar dari tandan dan belum mengalami fermentasi
mempunyai pH netral dengan kadar air sekitar 80-85% (Lalujan, 1995). Nira
yang dihasilkan dari pohon aren dapat mencapai lima liter dari satu mayang
untuk sekali penyadapan. Nira yang dihasilkan dari pohon kelapa volumenya
lebih sedikit dalam satu kali penyadapan yaitu berkisar antara 1 sampai 1,5
liter (Purnomo, 1997). Hal inilah yang menyebabkan mengapa lodong yang
digunakan untuk menampung nira aren berbentuk lebih besar dan lebih
panjang dibandingkan dengan lodong untuk menampung nira kelapa yang
betuknya lenih kecil dan lebih pendek. Volume nira yang dihasilkan semakin
berkurang sampai akhirnya tidak ada lagi nira yang menetes dari mayang.
Selain karena pengirisan mayang yang dilakukan setiap hari, berkurangnya
volume nira juga dipengaruhi oleh musim. Pada musim kemarau, nira yang
dihasilkan lebih sedikit sedangkan pada musim hujan sebaliknya, nira yang
dihasilkan lebih banyak.
Proses penyadapan nira yang sepenuhnya dilakukan secara manual
oleh penderes memungkinkan terjadinya kontaminasi silang. Staphylococcus aureus merupakan salah satu bakteri patogen yang keberadaannya berhubungan dengan higiene dari manusia yang mengelola bahan pangan
(Sunen, 1998). S.aureus merupakan bakteri gram positif berbentuk kokus yang tumbuh secara optimum pada suhu 350-370 C dengan pH 7,0 – 7,8. Kondisi
higiene penderes yang kurang baik merupakan suatu peluang bagi S.aureus
untuk tumbuh dengan baik pada nira.
2.4. Mikrobiologi Nira
Pengolahan cairan bergula alami seperti nira umumnya dilakukan
masyarakat Asia, Afrika, dan Amerika Latin. Penelitian-penelitian yang
berkembang tentang nira umumnya dihubungkan dengan proses pengolahan
fermentatif nira menjadi minuman beralkohol dan asam asetat. Hal inilah yang
menyebabkan reaksi perubahan psikokimia seperti perubahan pH, kadar gula,
total asam, dan kadar alkohol yang terjadi pada nira diidentikkan dengan hasil
Perubahan sifat nira akibat fermentasi mulai tampak satu sampai dua
jam setelah dikumpulkan. Perubahan yang terjadi berupa penuruan pH dan
peningkatan kadar alkohol. Organisme yang bertanggung jawab dalam
perubahan nira adalah S.cerevisiae dan Schizosaccharomyces pombe dari golongan khamir dan Lactobacillus plantarum serta Leuconostoc mesenteroides dari golongan bakteri. Jika fermentasi dibiarkan terus lebih dari 96 jam maka nira akan berubah menjadi cuka (vinegar). Selama 24 jam
penyimpanan, pH nira akan berubah dari 7,4-6,8 menjadi 5,5 dan kandungan
alkohol juga meningkat menjadi 1,5-2,1%. Selama 72 jam, kadar alkohol
dapat mencapai 4,5%-5,2% dan pH 4,0. Senyawa asam organik yang biasanya
terdapat pada nira asam ini adalah asam laktat, asam asetat, dan asam tartarat
(Battcock dan Azam-Ali, 1998).
Fermentasi yang terjadi pada pembuatan minuman dari sari buah
anggur juga tidak jauh berbeda. Fermentasi yang terjadi dapat bersifat spontan
dengan menggunakan khamir yang berada pada kulit anggur atau
menggunakan kultur starter berupa S.cerevisiae. Penggunaan khamir yang terdapat secara alami pada kulit buah anggur menyebabkan hasil akhir
fermentasi tidak terkontrol. Fermentasi akan terhenti secara alami ketika gula
yang dapat difermentasi telah habis atau ketika kadar alkohol mencapai kadar
limit toleransi bagi pertumbuhan khamir. Penghentian proses fermentasi juga
dapat dilakukan secara teknis dengan menambahkan alkohol atau dengan
sentrifugasi dan filtrasi steril (Battcock dan Azam-Ali, 1998).
Sumanti et al. (2004) dan Okrafor (1978) menyatakan fermentasi spontan yang terjadi pada nira adalah fermentasi laktat-alkohol-asetat yang
melibatkan bakteri asam laktat, khamir, dan bakteri asam asetat. Bakteri
Leuconostoc spp dan Lactobacillus spp merupakan mikroorganisme awal yang diduga dominan terdapat dalam nira segar. Saccharomyces cereviceae adalah khamir yang biasa melakukan fermentasi alkohol. Bakteri asam laktat dan
khamir bekerja secara bersama dalam proses fermentasi nira. Mikroorganisme
terakhir yang berperan adalah bakteri pembentuk asam asetat, antara lain
James dan Chen (1985) menyatakan bahwa nira memiliki kandungan
gula yang tidak cukup untuk menghambat pertumbuhan mikroorganisme,
bahkan merupakan media yang baik untuk petumbuhan mikroorganisme jika
nira dibiarkan beberapa waktu. Cahyaningsih (2006) melakukan isolasi
mikroorganisme pada beberapa waktu fermentasi (Tabel 7). Berdasarkan data
ini maka dapat dinyatakan bahwa BAL merupakan mikroorganisme awal yang
bertanggung jawab dalam fermentasi awal nira.
Tabel 7. Isolat Mikroorganisme dari Nira Lontar pada Berbagai Waktu Fermetasi
Bakteri asam laktat yang berhasil diisolasi oleh Cahyaningsih (2006)
diidentifikasi sebagai Lactobacillus plantarum dan Leuconostoc mesenteroides. Kehadiran BAL didalam fermentasi nira berlangsung selama 24 jam. Setelah itu mikroorganisme yang tetap bertahan adalah khamir dan
Bacillus.
Kehadiran BAL dalam proses fermentasi nira dan pengolahan sari
anggur menjadi minuman beralkohol sangat tidak diharapkan karena hasil
metabolisme BAL akan menyebabkan produk yang dihasilkan berasa asam.
Kerusakan produk akhir pada minuman beralkohol juga disebabkan oleh
kehadiran bakteri pembentuk asam asetat yang mengoksidasi alkohol menjadi
asam asetat sehingga minuman beralkohol tersebut memiliki bau yang
menyimpang dan rasa yang asam. Oleh karena itulah maka dalam tahap awal
pembuatan minuman anggur beralkohol pada skala industri dilakukan
penambahan potassium metabisulfit untuk mencegah pertumbuhan
2.5. Bakteri Asam Laktat (BAL) dan Fermentasi Nira
Penelitian Cahyaningsih (2006) mendukung pernyataan Okrafor
(1978) dan Sumanti et al. (2004). Berdasarkan hasil penelitiannya, BAL diduga kuat merupakan mikroba awal yang menyebabkan fermentasi nira.
Bakteri asam laktat adalah kelompok bakteri yang dicirikan dengan hasil
metabolisme terhadap karbohidrat yang membentuk asam laktat (sebagai
produk utama). Produksi asam oleh BAL sangat cepat sehingga dapat
menghambat pertumbuhan mikroorganisme lain. Bakteri asam laktat
merupakan bakteri gram positif, tidak membentuk spora, berbentuk bulat,
katalase dan oksidase negatif, non motil atau sedikit motil, mikroaerofilik
sampai anaerob, toleran terhadap asam, kemoorganotrofik, dan mesofilik
(Salminen et al. 2004; Stamer, 1979).
Jenis bakteri yang termasuk kedalam BAL adalah family
Lactobacilliceae yaitu Lactobacillus, serta family Streptoceae yaitu
Leuconostoc, Streptococus, dan Pediococus (Fardiaz, 1992). Nettless dan Brefort (1993) menyatakan genus BAL antara lain Lactococcus, Pediococcus, Leuconostoc, Lactobacillus dan Carnobacterium.
Bakteri asam laktat dibagi menjadi dua kelompok berdasarkan
kemampuannya memetabolisme karbohidrat dan produk akhir yang
dihasilkan, yaitu BAL homofermentatif dan heterofermentatif. Bakteri asam
laktat homofermentatif memfermentasi glukosa menjadi asam laktat. Bakteri
asam laktat heterofermentatif memetabolisme glukosa menjadi asam laktat,
asam asetat, etanol, dan CO2 (Sharpe, 1979). Salminen et al. (2004) juga menerangkan bahwa BAL homofermentatif memetabolisme gula melalui jalur
Embden-Meyerhoff-Parnass menghasilkan produk utama berupa asam laktat,
sedangkan BAL heterofermentatif memetabolisme gula melalui jalur
fosfoketolase menjadi asam laktat dan produk organik lainnya seperti alkohol,
asam asetat, asam lemak bebas, asam format, amonia, diasetil, asetonin, dan
CO2. Umumnya BAL bekerja pada kondisi mikroaerofilik dan anaerobic
(Ayres et al. 1980).
Battcock dan Azam-Ali (1998) menjelaskan metabolisme BAL
C6H12O6 2 CH3CHOHCOOH
Glukosa Asam Laktat
Sedangkan pada BAL heterofermentatif berlangsung dengan reaksi kimia
sebagai berikut :
C6H12O6 CH3CHOHCOOH+ C2H5OH+ CO2
Glukosa Asam Laktat Etanol Karbondioksida
Goutara dan Wijandi (1985) menjelaskan kerusakan nira akibat
aktivitas mikroorganisme ditandai dengan rasa asam pada nira, berbuih putih,
dan berlendir. Perlengkapan menyadap yang kurang bersih, kondisi
penyadapan yang terbuka, kebersihan tangan penderes serta waktu
penyadapan yang cukup lama merupakan faktor-faktor yang menyebabkan
nira terkontaminasi oleh mikroorganisme.Rasa asam yang timbul pada awal
kerusakan nira merupakan efek dari asam laktat yang dihasilkan oleh BAL.
Proses fermentasi selanjutnya dilakukan oleh BAL dan khamir secara
bersama-sama menghasilkan asam laktat, etanol dan terbentuknya gas CO2
yang diindikasikan dengan terbentuknya buih pada nira. Kekeruhan dan
penampakan pada nira yang lebih kental dan berlendir disebabkan oleh kerja
Saccharomyces spp. Keruskan nira diakhiri dengan terbentuknya asam asetat dari proses oksidasi etanol oleh bakteri asam asetat. Reaksi yang umum terjadi
pada proses fermentasi adalah sebagai berikut:
C6H12O6 Æ 2 C2H5OH + 2 CO2
Glukosa / Fruktosa Khamir Etanol Karbondioksida
C2H5OH + O2 Æ CH3COOH + H2O
Etanol Bakteri asam asetat Asam Asetat Air
Turunnya pH akibat asam laktat meningkatkan laju pertumbuhan dan
metabolisme BAL, menekan aktivitas bakteri tidak tahan asam, serta
meningkatkan laju degradasi sukrosa menjadi glukosa dan fruktosa. Glukosa
dan fruktosa yang terbentuk meningkatkan laju pertumbuhan dan metabolisme
pertumbuhan BAL dan khamir itu sendiri. Etanol selanjutnya dioksidasi oleh
bakteri asam asetat menjadi cuka.
2.6. Derajat Keasaman (pH) Nira dalam Pembuatan Gula Merah
Faktor utama yang menjadi kunci dalam pengolahan nira menjadi
gula padat adalah derajat keasaman nira. Nira yang baik untuk menjadi gula
merah adalah nira yang memiliki pH diatas 6. Jackson (1995) mengungkapkan
bahwa sukrosa dapat mengkristal dengan baik pada kondisi pH diatas 5,5.
Pada kondisi ini, reaksi degradasi sukrosa menjadi glukosa dan fruktosa
sangat sedikit sekali terjadi. pH nira akan dengan cepat mengalami penurunan
karena adanya fermentasi oleh mikroorganisme yang mengkontaminasinya.
Sukrosa akan mengalami degradasi akibat lingkungan yang asam,
panas, dan mineral tertentu melalui reaksi hidrolisis. Reaksi hidrolisis (reaksi
inversi) sukrosa dapat terjadi secara spontan pada kondisi asam (Wang, 2004).
Sebagai contoh, sirup sukrosa dengan pH 3,2 yang disimpan pada suhu 200C
selama tiga bulan akan mengalami inversi glukosa sebesar 10% dan hanya
0,1% pada pH 5,5 (Jackson, 1995). Banyaknya ion H+ pada kondisi asam
menyebabkan sukrosa mengalami inversi menjadi fruktosa dan glukosa.
Reaksi yang terjadi adalah sebagai berikut :
C12H22O11+ H2O + H+ Æ C6H12O6 + C6H12O6+ H+ (sukrosa) air ion (fruktosa) (glukosa)
Reaksi hidrolisis ini dipercepat dengan adanya pemanasan, dikatalisis oleh
enzim invertase, serta kehadiran mineral tertentu seperti mineral pada garam.
Reaksi ini bersifat endotermik dan irreversible dengan energi aktivasi 25,9 kkal/mol. Jackson (1995) menjelaskan bahwa pada pH diatas 5,5 hanya terjadi
sedikit inversi sukrosa. Jika dilakukan pemanasan pada nira yang memiliki
pH 4 – 3,5 atau lebih rendah maka sukrosa yang terdegradasi bisa mencapai
50%.
Tingginya kadar keasaman (nilai pH rendah) serta kadar glukosa dan
fruktosa dalam nira akan menghambat terjadinya proses pengkristalan sukrosa
Glukosa dan fruktosa sebagai hasil reaksi inversi memiliki kelarutan yang
sangat tinggi dalam air sehingga sulit untuk dikristalkan bahkan menghambat
proses kristalisasi (Winarno, 1992).
Laos et al. (2007) melakukan suatu simulasi kristalisasi supersaturasi sukrosa dengan kehadiran fruktosa dan glukosa. Secara umum, kehadiran
kedua gula pereduksi tersebut akan memperlambat proses kristalisasi. Agar
dapat terbentuk kristal, rasio minimal antara sukrosa dan glukosa adalah
80:20, sedangkan untuk rasio sukrosa dan fruktosa adalah 90:10. Hal ini
menunjukkan bahwa proses kristalisasi gula lebih dipengaruhi oleh kehadiran
fruktosa. Konsentrasi 10% fruktosa akan menghambat proses kristalisasi
sukrosa. Pada pengolahan gula merah, hal ini diindikasikan dengan hasil akhir
yang tidak bisa memadat.
2.7. Upaya-Upaya Pengawetan Nira
Penurunan pH nira akibat fermentasi menyebabkan kadar sukrosa
menurun dan kandungan gula pereduksi meningkat. Perubahan psikokimia
akibat fermentasi pada akhirnya mempengaruhi mutu gula yang dihasilkan.
Nira yang telah asam karena fermentasi tidak dapat diolah menjadi gula merah
yang padat. Hal ini mendorong petani penderes melakukan berbagai upaya
pengawetan untuk menjaga mutu nira agar tetap terjaga kesegarannya. Selain
pengawetan secara tidak langsung dengan mengasapi lodong, petani penderes
juga melakukan upaya pengawetan yang sifatnya tradisional.
Pengawetan tradisional yang dilakukan diantaranya dengan
menambahkan potongan atau irisan kulit batang kayu manggis, kayu ralu,
kayu kesambi, akar kawao, kulit buah manggis muda, daun manggis, dan
sebagainya. Penggunaan pengawet tradisional ini belum efektif karena setelah
penyadapan, petani penderes biasa menambahkan air kapur untuk menetralkan
nira yang sudah sedikit asam. Penambahan bahan tambahan ini akan
menurunkan kualitas gula merah.
Penelitian mengenai pengawetan nira telah banyak dilakukan.
Kusumah (1992) dan Mansyur (1992) menggunakan natrium metabisulfit dan
kapur. Penggunaan natrium metabisulfit dengan konsentrasi 70 sampai 100
nipah. Widyaningsih et al. (1985) menggunakan natrium metabisulfit, kapur, dan toluene masing-masing sebanyak 0,10% sebagai pengawet. Natrium meta
bisulfit efektif digunakan dalam pengawetan nira dan mampu menghambat
reaksi pencoklatan. Penggunaan kapur lebih berpengaruh pada warna gula
merah dimana warna gula yang dihasilkan menjadi lebih gelap. Penggunaan
toluene efektif untuk pengawetan nira, namun hasil gula merah yang
dihasilkan kurang baik dimana warna gula tidak sebaik gula yang diawetkan
dengan natrium metabisulfit.
Yasni et al. (1999) mengkaji penggunaan ekstrak kayu ralu. Kayu ralu yang dapat digunakan untuk mengawetkan nira adalah 10 gram serbuk
kayu untuk 2-3 liter nira aren. Ekstrak kayu ralu yang paling berpotensi untuk
digunakan sebagai pengawet nira adalah ekstrak polar pertengahan dengan
konsentrasi 300 ppm dan diduga mengandung senyawa fenol dan terpenoid.
Hamzah dan Hasbullah (1997) menggunakan pengawet alami untuk
pengawetan nira aren. Pengawet yang digunakan berupa kulit buah manggis
muda (3 g/l nira), kulit pohon rupih (3g/l nira), kulit pohon nangka (4g/l nira),
dan daun manggis (4g/l nira). Pemberian pengawet alami ini mampu
menghasilkan nira dengan pH 5,82 sampai 6,25 dan menghasilkan gula yang
memenuhi standar mutu gula semut (SII No. 2043 – 87). Penggunaan kulit
manggis muda memberikan hasil yang terbaik dalam menjaga pH, kadar gula
pereduksi, dan mutu gula akhir.
Sunantyo (1997) menggunakan pengawet tatal kayu nangka (10g/l
nira) ditambah susu kapur (10 ml 50Be/l nira) untuk menggantikan
penggunaan SO2 pada pengawetan nira kelapa pada pembuatan gula semut.
Azima (1997) melakukan pengawetan nira nipah dengan menggunakan kapur
sebanyak 0,5 – 1,5g/l nira selama pengumpulan dan menunggu proses
pengolahan. Penggunaan kapur dalam penelitian ini ditujukan untuk
menetralisir nira yang telah asam. Hasil yang terbaik adalah penambahan
kapur sebanyak 1,5g/l nira.
Lalujan (1995) dalam kajian pengawetan nira aren untuk industri
kecil merekomendasikan penggunaan kapur (CaO) sebanyak 300-500 ppm,
Penggunaan kapur lebih dari 800 ppm menghasilkan rasa, warna, dan bau
yang tidak disukai secara sensori.
Hasil penelitian ini telah banyak diadopsi oleh masyarakat termasuk
penggunaan zat aditif. Namun ternyata menjadi bumerang ketika gula merah
yang dihasilkan tertolak dari pasar (terutama ekspor) karena penggunaan zat
aditif yang digunakan dalam penelitian diatas tidak disukai bahkan dihindari
oleh konsumen luar negeri yang lebih memperhatikan aspek kemanan dan
kesehatan. Oleh karena itu perlu dilakukan upaya pengawetan lain yang lebih
efektif dan lebih terjamin dari segi keamanan pangan.
Pengasapan merupakan metode tradisional yang digunakan oleh
petani penderes untuk membantu membunuh mikroorganisme pada peralatan
penyadapan nira (lodong) dan merupakan pengawetan nira secara tidak
langsung. Aliudin (2009) dan Iskandar (1997) menerangkan bahwa kegiatan
pengasapan lodong atau memuput dilakukan oleh penderes untuk mengurangi atau membunuh mikroba. Proses pengasapan dapat juga dilakukan secara
khusus dengan menggunakan alat puputan atau pamuput selama kurang lebih sepuluh menit.
2.8. Aspek Keamanan Pangan dalam Penggunaan Zat Aditif
Penggunaan zat pengawet harus sesuai dengan ketentuan yang
berlaku seperti batas maksimal yang boleh masuk ke dalam tubuh atau
acceptable daily intake (ADI). Setiap zat pengawet telah ditentukan jumlah ADI-nya. CSPI (The Centre of Science in the Public Interest) mengkategorikan zat pengawet menjadi pengawet yang benar-benar aman,
harus diperhatikan jumlahnya agar aman, harus diwaspadai karena belum diuji
keamanannya, harus dihindari orang tertentu, serta kategori harus dihindari
setiap konsumen (Syah et al., 2005).
Natrium benzoat dan asam benzoat merupakan bahan pengawet yang
aman, tetapi jika jumlahnya berlebihan akan berpengaruh pada aftertaste yang menimbulkan gangguan secara sensori. Kelompok sulfit seperti sulfur
dioksida, natrium bisulfit, natrium metabisulfit dan sejenisnya, dikategorikan
sebagai zat pengawet yang harus dihindari oleh orang tertentu. Kelompok
buah kering, anggur (wine), dan kentang olahan. Penggunaan sulfit lebih khusus lagi digunakan sebagai senyawa untuk mencegah terjadinya reaksi
pencoklatan (Syah et al., 2005).
Mahakkapong (2004) merinci pengaruh penggunaan sulfit sebagai
zat aditif dalam gula kelapa di negara Thailand. Sulfit digunakan untuk
pengawet karena memiliki sifat antimikroba dengan cara berinteraksi dengan
membran, berpenetrasi kedalam sel, dan menghambat kerja enzim ATPase dan
bereaksi dengan komponen dalam sitoplasma sehingga terjadi gangguan pada
mikroba yang berakhir dengan kematian sel. Sulfit juga digunakan untuk
mencegah reaksi pencoklatan karena mampu menginhibisi kerja enzim
pencoklatan dan membentuk sulfonat bersama senyawa karbonil intermediet
pada reaksi pencoklatan non enzimatik. Dijelaskan pula bahwa penggunaan
sulfit dapat menyebabkan gangguan bagi orang-orang tertentu. Sulfit dapat
menginduksi terjadinya asma, menyebabkan timbulnya rasa panas dan
gangguan pada bagian abdomen, serta dapat merusak thiamin dalam tubuh.
2.9. Asap Cair
Asap cair merupakan suatu campuran larutan dan dispersi koloid dari
uap asap kayu dalam air yang diperoleh dari hasil pirolisa kayu (Putnam et al.,
1999). Kayu keras dan kayu lunak dapat digunakan sebagai bahan baku
pembuatan asap cair. Asap diperoleh melalui pembakaran kayu keras dan kayu
lunak yang banyak mengandung lignin, selulosa, dan hemiselulosa (Maga,
1988). Jaya et al. (1997) menyebutkan bahwa diantara kayu bakau, kesambi, jati dan tempurung kelapa, kadar lignin tertinggi terdapat pada tempurung
kelapa dan terendah pada kayu bakau. Kadar selulosa tertinggi terdapat pada
kayu jati sedangkan terendah pada tempurung kelapa.
Asap diproduksi melalui proses pirolisis dengan cara pembakaran
yang tidak sempurna yang melibatkan reaksi dekomposisi konstituen polimer
menjadi senyawa organik dengan berat molekul rendah karena pengaruh panas
yang meliputi reaksi oksidasi, dekomposisi, polimerisasi, dan kondensasi
(Girrard, 1992). Reaksi yang terjadi berupa penghilangan air pada suhu 1200-
pada 2000-2500C menghasilkan furfural, furan, serta asam asetat dan
homolognya. Pirolisis selulosa bersama dengan heksosan berlangsung pada
2800-3200C menghasilkan asam asetat dan homolognya. Lignin mengalami
degradasi pada suhu 3000-4000C menghasilkan senyawa fenol, dan eter
fenolik seperti guaiakol (2-metoksifenol) dan homolognya serta turunannya yang berperan dalan menghasilkan flavor asap.
Siskos et al. (2007) mengemukakan bahwa asap cair mengandung beberapa zat antimikroba yaitu asam dan turunannya (format, asetat, butirat,
propionat, dan metil ester), alkohol (metil, etil, propil, alkil, dan isobutil
alkohol), aldehid (formladehid, asetaldehid, furfural, dan metil furfural),
hidrokarbon (silene, kumene, dan simene), keton (aseton, metil etil keton,
metil propil keton, dan etil propil keton), fenol, piridin, dan metil piridin.
2.10. Aktivitas Antimikroba Asap Cair
Pelczar et al. (1988) menyatakan senyawa kimia utama yang memiliki sifat antibakteri adalah fenol dan senyawa fenolat, alkohol, halogen,
logam berat dan persenyawaannya, detrejen, aldehid, dan kemosterilisator gas.
Branen dan Davidson (1993) menjelaskan mekanisme senyawa antibakteri
tersebut dalam menghambat pertumbuhan mikroorganisme ada beberapa cara,
diantaranya :
1) Merusak struktur dinding sel dengan cara menghambat proses
pembentukan atau menyebabkan lisis pada dinding sel yang sudah
terbentuk. Adanya perbedaan struktur dinding sel mikroba menyebabkan
perbedaan resistensi terhadap senyawa antimikroba;
2) Mengubah permeabilitas membran sitoplasma. Komponen senyawa
antimikroba mengganggu integritas membran sitoplasma sehingga terjadi
kebocoran. Fenol dapat mengakibatkan lisis sel dan menyebabkan
denaturasi protein, menghambat pembentukan protein sitolpasma dan
asam nukleat, serta menghambat ikatan ATP-ase pada membran;
3) Menghambat kerja enzim sehingga metabolisme sel terganggu. Dengan
menghambat proses sintesis protein maka ketersediaan enzim intraseluler
sel. Senyawa fenol dapat bereaksi dengan enzim dehidrogenase sehingga
aktivitas enzim tersebut menjadi hilang;
4) Menginaktivasi fungsi material genetik. Senyawa antibakteri dapat
mengganggu kerja dari RNA dan DNA polimerase sehingga pembentukan
asam nukleat dan transfer informasi genetik menjadi terganggu.
Aktivitas antimikroba asap cair terutama disebabkan oleh adanya
senyawa kimia yang terkandung dalam asap seperti fenol, formaldehid, asam
asetat, dan kreosat. Semua senyawa tersebut menghambat pembentukan spora
dan pertumbuhan beberapa jenis jamur dan bakteri. Proses pemurnian asap
cair dilakukan dengan tujuan untuk memisahkan fraksi tar yang mengandung
hidrokarbon aromatik. Benzo[a]pirene merupakan salah satu Policyclic Aromatic Hydrocarbon (PAH) yang bersifat karsinogenik, memiliki titik cair 179 0C dan titik didih 312 0C (Jaya, et al., 1997).
Asap cair komersial dapat menghambat pertumbuhan Vibrio vulnivicus, Yersinia enterolitica, dan Lactococcus lactis dengan MIC masing-masing <0,2%, 0,6%, dan 0,8% secara berturut-turut (Sunen, 1998). Munoz et al. (1998) melaporkan bahwa asap cair komersial pada konsentrasi 8% dapat menghambat pertumbuhan E.coli O157:H7 yang diinokulasikan pada daging. Milly et al. (2005) melaporkan bahwa konsentrasi 0,75% asap cair komersil merupakan MIC untuk Lactobacillus plantarum.
Sunen (1998) menunjukkan bahwa asap cair komersial memiliki
efektivitas yang berbeda-beda dengan penghambatan terhadap
mikroorganisme yang berbeda pula, tergantung dari komponen antimikroba
yang dikandungnya. Rentang kisaran nilai MIC asap cair komersial mulai dari
0,4% sampai lebih dari 8% untuk menghambat satu jenis mikroorganisme
yang sama. Catte et al. (1999) menunjukkan juga bahwa penggunaan asap cair komersial pada konsentrasi 0,33 ml – 4,33ml/l tidak mampu menghambat
petumbuhan Lactobacillus plantarum ATCC 12315.
2.11. Asap Cair Tempurung Kelapa
Asap diperoleh melalui pembakaran kayu keras dan kayu lunak yang
Tempurung kelapa dikategorikan oleh Grimwood (1975) sebagai kayu keras
tetapi mempunyai kadar lignin yang lebih tinggi dan kadar selulosa lebih
rendah.
Zuraida (2008) membuktikan bahwa pada asap cair tempurung
kelapa tidak mengandung benzo[a]pirene. Keamanan asap cair tempurung
kelapa juga telah diteliti Zuraida (2008) dimana asap cair dari tempurung
kelapa dinyatakan aman untuk dikonsumsi karena berdasarkan uji toksisitas
menunjukkan bahwa nilai LD50 (konsentrasi tunggal bahan sebagai ransum
yang menyebabkan 50% populasi hewan percobaan mati) lebih besar dari
15.000 mg/kg berat badan mencit. Berdasarkan Peraturan Pemerintah RI
Nomor 74 Tahun 2001, suatu dengan nilai LD50 lebih besar dari 15.000 mg/kg
berat badan hewan uji, maka zat/ senyawa/ bahan kimia dikategorikan sebagai
bahan yang tidak toksik dan aman untuk digunakan dalam pangan.
Zuraida (2008) melaporkan beberapa komponen yang terdapat dalam
asap cair tempurung kelapa yang disajikan pada Tabel 8. Hasil identifikasi
asap cair tempurung kelapa dengan GC-MS menunjukkan bahwa senyawa
fenolik merupakan komponen utama. Guillen dan Ibargoitia (1998)
menyatakan bahwa fenolik juga merupakan senyawa yang menjadi flavor dari
asap cair. Senyawa guaiacol merupakan flavor rasa asap sedangkan syringol
merupakan flavor aroma asap.
Komponen yang bersifat sebagai zat antimikroba dari asap cair
tempurung kelapa adalah fenol dan turunannya (Munoz et al. 1998; dan Soldera et al. 2008). Selain itu, fenol juga memberikan efek antioksidan kepada makanan yang diawetkan. Yulistiani et al. (1997) melaporkan kandungan fenol dalam destilat asap tempurung kelapa sebesar 1,28%.
Tranggono (1996) menyatakan bahwa kandungan fenol pada asap cair dari
berbagai jenis kayu dan tempurung kelapa berkisar antara 2,0 – 5,13% .
Karseno et al. (2002) menjelaskan bahwa fenol dan turunannya dapat bersifat bakteriostatik maupun bakterisidal karena mampu menginaktifkan
enzim-enzim esensial, serta mengkoagulasikan SH grup dan NH grup pada
menyebabkan peningkatan permeabilitas membran sel yang berakibat pada
keluarnya materi intraseluler, inaktivasi enzim, dan perusakan atau inaktivasi
material genetik.
Tabel 8. Komponen-Komponen yang Teridentifikasi dari Fraksi Terlarut Asap Cair tempurung Kelapa dalam Dichloromethane
Golongan Nama Komponen
Keton 2-methyl-2cyclopentenone
Karbonil dan Asam 1-Cyclohexene-1-carboxaldehidyde 2,3-dihydroxy-benzoic acid
3-methoxybenzoic acid methyl ester 4-Hydroxy-benzioc acid methyl ester
Fenol dan turunannya Phenol
2-Methylphenol 3-Methylphenol 2,6-dimethylphenol 2,4-Dimethylphenol 3-Ethylphenol
Guaiakol dan Turunannya 2-Methoxyguaiacol 3- Methylguaiacol
Siringol dan Turunannya 2,6-Dimethoxyphenol 3,4- Dimethoxyphenol
4-(2-Propenyl)-2,6-Dimethoxyphenol Syringylaldehide
Acetosyringone
3,5-Dimethoxy-4-hydroxyphenylacetic acid
Alkil Aril eter 1,2-Dimethoxybenzene 2,3-Dimethoxytoluene 1,2,3-Trimethoxybenzene 1,2,4- Trimethoxybenzene 5-Methyl-1,2,3-trimethoxybenze Sumber : Zuraida (2008)
Asam-asam organik lemah yang terdapat dalam asap cair tempurung
bentuk tidak terdisosiasi lebih cepat berpenetrasi ke dalam membran sel
mikroorganisme. Senyawa asam dapat menurunkan pH sitoplasma,
mempengaruhi struktur dan fluiditas membran, serta mengkelat ion-ion dalam
dinding sel bakteri. Penurunan pH sitoplasma akan mempengaruhi protein
struktural sel, enzim-enzim, asam nukleat, dan fosfolipid membran (Davidson
et al. 2005).
Penggunaan asap cair kasar tempurung kelapa hasil pengendapan
dalam produk pangan dilakukan oleh Zuraida (2008) pada produk bakso ikan
serta Syabana dan Rusbana (2008) pada produk sate bandeng. Metode
pencampuran asap cair kasar pada adonan produk pangan yang akan
diawetkan menyebabkan warna, aroma dan rasa produk akhir terpengaruh.
Pada konsentrasi diatas 2,5% aroma asap pada produk sate bandeng terasa
sangat menyengat sehingga tidak disukai oleh panelis (Syabana dan Rusbana,
2008).
2.12. Redestilasi Asap Cair
Pemurnian asap cair yang dilakukan oleh produsen asap cair
dilakukan dengan cara pengendapan. Senyawa-senyawa yang tidak larut
dalam asap cair yang terkondensasi dari hasil pyrolisis ditampung dan
diendapkan sehingga selama beberapa hari sehingga diperoleh asap cair yang
lebih jernih. Asap cair yang diperoleh dari hasil pengendapan ini belum begitu
murni walaupun penampakannya bening berwarna coklat kehitaman sampai
coklat kekuningan. Jika disimpan dalam jangka waktu lama, senyawa
berwarna hitam yang terdapat didalam asap cair yang belum sempurna
pemurniannya tersebut akan kembali mengendap.
Council of Europe Comitee of Experts on Flavouring Substances
(CECEFS) (1992) menerangkan bahwa asap terdiri dari komponen gas, cairan,
dan partikel padat. Pada saat kondensasi asap, partikel padat tercampur dalam
asap cair kasar sehingga perlu dilakukan pemisahan karena partikel padat
tersebut bersifat karsinogenik. Partikel-pertikel tersebut diantaranya adalah
senyawa nitrogen oksida, polycyclic aromatic hydrocarbons (PAHs), senyawa fenolik, senyawa karbonil, furan, asam alifatik karboksilat, serta komponen tar
et al. (2001) menjelaskan bahwa komponen-komponen asap cair yang berwarna hitam merupakan komponen yang berbeda dengan komponen asap
cair yang digunakan sebagai ingredient dan flavor dalam pangan.
Komponen-komponen tersebut termasuk golongan levoglucosan, turunan karbohidrat,
senyawa bernitrogen, serta senyawa-senyawa yang belum teridentifikasi.
Ditemukannya sifat karsinogenik dari Polycyclic Aromatic Hydrocarbon (PAH) menyebabkan penelitian mengenai bahan pangan hasil pengasapan meningkat. Begitupun dengan penelitian terhadap kandungan
PAH dalam asap cair kasar yang merupakan kondensat langsung hasil proses
pirolisis. Berbagai metode pemurnian telah dilakukan diantaranya dengan
menurunkan suhu pirolisis (Daun, 1979), destilasi kondensat asap cair dan
penyaringan menggunakan pulp selulosa (Gorbatov et al., 1971), serta penggunaan zeolit sebagai penyaring molekuler (Jaya et al., 1997).
Salah satu proses yang digunakan adalah destilasi dengan
menggunakan destilator (Gambar 3). Prinsip destilasi adalah pemisahan
komponen dari campuran cairan berdasarkan titik. Komponen destilator terdiri
dari pemanas, wadah penampung asap cair yang akan didestilasi, kondensor,
serta wadah penampung destilat. Suhu pemanasan yang diberikan untuk
memanaskan asap cair berkisar antara 1000 – 2000C. Hal ini didasarkan pada
nilai titik didih fenol yaitu 1810C, sehingga pada kisaran suhu tersebut
diharapkan semua komponen fenolik dalam asap cair akan menguap dan dapat
terkonsentrasi sebagai destilat asap cair yang lebih murni. Proses pemanasan
dengan suhu lebih dari 300 0C sebaiknya dihindari karena pada suhu1790C
Polyciclic Aromatic Hydrocarbon (PAH) akan mencair dan mendidih pada suhu 3120C (Sax dan Lewis, 1987; diacu dalam Jaya et al., 1997).
Keterbatasan asap cair kasar yang memiliki warna hitam sampai
coklat kekuningan diharapkan bisa diatasi dengan perlakuan destilasi sehingga
aplikasi asap cair dalam pengolahan pangan dapat dilakukan lebih luas lagi.
Destilasi asap cair memungkinkan destilat yang dihasilkan untuk dijadikan
sebagai ingredient yang dapat ditambahkan langsung pada adonan pangan. Pengujian aktivitas antimikroba asap cair terhadap beberapa jenis
mikroorganisme telah dilakukan. Destilasi ulang asap cair dari tempurung
kelapa terhadap mikroorganisme perusak nira dan penggunaannya sebagai
pengawet nira belum pernah dilakukan. Penggunaan asap cair redestilasi ini
diharapkan menjadi alternatif pengawet nira yang lebih efektif dan lebih