ABSTRAK
PENGUNAAN ZEOLIT AKTIVASI KIMIA (H2S04 DAN HCl) – FISIK PADA BERAGAM NORMALITAS DALAM MENINGKATKAN PRESTASI MESIN DAN MENURUNKAN EMISI GAS BUANG SEPEDA
MOTOR BENSIN 4-LANGKAH
Oleh
LEONARD SINAMBELA
Peningkatan konsumsi bahan bakar pada saat ini disebabkan oleh pertumbuhan kendaraan bermotor yang meningkat. Usaha untuk menggunakan kendaraan tanpa menggunakan bahan bakar minyak belum banyak. Maka diperlukan usaha untuk menghemat bahan bakar tersebut. Salah satu cara yang dapat dilakukan yaitu dengan penggunaan zeolit alam. Penggunaan zeolit dilakukan karena fungsi zeolit yang sangat baik sebagai adsorben. Fungsi zeolit sebagai adsorben dapat ditingkatkan dengan cara aktivasi kimia - fisik. Aktivasi kimia berfungsi untuk meningkatkan selektifitas permukaan zeolit tersebut.
normalitasnya. Frame kemudian diletakkan di casing filter udara sepeda motor. Pengujian dilakukan dengan cara pengujian stasioner, berjalan dengan jarak 5 km, pengujian akselerasi dan pengujian emisi gas buang. Untuk emisi gas buang dilakukan dengan menggunakan alat gas analyzer. Adapun normalitas yang digunakan adalah 0,1 N, 0,2 N, 0,3 N dan 0,5 N serta dipadukan dengan variasi massa 40, 50 dan 60 gram pada setiap normalitasnya.
Setelah dilakukan percobaan, didapat hasil bahwa penggunaan zeolit aktivasi asam HCl dan H2SO4 dapat meningkatkan prestasi mesin kendaraan tersebut,
pengurangan terhadap konsumsi bahan bakar dan emisi gas buang buang kendaraan. Zeolit massa 50 gram memberikan hasil yang lebih baik daripada 40 dan 60 gram. Untuk normalitasnya, 0,3 N memberikan hasil lebih baik dibanding zeolit normalitas 0,1 N, 0,2 N dan 0,5 N. pada pengunaan aktivator asam HCl hasil pengujian konsumsi bahan bakar pada pengujian berjalan jarak 5 km diperoleh sebesar 117,66 ml (22,41%) dan pengujian stasioner pada putaran 2500 rpm sebesar 18,67 ml (28,20 %), terjadi pada penggunaan normalitas 0,3 N massa 50 gram. Sementara itu, pada aktivator asam H2SO4 diperoleh sebesar 18,67 ml
(28,20 %) pada penggunan normalitas 0,3 N massa 50 gram, dan pengujian berjalan jarak 5 km sebesar 111 ml (26,81 %) terjadi pada penggunaan normalitas 0,2 N dengan massa 50 gram. Penurunan emisi gas buang pada aktivator HCl untuk kandungan gas CO diperoleh sebesar 0,36 % (72,20 %), kandungan gas HC sebesar 82 ppm (64,73 %) dan kandungan gas CO2 sebesar 4,3 % (10,41 %),
sedangkan pada aktivator H2SO4 untuk kandungan gas CO diperoleh sebesar 0,46
% (64,47 %), kandungan gas HC sebesar 76 ppm (67,31 %) dan kandungan gas CO2 sebesar 4,5 % (6,25 %).
Kata kunci : zeolit aktivasi HCl dan H2SO4, normalitas aktivator, dan emisi gas
MOTOR BENSIN 4-LANGKAH
oleh
Leonard Sinambela
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA TEKNIK
Pada
Jurusan Teknik Mesin
Fakultas Teknik Universitas Lampung
FAKULTAS TEKNIK UNIVERSITAS LAMPUNG
RIWAYAT HIDUP
Penulis dilahirkan di Porsea pada tanggal 2 Februari 1990, sebagai anak ketika dari tiga bersaudara, dari pasangan Pikul Sinambela dan Hodlan Siregar.
Pendidikan di Sekolah Dasar Negeri 173631 Porsea, Toba Samosir diselesaikan pada tahun 2001, sekolah lanjutan tingkat pertama Budhi Dharma Balige diselesaikan pada tahun 2004, sekolah menengah atas Bintang Timur 1 Balige pada tahun 2007 penulis terdaftar sebagai mahasiswa Teknik Mesin Fakultas Teknik Universitas Lampung melalui jalur Seleksi Penerimaan Mahasisa Baru (SPMB).
Selama kuliah penulis aktif di Himpunan Mahasiswa Teknik Mesin (Himatem) Universitas Lampung di bidang Penelitian dan Pengembangan serta menjadi asisten laboratorium Motor Bakar di Universitas Lampung. Selain itu, penulis juga pernah menjadi anggota Forum Komunikasi Mahasiswa Keristen Fakultas Teknik (FKMK-FT).
Penulis mengambil konsentrasi mata kuliah pilihan pada bidang judul “Pengunaan
Zeolit Aktivasi Kimia (H2S04 Dan HCl) – Fisik Pada Beragam Normalitas Dalam Meningkatkan Prestasi Mesin Dan Menurunkan Emisi Gas Buang Sepeda Motor
Motto
Jika kita mencintai apa yang kita
kerjakan akan mendapatkan hasil
yang baik dan dalam waktu apapun
Dengan Kerendahan hati
Dan
Segala usaha untuk mencapai impian
Ku persembahankan karaya kecilku ini untuk
Ayahanda dan Ibunda
Atas segala doa, cinta dan kasih sayang yang tak kan
terbalaskan
Kakakku dan adik-adikku
Pemberi semangat dan nasehat
Keluarga Besar Penulis
Teman-teman seperjuangan penulis
SANWACANA
Segala Puji dan Syukur kehadirat Tuhan Yang Maha Esa atas rahmat yang diberikan dan curahan kasih karunia yang tak terbatas yang selalu menyertai sehingga tugas akhir ini dapat terselesaikan.
Tugas akhir yang berjudul “Pengunaan Zeolit Aktivasi Kimia (H2S04 Dan Hcl) – Fisik Pada Beragam Normalitas Dalam Meningkatkan Prestasi Mesin Dan
Menurunkan Emisi Gas Buang Sepeda Motor Bensin 4-Langkah”.
Penyelesaian tugas akhir dan laporan ini juga tidak terlepas dari bantuan banyak pihak yang sangat membantu penulis, baik secara materi maupun moril dan juga masukan saran serta bimbingan dari banyak pihak. Oleh karena itu, penulis mengucapkan terima kasih kepada:
1. Bapak Prof. Dr. Suharno, M.Sc. selaku Dekan Fakultas Teknik Universitas Lampung.
2. Bapak Harmen Burhanuddin, S.T., M.T selaku ketua jurusan Teknik Mesin Universitas Lampung.
4. Bapak A. Yudi Eka Risano, S.T., M.Eng. selaku pembimbing pendamping yang telah membimbing dan memberikan masukan selama penulis menyelesaikan Tugas akhir ini.
5. Bapak M. Dyan Susila E. S., S.T., M.Eng. selaku dosen Pembahas yang telah banyak sekali memberikan masukan dalam penulisan laporan tugas akhir ini. 6. Seluruh staf pengajar jurusan Teknik Mesin yang telah memberikan ilmunya
kepada penulis dan staf administrasi jurusan Teknik Mesin yang telah banyak membantu penulis dalam menyelesaikan studi di jurusan Teknik Mesin.
7. Ayah-ku yang telah memberikan bimbingan moril maupun spiritual dan juga atas nasehat dan do‟anya.
8. Kakak Martha dan kedua adikku sijogal Evi dan Shanny yang selalu memberikan saya nasehat supaya cepat lulus.
9. Punguan pemuda Sirajaoloan Bandar Lampung yang telah memberikan motivasinya.
10.Rekan-rekan Teknik Mesin ‟07 yang tidak sebutkan satu-persatu, terima kasih untuk semua rasa persaudaraan kalian dan juga untuk semua kenangan selama saya tinggal di Lampung.
11.Ito Chatty, Ria dan Chatty serta lae Bahar Marpaung yang selalu memberi saya nasehati.
12.Apara Jhon yang telah memberikan dukungan dan menghibur saya di setiap waktu.
dan saran yang bersifat membangun dari semua pihak. Besar harapan penulis agar laporan tugas akhir ini dapat berguna bagi penulis serta semua pembacanya.
Bandar Lampung, 31 Juli 2014
Penulis,
ii
C. Prosedur Pengujian ... 41
1. Pengujian konsumsi bahan bakar jarak 5 km ... 41
2. Pengujian Akselerasi 0 – 70 km/jam ... 42
3. Pengujian Akselerasi 40 – 70 km/jam ... 43
4. Pengujian Stasioner ... 44
5. Pengujian Emisi Ga Buang ... 46
D. Lokasi Penelitian ... 50
E. Diagram Alir Penelitian ... 50
IV. HASIL DAN PEMBAHASAN A. Hasil ... 52
B. Pembahasan ... 63
1. Pengujian Stasioner ... 63
2. Pengujian Berjalan Jarak 5 km ... 71
3. Pengujian Akselerasi ... 74
4. Pemgujian Emisi Gas Buang ... 79
V. SIMPULAN DAN SARAN A. Simpulan ... 97
B. Saran... 98
DAFTAR PUSTAKA LAMPIRAN A
Tabel Halaman
1. Perhitungan komposisi aktivasi konsentrasi ... 36
2. Pengujian konsumsi bahan jarak 5 km ... 42
3. Pengujian akselerasi 0 – 70 km/jam ... 43
4. Pengujian akselerasi 40 – 70 km/jam ... 44
5. Konsumsi bahan bakar pengujian stasioner ... 45
6. Pengujian emisi gas buang ... 48
7. Data pengujian stasione aktivator H2SO4 ... 53
8. Data pengujian stasione aktivator HCl ... 54
9. Data pengujian berjalan jarak 5 km H2SO4 ... 56
10.Data pengujian berjalan jarak 5 km HCl ... 56
11.Data pengujian akeselerasi H2SO4 ... 57
12.Data pengujian akeselerasi HCl ... 58
13.Pengujian emisi gas buang H2SO4 ... 59
26.Zeolit dalam kemasan ... 40
27.Alat uji emisi ... 47
28.Pengujian emisi di bengkel ... 48
29.Diagram alir pengujian ... 50
30.Pengaruh Aktivator H2SO4 massa 40 gram dengan Variasi Normalitas dan Putaran Mesin pada pengujian stasioner ... 64
31.Pengaruh Aktivator H2SO4 massa 50 gram dengan Variasi Normalitas dan Putaran Mesin pada pengujian stasioner ... 65
32.Pengaruh Aktivator H2SO4 massa 60 gram dengan Variasi Normalitas dan Putaran Mesin pada pengujian stasioner ... 66
33.Pengaruh Aktivator HCl massa 40 gram dengan Variasi Normalitas dan Putaran Mesin pada pengujian stasioner ... 68
34.Pengaruh Aktivator HCl massa 50 gram dengan Variasi Normalitas dan Putaran Mesin pada pengujian stasioner ... 69
35.Pengaruh Aktivator HCl massa 60 gram dengan Variasi Normalitas dan Putaran Mesin pada pengujian stasioner ... 70
36.Pengaruh aktivator H2SO4 dengan variasi massa dan normalitas terhadap konsumsi bahan bakar pada pengujian berjalan dengan jarak 5 km ... 71
37.Pengaruh aktivator HCl dengan variasi massa dan normalitas terhadap konsumsi bahan bakar pada pengujian berjalan dengan jarak 5 km ... 73
38. Pengaruh pengunaan aktivator H2SO4 pada pengujian akselerasi 0 – 70 km/jam ... 75
39.Pengaruh pengunaan aktivator HCl pada pengujian akselerasi 0 – 70 km/jam ... 76
40.Pengaruh pengunaan aktivator H2SO4 pada pengujian akselerasi 40– 70 km/jam ... 77
41.Pengaruh pengunaan aktivator HCl pada pengujian akselerasi 0 – 70 km/jam ... 78
vi
43.Pengaruh Aktivator H2SO4 massa 50 gram dengan Variasi Normalitas dan
Putaran Mesin terhadap kandungan emisi gas buang karbonmonoksida
(CO) ... 81 44.Pengaruh Aktivator H2SO4 massa 60 gram dengan Variasi Normalitas dan
Putaran Mesin terhadap kandungan emisi gas buang karbonmonoksida
(CO) ... 82 45.Pengaruh aktivator H2SO4 variasi massa 40 gram pada emisi gas
buang HC ... 83 46.Pengaruh aktivator H2SO4 variasi massa 50 gram pada emisi gas
buang HC ... 83 47.Pengaruh aktivator H2SO4 variasi massa 60 gram pada emisi gas
buang HC ... 84 48.Pengaruh aktivator H2SO4 variasi massa 40 gram pada emisi gas buang
CO2 ... 85
49.Pengaruh aktivator H2SO4 variasi massa 50 gram pada emisi gas buang
CO2 ... 86
50.Pengaruh aktivator H2SO4 variasi massa 60 gram pada emisi gas buang
CO2 ... 87
51.Pengaruh Aktivator HCl massa 40 gram dengan Variasi Normalitas dan Putaran Mesin terhadap kandungan emisi gas buang karbonmonoksida
(CO) ... 88 52.Pengaruh Aktivator HCl massa 50 gram dengan Variasi Normalitas dan
Putaran Mesin terhadap kandungan emisi gas buang karbonmonoksida
(CO) ... 89 53.Pengaruh Aktivator HCl massa 60 gram dengan Variasi Normalitas dan
Putaran Mesin terhadap kandungan emisi gas buang karbonmonoksida
(CO) ... 90 54.Pengaruh aktivator HCl variasi massa 40 gram pada emisi gas
buang HC ... 91 55.Pengaruh aktivator HCl variasi massa 50 gram pada emisi gas
56.Pengaruh aktivator HCl variasi massa 60 gram pada emisi gas
buang HC ... 93 57.Pengaruh aktivator HCl variasi massa 40 gram pada emisi gas buang
CO2 ... 94
58.Pengaruh aktivator HCl variasi massa 50 gram pada emisi gas buang
CO2 ... 95
59.Pengaruh aktivator HCl variasi massa 60 gram pada emisi gas buang
I. PENDAHULUAN
A. Latar Belakang
Kebutuhan bahan bakar minyak pada saat ini, sudah menjadi kebutuhan pokok oleh warga negara Indonesia untuk menjalankan kehidupan ekonomi. Kebutuhan akan bahan bakar minyak disebabkan oleh terjadinya peningkatan penggunaan kendaraan di Indonesia. Sementara ini, bahan bakar minyak di Indonesia masih disubsidi oleh pemerintah. Untuk itu, perlu diadakannya penghematan bahan bakar minyak. Pada Januari hingga Februari 2012, terjadi lonjakan konsumsi bahan minyak (BBM) dimana konsumsi bahan bakar dipatok 40 juta kiloliter dan setelah dilakukan perhitungan akan kebutuhan konsumsi mencapai 47,8 juta kiloliter atau terjadi lonjakan (Tempo, 2012).
banyak dan terdapat dibeberapa daerah. Ketersedian zeolit pada Kecamatan Sidolmulyo 4.023.505 ton, Kecamatan Kota Agung 4.950.000 ton, Kecamatan Kalianda 17.600.000 ton dan Kecamatan Cukuh Balak 4.600.000 ton (Bkpm, 2012).
Proses pembakaran merupakan salah satu proses yang terpenting dalam kendaraan. Komponen utama dalam pembakaran adalah udara, panas dan bahan bakar. Udara lingkungan yang dihisap masuk untuk proses pembakaran terdiri atas bermacam-macam gas, seperti nitrogen, oksigen, uap air, karbon monoksida, karbon dioksida, dan gas-gas lain. Sementara gas yang dibutuhkan pada proses pembakaran adalah oksigen untuk membakar bahan bakar yang mengandung molekul karbon dan hidrogen (Wardono, 2004). Udara merupakan campuran gas yang terdapat pada permukaan bumi. Udara mengandung 78 % nitrogen, 21% oksigen dan 1 % adalah uap air, karbondioksida dan gas lainnya (Wikipedia, 2012). Pada proses pembakaran, oksigen merupakan oxidizier utama pada proses pembakaran untuk menghasilkan pembakaran yang sempurna. Oleh karena itu, perlu dilakukannnya penyaringan filter udara pada kendaraan untuk menyaring nitrogen, uap air dan gas-gas lain agar mendapatkan oksigen sebagi oxidizier utama pembakaran.
3
Daya adsorb dari zeolit yang digunakan oleh Tobing M. HL belum maksimum karena zeolit yang digunakan masih alami (belum teraktivasi) dimana dalam pori-pori zeolit masih terdapat H2O, dan partikel-partikel pengotor yang
mempersempit pori-pori dari zeolit dan menghambat proses penyaringan oksigen.
Pada penelitiaan Mahdi (2006), kemampuan zeolit aktivasi fisik dalam meningkatkan kinerja motor diesel telah dibuktikan melalui penelitian ini. Hasil pengujian menunjukkan bahwa peningkatan temperatur aktivasi memberikan peningkatan kinerja motor diesel ini. Peningkatan daya engkol terbaik diperoleh sebesar 0,215 kW (12,088 %) pada penggunaan zeolit diameter 1,4 mm, berat 200 gram, temperatur aktivasi 325 °C, waktu pemanasan 2 jam dan putaran 2000 rpm. Penurunan konsumsi bahan bakar spesifik terbaik terjadi dengan menggunakan zeolit diameter 0,7 mm, berat 200 gram, temperatur aktivasi 325 °C, waktu pemanasan 2 jam dan putaran 1100 rpm yaitu sebesar 0,0123 kg/kWh (9,729 %).
150 gram, temperatur aktivasi 225 °C, waktu pemanasan 2 jam pada putaran 3500 rpm yaitu sebesar 0,028 kg/kWh (14,516 %).
Pada penelitian Susandi (2008), pemanfaatan zeolit alam Lampung dengan aktivasi kimia H2SO4 – fisik sebagai adsorben udara dapat meningkatkan
prestasi motor bensin 4-langkah 1500 cc. Penghematan konsumsi bahan bakar terbaik uji berjalan dengan menggunakan zeolit diameter 2,0 mm pada jarak 2,5 km sebesar 40ml (15,79 %) untuk jarak 2,5 km sebesar 46,66 ml (10,07 %). Pengujian stasioner terbaik pada putaran 3000 rpm sebesar 41,67 ml (7,55 %). Pengujian akselerasi 0-100 km/jam sebesar 3,05 detik (8,2 %) dan akselarasi 70-100 km/jam sebesar 2,01 detik (10,85 %)
Pada penelitian Pandapotan (2012), kemampuan zeolit yang diaktivasi fisik dengan menggunakan larutan H2SO4 dan HCl. Hasil pengujian menunjukkan
penggunaan zeolit pelet teraktivasi H2SO4 0,3N pada putaran 2500 rpm dapat
meningkatkan daya engkol sebesar 1,234 kW (0,120 %) dan menurunkan konsumsi bahan bakar spesifik sebesar 0,191 kg/kWh (7,414 %). Sedangkan pada penggunaan zeolit pelet teraktivasi HCl 0,3N pada putaran 2000 rpm dapat meningkatkan daya engkol sebesar 0,951 kW (2,988 %) dan menurunkan konsumsi bahan bakar spesifik sebesar 0,189 kg/kWh (8,161 %).
Dengan berdasarkan beberapa penelitian yang telah dilakukan, penulis ingin melakukan penelitian zeolit dengan aktivasi asam H2SO4 dan HCl dengan
normalitas 0,1N ; 0,2N dan 0,3N. Penelitian Susandi (2008) menggunakan aktivasi kimia (H2SO4) – fisik dan pengujian menggunakan mobil yaitu motor
5
(2012) menggunakan aktivasi kimia (H2SO4 dan HCl) – fisik dan pengujian
menggunakan motor diesel 4-langkah dengan normalitas 0,1N ; 0,2 N; 0,3N dan 0,5 N. Pengujian untuk sepeda motor bensin 4-langkah belum pernah dilakukan dengan aktivasi kimia (H2SO4 dan HCl) – fisik dengan variasi
normalitas. Oleh karena itu, penulis ingin melakukan pengujian pada sepeda motor bensin 4-langkah 100 cc, juga pengujian zeolit dengan aktivasi kimia-fisik asam klorida (HCl) belum pernah dilakukan. Dengan adanya aktivasi aktivasi kimia-fisik asam klorida (HCl), peneliti akan membandingkan hasilnya dengan aktivasi kimia-fisik asam sulfat (H2SO4). Pembatasan
menengahnya. Penulis ingin membandingkan hasil pengujian prestasi mesin dan juga uji emisi gas buang.
B. Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui pengaruh penggunaan aktivator H2SO4 dan HCl serta membandingkan penggunaan aktivatornya pada
aktivasi asam-fisik zeolit clinoptilolite terhadap emisi gas buang dan prestasi motor bensin 4-langkah yang berdasarkan :
1. Variasi jenis aktivator asam H2SO4 dan HCl.
2. Variasi normalitas aktivator asam 0,1 N ; 0,2 N ; 0,3 N dan 0,5 N. 3. Variasi massa zeolit pellet 40, 50 dan 60 gram.
4. Variasi putaran mesin 1500, 2500 dan 4000 rpm.
C. Batasan Masalah
Adapun batasan masalah yang diberikan pada penelitian ini adalah :
1. Mesin yang digunakan adalah motor bensin 4-langkah (110 cc), kondisi standar pabrik, dan dilakukan tune up atau servis ringan rutin sebelum dilakukan pengujian.
7
3. Pengaruh penggunaan larutan asam (H2SO4 dan HCl) dan normalitas larutan
pada aktivasi kimia-fisik terhadap emisi gas buang dan prestasi mesin 4. Perekat yang digunakan adalah tepung tapioka dicanpur dengan aquades
dimana komposisi yang digunakan 74% zeolit, 6% tepung tapioka dan 20%
aquades.
D. Sistematika Penulisan
Adapaun sistematika penulisan dari penelitian adalah : BAB I PENDAHULUAN
Terdiri dari latar belakang, tujuan, batasan masalah, hipotesa dan sistematika penulisan dari penelitian ini.
BAB II TINJAUAN PUSTAKA
Berisi tentang zeolit, sifat-sifat zeolit, aktivasi zeolit, larutan, motor bakar, proses pembakaran, saringan udara.
BAB III METODE PENELITIAN
Berisi beberapa tahapan persiapan sebelum pengujian, prosedur pengujian, dan diagram alir pengujian.
BAB IV HASIL DAN PEMBAHASAN
Yaitu berisikan pembahasan dari data-data yang diperoleh pada pengujian motor bensin 4-langkah.
BAB V SIMPULAN DAN SARAN
DAFTAR PUSTAKA
II. TINJAUAN PUSTAKA
A. Zeolit
Sejak awal tahun 1940-an, ilmuwan Union Carbide telah memulai penelitiannya untuk mensintesis zeolit dan mereka berhasil mensintesis zeolit A dan X murni pada tahun 1950. Penemuan zeolit di dunia dimulai dengan ditemukannya Stilbit pada tahun 1756 oleh seorang ilmuwan bernama A. F. Constedt. Constedt menggambarkan kekhasan mineral ini ketika berada dalam pemanasan terlihat seperti mendidih karena molekulnya kehilangan air dengan sangat cepat.
Sesuai dengan sifatnya tersebut maka mineral ini diberi nama zeolit yang berasal dari dua kata Yunani, zeo artinya mendidih dan lithos artinya batuan. Diberi nama zeolit karena sifatnya yaitu mendidih dan mengeluarkan uap jika dipanaskan . Pada tahun 1784, Barthelemy Faujas de Saint seorang profesor geologi Perancis menemukan sebuah formulasi yang cantik hasil penelitiannya tentang zeolit yang dipublikasikan dalam bukunya “Mineralogie des Volcans”. Akhirnya berkat jasanya, pada tahun 1842 zeolit
11
Gambar 1. Zeolit
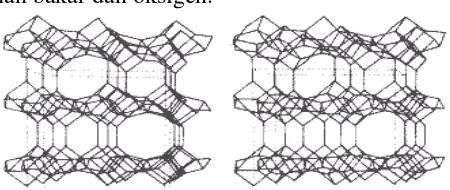
Pada Provinsi Lampung, Mineral zeolit yang paling umum ditemui adalah klinoptilolit, yang mempunyai komposisi kimia (Na3K3)(Al6Si30O72).24H2O.
Ion Na+ dan K+ merupakan kation yang dapat dipertukarkan, sedangkan atom Al dan Si merupakan struktur kation dan oksigen yang akan membentuk struktur tetrahedron pada zeolit. Karakterisasi dengan difraksi sinar-X menunjukkan bahwa jenis zeolit sidomulyo (Lampung) adalah klinoptilolit dengan komposisi kimia adalah 76,95 % SiO2, 8,9 % Al2O3, 0,12% Fe2O3,
1,5 % CaO, 1,21 % MgO, 1,88 % K2O, 2,02 % Na2O (Hendri, J. 2000 dalam
Octo, 2010).
Rumus kimia zeolit secara empiris ditunjukkan sebagai berikut (Bekkum, 1991 dalam Mahdi, 2006):
Mx/n.[(AlO2)x.(SiO2)y].wH2O,
dimana notasi M adalah kation logam alkali atau alkali tanah, x, y, dan w adalah bilangan-bilangan tertentu sedangkan n adalah muatan dari ion logam. Dari rumus zeolit diatas dapat dilihat adanya tiga komponen yang merupakan bagian dari zeolit, yaitu:
Logam Alkali (Mx/n) (Be,Mg,Ca,Sr,Ba,Ra) Air (wH2O)
Salah satu pemanfaatan zeolit alam ini adalah sebagai adsorben udara. Semakin tinggi konsentrasi oksigen dalam udara pembakaran, semakin tinggi mutu proses pembakaran yang terjadi, karena panas awal yang tersedia akan banyak diserap oleh bahan bakar dan oksigen.
Gambar 2. Struktur bangun ruang zeolit Klinoptilolit (batan.go.id)
B. Sifat-Sifat Zeolit
Zeolit mempunyai sifat-sifat kimia, antara lain : 1. Dehidrasi
Sifat dehidrasi zeolit berpengaruh terhadap sifat penyerapanya. Keunikan zeolit terletak pada struktur porinya yang spesifik. Pada zeolit alam di dalam pori-porinya terdapat kation atau molekul air. Bila kation-kation atau molekul air tersebut dikeluarkan dari dalam pori dengan suatu perlakuan tertentu maka zeolit akan meninggalkan pori yang kosong (Barrer, 1982 dalam Andrianus, 2012).
2. Penyerapan
13
sebagai penjerap gas atau cairan. Zeolit dalam proses penyerapannya, didasarkan pada 2 hal, yaitu :
a. Ukuran molekul
Berdasarkan ukuran molekul artinya apabila ukuran molekul adsorbat lebih besar dari ukuran pori zeolit maka molekul adsorbat tersebut tidak bisa melewati pori zeolit. Zeolit jenis klinoptilolit memiliki ukuran diameter pori 4 A0 sedangkan dalam udara N2 yang berbentuk
elips memiliki panjang sumbu mayor 4,1 A0 dan sumbu minor 3 A0. O2 yang juga berbentuk elips memiliki panjang sumbu mayor 3,9 A0
dan minor 2,8 A0 sehingga N2 yang berdiameter mayor akan terikat
dan tidak dapat melewati pori zeolit sedangkan N2 yang berdiameter
minor dan O2 dengan mudah melewati pori zeolit (Bekkum, 1991
dalam Andrianus, 2012). b. Selektifitas permukaan
Selektifitas permukaan artinya sifat dari molekul gas seperti gas N2
yang mempunyai 4 kutub (quadropole) lebih mudah ditangkap oleh zeolit dibandingkan gas O2 yang mempunyai 2 kutub. Kristal zeolit
(a). Berdasarkan perbedaan ukuran (b). Sifat zeolit yang selektif terhadap molekul polar molekul
Gambar 3. Analogi N2 yang terikat oleh zeolit (MSI. 2005)
3. Penukar Ion
Ion-ion pada rongga berguna untuk menjaga kenetralan zeolit. Ion-ion ini dapat bergerak bebas sehingga pertukaran ion yang terjadi tergantung dari ukuran dan muatan maupun jenis zeolitnya. Sifat sebagai penukar ion dari zeolit antara lain tergantung dari sifat kation, suhu, dan jenis anion (Poerwadi, B. Dkk., 1995 dalam Pandapotan, 2012).
4. Katalis
Zeolit sebagai katalis hanya mempengaruhi laju reaksi tanpa mempengaruhi kesetimbangan reaksi karena mampu menaikkan perbedaan lintasan molekular dari reaksi. Katalis berpori dengan pori-pori sangat kecil akan memuat molekul-molekul kecil tetapi mencegah molekul besar masuk. Selektivitas molekuler seperti ini disebut
molecular sieve yang terdapat dalam substansi zeolit alam (Poerwadi, B. Dkk., 1995 dalam Pandapotan, 2012).
5. Penyaring / Pemisah
15
disebabkan zeolit mempunyai ruang hampa yang cukup besar. Molekul yang berukuran lebih kecil dari ruang hampa dapat melintas sedangkan yang berukuran lebih besar dari ruang hampa akan ditahan. Beberapa penelitian yang telah dilakukan menunjukkan bahwa zeolit alam dimanfatkan sebagai adsorben limbah pencemar dari beberapa industri. Zeolit mampu menyerap berbagai macam logam, antara lain Ni, Np, Pb, U, Zn, Ba, Ca, Mg, Sr, Cd, Cu dan Hg (Kosmulski, 2001 dalan Andrianus, 2012).
Zeolit juga mempunyai kelebihan pada sifatnya, zeolit ini dapat dimodifikasi dan dapat digunakan berkali-kali. Dalam hal modifikasi, zeolit dapat juga dibuat sesuai kebutuhan baik dari segi ukuran maupun kegunaannya. Dari ukurannya zeolit dapat dibuat bentuk serbuk sampai bentuk padat lainnya sesuai keinginan dan kebutuhan sehingga cara kerja zeolit juga dapat dimodifikasi dengan cara dealuminasi, yaitu meningkatkan silika dan meningkatkan kandungan alami hydrophilic
yang diingikan dari zeolit (Ribeiro F.R., Rodrigues A.E., Rollmann L.D., Naccache C. 1984 dalam Tobing M.HL. 2004)
C. Aktivasi Zeolit
pengotor yang menutupi permukaan pori-porinya, dan jenis kation penetral yang masih beragam. Sehingga untuk lebih meningkatkan kualitas dari oksigen yang dibutuhkan dalam pembakaran maka diperlukan zeolit yang lebih baik lagi. Proses aktivasi zeolit alam dikelompokkan menjadi 3 cara yaitu :
1. Aktivasi Fisik
Pengaktivasian zeolit alam secara fisik dilakukan dengan pemanasan. Proses pemanasan zeolit alam dilakukan pada suhu 200-400 0C dan waktu pemanasan dalam sistem vakum 2-3 jam, sedangkan jika di ruang terbuka sekitar 5-6 jam (Suyartono dan Husaini, 1992 dalam Pandapotan, 2012).
2. Aktivasi Kimia
Aktivasi kimia adalah pengaktivasian dengan menggunakan bahan-bahan kimia, baik berupa asam ataupun basa. Fungsi asam atau basa adalah untuk mencuci kation-kation yang mengotori permukaan zeolit. Bahan kimia yang dapat digunakan untuk proses aktivasi zeolit alam adalah larutan asam (H2SO4, HCl dan HNO3) dan larutan basa (NaOH dan
17
Zeolit-Mn + H2SO4 Zeolit-H+ + MnSO4
Zeolit-Mn + NaOH Zeolit-Na+ + MnOH
Zeolit dapat meng-exclude (menahan) semua hidrokarbon, N2, dan semua
gas-gas yang permanen kecuali ammonia. Sedangkan zeolit sebagai penyerap karena adanya kation-kation di sekitar rongga zeolit, sehingga zeolit dapat menyerap molekul yang berbeda muatan. (Yang, 2003 dalam Marlene, 2011). Ukuran rongga atau pori dalam zeolit dapat diatur sesuai kebutuhan.Besarnya pori bergantung pada jenis ion yang terdapat di dalam zeolit. Ion kalium (K+) memiliki jari-jari ion yang paling besar jika dibandingkan dengan ion Na+,Mg2+, dan Ca2+, (Achmad, 2001 dalam Pandapotan, 2012). Besarnya jari-jari ion kalium menyebabkan pori zeolit semakin kecil, sehingga proses penyaringan menjadi lebih selektif.
D. Larutan
Larutan merupakan campuran yang homogen, yaitu campuran yang memiliki komposisi merata atau serba sama diseluruh bagian volumenya. Sedangkan konsetrasi larutan merupakan jumlah zat terlarut dalam satuan volume dan cara untuk menyatakan hubungan kuantitatif antara zat terlarut dan pelarut, semakin encer suatu suatu larutan makin rendah konsentrasinya.
Larutan pekat yaitu larutan yang mengandung relatif lebih banyak zat
terlarut (solute) dibanding pelarut (solvent).
Larutan encer yaitu larutan yang relatif lebih sedikit zat terlarut solute
Ada beberapa cara dalam menyatakan konsentrasi suatu larutan, yaitu sebagai berikut: molaritas, molalitas, normalitas, fraksi mol, persentase massa, ppm. Normalitas menyatakan jumlah mol ekivalen zat terlarut dalam 1000 ml larutan.
Untuk asam, valensi adalah jumlah mol ion H+. Untuk basa, valensi adalah jumlah mol ion OH-. Contoh:
NaOH → 1Na+ + OH 1 mol 1 mol
Jadi Setiap 1 mol NaOH setara dengan1 mol ekivalen.
Antara Normalitas dan Molaritas terdapat hubungan:
N = M x valensi (1)
Jika zat yang akan dicari molaritasnya ada dalam satuan gram dan volumenya dalam milliliter, maka molaritasnya dapat dihitung dengan rumus :
M =
Dengan persamaan tersebut dapat diketahui normalitas dan molaritas dari suatu larutan yang akan dibuat ( Scrib, 2012 dalam Andrianus, 2012).
1. Larutan Asam Sulfat (H2SO4)
Asam sulfat, H2SO4, merupakan asam mineral (anorganik) yang kuat. Zat
19
sulfat murni yang tidak diencerkan tidak dapat ditemukan secara alami di bumi oleh karena sifatnya yang higroskopis, asam sulfat terbentuk secara alami melalui oksidasi mineral sulfida. Reaksi hidrasi asam sulfat sangatlah eksotermik. Selalu tambahkan asam ke dalam air daripada air ke dalam asam. Air memiliki massa jenis yang lebih rendah daripada asam sulfat dan cenderung mengapung di atasnya, sehingga apabila air ditambahkan ke dalam asam sulfat pekat, ia akan dapat mendidih dan bereaksi dengan keras. Reaksi yang terjadi adalah pembentukan ion hidronium:
H2SO4 + H2O → H3O+ + HSO4
-HSO4- + H2O → H3O+ + SO42-
Asam sulfat merupakan komoditas kimia yang sangat penting, dan sebenarnya pula, produksi asam sulfat suatu negara merupakan indikator yang baik terhadap kekuatan industri negara tersebut. Kegunaan utama (60% dari total produksi di seluruh dunia) asam sulfat adalah dalam "metode basah" produksi asam fosfat, yang digunakan untuk membuat pupuk fosfat dan juga trinatrium fosfat untuk deterjen (Wikipedia, 2012).
2. Larutan Asam Klorida
Asam klorida pernah menjadi zat yang sangat penting dan sering digunakan dalam awal sejarahnya. Ia ditemukan oleh alkimiawan Persia Abu Musa Jabir bin Hayyan sekitar tahun 800. Senyawa ini digunakan sepanjang abad pertengahan oleh alkimiawan dalam pencariannya mencari batu filsuf, dan kemudian digunakan juga oleh ilmuwan Eropa termasuk Glauber, Priestley, dan Davy dalam rangka membangun pengetahuan kimia modern (Wikipedia, 2012).
E. Motor Bakar
Motor bakar adalah alat yang berfungsi untuk mengkonversikan energi termal dari pembakaran bahan bakar menjadi energi mekanis, dimana proses pembakaran berlangsung di dalam silinder mesin itu sendiri sehingga gas pembakaran bahan bakar yang terjadi langsung digunakan sebagai fluida kerja untuk melakukan kerja mekanis (Wardono, 2004). Motor bakar pada umumnya dibedakan menjadi dua, yaitu motor bensin dan motor diesel. Motor bensin juga terbagi dua yaitu motor bensin 4-langkah dan motor bensin 2-langkah.
1. Motor Bensin 4-Langkah
21
Gambar 4. Siklus motor bakar bensin 4-langkah (Heywood, 1998 dalam Pandapotan, 2012).
Untuk lebih jelasnya proses-proses yang terjadi pada motor bakar bensin 4-langkah dapat dijelaskan melalui siklus ideal dari siklus udara volume konstan seperti ditunjukkan pada gambar 4.
Gambar 5. Diagram P-v dari siklus ideal motor bakar bensin 4-langkah (Wardono, 2004)
Keterangan mengenai proses-proses pada siklus udara volume konstan dapat dijelaskan sebagai berikut (Wardono, 2004) :
a. Proses 0 1 : Langkah hisap (Intake)
Pada langkah hisap campuran udara-bahan bakar dari karburator terhisap masuk ke dalam silinder dengan bergeraknya piston ke bawah, (a) Langkah hisap (b) Langkah kompresi (c) Langkah ekspansi (d) Langkah buang
Katup keluar
Katup masuk busi
Kepala piston
Batang piston
dari TMA menuju TMB. Katup hisap pada posisi terbuka, sedang katup buang pada posisi tertutup. Di akhir langkah hisap, katup hisap tertutup secara otomatis. Fluida kerja dianggap sebagai gas ideal dengan kalor spesifik konstan. Proses dianggap berlangsung pada tekanan konstan.
b. 1) Proses 12 : Langkah kompresi (Compression)
Pada langkah kompresi katup hisap dan katup buang dalam keadaan tertutup. Selanjutnya piston bergerak ke atas, dari TMB menuju TMA. Akibatnya campuran udara-bahan bakar terkompresi. Proses kompresi ini menyebabkan terjadinya kenaikan temperatur dan tekanan campuran tersebut, karena volumenya semakin kecil. Campuran udara-bahan bakar terkompresi ini menjadi campuran yang sangat mudah terbakar. Proses kompresi ini dianggap berlangsung secara isentropik.
2) Proses 2 3 : Langkah pembakaran volume konstan
Pada saat piston hampir mencapai TMA, loncatan nyala api listrik diantara kedua elektroda busi diberikan ke campuran udara-bahan bakar terkompresi sehingga sesaat kemudian campuran udara-bahan bakar ini terbakar. Akibatnya terjadi kenaikan temperatur dan tekanan yang drastis. Kedua katup pada posisi tertutup. Proses ini dianggap sebagai proses pemasukan panas (kalor) pada volume konstan.
c. Proses 3 4 : Langkah kerja/ekspansi (Expansion)
23
TMA menuju TMB. Dengan bergeraknya piston menuju TMB, maka volume gas pembakaran di dalam silinder semakin bertambah, akibatnya temperatur dan tekanannya turun. Proses ekspansi ini dianggap berlangsung secara isentropik.
d. 1) Proses 4 1 : Langkah buang volume konstan (Exhaust)
Saat piston telah mencapai TMB, katup buang telah terbuka secara otomatis sedangkan katup hisap masih pada posisi tertutup. Langkah ini dianggap sebagai langkah pelepasan kalor gas pembakaran yang terjadi pada volume konstan.
2) Proses 1 0 : Langkah buang tekanan konstan
Selanjutnya piston bergerak kembali dari TMB menuju TMA. Gas pembakaran didesak keluar melalui katup buang (saluran buang) dikarenakan bergeraknya piston menuju TMA. Langkah ini dianggap sebagai langkah pembuangan gas pembakaran pada tekanan konstan.
F. Parameter Prestasi Mesin
Parameter prestasi mesin bagian yang paling penting dalam kinerja motor bakar. Parameter prestasi motor bensin 4-langkah dapat ditentukan dengan : 1. Konsumsi bahan bakar dengan uji berjalan pada kecepatan konstan pada
dengan menggunakan zeolit pada filter saringan udara pada jarak yang telah kita tentukan.
2. Pengujian stasioner pada putaran yang ditentukan. Parameter pengujian dilakukan pada saat kondisi diam, kemudian kita akan meningkatkan putaran mesin pada kondisi yang ditentukan beberapa saat setelah itu dilakukan pengukuran konsumsi bahan bakar pada kondisi normal dengan menggunakan zeolit pada filter saringan udara.
3. Uji akselerasi dari keadaan diam sampai kecepatan yang ditentukan. Pengujian parameter dilakukan uji akselerasi kendaraan mulai dari keadaan sampai kecepatan yang ditentukan kemudian mencatat waktu yang dibutukan dan membanding hasil yang didapat pada kondisi normal dengan menggunakan zeolit pada filter saringan udara.
4. Uji emisi gas buang, parameter dilakukan dengan menguji emisi gas buang pada alat uji emisi gas buang pada putaran tertentu dan membandingkan hasil yang didapat pada kondisi normal dengan menggunakan zeolit pada filter saringan udara.
G. Pembakaran
25
oksigen. Oksigen yang diperlukan untuk pembakaran diperoleh dari udara, yang merupakan campuran dari oksigen dan nitrogen.
Nitrogen adalah gas lembam dan tidak berpartisipasi dalam proses pembakaran. Selama proses pembakaran butiran-butiran halus minyak bahan bakar yang terdiri dari karbon dan hidrogen akan beroksidasi dengan oksigen membentuk air (H2O) dan karbon dioksida (CO2). Tetapi bila oksigen yang
disuplai tidak cukup, maka partikel karbon tidak akan seluruhnya beroksidasi dengan partikel oksigen untuk membentuk CO2, akibatnya terbentuklah
produk pembakaran yang lain seperti karbon monoksida (CO), dan gas buang yang lain seperti UHC (unburned hydrocarbons) (Maleev, 1995 dalam Mahdi, 2006).
Selama proses pembakaran, butiran minyak bahan bakar menjadi elemen komponennya, yaitu hidrogen dan karbon, akan bergabung dengan oksigen untuk membentuk air, dan karbon bergabung dengan oksigen menjadi karbon dioksida. Kalau tidak cukup tersedia oksigen, maka sebagian dari karbon akan bergabung dengan oksigen menjadi karbon monoksida. Akibat terbentuknya karbon monoksida, maka jumlah panas yang dihasilkan hanya 30% dari panas yang ditimbulkan oleh pembentukan karbon monoksida sebagaimana ditunjukkan oleh reaksi kimia berikut (Wardono, 2004).
reaksi cukup oksigen: CO2 CO2 393.5kJ,
Keadaan yang penting untuk pembakaran yang efisien adalah gerakan yang cukup antara bahan bakar dan udara, artinya distribusi bahan bakar dan bercampurnya dengan udara harus bergantung pada gerakan udara yang disebut pusaran. Energi panas yang dilepaskan sebagai hasil proses pembakaran digunakan untuk menghasilkan daya motor bakar tersebut.
Reaksi Campuran Stoikiometri :
C16H34 + 24,5 ( O2 + 3,76 N2 ) 16 CO2 + 17 H2O + 92,1 N2
Reaksi Campuran Miskin-Bahan bakar :
C16H34 + (1,2) 24,5 ( O2 + 3,76 N2 ) 16 CO2 + 17 H2O + 4,9 O2
+ 110,6 N2
Reaksi Campuran Kaya-Bahan bakar :
C16H34 + (0,8) 24,5 ( O2 + 3,76 N2 ) 9 CO2 + 14,2 H2O + 7 CO
+ 2,8 H2 + 73,7 N2
Secara lebih detail dapat dijelaskan bahwa proses pembakaran adalah proses oksidasi (penggabungan) antara molekul-molekul oksigen („O‟) dengan molekul-molekul (partikel-partikel) bahan bakar yaitu karbon („C‟) dan hidrogen („H‟) untuk membentuk karbon dioksida (CO2) dan uap air (H2O)
pada kondisi pembakaran sempurna. Di sini proses pembentukan CO2 dan
H2O hanya bisa terjadi apabila panas kompresi atau panas dari pemantik telah
mampu memisah/ memutuskan ikatan antar partikel oksigen (O-O) menjadi partikel „O‟ dan „O‟, dan juga mampu memutuskan ikatan antar partikel
27
dan „H‟ untuk membentuk CO2 dan H2O. Jadi dapat disimpulkan bahwa
proses oksidasi atau proses pembakaran antara udara dan bahan bakar tidak pernah akan terjadi apabila ikatan antar partikel oksigen dan ikatan antar partikel bahan bakar tidak diputus terlebih dahulu (Wardono, 2004).
H. Saringan Udara (Air Filter)
III. METODE PENELITIAN
A. Alat dan Bahan Pengujian
Adapun alat-alat dan bahan yang digunakan dalam proses pengujian ini antara lain :
1. Motor Bensin 4-langkah 110 cc
Pada penelitian ini, mesin uji yang digunakan adalah motor bensin 4-langkah dengan merk Honda Absolute Revo. Untuk spesikasi dari mesin uji yang digunakan adalah sebagai berikut :
Tipe mesin : 4 langkah, SOHC Sistem pendinginan : Udara
Diameter x langkah : 50 x 55,6 mm Volume langkah : 109,1 cc Rasio Kompresi : 9,0 :1
Daya Maksimum : 8,46 PS/7.500 rpm Torsi Maksimum : 0,86 kgf.m/5.500 rpm
Kopling : Tipe basah, ganda dan sentrifugal Sistem pengapian : DC-CDI, Battery
Gambar 7. Sepeda motor Honda Absolute Revo
2. Alat yang digunakan
Berikut ini adalah alat-alat yang digunakan selama penelitian : a. Mixer
Mixer digunakan untuk mengaduk campuran zeolit dan larutan asam (H2SO4 dan HCl) pada proses aktivasi kimia dan penetralan pH zeolit.
Gambar 8. Mixer
b. Timbangan
Timbangan digunakan untuk menimbang zeolit-zeolit yang akan digunakan dalam pengujian.
31
c. Stopwatch
Stopwatch digunakan untuk mengukur waktu pengujian stasisioner dan waktu akselerasi.
d. Gelas ukur dengan ukuran 500 ml
Gelas ukur 500 ml digunakan untuk mengukur volume air mineral yang digunakan dalam proses pembuatan tablet.
Gambar 10. Gelas ukur e. PH Meter
Digunakan untuk mengukur kadar PH air dalam proses pencucian sampai PH 7.
f. Ampia
Digunakan untuk memperhalus permukaan dan memadatkan campuran zeolit dan tepung tapioka dengan menggunakan ukuran tebal 3 mm.
g. Cetakan diameter 10 mm
Cetakan digunakan membuat cetakan tablet zeolit dengan ukuran diameter 10 mm.
Cetakan diameter 10 mm
Gambar 12. Cetakan zeolit h. Oven
Oven digunakan untuk mengeringkan zeolit yang telah diaktivasi kimia dan digunakan untuk aktivasi fisik.
Gambar 13. Oven i. Gelas ukur 50 ml
Gelas ukur digunakan untuk mengukur bensin yang digunakan dalam tabung bensin dan sisa bensin yang digunakan dalam pengujian.
33
j. Tabung bensin
Tabung bensin digunakan wadah tabung bahan bakar ketika proses pengambilan data sehingga tidak menggunakan tangki bahan bakar motor agar lebih mudah dalam proses pengukuran konsumsi bahan bakar .
Tabung bensin pengujian
Gambar 15. Tabung bensin pengujian k. Tachometer
Tachometer digunakan untuk mengukur putaran mesin.
Tachometer pengujian
Gambar 16. Tachometer sepeda motor l. Kemasan zeolit
Gambar 17. Kemasan zeolit 3. Bahan utama
a. Zeolit alami
Zeolit alami yang digunakan untuk pengujian dalam penelitian ini adalah jenis klinoptilolit, dengan komposisi kimia 64,37 % SiO2, 10,93
% Al2O3, 1,29 % Fe2O3, 0,16 % TiO2, 18,61 % L.O.I, 1,31 % CaO,
0,68 % MgO, 1,54 % K2O, 0,75 % Na2O (sumber: CV. MINATAMA).
Zeoli alam Gambar 18. Zeolit b. Larutan asam (H2SO4 dan HCl)
Larutan asam ini digunakan untuk mengaktivasi zeolit secara kimia
35
c. Air aquades
Air ini dipakai untuk mencuci zeolit baik yang alami maupun yang telah diaktivasi. Air ini digunakan sebagai bahan campuran untuk perekat dengan persentasi 6 % dari campuran perekat.
Gambar 19. Aquades dalam kemasan d. Air mineral
Air ini dipakai untuk mencuci zeolit baik yang alami maupun yang telah diaktivasi.Pada zeolit yang telah diaktivasi bertujuan untuk menetralkan kembali zeolit agar pHnya menjadi seimbang (pH 7). Dan air yang digunakan adalah air mineral “GRAND” yang di produksi
oleh PT. WATERINDEX TIRTA LESTARI, Lampung.
Gambar 20. Galon isi ulang e. Tepung tapioka
B. Persiapan Alat dan Bahan
1. Penimbangan Bahan
Setelah alat dan bahan dipersiapkan, maka terlebih dahulu massa zeolit ditimbang menggunakan timbangan digital sesuai dengan seberapa banyak zeolit yang akan diaktivasi. Selanjutnya membuat larutan aktivator sesuai konsentrasi yang telah ditentukan. Pada penelitian ini menggunakan larutan asam antara lain : H2SO4 dan HCl yang memiliki konsentrasi 0,1N;
0,2N; 0,3N; 0,5 N. Setiap proses pembuatan konsentrasi 0,1N; 0,2N; 0,3N; 0,5 N membutuhkan 1 kg zeolit untuk aktivasi kimia kimia asam H2SO4
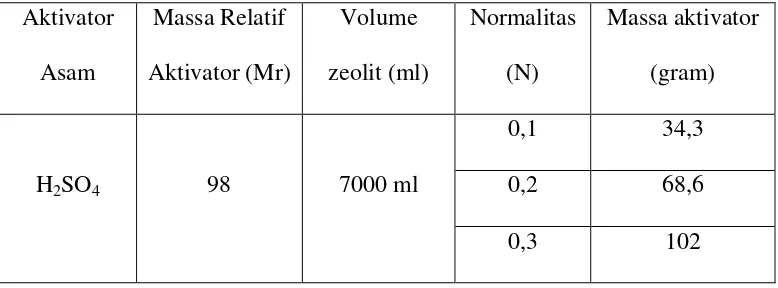
dan HCl. Perbandingan antara zeolit dengan larutan asam adalah 1 : 7. Larutan asam merupakan campuran dari air mineral ditambah dengan larutan aktivator asam. Aktivasi zeolit 1 kg zeolit dibutuhkan 7 liter atau 7000 mL larutan asam activator. Dan valensi H+ untuk HCl adalah 1 mol ekivalen dan H2SO4 adalah 2 mol ekivalen. Dari persamaan 1 dan
persamaan 2 massa aktivator yang dibutuhkan pada aktivasi dapat diketahui (untuk perhitungan campuran normalitas dapat dilihat dilampiran).
37
0,5 171,5
HCl 36,5
0,1 25,55
0,2 51,1
0,3 76,5
0,5 127,75
2. Aktivasi Zeolit
Berikut ini adalah langkah-langkah pengaktivasian zeolit dengan larutan asam-Fisik (H2SO4 dan HCl), yaitu :
1. Mempersiapkan zeolit, larutan asam, air mineral, timbangan digital, labu Erlenmeyer, motor pengaduk (mixer), saringan, dan furnace. 2. Menimbang zeolit sesuai dengan yang dibutuhkan.
3. Membuat larutan asam dengan konsentrasi (0,1 N; 0,2 N; 0,3 N). 4. Menambahkan larutan asam pada zeolit dengan perbandingan 1 : 7
(setiap 1 gram zeolit diaktivasi dengan 7 ml larutan H2SO4).
5. Mengaduk campuran zeolit dan larutan asam dengan menggunakan mixer selama 45 menit.
6. Setelah proses pengadukan, memisahakan antara zeolit dengan larutan asam
7. Mencuci zeolit dengan air mineral beberapa kali hingga pH 7.
8. Mengeringkan zeolit di dalam oven pada temperatur 110ºC selama 1 jam.
9. Menumbuk zeolit dan menyaring hingga berukuran 100 mesh.
Gambar 22. Tumpukan zeolit
10. Memanaskan air mineral dengan mencampurkan 6% tepung tapioka dari total keseluruhan yang akan dibuat menjadi pelet hingga mengental. (Perbandingan 74% zeolit, 6% tepung tapioka dan 20% air).
11. Mencampur serbuk zeolit dengan tepung tapioka yang telah mengental secara merata hingga membentuk campuran siap dicetak.
12. Menyeragamkan tebal campuran menggunakan ampia dengan ukuran ketebalan 3 mm.
39
13. Mencetak campuran menjadi pelet dengan ukuran diameter 10 mm.
Gambar 24. Zeolit pellet yang sudah dicetak
14. Memanaskan zeolit pelet dengan oven dengan temperatur 200 0C selama 1 jam (aktivasi fisik).
Prosedur pengaktivasian zeolit dapat diilustrasikan dalam diagram alir yang ditunjukkan pada gambar 25:
Mempersiapkan Alat dan Bahan
Menimbang zeolit
Membuat Larutan Kimia H2SO4 (0,1N;
0,2N; 0,3N) dan HCl (0,1N; 0,2N; 0,3N)
Mengaduk campuran zeolit dan larutan Kimia Menambahkan Larutan Kimia pada zeolit
Menyaring zeolit dari larutan Kimia
Gambar 25. Diagram alir proses pembuatan dan pengaktivasian zeolit
Zeolit pelet yang telah selesai diaktivasi selanjutnya akan dibungkus dengan wadah yang terdiri dari kawat jaring dengan lapisan dalam berupa kain tipis. Kawat jaring (kawat parabola) dimaksudkan agar zeolit pelet dapat tertata rapih dan kokoh (tidak mudah goyah). Dapat dilihat pada gambar berikut.
Gambar 26. Zeolit dalam kemasan
Zeolit pelet dikemas dengan beragam variasi berat, dari 40, 50 dan 60 gram. Mencuci zeolit hingga pH 7
Mencetak zeolit pelet Mengeringkan zeolit dengan oven
Menumbuk dan mengayak zeolit
Memanaskan zeolit pelet (aktivasi fisik) A
41
C. Prosedur Pengujian
Data yang diambil dalam pengujian ini adalah pengujian prestasi mesin pada pengujian berjalan ini untuk melihat perbandingan karakteristik kondisi tanpa zeolit dan menggunakan zeolit. Data yang diambil tiap pengujiannya pada cuaca dan lokasi pengujian yang sama (permukaan kering) dengan beban kendaraan dan cara berkendara yang juga sama. Adapun pengujian yang akan dilakukan yaitu :
1. Konsumsi bahan bakar pada kecepatan konstan (50 km/jam) pada jarak 5 km
Persiapan yang perlu dilakukan adalah tabung bensin berkapasitas 200 ml. Kemudian tabung bensin disambungkan dengan rapat bersama selang bensin dan diikat ke sisi samping sepeda motor, setelah itu botol tersebut diisi dengan bensin yang sudah disiapkan. Kemudian dilakukan pengujian dengan kondisi motor tanpa zeolit. Jarak tempuh dapat diukur pada
Tabel 2. Data pengujian konsumsi bahan bakar pada kecepatan
43
dalam keadaan berhenti (0 km/jam). Ketika gas mulai ditekan, stopwatch
mulai diaktifkan. Setelah sampai pada kecepatan yang diinginkan (70 km/jam), stopwatch dinon-aktifkan kemudian dicatat waktu tempuhnya. Untuk mencapai kecepatan yang diinginkan (70 km/jm), pengendara melakukan perpindahan gigi yang teratur dan sesuai setiap pengujian. Tabel 3 menampilkan format data akselerasi pada pengujian.
Tabel 3. Data pengujian akselerasi 0-70 km/jam (sekon)
No Normalitas (N) (Gram) Massa
Parameter zeolit yang digunakan dan langkah-langkahnya sama seperti pada pengambilan data pengujian akselerasi dari keadaan diam, hanya saja
kecepatan akhir yang diinginkan (70 km/jam) melakukan perpindahan perseneling dari gigi 1 sampai gigi 4. Pada Tabel 4 menampilkan data akselerasi pengujian kecepatan 40 hingga 70 km/jam.
Tabel 4. Data pengujian akselerasi 40-70 km/jam (detik)
No Normalitas
45
optimal. Kemudian putar setelan gas di bagian karburator untuk menentukan putaran mesin yang dipakai dalam pengujian. Putaran mesin yang dipakai pada pengujian ini yaitu 1500, 2500 dan 4000 rpm.
Pengujian dimulai dengan mengisi bahan bakar pada tangki buatan yang mana bahan bakar tersebut telah diukur terlebih dahulu melalui gelas ukur. Selanjutnya zeolit diletakkan pada saringan udara, setelah itu mesin dihidupkan dengan menghitung waktu pengujian menggunakan stopwatch
(5 menit). Setelah waktu pengujian selesai, mesin dimatikan serta stopwatch
dinon-aktifkan. Kemudian bahan bakar yang terisi dalam tangki buatan tersebut sisanya dituangkan kembali ke dalam gelas ukur untuk menghitung jumlah yang terpakai dalam menit/ml. Tabel 5 merupakan tabel pengujian data stasioner.
Tabel 5. Data pengujian konsumsi bahan bakar stasioner
2 0,2 N
5. Pengujian Emisi Gas Buang
Pengujian Emisi gas buang dilakukan di bengkel PT. Tunas Dihatsu Jl. Raya Natar No. 209 Hajimena Natar Lampung Selatan. Pengujian emisi dilakukan untuk mengetahui pengaruh penggunaan zeolit kelapa pada filter
47
diberikan. Pada kondisi stasioner dengan mengikuti prosedur sebagai berikut :
a. Pemanasan mesin
Pemanasan mesin dilakukan untuk mempersiapkan mesin pada kondisi kerja.
b. Kalibrasi gas analyzer
Setelah mesin berada pada kondisi kerja kemudian dilakukan kalibrasi gas analyzer. Kalibrasi analyzer ini ditempatkan di dalam saluran pembuagan sepeda motor (Knalpot). Kalibrasi ini dilakukan secara otomatis setelah tombol ON pada gas analyzer ditekan. Setelah beberapa menit nilai-nilai kadar gas buang mulai terbaca pada display gas analyzer.
Gambar 27. Alat Uji Emisi c. Pengujian tanpa menggunakan filter zeolit
Sepeda motor dihidupkan dan dijaga pada putaran 1500 rpm dan probe
sensor sudah dimasukkan dalam knalpot. Selanjutnya Nilai pada fuel gas analizer muncul lalu diprint datanya setelah 5 menit motor dihidupkan. Kemudian dengan langkah yang sama pula, pengukuran dilakukan kembali untuk putaran mesin yang berbeda yaitu 2500, 4000 rpm.
d. Pengujian menggunakan Filter zeolit
Setelah pengukuran pada kondisi normal selesai maka pengukuran kedua dilakukan dengan langkah-langkah sebagai berikut: Setelah sepeda motor dimatikan, filter zeolit dipasang di Filter udara. Sepeda motor dihidupkan kembali lalu pengukuran diulang kembali sesuai urutan pengukuran pertama. Pengukuran dilakukan dengan pergantian variasi normalitas dan massa Filter zeolit.
60 Dihatsu Jl. Raya Natar No. 209 Hajimena Natar Lampung Selatan, pengujian konsumsi bahan bakar dan akselerasi dilakukan di Jl. Ryacudu, KORPRI Bandar Lampung, pengujian stasioner dilakukan di daerah Kampung Baru Kedaton.
E. Diagram Alir Penelitian
Adapun diagram alir dalam pengujian zeolit dengan aktivasi kimia (H2SO4
dan HCl) – Fisik ditunjukkan pada gambar 29 :
Persiapan alat uji, bahan uji, alat ukur dan pengolahan
Aktivasi kimia (H2SO4 dan HCl) zeolit dengan
51
Gambar 29. Diagram alir prosedur pengujian Zeolit dengan variasi massa 40, 50 dan 60 gram
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil penelitian dan pengujian yang dilakukan terhadap arang sekam diperoleh data-data dari hasil pengujian tersebut dan telah dibahas dalam pembahasan, maka dapat diambil beberapa kesimpulan sebagai berikut:
1. Penghematan konsumsi bahan bakar terbaik untuk pengujian stasioner untuk aktivator HCl dan H2SO4 mempunyai hasil yang sama sebesar
28,20 % (18,67 ml) ada pada normalitas 0,3 N variasi massa 50 gram dengan putaran mesin 2500 rpm.
2. Penghematan konsumsi bahan bakar pada pengujian berjalan 5 km pada aktivator H2SO4 sebesar 26,81 % (111 ml) pada normalitas 0,2 N massa 50
gram, sedangkan aktivator HCl sebesar 22,41 % (117,67 ml) pada normalitas 0,3 N massa 50 gram.
3. Waktu jarak tempuh terbaik pada pengujian akselerasi 0 – 70 km/jam pada aktivator HCl sebesar 13,89 % (16,79 sekon) pada normalitas 0,1 N massa 60 gram dan H2SO4 sebesar 13,86 % (16,80 sekon) pada normalitas 0,3 N
massa 50 gram.
98
massa 50 gram dan H2SO4 sebesar 15,11 % (10,56 sekon) pada normalitas
0,3 N massa 50 gram.
5. Penurunan emisi gas buang terbaik untuk aktivator H2SO4, untuk emisi gas
buang CO sebesar 76,83 %, HC sebesar 67,31 % dan CO2 sebesar 4,54 %
sedangkan untuk aktivator HCl, emisi gas buang CO sebesar 72,20 %, HC sebesar 64,73 % dan CO2 sebesar 10,41 %.
6. Semakin tinggi normalitas aktivator mampu menurunkan konsumsi bahan bakar lebih tinggi (dari normalitas 0,1 N sampai 0,3 N) namun konsumsi bahan bakar meningkat pada normalitas 0,5 N. Urutan terbaik normalitas aktivator untuk konsumsi bahan bakar adalah 0,3 N, 0,2 N, 0,5 N dan 0,1 N. sementara itu, urutan aktivator terbaik untuk penurunan emisi gas buang adalah 0,2 N, 0,3 N, 0,5 N dan 0,1 N.
B. Saran
Adapun saran-saran yang dapat disampaikan, yaitu :
1. Perlu dilakukannya pengujian untuk normalitas yang tinggi seperti normalitas di atas 2 N dan variasi suhu aktivasi fisik zeolit.
2. Pengujian terhadap umur pakai zeolit perlu dilakukan agar dapat diketahui pengaruh penggunaan H2SO4 dan HCl pada aktivasi kimia-fisik
zeolit pelet perekat terhadap umur luas permukaan spesifik pori.
3. Perlu diadakan pengujian lebih lanjut untuk mengetahui pengaruh penggunaan H2SO4 dan HCl pada aktivasi kimia-fisik zeolit pelet perekat
DAFTAR PUSTAKA
Achmad, dkk. 2001. Kimia Unsurdan Radio Kimia, Bandung : PT. Citra Aditya Bakti.
Alfianto A., dkk. 2006. Optimasi Jumlah Lipatan Paper Pada Desain Automotif Air Filter Dan Pengaruhnya Terhadap Performansi Mesin. Jurnal teknik gelagar, vol. 17, no. 01, april 2006: 1 – 8. Universitas Surabaya. Surabaya. Andrianus, N.K. 2012. Pengaruh Normalitas NaOH dan KOH Pada Aktivasi
Basa-Fisik Zeolit Pelet Tekan Terhadap Prestasi Motor Diesel 4-Langkah. Skripsi Program Sarjana Jurusan Teknik Mesin – Fakultas Teknik Universitas Lampung. Bandar Lampung
Barrer, R. M.. 1982. Hydrotermal Chemistry of Zeolite. Academic Press, London. Bekkum, H. V. Flanigen, E.M., Jansen, J.C. 1991. Introduction to Zeolite Science
and Practice. Elsevier. Amsterdam.
Bkpm. Data Tambang Zeolit Lampung. Januari 2012. Akses 11 Oktober 2012.
http://regionalinvestment.bkpm.go.id/newsipid/id/commodityarea.php?ic= 744&ia=18.
Blogspot. Sejarah, Fungsi, dan Struktur Zeolit. Januari 2011. Akses 11 Oktober 2012. http://datachem.blogspot.com/2011/01/sejarah-fungsi-dan-struktur-zeolit.html.
Hartono, Budi. 2006. Pengaruh Pemanfaatan Zeolit Alam Lampung Teraktivasi Basa-Fisik Tethadap Prestasi Mobil Kijang Karburator 1500 cc. Skripsi JurusanTeknikMesin – Universitas Lampung. Bandar Lampung.
Hendri, J. 2000. Gabungan Aktivasi Asam Sulfat dan Pemanasan Zeolit Lampung Terhadap Daya Ion Amonium. Jurnal Sains Teknologi Vol. 6 No. 1 Tahun 2000. Jurusan Kimia – FMIPA Universitas Lampung.
Humam. 1996. Kemampuan Adsorpsi Zeolit Lampung yang Diaktifkan dengan Asam Sulfat dan Pemanasan Terhadap Ion Amonium, Skripsi Sarjana Kimia P. FMIPA Unila. Bandar Lampung.
Husaini. 1992. Daya Pertukaran Ion Zeolit Polmas Terhadap Ion Logam Berat. Buletin PPTM. Vol. 14 No. 2 Halaman 15-29.
Ismaryata. 1999. The Study of Acidic Washing Temperature and Calcination Effects on Modification Process of Natural Zeolite as an Anion Exchanger. LaporanPenelitian. Semarang: UNDIP
Kosmulski, M. 2001.Chemical Properties of Material Surfaces. Surfactant Science Series. 102. Marcel Dekker New York .
Mahdi. 2006. Pengaruh Pemanfaatan Zeolit Yang Diaktivasi Fisik Pada Beragam Temperatur dan Waktu Pemanasan Terhadap Kinerja Motor Diesel 4 – Langkah. Skripsi Program Sarjana Jurusan Teknik Mesin – Fakultas Teknik Universitas Lampung. Bandar Lampung.
Maleev V. L., terjemahan Priambodo B. 1995. Operasi dan Pemeliharaan Mesin Diesel. Erlangga, Jakarta.
Poerwadi, Bambang, dkk. 1995. Pemanfaatan Zeolit Alam Indonesia Sebagai Adsorben Limbah Cair dan Media Fluiditas dalam Kolom Fluidisasi.
Jurnal MIPA. Malang; Universitas Brawijaya.
Ribeiro F.R., Rodrigues A.E., Rollmann L.D., Naccache C. 1984. Zeolites: Science and Technology. MartinusNijhoffPublihers. Netherland.
Setiono, Marlene., 2011. Adsorpsi Repetitif Komponen Tetes Tebu Dengan Kalium Zeolit. Jurusan Teknik Kimia Fakultas Teknologi Industri Universitas Katolik Parahyangan, Bandung.
Jurusan Teknik Mesin – Fakultas Teknik Universitas Lampung. Bandar Lampung.
Tempo. Ini Alasan Pemerintah Menaikkan Harga BBM. Maret 2012. Akses 11 Oktober 2012. http://www.tempo.co/read/news/2012/03/26/092392550/Ini -Alasan-Pemerintah-Menaikkan-Harga-BBM.
Tobing, M. H. L. 2004. Pengaruh Pemanfaatan Zeolit Alam Lampung Terhadap Prestasi Motor Diesel 4 Langkah. Skripsi Program Sarjana Jurusan Teknik Mesin – Fakultas Teknik Universitas Lampung. Bandar Lampung.
Wardono, H. 2004. Modul Pembelajaran Motor Bakar 4-Langkah. Jurusan Teknik Mesin – Fakultas Teknik Universitas Lampung. Bandar Lampung. Wikipedia. Asam Klorida. Juni 2012. Akses Oktober 2012.
http://id.wikipedia.org /wiki/Asam_sulfat
Wikipedia. Asam Sulfat. Juni 2012. Akses Oktober 2012. http://id.wikipedia.org/ wiki/Asam_sulfat
Wikipedia. Udara. Agustus 2012. Akses 12 Oktober 2012. http://id.wikipedia.org/ wiki/Udara.
Yang, Ralph T., Adsorbents : Fundamentals and Application, John Wiley & Sons Inc, 2003