OPTIMASI TINGKAT HIDROLISIS ENZIMATIK MINYAK
IKAN UNTUK PRODUKSI OMEGA-3 DENGAN METODE
RESPON PERMUKAAN
SKRIPSI
IDA NUR RAKHMI
F34080135
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
OPTIMIZATION OF FISH OIL ENZYMATIC HYDROLYSIS DEGREE TO
PRODUCE OMEGA-3 USING
RESPONSE SURFACE METHOD
Sapta Raharja1) dan Ida Nur Rakhmi2)
1)Staff of Department of Agro-Industrial Technology, Faculty of Agricultural Technology,Bogor Agricultural University, Bogor, West Java, Indonesia
2)Division of Quality Control, Department of Agro-Industrial Technology, Faculty of Agricultural Technology, Bogor Agricultural University, Bogor, West Java, Indonesia
Email: [email protected]
ABSTRACT
Lemuru fish oil is one source of unsaturated fatty acids omega-3 which is good for health. Omega-3 fatty acids as food additives have been try to do. In order to maximize production of omega-3, optimization the effect factor need to be done. Response Surface Method (RSM) is the preferred method for developing and analyzing the response that is influenced by factors so it can optimize the response. The research was conducted with the aim of optimizing the enzymatic hydrolysis of fish oil using lipase from Aspergillus niger by varying the reaction factors such as: temperature, pH, addition of water, and stirring speed with RSM as the research design. Optimal result is given when the
temperature is at 44,68oC, pH at 5,01, addition of water as much as 5,04%
⁄
, and stirring speed
at
210,48 rpm. The software predict the value of hydrolysis rate is 51,7411%. The difference beetwen the predicted result and verification result is less than 5% indicating that the model is feasible to predict the hydrolysis rate of lemuru fish oil.IDA NUR RAKHMI. F34080135. Optimasi Tingkat Hidrolisis Enzimatik Minyak Ikan untuk Produksi Omega-3 dengan Metode Respon Permukaan. Di bawah bimbingan Sapta Raharja. 2013
RINGKASAN
Ikan mengandung nilai gizi yang sangat baik bagi pertumbuhan, namun pemanfaatan ikan laut di Indonesia masih terbatas pada tingkat konsumsi berupa pengolahan daging ikan, sehingga limbah dari pengolahan ikan ini belum dimanfaatkan dengan baik. Minyak ikan merupakan salah satu hasil samping pengolahan ikan yang belum dimanfaatkan lebih lanjut. Padahal minyak ikan merupakan sumber asam lemak jenuh berupa asam eikosapentanoat (EPA) dan asam dokosaheksanoat (DHA) yang penting bagi pertumbuhan dan kesehatan. Usaha untuk memanfaatkan minyak ikan berupa asam lemak omega-3 sebagai bahan tambahan pangan yang memberi asupan nutrisi bagi tubuh telah dicoba dilakukan. Berbagai faktor mempengaruhi hasil produksi omega-3 dalam proses hidrolisis, seperti suhu, pH, penambahan air, dan kecepatan pengadukan. Dalam rangka memaksimalkan produksi omega-3 dengan kualitas yang baik, perlu dilakukan optimalisasi faktor-faktor yang berpengaruh. Penggunaan metode yang tepat dapat menentukan titik-titik optimal setiap faktor dengan jumlah perlakuan dan waktu yang lebih singkat. Response Surface Method (RSM) menjadi pilihan dengan menggabungkan teknik matematika dengan teknik statistika yang digunakan untuk membuat serta menganalisa respon yang dipengaruhi oleh faktor-faktor yang ada sehingga mampu mengoptimalkan respon tersebut.
Penelitian ini dilakukan dengan tujuan untuk mengetahui kecepatan pengadukan terbaik sebagai titik nol pada desain penelitian utama dan mengetahui titik optimal faktor-faktor yang mempengaruhi hidrolisis enzimatik seperti: suhu, pH, penambahan air, dan kecepatan pengadukan dengan menggunakan metode RSM sehingga didapatkan produksi omega-3 optimum. Faktor reaksi yang digunakan dibagi dalam 5 level dengan nilai optimum tiap faktor sebagai posisi nol. Tahapan penelitian ini diawali dengan karakterisasi minyak ikan, pengukuran aktivitas lipase dari Aspergillus niger dengan metode spektrofotometri, hidrolisis enzimatik minyak ikan sesuai desain percobaan RSM menggunakan nilai faktor-faktor optimum. Analisa produk akhir yang dilakukan meliputi pengukuran tingkat hidrolisis dan analisa gas chromatography mass spectrometry (GC-MS).
Hasil karakterisasi sifat fisikokimia diketahui minyak ikan lemuru yang digunakan mempunyai bilangan asam 2,72 mg KOH/g, kadar asam lemak bebas 1,36% dan bilangan penyabunan 184,39 mg KOH/g. Dibandingkan kandungan minyak ikan komersial yang ada, bilangan asam minyak ikan lemuru yang digunakan bernilai lebih kecil, begitu pula dengan nilai bilangan penyabunan, dan kadar asam lemak bebasnya. Minyak ikan lemuru yang digunakan memiliki nilai komponen fisikokimia yang lebih kecil dibandingkan minyak ikan komersial, sehingga kualitasnya dapat dinyatakan baik.
Guna mengetahui titik-titik optimal tiap faktor, dilakukan perhitungan ANOVA menggunakan software Design Expert 7.0.0 seperti yang disajikan pada Lampiran 3. Pada perhitungan tersebut akan diketahui kesesuaian model dengan menggunakan uji Lack of Fit. Hipotesis yang digunakan dalam uji ini ialah H0 menyatakan tidak terdapat Lack of Fit dalam model, sedangkan H1 menyatakan terdapat Lack of Fit dalam model. Diketahui dari perhitungan bahwa p-value F Lack of Fit pada penelitian ini bernilai 0,0632 yang lebih besar dari tingkat signifikan 0,05 yang telah ditentukan, sehingga H0 diterima. Jika H0 diterima, maka dapat dinyatakan tidak terdapat ketidaksesuaian dalam model, hal ini menunjukkan model telah sesuai untuk respon penelitian ini. Hasil perhitungan juga diperoleh nilai R-square sebesar 0,9645 yang memiliki arti bahwa pengaruh variabel bebas A, B, C, dan D terhadap perubahan variabel terikat berupa respon Y ialah sebesar 96,45%. Sedangkan sisanya sebesar 3,55% dipengaruhi oleh faktor-faktor lain di luar variabel bebas yang digunakan dalam penelitian ini. Model yang dihasilkan dari pengolahan data penelitian ini disajikan dalam bentuk kode level sebagai berikut:
Y = 51,28 – 1,30A + 0,40B + 0,67C + 3,85D + 0,81AB – 1,00AC + 1,01AD – 0,84BC – 0,58BD + 0,38CD – 8,70A2 – 12,12B2 – 10,76C2 – 9,06D2
Titik-titik optimal terbaik yang diberikan memiliki nilai desirability sebesar 0,945, nilai ini dianggap cukup baik karena mendekati 1. Pada solusi ini titik 44,68oC merupakan suhu yang digunakan, sedangkan faktor pH sebesar 5,01. Faktor penambahan air diterapkan sebanyak 5,04%
⁄
dan kecepatan pengadukan pada 210,48 rpm. Pada perlakuan di titik-titik optimal tersebut, diprediksikan nilai respon tingkat hidrolisis sebesar 51,7411%. Hasil verifikasi pada kondisi optimum faktor suhu, pH, penambahan air, dan kecepatan pengadukan menunjukkan hasil respon tingkat hidrolisis sebesar 50,9276%. Ketika dibandingkan, nilai hasil verifikasi menunjukkan ketepatan pada respon yang diuji sebesar 98,4277% dengan selisih nilai keduanya sebesar 0,5711%. Perbedaan nilai yang tidak mencapai 5% mengindikasikan bahwa model tersebut cukup baik dan layak dalam memprediksi tingkat hidrolisis minyak ikan lemuru.OPTIMASI TINGKAT HIDROLISIS ENZIMATIK MINYAK
IKAN UNTUK PRODUKSI OMEGA-3 DENGAN METODE
RESPON PERMUKAAN
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh:
IDA NUR RAKHMI
F34080135
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
HALAMAN PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul “Optimasi Tingkat Hidrolisis Enzimatik Minyak Ikan untuk Produksi Omega-3 dengan Metode Respon Permukaan” adalah hasil karya saya sendiri dengan arahan Dosen Pembimbing Akademik, dan belum diajukan dalam bentuk apapun pada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, Februari 2013 Yang membuat pernyataan,
© Hak Cipta milik Institut Pertanian Bogor, tahun 2013 Hak cipta dilindungi
Dilarang mengutip dan memperbanyak tanpa izin tertulis dari
BIODATA PENULIS
i
KATA PENGANTAR
Puji dan syukur senantiasa dipanjatkan kepada Allah SWT atas berkat, rahmat, dan karuniaNya, sehingga skripsi ini dapat selesai dengan baik. Skripsi dibuat sesuai dengan penelitian yang telah dilakukan, dengan judul “Optimasi Tingkat Hidrolisis Enzimatik Minyak Ikan untuk Produksi Omega-3 dengan Metode Permukaan Respon” pada Februari hingga Desember 2012. Penelitian serta penyusunan skripsi ini dapat diselesaikan dengan bantuan dan dukungan dari berbagai pihak. Pada kesempatan ini, penulis ingin menyampaikan ucapan terima kasih sebesar-besarnya kepada :
1. Dr. Ir. Sapta Raharja, DEA selaku dosen pembimbing akademik atas arahan dan bimbingannya dalam melaksanakan penelitian dan penyelesaian skripsi.
2. Prof. Dr. Ir. Nastiti Siswi Indrasti sebagai Ketua Departemen Teknologi Industri Pertanian, beserta segenap dosen pengajar atas dukungan moral dan bimbingannya selama menjalani pendidikan di IPB.
3. Dr. Ir. M. Yani, MEng dan Dr. Ir. Dwi Setyaningsih, Msi selaku dosen penguji ujian S1 yang telah memberikan saran dan arahannya dalam penyempurnaan skripsi penulis.
4. Kedua orang tua penulis (Machmud A. Karim dan Warsi Mulati) serta kakak tercinta Annisa Nur Suminar atas cinta, doa, dan dukungan yang tiada henti dalam berbagai bentuk.
5. Seluruh laboran dan staf Departemen Teknologi Industri Pertanian yang telah memberi bantuan dan keramahan selama masa pendidikan.
6. Anas, Fanny, dan Fahrudin sebagai teman satu bimbingan yang senantiasa menemani dan memberi semangat.
7. Niza, Dhani, Dody, Tori, Teguh, Yudha, Panji Awak, Rosyid, semua penghuni Kost Pondok Harum, dan teman-teman Mahameru yang setia mendengar berbagai keluh kesah serta berbagi kehangatan dalam berbagai kesempatan.
8. Seluruh keluarga besar TIN 45 sebagai teman seperjuangan selama menempuh pendidikan di IPB untuk persahabatan, suka duka, dan dukungan yang menguatkan.
9. Seluruh pihak lainnya yang tidak dapat disebutkan satu per satu atas bantuannya dalam penyelesaian penelitian dan skripsi penulis.
Penulis menyadari skripsi ini belum sempurna, masih perlunya saran dan kritik yang membangun dalam penyempurnaannya. Semoga tulisan ini bermanfaat dan memberikan kontribusi yang nyata di bidang agroindustri, khususnya pada bidang optimalisasi proses.
Bogor, Februari 2013
ii
DAFTAR ISI
Halaman
KATA PENGANTAR... ... i
DAFTAR TABEL... iv
DAFTAR GAMBAR ... v
DAFTAR LAMPIRAN ... vi
I. PENDAHULUAN ... 1
1.1. LATAR BELAKANG ... 1
1.2. TUJUAN ... 2
II. TINJAUAN PUSTAKA ... 3
2.1. MINYAK IKAN ... 3
2.2. ASAM LEMAK OMEGA-3 ... 4
2.3. HIDROLISIS ENZIMATIK ... 5
2.4. LIPASE Aspergillus niger ... 6
2.5. FAKTOR-FAKTOR YANG MEMPENGARUHI HIDROLISIS ENZIMATIK ... 7
2.5.1. Suhu ... 7
2.5.2. Derajat Keasaman (pH) ... 8
2.5.3. Penambahan Air ... 8
2.5.4. Kecepatan Pengadukan ... 9
2.6. RESPONSE SURFACE METHOD ... 10
III. METODOLOGI PENELITIAN ... 11
3.1. ALAT DAN BAHAN... 11
3.2. WAKTU DAN TEMPAT PENELITIAN ... 11
3.3. METODE PENELITIAN ... 11
3.3.1. Karakterisasi Minyak Ikan ... 11
3.3.2. Penentuan Kecepatan Pengadukan ... 12
3.3.3. Penentuan Titik Optimal Faktor-faktor Hidrolisis ... 12
3.3.4. Penentuan Hubungan Tingkat Hidrolisis dengan Kandungan Total Omega-3 ... 13
IV. HASIL DAN PEMBAHASAN ... 15
4.1. KARAKTERISASI MINYAK IKAN ... 15
4.2. PENENTUAN KECEPATAN PENGADUKAN ... 16
4.3. ANALISA KOMBINASI FAKTOR TERHADAP RESPON ... 17
4.3.1. Faktor Suhu dan pH (AB)... 17
4.3.2. Faktor Suhu dan Penambahan Air (AC) ... 19
4.3.3. Faktor Suhu dan Kecepatan Pengadukan (AD) ... 21
4.3.4. Faktor pH dan Penambahan Air (BC) ... 23
4.3.5. Faktor pH dan Kecepatan Pengadukan (BD) ... 26
4.3.6. Faktor Penambahan Air dan Kecepatan Pengadukan (CD) ... 26
4.4. PENENTUAN TITIK OPTIMAL FAKTOR ... 27
iii
V. KESIMPULAN DAN SARAN ... 34
5.1. KESIMPULAN ... 34
5.2. SARAN ... 34
DAFTAR PUSTAKA ... 35
iv
DAFTAR TABEL
Halaman
Tabel 1. Sifat fisiko kimia minyak ikan lemuru ... 3
Tabel 2. Komponen asam lemak dalam minyak ikan lemuru dengan pemurnian alkali ... 4
Tabel 3. Kadar asam lemak omega-3 beberapa jenis ikan laut per 100 gram daging ... 5
Tabel 4. Spesifikasi lipase dari berbagai sumber mikroorganisme ... 7
Tabel 5. Level dari faktor-faktor hidrolisis enzimatik ... 13
Tabel 6. Desain matriks percobaan dan hasil respon ... 14
Tabel 7. Karakterisasi minyak ikan ... 15
Tabel 8. Kriteria pengolahan data untuk optimasi respon ... 30
v
DAFTAR GAMBAR
Halaman
Gambar 1. Rumus molekul asam linoleat, EPA, dan DHA ... 5 Gambar 2. Reaksi hidrolisis oleh enzim lipase secara sistematik ... 6 Gambar 3. Mekanisme pengikatan air dengan media pelarut organik dalam
reaksi hidrolisis ... 9 Gambar 4. Diagram alir tahapan penelitian ... 12 Gambar 5. Tingkat hidrolisis minyak ikan lemuru pada berbagai kecepatan pengadukan ... 16 Gambar 6a. Grafik 3D-surface respon permukaan proses hidrolisis pada perlakuan
suhu dan pH ... 18 Gambar 6b. Grafik kontur respon permukaan proses hidrolisis pada perlakuan suhu dan pH ... 18 Gambar 7a. Grafik 3D-surface respon permukaan proses hidrolisis pada perlakuan
suhu dan penambahan air ... 21 Gambar 7b. Grafik kontur respon permukaan proses hidrolisis pada perlakuan suhu
dan penambahan air ... 21 Gambar 8a. Grafik 3D-surface respon permukaan proses hidrolisis pada perlakuan suhu
dan kecepatan pengadukan ... 23 Gambar 8b. Grafik kontur respon permukaan proses hidrolisis pada perlakuan suhu
dan kecepatan pengadukan ... 23 Gambar 9a. Grafik 3D-surface respon permukaan proses hidrolisis pada perlakuan pH dan
penambahan air ... 25 Gambar 9b. Grafik kontur respon permukaan proses hidrolisis pada perlakuan pH dan
vi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Prosedur karakterisasi minyak ikan ... 39
Lampiran 2. Spesifikasi Amano Lipase A dari Aspergillus niger ... 41
Lampiran 3. Rumus tingkat hidrolisis minyak ikan ... 42
Lampiran 4. Data penentuan kecepatan pengadukan ... 43
Lampiran 5. Penentuan titik optimum faktor ... 44
Lampiran 6. Hasil GC-MS minyak ikan lemuru awal ... 47
1
I.
PENDAHULUAN
1.1. LATAR BELAKANG
Hasil laut telah menjadi salah satu komoditi ekspor Indonesia dengan pasar yang terbuka lebar di berbagai negara. Perairan Indonesia memiliki potensi yang sangat baik, hal ini terlihat dari tingginya hasil laut Indonesia, terutama di bidang perikanan. Daerah penangkapan di Pulau Jawa meliputi sepanjang perairan Kabupaten Banyuwangi dengan pusat perikanan terbesar terletak di Muncar. Muncar merupakan daerah penangkapan ikan dengan jumlah tangkapan yang sangat besar. Daerah penangkapan tersebut meliputi perairan Selat Bali yang luasnya 960 mil persegi, dengan potensi sumber perairan yang terkandung mencapai sekitar 200.000 ton pertahun dan terdiri dari jenis-jenis ikan permukaan (ikan pelagis) serta jenis-jenis ikan demersal lainnya. Ikan pelagis ini didominasi oleh jenis ikan lemuru lebih kurang hampir 80% yang tertangkap. Perikanan lemuru yang mendominasi perikanan Selat Bali menjadi sentra dalam pengelolaan sumberdaya ikan di Muncar. Potensi ini diikuti dengan tingkat konsumsi ikan masyarakat Indonesia yang tinggi, apalagi ikan lemuru termasuk jenis ikan yang mudah didapat dan terjangkau dari segi harga.
Ikan memang mengandung nilai gizi yang sangat baik bagi pertumbuhan, seperti protein, lemak, karbohidrat, abu, dan air. Pemanfaatan ikan laut di Indonesia masih terbatas pada tingkat konsumsi berupa pengolahan daging ikan. Terhitung jumlah limbah dari pengolahan ikan lemuru pada tahun 2009 mencapai 50-60 ton per bulan. Hal ini menjadi gambaran bahwa limbah dari pengolahan ikan ini belum dimanfaatkan dengan baik.
Minyak ikan merupakan salah satu hasil samping pengolahan ikan yang belum dimanfaatkan lebih lanjut. Padahal minyak ikan merupakan sumber asam lemak tak jenuh berupa asam eikosapentanoat (EPA) dan asam dokosaheksanoat (DHA) yang termasuk dalam golongan asam lemak omega-3. Kandungan asam lemak omega-3 di dalam minyak ikan penting bagi pertumbuhan dan kesehatan, terutama pada bayi dan anak-anak yang sedang dalam masa pertumbuhan.
Usaha untuk memanfaatkan minyak ikan berupa asam lemak omega-3 sebagai bahan tambahan pangan yang memberi asupan nutrisi bagi tubuh telah dicoba dilakukan. Namun, berbagai kendala menghambat perkembangan usaha ini, salah satunya ialah metode produksi omega-3 yang kurang mendukung. Produksi omega-3 menggunakan hidrolisis dengan suhu dan tekanan yang tinggi membutuhkan biaya dan investasi yang cukup besar. Sedangkan dengan proses hidrolisis enzimatik tidak membutuhkan kondisi suhu yang tinggi, pH yang digunakan juga mendekati netral sehingga biaya produksinya tergolong rendah. Hidrolisis enzimatik diharapkan mampu menjadi solusi dalam produksi omega-3 yang maksimal dan tidak membutuhkan biaya sebesar metode hidrolisis sebelumnya.
Penggunaan enzim yang tepat dapat memaksimalkan terbentuknya produk yang diinginkan pada proses hidrolisis. Asam lemak omega-3 menjadi prioritas produk yang diharapkan dapat dihasilkan dalam jumlah tinggi, dimana asam lemak ini terletak pada posisi 2 di ikatan triasilgliserol. Lipase dari kapang Aspergillus niger secara spesifik mampu memutus ikatan triasilgliserol pada posisi 1 dan 3, sehingga mampu menjaga asam lemak omega-3 yang terletak pada posisi 2.
2 kondisi lingkungannya mendukung. Suhu akan mempengaruhi aktivitas serta kestabilan dari lipase, dimana enzim yang berbasis protein akan terdenaturasi jika suhu yang digunakan melebihi 70oC. Kondisi pH pada media tempat enzim bekerja juga akan berpengaruh pada struktur dan aktivitas enzim tersebut. Perubahan pH media akan mengubah status ionisasi enzim. Pada proses hidrolisis tidak terlepas dari adanya air dalam media, namun penambahan air ini harus diperhatikan karena adanya air dalam jumlah tertentu dapat mengaktifkan sisi katalitik lipase, meningkatkan fleksibilitas, serta mobilitas enzim dalam menghidrolisis substratnya. Selama hidrolisis berlangsung, pengadukan dilakukan pada kecepatan tertentu, dimana pengadukan ini akan membantu kerja enzim dengan adanya tumbukan yang intensif dengan substrat.
Dalam rangka memaksimalkan produksi omega-3 dengan kualitas yang baik, perlu dilakukan optimalisasi faktor-faktor yang berpengaruh. Penggunaan metode yang tepat dapat menentukan titik-titik optimal setiap faktor dengan jumlah perlakuan dan waktu yang lebih singkat. Response Surface Method (RSM) atau yang juga dikenal dengan metode permukaan respon merupakan suatu metode yang memungkinkan peneliti untuk mendapatkan penjelasan yang menyeluruh, mulai dari desain penelitian, pengolahan data, dan solusi optimasi. RSM menggabungkan teknik matematika dengan teknik statistika yang digunakan untuk membuat serta menganalisa respon yang dipengaruhi oleh faktor-faktor yang ada, sehingga metode ini menjadi pilihan karena dirasa mampu mengoptimalkan respon tersebut.
1.2. TUJUAN
Penelitian ini dilakukan untuk mencapai tujuan berikut:
1. Menentukan pendekatan kecepatan pengadukan sebagai titik pusat
3
II.
TINJAUAN PUSTAKA
2.1.
MINYAK IKAN
Minyak ikan menjadi bahan utama dalam penelitian ini, dimana minyak ikan yang digunakan merupakan hasil samping dari proses penepungan dan pengalengan ikan lemuru di daerah Muncar, Jawa Timur. Menurut Yunizal (2002), ketika dilakukan proses penepungan, proses pemasakan, pengepresan, maupun tahap pre-cooking pada proses pengalengan akan dihasilkan cairan samping yang mengandung minyak. Cairan tersebut yang dikenal sebagai minyak ikan dan jika ditangani dengan baik akan memiliki mutu yang baik, sehingga dapat digunakan untuk makanan.
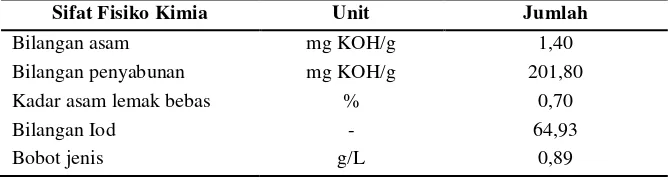
Minyak ikan memiliki kandungan serta sifat yang bervariasi, hal ini tergantung pada jenis kelamin, spesies, ukuran, tingkat kematangan (umur), musim, siklus bertelur, dan letak geografis ikan tersebut hidup (Swern, 1982). Minyak ikan telah menjadi salah satu produk komersial, dimana sifat fisiko kimianya memiliki standar seperti yang disajikan pada Tabel 1.
Tabel 1. Sifat fisiko kimia minyak ikan lemuru
Sifat Fisiko Kimia Unit Jumlah
Bilangan asam mg KOH/g 1,40
Bilangan penyabunan mg KOH/g 201,80
Kadar asam lemak bebas % 0,70
Bilangan Iod Bobot jenis - g/L 64,93 0,89 Sumber : Wajizah (2012)
Kualitas minyak ikan tergantung pada cara penyimpanan dan penanganan minyak, selain itu juga dipengaruhi oleh proses pengolahan ikan tersebut. Minyak ikan yang didapatkan dari pengalengan dan penepungan memiliki bau yang tengik serta kandungan asam lemak bebas (FFA) sebesar 4 – 20% (Murtini et al., 1992). Menurut Ketaren (1986), bau tengik disebabkan terjadinya oksidasi pada minyak/lemak dengan udara, adanya aksi mikroba, absorpsi bau oleh lemak serta aksi enzim dalam jaringan yang mengandung lemak. Bau amis pada minyak ikan karena proses oksidasi komponen trimetil amin oleh peroksida yang berinteraksi dengan asam lemak tak jenuh, sehingga menghasilkan senyawa trimetil amin oksida.
Minyak ikan yang diperoleh dari ikan air laut memiliki kandungan asam lemak tak jenuh lebih banyak dibandingkan yang berasal dari ikan air tawar. Hal ini terlihat dari banyaknya asam lemak tak jenuh berantai panjang seperti C20 dan C22 dalam minyak ikan air laut, sedangkan C16 dan C18 cenderung rendah. Kandungan asam lemak pada minyak dari ikan air tawar berkebalikan dengan minyak dari ikan air laut, dimana kandungan C16 dan C18 tinggi namun C20 dan C22 didalamnya rendah (Ackman, 1982).
4 ekonomis dan jumlahnya melimpah, sehingga mudah untuk diperoleh. Minyak ikan lemuru yang telah dimurnikan mempunyai komponen asam lemak ditunjukkan pada Tabel 2.
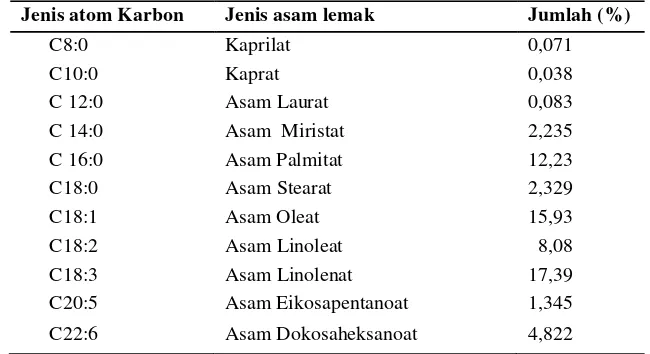
Tabel 2. Komponen asam lemak dalam minyak ikan lemuru dengan pemurnian alkali
Sumber : Yogaswara (2008)
2.2.
ASAM LEMAK OMEGA-3
Asam lemak secara umum dapat dibagi menjadi dua jenis, yaitu asam lemak jenuh dan asam lemak tidak jenuh. Asam lemak jenuh merupakan asam lemak yang hanya memiliki ikatan tunggal (tidak rangkap) pada rantai karbonnya, sedangkan asam lemak tidak jenuh memiliki ikatan rangkap pada rantai karbonnya (Naibaho, 1996). Asam lemak tak jenuh dapat dibagi lagi menjadi asam lemak tak jenuh tunggal (mono unsaturated fatty acid/ MUFA) yang hanya memiliki satu ikatan rangkap, dan asam lemak tak jenuh dengan ikatan rangkap dua atau lebih yang biasa disebut asam lemak tak jenuh jamak (poly unsaturated fatty acid/ PUFA) (Muchtadi et al., 1993).
Asam lemak jenuh cenderung dapat meningkatkan kadar kolesterol dalam darah, dimana semakin panjang rantai karbonnya akan semakin besar pula kecenderungan untuk meningkatkan kolesterol dalam darah (Barlow dan Stansby, 1982). Asam lemak tak jenuh jamak memiliki fungsi penting pada membran biologis dan proses penyampaian sinyal saraf pada setiap makhluk hidup (Wallis dan Watts, 2002).
Minyak ikan yang kaya akan asam lemak tak jenuh memiliki manfaat baik untuk tubuh, salah satu jenis yang ada pada minyak ikan lemuru ialah omega-3. Asam lemak omega-3 menjadi salah satu komponen yang penting bagi tubuh, dimana asam lemak ini termasuk dalam jenis asam lemak essensial. Asam lemak essensial merupakan komponen lemak dalam makanan yang tidak dapat disintesis oleh tubuh manusia dan harus diperoleh dari makanan (Simopoulos, 2008). Jenis asam lemak yang termasuk essensial antara lain asam lemak linoleat (C18:2n-6), asam linolenat (C18:3n-3), dan asam arakidonat (C20:4n-6) (Karyadi et al., 1987). Kekurangan asam lemak omega-3 dapat menimbulkan gangguan pada saraf dan penglihatan. Kekurangan asam lemak essensial akan menghambat pertumbuhan pada bayi dan anak-anak, selain itu dapat juga mengakibatkan gangguan sistem reproduksi serta gangguan kulit, ginjal, dan hati (Almatsier, 2000).
Jenis atom Karbon Jenis asam lemak Jumlah (%)
C8:0 C10:0 C 12:0 Kaprilat Kaprat Asam Laurat 0,071 0,038 0,083
C 14:0 Asam Miristat 2,235
C 16:0 Asam Palmitat 12,23
C18:0 Asam Stearat 2,329
C18:1 C18:2 Asam Oleat Asam Linoleat 15,93 8,08
C18:3 Asam Linolenat 17,39
C20:5 Asam Eikosapentanoat 1,345
5 Asam lemak omega-3 adalah asam lemak yang memiliki posisi ikatan rangkap pertama pada atom karbon nomor tiga dari ujung gugus metilnya (Ackman, 1982). Rumus molekul asam lemak tak jenuh EPA dan DHA dapat dilihat pada Gambar 1.
CH3-CH2-CH=CH-CH2-CH=CH-CH2-CH=CH-(CH2)7-COOH 9,12,15-linolenic acid (C18:3n-3)
CH3-CH2-CH=CH-CH2-CH=CH-CH2- CH=CH-CH2- CH=CH-CH2CH=CH-(CH2)3-COOH cis-5,8,11,14,17-eicosapentaenoic acid (C20:5)
CH3-CH2- CH=CH-CH2-CH=CH-(CH2)3-COOH
cis-4,7,10,13,16,19-docosahexanoic acid (C22:6)
Gambar 1. Rumus molekul asam linolenat, EPA, dan DHA
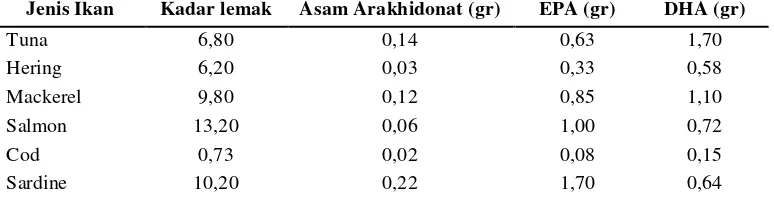
Kandungan EPA dan DHA pada berbagai jenis ikan laut berbeda-beda, jumlah kadar EPA dan DHA beberapa jenis ikan laut yang pernah diamati oleh Barlow dan Stansby (1982) dapat dilihat dalam Tabel 3. Terlihat bahwa kandungan EPA dan DHA pada jenis ikan sardine
ialah sebesar 2,34%. Hal ini menunjukkan potensi minyak ikan jenis sardine sebagai sumber asam lemak omega-3 yang sangat menjanjikan.
Tabel 3. Kadar asam lemak omega-3 beberapa jenis ikan laut per 100 gram daging
Jenis Ikan Kadar lemak Asam Arakhidonat (gr) EPA (gr) DHA (gr)
Tuna 6,80 0,14 0,63 1,70
Hering 6,20 0,03 0,33 0,58
Mackerel 9,80 0,12 0,85 1,10
Salmon 13,20 0,06 1,00 0,72
Cod 0,73 0,02 0,08 0,15
Sardine 10,20 0,22 1,70 0,64
Sumber: Stansby (1982)
Berbagai efek minyak omega-3 pada kesehatan manusia menjadi minat banyak lembaga ilmiah. Asam linoleat yang tergolong asam lemak essensial dapat diubah menjadi asam eikosapentanoat (EPA) dan asam dokosaheksanoat (DHA), namun hal ini tidak berjalan secara efisien pada manusia (Almatsier, 2000). Peran spesifik dari asam linoleat, EPA, dan DHA yang termasuk dalam golongan asam lemak omega-3 dalam mencegah penyakit jantung dan kanker merupakan subyek aktif dalam penelitian (Brunner, 2006).
2.3.
HIDROLISIS ENZIMATIK
6 pertama memerlukan energi yang cukup besar, sedangkan proses terakhir cukup menggunakan energi yang rendah karena dilakukan pada suhu 25-60oC dengan tekanan 1 atm (Herawan, 1993).
Penelitian yang dilakukan oleh Wanasundara dan Shahidi (1998) menunjukkan penggunaan enzim untuk menghasilkan konsentrat asam lemak n-3 memiliki keuntungan dibandingkan metode tradisional yang melibatkan pH ekstrim dan suhu tinggi dimana hal tersebut dapat menghancurkan semua –cis PUFA n-3 alami oleh oksidasi, dan cis-trans isomerisasi atau migrasi ikatan rangkap.
Proses hidrolisis enzimatik dengan menggunakan enzim lipase yang beroperasi pada kondisi suhu rendah dan tekanan atmosferik dianggap aman bagi lingkungan kerja. Selain itu, produk yang dihasilkan memiliki kualitas yang relatif lebih baik dibandingkan produk sejenis yang dibuat dengan proses kimia/fisika, hal ini dikarenakan penggunaan suhunya yang rendah, sehingga kerusakan akibat pemanasan juga cenderung rendah (Murni et al., 2011).
Oleh karena itu, kondisi ringan yang digunakan dalam hidrolisis enzimatik memberikan alternatif yang menjanjikan. Selain menghemat energi, hal tersebut juga meningkatkan selektivitas produk. Pertimbangan lainnya ialah hidrolisis enzimatik menghasilkan asam lemak n-3 dalam bentuk asilgliserol yang dianggap menguntungkan dalam menjaga gizinya (Wanasundara dan Shahidi, 1998).
2.4.
LIPASE
Aspergillus niger
Enzim merupakan protein yang tersusun atas asam-asam amino yang diikat dengan ikatan peptida. Enzim dapat berfungsi sebagai katalis biologis yang berfungsi mengkatalis semua proses metabolisme sel. Enzim dapat mempercepat reaksi kimia dengan menurunkan energi aktivitasnya, dimana energi aktivasi pada suatu reaksi merupakan jumlah energi yang dibutuhkan untuk membaca semua molekul pada satu mol senyawa pada suhu tertentu menuju tingkat transisi pada puncak batas energi (Lehninger, 1995).
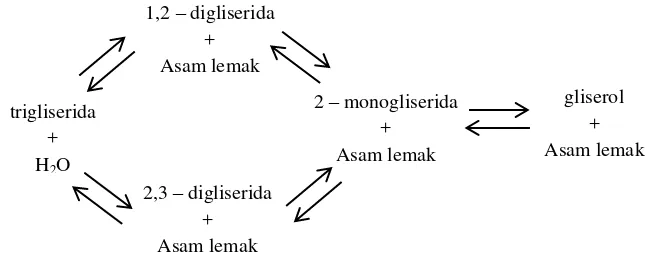
Penguraian minyak atau lemak dapat terjadi dengan bantuan enzim lipase. Enzim lipase mampu menghidrolisa trigliserida, digliserida, dan monogliserida dengan adanya substrat yang tidak larut air (minyak dan lemak) dan fase akueous dimana enzim berada. Dalam kondisi ekuaeous, dimana jumlah air berlebih, reaksi diarahkan ke proses hidrolisis. Sebaliknya dalam kondisi mikroakueous, yaitu ketika jumlah air terbatas, reaksi diarahkan ke esterifikasi (Macrae, 1983). Secara sistematik reaksi hidrolisis yang dikatalisis oleh enzim lipase ditunjukkan pada Gambar 2.
Gambar 2. Reaksi hidrolisis oleh enzim lipase secara sistematik (Macrae, 1983) 1,2 – digliserida
+ Asam lemak trigliserida
+ H2O
2,3 – digliserida + Asam lemak
2 – monogliserida + Asam lemak
7 Lipase menghidrolisis trigliserida menjadi asam lemak bebas, gliserida parsial, dan gliserol. Trigliserida sebagai substrat terdiri dari asam lemak rantai panjang yang tidak larut dalam air (Shahani, 1975). Lipase menghidrolisis ikatan ester pada permukaan antara fase cair, dimana enzim terlarut dan fasa substrat tidak terlarut. Pemanfaatan enzim ini semakin meningkat baik dalam industri pangan maupun non pangan.
Lipase bekerja secara berbeda tergantung dari sumber lipase tersebut, menurut Herawan (1993) berdasarkan cara kerjanya lipase dapat dibagi menjadi tiga:
a. Lipase non spesifik, yaitu lipase yang dapat mengkatalis seluruh ikatan trigliserida. b. Lipase spesifik 1,3 atau 2, yaitu lipase yang mengkatalis trigliserida pada ikatan 1,3 atau 2. c. Lipase spesifik, yaitu lipase yang hanya mengkatalis jenis asam lemak tertentu.
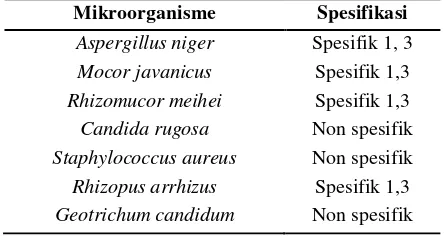
Lipase dapat dihasilkan dari berbagai sumber, antara lain tanaman, hewan, manusia, yeast, kapang, maupun bakteri. Menurut Lai et al. (1999), setiap lipase memiliki kecenderungan tersendiri dalam memotong rantai ester asam lemak dalam minyak, spesifikasi tersebut dapat dilihat lebih jelas pada Tabel 4.
Tabel 4. Spesifikasi lipase dari berbagai sumber mikroorganisme
Mikroorganisme Spesifikasi
Aspergillus niger Mocor javanicus Rhizomucor meihei Candida rugosa Staphylococcus aureus Rhizopus arrhizus Geotrichum candidum
Spesifik 1, 3 Spesifik 1,3 Spesifik 1,3 Non spesifik Non spesifik Spesifik 1,3 Non spesifik Sumber: Lai et al. (1999)
Lipase dapat digunakan untuk membuat konsentrat EPA dan DHA dari seluruh bagian komposisinya dengan efisien dan memiliki rendemen yang tinggi. Salah satu jenis lipase yang memberikan hasil hidrolisis selektif terbaik ialah lipase yang dihasilkan oleh Aspergillus niger. Menurut Wanasundara dan Shahidi (1998), lipase bekerja dengan baik pada kondisi suhu 30-40oC dan pH berkisar pada 5-7. Lipase tersebut spesifik memutus ikatan posisi stereochemical numbering (sn) 1 dan 3 pada triasilgliserol, sehingga asam lemak tak jenuh omega-3 yang umumnya terletak pada sn 2 dapat terjaga (Carvalho et al., 2009).
2.5.
FAKTOR-FAKTOR YANG MEMPENGARUHI HIDROLISIS
ENZIMATIK
2.5.1.
Suhu
Pengaturan suhu pada kondisi lingkungan hidrolisis dapat mempengaruhi hasil hidrolisis tersebut. Suhu akan berpengaruh pada aktivitas dan stabilitas lipase, pengaruhnya dapat bersifat positif maupun negatif. Reaksi akan berjalan lebih cepat apabila suhu dinaikkan, dimana kecepatan reaksi hidrolisis akan meningkat hampir 2 kali untuk setiap kenaikan suhu 10oC. Hal ini terjadi karena gerakan molekul-molekul menjadi lebih cepat seiring bertambahnya suhu reaksi (Groggins, 1958).
8 aktifnya, sehingga enzim menjadi inaktif (Lehninger, 1995). Selain itu suhu tinggi akan menyebabkan terjadinya migrasi alkil secara non enzimatik, oksidasi, dan isomerisasi (Wanasundara dan Shahidi, 1998).
Penggunaan suhu yang terlampau rendah juga akan mengakibatkan hidrolisis tidak sempurna karena reaksi berjalan lambat. Hal ini terjadi akibat tumbukan antar pereaksi yang rendah. Hidrolisis yang tidak sempurna akan mengurangi produk yang terbentuk, sehingga hasilnya akan lebih sedikit dibandingkan dengan reaksi sebenarnya.
Selain mempengaruhi enzim, suhu juga mempengaruhi substrat, dimana suhu yang tinggi akan menurunkan viskositas campuran minyak. Suhu yang semakin tinggi juga akan mengakibatkan turunnya densitas minyak media reaksi. Media dengan densitas rendah akan meningkatkan difusitas serta mengakibatkan peningkatan transfer massa substrat dan produk (Kim et al., 2004).
2.5.2.
Derajat Keasaman (pH)
Enzim yang merupakan protein atau polimer dari asam amino memiliki struktur yang rentan terhadap derajat keasaman (pH). Protein mudah terdenaturasi pada kondisi terlalu asam atau pH yang rendah, sedangkan pada pH tinggi (kondisi basa) protein akan cenderung inaktif (Lehninger, 1995).
Penggunaan larutan buffer bernilai pH tertentu dapat membantu menstabilkan pH media. Perubahan pH media juga dapat mengubah status ionisasi enzim, sehingga mempengaruhi aktivitas dan selektifitas enzim tersebut (Kamarudin et al., 2008). Lipase umumnya merupakan enzim yang mempunyai kisaran pH cukup besar, yaitu antara 4-8. Namun, hal tersebut tergantung dari jenis asal mikroorganisme yang menghasilkan. Kondisi substrat juga akan berpengaruh pada aktivitas enzim, stabilitas, dan ketergantungannya kepada pH, sehingga kemungkinan pengaruh interaksi antar variabel proses akan cukup besar (Fu, 1995).
Lipase memiliki sisi katalitik yang akan aktif pada nilai pH tertentu, tergantung dari asal dan status ionisasi asam amino penyusunnya. Asam amino asam, basa, dan netral hanya aktif pada satu bagian status ionisasi (Ozturk, 2001). Menurut Stauffer (1989), perubahan pH dari netral memungkinkan menjadi lemahnya kekuatan stabilitas bentuk protein, yang berakibat peningkatan denaturasi enzim dan pada akhirnya kehilangan aktivasi. Berdasarkan penelitian yang dilakukan Saxena et al. (2009) stabilitas lipase pada kondisi asam berada pada pH diatas 4, sedangkan stabilitas lipase pada kondisi basa berapa pada pH diatas 8.
2.5.3.
Penambahan Air
9 Seperti terlihat pada lipase Pseudomonas fluorescens yang tidak aktif pada media yang kering. Namun, ketika ditambahkan 0,5 mg air/mg katalis terjadi peningkatan tajam pada aktivitas enzim. Hal ini menunjukkan meski air tidak tidak ikut serta dalam produk yang dihasilkan, namun jumlah air pada suatu reaksi akan mempengaruhi mobilitas enzim, dimana mobilitas lipase akan menjelaskan pula aktivitas enzimatik (Salis et al., 2008).
Meski air dibutuhkan dalam reaksi, tetapi penambahan air yang terlalu banyak akan mengakibatkan peningkatan asam lemak bebas karena reaksi hidrolisis pada triasilgliserol yang berlebihan. Penambahan air perlu diatur dengan baik karena semua proses didasarkan pada termodinamika dari kesetimbangan reaksi kimia yang bersifat reversible atau bolak-balik (Dordick, 1991). Air yang terlalu banyak juga akan menghambat kontak yang terjadi antara minyak ikan dan lipase, sedangkan jumlah air yang terlalu sedikit akan mengurangi kemungkinan kontak lipase dengan air yang bertindak sebagai pereaksi. (Paez et al., 2003).
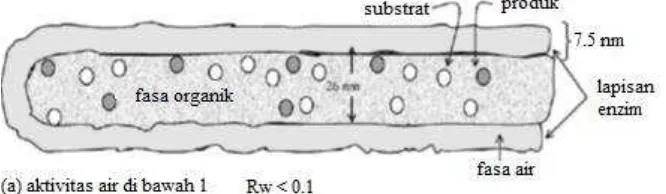
Sedikit air diperlukan untuk mencapai aktivitas maksimal enzim dalam pelarut hidrofobik dibandingkan pelarut hidrofilik. Pada penambahan air yang rendah, semakin rendah polaritas suatu pelarut akan mengakibatkan semakin tingginya aktivitas enzim (Medina et al., 2003). Mekanisme pengikatan air dengan media pelarut organik dapat dilihat pada Gambar 3.
Gambar 3. Mekanisme pengikatan air dengan media pelarut organik dalam reaksi hidrolisis (Medina et al., 2003)
2.5.4.
Kecepatan Pengadukan
Keberhasilan proses hidrolisis secara enzimatis tidak hanya tergantung dari substrat dan lingkungannya, tetapi juga tergantung dari transfer masa serta luas permukaan substrat yang dapat dikatalis oleh enzim serta kemudahan kontak antara enzim dan substrat. Berdasarkan penelitian yang dilakukan Sulaswatty (1998), pengadukan dengan kecepatan yang semakin tinggi akan meningkatkan tingkat hidrolisis minyak, dimana kecepatan dinaikkan dari 90 rpm ke 150 rpm. Namun, pada kecepatan 210 rpm produksi hasil hidrolisis yang diharapkan menurun.
10
2.6.
RESPONSE SURFACE METHOD
Optimasi menjadi bagian pada kegiatan penelitian dan pengembangan baik proses maupun produk yang dihasilkan. Optimasi dapat diterapkan pada penemuan baru maupun pada proses dan produk yang telah ada, kegiatan ini diharapkan dapat berlangsung dengan memanfaatkan fasilitas yang ada namun biaya yang dikeluarkan minimal. Menurut Hubeis (1997), penelitian yang menggunakan teknik optimasi pada prosesnya akan dipengaruhi peubah tidak bebas (respon) dan peubah bebas (faktor). Salah satu metode yang dapat digunakan dalam usaha optimasi adalah Response Surface Method (RSM).
Metode perancangan eksperimen RSM menggabungkan teknik matematika dengan statistika yang digunakan untuk membuat dan menganalisa suatu respon Y yang dipengaruhi oleh beberapa variabel bebas atau faktor X guna mengoptimalkan respon tersebut. Menurut Sudjana (1994), semua variabel ini dapat diukur dan diketahui bahwa Y merupakan fungsi dari faktor-faktor X, hubungan antara keduanya secara umum dapat ditulis dalam bentuk Y = f (X1,X2,...,Xk).
Proses optimasi menggunakan RSM melalui 2 tahap, yaitu orde pertama yang digunakan untuk mencari daerah optimal, kemudian dilanjutkan ke orde kedua guna mencari titik optimal. Hubungan antara respon Y dan faktor-faktor X untuk model orde pertama dapat ditulis sebagai berikut:
Y = 0 + 1X1+ 2X2 + ... + ϵ
Sementara, hubungan keduanya pada model orde kedua dirumuskan sebagai berikut:
Y = â0 + ∑ âiXi + ∑ âiXi 2
+ ∑ ∑ âijXiXj + å
dimana â melambangkan koefisien regresi, sedangkan å menunjukkan error.
Pelaksanaan RSM dalam suatu proses perlu melalui beberapa tahap perencanaan seperti yang diuraikan oleh Cochran and Cox (1962), yaitu:
a. Menentukan model persamaan orde pertama, dimana suatu desain eksperimen dilakukan untuk mengumpulkan data dan arah penelitian selanjutnya.
b. Menentukan level faktor untuk pengumpulan data selanjutnya.
c. Menentukan model persamaan orde kedua, dimana penentuan model ini dilakukan dengan melakukan desain eksperimen dengan level yang telah ditetapkan pada orde pertama. d. Menentukan titik optimum dari faktor-faktor yang diteliti.
Berdasarkan tahapan tersebut, perlu adanya pertimbangan dalam pelaksanaan RSM, yaitu bagaimana menentukan faktor dan level yang sesuai dengan model yang akan dikembangkan. Jika faktor atau level yang dipilih dalam suatu eksperimen tidak tepat akan besar kemungkinan terjadi ketidakcocokan model, hal ini akan membuat penelitian yang dilakukan bersifat bias.
Penggunaan RSM dalam kegiatan optimasi memiliki beberapa manfaat pada penerapannya, antara lain:
- Menunjukkan bagaimana variabel respon Y dipengaruhi oleh variabel bebas X di wilayah yang diperhatikan secara tertentu
- Menentukan pengaturan variabel bebas yang paling tepat dimana akan memberikan hasil yang memenuhi spesifikasi dari respon yang diharapkan
11
III.
METODOLOGI
3.1.
ALAT DAN BAHAN
Peralatan yang digunakan dalam proses hidrolisis minyak ikan ialah shaker incubator,
erlenmeyer 50 ml, sudip, pipet mikro, gelas piala, sumbat karet, dan alumunium foil. Sedangkan peralatan yang digunakan untuk analisa ialah erlenmeyer, gelas ukur, pipet tetes, penangas, alumunium foil, dan buret. Pada penelitian ini juga digunakan beberapa peralatan pendukung seperti neraca analitik, waterbath, dan Gas Chromatography Mass Spectrometry
(GC-MS).
Bahan-bahan yang diperlukan dalam hidrolisis antara lain minyak ikan lemuru yang diperoleh dari daerah Banyuwangi, enzim lipase Aspergillus niger yang diperoleh dari Amano Pharmaceutical Manufacturing Co., buffer sitrat fosfat (0,1M), aquades, pelarut organik heksana, metanol, dan gas nitrogen murni. Sedangkan bahan-bahan yang digunakan untuk analisa ialah alkohol netral, indikator phenolphtalein, KOH 0,1N, KOH beralkohol, serta HCl 0,5N.
3.2.
WAKTU DAN TEMPAT PENELITIAN
Penelitian ini dilakukan pada bulan Februari 2012 hingga Desember 2012. Penelitian pada tahap hidrolisis dilakukan di Laboratorium Teknologi Kimia, sedangkan tahap analisa dilakukan di Laboratorium Pengawasan Mutu dan Laboratorium Dasar Ilmu Terapan milik Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
3.3.
METODE PENELITIAN
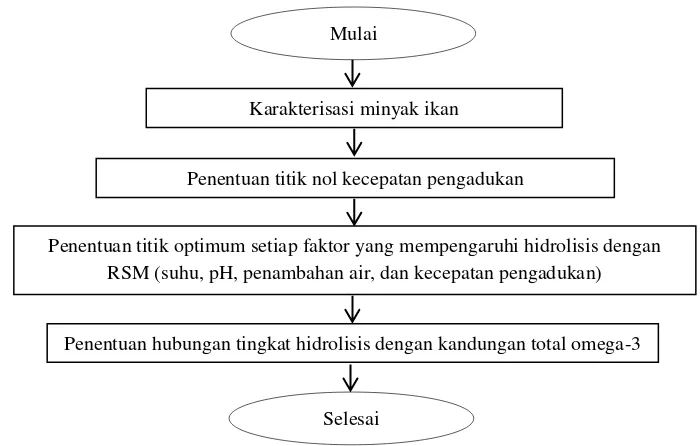
Penelitian ini dilakukan dalam dua tahap, yaitu tahap penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan terdiri atas karakterisasi minyak ikan sebagai bahan baku hidrolisis dan penentuan kecepatan pengadukan terbaik. Penelitian utama meliputi penentuan titik-titik optimum pada setiap faktor yang mempengaruhi hidrolisis enzimatik minyak ikan yaitu suhu, pH, penambahan air, dan kecepatan pengadukan. Diagram alir tahap penelitian dapat dilihat pada Gambar 4.
3.3.1.
Karakterisasi Minyak Ikan
12 Gambar 4. Diagram alir tahapan penelitian
3.3.2.
Penentuan Kecepatan Pengadukan
Kecepatan pengadukan merupakan parameter yang ditambahkan sebagai salah satu faktor yang mempengaruhi hidrolisis minyak ikan. Kecepatan pengadukan yang terpilih pada tahap ini akan menjadi titik pusat pada desain perlakuan penentuan titik optimum di tahap selanjutnya.
Minyak ikan sebanyak 4 gram dimasukkan ke dalam erlenmeyer, kemudian ditambahkan air sebanyak 5% ⁄ . Pelarut organik ditambahkan ke dalam campuran minyak dan larutan enzim tersebut dengan perbandingan 1:3 terhadap enzim yang telah dilarutkan dalam buffer (pH setting awal), setelah itu dibilas dengan gas nitrogen murni selama 30 detik. Erlenmeyer segera ditutup dengan sumbat karet, alumunium foil, dan diikat dengan karet gelang. Amano Lipase A dari Aspergillus niger sebanyak 800 unit (200 U/g substrat) (Lampiran 2) dimasukkan ke dalam larutan buffer sitrat fosfat pH 5 0,1 M sebanyak 6 ml. Larutan enzim tersebut ditambahkan ke dalam wadah gelas, kemudian wadah tersebut dimasukkan ke dalam shaker incubator
dengan perlakuan suhu 45oC dan kecepatan pengadukan sesuai yang diujikan selama 48 jam.
3.3.3.
Penentuan Titik Optimal Faktor-faktor Hidrolisis
Kajian ini menggunakan desain percobaan central Composite Design (CCD) dan dilakukan 2 ulangan pada titik pusat sehingga memenuhi model kuadratik. Terdapat 4 faktor yang mempengaruhi hidrolisis enzimatik, yaitu suhu, pH, penambahan air, dan kecepatan pengaduk. Dengan empat peubah tersebut, maka ditentukan nilai-nilai tiap level dan dibuat desain matriks untuk penentuan kondisi terbaik yang menjadi titik optimal pada setiap faktor. Tiga dari keempat faktor tersebut telah diketahui nilainya dari penelitian terdahulu, sedangkan faktor kecepatan pengadukan belum diketahui sehingga nilainya disimbolkan sebagai D. Masing-masing peubah uji terdiri dari lima level dengan rentang tertentu pada nilai setiap
Karakterisasi minyak ikan Mulai
Penentuan titik nol kecepatan pengadukan
Penentuan titik optimum setiap faktor yang mempengaruhi hidrolisis dengan RSM (suhu, pH, penambahan air, dan kecepatan pengadukan)
Penentuan hubungan tingkat hidrolisis dengan kandungan total omega-3
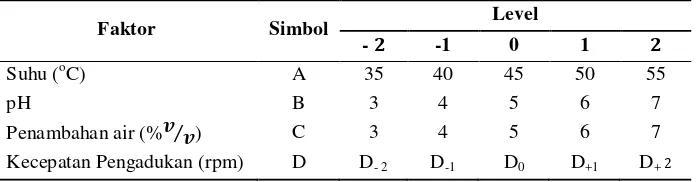
13 levelnya, rancangan tersebut disajikan pada Tabel 5 sedangkan desain matriks percobaan dapat dilihat pada Tabel 6.
Proses hidrolisis dilakukan sesuai prosedur pada penentuan kecepatan pengadukan, namun kondisi setiap faktor disesuaikan dengan kombinasi perlakuan pada desain percobaan. Hasil dari percobaan ini kemudian data akan diolah menggunakan software Design Expert 7.0.0 dan didapatkan hasil titik-titik optimal dalam hidrolisis enzimatik minyak ikan lemuru untuk memproduksi asam lemak omega-3 yang optimum.
Tabel 5. Level dari faktor-faktor hidrolisis enzimatik
3.3.4.
Penentuan Hubungan Tingkat Hidrolisis dengan Kandungan Total
Omega-3
Hasil hidrolisis terdiri atas dua lapisan, yaitu lapisan polar dan non polar. Lapisan non polar yang terdiri dari heksana yang bercampur dengan asam lemak, Triacylgliserol, Diacylgliserol, dan Monoacygliserol akan cenderung berada di atas. Lapisan polar akan berada di lapisan bawah. Lapisan non polar tersebut kemudian diuapkan dengan rotary evaporator guna menghilangkan sisa pelarut yang ada. Sampel tersebut kemudian dianalisa menggunakan GC-MS Agilent, hasil fragmentasinya dibandingkan dengan database wiley 7 untuk mengetahui jenis asam lemak dan persentase total omega-3-nya.
Faktor Simbol Level
- -1 0 1
Suhu (oC) A 35 40 45 50 55
pH B 3 4 5 6 7
Penambahan air (% ⁄ ) C 3 4 5 6 7
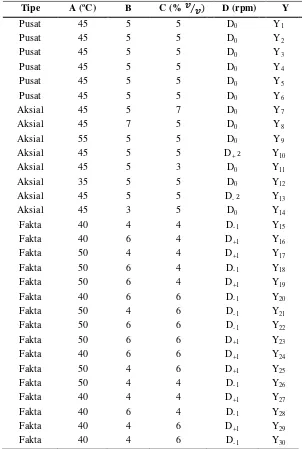
14 Tabel 6. Desain matriks percobaan dan hasil respon
Tipe A (oC) B C (% ⁄ D (rpm) Y
Pusat 45 5 5 D0 Y1
Pusat 45 5 5 D0 Y2
Pusat 45 5 5 D0 Y3
Pusat 45 5 5 D0 Y4
Pusat 45 5 5 D0 Y5
Pusat 45 5 5 D0 Y6
Aksial 45 5 7 D0 Y7
Aksial 45 7 5 D0 Y8
Aksial 55 5 5 D0 Y9
Aksial 45 5 5 D+ Y10
Aksial 45 5 3 D0 Y11
Aksial 35 5 5 D0 Y12
Aksial 45 5 5 D- Y13
Aksial 45 3 5 D0 Y14
Fakta 40 4 4 D-1 Y15
Fakta 40 6 4 D+1 Y16
Fakta 50 4 4 D+1 Y17
Fakta 50 6 4 D-1 Y18
Fakta 50 6 4 D+1 Y19
Fakta 40 6 6 D-1 Y20
Fakta 50 4 6 D-1 Y21
Fakta 50 6 6 D-1 Y22
Fakta 50 6 6 D+1 Y23
Fakta 40 6 6 D+1 Y24
Fakta 50 4 6 D+1 Y25
Fakta 50 4 4 D-1 Y26
Fakta 40 4 4 D+1 Y27
Fakta 40 6 4 D-1 Y28
Fakta 40 4 6 D+1 Y29
15
IV.
HASIL DAN PEMBAHASAN
4.1.
KARAKTERISASI MINYAK IKAN
[image:30.595.152.527.273.332.2]Minyak ikan lemuru yang digunakan pada penelitian ini diperoleh dari Banyuwangi, Jawa Timur yang menjadi sentra pengolahan ikan lemuru. Minyak ikan tersebut merupakan hasil samping industri pengalengan ikan lemuru yang telah melalui proses pemurnian. Karakterisasi minyak ikan dilakukan untuk mengetahui kondisi awal minyak yang menjadi bahan baku penelitian. Karakterisasi yang dilakukan meliputi pengujian bilangan asam, kadar asam lemak bebas (%FFA), dan bilangan penyabungan. Hasil pengujian tersebut disajikan dalam Tabel 8.
Tabel 7. Karakterisasi minyak ikan
Karakterisasi Sampel minyak ikan Minyak ikan lemuru*
Bilangan asam (mg KOH/g) 2,72 1,40
Kadar asam lemak bebas (%) 1,36 0,70
Bilangan penyabunan (mg KOH/g) 184,39 201,80
Sumber* :Wajizah (2012)
Berdasarkan hasil pengujian didapatkan bilangan asam minyak awal sebesar 2,72 mg KOH/g, sedangkan nilai rujukan dari Wajizah (2012) sebesar 1,40 mg KOH/g. Bilangan asam menunjukkan jumlah asam lemak bebas yang terdapat dalam minyak dan dinyatakan sebagai jumlah KOH 0,1N yang digunakan untuk menetralkan asam lemak bebas pada 1 gram minyak (Ketaren, 1986). Hasil pengujian bilangan asam minyak yang digunakan dalam penelitian ini lebih tinggi dibandingkan karakterisasi minyak ikan komersial dari rujukan. Selain itu, kadar asam lemak bebas minyak ikan yang digunakan sebesar 1,36% juga lebih tinggi dibandingkan rujukan yang bernilai 0,70%. Menurut Ketaren (1986), minyak memiliki kualitas yang semakin baik jika kandungan asam lemak bebas di dalamnya semakin rendah, kurang lebih sebesar 2%. Jika minyak mengandung asam lemak bebas yang tinggi, maka aktivitas katalitik enzim pada reaksi akan menurun. Hal ini tentu akan mempengaruhi hasil dari hidrolisis yang dilakukan.
Pada pengujian selanjutnya, bilangan penyabunan minyak ikan ialah 184,39 mg KOH/g. Nilai ini lebih rendah dibandingkan rujukan yang memiliki bilangan penyabungan 201,80 mg KOH/g. Bilangan penyabunan menunjukkan jumlah asam lemak yang tersabunkan di dalam minyak. Nilai ini nantinya akan ikut berperan dalam menentukan tingkat hidrolisis minyak. Nilai bilangan penyabunan yang lebih rendah dari rujukan menunjukkan bahwa minyak belum mengalami oksidasi yang cukup berarti. Apabila oksidasi terjadi, senyawa keton maupun aldehid yang merupakan hasil dari oksidasi akan dibaca juga sebagai asam lemak, sehingga akan meningkatkan total asam lemak yang tersabunkan dan nilai bilangan penyabunan akan semakin tinggi.
16
4.2.
PENENTUAN KECEPATAN PENGADUKAN
[image:31.595.157.476.253.445.2]Proses hidrolisis enzimatis juga dipengaruhi oleh transfer masa serta luas permukaan substrat yang mampu dikatalis oleh enzim. Hal tersebut juga akan memberi pengaruh pada tingkat kemudahan kontak enzim dengan substrat. Pada penelitian ini dilakukan pengamatan kondisi kecepatan pengadukan pada proses hidrolisis, pengadukan tersebut adalah salah satu cara untuk mempertinggi kontak antara enzim dan substrat (Buchler, 1987). Percobaan ini dilakukan pada lima tingkat kecepatan pengadukan, dimana setiap tingkat memiliki rentang 50 rpm. Tingkat terendah dilakukan pada kecepatan 50 rpm, sedangkan tingkat tertinggi diatur pada kecepatan 200 rpm. Data hasil penentuan kecepatan pengadukan tersebut disajikan dalam grafik pada Gambar 5.
Gambar 5. Tingkat hidrolisis minyak ikan lemuru pada berbagai kecepatan pengadukan
Hidrolisis lemak dan minyak terjadi pada antar fasa air-minyak, sehingga dapat dilakukan usaha untuk memperluas permukaan kontak yang akan memudahkan kontak antara enzim dan substrat (Buchler, 1987). Dari grafik terlihat adanya peningkatan tingkat hidrolisis yang cukup signifikan di setiap penambahan kecepatan. Hal ini menunjukkan adanya pengaruh perlakuan kecepatan pengadukan dengan tingkat hidrolisis minyak ikan. Pengadukan pada berbagai kecepatan akan memberikan hasil hidrolisis yang berbeda. Terlihat pada kecepatan pengadukan rendah dihasilkan pula tingkat hidrolisis minyak ikan yang rendah. Sedangkan tingkat hidrolisis tertinggi sebesar 50,47%dicapai pada saat kecepatan pengadukan 200 rpm, namun tingkat hidrolisis menurun saat kecepatan dinaikkan menjadi 250. Dimungkinkan pada kecepatan 200 rpm tersebut permukaan kontak telah melebar dan meningkatkan kontak antara enzim dan substrat, sehingga tingkat hidrolisis minyak semakin besar. Hasil tersebut juga sesuai dengan pernyataan Hui (1996), yaitu seiring bertambah tingginya kecepatan pengadukan akan menaikkan pergerakan molekul dan menyebabkan terjadinya tumbukan. Tumbukan tersebut akan membantu terjadinya kontak antara enzim dengan minyak lebih cepat. Berdasarkan Groggins (1958), diketahui dengan bertambahnya jumlah tumbukan tersebut maka akan bertambah pula nilai konstanta kecepatan reaksi yang terjadi.
Tingkat hidrolisis terbaik pada percobaan ini akan menentukan kecepatan pengadukan yang terpilih untuk digunakan pada penelitian utama. Berdasarkan data yang ada, kecepatan
0 10 20 30 40 50 60
0 50 100 150 200 250 300
T in g k at h id ro lis is ( %)
17 pengadukan yang menghasilkan respon berupa tingkat hidrolisis terbaik akan menjadi nilai titik pusat pada desain penelitian utama, yaitu ketika hidrolisis berjalan pada 200 rpm. Nilai ini akan direntangkan ke batas bawah dan batas atas, dimana setiap level akan memiliki selisih 50 rpm.
4.3.
ANALISA KOMBINASI FAKTOR TERHADAP RESPON
Penelitian ini mengamati empat faktor yang memiliki pengaruh pada tingkat hidrolisis minyak ikan. Data yang dihasilkan dari percobaan diolah menggunakan software Design Expert 7.0.0, dimana pada pilihan analisa dapat diketahui interaksi antar faktor dengan melihat tingkat hidrolisis yang dihasilkan. Analisa tersebut akan menghasilkan persamaan-persamaan matematis yang kemudian ditampilkan dalam grafik. Tampilan persamaan-persamaan ini dalam bentuk grafik disebut sebagai permukaan respon. Menurut Mason et al. (1989), permukaan respon merupakan bentuk geometri yang didapatkan jika suatu peubah respon diproyeksikan sebagai fungsi dari satu atau beberapa peubah kuantitatif. Design Expert memberi beberapa pilihan tampilan grafik, antara lain ialah grafik kontur dan 3D-Surface.
Berdasarkan perhitungan ANOVA yang dilakukan, terdapat informasi nilai F-hitung pada setiap kombinasi faktor. Nilai F-hitung tersebut memperlihatkan pengaruh kombinasi faktor terhadap respon, diketahui bahwa semakin besar nilai F-hitung maka pengaruhnya semakin nyata. Terdapat 4 kombinasi faktor yang memiliki nilai F-hitung lebih dari atau sama dengan 0,50 yaitu kombinasi suhu-pH (AB), suhu-penambahan air (AC), suhu-kecepatan pengadukan (AD), dan suhu-penambahan air (AC). Kombinasi faktor lainnya memiliki nilai F-hitung jauh dibawah 0,50 yaitu sebesar 0,25 untuk kombinasi faktor pH-kecepatan pengadukan (BD) dan 0,11 untuk kombinasi faktor penambahan air-kecepatan pengadukan (CD).
4.3.1.
Faktor Suhu dan pH (AB)
Kedua faktor ini mempengaruhi hidrolisis enzimatik minyak ikan yang dilakukan, dimana jika hidrolisis berlangsung pada suhu dan pH yang tepat akan menghasilkan produk yang optimum. Grafik kontur ini menunjukkan hubungan antara faktor A dan B, dimana A merupakan simbol dari suhu dan B adalah pH. Sementara itu, faktor C dan D menyimbolkan penambahan air dan kecepatan pengadukan. Grafik digambarkan dengan rentang dari 40 hingga 50oC untuk faktor A dan rentang nilai 4 hingga 5 untuk faktor B, sedangkan faktor C dan D pada kondisi nilai titik pusat, yaitu 5% ⁄ dan 200 rpm. Grafik kontur menampilkan kondisi kedua faktor dimana nilai respon maksimal, wilayah tersebut ditandai dengan warna merah.
Ditampilkan pada Gambar 6(a) berupa grafik tiga dimensi yang menampilkan permukaan model dari faktor suhu, pH, dan tingkat hidrolisis. Pada gambar ini dapat terlihat lebih jelas bentuk model yang menyerupai parabola, hal ini dianggap baik karena grafik ini menunjukkan adanya nilai maksimal sebelum pada akhirnya menurun. Posisi nilai respon tersebut ditunjukkan pada permukaan yang paling tinggi dibandingkan lainnya.
18 (a)
(b)
Gambar 6. (a) Grafik 3D-surface respon permukaan proses hidrolisis pada perlakuan suhu dan pH
(b) Grafik kontur respon permukaan proses hidrolisis pada perlakuan suhu dan pH
Pada gambar 6(b), terlihat garis-garis kontur melingkar dengan titik merah di tengah lingkaran terdalam. Hal ini menunjukkan bahwa nilai respon terbaik akan diperoleh pada kondisi yang mendekati titik pusat dari desain percobaan. Sebanyak
T
in
g
k
at
Hid
ro
lis
[image:33.595.158.526.100.638.2]19 enam titik merah pada gambar merupakan enam titik center point atau titik pusat dari percobaan yang dilakukan, dimana semua kondisi faktor menggunakan nilai pada titik pusat. Terlihat meski titik pusat memiliki nilai respon pada wilayah merah, namun letaknya tidak tepat di tengah lingkaran kontur terdalam, melainkan sedikit bergeser ke kanan. Kondisi tersebut menunjukkan bahwa nilai respon terbaik akan diperoleh dengan mengondisikan faktor-faktor tidak pada titik titik pusat, tetapi sedikit bergeser ke arah kiri.
Pada rentang suhu yang ada dalam desain penelitian, nilai terendah ialah 35oC dan setiap peningkatan level nilainya naik 5oC hingga level tertinggi pada nilai 55oC. Hasil hidrolisis terbaik dari desain percobaan diperoleh pada saat perlakuan suhu 45oC, yaitu hingga 54,64%. Hasil tersebut juga didapatkan pada penelitian yang dilakukan oleh Raharja et al. (2010), hidrolisis dilaksanakan pada suhu 25oC hingga 65oC dengan kenaikan 10oC setiap tingkatnya. Hasil penelitian menunjukkan nilai tingkat hidrolisis semakin besar seiring dengan peningkatan suhu yang digunakan dan mencapai hasil terbaik pada 45oC. Tingkat hidrolisis kemudian menurun pada 55oC dan hasilnya semakin menurun tajam pada 65oC. Menurut Groggins (1958), reaksi akan berjalan cepat apabila suhu dinaikkan, hal ini terjadi karena gerakan molekul menjadi lebih cepat seiring meningkatnya suhu. Kecepatan reaksi hidrolisis akan meningkat hingga dua kali pada setiap kenaikan suhu 10oC. Meski demikian, perlu diperhatikan bahwa protein merupakan penyusun utama enzim yang dapat terdenaturasi pada suhu tertentu. Suhu yang terlalu tinggi akan menyebabkan kerusakan struktur enzim yang akan mengakibatkan enzim menjadi terdeaktivasi, sehingga proses hidrolisis menjadi terhambat.
Selain suhu, kondisi pH berpengaruh penting pada proses hidrolisis. Penggunaan buffer dengan pH tertentu akan menjaga pH, karena aktivitas lipase sangat sensitif terhadap pH. Pada penelitian ini didapatkan tingkat hidrolisis terbaik pada saat kondisi pH 5, sedangkan pada pH dibawah dan di atas 5 tingkat hidrolisisnya terhitung lebih rendah. Kondisi pH dalam suatu reaksi sebaiknya tidak terlalu asam maupun basa karena akan menurunkan kecepatan reaksi dengan terdenaturasinya enzim. Pada umumnya enzim akan memiliki kestabilan dan kinerja yang baik pada pH 4,5-8 (Williamson dan Fieser, 1992). Rendahnya tingkat hidrolisis pada pH diatas 5 tersebut kemungkinan dikarenakan enzim mulai terdenaturasi sehingga aktivitasnya menurun.
Titik biru membantu peneliti melihat posisi tepat di tengah pada kontur terdalam. Titik biru inilah nilai respon yang diharapkan dapat diperoleh berdasarkan perhitungan dari software. Garis putus-putus berwarna hitam pada gambar dibuat untuk mempermudah perkiraan posisi perlakuan pada faktor suhu dan pH. Terlihat bahwa nilai respon terbaik diharapkan akan didapatkan jika kondisi suhu lebih kecil dari 45oC yang merupakan titik pusat. Kondisi tersebut masih sesuai dalam rentang suhu yang sebaiknya digunakan dalam hidrolisis enzimatik. Sedangkan faktor pH dikondisikan sedikit lebih tinggi dari nilai titik pusat, yaitu 5. Namun, nilai pastinya akan diperoleh menggunakan perhitungan dengan Design Expert.
4.3.2.
Faktor Suhu dan Penambahan Air (AC)
20 viskositas substrat yang digunakan. Pada plot data yang ditampilkan dalam grafik kontur, terlihat nilai respon optimum yang diharapkan mendekati titik pusat. Plot grafik ini dilakukan pada rentang 40oC hingga 50oC untuk faktor suhu dan rentang 4% ⁄ hingga 6% ⁄ untuk faktor penambahan air. Rentang tersebut merupakan rentang nilai respon optimum dapat terlihat dengan jelas karena nilainya yang dekat dengan titik pusat.
Gambar 7(a) menampilkan grafik 3D-surface untuk kombinasi faktor suhu dan penambahan air terhadap respon. Bentuknya yang menyerupai parabola terlihat seimbang dan titik tertinggi berada di tengah lengkungan. Informasi lain yang diperoleh dari perhitungan ANOVA ialah adanya nilai F-hitung kombinasi kedua faktor ini. Nilai F-hitung sebesar 0,76 menunjukkan bahwa kombinasi faktor suhu dan penambahan air memberikan pengaruh yang nyata terhadap respon dalam hidrolisis minyak ikan lemuru menggunakan Amano Lipase A dari Aspergillus niger.
Seperti ditampilkan pada Gambar 7(b), grafik kontur menunjukkan bahwa perlakuan suhu yang digunakan pada penelitian belum tepat untuk menghasilkan nilai respon optimum. Ketika ditarik garis vertikal ke bawah dari titik biru yang merepresentasikan nilai respon optimum, terlihat suhu sebaiknya dikondisikan sedikit dibawah 45oC. Apabila dibandingkan dengan suhu optimum pada spesifikasi lipase, nilai tersebut juga sedikit bergeser. Pengujian spesifikasi lipase yang digunakan seperti yang ditampilkan pada Lampiran 2 menunjukkan bahwa Amano Lipase A dari
Aspergillus niger akan bekerja dengan baik pada suhu optimum 45oC. Pergeseran nilai suhu ini oleh berbagai hal, diantaranya pada penentuan titik pusat di orde pertama hanya dilakukan pengamatan faktor tunggal, sehingga ketika dilakukan kombinasi faktor tersebut dengan faktor lainnya akan mempengaruhi proses yang berlangsung dalam hidrolisis. Selain itu, pergeseran tersebut terjadi karena adanya keterbatasan pada model yang tidak mampu merepresentasikan faktor-faktor lain yang juga mempengaruhi respon. Meski demikian, kondisi suhu yang tidak bergeser jauh dari spesifikasi lipase akan diverifikasi kembali sehingga dapat diketahui ketepatan kondisi tersebut dalam menghasilkan respon yang optimum.
21 (a)
(b)
Gambar 7. (a) Grafik 3D-surface respon permukaan proses hidrolisis pada perlakuan suhu dan penambahan air
(b) Grafik kontur respon permukaan proses hidrolisis pada perlakuan suhu dan penambahan air
4.3.3.
Faktor Suhu dan Kecepatan Pengadukan (AD)
Kombinasi faktor lain yang juga mempengaruhi hidrolisis minyak ikan ialah suhu dan kecepatan pengadukan. Plot data pada grafik kontur untuk faktor suhu dipetakan pada rentang 40oC hingga 50oC, sedangkan faktor kecepatan pengadukan pada rentang 150 hingga 250 rpm.
T
in
g
k
at
Hid
ro
lis
[image:36.595.159.528.94.596.2]22 Gambar 8(a) menampilkan plot data pada grafik 3D-surface yang memiliki bentuk seperti parabola. Puncak tertinggi pada grafik terlihat tidak persis berada di tengah-tengah, hal ini dikarenakan pergeseran kondisi kecepatan pengadukan yang cukup besar sehingga grafik sedikit lebih tinggi pada bagian kiri yang merepresentasikan faktor kecepatan pengadukan. Pada perhitungan ANOVA, diketahui bahwa kombinasi kedua faktor ini memiliki nilai F-hitung yang paling besar dibandingkan nilai F-hitung kombinasi faktor lainnya, yaitu 0,77. Nilai ini menunjukkan kombinasi faktor suhu dan kecepatan pengadukan memberikan pengaruh yang paling nyata terhadap respon. Perubahan perlakuan pada kedua faktor ini akan sangat mempengaruhi nilai respon yang dihasilkan.
Pada Gambar 8(b) terlihat bahwa titik pusat pada percobaan memiliki hasil yang berada dalam lingkaran kontur terdalam. Hal ini menunjukkan nilai respon pada titik pusat percobaan telah mendekati nilai respon optimum yang diharapkan. Diberikan bantuan dengan menambahkan titik biru pada kontur terdalam yang menampilkan titik respon yang diharapkan seharusnya berada. Ketika ditarik garis vertikal ke bawah, pada kombinasi ini suhu dikondisikan sedikit ke arah kiri dari titik pusat atau juga dapat dipahami sebagai kondisi suhu lebih kecil dari titik pusat.
Pada saat hidrolisis berjalan pada suhu yang tidak sesuai, proses hidrolisis akan terhambat. Terhambatnya proses hidrolisis tentunya juga akan mempengaruhi hasil hidrolisis yang terjadi. Menurut Fu (1995), lipase mampu menghidrolisis minyak dan lemak pada kisaran suhu 30-40oC. Pada kondisi suhu di atas dan dibawah optimalnya, aktivitas enzim akan berkurang. Peningkatan suhu mulai dari 50oC secara bertahap enzim akan menjadi inaktif karena denaturasi protein, sedangkan pada suhu yang sangat rendah enzim tidak benar-benar rusak namun aktivitasnya akan sangat berkurang.
23 (a)
(b)
Gambar 8. (a) Grafik 3D-surface respon permukaan proses hidrolisis pada perlakuan suhu dan kecepatan pengadukan
(b) Grafik kontur respon permukaan proses hidrolisis pada perlakuan suhu dan kecepatan pengadukan
4.3.4.
Faktor pH dan Penambahan Air (BC)
[image:38.595.136.518.91.595.2]24 hidrolisis, seperti diketahui bahwa pH akan mempengaruhi kinerja dari enzim lipase yang digunakan sedangkan jumlah air yang ditambahkan akan mempengaruhi aktivasi enzim dan proses hidrolisis yang berlangsung. Air yang digunakan pada penelitian ini adalah air yang telah disuling atau yang juga dikenal dengan akuades. Sebelum ditambahkan pada campuran bahan, dilakukan pengukuran pH terhadap air yang ditambahkan. Air tersebut memiliki pH netral yang bernilai 7, sedangkan buffer yang ditambahkan bervariasi tergantung kondisi pH pada desain percobaan.
Gambar 9(a) memperlihatkan grafik 3D-surface dari plot data penelitian yang dilakukan. Grafik ini berbentuk menyerupai parabola dan terlihat seimbang pada kedua sisi, titik pusat percobaan pun terletak tepat di tengah parabola. Hal ini menunjukkan hasil percobaan yang baik karena kondisi faktor yang diharapkan akan mengoptimumkan respon mendekati titik pusat percobaan.
Pada Gambar 9(b) ditampilkan grafik kontur kombinasi faktor pH dan penambahan air. Pada kombinasi kedua faktor, titik merah yang menyimbolkan titik pusat percobaan terlihat berada di lingkaran kontur terdalam. Apabila diberikan titik biru yang menyimbolkan respon optimum yang diharapkan, terlihat titik pusat percobaan tidak terletak jauh dari titik biru tersebut. Hal ini menunjukkan hasil perlakuan percobaan telah mendekati hasil respon yang diharapkan, sehingga kondisi faktor yang ada tidak bergeser terlalu jauh. Ketika ditarik garis secara horizontal ke arah kiri terlihat bahwa penambahan air sebaiknya sedikit lebih banyak dari 5% ⁄ , sedangkan ketika ditarik garis vertikal ke bawah diketahui bahwa nilai respon akan optimum apabila kondisi pH sedikit di atas 5. Berdasarkan hasil analisa lipase yang digunakan oleh Amano Pharmaceutical Manufacturing Co. seperti yang terlihat pada Lampiran 2, diketahui Amano Lipase A dari Aspergillus niger bekerja dengan baik pada pH 6,5 namun hasil percobaan menunjukkan bahwa tingkat hidrolisis tertinggi dicapai ketika pH pada kondisi di bawahnya. Kemungkinan hal ini disebabkan kondisi pengujian yang berbeda oleh Amano Pharmaceutical Manufacturing Co. dengan kondisi hidrolisis yang dilakukan selama penelitian ini. Adanya tambahan bahan-bahan yang juga berbeda dengan kondisi saat pengujian dapat mempengaruhi hasil.
Buffer juga dikenal dengan larutan penyangga, yaitu larutan yang mampu mempertahankan pH atau juga dapat didefinisikan sebagai larutan yang nilai pH-nya tidak mengalami perubahan apabila ditambahkan sedikit asam kuat maupun basa kuat. Buffer asam terbentuk dari campuran asam lemah dengan basa konjugasinya (A-), sedangkan buffer basa terbentuk dari campuran basa lemah dan asam konjugasinya (B-). Buffer asam akan mempertahankan pH pada daerah bernilai pH dibawah 7, sebaliknya untuk buffer basa akan menjaga pH tetap berada pada pH di atas 7.
25 lipase serta meningkatkan fleksibilitas dan mobilitas enzim dalam menghidrolisis substratnya. Ketika suatu campuran ditambahkan H2O, air tersebut akan terurai menjadi H+ dan OH-, namun konsentrasinya sangat kecil sehingga dapat diabaikan dan tidak akan mengganggu nilai pH.
(a)
(b)
Gambar 9. (a) Grafik 3D-surface respon permukaan proses hidrolisis pada perlakuan pH dan penambahan air
[image:40.595.140.529.159.700.2]26
4.3.5.
Faktor pH dan Kecepatan Pengadukan (BD)
Kombinasi faktor pH dan kecepatan pengadukan memiliki nilai F-hitung sebesar 0,25 pada perhitungan ANOVA. Nilai ini cukup rendah apabila dibandingkan dengan kombinasi faktor-faktor sebelumnya. Nilai tersebut mengindikasikan pengaruh kombinasi kedua faktor pada respon. Rendahnya nilai F-hitung menunjukkan bahwa kombinasi faktor pH dan kecepatan pengadukan tidak memberikan pengaruh yang nyata pada respon tingkat hidrolisis.
Seperti yang telah diketahui dari pembahasan sebelumnya bahwa pH akan mempengaruhi kinerja dan stabilitas enzim lipase yang digunakan, dengan penggunaan buffer diharapkan mampu mempertahankan pH selama hidrolisis berlangsung. Apabila dilihat dari grafik kontur kombinasi kedua faktor diketahui bahwa pH yang menghasilkan respon optimum terletak sedikit di atas 5, sedangkan faktor kecepatan pengadukan pada kondisi lebih dari 200 rpm. Pergeseran faktor kecepatan pengadukan cukup jauh dari titik respon optimum yang diharapkan. Hal ini juga mempengaruhi plot data pada grafik 3D-surface yang cenderung lebih tinggi pada permukaan lengkungan di sebelah kiri.
Setiap enzim memiliki pH optimal yang menjaga kinerja maupun strukturnya dalam suatu lingkungan tempat enzim bekerja. Perubahan pH media