PENGARUH EKSTRAK ETANOL DAUN BANGUN-BANGUN
(Plectranthus amboinicus, (Lour.) Spreng) TERHADAP
PENGHAMBATAN DEGRANULASI MASTOSIT
YANG TERSENSITISASI AKTIF PADA
MENCIT JANTAN SECARA IN VITRO
SKRIPSI
OLEH:
RONAL
NIM 111524079
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGARUH EKSTRAK ETANOL DAUN BANGUN - BANGUN
(Plectranthus amboinicus, (Lour.) Spreng) TERHADAP
PENGHAMBATAN DEGRANULASI MASTOSIT
YANG TERSENSITISASI AKTIF PADA
MENCIT JANTAN SECARA IN VITRO
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
RONAL
NIM 111524079
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 12 Oktober 2013 Pembimbing I,
Poppy Anjelisa Z. Hasibuan, M.Si., Apt. NIP 197506102005012003
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah melimpahkan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan
skripsi yang berjudul “Pengaruh Ekstrak Etanol Daun Bangun-Bangun
(Plectranthus amboinicus, (Lour.) Spreng) Terhadap Penghambatan
Degranulasi Mastosit Yang Tersensititasi Aktif Pada Mencit Jantan Secara In Vitro”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar
sarjana farmasi pada Fakultas Farmasi Universita Sumatera Utara.
Pada kesempatan ini penulis menyampaikan terima kasih yang sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan beserta pembantu Dekan Fakultas Farmasi Universitas Sumatera Utara yang telah
memberikan bantuan dan fasilitas selama masa pendidikan.
2. Ibu Dra. Salbiah, M.Si., Apt., selaku penasehat akademik yang memberikan bimbingan kepada penulis selama proses perkuliahan.
3. Ibu Poppy Anjelisa Z. Hasibuan, M.Si., Apt., dan Ibu Marianne, S.Si., M.Si., Apt., yang telah membimbing dengan penuh kesabaran, tulus dan
ikhlas selama penelitian dan penulisan skripsi ini berlangsung.
4. Ibu Prof. Dr. Rosidah, M.Si., Apt., Poppy Anjelisa Z. Hasibuan, M.Si., Apt., Drs. Saiful Bahri, M.S., Apt., dan Ibu Dra. Suwarti Aris, M.Si., Apt., selaku
5. Bapak dan Ibu staff pengajar Fakultas Farmasi Universitas Sumatera Utara yang telah mendidik penulis selama perkuliahan.
6. Ibu Dra. Suwarti Aris, M.Si., Apt., selaku Kepala Laboratorium
Farmakognosi, dan Marianne, S.Si., M.Si., Apt., selaku Kepala Laboratorium Farmakologi dan toksikologi.
7. Ayahanda Arisman Tambunan dan Ibunda Mastiara Pasaribu (alm), atas doa dan dukungan baik moril maupun materil, abang dan kakak, Sahat
Tambunan, Rosmelinda Naingolan, serta adik-adik tersayang, Joel Tambuan, Erni tambunan, dan juga Juni Dariyatyi Bancin, atas doa, dorongan dan semangat dalam penyelesaian Skripsi ini.
Penulis menyadari bahwa skripsi ini masih banyak kekurangannya, oleh karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari
semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, Oktober 2013 Penulis,
Ronal
PENGARUH EKSTRAK ETANOL DAUN BANGUN - BANGUN (Plectranthus amboinicus (Lour.) Spreng) TERHADAP
PENGHAMBATAN DEGRANULASI MASTOSIT YANG TERSENSITISASI AKTIF PADA
MENCIT JANTAN SECARA IN VITRO
ABSTRAK
Mastosit merupakan sumber penting dalam respon imun yang berpengaruh terhadap terjadinya reaksi alergi. Reaksi alergi terjadi karena adanya ikatan antara antigen dengan antibodi Imunoglobulin E (IgE) akan menyebabkan degranulasi mastosit dan basofil sehingga melepaskan mediator-mediator kimia seperti : histamin, prostaglandin, bradikinin, dan asam arakidonat. Tumbuhan bangun-bangun (Plectranthus amboinicus, (Lour.) Spreng, merupakan salah satu tumbuhan yang daunnya diduga memiliki aktivitas sebagai antialergi. Tujuan dari penelitian ini adalah untuk mengetahui pengaruh ekstrak etanol daun bangun-bangun terhadap penghambatan degranulasi mastosit yang tersensitisasi aktif pada mencit jantan secara in vitro.
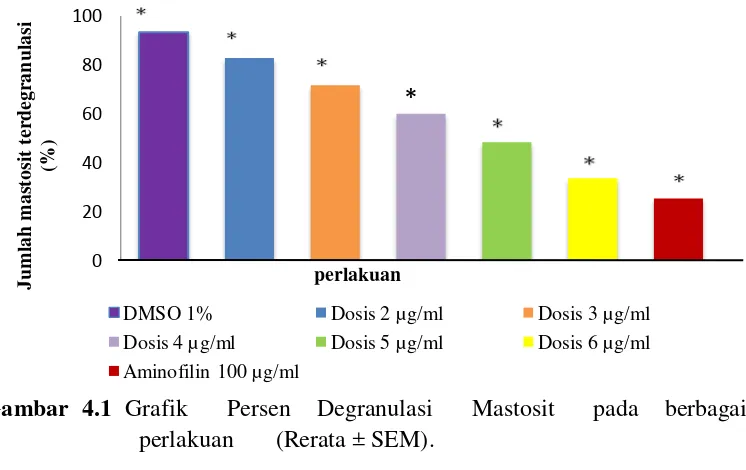
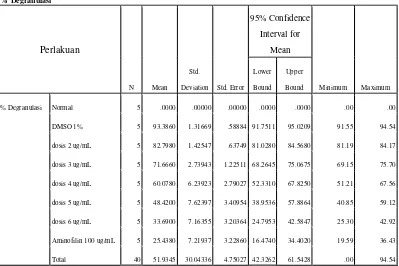
Pengujian dilakukan terhadap mencit jantan, yaitu diberi antigen putih telur ayam 50% untuk mensensititasi aktifkan mastositnya. Mastosit yang terdegranulasi diwarnai dengan larutan biru toluidin. Ekstrak etanol daun bangun-bangun (EEDBB) dengan dosis 2 µg/ml, 3 µ g/ml, 4 µ g/ml, 5 µ g/ml, 6 µg/ml sebagai bahan uji. Aminofilin dosis 100 µg/ml sebagai kontrol positif, dan larutan DMSO 1% sebagai kontrol negatif yang tidak diberikan EEDBB maupun aminofilin. Kemampuan ekstrak etanol daun bangun-bangun dalam menghambat degranulasi mastosit dilihat dari persen penurunan jumlah mastosit yang terdegranulasi. Dari hasil pengujian terhadap penghambatan degranulasi mastosit didapatkan kemampuan ekstrak etanol daun bangun-bangun dosis 2 µg/ml sebesar 82,79%, dosis 3 µg/ml sebesar 71,66%, dosis 4 µg/ml sebesar 60,07%, dosis 5 µ g/ml sebesar 48,42%, dosis 6 µg/ml sebesar 33,69%, kontrol positif (aminofilin 100 µg/ml) sebesar 25,43% dan kontrol negatif (DMSO 1%) sebesar 93,38%.
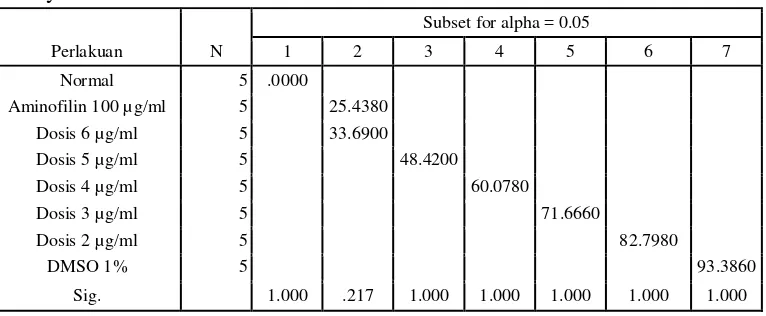
Dari hasil pengujian statistik, pemberian ekstrak etanol daun bangun-bangun mampu menghambat degranulasi mastosit tersensitisasi aktif secara signifikan terhadap kontrol negatif (p < 0,05). Dengan demikian disimpulkan bahwa ekstrak etanol daun bangun-bangun mempunyai aktivitas penghambatan degranulasi mastosit tersensitisasi aktif pada mencit jantan secara in vitro.
EFFECT OF ETHANOLIC EXTRACT OF PLECTRANTHY LEAVES
(Plectranthus amboinicus, (Lour.) Spreng) ON THE INHIBITION OF ACTIVE SENSITIZED MASTOCYTE DEGRANULATION mediators such as histamine, prostaglandins, bradykinin, arachidonic acid. Bangun-bangun (Plectranthus amboinicus, (Lour.) Spreng is a plant and its leaf has an activity as antiallergy. The objective of this study is to know the effect of amboinicus leaves ethanol extract on the inhibition of active sensitized mastocyte degranulation of male mice in vitro.
In this study tested to male mice, against mastocyte in actively sensitized by antigen hen egg white 50%. Staining of mastocyte degranulation is used toluidine blue. Amboinicus leaves ethanol extract (EEDBB) with the dose of 2 µg/ml, 3 µg/ml, 4 µg/ml, 5 µg/ml, 6 µg/ml as sample. Aminophylline dose of 100 µg/ml as a positive control, and hen egg white antigen 50% as a negative control which is not given both of (EEDBB) and aminophylline. The ability of amboinicus leaves ethanol extract in inhibits mastocyte degranulation seen from the percent reduction in the number of degranulated mastocyte.
From the results of mastocyte degranulation inhibition testing, it found that the ability of ethanol extract of amboinicus leaves at dose 2 µg/ml was 82.79%, dose 3 µg/ml was 71.66%, dose 4 µg/ml was 60.07%, dose 5 µg/ml was 48.42%, dose 6 µ g/ml was 33.69%, positive control (aminofilin 100 µg/ml) was 25.43% and negative control (DMSO 1%) was 93.38%.
From the results of statistical testing, administraton of amboinicus leaves ethanol extract is able to inhibited the degranulation of active sensitized mastocyte significantly to the negative control group (p < 0.05). Thus concluded that amboinicus leaves ethanolic extract has effects to inhibit the degranulation of active sensitized mastocyte of male mice in vitro.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGHANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Perumusan Masalah ... 4
1.3Hipotesis ... 4
1.4Tujuan Penelitian ... 4
1.5Manfaat penelitian ... 4
1.6Kerangka Pikir Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian Tumbuhan ... 6
2.1.1 Sistematika tumbuhan ... 6
2.1.3 Nama asing ... 7
2.1.4 Penggunaan tumbuhan ... 7
2.2 Ekstraksi ... 7
2.2.1 Metode ekstraksi ... 8
2.3 Aminofilin ... 9
2.4 Sistem Imun ... 11
2.4.1 Imunitas ... 11
2.5Alergi ... 12
2.6 Imunoglobulin ... 13
2.6.1 Klasifikasi imunoglobulin ... 14
2.6.1.1Imunoglobulin G ... 14
2.6.1.2Imunoglobulin A ... 14
2.6.1.3Imunoglobulin M ... 14
2.6.1.4Imunoglobulin D ... 15
2.6.1.5Imunoglobulin E ... 15
2.7 Mastosit ... 16
2.8 Reaksi Hipersensitivitas ... 18
BAB III METODE PENELITIAN ... 21
3.1Alat dan Bahan ... 21
3.1.1 Alat-alat ... 21
3.1.2 Bahan-bahan ... 22
3.2Hewan Percobaan ... 22
3.3Penyiapan Tumbuhan ... 23
3.3.2 Identifikasi Tumbuhan ... 23
3.3.3 Pengolahan Tumbuhan ... 23
3.4 Skrining Fitokimia Serbuk Simplisia ... 24
3.4.1 Pemeriksaan alkaloid ... 24
3.4.2 Pemeriksaan flavonoid ... 24
3.4.3 Pemeriksaan tanin ... 25
3.4.4 Pemeriksaan glikosida ... 25
3.4.5 Pemeriksaan saponin ... 25
3.4.6 Pemeriksaan steroida/triterpenoida ... 26
3.5 Karakterisasi Simplisia ... 26
3.5.1 Penetapan kadar air simplisia ... 26
3.5.2 Penetapan kadar sari yang larut dalam air ... 27
3.5.3 Penetapan kadar sari yang larut dalam etanol ... 27
3.5.4 Penetapan kadar abu total ... 28
3.5.5 Penetapan kadar abu tidak larut asam ... 28
3.6 Skrining Fitokimia Ekstrak Etanol Daun Bangun-bangun ... 28
3.6.1 Pemeriksaan alkaloid ... 28
3.6.2 Pemeriksaan flavonoida ... 29
3.6.3 Pemeriksaan tanin ... 29
3.6.4 Pemeriksaan glikosida ... 30
3.6.5 Pemeriksaan saponin ... 30
3.6.6 Pemeriksaan steroida/triterpenoida ... 30
3.7 Pembuatan Ekstrak Etanol Daun Bangun-bangun ... 31
3.9 Uji Aktivitas Penghambatan Degranulasi Mastosit ... 31
3.9.1 Penyiapan sediaan ... 31
3.9.2 Penyiapan larutan antigen putih telur ayam 50% ... 32
3.9.3 Penyiapan larutan phosphate buffered saline (PBS) ... 32
3.9.4 Penyiapan larutan biru toluidin ... 32
3.9.5 Penyiapan larutan trypan blue 0,4% ... 32
3.9.6 Penyiapan larutan ekstrak etanol daun bangun-bangun .. 33
3.9.7 Penyiapan larutan aminofilin 100 µg/ml ... 33
3.9.8 Penyiapan hewan percobaan ... 34
3.9.9 Cara perhitungan sel pada hemocytometer ... 35
3.9.10 Penyiapan suspensi mastosit ... 35
3.9.11 Uji ketahanan sel (Cell Viability Test) ... 36
3.9.12 Uji degranulasi mastosit tersensitisasi aktif ... 37
3.9.13 Perhitungan jumlah mastosit terdegranulasi ... 38
3.10 Analisis Data ... 38
BAB IV HASIL DAN PEMBAHASAN ... 40
4.1 Simplisia dan Ekstrak ... 40
4.2 Pengujian Efek Antialergi ... 41
4.3 Hasil Analisa Statistik ... 46
BAB V KESIMPULAN DAN SARAN ... 48
5.1 Kesimpulan ... 48
5.2 Saran ... 48
DAFTAR PUSTAKA ... 49
DAFTAR TABEL
Tabel Halaman
4.1 Hasil Karakterisasi Simplisia Daun Bangun-Bangun ... 40
4.2 Hasil Skrining Fitokima Simplisia Daun Bangun-Bangun ... 40
4.3 Hasil Karakterisasi Ekstrak Etanol Daun Bangun-Bangun ... 41
4.4 Hasil Skrining Fitokima Ekstrak Etanol Daun Bangun-Bangun .... 41
DAFTAR GAMBAR
Gambar Halaman
1.1 Diagram Kerangka Pikir Penelitian ... 5
2.1 Rumus Aminofilin ... 10
2.2 Mekanisme Umum Saat Terjadi Reaksi Alergi ... 13
2.3 Ikatan Silang Antigen-Antibodi ... 15
2.4 Bagian Hemositometer ... 17
2.5 Bentuk Kamar Hitung Pada Hemositometer ... 17
DAFTAR LAMPIRAN
Lampiran Halaman
1. Data Hasil Penelitian ... 52
2. Identifikasi Tumbuhan ... 58
3. Bagan Kerja Penelitian ... 59
4. Gambar Tumbuhan Bangun-Bangun ... 60
5. Gambar Alat Penelitian ... 62
6. Gambar Hewan Percobaan ... 64
7. Gambar Isolasi Mastosit Dari Peritoneal Mencit dan Pengukuran Mastosit Pada Hemocytometer ... 65
8. Rumus Thompson ... 71
9. Perhitungan Konsentrasi Larutan Uji Ekstrak Etanol Daun Bangun-Bangun (EEDBB) ... 72
10. Perhitungan Konsentrasi Larutan Uji Aminopilin 100 µg/ml dan antigen putih telur ayam 50% ... 74
11. Perhitungan Uji Ketahanan Sel (Cell Viability Test) ... 75
12. Perhitungan Jumlah Sel Pada Hemositometer ... 76
PENGARUH EKSTRAK ETANOL DAUN BANGUN - BANGUN (Plectranthus amboinicus (Lour.) Spreng) TERHADAP
PENGHAMBATAN DEGRANULASI MASTOSIT YANG TERSENSITISASI AKTIF PADA
MENCIT JANTAN SECARA IN VITRO
ABSTRAK
Mastosit merupakan sumber penting dalam respon imun yang berpengaruh terhadap terjadinya reaksi alergi. Reaksi alergi terjadi karena adanya ikatan antara antigen dengan antibodi Imunoglobulin E (IgE) akan menyebabkan degranulasi mastosit dan basofil sehingga melepaskan mediator-mediator kimia seperti : histamin, prostaglandin, bradikinin, dan asam arakidonat. Tumbuhan bangun-bangun (Plectranthus amboinicus, (Lour.) Spreng, merupakan salah satu tumbuhan yang daunnya diduga memiliki aktivitas sebagai antialergi. Tujuan dari penelitian ini adalah untuk mengetahui pengaruh ekstrak etanol daun bangun-bangun terhadap penghambatan degranulasi mastosit yang tersensitisasi aktif pada mencit jantan secara in vitro.
Pengujian dilakukan terhadap mencit jantan, yaitu diberi antigen putih telur ayam 50% untuk mensensititasi aktifkan mastositnya. Mastosit yang terdegranulasi diwarnai dengan larutan biru toluidin. Ekstrak etanol daun bangun-bangun (EEDBB) dengan dosis 2 µg/ml, 3 µ g/ml, 4 µ g/ml, 5 µ g/ml, 6 µg/ml sebagai bahan uji. Aminofilin dosis 100 µg/ml sebagai kontrol positif, dan larutan DMSO 1% sebagai kontrol negatif yang tidak diberikan EEDBB maupun aminofilin. Kemampuan ekstrak etanol daun bangun-bangun dalam menghambat degranulasi mastosit dilihat dari persen penurunan jumlah mastosit yang terdegranulasi. Dari hasil pengujian terhadap penghambatan degranulasi mastosit didapatkan kemampuan ekstrak etanol daun bangun-bangun dosis 2 µg/ml sebesar 82,79%, dosis 3 µg/ml sebesar 71,66%, dosis 4 µg/ml sebesar 60,07%, dosis 5 µ g/ml sebesar 48,42%, dosis 6 µg/ml sebesar 33,69%, kontrol positif (aminofilin 100 µg/ml) sebesar 25,43% dan kontrol negatif (DMSO 1%) sebesar 93,38%.
Dari hasil pengujian statistik, pemberian ekstrak etanol daun bangun-bangun mampu menghambat degranulasi mastosit tersensitisasi aktif secara signifikan terhadap kontrol negatif (p < 0,05). Dengan demikian disimpulkan bahwa ekstrak etanol daun bangun-bangun mempunyai aktivitas penghambatan degranulasi mastosit tersensitisasi aktif pada mencit jantan secara in vitro.
EFFECT OF ETHANOLIC EXTRACT OF PLECTRANTHY LEAVES
(Plectranthus amboinicus, (Lour.) Spreng) ON THE INHIBITION OF ACTIVE SENSITIZED MASTOCYTE DEGRANULATION mediators such as histamine, prostaglandins, bradykinin, arachidonic acid. Bangun-bangun (Plectranthus amboinicus, (Lour.) Spreng is a plant and its leaf has an activity as antiallergy. The objective of this study is to know the effect of amboinicus leaves ethanol extract on the inhibition of active sensitized mastocyte degranulation of male mice in vitro.
In this study tested to male mice, against mastocyte in actively sensitized by antigen hen egg white 50%. Staining of mastocyte degranulation is used toluidine blue. Amboinicus leaves ethanol extract (EEDBB) with the dose of 2 µg/ml, 3 µg/ml, 4 µg/ml, 5 µg/ml, 6 µg/ml as sample. Aminophylline dose of 100 µg/ml as a positive control, and hen egg white antigen 50% as a negative control which is not given both of (EEDBB) and aminophylline. The ability of amboinicus leaves ethanol extract in inhibits mastocyte degranulation seen from the percent reduction in the number of degranulated mastocyte.
From the results of mastocyte degranulation inhibition testing, it found that the ability of ethanol extract of amboinicus leaves at dose 2 µg/ml was 82.79%, dose 3 µg/ml was 71.66%, dose 4 µg/ml was 60.07%, dose 5 µg/ml was 48.42%, dose 6 µ g/ml was 33.69%, positive control (aminofilin 100 µg/ml) was 25.43% and negative control (DMSO 1%) was 93.38%.
From the results of statistical testing, administraton of amboinicus leaves ethanol extract is able to inhibited the degranulation of active sensitized mastocyte significantly to the negative control group (p < 0.05). Thus concluded that amboinicus leaves ethanolic extract has effects to inhibit the degranulation of active sensitized mastocyte of male mice in vitro.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Imunitas merupakan suatu mekanisme untuk mengenal suatu zat atau
bahan yang dianggap sebagai benda asing terhadap dirinya, selanjutnya tubuh akan mengadakan tanggapan (respon imun) dengan berbagai cara, seperti
netralisasi atau melenyapkan, dengan akibat tidak selalu menguntungkan bagi tubuh yaitu terjadinya kerusakan jaringan tubuh sendiri (Subowo, 2009).
Respon imun adalah respon tubuh berupa satu urutan kejadian yang
kompleks terhadap antigen, untuk mengeliminasi antigen tersebut. Respon imun ini dapat melibatkan berbagai macam sel dan protein, terutama sel
makrofag, sel limfosit, komplemen, dan sitokin yang saling berinteraksi secara kompleks. Mekanisme pertahanan tubuh terdiri atas mekanisme pertahanan non spesifik dan mekanisme pertahanan spesifik (Akip, dkk., 2010).
Respon imun non spesifik (innate immunity) merupakan imunitas alamiah yang telah ada sejak lahir. Imunitas ini tidak ditujukan hanya untuk
satu jenis antigen, tetapi untuk berbagai macam antigen, jadi bukan merupakan pertahanan khusus untuk antigen tertentu. Respon imun spesifik merupakan mekanisme pertahanan yang ditujukan khusus terhadap satu jenis antigen,
karena itu tidak dapat berperan terhadap antigen jenis lain. Imun spesifik mampu mengenali kembali antigen yang pernah dijumpainya (memiliki
Pada beberapa kondisi, salah satu efek samping imunitas yang penting adalah timbulnya alergi atau hipersensitivitas imun lainnya. Ada beberapa tipe alergi dan hipersensitivitas lainnya, beberapa diantaranya hanya terjadi pada
orang yang mempunyai kecenderungan alergi yang spesifik (Hall, 2007). Bila suatu alergen spesifik disuntikkan secara langsung ke dalam
sirkulasi, maka alergen tersebut dapat bereaksi dengan basofil dalam darah dan mastosit pada jaringan yang terletak di luar pembuluh darah kecil, jika basofil
dan mastosit tersebut telah disensititasi oleh pelekatan reagin IgE. Oleh karena itu terjadilah reaksi alergi yang luas di seluruh pembuluh darah dan jaringan yang berkaitan erat. Hal ini disebut anafilaksis. Basofil dan mastosit yang
teraktivasi juga melepaskan suatu campuran leukotrien substansi anafilaksis bereaksi-lambat. Leukotrien-leukotrien dapat menyebabkan spasme otot polos
bronkiolus, sehingga menimbulkan serangan seperti asma dan kadang-kadang menimbulkan kematian akibat mati lemas (Hall, 2007).
Mastosit berisi simpanan histamin tubuh dan terdapat pada hampir
seluruh jaringan. Dalam mastosit, histamin berikatan dengan heparin pada granula sitoplasma. Secara normal pelepasan histamin melibatkan influks ion
Ca2+, permebilitas membran sel terhadap ion Ca2+ berkurang ketika kadar adenosin monofosfat siklik (cAMP) intraseluler meningkat, obat-obat yang
menstimulasi sintesis cAMP (agonis adrenoseptor 2) mengurangi pelepasan
histamin (Neal, 2006).
Menurut Kaliappan dan Viswanathan (2008) dan Mangathayaru (2008),
banyak ditemukan di India dan Ceylon dan Afrika Selatan, memiliki bunga yang bentuknya tajam dan mengandung minyak atsiri sehingga disebut juga Coleus aromaticus. Daun tanaman ini juga telah dibuktikan sebagai
antiinflamasi karena bekerja menghambat respon inflamasi yang diinduksi oleh siklooksigenase, juga terbukti sebagai anti kanker dan anti tumor (Anonima,
2013). Manfaat lain dari tumbuhan bangun-bangun adalah sebagai obat asthma dan bronchitis, dan khasiat lainnya yang perlu diteliti lebih lanjut (Dalimartha,
2008).
Berdasarkan penelitian yang dilakukan oleh Santosa dan Hartiani (2005), yang menguji ekstrak air daun bangun-bangun terhadap sel netrofil
tikus putih, menyatakan daun bangun-bangun mengandung senyawa polifenol, saponin, glikosida, flavonol dan minyak atsiri. Daun bangun-bangun memiliki
efek anti alergi dengan cara pemberian ekstrak daun bangun-bangun terhadap tikus dengan dosis sebesar 19,0 g/kg BB dan 13,5 g/kg BB, mampu memberikan efek fagositosis sel netrofil sebesar 80% pada pengamatan hari
ke-60. Selanjutnya dijelaskan oleh Choudhary (2010) bahwa tumbuhan yang mengandung flavonoid telah dilaporkan mempunyai efek antihistamin dan
berperan dalam proses penghambatan degranulasi mastosit.
Berdasarkan uraian di samping, peneliti tertarik untuk melakukan uji aktivitas penghambatan degranulasi mastosit yang tersensitisasi aktif secara in
1.2 Perumusan Masalah
Berdasarkan latar belakang, maka perumusan masalah pada penelitian ini adalah apakah ekstrak etanol daun bangun-bangun dapat menghambat
degranulasi mastosit yang tersensitisasi aktif secara in vitro pada mencit jantan.
1.3 Hipotesis
Hipotesis pada penelitian ini yaitu ekstrak etanol daun bangun-bangun dapat menghambat degranulasi mastosit yang tersensitisasi aktif secara in vitro
pada mencit jantan.
1.4Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui efek anti alergi
ekstrak etanol daun bangun-bangun melalui penghambat degranulasi mastosit yang tersensitisasi aktif secara in vitro pada mencit jantan.
1.5 Manfaat Penelitian
Manfaat dari penelitian ini adalah sebagai berikut:
a. Mengembangkan daun bangun-bangun menjadi suatu sediaan herbal terstandar dengan efek anti alergi.
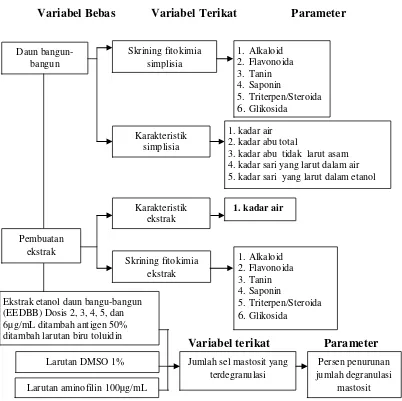
1.6 Kerangka Pikir Penelitian
Adapun kerangka pikir penelitian ini dapat dilihat pada Gambar 1.1 berikut:
Variabel Bebas Variabel Terikat Parameter
Variabel terikat Parameter
Gambar 1.1 Diagram kerangka pikir penelitian Daun 4. kadar sari yang larut dalam air
5. kadar sari yang larut dalametanol
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Tumbuhan bangun-bangun (Plectranthus amboinicus,(Lour). Spreng), sebutan yang lazim dipakai suku Batak, merupakan salah satu menu sayuran
sehari-hari yang digunakan masyarakat Sumatera Utara dan terutama disajikan untuk ibu-ibu yang baru melahirkan. Tanaman ini diperkirakan berasal dari
India, kemudian tersebar dikawasan tropika dan pantropika (Dalimartha, 2008). 2.1.1 Sistematika tumbuhan
Menurut Pandey (2003), sistematika tanaman bangun-bangun adalah
sebagai berikut:
Divisi : Spermatophyta
Sub divisi : Angiospermae Kelas : Dicotyledoneae Ordo : Solanales
Famili : Lamiaceae Suku : Plectranthus
Spesies : Plectranthus amboinicus Lour. Spreng. Sinonim : Coleus amboinicus Lour
2.1.2 Nama daerah
Sumatera: bangun-bangun, daun hati-hati, sukan, tramun. Jawa: ajeran, acerang (Sunda), daun jintan, daun kucing, daun kambing. Nusatenggara: iwak,
2.1.3 Nama asing
Inggris: Caraway seed atau cemin. Cina: Panling moung (Hariana, 2008).
2.1.4Penggunaan tumbuhan
Daun bangun-bangun (Plectranthus amboinicus (Lour.) Spreng)
digunakan sebagai obat sariawan, obat batuk, karminatif, meningkatkan keluarnya ASI (laktagoga), analgesik, antipiretik, antiseptik (Dalimartha,
2008).
2.2 Ekstraksi
Ekstraksi berasal dari kata “extrahere”, “to draw out”, yaitu suatu cara
untuk menarik satu atau lebih zat dari asalnya. Umumnya zat berkhasiat
tersebut dapat ditarik, namun khasiatnya tidak berubah. Tujuan utama ekstraksi adalah mendapatkan atau memisahkan sebanyak mungkin zat-zat yang
memiliki khasiat pengobatan dari zat-zat yang tidak dibutuhkan, agar lebih mudah dipergunakan (kemudahan diabsorpsi, rasa, dan pemakaian) dan disimpan dibandingkan simplisia asal, dan tujuan pengobatannya lebih terjamin
(Syamsuni, 2006). Hasil ekstraksi disebut dengan ekstrak, yaitu sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau
simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan. Simplisia yang digunakan dalam proses
2.2.1 Metode Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair
(Depkes, 2000)
Ekstraksi dengan menggunakan pelarut dapat dilakukan dengan beberapa cara
yaitu :
1. Cara dingin
a. Maserasi
Maserasi adalah proses ekstraksi simplisia dengan menggunakan pelarut dengan beberapa kali pengadukan pada temperatur ruangan (Depkes, 2000).
b. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses ini terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) (Depkes, 2000).
2. Cara panas a. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada
b. Soxhlet
Soxhlet adalah ekstraksi menggunakan pelarut yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah
pelarut relatif konstan dengan adanya pendingin balik (Depkes, 2000). c. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur yang lebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada
temperatur 40-50 (Depkes, 2000).
d. Infus
Infus adalah sediaan cair yang dibuat dengan menyari simplisia nabati
dengan air pada suhu 90 selama 15 menit (Depkes, 1979).
e. Dekok Dekok adalah sediaan cair yang dibuat dengan menyari simplisia nabati dengan air pada waktu yang lebih lama ± 30 menit dangan temperatur sampai
titik didih air (Depkes, 2000).
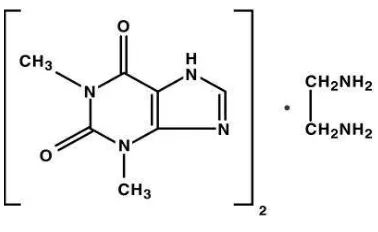
2.3 Aminofilin
Aminofilin (suatu kompleks teofilin-etilendiamin) merupakan preparat
teofilin yang paling umum digunakan untuk penyakit asma yang diinduksi alergi. Aminofilin memiliki kelarutan yang lebih besar daripada teofilin sehingga senyawa ini lebih sering digunakan untuk sediaan asma. Struktur
Gambar 2.1 Aminofilin (Depkes RI, 1995)
Nama kimia : 1H-Purin-2,6-dione, 3,7-dihidro- 1,3-dimetil dengan 1,2- etilendiamin (2:1)
Rumus molekul : C16H24N20O4.2H2O Berat molekul : 456,46
Pemerian : Butir atau serbuk putih atau agak kekuningan, bau ammonia
lemah, rasa pahit. Jika dibiarkan di udara terbuka, perlahan- lahan kehilangan etilena-diamina dan menyerap karbon
dioksida dengan melepaskan teofilin.
Kandungan : Tidak kurang dari 84,0% dan tidak lebih dari 87,4% teofilin anhidrat, C7H8N4O2, dihitung terhadap zat anhidrat.
Kelarutan : 1 g aminofilin larut dalam 25 ml air (Depkes RI, 1995). Adapun mekanisme kerja dari teofilin yaitu dengan cara menghambat
enzim fosfodiesterase sehingga mencegah pemecahan cAMP dan cGMP masing-masing menjadi 5’-AMP dan 5’-GMP. Penghambatan fosfodiesterase menyebabkan akumulasi cAMP dan cGMP dalam sel sehingga menyebabkan
2.4 Sistem Imun
Yang dimaksudkan dengan sistem imun ialah semua mekanisme yang digunakan badan untuk mempertahankan keutuhan tubuh sebagai perlindungan
terhadap bahaya yang dapat ditimbulkan berbagai bahan dalam lingkungan hidup. Lingkungan hidup manusia yang tercemar berbagai bahan organik dan
anorganik, baik yang hidup seperti bakteri, virus, jamur, parasit maupun yang mati. Debu dan polusi, yang setiap saat dapat masuk kedalam tubuh dapat
menimbulkan kerusakan jaringan atau penyakit (Baratawidjaja, 1996). 2.4.1 Imunitas
Imunitas merupakan suatu mekanisme untuk mengenal suatu zat atau
bahan yang dianggap sebagai benda asing terhadap dirinya, selanjutnya tubuh akan mengadakan tanggapan (respon imun) dengan berbagai cara, seperti
netralisasi atau melenyapkan, dengan akibat tidak selalu menguntungkan bagi tubuh yaitu terjadinya kerusakan jaringan tubuh sendiri (Subowo, 2009).
Respon imun adalah respon tubuh berupa satu urutan kejadian yang
kompleks terhadap antigen, untuk mengeliminasi antigen tersebut. Respon imun ini dapat melibatkan berbagai macam sel dan protein, terutama sel
makrofag, sel limfosit, komplemen, dan sitokin yang saling berinteraksi secara kompleks. Mekanisme pertahanan tubuh terdiri atas mekanisme pertahanan non spesifik dan mekanisme pertahanan spesifik (Akip, 2010).
Respon imun non spesifik (innate immunity) merupakan imunitas alamiah yang telah ada sejak lahir. Imunitas ini tidak ditujukan hanya untuk satu jenis
mekanisme pertahanan tubuh yang ditujukan khusus terhadap satu jenis antigen, karena itu tidak dapat berperan terhadap antigen jenis lain. Imun spesifik mampu mengenali kembali antigen yang pernah dijumpainya
(memiliki memori), sehingga paparan berikutnya akan meningkatkan efektifitas mekanisme pertahanan tubuh (Kresno, 2003).
2.5 Alergi
Prinsip alergi adalah suatu keadaan yang disebabkan oleh reaksi imunologik
yang spesifik, atau suatu keadaan yang ditimbulkan oleh alergen atau antigen, sehingga terjadi gejala-gejala patologik. Pada individu yang rentan terhadap
alergi, paparan dengan alergen menyebabkan aktivasi sel Th2 dan memproduksi antibodi IgE. Reaksi kerusakan jaringan yang disebabkan oleh respon imun tersebut merupakan reaksi hipersensitivitas dan istilah alergi
sering disamakan oleh hipersensitivitas (Lease, 2010).
Reaksi alergi terjadi ketika antibodi IgE terikat dengan afinitas tinggi
melelui bagian Fc dengan reseptor FcεRI pada mastosit. Tubuh tidak akan
menunjukan reaksi apa-apa saat alergen masuk pertama kali, karena tubuh masih membutuhkan waktu yang disebut masa sensitisasi. Sensitisasi
merupakan proses pelapisan mastosit oleh IgE. Pelapisan ini menyebabkan mastosit menjadi sensitif bila terjadi paparan ulang oleh alergen yang sama.
Apabila mastosit yang telah tersensitisasi terpapar kembali oleh alergen yang sama, sel akan teraktivasi mengeluarkan mediator. Aktivasi mastosit ini terjadi sebagai hasil ikatan alergen dengan 2 atau lebih antibodi IgE pada mastosit
Salah satu yang paling berperan dalam reaksi patologi sistem imun adalah imunoglobulin E (IgE), yang menstimulasi jaringan mastosit. Antibodi IgE dihasilkan saat antigen berikatan dengan reseptor Fc pada mastosit. Ketika
mastosit berhubungan dengan antibodi yang berikatan silang dengan antigen, mastosit diaktifkan secara cepat untuk mengeluarkan berbagai mediator seperti
histamin, prostaglandin, serotonin dan lain-lain. Mediator-mediator ini secara bersamaan meningkatkan permeabilitas pembuluh darah, pelebaran pembuluh
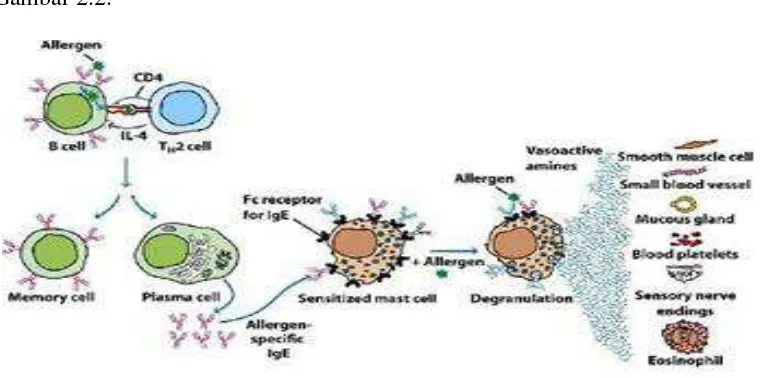
darah bronkus, otot polos berkontraksi dan inflamasi lokal (Abbas dan Lichtman, 2004). Mekanisme umum saat terjadi alergi dapat dilihat pada Gambar 2.2.
Gambar 2.2 Mekanisme umum saat terjadi reaksi alergi (Baratawidjaja, 2012).
2.6 Imunoglobulin
Imunoglobulin merupakan substansi utama pertama yang diidentifikasi sebagai molekul dalam serum yang mampu menetralkan sejumlah
mikroorganisme penyebab infeksi. Molekul ini disintesis oleh sel B dalam 2 bentuk yang berbeda, yaitu sebagai reseptor permukaan (untuk mengikat
ekstraselular. Imunoglobulin merupakan molekul glikoprotein yang terdiri atas komponen polipeptida sebanyak 82-92% dan selebihnya karbohidrat (Kresno, 2003).
2.6.1 Klasifikasi imunoglobulin
Imunoglobulin dikenal dengan 5 kelas utama.
2.6.1.1 Imunoglobulin G (IgG)
IgG mempunyai rantai beratnya adalah , merupakan imunoglobulin
utama yang dibentuk atas rangsangan antigen. IgG dapat menembus plasenta dan masuk kedalam peredaran darah janin, sehingga bayi baru lahir IgG yang berasal dari ibulah yang melindungi bayi terhadap infeksi. Dalam serum orang
dewasa normal, IgG merupakan 75% dari imunoglobulin total (Kresno, 2003).
2.6.1.2 Imunoglobulin A (IgA)
IgA mempunyai rantai beratnya adalah α. IgA ditemukan dalam jumlah sedikit dalam serum, tetapi kadarnya dalam cairan sekresi saluran napas, saluran cerna, saluran kemih, air mata, keringat, ludah dan air susu lebih tinggi.
IgA dalam serum dapat mengaglutinasikan dan mengganggu motilitas kuman sehingga memudahkan fagositosis (Bratawidjaja, 1996).
2.6.1.3 Imunoglobulin M (IgM)
IgM dalam serum biasanya berbentuk pentamer, dan banyak diproduksi pada awal respon imun primer. IgM merupakan antibodi yang paling efesien
2.6.1.4 Imunoglobulin D (IgD)
Imunoglobulin D merupakan monomer dan konsentrasinya dalam serum hanya sedikit, tetapi konsentrasinya dalam darah tali pusat cukup tinggi.
Peran biologiknya sebagai antibodi humoral belum jelas, yang telah diketahui adalah perannya sebagai antibodi dalam reaksi hipersensitifitas terhadap
penisilin.
2.6.1.5 Imunoglobulin E (IgE)
Kadar imunoglobulin E dalam serum orang dewasa normal sangat rendah, tetap dapat meningkat pada orang yang menderita hipersensitivitas. Selain itu imunoglobulin E dapat dijumpai dalam cairan sekresi. Salah satu
sifat penting dari IgE adalah kemampuannya melekat secara erat pada permukaan mastosit atau basofil melalui reseptor Fc. Terikatnya bagian Fc
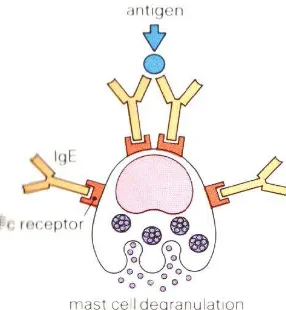
antibodi dengan reseptor pada mastosit, diikuti oleh ikatan silang molekul yang berdekatan oleh antigen, memicu degranulasi oleh suatu mekanisme yang melibatkat influks Ca2+ (Kresno, 2003). Ikatan silang atibodi-antigen yang
menyebabkan degranulasi mastosit dapat dilihat pada Gambar 2.3.
2.7 Mastosit
Mastosit merupakan sel-sel besar bulat dengan penuh butir-butir dalam sitoplasmanya, yang dapat diperlihatkan dengan pewarnaan biru toluidin.
Efektor utama dalam reaksi hipersensititivitas tipe I adalah mastosit yang umumnya terdapat dalam jaringan pengikat di sekitar pembuluh darah, dinding
mukosa usus, dan saluran pernapasan. Sel mastosit berisi simpanan histamin tubuh dan terdapat pada hampir seluruh jaringan. Dalam mastosit, histamin
berikatan dengan heparin pada granula sitoplasma. Secara normal pelepasan histamin melibatkan influks ion Ca2+, permeabilitas membran sel terhadap ion Ca2+ berkurang ketika kadar adenosin monofosfat siklik (cAMP) intraseluler
meningkat, obat-obat yang menstimulasi sintesis cAMP (agonis adrenoseptor
2) mengurangi pelepasan histamin (Subowo, 2009; Neal, 2006).
Identifikasi sel mastosit bisa dilakukan dengan beberapa pewarnaan, misalnya dengan biru toluidin, alcian blue, safranin. Pewarnaan sel mast yang sering digunakan toluidin dan alcian blue. Sel akan teramati cukup jelas pada
pewarnaan biru toluidin dibanding alcian blue. Biru toluidin akan mewarnai sel mast dengan warna merah-ungu (pewarnaan metakromatik) (Nugroho, 2011).
Jumlah sel dihitung dengan menggunakan bilik hitung improved Neubauer (hemositometer). Suspensi sel diambil 10 μl kemudian diletakkan ke
dalam bilik hitung (hemositometer), setelah itu ditutup dengan gelas penutup.
Pada saat menutup dengan gelas penutup gelembung udara tidak boleh terbentuk. Hemositometer yang telah berisi suspensi sel kemudian diamati di
sedangkan sel yang terletak di tepi bilik bagian kanan dan bawah tidak dihitung.
Gambar 2.4 Bagian dari hemositometer.
1 mm
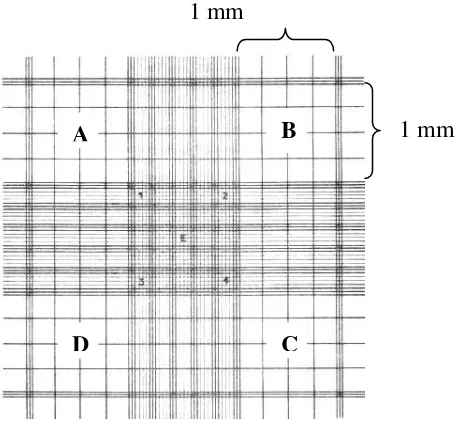
Gambar 2.5 Bentuk kamar hitung pada hemositometer.
Rata-rata jumlah sel (n) diperoleh dari sel yang ada di setiap kamar dibagi menjadi 4. Panjang setiap kamar adalah 1 mm dan tinggi 0,1 mm, sehingga
volume setiap kamar = 0,1 mm3 (1,0 mm2 x 0,1 mm).
A B
D C
Penghitungan jumlah sel per ml adalah sebagai berikut (Bijanti et al, 2002): Volume tiap bujur sangkar =1/4 mm x 1/4 mm x 1/10 mm = 1/160 mm3 Volume tiap kamar hitung =16 x 1/160 = 0,1 mm3
= 0,1 x 10-3 cm3 = 10-4 cm3
= 10-4 ml
=
Metode pewarnaan yang tradisional digunakan untuk uji ketahanan sel
adalah dengan trypan blue. Trypan blue adalah pewarna yang tertinggal pada sel yang mati dengan warna biru yang khas ketika dilihat di bawah mikroskop, sedangkan sel yang sehat tidak menunjukkan warna. Sel yang sehat memiliki
membran sel yang utuh karenanya tidak menyerap medium disekitarnya. Di sisi lain, sel yang tidak sehat tidak mempunyai membran yang utuh dan
menyerap medium disekitarnya (Louis, 2011).
Hitung jumlah sel per ml dengan rumus (Louis, 2011):
2.8 Reaksi Hipersensitivitas
pertumbuhan kanker, tetapi dapat pula menimbulkan hal yang tidak menguntungkan bagi tubuh berupa penyakit yang disebut reaksi hipersensitivitas. Hipersensitivitas ialah peningkatan reaktivitas atau
sensitivitas terhadap antigen yang pernah dikenal sebelumnya. Reaksi hipersensitivitas dibagi atas 4 tipe reaksi berdasarkan kecepataan terjadinya
dan mekanisme imun yang terjadi (Baratawidjaja, 2012). a. Reaksi tipe I
Reaksi tipe I disebut juga reaksi cepat, terjadi hanya dalam hitungan detik, menghilang dalam 2 jam. Alergen yang masuk kedalam tubuh akan menimbulkan respon imun dengan dibentuknya IgE yang kemudian diikat oleh
reseptor Fc pada permukaan sel mastosit atau basofil. Bila tubuh terpapar oleh antigen yang sama, dan berikatan dengan molekul IgE yang sebelumnya sudah
melekat pada permukaan sel mastosit atau basofil, maka hal ini akan menyebabkan degranulasi mastosit. Degranulasi tersebut mengeluarkan mediator antara lain ialah histamin.
b. Reaksi tipe II
Reaksi tipe II yang disebut juga reaksi sitotoksik terjadi oleh karena dibentuk
oleh antibodi jenis IgG dan IgM terhadap antigen yang merupakan bagian sel penjamu.
c. Reaksi tipe III
Reakasi ini disebut juga reaksi kompleks imun terjadi akibat penimbunan kompleks antigen-antibodi dalam jaringan atau pembuluh darah. Antigen
d. Reaksi tipe IV
Reaksi tipe IV yang juga disebut reaksi tipe lambat, timbul lebih dari 24 jam setelah tubuh terpapar oleh antigen. Reaksi terjadi karena respon sel T yang
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah penelitian eksperimental. Penelitian meliputi beberapa tahapan yaitu penyiapan sampel, karakterisasi
simplisia, karakterisasi ekstrak, skrining fitokimia serbuk simplisia, skrining fitokimia ekstrak, pembuatan ekstrak, pembuatan sediaan, penyiapan hewan
percobaan, dan pengujian penghambatan degranulasi mastosit pada hewan percobaan secara in vitro dengan menggunakan alat improved neubauer hemocytometer. Data hasil penelitian dianalisis secara ANAVA (analisis
variansi) dan dilanjutkan dengan uji Post Hoc Tukey meggunakan program SPSS 17 (Statistical Product and Service Solution).
3.1Alat dan Bahan
3.1.1 Alat-alat
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas,
aluminium foil, blender (National), oven listrik, neraca listrik (Vibra), seperangkat alat destilasi penetapan kadar air, rotary evaporator (Heidolph
WB 2000), seperangkat alat bedah, spuit 1 ml dan 10 ml, improved neubauer hemocytometer (Marienfield), alat sentrifuge (Dynamic), waterbath, termometer, mikroskop (Boeco), neraca hewan, microtube, pipet mikro
3.1.2 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah daun bangun-bangun, etanol 96% (destilasi), toluen (p.a), putih telur ayam, aminofilin
injeksi, dimetil sulfoksida (DMSO), larutan NaCl fisiologis 0,9%, kalium iodida, merkuri (II) klorida, bismut nitrat, asam nitrat, iodium, asam asetat
anhidrat, asam sulfat 98%, amil alkohol, kloroform, besi (III) klorida, timbal (II) asetat, natrium hidroksida, asam klorida 37%, metanol (teknis), etil asetat
(teknis), serbuk seng, serbuk magnesium, isopropanol, biru toluidin, trypan blue 0,4%, gelatin 0,1 %, heparin, asam asetat glasial, formaldehid 37%, natrium klorida (NaCl), kalium klorida (KCl), dinatrium hidrogen fosfat
(Na2HPO4), kalium dihidrogen fosfat (KH2PO4),aqua bidestilasi.
3.2 Hewan Percobaan
Hewan percobaan yang digunakan dalam penelitian adalah mencit jantan sehat dengan berat 35 gram berumur 3 bulan sebanyak 5 ekor yang
diambil cairan intraperitonealnya untuk perlakuan degranulasi mastosit tersensitisasi aktif. Sebelum digunakan sebagai hewan percobaan, semua mencit dipelihara terlebih dahulu selama satu minggu untuk penyesuaian
lingkungan, mengontrol kesehatan dan berat badan serta menyeragamkan makanannya. Mencit yang sehat ditandai dari berat badan yang tetap atau
3.3 Penyiapan Tumbuhan
Penyiapan tumbuhan meliputi pengambilan tumbuhan, identifikasi tumbuhan dan pengolahan tumbuhan.
3.3.1 Pengambilan Tumbuhan
Pengambilan tumbuhan daun bangun-bangun dilakukan secara purposif
yaitu tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. sampel diperoleh di, Jl. Pales V No. 57 Pokok Mangga Padang Bulan,
Simpang Selayang Medan, Provinsi Sumatera Utara. 3.3.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang
Botani Pusat Penelitian Biologi-LIPI Bogor.
3.3.3 Pengolahan Tumbuhan
Bahan baku daun bangun-bangun yang masih segar dikumpulkan, dibuang bagian yang tidak diperlukan (sortasi basah), dicuci bersih di bawah air mengalir, ditiriskan, dan ditimbang berat basahnya (7.765 g). Selanjutnya
dikeringkan dengan menggunakan lemari pengering dengan tujuan agar daun tidak membusuk pada saat proses pengeringan. Daun kering ditandai dengan
daun mudah diremukkan, kemudian daun ditimbang kembali sebagai berat kering (870 g) lalu diblender dan ditimbang sebagai berat serbuk simplisia (793 g). Serbuk simplisia dimasukkan ke dalam wadah plastik, diberi etiket dan
3.4Skrining Fitokimia Serbuk Simplisia
Skrining fitokimia serbuk simplisia meliputi pemeriksaan alkaloida, pemeriksaan flavonoida, pemeriksaan tanin, pemeriksaan glikosida,
pemeriksaan saponin, pemeriksaan steroid/triterpenoid.
3.4.1 Pemeriksaan alkaloida
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2
menit, didinginkan lalu disaring. Filtrat dipakai untuk percobaan berikut (Ditjen POM, 1995):
a. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereksi Mayer akan
terbentuk endapan berwarna putih atau kuning
b. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereksi Bouchardat akan
terbentuk endapan berwarna coklat-hitam
c. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereksi Dragendorff akan terbentuk endapan berwarna merah atau jingga.
Alkaloida dinyatakan positif jika terjadi endapan atau terjadi endapan paling sedikit dua atau tiga dari percobaan di atas.
3.4.2 Pemeriksaan flavonoida
Sebanyak 0,5 g serbuk simplisia ditambahkan 100 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas. Kedalam 5 ml
filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika
3.4.3 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia disari dengan 10 ml air suling lalu
disaring, filtratnya diencerkan dengan air suling sampai tidak berwarna. Diambil 2 ml larutan dan ditambahkan 1-2 tetes pereaksi besi (III) klorida
1%. Jika terjadi warna biru kehitaman atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.4.4 Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g kemudian disari dengan 30 ml campuran 7 bagian volume etanol 96% dan 3 bagian volume air suling,
selanjutnya ditambahkan 10 ml HCl 2 N, dipanaskan selama 10 menit, didinginkan dan disaring. Pada 30 ml filtrat ditambahkan 25 ml air suling dan
25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan selama 5 menit lalu disaring. Filtrat disari sebanyak 3 kali, tiap kali dengan 20 ml campuran 3 bagian volume kloroform dan 2 bagian volume isopropanol. Diambil lapisan
air kemudian ditambahkan 2 ml air dan 5 tetes pereaksi Molisch, ditambahkan hati-hati 2 ml asam sulfat pekat terbentuk cincin warna ungu pada batas kedua
cairan menunjukkan adanya ikatan gula (Ditjen POM, 1995). 3.4.5 Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisia dimasukkan ke dalam tabung reaksi
dan ditambahkan 10 ml air suling panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik, timbul busa yang mantap tidak kurang dari 10 menit
3.4.6 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml eter selama 2
jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa dalam cawan penguap ditambahkan 2 tetes asam asetat anhidrat dan 1 tetes
asam sulfat pekat. Timbul warna ungu atau merah kemudian berubah menjadi hijau kebiruan menunjukkan adanya steroida triterpenoida (Harborne,
1987).
3.5 Karakterisasi Simplisia
Karakterisasi simplisia meliputi pemeriksaan penetapan kadar air, penetapan kadar sari yang larut dalam air, penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total, dan penetapan kadar abu tidak larut
asam (Ditjen POM, (1995).
3.5.1 Penetapan kadar air simplisia
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluene). Alat terdiri dari labu alas bulat 500 ml, alat penampung, pendingin, tabung penyambung dan tabung penerima (WHO, 1998).
Cara penetapan:
Kedalam labu bulat dimasukkan 200 ml toluene dan 2 ml air suling, didestilasi
selama 2 jam. Setelah toluen mendidih, kecepatan tetesan diatur 2 tetes per detik sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes per detik sampai semua air terdestilasi. Setelah itu
Kemudian kedalam labu alas bulat dimasukkan 5 g serbuk simplisia yang telah ditimbang, Setelah 2 jam didestilasi, kemudian toluene dibiarkan dingin, bagian dalam pendingin dibilas dengan toluene yang telah dijenuhkan.
Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin sampai suhu kamar. Setelah air dan toluene memisah sempurna,
volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa.
Kadar air dihitung dalam persen.
3.5.2 Penetapan kadar sari yang larut dalam air
Sebanyak 5 gram serbuk simplisia, dimaserasi selama 24 jam dalam
100 ml air kloroform (2,5 ml kloroform dalam air suling 1000 ml) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18
jam, kemudian disaring. Diuapkan 20 ml filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105°C sampai bobot tetap. Kadar dalam persen sari
yang larut dalam air dihitung terhadap bahan yang telah dikeringkan di udara (Ditjen POM, 1995).
3.5.3 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 gram serbuk simplisia, dimaserasi selama 24 jam dalam etanol 96% dalam labu bersumbat sambil sesekali dikocok selama 6 jam
pertama, dibiarkan selama 18 jam, kemudian disaring. Diuapkan 20 ml filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan
persen sari yang larut dalam etanol (96%) dihitung terhadap bahan yang telah dikeringkan di udara (Ditjen POM, 1995).
3.5.4 Penetapan kadar abu total
Sebanyak 2 gram serbuk yang telah digerus dan ditimbang seksama dimasukkan dalam krus platina atau krus silikat yang telah dipijar dan ditara,
kemudian diratakan. Krus dipijar perlahan-lahan sampai arang habis, pemijaran dilakukan pada suhu 600°C selama 3 jam. Kemudian didinginkan dan
ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan di udara (Ditjen POM, 1995).
3.5.5 Penetapan kadar abu tidak larut asam
Abu yang telah diperoleh dalam penetapan abu dididihkan dengan 25 ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring dengan kertas masir atau kertas saring bebas abu, cuci dengan air panas, dipijarkan sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bobot
yang dikeringkan di udara (Ditjen POM, 1995).
3.6 Skrining Fitokimia Ekstrak Etanol Daun Bangun-bangun
Skrining fitokimia ekstrak etanol daun bangun-bangun meliputi pemeriksaan alkaloida, pemeriksaan flavonoida, pemeriksaan tanin,
pemeriksaan glikosida, pemeriksaan saponin, pemeriksaan steroid/triterpenoid.
3.6.1 Pemeriksaan alkaloida
Ekstrak ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam
menit, didinginkan lalu disaring. Filtrat dipakai untuk percobaan berikut (Ditjen POM, 1995):
a. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereksi Mayer akan
terbentuk endapan berwarna putih atau kuning
b. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereksi Bouchardat akan
terbentuk endapan berwarna coklat-hitam
c. Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereksi Dragendorff
akan terbentuk endapan berwarna merah atau jingga.
Alkaloida dinyatakan positif jika terjadi endapan atau terjadi endapan paling sedikit dua atau tiga dari percobaan di atas.
3.6.2 Pemeriksaan flavonoida
Sebanyak 0,5 g serbuk simplisia ditambahkan 100 ml air panas,
dididihkan selama 5 menit dan disaring dalam keadaan panas. Kedalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika
terjadi warna merah, kuning, jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3 Pemeriksaan tanin
Sebanyak 0,5 g ekstrak disari dengan 10 ml air suling lalu disaring, filtratnya diencerkan dengan air suling sampai tidak berwarna. Diambil 2 ml
larutan dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%. Jika terjadi warna biru kehitaman atau hijau kehitaman menunjukkan adanya tanin
3.6.4 Pemeriksaan glikosida
Ekstrak ditimbang sebanyak 3 g kemudian disari dengan 30 ml campuran 7 bagian volume etanol 96% dan 3 bagian volume air suling,
selanjutnya ditambahkan 10 ml HCl 2 N, dididihkan selama 10 menit, didinginkan dan disaring. Pada 30 ml filtrat ditambahkan 25 ml air suling dan
25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan selama 5 menit lalu disaring. Filtrat disari sebanyak 3 kali, tiap kali dengan 20 ml campuran 3
bagian volume kloroform dan 2 bagian volume isopropanol. Diambil lapisan air kemudian ditambahkan 2 ml air dan 5 tetes pereaksi Molisch, ditambahkan hati-hati 2 ml asam sulfat pekat terbentuk cincin warna ungu pada batas kedua
cairan menunjukkan adanya ikatan gula (Ditjen POM, 1995).
3.6.5 Pemeriksaan saponin
Sebanyak 0,5 g ekstrak dimasukkan ke dalam tabung reaksi dan ditambahkan 10 ml air suling panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik, timbul busa yang mantap tidak kurang dari 10 menit setinggi
1-10 cm. Ditambahkan 1 tetes larutan asam klorida 2 N, bila buih tidak hilang menunjukkan adanya saponin (Ditjen POM, 1995).
3.6.6 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g ekstrak dimaserasi dengan 20 ml eter selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa dalam cawan penguap
ditambahkan 2 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat. Timbul warna ungu atau merah kemudian berubah menjadi hijau
3.7 Pembuatan Ekstrak Daun Bangun-bangun
Pembuatan ekstrak dilakukan secara maserasi dengan menggunakan
pelarut etanol 96%. Caranya, serbuk simplisia (700 g) dimasukkan kedalam bejana yang tertutup, cairan penyari dituangi sampai semua simplisia terendam
dan ditutup, dibiarkan selama 5 hari terlindung dari cahaya sambil sesekali diaduk. Kemudian, setelah 5 hari campuran tersebut diserkai, ampasnya
dimaserasi dengan etanol 96% disimpan dalam bejana tertutup dan dibiarkan di tempat sejuk, terlindung dari cahaya selama 2 hari, kemudian dienaptuangkan. Maserat yang diperoleh dipekatkan dengan alat rotary evaporator sehingga
diperoleh ekstrak kental (Depkes RI, 1979).
3.8 Pemeriksaan Karakterisasi Ekstrak Daun Bangun-bangun
Pemeriksaan karakterisasi ekstrak daun bangun-bangun sama seperti
karakterisasi yang dilakukan pada simplisia meliputi penetapan kadar air, penetapan adar abu total, dan penetapan kadar abu tidak larut dalam asam.
3.9 Uji Aktivitas Penghambatan Degranulasi Mastosit
Uji aktivitas penghambatan degranulasi mastosit meliputi penyiapan sediaan,
penyiapan hewan percobaan dan uji degranulasi mastosit tersentisasi aktif. 3.9.1 Penyiapan sediaan
Penyiapan sediaan meliputi penyiapan larutan antigen putih telur ayam
ekstrak etanol daun bangun-bangun (EEDBB) dengan berbagai konsentrasi, penyiapan larutan aminofilin 100 µg/ml (Alvianti, dkk., 2012).
3.9.2 Penyiapan larutan antigen putih telur ayam 50%
Sebanyak 5 ml putih telur ayam ditambahkan dalam 5 ml NaCl fisiologis 0,9%, kemudian dilakukan pengenceran dengan mengambil 5 ml
larutan di atas lalu dicukupkan volumenya hingga 10 ml dengan larutan NaCl fisiologis 0,9% sehingga diperoleh induk, kemudian diambil 5 ml larutan induk
dan dicukupkan volumenya hingga 10 ml dengan larutan NaCl fisiologis 0,9% sehingga diperoleh konsentrasi 50% (Alvianti, dkk., 2012).
3.9.3 Penyiapan larutan phosphate buffered saline (PBS)
Phosphate Buffered Saline (PBS) adalah larutan penyangga yang umum digunakan dalam penelitian. Pembuatan PBS dilakukan dengan cara sebagai
berikut: sebanyak 8 gram NaCl, 0,2 gram KCl, 1,44 gram Na2HPO4, 0,24 gram KH2PO4, dilarutkan dalam 800 ml aqua bidestilasi, kemudian dicek pH dengan indikator pH hingga pH ± 7 dan dapat disesuaikan dengan penambahan HCl
atau NaOH, tambahkan aqua bidestilasi hingga 1 L (Alvianti, dkk., 2012).
3.9.4 Penyiapan larutan biru toluidin
Sebanyak 39 ml larutan NaCl fisiologis 0,9% dicampur dengan 1 ml asam asetat glasial, 10 ml formaldehid 37% (v/v) dan 50 ml etanol 95% (v/v), kemudian campuran dikocok dan ditambahkan biru toluidin sebanyak 100 mg
dan dikocok lagi hingga larut (Handayani, dkk., 2008).
3.9.5 Penyiapan larutan trypan blue 0,4%
3.9.6 Penyiapan larutan ekstrak etanol daun bangun-bangun (EEDBB)
Sebanyak 100 mg ekstrak etanol daun bangun-bangun dilarutkan dalam 1 ml larutan DMSO 1% sehingga didapatkan konsentrasi 100 mg/ml, kemudian
dilakukan pengenceran dengan mengambil 0,1 ml larutan ekstrak etanol daun bangun-bangun konsentrasi 100 mg/ml di atas lalu ditambahkan dengan larutan
DMSO 1% hingga 1 ml sehingga diperoleh konsentrasi 10.000 μg/ml,
kemudian diambil 0,1 ml larutan ekstrak etanol daun bangun-bangun
konsentrasi 10.000 μg/ml di atas dan ditambahkan dengan larutan DMSO 1% hingga volume 1 ml sehingga diperoleh konsentrasi 1.000 μg/ml, lalu diambil 0,1 ml larutan ekstrak etanol daun bangun-bangun konsentrasi 1.000 μg/ml
ditambahkan dengan larutan DMSO 1% hingga 1 ml sehingga diperoleh konsentrasi 100 ug/ml, lalu diambil 0,36 ml larutan ekstrak etanol daun
bangun-bangun konsentrasi 100 μg/ml ditambahkan dengan larutan DMSO 1% hingga 6 ml sehingga diperoleh konsentrasi 6 ug/ml, demikian seterusnya
sampai diperoleh konsentrasi 5 μg/ml, 4 μg/ml, γ μg/ml, β μg/ml. Perhitungan
terlampir pada Lampiran 9, halaman 71.
3.9.7 Penyiapan larutan aminofilin 100 µg/ml
Sebanyak β1 μl larutan aminofilin injeksi dengan konsentrasi dosis 24
mg/ml, dipipet dengan menggunakan mikropipet dan dimasukkan ke dalam labu tentukur 5 ml. Kemudian dilakukan pengenceran dengan penambahan
larutan dimetil sulfoksida (DMSO) 1% hingga 5 ml, sehingga diperoleh
konsentrasi 100 μg/ml (Alvianti, dkk., β01β). Perhitungan terlampir pada
3.9.8 Penyiapan hewan percobaan
Hewan yang digunakan adalah mencit jantan sehat dengan berat 35 g berumur 3 bulan sebanyak 5 ekor yang mendapat perlakuan yang sama. Tiap 1
ekor mencit diambil cairan intraperitonealnya dan dibagi atas 8 kelompok: Kelompok 1 (Normal):
Suspensi mastosit yang tidak diberi penambahan larutan antigen (putih telur ayam) maupun EEDBB dan aminofilin.
Kelompok 2 (Kontrol positif):
Suspensi mastosit yang diberikan larutan antigen putih telur ayam 50% dan larutan aminofilin 100 µg/ml.
Kelompok 3 (Kontrol negatif):
Suspensi mastosit yang diberikan larutan antigen putih telur
ayam 50% dan DMSO 1% tetapi tidak diberikan EEDBB ataupun aminofilin.
Kelompok 4 (Uji 1):
Suspensi mastosit yang diberikan larutan antigen putih telur ayam 50% dan EEDBB 2µ g/ml.
Kelompok 5 (Uji 2):
Suspensi mastosit yang diberikan larutan antigen putih telur ayam 50% dan EEDBB 3µ g/ml.
Kelompok 6 (Uji 3):
Suspensi mastosit yang diberikan larutan antigen putih telur
Kelompok 7 (Uji 4):
Suspensi mastosit yang diberikan larutan antigen putih telur ayam 50% dan EEDBB 5µ g/ml.
Kelompok 8 (Uji 5):
Suspensi mastosit yang diberikan larutan antigen putih telur
ayam 50% dan EEDBB 6µ g/ml.
3.9.9 Perhitungan sel pada hemocytometer
Hemositometer terdiri dari 4 kamar hitung (A, B, C, dan D), setiap kamar hitung terdiri dari 16 kotak, hitung sel pada 4 kamar hemositometer dengan menggunakan mikroskop.
Hitung jumlah sel per ml dengan rumus (Louis, 2011):
3.9.10 Penyiapan suspensi mastosit tersensitisasi aktif
Sebanyak 5 ekor mencit sehat dengan berat badan 35 g disensitisasi
oleh antigen putih telur ayam. Mencit disuntik secara intraperitoneal dengan 0,3 ml antigen putih telur ayam 50%, pada hari ke-1. Pada hari ke-3 dan hari ke-5 diulangi lagi penyuntikan antigen putih telur ayam 50% sebanyak 0,05 ml
secara intra plantar. Pada hari ke-10 setelah penyuntikan pertama dilakukan isolasi mastosit dari cairan intraperitoneal (Choudary, 2010; Vogel, 2008),
mencit dipuasakan selama 18 jam, kemudian mencit yang telah dipuasakan langsung dikorbankan dengan cara dislokasi leher dan segera disuntik dengan 10 ml larutan PBS yang telah ditambah dengan gelatin 0,1% dan heparin 50
selama 10 menit, dibedah secara hati-hati dan diambil cairan peritoneal sebanyak mungkin, masukkan ke dalam tabung sentrifuge dan sentrifuge selama 15 menit dengan kecepatan 3000 rpm, bagian supernatan dibuang dan
endapan dicuci dua kali dengan larutan PBS sama banyak, kemudian endapan diambil dan dicukupkan volume hingga 2 ml dengan larutan PBS dan siap
untuk pengujian (Alvianti, dkk., 2012).
3.9.11Uji ketahanan sel (Cell Viability Test)
Uji ketahanan sel dilakukan untuk melihat sel uji yang tetap utuh dengan penambahan larutan uji dosis maksimal dan diinkubasi selama beberapa jam. Pengujian ini menggunakan metode pewarnaan oleh trypan blue,
sel yang utuh adalah sel yang tidak berwarna, sedangkan sel yang terdegranulasi adalah sel yang berwarna biru.
Sebanyak 50 µl suspensi mastosit yang telah diisolasi dari peritoneal mencit, dimasukkan ke dalam tabung reaksi. Kemudian ditambahkan 50 µl larutan uji EEDBB 6 µg/ml dan ditepuk-tepuk secara perlahan sampai homogen. Inkubasi
pada suhu 37oC selama 1 jam. Diambil 100 µl larutan tersebut kemudian ditambahkan 100 µl larutan trypan blue 0,4% dan ditepuk-tepuk secara
perlahan sampai homogen. Teteskan larutan 10 µl di atas hemositometer dan hitung sel yang berwarna biru dibawah mikroskop dengan perbesaran 10 x 40. Persen ketahanan sel dihitung dengan rumus sebagai berikut (Sudira, 2011):
3.9.12 Uji degranulasi mastosit tersensitisasi aktif
Sebanyak 5 ekor mencit yang diambil cairan intraperitonialnya mendapat perlakuan yang sama sebagai berikut:
1. Penghitungan jumlah mastosit tersensitisasi (kelompok normal).
Sebanyak 50 µl suspensi mastosit ditambahkan 40 µl PBS, 10 µl biru
toluidin.
2. Penghitungan jumlah mastosit yang tidak terdegranulasi oleh DMSO 1%
(kelompok kontrol negatif).
Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl DMSO 1%, 10 µl antigen putih telur ayam 50%, dan 10 µl biru toluidin.
3. Pengujian aktivitas penghambatan degranulasi mastosit oleh aminofilin (kelompok kontrol positif).
Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl Aminofilin 100 µg/ml, 10 µl antigen putih telur ayam 50%, dan 10 µl biru toluidin.
4. Pengujian aktivitas penghambatan degranulasi mastosit oleh ekstrak etanol
daun bangun-bangun (kelompok uji) dengan konsentrasi sebagai berikut: - Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl EEDBB 2 µg/ml,
10 µl antigen putih telur ayam 50%, dan 10 µl biru toluidin.
- Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl EEDBB 3 µg/ml, 10 µl antigen putih telur ayam 50%, dan 10 µl biru toluidin.
- Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl EEDBB 4 µg/ml, 10 µl antigen putih telur ayam 50%, dan 10 µl biru toluidin.
- Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl EEDBB 6 µg/ml, 10 µl antigen putih telur ayam 50%, dan 10 µl biru toluidin.
Tiap campuran yang diperoleh dari tiap kelompok ditepuk-tepuk secara
perlahan agar campuran homogen, kemudian diinkubasi selama 30 menit padasuhu 37oC. Kemudian campuran diteteskan di atas hemositometer dan
dihitung jumlah mastosit di bawah mikroskop dengan pembesaran 10 x 40. mastosit yang tidak terdegranulasi akan tampak berwarna keunguan karena
adanya pewarnaan oleh larutan biru toluidin (Handayani, dkk., 2008). 3.9.13 Penghitungan persen jumlah mastosit terdegranulasi
Efek penghambatan degranulasi mastosit oleh ekstrak etanol daun
bangun-bangun ditentukan dengan menghitung jumlah mastosit yang tidak terdegranulasi menggunakan alat hemositometer. Kemudian dari jumlah
mastosit yang didapat, dihitung persentase degranulasi mastosit dengan cara sebagai berikut (Handayani, dkk., 2008).
% Degranulasi = x 100 %
Dimana:
P = Jumlah mastosit sebelum perlakuan S = Jumlah mastosit setelah perlakuan
3.10 Analisis Data
Data hasil penellitian dianalisis dengan menggunakan program SPSS. Data
hasil penelitian ditentukan homogenitas dan normalitasnya untuk menentukan analisis statistik yang digunakan. Data dianalisis dengan menggunakan uji ANAVA satu arah untuk menentukan perbedaan rata-rata di antara perlakuan.
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah penelitian eksperimental. Penelitian meliputi beberapa tahapan yaitu penyiapan sampel, karakterisasi
simplisia, karakterisasi ekstrak, skrining fitokimia serbuk simplisia, skrining fitokimia ekstrak, pembuatan ekstrak, pembuatan sediaan, penyiapan hewan
percobaan, dan pengujian penghambatan degranulasi mastosit pada hewan percobaan secara in vitro dengan menggunakan alat improved neubauer hemocytometer. Data hasil penelitian dianalisis secara ANAVA (analisis
variansi) dan dilanjutkan dengan uji Post Hoc Tukey meggunakan program SPSS 17 (Statistical Product and Service Solution).
3.2Alat dan Bahan
3.2.1 Alat-alat
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas,
aluminium foil, blender (National), oven listrik, neraca listrik (Vibra), seperangkat alat destilasi penetapan kadar air, rotary evaporator (Heidolph
WB 2000), seperangkat alat bedah, spuit 1 ml dan 10 ml, improved neubauer hemocytometer (Marienfield), alat sentrifuge (Dynamic), waterbath, termometer, mikroskop (Boeco), neraca hewan, microtube, pipet mikro