LAMPIRAN 1
DATA HASIL PERCOBAAN
L1.1 Yield Karbon Aktif
Tabel L1.1 Data Yield Karbon Aktif
No Konsentrasi Aktivator (%) Berat Raw Material (gram) Berat Karbon Aktif (gram) Yield Karbon Aktif (%) 1 2 3 20 40 60 33 15,02 15,39 15,67 45,53 46,65 47,50
L1.2 Kadar Air Karbon Aktif
Tabel L1.2 Data Kadar Air Karbon Aktif
No Karbon Aktif dengan Aktivator Berat Cawan ( gram)
Berat cawan + Karbon Aktif
(gram)
Berat cawan + Karbon Aktif
Setelah Pengeringan
Kadar Air (%)
1 20 58,2583 59,2594 59,0581 0,3408
2 40 57,5353 58,5459 58,3449 0,3445
3 60 57,2077 58,2213 57,9920 0,5141
L1.3 Kadar Abu Karbon Aktif
Tabel L1.3 Data Kadar Abu Karbon Aktif
No Karbon Aktif dengan Aktivator Berat Cawan ( gram)
Berat cawan + Karbon Aktif
(gram)
Berat cawan + Karbon Aktif
Setelah Pemanasan
Kadar Abu (%)
1 20 45,3201 46,1004 45,4140 12,034
2 40 45,3650 46,1445 45,4480 10,648
85 L1.4 Kadar Zat Menguap Karbon Aktif
Tabel L1.4 Data Kadar Zat Menguap Karbon Aktif
No Karbon Aktif dengan Aktivator Berat Cawan ( gram)
Berat cawan + Karbon Aktif
(gram)
Berat cawan + Karbon Aktif Setelah Pemanasan Kadar Zat Menguap (%)
1 20 32,60 33,60 32,72 2,62
2 40 34,28 35,28 34,40 2,49
3 60 62,59 63,59 62,65 1,48
L1.5 Data Hasil Percobaan BET
Tabel L1.5 Data Hasil Analisis BET
No Konsentrasi Aktivator (%) Luas Permukaan
(m2/g)
Volume Pori (cc/g)
Luas Area Mikropori
(m2/g)
Luas Permukaan
Ekternal (m2/g) 1 2 3 20 40 60 927,58 1215,11 1502,84 0,57 0,78 1,11 774,98 961,63 1075,99 152,60 253,48 426,84
L1.6 Data Hasil Penentuan Jumlah Logam Pb(II) yang Terjerap Karbon
Aktif
Tabel L1.6 Data Hasil Penjerapan Pb(II)
No Konsentrasi Aktivator (%) Berat karbon Aktif (gram) Konsentrassi Larutan Pb(II) (ppm) Konsentrasi Larutan Pb(II) setelah dijerap (ppm) Persentase Penjerapan (%)
1 20
3 100
26 74
2 40 34,4 65,6
L1.7 Data Hasil Pengaruh berat karbon aktif terhadap adsorpsi Pb(II) Tabel L1.7 Data Hasil Penjerapan Pb(II)
No
Berat karbon
Aktif (gram)
Konsentrasi Aktivator
(%)
C1 C2 q 1/C2 1/q Log
C2
Log q
1 1
20 100
60,4 3,96 0,016 0,252 1,781 0,597
2 2 32,8 3,36 0,030 0297 1,515 0,526
3 3 26 2,46 0,038 0,405 1,414 0,392
4 4 25 1,87 0,04 0,533 1,397 0,273
L1.8 Nilai Isoterm Langmuir dan Freunlich Penjerapan Pb(II)
Tabel L1.8 Nilai Isoterm Langmuir dan Freunlich Penjerapan Pb(II)
Model Konstanta R2
Langmuir k = 176,1 0,741
qm = 17,54 (mg/g)
87
LAMPIRAN 2
CONTOH PERHITUNGAN
L2.1 Perhitungan Yield Karbon Aktif
Berikut merupakan data hasil penentuan Yield untuk karbon aktif yang diimpregnasi dengan aktivator asam fosfat 20%.
Data percobaan: Berat raw material = 33 g Berat karbon aktif= 15,67 g
% = 45,53%
L2.2 Perhitungan Kadar Air Karbon Aktif
Berikut merupakan data hasil penentuan kadar air untuk karbon aktif yang diimpregnasi dengan aktivator asam fosfat 20%.
Data percobaan:
Berat cawan kosong = 58,2583g
Berat cawan + karbon aktif sebelum pengeringan = 59,2594 g Berat cawan + karbon aktif setelah pengeringan = 59,0581g
L2.3 Perhitungan Kadar Abu Karbon Aktif
Berikut merupakan data hasil penentuan kadar abu untuk karbon aktif yang diimpregnasi dengan aktivator asam fosfat 20%.
Data percobaan:
Berat cawan kosong (B) = 45,3201g
Berat cawan + karbon aktif sebelum pengeringan (C) = 46,1004 g Berat cawan + karbon aktif setelah pengeringan (D) = 45,4140 g
% Abu = 12,034 %
L2.4 Perhitungan Kadar Zat Menguap Karbon Aktif
Berikut merupakan data hasil penentuan kadar zat menguap untuk karbon aktif yang diimpregnasi dengan aktivator asam fosfat 20%.
Data percobaan:
Berat cawan kosong = 32,60 g
Berat cawan + karbon aktif sebelum pengeringan = 33,60 g Berat cawan + karbon aktif setelah pengeringan = 32,72 g
89
L2.5 Perhitungan Jumlah Logam Pb(II) yang Terjerap Karbon Aktif
Dalam penentuan jumlah logam Pb(II)yang terjerap maka akan digunakan salah satu karbon aktif yaitu karbon aktif yang diaktivasi dengan asam fosfat 20% dengan konsentrasi awal (Co) yang ditentukan sebesar 100 ppm dan C adalah
konsentrasi setelah analisis AAS.
L2.6 Perhitungan Konsentrasi Kesetimbangan
Berikut merupakan data hasil perhitungan isotermal adsorpsi langmuir karbon aktif yang diimpregnasi dengan aktivator asam fosfat 20%.
qf M + cf S = q M + c S
Berikut contoh perhitungannya, diketahui: qf = 0
M = 1g cf = 100 ppm
c = 60,4 ppm ( Hasil Analisa Absorpsi Serapan Atom ) S = 100 ml
M
(S) c -(S) cf (M ) qf
q
1
(100) 60,4 (100) 100 (1) 0
q
LAMPIRAN 3
FOTO PENELITIAN
L3.1 Foto Cangkang Buah Karet 100 mesh
Gambar L3.1 Cangkang Buah Karet 100 mesh
L3.2 Foto Impregnasi Cangkang Buah Karet Dengan Aktivator H3PO4
91
L3.3 Foto Alat Karbonisasi Karbon Aktif Cangkang Buah Karet
Gambar LC.3 Alat Karbonisasi Karbon Aktif Cangkang Buah Karet
L3.4 Foto Penjerapan Logam dengan Karbon Aktif Cangkang Buah Karet
DAFTAR PUSTAKA
[1] Julius Marinus Bangun, „„Kandungan Logam Berat Timbal (Pb) dan Kadmium (Cd) dalam Air, Sedimen dan Organ Tubuh Ikan Sokang (Triacanthus Nieuhofi) di Perairan Ancol, Teluk Jakarta,‟‟ Departemen Manajemen Sumberdaya Perairan Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor Bogor, 2005.
[2] Sunil Kumar Yadav, Dhruv Kumar Singh dan Shishir Sinha, “Chemical Carbonization of Papaya Seed Originated Charcoals for Sorption Of Pb(II)
From Aqueous Solution”, Journal of Environmental Chemical Engineering (2) 9–19, 2014.
[3] Quano, “Training Manual on Assesment of the Quality ond Type of Land Based Pollution Discharges Into The Marine and Coastal Environment.” Unep. Bangkok. (1993).
[4] Ashraf, Ma., Maah, Mj., dan Yusoff, I., “Study Of Banana Peel (Musa
Sapientum) As A Cationic Biosorben”, American-Eurasian J. Agric & Environ. Sci, Vol. 8(1): 7-17, 2010
[5] Igwe, Jc., Abia, Aa., “A Bioseparation Process for Removing Heavy Metals From Waste Water using Biosorbents”, African Journal Of Biotechnology, 5(12): 1167-1179, 2006
[6] L.O. Ekebafe A, J.E. Imanah A, dan F.E. Okieimen., “Effect Of Carbonization on The Processing Characteristics of Rubber Seed Shell”. Arabian Journal Of Chemistry . 2012
[7] Haris Fadillah, Alivia Alfiarty, “ The Influence of Pyrolysis Temperature and Time to The Yield and Quality of Rubber Fruit (Hevea Brasiliensis)
Shell Liquid Smoke”. Program Studi Teknologi Pertanian, Fakultas Pertanian, Universitas Lambung Makurat, Banjarbaru, Kalimantan Selatan, Irgsc, Kupang, Ntt
79
[9] Rananda Vinsiah, Andi Suharman, dan Desi.“Pembuatan Karbon Aktif dari Cangkang Kulit Buah Karet (Hevea Brasilliensis)”. Program Studi Pendidikan Kimia FKIP Universitas Sriwijaya. 2015.
[10] C.Srinivasakannan, Mohamad Zailani Abu Bakar. “Production of
Activated Carbon From Rubber Wood Sawdust”. Biomass And Bioenergy, 27 (2004) 89 – 96.2004.
[11] Azry Borhan, Ahmad Fikree Kamil. “Preparation and Characterization of Activating Carbon from Rubber-Seed Shell By Chemical Activation”. Jornal Of Applied Sciences. 12 (11): 1124-1129, 2012.
[12] F E Okieimen, Co Okieeen dan F I Ojokoh. “ Rubber Seed Shell Carbon as Sequestrant af Heavy Metals and Organic Compound from Aqueous
Solution”. University Of Benin. Indian Journal of Chemical Technology. 2005
[13] Siti Zaharah Binti Sulaiman. “Adsorption of Pb(II), Zn(II) And Fe(II) using Rubber Seed Shell. Faculty Of Chemical and Natural Resources. Universiti Malaysia Pahang: Malaysia
[14] T. Karthikeyan, S. Rajgopal dan Lima Rose Miranda. “Chromium(VI) Adsorption from Aqueous Solution by Hevea Brasilinesis Sawdust
Activated Carbon”. Journal of Hazardous Materials, B124 (2005) 192– 199, 2005.
[15] Vinod Kumar Gupta,Imran Ali,Tawfik A. Saleh, M. N. Siddiqui dan Shilpi
Agarwal. “Chromium Removal from Water by Activated Carbon Developed from Waste Rubber Tires”.Environ Sci Pollut Res, 20:1261– 1268, 2013.
[16] Kasam., Andik Yulianto., dan Titin Sukma, “Penurunan COD (Chemical Oxygen Demand) dalam Limbah Cair Laboratorium Menggunakan Filter Karbon Aktif Arang Tempurung Kelapa”, Jurusan Teknik Lingkungan FTSP UII, 2006, Vol. 2, No. 2.
[18] Benefield, L.D., Judkins Jr., J.F., Weand, B.L., “Process Chemistry for Water and Wastewater Treatment”, (Ney Jersey Prentice: Hall, Inc, 1982). [19] Arvina Sari. “Penentuan Bilangan Swelling Indeks Compound Lateks pada
Pembuatan Benang Karet di PT.Industri Karet Nusantara Tanjung Morawa
Medan”. Program Studi Diploma III Kimia Analis Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatra Utara, 2010.
[20] Reza Ramdan Rivai1, Frisca Damayanti1, dan Marlia Handayani., “ Pengembangan Potensi Biji Karet (Hevea Brasiliensis) Sebagai Bahan Pangan Alternatif di Bengkulu Utara”. Pros Sem Nas Masy Biodiv Indon Volume 1, Nomor 2, April ISSN: 2407-8050 Halaman: 343-346, 2015 [21] Direktorat Jenderal Perkebunan. “Peningkatan Produksi, Produktivitas dan
Mutu Tanaman Tahunan”. Kementerian Pertanian,2013.
[22] Vevi Oktavia, Erdi Suroso dan Tanto Pratondo Utomo. “Strategi Optimalisasi Bahan Baku Lateks pada Industri Karet Jenis Ribbed Smoked Sheet (RSS)”. Jurusan Teknologi Hasil Pertanian, Fakultas Pertanian, Universitas Lampung, 2014.
[23] Kang Sun, Jian Chun Jiang,. “Preparation and Characterization of Activated Carbon From Rubber-Seed Shell by Physical Activation with
Steam”. Biomass and Bioenergy 3 4 . 5 3 9 – 5 4 4. 2010
[24] Puspita, Yohanna Vinia Dewi, Mohammad Shodiq Ibnu dan Surjani
Wonorahardjo, “Karakterisasi dan Uji Kemampuan Serbuk Ampas Kelapa Asetat sebagai Adsorben Belerang Dioksida (SO2)”, Jurusan Kimia,
FMIPA, Universitas Negeri Malang, 2013.
[25] Abdul Rahman Mohamed A, Maedeh Mohammadib, dan Ghasem
Najafpour Darzi.” Preparation of Carbon Molecular Sieve from
Lignocellulosic Biomass.” Renewable and Sustainable Energy Reviews 14 (2010) 1591–1599
[26] Suhas, P.J.M. Carrott *, M.M.L. Ribeiro Carrott. “Lignin–from Natural Adsorbent to Activated Carbon: A Review.‟‟ Bioresource Technology. 2007
81
Shells. Journal of Hazardousmaterials, Vol. 165, No. 1-3, (June 2009), PP. (1159-1164), Issn 0304-3894. 2009.
[28] Dastgheib, S.A. dan Rockstraw, D.A. Pecan Shell Activated Carbons: Synthesis, Characterization, and Application for The Removal of Copper from Aqueous Solution.Carbon, Vol. 39, No. 12, (October 2001), PP. (1849-1855), ISSN 0008-6223. 2001.
[29] Álvarez, P., Blanco, C. dan Granda, M. The Adsorption of Chromium (VI) Fromindustrial Wastewater by Acid and Base-Activated Lignocellulosic Residues. Journal Ofhazardous Materials, Vol. 144, No. 1-2, (June 2007), Pp. (400-405), ISSN 0304-3894.2007.
[30] Giraldo, L. Moreno-Piraján, J.C. Pb2+ Adsorption from Aqueous Solutions Onactivated Carbons Obtained from Lignocellulosic Residues. Brazilian Journal of Chemicalengineering, Vol. 25, No. 1, (January 2008), Pp.
(143-151), Issn 0104-6632. 2008.
[31] Bridgid Lai Fui Chin, dkk., “ Kinetic Studies of Co-Pyrolysis of Rubber Seed Shell with High Density Polyethylene”, Energy Conversion and
Management 87 (2014) 746–753, 2014
[32] Kunquan Li, Zheng Zheng dan Ye Lia. “Characterization and Lead Adsorption Properties of Activated Carbons Prepared from Cotton Stalk By One-Step H3PO4Activation”. Journal of Hazardous Materials. Journal
of Hazardous Materials 181 (2010) 440–447, 2010.
[33] N. A. Oladoja. “Studies on the Sorption of Basic Dye by Rubber (Hevea
Brasiliensis) Seed Shell”. Turkish J. Eng. Env. Sci. 32 (2008) , 143 – 152.
[34] M. Al Bahri, L. Calvo, dan M.A. Gilarranz, J.J. Rodriguez. “Activated Carbon from Grape Seeds Upon Chemical Activation with Phosphoric Acid: Application to the Adsorption of Diuron from Water. Chemical Engineering Journal 203 (2012) 348–356
[35] Esty Rahmawati, Leny Yuanita. “Adsorption of Pb2+ by Siwalan Fiber (Borassus Flabellifer) Activated Carbon”. Unesa Journal of Chemistry Vol. 2 , No. 3, September 2013
[37] Abdul Gani Haji. “Pembuatan Arang Aktif dari Sampah Organik Padat dengan Aktivator Asam Fosfat‟‟. Program Studi Kimia FKIP Universitas Syiah Kuala Darussalam, Banda Aceh. Seminar Nasional Sains dan Teknologi, Oktober 2010
[38] Yakout, S.M., Sharaf, El-Deen, G.. Characterization of Activated Carbon Prepared by Phosphoric Acid Activation of Olive Stones. Arabian Journal of Chemistry. DOI:10.1016/J.Arabjc.2011.12.002. 2011
[39] Indah Subadra, Bambang Setiaji, dan Iqmal Tahir. “Activated Carbon Production from Coconut Shell with (NH4)HCO3 Activator as an
Adsorbent in Virgin Coconut Oil Purification”. Physical Chemistry Laboratory, Department of Chemistry Gadjah Mada University. 2005 [40] Yuyun Indriani S Bidullah, Ishak Isa, dan La Alio. “Uji Daya Serap
Arang Aktif dari Kayu Mangrove terhadap Logam Pb Dan Cu”. Jurusan Kimia Fakultas MIPA Universitas Negeri Gorontalo. 2015
[41] Pari, G. Sifat dan Kualitas Arang Aktif dari Gambut. Bul. Penel. Hasil Hutan 16(5):267-278. 1999
[42] Raymon Chang. “Kimia Dasar: Konsep- Konsep Inti. Jakarta. Erlangga. 2005
[43] Sukir. “ Pembuatan dan Karakterisasi Karbon Aktif dari Sekam Padi. Teknik Kimia ITB; Bandung. 2008
[44] Riski Kurniawan*, Musthofa Lutfi, dan Wahyunanto Agung N. „‟ Karakterisasi Luas Permukaan BET (Braunanear, Emmelt dan Teller) Karbon Aktif dari Tempurung Kelapa dan tandan Kosong Kelapa Sawit dengan Aktivasi Asam Fosfat (H3PO4). Jurnal Keteknikan Pertanian
Tropis dan Biosistem. Vol. 2 No. 1, Februari 2014. Jurusan Keteknikan Pertanian - Fakultas Teknologi Pertanian - Universitas Brawijaya
83
[46] Anita Imawati, Adhitiyawarman. „‟ Kapasitas Adsorpsi Maksimum Ion Pb(II) oleh Arang Aktif Ampas Kopi Teraktivasi HCl Dan H3PO4. Jkk,
Tahun 2015, Volume 4(2), Halaman 50-61 ISSN 2303-1077 51. Program Studi Kimia, Fakultas MIPA, Universitas Tanjungpura
[47] Sri Lestari. „‟ Pengaruh Berat dan Waktu Kontak untuk Adsorpsi Timbal(II) oleh Adsorben dari Kulit Batang Jambu Biji (Psidium Guajava L.) Program Studi Pendidikan Kimia Jurusan FMIPA FKIP Universitas Mulawarman. Samarinda Kaltim
[48] Nailul Fauziah, Pembuatan Arang Aktif secara Langsung dari Kulit Acacia (Mangium Wild) dengan Aktivasi Fisika dan Aplikasinya sebagai Adsorben, Skripsi, Fakultas Kehutanan, Institut Pertanian Bogor, Bogor, 2009.
BAB III
METODOLOGI PENELITIAN
5.1 LOKASI DAN WAKTU PENELITIAN
Penelitian dilakukan di Laboratorium Penelitian, Departemen Teknik Kimia,
Fakultas Teknik, Universitas Sumatera Utara. Penelitian ini dilaksanakan selama lebih
kurang 4 bulan.
5.2 BAHAN DAN PERALATAN
3.2.1 Bahan Penelitian
Pada penelitian ini bahan yang digunakan antara lain: 1. Cangkang Buah Karet (Hevea brasilliensis)
2. Aquadest (H2O)
3. Asam Fosfat (H3PO4)
4. Larutan Pb(II)
3.2.2 Peralatan Penelitian
Pada penelitian ini peralatan yang digunakan antara lain: 1. BET
2. Spektrofotometer Serapan Atom (SSA) 3. Oven
4. Furnace 5. Palu
6. Ayakan 100 mesh 7. Desikator
8. Piknometer 25 ml 9. Magnetic Stirrer
10. Kertas Saring Whatman 42 11. Beaker Glass
57 13. Timbangan Digital
14. Batang Pengaduk 15. Corong Gelas 16. Pipet Tetes 17. Stopwatch 18. Erlenmeyer 19. Cawan Porselen 20. Penjepit Tabung 21. Spatula
22. Akuades dan akuabides
5.3 PROSEDUR PENELITIAN
3.3.1 Prosedur Pembuatan Karbon Aktif dari Cangkang Buah Karet
Prosedur pembuatan karbon aktif dari cangkang buah karet [7] 1. Cangkang buah karet diperkecil ukurannya dengan palu.
2. Dicuci dengan air beberapa kali hingga kotoran hilang kemudian dikeringkan pada suhu 110 oC di oven selama 2 jam.
3. Cangkang buah karet dihaluskan dengan blender serta diayak dengan ayakan 100 mesh.
4. Cangkang buah karet yang telah halus kemudian direndam dengan asam fosfat dengan rasio 1 : 2 berat selama 1 jam
5. Sampel dikarbonisasi pada suhu 500 oC selama 1 jam. 6. Dicuci karbon aktif dengan air dan dikeringkan.
3.3.2 Prosedur Analisis
3.3.2.1 Analisis Kadar Air
Prosedur penentuan kadar air karbon aktif menggunakan metode ASTM
2867-99.
1. Wadah kosong ditimbang.
3. Wadah dengan karbon aktif dimasukkan ke dalam oven pada 105 oC selama 3 jam.
4. Karbon aktif dibiarkan dingin sampai temperatur ruang dalam desikator. 5. Sampel dengan wadah ditimbang
6. Prosedur 3-5 sampai berat konstan (B) dan kadar air dihitung menurut persamaan di bawah ini.
Kadar air, % = (A-B)/B x 100
3.3.2.2 Analisis Kadar Abu
Untuk Analisis kadar abu karbon aktif menggunakan metode ASTM D 2866 – 94. Kadar abu karbon aktif dihitung menggunakan rumus sebagai berikut: 7. Wadah kosong ditimbang (B).
8. Wadah dengan karbon aktif ditimbang (C).
9. Wadah dengan karbon aktif dimasukkan ke dalam furnace kira-kira pada 600 oC selama 3 jam.
10. Sampel dibiarkan dingin sampai temperatur ruang dalam sebuah desikator. 11. Sampel dengan wadah ditimbang (D) dan kadar abu dihitung menurut
persamaan di bawah ini.
Kadar abu, % = 100*(D - B)/(C - B)
3.3.2.3 Analisis Kadar Zat Menguap
Untuk Analisis kadar zat menguap karbon aktif menggunakan metode ASTM 2866 – 94.
1. Cawan kosong beserta tutupnya telebih dahulu dipijarkan di dalam furnace selama 30 menit dan didinginkan di dalam desikator.
2. Kemudian ditimbang dengan teliti sebanyak 1 gram sampel ke dalam cawan kosong tersebut.
3. Cawan selanjutnya ditutup dan dimasukkan ke dalam furnace dengan suhu 950 oC selama 7 menit.
59 Kadar zat menguap, %
Dimana:
wo = Berat sampel awal (gram)
w1 = Berat sampel setelah pemanasan (gram)
3.3.2.4 Karakterisasi Karbon Aktif dari Cangkang Buah Karet
Prosedur karakterisasi adsorben cangkang buah karet dilakukan dengan
prosedur yaitu :
Karbon aktif yang sudah dihasilkan kemudian diukur luas permukaannya dengan menggunakan peralatan BET untuk mengetahui luas permukaan karbon aktif.
3.3.2.5 Analisis Banyaknya Logam Timbal yang Dijerap dengan Atomic
Adsorption Spektrofotometer (AAS)
Analisa adsorpsi Pb(II) dari karbon aktif cangkang buah karet dilakukan
menggunakan larutan logam Pb(II) yang didapatkan dari Balai Riset dan Standardisasi
Industri Medan. Karbon aktif dari cangkang buah karet dengan variasi konsentrasi
aktivator H3PO4 kemudian digunakan untuk menjerap logam Pb(II) 100 ppm, volume 100
ml berlangsung pada suhu ruang. Konsentrasi Pb(II) yang berhasil dijerap oleh karbon
aktif kemudian ditentukan dengan atomic adsorption spektrofotometer (AAS).
3.4 FLOWCHART PENELITIAN
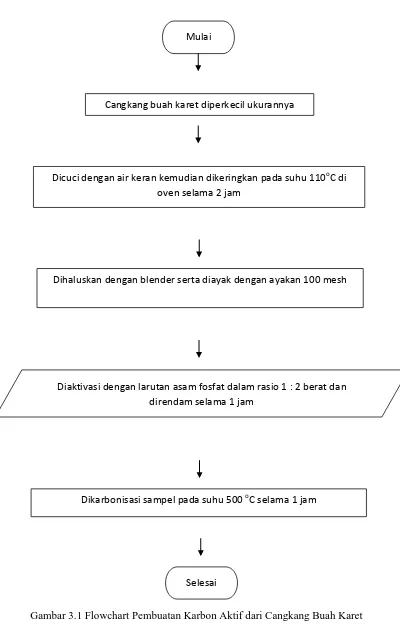
Gambar 3.1 Flowchart Pembuatan Karbon Aktif dari Cangkang Buah Karet
3.4.2 Analisis Kadar Air
Mulai
Cangkang buah karet diperkecil ukurannya
Dikarbonisasi sampel pada suhu 500 oC selama 1 jam Dihaluskan dengan blender serta diayak dengan ayakan 100 mesh
Diaktivasi dengan larutan asam fosfat dalam rasio 1 : 2 berat dan direndam selama 1 jam
Dicuci dengan air keran kemudian dikeringkan pada suhu 110oC di oven selama 2 jam
Selesai
61
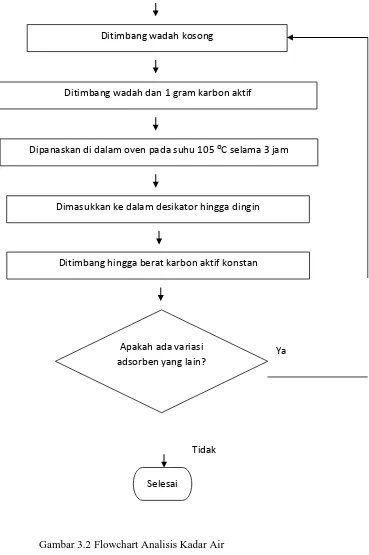
Gambar 3.2 Flowchart Analisis Kadar Air
3.4.3 Analisis Kadar Abu
Mulai
Ditimbang wadah kosong
Ditimbang wadah dan 1 gram karbon aktif
Dimasukkan ke dalam desikator hingga dingin
Ditimbang hingga berat karbon aktif konstan
Apakah ada variasi adsorben yang lain?
Selesai
Tidak
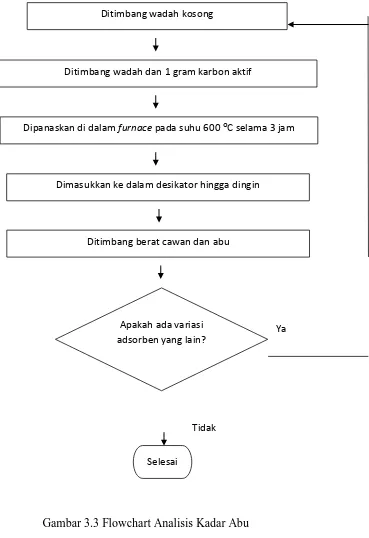
Gambar 3.3 Flowchart Analisis Kadar Abu
3.4.4 Analisis Kadar Zat Menguap
Ditimbang wadah dan 1 gram karbon aktif
Dimasukkan ke dalam desikator hingga dingin
Ditimbang berat cawan dan abu Ditimbang wadah kosong
Apakah ada variasi adsorben yang lain?
Selesai
Tidak
Ya Dipanaskan di dalam furnace pada suhu 600 ᴼC selama 3 jam
63
Gambar 3.4 Flowchart Analisis Kadar Zat Mengu
3.4.5 Flowchart Penentuan Banyaknya Pb(II) yang Terjerap dalam Karbon Aktif
Sebanyak 3 gram sampel karbon aktif yang halus dimasukkan sebanyak 100 ml larutan Pb(II) ke dalam
Erlenmeyer dengan konsentrasi100 ppm. Mulai
Selesai
Ditimbang wadah kosong
Ditimbang wadah dan 1 gram sampel ke dalam cawan kosong
Dimasukkan ke dalam desikator hingga dingin
Ditimbang hingga berat serbuk cangkang buah karet konstan
Apakah ada variasi adsorben yang lain?
Tidak
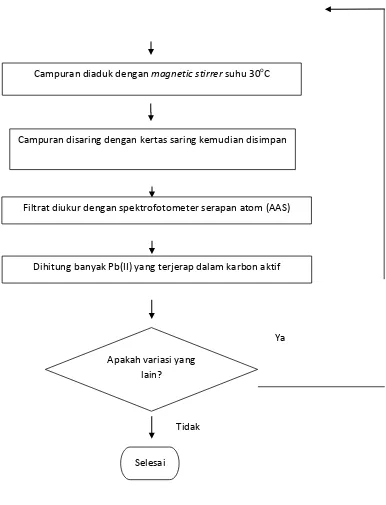
Gambar 3.5 Flowchart Penentuan Jumlah Pb(II) yang Terjerap dalam Karbon
BAB IV
HASIL DAN PEMBAHASAN
4.1 PEMBUATAN KARBON AKTIF DARI CANGKANG BUAH KARET
Campuran diaduk dengan magnetic stirrer suhu 30oC
Campuran disaring dengan kertas saring kemudian disimpan
Dihitung banyak Pb(II) yang terjerap dalam karbon aktif
Selesai
Filtrat diukur dengan spektrofotometer serapan atom (AAS)
Apakah variasi yang lain?
Tidak
65
Pada penelitian ini, karbon aktif dibuat dari bahan baku cangkang buah karet yang diimpregnasi dengan aktivator asam fosfat (H3PO4) dengan rasio bahan
cangkang buah karet : asam fosfat (b:b) sebesar 1:2 dan variasi konsentrasi H3PO4
sebesar 20%, 40%, dan 60% pada suhu ruangan. Selanjutnya bahan cangkang buah karet yang telah lolos ayakan 100 mesh dikarbonisasi pada suhu 500 oC selama 1 jam.
4.2 KARAKTERISASI KARBON AKTIF
4.2.1 Pengaruh Konsentrasi Aktivator terhadap Yield Karbon Aktif
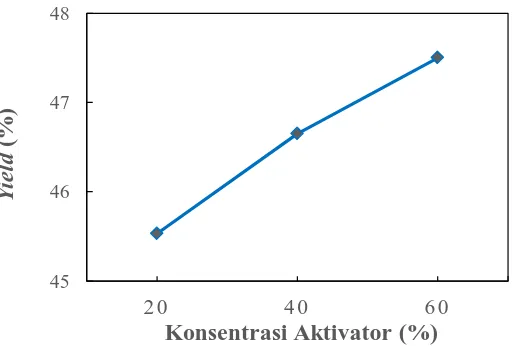
Pada penelitian ini dapat dilihat bahwa konsentrasi aktivator asam fosfat berpengaruh terhadap yield yang dihasilkan, sebagaimana dapat dilihat melalui gambar 4.1
Gambar 4.1 Pengaruh Konsentrasi Aktivator terhadap Yield Karbon Aktif
Pada Gambar 4.1 dapat dilihat yield yang dihasilkan cenderung meningkat seiring dengan semakin tingginya konsentrasi aktivator asam fosfat yang digunakan. Impregnasi yang dilakukan menggunakan konsentrasi aktivator asam fosfat 60% menghasilkan yield terbesar yaitu 47,50%.
Perubahan variasi konsentrasi aktivator H3PO4 akan sangat mempengaruhi
yield arang aktif yang dihasilkan. Peningkatan yield karbon aktif seiring dengan meningkatnya konsentrasi aktivator asam fosfat disebabkan karena reaksi pada bahan arang aktif dengan H3PO4 sehingga tidak terjadi oksidasi lanjutan. Hasil ini
sejalan dengan hasil penelitian yang dilakukan oleh Haji (2010) dimana
45 46 47 48
2 0 4 0 6 0
Y
ie
ld
(%
)
konsentrasi aktivator H3PO4 berbanding lurus dengan yield karbon aktif dari bahan
lignoselulosa [37].
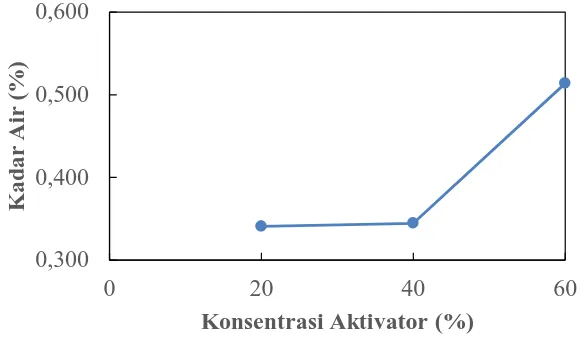
4.2.2 Pengaruh Konsentrasi Aktivator terhadap Kadar Air Karbon Aktif Adanya kandungan air di dalam karbon aktif akan mempengaruhi daya serap dari karbon aktif yang dihasilkan, pada umumnya semakin rendah kandungan air di dalam karbon aktif maka daya serapnya akan lebih baik, jika ditinjau secara grafis kandungan air karbon aktif yang dihasilkan terlihat pada gambar 4.2
Gambar 4.2 Pengaruh Konsentrasi Aktivator terhadap Kadar Air Karbon Aktif
Pada Gambar 4.2 dapat dilihat kadar air yang dihasilkan cenderung meningkat seiring dengan semakin tingginya konsentrasi aktivator asam fosfat yang digunakan. Kadar air dari semua sampel karbon aktif telah memenuhi standar SNI yaitu kurang dari 15%. Kadar air terendah dimiliki oleh sampel karbon aktif yang diimpregnasi dengan konsentrasi aktivator 20% sebesar 0,341%.
Menurut Yakout & Sharaf El-Deen (2011), kadar air dipengaruhi oleh sifat higroskopis karbon aktif dan jumlah uap air di udara [38]. Peningkatan konsentrasi aktivator asam fosfat menyebabkan semakin besar dan banyaknya pori yang terbentuk sehingga meningkatkan sifat higroskopis karbon aktif dan penyerapan air dari udara oleh karbon aktif [39].
0,300 0,400 0,500 0,600
0 20 40 60
K
ad
ar
A
ir
(%
)
67
4.2.3 Pengaruh Konsentrasi Aktivator terhadap Kadar Abu Karbon Aktif Kadar abu karbon aktif yang dihasilkan cenderung menurun seiring dengan semakin tingginya konsentrasi aktivator asam fosfat. Pada penelitian ini dihasilkan kadar abu paling rendah yaitu 9,90% dengan aktivasi asam fosfat 60% sebagaimana digambarkan pada grafik 4.3
Gambar 4.3 Pengaruh Konsentrasi Aktivator terhadap Kadar Abu Karbon Aktif
Pada Gambar 4.3 dapat dilihat bahwa sampel karbon aktif yang memenuhi standar SNI adalah karbon aktif yang diaktivasi dengan asam fosfat 60% dengan kadar abu 9,90 %.
Penurunan kadar abu seiring dengan meningkatnya konsentrasi aktivator asam fosfat dapat dikarenakan pengotor yang masih tersisa pada bahan ikut larut dalam asam fosfat konsentrasi tinggi. Karbon aktif dari bahan alam selain mengandung karbon juga mengandung mineral, sebagian mineral diperkirakan tidak hilang pada saat aktivasi sehingga menyebabkan masih adanya kadar abu yang tinggi [40]. Kadar abu yang tidak sesuai SNI bukan berarti karbon aktif tidak dapat dimanfaatkan sebagai adsorben, hal ini sesuai hasil penelitian yang dilakukan oleh Pari, (1999) bahwa walaupun kadar abu tidak memenuhi persyaratan namun masih dapat dijadikan sebagai karbon aktif [41]. Mineral-mineral yang terdapat pada bahan karbon aktif akan senantiasa melarut seiring meningkatnya konsentrasi asam sebagai aktivator [42]. Pengotor berupa mineral tersebut akan larut dalam asam fosfat menghasilkan garam-garam fosfat yang kemudian akan hilang pada saat pencucian karbon aktif dengan air panas [43].
5 8 11 14
2 0 4 0 6 0
K
ad
ar
A
b
u
(%
)
4.2.4 Pengaruh Konsentrasi Aktivator terhadap Kadar Zat Menguap
Kadar zat menguap karbon aktif yang dihasilkan cenderung menurun seiring dengan semakin tingginya konsentrasi aktivator asam fosfat yang digunakan, sebagaimana digambarkan pada grafik 4.4
Gambar 4.4 Pengaruh Konsentrasi Aktivator terhadap Kadar Zat Menguap
Berdasarkan gambar 4.4 dapat dilihat kadar zat yang menguap yang dihasilkan pada penelitian ini telah memenuhi standar SNI yaitu dibawah 25%. Kadar zat menguap terendah dimiliki oleh sampel karbon aktif yang diimpregnasi dengan konsentrasi aktivator 60% sebesar 1,48% sedangkan kadar zat menguap tertinggi terdapat pada karbon aktif yang diimpregnasi dengan konsentrasi aktivator 20% sebesar 2,62%.
Penurunan kadar zat menguap dari karbon aktif yang dihasilkan disebabkan pengaruh nyata dari aktivator asam fosfat pada penelitian ini. Seiring dengan semakin meningkatnya konsentrasi larutan aktivator asam fosfat maka akan semakin tinggi kemampuan aktivator dalam mengikat pengotor dan mineral yang terdapat di dalam bahan karbon aktif. Residu yang terdapat pada bahan karbon aktif menjadi semakin mudah menguap dikarenakan sangat kecil jumlahnya, hal ini menyebabkan kadar zat menguap pada karbon aktif semakin menurun [39].
4.2.5 Pengaruh Konsentrasi Aktivator terhadap Luas Permukaan Karbon Aktif dengan Metode BET
0 1 2 3
2 0 4 0 6 0
K
ad
ar
Z
at
M
en
gu
ap
(%
)
69
Luas permukaan dan volume pori karbon aktif dapat dilihat pada gambar 4.5 di bawah ini.
Gambar 4.5 Luas Permukaan dan Volume Pori Karbon Aktif
Dari data gambar 4.5 diatas terlihat bahwa luas permukaan dan volume pori karbon aktif yang dihasilkan meningkat seiring meningkatnya konsentrasi aktivator asam fosfat. Karbon aktif yang diimpregnasi pada konsentrasi aktivator 60% memiliki luas permukaan yang paling besar, yaitu 1502,84 m2/g dan volume pori 1,11 cc/g. Luas permukaan merupakan salah satu karakter fisik yang berhubungan langsung dengan kemampuan adsorpsi terhadap adsorbat yang akan dijerap. Peningkatan luas permukaan karbon aktif seiring meningkatnya konsentrasi aktivator asam fosfat dikarenakan asam fosfat memiliki unsur-unsur mineral dari persenyawaan kimia yang akan meresap ke dalam arang dan membuka permukaan yang mula-mula tertutup oleh komponen kimia sehingga luas permukaan yang aktif bertambah besar [44].
4.3 PENENTUAN JUMLAH PB(II) YANG TERJERAP DALAM KARBON AKTIF
Dalam penelitian ini, diaplikasikan karbon aktif yang telah diaktivasi dengan variasi H3PO4 dengan konsentrasi 20%, 40%, dan 60% ke dalam larutan
Pb(II) 100 ppm 100 ml. Karbon aktif yang digunakan untuk penjerapan sebanyak 3 gram. Penjerapan logam Pb(II) dilakukan pasa suhu ruangan selama 3 jam.
0 0,2 0,4 0,6 0,8 1 1,2 -20 200 420 640 860 1080 1300 1520
20 40 60
V o lu m e P o ri (c c/ g) Lu as P er m u k aan (m 2 /g)
Konsentrasi Aktivator (%)
Persentase penjerapan terbesar terdapat pada konsentrasi aktovator 20% dengan massa karbon aktif 3 gram. Untuk menentukan persentase penjerapan terhadap logam Pb(II) digunakan rumus perhitungan berikut [46] :
Karbon aktif yang diaktivasi menggunakan H3PO4 efektif untuk
mengadsorpsi logam Pb. Grafik 4.6 menampilkan daya adsorpsi karbon aktif terhadap logam Pb(II).
Gambar 4.6 Grafik daya adsorpsi karbon aktif
Dari Gambar 4.6 terlihat bahwa semakin bertambah konsentrasi H3PO4
yang digunakan, maka nilai efisiensi adsorpsinya terhadap logam Pb(II) semakin rendah. Pada grafik di atas daya jerap karbon aktif terbesar adalah pada konsentrasi aktivator H3PO4 20% dengan daya jerap sebesar 74%.
Semakin menurunnya daya jerap karbon aktif terhadap larutan Pb(II) dapat disebabkan karena ion logam memiliki ukuran jari-jari relatif kecil sehingga interaksi yang terjadi antara adsorbat dan karbon aktif yang terjadi akan dipengaruhi oleh jarak antar spesi yang ada [45]. Karbon aktif yang diaktivasi dengan asam fosfat konsentrasi 20% memiliki kemampuan penjerapan tertinggi, hal ini disebabkan ion logam masuk ke bagian interlayer dengan lebih mudah dan akan sulit terlepas saat dilakukan proses pengadukan. Terbentuknya ikatan yang lemah antara adsorben dan adsorbat menyebabkan terlepasnya ion logam Pb(II) saat dilakukan pengadukan, sehingga ukuran luas permukaan karbon aktif pada
0 20 40 60 80
20 40 60
D
ay
a
S
er
ap
(%
)
71
konsentrasi asam fosfat 20% lebih kuat dalam mengikat ion logam Pb(II) saat di lakukan pengadukan.
Kadar air yang terkandung di dalam karbon aktif juga akan mempengaruhi kemampuan daya jerap terhadap larutan adsorbat, semakin rendah kadar air yang terdapat didalam karbon aktif akan meningkatkan kemampuan daya jerap karbon aktif [40]. Rendahnya kadar air menunjukkan sedikitnya kandungan air yang menutupi pori-pori karbon aktif sehingga semakin banyak ruang yang ditempati oleh adsorbat sehingga adsorpsi akan berlangsung secara optimal [46].
Karbon aktif yang diaktivasi dengan asam fosfat 20% ternyata memberikan kadar air yang paling rendah, setelah dilakukan penjerapan terhadap larutan Pb(II) dihasilkan daya jerap yang memiliki kemampuan yang paling baik dengan nilai persentaase daya jerap mencapai 74% .
4.4 PENGARUH BERAT KARBON AKTIF TERHADAP ADSORPSI Pb(II)
Gambar 4.7 Grafik pengaruh berat karbon aktif terhadap daya adsorpsi Pb(II)
Dari data gambar 4.7 terlihat bahwa semakin bertambah berat karbon aktif yang digunakan, maka nilai kapasitas adsorpsinya terhadap logam Pb(II) semakin tinggi. Pada grafik diatas daya serap karbon aktif terbesar adalah pada jumlah karbon aktif 3 dan 4 gram sebesar 74 dan 75%.
Penambahan berat adsorben mempengaruhi peningkatan kadar Pb(II) yang teradsorpsi. Peningkatan kadar Pb(II) yang teradsorpsi terjadi karena semakin banyak adsorben yang digunakan, semakin banyak pula situs aktif (C=O) yang terdapat dalam karbon aktif yang mengadsorpsi logam Pb(II) [47].
0 20 40 60 80
1 2 3 4
D
ay
a
Je
rap
(%
)
73
4.5 PENENTUAN ADSORPSI ISOTERM LOGAM Pb2+ YANG
TERJERAP OLEH KARBON AKTIF
Penentuan model adsorpsi isoterm adalah untuk mengetahui jenis adsorpsi yang terjadi pada karbon aktif. Pada penelitian ini konsentrasi awal larutan timbal digunakan sebesar 100 ppm. Adsorben yang digunakan adalah adsorben dengan konsentrasi aktivator H3PO4 20% dengan memvariasikan berat karbon aktif 1,2, 3
dan 4 gram.
[image:32.595.100.524.277.426.2]Dengan menggunakan adsorben yang telah diaktivasi dengan aktivator H3PO4 didapat konsentrasi terjerap pada tabel 4.1
Tabel 4.1 Data Konsentrasi Larutan Timbal Berat karbon
aktif (gr)
Konsentrasi Awal C1 (ppm)
Konsentrasi Akhir C2 (ppm)
Daya Serap (%)
1 60,4 39,6
2 100 32,8 67,2
3 26 74
4 25 75
Perhitungan dilakukan dengan pendekatan model adsorpsi Langmuir dan Freundlich, dimana adsorpsi yang terjadi diasumsikan berlangsung secara isoterm. Hubungan yang menggambarkan antara adsorpsi dan adsorbat secara teoritis seperti persamaan berikut (Geankoplis, 2003):
Persamaan di atas disusun menjadi persamaan garis lurus sebagai berikut :
Atau :
⌊ ⌋ [ ] ⌊ ⌋
Dengan memplot 1/q vs 1/C didapat persamaan garis lurus dimana slope garis tersebut adalah dengan interceptnya adalah
(pers...2.3)
Tabel 4.2 adalah data yang digunakan untuk mendapatkan model adsorpsi secara Langmuir.
Tabel 4. 2 Data Perhitungan Untuk Model Adsorpsi Langmuir
1/C2 1/q
0,0165 0,2525
0,0304 0,2976
0,0384 0,4054
0,04 0,5333
Sedangkan untuk persamaan adsorpsi dengan model Adsorpsi Freundlich dinyatakan dengan persamaan :
Persamaan diatas disusun menjadi persamaan garis lurus sebagai berikut :
Atau :
[image:33.595.166.458.549.662.2]
Dengan memplot log q vs log C didapat persamaan garis lurus dimana slope garis tersebut adalah n dengan interceptnya adalah log k. Tabel 4.3 adalah data yang digunakan untuk mendapatkan model adsorpsi secara Freundlich. Grafik untuk masing-masing model adsorpsi isoterm disajikan pada gambar 4.8 dan 4.9
Tabel 4.3 Data Perhitungan Untuk Model Adsorpsi Freundlich
Log C2 Log q
1,7810 0,5976
1,5158 0,5263
1,4149 0,3921
1,3979 0,2730
(pers...2.1)
75
[image:34.595.135.464.131.328.2]Berikut adalah grafik Isoterm Langmuir dan Isoterm Freundlich terhadap logamPb2+.
Gambar 4.8 Kurva Adsorpsi Isoterm Langmuir Untuk Logam Pb(II)
Gambar 4.9 Kurva Adsorpsi Isoterm Freundlich Untuk Logam Pb(II) Dari grafik didapat nilai konstanta masing-masing model adsorpsi seperti yang disajikan dalam tabel 4.4
y = 10,04x + 0,057 R² = 0,741
0 0,1 0,2 0,3 0,4 0,5 0,6
0 0,01 0,02 0,03 0,04 0,05
1/
q
1/c
y = 0,703x - 0,626 R² = 0,745
0 0,2 0,4 0,6 0,8
0 0,9 1,8 2,7
Lo
g
Q
[image:34.595.135.465.393.597.2]Tabel 4.4 Nilai Konstanta Masing-Masing Adsorpsi
Model Konstanta R2
Langmuir k = 176,1 0,741 qm = 17,54
Freundlich k = 0,236 0,745 1/n = 0,703
Daya jerap (adsorpsi) adalah peristiwa terjadinya perubahan kepekatan dari molekul, ion atau atom antar permukaan dalam dua fasa. Hal ini terjadi bila dua fasa saling bertemu, sehingga di antara kedua fasa tersebut terbentuk daerah antar muka yang sifatnya berbeda. Pada kondisi tertentu atom, ion atau molekul dalam daerah ini mengalami ketidakseimbangan gaya sehingga mampu menarik molekul lain sampai keseimbangan gaya tercapai [48].
Keabsahan kurva adsorpsi isoterm dapat diuji dengan menentukan harga koefisien korelasi (R2) atau uji kelinieran yang menyatakan ukuran kesempurnaan hubungan antara konsentrasi akhir larutan Pb(II) dan konsentrasi terjerap. Korelasi dinyatakan sempurna jika nilai R2 mendekati 1.
77
BAB V
KESIMPULAN DAN SARAN
5.4 KESIMPULAN
Adapun kesimpulan yang dapat diperoleh antara lain sebagai berikut:
1. Karbon aktif yang dihasilkan memiliki persentase yield 45,53%; 46,65%; dan 47,50%.
2. Karakteristik karbon aktif yang diaktivasi dengan asam fosfat dengan konsentrasi 60% berupa kadar air, kadar abu dan kadar zat menguap sesuai dengan Standar nasional Indonesia (SNI).
3. Karakterisasi karbon aktif dengan metode BET menunjukkan luas permukaan masing-masing karbon aktif telah memenuhi luas permukaan minimal untuk menjadi adsorben yang efektif dan komersil yaitu sebesar 927,58 m2/g; 1215,11 m2/g; dan 1502,84 m2/g.
4. Penjerapan ion logam Pb(II) menggunakan karbon aktif dari cangkang buah karet paling besar adalah pada karbon aktif yang diaktivasi asam fosfat 20%. 5. Isotermal adsorpsi karbon aktif yang dibuat adalah isoterm Freunlich
6. Adsorben yang dibuat dari cangkang buah karet mampu menjerap logam Pb(II)
5.5 SARAN
Adapun saran yang perlu dilakukan penelitian lanjutan seperti: 1. Menggunakan reaktor pirolisis pada proses karbonisasi.
2. Perlu dilakukan proses aktivasi secara fisika untuk membandingkan karbon aktif sehingga dapat diketahui karbon aktif yang lebih bagus dalam menjerap logam.
BAB II
TINJAUAN PUSTAKA
2.1 CANGKANG BUAH KARET (Hevea brasilliensis) SEBAGAI ADSORBEN
Adsorpsi merupakan proses yang menunjukkan kemampuan adsorbat untuk menempel pada bahan penjerap. Penerapan proses adsorpsi yaitu pada pemisahan polutan terlarut atau untuk mengambil kembali bahan yang bernilai memiliki nilai lebih namun berjumlah sedikit pada suatu campuran [5]. Proses adsorpsi terjadi pada permukaan suatu zat padat yang berkontak dengan suatu larutan dimana terjadi akumulasi molekul-molekul larutan pada permukaan zat padat tersebut [16].
Secara umum proses penggumpalan substansi terlarut yang ada dalam larutan oleh permukaan zat atau benda penyerap, dimana terjadi suatu ikatan kimia-fisika antara substansi terlarut (adsorbat) dengan penyerapnya (adsorben) disebut dengan proses adsorpsi. Proses interaksi dapat saja terjadi antara cairan dan gas, padatan atau cairan lain. Ikatan Van der waals menyebabkan terjadinya adsorpsi fisika dan zat terlarut akan dapat diadsorpsi jika ikatan tarik antar molekul adsorbat dengan adsorben lebih besar dari ikatan antara molekul zat terlarut dengan pelarutnya [17]. Sedangkan adsorpsi kimia merupakan hasil dari reaksi kimia pertukaran elektron antara adsorben dengan molekul adsorbat [18].
Penggunaan bahan-bahan alami bahan lignoselulosa menunjukkan kemampuan biomassa untuk mengikat logam berat dari dalam larutan melalui langkah-langkah metabolisme atau kimia-fisika [4], dan termasuk penghilangan racun dari bahan-bahan yang berbahaya [5]. Proses pengolahan ini dapat dilakukan di tempat, sehingga tidak diperlukan proses pemindahan bahan yang akan diolah. Keuntungan lain dalam pemakaian bahan alam ini adalah bahan baku yang melimpah, murah, proses pengolahan yang efisien [4].
48
Sumatera merupakan salah satu wilayah sentra karet di Indonesia, termasuk Provinsi Sumatera Utara. Cangkang buah karet belum sepenuhnya dimanfaatkan oleh masyarakat atau pemerintah [20], padahal tanaman karet menghasilkan cangkang buah yaitu sebesar 500 kg/Ha/tahun [7].
Perkebunan karet Indonesia merupakan yang terluas di dunia. Pada tahun 2012 luasnya mencapai 3,4 juta Ha, atau 15 % dari luas total perkebunan di Indonesia seluas 22,76 juta ha. Indonesia dengan produksi sebesar 3,04 juta ton merupakan negara produsen karet alam terbesar ke-2 di dunia. Dengan produksi tersebut, ekspornya mencapai sebesar 2,4 juta Ton [21]. Karet merupakan komoditas ekspor yang mampu memberikan kontribusi dalam upaya peningkatan devisa Indonesia [22].
[image:38.595.208.447.562.697.2]Cangkang buah karet adalah jenis limbah pertanian yang menyebabkan masalah seperti pencemaran lingkungan di perkebunan karet [23]. Limbah hasil pertanian sebagai produk dan hasil samping dari pertanian dan pengolahan produk pertanian merupakan bahan baku besar sumber daya yang kurang dimanfaatkan yang dapat digunakan langsung atau diubah oleh proses kimia yang cukup sederhana untuk meningkatkan nilai dari segi ekonominya. Cangkang buah karet adalah produk sampingan pertanian pohon karet. Selama ini pemanfaatan dari pohon karet sebagian besar berfokus pada lateks karet dengan sedikit perhatian terhadap potensi produk sampingnya. Sementara kemajuan yang signifikan telah dibuat dalam pengembangan dan pemanfaatan memodifikasi produk pertanian di dalam air dan pengolahan air limbah [6].
Adapun komposisi kimia dari cangkang buah karet diberikan pada Tabel 2.1 Tabel 2.1 Komposisi cangkang buah karet [7]
Konstituen Presentase
(%)
Hemiselulosa 18
Selulosa 61,04
Lignin 21,60
[image:39.595.103.519.481.565.2]Tabel 2.1 menunjukkan bahwa cangkang buah karet memiliki kandungan lignin sebesar 21,60 dan Selulosa 61,04 %. Lignin dan selulosa adalah senyawa organik yang termasuk dalam golongan senyawa polimer. Polisakarida yang memiliki gugus –OH sehingga dapat digunakan sebagai adsorben. Molekul-molekul selulosa seluruhnya membentuk linear dan mempunyai kecenderungan kuat membentuk ikatan-ikatan hidrogen intramolekul dan intermolekul. Ikatan hidrogen intramolekul terbentuk antara gugus-gugus –OH dari unit-unit glukosa yang berdekatan dalam molekul selulosa yang sama. Karena interaksinya dengan komponen adsorbat maka struktur yang mengandung selulosa mempunyai potensi yang cukup besar untuk dijadikan sebagai adsorben [24]. Kualitas karbon aktif dapat dinilai berdasarkan persyaratan (SNI) 06–3730-1995 pada Tabel 2.2
Tabel 2.2 Standar Karbon Aktif (SNI) 06–3730-1995 [9]
Jenis Persyaratan Parameter
Kadar Air Mak. 15 %
Kadar Abu Mak. 10 %
Kadar Zat Menguap Mak. 25 %
50
Lignin yang terdiri sekitar 27% konten dari biomassa memiliki kapasitas adsorpsi yang rendah dalam bentuk alami. Tapi potensi sebagai karbon aktif dapat ditingkatkan di bawah kondisi yang tepat [25]. Lignin adalah sebuah mononuklear polimer aromatik yang ditemukan di dinding sel tertentu pada biomassa, terutama jenis kayu, yang berfungsi untuk semen serat selulosa dalam tanaman. Lignin adalah produk limbah yang paling terbukti memiliki potensi yang cukup besar dalam bidang adsorpsi dan persiapan karbon aktif. Bahkan, lignin kaya karbon dan struktur molekul mirip dengan batubara bituminous yang membuatnya menjadi prekursor yang cocok untuk produksi karbon aktif [26].
[image:40.595.99.527.316.701.2]Beberapa penelitian pembuatan karbon aktif dari bahan lignoselulosa dengan aktivasi kimia dan fisika serta aplikasinya dalam menjerap ion logam berat
Tabel 2.3 Aplikasi karbon aktif dalam penjerapan logam Nama
(Tahun) Prekursor Polutan Aktivasi
Temperatur Karbonisasi
(oC)
qmax mg/g
Tajar et al
(2009) [27] Nut shell Kadmium H3PO4 500 90 - 120 Dastgheib &
Rockstraw (2001) [28]
Pecan
shell Tembaga Air, H3PO4 300 -500 33 - 40
Álvarez et al (2007) [29] Pinus sylvestris sawdust Kromium HCl, H3PO4,NaOH,
H2SO4
450 - 650 0,5 - 1,83
Giraldo & Moreno-Piraján (2008)
[30]
African
palm pit Timah HNO3, steam 900 4,7 - 15,2
Giraldo & Moreno-Piraján (2008) [30] Cane sugar bagasse
Timah HNO3, steam 900 6,4 - 13,7
Sulaiman (2012) [13] Cangkang buah karet Pb(II), Zn(II) and Fe(II) NaOH dan HCl sebagai pengatur pH
80 0 C
14.41mg/g Untuk Pb(II)
penelitian yang dilakukan Sulaiman (2012) kapasitas penjerapan maksimum bagi logam Pb (II) dengan hasil 14.41mg/g, proses yang dilakukan menggunakan karbon aktif dari cangkang buah karet pada pH 2 memberikan hasil yang terbaik [13].
2.2 PIROLISIS
Karbonisasi adalah konversi pirolitik yang dilakukan pada pemanasan lambat imana produk akhir yang diinginkan adalah arang. Konversi pirolitik biomassa lignoselulosa menghasilkan tiga fase yaitu char (arang ), minyak (tar) dan gas. Arang adalah residu karbon dari proses karbonisasi setelah menghapus elemen non-karbon seperti hidrogen dan oksigen dari bahan awal, memiliki struktur berpori dasar yang dapat digunakan untuk karbon aktif. Char memiliki kandungan karbon tetap tinggi yang membuatnya menjadi prekursor cocok untuk pembuatan karbon aktif [25].
Hasil penelitian yang dilakukan oleh Ekebafe, et al, 2012 menunjukkan
bahwa suhu pemanasan mempengaruhi sifat cangkang buah karet, sehingga
menunjukkan bahwa karbonisasi memiliki pengaruh signifikan pada karakteristik
pengolahan cangkang buah karet [6]. Para peneliti menegaskan bahwa lignin merupakan sumber utama arang, sedangkan selulosa dan hemiselulosa adalah fraksi volatile biomassa. Dekomposisi lignin dimulai pada suhu rendah (160-170
0
C) dan proses ini berlanjut pada tahap rendah sampai suhu tinggi 900 0C. Komponen kedua yang mulai terurai adalah hemiselulosa, diikuti oleh selulosa. Dekomposisi dari dua polimer ini berlangsung pada kisaran suhu 200-400 0C. Oleh karena itu, komposisi biomassa lignoselulosa adalah parameter penting dalam pembentukan arang [25].
Pirolisis merupakan teknologi penting yang banyak dipilih karena teknologi
lebih ramah bagi lingkungan dibandingkan dengan metode insinerasi, hal ini
dikarenakan tidak adanya oksigen yang dipasok ke dalam sistem. Dengan
demikian memiliki kecenderungan yang rendah menghasilkan dioksin dan furan,
serta sumber energi dapat dicapai dari banyak pilihan teknologi sehingga
52 2.3 AKTIVASI KIMIA DENGAN H3PO4
Asam fosfat karbon aktif menunjukkan kapasitas tukar kation yang luar biasa, yang telah terbukti sangat efektif adsorben untuk menghilangkan ion logam berat konsentrasi rendah dari fase cair, dan kapasitas kimia dan termal ini stabil.
Oleh karena itu, asam fosfat karbon aktif telah banyak digunakan untuk menghilangkan ion logam berat dari fase air [32].
Dalam 20 tahun terakhir, aktivasi bahan lignoselulosa dengan H3PO4 telah
menjadi metode paling banyak digunakan untuk pembuatan skala besar karbon aktif karena penggunaan ini reagen memiliki beberapa keunggulan lingkungan seperti biaya energi yang rendah, kemudahan recovery, dan yield karbon yang tinggi. H3PO4 memainkan dua peran selama persiapan pembuatan karbon aktif : i)
H3PO4 dapat berfungsi sebagai wadah karena volume yang ditempati oleh asam
fosfat di interior dari prekursor diaktifkan bertepatan dengan volume mikropori dari karbon yang diaktifkan; ii) H3PO4 bertindak sebagai katalis asam untuk
mempromosikan pembelahan ikatan, hidrolisis, dehidrasi dan kondensasi, disertai dengan silang reaksi antara asam fosfat dan biopolymer [33].
Keuntungan dari aktivasi kimia adalah biaya energi yang rendah, karena biasanya terjadi pada suhu lebih rendah dibandingkan aktivasi fisika, dan tingginya hasil yang didapatkan. Aktivasi kimia dengan H3PO4 telah menjadi
yang paling umum untuk mengaktifkan agen karena kemampuannya untuk memberikan porositas dari lebar bahan awal sangat baik, toksikologi bagi lingkungan yang lebih rendah jika dibandingkan dengan ZnCl2 dan temperatur
kerja rendah dibandingkan dengan aktivasi KOH [34]. Berikut adalah beberapa keuntungan aktivasi kimia [33]:
a) Karbon aktif yang diperoleh hanya dalam satu langkah percobaan b) Waktu aktivasi singkat
c) Suhu pirolisis rendah (600 sampai 800 ºC) d) Kontrol yang lebih baik dari sifat tekstural e) Hasil (Yield) tinggi
f) Luas permukaan tinggi dari microporosit karbon aktif
Isoterm adsorpsi adalah hubungan yang menunjukkan distribusi adsorben antara fasa teradsorpsi pada permukaan adsorben dengan fasa ruah saat kesetimbangan pada temperatur tertentu. Ada tiga pola isoterm adsorpsi, yaitu isoterm adsorpsi Freundlich, Langmuir, dan BET (Brunauer, Emmet dan Teller). Akan tetapi, karena adsorpsi fase padat cair dimana molekul atau ion pada permukaan padatan umumnya terbatas pada lapisan satu molekul (monolayer) maka adsorpsi tersebut mengikuti persamaan adsorpsi Freundlich dan atau Langmuir [35].
2.4.1. Isoterm Freundlich
Pendekatan isoterm adsorpsi dijelaskan oleh Freundlich. Menurut Freundlich, q adalah berat zat terlarut per gram adsorben dan c adalah konsentrasi zat terlarut dalam larutan. Dari konsep tersebut dapat diturunkan persamaan sebagai berikut:
Persamaan diatas disusun menjadi persamaan garis lurus sebagai berikut :
Dengan memplot log q vs log C didapat persamaan garis lurus dimana slope garis tersebut adalah 1/n dengan interceptnya adalah log k [36].
2.4.2. Isoterm Langmuir
Model ini mendefinisikan bahwa kapasitas adsorpsi maksimum terjadi akibat adanya lapisan tunggal (monolayer) adsorbat di permukaan adsorben. Pendekatan Langmuir meliputi lima asumsi mutlak, yaitu:
1. Molekul yang teradsorpsi berkelakuan ideal
2. Molekul yang teradsorpsi dibatasi sampai lapisan monolayer.
3. Permukaan adsorbat homogen, artinya afinitas setiap kedudukan ikatan untuk molekul sama.
4. Tidak ada antaraksi lateral antar molekul adsorbat.
5. Molekul yang teradsorpsi terlokalisasi, artinya mereka tidak bergerak pada permukaan.
(2.1)
54
Dimana persamaan Langmuir ditulis sebagai berikut:
Persamaan diatas disusun menjadi persamaan garis lurus: [ ]
Dengan memplot 1/q vs 1/C didapat persamaan garis lurus dimana slope garis tersebut adalah dengan interceptnya adalah [36].
2.5 PENCEMARAN LINGKUNGAN
Cukup banyak golongan logam yang sama sekali belum diketahui manfaatnya bagi organisme perairan, seperti Hg, Cd, dan Pb. Timbal adalah jenis logam lunak berwarna coklat kehitaman dan mudah dimurnikan memiliki nomor atom (NA) 82 dengan berat atom (BA) 207,2. Kebanyakan logam toksik seperti logam Pb lebih tersebar luas dibanding kebanyakan logam toksik. Peningkatan kadar Pb di lingkungan disebabkan meningkatnya penggunaan logam ini di dalam pertambangan, logam ini berbentuk sulfida logam (PbS). Logam Pb banyak digunakan dalam industri misalnya sebagai zat tambahan bahan bakar dan juga pigmen timbal dalam cat [1]. Limbah ini akan menyebabkan pencemaran serius terhadap lingkungan jika kandungan logam berat yang terdapat di dalamnya melebihi ambang batas dan akan menyebabkan penyakit serius bagi manusia apabila terakumulasi di dalam tubuh. Timbal (Pb) merupakan salah satu pencemar yang dipermasalahkan karena bersifat sangat toksik dan tergolong sebagai bahan buangan beracun dan berbahaya [35].
Timbal adalah logam yang merusak saraf makhluk hidup dan merupakan satu dari tiga logam berbahaya lainnya yaitu (Cd dan Hg) menyebabkan meningkatnya risiko kesehatan pada manusia dan hewan karena pencemaran air oleh logam berat karena toksisitas yang berbahaya dan potensi bahaya besar untuk lingkungan dan organisme [2]. Limbah Pb ini dapat berasal dari aktivitas manusia yang berasal dari pembuangan sampah kapal-kapal, penambangan logam di laut dan lain-lain dan yang berasal dari darat seperti limbah perindustrian.
Kadar normal dan maksimum logam berat yang masuk ke lingkungan laut dapat dilihat pada Tabel 2.3
(2.3)
Tabel 2.4 Kadar normal dan maksimum logam berat yang masuk ke lingkungan laut
Unsur Kadar (ppm)
Normal (A) Maksimum (B)
Kadmium 0,00011 0,01
Timbal 0,00003 0,01
Tembaga 0,002 -
42
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Timbal adalah jenis logam lunak berwarna coklat kehitaman dan mudah dimurnikan. Kebanyakan logam toksik seperti logam Pb lebih tersebar luas dibanding kebanyakan logam toksik lainnya. Peningkatan kadar Pb di lingkungan disebabkan meningkatnya penggunaan logam ini di dalam pertambangan, logam ini berbentuk sulfida logam (PbS) yang sering disebut galena. Secara luas logam Pb banyak digunakan dalam industri misalnya sebagai zat tambahan bahan bakar, pigmen timbal dalam cat [1].
Timbal dapat menyebabkan kerusakan parah pada sistem saraf, ginjal, otak dan sistem reproduksi bahkan pada tingkat mg/L. Ion logam timbal yang ada di air limbah dari berbagai industri seperti penyimpanan asam baterai, solder, lukisan, pigmen, pestisida, peleburan, pelapisan logam, pertambangan, dan pertanian. Oleh karena itu, pengembangan metode yang dapat diandalkan untuk menghilangkan Pb (II) dalam limbah air menjadi penting supaya bahaya besar untuk lingkungan dan organisme dapat dihindari [2].
Saat ini telah banyak metode yang berkembang untuk menurunkan kadar ion logam berat dari perairan atau badan tanah, misalnya metoda pengendapan, evaporasi, elektrokimia dan penyerapan menggunakan adsorben baik berupa resin sintetik maupun karbon aktif. Namun metode tersebut dianggap kurang efektif sebab memerlukan biaya yang tinggi. Maka untuk itu perlu dicari metode penyerapan dengan menggunakan bahan yang relatif murah dan mudah didapat serta memiliki daya serap tinggi [3].
pengembangan dan pemanfaatan memodifikasi produk pertanian dalam
pengolahan air limbah [6]. Saat ini, cangkang buah karet tidak termanfaatkan dan tidak bernilai ekonomis. Limbah tanaman karet berupa cangkang buah memiliki potensi untuk dijadikan bahan yang lebih bermanfaat karena tanaman karet menghasilkan cangkang buah yaitu sebesar 500 kg/Ha/tahun [7].Perkebunan karet Indonesia merupakan yang terluas di dunia, pada tahun 2012, luasnya mencapai 3,4 juta Ha, atau 15 % dari luas total perkebunan di Indonesia [8].
Penelitian terdahulu yang telah dilakukan dalam pembuatan karbon aktif dari tanaman karet diantaranya Vinsiah, dkk., (2015) mempelajari pembuatan karbon aktif dari cangkang buah buah karet (Hevea brasilliensis) dengan aktivator H3PO4 7% dan ukuran 100 mesh serta rasio impregnasi 1:4 pada temperatur 300 o
C, 400 oC, 500 oC, dan 600 oC selama ±1 jam didapatkan hasil karbon aktif terbaik dicapai oleh karbon aktif dengan suhu furnace 600 oC [9]. Juga pada penelitian Srinivasakannan dkk., (2004) mempelajari Production of activated carbon from rubber wood sawdust, dimana digunakan H3PO4 60 % sebagai agen
aktivasi dengan rasio perbandingan 1; 1,5 dan 2 pada temperatur aktivasi 400 oC dan 500oC didapat karbon aktif terbaik yaitu pada Semi-karbonisasi pada 200 oC 15 menit diikuti aktivasi pada 500 oC 45 menit dengan rasio impregnasi 1,5 menghasilkan produk dengan bilangan iodin 1096, luas permukaan of 1496 m2/g dengan yield 35% [10]. Sedangkan pada penelitian Borhan dan kamil (2012) mempelajari Preparation and Characterization of Activated Carbon from Rubber-seed Shell by Chemical Activstion, dimana digunakan KOH sebagai agen aktivasi dengan rasio impregnasi 1:1 pada temperatur aktivasi 500 oC dan 600 oC dan waktu aktu aktivasi 30 – 210 menit didapat hasil pada tempertaur 500 oC dan waktu aktivasi 180 menit adalah yang terbaik [11].
44
pengaktivasi digunakan dalam menghilangkan ion Zn(II) dari larutan air, dan itu menunjukkan bahwa karbon aktif dari cangkang buah karet adalah penjerap efektif bagi ion logam dan senyawa organik [12]. Sulaiman, Siti Zaharah Binti (2012) melakukan penelitian menjerap Pb(II), Zn(II) dan Fe(II) ion-ion logam berat dengan menggunakan variasi larutan pH, masa dan kepekatan awal. Adsorbat disediakan dengan melarutkan 100 mg/L logam berat yang akan digunakan untuk menguji penjerapan ion-ion logam berat. Penjerapan logam Pb(II), Zn(II) dan Fe(II) diterangkan oleh model Langmuir dan Freundlich Hasil yang diperoleh dimana kapasitas penjerapan maksimum karbon aktif cangkang buah karet adalah Pb(II) dengan 14.41mg/g. Hasil penjerapan logam Pb(II), Zn(II) dan Fe(II) dengan nilai R² secara berurut yaitu 0.7081, 0.9768 dan 0.9982 [13].
Berdasar potensi dari cangkang buah karet sebagai karbon aktif yang cukup besar, maka dirasa perlu bagi penulis untuk memanfaatkan cangkang buah karet yang memiliki potensi untuk dijadikan karbon aktif dengan menggunakan
aktivasi kimia yang diaplikasikan untuk menjerap ion logam berat terutama logam timbal.
1.2 PERUMUSAN MASALAH
Adapun yang menjadi rumusan masalah dari penelitian ini adalah :
1. Sejauh mana limbah cangkang buah karet dapat dimanfaatkan sebagai karbon aktif.
2. Seberapa efektif pemanfaatan cangkang buah karet sebagai karbon aktif dalam menjerap logam timbal.
1.3 TUJUAN PENELITIAN
Tujuan dari penelitian ini adalah :
1. Untuk mengetahui karakteristik dari karbon aktif yang dibuat dari cangkang buah karet
2. Untuk mengetahui kemampuan karbon aktif yang telah diaktivasi asam fosfat dalam menjerap Pb(II).
1.4 MANFAAT PENELITIAN
Adapun manfaat yang didapat dalam penelitian ini adalah:
1. Memberikan informasi mengenai pemanfaatan cangkang buah karet menjadi alternatif dalam penjerapan logam timbal.
2. Meningkatkan nilai ekonomis limbah cangkang buah karet yang selama ini hanya dibuang sehingga menjadi karbon aktif yang bermanfaat.
1.5 RUANG LINGKUP PENELITIAN
Penelitian ini akan dilaksanakan di Laboratorium Penelitian Teknik Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan. Proses utama yang digunakan dalam penelitian ini adalah aktivasi dan karbonisasi.
Penelitian ini memiliki ruang lingkup dan batasan sebagai berikut: Variabel yang digunakan adalah :
Pembuatan Adsorben Cangkang Buah Karet : a. Variabel tetap :
1. Ukuran karbon aktif = 100 mesh
2. Suhu pemanasan oven dan karbonisasi = 110 oC [9] dan 500 oC [10]; [11]
3. Waktu pemanasan oven dan karbonisasi = 2 jam dan 1 jam [14] 4. Rasio cangkang buah karet : H3PO4 = 1 : 2 [14]
5. Waktu impregnasi = 1 jam [15]
b. Variabel berubah :
Konsentrasi Aktivator = 20, 40, 60 %
Penjerapan Logam : a. Variabel tetap :
b. Konsentrasi larutan timbal yang digunakan100 ppm. c. Waktu Penjerapan= 180 menit
d. Variabel berubah :
1. Jumlah adsorben 1, 2, 3, dan 4 gram / 100 ml larutan Pb(II). 2. Konsentrasi aktivator asam fosfat 20, 40, 60 %
46 a. Analisis pada karbon aktif :
1. Kadar yield 2. Kadar air. 3. Kadar abu.
4. Kadar zat menguap
5. Karakteristik luas permukaan karbon aktif dengan BET.
ABSTRAK
Kebutuhan karbon aktif di Indonesia semakin meningkat seiring berkembangnya era industri. Jika ditinjau dari sumber daya alam di Indonesia, sangatlah mungkin kebutuhan karbon aktif dapat dipenuhi dengan produksi dari dalam negeri. Cangkang buah karet merupakan limbah padat yang sangat berpotensial untuk beragam kegunaan, diantaranya adalah untuk bahan baku pembuatan karbon aktif. Dalam penelitian ini, limbah cangkang buah karet tersebut diolah menjadi arang aktif. Tujuan penelitian ini adalah untuk mengetahui pengaruh konsentrasi aktivator asam fosfat terhadap karakteristik karbon aktif serta daya serap karbon aktif terhadap logam Pb(II). Cangkang buah karet yang lolos pada ayakan 100 mesh diimpregnasi dengan aktivator asam fosfat (H3PO4) dengan rasio cangkang
buah karet : asam fosfat (b:b) sebesar 1:2 dan variasi konsentrasi (H3PO4) sebesar
20%, 40%, dan 60% selama 1 jam. Setelah proses perendaman dengan asam tersebut, bahan dikarbonisasi di dalam furnace pada suhu 500oC selama 1 jam. Analisa luas permukan karbon aktif menggunakan alat Braunanear, Emmelt dan Teller dan konsentrasi hasil penjerapan logam Pb(II) diukur dengan Spektroskopi Serapan Atom. Hasil penelitian menunjukkan karakteristik karbon aktif secara umum telah memenuhi Standar Nasional Indonesi. Karbon aktif hasil aktivasi asam fosfat dengan konsentrasi 20% mampu menghilangkan kadar ion Pb(II) sebesar 74%.
32
ABSTRACT
Activated carbon needs in Indonesia was increasing along with the developments of the industriaization era. Based on natural product in Indonesia, probably activated carbon needs could be guaranteed by domestic production. Rubber shells were solid waste which has potential for multiple uses such as raw materials for the manufacture of activated carbon. In this, rubber shells waste were processed into activated charcoal. The aim of this research was to determine the effect of the concentration of phosphoric acid activator on the characteristics of the activated carbon and activated carbon absorption capacity to Pb(II). Shells rubber that passed by the 100 mesh sieve was impregnated with phosphoric acid (H3PO4) as activator in the ratio fruit shells rubber: phosphoric acid (b:b) of 1:2
and varying concentrations of H3PO4 at 20%, 40%, and 60% for 1 hour. After
immersion in the acid, material was carbonized in a furnace at temperature 500 oC for 1 hour. Surface area of activated carbon was analyzed by using Braunanear, Emmelt and Teller and concentration of adsorption of Pb(II) was measured by Atomic Absorption Spectroscopy. The results showed the general characteristics of activated carbon where comparable to the Indonesian National Standard. The largest adsorption capasity percentage 74% is obtained using Rubber shell activated carbon that activated by 20% phosphoric acid.
PEMBUATAN KARBON AKTIF DARI CANGKANG BUAH
KARET (Hevea brasilliensis) DENGAN AKTIVATOR H3PO4
DAN APLIKASINYA SEBAGAI PENJERAP Pb(II)
SKRIPSI
Oleh
JOKO MURTONO
120405118
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
25
PEMBUATAN KARBON AKTIF DARI CANGKANG BUAH
KARET (Hevea brasilliensis) DENGAN AKTIVATOR H3PO4
DAN APLIKASINYA SEBAGAI PENJERAP Pb(II)
SKRIPSI
Oleh
JOKO MURTONO
120405118
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
2017
Saya menyatakan dengan sesungguhnya bahwa skripsi dengan judul:
PEMBUATAN KARBON AKTIF DARI CANGKANG BUAH
KARET (Hevea brasilliensis) DENGAN AKTIVATOR H3PO4
DAN APLIKASINYA SEBAGAI PENJERAP Pb(II)
Dibuat untuk melengkapi sebagian persyaratan menjadi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini adalah hasil karya saya kecuali kutipan-kutipan yang telah saya sebutkan sumbernya. Demikian pernyataan ini diperbuat, apabila dikemudian hari terbukti bahwa karya ini bukan karya saya atau merupakan hasil jiplakan maka saya bersedia menerima sanksi sesuai aturan yang berlaku.
Medan, Januari 2017
Joko Murtono
NIM : 120405118
27 Skripsi dengan judul :
Pembuatan Karbon Aktif Dari Cangkang Buah Karet (Hevea
brasilliensis) Dengan Aktivator H
3PO4 Dan Aplikasinya SebagaiPenjerap Pb(II)
dibuat untuk melengkapi persyaratan menjadi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini telah diajukan pada sidang ujian skripsi pada 25 Januari 2017 dan dinyatakan memenuhi syarat/sah sebagai skripsi pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara.
Mengetahui, Medan, 2017
Koordinator Skripsi, Dosen Pembimbing
Ir. Renita Manurung, M.T Dr. Ir. Iriany, M.Si.
NIP : 19681214 199702 2 002 NIP : 19640613 199003 2 001
Dosen Penguji I Dosen Penguji II
Dra.Siswarni MZ, M.S Okta Bani, ST. MT
Puji dan syukur kehadirat Allah SWT atas limpahan rahmat dan karunia-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan skripsi dengan judul “Pembuatan Karbon Aktif dari Cangkang Buah Karet (Hevea brasilliensis) dengan Aktivator H3PO4 dan Aplikasinya Sebagai Penjerap Pb(II)” berdasarkan hasil penelitian yang penulis lakukan di Departemen Teknik Kimia Universtas Sumatera Utara. Skripsi ini merupakan salah satu syarat untuk mendapatkan gelar Sarjana Teknik.
Melalui penelitian ini diperoleh hasil karbon aktif dari cangkang buah karet, sehingga hasil yang diperoleh dapat dimanfaatkan untuk mengurangi jumlah limbah cangkang buah karet dan mengurangi limabah ion logam Pb(II).
Selama melakukan penelitian hingga penulisan skripsi ini, penulis banyak mendapat pengarahan dan bimbingan dari dosen pembimbing penulis. Untuk itu secara khusus penulis mengucapkan terima kasih dan penghargaan yang sebesar-besarnya kepada Ibu Dr. Ir. Iriany, M.Si.
Penulis menyadari bahwa skripsi ini masih