PENGARUH KEDALAMAN LUBANG INJEKSI DAN BAGIAN
BATANG INJEKSI TERHADAP PEMBENTUKAN GUBAL
GAHARU (Aquilaria malaccensis Lamk.)
SKRIPSI
Oleh :
SUDYANTO D P S 091201117
PROGRAM STUDI KEHUTANAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
LEMBAR PENGESAHAN
Judul Penelitian : Pengaruh Kedalaman Lubang Injeksi dan Bagian Batang Injeksi terhadap Pembentukan Gubal Gaharu
(A. malaccensis Lamk.)
Nama : Sudyanto D P S
NIM : 091201117
Jurusan : Budidaya Hutan
Disetujui oleh Komisi Pembimbing
Dr. Ir. Edy Batara M. S, MS Nelly Anna, S.Hut, M.Si
Ketua Anggota
Mengetahui
Siti Latifah, S.Hut, M.Si., Ph.D Ketua Program Studi Kehutanan
ABSTRAK
SUDYANTO D. P. SAMOSIR: Pengaruh Kedalaman Lubang Injeksi dan Bagian Batang Injeksi terhadap Pembentukan Gubal Gaharu (A. malaccensis Lamk.). Dibimbing oleh EDY BATARA MULYA SIREGAR dan NELLY ANNA.
Indonesia adalah produsen gaharu terbesar di dunia dan menjadi tempat tumbuh endemik beberapa spesies gaharu komersial dari marga Aquilaria. Saat ini tanaman gaharu berada diambang kepunahan, maka perlu dilakukan upaya peningkatan produksi gubal gaharu.Penelitian ini bertujuan untuk mengukur pembentukan dan kualitas gubal gaharu dengan kombinasi perlakuan kedalaman lubang injeksi dan bagian batang injeksi pada pohon A. malaccensis.Penelitian ini dilaksanakan di Lahan pohon A. malaccensis milik Bapak Petro Sembiring di Desa Tuntungan, Kecamatan Medan Tuntungan, Kota Medan.Penelitian ini menggunakan rancangan acak lengkap faktorial dengan 2 faktor yaitu kedalaman lubang injeksi (3 cm, 5 cm, dan 7 cm) dan bagian batang injeksi (bawah, tengah, dan atas).Inokulum yang diinjeksikan sebanyak 5 ml pada setiap lubang.Parameter yang diamati adalah persentase infeksi, waktu inkubasi, perkembangan infeksi, kualitas gubal, dan reisolasi Fusariumsp.
Hasil penelitian menunjukkan bahwa kombinasi kedalaman lubang injeksi dengan bagian batang injeksi tidak berpengaruh nyata terhadap semua parameter yang diamati. Infeksi inokulum terjadi pada minggu keempat setelah proses injeksi inokulum. Perubahan warna terjadi dari putih menjadi kecoklatan dan terdapat aroma yang tidak kuat pada gubal gaharu yang terbentuk.Reisolasi Fusariumsp. menunjukkan gubal gaharu terbentuk akibat infeksi inokulum.Persentase infeksi terbesar terjadi pada kedalaman injeksi 3 cm dan persentase terkecil terjadi pada kedalaman injeksi 5 cm.
ABSTRACT
SUDYANTO D. P. SAMOSIR: Effect Of depth of the hole injection And The Injection Stem Against Establishment Agarwood (A. malaccensis Lamk.).Under Supervision ofEDY BATARA MULYA SIREGAR and NELLY ANNA.
Indonesia is the world's largest agarwood producer and a place to grow some of the endemic species of the genus Aquilaria commercial agarwood.Agarwood is currently on the verge of extinction, it is necessary to increase in production agarwood. The objective of this research was to measure the formation and quality of agarwood with a combination of treatments is the depth of the hole injection and injection stem of the tree A. malaccensis. The research was conducted in the Land of trees A. malaccensis owned by Mr. Petro Sembiring,in Tuntungan Village, Kecamatan Medan Tuntungan, Medan. This research used a factorial completely randomized design with 2 factors that depth of the injection hole (3 cm, 5 cm, and 7 cm )and and the injection stem (rootstock, middle trunk, and upper trunk). Inoculum were injected as much as 5 ml in each hole.The parameters measured werepercentage of infection, incubation time, development of infection, the quality of gubal, and reisolasi Fusarium sp.
The results showed that the combination of the depth of the hole injection to injection stem had no significant effect on all parameters were observed. Inoculum infections occurred in the fourth week after the injection of inoculum. The Color change from white to brown occurred and there is no strong aroma of agarwood formed. Reisolasi Fusarium sp. show agarwood formed by injection of inoculum. The percentage of infection occurred at a depth of 3 cm and the smallest percentage of injection occurred at a depth of 5 cm.
RIWAYAT HIDUP
Penulis dilahirkan di kota Pematangsiantar pada tanggal 20 Juni 1991 dari
ayahanda Oberlin Samosir dan Ibunda Rusly Hutabalian. Penulis merupakan anak pertama dari tiga bersaudara.
Penulis memulai pendidikan di SDN 102074 Sei Birung, Bandar Khalipah
dan lulus pada tahun 2003, kemudian melanjutkan pendidikan di SMP Negeri 1 Bandar Khalipah dan lulus pada tahun 2006. Penulis melanjutkan pendidikan di SMA
Negeri 1 Tebing Tinggi dan lulus pada tahun 2009. Penulis diterima masuk di Fakultas Pertanian USU melalui jalur ujian tertulis Ujian Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN) pada tahun 2009.Penulis memilih jurusan
Budidaya Hutan, Program Studi Kehutanan, Universitas Sumatera Utara.
Selama mengikuti perkuliahan, penulis aktif sebagai anggota Himpunan
Mahasiswa Sylva (HIMAS).Penulis mengikuti kegiatan Praktek Pengenalan Ekosisten Hutan di TAHURA Bukit Barisan pada tahun 2011.Penulis melaksanakan praktek kerja lapangan (PKL) di Taman Nasional Ujung Kulon, Tangerang, Banten,
dari tanggal 01 Februari sampai 01 Maret 2013.
Penulis melaksanakan penelitian dari bulan Mei sampai Oktober 2013 dengan
KATA PENGANTAR
Penulis mengucapkan puji dan syukur kepada Tuhan Yang Maha Esa dimana
atas kasih dan rahmat-Nya sehingga Penulis dapat menyelesaikan penelitian ini.Judul penelitian ini adalah “Pengaruh Kedalaman Lubang Injeksi dan Bagian Batang Injeksi terhadap Pembentukan Gubal Gaharu (Aquilaria malaccensis Lamk)”.
Penelitian ini bertujuan untuk mengukur pembentukan dan kualitas gubal gaharu dengan kombinasi perlakuan kedalaman lubang injeksi dan bagian batang
injeksi pada pohon A. malaccensis sehingga diperoleh data yang diharapkan mampu memberikan informasi terbaru tentang percepatan produksi gubal gaharu dan menjadi acuan untuk pengelolaan gaharu yang lestari.Skripsi ini merupakan syarat kelulusan
di Program Studi Kehutanan, Fakultas Pertanian, Universitas Sumatera Utara, Medan. Pada kesempatan ini Penulis mengucapkan terima kasih kepada dosen
pembimbing skripsi saya, Bapak Dr. Ir. Edy Batara Mulya Siregar, MS., dan Ibu Nelly Anna, S. Hut, M.Si., yang telah membimbing Penulis dalam penulisan skripsi ini.
Penulis juga menyampaikan terima kasih kepada seluruh pegawai dan dosen pengajar di Program Studi Kehutanan serta kepada teman-teman mahasiswa yang
DAFTAR ISI
Syarat Tumbuh dan Penyebaran gaharu di Indonesia ... 6
HASIL DAN PEMBAHASAN
Persentase Infeksi ... 18
Waktu Inkubasi ... 20
Perkembangan Infeksi ... 21
Kualitas Gubal ... 22
Reisolasi Gubal Gaharu ... 27
KESIMPULAN DAN SARAN Kesimpulan ... 29
Saran ... 29 DAFTAR PUSTAKA
DAFTAR TABEL
No. Halaman
1. Klasifikasi mutu produk gaharu berdasarkan Standar Nasional Indonesia
(SNI) ... 7
2. Persentase infeksi gubal gaharu ... 18
3. Panjang infeksi Fusarium sp. ... 21
4. Lebar infeksi Fusarium sp. ... 22
5. Kualitas warna gubal gaharu ... 25
DAFTAR GAMBAR
No. Halaman
1. Sketsa injeksi pada batang pohon ... 14
2. Infeksi gubal gaharu ... 19
3. Warna gubal gaharu yang terinfeksi pada kedalaman 3 cm pada batang ... 23
4. Warna gubal gaharu yang terinfeksi pada kedalaman 5 cm pada batang ... 24
5. Warna gubal gaharu yang terinfeksi pada kedalaman 7 cm pada batang. .... 24
DAFTAR LAMPIRAN
No. Halaman
1. Data persentase infeksi gubal gaharu... 34
2. Data infeksi gubal gaharu... 39
3. Analisis sidik ragam pekembangan infeksi... 50
ABSTRAK
SUDYANTO D. P. SAMOSIR: Pengaruh Kedalaman Lubang Injeksi dan Bagian Batang Injeksi terhadap Pembentukan Gubal Gaharu (A. malaccensis Lamk.). Dibimbing oleh EDY BATARA MULYA SIREGAR dan NELLY ANNA.
Indonesia adalah produsen gaharu terbesar di dunia dan menjadi tempat tumbuh endemik beberapa spesies gaharu komersial dari marga Aquilaria. Saat ini tanaman gaharu berada diambang kepunahan, maka perlu dilakukan upaya peningkatan produksi gubal gaharu.Penelitian ini bertujuan untuk mengukur pembentukan dan kualitas gubal gaharu dengan kombinasi perlakuan kedalaman lubang injeksi dan bagian batang injeksi pada pohon A. malaccensis.Penelitian ini dilaksanakan di Lahan pohon A. malaccensis milik Bapak Petro Sembiring di Desa Tuntungan, Kecamatan Medan Tuntungan, Kota Medan.Penelitian ini menggunakan rancangan acak lengkap faktorial dengan 2 faktor yaitu kedalaman lubang injeksi (3 cm, 5 cm, dan 7 cm) dan bagian batang injeksi (bawah, tengah, dan atas).Inokulum yang diinjeksikan sebanyak 5 ml pada setiap lubang.Parameter yang diamati adalah persentase infeksi, waktu inkubasi, perkembangan infeksi, kualitas gubal, dan reisolasi Fusariumsp.
Hasil penelitian menunjukkan bahwa kombinasi kedalaman lubang injeksi dengan bagian batang injeksi tidak berpengaruh nyata terhadap semua parameter yang diamati. Infeksi inokulum terjadi pada minggu keempat setelah proses injeksi inokulum. Perubahan warna terjadi dari putih menjadi kecoklatan dan terdapat aroma yang tidak kuat pada gubal gaharu yang terbentuk.Reisolasi Fusariumsp. menunjukkan gubal gaharu terbentuk akibat infeksi inokulum.Persentase infeksi terbesar terjadi pada kedalaman injeksi 3 cm dan persentase terkecil terjadi pada kedalaman injeksi 5 cm.
ABSTRACT
SUDYANTO D. P. SAMOSIR: Effect Of depth of the hole injection And The Injection Stem Against Establishment Agarwood (A. malaccensis Lamk.).Under Supervision ofEDY BATARA MULYA SIREGAR and NELLY ANNA.
Indonesia is the world's largest agarwood producer and a place to grow some of the endemic species of the genus Aquilaria commercial agarwood.Agarwood is currently on the verge of extinction, it is necessary to increase in production agarwood. The objective of this research was to measure the formation and quality of agarwood with a combination of treatments is the depth of the hole injection and injection stem of the tree A. malaccensis. The research was conducted in the Land of trees A. malaccensis owned by Mr. Petro Sembiring,in Tuntungan Village, Kecamatan Medan Tuntungan, Medan. This research used a factorial completely randomized design with 2 factors that depth of the injection hole (3 cm, 5 cm, and 7 cm )and and the injection stem (rootstock, middle trunk, and upper trunk). Inoculum were injected as much as 5 ml in each hole.The parameters measured werepercentage of infection, incubation time, development of infection, the quality of gubal, and reisolasi Fusarium sp.
The results showed that the combination of the depth of the hole injection to injection stem had no significant effect on all parameters were observed. Inoculum infections occurred in the fourth week after the injection of inoculum. The Color change from white to brown occurred and there is no strong aroma of agarwood formed. Reisolasi Fusarium sp. show agarwood formed by injection of inoculum. The percentage of infection occurred at a depth of 3 cm and the smallest percentage of injection occurred at a depth of 5 cm.
PENDAHULUAN
Latar Belakang
Indonesia adalah produsen gaharu terbesar di dunia dan menjadi tempat
tumbuh endemik beberapa spesies gaharu komersial dari marga Aquilaria sepertiA. malaccensis, A. microcarpa, A. hirta, A. beccariana, A. filaria dan lain-lain (Sidiyasa & Suharti, 1987). Menurut Burkill (1935), perdagangan gaharu Indonesia sudah
dikenal sejak lebih dari 600 tahun silam yakni dalam perdagangan Pemerintah Hindia Belanda dan Portugis. Gaharu dari Indonesia banyak yang dikirim ke Negara Cina,
Taiwan dan Saudi Arabia.
Komoditas gaharu telah cukup lama dikenal masyarakat secara umum.Beberapa jenis tanaman gaharu yang dikenal antara lain Aquilaria malaccensis
(A. malaccensis), A. filaria, A. hirta, A. agalloccha, A. macrophylum dan beberapa puluh jenis lainnya.Dari puluhan jenis tanaman yang berpotensi tersebut, A.
malaccensis adalah tanaman penghasil gaharu berkualitas terbaik dengan nilai jual yang sangat tinggi.Jenis ini juga merupakan jenis yang paling banyak ditemukan di Sumatera Utara (Yusnita, 2003).
A. malaccensis sangat terkenal karena memiliki aroma yang sangat khas yang pada umumnya banyak dimanfaatkan untuk bahan wewangian dan kosmetik serta
pewangi ruangan. Selain itu, secara klinis juga dapat bermanfaat sebagai obat-obatan, antara lain obat penghilang stress, gangguan ginjal, hepatitis, sirosis, pembengkakan liver dan ginjal, TBC, reumatik, kanker, malaria dan radang lambung. Beragamnya
meningkat. Data terakhir menyebutkan bahwa saat ini harga A. malaccensis kelas super king adalah Rp 60 juta/kg sedangkan untuk kelas biasa Rp 2 juta/kg. Saat ini
tanaman gaharu berada diambang kepunahan. Hal ini sesuai dengan hasil penelitian dari CITES yang memasukkan tanaman A. malaccensis kedalam jenis tanaman terancam punah (Apendix II) (Sumarna, 2005).
Penelitian mengenai berbagai aspek yang terkait dengan gaharu sudah dilakukan sejak lama dan semakin berkembang dewasa ini.Penelitian-penelitian ini
terutama didorong oleh berbagai hal seperti pasokan komersil untuk gaharu yang masih sangat tergantung dari produksi alam (Siran, 2010).Masyarakat masih belum banyak memiliki informasi mengenai teknik produksi gubal gaharu.Sehingga
budidaya A. malaccensis sangat jarang ditemukan di beberapa daerah.
Keinginan untuk meningkatkan kuota yang dikeluarkan oleh Indonesia sering
menjadi bahan pertanyaan banyak pihak akan potensi sebenarnya dan kondisi populasi gaharu di alam. Konsentrasi populasi padat Aquilaria dilaporkan terdapat Sumatera, Kalimantan, dan Papua (Soehartono dan Newton, 2000).
Untuk memenuhi permintaan ekspor yang semakin meningkat, maka perlu dilakukan upaya peningkatan produksi gubal gaharu.Selain itu, upaya mempercepat
hasil gubal gaharu juga harus dilakukan untuk mengantisipasi kelangkaan gubal gaharu. Sehingga akan diperoleh produk gaharu yang tinggi dalam waktu yang relatif singkat.
Proses inokulasi dapat dilakukan dengan cara (1) melukai bagian batang pohon, (2) menyuntikkan mikroorganisme jamur (inokulum), (3) menyuntikkan oli
tanaman. Untuk penelitian ini dilakukan cara yang kedua yaitu dengan menyuntikkan jamur kedalam batang pohon A. mallaccensis Lamk. Kelebihan tekhnik ini ialah
tingkat keberhasilan infeksinya paling besar dan cukup mudah dilakukan. Sedangkan kelemahannya ialah memerlukan biaya lebih dibandingkan ketiga tekhnik yang lain.
Tujuan Penelitian
Tujuan penelitian ini adalah :
1. Mengukur pembentukan gubal gaharu dengan kombinasi perlakuan kedalaman
injeksi dan bagian batang pada pohon A. malaccensis.
2. Mengukur kualitas gubal gaharu dengan kombinasi perlakuan kedalaman injeksi dan bagian batangpada pohon A. malaccensis.
3. Mengetahui hasil reisolasi inokulum dari gubal gaharu yang terbentuk. Hipotesis Penelitian
Hipotesis penelitian ini adalah terdapat perbedaan pembentukan gubal gaharu akibat kombinasi perlakuan kedalaman injeksi dengan bagian batang injeksi pada pohon A. malaccensis.
Manfaat Penelitian
Hasil penelitian ini diharapkan mampu memberikan informasi terbaru tentang
TINJAUAN PUSTAKA
Botani Tanaman Gaharu
Gaharu (Aquilaria malaccensis Lamk.) merupakan nama perdagangan dari
produk kayu (incense) yang dihasilkan oleh beberapa spesies pohon penghasil gaharu. Dalam perdagangan internasional, produk ini dikenal sebagai agarwood, aloeswood, atau oudh. A.malaccensis adalah salah satu jenis tanaman hutan yang memiliki mutu
sangat baik dengan nilai ekonomi tinggi karena kayunya mengandung resin yang harum. Bagian tanaman penghasil gaharu yang digunakan adalah bagian kayu yang
membentuk gubal resin, sebagai produk metabolit sekunder (Santoso dkk., 2007). Gaharu adalah sejenis resin tapi bukan resin yang dihasilkan oleh pohon gaharu, melainkan resin yang terbentuk karena adanya infeksi pada pohon tersebut.
Infeksi ini mengakibatkan sumbatan pada pengaturan makanan, sehingga menghasilkan suatu zat phytalyosin sebagai reaksi dari infeksi tersebut. Infeksi
didapat dari hasil perlukaan yang disebabkan oleh alam (serangan hama dan penyakit seperti serangga, jamur, bakteri) atau karena sengaja dilukai oleh manusia. Zat phytalyosin inilah yang merupakan resin gubal gaharu di dalam pohon karas dari jenis
Aquilaria spp. Zat yang berbau wangi jika dibakar ini tidak keluar dari batang gubalnya, tetapi mengendap menjadi satu dalam batang. Hal ini terjadi pada tanaman
Taksonomi tanaman gaharu (A. malaccensis Lamk.) adalah : Kingdom : Plantae (tumbuhan)
Divisi : Spermatophyta (tumbuhan biji)
Sub Divisi : Angiospermae (tumbuhan biji tertutup) Kelas : Dikotil (berbiji belah dua)
Sub Kelas : Dialypetale (bebas daun bermahkota)
Ordo : Myrtales (daun tunggal duduknya bersilang)
Famili : Thymeleaceae (akar berserabut jala) Genus : Aquilaria
Species : A. malaccensis Lamk. (Tarigan, 2004).
A. malaccensis memiliki morfologi atau ciri-ciri fisiologi yang sangat unik, dimana tinggi pohon ini mencapai 40 meter dengan diameter 60 cm. Pohon ini
memiliki permukaan batang licin, warna keputihan, kadang beralur dan kayunya agak keras. Tanaman ini memiliki bentuk daun lonjong agak memanjang, panjang 6-8 cm, lebar 3-4 cm, bagian ujung meruncing.Daun yang kering berwarna abu-abu kehijaun,
agak bergelombang, melengkung, permukaan daun atas-bawah licin dan mengkilap, tulang daun sekunder 12-16 pasang.Tanaman ini memiliki bunga yang terdapat
diujung ranting, ketiak daun, kadang-kadang di bawah ketiak daun.Berbentuk lancip, panjang sampai 5 mm. Dan buahnya berbentuk bulat telor, tertutup rapat oleh rambut-rambut yang berwarna merah. Biasanya memiliki panjang hingga 4 cm lebar 2,5 cm
Syarat Tumbuh dan Penyebaran Gaharu di Indonesia
A. malaccensis sesuai ditanam di antara kawasan dataran rendah hingga ke
pergunungan pada ketinggian 0 – 750 meter dari permukaan laut dengan curah hujan kurang dari 2000 mm/tahun. Suhu yang sesuai adalah antara 27°C hingga 32°C dengan kadar cahaya matahari sebanyak 70%. Kesesuaian tanah adalah jenis lembut
dan liat berpasir dengan pH tanah antara 4.0 hingga 6.0 (Sumarna, 2005).
Gaharu merupakan salah satu komoditi Hasil Hutan Non Kayu (HHNK) yang
harganya lebih tinggi dibandingkan HHNK lainnya (Wiyono dan Sumaliani, 1998).Gaharu digunakan sebagai bahan dasar dalam industri parfum, dupa, kosmetik, dan obat-obatan.Sehingga gaharu bisa dikatakan sebagai salah satu jenis komoditi
HHNK yang memliki nilai multiguna.Genus Aquilaria merupakan tanaman yang menjadi sumber utama penghasil gaharu, selain Gyrynops sp, Gonystylus sp, dan Aetoxylonsympetallum (Sumarna, 2002).
Di Indonesia letak tanaman gaharu menyebar dari Sumatera hingga Irian Jaya. Dari hasil survei tahun 2001 yang dilakukan oleh ASGARIN diketahui bahwa sisa
pohon gaharu di daerah penghasil utama gaharu adalah Sumatera 26%, Kalimantan 27%, Nusa Tenggara 5%, Sulawesi 4%, Maluku 6% dan Papua 37% (Tarigan, 2004).
Ada beberapa jenis pohon gaharu yang berpotensi untuk memproduksi gubal dan sudah banyak dieksplorasi. Jenis pohon gaharu tersebut antara lain Aquilariasp, Aetoxylon sympetallum, Gyrinops, dan Gonsystylus yang tersebar di Kalimantan,
Sumatera, Sulawesi, Nusa Tenggara, dan Papua. Pohon gaharu dapat tumbuh di dataran rendah hingga dataran tinggi dan hampir pada semua jenis tanah(Sidiyasa &
Kelas Produksi Gaharu
Sesuai Standar Nasional Indonesia (SNI) yang ditetapkan oleh Dewan
Standardisasi Nasional (DSN), masing-masing kelompok produk gahru tersebut masih dibagi menjadi beberapa kelas, seperti pada tabel berikut.
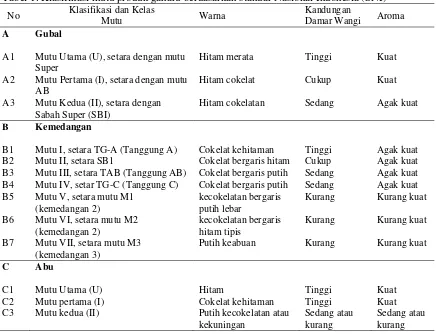
Tabel 1. Klasifikasi mutu produk gaharu berdasarkan standar Nasional Indonesia (SNI)
No Klasifikasi dan Kelas
Mutu Warna
Kandungan
Damar Wangi Aroma A Gubal
A1 Mutu Utama (U), setara dengan mutu Super
Hitam merata Tinggi Kuat
A2 Mutu Pertama (I), setara dengan mutu AB
Hitam cokelat Cukup Kuat
A3 Mutu Kedua (II), setara dengan Sabah Super (SBI)
Hitam cokelatan Sedang Agak kuat
B Kemedangan
B1 Mutu I, setara TG-A (Tanggung A) Cokelat kehitaman Tinggi Agak kuat B2 Mutu II, setara SB1 Cokelat bergaris hitam Cukup Agak kuat B3 Mutu III, setara TAB (Tanggung AB) Cokelat bergaris putih Sedang Agak kuat B4 Mutu IV, setar TG-C (Tanggung C) Cokelat bergaris putih Sedang Agak kuat B5 Mutu V, setara mutu M1
(kemedangan 2)
kecokelatan bergaris putih lebar
Kurang Kurang kuat
B6 Mutu VI, setara mutu M2 (kemedangan 2)
kecokelatan bergaris hitam tipis
Kurang Kurang kuat
B7 Mutu VII, setara mutu M3 (kemedangan 3)
Putih keabuan Kurang Kurang kuat
C Abu
C1 Mutu Utama (U) Hitam Tinggi Kuat
C2 Mutu pertama (I) Cokelat kehitaman Tinggi Kuat C3 Mutu kedua (II) Putih kecokelatan atau
kekuningan
Menurut Raffa et al. (1985) gaharu terbentuk karena adanya produksi dan akumulasi senyawa resin di dalam jaringan batang tanaman penghasil gaharu.
Banyak pendapat yang berkembang mengenai proses pembentukan gaharu. Menurut Ng et al. (1997) gaharu terbentuk karena adanya pelukaan atau pelukaan
yang diikuti infeksi cendawan.Mohamed et al. (2010) menemukan pembentukan gaharu yang wangi pada bekas luka yang disertai adanya miselium cendawan. Namun secara umum cendawan banyak dilaporkan berpengaruh dalam proses pembentukan
gaharu (Qi et al. 2005). Gaharu dihasilkan tanaman sebagai respon tanaman terhadap
adanya cendawan yang masuk kedalam jaringan tanaman yang luka
(Bhuiyan et al. 2009).
Gubal dihasilkan pohon gaharu sebagai respon terhadap infeksi mikroba/cendawan yang masuk ke dalam jaringan luka (Oldfield et al., 1998 dalam
Barden et al., 2000), luka dapat disebabkan secara alami maupun secara sengaja dengan pengeboran dan penggergajian. Masuknya mikroba ke dalam jaringan
tanaman dianggap sebagai benda asing sehingga sel tanaman akan menghasilkan senyawa fitoaleksin yang berfungsi sebagai pertahanan terhadap infeksi patogen (Zubair, 2008). Menurut Shimada et al., (1982) dalam Yagura et al., (2003) senyawa
fitoaleksin dapat berupa resin aromatik yang pada gaharu didominasi oleh seskuiterpen dan kromon yang berwarna coklat atau hitam serta merupakan senyawa
harum penentu kualitas gubal gaharu.
Gubal gaharu adalah bagian dari pohon yang terinfeksi cendawan, berwarna coklat kehitaman dan harum baunya bila dibakar. Santoso et al., (2007) menduga
bahwa terbentuknya gaharu berkaitan dengan gejala patologis sedangkan menurut Burkill (1935),gubal gaharu terbentuk sebagai reaksi pohon gaharu terhadap serangan
jaringan kayu, akibatnya jaringan kayu mengeras, berwarna kehitaman dan berbau wangi (Zubair, 2008).
Menurut Sumarna (2007) mengatakan kedalaman pemboran disesuaikan dengan diameter batang pohon, biasanya sekitar 1/3 dari diameter batang.Diameter infeksi merupakan tahapan cendawan yang berada pada kondisi stabil dan menetap di
dalam sel atau jaringan inang dan memperoleh nutrisi dari inangnya.Cendawan membentuk hifa infeksi setelah cendawan masuk ke dalam sel inang.Hifa infeksi
merupakan perpanjangan hifa penetrasi.Pada beberapa cendawan setelah terbentuk hifa penetrasi terbentuk vesikel dan selanjutnya membentuk hifa infeksi. Terakhir cendawan akan menghasilkan haustorium agar dapat memanfaatkan nutrisi sel inang
(Mendgen & Deising 1993). Secara umum Fusarium spp. membentuk struktur seperti haustorium (Kikot et al. 2009). Setelah proses infeksi, cendawan melakukan
kolonisasi dengan berkembang atau memperbanyak diri, atau dua-duanya dalam jaringan tanaman (Prins et al. 2000; Lee & Bostock 2006).
Menurut Susilo (2003) bahwa reaksi pohon penghasil gaharu tidak sama baik
waktu maupun jenis gubal gaharu yang akan dihasilkannya. Universitas Mataram telah menemukan bahwa pembentukan kayu gaharu atau gubal disebabkan oleh Fusarium lateritium dan Fusarium popularia tetapi badan penelitian dan
pengembangan kehutanan menemukan bahwa semua jenis Fusarium dapat menginfeksi tanaman gaharu dan menghasilkan gubal gaharu.
Fusarium sp. termasuk ke dalam kelompok cendawan bermitospora.Bentuk spora aseksual (konidia) merupakan ciri utama dari cendawan ini.Fusarium sp.
terdiri atas satu atau dua sel atau makrokonidia yang terdiri atas beberapa sel (2-10 sel) yang berbentuk seperti bulan sabit.Konidia dibentuk di atas monopialid.Selain
membentuk makro dan mikro konidia, Fusarium sp.(Wang & Jeffer, 2000; Ploetz, 2005) juga membentuk klamidospora ketika kondisi lingkungan dan bahan makan kurang menguntungkan.Selain dapat menginduksi terbentuknya gaharu, Fusarium sp.
merupakan cendawan patogen tanaman yang sering menyebabkan berbagai penyakit pada tanaman seperti busuk pangkal batang, tumor akar (root crown), dan penyakit
pembuluh xylem (Groenewald, 2005).
Inokulasi adalah kontak awal patogen pada suatu tanaman yang mungkin terinfeksi.Inokulum adalah bagian dari patogen yang dapat memulai infeksi.Tidak
semua inokulum mampu melakukan infeksi pada tanaman, hanya inokulum patogen berpotensi untuk menginfeksi tumbuhan (Agrios, 1996).
Cendawan yang secara umum telah diketahui dapat menginduksi pembentukan gubal gaharu adalah dari genus Fusarium (Budi et al., 2010). Cendawan-cendawantersebut diperoleh dari hasil isolasi pada gubal yang sudah
terbentuk di alam, namum demikian efektivitasnya tersebut dalam menginduksi pembentukan gubal belum diketahui secara jelas. Oleh karena itu dibutuhkan suatu
kajian untuk melihat potensinya melalui proses inokulasi buatan.
Gejala umum yang ditimbulkan akibat infeksi cendawan diantaranya terjadi perubahan warna pada daerah yang diinfeksi dan klorosis daun (Putri et al.
2008).Gejala yang terjadi bisa teramati beberapa hari setelah tanaman diinokulasi cendawan.Namun, pada pohon gaharu alam yang terbentuk secara alami dan
bagian kayu tapi terjadinya klorosis daun tidak terlihat lagi, sehingga ketika dilihat secara visual tanaman terlihat sehat (Barden et al. 2000).
Cendawan kadang menghasilkan senyawa toksin yang disekresikan saat penetrasi jaringan inang untuk merubah fisiologi tanaman dan mengganggu permeabilitas dinding sel tanaman (Bushnell 1995).Terganggunya permeabilitas sel
tanaman akibat ikatan toksin pada membran sel menyebabkan kerusakan struktur membran (Bushnell 1995).Kebanyakan toksin merupakan senyawa sekunder
berbobot molekul rendah yang dikeluarkan secara ekstraseluler oleh cendawan (Prins et al. 2000). Beberapa jenis toksin yang dihasilkan Fusarium spp. diantaranya enniatin, fumonisin, sambutoksin, dan trikotesen (Kim et al. 1995; Hermann et al.
1996; Seo et al. 1996; Kang & Buchenenauer 2002; Langevin et al. 2004).
Proses pembentukan gubal pada pohon gaharu, hingga saat ini masih terus
diteliti. Gubal gaharu diduga dapat terbentuk melalui infeksi cendawan (Nobuchi & Siripatanadilok, 1991). Beberapa cendawan yang berasosiasi dengan gubal gaharu, yaitu: Fusariumoxyporum, F. bulbigenium dan F. lateritium telah
berhasil diisolasi oleh Santoso (1996).
Pada proses interaksi antara cendawan dengan inangnya, patogenesitas
cendawan merupakan hal yang terpenting. Keberhasilan cendawan dalam interaksi dengan inangnya bergantung pada strategi cendawan dalam melakukan penetrasi tanaman inangnya (Mendgen & Deising 1993). Interaksi cendawan patogen akan
menyebabkan terjadinya perubahan fisiologis pada tanaman yang berdampak terhadap terjadinya perubahan visual pada sel, jaringan, atau organ tanaman. Diantara
informasi yang lebih akurat tentang terjadinya perubahan fisiologi saat terjadi interaksi cendawan dengan inangnya (Kunoh, 1995).
Senyawa terpenoid merupakan salah satu metabolit sekunder yang diproduksi
oleh tumbuhan sebagai respon terhadap luka dan infeksi cendawan (Nobuchi & Siripatanadilok, 1991). Terpenoid terdiri atas beberapa senyawa , mulai
dari komponen miyak atsiri, yaitu monoterpenoid dan sesquiterpenoid yang mudah menguap, diterpen yang lebih sukar menguap, dan senyawa yang tidak menguap yaitu
tripernoid daan sterol (Harbone, 1987).
Tidak semua inokulum mampu melakukan infeksi pada tanaman, hanya inokulum patogen berpotensi untuk menginfeksi tumbuhan.Inokulum memiliki
mekanisme bertahan, misalnya dorman pada kondisi inang dan atau lingkungan yang kurang sesuai.Inokulum adalah struktur dari patogen yang dapat menimbulkan infeksi
(Rukmana dan Saputra, 1997).
Serangan dan infeksi cendawan dapat mengganggu proses fisiologis dan morfologi tanaman (Nieamann & visintini 2005; Lee & Bostock 2006). Berdasarkan
perluasan gejala yang terjadi dikenal gejala lokal dan gejala sistimetik (Christiansen et al. 1999).Gejala lokal adalah gejala yang hanya terdapat di daerah inokulasi
METODOLOGI PENELITIAN
Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di lahan pohon A. malaccensis milik Bapak Petro
Sembiring di Desa Tuntungan, Kecamatan Medan Tuntungan, Kota Medan.Waktu penelitian dilaksanakan pada Mei 2013 - Oktober 2013.
Bahan dan Alat Penelitian
Bahan – bahan yang digunakan dalam penelitian ini adalah pohon A. malaccensis yang berusia 5 tahun, Fusarium sp, aquades, dan alkohol. Sedangkan
alat – alat yang digunakan adalah pinset, cawan petri, gelas ukur, bor kayu dan mata bor, genset, kabel sepanjang 12 m, spidol, kapas, jarum suntik, ranting kayu, kalkulator, pita ukur, buku, alat tulis, dan penggaris.
Metode Penelitian
1. Melakukan inventarisasi pohon, dengan mengukur tinggi dan diameter supaya
didapat pohon yang sesuai kriteria dengan syarat pohon yang dapat di injeksi. Pohon yang dapat di injeksi adalah pohon yang memiliki diameter 10 cm. Lalu pilih 15 pohon sebagai objek penelitian.
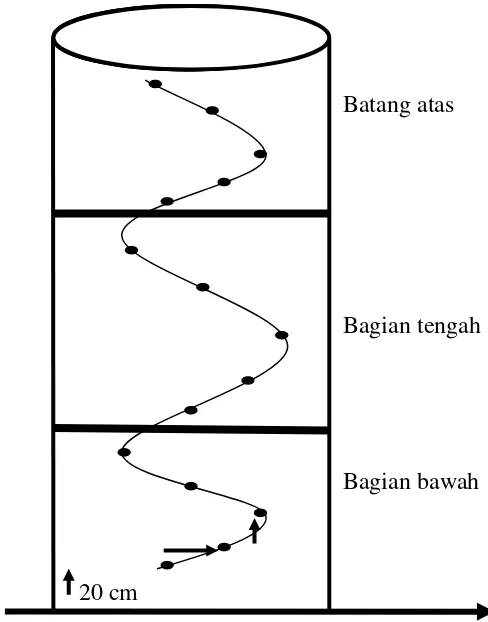
2. Pohon kemudian diberi tanda di lapisan kulitnya dengan spidol untuk menentukan bidang pengeboran. Titik pengeboran terbawah, 20 cm dari permukaan tanah.
Buat lagi titik pengeboran di atasnya dengan menggeser ke arah horizontal sejauh 10 cm dan ke vertikal 10 cm. Dengan cara sama dibuat beberapa titik berikutnya hingga dihubungkan membentuk garis spiral (5 titik pohon bagian atas, 5 titik
3. Titik – titik yang sudah ditandai pada pohon, kemudian dilubangi dengan menggunakan bor listrik sedalam 3 cm, 5 cm, dan 7 cm pada setiap pohon yang
berbeda.
Batang atas
Bagian tengah
Bagian bawah 10 cm 10 cm
20 cm
Gambar 1. Sketsa injeksi pada batang pohon
4. Kemudian lubang dibersihkan dengan kapas yang dibasuh alkohol 70%untuk
mencegah infeksi mikrobalain. Tangan peneliti juga harus dibersihkan dengan air bersih dan alkohol supaya benar – benar steril.
5. Setelah tangan dan lubang sudah steril, dimasukkan inokulum (Fusarium sp.)
a. Kedalaman lubang 3 cm yang dimasukkan inokulum sebanyak 15 ulangan pada 5 pohon yang berbeda.
b. Kedalaman lubang 5 cm yang dimasukkan inokulum sebanyak 15 ulangan pada 5 pohon yang berbeda.
c. Kedalaman lubang 7 cm yang dimasukkan inokulum sebanyak 15 ulangan
pada 5 pohon yang berbeda.
6. Lubang – lubang yang sudah terisi penuh oleh inokulum kemudian ditutup
denganranting agar tidak terjadi kontaminasi.
7. Pengamatan dilakukan 2 minggu sekali selama 4 bulan untuk melihat keberhasilan injeksi.
8. Setelah 4 bulan pengamatan, dilakukan kegiatan reisolasi. Yaitu kegiatan mengisolasi kembali gubal gaharu yang telah terinfeksi fungi.
Parameter Pengamatan
a. Persentase Infeksi
Persentase infeksi berguna untuk menunjukkan berapa persen keberhasilan
injeksi yang dilakukan dalam tiap perlakuan. Diamati setelah lubang terinfeksi. Tanda – tanda tanaman yang terinfeksi dengan melihat lubang infeksi terlihat
kecoklatan sampai menghitam dan sekitar lubang infeksi akan terlihat batang menjadi kecoklatan. Berikut adalah rumus menghitung jumlah lubang yang terinfeksi.
∑ Lubang injeksi yang terinfeksi pada pohon
X = x 100%
X1 + X2 + …+ Xn X =
n Keterangan :
X = persentase lubang injeksi yang terinfeksi
X = rata – rata persentase lubang injeksi yang terinfeksi n = jumlah lubang yang terifeksi
b. Waktu Inkubasi
Parameter ini menunjukkan kapan tepatnya lubang – lubang injeksi mulai terinfeksi.Pengamatannya dilakukan tiap dua minggu sekali.Sehingga data yang
didapat lebih akurat. c. Perkembangan Infeksi
Perkembangan infeksi dihitung dengan cara mengukur perkembangan gejala
pada titik – titik yang terinfeksi dengan menggunakan penggaris. Penyebaran infeksi dapat dilihat dari tanda – tanda sekitar lubang injeksi, akan terlihat perubahan warna
mulai dari kecoklatan sampai kehitaman. d. Kualitas gubal
Kualitas gubal yang diukur adalah perubahan warna dan aroma dari gubal yg
terbentuk.Warna gubal yang terbentuk diamati dengan menggunakan tabel klasifikasi mutu produk gubal gaharu (SNI).Dipilih sepuluh responden untuk menguji aroma
gubal yang terbentuk. Pengujian dilakukan dengan cara menyayat bagian gubal yang terinfeksi sedalam 0.3 cm, setelah itu membakar dan mencium aromanya.Standar pengujiannya adalah dengan memberi contoh aroma kualitas gubal gaharu yang
e. Reisolasi Fusarium sp.
Uji ulang dilakukan untuk mengetahui patogen lain yang mungkin
menginfeksi gubal telah terinfeksi oleh Fusarium sp. Kandungan tersebut dicari dengan menyayat bagian gubal yang terinfeksi, lalu mengisolasinya. Setelah diisolasi, maka dilakukan pengamatan di mikroskop.
Analisis Data
Rancangan yang digunakan dalam penelitian ini adalah Rancangan Acak
Lengkap dengan faktorial dengan model matematis sebagai berikut:
Yijk = µ +αi +βj + (αβ )ij +εijk
Keterangan :
Yijk :nilai pengamatan pengaruh bagian batang ke-i, pengaruh kedalaman lubang
ke-j, serta ulangan ke-k pada batang atas atau batang bawah i : bagian batang bawah, tengah, dan atas
j : 3 cm, 5 cm, dan 7 cm k : ulangan 1, 2, dan 3 µ : rataan umum
αi : pengaruh bagian batang ke-i
βj : pengaruh kedalaman lubang ke-j
αβij : interaksi bagian batang ke-i dengan kedalaman lubang ke-j
εijk : pengaruh galat pada faktor α ke-i, faktor β ke-j, dan ulangan ke-k pada batang
HASIL DAN PEMBAHASAN
A. Persentase infeksi
Besarnya persentase infeksi sangat dipengaruhi oleh kedalaman lubang injeksi
dan bagian batang. Jumlah persentase infeksi terbesar terdapat pada kedalamanlubang 3 cm di bagian batang tengah sebesar 100 %.
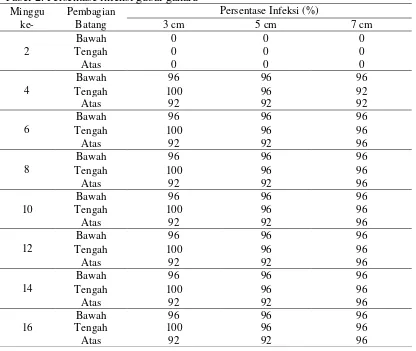
Tabel 2. Persentase infeksi gubal gaharu
Minggu
Hasil pengamatan kedalaman 3 cm selama 16 minggu menunjukkan persentase infeksi sebesar 96% pada batang bagian bawah, 100% pada batang bagian
dan 92% pada bagian atas. Sedangkan pada kedalaman 7 cm menunjukan persentase infeksi sebesar 96% pada batang bagian bawah, bagian tengah, dan bagian atas.
Fusarium sp. yang disuntikkan pada lubang injeksi dapat berkembangbiak
dengan baik sehingga mampu menginfeksi yang ditunjukkan oleh gejala perubahan warna.Mendgen dan Deising (1993) bahwapada proses interaksi antara cendawan
dengan inangnya, patogenesitas fungi merupakan hal yang terpenting. Keberhasilan cfungi dalam interaksi dengan inangnya bergantung pada strategi fungi dalam
melakukan penetrasi tanaman inangnya.
(a) (b)
Gambar 2. Infeksi gubal gaharu (a) tidak terjadi infeksi, (b) terjadi infeksi Sebenarnya reaksi yang diinginkan adalah adanya resin yang terbentuk akibat respon inangnya terhadap infeksi inokulum. Interaksi yang terjadi antara Fusarium
sp. dan inangnya dapat mengubah bentuk fisiologis dari pohon tersebut, misalnya perubahan sel. Perubahan sel tersebut yang akhirnya menghasilkan senyawa
yang pada gaharu didominasi oleh seskuiterpen dan kromon yang berwarna coklat atau hitam serta merupakan senyawa harum penentu kualitas gubal gaharu.
B. Waktu Inkubasi
Waktu inkubasi merupakan waktu antara proses dimulainya injeksi sampai munculnya gejala infeksi. Proses produksi gaharu pada umumnya terjadi akibat
pohon terluka dan terinfeksi penyakit. Namun proses infeksi tersebut tidak begitu saja terjadi, dibutuhkan waktu yang lama bagi fungi agar bisa masuk kedalam jaringan
gubal gaharu. Selain itu, fungi juga harus menyesuaikan diri terhadap inangnya agar mampu mempertahankan hidup dan berkembang biak. Sumarna (2002) menyatakan bahwa untuk mempertahankan hidup dan perkembangan secara fisiologis, mikroba
akan memanfaatkan cairan sel pembuluh batang sebagai sumber energi hidup secara perlahan-lahan.
Bagian batang injeksi dan kedalaman lubang injeksi tidak begitu mempengaruhi waktu inkubasi. Karena hampir keseluruhan dari perlakuan menunjukkan waktu inkubasi yang sama. Pengamatan yang dilakukan dilapangan
menunjukkan infeksi terjadi pada pengamatan kedua atau bulan pertama setelah penyuntikan. Situmorang (2009) menyatakan produksi gubal gaharu akan dapat
diamati mulai terbentuk setelah satu bulan perlakuan. Pemanenan gubal gaharu akan dilakukan mulai dari 3, 4, 5 tahun sampai waktu lebih lama setelah bioproses gaharu. Waktu infeksi yang terjadi dapat menjadi tolak ukur bahwa nutrisi yang diperoleh
oleh Fusarium sp. telah stabil.Sehingga Fusarium sp. dapat tumbuh pada gubal.Hal tersebut juga yang mendorong agar perkembangan infeksi semakin baik.Mendgen
berada pada kondisi stabil dan menetap di dalam sel atau jaringan inang dan memperoleh nutrisi dari inangnya.
C. Perkembangan infeksi
Pengukuran perkembangan infeksi dilakukan untuk mengetahui efektifitas dari interaksi perlakuan yang dilakukan.Pengukuran perkembangan dilakukan pada
panjang dan lebar infeksi dari inokulum.Data pengamatan yang digunakan adalah data pengukuran terakhir.
1. Panjang infeksi
Pengamatan menunjukkan terjadi perbedaan panjang pada setiap perlakuan.Namun hasil analisis sidik ragam menunjukkan bahwa tidak ada pengaruh
dari kombinasi perlakuan kedalaman lubang injeksi dengan bagian batang.Kombinasi yang terjadi kemungkinan saling menekan, sehingga tidak terjadi perkembangan
infeksi yang cukup baik.
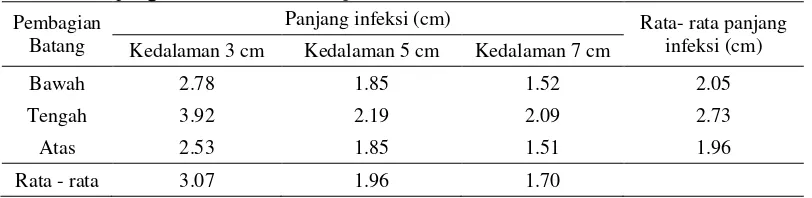
Tabel 3.Panjang infeksi Fusarium sp. Pembagian
Batang
Panjang infeksi (cm) Rata- rata panjang infeksi (cm) Kedalaman 3 cm Kedalaman 5 cm Kedalaman 7 cm
Bawah 2.78 1.85 1.52 2.05
Tengah 3.92 2.19 2.09 2.73
Atas 2.53 1.85 1.51 1.96
Rata - rata 3.07 1.96 1.70
Panjang infeksi Fusarium sp. pada batang bagian tengah lebih tinggi dibandingkan bagian lainnya. Panjang infeksi terbesar terdapat pada batang bagian
menyatakan bahwa gaharu dapat terbentuk pada cabang, akar, dan batang tetapi gubal gaharu terbentuk dengan baik pada batang bagian tengah sampai ke bagian bawah
Perbedaan panjang pada setiap perlakuan menunjukkan adanya pengaruh kontak Fusarium sp. dengan inangnya.Menurut Abadi (2003) bahwa tumbuhan dapat terinfeksi jika terinokulasi suatu parasit dimana inokulasi merupakan terjadinya
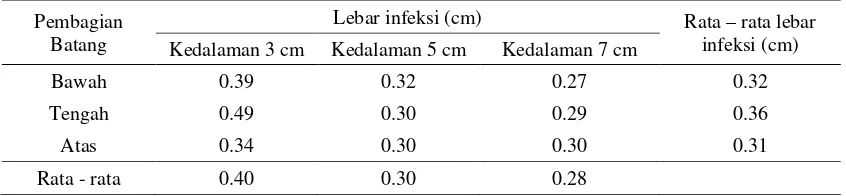
kontak antara patogen dengan inangnya. 2. Lebar infeksi
Hasil analisis sidik ragam menunjukkan tidak terjadi pengaruh nyata terhadap kombinasi perlakuan kedalaman lubang injeksi dengan bagian batang injeksi.Pengamatan menunjukkan terjadi perbedaan lebar infeksi pada setiap
perlakuan.Namun perbedaan lebar infeksi tidak begitu besar.Hal tersebut diakibatkan perkembangan injeksi pada batang adalah arah vertikal mengikuti jaringan pembuluh.
Lebar infeksi terbesar terdapat pada kedalaman lubang 3 cm di bagian batang tengah sebesar 0.49 cm. Sedangkan lebar infeksi terkecil terdapat pada kedalaman lubang 7 cm di bagian batang bawah sebesar 0.27 cm.
Tabel 4.Lebar infeksi Fusarium sp. Pembagian
Batang
Lebar infeksi (cm) Rata – rata lebar infeksi (cm) Kedalaman 3 cm Kedalaman 5 cm Kedalaman 7 cm
Bawah 0.39 0.32 0.27 0.32
Tengah 0.49 0.30 0.29 0.36
Atas 0.34 0.30 0.30 0.31
Rata - rata 0.40 0.30 0.28
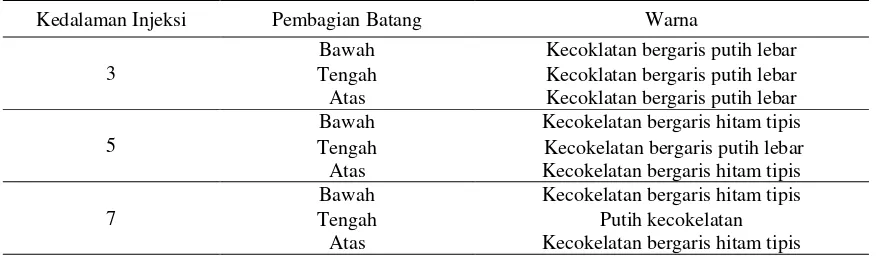
D. Kualitas gubal
Kualitas gubal merupakan parameter untuk mengetahui kelas mutu gubal yang
1. Warna gubal
Perubahan warna merupakan salah salah indikasi terjadi infeksi pada gubal
gaharu.Pada penelitian ini, menunjukkan bahwa Fusarium sp. mampu menginfeksi sehingga terbentuk gubal gaharu.Kedalaman injeksi dan bagian batang mempengaruhi warna gubal yang terbentuk.Rahayu dan Situmorang (2006) bahwa
perubahan warna dari putih menjadi coklat kehitaman merupakan gejala awal terbentuknya gubal gaharu.Putri et al. (2008) bahwa terbukti bahwa terjadi perubahan
warna pada pohon yang diinjeksi, seperti warna coklat dan kuning. Gejala umum yang ditimbulkan akibat infeksi cendawan diantaranya terjadi perubahan warna pada daerah yang diinfeksi dan klorosis daun.
(a) (b) (c)
Gambar 3. Warna gubal gaharu yang terinfeksi pada kedalaman 3 cm pada batang (a) bagian bawah, (b) bagian tengah, dan (c) bagian atas
Kualitas warna dari gubal gaharu yang terbentuk belum dapat diketahui secara pasti, karena pengujiannya tidak bisa dilakukan hanya secara responden.Namun, dugaan sementara bahwa kualitas gubal gaharu yang terbentuk menurut parameter
(a) (b) (c)
Gambar 4. Warna gubal gaharu yang terinfeksi pada kedalaman 5 cm pada batang (a) bagian bawah, (b) bagian tengah, dan (c) bagian atas
(a) (b) (c)
Gambar 5. Warna gubal gaharu yang terinfeksi pada kedalaman 7 cm pada batang (a) bagian bawah, (b) bagian tengah, dan (c) bagian atas
Perubahan warna gubal terjadi pada semua perlakuan dari putih menjadi
coklat dan kehitaman.Perubahan warna tersebut terjadi akibat infeksi patogen dan reaksi yang dilakukan pohon yaitu dengan mengubah senyawa - senyawa metabolit
terbentuknya gubal gaharu.Rahayu dan Situmorang (2006) menyatakan gubal gaharu terdeposit pada jaringan kayu.
Tabel 5. Kualitas warna gubal gaharu
Kedalaman Injeksi Pembagian Batang Warna
3
Bawah Kecoklatan bergaris putih lebar Tengah Kecoklatan bergaris putih lebar Atas Kecoklatan bergaris putih lebar
5
Bawah Kecokelatan bergaris hitam tipis Tengah Kecokelatan bergaris putih lebar
Atas Kecokelatan bergaris hitam tipis
7
Bawah Kecokelatan bergaris hitam tipis
Tengah Putih kecokelatan
Atas Kecokelatan bergaris hitam tipis
Inokulasi fungi menyebabkan terjadinya perubahan warna lebih gelap dibanding
pelukaan.Selain itu, inokulasi fungi juga menyebabkan panjang dan dalam zona
perubahan warna yang sangat berbeda nyata bila dibandingkan akibat pelukaan.Ng et al.
(1997) dan Barden et al. (2000) menyatakan bahwainfeksi cendawan diduga
menyebabkan peningkatan akumulasi senyawa terpenoid, sehingga warna menjadi lebih
gelap dan lebih panjang. Perubahan warna masih digunakan sebagai indikator kayu
gaharu akan menghasilkan senyawa gaharu. Semakin gelap warna yang dihasilkan,
semakin tinggi tingkat gubal gaharu yang dihasilkan.
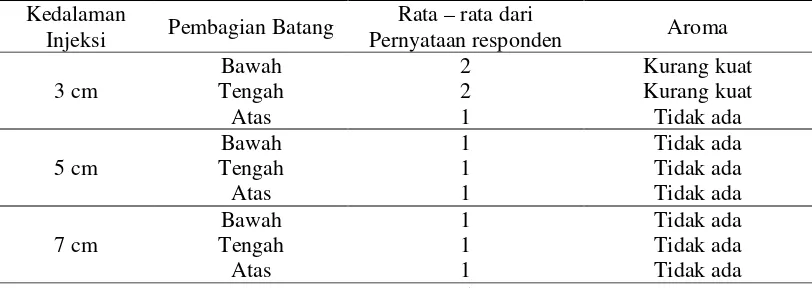
2. Aroma gubal yang terinfeksi
Hasil pengamatan menunjukkan bahwa kedalaman lubang mempengaruhi aroma dari gubal gaharu yang terbentuk.Pada Tabel 6 disajikan data aroma gubal
gaharu yang terbentuk.Gubal gaharu yang terinfeksi masih belum menunjukkan kualitas yang baik dari faktor aroma.Bahkan pada kedalaman injeksi 5 cm dan 7 cm tidak menunjukkan adanya aroma. Proses produksi gaharu sangat ditentukan
waktu sejak proses injeksi hingga panen. Semakin lama waktu panen, maka semakin banyak resin wangi sehingga meningkatkan kualitas gaharu.
Tabel 6. Aroma gubal gaharu
Kedalaman
Dari 10 responden yang menguji aroma gubal gaharu menyatakan bahwa
aroma yang terbentuk hamper sama. Aroma gubal gaharu hanya terdapat pada kedalaman lubang injeksi 3 cm pada batang bagian bawah dan tengah yaitu aroma yang kurang kuat.Tidak adanya aroma diduga akibat sedikitnya akumulasi gaharu
terhadap pohon gaharu (rendahnya senyawa terpenoid).Hal ini sesuai dengan pernyataan Rahayu dan Situmorang (2006) bahwa senyawa gaharu merupakan
metabolit sekunder yang dibentuk dari metabolit primer.
Terjadinya perubahan peningkatan dan penurunan gejala pembentukan gaharu diduga karena metabolit sekunder yang berperan dalam pembentukan senyawa gaharu
terus berubah-ubah di dalam pohon gaharu.Perubahan tersebut diduga berhubungan
dengan aktivitas infeksi cendawan. Senyawa gaharu yang dihasilkan akan meningkat
bersamaan dengan mulai terjadinya proses infeksi dan aroma wangi menurun dan hilang
bersamaan dengan berhentinya proses infeksi cendawan dan juga disebabkan karena
Okudera dan Ito (2009) bahwa senyawa seskuiterpenoid merupakan senyawa yang
mudah menguap dan diduga berpengaruh terhadap perubahan warna dan terbentuknya
aroma. Hal yang sama juga dilaporkan oleh Okudera dan Ito (2009) bahwa terjadi
penurunan jumlah senyawa seskuiterpenoid yang dihasilkan Aquilaria sp. setelah
beberapa minggu diberi perlakuan metil jasmonat, asam salisilat, atau ß-glucan, diduga
hal tersebut terjadi karena senyawa seskuiterpenoid yang dihasilkan menguap ke udara.
E. Reisolasi gubal gaharu
Reisolasi dilakukan membuktikan bahwa gejala yang muncul pada gubal
gaharu adalah akibat infeksi dari inokulum yang diinjeksi.Dari hasil reisolasi diperoleh Fusarium sp. Sehingga membuktikan bahwa yang menginfeksi gubal gaharu adalah Fusarium sp. Mendgen dan Deising (1993) bahwafungi membentuk
hifa infeksi setelah cendawan masuk ke dalam sel inang.Hifa infeksi merupakan perpanjangan hifa penetrasi.Pada beberapa cendawan setelah terbentuk hifa penetrasi
terbentuk vesikel dan selanjutnya membentuk hifa infeksi. Terakhir cendawan akan menghasilkan haustorium agar dapat memanfaatkan nutrisi sel inang. Inokulasi adalah kontak awal patogen pada suatu tanaman yang mungkin terinfeksi.Agrios
(1996) menyatakan bahwa inokulum adalah bagian dari patogen yang dapat memulai infeksi.Tidak semua inokulum mampu melakukan infeksi pada tanaman, hanya
(a) (b)
Gambar 6. Hifa Fusarium sp. (a) inokulum dan (b) hasil reisolasi
Inokulum yang diinjeksikan kedalam lubang injeksi mampu berkembang biak dengan baik. Dari gambar dapat dilihat bahwa hifa hasil reisolasi menunjukkan jumlah yang lebih banyak dibandingkan hifa inokulum.Hal tersebut sesuai dengan
pernyataan Lee dan Bostock (2006) dan Prins (2000) bahwa setelah proses infeksi, cendawan melakukan kolonisasi dengan berkembang atau memperbanyak diri, atau
KESIMPULAN DAN SARAN
Kesimpulan
1. Hasil pengamatan menunjukkan bahwa kisaran persentase infeksi dari
perlakuan faktor kedalaman injeksi dan bagian batang sebesar 92-100%. 2. Hasil pengamatan menunjukkan bahwa tidak terjadi pengaruh nyata dari
kombinasi perlakuan kedalamanan lubang injeksi dengan bagian batang
injeksi terhadap panjang dang lebar infeksi.
3. Infeksi inokulum terjadi pada minggu keempat setelah proses injeksi
inokulum.
4. Terjadi perubahan warna dari putih menjadi kecoklatan dan terdapat aroma yang kurang kuat pada gubal gaharu yang terbentuk.
5. Hasil reisolasi menunjukkan bahwa gubal gaharu terbentuk akibat infeksi inokulum.
Saran
Perlu diadakannya penelitian lebih lanjut agar hasil pengamatan yang lebih maksimal. Sehingga diperoleh data yang signifikan yang mampu menunjang proses
DAFTAR PUSTAKA
Abadi, L. A. 2003. Ilmu penyakit Tumbuhan. Banyumedia Publishing. Malang. Agrios, G. N. 1996. Ilmu Penyakit Tumbuhan. Penerjemah: Munzir Busnia. Gadjah
Mada University Press.Yogyakarta.
Barden, A., N. A. Anak, T. Mulliken, and M. Song. 2000. Heart of The Matter :
Agarwood Use and Trade and Cites Implementation for Aquilaria malaccensis. Cambridge, UK: TRAFFIC NETWORK REPORT.
Bhuiyan NI, Jaripa B, Nurul HB. 2009. Analysis of essential oil of eaglewood tree (Aquilaria agalocha Roxb) by gas chromatography mass spectrometry. J Bangl Pharma Soc 4: 24-28.
Budi, S. W., E. Santoso, dan A. Wahyudi. (2010). Identifikasi Jenis-Jenis Fungi yang Potensial Terhadap Pembentukan Gaharu dari Batang Aquilaria spp. Jurnal Silvikultur Tropika Vol. 1, No.1. pp 1 – 5.
Burkhill, I. H. 1935. “Dictionary of Economic Products of the Malay Peninsula” Vols 1-2 Crown Agents for the Colonies, London, Vol 1 A-H.
Bushnell WR. 1995. Pogress in Understanding Host-Parasite Interaction-the U.S.-Japan Seminar Series, 1966-1955. Di dalam Mills D et al, editor.Moleculer Aspect of Pathogenicity and Resistance: Requirement for Signal Tranduction. United States of America: APS Press. Hlm 1-10.
Christiansen E et al. 1999. Mechanical injury and fungal infection induce acquired resistance in norway spruce. J Tree Physiol 19: 399-403.
Groenewald S. 2005. Biology, pathogenicity and diversity of Fusarium oxysporum f.sp.cubense [Thesis]. Universitas of Pretoria: Pretoria.
Harborne, J. B. 1987. Metode Fitokimia: Penuntun Cara Modern Menganalisis Tumbuhan. Bandung: Penerbit ITB.
Hermann M, Zocher R, Haese A. 1996. Enniatin produced by Fusarium strains and its effect on potato tuber tissue. App Environ Microbiol 62: 393-398.
Kikot, G. E., A. H. Roque, and M. A. Teresa. 2009. Review contribution of cell wall degrading enzymes to pathogenesis of Fusarium graminearum: a review. J Basic Microbiol 49: 231-241.
Kim JC, Lee Y, Yu SH. 1995. Sambutoxin-producing isolates of Fusarium species and occurrence of sambutoxin in rotten patato tuber. Appl Environ Microbiol 61: 3750-3757.
Kunoh H. 1995. Cytological approaches in understanding host-parasite interaction. Di dalam Mills D et al, editor.Moleculer Aspect of Pathogenicity and Resistance: Requirement for Signal Tranduction. United States of America: APS Press. Hlm 15-26.
Langevin FO, F Eudes, Andre C. 2004. 2004 Effect of trichothecenes produced by Fusarium graminearum during Fusarium head blight development in six cereal species. Europ J Plant Pathol 110: 735–746.
Lee, M. H and R. M. Bostock. 2006. Induction, regulation, and role in pathogenesis of appressoria in Monilinia fructicola. Phytopathology 96:1072-1080.
Mendgen, K dan H. Deising. 1993. Infection structures of fungal plant pathogen-a cytological and physiological evaluation. New Phytol 124: 193-213.
Mohamed R, Jong PL, S. Zali. 2010. Fungal diversity in wounded stems of Aquilaria malaccensis. Fungal Divers 43:67–74.
Ng LT, Chang YS, Kadir AA. 1997. A review on agar (gaharu) producing Aquilaria species. Trop Forest Product 2:272-285.
Nieamann KO, Visintini. 2005. Assessment of potential for remote sensing detection of bark beetle-infested areas during green attack: a Literature Review. Canada: Mountain Pine Beetle Initiative.
Nobuchi, T dan Siripatadilok. 1991. Preliminary Observation of Aquilaria Crassnawood Associated With the Formation of Aloeswood. Bull Kyoto Univ Forest 63: 226-235.
Okudera Y, Ito M. 2009.Production of agarwood fragrant constituents in Aquilaria calli and cell suspension cultures.Plant Biotechnol 26: 307–315.
Prins, T. W. 2000. Infection strategy of Botrytis cinera and related necrotrophic pathogens. Di dalam: JW Kronstad, editor. Fungal Pathology. London: Kluwer Academic Publishers. Hlm 33-64.
Putri AL, Gayuh R, Juliarni. 2008. Induksi pembentukan senyawa terpenoid pada pohon gaharu (Aquilaria crassna) dengan Acremonium sp. dan metil jasmonat. Enviagro 2: 23-28.
Qi SY et al. 2005. Production of 2-(2-phenylethyl) chromones in Cell Suspension cultures of Aquilaria sinensis. Plant Cell Tissue Organ Cult 83: 217–221. Raffa, K. F., A. A. Berryman, J. Simasko, W. Teal, dan B. L. Wong. 1985. Effect of
grand fir monoterpenes on the firengraver, Scolytus ventralis, and its symbiotic fungus. Environ Entomol 14: 552-556.
Rahayu, G dan J. Situmorang. 2006. Menuju Produksi Senyawa Gaharu Secara Lestari. Laporan Penelitian Bersaing XI. Bogor: Lembaga Penelitian Masyarakat. IPB.
Rukmana, R dan S. Saputra. 1997. Penyakit Tanaman Dan Teknik Pengendalian. Penerbit Kanisius. Yogyakarta.
Santoso, E. 1996. Pembentukan Gaharu Dengan Cara Inokulasi. Bogor: Badan Litbang Kehutanan Pusat Litbang Hutan dan Konservasi Alam. Hlm 1-3
Santoso, E., Luciasih Agustini, R. Irnayuli, R. Sitepu, dan Maman Turjaman. 2007. Efektifivitas Pembentukan Gaharu dan Komposisi Senyawa Resin pada Aquilaria spp. Bogor.Jurnal Penelitian Hutan dan Konservasi Alam vol IV no 6: 543-551.
Seo JA, Kim JC, Lee YW. 1996. Isolation and characterization of two new type C fumonisins produced by Fusarium oxysporum. Nat Prod 59: 1003-1005.
Sidiyasa, K dan M. Suharti. 1987. Jenis-Jenis Tumbuhan Pengahasil Gaharu. Makalah Utama Diskusi Pemanfaatan Kayu Kurang dikenal. Cisarua, Bogor, 13-14 Januari 1987.
Siran, S.A. 2010. Perkembangan Pemanfaatan Gaharu. Dalam: Pengembangan Teknologi Produksi Gaharu Berbasis Pemberdayaan Masyarakat. Pusat Penelitian dan Pengembangan Hutan dan Konservasi Alam. Bogor. hlm.1-29. Situmorang, Jonner. 2009. Upaya Peningkatan Produksi Gaharu. Menuju Produksi
Soehartono, T. and A.C. Newton. 2000. Conservation and Sustainable Use of Tropical Trees in the Genus Aquilaria I. Status and Distribution in Indonesia. Biological Conservation 96:83-94.
Standar Nasional Indonesia. 1999. Gaharu. Jakarta. Diakses dari http://www.bpdas musi.net/_userdata/BkGaharu.pdf. [07 April 2013].
Sumarna, Y. 2002. Budidaya Gaharu. Seri Agribisnis. Jakarta: Penebar Swadaya. Sumarna, Y. 2005. Budidaya Gaharu. Penebar Swadaya. Edisi ke II. Jakarta.
Susilo, K. A. 2003. Sudah Gaharu Super Pula: Budidaya Gaharu dan Masalahnya. PT. Pustaka Sinar Harapan.Jakarta Timur.
Suwadiwangsa, S. dan Zulnely. 1999. Catatan Mengenai Gaharu di Kalimantan Timur dan Nusa Tenggara Barat. Info Hasil Hutan Badan Penelitian Kehutanan dan Perkebunan.Pusat Penelitian dan Pengembangan Hasil Hutan dan Sosial Ekonomi Kehutanan. Bogor. Hal: 80-90.
Tarigan, Kelin. 2004. Profil Pengusahaan (Budidaya) Gaharu. Pusat Bina Penyuluhan Kehutanan. Oepartemen Kehutanan.
Wang B, and Jeffers SN. 2000. Fusarium root and crown rot: A disease of container-grown hosts. Plant Dis. 84:980-988.
Wulandari, Y. F. 2000. Gaharu. http:/www.Manggala.or.id. [07 April 2013].
Yagura, T., N. Shibayama, M. Ito, F. Kiuchi, and G. Honda. 2003. Three Novel Diepoxy Tetrahydrochomones from Agarwood Artificially Produced by Intentional Wounding. Tetrahedron Letters, Vol, 46. pp 4395 – 4398.
Yusnita.2003. Cara Perbanyakan Tanaman secara Efisien. Cetakan I. Agromedia Pustaka. Jakarta.
Lampiran 3. Analisis sidik ragam perkembangan infeksi
Lampiran 4. Data pengujian aroma gubal gaharu
B = bagian batang bawah, T = bagian batang tengah, A = bagian batang atas