PENYERAPAN MERKURI DALAM LIMBAH SIMULASI
MENGGUNAKAN ZEOLIT KLINOPTILOLIT
AMSIRI
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
PENYERAPAN MERKURI DALAM LIMBAH SIMULASI MENGGUNAKAN ZEOLIT KLINOPTILOLIT
Skripsi
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Program Studi Kimia
Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
Oleh :
AMSIRI
102096026529
PROGRAM STUDI KIMIA FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH JAKARTA
PENYERAPAN MERKURI DALAM LIMBAH SIMULASI MENGGUNAKAN ZEOLIT KLINOPTILOLIT
Skripsi
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Program Studi Kimia
Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
Oleh
AMSIRI
NIM. 102096026529
Menyetujui,
Pembimbing I Pembimbing II
Dr. Thamzil Las Hendrawati, M.Si NIP. 19490516 197703 1 001 NIP. 19720815 200312 2 001
Mengetahui,
Ketua Program Studi Kimia
PENGESAHAN UJIAN
Skripsi yang berjudul “Penyerapan Merkuri dalam Limbah Simulasi Menggunakan Zeolit Klinoptilolit” yang ditulis oleh Amsiri NIM 102096026529 telah diuji dan dinyatakan LULUS dalam sidang Munaqosyah Fakultas Sains dan Teknologi Universitas Islam Negeri Syarif Hidayatullah Jakarta pada hari Senin tanggal 21 Juni 2010. Skripsi ini telah diterima sebagai salah satu syarat untuk memperoleh gelar Sarjana Strata Satu (S1) Program Studi Kimia.
Menyetujui,
Penguji I Penguji II
Dr. Mirzan T. Razzak, M.Eng, APU Nurhasni, M.Si NIP. 330 001 086 NIP. 19740618 200501 2 005
Pembimbing I Pembimbing II
Dr. Thamzil Las Hendrawati, M.Si NIP. 19490516 197703 1 001 NIP. 19720815 200312 2 001
Mengetahui,
Dekan Fakultas Sains dan Teknologi Ketua Program Studi Kimia
PERNYATAAN
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI ADALAH HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU LEMBAGA MANAPUN.
Jakarta, Juni 2010
ABSTRACT
Amsiri. MERCURY ABSORPTION IN WASTE SIMULATOR BY ZEOLITE
CLINOPTILOLITE. Under Tuition of Dr. Thamzil Las and Hendrawati, M.Si.
Mercury is pollutant that can decrease environment quality. Research on Zeolite
Clinoptilolite as ion exchange resin and filter has been carried out at Environmental
Analysis Department Center for Integrated Laboratory UIN Syarif Hidayatullah Jakarta.
The goal of the research was to investigate the ability of Zeolite Clinoptilolite on
mercury absorption. The zeolite used on this research were natural zeolite, Na-Zeolite
with 1 N NaCl, and Ca-Zeolite with 0.02 N CaCl
2. Effects of particle size, treatment, and
zeolite-mercury contact duration were observed based on 3 different particle sizes thet
were 500 µm - >355 µm, 355 µm - >212 µm and
≤
212 µm; 3 different treatments:
natural zeolite, Na-zeolite dan Ca-zeolite; and 6 different contact duration thet were ½, 1,
2, 4, 6 dan 8 hours. Percentage of Mercury absorption and kation excange capacity was
determined by Atomic Absorption Spectrophotometer (AAS). The AAS measuring
showed the best mercury absorption was reached by
≤
212 µm Na-Zeolite at 8 hours
contact. The kation exchange capacity of zeolite that was range by 0.32 meq/g to 0.81
meq/g was affected by treatment process and particle size.
ABSTRAK
Amsiri. PENYERAPAN MERKURI DALAM LIMBAH SIMULASI MENGGUNAKAN ZEOLIT KLINOPTILOLIT. Dibawah Bimbingan Dr. Thamzil Las dan Hendrawati, M.Si.
Merkuri adalah sumber polutan yang dapat menurunkan kualitas lingkungan. Penelitian terhadap zeolit Klinoptilolit yang digunakan sebagai bahan penukar ion dan penyaring merkuri dalam limbah simulasi telah dilakukan. Penelitian ini dilakukan di Pusat Laboratorium Terpadu Bidang Analisa Lingkungan UIN Syarif Hidayatullah Jakarta. Tujuan penelitian ini adalah untuk mengetahui kemampuan zeolit Klinoptilolit dalam menyerap merkuri. Zeolit Klinoptilolit ada yang dibiarkan natural dan ada yang terlebih dahulu diperlakukan menjadi Na-zeolit dengan menggunakan NaCl 1 N dan Ca-zeolit menggunakan CaCl2 0,02 M.
Pengaruh ukuran partikel zeolit, perlakuan zeolit dan waktu kontak zeolit terhadap penyerapan diamati dengan menggunakan 3 perbedaan ukuran partikel zeolit yaitu 500 µm - >355 µm, 355 µm - >212 µm dan ≤212 µm: 3 perbedaan perlakuan zeolit yaitu natural zeolit, Na-zeolit dan Ca-zeolit dan 6 perbedaan waktu kontak yaitu ½, 1, 2, 4, 6 dan 8 jam. Persen penyerapan merkuri dan nilai Kapasitas Tukar Kation (KTK) diukur dengan Spektrofotometer Serapan Atom (SSA). Pengukuran SSA menunjukkan bahwa persen penyerapan merkuri terbaik didapat pada ukuran partikel ≤212 dengan zeolit yang diperlakukan dengan NaCl dan waktu kontak 8 jam, yaitu sebesar 87,24 %. Nilai Kapasitas Tukar Kation (KTK) zeolit Klinoptilolit dipengaruhi oleh proses perlakuan dan ukuran partikel zeolit yaitu berkisar antara 0,32 meq/g sampai 0,81 meq/g.
Bacalah dengan Menyebut Nama Tuhanmu
“Tunjukilah kami jalan yang lurus”
“Di atas segalanya adalah nilai kemanusiaan” (Almarhum Gus Dur)
“kepada seluruh saudara saudara bangsa Indonesia adilkan pikiran untuk melihat cahaya
yang terbit dari hati sesama saudara kita sebangsa” (Emha Ainun Nadjib)
“Tetap semangat dan teguhkan hati disetiap hari sampai nanti, sampai mati” (Letto).
Dengan cinta kupersembahkan karya ini kepada:
1. Bapakku (Suja’i bin Master) dan Mamaku (Asmida binti Biralih) tercinta
2. Paman dan Bibiku: Om Ammar, Muhawwin, Agus Salim, Pa’i, Almarhumah
Jamilah
3. Saudara-saudara sepupuku:Mba Surayah, Mas Da’i, Mas Mulyono,
Jamaludin, Sofi, Adon, Hindun, Wardah, Rahman.
4. Keluarga Suwandi, Keluarga Mukminin, Keluarga Darsono, Keluarga Holes,
Keluarga Rejjeh Kuncoro, Keluarga Mustaqim
5. Adik-adikku: Kamelia, Ariel, Angga, Ubay, Nafila, Flora, Nayla, Aan,
Fania, Zainal, Hakam, Syafi’i, Lukman, Iim, Ari, Rohmah, Hamid, Hairul,
Yani, Moekep.
6. Murid-Muridku Rahma, Lia, Dhea, Sholeha, Yani, Elvira, Fauza, Deni,
Kristo, Eri, Rubi.
KATA PENGANTAR
Bismillaahirrohmaanirrohiim,
Assalaamu’alaikum WR.WB.
Segala puji dan syukur penulis haturkan ke hadirat Allah SWT Tuhan Yang Maha Esa yang telah menciptakan langit dan bumi lengkap dengan segala misterinya. Sholawat dan salam juga disampaikan kepada penggenggam kebenaran, pendobrak kebatilan, pengobat dikala luka dan penghibur dikala duka yaitu nabi besar Nabi Muhammad SAW yang telah memimpin umat manusia menjadi ciptaan Allah SWT yang paling mulia di bumi ini.
Perubahan dan pembaruan di segala bidang sangat penting untuk dilakukan. Untuk itu saat inilah waktu yang tepat untuk merubah wajah bumi menjadi lebih bersih.
Penulisan skripsi ini bertujuan untuk memenuhi persyaratan Akademik Program Studi Kimia Fakultas Sains dan Teknologi Universitas Islam Negeri Syarif Hidayatullah Jakarta, untuk memperoleh gelar Sarjana Sains pada bidang kimia.
Skripsi dengan judul Penyerapan Merkuri dalam Limbah Simulasi Menggunakan Zeolit Klinoptilolit disusun berdasarkan hasil penelitian di Pusat
1. Bapak Dr. Syopiansyah Jaya Putra, M.Sis. selaku Dekan Fakultas Sains dan Teknologi.
2. Ibu Sri Yadial Chalid, M.Si selaku Ketua Program Studi Kimia yang bersedia membantu dan memberi nasehat untuk penulis.
3. Bapak Dr. Thamzil Las selaku pembimbing I yang bersedia menerima dan membimbing penulis untuk meneliti di laboratorium Bidang Analisa Lingkungan.
4. Ibu Hendrawati, M.Si selaku pembimbing II yang bersedia meluangkan waktunya untuk membimbing dan memberi masukan kepada penulis. 5. Seluruh staf Laboratorium Bidang Analisa Lingkungan khususnya Bapak
Maryoto, Ibu Etyn, Nita Rosita, dan Fitriah Hatiningsih.
6. Seluruh dosen program studi kimia yang telah memberikan masukan serta dorongan untuk menyelesaikan skripsi ini.
7. Gus Adi yang telah banyak membantu dan ikut bersama merasakan lika-liku di dalam maupun di luar kelas kimia.
9. Adik-adik kelasku Banu, Ali M Akbar, Garry yang telah menemani penulis ke acara Kenduri Cinta, Janzuar Ramadhani yang telah mengajarkan keyboard, Aji, Ridho dan Subhan yang telah memberikan tumpangan kostannya, Dendi, Laits, Febri, Surya, Andri, Aulia Faturohman dan Heru yang telah memberikan bantuan kepada penulis Jujul, Ayi, Evi dan Susi yang telah tertawa apabila penulis bercerita.
10.Teman-teman Kimia 2003-2009 yang tidak dapat disebutkan satu-persatu terimakasih ku ucapkan.
11.Bapak Polisi Surahmadi selaku RW 09 Bantargebang yang perhatian kepada penulis. “Memang apa kendalanya dalam menyusun skripsi Amsiri?”
12.Teman-teman di Jl H. Ibong Ustadz Ahmad, Mba Russ, Setiawan, Aswadi, Irpan Tigor, Opick, Darman, Hasan, Dede dan Yuni.
Penulis menyadari bahwa skripsi ini belum sempurna, oleh karena itu penulis mengharapkan kritik dan saran yang bersifat membangun untuk sempurnanya skripsi ini. Semoga Allah SWT bersama orang-orang yang berusaha. Amiin.
Wassalaamu’alaikum.WR.WB..
Jakarta, Juni 2010
DAFTAR ISI
Halaman
KATA PENGANTAR... v
DAFTAR ISI... viii
DAFTAR TABEL... xi
DAFTAR GAMBAR... xii
DAFTAR LAMPIRAN... xiii
ABSTRAK... xiv
ABSTRACT... xv
BAB I PENDAHULUAN 1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 4
1.3. Tujuan Penelitian ... 4
1.4. Manfaat Penelitian ... 4
1.5. Hipotesis... 4
1.6. Kerangka Berpikir... 5
BAB II TINJAUAN PUSTAKA 2.1. Pencemaran Lingkungan………... 6
2.2. Zeolit ... 7
2.2.1. Struktur Zeolit ... 8
2.2.2. Sifat-Sifat Zeolit... 9
2.2.3. Jenis Zeolit ... 14
2.2.5. Klinoptilolit ... 18
2.3. Merkuri... 19
2.3.1. Sifat Fisik dan Kimia Merkuri ... 21
2.3.2. Sumber Keberadaan Merkuri di Alam ... 24
2.3.3. Pajanan dan Distribusi Merkuri ... 27
2.3.4. Pemanfaatan Merkuri ... 28
2.3.5. Efek Merkuri Terhadap Lingkungan ... 30
2.3.6. Efek Merkuri Terhadap Kesehatan Manusia ... 32
2.3.7. Perlindungan dan Pencegahan ... 37
2.4. Spektrometer Serapan Atom ... 38
2.4.1. Atomisasi dengan Nyala ... 39
2.4.2. Prinsip Spektrometer Serapan Atom... 40
2.4.3. Instrumentasi Spektrometer Serapan Atom ... 40
2.5. Metode Batch ... 43
BAB III METODE PENELITIAN 3.1. Tempat dan Waktu Penelitian... ... 45
3.2. Alat dan Bahan... 45
3.2.1. Alat... 45
3.2.2. Bahan ... 45
3.3. Prosedur Kerja... 46
3.3.1. Persiapan bahan... 46
3.3.2. Persiapan Natural Zeolit... 47
3.3.4. Pembuatan Ca-zeolit ... 47
3.3.5. Pembuatan Limbah Simulasi ... 48
3.3.6. Mengaplikasikan Zeolit pada Limbah Simulasi... 48
3.3.7. Pembuatan Deret Larutan Baku Merkuri ... 50
3.4. Pengukuran SSA ... 50
3.4.1. Pembuatan Kurva Kalibrasi ... 50
3.4.2. Pengukuran Sampel... 51
3.5. Penentuan Persen Efisiensi Penyerapan (% EP) ... 52
3.6. Penentuan KTK (Kapasitas Tukar Kation)... 52
BAB IV HASIL DAN PEMBAHASAN 4.1. Persen Penyerapan ... 54
4.1.1. Penyerapan Merkuri oleh Zeolit I ... 54
4.1.2. Penyerapan Merkuri oleh Zeolit II... 55
4.1.3. Penyerapan Merkuri oleh Zeolit III... 56
4.1.4. Penyerapan Zeolit... ... 57
4.1.5. Pengaruh Ukuran Zeolit... 59
4.2. Nilai Kapasitas Tukar Kation ... 59
BAB V KESIMPULAN DAN SARAN 5.1. Kesimpulan ... 63
5.2. Saran ... 63
DAFTAR PUSTAKA... 64
DAFTAR GAMBAR
Halaman
Gambar 1. Kerangka Berpikir... 5
Gambar 2. Kerangka Dasar Aluminasilika pada Zeolit... 9
Gambar 3. Strutur Stereotip Klinoptilolit... 19
Gambar 4. Hubungan antara Senyawa Merkuri yang bersifat Racun... 36
Gambar 5. Diagram Kerja SSA... 40
Gambar 6. Bagan Alir Kerja... 53
Gambar 7. Penyerapan Merkuri oleh Zeolit I (500 µm - >355 µm)... 54
Gambar 8. Penyerapan Merkuri oleh Zeolit II (355 µm - >212 µm)... 55
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Gambar Diagram Alir Persiapan Zeolit... 67
Lampiran 2. Gambar Diagram Alir Modifikasi Zeolit... 68
Lampiran 3. Gambar Diagram Alir Mengaplikasikan Zeolit pada Limbah Simulasi (Persen Penyerapan)... 69
Lampiran 4. Gambar Diagram Alir Mengaplikasikan Zeolit pada Limbah Simulasi (KTK)... 70
Lampiran 5. Contoh Perhitungan Persen Penyerapan... 71
Lampiran 6. Data % Penyerapan Merkuri oleh Zeolit I (500 µm - >355 µm)... 73
Lampiran 7. Data % Penyerapan Merkuri oleh Zeolit II (355 µm – >212 µm)... 74
Lampiran 8. Data % Penyerapan Merkuri oleh Zeolit III (≤212 µm)... 75
Lampiran 9. Data KTK (Kapasitas Tukar Kation) Zeolit Klinoptilolit Terhadap Merkuri... 76
Lampiran 10. Gambar Alat... 77
DAFTAR TABEL
Halaman
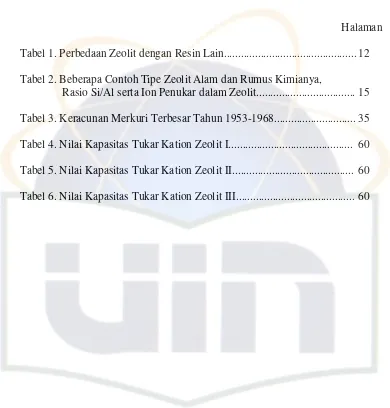
Tabel 1. Perbedaan Zeolit dengan Resin Lain... 12
Tabel 2. Beberapa Contoh Tipe Zeolit Alam dan Rumus Kimianya, Rasio Si/Al serta Ion Penukar dalam Zeolit... 15
Tabel 3. Keracunan Merkuri Terbesar Tahun 1953-1968... 35
Tabel 4. Nilai Kapasitas Tukar Kation Zeolit I... 60
Tabel 5. Nilai Kapasitas Tukar Kation Zeolit II... 60
BAB I PENDAHULUAN
1.1. Latar Belakang
Pembangunan selama tiga dasawarsa terakhir ini telah menyebabkan industri semakin meningkat yang secara nyata telah mengangkat perekonomian masyarakat untuk jangka pendek. Namun karena industri yang dikembangkan adalah industri yang kurang memperhatikan lingkungan, sehingga memperburuk penurunan kualitas lingkungan hidup yang mempengaruhi kehidupan manusia di muka bumi. Kondisi ini seiring dengan bertambahnya jumlah penduduk dunia yang tidak seimbang dengan ketersediaan sumber daya alam bagi pemenuhan kebutuhan akan pangan dan energi di berbagai negara termasuk di Indonesia (Witoelar, R. 2009).
Sebagai konsekuensinya aktivitas pembangunan terutama dalam rangka mengatasi krisis pangan dan energi kerapkali melupakan prinsip-prinsip pembangunan berkelanjutan, sehingga terjadi pengalihan fungsi pemanfaatan ruang yang merusak hutan dan lahan, eksploitasi sumber daya alam yang tidak memperhatikan kaidah-kaidah lingkungan serta pelepasan emisi gas rumah kaca yang secara nyata menurunkan kualitas lingkungan hidup.
pencemaran lingkungan. Begitu juga berbagai jenis industri yang menghasilkan limbah berbahaya.
Salah satu limbah yang sangat berbahaya adalah limbah merkuri. Merkuri sekarang ini banyak terdapat dimana-mana di dalam ikan, air, lumpur, kosmetik hingga lampu.
Limbah merkuri dihasilkan dari berbagai-macam kegiatan industri, seperti dari industri peralatan-peralatan elektris (electroplating), baterai, bahan kimia, penambangan emas dan sebagainya. Demikian luasnya pemakaian merkuri, mengakibatkan semakin mudah pula organisme mengalami keracunan merkuri (Palar, H. 1994).
Pengolahan air limbah mengandung merkuri dapat dilakukan dengan proses penyerapan (sorpsi) bahan pencemar dengan menggunakan resin-organik yang berfungsi sebagai penukar ion baik berupa anion atau kation (Michael dan Pierre, 1994 dan Jianlong et al, 2000), karbon aktif (Giequel et al., 1997), dan silika gel (Leéis et al., 1996), tetapi harganya relatif mahal. Hal tersebut telah mendorong beberapa peneliti untuk mencari penyerap alternatif yang lebih murah.
Di Indonesia zeolit pertama kali ditemukan pada tahun 1985 oleh Pusat Pengembangan Teknologi Mineral (PPTM) Bandung dalam jumlah yang besar, diantaranya tersebar di beberapa daerah di pulau Sumatera dan Jawa. Namun dari 46 lokasi penemuan zeolit, baru beberapa daerah yang ditambang secara intensif yaitu: Bayah, Cikalong, Tasikmalaya, Sukabumi dan Lampung. Jenis mineral zeolit yang sering ditemukan adalah Klinoptilotit dan Modernit (Las, T. 1998).
Zeolit adalah senyawa alumino silikat dengan struktur rangka (frameworks) dan mempunyai pori (rongga) dan saluran yang diisi oleh kation dan molekul air yang dapat mudah dipertukarkan (exchangeable) sehingga dapat mengadsorpsi ion (Sand, L. 1978).
Berdasarkan sifat tersebut penggunaan zeolit semakin luas, bukan saja sebagai penukar ion tetapi juga sebagai bahan penyerap, seperti yang telah digunakan dalam industri, misalnya pada pemurnian minyak bumi. Zeolit merupakan mineral alam yang ditemukan dalam keadaan campur dengan mineral-mineral lain, seperti kalsit, batuan lempung (clay) dan feldspar (Day, D.H. 1985).
1.2. Perumusan Masalah
Secara sederhana pengolahan limbah dapat dilakukan dengan mencampurkan bahan penukar ion dengan cairan limbah, sehingga terjadi pemekatan kontaminan dalam penukar ion. Dengan cara ini limbah dapat diserap oleh penukar ion. Penggunaan penukar ion lebih efisien dapat dicapai dengan merendam cairan limbah dalam botol berisi zeolit.
1.3. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui efisiensi penyerapan dan kapasitas tukar kation (KTK) limbah merkuri dengan zeolit menggunakan teknik batch.
1.4. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi tentang pemanfaatan zeolit sebagai salah satu bahan penyerap limbah industri yang mengandung merkuri.
1.5. Hipotesis
a. Ukuran partikel zeolit berpengaruh terhadap penyerapan.
b. Waktu kontak antara zeolit dan limbah berpengaruh terhadap penyerapan. c. Zeolit alam berpengaruh terhadap penyerapan
1.6. Kerangka Berpikir
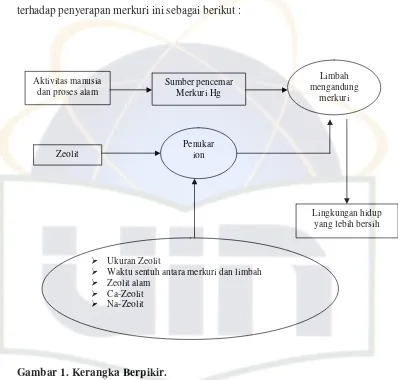
Dari uraian diatas peneliti menyusun kerangka berpikir dalam penelitian terhadap penyerapan merkuri ini sebagai berikut :
Gambar 1. Kerangka Berpikir. Aktivitas manusia
dan proses alam
Sumber pencemar Merkuri Hg
Limbah mengandung
merkuri
Lingkungan hidup yang lebih bersih Zeolit
Penukar ion
¾ Ukuran Zeolit
¾ Waktu sentuh antara merkuri dan limbah
¾ Zeolit alam
¾ Ca-Zeolit
BAB II
TINJAUAN PUSTAKA
2.1. Pencemaran Lingkungan
Pencemaran atau polusi adalah suatu kondisi yang telah berubah dari
bentuk asal pada keadaan yang lebih buruk. Pergeseran bentuk tatanan dari
kondisi asal pada kondisi yang buruk ini dapat terjadi sebagai akibat masukan dari
bahan-bahan pencemar atau polutan. Bahan polutan tersebut pada umumnya
mempunyai sifat racun (toksik) yang berbahaya bagi organisme hidup. Toksisitas
atau daya racun dari polutan itulah yang kemudian menjadi pemicu terjadinya
pencemaran.
Lingkungan dapat diartikan sebagai media atau suatu areal, tempat atau
wilayah yang didalamnya terdapat bermacam-macam bentuk aktivitas yang
berasal dari ornamen-ornamen penyusunnya. Suatu lingkungan hidup dikatakan
tercemar apabila telah terjadi perubahan-perubahan dalam tatanan lingkungan itu
sehingga tidak sama lagi dengan bentuk asalnya, sebagai akibat dari masuk atau
dimasukannya suatu zat atau benda asing ke dalam tatanan lingkungan itu. Jadi
pencemaran lingkungan adalah terjadinya perubahan dalam suatu tatanan
lingkungan asli menjadi suatu tatanan baru yang lebih buruk dari tatanan aslinya.
Suatu tatanan lingkungan hidup dapat tercemar atau menjadi rusak
disebabkan oleh banyak hal. Namun yang paling utama dari sekian banyak
2.2. Zeolit
Istilah zeolit berasal dari dua kata dalam bahasa Yunani, yaitu Zein yang
berarti membuih dan Lithos yang berarti batu. Nama ini sesuai dengan sifat zeolit
yang akan membuih bila dipanaskan pada suhu 100oC
Zeolit pertama kali ditemukan pada tahun 1756 oleh Axel Cronstedt
seorang ahli mineral dari Swedia. Jenis mineral yang ditemukan adalah stilbit.
Menurut penelitian yang dilakukan Cronstedt, mineral ini akan mendidih apabila
dipanaskan, hal ini disebabkan oleh proses dehidrasi dari mineral tersebut. Pada
tahun 1954 zeolit diklasifikasikan sebagai golongan mineral tersendiri yang saat
itu dikenal sebagai molecular sieve materials.
Pada tahun 1984 profesor Joseph V. Smith ahli kristalografi Amerika
Serikat mendefinisikan zeolit sebagai mineral yang terdiri dari kristal
aluminosilikat terhidrasi yang mengandung kation alkali atau alkali tanah dalam
kerangka tiga dimensi. Ion-ion logam tersebut dapat diganti oleh kation lain tanpa
merusak struktur zeolit dan dapat menyerap air secara reversibel
Pada saat ini dikenal sekitar 40 jenis zeolit alam yang dipengaruhi oleh
kondisi lingkungan seperti suhu, tekanan uap air dan komposisi tanah tempat
zeolit ditemukan, sehingga komposisi dari suatu zeolit tidak sama. Dari 40 jenis
zeolit alam yang mempunyai nilai komersial hanya 12 jenis, diantaranya
klinoptilotit, modernit, kabasit dan eriotit (Mumpton, 1978). Di Indonesia zeolit
ditemukan pada tahun 1985 oleh Pusat Pengembangan Teknologi Mineral
(PPTM) Bandung dalam jumlah besar. Penyebaran zeolit tersebut pada beberapa
ditambang secara intensif antara lain di Bayah, Banten, Cikalong, Tasikmalaya,
Nanggung dan Lampung (Suryartono, 1986).
2.2.1. Struktur Zeolit
Zeolit merupakan mineral yang terdiri dari kristal aluminosilikat terhidrasi
yang mengandung kation alkali atau alkali tanah dalam kerangka tiga dimensi.
Zeolit disusun oleh tatrahedral silika dan alumina yang saling berikatan melalui
atom oksigen, struktur ruang yang berisi kation-kation dan molekul air yang
berfungsi sebagai kerangka zeolit memiliki muatan negatif. Secara umum rumus
zeolit adalah :
Mx/n[(AlO2)x (SiO2)y] wH2O
M : Kation
n : Valensi kation M
w : Jumlah molekul air per unit sel
X dan Y : Jumlah tetrahedral persatuan sel
Kerangka dasar struktur zeolit terdiri dari unit-unit tetrahedral AlO4-dan
SiO4 yang saling berhubungan melalui atom O. Zeolit terdiri dari tiga komponen
yaitu: kation yang dipertukarkan, kerangka aluminosilikat dan fase air (Army,
2006). Ikatan ion Al-Si-O membentuk struktur kristal, sedangkan logam alkali
merupakan sumber kation yang mudah dipertukarkan. Zeolit mempunyai struktur
berongga dan biasanya struktur rongga ini diisi oleh air dan kation yang bisa
dipertukarkan dan memiliki pori dengan ukuran tertentu. Struktur tersebut
membuat zeolit banyak dimanfaatkan sebagai: penyaring molekuler (molekuler
berupa kristal yang berwarna putih, kehijaun dan sedikit agak kecoklatan.
Stabilitas zeolit terhadap panas dan radiasi sangat tinggi, hal ini disebabkan oleh
susunan kimianya terdiri dari kristal hidrat dan alumina silikat.
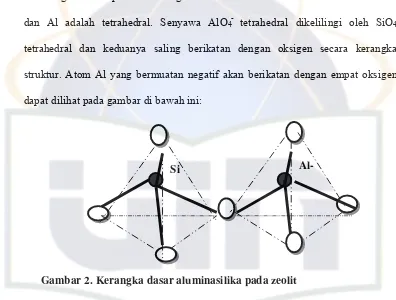
Atom Si dan Al adalah pusat dari tiga dimensi tetrahedral. Seluruh sudut
dikelilingi oleh empat atom oksigen. Secara rumus kimia ikatan antara atom Si
dan Al adalah tetrahedral. Senyawa AlO4- tetrahedral dikelilingi oleh SiO4
tetrahedral dan keduanya saling berikatan dengan oksigen secara kerangka
struktur. Atom Al yang bermuatan negatif akan berikatan dengan empat oksigen
dapat dilihat pada gambar di bawah ini:
Gambar 2. Kerangka dasar aluminasilika pada zeolit
2.2.2. Sifat-Sifat Zeolit a. Dehidrasi
Merupakan pelepasan molekul air dari rongga permukaan zeolit. Sifat
dehidrasi ini sangat penting, karena tanpa melakukan dehidrasi zeolit sulit
digunakan sebagai penyerap (hilangnya molekul air dapat mempermudah interaksi
antara molekul yang diserap dengan sisi aktif zeolit). (Winarko, 1997).
Sifat dehidrasi dari zeolit akan berpengaruh terhadap sifat adsorpsi. Zeolit
dapat melepaskan molekul air dari dalam rongga permukaan yang menyebabkan
medan listrik meluas ke dalam rongga utama dan akan efektif terinteraksi dengan
molekul yang akan di adsorpsi. Jumlah molekul air sesuai dengan pori-pori ruang
hampa yang akan terbentuk bila unit sel kristal zeolit tersebut dipanaskan.
b. Adsorpsi
Adsorpsi merupakan peristiwa terakumulasinya atom atau molekul suatu
zat pada permukaan zat lain, karena ketidakseimbangan antara gaya kohesi
partikel sefase dengan gaya adhesi partikel antar fase pada bidang batas suatu fase
dengan fase lainnya. Ketidakseimbangan ini berakibat senyawa tersebut
teradsorpsi pada permukaan adsorben. Fase pengadsorpsi disebut adsorben,
sedangkan fase teradsorpsi disebut adsorbat. Secara umum jenis adsorpsi dibagi
menjadi dua yaitu:
i. Fisisorpsi (adsorpsi secara fisika)
Adsorpsi ini terjadi karena adanya gaya Van Der Waals antara adsorben
dengan adsorbat membentuk ikatan yang lemah dan lapisan dipermukaan
adsorben.
ii. Kemisorpsi (adsorpsi secara kimia)
Adsorpsi ini merupakan interaksi antara molekul dengan valensi-valensi bebas
dan membentuk ikatan kimia antara molekul adsorbat dan permukaan
adsorben. Kemisorpsi mempunyai selektifitas yang tinggi, yaitu
molekul-molekul tertentu yang dapat diserap oleh partikel zat padat. Adsorpsi secara
Menurut Sharma, (1986) dalam banyak kasus adsorpsi tidak hanya terjadi
secara fisika atau kimia saja. Tetapi peristiwa ini umumnya merupakan gabungan
kedua jenis adsorpsi tersebut. Zat yang dapat digunakan sebagai adsorben harus
mempunyai struktur yang berpori atau berongga, atau struktural kimia senyawa
padatan tersebut memiliki sisi aktif yang dapat berinteraksi dengan adsorbat
(Yateman, 1994). Proses adsorpsi pada adsorben yang berongga terjadi karena
terjebaknya molekul adsorbat dalam rongga mengalami penyaringan sedangkan
pada sisi aktifnya terjadi interaksi dengan molekul adsorbat.
Zeolit dapat bertindak sebagai adsorben penukar kation, karena adanya
kation alkali dan alkali tanah yang dapat bergerak secara bebas dalam rongga
yang dapat dipertukarkan dengan kation lain dengan jumlah yang sama. Dalam
keadaan normal ruang hampa dalam kristal zeolit terisi oleh molekul air bebas
yang berada di sekitar kation. Bila kristal zeolit dipanaskan pada suhu 300-4000 C,
maka air tersebut akan keluar sehingga zeolit berfungsi sebagai penyerap gas atau
cairan. Selain mampu menyerap gas atau zat, zeolit juga mampu memisahkan
molekul berdasarkan ukuran kepolarannya.
c. Penukar Ion
Rongga-rongga zeolit diisi oleh logam alkali dan alkali tanah yang
merupakan sumber dari kation. Al sebagai pusat dari kerangka tiga dimensi akan
berkoordinasi dengan empat atom oksigen sehingga bermuatan negatif dan akan
dinetralkan oleh kation-kation dalam kerangka zeolit. Kation-kation ini mampu
dipengaruhi oleh; jenis kation, ukuran kation dan muatan kation mempengaruhi
proses pertukaran kation.
Mekanisme pertukaran ion dapat digunakan untuk penyisihan anion dan
kation. Sebagai media pertukaran ion pada dasarnya digunakan resin. Pertukaran
ion pada dasarnya terjadi dalam suatu larutan yang mengandung anion, kation dan
molekul air yang mana salah satu atau sebagian ion akan terikat pada resin
penukar ion. Molekul air dapat berada dalam mikropori bersama ion (Anion dan
kation) dengan muatan yang berlawanan dari resin sehingga terjadi keseimbangan
muatan untuk mencapai keadaan netral. Salah satu resin penukar ion yang
digunakan adalah zeolit. Hal ini disebabkan karena zeolit mempunyai komposisi
kimia dan struktur yang unik. Perbedaan zeolit dengan tanah lempung dapat
ditunjukkan oleh tabel berikut (Las, T. 1989).
Tabel 1. Perbedaan Zeolit dengan Resin lain
No Sifat Lempung Zeolit
1 Struktur Layer 2 dms Kristal
2 Swelling Besar Kecil
3 Sorpsi Tinggi Tinggi
4 Penyaring Rendah Tinggi
5 Kestabilan terhadap panas Rendah Tinggi
6 Kestabilan terhadap kimia Tinggi Rendah
7 Kestabilan terhadap radiasi Rendah Tinggi
Kation-kation yang dipertukarkan tidak terikat secara kuat pada kerangka
alumina silikat sehingga mudah untuk dipisahkan. Kemampuan pertukaran ion
zeolit merupakan parameter utama dalam menentukkan kualitas zeolit yang akan
digunakan. Kapasitas Tukar Kation (KTK) adalah jumlah ion logam yang dapat
diserap maksimum oleh 1 gram zeolit dalam kondisi kesetimbangan. KTK dari
zeolit bervariasi dari 1,5 sampai 2 meq/gram. Nilai KTK zeolit ini banyak
bergantung pada jumlah atom Al dalam struktur kerangka (Las, T. 1994). Makin
besar pergantian semakin besar kekurangan muatan positif, sehingga makin
banyak pula jumlah kation alkali atau alkali tanah yang dibutuhkan dari unsur
zeolit.
d. Penyaring atau Pemisah (Molekuler Sievies)
Selain mampu menyerap gas, zeolit juga mampu memisahkan molekul
berdasarkan ukuran kepolarannya. Molekul-molekul akan masuk ke dalam rongga
zeolit dan akan diserap berdasarkan kepolarannya. untuk molekul- molekul yang
polar, berukuran kecil dan tidak jenuh akan diadsorpsi oleh zeolit secara efektif
karena zeolit juga bersifat polar. Sifat zeolit sebagai penyaring atau pemisah
didasarkan pada volume dan ukuran garis tengah ruang hampa dalam kisi-kisi
kristal. Diameter pori-pori zeolit bervariasi sesuai dengan jenis zeolit, sedangkan
volume rongga kosong dapat mencapai 30% sampai 50% dari volume total zeolit
e. Katalis
Zeolit juga digunakan sebagai katalis yang dapat mempercepat reaksi,
karena pori yang terdapat dalam zeolit uniform. Zeolit yang digunakan sebagai
katalis dengan pori yang besar, luas permukaan maksimum dan volume kosong
yang tersedia dalam jumlah yang banyak. Semakin besar ukuran pori zeolit maka
proses katalisasi akan semakin cepat.
2.2.3. Jenis Zeolit
Zeolit terbentuk karena proses perubahan alam (zeolitisasi) dari batuan
vulkanik dan sengaja disintesis oleh manusia melalui proses kimia. Berdasarkan
proses pembentukkannya zeolit digolongkan menjadi dua kelompok yaitu: zeolit
alam dan zeolit buatan (sintesis). (Dyer, A. 1988)
a. Zeolit alam
Mineral zeolit ditemukan pertama kali oleh ahli mineralogi Swedia yang
bernama F.A.F. Cronstendt. Zeolit banyak dijumpai dalam lubang-lubang batuan
lava dan batuan sedimen piroklastik berbutir halus. Telah diketahui terdapat 40
jenis zeolit dalam tetapi hanya 20 jenis saja yang terdapat pada batuan sedimen,
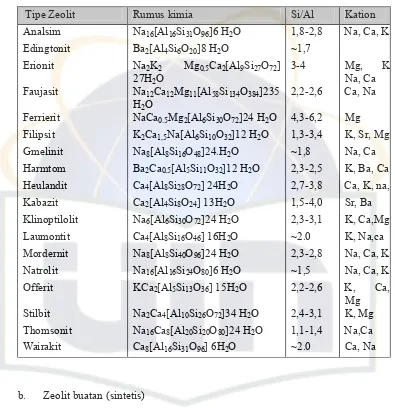
Tabel 2. Beberapa Contoh Tipe Zeolit Alam dan Rumus Kimianya Rasio Si/Al serta Ion Penukar dalam Zeolit
Tipe Zeolit Rumus kimia Si/Al Kation
b. Zeolit buatan (sintetis)
Zeolit memiliki sifat yang unik, yaitu susunan atom maupun komponennya
dapat dimodifikasikan, maka para peneliti berupaya untuk membuat zeolit sintetis
yang mempunyai sifat khusus sesuai keperluannya. Dari usaha ini dapat
direkayasa bermacam-macam zeolit. Sifat zeolit sangat tergantung dari jumlah
2.2.4. Pemanfaatan Zeolit
a. Pengolahan Limbah Industri dan Nuklir
Klinoptilolit dapat memisahkan 99 % ammoniak / ammonium dari limbah
industri. Klinoptilolit juga dapat memisahkan logam berat baik dalam limbah
industri atau pada tanah pertanian. (Tsitsisvii, 1980) (Blanchard, 1984).
Menurut Ames (1962) klinoptilolit dapat juga digunakan untuk pemisahan
zat radioaktif. Pada tahun 1979 klinoptilolit juga dipakai untuk dekontaminasi air
pendingin reaktor pada kecelakaan reaktor Three Mile Island di Amerika.
Zeolit juga digunakan untuk dekontaminasi air pendingin reaktor Three
Mile Island Unit II dan pada tahun 1987 untuk penyerapan gas radioaktif reaktor
Chernobiel yang terbakar. (Las, T. 2005).
b. Proses Industri
Berdasarkan sifat sorpsinya terhadap gas dan hidrasi molekul air, zeolit
digunakan untuk pengeringan pada berbagai produk industri.
Pada bidang proses industri zeolit digunakan antara lain:
• Pada proses pemurnian metil khlorida dalam industri karet.
• Pemurnian fraksi alkohol, metanol, benzen, xylene, LPG dan LNG pada
industri petro- kimia.
• Untuk hidrokarbon propellents-fillers aerosol untuk pengganti freons.
• Penyerap klorin, bromin dan fluorin.
Zeolit digunakan dalam proses penyerapan gas seperti :
• Gas mulia antara lain Ar, Kr dan gas He.
• Gas rumah kaca ( NH3, CO2, SO2, SO3 dan NOx ).
• Gas organik CS2, CH4, CH3CN, CH3OH, termasuk pirogas dan fraksi
etana/etilen.
• Pemurnian udara bersih mengandung O2.
• Penyerapan gas N2 dari udara sehingga meningkatkan kemurnian O2
diudara.
• Campuran filter pada rokok.
• Penyerapan gas dan penghilangan warna dari cairan gula pada pabrik gula.
Zeolit juga digunakan dalam industri petrokimia pada proses isomerisasi,
hidro sulforisasi, hidrocracking, hidrogenasi, reforming, dehidrasi, dehidrogenasi
dan de-alkilasi, cracking parafin, disportion toluen/benzen dan xylen. (Las. T,
2005).
Di Jepang klinoptilolit digunakan untuk filter kertas, karet dan polimer. Di
Amerika Serikat, zeolit alam juga digunakan untuk campuran semen dan
Tchernev telah mendemontrasikan penggunaan zeolit yang sama untuk “solar
heating/cooling” pada panel energi cahaya matahari berdasarkan adsorpsi/desorpsi
c. Bidang Pertanian dan Lingkungan
Zeolit digunakan sebagai “soil conditioning” yang dapat mengontrol dan
menaikan pH dan kelembaban tanah. Petani di Jepang menambahakan zeolit pada
pupuk tanaman bervariasi dari 15 % sampai 63 % terutama untuk tanaman apel
dan gandum. Penambahan zeolit pada pupuk kandang ternyata juga meningkatkan
proses nitrifikasi. Pada saat ini bidang pertanian merupakan pemakai zeolit
terbesar di Indonesia.
Dalam bidang peternakan, zeolit juga digunakan sebagai “food suplement”
pada ternak ruminansia dan non-ruminansia masing-masing dengan dosis 2.5 – 5
% dari rasio pakan perhari, hal ini dapat meningkatkan produktivitas susu, daging
dan telur, laju pertumbuhan serta memperbaiki kondisi lingkungan kandang dari
bau yang tidak sedap.
Zeolit juga pernah ditaburkan dari pesawat terbang di atas reaktor
Chernobiel untuk maksud menyerap hasil fisi yang terdapat dalam jatuhan debu
radioaktif (fall out) akibat kebakaran reaktor sovyet tahun 1985. (Las, T. 2005).
2.2.5. Klinoptilolit
Penelitian ini menggunakan sampel zeolit yang berasal dari Lampung.
Zeolit ini diperoleh dari lokasi penambangan PT. Winatama Mineral Perdana di
Desa Kalianda Lampung, melalui salah satu agennya di Cempaka Putih. Zeolit ini
berwarna putih dan diperoleh pada kedalaman lebih kurang 13 m di bawah
densitas antara 1,9942 g/ml - 2,1781 g/ml, volume pori total zeolit adalah 86,26 x
10 -3, dengan luas permukaan 38,93 m2 (Las, T. 1989).
Gambar 3. Strutur Stereotip Klinoptilolit
2.3. Merkuri
Merkuri atau raksa adalah unsur kimia pada tabel periodik dengan simbol
Hg dan nomor atom 80. unsur golongan logam transisi ini berwarna keperakan
dan merupakan satu dari lima unsur yang berbentuk cair dalam suhu kamar.
Merkuri banyak digunakan sebagai bahan amalgam gigi, termometer, barometer,
dan peralatan ilmiah lain.
Merkuri juga dikenal sebagai salah satu logam berat yang paling kuat
racunnya (Connell and Miller, 1984). Logam berat dikelompokan sebagai zat
pencemar karena tidak dapat terurai melalui biodegradasi. Selain itu logam berat
berikatan dengan senyawa-senyawa organik dan anorganik melalui pembentukan
senyawa kompleks dan absorpsi (Connell and Miller, 1984).
Menurut Bryan (1976), daya racun logam berat ditentukan oleh
faktor-faktor sebagai berikut, bentuk senyawa logam berat yang terdapat di dalam air,
adanya unsur logam berat lain dan faktor lingkungan yang mempengaruhi
fisiologis organisme, misalnya suhu, oksigen terlarut (DO), cahaya dan salinitas,
perubahan siklus hidup, umur, seks, makanan dan adaptasi terhadap logam berat
merkuri.
Berdasarkan sudut pandang toksikologi, logam berat dapat dibagi dalam
dua jenis. Jenis pertama adalah logam berat esensial, di mana keberadaannya
dalam jumlah tertentu sangat dibutuhkan oleh organisme hidup, namun dalam
jumlah yang berlebihan dapat menimbulkan efek racun. Contoh logam berat ini
adalah Zn, Cu, Fe, Co, Mn dan lain sebagainya. Sedangkan jenis kedua adalah
logam berat tidak esensial atau beracun, di mana keberadaannya dalam tubuh
masih belum diketahui manfaatnya atau bahkan dapat bersifat racun, seperti Hg,
Cd, Pb, Cr dan lain-lain. Logam berat ini dapat menimbulkan efek kesehatan bagi
manusia tergantung pada bagian mana logam berat tersebut terikat dalam tubuh.
Daya racun yang dimiliki akan bekerja sebagai penghalang kerja enzim, sehingga
proses metabolisme tubuh terputus. Lebih jauh lagi, logam berat ini akan
bertindak sebagai penyebab alergi, mutagen, teratogen atau karsinogen bagi
manusia. Jalur masuknya adalah melalui kulit, pernapasan dan pencernaan.
Merkuri dapat terkumpul di dalam tubuh suatu organisme dan tetap berada
tersebut, maka limbah yang mengandung merkuri tergolong sebagai limbah B3
(bahan berbahaya dan beracun) yang memerlukan penanganan khusus pada proses
pembuangannya. Merkuri logam cair yang berwarna putih-perak adalah suatu
neurotoksin yang kuat mampu menyebabkan kerusakan otak pada perkembangan
janin, gangguan tremor, dan keseimbangan emosi pada orang dewasa.
Makanan laut merupakan sumber terbesar pajanan terhadap merkuri saat
ini, merkuri terakumulasi dalam hewan di perairan dan mencapai kadar yang
berarti dalam rantai makanan paling tinggi baik di air tawar maupun air laut yang
sudah tercemar merkuri.
2.3.1. Sifat Fisik dan Kimia Merkuri
Merkuri adalah unsur kimia yang mempunyai nomor atom 80, berat atom
200,61 gram/mol, merupakan satu-satunya unsur logam yang berbentuk cair pada
suhu kamar (25oC) yang sangat mudah menguap. Uap merkuri lebih berbahaya
dari merkuri cair karena dapat terhirup dan dengan mudah terserap ke dalam
darah, merkuri membeku pada suhu -38,87oC dan mendidih pada suhu 356,9oC
warna merkuri tergantung pada bentuk fasanya, fasa cair berwarna putih perak
sedangkan fasa padat berwarna keabu-abuan. Densitas merkuri yaitu 13,534 g ml-1
merupakan densitas tertinggi dari semua benda cair (Hutagalung, 1985).
Berdasarkan daya hantar panas dan listriknya merkuri dimasukkan dalam
golongan logam. Sedangkan berdasarkan densitasnya, dimasukkan ke dalam
Disamping merkuri murni (uap dan cair), senyawa-senyawa merkuri dapat
juga berbahaya. Senyawa anorganik yang digunakan dalam cat sebagai anti jamur
dan di dalam batere tidak terlalu toksik secara sendiri, namun dengan mudah
diubah oleh bakteri menjadi bentuk organik yang jauh lebih berbahaya salah
satunya adalah metil merkuri.
Merkuri yang terdapat dalam limbah atau waste di perairan umum diubah
oleh aktifitas mikro-organisme menjadi komponen metil-merkuri (Me-Hg) yang
memiliki sifat racun (toksik) dan daya ikat yang kuat disamping kelarutannya yang
tinggi terutama dalam tubuh hewan air. Hal tersebut mengakibatkan merkuri
terakumulasi baik melalui proses bioakumulasi maupun biomagnifikasi yaitu
melalui rantai makanan (food chain) dalam jaringan tubuh hewan-hewan air,
sehingga kadar merkuri dapat mencapai level yang berbahaya baik bagi kehidupan
hewan air maupun kesehatan manusia yang makan hasil tangkap hewan-hewan air
tersebut. Terjadinya proses akumulasi merkuri di dalam tubuh hewan air, karena
kecepatan pengambilan merkuri (up take rate) oleh organisme air lebih cepat
dibandingkan dengan proses ekresi, yaitu karena metil-merkuri memiliki paruh
waktu sampai beberapa ratus hari di tubuh hewan air, sehingga zat ini menjadi
terakumulasi dan konsentrasinya beribu kali lipat lebih besar dibanding air
disekitarnya. (Arifin, 2008).
Metil merkuri dengan cepat terakumulasi di dalam ikan dan terkonsentrasi
dalam mata rantai akuatik yang panjang mencapai konsentrasi yang tinggi pada
predator dengan cara proses biomagnifikasi. Merkuri juga dengan mudah diserap
hamil menyebabkan gangguan perkembangan janin, serta melalui barier
otak-darah (blod-brain barrier) masuk ke dalam otak.
Merkuri memiliki sifat-sifat :
i. Kelarutan rendah
ii. Satu-satunya logam yang berbentuk cair pada suhu kamar (25oC), titik
bekunya paling rendah dari semua logam (–39oC).
iii. Masih berwujud cair pada suhu 396oC. Pada temperatur 396oC ini telah
terjadi pemuaian secara menyeluruh.
iv. Sifat kimia yang stabil terutama di lingkungan sedimen.
v. Merupakan logam yang paling mudah menguap jika dibandingkan dengan
logam-logam yang lain.
vi. Uap merkuri di atmosfir dapat bertahan selama 3 (tiga) bulan sampai 3 (tiga)
tahun sedangkan bentuk yang melarut dalam air hanya bertahan beberapa
minggu.
vii. Tahanan listrik merkuri sangat rendah, sehingga menempatkan merkuri
sebagai logam yang sangat baik untuk menghantarkan daya listrik.
viii. Dapat melarutkan bermacam-macam logam untuk membentuk alloy yang
disebut juga sebagai amalgam.
ix. Pada fase padat berwarna abu-abu dan pada fase cair berwarna putih perak
x. Mempunyai sifat yang mengikat protein, sehingga mudah terjadi
biokonsentrasi pada tubuh organisme air melalui rantai makanan
xi. Merupakan unsur yang sangat beracun bagi semua makhluk hidup, baik
Hampir semua merkuri di produksi dengan cara pembakaran merkuri
sulfida (HgS) di udara dengan reaksi sebagai berikut:
HgS + O2→ Hg + SO2
Merkuri dilepaskan sebagai uap yang kemudian mengalami kondensasi,
sedangkan gas-gas lainnya mungkin terlepas di atmosfir untuk dikumpulkan.
Merkuri di alam terdapat dalam berbagai bentuk sebagai berikut:
a. Merkuri anorganik, termasuk logam merkuri (Hg2+) dan garam-garamnya,
seperti merkuri khlorida (HgCl2) dan merkuri oksida (HgO).
b. Komponen merkuri organik atau organomerkuri, terdiri dari:
Aril merkuri, mengandung hidrokarbon aromatik seperti fenil merkuri asetat.
Alkil merkuri, mengandung hidrokarbon alifatik dan merupakan merkuri yang
paling beracun, misalnya metil merkuri, etil merkuri, dan sebagainya.
Alkosialkil merkuri (R-O-RHg).
2.3.2. Sumber Keberadaan Merkuri di Alam
Sumber utama dari merkuri yang ada di alam adalah proses pelepasan gas
(degassing) dari lapisan kulit bumi, yang menghasilkan 25.000 sampai 125.000
ton merkuri per tahun. Sedangkan merkuri yang dihasilkan dari proses
penambangan dan peleburan kurang lebih sebesar 10.000 ton/tahun (1973) dan
diperkirakan meningkat 2 % tiap tahun. (Kusnoputranto, 1996).
Merkuri terdapat sebagai komponen renik dari banyak mineral, dengan
bantuan kontinental rata-rata sekitar 80 ppb atau lebih kecil lagi. Sinabar (HgS),
(Manahan, 1994). Unsur ini di alam terdapat dalam bentuk gabungan dengan
elemen lainnya, dan jarang ditemukan dalam bentuk elemen terpisah. Komponen
merkuri banyak tersebar di karang-karang, tanah, udara, air dan organisme hidup
melalui proses-proses fisik, kimia dan biologi yang kompleks (Fardiaz, 1992).
Secara alamiah, pencemaran oleh merkuri dan logam-logam lain ke
lingkungan umumnya berasal dari kegiatan-kegiatan gunung api,
rembesan-rembesan air tanah yang melewati daerah deposit merkuri dan lain-lainya. Namun
demikian, meski sangat banyak sumber keberadaan merkuri di alam, dan masuk
ke dalam suatu tatanan lingkungan tertentu secara alamiah, tidaklah menimbulkan
efek-efek merugikan bagi lingkungan karena masih dapat ditolerir oleh alam itu
sendiri.
Seperti unsur-unsur logam berat lainnya, merkuri juga terdapat diseluruh
alam, namun distribusinya tidak merata. Dalam air tanah (ground water) kadar
merkuri berkisar antara 0,01-0,07 ppb, dalam danau dan sungai 0,08-0,12 ppb
(Hutagalung, 1985). Kadar merkuri dalam udara umumnya sangat rendah.
Kadarnya dalam air di daerah yang tidak tercemar sekitar 0,1 µg/l, tetapi angka ini
dapat setinggi 80 µg/l ditempat yang dekat dengan endapan bijih merkuri. Dalam
makanan, kecuali ikan, kadarnya sangat rendah, biasanya dalam rentang 5-20
µg/kg. Sebagian besar ikan mengandung kadar yang lebih tinggi, pada ikan tuna
dan ikan cucut biasanya kadarnya berkisar antara 200 sampai 1000 µg/kg.
Telah lama diketahui bahwa merkuri dan turunannya sangat beracun,
sehingga kehadirannya di lingkungan perairan dapat mengakibatkan kerugian
organisme air. Selain itu, pencemaran perairan oleh merkuri mempunyai pengaruh
terhadap ekosistem setempat yang disebabkan oleh sifatnya yang stabil dalam
sedimen, kelarutannya yang rendah dalam air dan kemudahannya diserap dan
terkumpul dalam jaringan tubuh organisme air, baik melalui proses bioakumulasi
maupun biomagnifikasi yaitu melalui rantai makanan.
Metil merkuri yang terdapat dalam perairan umumnya bersifat sangat
toksik yang bersifat akut maupun kronis terhadap kehidupan air. Hal ini antara
lain disebabkan oleh sifat senyawa tersebut yang relatif stabil dan memiliki umur
paruh biologis yang relatif lama dalam tubuh organisme air (Halimah, 2003).
Karena sifatnya yang sangat beracun, maka U.S Food and Administration
(FDA) menentukan pembakuan atau Nilai Ambang Batas (NAB) kadar merkuri
yang ada dalam jaringan tubuh badan air yaitu sebesar 0,005 ppm. Dimana Nilai
Ambang Batas yaitu suatu keadaan dimana suatu larutan kimia, dalam hal ini
merkuri dianggap belum membahayakan bagi kesehatan manusia. Bila dalam air
atau makanan, kadar merkuri sudah melampaui NAB, maka air maupun makanan
yang diperoleh dari tempat tertentu harus dinyatakan berbahaya.
Proses metilasi terpengaruh dengan adanya dominasi unsur sulfur (S),
yaitu pada keadaan anaerob dan redokpotensial yang rendah. Faktor-faktor yang
sangat berpengaruh di dalam pembentukan metil merkuri antara lain : suhu, kadar
ion Cl-, kandungan organik, derajat keasaman (pH), dan kadar merkuri.
Beberapa kemungkinan bentuk merkuri yang masuk ke dalam lingkungan
1. Sebagai merkuri anorganik, melalui hujan, run-off ataupun aliran
sungai dan unsur ini mempunyai sifat stabil pada keadaan pH rendah.
2. Dalam bentuk merkuri organik, yaitu phenyl merkuri (C6H5-Hg), metil
merkuri (CH3-Hg) dan alkoxyalkyl merkuri atau methoxy-ethyl
merkuri (CH3-CH2-CH2-Hg+).
Dalam bentuk suspended solid sebagai Hg2+2 (ion merkuro), mempunyai
sifat reduksi yang baik.
2.3.3. Pajanan dan Distribusi Merkuri
Pajanan atau asupan merkuri tergantung dari bentuknya, dimana uap dan
metil merkuri merupakan bentuk yang sering dijumpai karena hampir seluruhnya
di absorpsi ke dalam tubuh. Metil merkuri di dalam ikan dan hasil-hasil perikanan
sejauh ini merupakan sumber utama pajanan merkuri (94%), diikuti oleh
menghirup uap merkuri dari udara (6%), air minum dapat dikatakan sangat kecil
kontribusinya.
Karena sifat fisik dan penggunaannya yang luas merkuri dapat masuk ke
dalam tubuh manusia melalui beberapa cara yakni; inhalasi, oral, dan melalui
kulit, merkuri dalam bentuk uap akan terhirup melalui saluran pernafasan dan
dengan cara difusi menembus dinding alveoli, masuk ke dalam peredaran darah
dan sampai ke otak. Absorpsi melalui saluran pencernaan dari merkuri anorganik
hanya berkisar antara 7-15% sedangkan pada merkuri organik absorpdinya bisa
Distribusi dari merkuri organik dan anorganik pada sel darah merah,
plasma, rambut dan organ-organ lain juga berbeda. Merkuri dalam bentuk uap dan
garam anorganik mempunyai afinitas yang besar pada ginjal, sedangkan merkuri
organik afinitasnya terutama pada otak (korteks posterior). Di dalam sel-sel
jaringan tubuh (ginjal, hati, dan lain-lain), merkuri berikatan dengan enzim-enzim
dan menyebabkan kerusakan dari sel-sel tersebut.
Ekskresi merkuri dari dalam tubuh adalah melalui rambut, kuku, urin dan
tinja, tergantung pada bentuk senyawa merkuri, dosis pamajanan, dan lamanya
waktu setelah pamajanan. Absorpsi merkuri organik di ginjal terjadi pada tubulus
proksimal, dan hal ini akan menghambat transpor sodium.
Semua bentuk senyawa merkuri bisa menembus barier plasenta, dan dari
percobaan pada hewan didapatkan hasil, bahwa konsentrasi merkuri di dalam
tubuh janin setelah terpajan oleh senyawa alkil merkuri dua kali lebih besar
dibanding konsentrasi di dalam tubuh induknya.
Di lingkungan merkuri dapat menyebabkan pencemaran pada badan-badan
air atau terakumulasi pada organisme hidup, seperti pada manusia,
tumbuh-tumbuhan dan hewan.
2.3.4. Pemanfaatan Merkuri
Menurut Goodman and Gillman’s, 1985 yang dikutip oleh Leo Saputra,
merkuri digunakan dalam berbagai bentuk dan untuk berbagai keperluan,
misalnya indutri khlor-alkali, alat-alat listrik, cat, instrumen, sebagai katalis,
amalgam dan sebagainya. Tanda keracunan merkuri dari obat-obatan jarang
terjadi, namun keracunan merkuri dari lingkungan semakin meningkat.
Penggunaan merkuri yang terbesar adalah industri khlor-alkali, dimana
diproduksi khlorin (Cl2) dan soda kaustik (NaOH) dengan cara elektrolisis larutan
garam NaCl. Fungsi merkuri dalam proses ini adalah sebagai katoda dari sel
elektrolisis. Penggunaan kedua yang terbesar adalah dalam produksi alat-alat
listrik, misalnya lampu uap merkuri dan batere. Penggunaan merkuri sebagai
fungisida merupakan penggunaan ketiga terbesar dari merkuri, dalam hal ini
merkuri digunakan untuk membunuh jamur di dalam cat, kertas, dan
industri-industri pertanian. Cat yang digunakan untuk kapal-kapal sering ditambahkan
merkuri oksida (HgO) sebagai anti jamur atau fenil merkuri sebagai anti lapuk.
Industri-indutri pertanian menggunakan komponen organomerkuri sebagai pelapis
benih untuk mencegah pertumbuhan kapang, penggunaan merkuri dalam kegiatan
di bidang pertanian ini amat potensial sebagai sumber pencemaran merkuri dalam
makanan.
Logam merkuri digunakan sebagai katalis dalam proses di industri-indutri
kimia, terutama pada industri vinil khlorida yang merupakan bahan dasar dari
berbagai plastik. Logam merkuri juga digunakan di dalam termometer dan
alat-alat pencatat suhu karena bentuknya yang cair pada kisaran suhu yang lebar,
sifatnya seragam, koefisien pengembangan panasnya besar, dan konduktivitas
Beberapa aktifitas manusia yang secara tidak langsung juga melepaskan
merkuri ke dalam lingkungan, antara lain pembakaran bahan bakar fosil, industri
baja, semen, dan fosfat, serta peleburan logam.
2.3.5. Efek Merkuri Terhadap Lingkungan
Penggunaan merkuri dalam industri sering menyebabkan pencemaran
lingkungan, baik melalui air buangan maupun melalui sistem ventilasi udara.
Merkuri yang terbuang ke sungai pantai atau badan air di sekitar industri tersebut
kemudian dapat mengkontaminasi ikan-ikan dan makhluk air lainnya, termasuk
ganggang dan tanaman air, ikan-ikan kecil dan makhluk air lainnya tersebut
kemudian dimakan oleh ikan-ikan atau hewan lainnya yang lebih besar. Ikan-ikan
dan hewan tersebut kemudian dikonsumsi oleh manusia, dan menyebabkan
merkuri terakumulasi di dalam tubuh.
Ada dua proses yang terjadi di lingkungan yang menghasilkan pejanan
terhadap manusia. Merkuri anorganik yang terkandung dalam limbah cair industri
diubah oleh bakteria di dalam air tawar, air laut dan sedimen menjadi metil
merkuri, metil merkuri dimakan ikan dan dengan cepat dapat masuk kedalam
tubuh serta disimpan di otot ikan. Melalui biomagnifikasi, ikan kecil dalam rantai
makanan akuatik dimakan oleh ikan yang lebih besar, menyebabkan konsentrasi
metil merkuri meningkat dalam jaringan ikan, bila manusia makan ikan yang
terakumulasi metil merkuri, maka akan didapatkan metil merkuri dengan
konsentrasi yang jauh lebih besar dibandingkan dengan konsentrasi metil merkuri
merkuri terhadap sebagian besar manusia. Proses kedua berkaitan dengan hujan
asam dan peningkatan keasaman dari air permukaan yang diakibatkannya. Makin
asam kondisi suatu perairan akan meningkatkan pembentukan merkuri menjadi
metil merkuri yang mudah di absorpsi oleh ikan (di-metil menjadi mono metil
merkuri), yang akan meningkatkan konsentrasi merkuri di dalam tubuh ikan yang
menyebabkan manusia terpajan.
Merkuri yang berada di lingkungan biasanya berupa merkuri anorganik,
yang kemudian mengalami perubahan menjadi metil merkuri (merkuri organik) di
dalam tubuh ikan atau organisme lain (proses metilasi) yang disebabkan oleh
mikroba (Rita, 2000).
Elimanasi dari metil merkuri di dalam tubuh ikan maupun organisme air
yang lain berjalan sangat lambat. Beberapa penelitian menunjukan, bahwa semua
ikan yang tidak terkontaminasi secara langsung dengan merkuri selama
pertumbuhan masih mangandung merkuri di dalam tubuhnya pada konsentrasi
yang rendah, yaitu 0,005-0,075 ppm.
Pada organisme air merkuri organik biasanya mempunyai efek toksik yang
lebih kuat dibanding merkurianorganik. Sedangkan toksisitas itu sendiri
dipengaruhi oleh suhu, pH, oksigen terlarut (dissolved oxygen), dan kesadahan air.
Beberapa hewan yang berada di darat, misalnya burung laut, juga bisa
terkontaminasi oleh merkuri. Residu yang terdeteksi di dalam telur burung
tersebut ternyata berhubungan dengan kematian embrio yangberada didalamnya.
Bentuk merkuri yang terakumulasi bervariasi, tergantung spesies, organ, dan letak
Penggunaan merkuri di bidang pertanian sebagai pelapis benih dapat
mencemari tanah-tanah pertanian, yang berakibat pencemaran terhadap hasil-hasil
pertanian terutama sayur-sayuran. Food and Drug Administration (FDA) Amerika
serikat menetapkan batasan kandungan merkuri maksimum adalah 0,005 ppm
untuk air dan 0,5 ppm untuk mmakanan; sedangkan Organisasi Kesehatan Dunia
(WHO) menetapkan batasan maksimum yang lebih rendah, yaitu 0,001 ppm untuk
air (Kusnoputranto, 1996).
2.3.6. Efek Merkuri Terhadap Kesehatan Manusia
Efek toksik dari merkuri tergantung pada bentuk kimianya, uap merkuri
yang terhirup, sangat berbahaya terhadap pekerja yang terpajan di lingkungan
kerja, yang menyebabkan kerusakan pada sistem saraf, kehilangan memori,
tremor, ketidak-stabilan emosi (gelisah dan mudah marah), insomnia, dan
kehilangan nafsu makan merupakan gejala-gejala khas pajanan ringan. Pajanan
sedang lebih diwarnai dengan kerusakan mental yang signifikan dan gangguan
gerak, disamping terdapat kerusakan ginjal. Pajanan singkat dengan konsentrasi
tinggi uap merkuri dapat menyebabkan kerusakan paru-paru dan kematian. Efek
ringan dari uap dapat menghilang setelah pajanan berhenti, dengan gangguan otot
lebih cepat pulih dibandingkan dengan gangguan mental, uap merkuri dapat
menembus plasenta mencapai janin, namun informasi yang dilaporkan mengenai
efek pranatal terhadap manita hamil yang terpajan sedikit sekali, kejadian yang
dilaporkan adalah terjadinya tingkat absorpsi spontan yang cukup tinggi dari
Kasus kercunan yang paling ringan menunjukan gejala yang tidak spesifik,
seperti mata lelah, mata kabur, dan kesemutan. Gejala biasanya tampak setelah
periode laten selama beberapa minggu sampai beberapa bulan selama pajanan
kronik konsentrasi rendah atau setelah pajanan akut konsentrasi tingggi. Kasus
yang lebih berat menunjukan gangguan penglihatan, kehilangan pendengaran,
gangguan pembicaraan, dan pergerakan yang lemah dan tidak stabil. Kasus yang
paling berat menunjukan gangguan mental dan koma, kadang-kadang dapat
disertai kematian.
Masa prenatal dan usia anak-anak merupakan tahapan paling sensitif
terhadap keracunan metil merkuri karena pada periode waktu tersebut otak
berkembang dengan pesat. Jika pajanan ringan dari merkuri terhadap wanita hamil
mungkin akan menyebabkan tingkat perkembangan yang sedikit lambat dan
gangguan neurologi yang ringan pada bayi. Pajanan yang lebih berat dapat
menghasilkan efek dramatik pada perkembangan, termasuk letak struktur otak
yang abnormal dan gangguan umum dari perkembangan mental dan motorik
(kebutaan, dan gangguan perkembangan bicara).
Dua kejadian utama dari keracunan metil merkuri terjadi di Jepang di
daerah Teluk Minamata dan Sungai Nigata, serta di daerah pedesaan Irak. Di
Jepang, terjjadi karena ikan terkontaminasi limbah cair industri yang kemudian
dimakan oleh manusia, sedangkan di Irak, gandum yang terkontaminasi kemudian
digunakan untuk membuat roti untuk dimakan.
Pemajanan sementara dari uap merkuri bisa menyebabkan beberapa
pneumonitis. Sedangkan pamajanan yang terus menerus akan mengakibatkan
gangguan terutama di sususnan saraf pusat (otak). Beberapa tanda dan gejala yang
timbul, antara lain adalah: tremor, sulit berkonsentrasi, gugup, depresi, psikosis,
paralisis, kesulitan bernafas karena kelumpuhan otot-otot pernafasan, denyut
jantung cepat (takhikardi), ginggivitis,dan sebagainya.
Pamajanan melalui oral akan memberikan gejala seperti perasaan mual,
muntah-muntah, kejang pada perut, tinja bercampur darah, dan hambatan terhadap
produksi urin. Kontak merkuri dengan kulit akan merangsang timbulnya reaksi
alergi, berupa vesodilatasi (eritema), hiperkeratosis, dan hipersekresi kelenjar
keringat.
Senyawa merkuri anorganik tidak terlalu toksik karena zat tersebut tidak
dapat diabsorpsi tubuh dengan baik dan tidak mudah menembus barier otak-darah
atau plasenta. Konsumsi dari beberapa gram senyawa merkuri dapat menyebabkan
kematian karena kegagalan ginjal, dan dosis lebih kecil untuk jangka panjang
dapat menyebabkan kerusakan ginjal dan saraf. Sejauh ini hasil studi laboratorium
atau pada manusia tidak mengkaitkan merkuri dengan kanker, studi laboratorium
menunjukan bahwa emtil merkuri merupakan suatu mutagen yang lemah.
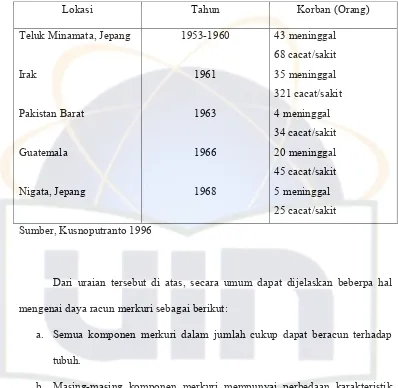
Keracunan merkuri telah sering terjadi dan merupakan keracunan yang
cukup serius karena dapat mengakibatkan kematian dan cacat seumur hidup.
Berikut menunjukan lima keracunan merkuri yang menelan korban cukup
Tabel 3. Keracunan Merkuri Terbesar Tahun 1953-1968
Lokasi Tahun Korban (Orang)
Teluk Minamata, Jepang
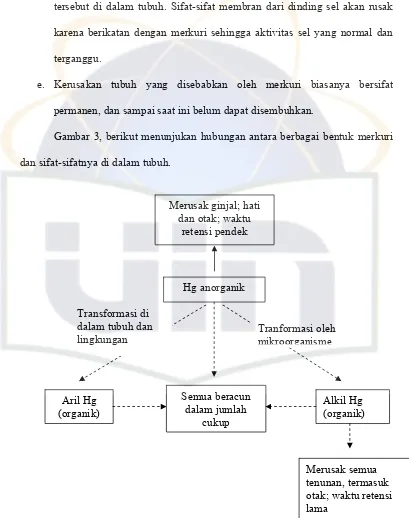
Dari uraian tersebut di atas, secara umum dapat dijelaskan beberpa hal
mengenai daya racun merkuri sebagai berikut:
a. Semua komponen merkuri dalam jumlah cukup dapat beracun terhadap
tubuh.
b. Masing-masing komponen merkuri mempunyai perbedaan karakteristik
dalam daya racunnya, distribusi, akumulasi atau pengumpulan, dan waktu
retensinya di dalam tubuh.
c. Transformasi biologi dapat terjadi di lingkungan atau dalam tubuh dimana
komponen merkuri diubah dari satu bentuk menjadi bentuk lainnya.
d. Pengaruh merkuri di dalam tubuh diduga dapat menghambat kerja enzim
dan menyebabkan kerusakan sel, disebabkan kemampuan merkuri untuk
terdapat di dalam enzimdan dinding sel. Keadaan ini mengakibatkan
penghabatan aktivitas enzim dan reaksi kimia yang dikatalis oleh enzim
tersebut di dalam tubuh. Sifat-sifat membran dari dinding sel akan rusak
karena berikatan dengan merkuri sehingga aktivitas sel yang normal dan
terganggu.
e. Kerusakan tubuh yang disebabkan oleh merkuri biasanya bersifat
permanen, dan sampai saat ini belum dapat disembuhkan.
Gambar 3, berikut menunjukan hubungan antara berbagai bentuk merkuri
dan sifat-sifatnya di dalam tubuh.
Merusak ginjal; hati
Masyarakat yang mempunyai resiko terpajanan merkuri diantaranya
adalah pekerja terutama wanita dalam usia reproduksi, yang terpajan terhadap uap
merkuri dalam pekerjaan.
2.3.7. Perlindungan dan Pencegahan
Sumber pencemaran merkuri di lingkungan mudah di detekasi dari
industri-industri yang menggunakan merkuri di dalam prosesnya. Masalah yang
dihadapi adalah bagaimana mencegah terjadinya pencemaran merkuri tersebut.
Kesulitan dalam mencegah terjadinya pencemaran merkuri mempunyai sifat-sifat
sebagai berikut:
a. merkuri bersifat volatil sehingga dapat mencemari udara.
b. Merkuri berbentuk cair sehingga mudah menyebar di permukaan air dan
sulit untuk dikumpulkan.
c. Merkuri mengalami translokasi di dalam tanaman dan hewan.
d. Merkuri atau komponen merkuri dapat diubah oleh mikroorganisme yang
terdapat di dalam laut, sungai atau danau menjadi komponen metil merkuri
yang sangat beracun, dimana dengan adanya rantai makanan
memungkinkan terkumpul di dalam tubuh hewan dan manusia.
Suatu laporan yang dibuat oleh U.S. Environmental Protection Agency (US-EPA)
yang dikutip oleh Kusnoputranto memuat beberapa rekomendasi untuk mencegah
terjadinya polusi merkuri di lingkungan. Beberapa rekomendasi tersebut adalah
a. pestisida alkil merkuri seharusnya tidak boleh digunakan lagi.
b. Penggunaan pestisida yang mengandung komponen merkuri lainnya di
batasi untuk daerah-daerah tertentu:
c. Semua industri yang menggunakan merkuri harus membuang limbah
industrinya dengan terlebih dahulu mengurangi jumlah merkuri sampai
batas normal.
Pelaksanaan rekomendasi tersebut tidak seluruhnya dapat memecahkan
masalah polusi merkuri di lingkungan. Pencemaran merkuri tetap terjadi pada
lumpur di dasar sungai atau danau, dan mengahsilkan CH3Hg+ yang dilepaskan ke
dalam badan air di sekelilingnya. Beberapa cara dekontaminasi merkuri telah
dicoba dilakukan di Swedia, dintaranya adalah sebagai berikut:
a. Sedimen pada dasar sungai atau danau ditutupi dengan bahan-bahan
mempunyai kemampuan absorpsi tinggi.
b. Sedimen pada dasar sungai atau danau ditutupi dengan bahan organik yang
tidak bereaksi.
c. Sedimen yang mengandung merkuri dihilangkan dengan cara dikeruk atau
dipompa.
2.4. Spektrofotometer Serapan Atom (SSA)
Spektrofotometer serapan atom ditemukan pertama kali oleh Alan Walsh
pada tahun 1953, dan penggunaan pertama kali pada tahun 1958. SSA merupakan
metode analisis untuk logam yang berdasarkan pada pengukuran penyerapan sinar
yang mengandung unsur logam diaspirasikan ke dalam nyala. Spektrofotometer
serapan atom merupakan suatu metode analisis kimia secara instrumental
berdasarkan pengukuran berkurangnya intensitas spektrum sinar karena diserap
oleh suatu medium yang terdiri atas atom-atom yang berbeda pada tingkat tenaga
dasar dari unsur yang dianalisis (PUSARPEDAL-BAPEDAL, 1998).
2.4.1. Atomisasi dengan Nyala
Atomisai dengan nyala api merupakan salah satu cara pengatoman dalam
SSA. Pengubahan unsur ke dalam larutan menjadi atom-atomnya. Dilakukan
dengan memasukkan larutan ke dalam nyala. Mula-mula larutan dikabutkan
(dalam sistem pengabut) kemudian diatomisasikan dalam nyala (dalam sistem
pembakar / burner).
SSA dengan menggunakan cara elektrotermal dalam pengatoman
mempunyai kepekaan yang jauh lebih tinggi daripada yang menggunakan panas
nyala. Pada SSA nyala, proses atomisasi dari molekul-molekul terjadi dalam
bagian burner. Pertama-tama larutan contoh diuapkan dalam bagian
nebulizer.Tetesan dari larutan contoh akan dibuang melalui bagian drain dan
hanya larutan berkabut halus yang akan memasuki bagian nyala bercampur
dengan gas pembawa dan pembakar. Dalam nyala terjadi penyerapan pelarut yang
meninggalkan partikel-partikel garam tersuspensi. Partikel-partikel ini akan
menyerap sebagian atau semuanya, uap yang dihasilkan terurai membentuk
2.4.2. Prinsip Spektrofotometer Serapan Atom
Spektrofotometer serapan atom adalah suatu metode analisis yang
berdasarkan pada penyerapan energi radiasi oleh atom-atom yang berbeda-beda
pada tingkat tenaga dasar. Penyerapan tersebut menyebabkan tereksitasimya atom
ke tingkat yang lebih tinggi. Dengan mengukur intensitas radiasi yang diteruskan
atau mengukur intensitas yang diserap maka konsentrasi unsur dalam larutan
contoh dapat ditetapkan (Cantle, 1982).
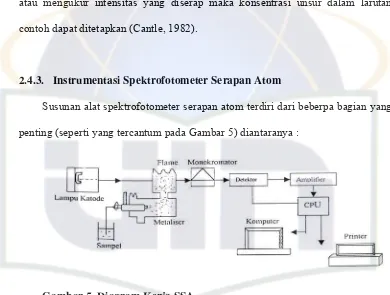
2.4.3. Instrumentasi Spektrofotometer Serapan Atom
Susunan alat spektrofotometer serapan atom terdiri dari beberpa bagian yang
penting (seperti yang tercantum pada Gambar 5) diantaranya :
Gambar 5. Diagram Kerja SSA.
a. Sistem Emisi (Emission System)
Pada proses eksitasi atom menerima energi pengeksitasi dalam bentuk energi
panas, misalnya dari nyala, sebagian dari energi tersebut digunakan untuk
pelepasan energi yang berbentuk gelombang elektromagnetik (hv), yang dikenal
sebagai sinar emisi. Besarnya energi yang diemisikan sesuai perbedaan kedua
tingkat energi. Emisi gelombang energi magnetik dipancarkan ke segala arah,
sehingga intensitas sinar yang sampai pada detektor hanya sebagian kecil saja.
b. Sistem Absorpsi (Absorption System)
Sistem absorpsi menentukan sensitivitas dan ketelitian dari spektrofotometer
serapan atom secara keseluruhan. Bagian yang penting dari sistem absorpsi ini
adalah nyala (burner) dan sistem pengabutan (nebulizer), sehingga sistem
atomizer dalam SSA biasa disebut Sistem Pengabut Pembakar (Burner Nebulizer
System).
¾ Nebulizer (Pengabut)
Sistem ini berfungsi mengubah larutan menjadi butir-butir dengan cara
menarik larutan melalui kapiler dengan pengisapan pancaran gas bahan
bakar dan gas-gas oksigen yang kemudian disemprotkan ke ruang
pengabut.
Partikel-partikel kabut halus kemudian bersama-sama aliran gas bakar
masuk ke dalam nyala sedangkan titik kabut yang besar dialirkan
¾ Burner (Pembakar)
Pada sistem ini terjadi atomisasi yaitu pengubahan kabut uap garam
suatu unsur yang akan dianalisis menjadi atom-atom normal atau bebas
di dalam nyala.
c. Sistem Seleksi (Selection System)
Setelah radiasi resonansi dari lampu katoda rongga melalui populasi atom
dalam media, energi radiasi ini sebagian lagi diteruskan. Fraksi radiasi yang
diteruskan dipisahkan dari radisi lainnya. Pemilihan atau pemisahan radiasi
tersebut dilakukan oleh monokromatik yang terdiri dari sistem optik, celah,
cermin, dan grating, sehingga hanya dilewatkan cahaya yang mempunyai satu
panjang gelombang dengan frekuensi tertentu melaui celah (slit).
d. Sistem Fotometrik (Photometric System)
Adalah alat yang digunakan untuk mengukaur intensitas cahaya yang
diteruskan oleh populasi atom dalam media. Intensitas radiasi yang diteruskan ini
akan diubah menjadi energi listrik oleh ”Photomultifier” selanjutnya diukur
dengan detektor dan dicatat oleh pencatat yang biasa berupa printer, pengamatan