Formulasi dan Uji Aktivitas Antioksidan Krim
Anti-Aging
Ekstrak Etanol 50% Kulit Buah Manggis (
Garcinia
magostana
L.) dengan Metode DPPH (
1,1
-
Diphenyl-2-Picril Hydrazil
)
SKRIPSI
DESI SYIFA NURMILLAH HARUN NIM : 1110102000010
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
ii
UIN SYARIF HIDAYATULLAH JAKARTA
Formulasi dan Uji Aktivitas Antioksidan Krim
Anti-Aging
Ekstrak Etanol 50% Kulit Buah Manggis (
Garcinia
magostana
L.) dengan Metode DPPH (
1,1
-
Diphenyl-2-Picril Hydrazil
)
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
DESI SYIFA NURMILLAH HARUN NIM : 1110102000010
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
Skripsi ini adalah hasil karya saya sendiri,
dan semua sumber baik yang dikutip maupun dirujuk telah saya
nyatakan dengan benar
.Nama : Desi Syifa Nurmillah H.
NIM : 1110102000010
Tanda Tangan :
iv Nama : Desi Syifa Nurmillah Harun
NIM : 1110102000010
Program Studi : Farmasi
Judul Skripsi : Formulasi dan Uji Aktivitas Antioksidan Krim Anti-Aging
Ekstrak Etanol 50% Kulit Buah Manggis (Garcinia magostana
L.) dengan Metode DPPH (1,1-Diphenil-2-Picril Hidrazil).
Pembimbing I
Sabrina, M. Farm., Apt NIP. 197902222007102001
Pembimbing II
Nelly Suryani, Ph. D., Apt NIP. 196510242005012001
Mengetahui,
Kepala Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta
Skripsi ini diajukan oleh
Nama : Desi Syifa Nurmillah Harun
NIM : 1110102000010
Program Studi : Farmasi
Judul Skripsi : Formulasi dan Uji Aktivitas Antioksidan Krim Anti-Aging
Ekstrak Etanol 50% Kulit Buah Manggis (Garcinia magostana
L.) dengan Metode DPPH (1,1-Diphenil-2-Picril Hidrazil).
Telah berhasil dipertahankan di hadapan Dewan Penguji dan diterima sebagai bagian persyaratan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
DEWAN PENGUJI
Pembimbing 1: Sabrina, M. Farm, Apt ( )
Pembimbing 2: Nelly Suryani, Ph. D, Apt ( ) Penguji 1 : Ofa Suzanti Betha, M. Si, Apt ( )
Penguji 2 : Eka Putri, M. Si, Apt ( )
Ditetapkan di : Jakarta
vi UiN Syarif Hidayatullah Jakarta Nama : Desi Syifa Nurmillah Harun.
Program Studi : Farmasi
Judul : Formulai dan Uji Aktivitas Antioksidan Krim Anti-Aging
Ekstrak Etanol 50% Kulit Buah Manggis (Garcinia mangostana L.) dengan Metode DPPH (1,1 Dipenil-2 PicrilHidrazil).
Kulit buah manggis (garcinia mangostana L) memiliki aktivitas antioksidan karena mengandung senyawa α mangostin, mangostin, dan mangostin. Senyawa tersebut mencegah radikal bebas yang dapat menyebabkan penuaan dini. Penentuan aktivitas antioksidan dilakukan dengan metode peredaman radikal bebas DPPH dengan menghitung nilai IC50 dimana nilai IC50 ekstrak etanol 50%
kulit buah manggis yang didapatkan adalah 9,725 g/mL. Pada penelitian ini,
ekstrak etanol 50% kulit buah manggis diformulasikan menjadi sediaan krim anti-aging dengan menggunakan variasi nilai HLB emulgator span 60 dan tween 80 (4,95; 5,7; 6,8). Krim disimpan pada tiga suhu yakni suhu ruang, suhu 30oC dan suhu 35oC selama 10 hari. Selanjutnya dilakukan uji stabilitas fisik krim meliputi organoleptis, pH, viskositas dan sentrifugasi yang dilakukan pada hari ke-0 dan hari ke-10. Berdasarkan hasil uji stabilitas fisik terhadap ketiga krim anti-aging
Name : Desi Syifa Nurmillah Harun. Program Study : Pharmacy
Title : Formulation and determination the antioxidant activity of anti-aging cream of the 50% ethanolic extract of mangosteen rind (Garcinia mangostana L.) by using DPPH method
Mangosteen rind (Garcinia mangostana L.) has the antioxidant activity, because it is rich of α mangostin, mangostin, and mangostin. These compounds have the ability to prevent free radical which can cause premature aging. The previous study has determined the antioxidant activity of mangosteen rind (Garcinia mangostana L.) extract and the result showed IC50 of mangosteen rind (Garcinia
mangostana L.) extract is 9.725 g/mL. In this study, 50% ethanolic extract of
mangosteen rind (garcinia mangostana L.) formulated into anti-aging cream by varying the value of HLB emulgators span 60 and tween 80 (4,95; 5,7; 6,8). Cream is stored at three different temperatures ie room temperature, 30oC and 35oC temperature for 10 days. Furthermore, physical stability test of creams was determined based on organoleptic test, pH, viscosity and centrifugation were performed on day 0 and 10th day. Based on test results of physical stability of three anti-aging cream 50% ethanolic extract of mangosteen rind (Garcinia mangostana L.), creams formula II with the HLB value of 5,7 indicated as the best formula. Antioxidant activity test carried out on the best cream formula that has been stored 10 days at room temperature, 30oC and 35oC temperature. The IC50 value of cream formula II at room temperature is (18,2338 g/mL), which had
better antioxidant activity than at temperature 30oC and 35oC with IC50 value
respectively of (18,409 g/mL) and (19,44 g/mL).
viii UiN Syarif Hidayatullah Jakarta
Alhamdulillahirobbil’alamin, segala puji bagi Allah SWT yang telah
melimpahkan rahmat, taufik dan hidayah-Nya sehingga penulis dapat
menyelesaikan penelitian dan menyusun skripsi dengan judul “ Formulasi dan
Uji Aktivitas Antioksidan Krim Anti-Aging Ekstral Etanol 50% Kulit Buah Manggis (Garinia mangotana L.) dengan metode DPPH (1,1-Dipinil-2-Picril Hirazil).” Shalawat serta salam penulis curahkan kepada junjungan kita Nabi Muhammad SAW beserta keluarga, para sahabat serta kita sebagai umatnya.
Penulis menyadari bahwa dalam penelitian dan penyusunan skripsi ini tidak
akan terwujud tanpa adanya bantuan, pembimbing, dan dukungan dari berbagai
pihak. Oleh karena itu penulis mengucapkan terima kasih kepada :
1. Prof. Dr. (hc). Dr. M.K. Tadjudin, Sp.And selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
2. Drs. Umar Mansur, M.Sc selaku Ketua Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
3. Sabrina, M.Farm. Apt. dan Nelly Suryani, Ph. D., Apt. sebagai dosen
pembimbing yang dengan sabar telah memberikan banyak masukan,
bimbingan dan dukungan kepada penulis.
4. Ayahanda tercinta Harun Al-rasyid dan ibunda tercinta Marpuah yang
selalu memberikan kasih sayang, semangat, dukungan baik moril maupun
materi serta doa yang tak terhingga di setiap langkah penulis.
5. Adikku tersayang Ismi Yunita H. dan Ray. Ramadhani yang telah
meluangkan waktu untuk membantu penulis dalam menyelesaikan skripsi
ini.
6. nenekku tersayang yang telah memberikan dukungan kepada penulis.
7. Bapak dan Ibu Dosen yang telah memberikan ilmu dan pengetahuan
hingga penulis dapat menyelesaikan studi di Program Studi Farmasi
FIKIK UIN Syarif Hidayatullah Jakarta.
9. Temen-temen seperjuangan manggis, Liana Puspita Cahyaningrum, Mira
Karisma, Nirmala Kasih, dan Hanny Narulita, terima kasih buat dukungan,
semangat, dan motivasi sejak awal penelitian sampai akhir penelitian.
10.Teman – teman Farmasi 2010 Andalusia atas persaudaraan, kebersamaan telah banyak membantu penulis baik selama pengerjaan skripsi ini maupun
selama di bangku perkuliahan.
11. Teman-teman satu kosan, teman satu kamar Farida Kusuma Ningrum dan
Ibu kosan Ibu Selli yang banyak membantu penulisan baik selama
pengerjaan skripsi ini maupun di bangku perkuliahan.
12.Laboran Farmasi UIN Syarif Hidayatullah Jakarta yang telah membantu
mempersiapkan alat dan bahan selama penelitian.
13.Semua pihak yang telah membantu selama penelitian dan penyelesaian
skripsi baik secara langsung maupun tidak langsung yang namanya tidak
dapat penulis sebutkan satu persatu.
Semoga Allah SWT memberikan balasan yang berlipat ganda atas semua bantuan,
dan dukungan yang diberikan.
Akhir kata, penulis menyadari bahwa penyusunan skripsi ini masih belum
sempurna dan banyak kekurangan. Oleh karena itu saran serta kritik yang
membangun sangat diharapkan. Semoga skripsi ini dapat bermanfaat bagi penulis
dan pembaca. Amiin Ya Rabbal‟alamiin.
Jakarta, September 2014
x UiN Syarif Hidayatullah Jakarta Sebagai sivitas akademika Universitas Islam Negeri (UIN) Syarif Hidayatullah
Jakarta, saya yang bertanda tangan di bawah ini:
Nama : Desi Syifa Nurmillah Harun
NIM : 1110102000010
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan
Jenis Karya : Skripsi
demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah
saya, dengan judul :
FORMULASI DAN UJI AKTIVITAS ANTIOKSIDAN KRIM ANTI-AGING EKSTRAK ETANOL 50% KULIT BUAH MANGGIS (Garcinia magostana L.) DENGAN METODE DPPH (1,1-Diphenil-2-Picril Hidrazil)
untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu Digital
Library Perpustakaan Universitas islam Negeri (UIN) Syarif Hidayatullah Jakarta
untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Demikian pernyataan persetujuan publikasi karya ilmiah ini saya buat dengan
sebenarnya.
Dibuat di : Jakarta
Pada Tanggal : 26 September 2014
Yang menyatakan,
JUDUL SKRIPSI ... ii
HALAMAN PERNYATAAN ORISINILLITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... vi
HALAMAN PENGESAHAN ... v
ABSTRAK ... vi
ABSTRACT ... vii
KATA PENGANTAR ... vii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... x
xii UiN Syarif Hidayatullah Jakarta
2.5 Proses Penuaan pada Kulit ... 13
2.5.1 Mekanisme Photoaging ... 14
2.6 Radikal Bebas ... 15
2.7 Antioksidan ... 16
2.8 Uji Aktivitas Antioksidan... 17
2.8.1 Metode DPPH ... 17
2.8.2 Metode Reducing Power ... 18
2.8.3 Metode Aktivitas Radikal Bebas Nitrogen Monookisda ... 19
2.8.4 Metode Aktivitas Radikal Bebas Ion Ferro (Pembentukkan logam Kelat) ... 19
3.3.1 Uji Aktivitas Antioksidan Ekstrak Etanol 50% Kulit Buah Manggis (Garcinia mangostana L.) ... 28
3.3.2 Formulasi Krim Anti-aging Ekstrak Etanol 50% Kulit Buah Manggis (Garcinia mangsotana L.) ... 29
Buah Manggis (Garcinia mangostana L.) ... 31
BAB IV HASIL DAN PMBAHASAN ... 34
4.1 Hasil Uji Aktivitas Antioksidan Ekstrak Etanol 50% Kulit Buah Manggis (Gaecinia mangostana L.)... 34
4.2 Evaluasi Hasil Uji Stabilitas Krim pada Penyimpanan Suhu Ruang, Suhu 30oC, dan Suhu 35oC ... 35
4.3 Evaluasi Hasil Uji Stabilitas Cycling Test pada Suhu 4oC dan 40oC ... 39
4.4 Hasil Uji Aktivitas Antioksidan Krim Hari Ke-0... 41
4.5 Hasil Uji Aktivitas Krim Terbaik Setelah Hari Ke-10 ... 42
BAB V KESIMPULAN DAN SARAN ... 45
5.1 Kesimpulan... 45
5.2 Saran ... 45
DAFTAR PUSTAKA ... 46
xiv UiN Syarif Hidayatullah Jakarta Halaman
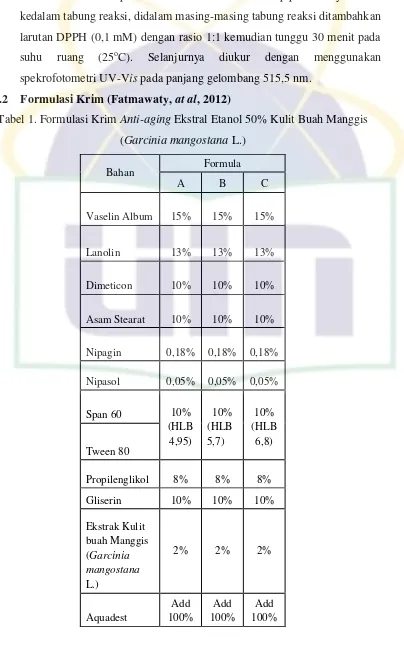
Tabel 1. Formula Krim Anti-aging Ekstrak Etanol 50% Kulit Buah Manggis
(Garcinia mangostana L.) ... 30
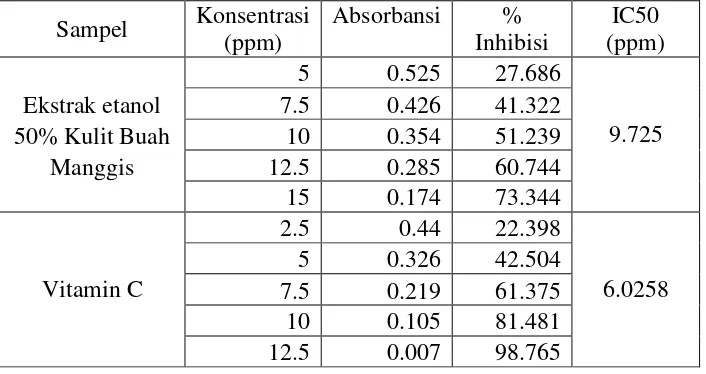
Tabel 2. Hasil Absorbansi, % Inhibisi Dan IC50 Ekstrak Dan Vitamin C ... 35
Tabel 3. Hasil Pemeriksaan Viskositas ... 36
Tabel 4. Hasil Pemeriksaan Sentrifugasi ... 37
Tabel 5. Hasil Pemeriksaan pH ... 37
Tabel 6. Hasil Pemeriksaan Penampilan dan Homogenitas Krim pada suhu ruang, suhu 30oC dan suhu 35oC... 38
Tabel 7. Hasil Pemeriksaan Penampilan dan Homogenitas Krim pada Uji Cycling Test ... 39
Tabel 8. Hasil Pemeriksaan Sentrifugasi Cycling Test ... 40
Tabel 9. Hasil Pemeriksaan pH Cycling Test ... 40
Tabel 10. Hasil Absorbansi, % Inhibisi Dan IC50 Formula Krim I, II dan III ... 41
Halaman
Gambar 1. Pohon dan Buah Manggis (Garcinia mangostana L.) ... 4
Gambar 2. Inti xanthone dengan jumlah IUPAC karbon dan struktur
kimia dari xanthones yang paling banyak dipelajari ... 6
Gambar 3. Struktur Kulit ... 9
Gambar 4. Mekanisme Photoaging ... 15
Gambar 5. Mekanisme penangkapan radikal DPPH oleh antioksian
xvi UiN Syarif Hidayatullah Jakarta Halaman
Lampiran 1. Data Karakterisasi Ekstrak Etanol 50% Kulit Buah Manggis ... 51
Lampiran 2. CoA Asam Askorbat. ... 52
Lampiran 3. CoA Asam Askorbat ... 53
Lampiran 4. CoA DPPH ... 54
Lampiran 5. Alat Penelitian ... 57
Lampiran 6. Alur Penelitian ... 58
Lampiran 7. Perhitungan HLB ... 60
Lampiran 8. Perhitungan Bahan Krim ... 61
Lampiran 9. Pembuatan Larutan Uji Aktivitas Antioksidan Ekstrak dan Kontrol Positif Vitamin C ... 63
Lampiran 10. Pembuatan Larutan Uji Aktivitas Antioksidan Formula Krim ... 65
Lampiran 11. Skema Uji Aktivitas Antioksidan Ekstrak Etanol 50% Kulit Buah Manggis Menggunakan Metode DPPH ... 66
Lampiran 12. Perhitungan % Inhibisi, IC50 dan AAI Ekstrak dan Vitamin C .... 68
Lampiran 13. Perhitungan % Inhibisi, IC50 dan AAI Formula Krim I, II dan III ... 71
Lampiran 14. Perhitungan % Inhibisi, IC50 dan AAI Formula Krim II pada Suhu 25oC, 30oC dan 35oC ... 74
Lampiran 15. Panjang Gelombang DPPH ... 75
HLB : Hydrophylic Lipophylic Balance
DPPH : 1,1-dipheny-2-lpricyl hydrazil
UV-Vis : Ultraviolet-Visible
rpm : Rotation Per Minute
AAI : Antioxidant Activity Index
Cp : CentiPoise
CO2 : Karbon Dioksida
ROS : Reaktive Oxygen Species
GML : Garcinia mangostana L
UV : Ultra Violet
DNA : Deoxyribose Nucleic Acid
IC50 : Inhibitor Concentration 50
nm : Nanometer
mM : Milimolar
1 UIN Syarif Hidayatullah Jakarta
merupakan suatu proses biologis kompleks yang dihasilkan dari penuaan intrinsik
(dari dalam tubuh seperti genetik) dan perubahan yang berkembang seiring waktu
serta dampak ekstrinsik disebabkan oleh faktor lingkungan. Faktor ekstrinsik yang
sangat berperan dalam penuaan adalah ekspresi wajah repetitive, posisi tidur yang
buruk, merokok dll. Tanda-tanda eksternal dari penuaan kulit yakni kerutan halus,
kulit tipis dan transparan, bintik-bintik pigmen, kulit kendur, kulit kering dengan
atau tanpa gatal, ketidak mampuan untuk berkeringat cukup, rambut beruban,
rambut rontok, rambut yang tidak diinginkan, penipisan lempeng kuku, hilangnya
kuku setengah bulan dll. (Mackiewicz and Rimkevicius, 2008)
Dari semua faktor tersebut, teori radikal bebas merupakan teori yang
sering dikaitkan sebagai penyebab faktor-faktor penuaan dini. Radikal UV
merupakan pemicu yang sangat potensial dalam pembentukan radikal bebas ROS
(Reaktive Oxygen Species) pada kulit (Masaki, 2010). Radikal bebas adalah suatu
atom atau molekul yang sangat reaktif dengan elektron yang tidak memiliki
pasangan (Winarsi, M.S, 2007). Pada kulit, radikal bebas yang diproduksi
berlebih akan merusak kolagen pada membran sel kulit, sehingga kulit menjadi
kehilangan elastisitasnya dan menyebabkan terjadinya keriput (Pamela, 2008)
Senyawa yang dapat menangkal radikal bebas adalah antioksidan. Sebagai
bahan aktif, antioksidan digunakan untuk melindungi kulit dari kerusakan akibat
oksidasi sehingga dapat mencegah penuaan dini (Masaki, 2010). Antioksidan
memiliki berat molekul kecil, tetapi mampu menginaktivasi berkembangnya
radikal. Antioksidan juga merupakan senyawa yang dapat menghambat reaksi
oksidasi, dengan mengikat radikal bebas dan molekul yang sangat reaktif,
akibatnya kerusakan sel akan dihambat. Salah satu antioksidan yang terdapat di
alam adalah kulit buah manggis.
Kulit buah manggis merupakan bagian dari buah manggis yang umumnya
kulit buah manggis sebelumnya telah diketahui bahwa kulit buah manggis
mempunyai aktifitas biologis sebagai antibakteri, antifungi, antiinflamasi,
antileukimia, anti-agregasi platelet, dan juga memiliki aktivitas antituberkulosis
(Pradipta, nikodemus, & susilawati, 2009).
Dalam penelitian Weecharangsan et al (2006) disebutkan bahwa aktivitas
antioksidan ekstrak kulit buah manggis yang diekstrasi dengan pelarut air, etanol
50% dan 95% serta etil asetat memiliki aktivitas antioksidan dengan
menggunakan metode perendaman radikal bebas DPPH. Potensi antioksidan
terbesar dimiliki oleh ekstrak air dan etanol 50% dengan IC50 berturut-urut adalah
34,8 dan 30,78 ppm. Jung et al (2006) melakukan isolasi senyawa kandungan
pada kulit buah manggis. Dari hasil penelitian tersebut yang mempunyai aktivitas
antioksidan paling tinggi adalah 8-hidroksikudraxanton, gartanin,
alpha-mangostin, gamma-mangostin dan smeathxanton.
Antioksidan dapat digunakan sebagai anti-aging yang dapat mencegah
penuaan dini, untuk penggunaan yang menyenangkan maka diperlukan kosmetik
anti-aging dengan antioksidan tinggi agar dapat merawat kulit wajah (Winarsi,
M.S, 2007). Antioksidan ini dapat diformulasikan sebagai sediaan kosmetik baik
sediaan yang berbentuk krim, gel ataupun lotion.
Salah satu bentuk sediaan kosmetik yang sering digunakan adalah krim.
Krim merupakan sediaan setengah padat berupa emulsi kental yang mengandung
air tidak kurang dari 60% dan dimaksudkan untuk pemakaian luar (DepKes RI,
1978). Keuntungan penggunaan krim yakni memiliki nilai estetika yang cukup
tinggi dan tingkat kenyamanan dalam penggunaan yang cukup baik. Disamping
itu, sediaan krim ini merupakan sediaan yang mudah dicuci, bersifat tidak lengket,
memberikan efek melembabkan kulit serta memiliki kemampuan penyebaran
yang baik.
Pada penelitian ini, Ekstrak etanol 50% kulit buah manggis (Garcinia
mangostana L.) diformulasikan dalam bentuk sediaan krim anti-aging dengan
berbagai formulasi menggunakan variasi nilai HLB span 60 dan tween 80 (4,95;
5,7; 6,8). Formulasi krim anti-aging yang terbaik kemudian diuji aktivitas
1.2 Rumusan Masalah
1. Apakah formulasi krim anti-aging ekstrak etanol 50% kulit buah
manggis dengan menggunakan variasi nilai HLB emulgator sorbitan
monostearat Span 60 dan Tween 80 stabil secara fisik?
2. Bagaimana aktivitas antioksidan formulasi krim anti-aging yang
terbaik dari ekstrak etanol 50% kulit buah manggis jika dibandingkan
terhadap kontrol positif dan ektrak etanol 50% kulit buah manggis?
1.3 Tujuan
1. Mendapatkan formulasi terbaik krim anti-aging ekstrak etanol 50%
kulit buah manggis yang stabil secara fisik.
2. Membandingkan aktivitas antioksidan kontrol positif vitamin C,
formulasi krim anti-aging ekstrak etanol 50% kulit buah manggis dan
ekstrak etanol 50% kulit buah manggis.
1.4 Hipotesis
Bagian kulit buah memiliki aktivitas antioksidan.
1.5 Manfaat
Adapun manfaat dari penelitian ini adalah memberikan informasi
mengenai aktivitas antioksidan dan stabilitas fisik formulasi krim anti-aging
BAB II
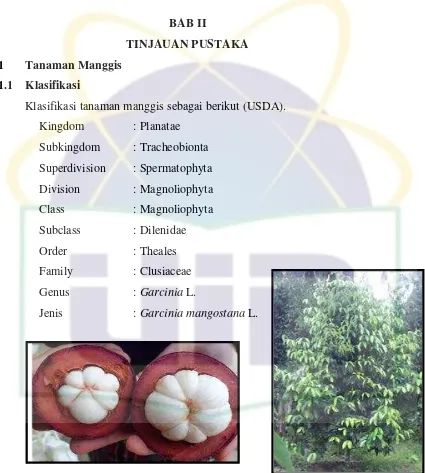
TINJAUAN PUSTAKA 2.1 Tanaman Manggis
2.1.1 Klasifikasi
Klasifikasi tanaman manggis sebagai berikut (USDA).
Kingdom : Planatae
Subkingdom : Tracheobionta
Superdivision : Spermatophyta
Division : Magnoliophyta
Class : Magnoliophyta
Subclass : Dilenidae
Order : Theales
Family : Clusiaceae
Genus : Garcinia L.
Jenis : Garcinia mangostana L.
Gambar 1. Pohon dan buah manggis (Garcinia mangostana L.) (Sumber : Koleksi pribadi)
2.1.2 Nama Latin
Di Indonesia manggis disebut dengan berbagai macam nama lokal seperti
manggoita (Aceh), manggista (Sumatera Utara), manggih (Sumatera Barat),
manggu (Jawa Barat), mangghis (Madura), kisara (Makasar), mangustang
2.1.3 Ekologi
Garcinia mangostana L.merupakan tanaman buah yang banyak tumbuh di
daerah iklim tropis yang hangat dan lembab. Tanaman manggis ini dapat
diemukan di negara-negara Asia Selatan dan Asia Tenggara. Garcinia mangostana
berhubungan erat dengan daerah elevasi rendah dengan ketinggian kurang dari
500 m atau 600 diatas permukaan laut. Sehingga Garcinia mangostana L. dapat
dibudidayakan di dataran tinggi namun memiliki tingkat pertumbuhan yang lebih
lambat (Osman, & Milan, 2001).
2.1.4 Morfologi
Garcinia mangostana L. merupakan pohon buah yang dapat tumbuh
hingga mencapai 7 sampai 25 meter (Al-Fattah,2011). Bentuk pohon buah
manggis yang beragam yakni bisa bentuk elliptical atau pyramidal, namun bentuk
pohon yang sering ditemukan adalah bentuk pyramidal (Mansyah et al, 2010).
Memiliki daun yang ringkas, tebal, berkilat, permukaan atas berwarna hijau zaitu,
permukaan bawah berwarna hijau kekuning-kuningan, daun muda merah, tangkai
daun pendek, susunan bertentangan, ukuran panjang daun 15-25 cm, lebar 7-13
cm. Berbunga tunggal atau berpasangan di ujung ranting. Tangkai bunga pendek
dan tebal. Sedangkan buahnya berbentuk bola, berwarna hijau muda sebelum
masak, menjadi merah atau merak keunguan setelah masak dan hitam apabila
sangat masak. Isi buah berwarna putih (Chooi, 2007).
2.1.5 Kandungan Kimia dan Manfaat
Kandungan kimia kulit buah manggis antara lain adalah derivat xanthon
yang meliputi mangostin, mangostenol, mangostinon A, mangostinon B,
trapezifolixanthon, tovophyllin B, α mangostin, mangostin, garcinon B,
mangostanol, flavonoid epicatechin, gartanin (Al-fatah, 2011).
Xanton adalah pigmen fenol kuning yang reaksi warnanya serta gerakan
kromatografinya serupa dengan flavonoid, namun secara kimia xanton berbeda
dengan flavonoid dan mudah dibedakan dari spectrum yang khas hampir semua
xanton yang diketahui terdapat terbatas pada empat suku : Guttiferae,
Gentianaceae, Moraceae, dan Polygalaceae. Tetapi, satu xanton, yaitu mangiferin
yang ter-C- glikosilasi, sangat tersebar luas, terdapat baik dalam paku-pakuan
jenis xanton yang diisolasi dari kulit manggis, diantaranya adalah α-, - dan -mangostins, garcinone E, 8- deoxygartanin, dan gartanin. Xanton dapat diisolasi
dari pericarp, buah utuh, kulit batang, dan juga pada daun manggis. Beberapa
studi menunjukkan bahwa xanton yang diperoleh dari manggis mempunyai
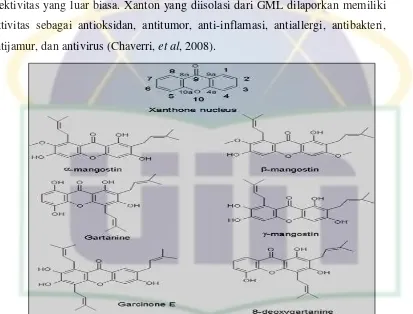
efektivitas yang luar biasa. Xanton yang diisolasi dari GML dilaporkan memiliki
aktivitas sebagai antioksidan, antitumor, anti-inflamasi, antiallergi, antibakteri,
antijamur, dan antivirus (Chaverri, et al, 2008).
Gambar 2. Inti xanthone dengan jumlah IUPAC karbon dan struktur kimia dari xanthones yang paling banyak dipelajari.
(Sumber: Chaverri, et al, 2008).
Ekstrak etanol 50% kulit buah manggis telah dilaporkan berpotensi
sebagai pelindung saraf dari stres oksidatif yang disebabkan karena kerusakan sel
pada penyakit neurodegenerative seperti penyakit Alzaimer, penyakit Parkinson
dan stroke,(Weecharangsan et al, 2005). Selain itu ekstrak kulit buah manggis
dapat menghambat produksi ROS, serta mempunyai aktivitas antioksidan yang
2.2 Ekstraksi
2.2.1 Pengertian Ekstraksi
Ekstraksi adalah teknik pemisahan suatu senyawa berdasarkan perbedaan
distribusi zat terlarut di antara dua pelarut yang saling bercampur. Pada umumnya
zat terlarut yang diekstraksi bersifat tidak larut atau larut sedikit dalam suatu
pelarut tetapi mudah larut dengan pelarut lain. Metode ekstraksi yang tepat
ditentukan oleh tekstur kandungan air bahan-bahan yang akan diekstrak dan
senyawa-senyawa yang akan diisolasi (Harborne, 1996). Senyawa yang aktif yang
terdapat dalam berbagai simplisia dapat digolongkan kedalam golongan miyak
atsiri, alkaloid, flavonoid, dan lain-lain. Struktur kimia yang berbeda-beda akan
mempengaruhi kelarutan serta stabilitas senyawa-senyawa tersebut terhadap
pemanasan, udara, cahaya, logam berat, dan derajat keasaman. Dengan
diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah
pemiliha pelarut dan cara ekstraksi yang tepat (Depkes RI, 2000).
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang
sesuai, kemudian semua atau hampir semua pelarut diuapkan dan masa atau
serbuk yang tesisa diperlakukan sedemikian hingga memenuhi baku yang
ditetapkan (DepKes RI, 1995)
2.2.2 Metode-metode Ekstraksi
Ditjen POM (2000), membagi beberapa metode ekstraksi dengan
menggunakan pelarut yaitu :
1) Cara dingin
a. Maserasi
Maserasi ialah proses pengekstrakan simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokkan atau pengadukkan pada temperatur
ruang (kamar). Secara teknologi termasuk ekstraksi dengan prinsip metode
pencapaian konsentrasi pada keseimbangan. Maserasi kinetik berarti dlakukan
pengadukkan yang kontinyu (terus-menerus). Remaserasi berarti dilakukan
pengulangan penambahan pelarut setelah dilakukan penyaringan maserat
b. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna (exhaustive extraction) yang umumnya dilakukan pada temperatur
ruang. Proses ini terdiri dari tahapan pengembangan bahan, tahap maserasi antara,
tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus-menerus
sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali bahan.
2) Cara panas
a. Refluks
Refluks merupakan ekstraksi dengan pelarut pada temperatur titik
didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan
dengan adanya pendingin balik. Umumnya dilakuka pengulangan proses pada
residu pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi
sempurna.
b. Soxhletasi
Soxhletasi adalah ekstraksi dengan menggunakan pelarut yang selalu baru
yang umumnya dilakukan dnegan alat khusus sehingga terjadi ekstraksi kontinyu
dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
c. Digesti
Digesti merupkan maserasi kinetik (dengan pengadukan kontinyu) pada
temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum
dilakukan pada temperatur 40-50oC. d. Infusa
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air
tubuh yang perlu mendapatkan perhatian khusus untuk memperindah kecantikkan,
selain itu kulit dapat membantu menemukan penyakit yang diderita pasien.
Kulit mencakup kulit pembungkus permukaan tubuh berikut turunannya
termasuk kuku, rambut, dan kelenjar. Kulit adalah lapisan jaringan yang terdapat
pada bagian luar untuk menutupi dan melindungi permukaan tubuh. Kulit
berhubungan dengan selaput lendir yang melapisi rongga lubang masuk. Pada
permukaan kulit bermuara kelenjar keringat dan kelenjar mukosa.
Kulit disebut juga integumen atau kutis yang tumbuh dari dua macam
jaringan yaitu jaringan epitel yang menumbuhkan lapisan epidermis dan jaringan
pengikat (penunjang) yang menumbuhkan lapisan dermis (kulit dalam). Kulit
mempunyai susunan serabut saraf yang teranyam secara halus berguna untuk
merasakan sentuhan atau sebagai alat raba dan merupakan indikator untuk
memperoleh kesan umum dengan melihat perubahan pada kulit (Syaifuddin,
2009).
Gambar 3. Struktur Kulit
2.3.1 Lapisan Kulit 1. Epidermis
Lapisan paling luar yang terdiri atas lapisan epitel gepeng. Unsur
utamanya adalah sel-sel tanduk (keratinosit) dan sel melanosit. Lapisan
epidermis tumbuh terus karena lapisan sel induk yang berada dilapisan bawah
bermitosis terus-menerus, sedangkan lapisan paling luar epidermis akan
mengelupas dan gugur. Epidermis dibina oleh sel-sel epidermis terutama
serat-serat kolagen dan sedikit serat elastis.
Dari sudut kosmetik, epidermis merupakan bagian kulit yang menarik
karena kosmetik dipakai pada epidermis itu. Meskipun ada beberapa jenis
kosmetik yang digunakan sampai ke dermis, namun tetap penampilan
epidermis menjadi tujuan utama. Ketebalan epidermis berbeda-beda pada
berbagai tubuh, yang paling tebal berukuran 1 milimeter, misalnya ada
telapak kaki dan telapak tangan, dan lapisan yang tipis berukuran 0,1
milimeter terdapat pada kelopak mata, pipi, dahi, dan perut (Tranggono, &
Latifah, 2007).
Epidermis terdiri atas beberapa lapisan sel. Sel-sel ini berbeda dalam
beberapa tingkat pembelahn sel secara mitosis. Lapisan permukaan dianggap
sebagai akhir keaktifan sel, lapisan tersebut terdiri dari 5 lapis (Syaifuddin,
2009).
a. Stratum korneum (Stratum corneum)
Lapisan ini terdiri atas banyak lapisan sel tanduk (keratinasi), gepeng,
kering, dan tidak berinti. Sitoplasmanya diisi dengan serat keratin, makin ke
luar letak sel makin gepeng seperti sisik lalu terkelupas dari tubuh. Sel yang
terkelupas akan digantikan oleh sel yang lain. Zat tanduk merupakan keratin
lunak yang susunan kimianya berada dalam sel-sel keratin keras. Lapisan
tanduk hampir tidak mengandung air karena adanya penguap air, elastisnya
kecil, dan sangat efektif untuk pencegahan penguapan air dari lapisan yang
lebih dalam (Syaifuddin, 2009).
b. Stratum lusidum (Stratum lucidum)
Lapisan ini terdiri atas beberapa lapis sel yang sangat gepeng dan bening.
secara keseluruhan seperti kesatuan yang bening. Lapisan ini ditemukan pada
daerah tubuh yang berkulit tebal (Syaifuddin, 2009). Lapisan ini terletak
dibawah stratum corneum. Antara stratum lucidum dan stratum granulosum
terdapat lapisan keratin tipis yang disebut rein’s barrier (Szakall) yang tidak
bisa ditembus (impermeable) (Tranggono, & Latifah, 2007).
c. Stratum granulosum
Lapisan ini terdiri atas 2-3 lapis sel poligonal yang agak gepeng dengan
inti ditengah dan sitoplasma berisi butiran (granula) keratohialin atau
gabungan keratin dengan hialin. Lapisan ini menghalangi masuknya beda
asing, kuman, dan bahan kimia masuk ke dalam tubuh (Syaifuddin, 2009).
d. Stratum spinosum
Lapisan ini terdiri atas banyak lapisan sel berbentuk kubus dan poligonal,
inti terdapat di tengah dan sitoplasmanya berisi berkas-berkas serat yang
terpaut pada desmosom (jembatan sel). Seluruh sel terikat rapat lewat
serat-serat tersebut sehingga secara keseluruhan lapisan sel-selnya berduri. Lapisan
ini untuk menahan gesekkan dan tekanan dari luar, tebal dan terdapat di
daerah tubuh yang banyak bersentuhan atau menahan beban dan tekanan
seperti tumit dan pangkal telapak kaki (Syaifuddin, 2009).
e. Stratum malpigi
Unsur-unsur lapis taju yang mempunyai susunan kimia yang khas. Inti
bagian basal lapis taju mengandung kolesterol dan asam-asam amino. Stratum
malpigi merupakan lapisan terdalam dari epidermis yang berbatasan dengan
dermis dibawahnya dan terdiri atas selapis sel berbentuk kubus (batang)
(Syaifuddin, 2009).
f. Stratum basal (Stratum germinativum atau membran basalis)
Lapisan terbawah epidermis. Di dalam stratum germinativum juga terdapat
sel-sel melanosit, yaitu sel-sel yang tidak mengalami keratinisasi dan
fungsinya hanya membentuk pigmen melanin dan memberikannya kepada
sel-sel keratinosit melalui dendrit-dendritnya. Satu sel melanosit melayani
sekitar 36 sel keratinosit. Kesatuan ini diberi nama unit melanin epidermal
2. Dermis
Berbeda dengan epidermis yang tersusun oleh sel-sel dalam berbagai
bentuk dan keadaan, Dermis terutama terdiri dari bahan dasar serabut kolagen
dan elastin, yang berada di dalam substansi dasar yang bersifat koloid dan
terbuat dari gelatin mukopolisakarida. Batas dermis sulit ditentukan karena
menyatu dengan lapisan subkutis (hipodermis), ketebalannya antara 0,5-3
mm, beberapa kali lebih tebal dari epidermis. Dermis bersifat ulet dan elastis
yang berguna untuk melindungi bagian yang lebih dalam. Serabut kolagen
dapat mencapai 72 persen dari keseluruhan berat kulit manusia bebas lemak.
Di dalam dermis terdapat adneksa-adneksa kulit seperti folikel rambut,
papila rambut, kelenjat keringat, saluran keringat, kelenjar sebasea, otot
penegak rambut, ujung pembuluh darah dan ujung saraf, juga sebagian
serabut lemak yang terdapat pada lapisan lemak bawah kulit (subkutis /
hipodermis) (Tranggono, & Latifah, 2007; Syaipfuddin, 2009).
3. Lapisan Subkutan
Hipodermis adalah lapisan bawah kulit (fasia superfisialis) yang terdiri
atas jaringan pengikat longgar, komponennya serat longgar, elastis, dan sel
lemak. Sel-sel lemak membentuk jaringan lemak pada lapisan adiposa yang
terdapat susunan lapisan subkutan untuk menentukan mobilitas kulit
diatasnya, bila terdapat lobulus lemak yang merata, hipodermis membentuk
bantal lemak yang disebut pannikulus adiposa. Pada daerah perut, lapisan ini
dapat mencapai ketebalan 3 cm. Sedangkan pada kelopak mata, penis, dan
skortum, lapisan subkutan tidak mengandung lemak. Dalam lapisan
hipodermis terdapat anyaman pembuluh arteri, pembuluh vena, dan anyaman
saraf yang berjalan sejajar dengan permukaan kulit bawah dermis. Lapisan ini
mempunyai ketebalan bervariasi dan mengikat kulit secara longgar terhadap
jaringan di bawahnya (Syaifuddin, 2009).
2.4 Kosmetik
Kosmetik berasal dari kata yunani “kosmetikos” yang berarti keterampilan
445/MenKes/Permenkes/1998 adalah sediaan atau paduan bahan yang siap untuk
digunakan pada bagian luar badan (epidermis, rambur, kuku, bibir, dan organ
kelamin bagian luar), gigi, dan rongga mulut untuk membersihkan, menambah
daya tarik, mengubah penampakan, melindungi supaya tetap dalam keadaan baik,
memperbaiki bau badan tetapi tidak dimaksudkan untuk mengobati atau
menyembuhkan suatu penyakit.
Tujuan utama penggunaan kosmetik pada masyarakat modern adalah
untuk kebersihan pribadi, meningkatkan daya tarik melalui make-up,
meningkatkan rasa percaya diri dan perasaan tenang, melindungi kulit dan rambut
dari kerusakan sinar UV, polusi dan faktor lingkungan yang lain, mencegah
penuaan, dan secara umum, membantu seseorang lebih menikmati hidup.
Menurut Peraturan Mentri Kesehatan RI, penggolongan kosmetik menurut
menurut kegunaannya bagi kulit dibagi menjadi kosmetik perawatan kulit (skin
-care cosmetics) dan kosmetik riasan (dekoratif atau make-up). kosmetik
perawatan kulit (skin-care cosmetics) terdiri dari kosmetik untuk membersihkan
kulit (cleanser) (sabun, cleansing cream, cleansing milk, penyegar kulit
(freshener)), kosmetik untuk melembabkan kulit (moisturizer) (moisturizing
cream, night cream, anti wrinkle cream), kosmetik pelindung kulit (sunscreen
cream, dan sunscreen foundation, sun block cream/lotion), kosmetik untuk
menipiskan atau mengampelas kulit (peeling) (scrub cream yang berisi
butiran-butiran halus yang berfungsi sebagai pengampelas (abrasiver)). Kosmetik riasan
(dekoratif atau make-up) diperlukan untuk merias dan menutup cacat pada kulit
sehingga menghasilkan penampilan yang menarik serta menimbulkan efek
psikologis yang baik, seperti percaya diri (self confidence). Dalam kosmetik
riasan, peran zat pewarna dan zat pewangi sangat besar (Tranggono, & Latifah,
2007).
2.5 Proses Penuaan Kulit
Proses penuaan antara lain tampak dari kerutan dan keriput pada kulit atau
kemunduran lain ketika masih muda. Ada dua teori yang dapat menjelaskan
proses penuaan yakni, penuaan merupakan proses alami yang tidak dapat
maupun fisiologi pada semua organ tubuh, mulai dari pembuluh darah dan organ
tubuh lainnya sampai kulit.
Perubahan akibat proses penuaan yang terjdi pada kulit dapat dibagai atas
perubahan anatomi, fisiologis, serta kimiawi. Beberapa perubahan anatomi dapat
terlihat langsung, seperti hilangnya elastisitas kulit dan fleksibilitas kulit yang
menyebabkan timbulnya kerut dan keriput, berkurangnya jumlah rambut dikepala
walaupun pada wanita justru sering tumbuh kumis atau rambut panjang di leher
tau pipi, hiperpigmentasi dan tumor kulit terutama diusia 40 tahun ke atas akibat
terlalu lama terpapar sinar matahari, penebalan kulit, epidermis kering dan
pecah-pecah, , perubahan bentuk kuku dan rambut dan sebagainya.
Banyak faktor yang mempengaruhi penuaan kulit, tetapi yang terkuat
adalah sinar matahari (photoaging), khususnya sinar UV yang terdapat di dalam
sinar matahari. Knox et al. Menemukan perbedaan yang nyata antara kulit yang
tidak tertutup pakaian sehingga sering terpapar sinar matahari dan kulit yang
sering tertutup pakaian. Kulit yang terbuka cepar kering, keriput, kasar, dan
menderita kerusakan lain akibat sinar UV matahari.
2.5.1 Mekanisme Photoaging
Ketika kulit terpapar oleh sinar matahari, radiasi UV yang terserap oleh
kulit yang dapat menghasilkan komponen yang berbahaya yaitu Reactive Oxygen
Species (ROS) yang dapat menyebabkan kerusakan oksidatif pada komponen
selular seperti dinding sel, membran lipid, mitokondria, dan DNA. Radiasi UV
menyebabkan pembentukan ROS dan menginduksi activator protein (AP)-1 yang
merupakan faktor transkripsi yang menghambat produksi kolagen dan
meningkatkan penghancuran kolagen dengan memperbanyak enzim yang disebut
matrix metalloproteinase (MMPs). Selain itu, radiasi UV juga menyebabkan
penurunan transforming growth factor (TGF)- yang merangsang pembentukkan kolagen, sehingga pembentukkan kolagen menurun. Peningkatan penghancuran
kolagen dan penurunan produksi kolagen akibat radiasi sinar UV inilah penyebab
Gambar 4. Mekanisme photoaging (Sumber : Helfrich, Sachs, & Voorhees, 2008)
2.6 Radikal Bebas
Oksigen adalah atom yang sangat reaktif yang mampu menjadi bagian dari
molekul yang berpotensi merusak yang biasa disebut "radikal bebas." Radikal
bebas mampu menyerang sel-sel sehat tubuh, menyebabkan mereka kehilangan
struktur dan fungsi mereka (Percival, 1998). Radikal bebas adalah suatu atom atau
molekul yang sangat reaktif dengan elektron yang tidak memiliki pasangan
(Corwin, 2007). Radikal bebas mencari reaksi-reaksi agar dapat memperoleh
kembali elektron pasangannya. Radikal bebas sangat reaktif, secara kimiawi tidak
stabil, umumnya terdapat hanya dalam kadar yang kecil, dan cenderung ikut serta
atau mengawali reaksi rantai (Underwood, 1994). Serangkaian reaksi dapat
terjadi, yang menghasilkan serangkaian radikal bebas. Setelah itu, radikal bebas
dapat mengalami tubrukan kaya energi dengan molekul lain, yang merusak ikatan
dalam molekul (Corwin, 2007). Ketika hal tersebut terjadi di dalam tubuh, maka
dapat terjadi kerusakan pada sel, asam nukleat, protein dan lemak dikarenakan
serangan terhadap molekul biologi akan menyebabkan kerusakan jaringan sistem
imun. Radikal bebas menyebabkan lipid peroksidase yang dapat mempermudah
Radikal bebas dapat timbul melalui dua mekanisme utama yaitu,
penimbunan energi (ionisasi air oleh radiasi, elektron terepas, dan terjadi radikal
bebas) , dan interaksi antara oksigen (substansi lain, dan elektron bebas dengan
reaksi oksidasi-reduksi) Dalam hal ini akan terbentuk radikal superoksid
(Underwood., 1994).
Para ahli biokimia menyebutkan bahwa radikal bebas merupakan salah
satu bentuk senyawa oksigen reaktif. Senyawa ini terbentuk di dalam tubuh,
dipicu oleh bermacam-macam faktor. Radikal bebas bisa terbentuk misalnya
ketika komponen makanan diubah menjadi bentuk energi melalui proses
metabolisme. Pada proses metabolisme ini, seringkali terjadi kebocoran elektron
dan mudah terbentuknya radikal bebas. Misalnya hidrogen peroksida (Winarsi,
2007).
Radikal bebas merupakan Reaktive Oxygen species (ROS) yang akan
menyerang molekul lain disekitarnya sehingga menyebabkan reaksi berantai
terjadi dan menghasilkan radikal bebas yang beragam, seperti anion peroksida
(O2-), dan hidrogen peroksida (H2O2) yang sudah dijelaskan sebelumnya, hidrogen
bebas (OH), asam hipoklorous (HOCl), dan peroksinitrat (ONOO-) (Vimala, et al., 2003).
2.7 Antioksidan
Antioksidan adalah senyawa-senyawa yang mampu menghilangkan,
membersihkan, menahan pembentukkan ataupun memasdukan efek spesies
oksigen reaktif. Antioksidan merupakan senyawa pemberi donor (electron donor)
atau reduktan. Senyawa ini memiliki berat molekul kecil, tetapi mampu
menginaktivasi berkembangnya reaksi oksidasi dengan cara mencegah
terbentuknya radikal. Penggunaan senyawa antioksidan juga anti radikal saat ini
semakin meluas seiring dengan semakin besarnya pemahaman masyarakat tentang
peranannya dalam menghambat penyakit generatif seperti penyakit jantung,
arteriosclerosis, kanker, serta gejala penuaan. Masalah-masalah ini berkaitan
dengan kemampuan antioksidan untuk bekerja sebagai inhibitor (penghambat)
reaksi oksidasi oleh radikal bebas reaktif yang menjadi salah satu pencetus
Antioksidan terbagi menjadi dua yakni antioksidan enzim (superoksida
dismutase (SOD), katalase dan glutation peroksidase (GSH.Prx)) dan antioksidan
vitamin (alfa tokoferol/ vitamin E, beta karoten dan asam askorbat/vitamin C)
yang banyak didapatkan dari tanaman dan hewan .
Tubuh mengasilkan senyawa antioksidan, tetapi jmlahnya sering kali tidak
cukup untuk menetralkan radikal bebas yang masuk kedalam tubuh. Sebagai
contoh tubuh dapat menghasilkan glutathione, salah satu antioksidan yang sangat
kuat, hanya tubuh memerlukan asupan vitamin C sebesar 100 mg untuk memicu
tubuh mengasilkan glutathione ini. Kekurangan antioksidan dalam tubuh yakni
memerlukan asupan dari luar (Kuncahyo & Sunardi., 2007; Winarsi 2007).
2.8 Uji Aktivitas Antioksidan 2.8.1 Metode DPPH
Pengukuran aktivitas antioksida dapat dilakukan dengan beberapa cara
antara lain dengan metode lipid peroksida, tiobarbiturat, malonaldehid,8-karoten
bleaching, DPPH, dan tiosianat. Metode DPPH adalah salah satu yang paling
populer karena praktis dan sensitif (Molyneux, 2004). DPPH merupakan senyawa
radikal bebas yang stabil dan apabila digunakan sebagai pereaksi cukup
dilarutkan,. Senyawa ini jika disimpan dalam keadaan dan kondisi penyimpanan
yang baik akan tetap stabil selama bertahun-tahun (Winarsi, 2007).
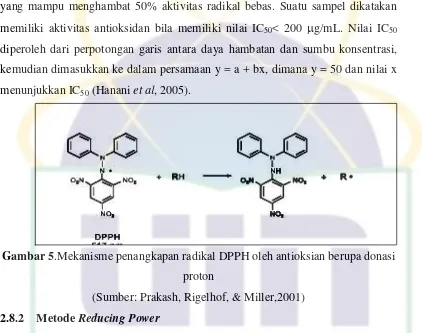
Prinsip pengujian antioksidan menggunakan DPPH adalah senyawa
antioksidan akan bereaksi dengan radikal DPPH melalui mekanisme donasi atom
hidrogen dan menyebabkan terjadinya peluruhan warna DPPH dari ungu ke
kuning yang diukur pada panjang gelombang 515,5 nm (Hanani et al.,2005).
Rumus penghambatan aktivitas radikal bebas (%)
Keterangan: % inhibisi = persentase hambat antioksidan
A0 = absorbansi blanko
A1 = absorbansi larutan uji
Nilai IC50 (Inhibition Concentration) adalah konsentrasi antioksidan (g/mL)
yang mampu menghambat 50% aktivitas radikal bebas. Suatu sampel dikatakan
memiliki aktivitas antioksidan bila memiliki nilai IC50< 200 g/mL. Nilai IC50
diperoleh dari perpotongan garis antara daya hambatan dan sumbu konsentrasi,
kemudian dimasukkan ke dalam persamaan y = a + bx, dimana y = 50 dan nilai x
menunjukkan IC50 (Hanani et al, 2005).
Gambar 5.Mekanisme penangkapan radikal DPPH oleh antioksian berupa donasi proton
(Sumber: Prakash, Rigelhof, & Miller,2001)
2.8.2 Metode Reducing Power
Pada metode reducing power, antioksidan yang terdapat pada sampel akan
mereduksi senyawa Fe3+ menjadi senyawa Fe2+ dengan cara memberikan satu elektron yang dimilikinya. Banyaknya jumlah Fe2+ selanjutnya dapat diamati pada spektrofotometri UV-Vis pada panjang gelombang maksimum (588-598 nm).
Peningkatan absorbansi atau penyerapan yang terjadi menunjukkan peningkatan
reduksi yang bagus. Peningkatan reduksi yang bagus pada metode reducing power
berbanding lurus dengan konsentrasinya.
Artinya semakin besar konsentrasi sampel maka semakin besar pula
tingkat reduksinya. Fe3+ yang berwarna hijau akan mengalami reduksi menjadi Fe2+ yang berwarna kuning (Aiyegoro, 2009).
Metode ini menggunakan kompleks Fe(CN)63- sebagai pereaksi. Kompleks
anion Fe(CN)63- yang berwarna hijau akan berfungsi sebagai zat pengoksidasi dan
akan mengalami reduksi menjadi Fe(CN)64- yang berwarna kuning dengan reaksi
Benzie dan Strain (1996), menggunakan Fe(TPTZ)23+ kompleks besi-ligan
2,4,6-tripiridil-triazin sebagai pereaksi. Kompleks biru Fe(TPTZ)23+ akan
berfungsi sebagai zat pengoksidasi dan akan mengalami reduksi menjadi
Fe(TPTZ)22+ yang berwarna kuning dengan reaksi berikut:
2.8.3 Metode Aktivitas Radikal Bebas Nitrogen Monoksida
Metode Garrat telah diadopsi untuk menentukan aktivitas radikal bebas
dari ekstrak air H. pedunculatum.Sodium Nitroprusside di dalam pelarut air pada
pH psikologis secara spontan menghasilkan nitrogen monoksida yang berinteraksi
dengan oksigen untuk membentuk ion nitrit yang ditentukan dengan pereaksi
Grisses.
Selanjutnya dianalisis nilai absorbansinya dengan menggunakan
spektrofotometri ultraviolet dan sinar tampak pada panjang gelombang 540 nm.
Jumlah radikal bebas nitrogen monoksida yang dihitung berdasarkan nilai
absorbansinya yaitu :
% inhibisi = (Ao-A1) X 100%
Ao
Dimana % inhibisi merupakan persentase hambat antioksidan,Ao
merupakan absorbansi sebelum reaksi dan A1 merupakan absorbansi sesudah
reaksi (Aiyegoro, 2009).
2.8.4 Metode Aktivitas Radikal Bebas Ion Ferro (Pembentukan Logam Kelat)
Aktivitas pembentukan khelat pada ion ferro diukur menurut Zao ().
Campuran pereaksi yang mengandung ekstrak, air destilasi, FeCl2 dan ferrozine
yang kemudian diinkubasi selama 10 menit pada suhu 40oC dan diukur absorbansinya pada panjang gelombang 562 nm. Setelah itu aktivitas
pembentukan khelat dihitung menggunakan rumus :
Fe(TPTZ)23+ + AROH → Fe(TPTZ)22+ + H+ + AR=O
Rata-rata Khelat = [1- (A1-A2) ] X 100 (Ao)
dimana Ao merupakan nilai absorbansi kontrol positif tanpa tambahan
eksrak, A1 merupakan nilai absorbansi campuran reaksi, A2 merupakan nilai
absorbansi tanpa penambahan FeCl2 (Arora, 2011).
2.8.5 Metode Tiosianat
Pengujian aktivitas antioksidan dengan metode ini didasarkan pada
kemampuan senyawa antioksidan dalam menghambat terbentuknya radikal yang
reaktif.Pembentukan radikal bebas disebabkan oleh oksidasi asam
linoleat.Oksidasi lipid sering disebut autooksidasi karena reaksi tetap berlangsung
walaupun tidak ada zat pengoksidasi.
Hasil oksidasi asam linoleat adalah malonaldehida dan radikal peroksida
yang reaktif. Radikal bebas yang terbentuk akan berubah menjadi senyawa
karbonil, yaitu aldehida dan keton. Oksidasi asam linoleat membentuk
malonaldehid merupakan indikasi adanya oksidasi lemak (Fardiaz, 1996). Selain
itu, asam linoleat yang mengalami kerusakan akan menghasilkan senyawa
peroksida yang sangat reaktif dan bersifat radikal bebas. Penambahan antioksidan
menyebabkan oksidasi asam linoleat terhenti (Schulz, 1985).
Aktivitas antioksidan yang ditentukan dengan metode tiosianat
membutuhkan suatu kontrol positif, pembanding ini biasanya merupakan senyawa
yang telah diketahui sifat antioksidannya seperti vitamin C, butil hidroksi toluen
(BHT) atau tokoferol (vitamin E). Oksidasi asam linoleat dalam kondisi buffer
yang diinkubasi pada suhu 37oC menggunakan FeCl2 dan amonium tiosianat
sebagai pereaksi oksodator dapat mengoksidasi Fe2+ menjadi Fe3+ sehingga menghasilkan warna merah darah yang menyerap sinar tampak pada panjang
gelombang 500 nm. Intensitas warna dinyatakan sebagai nilai absorbansi dengan
pengukuran menggunakan spektrofotometer UV/Vis. Peroksida lemak
2.8.6 Metode Deoksiribosa
Reaksi degradasi gula deoksiribosa akan menghasilkan suatu produk
karbonil dan dikarbonil di antaranya malonaldehid (MDA). Adanya MDA dapat
dideteksi dengan asam tiobarbiturat (TBA) dalam suasana asam membentuk suatu
kromogen yang berwarna merah muda.Jumlah kromogen MDA-TBA yang
terbentuk sangat bergantung dari jumlah deoksiribosa yang didegradasi. Semakin
tinggi konsentrasi deoksiribosa yang ditambahkan akan menyebabkan
peningkatan absorbansi kromogen MDA-TBA (Halliwell, 1999).
Uji kemampuan antioksidan suatu sampel untuk menghalangi jalan
katalitik dari biosintesis pigmen melanin, pigmen yang membuat kulit putih.
Tirosin mengatur tiga tahap di dalam jalan biosintesis melanin, dengan perubahan
tirosin menjadi dopa, dopa menjadi dopaquinone dan DHI menjadi
indole-5,6-quinone (Vimala, et al., 2003).
2.9 Spektrometer UV-Vis
Spektrofotometer UV-Vis adalah alat yang digunakan untuk mengukur
serapan yang dihasilkan dari interaksi kimia antara radiasi elektromagnetik
dengan molekul atau atom dari suatu zat kimia pada daerah ultraviolet (200-400
nm) dan sinar tampak (400-800 nm).
Spektrofotometer yang sesuai untuk pengukuraan di daerah spektrum
ultraviolet dan cahaya tampak terdiri dari suatu sistem optik dengan kemampuan
menghasilkan cahaya monokromatik dalam jangkauan 200 nm hingga 800 nm dan
suatu alat yang sesuai untuk menetapkan serapan. Kedua sel yang digunakan
untuk larutan yang diperiksa dan larutan pembanding harus mempunyai
karakteristik spektrum yang sama. Bila digunakan instrumen bekas ganda dengan
perekan, sel yang berisi pelarut ditempatkan pada jalur berkas pembanding.
Jika tidak dinyatakan lain, serapan diukur pada panjang gelombang yang
ditetapkan degan menggunkan kuvet yang panjangnya 1 cm pada suhu 19oC hingga 20oC. Jika hal tersebut tidak sesuai untuk instrumen tertentu, panjang gelombang kuvet dapat diubah atau sebagai gantinya kadar dapat diubah, asalkan
telah ditunjukkan bahwa Hukum Beer dipenuhi untuk jangkauan kadar tersebut.
untuk membuat larutan uji sebagai pembanding. Dalam hal tertentu, pengukuran
dilakukan terhadap suatu campuran pereaksi sebagai pembanding.
Suatu pernyataan dalam suatu penetapan kadar atau pengujian mengenai
panjang gelombang serapan maksimum mengandung implikasi bahwa maksimum
tersebut tepat pada atau dalam batas 2 nm dari panjang gelombang yang
ditetapkan (Soemitro, et al., 1995). Suatu spektrofotometri UV-Vis tersusun dari
sumber spektrum tampak yang kontinyu, monokromator, sel pengabsorbsi untuk
larutan sampel atau blanko dan suatu alat untuk mengukur perbedaan absobsi
antara sampel dan blanko ataupun pembanding (Khopkar, 2003).
2.10 Krim
Definisi krim adalah bentuk sediaan setengah padat mengandung satu atau
lebih bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai. Sediaan
ini merupakan sediaan setengan padat (semisolid) dari emulsi yang terdiri dari
campuran antara fase minyak dan fase air (DepKes RI, 1995).
Krim umunya kurang kental dan lebih ringan daripada salep, sehingga
krim lebih disukai daripada salep. Umumnya krim mudah menyebar rata dan
karena krim merupakan emulsi minyak dalam air, maka akan lebih mudah
dibersihkan daripada sebagian besar salep. Krim dianggap mempunyai daya tarik
estetik lebih besar karena sifatnya yang tidak berminyak dan kemampuannya
berpenetrasi dengan cepat ke dalam kulit (Ansel, 1989).
2.11 Formulasi Krim
Sebagai bahan emulgator, yang digunakan dalam penelitian ini adalah
emulgator nonionik (dalam medium air tidak membentuk ion).Pemilihan
emulgator nonionik ini karena emulgator ini bereaksi netral, dapat sedikit
dipengaruhi oleh elektrolit dan selanjutnya netral terhadap pengaruh
kimia.Aktivitasnya relatif tidak dipengaruhi oleh suhu (Voigt, 1995), selain itu
digunakan juga bahan tambahan yang meliputi emolien, humektan, antioksidan,
dan pengawet. Profil dari bahan-bahan yang digunakan dalam formula krim pada
a. Bahan pengemulsi
1. Sorbitan monostearate (span 60)
Pada formulasi farmasetik, sorbitan monostearat biasa digunakan sebagai
bahan pegemulsi untuk krim, emulsi, dan salep untuk penggunaan topikal.
Sorbitan monostearate berbentuk padatan malam berwarna kuning pucat dengan
minyak yang lemah. Bahan ini larut dalam minyak, dan juga sebagian besar
pelarut organik. Meskipun tidak larut dalam air, namun akan cepat terdispersi.
Umumnya bahan ini tidak toksik dan tidak mengiritasi. Konsentrasi yang biasa
digunakan untuk emulasi air dalam minyak adalah 15% jika dikombinaikan
1-10%.
2. Tween 80
Sebagai pengemulsi untuk mendapatkan sediaan emulsi yang stabil, biasa
digunakan tween 80 yang merupakan surfaktan hidrofilik nonionik. Tween 80
berbentuk cairan berminyak berwarna kuning. Bahan ini larut dalam etanol dan
air. Umumnya bahan ini tidak toksik dan tidak mengiritasi. Konsetrasi yang biasa
digunakan adalah 1-10%. (Wade, & Weller, 1994).
b. Bahan emolien
1. Dimethicon
Dimethicon biasa digunaka dalam kosmetik dan formulasi farmasi.
Dimethicon bersifat hidrofobik dan sering digunakan dalam sediaan topikal.
Dimethicon merupakan cairan berwarna jernih atau bening, dan tersedia dalam
berbagai macam viskositas. Bahan ini sangat mudah larut dalam dalam etil asetat,
metil etil keton, minyak mineral, eter, kloroform, dan toluena, larut dalam
isopropil miristat, sedikit larut dalam etanol, praktis tidak larut dalam gliserin,
propilenglikol dan air. Konsentrasi yang biasa digunakan untuk emolien adalah
10-30%.
2. Vaselin Album
Vaselin mempunyai masa yang lunak, lengket, bening, putih, sifat vaselin
ini tetap setelah zat dileburkan dan didiamkan hingga dingin tanpa diaduk.
kloroform, eter, dan eter minyak tanah. Vaselin sering digunakan sebagai
emollien.
3. Lanolin anhidrat
Lanolin digunakan sebagai bahan pengemulsi yang biasanya digunakan
dalam formulasi farmasi topikal dan kosmetik. Lanolin juga dapat digunakan
sebagai hydrophobic vehicle dalam pembuatan krim air dalam minyak dan salep.
Lanolin berwarna kuning pucat, mempunyai rasa yang manis, dan berbentuk lilin
dengan bau khas yang lemah, lanolin yang dicairkan berupa cairan jernih atau
hampir jernih, cairan kuning. Bahan ini sangat mudah larut dalam benzen,
kloroform, eter, dan minyak bumi (petrolatum), sedikit larut dalam etanol dingin
(95%), lebih mudah larut dalam etanol mendidih (95%), praktis tidak larut dalam
air.
c. Bahan Humektan
1. Propilenglikol
Selain sebagai humektan, propilen glikol biasa digunakan sebagai pelarut
untuk ekstrak dan juga pengawet pada berbagai formulasi kosmetik.Bahan ini
nontoksik dan sedikit mengiritasi.Propilen glikol merupakan larutan jernih, tidak
berwarna, dan praktk tidak berbau.Propilen glikol pada sediaan topikal biasa
digunakan sebagai humektan dengan konsentrasi hingga 15%.
2. Gliserin
Dalam formuasi sediaan topikal dan kosmetik, gliserin biasa digunakan sebagai
humektan dan emolien. Gliserin merupakan larutan jernih, tidak berwarna, tidak
berbau, kental, dan higroskopis. Bahan ini sedikit larut dalam aseton, praktis tidak
larut dalam benzene, kloroform, dan minyak, dapat bercampur dengan etanol,
metanol, dan air. Konsentrasi gliserin yang biasa digunakan sebagai humektan
bisa digunakan kurang dari 30% (Wade, & Weller, 1994).
d. Bahan pengental (Stiffening agent)
1. Asam Stearate
Asam stearat biasa digunakan dalam formulasi sediaan oral dan topikal. Dalam
solubilizing agent. Asam stearat merupakan bubuk putih keras, berwarna putih
atau agak kuning, sedikit mengkilap, kristal padat putih atau kekuningan. Bahan
ini sangat larut dalam benzene, kloroform, eter, dan larut dalam etanol (95%),
heksana, dan propilenglikol, praktis tidak larut dalam air. Konsentrasi asam
stearatyang biasa digunakan sebagai solubilizing agent 1-20%.
e. Bahan pengawet
1. Metilparaben
Dalam formulasi farmasetika, produk makanan, dan terutama dalam
kosmetik biasanya digunakan metil paraben sebagai bahan pengawet, dengan
aktivitas paling efektif untuk jamur dan kapang. Metilparaben larut dalam air,
etanol 95%, eter (1:10), dan metanol. Bahan ini dapat digunakan tunggal maupun
kombinasi dengan jenis paraben lain. Efektifitas pangawet ini memili rentang pH
4-8. Dalam sediaan topikal, konsentrasi yang umum digunakan adalah 0,02-0,3%.
2. Propilparaben
Bahan pengawet propilparaben secara luas digunakan dalam kosmetik,
makanan, dan produk farmasetika. Aktivitas antimikroba ditunjukkan pada pH
antara 4-8. Propilparaben sangat efektif terhadap jamur dan kapang. Di samping
itu, propil paraben propil paraben lebih aktif terhadap bakteri gram positifdaripada
gram negatif. Penggunaan kombinasi paraben dapat meningkatkan aktifitas
antimikroba. Bahan ini sangat larut dalam aseton, ester dan minyak, mudah larut
dalam etanol dan metanol, sangatsedikit larut dalam air. Konsentrasi yang biasa
digunakan untuk sediaan topikal adalah 0.001-0.6 (Wade, & Weller, 1994).
f. Aquadest
Air murni yang diperoleh dengan cara penyulingan disebut aquadest. Air
murni ini dapat diperoleh dengan cara penyulingan, pertukaran ion, osmosis
terbalik, atau dengan cra yang cara yang sesuai. Air murni lebih bebas dari
kotoran maupun mikroba.Air murni digunkan dalam sediaan-sediaan yang
membutuhkan air, terkecuali untuk parenteral, aquadest tidak padat digunakan
2.12 Stabilitas Krim
Umumnya suatu emulsi diangkap tidak setabil secara fisika jika, fase
dalam atau fase terdispersi pada pendiaman cenderung untuk membentuk agregat
dari bulatan-bulatan, jika bulatan-bulata atau agregat dari agregat naik ke
permukaan atau turun kedasar emulsi tersebut akan membentuk suatu lapisan
bekat dari fase dalam, dan jika semua atau sebagian dari cairan fase dalam tidak
teremulsikan dan membentuk suatu lapisan yang berbeda pada permukaan atau
pada dasar emulsi, yang merupakan hasil dari bergabungnya bulatan-bulatan fase
dalam. Disamping itu suatu emulsi mungkin sangat dipegaruhi oleh kontaminasi
dan pertumbuhan mikroba (Ansel,.2005).
Ketidakstabilan fisika dari sediaan ditandai dengan adanya pemucatan
warna atau munculnya warna, timul bau, perubahan atau emisahan fase, pecahnya
emulsi, pengendapan suspensi atau caking, perubahan konsistensi, pertumbuhan
kristal, terbentuknya gas, dan perubahan fisik lainnya. Kestabilan dari emulsi
ditandai dengan tidak adanya penggabungan fase dalam, tidak adanya creaming,
dan memberikan penampilan, bau, warna dan fisik lainnyayang baik (Martin, et
al., 1983) Ketidakstabilan dalam emulsi farmasi dapat digolongkan sebagai
berikut :
a. Flokulasi dan creaming
‘Creaming’ merupakan pemisahan dari emulsi menjadi beberapa lapis cairan, dimana masing-masing lapis mengandung fase dispersi yang berbeda
(Anief., 1987). Creaming ke arah atas terjadi dalam suatu emulsi a/m atau m/a
yang tidak stabil dimana fase terdispersi mempunyai kerapatan lebih kecil
daripada kerapatan fase luar. Creaming ke arah bawah dalam emulsi yang tidak
stabil dimana kerapatan fase dalam lebih besar daripada kerapatan fase luar
(Ansel,.2005).
b. Koalesen dan pecahnya emulsi (crecking atau breaking)
Creaming adalah suatu proses yang bersifat dapat kembali, berbeda
dengan proses creaking (pecahnya emulsi) yang bersifat tidak dapat kembali
(Anief.,1987). Hal ini dikarenakan lapisan pelindung disekitar bulatan-bulatan
27 UIN Syarif Hidayatullah Jakarta BAB III
METODOLOGI PENELITIAN 3.1 Waktu dan Tempat Penelitian
3.1.1 Waktu Penelitian
Penelitian dilakukan mulai Maret 2014 hingga September 2014.
3.1.2 Tempat Penelitian
Untuk proses ekstraksi kulit buah manggis (Garcinia mangostana L.) dan
uji aktivitas dilakukan di laboratorium penelitian 1 sedangkan formulasi dilakukan
di laboratorium penelitian 2 Program Strudi Famasi Fakultas Kedokteran dan Ilmu
Kesehatan, Universitas Islam Negri Syarif Hidayatullah, Jakarta.
3.2 Bahan dan Alat 3.2.1 Bahan Penelitian
Ekstrak etanol 50% kulit buah manggis (Garcinia mangostana L.) yang
telah dikarakterisasi oleh Narulita (2014), Vitamin C, Lanolin anhidrat (Bratako),
Vaselin (Bratako), Asam stearat (Bratako), Dimeticon (Bratako), Gliserin
(Bratako), Span 60, Tween 80, Propilenglikol (Bratako), Metylparaben (Bratako),
Propylparaben (Bratako), DPPH (Sigma), Metanol P.A (Merck), aquadest.
3.2.2 Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah rotary evaporator
(EYELA digital water bath), gelas ukur 100 ml (Pyrex), batang pengaduk besar,
corong besar, erlenmeyer 500 ml (Schot Duran), spatula besar, botol maserasi,
cawan penguap besar, gelas kimia 100 ml (Pyrex), refrigerator (Panasonic),
corong buchner (Pyrex), neraca analitik digital (Wiggen Hauser), hot plate,
lumpag, alu, spektrofotometer UV-Vis (Hitachi), pH meter, erlenmayer 2000 ml
(Schot Duran), gelas ukur, pipet tetes, batang pengaduk, cawan penguap,
termometer, sentrifugator, vakum, kertas saring, Homogenizer, pH meter (Navi),
micropipet effendrof reference 100 L, 200 L, dan 1000 L, Viskometer
3.3 Prosedur Kerja
3.3.1 Uji Aktivitas Antioksidan Ekstrak Etanol 50% Kulit Buah Manggis (Garcinia mangsotana L.) (Sharon Nela, Aman Syariful, & Yuliet., 2013)
1) Pembuatan larutan DPPH (0,1 mM)
Ditimbang seksama lebih kurang 1,98 mg DPPH (BM 394,32). Lalu
dilarutkan dengan metanol pro analisis hingga 50 mL, kemudian
ditempatkan dalam botol gelap. Cukupkan pelarutnya hingga tanda batas
kemudian kocok hingga homogen
2) Pembuatan larutan blanko dan optimasi panjang gelombang DPPH Dipipet 2 mL larutan DPPH (0,1 mM) ke dalam tabung reaksi. Lalu
ditambahkan metanol sebanyak 2 ml. Dan homogenkan dengan vortex.
Mulut tabung ditutup dengan alumunium foil. kemudian diinkubasi dalam
ruangan gelap selama 30 menit (Molyneux, 2004). Tentukan spektrum
serapannya menggunakan spektrofotometer UV-Vis pada panjang
gelombang 400-800 nm dan tentukan pajang gelombang maksimumnya.
3) Pembuatan larutan vitamin C
Ditimbang vitamin C pro analisis sebanyak 1 mg. Dilarutkan dengan
metanol pro analisis, dimasukkan dalam labu ukur lalu ditambahkan
metanol pro analisis hingga 10 ml (100 g/mL). Selanjutnya dibuat seri
konsentrasi 2,5; 5; 7,5; 10 dan 12,5 g/mL.
Pada masing-masing konsentrasi dimasukkan dalam labu ukur dan
ditambanhkan metanol p.a hingga tanda batas. Masing masing larutan uji
di pipet sebanyak 2 mL, dimasukkan ke dalam tabung reaksi, ditambahkan
DPPH 0,1mM sebanyak 2 mL, kemudian dikocok degan vortex hingga
homogen dan diinkubasi pada suhu kamar selama 30 menit. Selanjutnya
larutan uji diukur serapannya menggunakan alat spektrofotometer
UV-Vispada panjang gelombang 515,5 nm.
4) Pembuatan larutan uji ekstrak
Ditimbang lebih kurang 50 mg ekstrak, lalu dilarutkan dalam 50 ml
metanol pro analisis (konsentrasi 1000 g/mL), larutan ini merupakan
15g/mL. Dari beberapa konsentrasi tadi kemudian dipipet sebanyak 2 ml
kedalam tabung reaksi, didalam masing-masing tabung reaksi ditambahkan
larutan DPPH (0,1 mM) dengan rasio 1:1 kemudian tunggu 30 menit pada
suhu ruang (25oC). Selanjurnya diukur dengan menggunakan spekrofotometri UV-Vis pada panjang gelombang 515,5 nm.
3.3.2 Formulasi Krim (Fatmawaty, at al, 2012)
Tabel 1. Formulasi Krim Anti-aging Ekstral Etanol 50% Kulit Buah Manggis