SINTESIS PARFUM 1-FENIL-1,3-BUTANADION
DARI ASETOFENON DAN ETIL ASETAT SERTA
ANALISISNYA DENGAN GCMS
SKRIPSI
OLEH:
HERLINA JULIANA SINAGA
NIM 081501026
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
SINTESIS PARFUM 1-FENIL-1,3-BUTANADION DARI
ASETOFENON DAN ETIL ASETAT SERTA
ANALISISNYA DENGAN GCMS
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
HERLINA JULIANA SINAGA
NIM 081501026
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
SINTESIS PARFUM 1-FENIL-1,3-BUTANADION DARI
ASETOFENON DAN ETIL ASETAT SERTA
ANALISISNYA DENGAN GCMS
OLEH:
HERLINA JULIANA SINAGA
NIM 081501026
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : Oktober 2012
Pembimbing I, Panitia Penguji,
Drs. Ismail, M.Si., Apt. Dr. Ginda Haro, M.Sc., Apt. NIP 195006141980031001 NIP 195108161980031002
Pembimbing II, Drs. Ismail, M.Si., Apt. NIP 195006141980031001
Drs. Syahrial Yoenoes, SU., Apt. Dra. Masria Lasma Tambunan, M.Si., Apt. NIP 195112061983031001 NIP 195005081977022001
Dra. Saleha Salbi, M.Si., Apt. NIP 194909061980032001
Medan, Oktober 2012 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan
rahmat, kasih dan karunia-Nya, sehingga penulis dapat menyelesaikan skripsi ini
yang berjudul ”Sintesis Parfum 1-Fenil-1,3-Butanadion Dari Asetofenon Dan Etil
Asetat Serta Analisisnya Dengan GCMS”. Skripsi ini diajukan sebagai salah satu
syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas
Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih yang tulus dan
ikhlas kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan
Fakultas Farmasi USU Medan yang telah memberikan fasilitas sehingga penulis
dapat menyelesaikan pendidikan. Bapak Drs. Ismail, M.Si., Apt., dan Bapak Drs.
Syahrial Yoenoes, SU., Apt., selaku pembimbing yang telah memberikan waktu,
bimbingan, dan nasehat selama penelitian hingga selesainya penyusunan skripsi
ini serta kepada Ibu Dr. Marline Nainggolan, M.S., Apt., selaku penasehat
akademis yang telah memberikan bimbingan kepada penulis. Bapak Dr. Ginda
Haro, M.Sc., Apt., Ibu Dra. Saleha Salbi, M.Si., Apt., dan Ibu Masria Lasma
Tambunan, M.Si., Apt., selaku dosen penguji yang telah memberikan saran dan
arahan kepada penulis dalam menyelesaikan skripsi ini. Kepada Bapak dan Ibu
staf pengajar Fakultas Farmasi USU yang telah mendidik selama perkuliahan serta
Bapak kepala Laboratorium Sintesa Obat, Kimia Anorganik dan Penelitian yang
telah memberikan bantuan dan fasilitas selama penulis melakukan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada
terhingga kepada Ibunda tercinta, S. boru Purba, yang tiada hentinya berkorban
adikku yang selalu setia memberi doa, dukungan dan motivasi selama melakukan
penelitian.
Penulis menyadari skripsi ini masih belum sempurna, oleh karena itu
diharapkan kritik dan saran yang membangun untuk penyempurnaannya. Harapan
saya semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan kefarmasian.
Medan, Oktober 2012
Penulis
Herlina Juliana Sinaga
SINTESIS PARFUM 1-FENIL-1,3-BUTANADION DARI ASETOFENON DAN ETIL ASETAT SERTA ANALISISNYA DENGAN GCMS
ABSTRAK
Parfum adalah campuran senyawa yang dibuat untuk digunakan berbagai keperluan. Parfum ini dibuat dari ribuan senyawa yang kebanyakan dibuat melalui proses kimia. Senyawa parfum 1-fenil-1,3-butanadione yang mepunyai bau balsamik, yaitu parfum yang besar dan bertahan dapat didiskoneksi jadi enolat keton dan suatu ester. Reaksi dapat dilaksanakan dengan mengkombinasikan keton dengan ester dan basa yang cukup kuat. Reaksi ini dapat berlangsung melalui reaksi kondensasi karbonil yang melibatkan kombinasi dari substitusi-α
dan adisi nukleofilik.
Katalis yang digunakan adalah NaOH-etanol dan natrium etanolat. Penelitian ini dilakukan dalam 4 jenis perlakuan. Pertama, NaOH-etanol dimasukkan ke dalam campuran 24 ml asetofenon dan 20 ml etil asetat kemudian dikocok. Kedua, 13,5 g natrium etanolat dimasukkan ke dalam campuran 24 ml asetofenon dan 20 ml etil asetat, direfluks pada suhu 78oC lalu diekstraksi dengan 6 ml HCl 1N dan 15 ml akuades sehingga diperoleh larutan berwarna coklat. Ketiga, 13,5 g natrium etanolat dimasukkan ke dalam campuran 24 ml asetofenon dan 20 ml etil asetat, dihomogenkan campuran, lalu diekstraksi dengan 6 ml HCl 1N dan 15 ml akuades sehingga diperoleh larutan berwarna kuning. Keempat, 7,5 g natrium etanolat dimasukkan ke dalam campuran 24 ml asetofenon dan 20 ml etil asetat, dihomogenkan campuran, lalu diekstraksi dengan 6 ml HCl 1N dan 15 ml akuades sehingga diperoleh larutan berwarna kuning. Kemudian dilakukan penentuan titik didih senyawa hasil sintesis.
Hasil menunjukkan bahwa perlakuan pertama dan kedua tidak terjadi reaksi kondensasi karbonil. Sedangkan pada perlakuan ketiga dan keempat terjadi kondensasi karbonil dimana diperoleh 1-fenil-1,3-butanadion sebagai hasil sintesisnya. Hal ini dibuktikan dari hasil analisis dengan menggunakan GCMS dan dari penentuan titik didih hasil sintesis.
SYNTHESIS PERFUME 1-PHENYL-1,3-BUTANADIONE FROM ACETOPHENONE AND ETHYL ACETATE WITH ANALIZED BY
GCMS
ABSTRACT
Perfumes are mixtures created for use in a wide variety of applications. They are created from a palette of several thousand materials, most of which are manufactured by chemical processing methods. Perfume, 1-phenyl-1,3-butanadione having balsamic odor could occurred disconnection from ketone and ester. The reaction can be carried out by combining esters and ketones with a strong base. his reaction can take place through the carbonyl condensation reactions involving the combination ofα-substitution and nucleophilic addition.
The catalyst used is NaOH-ethanol and sodium ethoxide. The research was done in 4 different types of catalysts. First, the NaOH-ethanol was incorporated into the mixture of 24 ml acetophenone and 20 ml of ethyl acetate and then was shuffled. Second, 13.5 g of sodium ethoxide was incorporated into the mixture of 24 ml acetophenone and 20 ml of ethyl acetate, was refluxed at a temperature of 78oC and then was extracted with 6 ml 1N HCl and 15 ml of aquadest, and showed a brown solution. Third, 13.5 g of sodium ethoxide was incorporated into the mixture of 24 ml acetophenone and 20 ml of ethyl acetate, homogenized, then extracted with 6 ml 1N HCl and 15 ml of aquadest, and showed a yellow solution. Fourth, 7.5 g of sodium ethoxide was incorporated into the mixture of 24 ml acetophenone and 20 ml of ethyl acetate, homogenized, then extracted with 6 ml 1N HCl and 15 ml of aquadest, showed a yellow solution. After awards, boiling point was determined.
The results showed that there was not carbonyl condensation reactions at the first and the second. While, it was occurred at the third and fourth which produced 1-phenyl-1,3-butanedione. It was proved by the analyzed using GCMS and by the determined of its boiling point.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Rancangan Analisis ... 5
2.2 Elektronegativitas dan Polaritas ... 8
2.3 Elektofilik dan nukleofilik ... 9
2.4 Karbokation dan Karbanion ... 9
2.6 Sintesis Organik ... 10
2.7 Reaksi Umum dari Senyawa Karbonil ... 11
2.8 Reaksi adisi nukleofilik ... 11
2.9 Spektrometri Massa ... 13
BAB III METODE PENELITIAN ... 15
3.1 Alat dan Bahan ... 15
3.1.1 Alat ... 15
3.1.2 Bahan ... 15
3.2 Penyiapan Bahan dan Pereaksi ... 16
3.2.1 Penyiapan bahan ... 16
3.2.2 Pembuatan pereaksi ... 16
3.2.2.1 Larutan asam klorida (HCl) 1 N ... 16
3.3 Prosedur ... 16
3.3.1 Prosedur pembuatandry ethanol ... 16
3.3.2 Pembuatan natrium etanolat ... 17
3.3.3 Sintesis Parfum ... 17
3.3.3.1 Dengan katalis NaOH - etanol ... 17
3.3.3.2 Dengan katalis natrium etanolat dibantu dengan pemanasan ... 17
3.3.3.3 Dengan katalis natrium etanolat tanpa bantuan pemanasan ... 18
3.3.4 Elusidasi struktur senyawa hasil sintesis ... 19
3.3.5 Penentuan titik didih hasil sintesis ... 19
BAB IV HASIL DAN PEMBAHASAN ... 21
4.1.1 Hasil analisis sintesis dengan katalis
NaOH-etanol ... 21
4.1.2 Hasil analisis sintesis dengan katalis natrium etanolat dibantu pemanasan ... 21
4.1.3 Hasil analisis sintesis dengan katalis natrium etanolat tanpa bantuan pemanasan ... 33
4.1.4 Penentuan titik didih senyawa hasil sintesis ... 40
BAB V KESIMPULAN DAN SARAN ... 42
5.1 Kesimpulan ... 42
5.2 Saran ... 42
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Tabel Halaman
DAFTAR GAMBAR
Gambar Halaman
2.1 Sinton dan senyawa sinton ... 5
2.2 Retrosintetik parfum ... 7
2.3 Mekanisme reaksi sintesis parfum ... 8
2.4 Rumus umum senyawa karbonil ... 11
2.5 Rumus umum senyawa aldehid dan keton ... 11
2.6 Reaksi adisi nukleofilik ... 13
4.1 Kromatogram larutan hasil sintesis dengan bantuan pemanasan ... 22
4.2 Spektrum massapeakpertama ... 23
4.3 Spektrum massa senyawa hasil sintesis dengan bantuan pemanasan (1,3-difenil-2-buten-1-one) ... 24
4.4 Mekanisme reaksi autokondensasi ... 25
4.5 Fragmentasi senyawa 1,3-difenil-2-buten-1-one ... 27
4.6 Spektrum massapeakkedua ... 29
4.7 Spektrum massa senyawa hasil sintesis dengan bantuan pemanasan (3-metil,1-fenil, 1-butanone) ... 30
4.8 Mekanisme reaksi kondensasi berlanjut ... 31
4.9 Fragmentasi senyawa 1-metil-1-fenil-1-butanone ... 32
4.10 Kromatogram larutan hasil sintesis tanpa bantuan pemanasan .... 34
4.11 Spektrum massa larutan hasil sintesis tanpa bantuan pemanasan ... 35
4.12 Spektrum massa senyawa hasil sintesis dengan bantuan pemanasan (1-fenil-1,-butanadione) ... 36
DAFTAR LAMPIRAN
Lampiran Halaman
1 Flowsheet pembuatandry ethanol ... 45
2 Flowsheet pembuatan natrium etanolat ... 46
3 Flowsheet sintesis parfum ... 47
4 Flowsheet penentuan titik didih hasil sintesis ... 50
5 Kromatogram hasil sintesis ... 51
6 Spektrum massa hasil sintesis ... 53
7 Perhitungan statistik titik didih senyawa hasil sintesis ... 55
8 Daftar Tabel t ... 58
9 Gambar alat yang digunakan ... 59
10 Rangkaian alat pembuatan natrium etanolat ... 60
11 Rangkaian alat penentuan titik didih ... 61
SINTESIS PARFUM 1-FENIL-1,3-BUTANADION DARI ASETOFENON DAN ETIL ASETAT SERTA ANALISISNYA DENGAN GCMS
ABSTRAK
Parfum adalah campuran senyawa yang dibuat untuk digunakan berbagai keperluan. Parfum ini dibuat dari ribuan senyawa yang kebanyakan dibuat melalui proses kimia. Senyawa parfum 1-fenil-1,3-butanadione yang mepunyai bau balsamik, yaitu parfum yang besar dan bertahan dapat didiskoneksi jadi enolat keton dan suatu ester. Reaksi dapat dilaksanakan dengan mengkombinasikan keton dengan ester dan basa yang cukup kuat. Reaksi ini dapat berlangsung melalui reaksi kondensasi karbonil yang melibatkan kombinasi dari substitusi-α
dan adisi nukleofilik.
Katalis yang digunakan adalah NaOH-etanol dan natrium etanolat. Penelitian ini dilakukan dalam 4 jenis perlakuan. Pertama, NaOH-etanol dimasukkan ke dalam campuran 24 ml asetofenon dan 20 ml etil asetat kemudian dikocok. Kedua, 13,5 g natrium etanolat dimasukkan ke dalam campuran 24 ml asetofenon dan 20 ml etil asetat, direfluks pada suhu 78oC lalu diekstraksi dengan 6 ml HCl 1N dan 15 ml akuades sehingga diperoleh larutan berwarna coklat. Ketiga, 13,5 g natrium etanolat dimasukkan ke dalam campuran 24 ml asetofenon dan 20 ml etil asetat, dihomogenkan campuran, lalu diekstraksi dengan 6 ml HCl 1N dan 15 ml akuades sehingga diperoleh larutan berwarna kuning. Keempat, 7,5 g natrium etanolat dimasukkan ke dalam campuran 24 ml asetofenon dan 20 ml etil asetat, dihomogenkan campuran, lalu diekstraksi dengan 6 ml HCl 1N dan 15 ml akuades sehingga diperoleh larutan berwarna kuning. Kemudian dilakukan penentuan titik didih senyawa hasil sintesis.
Hasil menunjukkan bahwa perlakuan pertama dan kedua tidak terjadi reaksi kondensasi karbonil. Sedangkan pada perlakuan ketiga dan keempat terjadi kondensasi karbonil dimana diperoleh 1-fenil-1,3-butanadion sebagai hasil sintesisnya. Hal ini dibuktikan dari hasil analisis dengan menggunakan GCMS dan dari penentuan titik didih hasil sintesis.
SYNTHESIS PERFUME 1-PHENYL-1,3-BUTANADIONE FROM ACETOPHENONE AND ETHYL ACETATE WITH ANALIZED BY
GCMS
ABSTRACT
Perfumes are mixtures created for use in a wide variety of applications. They are created from a palette of several thousand materials, most of which are manufactured by chemical processing methods. Perfume, 1-phenyl-1,3-butanadione having balsamic odor could occurred disconnection from ketone and ester. The reaction can be carried out by combining esters and ketones with a strong base. his reaction can take place through the carbonyl condensation reactions involving the combination ofα-substitution and nucleophilic addition.
The catalyst used is NaOH-ethanol and sodium ethoxide. The research was done in 4 different types of catalysts. First, the NaOH-ethanol was incorporated into the mixture of 24 ml acetophenone and 20 ml of ethyl acetate and then was shuffled. Second, 13.5 g of sodium ethoxide was incorporated into the mixture of 24 ml acetophenone and 20 ml of ethyl acetate, was refluxed at a temperature of 78oC and then was extracted with 6 ml 1N HCl and 15 ml of aquadest, and showed a brown solution. Third, 13.5 g of sodium ethoxide was incorporated into the mixture of 24 ml acetophenone and 20 ml of ethyl acetate, homogenized, then extracted with 6 ml 1N HCl and 15 ml of aquadest, and showed a yellow solution. Fourth, 7.5 g of sodium ethoxide was incorporated into the mixture of 24 ml acetophenone and 20 ml of ethyl acetate, homogenized, then extracted with 6 ml 1N HCl and 15 ml of aquadest, showed a yellow solution. After awards, boiling point was determined.
The results showed that there was not carbonyl condensation reactions at the first and the second. While, it was occurred at the third and fourth which produced 1-phenyl-1,3-butanedione. It was proved by the analyzed using GCMS and by the determined of its boiling point.
BAB I PENDAHULUAN
1.1 Latar Belakang
Parfum adalah campuran senyawa yang dibuat untuk digunakan berbagai
keperluan. Parfum ini dibuat dari ribuan senyawa yang kebanyakan dibuat melalui
proses kimia. Sampai abad ke-19, parfum diperoleh dari bahan alami. Peningkatan
penggunaan parfum menyebabkan tidak memungkinkan pembuatan parfum tanpa
proses kimia (Berger, 2007).
Sejarah parfum selalu ditandai dengan adanya perubahan atau evolusi.
Perancang parfum akan selalu mempelajari parfum yang dikaguminya dan
mengembangkannya, mengganti komponen strukturnya yang mengarah kepada
senyawa baru, dan menghasilkan nuansa baru. Inti dari proses ini adalah
ketersediaanmaster formula, kemudian memodifikasinya sehingga menghasilkan
senyawa parfum yang baru (Calkin dan Jellinek, 1994).
Senyawa parfum 1-fenil-1,3-butanadione yang mepunyai bau balsamik,
yaitu parfum yang besar dan bertahan dapat didiskoneksi jadi enolat keton dan
suatu ester. Reaksi dapat dilaksanakan dengan mengkombinasikan keton dengan
ester dan basa yang cukup kuat. Reaksi ini dapat berlangsung melalui reaksi
kondensasi karbonil yang melibatkan kombinasi dari substitusi-α dan adisi
nukleofilik (Warren, 1982).
Salah satu contoh senyawa dari golongan keton adalah asetofenon.
tidak berwarna, berupa larutan dan digunakan sebagai prekursor dalam pembuatan
resin dan parfum (Windholz, et al., 1983).
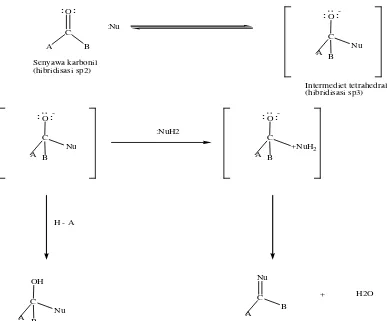
Reaksi kondensasi karbonil terjadi antara dua senyawa karbonil dan
melibatkan kombinasi dari substitusi-α dan adisi nukleofilik. Salah satu dari
senyawa karbonil akan mengalami pergantian menjadi ion enolat nukleofil yang
kemudian akan ditambahkan dengan senyawa karbonil kedua yang bertindak
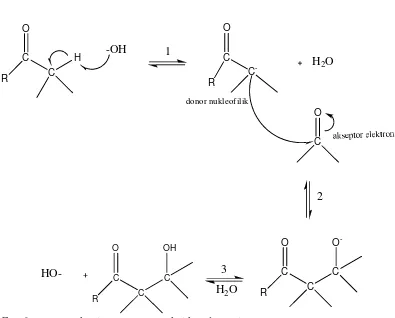
sebagai elektrofil. Mekanisme umum dari reaksi di atas ditunjukkan pada Gambar
1.1.
Gambar 1.1Mekanisme umum reaksi kondensasi (McMurry, 2007). Keterangan:
1. Senyawa karbonil dengan atom Cα yang diubah oleh basa menjadi ion enolat
2. Ion enolat ini bertindak sebagai donor nukleofilik dan direaksikan dengan senyawa karbonil yang bertindak sebagai akseptor elektron
Atas pertimbangan tersebut, penulis tertarik untuk melakukan penelitian
sintesis parfum. Parfum dibuat dari senyawa asetofenon dan etil asetat, dimana
kedua senyawa ini merupakan golongan senyawa karbonil yang dapat mengalami
reaksi kondensasi sehingga menghasilkan senyawa parfum.
1.2 Perumusan Masalah
Berdasarkan latar belakang di atas, maka perumusan masalah pada
penelitian ini adalah:
1. Apakah hasil reaksi kondensasi karbonil antara senyawa asetofenon dan etil
asetat?
2. Apakah sintesis dapat berlangsung dengan penggunan jenis katalis yang
berbeda?
3. Adakah perbedaan hasil reaksi yang diperoleh dengan penggunaan jumlah
katalis yang berbeda?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis pada penelitian
ini adalah:
1. Hasil reaksi kondensasi karbonil dari asetofenon dan etil asetat adalah
1-fenil-1,3-butanadion.
2. Sintesis dapat berlangsung dengan penggunaan jenis katalis yang berbeda.
3. Ada perbedaan hasil reaksi yang diperoleh dengan penggunaan jumlah katalis
1.4 Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah:
1. Untuk mengetahui hasil reaksi kondensasi dari asetofenon dan etil asetat
dengan bantuan katalis natrium etanolat.
2. Untuk mengetahui perbedaan hasil reaksi yang terjadi dengan penggunaan
katalis yang berbeda.
3. Untuk mengetahui hasil reaksi yang diperoleh dengan penggunaan jumlah
katalis yang berbeda.
1.5 Manfaat Penelitian
Diharapkan penelitian ini dapat:
1. Memberikan informasi tentang sintesis parfum 1-fenil-1,3-butanadion.
2. Memberikan informasi tentang reaksi kondensasi karbonil pada senyawa
BAB II
TINJAUAN PUSTAKA
2.1 Rancangan Analisis
Dalam sintesis suatu senyawa kimia atau senyawa obat yang baik,
diperlukan beberapa persiapan. Persiapan tersebut antara lain berupa bahan dasar
sintesis, pereaksi, pengertian yang mendalam mengenai mekanisme reaksi yang
akan berlangsung selama sintesis, serta alat-alat yang diperlukan untuk sintesis.
Untuk dapat memperoleh hasil sintesis yang baik serta hasil sampingan sedikit
mungkin sehingga memudahkan pada waktu pemurnian perlu dipakai bahan dasar
sintesis yang tepat, mudah didapat, maka diperlukan suatu rancangan atau pola
analisis, yang dikenal dengan nama analisis desain. Rancangan atau pola analisis
ini didasarkan pada pemecahan bagian-bagian tertentu dari senyawa yang
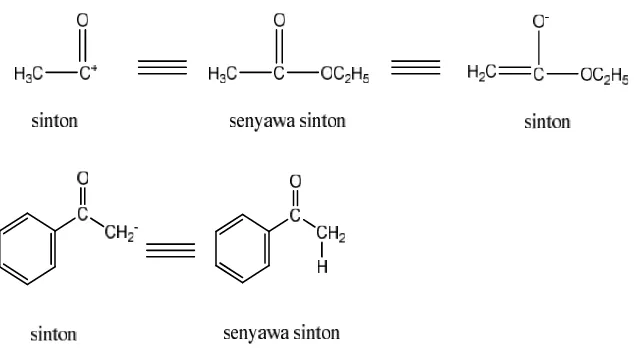
disintesis menjadi bagian yang lebih kecil yang disebut sinton. Sehingga senyawa
yang lebih kecil hasil pemecahan senyawa yang disintesis disebut senyawa sinton.
Sinton dan senyawa sinton seperti Gambar 2.1.
Senyawa sinton hasil pemecahan ini mungkin masih belum sederhana atau
belum terdapat dalam laboratorium maupun belum diperdagangkan. Kalapun ada,
harganya sangat mahal, maka perlu diadakan pemecahan lebih lanjut sehingga
didapatkan senyawa sinton yang lebih sederhana dan mudah didapat. Karena
rancangan atau pola analisis ini berdasarkan pemecahan senyawa besar menjadi
senyawa sinton yang lebih kecil, maka cara analisis ini dikenal dengan nama
diskoneksi. Tanda atau simbol dilakukannya diskoneksi adalah . Untuk
dapat mengadakan diskoneksi sehingga mendapatkan bahan-bahan dasar yang
tepat di atas, serta pereaksi yang tepat untuk katalisator, diperlukan pendalaman
mekanisme reaksi kimia, sehingga dalam sintesis senyawa kimia atau obat, setelah
didapatkan bahan dasar atau senyawa sinton, perlu diadakan penulisan kembali
mekanisme reaksi pembentukan senyawa yang akan disintesis, untuk mengetahui
suasana selama sintesis, reagen-reagen dan alat-alat yang diperlukan (Warren,
1981).
Retrosintetik adalah proses pembelahan molekul target ke dalam bahan
awal. Proses ini dapat terjadi melaui 2 cara, yaitu melalui proses Interkonversi
Gugus Fungsional (IGF) dan diskoneksi. Diskoneksi adalah proses analisis, yaitu
pemecahan sebuah ikatan dan mengkonversikannya menjadi sebuah molekul yang
dapat digunakan sebagai bahan awal. Diskoneksi ini adalah kebalikan dari
mekanisme reaksi. Interkonversi gugus fungsi adalah proses pengubahan suatu
gugus fungsional kedalam gugus yang lain dengan substitusi, eliminasi, oksidasi
dan reduksi serta operasi balik yang digunakan dalam analisis. Sinton adalah
fragmen ideal, biasanya suatu kation atau anion, akibat suatu diskoneksi. Reagen
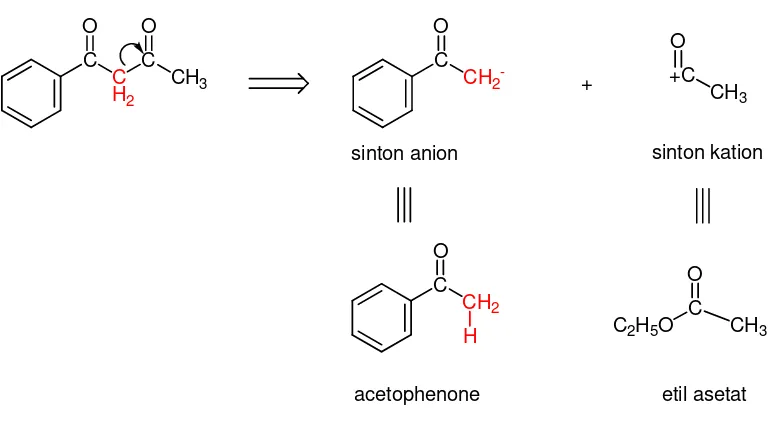
Parfum disintesis berdasarkan analisis retrosintetik terhadap senyawa
1-fenil-1,3-butanadione yaitu melalui pendekatan diskoneksi. Retrosintetik senyawa
parfum dapat dilihat pada Gambar 2.2.
C
sinton anion sinton kation
C
Gambar 2.2Retrosintetik parfum
Dari analisis retrosintetik tersebut diperoleh starting material berupa
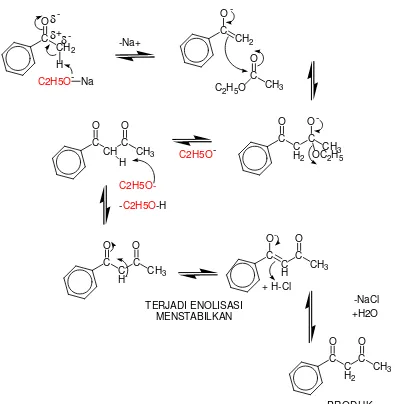
asetofenon dan etil asetat. Maka, dapat dibuat mekanisme reaksi pembentukan
C
Gambar 2.3Mekanisme reaksi sintesis parfum 2.2 Elektronegativitas dan Polaritas
Kebanyakan reaksi organik tergantung pada interaksi molekul yang
mempunyai muatan fraksi positif dengan molekul yang mempunyai muatan fraksi
negatif. Dalam senyawa organik netral (tanpa muatan), keberadaan muatan dapat
terjadi akibat adanya perbedaan elektronegativitas. Nilai elektronegativitas
ditemukan oleh Linus Pauling. Semakin besar nilai elektronegativitas akan
Kemampuan suatu atom yang terikat dalam suatu molekul untuk menarik
elektron dinyatakan dalam aturan elektronegativitas. Dengan nilai
elektronegativitas yang tinggi, maka suatu atom akan semakin mudah untuk
menangkap elektron. Ikatan yang dibentuk oleh atom-atom yang mempunyai
keelektronegatifan yang berbeda disebut ikatan polar. Ikatan nonpolar dibentuk
oleh atom-atom yang mempunyai perbedaan elektronegativitas yang kecil atau
bahkan nol. Atom yang mempunyai keelektronegatifan yang lebih besar dalam
suatu ikatan kovalen akan bermuatan negatif, sedangkan atom yang lain
bermuatan positif (Meislich, et al., 1980).
2.3 Elektofilik dan nukleofilik
Secara umum reaksi terjadi pada gugus yang reaktif dari suatu molekul
atau ion. Gugus yang dimaksud dibagi dalam dua kategori. Yang pertama, gugus
yang mengandung banyak elektron. Hal ini bisa disebabkan oleh: (a) memiliki
pasangan elektron bebas (b) bermuatan parsial negatif pada ikatan polar (c)
memiliki elektron phi. Gugus yang kaya elektron bersifat nukleofilik disebut
nukleofil atau donor elektron. Yang kedua (a) kemampuan menarik elektron (b)
bermuatan parsial positif pada ikatan polar. Gugus yang kehilangan elektron
bersifat elekrofilik disebut elektrofil atau akseptor elektron (Meislich, et al.,
1980).
2.4 Karbokation dan Karbanion
Karbokation merupakan perantara pada beberapa jenis reaksi. Stablitas
karbokation tersier lebih besar daripada sekunder dan primer. Stabilitas dari
karbokation yang paling stabil dapat mengalami resonansi. Karbanion memiliki
menarik sebuah proton,maka secara langsung diubah menjadi konjugat asam.
Stabilitas karbanion berhubungan dengan kekuatan konjugat asam. Asam lemah
yang kekuatan basanya tinggi mempunyai stabilitas karbokation yang lemah.
Stabilitas yang dimaksud di sini adalah stabilitas ke arah elektron donor (March,
1992).
2.5 Reaksi Organik
Reaksi kimia organik dapat terjadi dalam dua cara, yaitu berdasarkan jenis
reaksi apa yang terjadi dan bagaimana reaksinya terjadi. Ada 4 jenis reaksi
organik: adisi, eliminasi, substitusi dan penataan ulang, reaksi oksidasi reduksi.
Reaksi adisi terjadi ketika dua reaktan dicampurkan bersama-sama unutk
membentuk produk tunggal tanpa ada hasil samping. Reaksi eliminasi adalah
kebalikan dari reaksi adisi. Eliminasi terjadi ketika reaktan tunggal dipecah
menjadi dua produk. Reaksi substitusi terjadi ketika dua reaktan berpindah posisi
untuk menghasilkan 2 produk baru. Reaksi penataan ulang terjadi ketika reaktan
tunggal mengalami perubahan ikatan untuk menghasilkan produk yang isomer
(McMurry, 1992).
2.6 Sintesis Organik
Sintesis senyawa organik dari prekursor sederhana di laboratorium dapat
terjadi karena beberapa alasan. Dalam industri farmasi, senyawa organik baru
dirancang dan kemudian disintesis dengan harapan akan menghasilkan sebagian
obat baru yang berguna. Dalam industri kimia, sintesis sering dilakukan untuk
2.7 Reaksi Umum dari Senyawa Karbonil
Aldehid keton, dan ester merupakan senyawa karbonil, yaitu senyawa
dimana atom karbon (C) membentuk ikatan rangkap dengan atom oksigen (O).
Rumus senyawa karbonil dapat dilihat pada Gambar 2.4.
Gambar 2.4Rumus umum senyawa karbonil
Senyawa karbonil pada golongan aldehid diikat oleh minimal satu atom H,
sedangkan pada golongan keton diikat oleh 2 atom karbon. Rumus umum untuk
senyawa golongan aldehid dan keton adalah dapat dilihat pada Gambar 2.5.
Gambar 2.5Rumus umum senyawa aldehid dan keton 2.8 Reaksi adisi nukleofilik
Nukleofil adalah spesies yang reaktif yang menyerang spesies yang
kekurangan elektron. Nukleofil ini memiliki atom dengan muatan parsial negatif
dan atom ini disebut sebagai atom nukleofilik. Spesies reaktif yang kekurangan
elektron disebut elektrofil. Elektrofil ini memiliki atom yang bermuatan parsial
positif (Miller dan Solomon, 1985).
R C O
R R C
O
H
C O
keton
Reaksi dari senyawa karbonil dapat terjadi dalam 4 mekanisme umum
yaiut adisi nukleofilik, substitusi asil nukleofilik, substitusi alfa, dan kondensasi
karbonil (McMurry, 1992).
Reaksi umum dari aldehid dan keton adalah reaksi adisi nukleofilik, di
mana nukleofil ditambahkan ke karbon elektrofil dari gugus karbonil. Karena
nukleofil menggunakan pasangan elektron bebas unutk membentuk ikatan karbon
baru, dua elektron dari ikatan rangkap karbon-oksigen harus berpindah ke atom
oksigen yang elektronegatifnya lebih besar, yang kemudian akan distabilkan oleh
anion alkoksida. Karbon karbonil akan terhibridisasi darisp2kesp3selama proses
berlangsung dan menghasilkan intermediet geometri tetrahedral. Setelah
terbentuk, intermediet tetrahedral dapat mengalami berbagai jenis reaksi.
Intermediet tetrahedral dapat terprotonasi oleh air atau asam untuk membentuk
alkohol, seperti pada reaksi adisi Grignard. Dan juga intermediet tetrahedral dapat
mengusir oksigen untuk membentuk ikatan rangkap antara senyawa karbonil.
Gambar 2.6Reaksi adisi nukleofilik (McMurry, 1992) 2.9 Spektrometri Massa
Spektrometri massa, salah satu aplikasi dari alat analisis, menyajikan
informasi kualitatif dan kuantitatif tentang atom atau komposisi molekular dari
senyawa organik ataupun anorganik. Spektrometer massa pertama kali digunakan
oleh Thompson pada tahun 1912 dan Aston tahun 1919. Spectrometer massa
menghasilkan data berupa muatan partikel yang terdiri dari fragmentasi ionik dari
molekul awal, dan urutan-urutannya berdasarkan perbandingan massanya
Keuntungan utama yang diperoleh dari spektrometri massa ini sebagai
teknik analisis adalah sensitivitas yang tinggi dibandingkan teknik analisis lain
dan spesifikasi dalam mengidentifikasi senyawa yang tidak diketahui (Silverstein,
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan meliputi pengumpulan bahan, pembuatan
katalis natrium etanolat, sintesis senyawa parfum, penentuan titik didih hasil
sintesis dan elusidasi struktur senyawa hasil sintesis dengan Kromatografi Gas
Spektroskopi Massa. Penelitian ini dilakukan di Laboratorium Sintesa Obat
Fakultas Farmasi USU. Elusidasi struktur senyawa dengan Kromatografi Gas
Spektroskopi Massa dilakukan di Laboratorium Penelitian Fakultas Farmasi USU.
3.1 Alat dan Bahan 3.1.1 Alat
Alat-alat yang digunakan pada penelitian ini adalah adaptor, alat-alat
gelas, botol timbang, hot plate stirer (Cimarec), indikator universal, labu alas
bulat, labu alas bulat berleher dua, labu alas bulat berleher tiga, neraca analitik
(Mettler AE 200), pendingin bola, pendingin liebig, pipa bengkok, termometer,
vial dan GCMS (GCMS-QP 2010,Gas Chromatograph Mass Spectrometer serial
No. O205046 Shimadzu, Laboratorium Penelitian Fakultas Farmasi Universitas
Sumatera Utara).
3.1.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini meliputi bahan-bahan
yang kecuali dinyatakan lain adalah berkualitas pro analisis, etanol, natrium sulfat
3.2 Penyiapan Bahan dan Pereaksi 3.2.1 Penyiapan bahan
Bahan yang digunakan dalam penelitian ini antara lain etanol absolut
(C2H5OH 99,7% v/v), natrium sulfat anhidrat (Na2SO4), logam Natrium (Na),
asetofenon (C8H8O), etil asetat for analysis (C4H8O2), asam klorida (HCl) 1N, dan
akuades.
3.2.2 Pembuatan pereaksi
3.2.2.1 Larutan asam klorida (HCl) 1 N
Sebanyak 8,3 ml asam klorida pekat diencerkan dengan air suling sampai
100 ml (Ditjen POM, 1979).
3.3 Prosedur
3.3.1 Prosedur pembuatandry ethanol
Ke dalam beaker glass dimasukkan sejumlah etanol p.a., kemudian
ditambahkan natrium sulfat anhidrat. Wadah ditutup dengan plastik dan karet
untuk menghindari kontak langsung dengan udara. Digoyang lalu didiamkan
selama 24 jam. Etanol dimasukkan ke dalam labu alat bulat berleher dua,
dirangkai alat destilasi, dihubungkan dengan gas N2 ultra high purity (UHP).
Kemudian etanol tersebut didestilasi pada suhu 78oC dimana pada saat proses
berlangsung, rangkaian alat destilasi dialiri dengan gas N2 UHP untuk
menghilangkan udara. Destilat yang diperoleh adalah dry ethanol (Singh, et al.,
3.3.2 Pembuatan natrium etanolat
Ke dalam labu alas bulat berleher tiga yang sudah dilengkapi dengan
magnetik bar dimasukkan dry ethanol hasil destilasi. Dirangkai alat refluks,
dihubungkan dengan gas N2 UHP. Dari salah satu leher labu, dimasukkan logam
Na secukupnya. Lalu magnetik bar diputar supaya logam Na terlarut. Proses ini
dibantu dengan pemanasan. Penambahan logam Na dilakukan sampai etanol
tersebut jenuh (logam Na sudah tidak larut lagi). Setelah reaksi selesai, labu alas
tersebut didinginkan, kemudian disimpan pada suhu dingin (Chandran, et al.,
2006).
3.3.3 Sintesis parfum
Prosedur sintesis parfum secara umum belum ada. Oleh karena itu, maka
sintesis parfum ini dilakukan berdasarkan analisis retrosintetik, kemudian
dirancang mekanisme reaksi sintesis. Dari hasil rancangan tersebut diperoleh
bahwa reaksi akan cepat berlangsung dengan adanya katalis basa. Oleh sebab itu,
digunakan dua jenis katalis untuk prosedur sintesis ini yaitu:
3.3.3.1 Dengan katalis NaOH-etanol
Ke dalam erlenmeyer dimasukkan sebanyak 12 ml etanol, kemudian
ditambahkan pellet NaOH, dikocok, kemudian dicek pH nya hingga diperoleh pH
13-14. Lalu dimasukkan ke dalam erlenmeyer yang telah berisi campuran 24 ml
asetofenon dan 20 ml etil asetat. Kemudian dikocok. Diamati perubahan yang
terjadi.
3.3.3.2 Dengan katalis natrium etanolat dibantu dengan pemanasan
Sebanyak 24 mL asetofenon dan 13,5 g natrium etanolat dimasukkan ke
suhu 78oC selama 10 menit, ditunggu hingga reaksi sempurna. Kemudian
ditambahkan 20 ml etil asetat, lalu direflus kembali selama 5 menit. Dari hasil ini
akan terlihat massa kental berwarna coklat. Hal ini menandakan bahwa sudah
terjadi reaksi. Magnetik bar dihentikan. Hasil sintesis dipindahkan ke dalam
corong pisah. Kemudian dimasukkan sebanyak 6 ml HCl 1N dan akuades 15 ml,
dikocok hingga sempurna. Didiamkan hingga terbentuk 2 lapisan yaitu lapisan
atas berwarna coklat dan lapisan bawah berwarna bening. Diambil lapisan atas
dan dimasukkan ke dalam corong pisah kembali. Dilakukan pencucian sebanyak 5
kali, yaitu dengan menambahkan sebanyak 15 ml akuades. Dikocok dan
didiamkan hingga memisah. Diambil lapisan atas. Diukur volume yang didapat
dan dimasukkan ke dalam vial.
3.3.3.3 Dengan katalis natrium etanolat tanpa bantuan pemanasan
Prosedur ini dilakukan dengan menggunakan jumlah katalis yang berbeda.
a. Sebanyak 24 ml asetofenon dan 20 ml etil asetat dimasukkan ke dalam labu
alas bulat yang telah dilengkapi dengan magnetik bar. Kemudian sebanyak
13,5 g natrium etanolat dimasukkan ke dalam campuran tersebut. Magnetik
bar diputar, ditunggu hingga reaksi sempurna. Dari hasil ini akan terlihat
massa kental berwarna kuning. Hal ini menandakan bahwa sudah terjadi
reaksi. Magnetik bar dihentikan. Hasil sintesis dipindahkan ke dalam corong
pisah. Kemudian dimasukkan sebanyak 6 ml HCl 1N dan akuades 15 ml,
dikocok hingga sempurna. Didiamkan hingga terbentuk 2 lapisan yaitu lapisan
atas berwarna kuning dan lapisan bawah berwarna bening. Diambil lapisan
atas dan dimasukkan ke dalam corong pisah kembali. Dilakukan pencucian
Dikocok dan didiamkan hingga memisah. Diambil lapisan atas. Diukur
volume yang didapat dan dimasukkan ke dalam vial.
b. Sebanyak 24 ml asetofenon dan 20 ml etil asetat dimasukkan ke dalam labu
alas bulat yang telah dilengkapi dengan magnetik bar. Kemudian sebanyak 7,5
g natrium etanolat dimasukkan ke dalam campuran tersebut. Magnetik bar
diputar, ditunggu hingga reaksi sempurna. Dari hasil ini akan terlihat massa
kental berwarna kuning. Hal ini menandakan bahwa sudah terjadi reaksi.
Magnetik bar dihentikan. Hasil sintesis dipindahkan ke dalam corong pisah.
Kemudian dimasukkan sebanyak 6 ml HCl 1N dan akuades 15 ml, dikocok
hingga sempurna. Didiamkan hingga terbentuk 2 lapisan yaitu lapisan atas
berwarna kuning dan lapisan bawah berwarna bening. Diambil lapisan atas
dan dimasukkan ke dalam corong pisah kembali. Dilakukan pencucian
sebanyak 5 kali, yaitu dengan menambahkan sebanyak 15 ml akuades.
Dikocok dan didiamkan hingga memisah. Diambil lapisan atas. Diukur
volume yang didapat dan dimasukkan ke dalam vial.
3.3.4 Elusidasi struktur senyawa hasil sintesis
Hasil sintesis dimasukkan ke dalam alat GCMS, kemudian diinjeksikan
larutan zat ke dalam kromatografi gas untuk menentukan berat molekul dan pola
fragmentasi senyawa (pengukuran dengan Kromatografi Gas Spektroskopi Massa
dikerjakan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera
Utara).
3.3.5 Penentuan titik didih hasil sintesis
Hasil sintesis dimasukkan ke dalam tabung reaksi sebanyak 4 ml,
dan baca suhu yang tertera pada termometer. Rangkaian alat dapat dilihat pada
Lampiran 11 halaman 61. Percobaan dilakukan sebanyak 6 kali (Reksohadiprodjo,
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Sintesis Parfum
Hasil sintesis parfum yaitu berupa larutan berwarna kuning jernih yang
tidak larut dalam air. Senyawa yang diinginkan dari hasil sintesis ini adalah
1-fenil-1,3-butanadion.
4.1.1 Hasil analisis sintesis dengan katalis NaOH-etanol
Pada saat penambahan NaOH-etanol ke dalam campuran asetofenon dan
etil asetat, tidak terjadi perubahan. Tetapi apabila didiamkan selama 24 jam
sambil dikocok sesekali, maka akan terbentuk larutan yang berwarna kuning.
Larutan kuning kemudian dipanaskan menghasilkan warna kuning
kecoklatan,tetapi tidak timbul endapan.
4.1.2 Hasil analisis sintesis dengan katalis natrium etanolat dibantu pemanasan
Hasil sintesis yang diperoleh yaitu berupa larutan berwarna coklat
sebanyak 32 ml, kemudian dielusidasi dengan Kromatografi Gas Spektroskopi
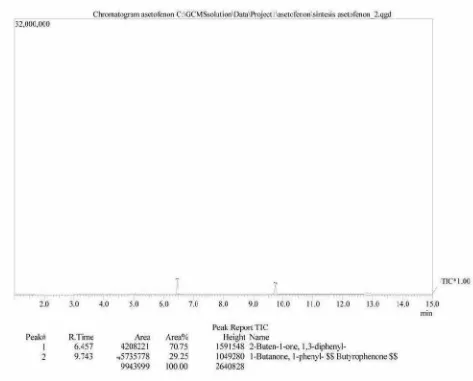
Gambar 4.1Kromatogram larutan hasil sintesis dengan bantuan pemanasan Dari gambar tersebut diperlihatkan bahwa ada 2 peak yang muncul.
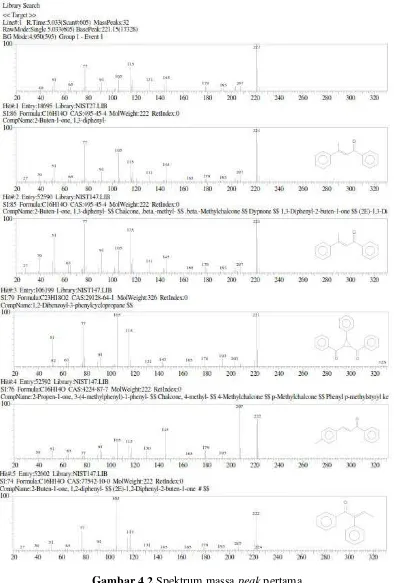
Analisis spektrum massa dilanjutkan terhadappeakpertama. Hasil yang diperoleh
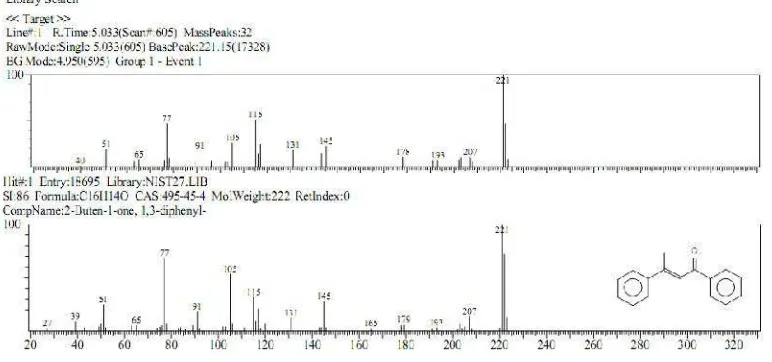
Setelah menganalisis hasil Spektroskopi Massa dari peak, maka
dimungkinkan senyawa yang muncul dari peak pertama tersebut adalah
1,3-difenil-2-buten-1-one. Spektrum massanya ditunjukkan pada Gambar 4.3.
Gambar 4.3 Spektrum massa senyawa hasil sintesis dengan bantuan pemanasan (1,3-difenil, 2-buten-1-one)
Senyawa ini dapat terjadi karena adanya proses autokondensasi
antarmolekul asetofenon. Autokondensasi ini terjadi akibat adanya proses
pemanasan pada saat sintesis parfum dilakukan. Pemanasan ini akan menghalangi
senyawa etil asetat untuk bergabung dengan asetofenon, sehingga proses
penggabungan (kondensasi) terjadi antara asetofenon dengan asetofenon.
Gambar 4.4Mekanisme reaksi autokondensasi (Miller, 1985)
Dari hasil analisis dengan kromatografi gas pada Gambar 4.1 didapat
puncak senyawa 1,3-difenil-2-buten-1-one dengan waktu retensi 6,457 menit.
Berat molekul senyawa pada spektroskopi massa adalah 221. Dari spektrum
massanya dapat di analisis fragmen-fragmen (sibir-sibir) baik yang muncul
C
m/z: 222.10 (100.0%), 223.11 (17.5%), 224.11 (1.6%) C, 86.45; H, 6.35; O, 7.20
m/z: 207.08 (100.0%), 208.08 (16.2%), 209.09 (1.5%) C, 86.93; H, 5.35; O, 7.72
CH3: Exact Mass: 15,02 Molecular Weight: 15,03 m/z: 15.02 (100.0%), 16.03 (1.1%)
C, 79.89; H, 20.11
m/z: 194.07 (100.0%), 195.08 (15.3%), 196.08 (1.3%) C, 86.57; H, 5.19; O, 8.24
m/z: 179.09 (100.0%), 180.09 (15.3%), 181.09 (1.1%) C, 93.81; H, 6.19 m/z: 49.01 (100.0%), 50.01
(4.3%) m/z: 27.99 (100.0%), 29.00 (1.1%)
C, 42.88; O, 57.12 m/z: 131.05 (100.0%), 132.05 (9.8%)
C, 82.42; H, 5.38; O, 12.20 ;;CH2
Exact Mass: 14.02 Molecular Weight: 14.03 m/z: 14.02 (100.0%), 15.02 (1.1%) C, 85.63; H, 14.37
Exact Mass: 64,03 Molecular Weight: 64,09 m/z: 64.03 (100.0%), 65.03 (5.4%) C, 93.71; H, 6.29 m/z: 115.05 (100.0%), 116.06 (9.8%)
C, 93.87; H, 6.13
C O
Exact Mass: 105,03 Molecular Weight: 105,11 m/z: 105.03 (100.0%), 106.04 (7.7%)
C, 79.98; H, 4.79; O, 15.22 m/z: 28.03 (100.0%), 29.03 (2.2%)
C, 85.63; H, 14.37
Exact Mass: 145.06 Molecular Weight: 145.18 m/z: 145.07 (100.0%), 146.07 (11.0%)
C, 82.73; H, 6.25; O, 11.02
HC CH
Gambar 4.5Fragmentasi senyawa 1,3-difenil-2-buten-1-one
Dari fragmentasi 1,3-difenil-2-buten-1-one hasil sintesis diatas dapat
diketahui rumus molekul yang muncul dan yang hilang, uraiannya sebagai
berikut:
1. Dari C16H14O BM 222,10 melepaskan CH3 BM 15,02 akan memunculkan
spektrum C15H11O BM 207,08. Kemudian melepaskan CO BM 27,99
memunculkan spektrum C14H11BM 179,09. Kemudian melepaskan C4H3 BM
64,03 menghasilkan C9H7BM 115,05
2. Dari C16H14O BM 222,10 melepaskan C2H4 BM 28,03 akan memunculkan
spektrum C14H10O BM 194,07. Kemudian melepaskan C4H BM 49,01
14,02 memunculkan spektrum C9H7O BM 131,05. Kemudian melepaskan
C2H2 BM 26,02 memunculkan spektrum C7H5O BM 105,03. Kemudian
melepaskan CH2 BM 14,02 memunculkan spektrum C6H3O BM 91,02.
Kemudian melepaskan CH2 BM 14,02 memunculkan spektrum C5HO BM
77,00. Kemudian melepaskan C BM 12,00 memunculkan spektrum C4HO BM
65,00. Kemudian melepaskan C BM 12,00 memunculkan spektrum C3HO BM
53,00.
Analisis spektrum massa dilanjutkan terhadap peak kedua. Hasil yang
Setelah menganalisis hasil Spektroskopi Massa dari peak, maka
dimungkinkan senyawa yang muncul dari peak kedua tersebut adalah
3-metil-1-fenil-1-butanone. Spektrum massanya ditunjukkan pada Gambar 4.7.
Gambar 4.7Spektrum massa senyawa hasil sintesis dengan bantuan pemanasan (3-metil-1-fenil-1-butanone)
Senyawa ini dapat terjadi karena adanya proses kondensasi berlanjut.
Kondensasi berlanjut ini terjadi akibat adanya pemanasan. Mekanisme kondensasi
Gambar 4.8Mekanisme reaksi kondensasi berlanjut
Dari hasil analisis dengan kromatografi gas pada Gambar 4.1 didapat
puncak senyawa 3-metil-1-fenil-1-butanone dengan waktu retensi 9,743 menit.
Berat molekul senyawa pada spektroskopi massa adalah 162. Dari spektrum
massanya dapat di analisis fragmen-fragmen (sibir-sibir) baik yang muncul
maupun yang hilang, pola fragmentasinya dapat dilihat pada Gambar 4.9.
C H2 dari sisa pembuatan C2H5ONa
C m/z: 162.10 (100.0%), 163.11 (12.1%)
C, 81.44; H, 8.70; O, 9.86 m/z: 15.02 (100.0%), 16.03 (1.1%)
C, 79.89; H, 20.11
Exact Mass: 147,08 Molecular Weight: 147,19 m/z: 147.08 (100.0%), 148.08 (10.8%)
C, 81.60; H, 7.53; O, 10.87 m/z: 129.07 (100.0%), 130.07 (10.8%)
C, 92.98; H, 7.02 m/z: 105.07 (100.0%), 106.07 (8.7%)
C, 91.37; H, 8.63
:C
C+
Exact Mass: 24,00 Molecular Weight: 24,02 m/z: 24.00 (100.0%), 25.00 (2.2%)
C, 100.00
CH2+
C+ H
Exact Mass: 91,05 Molecular Weight: 91,13 m/z: 91.05 (100.0%), 92.06 (7.7%)
C, 92.26; H, 7.74
C+
Exact Mass: 77,04 Molecular Weight: 77,10 m/z: 77.04 (100.0%), 78.04 (6.5%)
C, 93.46; H, 6.54
Exact Mass: 26,02 Molecular Weight: 26,04 m/z: 26.02 (100.0%), 27.02 (2.2%)
C, 92.26; H, 7.74
C+
Exact Mass: 51,02 Molecular Weight: 51,07 m/z: 51.02 (100.0%), 52.03
(4.4%) C, 94.08; H, 5.92 Exact Mass: 24,00
Molecular Weight: 24,02 m/z: 24.00 (100.0%), 25.00 (2.2%)
C, 100.00
H2C CH+
Exact Mass: 27,02 Molecular Weight: 27,04 m/z: 27.02 (100.0%), 28.03 (2.2%)
C, 88.82; H, 11.18 m/z: 41.04 (100.0%), 42.04 (3.2%)
C, 87.73; H, 12.27
:CH2
Exact Mass: 14,02 Molecular Weight: 14,03 m/z: 14,02 (100,0%), 15,02 (1,1%)
C, 85.63; H, 14.37 m/e: 36.00 (100.0%), 37.00 (3.3%)
C, 100.00
Dari fragmentasi 1-metil-1-fenil-1-butanone hasil sintesis diatas dapat
diketahui rumus molekul yang muncul dan yang hilang, uraiannya sebagai
berikut :
1. Dari C11H14O BM 162,10 melepaskan CH3 BM 15,02 akan memunculkan
spektrum C10H11O BM 147,08. Kemudian melepaskan H2O BM 20,16
memunculkan spektrum C10H9 BM 129,07. Kemudian melepaskan C2 BM
24,00 memunculkan spektrum C8H9 BM 105,07. Kemudian melepaskan CH2
BM 14,02 memunculkan spektrum C7H7 BM 91,05. Kemudian melepaskan
CH2 BM 14,02 memunculkan spektrum C6H5 BM 77,04. Kemudian
melepaskan C2H2 BM 26,02 memunculkan spektrum C4H3 BM 51,02.
Kemudian melepaskan C2BM 24,00 memunculkan spektrum C2H3BM 27,02.
2. Dari C11H14O BM 162,10 melepaskan CH3 BM 15,02 akan memunculkan
spektrum C10H11O BM 147,08. Kemudian melepaskan H2O BM 20,16
memunculkan spektrum C10H9 BM 129,07. Kemudian melepaskan C2 BM
24,00 memunculkan spektrum C8H9 BM 105,07. Kemudian melepaskan CH2
BM 14,02 memunculkan spektrum C7H7 BM 91,05. Kemudian melepaskan
CH2 BM 14,02 memunculkan spektrum C6H5 BM 77,04. Kemudian
melepaskan C3BM 36,00 memunculkan spektrum C3H5BM 41,04.
4.1.3 Hasil analisis sintesis dengan katalis natrium etanolat tanpa bantuan pemanasan
Hasil sintesis yang diperoleh yaitu berupa larutan berwarna kuning
sebanyak 30 ml, kemudian dielusidasi dengan kromatografi gas spektroskopi
Gambar 4.10Kromatogram larutan hasil sintesis tanpa bantuan pemanasan Dari gambar tersebut diperlihatkan bahwa ada peaktunggal yang muncul.
Analisis spektrum massa dilanjutkan terhadappeaktersebut. Hasil yang diperoleh
Setelah menganalisis hasil Spektroskopi Massa dari peak, maka
dimungkinkan senyawa yang muncul dari peak tersebut adalah
1-fenil-1,3-butanadione. Spektrum massanya ditunjukkan pada Gambar 4.12.
Gambar 4.12Spektrum massa senyawa hasil sintesis dengan bantuan pemanasan (1-fenil-1,-butannadione)
Dari hasil analisis dengan Kromatografi Gas pada Gambar 4.10 didapat
puncak senyawa 1-fenil-1,3-butanadion dengan waktu retensi 9,196 menit. Berat
molekul senyawa pada spektroskopi massa adalah 162. Dari spektrum massanya
dapat di analisis fragmen-fragmen (sibir-sibir) baik yang muncul maupun yang
Gambar 4.13Fragmentasi senyawa 1-fenil-1,3-butanadion
Dari fragmentasi 1-fenil-1,3-butanadion hasil sintesis diatas dapat
diketahui rumus molekul yang muncul dan yang hilang, uraiannya sebagai
berikut :
1. Dari C10H10O2 BM 162,07 melepaskan CH3 BM 15,02 akan memunculkan
2. Dari C10H10O2BM 162,07 melepaskan C2H2O BM 42,01 akan memunculkan
spektrum C8H8O BM 120,06. Kemudian melepaskan CH3 BM 15,02 akan
memunculkan spektrum C7H5O BM 105,03. Kemudian melepaskan H2O dan
H2BM 20,03 akan memunculkan spektrum C7H BM 85,01.
3. Dari C10H10O2BM 162,07 melepaskan C2H2O BM 42,01 akan memunculkan
spektrum C8H8O BM 120,06. Kemudian melepaskan CH3 BM 15,02 akan
memunculkan spektrum C7H5O BM 105,03. Kemudian melepaskan C2H4BM
28,03 akan memunculkan spektrum C5HO BM 77,00.
4. Dari C10H10O2BM 162,07 melepaskan C2H2O BM 42,01 akan memunculkan
spektrum C8H8O BM 120,06. Kemudian melepaskan CH3 BM 15,02 akan
memunculkan spektrum C7H5O BM 105,03. Kemudian melepaskan CO BM
27,99 akan memunculkan spektrum C6H5BM 77,04.
5. Dari C10H10O2BM 162,07 melepaskan C2H2O BM 42,01 akan memunculkan
spektrum C8H8O BM 120,06. Kemudian melepaskan CH3 BM 15,02 akan
memunculkan spektrum C7H5O BM 105,03. Kemudian melepaskan C2H4O
BM 66,01 akan memunculkan spektrum C3H3BM 39,02.
6. Dari C10H10O2BM 162,07 melepaskan C2H2O BM 42,01 akan memunculkan
spektrum C8H8O BM 120,06. Kemudian melepaskan CH3 BM 15,02 akan
memunculkan spektrum C7H5O BM 105,03. Kemudian melepaskan C5H2BM
62,02 akan memunculkan spektrum C2H3O BM 43,02.
7. Dari C10H10O2BM 162,07 melepaskan C2H2O BM 42,01 akan memunculkan
spektrum C8H8O BM 120,06. Kemudian melepaskan CH3 BM 15,02 akan
memunculkan spektrum C7H5O BM 105,03. Kemudian melepaskan C3H BM
8. Dari C10H10O2BM 162,07 melepaskan C2H2O BM 42,01 akan memunculkan
spektrum C8H8O BM 120,06. Kemudian melepaskan CH3 BM 15,02 akan
memunculkan spektrum C7H5O BM 105,03. Kemudian melepaskan C5H2O
BM 78,01 akan memunculkan spektrum C2H3BM 27,02.
4.1.4 Penentuan titik didih senyawa hasil sintesis
Sintesis dengan menggunakan jumlah katalis yang berbeda juga dapat
berlangsung. Hal ini disebabkan karena katalis hanya digunakan untuk
mempercepat reaksi. Karena hasil sintesis dengan menggunakan jumlah katalis
sebanyak 7,5 g tidak dielusidasi, maka dilakukan uji kemurnian terhadap senyawa
tersebut, yaitu dengan penentuan titik didih. Titik didih hasil sintesis adalah
260-262oC. Dari hasil percobaan sebanyak 6 kali, diperoleh data titik didih seperti
Tabel 4.1Titik didih bahan baku dan senyawa hasil sintesis Maka, dari hasil penelitian diperoleh hasil bahwa:
1. Dengan penggunaan katalis NaOH-etanol, reaksi sintesis tidak atau sangat
terbentuk larutan yang berwarna kuning. Larutan kuning kemudian
dipanaskan menghasilkan warna kuning kecoklatan,tetapi tidak timbul
endapan. Tidak terjadinya reaksi ini disebabkan OH-yang berasal dari
NaOH-etanol bersifat kurang nukleofilik dibandingkan C2H5O-dari natrium etanolat.
2. Dengan penggunaan katalis natrium etanolat yang dibantu dengan pemanasan,
tidak terjadi reaksi yang diinginkan. Hal ini disebabkan adanya pemanasan
sehingga terjadi autokondensasi antarasetofenon.
3. Dengan penggunaan katalis natrium etanolat tanpa bantuan pemanasan
diperoleh hasil sintesis yang diinginkan. Hal ini disebabkan oleh karena
C2H5O- lebih bersifat pemberi elektron. Suatu gugus yang berperan sebagai
donor elektron akan semakin bersifat nukleofilik. Dengan demikian akan
semakin bersifat basa gugus tersebut. Demikian sebaliknya, gugus yang
berperan sebagai akseptor elektron akan semakin bersifat elektrofilik. Dengan
demikian akan semakin bersifat asam gugus tersebut.
4. Dari pengujian titik didih senyawa hasil sintesis senyawa sintesis, disimpulkan
bahwa senyawa yang diidentifikasi adalah sama, yaitu 1-fenil-1,3-butanadion
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan
bahwa:
1. Hasil reaksi kondensasi dari asetofenon dan etil asetat dengan bantuan katalis
natrium etanolat adalah senyawa 1-fenil-1,3-butanadion.
2. Sintesis dengan menggunakan katalis NaOH-etanol tidak dapat terjadi,
sedangkan dengan katalis natrium etanolat dapat terjadi.
3. Tidak ada perbedaan hasil sintesis yang dihasilkan dengan penggunaan katalis
dalam jumlah yang berbeda.
5.2 Saran
1. Disarankan untuk peneliti selanjutnya melakukan analisis lain dengan
menggunakan alat NMR (Nuclear Magnetic Resonance), Spektroskopi
Inframerah.
DAFTAR PUSTAKA
Berger, R.G. (2007).Flavours and Fragrances Chemistry, Bioprocessing and Sustainability. New York: Verlag Berlin Heidelberg. Hal. 9.
Calkin, R.R., dan Jellinek, J.S. (1994). Perfumery Practice and Principles. Canada: John Wiley & Sons, Inc. Hal. 9-10.
Chandran, K.,, Nithya, R., Sankaran, K., dan Gopalan, A. (2006). Synthesis and characterization of sodium alkoxides. Indian Academy of Sciences.
29(2): 173-179.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Depkes RI. Hal. 649.
March, J. (1992).Advanced Organic Chemistry Reaction, Mechanisms, and Structure. Edisi Keempat. New York: John Wiley & Sons. Hal. 166, 175.
McMurry, J. (1992). Organic Chemistry. Edisi Ketiga. California: Brooks/Cole Publishing Company. Hal. 140-142, 573-574, 588.
McMurry, J. (2007). Organic Chemistry A Biological Approach. International Student Edition. New York: Thomson Brooks/ Cole. Hal. 701-704.
Meislich, H., Howard N., dan Jacob, S. (1980). Theory and Problems of organic Chemistry. New York: McGraw-Hill Book Company. Hal. 12-13.
Miller, A., dan Philippa H.S. (1985). Writing Reaction Mechanisms in Organic Chemistry. New York: Academic Press. Hal. 37, 130-131.
Reksohadiprodjo, S. (1976). Kuliah dan Praktika Kimia Farmasi Preparatif. Yogyakarta: Buku Gunung Agung. Hal. 17-20.
Reksohadiprodjo, S. (1981). Karbanion dan Enolisasi, Adisi dan Substitusi pada Ikatan Rangkap Karbon –Oksigen. Yogyakarta: Gadjah Mada University Press. Hal. 96.
Silverstein, R. M., Bassler, G.C., dan Morril, T.C. (1981). Spectrometric Identification of Organic Compounds. Edisi Keeempat. New York: Hojn Wiley & Sons. Hal. 3-4.
Solomons, T.W.G. (1988). Organic Chemistry. Edisi Keempat. New York: John Wiley & Sons. Page 747.
Warren, S. (1981). Designing Organic Syntheses A Programmed Introduction to
the Synthon Approach. New York: John Wiley & Sons. Hal. 84, 93.
Warren, S. (1982).Sintesis Organik Pendekatan Diskoneksi. Diterjemahkan oleh
Reksohadiprodjo. New York: John Wiley & Sons. Hal. 198.
Lampiran 1.Flowsheetpembuatandry ethanol
Dimasukkan ke dalambeaker glass
Ditambahkan natrium sulfat anhidrat secukupnya
Ditutup dengan plastik dan karet Digoyang
Didiamkan selama 24 jam Dipindahkan ke dalam labu alas bulat berleher tiga yang kering Dipasang alat destilasi, dialirkan dengan gas N2Ultra High Purity
(UHP)
Didestilasi pada suhu 78oC, sambil dialiri gas N2UHP
Etanol p.a
Residu
Lampiran 2.Flowsheetpembuatan natrium etanolat
Dimasukkan ke dalam labu alas bulat berleher dua yang sudah dilengkapi dengan magnetik bar
Dirangkai alat refluks, dihubungkan dengan gas N2UHP
Dimasukkan logam Na secukupnya Diputar supaya logam Na terlarut, dan dibantu dengan pemanasan Penambahan logam Na dilakukan sampai etanol tersebut jenuh Didinginkan
Dry ethanol
Lampiran 3.Flowsheetsintesis parfum a. Dengan katalis NaOH-etanol
Dimasukkan ke dalam Erlenmeyer Ditambahkan pellet NaOH
Dicek pH nya hingga 13-14
Dicampurkan Dikocok
Diamati perubahan yang terjadi
Etanol 24ml asetofenon +
20ml etil asetat
Lampiran 3.(lanjutan)
b. Dengan katalis natrium etanolat dengan bantuan pemanasan
Dimasukkan ke dalam labu alas bulat yang telah dilengkapi dengan
magnetik bar
Ditambahkan 13,5g natrium etanolat Direfluks pada suhu 78oC dan magnetik bar diputar
Dipindahkan ke dalam corong pisah Dimasukkan sebanyak 6 ml HCl 1N dan akuades 15 ml
Dikocok hingga sempurna Didiamkan hingga terbentuk 2 lapisan
Dimasukkan ke dalam corong pisah Dilakukan pencucian sebanyak 5 kali dengan akuades 15 ml
Diambil lapisan atas Dimasukkan ke dalam vial
Lampiran 3.(lanjutan)
c. Dengan katalis natrium etanolat tanpa bantuan pemanasan
Dimasukkan ke dalam labu alas bulat yang telah dilengkapi dengan
magnetik bar
Ditambahkan 13,5g natrium etanolat Magnetik bar diputar
Dipindahkan ke dalam corong pisah Dimasukkan sebanyak 6 ml HCl 1N dan akuades 15 ml
Dikocok hingga sempurna Didiamkan hingga terbentuk 2 lapisan
Dimasukkan ke dalam corong pisah Dilakukan pencucian sebanyak 5 kali dengan akuades 15 ml
Diambil lapisan atas Dimasukkan ke dalam vial
Lampiran 4.Flowsheet penentuan titik didih hasil sintesis
Dimasukkan ke dalam tabung reaksi sebanyak 4ml
Dirangkai alat
Dipanaskan pada api bunsen secara perlahan-lahan
Ditunggu sampai mendidih dan dibaca suhu pada termmeter Lapisan
atas
Lampiran 5.Kromatogram hasil sintesis
Lampiran 5.(lanjutan)
Lampiran 6.Spektrum massa hasil sintesis
Lampiran 6.(lanjutan)
Lampiran 7.Perhitungan statistik titik didih senyawa hasil sintesis 1. Jumlah katalis 13,5 g
No
Pada interval kepercayaan 99% dengan nilaiα= 0.01, dk = n-1 = 6-1 =5 diperoleh nilai t tabel(α/2, dk)= 4,0321.
Data diterima jika thitung< ttabel.
thitung1 =
= 0,812 (Data diterima)
thitung2 =
= 0,812 (Data diterima)
thitung3 =
= 0,812 (Data diterima)
thitung4 =
= 4,652 (Data ditolak)
thitung5 =
= 0,812 (Data diterima)
thitung6 =
= 0,812 (Data diterima)
2. Jumlah katalis 7,5 g
SD =
Pada interval kepercayaan 99% dengan nilaiα= 0.01, dk = n-1 = 6-1 =5 diperoleh nilai t tabel(α/2, dk)= 4,0321.
Data diterima jika thitung< ttabel.
thitung =
= 3,027 (Data diterima)
thitung2 =
= 1,297 (Data diterima)
thitung3 =
= 1,297 (Data diterima)
thitung4 =
= 3,027 (Data diterima)
thitung5 =
= 1,297 (Data diterima)
thitung6 =
Lampiran 9.Gambar alat yang digunakan