ANALISA KADAR TIMBAL PADA AIR BAKU DELITUA DI PDAM
TIRTANADI PROVINSI SUMATERA UTARA
KARYA ILMIAH
Rodhiyah Aslam
082401011
PROGRAM STUDI DIPLOMA 3 KIMIA ANALIS
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
ANALISA KADAR TIMBAL PADA AIR BAKU DELITUA DI PDAM
TIRTANADI PROVINSI SUMATERA UTARA
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Ahli Madya
RODHIYAH ASLAM
082401011
PROGRAM STUDI DIPLOMA 3 KIMIA ANALIS
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Nomor Induk Mahasiswa : 082401011
Program Studi : DIPLOMA (D3) KIMIA ANALIS
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU
PERNYATAAN
ANALISA KADAR TIMBAL PADA AIR BAKU DELITUA DI PDAM
TIRTANADI PROVINSI SUMATERA UTARA
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dari ringkasan masing-masing yang disebutkan sumbernya.
Medan, Juli 2011
PENGHARGAAN
Kepada Allah kita bersyukur, Kepada NYA jua segala Puji kita sampaikan, yang atas Pemeliharaan dan Bimbingan NYA lah kita dapat melakukan berbagai kegiatan dengan menikmati segala nikmat yang diberikan NYA, termasuk diantaranya kegiatan Penulis didalam membuat Karya Ilmiah ini.
Karya ilmiah ini merupakan Tugas Akhir yang diajukan untuk memenuhi / melengkapi persyaratan dalam menyelesaikan Program Studi D3 Kimia Analis FMIPA USU Medan.
Pada waktu berusaha menyiapkan tulisan ini, Penulis mendapat banyak bantuan, berupa dukungan moriel, materiel, tenaga, pikiran, waktu, petunjuk dan nasehat dari beberapa pihak. Yang atas semuanya itu Penulis mengucapkan terima kasih sebesar-besarnya, terutama kepada :
1. Ayah dan Bunda serta saudara-saudara tersayang.
2. Ibu DR. Rumondang Bulan, M.S selaku Ketua Jurusan dan Bapak Drs. Albert Pasaribu, M.Sc selaku Sekretaris Jurusan Departemen Kimia FMIPA USU.
3. Ibu Dra. Emma Zaidar Nasution, M.Si selaku Ketua Program Studi D3 Kimia FMIPA USU.
4. Ibu Dra. Herlince Sihotang, M.Si selaku Dosen Pembimbing.
5. Bapak/Ibu staf pengajar FMIPA USU yang telah mengajarkan berbagai ilmu pengetahuan.
6. Ibu Syafrita Oktalina,S selaku Kepala Laboratorium dan Ibu Siti Zainab Lubis selaku Kepala Bagian Laboratorium Pengujian Kualitas Air PDAM Tirtanadi Provinsi Sumatera Utara.
7. Abang-abang dan kakak-kakak pegawai PDAM Tirtanadi Provinsi Sumatera Utara.
8. Rekan-rekan Mahasiswa Kimia Analis FMIPA USU.
Selain ucapan terima kasih, tidak ada lagi yang bisa Penulis berikan kecuali menyerahkannya kepada Allah dibarengi pinta dan doa kiranya semua kebaikan itu dibalas NYA dengan berlipat ganda.
Dan dikarenakan kemampuan Penulis yang terbatas, tentu saja tulisan ini masih memerlukan perbaikan-perbaikan disana sini. Untuk mana Penulis mengharapkan adanya kritik dan saran agar tulisan ini menjadi bertambah baik.
Akhirnya, Penulis berharap semoga tulisan yang sederhana ini bermanfaat buat kita sekalian.
ANALISA KADAR TIMBAL PADA AIR BAKU DELITUA DI PDAM TIRTANADI PROVINSI SUMATERA UTARA
ABSTRAK
ANALYSIS OF VALUE LEAD IN BASE WATER DELITUA IN PDAM TIRTANADI OF THE PROVINCE OF NORTH SUMATERA
ABSTRACT
One of the source of water that to process by PDAM Tirtanadi of the Province of North Sumatera to be higienis water and peaceful to consume, is base water Delitua. Water come from the river of course in it dissolve kinds of element such as Lead or Plumbum (Pb). As for value maximum of Lead (Pb) to be based on Government role Republic Indonesian No. 82 December 14th 2001 for base water is 0,03 mg/L. Temporary whilefor result of experiment base water in Delitua in the laboratory PDAM Tirtanadi of the Province of North Sumatera with Dithizone method and then the use of Spectrofotometer DR 2010, for December 11st 2010 until January 4th 2011, we know that value of Lead (Pb) in that water is about 0,008 mg/L until 0,015 mg/L. So this value Lead (Pb) in the base water Delitua to past by value maximum that permanently.
3.1.2. Bahan 29
3.2. Pengambilan dan Penyimpanan Sampel 30
3.3. Prosedur 30
3.3.1. Pembuatan Larutan 30
3.3.2. Prosedur analisa 31
BAB 4 HASIL DAN PEMBAHASAN 33
4.1. Hasil 33
4.2. Perhitungan 34
4.2.1. Penentuan Persamaan Garis Regresi 34
4.2.2. Penentuan Koefisien Korelasi 35
4.2.3. Grafik Linieritas Parameter Uji Pb (DR-20100) 36
4.2.4. Perhitungan Konsentrasi 37
4.3. Pembahasan 39
BAB 5 KESIMPULAN DAN SARAN 41
5.1. Kesimpulan 41
5.2. Saran 41
DAFTAR PUSTAKA 42
ANALISA KADAR TIMBAL PADA AIR BAKU DELITUA DI PDAM TIRTANADI PROVINSI SUMATERA UTARA
ABSTRAK
ANALYSIS OF VALUE LEAD IN BASE WATER DELITUA IN PDAM TIRTANADI OF THE PROVINCE OF NORTH SUMATERA
ABSTRACT
One of the source of water that to process by PDAM Tirtanadi of the Province of North Sumatera to be higienis water and peaceful to consume, is base water Delitua. Water come from the river of course in it dissolve kinds of element such as Lead or Plumbum (Pb). As for value maximum of Lead (Pb) to be based on Government role Republic Indonesian No. 82 December 14th 2001 for base water is 0,03 mg/L. Temporary whilefor result of experiment base water in Delitua in the laboratory PDAM Tirtanadi of the Province of North Sumatera with Dithizone method and then the use of Spectrofotometer DR 2010, for December 11st 2010 until January 4th 2011, we know that value of Lead (Pb) in that water is about 0,008 mg/L until 0,015 mg/L. So this value Lead (Pb) in the base water Delitua to past by value maximum that permanently.
BAB 1
PENDAHULUAN
1.1.Latar Belakang
Air adalah sesuatu yang sangat vital bagi kehidupan. Selain dikonsumsi untuk
mencuci, mandi, makan dan minum, air juga digunakan untuk pembangkit tenaga listrik,
transportasi, perikanan, pertanian, proses pabrik atau industri dan lain
sebagainya.(Wardhana,W.A. 2001)
Tetapi dengan semakin meningkatnya perkembangan sektor industri dan
transportasi, baik industri migas, pertanian, industri kimia, industri logam dasar dan jenis
aktivitas manusia lainnya, maka semakin meningkat pula pencemaran (polusi) pada
air.(Fardiaz,S. 1992)
Beberapa bahan pencemar (polutan), seperti bahan mikrobiologi (bakteri, virus,
parasit), bahan organik (pestisida, deterjen) dan bahan anorganik (garam, asam, logam)
serta bahan kimia lainnya sudah banyak ditemukan dalam air, yang pada konsentrasi
tertentu dapat menimbulkan gangguan kesehatan bagi konsumen.(Darmono, 2001)
Mengantisipasi terjadinya dampak negatif tersebutlah Pemerintah mengambil
kebijaksanaan dengan mengeluarkan Peraturan / Ketetapan, antara lain mengenai kadar
maksimum beberapa parameter kualitas air untuk air baku, air bersih dan air minum,
yang mencakup tiga pokok persyaratan yaitu : fisis, kimia dan biologis.(Suriawiria,U.
Pengolahan air hingga menjadi higienis dan aman dikonsumsi, seperti untuk
mencuci, mandi makan dan minum, hendaknya berpedoman kepada Peraturan /
Ketetapan dimaksud. Terutama di dalam melakukan penilaian terhadap produk air yang
dihasilkan maupun dalam merencanakan sistem dan proses pengolahan. Dimana di dalam
hal ini Pemerintah Indonesia telah mendirikan Perusahan Daerah Air Minum (PDAM) di
seluruh wilayah.(Sutrisno,T. 2004)
PDAM Tirtanadi Provinsi Sumatera Utara yang terletak di Jalan
Sisingamangaraja No. 1 Medan, dalam upayanya melayani kebutuhan masyarakat akan
air yang higienis dan aman dikonsumsi telah melakukan proses dengan mengolah air
baku dari beberapa sumber, yang antara lain adalah dari air baku Delitua.
Air baku Delitua yang berasal dari sungai ini, sebagaimana telah diterangkan di
atas juga tidak luput dari polusi beberapa bahan pencemar (polutan) yang salah satunya
adalah Timbal.
Timbal atau Plumbum (Pb) merupakan jenis logam yang termasuk bahan
pencemar (polutan) anorganik yang pada perairan ditemukan dalam bentuk terlarut dan
tersuspensi. Walaupun kelarutan Timbal (Pb) cukup rendah sehingga kadarnya didalam
air relatif sedikit, namun unsur ini tidak esensial bagi makhluk hidup, bahkan jika sampai
melewati kadar maksimum bisa bersifat toksik yang berakibat buruk bagi hewan dan
manusia.(Effendi,H. 2003)
Oleh karena itu, maka di Laboratorium PDAM Tirtanadi Provinsi Sumatera Utara
mikrobiologi. Dimana parameter kimia merupakan kelompok penting untuk mengetahui
kualitas air, misalnya penentuan kadar Timbal (Pb).
1.2.Permasalahan
Apakah kadar Timbal (Pb) dalam air baku Delitua yang di analisa di Laboratorium
PDAM Tirtanadi Provinsi Sumatera Utara masih memenuhi persyaratan sesuai dengan
Peraturan Pemerintah Republik Indonesia No. 82 tanggal 14 Desember 2001 (Baku Mutu
Kelas I) untuk air baku.
1.3.Tujuan
Untuk mengetahui kadar Timbal (Pb) pada air baku Delitua yang diproses menjadi air
yang higienis dan aman dikonsumsi.
1.4.Manfaat
- Memberikan informasi tentang adanya Timbal (Pb) yang terlarut dalam air.
- Menginformasikan tentang besarnya kadar Timbal (Pb) dan pengaruhnya terhadap
BAB 2
TINJAUAN PUSTAKA
2.1. Air
Air adalah sumber daya alam berupa zat cair dan merupakan salah satu dari
komponen yang membentuk bumi. Keberadaanya sangat dibutuhkan oleh makhluk hidup.
Selain untuk minum, makan dan kegiatan domestik (rumah tangga), air juga digunakan
untuk menunjang aktivitas lainnya seperti perikanan, pertambangan, transportasi, industri
dan lain sebagainya.(Wardhana,W.A. 1995)
Dari jumlah 40 juta mil kubik air yang berada di planet bumi ini, baik yang di
dalam atau dipermukaannya ternyata hanya 0,5% atau 0,2 juta mil kubik yang secara
langsung dapat dipergunakan. Sisanya, yaitu 97% berbentuk air laut, dan 2,5% berbentuk
salju dan es abadi yang dalam keadaan cair baru dapat dipergunakan.(Suriawiria,U.2005)
2.1.1. Golongan Air
Penggolongan air menurut peruntukannya adalah sebagai berikut :
1. Golongan A, yaitu air yang dapat digunakan sebagai air minum secara langsung
tanpa diolah terlebih dahulu.
2. Golongan B, yaitu air yang dapat digunakan sebagai air baku untuk diolah
3. Golongan C, yaitu air yang dapat digunakan untuk keperluan perikanan dan
peternakan.
4. Golongan D, yaitu air yang dapat digunakan untuk keperluan pertanian dan dapat
digunakan untuk usaha perkotaan, industri, dan listrik tenaga air.(Kristanto,P.
2002)
2.1.2. Sumber Air
Secara garis besar air bersumber dari :
1. Air laut
2. Air atmosfir / air hujan
3. Air Permukaan
4. Air Tanah
2.1.2.1. Air Laut
Sebagian besar dari air yang terdapat di planet bumu ini adalah air laut (80%).
Sisanya adalah berupa air tanah, salju, es dan air hujan. Kadar dan komponennya
ditentukan oleh sejumlah reaksi kimia fisik dan biokimia yang terjadi di laut. Sementara
kadar garamnya bervariasi disetiap tempat, misalnya Laut Hitam memiliki kadar garam
yang sangat tinggi dibandingkan dengan kadar garam pada Samudra Fasifik.(Gabriel,J.F.
2001)
Air laut rata-rata mengandung kadar garam (NaCl) sebesar 3%. Karena ini air laut
tidak memenuhi syarat untuk air minum.(Sutrisno,T. 2004)
Laut, sungai, danau, rawa-rawa, sumur dan semua yang terkena sinar matahari
biasanya akan mengalami evaporasi (penguapan). Uap inilah yang naik sampai kesuatu
titik yang suhu udaranya sama dengan uap air tersebut, kemudian terjadi titik kondensasi
dan terbentuklah awan. Pada saat itu terjadi proses presipitasi, selanjutnya jatuh ke bumi
berupa titik –titik air yang disebut hujan.(Gabriel,J.F. 2001)
Karena adanya pengotoran udara yang disebabkan oleh industri, debu dan
lain-lain, maka untuk menjadikannya sebagai sumber air minum, hendaknya ditampung
sesudah hujan turun beberapa saat.(Sutrisno,T. 2004)
2.1.2.3. Air Permukaan
Air permukaan adalah air hujan yang mengalir di permukaan bumi. Pada
umumnya air permukaan ini akan mendapat pengotoran selama pengalirannya, misalnya
oleh lumpur, batang-batang kayu, daun-daun, kotoran industri kota dan sebagainya.
Udara yang mengandung Oksigen akan membantu mengalami poses pembusukan
yang terjadi pada air permukaan yang telah mengalami pengotoran, karena selama dalam
perjalanan, Oksigen akan meresap ke dalam air permukaan.(Sutrisno,T. 2004)
Air permukaan ada 2 macam yakni :
a. Air Sungai
Di negara-negara berkembang kebutuhan air minum tidak banyak
dimungkinkan dari sistem perpipaan, tetapi banyak menggunakan air permukaan
secara langsung tanpa treatment (pengolahan). Karena peledakan penduduk yang
memungkinkan secara luas tersebar dan terkontaminirnya air permukaan dengan
berbagai kotoran, maka pengendalian terhadap penggunaan air dari sumber ini
Penggunaan sumber air minum bagi PAM di kota-kota besar masih
menggantungkan dari sungai-sungai yang telah dicemari sepanjang berkilo-kilo
meter sehingga treatment yang sempurna sangat diperlukan secara mutlak.
Lebih-lebih bila disekitar sungai terdapat daerah industri yang membuang bahan
buangan logam atau bahan racun. Penggunaan sumber air yang telah mengalami
pencemaran total merupakan problema di mana treatment harus dilakukan secara
modern dan intensif.(Ryadi,S. 1984)
b. Air Rawa / Danau
Kebanyakan air rawa ini berwarna yang disebabkan oleh adanya zat-zat
organik yang telah membusuk, misalnya asam humus yang larut dalam air yang
menyebabkan warna kuning coklat. Dengan adanya pembusukan kadar zat
organik tinggi, maka umumnya kadar Fe dan Mn akan tinggi pula dan dalam
keadaan kelarutan O2 kurang sekali (anaerob), maka unsur-unsur Fe dan Mn ini
akan larut.
Jadi untuk pengambilan air, sebaiknya pada kedalaman tertentu di
tengah-tengah agar endapan-endapan Fe dan Mn tak terbawa, demikian pula dengan
lumut yang ada pada pemukaan rawa / danau.(Sutrisno,T. 2004)
2.1.2.4. Air Tanah
Air tanah terbagi atas :
a. Air Tanah Dangkal
Terjadi karena daya proses peresapan air dari pemukaan tanah. Lumpur
akan tertahan, demikian pula dengan sebagian bakteri, sehingga air tanah akan
karena melalui lapisan tanah yang mempunyai unsur-unsur kimia tertentu untuk
masing-masing lapisan tanah. Lapisan tanah di sini berfungsi sebagai saringan.
Air tanah ini dimanfaatkan untuk sumber air minum melalui sumur-sumur
dangkal.
b. Air Tanah Dalam
Terdapat setelah lapis rapat air yang pertama. Pengambilan air tanah
dalam, tak semudah pada air tanah dangkal. Dalam hal ini harus digunakan bor
dan memasukkan pipa kedalamnya sehingga dalam suatu kedalaman (biasanya
antara 100-300 m) akan didapatkan suatu lapis air. Jika tekanan air tanah ini
besar, maka air dapat menyembur ke luar. Jika air tak dapat ke luar dengan
sendirinya, maka digunakanlah pompa untuk membantu pengeluaran air tanah
dalam ini.
c. Mata Air
Mata air adalah air tanah yang keluar dengan sendirinya ke permukaan
tanah. Mata air yang berasal dari tanah dalam, hampir tidak terpengaruh oleh
musim dan kualitasnya sama dengan keadaan air dalam.(Sutrisno,T. 2004)
2.1.3. Sifat Air
Air memiliki karakteristik yang khas yang tidak dimiliki oleh senyawa kimia yang
a. Pada kisaran suhu yang sesuai bagi kehidupan, yakni 0ºC (32ºF) - 100ºC, air
berwujud cair. Suhu 0ºC merupakan titik beku (freezing point) dan suhu 100ºC
merupakan titik didih (boiling point) air.
b. Perubahan suhu air berlangsung lambat sehingga air memiliki sifat sebagai
penyimpan panas yang sangat baik. Sifat ini memungkinkan air tidak menjadi
panas ataupun dingin dalam seketika.
c. Air memerlukan panas yang tinggi dalam proses penguapan. Penguapan
(evaporasi) adalah proses perubahan air menjadi uap air. Proses ini memerlukan
energi panas dalam jumlah yang besar. Sebaliknya, proses perubahan uap air
menjadi cairan (kondensasi) melepaskan energi panas yang besar.
d. Air merupakan pelarut yang baik, yang mampu melarutkan berbagai jenis
senyawa kimia.
e. Air memiliki tegangan permukaan yang tinggi. Suatu cairan dikatakan memiliki
tegangan permukaan yang tinggi jika tekanan antar-molekul cairan tersebut tinggi.
Tegangan permukaan yang tinggi menyebabkan air memiliki sifat membasahi
suatu bahan secara baik (higher wetting ability).
f. Air merupakan satu-satunya senyawa yang merenggang ketika membeku. Pada
saat membeku, air merenggang sehingga es memiliki nilai densitas
(massa/volume) yang lebih rendah daripada air. Dengan demikian, es akan
2.1.4. Batasan-batasan Air Bersih dan Aman
Air yang diperuntukan bagi konsumsi manusia harus berasal dari sumber yang
bersih dan aman. Batasan-batasan sumber air yang bersih dan aman, antara lain :
a. Bebas dari kontaminasi kuman atau bibit penyakit.
b. Bebas dari substansi kimia yang berbahaya dan beracun.
c. Tidak berasa dan tidak berbau.
d. Dapat dipergunakan untuk mencukupi kebutuhan domestik dan rumah tangga.
e. Memenuhi standar minimal yang ditentukan oleh WHO atau Departemen
Kesehatan RI.(Chandra,B. 2006)
2.1.5. Syarat-syarat Air Minum
Disamping pertimbangan akan kegunaan air bagi manusia maupun organisme,
maka persyaratan untuk standar kualitas air ditentukan oleh beberapa aspek. Persyaratan
ini dikarenakan jaringan air yang demikian luas, hingga melalui tempat-tempat yang
dapat berakibat buruk bagi kesehatan.
Lebih-lebih bila digunakan untuk air minum, maka persyaratan-pesyaratan itu
secara mutlak dan ketat harus mendasari penentuan standar kualitas air minum.
Persyaratan-persyaratan tersebut adalah menyangkut beberapa aspek, yang antara lain
adalah :
1. Persyaratan Fisika
2. Persyaratan Kimia
2.1.5.1. Persyaratan Fisika
Syarat-syarat fisika untuk air minum ditentukan oleh beberapa faktor, yaitu :
a. Air tidak boleh berwarna
b. Air tidak boleh berasa
c. Air tidak boleh berbau
d. Suhu air hendaknya dibawah sela udara (sejuk ± 25oC)
e. Air harus jernih.(Sutrisno,T. 2004)
Memang penilaian untuk bau ditentukan secara subyektif, yakni dengan jalan air
diencerkan berturut-turut hingga tidak lagi berbau. Dan pada umumnya penilaian bau dan
rasa sering dilakukan bersamaan sebagai suatu indikator, dimana antara keduanya sulit
dipisahkan secara kualitatif. Tetapi faktor-faktor lainnya, juga harus diperhatikan dan
dipenuhi sebagai syarat air minum.(Ryadi,S.1984)
2.1.5.2. Persyaratan Kimia
Bagi air minum khususnya, persyaratan kimia mempunyai hubungan dengan
pengaruh toksisitas. Karenanya diantara beberapa bahan kimia yang pada umumnya
mudah larut dalam air, perlu dinilai kadarnya untuk mengetahui sejauh mana kadar
maksimum yang diperbolehkan.(Ryadi,S. 1984)
Adapun bahan-bahan kimia tersebut antara lain adalah :
1. Ammonia (NH3-N), dan garam-garamnya bersifat mudah larut dalam air. Kadar
maksimum ammonia bagi air minum adalah 1,5 mg/L.
2. Flourida (F) termasuk unsur yang larut dalam air. Perairan yang diperuntukkan
3. Mangan (Mn) pada air minum kadar maksimum mangan adalah 0,05 mg/L.
4. Nitrat (NO3) adalah bentuk utama nitrogen di perairan. Kadar nitrat untuk
keperluan air minum sebaiknya tidak melebihi 10 mg/L.
5. Timbal (Pb), kelarutan timbal cukup rendah hingga kadarnya di dalam air relatif
sedikit. Untuk air minum kadar maksimum timbal adalah 0,05 mg/L.(Effendi,H.
2003)
2.1.5.3. Persyaratan Biologis
Ditentukan oleh kehadiran mikroorganisme yang pathogen (penyebab penyakit)
dan yang non pathogen. Karena mikroorganisme pathogen memang mengandung bakteri
penyebab penyakit, maka penilaian terhadap persyaratan biologis harus lebih
diperhatikan.
Sebaliknya, sekalipun mikroorganisme non pathogen relatif tidak berbahaya bagi
kesehatan, tetapi karena jumlahnya yang selalu berlebih, dapat mempengaruhi rasa, bau
dan lain-lain. Juga berakibat menyulitkan pengolahan air (water processing). Seperti
munculnya ganggang dan bakteri-bakteri besi (non bacteria) yang mempercepat
tersumbatnya saringan pasir (sand filter) dan hambatan pada saringan pompa.
Begitupun juga dengan adanya mikroorganisme Coli yang berasal dari usus besar
(faeces) dan tanah, yang juga non pathogen, namun air yang mengandung
mikroorganisme Coli dianggap telah terkontaminasi dengan kotoran
2.1.6. Pencemaran (Polusi) Air
Yang dimaksud dengan pencemaran atau polusi air adalah masuk atau
dimasukkannya makhluk hidup, zat energi atau komponen lain kedalam air dan atau
berubahnya komposisi air oleh aktivitas manusia. Sehingga kualitas air menurun sampai
ke tahap tertentu yang menyebabkan air menjadi kurang atau tidak berfungsi lagi sesuai
dengan peruntukannya.(Fardiaz,S. 1992)
Air di alam semesta ini walaupun tidak semuanya dikatakan tercemar, tetapi tidak
ada yang berbentuk murni. Sekalipun di daerah pegunungan atau di hutan yang terpencil
dengan udara yang bersih dan bebas polusi, namun air hujan yang turun selalu
mengandung bahan-bahan terlarut dan bahan-bahan tersuspensi. Apalagi air yang
melintasi atau berada di pemukiman penduduk, baik di pedesan maupun di perkotaan dan
tempat-tempat lain sudah tentu lebih mudah tercemar oleh lingkungannya dan
tekontaminasi oleh aktivitas manusia.(Kristanto,P. 2002)
2.1.6.1. Sumber Pencemar
Sumber pencemar dapat berupa suatu lokasi tertentu (point source) atau tak tentu
(non-point source). Sumber pencemar point source misalnya knalpot mobil, cerobong
asap pabrik, dan saluran limbah industri. Pencemar yang berasal dari point source bersifat
lokal. Efek yang ditimbulkan dapat ditentukan berdasarkan karakteristik kualitas air.
Volume pencemar dari point source biasanya relatife tetap.
Sumber pencemar non-point source dapat berupa point source dalam jumlah yang
limbah dari daerah pemukiman (domestik), dan limbah dari daerah perkotaan.(Effendi,H.
2003)
2.1.6.2. Bahan Pencemar (Polutan)
Bahan pencemar (polutan) air adalah bahan-bahan yang bersifat asing bagi air itu,
yang masuk ke air, sehingga mengganggu peruntukan air tersebut.
Dari hal masuknya ke air, polutan dikelompokkan menjadi 2 yaitu polutan
alamiah dan polutan antropogenik.
Adapun polutan alamiah adalah polutan yang masuk ke air secara alami, misalnya
akibat letusan gunung berapi, tanah longsor, banjir dan fenomena alam yang lain. Polutan
alamiah ini tentu saja sulit dikendalikan.
Sedangkan polutan antropogenik adalah polutan yang masuk ke air dikarenakan
aktivitas manusia, misalnya kegiatan domestik (rumah tangga), kegiatan urban
(perkotaan), pertanian, perikanan, industri dan lain-lain. Intensitas polutan antropogenik
dapat dikendalikan dengan cara mengontrol aktivitas yang menyebabkan timbulnya
polutan tersebut.
Berdasarkan toksisitasnya, polutan dibedakan menjadi 2, yakni polutan tidak
toksik (non toxic pollutans) dan polutan toksik (toxic pollutans).
1. Polutan Tidak Toksik (non toxic pollutans)
Polutan tidak toksik biasanya telah berada pada air secara alami. Sifat
destruktif polutan ini muncul apabila berada dalam jumlah yang berlebihan sehingga
dapat mengganggu kesetimbangan melalui perubahan proses kimia-fisika perairan.
tersuspensi dapat mempengaruhi sifat fisika perairan, antara lain meningkatkan
kekeruhan sehingga menghambat penetrasi cahaya matahari. Dengan demikian,
intensitas cahaya matahari pada air menjadi lebih kecil dari intesitas yang dibutuhkan
untuk melangsungkan proses fotosintesis. Keberadaan nutrient atau unsur hara yang
berlebihan dapat memacu terjadinya pengayaan (eutofikasi) perairan dan dapat
memacu pertumbuhan mikroalga dan tumbuhan air secara pesat.
2. Polutan Toksik (toxic pollutans)
Polutan ini dapat mengakibatkan kematian (lethal), ataupun akibat buruk lain
seperti terganggunya pertumbuhan, tingkah laku dan karakteristik morfologi berbagai
organisme akuatik. Polutan toksik ini biasanya berupa bahan-bahan yang bukan
alami, misalnya pestisida, detergen, dan bahan lainnya. Polutan berupa bahan yang
bukan alami ini dikenal dengan istilah xenobiotik, yaitu polutan yang diproduksi oleh
manusia. Polutan toksik dikelompokkan menjadi 5, yaitu :
a. Logam, meliputi : timbal, nikel, cadmium, zinc dan merkuri. Logam berat
diartikan sebagai logam dengan nomor atom > 20, tidak termasuk logam alkali,
alkali tanah, lantanida, dan aktinida.
b. Senyawa organik, meliputi pestisida organoklorin, hidrokarbon alifatik berklor,
pelarut (solvents), fenol, formaldehid dan sebagainya. Senyawa ini berasal dari
kegiatan industri, pertanian dan domestik.
c. Gas, misalnya klorin dan amonia.
d. Anion, misalnya sianida, fluorida, sulfida, dan sulfat.
Polutan yang berupa gas, bahan terlarut dan partikulat sangat berpengaruh
terhadap perairan.(Effendi,H. 2003)
2.1.6.3. Pencegahan Pencemaran Air
Sebagaimana diketahui bahwa kemajuan industri dan teknologi memang mampu
meningkatkan kesejahteraan, tetapi juga menimbulkan pencemaran air yang merugikan
bagi manusia.
Salah satu kerugian itu adalah apabila akibat dari pencemaran tersebut merusak
lingkungan sehingga daya dukung alam terhadap kelangsungan hidup jadi
berkurang.(Wardhana,W.A. 1995)
Oleh karenanya, usaha-usaha pencegahan pencemaran air perlu dilakukan, yang
dalam hal ini melibatkan faktor-faktor sebagai berikut :
1. Air limbah yang akan dibuang ke perairan harus diolah lebih dahulu sehingga
memenuhi standar air limbah yang telah ditetapkan pemerintah.
2. Menentukan dan mencegah terjadinya interaksi sinergisma antarpolutan satu
dengan lainnya.
3. Menggunakan bahan yang dapat mencegah dan menyerap minyak yang tumpah di
perairan.
4. Tidak membuang air limbah rumah tangga langsung ke dalam perairan. Hal ini
untuk mencegah pencemaran air oleh bakteri.
5. Limbah radioaktif harus diproses dahulu agar tidak mengandung bahaya radiasi
6. Mengeluarkan atau menguraikan deterjen atau bahan kimia lain dengan
menggunakan aktivitas mikroba tertentu sebelum dibuang ke dalam perairan
umum.(Supardi,I. 2003)
Selain faktor-faktor tersebut, maka dalam usaha pencegahan pencemaran air
hendaknya memperhatikan pula sumber pencemarannya, yaitu non point source dan point
source (sebagaimana yang telah diterangkan sebelumnya). Dengan demikian, usaha yang
dilakukan itu akan dapat melestarikan air untuk tetap bermanfaat sesuai peruntukannya,
sekaligus juga mencakup kebaikan secara umum dan kesehatan.(Darmono, 2001)
Selanjutnya, pemeliharaan atas air yang bersih dan sehat, akan selalu memberikan
fasilitas dan juga menjaga atau memelihara tata kehidupan bagi flora dan fauna yang
hidup di air.(Mahida,U.N. 1984)
2.2. Timbal atau Plumbum (Pb)
Timbal atau Plumbum adalah elemen kimia dengan simbol Pb, termasuk kedalam
kelompok logam golongan IV-A, mempunyai nomor atom (NA) 82, dengan bobot atau
berat atom (BA) 207,2. Dalam keseharian dikenal dengan sebutan timah hitam, yang
merupakan logam berwarna kebiru-biruan sampai hitam kelam.((Palar,H. 1994)
Logam ini pada awalnya secara alami terdapat didalam kerak bumi. Namun, bisa
juga berasal dari aktivitas manusia yang bahkan mampu mencapai jumlah 300 kali lebih
Perbandingan yang begitu besar jumlahnya, adalah sehubungan dengan
meningkatnya aktivitas manusia baik di sektor industri maupun yang lainnya yang
menghasilkan timbal, seperti : penambangan, pembakaran bahan aditif bensin kendaraan
bermotor, partikel-partikel yang berasal dari pabrik, pembakaran arang dan lain
sebagainya.(Fardiaz,S. 1992)
2.2.1. Sumber-sumber Timbal
Seperti sudah dikemukakan, bahwa timbal ada yang secara alami terdapat dalam
kerak bumi, dan ada yang berasal dari aktivitas manusia. Sumber-sumber timbal tersebut
adalah sebagai berikut :
1. Timbal yang secara alami terdapat dalam kerak bumi, jumlahnya sangat sedikit
sekali, yaitu hanya 0,0002% dari jumlah seluruh kerak bumi dan di alam ini
terdapat 4 macam isotop timbal yaitu :
a. Timbal-204, dipekirakan berjumlah sebesar 1,48% dari seluruh isotop timbal.
b. Timbal-206, ditemukan dalam jumlah sebesar 23,60% dari seluruh isotop
timbal yang tedapat di alam.
c. Timbal-207, sebanyak 22,60% dari semua isotop timbal yang terdapat di
alam.
d. Timbal-208, ditemukan sebanyak 52,32% dari seluruh isotop timbal yang
Isotop-isotop tersebut merupakan hasil peluruhan radio aktif alam. Melalui proses
geologi timbal terkonsentrasi dalam deposit seperti : bijih logam, yang tergabung
dengan logam-logam lain seperti : perak, seng, arsen dan lain-lain.(Palar,H. 1994)
2. Sedangkan timbal yang berasal dari aktivitas manusia antara lain adalah :
a. Hasil penambangan
Bijih-bijih timbal yang terdapat dari hasil penambangan mengandung sekitar
3% sampai 10% timbal, yang selanjutnya akan dipekatkan lagi sehingga
diperoleh logam timbal murni.(Palar,H. 1994)
b. Timbal berbentuk gas
Terutama berasal dari pembakaran bahan aditif bensin dari kendaraan
bermotor.
c. Timbal berbentuk partikel-partikel
Umumnya bersumber dari pabrik-pabrik, pembakaran arang dan lain
sebagainya.(Fardiaz,S. 1992)
2.2.2. Sifat-sifat Timbal
Sebagaimana elemen yang lain timbal juga mempunyai sifat-sifat khusus sebagai
berikut:
1. Sifat fisik
a. Merupakan logam berat
c. Merupakan logam yang lunak, sehingga dapat dipotong dengan menggunakan
pisau atau dengan tangan dan dapat dibentuk dengan mudah.
d. Titik lebur 327,4oC
e. Mendidih pada suhu 1740oC
f. Mempunyai kerapatan yang lebih besar dibandingkan dengan logam-logam
biasa, kecuali emas dan merkuri.
2. Sifat kimia
a. Mempunyai valensi 2 dan 4
b. Relatif tahan terhadap asam sulfat dan HCl
c. Merupakan logam yang tahan terhadap peristiwa korosi atau karat, sehingga
logam timbal sering digunakan sebagai bahan coating (lapisan).
d. Larut secara perlahan terhadap asam nitrat.
e. Merupakan amphoteric, garam Pb terbentuk dari asam plumbic.
f. Merupakan penghantar listrik yang tidak baik.
3. Senyawa Plumbum (Pb)
Senyawa Pb yang penting adalah Plumbum oksida dan Plumbum tetraethyl,
Plumbum carbonate, Plumbum silicate, Plumbum azida [Pb(N3)2].
4. Alloi Pb
Pb bersenyawa dengan berbagai elemen membentuk alloi Pb. Elemen yang
dimaksud adalah Sn, Cu, arsenik, antimon, bismut, cadmium dan Na.(Gabriel,J.F.
2001)
Timbal dan persenyawaannya banyak digunakan diberbagai bidang yang antara
lain adalah sebagai berikut :
a. Dipakai lapisan pelindung X-ray dengan ketebalan 1,5 mm , 3 mm.
b. Dipakai pada kabel telepon dan kabel TV (dibungkus dengan Pb).
c. Dipakai pada konstruksi bangunan dan industri kimia untuk mencegah
korosif.
d. Dipakai pada baterai, solder dan amunisi.
e. Senyawa Pb sulfida, Pb chromate, Pb putih, 2PbCO3, Pb(OH)2 dipakai sebagai
pigmen (pewarna).
f. Pb silikat, Pb karbonat, garam Pb dan asam organik dipakai untuk stabilisator
panas dan cahaya, untuk plastik polyvinyl khlorida.
g. Pb silikat dipakai pada gelas dan keramik.
h. Pb(NH3)2 standar detonator letupan.
i. Pb arseni dipakai dalam jumlah banyak untuk insektisida (membasmi
serangga) pada tanaman.
j. Pb oksida (litharge) dipakai untuk memeperbaiki mutu magnet (magnet
barium ferrite keramik).
k. Senyawa organo Pb, dipakai sebagai katalisator pada pembuatan foam
polyurethane, mencegah rusaknya cat pada kapal laut, membunuh bakteri
gram positif, mencegah bocornya kapal kayu, mencegah serangan jamur pada
kain katun, pembasmi cacing, mencegah korosif pada baja.
m. Alloi tahan kimia dipakai pada metal lainnya agar tahan korosif terhadap air,
udara atau zat kimia lainnya.(Gabriel,J.F. 2001)
Adapun bijih-bijih logam timbal yang diperoleh dari hasil penambangan, seperti
tersebut diatas, hanya mengandung sekitar 3% sampai 10% timbal. Hasil ini akan
dipekatkan lagi, sampai 40% sehingga didapatkan logam timbal murni.
Logam ini digabung dengan logam-logam lain seperti perak (Ag), seng (Zn),
arsen (Ar), logam stibium (Sb) dan dengan logam bismut (Bi).
Dalam hal timbal digunakan pada industri pembuatan baterai, alloi timbale
dengan logam bismut (Pb-Bi) berfungsi sebagai grid (jaringan listrik), sedangkan timbal
oksida (PbO4) dipakai sebagai bahan yang aktif dalam pengaliran arus elektron.(Palar,H.
1994)
2.2.4. Pencemaran Air oleh Timbal
Sebelumnya sudah dikemukakan bahwa timbal atau plumbum (Pb) adalah logam
(metal) yang termasuk polutan (bahan pencemar) toksik.
Timbal (Pb) dan persenyawaannya dapat berada di dalam perairan melalui
pengkristalan Pb di udara dengan bantuan air hujan. Di samping itu, proses korosifikasi
dari bantuan mineral akibat hempasan gelombang dan angin, juga merupakan salah satu
jalur sumber Pb yang akan masuk ke dalam badan perairan.
Pb yang masuk ke dalam badan perairan sebagai dampak dari aktivitas kehidupan
manusia ada bermacam bentuk. Di antaranya adalah air buangan (limbah) dari industri
yang berkaitan dengan Pb, air buangan dari pertambangan bijih timah hitam dan buangan
seperti anak-anak sungai untuk kemudian akan dibawa terus menuju lautan. Umumnya
jalur buangan dari bahan sisa perindustrian yang menggunakan Pb akan merusak tata
lingkungan perairan yang dimasukinya (menjadikan sungai dan alurnya tercemar).
Senyawa Pb yang ada dalam badan perairan ditemukan dalam bentuk ion-ion divalen atau
ion-ion tetravalent (Pb2+ , Pb4+).
Badan perairan yang sudah mengandung senyawa-senyawa atau ion-ion Pb
sehingga melebihi konsentrasi yang semestinya, dapat mengakibatkan kematian bagi
biota perairan tersebut. Seperti konsentrasi Pb yang mencapai 188 mg/L dapat mematikan
beberapa jenis ikan, konsentrasi Pb 2,75 mg/L sampai dengan 49 mg/L dapat mematikan
ctustacea (binatang air berkulit keras) setelah 245 jam, dan Pb dengan konsentrasi 64
mg/L akan mematikan golongan insekta (serangga) dalam rentang waktu 168 jam sampai
dengan 336 jam.
Di dalam air minum juga bisa terdapat Pb, jika air minum tersebut dialirkan
melalui pipa-pipa yang merupakan alloi dari logam Pb.(Palar,H. 1994)
Meskipun timbal (Pb) pada perairan ditemukan dalam bentuk terlarut dan
tersuspensi, dengan kelarutan yang cukup rendah sehingga kadarnya relatife sedikit,
tetapi timbal termasuk unsur yang tidak esensial bagi makhluk hidup, bahkan dalam
konsentrasi tertentu unsur ini bisa bersifat toksik.
Selain dari kadar maksimum timbal yang diperuntukan bagi air minum, air bersih
maupun air baku telah ditetapkan oleh Pemerintah, maka kadar timbal di perairan yang
diperuntukkan bagi hewan ternak hendaknya tidak melebihi 0,1 mg/L, bagi keperluan
pertanian pada tanah yang bersifat netral dan alkalis adalah 10 mg/L, sedangkan pada
2.2.5. Toksisitas Timbal
Karena sifatnya yang lunak sehingga mudah dipotong dengan pisau dan dibentuk
dengan tangan, tahan terhadap peristiwa korosi (pengkaratan), mempunyai titik lebur
yang rendah dan lain-lain, maka timbal (Pb) banyak digunakan oleh manusia. Namun,
disisi lain (sebagaimana yang telah diterangkan sebelumnya) timbal juga dalam
konsentrasi tertentu dapat bersifat toksik.
Toksisitas (keracunan) yang ditimbulkan oleh persenyawaan logam Pb dapat
terjadi karena masuknya persenyawaan logam tersebut ke dalam tubuh. Proses masuknya
Pb ke dalam tubuh dapat melalui beberapa jalur, yaitu melalui makanan dan minuman,
udara dan perembesan atau penetrasi pada selaput atau lapisan kulit.
Bentuk-bentuk kimia dari senyawa-senyawa Pb, merupakan faktor yang
mempengaruhi sifat-sifat Pb dalam tubuh manusia. Senyawa-senyawa Pb organik relatif
lebih mudah untuk diserap tubuh melalui selaput lendir atau melalui lapisan kulit, bila
dibandingkan dengan senyawa-senyawa Pb anorganik. Namun, hal itu bukan berarti
semua senyawa Pb dapat diserap oleh tubuh, melainkan hanya sekitar 5-10% dari jumlah
Pb yang masuk melalui makanan dan atau sebesar 30% dari jumlah Pb yang terhirup
yang akan diserap oleh tubuh. Dari jumlah yang terserap itu, hanya 15% yang akan
mengendap pada jaringan tubuh, dan sisanya akan turut terbuang bersama bahan sisa
metabolisme seperti urin dan feces.
partikel dari senyawa Pb yang ada dan volume udara yang mampu dihirup pada saat
peristiwa bernafas berlangsung. Makin kecil ukuran partikel debu, serta makin besarnya
volume udara yang mampu terhirup, maka akan semakin besar pula konsentrasi Pb yang
diserap oleh tubuh. Logam Pb yang masuk ke paru-paru melalui peristiwa pernafasan
akan terserap dan berikatan dengan darah paru-paru untuk kemudian diedarkan ke
seluruh jaringan dan organ tubuh. Lebih dari 90% logam Pb yang terserap oleh darah
berikatan dengan sel-sel darah merah (erytrocyt).(Palar,H. 1994)
Bentuk ion Pb2+ mampu menggantikan keberadaan ion Ca2+ yang terdapat dalam
jaringan tulang. Hal ini disebabkan oleh senyawa-senyawa timbal yang bisa memberikan
efek toksik terhadap berbagai macam fungsi organ tubuh, yang antara lain adalah :
1. Menghambat sistem pembentukan hemoglobin (Hb) sehingga menyebabkan
anemia
2. Menimbulkan kerusakan otak, dengan gejala epilepsy, halusinansi dan delirum
(keadaan pikiran tidak waras atau kegila-gilaan).
3. Menyebabkan pucat, lesu, hilang semangat.
4. Menyebabkan sakit perut dan susah buang air besar.
5. Menyebabkan peningkatan permiabilitas (kebocoran) pembuluh darah.
6. Gangguan menstruasi dan mengakibatkan ibu hamil bisa mengalami keguguran.
7. Mengakibatkan gangguan fungsi adrenal (kelenjar).
8. Bersifat karsinogenik (penyebab kanker) dalam dosis tinggi.
Lebih lanjut, toksisitas (keracunan) timbal juga bersifat kronis dan akut. Dimana
pembuatan baterai, percetakan, pelapis logam dan pengecatan. Sedangkan toksisitas akut
bisa terjadi jika timbal (Pb) masuk kedalam tubuh seseorang melalui makanan / minuman
atau menghirup gas Pb dalam waktu yang relatif pendek dengan dosis atau kadar yang
tinggi.(Widowati,W. 2008)
2.2.5.1. Pencegahan Toksisitas Timbal (Pb)
Berbagai upaya untuk mencegah dan menghindari efek toksik Pb antara lain :
1. Melakukan tes medis (Pb dalam darah), terutama bagi pekerja yang beresiko
terpapar Pb.
2. Menghindari penggunaan peralatan-peralatan dapur atau tempat makanan atau
minuman yang mengandung Pb (keramik berglasur, wadah atau kaleng yang
dipatri atau mengandung cat).
3. Pemantauan kadar Pb di udara dan kadar Pb dalam makanan atau minuman secara
berkesinambungan.
4. Mencegah anak menelan atau menjilat mainan bercat atau berbahan mengandung
cat.
5. Tidak makan, tidak minum, tidak merokok di kawasan yang tercemar Pb.
6. Menyediakan fasilitas ruang makan yang terpisah dari lokasi pencemaan Pb.
7. Tempat penyimpanan makanan atau minuman tertutup sehingga tidak kontak
dengan debu atau asap Pb.
8. Mengurangi emisi gas buang yang mengandung Pb, baik dari kendaraan bermotor
9. Bagi para pekerja yang kontak dengan Pb sebaiknya mereka menggunakan
peralatan standar keamanan dan keselamatan kerja.(Widowati,W. 2008)
2.2.5.2. Pengobatan Toksisitas Timbal (Pb)
Untuk mengurangi efek toksiknya pada orang yang telah terpapar Pb, dapat
menggunakan kelator, yang antara lain adalah BAL (British Anti Lewisite), CaNa2EDTA
dan Penicillamine.
Walaupun terjadi efek samping seperti demam, sakit kepala, mual, muntah, tetapi
kelator yang digunakan itu dapat mengikat Pb dan memeindahkannya dari molekul
biologis aktif serta membentuk senyawa kompleks yang larut dalam air dan lebih mudah
diekskresikan melalui urin.(Widowati,W. 2008). Begitupun dalam hal pemberian kelator,
harus ditentukan lebih dulu kadar Pb darah. Adapun ketiga kelator (BAL, CaNa2EDTA
dan Penicillamine) biasa diberikan kepada penderita dengan kadar Pb darah 0,5 – 0,6
ppm.
Caranya adalah dengan mengkombinasikan CaNa2EDTA dan BAL (dimercaprol)
yang diberikan, kemudian menyusul pemberian Penicillamine untuk pengobatan jangka
panjang.
Atau dengan cara, CaNa2EDTA pada dosis tertentu dibagi dalam 2 kali pemberian
pemberian CaNa2EDTA belangsung selama 4 jam BAL (dimercaprol) pun diberikan.
Cara ini bias diulang kembali sesudah pengobatan dihentikan 2 hari.
Setiap cara pengobatan dengan menggunakan CaNa2EDTA maupun BAL
(dimercaprol), hendaknya jangan melebihi dari dosis yang ditetapkan, dan produksi urin
pun harus tetap dipantau, karena biasanya pengeluaran Pb melalui urin selalu terjadi
selama berlangsungnya infus awal.
BAL (dimercaprol) dengan dosis tertentu yang diberikan setiap 4 jam selama 48
jam, kemudian setiap 6 jam selama 48 jam berikutnya, dan akhirnya setiap 6 – 12 jam
selama 17 hari serta mengkombinasikannya dengan CaNa2EDTA, sebenarnya akan
BAB 3
BAHAN DAN METODE
3.1. Alat dan Bahan
3.1.1. Alat
- Spektrofotometer DR 2010
- Labu ekstraksi 500 ml
- Stopcock
- Gelas ukur 5 ml, 50 ml, 250 ml
- Kuvet 25 ml
- Kapas
- Support ring dan stand
- Botol kaca
- Neraca analitik
- Beaker glass 250 ml
- Labu ukur 100 ml
3.1.2. Bahan
- 1 bungkus bubuk buffer sitrat
- Kloroform 50 ml
- 1 bungkus bubuk reagen logam dithiver
- Larutan standar NaOH 5 N
- Aquadest
- Indikator universal
- H2SO4 5,25 N
- Sampel Air Baku Delitua
3.2. Pengambilan dan Penyimpanan sampel
- Sampel uji disimpan dalam botol kaca bebas asam atau wadah plastik.
- pH sampel uji diatur sampai pH < 2 dengan HNO3 sekitar 2 ml per liter (tahan
sampai 6 bulan pada suhu kamar)
- Atur kembali pH sampel uji yang diawetkan hingga mencapai 2,5-4,5 dengan
menambahkan NaOH 5N.
3.3.Prosedur
2.3.1. Pembuatan larutan
1. Larutan Dithiver
Dimasukkan 50 ml kloroform kedalam gelas ukur 50 ml. Ditambahkan 1 bungkus
bubuk reagen logam dithiver. Ditutup gelas ukur lalu dikocok beberapa saat
2. Larutan standar NaOH 5 N
Ditimbang sebanyak 20 g, kemudian dilarutkan dengan aquadest dalam labu ukur
100 ml dan ditepatkan sampai tanda tera, lalu dihomogenkan.
3. Larutan H2SO4 5,25 N
Dipipet 26,28 mL H2SO4 19,98 N dimasukkan kedalam labu ukur 100 mL,
kemudian ditambahkan aquades sampai tanda tera, lalu dihomogenkan.
2.3.2. Prosedur analisa
1. Ditekan power alat spektrofotometer DR 2010.
2. Ditekan stored programs dan dipilih 280 lead Dithizone.
3. Ditekan start dan layar akan menampilkan “ Dial nm to 515 “ diputar pengatur
panjang gelombang hingga muncul 515 nm, layar akan menampilkan mg/L Pb.
4. Diisi sampel air sebanyak 250 ml kedalam gelas ukur 250 ml dan dipindahkan
kedalam labu ekstraksi 500 ml.
5. Ditambahkan 1 bungkus bubuk buffer sitrat. Ditutup labu ekstraksi lalu dikocok
hingga larut.
6. Dimasukkan 30 ml larutan Dithiver kedalam labu ekstraksi . Ditutup lalu dikocok
beberapa kali dan dibuka stopcock untuk melepaskan udara dan tutup stopcock.
7. Ditambahkan 5 ml larutan standart NaOH 5 N
8. Ditutup dan dikocok labu ekstraksi lalu dibuka stopcock untuk melepaskan udara.
Ditutup stopcock dan dikocok labu ekstraksi sekali atau 2 kali dan kemudian
Jika larutan berwarna orange setelah dikocok menunjukkan pH tinggi.
Ditambahkan beberapa tetes H2SO4 5,25 N kedalam larutan untuk menurunkan
pH. Warna biru kehijauan akan muncul lagi maka ulangi dengan sampel baru dan
digunakan NaOH lebih sedikit.
9. Dilanjutkan dengan penambahan larutan standar NaOH 5 N beberapa tetes dan
dikocok labu ekstraksi sampai warna larutan setelah dikocok berubah dari biru
kehijauan menjadi orange.
10.Ditambahkan 5 tetes larutan standart NaOH warna merah muda pada lapisan
bawah (kloroform) tidak menunjukkan adanya Timbal hanya setelah penambahan
KCN pada langkah berikutnya terbentuk warna merah muda menunjukkan adanya
Timbal.
11.Ditambahkan 2,0 g KCN kedalam labu ekstraksi. Ditutup labu ekstraksi lalu
dikocok sampai KCN larut (sekitar 15 detik).
12.Diletakkan labu ekstraksi pada support ring dan stand, dan ditunggu 1 menit
untuk pemisahan lapisan. Lapisan bawah (kloroform) berwarna merah muda
menunjukkan adanya Timbal.
13.Dimasukkan sedikit kapas pada bagian ujung labu ekstraksi lalu dibuka kran
secara perlahan dan dimasukkan kedalam kuvet 25 ml. Timbal-Dithizone
kompleks akan stabil selama 30 menit bila kuvet tetap tertutup rapat dan terhindar
dari cahaya.
14.Dimasukkan 25 ml larutan kloroform kedalam kuvet 25 ml sebagai blanko.
15.Dimasukkan blanko kedalam cell holder lalu ditekan “ZERO” pada alat. Pada
dimasukkan kedalam cell holder pastikan dinding luar dari kuvet terbebas dari
kotoran, noda dan lemak.
16.Dimasukkan sampel uji kedalam cell holder dan ditekan “READ” untuk
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil
Hasil pemeriksaan sampel air baku Delitua yang dilaksanakan di Laboratorium PDAM
Tirtanadi Provinsi Sumatera Utara.
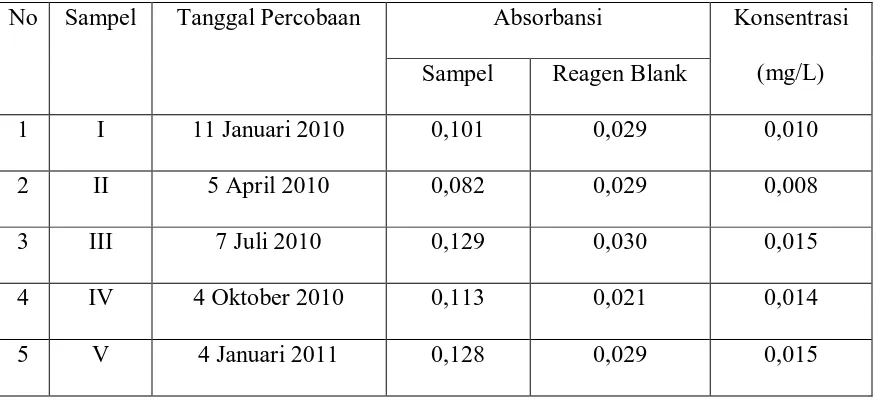
Tabel 4.1. Hasil analisa kadar Timbal pada sampel air baku Delitua
No Sampel Tanggal Percobaan Absorbansi Konsentrasi
(mg/L) Sampel Reagen Blank
1 I 11 Januari 2010 0,101 0,029 0,010
2 II 5 April 2010 0,082 0,029 0,008
3 III 7 Juli 2010 0,129 0,030 0,015
4 IV 4 Oktober 2010 0,113 0,021 0,014
4.2. Perhitungan
4.2.1. Penentuan Persamaan Garis Regresi
Kuvet 25 ml – DR 2010 – Dengan Reagen Blank = 0,029
TIMBAL (0 – 160 mg/L)
No Faktor Konsentrasi Absorbansi XiYi
X1 X2 X3 X4 X5 Xi Xi2 Y1 Y2 Y3 Y4 Y5 Yi Yi2
Maka persamaan garis regresinya adalah :
Y = a x + b
Y = 0,0063X + 0,003
4.2.2. Penentuan Koefisien Korelasi
4.2.3. Grafik Linieritas Parameter Uji Pb (DR-2010)
Untuk Grafik Linier, menggunakan faktor (sebagai Xi) dan Yi :
X 0 5 15 25 30 35 40 60 70 80 90 100
Y 0,000 0,045 0,093 0,152 0,190 0,228 0,258 0,371 0,429 0,508 0,574 0,629
Grafik 4.1. Grafik Linieritas Parameter Uji Pb (DR-2010)
Konsentrasi sampel dapat dihitung dengan mensubstitusikan harga absorbansi dan reagen
blank kedalam persamaan garis regresi y = ax + b, maka untuk sampel dapat dihitung
dengan, x =
Persamaan garis regresi : Y = 0,0063 X + 0,003
X =
a. Sampel I
Absorbansi :
Sampel (Y”) = 0,101
Reagen Blank (RB) = 0,029
Y = Y” - RB
= 0,101 – 0,029
= 0,072
b. Sampel II
Absorbansi :
Sampel (Y”) = 0,082
Reagen Blank (RB) = 0,029
= 0,082 – 0,029
= 0,053
c. Sampel III
Absorbansi :
Sampel (Y”) = 0,129
Reagen Blank (RB) = 0,030
Y = Y” - RB
= 0,129 – 0,030
= 0,099
d. Sampel IV
Absorbansi (Y”) = 0,113
Reagen Blank (RB) = 0,021
Y = Y” - RB
= 0,113 – 0,021
e. Sampel V
Absorbansi :
Sampel (Y”) = 0,128
Reagen Blank (RB) = 0,029
Y = Y” - RB
= 0,128 – 0,029
= 0,099
4.3 Pembahasan
Timbal atau Plumbum (Pb) adalah logam yang bersifat lunak, mudah dibentuk,
tahan korosi (pengkaratan) dan lain sebagainya, sehingga banyak digunakan oleh
manusia.
Tetapi timbal juga merupakan polutan (bahan pencemar) yang pada perairan
ditentukan dalam bentuk terlarut dan tersuspensi. Dalam konsentrasi tertentu timbal bisa
besifat toksik yang berakibat buruk terutama bagi manusia dan hewan karena dapat
terakumulasi pada jaringan tulang. Juga dapat merusak jaringan saraf, fungsi ginjal,
Adapun kadar maksimum timbal berdasarkan Peraturan Pemerintah Republik
Indonesia No. 82 Tanggal 14 Desember 2001 (Baku Mutu Kelas I) untuk air baku adalah
0,03 mg/L.
Sementara itu hasil analisa di Laboratorium PDAM Tirtanadi Provinsi Sumatera
Utara melalui metode Dithizone dengan menggunakan Spektrofotometer DR-2010
diperoleh kadar timbal pada air baku Delitua adalah sebagai berikut : pada sampel I
adalah 0,010 mg/L, sampel II adalah 0,008 mg/L, sampel III adalah 0,015 mg/L, sampel
IV adalah 0,014 mg/L dan sampel V adalah 0,015 mg/L. Dengan demikian kadar timbal
pada air baku Delitua tidak melebihi kadar maksimum yang telah ditetapkan.
Juga air baku Delitua yang berasal dari sungai, sepanjang alirannya sampai
digunakan menjadi air baku, memang melintasi daerah pedesan, tetapi tidak melintasi
daerah perkotaan dan kawasan industri. Sebab itulah pencemaran yang masuk ke badan
air kemungkinan tidak terlalu mempengaruhinya. Karena berupa limbah rumah tangga
(domestik), buangan asap kendaraan bermotor yang jumlahnya tidak banyak, sehingga
kadar timbal (Pb) yang terkandung didalamnya pun relatif sedikit. Hal ini tentu saja
menjadi salah satu rendahnya kadar timbal pada air baku Delitua.
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Sesuai dengan hasil analisa air baku Delitua di Laboratorium PDAM Tirtanadi
Provinsi Sumatera Utara diketahui bahwa kadar timbal (Pb) pada air tersebut berkisar
antara 0,008 mg/L sampai dengan 0,015 mg/L. Sementara itu kadar maksimum timbal
berdasarkan Peraturan Pemerintah Republik Indonesia No. 82 Tanggal 14 Desember
2001 untuk air baku adalah 0,03 mg/L. Dengan demikian dapat disimpulkan bahwa air
baku Delitua memenuhi persyaratan untuk diolah menjadi air yang higienis dan aman
dikonsumsi.
5.2. Saran
Dalam menganalisa timbal (Pb) atau unsur lainnya pada air, penulis berikut
hendaknya menggunakan metode lain yang lebih akurat, sehingga diperoleh hasil yang
DAFTAR PUSTAKA
Chandra,B. 2006. Pengantar Kesehatan Lingkungan. Cetakan Pertama. Jakarta : Penerbit Buku Kedokteran EGC.
Darmono. 2001. Lingkungan Hidup dan Pencemaran. Jakarta : Penerbit Universitas Indonesia (UI-Press).
Departemen Farmakologi dan Terapeutik. 2007. Farmakologi dan Terapi. Edisi Kelima. Jakarta : Penerbit Universitas Indonesia (UI-Press).
Effendi,H. 2003. Telaah Kualitas Air. Cetakan Ketiga. Yogyakarta : Penerbit Kanisius. Fardiaz,S. 1992. Polusi Air dan Udara. Cetakan Kedelapan. Yogyakarta : Penerbit
Kanisius.
Gabriel,J.F. 2001. Fisika Lingkungan. Cetakan Pertama. Jakarta : Penerbit Hipokrates. Kistanto,P. 2002. Ekologi Industri. Yogyakarta : Penerbit Andi.
Mahida,U.N. 1984. Pencemaran Air dan Pemanfaatan Limbah Industri. Cetakan Pertama. Jakarta : Penerbit CV. Rajawali.
Palar,H. 1994. Pencemaran dan Toksikologi Logam Berat. Jakarta : Penerbit Rineka Cipta.
Ryadi,S. 1984. Pencemaran Air. Surabaya : Penerbit Karya Anda.
Supardi,I. 2003. Lingkungan Hidup dan Kelestariannya. Edisi kedua. Cetakan Kedua. Bandung : Penerbit PT. Alumni.
Suriawiria,U. 2005. Air dalam Kehidupan dan Lingkungan yang Sehat. Bandung : Penerbit PT. Alumni.
Sutrisno,T. 2004. Teknologi Penyediaan Air Bersih. Cetakan Kelima. Jakarta : Penerbit Rineka Cipta.
Wardhana,W.A. 2001. Dampak Pencemaran Lingkungan. Edisi Kedua. Cetakan Pertama. Yogyakarta : Penerbit Andi.
LAMPIRAN
Lampiran 1. Tabel Peraturan Pemerintah Republik Indonesia No. 82 Tanggal 14 (Baku Mutu Kelas I) Desember 2001 Tentang Standar Kualitas Air Baku
No. Parameter Satuan Kadar
Maksimum Yang
Diperbolehkan
14. Sianida (CN) mg/L 0,02 Spektrofotometer
15. Sulfat (SO4) mg/L 400 Spektrofotometer
16. Sulfida (H2S) mg/L 0,002 Spektrofotometer
17. Tembaga (Cu) mg/L 0,02 Spektrofotometer
23. Kadmium (Cd) mg/L 0,01 Spektrofotometer
24. Timbal (Pb) mg/L 0,03 Spektrofotometer
C . Kimia Organik
1. Zat Organik (sebagai KMnO4)
mg/L - SNI
06-6989.22-2004
D. Mikrobiologi
1. Total Coliform Jlh/100ml 1000 SNI 06-4158-1996 2. Faecal Colioform Jlh/100ml 100 SNI