UJI PENGEMBANGAN DAN EFEK IRITASI SECARA HISTOLOGI DARI MATRIKS KALSIUM ALGINAT KITOSAN YANG
MENGANDUNG ASPIRIN
SKRIPSI
OLEH:
YULI DWI PAYANTI NIM 071524086
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
UJI PENGEMBANGAN DAN EFEK IRITASI SECARA HISTOLOGI DARI MATRIKS KALSIUM ALGINAT KITOSAN YANG
MENGANDUNG ASPIRIN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
YULI DWI PAYANTI NIM 071524086
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
UJI PENGEMBANGAN DAN EFEK IRITASI SECARA HISTOLOGI DARI MATRIKS KALSIUM ALGINAT KITOSAN YANG
MENGANDUNG ASPIRIN OLEH:
YULI DWI PAYANTI NIM 071524004
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal : Juli 2011
Pembimbing I, Panitia Penguji,
Dra. Anayanti Arianto, M.Si., Apt. Prof. Dr. Karsono, Apt. NIP 195306251986012001 NIP 195409091982011001
Pembimbing II, Dra. Anayanti Arianto, M.Si., Apt.
NIP 195306251986012001
dr. Alya Amila Fitrie, M.Kes NIP 197610042001122002
Dr. Edy Suwarso, SU., Apt.
NIP 130935857
Drs. David Sinurat, M.Si., Apt. NIP 194912281978031002
Medan, Juli 2011 Fakultas Farmasi Universitas Sumatera Utara
Dekan,
Uji Pengembangan, Uji Disolusi, Dan Efek Iritasi Secara Histologi Dari Matriks Kalsium Alginat-Kitosan Yang Mengandung Aspirin
Abstrak
Larutan natrium alginat bila dicampurkan dengan larutan kalsium klorida akan membentuk gel kalsium alginat. Kalsium alginat sebelumnya telah
digunakan dalam sistem pelepasan obat terkontrol. Kalsium alginat. dapat direaksikan dengan kitosan membentuk kompleks polielektrolit yang dapat digunakan untuk pembuatan matriks dari obat yang bersifat mengembang dan bertahan dalam lambung. Aspirin digunakan sebagai obat analgetik, antipiretik, dan anti inflamasi, namun demikian aspirin dapat menyebabkan iritasi pada saluran pencernaan. Tujuan penelitian ini adalah untuk melihat pengembangan, laju pelepasan obat, serta mengetahui efek iritasi dari matriks kalsium alginat-kitosan yang mengandung aspirin.
Matriks dibuat dengan mencampurkan 80 mg aspirin dengan campuran dari perbandingan yang sama antara alginat dengan kitosan, lalu ditambahkan mucilago amili 5 % (b/v) sampai terbentuk masa yang kompak, masa ini lalu dibulatkan menjadi butir-butir matriks dan di rendam dalam larutan CaCl2 0,15 M selama 35 menit, lalu dikeringkan selama 3 hari pada suhu kamar. Pengujian pengembangan dilakukan dengan melihat perubahan berat dan diameter dalam medium pH 1,2, pH 6,8, dan pH berganti dari masing-masing formula yakni Formula I aspirin dengan alginat : kitosan (10mg : 10mg), Formula II aspirin dengan alginat : kitosan (30mg : 30mg), Formula III aspirin dengan alginat : kitosan (60mg : 60mg). Uji efek iritasi terhadap saluran cerna dilakukan terhadap 17 ekor kelinci, yang dibagi menjadi 5 kelompok, kelompok I tanpa pemberian obat (kontrol) sebanyak 1 ekor, kelompok II pemberian aspirin dalam kapsul gelatin sebanyak 1 ekor, kelompok III Formula I sebanyak 5 ekor, kelompok IV Formula II sebanyak 5 ekor , kelompok V Formula III sebanyak 5 ekor.
Hasil yang diperoleh pada uji pengembangan menunjukkan bahwa matriks formula III lebih cepat mengembang dari pada formula I dan II.. Semua kelinci yang diberi ketiga formula menunjukkan iritasi pada lambung secara histologi, sedangkan 10 kelinci yang di berikan formula I dan II menunjukkan iritasi secara makroskopik, namun formula III tidak menunjukkan iritasi.
Swelling, Dissolution Testing, Stock And Irritation In Histology Of Calcium Alginate-Chitosan Matrix Containing Aspirin
Absrtract
Sodium alginate solution when mixed with a solution of calcium chloride to form calcium alginate gel. Calcium alginate has been previously used in controlled drug release system. Calcium alginate. can be reacted with chitosan to form complex polyelectrolytes which can be used for the manufacture of the drug matrix that is expanded and survive in the stomach. Aspirin is used as analgesics, antipyretics, anti-inflammatory, however, aspirin can cause irritation of the digestive tract . The purpose of this study is to see swelling as well as the rate of drug release and also know the effect iritasi from chitosan matrix of calcium alginate containing aspirin.
The matrix is made by mixing 80 mg of aspirin with a mixture of the same comparison between the alginate with chitosan, and then added mucilago amili 5% (w / v) to form the compact, this period then rounded to the matrix grains and soak in a solution of CaCl2 0,15 M for 35 minutes, then dried for 3 days at room temperature. Swelling is done by seeing changes in weight and diameter in the medium pH 1.2, pH 6.8, and pH change of each of the Formula I of aspirin with alginate: chitosan (10mg:10mg), Formula II aspirin with alginate: chitosan (30mg:30mg), Formula III aspirin with alginate : chitosan (60mg:60mg). The dissolution test was performed at medium pH 1.2. Test the effects of irritation to the gastrointestinal tract performed on 17 rabbits, divided into 5 groups, group I without medication (control) of a tail, the second group of aspirin in gelatin capsule as much as 1 rabbits, group III Formula I by a 5 rabbits, the group IV Formula II as much as 5 rabbits, Formula III V group of 5 rabbits.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT ... iv
DAFTAR ISI ... v
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 5
1.5 Manfaat Penelitian ... 5
1.6 Kerangka Konsep Penelitian...6
BAB II. TINJAUAN PUSTAKA...7
2.1 Uraian Umum ... 7
2.2 Dosis Aspirin ... 7
2.3 Efek samping Aspirin ... 7
2.4 Farmakokinetika Aspirin ... 8
2.5 Alginat ... 7
2.6 Kitosan ... 7
2.8 Saluran Pencernaan... 8
2.9 Mekanisme terjadi perdarahan pada lambung... 8
2.10 Preparasi jaringan ... 7
BAB III METODOLOGI PENELITIAN ... 7
3.1 Alat - Alat ... 7
3.2 Bahan - Bahan ... 7
3.3 Hewan percobaan ... 7
3.4 Pembuatan Pereaksi ... 8
3.5 Pembuatan kurva serapan dan kurva kalibrasi asam salisilat .... 9
3.5.1 Pembuatan larutan induk baku medium pH 1,2 ... 9
3.9 Pengamatan makroskopik ... 14
3.10 Pengamatan mikroskopik ... 14
3.11 Pembuatan preparat jaringan organ lambung ... 15
BAB IV HASIL DAN PEMBAHASAN... 17
4.1 Pembuatan matriks kalsium alginat-kitosan yang mengandung aspirin ... 17
4.2.1 Pengaruh konsentrasi alginat dan kitosan terhadap Disolusi matriks dalam medium pH 1,2 pada
suhu 37±0.5oC ... 18
4.3 Uji pengembangan matriks kalsium alginat-kitosan secara
In Vitro ... 20
4.3.1 Uji pengembangan matriks kalsium alginat-kitosan pada medium pH1,2 ... 20
4.3.2 Uji pengembangan matriks kalsium alginat-kitosan pada medium pH 6,8. ... 23
4.3.3 Uji pengembangan matriks kalsium alginat-kitosan pada medium pH berganti ... 26
4.4 Pengamatan efek iritasi pada saluran cerna kelinci ... 30
4.4.1 Pengamatan efek iritasi pada saluran cerna kelinci tanpa pemberian obat... 30
alginat-kitosan (10 mg : 10 mg)... 38
4.4.4 Pengamatan efek iritasi pada saluran cerna kelinci yang diberi aspirin dalam matriksk alginat-kitosan
4.4.5 Pengamatan efek iritasi pada saluran cerna kelinci yang diberi aspirin dalam matriksk alginat-kitosan
BAB V KESIMPULAN DAN SARAN ... 51
5.1 Kesimpulan ... 51
5.2 Saran ... 51
DAFTAR PUSTAKA ... 52
DAFTAR TABEL
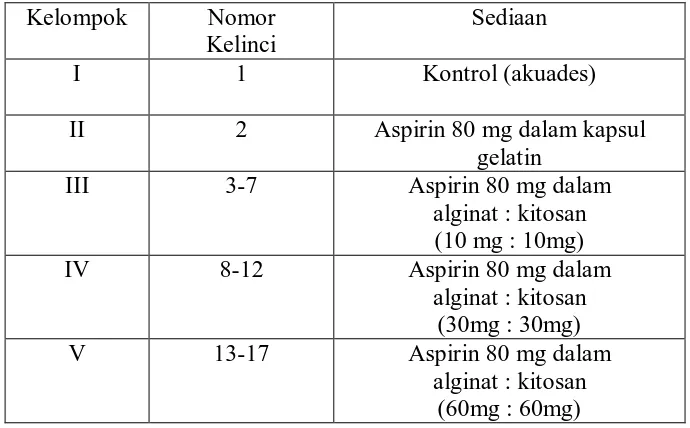
Tabel 1. Kelompok pengujian efek Iritasi terhadap saluran cerna kelinci dari matriks kalsium alginat-kitosan yang
mengandung aspirin ... 14
Tabel 2. Pelepasan aspirin dari matriks kalsium alginat-kitosan dalam
medium pH 1,2 pada suhu 37±0.5oC ... 18
Tabel 3. Perubahan berat dan diameter pada perendaman matriks dalam medium pH 1,2 pada suhu 37±0.5oC ... 20
Tabel 4. Perubahan berat dan diameter pada perendaman matriks dalam medium pH 6,8 pada suhu 37±0.5oC ... 23
DAFTAR GAMBAR
Gambar 1. Formula I (alginat : kitosan 10mg : 10 mg) ... 17
Gambar 2. Formula II (alginat : kitosan 30 mg: 30 mg) ... 17
Gambar 3. Formula III (alginat : kitosan 60 mg: 60 mg) ... 18
Gambar 4. Grafik pelepasan aspirin dari matriks kalsium alginat-kitosan dalam medium pH 1,2 pada suhu 37oC±0,5oC ... 19
Gambar 5. Grafik pertambahan berat matriks selama perendaman dalam medium pH 1.2 pada suhu 37±0.5oC ... 21
Gambar 6. Grafik perubahan diameter matriks selama perendaman dalam medium pH 1.2 pada suhu 37±0.5oC ... 21
Gambar 7. Foto pengembangan matriks pada menit ke-240 menit dalam medium pH 1,2 pada suhu 37±0,50C ... 22
Gambar 8. Foto pengembangan matriks pada menit ke-480 menit dalam medium pH 1,2 pada suhu 37±0,50C ... 23
Gambar 9. Grafik pertambahan berat matriks selama perendaman dalam medium pH 6,8 pada suhu 37±0.5oC ... 24
Gambar 10. Grafik perubahan diameter matriks selama perendaman
dalam medium pH 6,8 pada suhu 37±0.5oC ... 24
Gambar 11. Foto pengembangan matriks pada menit ke-240 menit dalam medium pH 6,8 pada suhu 37±0,50C ... 25
Gambar 12. Foto pengembangan matriks pada menit ke-480 menit dalam medium pH 6,8 pada suhu 37±0,50C ... 26
Gambar 14. Grafik perubahan diameter matriks selama perendaman dalam medium pH berganti pada suhu 37±0.5oC ... 27
Gambar 15. Foto pengembangan matriks pada menit ke-240 menit dalam medium pH berganti pada suhu 37±0,50C ... 28
Gambar 16. Foto pengembangan matriks pada menit ke-480 menit dalam medium pH berganti pada suhu 37±0,50C ... 29
Gambar 17. Foto makroskopik lambung kelinci tanpa pemberian obat
(pemberian akuades) ... 30
Gambar 18. Foto makroskopik usus halus kelinci tanpa pemberian obat (pemberian akuades) ... 31
Gambar 19. Foto makroskopik kolon kelinci tanpa pemberian obat
(pemberian akuades) ... 31
Gambar 20. Foto mikroskopik jaringan lambung kelinci tanpa
pemberian obat (pemberian akuades) dengan pewarnaan
Hematoxylin Eosin ... 31
Gambar 21. Foto makroskopik lambung, usus halus, dan kolon kelompok kelinci yang diberi aspirin dalam kapsul
gelatin... 33
Gambar 22. Foto mikroskopik lambung, duodenum, dan ileum kelinci yang diberi aspirin dalam kapsul gelatin dengan
pewarnaan Hematoxylin Eosin ... 35
Gambar 23. Foto makroskopik lambung kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
(10 mg: 10 mg) ... 36
Gambar 24. Foto makroskopik usus halus kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
Gambar 25. Foto makroskopik kolon kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
(10 mg : 10 mg) ... 38
Gambar 26. Foto mikroskopik lambung kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan (10 mg : 10 mg)
dengan pewarnaan Hematoxylin Eosin ... 39
Gambar 27. Foto makroskopik lambung kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
(30 mg: 30 mg) ... 40
Gambar 28. Foto makroskopik usus halus kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
(30 mg : 30 mg) ... 41
Gambar 29. Foto makroskopik kolon kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
(30 mg : 30 mg) ... 42
Gambar 30. Foto mikroskopik lambung kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan (30 mg : 30 mg)
dengan pewarnaan Hematoxylin Eosin ... 44
Gambar 31. Foto makroskopik lambung kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
(60 mg: 60 mg) ... 46
Gambar 32. Foto makroskopik usus halus kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
(60 mg: 60 mg) ... 47
Gambar 33. Foto makroskopik kolon kelompok kelinci yang diberi aspirin dalam matriks kalsium alginat-kitosan
dalam matriks kalsium alginat-kitosan (60 mg : 60 mg)
DAFTAR LAMPIRAN
Lampiran 1. Bagan alur pembuatan matriks kalsium alginat-kitosan ... 53
Lampiran 2. Bagan alur uji pengembangan ... 54
Lampiran 3. Bagan alur pemeriksaan makroskopik saluran cerna ... 56
Lampiran 4. Bagan alur pemeriksaan mikroskopik saluran cerna... 57
Lampiran 5. Data uji pengembangan matriks formula I alginat:kitosan (10 mg : 10 mg) dalam medium pH 1,2; 6,8 dan pH berganti ... 58
Lampiran 6. Data uji pengembangan matriks formula II alginat:kitosan (30 mg : 30 mg) dalam medium pH 1,2; 6,8 dan pH berganti ... 59
Lampiran 7. Data uji pengembangan matriks formula III alginat:kitosan (60 mg : 60 mg) dalam medium pH 1,2; 6,8 dan pH berganti ... 60
Lampiran 98 Data rat-rata uji pengembangan matriks formula I,II,dan III . dalam medium pH 1,2; 6,8 dan pH berganti ... 61
Lampiran 9. Data rat-rata pertambahan berat (%) matriks formula I,II, dan III dalam medium pH 1,2; 6,8 dan pH berganti ... 63
Lampiran 10. Foto alat mikrotom ... 83
Lampiran 111. Foto alat oven ... 84
Lampiran 213 Foto blok parafin ... 86
Lampiran 14. Foto perendaman dalam alkohol pada proses
KATA PENGANTAR
Puji syukur kehadirat Allah Subhana wata’ala yang telah memberi rahmat
dan karuniya-Nya, sehingga penulis dapat menyelesaikan penelitian dan penulisan
skripsi ini untuk memenuhi syarat dalam mencapai gelar sarjana farmasi di
Fakultas Farmasi Universitas Sumatera Utara. Terima kasih dan rasa hormat yang
besar kepada Ayahanda H.Supian dan Ibunda Hj.Anizar yang tercinta, serta
kepada abang dan adik ku yang selalu mendukung, memberi semangat dan do’a
kepada penulis selama masa perkuliahan hingga selesainya skripsi ini.
Penulis menyadari dalam penulisan skripsi ini banyak mendapatkan
bimbingan, bantuan, dan fasilitas yang sangat berharga dari berbagai pihak. Pada
kesempatan ini dengan segala kerendahan hati penulis juga ingin mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Ibu Dra. Anayanti Arianto M.Si., Apt dan dr. Alya Amila Fitrie, M.Kes
sebagai pembimbing I dan pembimbing II yang telah membimbing penulis
dengan penuh kesabaran dan tanggung jawab selama penelitian hingga
selesainya penulisan skripsi ini.
2. Bapak Prof. Dr. Sumadio Hadisahputra, Apt sebagai Dekan Fakultas
Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas
kepada penulis sehingga dapat menyelesaikan pendidikan.
3. Bapak Prof. Dr. Karsono, Apt, Dr. Edy Suwarso, SU., Apt, Drs. David
Sinurat, M.Si, Apt selaku dosen penguji yang telah memberikan masukan
dalam penulisan skripsi ini.
4. Bapak dan Ibu pengajar Fakultas Farmasi Universitas Sumatera Utara
5. Bapak kepala Laboratorium Farmasi Fisik beserta staf yang telah banyak
memberikan fasilitas dan bantuan selama penelitian.
6. Sahabat-sahabat ku dan teman-teman mahasiswa/i Fakultas Farmasi
Universitas Sumatera Utara khususnya ekstensi 2007 yang telah
memberikan bantuan dan dorongan kepada penulis selama perkuliahan
hingga selesainya pendidikan.
Semoga Allah subhana wata’ala melindungi dan melimpahkan rahmat dan
karunia-Nya kepada kita semua. Penulis berharap semoga skripsi ini menjadi
sumbangan yang berarti bagi ilmu pengetahuan khususnya dibidang Farmasi.
Medan, Juli 2011 Penulis
Uji Pengembangan, Uji Disolusi, Dan Efek Iritasi Secara Histologi Dari Matriks Kalsium Alginat-Kitosan Yang Mengandung Aspirin
Abstrak
Larutan natrium alginat bila dicampurkan dengan larutan kalsium klorida akan membentuk gel kalsium alginat. Kalsium alginat sebelumnya telah
digunakan dalam sistem pelepasan obat terkontrol. Kalsium alginat. dapat direaksikan dengan kitosan membentuk kompleks polielektrolit yang dapat digunakan untuk pembuatan matriks dari obat yang bersifat mengembang dan bertahan dalam lambung. Aspirin digunakan sebagai obat analgetik, antipiretik, dan anti inflamasi, namun demikian aspirin dapat menyebabkan iritasi pada saluran pencernaan. Tujuan penelitian ini adalah untuk melihat pengembangan, laju pelepasan obat, serta mengetahui efek iritasi dari matriks kalsium alginat-kitosan yang mengandung aspirin.
Matriks dibuat dengan mencampurkan 80 mg aspirin dengan campuran dari perbandingan yang sama antara alginat dengan kitosan, lalu ditambahkan mucilago amili 5 % (b/v) sampai terbentuk masa yang kompak, masa ini lalu dibulatkan menjadi butir-butir matriks dan di rendam dalam larutan CaCl2 0,15 M selama 35 menit, lalu dikeringkan selama 3 hari pada suhu kamar. Pengujian pengembangan dilakukan dengan melihat perubahan berat dan diameter dalam medium pH 1,2, pH 6,8, dan pH berganti dari masing-masing formula yakni Formula I aspirin dengan alginat : kitosan (10mg : 10mg), Formula II aspirin dengan alginat : kitosan (30mg : 30mg), Formula III aspirin dengan alginat : kitosan (60mg : 60mg). Uji efek iritasi terhadap saluran cerna dilakukan terhadap 17 ekor kelinci, yang dibagi menjadi 5 kelompok, kelompok I tanpa pemberian obat (kontrol) sebanyak 1 ekor, kelompok II pemberian aspirin dalam kapsul gelatin sebanyak 1 ekor, kelompok III Formula I sebanyak 5 ekor, kelompok IV Formula II sebanyak 5 ekor , kelompok V Formula III sebanyak 5 ekor.
Hasil yang diperoleh pada uji pengembangan menunjukkan bahwa matriks formula III lebih cepat mengembang dari pada formula I dan II.. Semua kelinci yang diberi ketiga formula menunjukkan iritasi pada lambung secara histologi, sedangkan 10 kelinci yang di berikan formula I dan II menunjukkan iritasi secara makroskopik, namun formula III tidak menunjukkan iritasi.
Swelling, Dissolution Testing, Stock And Irritation In Histology Of Calcium Alginate-Chitosan Matrix Containing Aspirin
Absrtract
Sodium alginate solution when mixed with a solution of calcium chloride to form calcium alginate gel. Calcium alginate has been previously used in controlled drug release system. Calcium alginate. can be reacted with chitosan to form complex polyelectrolytes which can be used for the manufacture of the drug matrix that is expanded and survive in the stomach. Aspirin is used as analgesics, antipyretics, anti-inflammatory, however, aspirin can cause irritation of the digestive tract . The purpose of this study is to see swelling as well as the rate of drug release and also know the effect iritasi from chitosan matrix of calcium alginate containing aspirin.
The matrix is made by mixing 80 mg of aspirin with a mixture of the same comparison between the alginate with chitosan, and then added mucilago amili 5% (w / v) to form the compact, this period then rounded to the matrix grains and soak in a solution of CaCl2 0,15 M for 35 minutes, then dried for 3 days at room temperature. Swelling is done by seeing changes in weight and diameter in the medium pH 1.2, pH 6.8, and pH change of each of the Formula I of aspirin with alginate: chitosan (10mg:10mg), Formula II aspirin with alginate: chitosan (30mg:30mg), Formula III aspirin with alginate : chitosan (60mg:60mg). The dissolution test was performed at medium pH 1.2. Test the effects of irritation to the gastrointestinal tract performed on 17 rabbits, divided into 5 groups, group I without medication (control) of a tail, the second group of aspirin in gelatin capsule as much as 1 rabbits, group III Formula I by a 5 rabbits, the group IV Formula II as much as 5 rabbits, Formula III V group of 5 rabbits.
BAB I PENDAHULUAN 1.1Latar Belakang
Alginat merupakan suatu polisakarida anionik yang diperoleh dari alga
coklat yang merupakan suatu polimer yang terdiri dari β-D asam manuronat (M)
dan α (1,4)-L asam guluronat (G). Polimer ini tidak bersifat toksik, tidak
memberikan reaksi alergi dan dapat teruai dalam tubuh (Mambo,2010). Natrium
alginat merupakan salah satu bentuk garam dari alginat. Salah satu sifat natrium
alginat adalah kemampuannya membentuk gel dengan penambahan larutan
garam-garam kalsium seperti kalsium klorida. Natrium alginat banyak digunakan
dalam bidang industri diantaranya: makanan, minuman, obat-obatan, kosmetik,
detergen, cat, textile, dan lain-lain. Dalam industri natrium alginat tersebut
digunakan sebagai pembentuk gel, pengemulsi dan penstabil, dan lain-lain
(Morris,et all, 1980).
Kitosan merupakan polisakarida kationik yang diperoleh melalui deasetilasi
kitin yang secara khusus ditemukan pada kulit binatang air berkulit keras seperti
kepiting dan udang. Kitosan telah dikenal dapat menjadi bahan yang baik sekali
untuk sediaan obat Karena polimer alami ini mempunyai keunggulan yang utama
seperti tidak toksik, biokompatibel, biodegradasi, mukoadesif, serta mampu
membentuk gel dan mengembang dalam suasana asam. Banyak kegunaan kitosan
didasarkan pada sifat kationik yang membuatnya dapat berinteraksi dengan
biomolekul bermuatan negatif seperti protein, polisakarida anionik dan asam
membentuk kompleks polielektrolit yang dapat digunakan untuk pembuatan
matriks dari obat yang dapat mengembang dan mempunyai sifat bertahan dalam
lambung sehingga dapat digunakan untuk pembuatan pelepasan obat terkontrol
(Mambo,2010).
Aspirin adalah obat anti nyeri yang tertua (1899) yang paling banyak
digunakan di seluruh dunia. Aspirin menimbulkan efek-efek spesifik seperti reaksi
alergi kulit dan telinga berdengung. Efek samping yang paling sering terjadi
berupa iritasi mukosa lambung dengan resiko tukak lambung dan perdarahan
samar. Penyebabnya adalah sifat asam dari aspirin, yang dapat dikurangi melalui
kombinasi dengan suatu antasid (MgO,aluminiumhidroksida,CaCO3)
(Tjay,2003).
Aspirin bersifat asam pada pH lambung, aspirin tidak dibebaskan, akibatnya
mudah menembus sel mukosa dan aspirin mengalami ionisasi dan terperangkap,
jadi berpotensi menyebabkan kerusakan sel secara langsung (Mycek,et al.,1995).
Suatu pengembangan obat AINS telah mengembangkan efikasi terapeutik
dan mengurangi efek samping pada saluran cerna bagian atas melalui pelepasan
yang dimodifikasi seperti sediaan salut enterik. Namun hal ini memungkinkan
terjadinya kenaikan pemaparan obat pada bagian duodenum dan oleh karena itu
meningkatkan toksisitas pada bagian duodenum. Obat AINS dalam bentuk salut
enterik telah diasosiasikan dengan terjadinya perdarahan pada usus halus dan
usus besar, berupa ulkus dan perforasi. Suatu studi membandingkan perdarahan
yang diakibatkan aspirin biasa dengan aspirin dalam bentuk salut enterik
menunjukkan terjadinya peningkatan perdarahan pada saluran cerna oleh aspirin
tetap menunjukkan terjadinya peningkatan perdarahan dibandingkan kontrol.
Studi tersebut menyimpulkan bahwa dapat terjadi kegagalan mengabsorbsi
aspirin dalam bentuk salut enterik pada pasien, terutama pasien dewasa, yang
menyebabkan tingginya konsentrasi obat yang tinggi pada ileum dan kolon dan
menyebabkan kerusakan pada saluran cerna (Davies, 2006).
Penelitian tentang alginat-kitosan sebagai bahan pembawa obat controlled
release semakin meningkat, salah satu peneliti yaitu Gaserod, dkk. (1999)
meneliti tentang pengaruh jumlah berat molekul kitosan dengan ikatan antara
alginat-kitosan. Dari hasil penelitian tersebut diketahui bahwa ikatan antara
alginat dan kitosan akan semakin meningkat seiring dengan menurunnya jumlah
molekul kitosan. Penelitian selanjutnya juga telah menguji efek iritasi kronik
lambung dengan pemberian kapsul alginat dan kapsul gelatin yang mengandung
aspirin. Hasil yang diperoleh aspirin dalam kapsul natrium alginat aman untuk
diberikan, sementara aspirin dalam kapsul gelatin menimbulkan iritasi pada
lambung (Susanti, 2006). Uji iritasi kronik aspirin juga telah di lakukan
sebelumnya dan memberikan hasil bahwa 2 dari 6 ekor kelici dengan pemberian
tablet salut enterik aspirin (Ascardia) secara kronik menimbulkan iritasi pada
bagian duodenum sedangkan pemberian kapsul alginat aspirin tidak menimbulkan
iritasi (Tandean,2009).
Uji perbandingan disolusi antara aspirin dalam matriks kalsium
alginat-kitosan dan aspirin dalam matriks kalsium alginat menunjukkan bahwa
penambahan kitosan pada matriks kalsium alginat dapat mempengaruhi laju
pH 6,8 sedangkan dalam medium pH berganti tidak menunjukkan pengaruh yang
signifikan ( Erani, 2006).
Berdasarkan hasil penelitian tersebut, maka dalam penelitian ini peneliti
ingin meneliti perbedaan pengaruh formulasi alginat kitosan terhadap efek iritasi
pada saluran pencernaan kelinci secara akut. Obat yang digunakan dalam
penelitian ini adalah aspirin. Aspirin merupakan obat yang paling sering
digunakan dan cukup efektif sebagai analgetik, antipiretik, antiinflamsi, dan
antiplatelet, namun mempunyai efek samping yang lebih sering dan lebih
berbahaya jka diberikan dalam dosis yang berlebihan.
1.2 Perumusan Masalah
Berdasarkan latar belakang diatas maka rumusan masalah penelitian adalah :
a. Pada formula matriks kalsium alginat-kitosan manakah lebih cepat
mengembang.
b. Pada formula matriks kalsium alginat-kitosan manakah yang dapat
mencegah efek iritasi.
1.3 Hipotesis
Berdasarkan perumusan masalah diatas maka dibuat hipotesis sebagai berikut:
a. Formula III matriks kalsium alginat-kitosan (60mg:60mg) yang
mengandung aspirin lebih cepat mengembang.
c. Formula III matriks kalsium alginat-kitosan (60mg:60mg) yang
mengandung aspirin dapat mencegah efek iritasi.
1.4 Tujuan
a. Untuk mengetahui sifat mengembang matriks kalsium alginat-kitosan
yang mengandung aspirin dari formula dengan jumlah alginat-kitosan
yang berbeda (Formula I, II, dan III).
b. Untuk mengetahui efek iritasi matriks kalsium alginat-kitosan yang
mengandung aspirin dari formula dengan jumlah alginat-kitosan yang
berbeda (Formula I, II, dan III).
1.5 Manfaat Penelitian
Sebagai bahan informasi mengenai aspirin dalam matriks alginat kitosan
dalam pengembangan sediaan untuk mengurangi efek iritasi saluran cerna
akibat dari pemberian obat aspirin.
1.6 Kerangka Konsep Penelitian
BAB II
TINJAUAN PUSTAKA
2.1. Uraian Umum
C O
OH
O C CH3
O
Gambar 1. Rumus bangun aspirin
Rumus Molekul : C9H8O4
Berat molekul : 180,16
Nama kimia : Asam asetil salisilat
Pemerian : Hablur putih, umumnya seperti jarum atau lempengan
tersusun, atau serbuk hablur putih, tidak barbau atau
barbau lemah. Stabil diudara kering, didalam udara
lembab secara bertahap terhidrolisa menjadi asam
salisilat dan asam asetat.
Kelarutan : Sukar larut dalam air, mudah larut dalam etanol, larut
dalam kloroform, dan dalam eter,agak sukar larut
Asam asetil salisilat yang lebih dikenal sebagai asetosal atau aspirin
merupakan salah satu senyawa yang secara luas digunakan, aspirin digunakan
sebagai obat analgetik, antipiretik, dan antiinflamasi yang sangat luas digunakan.
(Wilmana,1995).
2.2 Dosis Aspirin
Dosis aspirin secara oral untuk mendapatkan efek analgetik dan
antipiretik adalah 300-900 mg, diberikan setiap 4-6 jam dengan dosis maksimum
4 g sehari dan konsentrasi dalam plasma 150-300 mcg/ml. Untuk mendapatkan
efek antiinflamasi, doss yang digunakan adalah 4-6 g secara oral per hari. Untuk
mendapatkan efek antiagregasi platelet, dosis yang digunakan adalah 60-80 mg
secara oral per hari (Katzung, et al.,2004)
Dosis aspirin 80 mg per hari (dosis tunggal dan rendah) dapat
menghasilkan efek antiplatelet (penghambat agregasi trombosit). Secara normal,
trombosit tersebar dalam darah dalam bentuk tidak aktif, tetapi menjadi aktif
karena berbagai rangsangan. Membran luar trombosit mengandung berbagai
reseptor yang berfungsi sebagai sensor peka atas sinyal-sinyal fisiologik yang ada
dalam plasma. Efek antiplatelet aspirin adalah dengan menghambat sintesiss
tromboksan A2 (TXA2) dari asam arakidonat dalam trombosit oleh adana proses
asetilasi irreversibel dan inhibisi siklooksigenase, suatu enzim penting dalam
sintesis prostaglandin dan tromboksan A2 ( Mycek,et al.,1995).
2.3 Efek Samping Aspirin
Pada dosis biasa, efek samping utama aspirin adalah gangguan pada
lambung tidak terlarut sempurna dan partikel aspirin dapat berkontak langsung
dengan mukosa lambung. Akibatnya mudah merusak sel mukosa lambung
bahkan sampai timbul perdarahan pada lambung. Gejala yang timbul akibat
perusakan sel mukosa lambung oleh pemberian aspirin adalah nyeri epigastrum,
indigest rasa seperti terbakar, mual dan muntah. Oleh karena itu sangat
dianjurkan aspirin diberi bersama makanan dan cairan volume besar untuk
mengurangi gangguan saluran cerna (Katzung,et al.,2004).
2.4 Farmakokinetika Aspirin
Aspirin diabsorpsi dengan cepat dan praktis lengkap terutama di bagian
pertama duodenum. Namun, karena bersifat asam sebagian zat diserap pula di
lambung. Aspirin diserap dalam bentuk utuh, dihidrolisis menjadi asam salisilat
terutama dalam hati (Tjay, 2003).
2.5 Alginat
Alginat merupakan suatu polisakarida anionik yang diperoleh dari alga
coklat yang merupakan suatu polimer yang terdiri dari β-D asam manuronat (M)
dan α (1,4)-L asam guluronat (G). Polimer ini tidak bersifat toksik, tidak
memberikan reaksi alergi dan dapat teruai dalam tubuh (Mambo,2010). Natrium
alginat merupakan salah satu bentuk garam dari alginat. Salah satu sifat natrium
alginat adalah kemampuannya membentuk gel dengan penambahan larutan
garam-garam kalsium seperti kalsium klorida. Natrium alginat banyak digunakan
dalam bidang industri diantaranya: makanan, minuman, obat-obatan, kosmetik,
digunakan sebagai pembentuk gel, pengemulsi dan penstabil, dan lain-lain
(Morris,et all, 1980).
2.6 Kitosan
Kitosan merupakan polisakarida kationik yang diperoleh melalui deasetilasi
kitin yang secara khusus ditemukan pada kulit binatang air berkulit keras seperti
kepiting dan udang. Kitosan telah dikenal dapat menjadi bahan yang baik sekali
untuk sediaan obat Karena polimer alami ini mempunyai keunggulan yang utama
seperti tidak toksik, biokompatibel, biodegradasi, mukoadesif, serta mampu
membentuk gel dan mengembang dalam suasana asam. Kitosan mempunyai
aktivitas sebagai antasida yang mencegah atau mengurangi iritasi obat pada
lambung. Formula matriks kitosan muncul mengapung dan perlahan-lahan
mengembang dalam medium asam. Banyak kegunaan kitosan didasarkan pada
sifat kationik yang membuatnya dapat berinteraksi dengan biomolekul bermuatan
negatif seperti protein, polisakarida anionik dan asam nukleat. Maka alginat dan
kitosan yang berbeda muatan dapat berinteraksi membentuk kompleks
polielektrolit yang dapat digunakan untuk pembuatan matriks dari obat yang dapat
mengembang dan mempunyai sifat bertahan dalam lambung sehingga dapat
digunakan untuk pembuatan pelepasan obat terkontrol (Mambo,2010).
2.7 Matriks
Suatu matriks dapat digambarkan sebagai pembawa padat inert yang
didalamnya obat tercampur secara merata. Suatu matriks dapat dibentuk secara
bersama-sama. Sebagian besar bahan matriks tidak larut dalam air meskipun ada
beberapa bahan yang dapat mengembang secara lambat dalam air. Jenis matriks
dari pelepasan obat dapat dibentuk menjadi suatu bentuk atau butir-butir kecil
(Shargel dan Yu, 2005). Matriks dapat digolongkan menjadi 3 karakter yaitu :
a. Matriks tidak larut, inert
Polimer inert yang tidak larut seperti polietilen, polivinil klorida,
kopolimer akrilat-metakrilat dan etilselulosa telah digunakan sebagai
dasar untuk banyak formulasi di pasaran. Tablet yang dibuat dari
bahan-bahan ini di desain untuk dimakan dan tidak pecah dalam saluran cerna.
b. Matriks tidak larut, terkikis
Matriks jenis ini mengontrol pelepasan obat melalui difusi pori dan erosi.
Bahan-bahan yang termasuk dalam golongan ini adalah asam asetat,
stearil alkohol, malam carnauba, polietilen glikol monostearat dan
trigliserida.
c. Matriks hidrofilik
Sistem ini mampu mengembang dan diikuti oleh erosi dari bentuk gel
sehingga obat dapat terdisolusi dalam media air. Media hidrofilik
diantaranya adalah metil selulosa, hidroksietil selulosa, hidroksipropil
metilselulosa, natrium karboksimetilselulosa dan natrium alginat. Bila
bahan-bahan tersebut berkontak dengan air, maka akan terbentuk lapisan
matriks terhidrasi. Lapisan ini bagian luarnya akan mengalami erosi
2.8 Saluran Pencernaan 2.8.1 Lambung
Lambung adalah organ berbentuk huruf J terletak pada bagian kiri atas
rongga perut di bawah diafragma. Lambung terdiri dari epitel selapis toraks
dengan lekukan-lekukan, sehingga terbentuk lubang-lubang pada permukaaan
lambung. Lubang-lubang ini merupakan muara dari kelenjar-kelenjar lambung.
Lambung dapat diregangkan sehingga mampu menampung sejumlah besar
makanan. Lambung terdiri dari kardia, fundus, korpus dan antrum. Lekukan
sebelah medal disebut kurvatur minor sedangkan sebelah lateral disebut kuvatur
mayor. Di sebelah atas di antara kardia dan esofagus terdapat penempitan yang
disebut sfinkter esofagus. Di sebelah bawah di antara pilorus dengan duodenum
terdapat penyempitan lain yang disebut sfinkter pilorus. Kedua sfinkter ini harus
membuka sewaktu makanan melaluinya (Leeson,1985).
Lambung terdiri dari empat lapisan umum yaitu : mukosa, submukosa,
muskularis, dan serosa. Epitel pelapis permukaan dan sumur lambung adalah
epitel selapis silindris, dan menghasilkan mucus. Sel – sel epitel itu sekitar 20-40
mikrometer, intinya bulat dan mengandung banyak granul mukosa (Junquiera,
2005).
2.8.2 Usus Halus
Usus halus panjang dan bergelung (berbelit-belit) dalam rongga abdomen,
panjang usus halus adalah sekitar 10-14 kaki. Usus halus terdiri atas 3 bagian :
duodenum, jejunum, dan ileum. Duodenum panjangnya sekitar 25 cm, mulai dari
pirolus sampai jejenum. Pemisahan duodenum dan jejenum ditandai oleh
perlima bagian terminalnya adalah ileum. Pada usus halus terdapat vilus yang
merupakan tonjolan kecil mirip jari atau daun pada membran mukosa. Vili
duodenum merupakan bangunan lebar mirip spatula, tetapi di ileum bentuknya
mirip jari. Untuk memperluas permukaan, sel silindris absorptif yang meliputi
vili terdiri atas banyak mikrovilus. Masing –masing mikrovilus diliputi oleh
membran plasma yang lapisan luarnya dilengkapi dengan jala filamen halus
(Leeson,1985).
2.8.3 Usus Besar
Usus besar merupakan tabung muskular berongga dengan panjang sekitar
5 kaki(sekitar 1,5 m). Diameter usus besar lebih besar dari usus halus. Diameter
rata-rata sekitar 2,5 inci (sekitar 6,5 m), tetapi semakin mendekati anus
diameternya semakin kecil. Usus besar mempunyai bernagai fungsi yang
semuanya berkaitan dengan proses akhir di usus. Fungsi usus besar yang paling
penting adalah absorpsi air dan elektrolit (Price dan Wilson, 1994).
2.9 Mekanisme Terjadi Perdarahan Pada Lambung
Obat-obat anti inflamasi nonsteroid (AINS) termasuk aspirin dapat
menyebabkan terjadinta perdarahan karena kristal-kristal obat berkontak
langsung dengan mukosa lambung. Aspirin merusak mukosa lambung sehingga
mengubah permeabilitas sawar epitel, memungkinkan difusi balik asam klorida
dengan akibat kerusakan jaringan khususnya pembuluh darah. Histamin
dikeluarkan, merangsang sekresi asam dan pepsin, sejumlah protein plasma dapat
hilang sehingga mukosa kapiler dapat rusak dan dapat mengakibatkan perdarahan
2.10 Preparasi Jaringan 2.10.1 Fiksasi
Fiksasi adalah suatu usaha manusia untuk mempertahankan
elemen-elemen sel atau jaringan agar tetap pada tempatnya dan tidak mengalami
perubahan bentuk maupun ukuran. Untuk mencapai tujuan tersebut maka para ahli
sitologi berusaha mencari suatu media yang terdiri dari unsure-unsur kimia, yang
kemudian dibuat suatu larutan. Media ini kemudian disebut fiksatif. Dalam hal
ini digunakan formaldehid sebagai fiksatif. Formaldehid diketahui dapat
mengeraskan jaringan bahkan dapat mengendapkan protein jaringan, terutama bila
yang digunakan formaldehid 40%. Oleh karena itu konsentrasi yang biasa
digunakan untuk fiksasi adalah 4%-10% (Jones,1985).
2.10.2 Pencucian dan Dehidrasi
Setelah proses fiksasi maka dilakukan pencucian. Hal ini dimaksudkan
untuk menghilangkan larutan fiksatif dari jaringan. Setelah proses pencucian
selesai maka dilakukan dehidrasi. Istilah dehidrasi disini berarti penarikan
molekul air dari dalam jaringan. Proses ini dimaksudkan untuk menarik air yang
terdapat dalam jaringan agar nantinya seluruh ruangan antar sel dalam jaringan
dapat diisi oleh molekul-molekul parafin (Jones,1985).
Dalam proses ini, dehidran yang digunakan adalah alkohol.. Proses ini
biasanya dimulai dari alkohol persentase rendah kemudian setingkat demi
setingkat menuju ke alkohol persentase tinggi(alkohol absolute). Proses ini
dimaksudkan untuk menjaga agar tidak terjadi perubahan yang tiba-tiba terhadap
sel jaringan, sehingga perubahan struktur sel yang terjadi sekecil mungkin
2.10.3 Penjernihan (clearing) dan infiltrasi Parafin
Pada proses penjernihan digunakan xilol atau xylene. Proses ini
dimaksudkan untuk menarik alkohol atau dehidran yang lain dalam jaringan, agar
nantinya dapat digantikan oleh molekul parafin (Jones,1985).
Setelah proses penjernihan , selanjutnya dimulai proses infiltrasi parafin.
Parafin yang digunakan adalah yang titik cairnya berkisar 50-56 ºC. Proses ini
seluruhnya dikerjakan di dalam oven. Waktu yang diperlukan oleh suatu jaringan
di dalam campuran zat parafin murni tidak terlalu lama cukup berkisar antara 60
menit. Jaringan dipindahkan mulai dari parafin I, parafin II, parafin III, hal ini
dimaksudkan agar jaringan mendapatkan suatu lingkungan parafin yang
betul-betul murni. Selain itu tingkatan parafin ini dimaksudkan untuk mencegah
tertahannya sejumlah besar zat penjernih di dalam jaringan, karena akan
melunakkan jaringan dan membuat jaringan sukar diiris. Setelah proses ini maka
dibuatlah suatu blok jaringan sehingga diperoleh massa yang keras dan padat
sehingga dapat di potong menjadi jaringan yang tipis (Jones,1985).
2.10.4 Deparafinasi dan Pewarnaan
Deparafinasi adalah suatu proses menghilangkan parafin yang terdapat di dalam
jaringan. Proses ini dimaksudkan untuk mempermudah proses masuknya zat
warna ke dalam jaringan. Caranya adalah dengan merendam irisan jaringan ke
dalam xylene sekurang-kurangnya 15 menit. (Jones,1985).
Setelah proses deparafinasi dilakukan proses pewarnaan. Kebanyakan
jaringan tidak berwarna sehingga sulit memeriksa jaringan yang tidak di warnai di
histologik bersifat seperti senyawa asam atau basa dan mempunyai
kecenderungan membentuk ikatan garam dengan gugus-gugus jaringan yang
dapat berionisasi. Zat warna yang paling sering digunakan adalah hematoksilin
eosin (Junqueira dan Carneiro, 2005).
Jaringan tersebut tidak langsung dimasukkan ke dalam zat warna
hematoksilin tetapi direndam dahulu dengan larutan alcohol bertingkat dari
konsentrasi tinggi sampai ke konsentrasi rendah kemudian baru dicelupkan ke
dalam larutan hematoksilin. Hal ini dilakukan karena pewarna hematoksilin
adalah zat warna yang larut dalam air sehingga jaringan dari media xylene harus
dibawa ke media aquosa. Kemudian jaringan akan diwarnai dengan eosin 0,5%
(dalam alkohol 70%) yamg sebelumnya jaringan harus dimasukkan sebentar,
berturut-turut dari alkohol 30%, kemudian 50%, dan 70% (Jones,1985).
Eosin banyak digunakan sebagai background stain atau disebut juga
counterstain, yaitu zat warna yang berfungsi untuk memberikan warna yang
kontras dengan zat warna yang diberikan oleh zat warna yang terdahulu (jones,
BAB III
METODOLOGI PENELITIAN
3.1 Alat – Alat
Neraca listrik (Mettler Toledo), alat disolusi metode dayumg(veego), pH
meter (Hanna), Stop Watch, kandang kelinci, kamera digital (Canon), jangka
sorong, timbangan kelinci (Warce-Liege), peralatan bedah, mikroskop cahaya dan
alat – alat laboratorium yang biasa digunakan.
3.2. Bahan – Bahan
Natrium alginat 300-400 cp adalah produk Wako Pure Chemical
industries, Ltd Japan, Kitosan diperoleh dari Funakoshi, Ltd Japan, kalsium
klorida, asam klorida, formalin, kloroform, etanol,natrium klorida produk Merck
KgA 6404, kalium dihidrogen fospat, natrium hidroksida produk Merck KgA
6404, kapsul gelatin diperoleh dari Brataco Chemica Medan .
3.3. Hewan percobaan yang digunakan pada uji iritasi
Kelinci sebanyak 17 ekor dengan perincian sebagai berikut :
Kelompok I : tanpa pemberian obat (kontrol) : 1 ekor
Kelompok II : pemberian aspirin dalam kapsul gelatin : 1 ekor
Kelompok III : Formula I pemberian aspirin dengan alginat : kitosan
(10mg : 10mg) : 5 ekor
Kelompok IV : Formula II pemberian aspirin dengan alginat : kitosan
(30mg : 30mg) : 5 ekor
Kelompok V : Formula III pemberian aspirin dengan alginat : kitosan
3.4. Pembuatan pereaksi
3.4.1. Pembuatan larutan Kalsium Klorida 0,15 M
Kalsium Klorida sebanyak 16,65 gram dilarutkan dalam akuades
secukupnya sampai 1000 ml (DitJen POM, 1995).
3.4.2 Pembuatan larutan fisiologis 0,9%
Natrium klorida sebanyak 0,9 gram dilarutkan dalam akuades secukupnya
sampai 100 ml (DitJen POM, 1995).
3.4.3 Pembuatan larutan formalin 10 %
Formalin pekat (40%) sebanyak 25 ml diencerkan dengan akuades
secukupnya sampai 100 ml (Jones,1950)..
3.4.4 Pembuatan larutan Bouin
Asam pikrat 5 % b/v sebanyak 75 ml dicampurkan dengan 25 ml formalin
dan 5 ml asam asetat glasial (Jones,1950)..
3.4.5 Pembuatan Albumin Meyer
Natrium salisilat sebanyak 1 gram dicampur dengan putih telur dan gliserin
masing - masing sebanyak 50 ml (Jones,1950)..
3.4.6 Pembuatan alkohol 70%, 80%, 90%, 95%, dan 96%
Alkohol absolut sebanyak masing – masing 70 ml; 80 ml; 90 ml; 95 ml; 96
ml masing – masing diencerkan dengan akuades sampai 100 ml
(Jones,1950).
3.4.7 Pembuatan larutan Hematoxylin Erlich
Hematoxylin sebanyak 0,67 gram dilarutkan dalam alkohol absolut
sebanyak 33 ml kemudian ditambahkan gliserol sebanyak 33 ml, asam asetat
3.4.8 Pembuatan Larutan Eosin 0,5%
Eosin sebanyak 0,5 gram dilarutkan dalam 100 ml alkohol 95% dan
dicampurkan dengan asam asetat glasial sebanyak 0,5 ml (Jones,1950).
3.4.9 Pembuatan Medium pH 1,2
Natrium klorida sebanyak 2 gram ditambahkan dengan asam klorida pekat
sebanyak 7 ml, lalu tambahkan akuades hingga 1000 ml (DitJen POM,
1995).
3.4.10 Pembuatan Medium pH 4,5
Natrium asetat trihidrat 2,99 gram ditambahkan dengan 1,66 ml asam
asetat glasial lalu di larutkan dengan akuades hingga 1000 ml (DitJen
POM, 1995).
3.4.11 Pembuatan Medium pH 6,8
Kalium dihidrogen fosfat sebanyak 6,8 gram di larutkan dalam 250 ml
akuades, lalu ditambahkan dengan natrium hidroksida 0,2 N sebanyak 112
ml, lalu ditambahkan akuades hingga 1000 ml (DitJen POM, 1995).
3.4.12 Pembuatan larutan natrium hidroksida 0,2 N
Natrium hiroksida sebanyak 8 gram dilarutkan dalam akuades secukupnya
sampai 1000 ml (DitJen POM, 1995).
3.5 Uji Pengembangan matriks
3.5.1 Parameter uji pengembangan matriks
Medium disolusi : a. Medium pH 1,2
b. Medium pH 6,8
c. Medium pH Berganti, yaitu :
- medium pH 4,5 selama 30 menit
- medium pH 6,8 selama 5,5 jam
Kecepatan pengadukan : 100 rpm
Volume medium : 900 ml
3.5.2 Prosedur uji pengembangan matriks kalsium alginat-kitosan Medium pH 1,2; medium pH 6,8
Kedalam wadah disolusi dimasukkan 900 ml medium disolusi dan diatur
suhu 37± 0,5ºC dengan kecepatan pengadukan alat disolusinya 100 rpm.
Kedalam wadah tersebut dimasukkan sebutir matriks kalsium alginat
kitosan yang terlebih dahulu telah di foto, ditimbang berat dan diukur
diameternya. Pada interval waktu tertentu matriks tersebut dikeluarkan
dan kemudian ditimbang berat dan diukur diameternya.Hal ini dilakukan
sebanyak 3 kali untuk masing-masing medium yang digunakan.
Medium pH Berganti
Pada 2 jam pertama yang digunakan adalah medium pH 1,2. Setelah itu
medium diganti dengan medium pH 4,5 selama 30 menit, selanjutnya
medium diganti dengan medium pH 6,8 dan di lanjutkan sampai 5 jam
30 menit.Pada interval waktu tertentu matriks tersebut dikeluarkan dan
3.6 Pembuatan matriks kalsium alginat - kitosan
Pembuatan untuk 10 matriks kalsium alginat- kitosan yang mengandung
aspirin dilakukan berdasarkan formula berikut:
Formula I alginat : kitosan (10 mg : 10mg) :
Aspirin 0,80 g
Natrium alginat 0,10 g
Kitosan 0,10 g
Mucilago amyli 5% secukupnya
Formula II alginat : kitosan (30mg : 30mg) :
Aspirin 0,80 g
Natrium alginat 0,30 g
Kitosan 0,30 g
Mucilago amyli 5% secukupnya
Formula III alginat : kitosan (60 mg : 60mg) :
Aspirin 0,80 g
Natrium alginat 0,60 g
Kitosan 0,60 g
Mucilago amyli 5% secukupnya
Aspirin dimasukkan kedalam lumpang lalu digerus, ditambah natrium
alginat, digerus homogen kemudian ditambahkan kitosan dalam jumlah yang
sama banyak dengan natrium alginat, sedikit demi sedikit ditambahkan mucilago
amyli secukupnya hingga diperoleh massa yang kompak. Untuk membulatkan
matriks digunakan lumpang berukuran kecil. Butir – butir matriks tersebut
menghasilkan matriks alginat kitosan yang telah sempurna bereaksi dengan
kalsium klorida, kemudian matriks dikeringkan dalam suhu kamar selama 3 hari.
3.7 Pengujian efek iritasi terhadap saluran cerna kelinci dari matriks kalsium alginat-kitosan yang mengandung aspirin.
Kelinci di beli di Brayan, lalu diadaptasi terhadap lingkungan, makanan,
dan minuman selama 1 minggu. Setelah diadaptasikan, kelinci tersebut telah dapat
digunakan sebagai hewan percobaan. Untuk pengujian efek iritasi lambung kelinci
ini, kelinci si bagi atas lima kelompok yaitu :
Tabel 1. Kelompok pengujian efek iritasi terhadap saluran cerna kelinci dari matriks kalsium alginat-kitosan yang mengandung aspirin.
Kelompok Nomor
Hewan percobaan dipuasakan terlebih dahulu selama 24 jam, kemudian
hewan percobaan di berikan obat sesuai kelompoknya masing – masing selama 24
jam.
Pengujian efek iritasi terhadap saluran cerna kelinci dilakukan dengan
3.8 Pengamatan makroskopik
Semua kelompok kelinci di bunuh dengan menggunakan kloroform secara
inhalasi dan dilakukan pembedahan untuk mengambil saluran cernanya.
Kemudian saluran cernanya di buka dan di cuci dengan larutan fisiologis, lalu
difoto dengan kamera digital untuk melihat apakah ada luka pada saluran
cernanya. Kemudian organ tersebut direndam dalam larutan formalin 10%.
3.9 Pengamatan mikroskopik
Lambung kelinci yang telah diamati secara makroskopik, kemudian diamati secara mikroskopik secara histologi.
3.10 Pembuatan Preparat Jaringan Organ Lambung
Organ lambung difiksasi dalam larutan formalin 10% selama 2 hari. Lalu
didehidrasi dalam alkohol bertingkat dimulai dengan merendam di dalam alkohol
70% v/v selama 30 menit, selanjutnya dalam alkohol 80% v/v, 90% v/v, 96% v/v,
dan alkohol absolut masing-masing selama 24 jam. Kemudian organ lambung
dijernihkan dalam xylol murni lebih kurang 2 x 30 menit. Lalu organ lambung
tersebut dimasukkan ke dalam larutan toluol parafin yang telah mencair di dalam
oven dengan volume 1:1 selama 60 menit. Selanjutnya berturut-turut organ
lambung tersebut dimasukkan dalam parafin murni I, II, III masing-masing 60
menit. Setelah organ lambung dimasukkan ke dalam cetakan yang berisi parafin
cair dan dibiarkan mengeras. Blok parafin cair yang berisi organ lambung tersebut
diiris setebal 6 µ m dengan menggunakan mikrotom kemudian irisan tersebut
diletakkan pada kaca objek yang telah diolesi dengan albumin meyer dan ditetesi
kaca objek. Lalu jaringan dimasukkan ke dalam larutan xylol selama 15 menit.
Setelah itu jaringan dicelupkan berturut-turut ke dalam alkohol absolut, 96% v/v ,
90% v/v, 80% v/v, 70% v/v, dan akuades. Kemudian dilakukan pewarnaan
terhadap jaringan dengan memasukkannya ke dalam larutan erlich hematosiklin
selama 3-7 detik dan selanjutnya dicuci dengan air mengalir lebih kurang 10
menit. Setelah itu dilakukan lagi pewarnaan dengan memasukkannya ke dalam
larutan eosin 0,5% selama 3 menit dan dilanjutkan dengan pencelupan dalam
alkohol 70% v/v, 80% v/v, 90% v/v, 96% v/v dan alkohol absolut, kemudian
dikeringkan dengan kertas penghisap, selanjutnya jaringan tersebut ditetesi
dengan kanada balsem dan ditutup dengan gelas penutup. Jaringan diamati
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pembuatan Matriks Kalsium Alginat-Kitosan Yang Mengandung Aspirin
Matriks kalsium alginat-kitosan yang mengandung aspirin dibuat dengan
cara mencampurkan aspirin dengan natrium alginat dan kitosan dengan jumlah
yang sama banyak (perbandingan 1:1). Lalu ditambahkan mucilago amili sedikit
demi sedikit. Penambahan mucilago amili 5% (b/v) berfungsi sebagai bahan
pengikat untuk memperoleh massa yang kompak dan dapat dibentuk. Dari hasil
percobaan diketahui bahwa untuk membuat 10 matriks formula I diperlukan
mucilago amili sebanyak 1,90 g, formula II sebanyak 2,.348 g, formula III
sebanyak 2,657 g. Massa yang telah dibulatkan menjadi butir- butir matriks
kemudian direndam dalam larutan kalsium klorida 0,15 M selama 35 menit.
Perendaman selama 35 menit bertujuan agar ion Ca2+ dari larutan CaCl2 dapat
bereaksi sempurna dengan natrium alginat-kitosan membentuk gel kalsium
alginat-kitosan dengan bentuk yang bulat, kuat dan keras. Setelah itu matriks
dikeringkan pada suhu kamar selama 3 hari untuk memperoleh matriks dengan
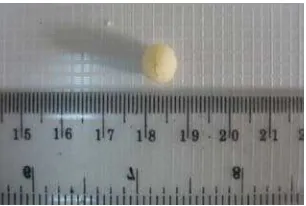
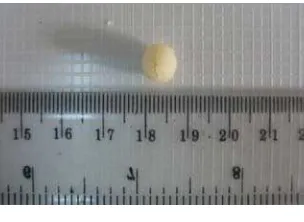
berat yang sudah stabil. Gambar matriks kalsium alginat-kitosan dapat dilihat
pada Gambar 6-8.
Gambar 6 Gambar 7
Gambar 8
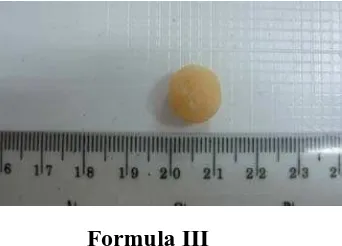
Matriks dengan Formula III alginat : kitosan (60 mg: 60 mg)
4.2 Uji Pengembangan Matriks Kalsium Alginat-Kitosan
Uji pengembangan matriks dilakukan untuk mengetahui sifat fisik matriks
dalam saluran pencernaan dengan melihat pengaruh medium terhadap perubahan
berat dan diameter matriks. Perubahan berat matriks dilakukan dengan
membandingkan selisih berat matriks sebelum dan setelah perendaman dengan
berat awal matriks, sedangkan perubahan diameter dilakukan dengan
membandingkan diameter setelah perendaman dengan diameter awal matriks.
4.2.1 Uji Pengembangan Matriks Kalsium Alginat-Kitosan pada Medium pH 1,2
Perubahan berat dan diameter matriks pada perendaman dalam medium
pH 1,2 pada waktu-waktu tertentu dapat dilihat pada tabel 2.
Tabel 2. Perubahan berat dan diameter pada perendaman matriks dalam medium pH 1,2 pada suhu 37±0,5oC. Tabel 2 menunjukkan bahwa pada t480, matriks formula I mengalami
mengalami perubahan berat menjadi 119,14% dan diameternya menjadi 9,266
mm, formula III mengalami perubahan berat menjadi 127,06% dan diameternya
menjadi 11,325 mm.
Grafik pengembangan matriks kalsium alginat-kitosan dapat dilihat pada
gambar 9 dan gambar 10.
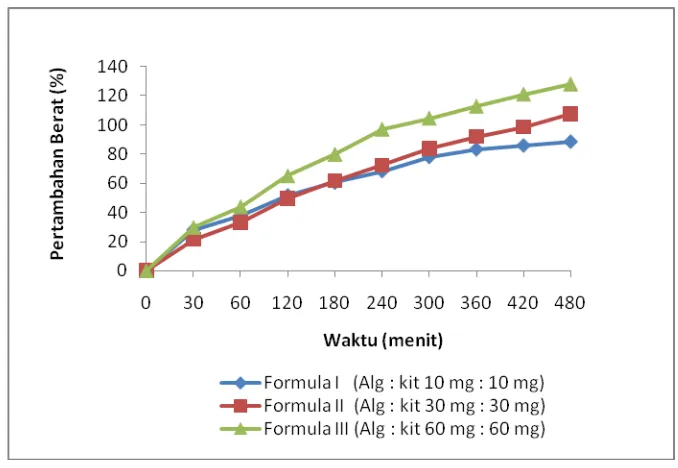
Gambar 9. Grafik pertambahan berat (%) matriks selama perendaman dalam
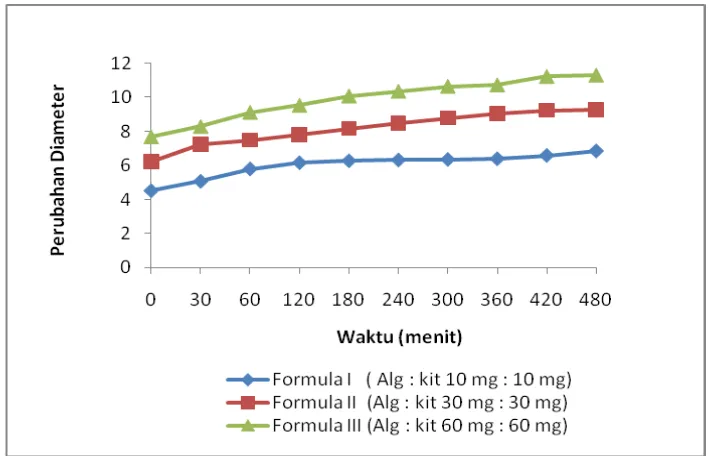
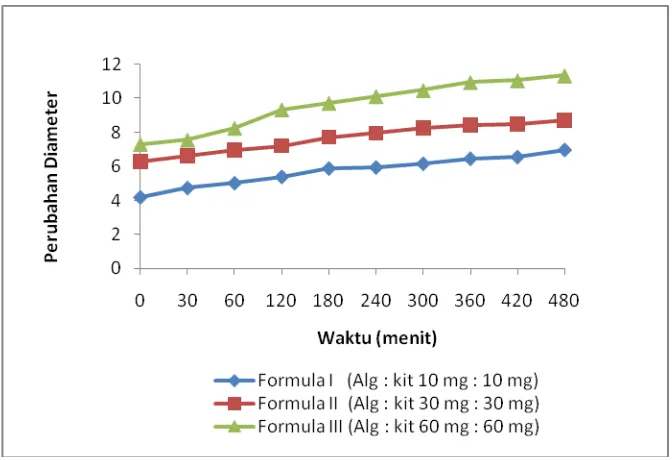
Gambar 10. Grafik perubahan diameter matriks selama perendaman dalam
medium pH 1,2 pada suhu 37±0,5oC.
Dari grafik diatas dapat dilihat bahwa semakin besar jumlah kitosan maka
pertambahan berat dan diameter semakin bertambah. Penambahan berat dan
diameter terjadi karena difusi air ke dalam pori-pori yang terdapat dalam matriks
kalsium alginat-kitosan. Pori-pori ini terbentuk karena pada saat pengeringan
partikel-partikel air meninggalkan matriks dan membentuk pori-pori kosong. Pada
saat matriks dimasukkan ke dalam medium pH 1,2 terjadi pengisian pori-pori
tersebut sehingga terjadi pertambahan berat dan diameter dari matriks tersebut.
Semakin besar jumlah kitosan maka pertambahan berat dan diameter semakin
bertambah, hal ini terjadi karena kitosan bersifat mengembang dalam medium
asam sehingga partikel air dapat berdifusi lebih banyak dan matriks menjadi
mengembang, ini terjadi karena adanya gugus amina (NH2) dari kitosan
membentuk gugus amina yang bermuatan kationik (NH3+) yang bersifat hidrofilik.
Dengan demikian, air dapat berdifusi ke dalam matriks dan membuat matriks
mengembang. Foto perbandingan dari ketiga formula pada medium ini dapat
dilihat dari gambar 11 dan 12.
Formula III
Gambar 11. Foto pengembangan matriks pada menit ke-240 menit dalam
medium pH 1,2 pada suhu 37±0,50C.
Formula I Formula II
Formula III
Gambar 12. Foto pengembangan matriks pada menit ke-480 menit dalam
medium pH 1,2 pada suhu 37±0,50C.
4.2.2 Uji Pengembangan Matriks Kalsium Alginat-Kitosan pada Medium Medium pH 6,8
Perubahan berat dan diameter matriks pada perendaman dalam medium
pH 6,8 pada waktu-waktu tertentu dapat dilihat pada tabel 3.
Tabel 3. Perubahan berat dan diameter pada perendaman matriks dalam medium
Formula
Pertambahan berat (%) Diameter Ф (mm) t30 t240 t480 t30 t240 t480
I 28,07% 68,42% 88,59% 4,738 5,938 6,96 II 21,42% 72,32% 107,58% 6,6 7,944 8,705 III 29,71% 97.,5% 128,16% 7,572 10,133 11,344
Tabel 3 menunjukkan bahwa pada t480, matriks formula I mengalami
perubahan berat menjadi 88,59% dan diameternya menjadi 6,96 mm, formula II
mengalami perubahan berat menjadi 107,58% dan diameternya menjadi 8,705
mm, formula III mengalami perubahan berat menjadi 128,16% dan diameternya
menjadi 11,344 mm.
Grafik pengembangan matriks kalsium alginat-kitosan dapat dilihat pada
gambar 13 dan gambar 14.
Gambar 13. Grafik pertambahan berat (%) matriks selama perendaman dalam
Gambar 14. Grafik perubahan diameter matriks selama perendaman dalam
medium pH 6,8 pada suhu 37±0,5oC.
Pengembangan matriks dalam medium pH 6,8 menunjukkan bahwa
pertambahan berat (%) matriks dan diameter terus bertambah. semakin besar
jumlah alginat maka pengembangan matriks semakin besar, hal ini disebabkan
karena asam alginat bereaksi dengan NaOH dan membentuk natrium alginat yang
bersifat hidrofilik sehingga matriks menjadi lebih mengembang Foto
perbandingan dari ketiga formula pada medium pH 6,8 ini dapat dilihat dari
gambar 15 dan 116.
Formula III
Gambar 15. Foto pengembangan matriks pada menit ke-240 menit dalam
medium pH 6,8 pada suhu 37±0,50C.
Formula I Formula II
Formula III
Gambar 16. Foto pengembangan matriks pada menit ke-480 menit dalam
medium pH 6,8 pada suhu 37±0,50C.
4.2.3 Uji Pengembangan Matriks Kalsium Alginat-Kitosan pada Medium pH berganti
Perubahan berat dan diameter matriks pada perendaman dalam medium
pH berganti pada waktu-waktu tertentu dapat dilihat pada tabel 4.
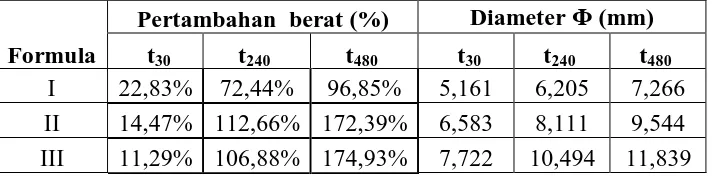
Tabel 4. Perubahan berat dan diameter pada perendaman matriks dalam medium
Formula
Pertambahan berat (%) Diameter Ф (mm) t30 t240 t480 t30 t240 t480
I 22,83% 72,44% 96,85% 5,161 6,205 7,266 II 14,47% 112,66% 172,39% 6,583 8,111 9,544 III 11,29% 106,88% 174,93% 7,722 10,494 11,839
Tabel 4 menunjukkan bahwa pada t480, matriks formula I mengalami
pertambahan berat menjadi 96,85% dan diameternya menjadi 7,266 mm, formula
II mengalami perubahan berat menjadi 172,39% dan diameternya menjadi 9,544
mm, formula III mengalami perubahan berat menjadi 106,88% dan diameternya
menjadi 11,839 mm.
Grafik pengembangan matriks kalsium alginat-kitosan dapat dilβihat pada
gambar 17 dan gambar 18.
Gambar 17. Grafik pertambahan berat matriks selama perendaman dalam
Gambar 18. Grafik perubahan diameter matriks selama perendaman dalam
medium pH berganti pada suhu 37±0,5oC.
Pengembangan matriks pada pH berganti diawali dengan pengembangan
pada medium pH 1,2 selama 2 jam, setelah itu diganti dengan medium 6,8 selama
6 jam. Pengembangan matriks dalam medium pH berganti menunjukkan bahwa
pertambahan berat (%) matriks dan diameter terus bertambah. Hal ini terjadi
karena pada waktu matriks di rendam dalam medium pH 1,2 kitosan yang ada
dalam matriks mengembang sehingga matriks juga mengembang, sementara
alginat menjadi bebas dan bereaksi dengan asam membentuk asam alginat yang
tidak larut. Setelah dimasukkan dalam medium pH 6,8 asam alginat bereaksi
dengan NaOH dan membentuk natrium alginat yang bersifat hidrofilik sehingga
matriks menjadi lebih mengembang. Foto perbandingan dari ketiga formula pada
Formula I Formula II
Formula III
Gambar 19. Foto pengembangan matriks pada menit ke-240 menit dalam
medium pH berganti pada suhu 37±0,50C.
Formula I Formula II
Formula III
Gambar 20. Foto pengembangan matriks pada menit ke-480 menit dalam
medium pH berganti pada suhu 37±0,50C.
Pengamatan efek iritasi pada saluran cerna kelinci dilakukan secara
makroskopik dan mikroskopik. Untuk pengamatan makroskopik organ saluran
cerna kelinci yang diamati meliputi lambung, usus halus, dan usus besar
sedangkan untuk pengamatan mikroskopik, organ yang diamati hanya meliputi
lambung.
4.3.1 Pengamatan Efek Iritasi pada Saluran Cerna Kelinci tanpa Pemberian Obat
4.3.1.1 Pengamatan Makroskopik Saluran Cerna Kelinci tanpa Pemberian Obat
Untuk melihat organ saluran cerna yang normal, maka dilakukan
pembedahan kelinci kelompok I tanpa pemberian obat. Kelinci dipuasakan
terlebih dahulu selama 24 jam, lalu dibedah dan diamati saluran cernanya. Hasil
pengamatan saluran cerna secara makroskopik dapat dilihat pada Gambar 17-19.
Kelinci 1
Gambar 21. Foto makroskopik lambung kelinci 1 tanpa pemberian obat
(pemberian akuades)
Dari Gambar 21 terlihat bahwa lambung kelinci dalam keadaan normal.
Tanda-tanda iritasi berupa luka, kemerahan maupun penipisan lapisan tidak
Gambar 22. Foto makroskopik usus halus kelinci 1 tanpa pemberian obat
(pemberian akuades)
Dari Gambar 22 terlihat bahwa usus halus kelinci dalam keadaan normal.
Tanda-tanda iritasi berupa luka, kemerahan maupun penipisan lapisan tidak
dijumpai pada usus halus kelinci.
Gambar 23. Foto makroskopik kolon kelinci 1 tanpa pemberian obat (pemberian
akuades)
Dari Gambar 23 terlihat bahwa usus besar kelinci dalam keadaan normal
(tidak terjadi iritasi).
4.3.1.2 Pengamatan Mikroskopik Lambung Kelinci tanpa Pemberian Obat
Untuk melihat sel-sel lambung normal pada hewan percobaan maka
lambung kelinci yang telah diamati secara makroskopik kemudian diamati lebih
lanjut secara mikroskopik. Hasil pengamatan mikroskopik lambung kelinci tanpa
Perbesaran 100 x
Perbesaran 400 x
Kelinci 1
Gambar 24. Foto mikroskopik jaringan lambung kelinci 1 tanpa pemberian obat
(pemberian akuades) dengan pewarnaan Hematoxylin Eosin
Dari Gambar 24 terlihat bahwa secara mikroskopik (histologi) lambung
kelinci dalam keadaan normal. Hal ini dapat dilihat dari struktur juluran–juluran
(sumur-sumur) pada permukaan epitel pada lapisan mukosa yang mengarah ke
lumen lambung.
Mukosa
Muskularis mukosa
Submukosa
Sumur-sumur
(Foveolae) Sel- sel epitel
4.3.2 Pengamatan Efek Iritasi pada Saluran Cerna Kelinci yang Diberi Aspirin dalam Kapsul Gelatin
4.3.2.1 Pengamatan Makroskopik Saluran Cerna Kelinci yang Diberi Aspirin dalam Kapsul Gelatin
Pada pengujian ini, kelinci diberikan aspirin dengan dosis 80 mg dan
dimasukkan ke dalam kapsul gelatin. Setelah 24 jam kelinci dibedah dan
dilakukan pengamatan makroskopik pada saluran cerna kelinci. Hasil pengamatan
makroskopik organ saluran cerna kelinci lambung, usus, dan kolon dapat dilihat
pada Gambar 25.
Lambung Usus
Kolon
Kelinci 2
Gambar 25. Foto makroskopik lambung, usus halus, dan kolon kelinci 2 yang
Dari Gambar 25 terlihat bahwa lambung dan usus halus kelinci yang diberi
dalam kapsul gelatin terlihat adanya luka kemerahan namun pada kolon tidak
terlihat adanya iritasi.
4.3.2.2 Pengamatan Mikroskopik Salurn Cerna Kelinci yang Diberi aspirin dalam Kapsul Gelatin
Lambung kelinci yang diberi aspirin dalam kapsul gelatin yang telah
diamati secara makroskopik kemudian diamati lebih lanjut secara mikroskopik.
Dari hasil pengamatan terlihat bahwa lambung dan usus halus kelinci yang diberi
dalam kapsul gelatin terlihat adanya luka kemarahan namun pada kolon tidak
terlihat adanya iritasi, Hal ini dapat dilihat pada Gambar 26.
Lambung
Perbesaran 100 x Perbesaran 400 x
Duodenum
Perbesaran 100 x Perbesaran 400 x
Ileum
Perbesaran 100 x Perbesaran 400 x
Kelinci 2
Gambar 26. Foto mikroskopik lambung, duodenum, dan ileum kelinci 2 yang
diberi aspirin dalam kapsul gelatin dengan pewarnaan Hematoxylin Eosin
Dari Gambar 26 terlihat bahwa lambung kelinci yang diberi aspirin dalam
kapsul gelatin mengalami iritasi yang ditandai dengan melebarnya sumur-sumur
pada lapisan mukosa dan menipisnya sel epitel. Pada duodenum dan ileum iritasi
ditandai dengan adanya pelebaran pembuluh darah.
4.3.3 Pengamatan Efek Iritasi pada Saluran Cerna Kelinci yang Diberi Aspirin dalam Matriks Kalsium Alginat-Kitosan (10 mg : 10 mg) 4.3.3.1 Pengamatan Makroskopik Saluran Cerna Kelinci yang Diberi Aspirin
dalam Matriks Kalsium Alginat-Kitosan (10 mg : 10 mg)
Pada pengujian ini, kelinci diberikan aspirin dalam matriks kalsium
alginat-kitosan (10 mg : 10 mg) dengan dosis 80 mg. Setelah 1 hari kelinci
tersebut dibedah dan dilakukan pengamatan makroskopik pada saluran cerna. Dari
hasil pengamatan terlihat bahwa secara makroskopik semua saluran cerna kelinci
mengalami iritasi Gambar 27 menunjukkan saluran cerna kelinci 3, 4, 5, 6 dan 7
yang diamati secara makroskopik.
Kelinci 3 Kelinci 4
Kelinci 5 Kelinci 6
Kelinci 7
Gambar 27. Foto makroskopik lambung kelinci no 3-7 yang diberi aspirin dalam matriks kalsium alginat-kitosan (10 mg: 10 mg)
Dari Gambar 23 terlihat bahwa secara makroskopik dijumpai adanya
tanda-tanda iritasi berupa luka, kemerahan maupun penipisan lapisan pada
lambung kelinci 3, 4, 5, 6, dan 7.
luka luka
luka
luka
Kelinci 3 Kelinci 4
Kelinci 5 Kelinci 6
Kelinci 7
Gambar 28. Foto makroskopik usus halus kelinci no 3-7 yang diberi aspirin
dalam matriks kalsium alginat-kitosan (10 mg : 10 mg)
Dari Gambar 28 terlihat bahwa secara makroskopik tidak dijumpai adanya
tanda-tanda iritasi berupa luka, kemerahan maupun penipisan lapisan pada usus
Kelinci 1 Kelinci 2
Kelinci 3 Kelinci 4
Kelinci 7
Gambar 29. Foto makroskopik kolon kelinci no 3-7 yang diberi aspirin dalam
matriks kalsium alginat-kitosan (10 mg : 10 mg)
Dari Gambar 29 terlihat bahwa secara makroskopik tidak dijumpai adanya
tanda-tanda iritasi berupa luka, kemerahan maupun penipisan lapisan pada usus
halus kelinci 3, 4, 5, 6, dan 7.
4.3.3.2 Pengamatan Mikroskopik Saluran Cerna Kelinci yang Diberi Aspirin dalam Matriks Kalsium Alginat-Kitosan (10 mg : 10 mg)
Lambung kelinci yang telah diamati secara makroskopik kemudian
diamati lebih lanjut secara mikroskopik. Dari hasil pengamatan terlihat bahwa
menipisnya sel-sel epitel dan terjadinya dilatasi pembuluh darah. Hal ini dapat
dilihat pada Gambar 30.
Perbesaran 100 x Perbesaran 400 x
Gambar 30. Foto mikroskopik lambung kelinci no 3-5 yang diberi aspirin
dalam matriks kalsium alginat-kitosan (10 mg : 10 mg) dengan pewarnaan Hematoxylin Eosin
Dari Gambar 30 terlihat bahwa secara mikroskopik lambung kelinci 3, 4,
dan 5 mengalami iritasi. Pada kelinci 3 iritasi ditandai dengan adanya penipisan