PREDIKSI KEBERADAAN
PELARGONIDIN-3-(FERULOIL)DIGLUKOSIDA-5-(MALONIL)
GLUKOSIDA FRAKSI TERLARUT ETIL ASETAT
DARI EKSTRAK METANOL DAUN TRENGGULI
(Cassia fistula)
ICHSAN IRWANTO
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Prediksi Pelargonidin-3-(feruloil)diglukosida-5-(malonil)glukosida pada Daun Trengguli (Cassia fistula) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
ICHSAN IRWANTO. Prediksi Keberadaan Pelargonidin-3-(feruloil)diglukosida-5-(malonil)glukosida Fraksi Terlarut Etil Asetat dari Ekstrak Metanol Daun Trengguli (Cassia fistula). Dibimbing oleh PURWANTININGSIH SUGITA dan GUSTINI SYAHBIRIN.
Studi pendahuluan telah dilakukan untuk mengidentifikasi komponen bioaktif pada daun trengguli (Cassia fistula). Secara tradisional, daun trengguli telah digunakan sebagai obat penyakit malaria. Hasil uji fitokimia pada ekstrak metanol daun trengguli dari Kebun Raya Bogor menggandung alkaloid, flavonoid, fenolik, tanin, dan steroid. Fraksionasi ekstrak metanol tersebut dilakukan dengan beberapa metode kromatografi dan hasil fraksionasi telah dianalisis dengan spektrometer resonans magnet inti dan kromatograf cair-spektrometer massa. Hasil analisis menunjukkan bahwa fraksi n-heksana-etil asetat 3:7 diduga mengandung pelargonidin-3-(feruloil)diglukosida-5-(malonil)glukosida dengan m/z 1019 dan beberapa jenis asam lemak.
Kata kunci: Cassia fitula, kromatografi, pelargonidin, trengguli
ABSTRACT
ICHSAN IRWANTO. Prediction of Pelargonidin-3-(feruloyl)diglucoside-5-(malonyl)glucoside Ethyl Acetate Soluble Fraction from Methanol Extract Trengguli (Cassia fistula) Leaves’. Supervised by PURWANTININGSIH SUGITA and GUSTINI SYAHBIRIN.
Preliminary study has been conducted to identify bioactive compounds in trengguli (Cassia fistula) leaves. Traditionally, C. fistula leaves were used for treatment of malaria disease. Phytochemical investigations on leaves’ methanol extract of C. fistula from Bogor Botanical Garden showed the presence of alkaloid, flavonoid, phenolic, tannin, and steroid. Fractionation of the methanol extract was conducted through some chromatography methods and the results have been analyzed with nuclear magnetic resonance spectrophotometer and liquid chromatograph-mass spectrometer. The analysis showed that the n -hexane-ethyl acetate 3:7 fraction was predicted to contain pelargonidin-3-(feruloyl) diglucoside-5-(malonyl)glucoside (m/z 1019) and various fatty acids.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
PREDIKSI KEBERADAAN
PELARGONIDIN-3-(FERULOIL)DIGLUKOSIDA-5-(MALONIL)
GLUKOSIDA FRAKSI TERLARUT ETIL ASETAT
DARI EKSTRAK METANOL DAUN TRENGGULI
(Cassia fistula)
ICHSAN IRWANTO
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi: Prediksi Keberadaan Pelargonidin-3-(feruloil)diglukosida-5 (malonil)glukosida pada Fraksi Terlarut Etil Asetat dari Ekstrak Metanol Daun Trengguli (Cassia fistula)
Nama : Ichsan Irwanto NIM : G44090035
Disetujui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Pembimbing I
Dr Dra Gustini Syahbirin, MS Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah yang berjudul Prediksi Keberadaan Pelargonidin-3-(feruloil)diglukosida-5-(malonil)glukosida Fraksi Terlarut dari Ekstrak Metanol Daun Trengguli (Cassia fistula) berhasil diselesaikan. Karya ilmiah ini diselesaikan dari bulan Februari hingga Oktober 2013 di Laboratorium Kimia Organik, Departemen Kimia, IPB.
Penulis mengucapkan terima kasih kepada Prof Dr Dra Purwantiningsih Sugita, MS selaku pembimbing utama dan Dr Dra Gustini Syahbirin, MS selaku pembimbing anggota yang telah memberikan bimbingan dan nasehat selama penelitian. Ucapan terima kasih juga disampaikan kepada Pusat Konservasi Tumbuhan Kebun Raya Bogor atas bantuannya menyediakan sampel daun C. fistula, kepada Pusat Penelitian Kimia (P2K) LIPI, Serpong atas izin menggunakan instrumen NMR dan LCMS. Di samping itu, penghargaan penulis sampaikan kepada Budi Arifin, MSi, Luthfan Irfana, SSi, dan Drs M Farid, MSi, atas segala saran dan diskusi bermanfaat dalam penyusunan karya ilmiah ini. Ungkapan terima kasih juga disampaikan kepada kedua orang tua, atas doa dan bantuan selama perkuliahan, penelitian, dan penulisan karya ilmiah ini dan kepada Pak Sabur, Bu Yenni, dan Bu Nia atas bantuan di laboratorium selama penelitian. Tak lupa disampaikan ucapan terima kasih kepada teman-teman seperjuangan Nisfiyah, Sigit, Febrina, Wahyu, dan Selvia atas segala dorongan dan semangat bagi penulis untuk menyelesaikan karya ilmiah ini. Semoga Allah SWT dapat membalas kebaikan semua. Amin.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN vii
PENDAHULUAN 1
BAHAN DAN METODE 2
Alat dan Bahan 2
Metode Penelitian 2
HASIL DAN PEMBAHASAN 3
Kadar Air dan Ekstraksi 3
Fitokimia Ekstrak Metanol 4
Komponen Kimia dalam Fraksi Polar Fraksi Terlarut Etil Asetat Ekstrak
Metanol 5
SIMPULAN DAN SARAN 11
Simpulan 11
Saran 11
DAFTAR PUSTAKA 11
LAMPIRAN 13
DAFTAR TABEL
1 Fitokimia ekstrak metanol daun trengguli 4
2 Fraksi-fraksi hasil KCV ekstrak EtOAc bebas klorofil dan tanin 5 3 Fraksi-fraksi hasil KKG fraksi E dengan elusi gradien berundak n-heksana-
DCM 6
DAFTAR GAMBAR
1 Kromatogram eluat hasil KCV ekstrak EtOAc bebas klorofil dan tanin dengan eluen CHCl3-MeOH (19:1), diamati di bawah lampu UV dengan
λ 366 nm 5
2 Kromatogram fraksi E menggunakan KKG 6
3 Pemisahan fraksi E4 menggunakan KR 7
4 Kromatogram fraksi E18 dalam eluen terbaik n-heksana-EtOAc (8:2),
diamati di bawah lampu UV 366 nm 7
5 Kromatogram fraksi E18-4 8
6 Spektrum massa puncak dominan dalam fraksi E18-4 9
7 Dugaan struktrur pelargonidin 9
8 Dugaan fragmentasi pelargonidin-3-(feruloil)diglukosida-5- (malonil) glukosida membentuk fragmen dengan m/z =187, 269, dan 926
(Montgomery et al. 2007) 10
DAFTAR LAMPIRAN
1 Bagan alir penelitian 13
2 Metode uji fitokimia 14
3 Kadar air simplisia sampel kering 14
4 Spektrum 1H NMR fraksi E4-1 16
5 Spektrum 1H NMR fraksi E4-2 17
PENDAHULUAN
Trengguli (Cassia fistula)merupakan salah satu tanaman obat yang tersebar di berbagai belahan dunia, seperti Asia, Afrika Selatan, Cina, India Barat, dan Brasil, dikenal sebagai golden shower (hujan mas) (Prashanth et al. 2006). Di Indonesia, trengguli banyak digunakan sebagai tanaman hias dan tidak jarang tumbuh secara alami sehingga mudah ditemukan di berbagai wilayah. Pemanfaatan trengguli di Indonesia baru sebatas obat tradisional untuk mengobati malaria dan sakit kudis. Berbagai manfaat trengguli telah banyak dilaporkan di India, misalnya sebagai analgesik, obat penyakit kulit, tekanan darah tinggi, dan radang mata (Rizvi et al. 2010). Selain itu, dalam pengobatan tradisional India (Ayurveda), Cassia juga digunakan sebagai obat pencahar dan bisa meredakan batuk.
Begitu banyaknya manfaat tanaman C. fistula sehingga telah banyak dilakukan penelitian untuk menguji komponen aktif yang terkandung di dalamnya. C. fistula yang tumbuh di India telah diketahui di antaranya berkhasiat sebagai antibakteri pada ekstrak biji (Ali et al. 2003), antimikrob, antioksidan, dan antiradang pada ekstrak kulit batang (Ali et al. 2004; Ilavarasan et al. 2005), serta antijamur pada ekstrak daun (Padma dan Pratina 2006).
Beberapa penelitian di India telah berhasil mengidentifikasi komponen metabolit sekunder trengguli. Bagian batangnya mengandung fistuasidin (Padmanabha dan Venkateswarlu 1965). Dari bagian kulit batang berhasil diisolasi senyawa oksiantrakuinon dan dihidroksiantrakuinon (Rani dan Kalidar 1998), dari bagian daun berhasil diisolasi senyawa (−)-epiafzelekin-3-O-glukosida, (−)-epikatekin, dan prosianidin B-2 (Kashiwada et al. 1996), asam heksadekanoat, vitamin E, asam 9, 12, 15-oktadekatrienoat (Bayu 2013) dan dari bagian bunga berhasil diisolasi kaemferol, tetramer leukopelargonidin (bebas glikol) (Narayanan dan Seshadri 1972), rein, fistulin, biantrakuinon glikosida, dan triterpena (Kumar et al. 1966). Bagian polongnya mengandung senyawa asam fistulat, 3-formil-1-hidroksi-8-metoksiantrakuinon, 3B-hidroksi-17-norpimar-8(9)-en-15-on (Misra et al. 1997), bagian akarnya mengandung 3-O-gentibiosida (Vaishnav dan Gupta 1996), dan dari bagian biji berhasil diisolasi senyawa krisofanol (Khanna dan Chandra 1996), serta 5-(2-hidroksifenoksimetil)furfural, (2'S)-7-hidroksi-5-hidroksimetil-2-(2'-hidroksipropil) kromon, benzil 2-hidroksi-3,6-dimetoksibenzoat, benzil 2β-O-D-glukopiranosil-3,6-dimetoksibenzoat, 5-hidroksimetilfurfural, dan (2'S)-7-hidroksi-2-(2'-hidroksipropil)-5-metilkromon (Kuo et al. 2002).
2
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan antara lain penguap putar, kromatografi cair vakum (KCV), kromatografi radial (KR), dan peralatan kaca di laboratorium. Instrumen spektrofotometer resonans magnet inti proton (1H NMR) dan kromatograf cair-spektrometer massa (LC-MS) terdapat di Pusat Penelitian Kimia (P2K) LIPI, Serpong. Bahan-bahan yang dipakai adalah daun trengguli yang diperoleh dari Kebun Raya Bogor, metanol teknis, etil asetat teknis, n-heksana teknis, diklorometana (DCM) teknis, kloroform teknis, aseton teknis, kloroform-amoniak, asam sulfat p.a. (Merck), pereaksi Meyer, Dragendorf, dan Wagner, dietil eter p.a., asam asetat glasial, serbuk Mg, asam klorida p.a. (Merck), pereaksi FeCl3 1%, silika gel Merck 60G untuk KCV, silika gel 60 (0.2−0.5 mm) untuk
impregnasi sampel, silika gel GF254 untuk KR, penampak noda Ce(SO4)2, dan
pelat kromatografi lapis tipis (KLT) GF254.
Metode Penelitian
Tahapan penelitian yang dilakukan meliputi penyiapan sampel, ekstraksi dengan metode maserasi, uji fitokimia, isolasi, dan pencirian komponen fraksi polar. Bagian alirnya disajikan dalam Lampiran 1.
Preparasi dan Ekstraksi
Daun trengguli dibersihkan, selanjutnya dikering-anginkan dan dihaluskan dalam blender sebelum dimaserasi dalam pelarut MeOH selama 24 jam sebanyak 3 kali ulangan. Ekstrak MeOH dikumpulkan kemudian dipekatkan dengan penguap putar hingga diperoleh ekstrak kasar. Klorofil dihilangkan dengan cara merendam ekstrak kasar dalam MeOH-air (1:1) selama 24 jam sebanyak 3 kali ulangan. Filtrat MeOH dipisahkan dari endapan klorofil dengan cara penyaringan gravitasi, kemudian dihilangkan taninnya melalui ekstraksi cair-cair menggunakan EtOAc sebanyak 3 kali ulangan. Lapisan air (bawah) diasumsikan mengandung tanin, lapisan EtOAc (atas) dipekatkan dengan penguap putar.
Penentuan Kadar Air (AOAC 2005)
Sebanyak 1 g simplisia dimasukkan ke dalam cawan porselen yang telah dipanaskan sebelumnya di dalam oven bersuhu 105 oC selama 30 menit sampai bobotnya konstan. Cawan porselen berisi sampel kemudian dipanaskan di dalam oven bersuhu 105 oC selama 3 jam lalu didinginkan dalam eksikator dan ditimbang. Pemanasan kembali dilakukan di dalam oven hingga diperoleh bobot konstan. Kadar air contoh ditentukan dengan persamaan
Kadar air (%) =
×
100% Keterangan: A = bobot contoh basah (g)Uji Fitokimia
Uji fitokimia ekstrak metanol dilakukan untuk mengetahui kandungan komponen metabolit sekunder seperti alkaloid, flavonoid, triterpenoid, saponin, tanin, dan steroid. Prosedur pengujian mengikuti prosedur standar dari Harborne (1996) pada Lampiran 2.
Penentuan Eluen Terbaik dan Jumlah Komponen dalam Fraksi Polar
Analisis jumlah komponen dilakukan dengan metode KLT. Pelarut yang diujikan ialah kloroform, etil asetat, metanol, etanol, dan aseton sebagai eluen tunggal. Dua jenis eluen, yaitu yang memiliki karakteristik nonpolar dan polar dicampur dengan berbagai komposisi untuk menentukan eluen yang menghasilkan noda terbanyak dan terbaik pemisahannya. Jumlah noda terbanyak tersebut diasumsikan sebagai jumlah komponen yang terkandung dalam ekstrak metanol dan eluennya diasumsikan sebagai eluen terbaik dalam pemisahan komponen (Zulhipri et al. 2007).
Pemisahan dan Pemurnian Komponen Fraksi Polar
Fraksi EtOAc bebas klorofil dan tanin dari ekstrak metanol daun trengguli difraksionasi lebih lanjut dengan metode KCV. Eluen yang digunakan adalah n -heksana-etil asetat yang ditingkatkan kepolarannya dan fase diam yang digunakan ialah silika gel. Eluat yang dihasilkan dianalisis pola pemisahannya dengan KLT menggunakan eluen terbaik. Eluat dengan pola pemisahan yang sama digabung menjadi 1 fraksi. Fraksi polar dimurnikan lebih lanjut menggunakan KR dengan eluen kloroform-metanol yang ditingkatkan kepolarannya. Hasil pemurnian dianalisis pola pemisahannya dengan KLT menggunakan eluen terbaik dan disemprot dengan penampak noda Ce(SO4)2. Prosedur KCV dan KR diulangi
apabila noda yang terbentuk belum tunggal. Pencirian Komponen dalam Fraksi Polar
Analisis komponen metabolit sekunder dilakukan dengan instrumen NMR merek Jeol® 500 MHz dan LC-MS merek Mariner Biospectrometry® yang dilengkapi dengan sistem pompa ganda. Kondisi kolomnya adalah Supelco 5 µm C18, 250 mm × 2 mm, sistem elusi isokratik dengan eluen metanol-air (95:5), laju alir eluen 1 mL/menit, injeksi volume sampel 10 µL, dengan suhu kolom sama dengan suhu kamar. Kolom dihubungkan dengan spektrometer massa dengan modus ionisasi semprotan-elektron (ESI) dan modus deteksi kuadrupol waktu-terbang (Q-TOF).
HASIL DAN PEMBAHASAN
Kadar Air dan Ekstraksi
4
kurang dari 10% menunjukkan bahwa simplisia daun trengguli dapat digunakan dalam jangka waktu lama tanpa ditumbuhi oleh mikrob (Winarno 1992).
Ekstrak kasar daun trengguli yang diperoleh dari hasil maserasi sebesar 406.75 g, berwujud pasta berwarna hijau tua. Metanol dipilih sebagai pelarut untuk maserasi di antaranya karena metanol dapat menerobos sebagian besar matriks bahan alam dan masuk ke dalam sel-sel daun untuk mengambil semua senyawa metabolit sekunder dalam daun (Hermawati 2009).
Selanjutnya klorofil dihilangkan dengan cara melarutkan ekstrak kasar metanol dalam metanol-air (1:1). Sebanyak 242.34 g ekstrak kasar dilarutkan dalam 2 L metanol-air (1:1). Endapan klorofil yang dihasilkan sebanyak 33.0 g. Pemisahan klorofil dengan metanol-air (1:1) didasarkan pada sifat klorofil yang larut baik dalam metanol, tetapi tidak larut dalam metanol-air (1:1), sehingga klorofil akan mengendap dalam bentuk gom yang berwarna hijau tua. Filtrat bebas klorofil yang diperoleh berwarna cokelat tua dan selanjutnya dipartisi dengan EtOAc untuk menghilangkan tanin ke dalam fase air. Fraksi EtOAc kemudian dipisahkan dan dipekatkan dengan penguap putar. Ekstrak bebas klorofil dan tanin ini diperoleh sebanyak 92.39 g.
Fitokimia Ekstrak Metanol
Hasil uji fitokimia (Tabel 1) menunjukkan bahwa ekstrak metanol daun trengguli mengandung senyawa metabolit sekunder golongan tanin, alkaloid, steroid, fenolik, dan flavonoid. Hasil uji fitokimia yang diperoleh berbeda dengan dilaporkan oleh Panda et al. (2011) dan Pandya et al. (2012). Hal ini disebabkan tempat dan lingkungan tumbuh yang berbeda, yaitu Bogor (Indonesia), Orissa (India), dan Gujarat (India).
Tabel 1 Fitokimia ekstrak metanol daun trengguli Golongan Hasil
Komponen Kimia dalam Fraksi Terlarut Etil Asetat dari Ekstrak Metanol
Tahapan setelah pemisahan klorofil dan tanin adalah fraksionasi komponen kimia dengan metode KCV. Sebanyak 21.72 g ekstrak EtOAc bebas klorofil dan tanin diimpregnasi dengan 40 g silika gel 60 (0.2−0.5 mm). Ekstrak tersebut dilarutkan dalam aseton hingga tepat larut dan diteteskan secara merata ke atas silika gel yang sudah berada dalam labu bulat. Silika yang telah mengimpregnasi contoh kemudian dikeringkan dengan menggunakan penguap putar.
Eluen yang digunakan dalam KCV adalah n-heksana dan EtOAc dengan sistem elusi gradient berundak. Deret eluen yang digunakan ialah n-heksana 100% (1× elusi); n-heksana-EtOAc 8:2 (3× elusi), 7:3 (3× elusi), 6:4 (2× elusi), dan 3:7 (2× elusi); EtOAc 100% (2× elusi); dan terakhir dicuci dengan MeOH 100% (8× elusi) dengan masing-masing 200 mL eluen per elusi. Sebanyak 21 eluat yang didapatkan diuji pola pemisahannya pada eluen terbaik, yaitu CHCl3-MeOH
(19:1). Hasil elusi ditunjukkan pada Gambar 1. Eluat-eluat yang memiliki pola keterpisahan yang hampir sama kemudian digabungkan. Secara keseluruhan diperoleh 7 fraksi dengan bobot dan rendemen yang disajikan pada Tabel 2.
Gambar 1 Kromatogram eluat hasil KCV ekstrak EtOAc bebas klorofil dan tanin dengan eluen CHCl3-MeOH (19:1), diamati di bawah lampu UV
dengan λ 366 nm
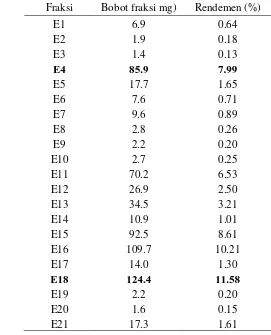
Tabel 2 Fraksi-fraksi hasil KCV ekstrak EtOAc bebas klorofil dan tanin Fraksi Bobot (g) Rendemen (%) Asal Fraksi
6
sehingga lebih mudah dipisahkan. Eluen yang digunakan dalam KKG adalah n -heksana-DCM secara gradien berundak. Fraksi E seluruhnya dipisahkan dengan KKG, dan eluat yang memiliki pola pemisahan hampir sama dengan eluen terbaik digabungkan. Secara keseluruhan diperoleh 21 fraksi (Tabel 3). Sebagai contoh, fraksi E1 didapat dari eluat a−f, fraksi E2 merupakan gabungan eluat g−h. Kromatogram hasil KKG dapat dilihat pada Gambar 2.
Gambar 2 Kromatogram fraksi E menggunakan KKG
Tabel 3 Fraksi-fraksi hasil KKG fraksi E dengan elusi gradien berundak n -heksana-DCM
Fraksi Bobot fraksi mg) Rendemen (%)
Fraksi E4 memiliki bobot dan rendemen yang besar. Masih terdapat campuran senyawa, tetapi pola pemisahan noda cukup baik untuk dipisahkan lebih lanjut menggunakan kromatografi radial (KR).
Gambar 3 Pemisahan fraksi E4 menggunakan KR
Pemisahan dengan KR dihasilkan 2 fraksi, yaitu E4-1 dan E4-2 dengan bobot masing-masing 5.3 dan 11.3 mg. Jumlah bobot fraksi E4-1 dan E4-2 lebih kecil daripada fraksi E4 awal. Hal ini dapat dikarenakan terdapat senyawa selain fraksi E4-1 dan E4-2 yang tidak berpendar di bawah lampu UV 254 dan 366 nm. Fraksi E4-1 dan E4-2 telah dianalisis dengan NMR tetapi hasilnya (Lampiran 4 dan 5) belum dapat diinterpretasikan sebagai suatu senyawa murni.
Penentuan senyawa metabolit sekunder lain beralih ke fraksi E18. Pemilihan fraksi ini didasarkan pada bobotnya yang relatif besar. Pemilihan eluen terbaik kembali dilakukan untuk pemisahan fraksi E18 menggunakan kromatografi lapis tipis preparatif (KLTP). n-Heksana-EtOAc 8:2 diperoleh sebagai eluen terbaik dan menghasilkan 5 noda yang terpisah dengan baik, dapat dilihat pada Gambar 4.
Gambar 4 Kromatogram fraksi E18 dalam eluen terbaik n-heksana-EtOAc (8:2), diamati di bawah lampu UV 366 nm
Pemisahan dengan KLTP menghasilkan fraksi E18-1 hingga E18-5 dengan bobot berturut-turut 2.46, 3.24, 4.83, 10.7, dan 3.75 mg. Jumlah bobot tersebut jauh menurun dibandingkan dengan bobot fraksi E18 awal, diduga karena sebagian senyawa terjerap kuat pada silika KLTP dan tidak dapat dilarutkan dengan aseton. Selain itu, kemungkinan ada senyawa lain yang tidak berpendar di bawah lampu UV 254 maupun 366 nm. Dari kelima fraksi E-18, hanya satu yaitu E-18-4 yang dianalisis dengan spektrofotometer 1H NMR, karena keempat fraksi lainnya memiliki bobot yang tidak mencukupi.
8
Hasil analisis spektrum 1H NMR fraksi E18-4 masih menunjukkan campuran senyawa. Spektrum 1H NMR menunjukkan geseran kimia (δ) berturut-turut pada 0.8−1.7, 3.3−4.0, dan 5.8−7.3 ppm. Geseran kimia pada 0.8−1.7 ppm geseran proton gula di daerah ikatan eter glikosidik yang terhubung dengan cincin aromatik. Senyawa yang pernah berhasil diisolasi oleh peneliti sebelumnya yang memiliki ciri-ciri tersebut adalah (−)-epiafzelekin-3-O-glukosida. Proton aromatik diduga berasal dari gabungan 2 jalur biosintesis flavonoid yaitu, jalur asam malonat, dan turunan senyawaan turunan asam sikimat seperti asam ferulat, asam sinapat, dan asam vanilat. Hal ini dibuktikan dengan adanya sinyal proton aromatik pada geseran di sekitar 5.8−7.3 ppm (Crews et al. 1998). Senyawa flavonoid yang pernah diisolasi dari daun trengguli adalah (−)-epikatekin, dan prosianidin B-2 (Kashiwada et al. 1996), dan dari bunga trengguli adalah senyawa kaemferol, tetramer leukopelargonidin (bebas glikol) (Narayanan dan Seshadri 1972).
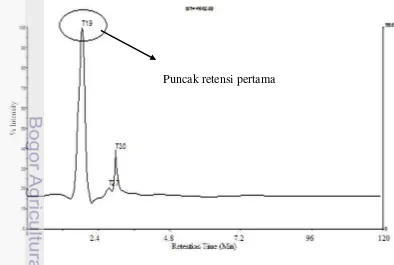
Analisis lanjutan dengan LC-MS pada fraksi E18-4 menunjukkan 3 puncak pada kromatogram LC dengan waktu retensi 1.85, 2.75, dan 2.98 menit (Gambar 5) dan luas puncaknya berturut-turut 873.16, 84.88, dan 98.66 satuan luas. Puncak pertama yang memiliki waktu retensi 1.85 menit dan luas 873.16 satuan luas merupakan puncak dominan di dalam fraksi E18-4. Kajian lanjut terhadap puncak tersebut, spektrum massanya menunjukkan bobot molekul 1019 (Gambar 6.).
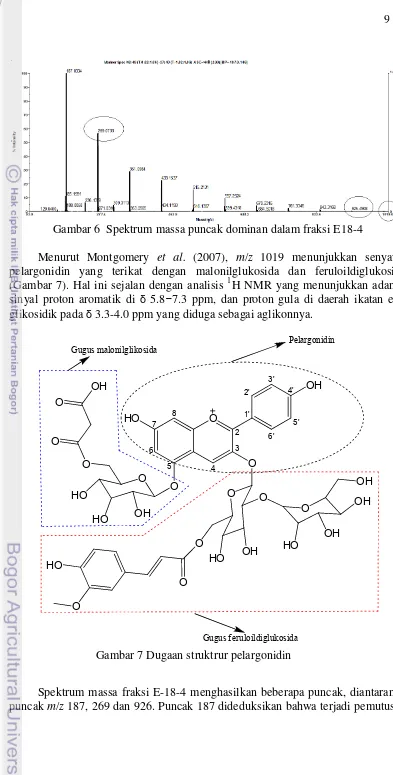
Gambar 6 Spektrum massa puncak dominan dalam fraksi E18-4
Menurut Montgomery et al. (2007), m/z 1019 menunjukkan senyawa pelargonidin yang terikat dengan malonilglukosida dan feruloildiglukosida (Gambar 7). Hal ini sejalan dengan analisis 1H NMR yang menunjukkan adanya sinyal proton aromatik di δ 5.8−7.3 ppm, dan proton gula di daerah ikatan eter glikosidik pada δ 3.3-4.0 ppm yang diduga sebagai aglikonnya.
7
Gambar 7 Dugaan struktrur pelargonidin
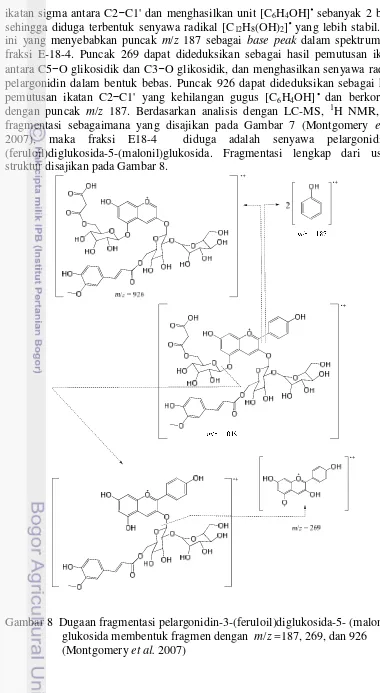
Spektrum massa fraksi E-18-4 menghasilkan beberapa puncak, diantaranya puncak m/z 187, 269 dan 926. Puncak 187 dideduksikan bahwa terjadi pemutusan
10
ikatan sigma antara C2−C1' dan menghasilkan unit [C6H4OH] sebanyak 2 buah,
sehingga diduga terbentuk senyawa radikal [C12H8(OH)2] yang lebih stabil. Hal
ini yang menyebabkan puncak m/z 187 sebagai base peak dalam spektrum MS fraksi E-18-4. Puncak 269 dapat dideduksikan sebagai hasil pemutusan ikatan antara C5−O glikosidik dan C3−O glikosidik, dan menghasilkan senyawa radikal pelargonidin dalam bentuk bebas. Puncak 926 dapat dideduksikan sebagai hasil pemutusan ikatan C2−C1' yang kehilangan gugus [C6H4OH] dan berkorelasi
dengan puncak m/z 187. Berdasarkan analisis dengan LC-MS, 1H NMR, dan fragmentasi sebagaimana yang disajikan pada Gambar 7 (Montgomery et al. 2007), maka fraksi E18-4 diduga adalah senyawa pelargonidin-3-(feruloil)diglukosida-5-(malonil)glukosida. Fragmentasi lengkap dari usulan struktur disajikan pada Gambar 8.
SIMPULAN DAN SARAN
Simpulan
Hasil uji fitokimia, ekstrak metanol daun trengguli asal Kebun Raya Bogor, mengandung senyawa metabolit sekunder golongan flavonoid, alkaloid, steroid, fenolik, dan tanin. Senyawa metabolit sekunder yang berhasil diisolasi dari fraksi terlarut etil asetat dari ekstrak metanol daun trengguli diduga pelargonidin-3-(feruloil)diglukosida-5-(malonil)glukosida.
Saran
Penelitian ini belum mendapatkan senyawa murni, sehingga perlu dilakukan pemisahan lebih lanjut. Pemisahan asam lemak perlu dilakukan di tahap awal agar tidak terbawa pada tahap ekstraksi lebih lanjut.
DAFTAR PUSTAKA
Ali MA, Sayeed MA, Absar N. 2003. Antibacterial activity and cytotoxicity of three lecitins purified from C. fistula L. seeds. J Med Sci. 3(3):240-244. Bayu I. 2013. Pencirian Komponen Kimia Fraksi Nonpolar Ekstrak Daun
Trengguli (Cassia fistula L.) [Skripsi]. Bogor (ID): Institut Pertanian Bogor. Crews P, Rodriguez J, Jaspar M. 1998. Organic Structure Analysis. New York
(US): Oxford Univ Pr.
Harborne JB. 1996. Metode Fitokimia: Penuntun Cara Modern Menganalisis Tumbuhan. Padmawinata K, Soediro I, penerjemah. Bandung (ID): Penerbit ITB. Terjemahan dari: Phytochemical Methods.
Hermawati E. 2009. Metabolit Sekunder dari Salah Satu Tumbuhan Obat Indonesia: Daun Desmodium triquetrum Linn. (Fabaceae) [Skripsi]. Bandung (ID): Institut Teknologi Bandung.
Ilavarasan R, Mallika M, Venkataraman S. 2005. Anti-inflammatory and antioxidant activities of Cassia fistula Linn bark extract. Afr J Traditional. 2 (1):70-85.
Kashiwada Y, Toshika K, Chen R, Nonaka G, Nishoka I. 1996. Tannins and related compounds. XCIII. Occurence of enantiomeric proantocyanidins in the Leguminosae plants, C. fistula L., C. javanica L. Chem Pharm Bull. 38:888-893
Kumar A, Pande CS, Kaul RK. 1966. Chemical examination of C. fistula flowers. Indian J. Chem. 4:460.
Kuo YH. Lee PH, Wein YS. 2002. Four new coumpounds from the seeds of C. fistula. J Nat Prod. 65:1165-1167.
12
Montgomery HV, Ginter GM, Tanaka K. 2007. MSn Analysis of Natural Nutraceutical Supplements. ASMS
Narayanan V, Seshadri TR. 1972. Proantocyanidins of C. fistula. Indian J. Chem. 10:379-381.
Padma S, Pratima K. 2006. Antifungal activity of Cassia fistula leaf extract against Candida albicans.Indian J Microbiol. 46(2):169-170.
Padmanabha RTV, Venkateswarlu V. 1965. “Fistucacidin” from the bark and heartwood of Cassia fistula Linn. Bull Nat Int Sci. 31:28-33.
Panda SK, Padhi LP, Mohanty G. 2011. Selective antifungal action of crude extracts of Cassia fistula, a preliminary study. Malaysian J Microbiol. 6(1):62-68.
Pandya DJ, Patel VL, Desai TR, Lunagaria RR, Gajera SD, Mehta AJ. 2012. Pharmacognostic and phytochemical evaluation of leaves of Cassia fistula. Int J Pharm & Life Sci. 3(2):1424-1429.
Prashanth KV, Chauhan NS, Padh H, Rajani M. 2006. Search for antibacterial antifungal agents from selected Indian medicinal plants. J Ethnopharmacol. 107:182-188
Rani M, Kalidhar SB. 1998. A new anthraquinone derivative from Cassia fistula L. pods. Indian J Chem. 37B:1314-1315.
Rizvi MA, Irshad M, Singh M. 2010. Assessment of anthelmintic activity of C. fistula L. Middle-East J Scientific Res. 5(5):346-349.
Vaishnav MM, Gupta KR. 1996. Rhamnetin 3-O-gentiobioside from C. fistula roots. Fitoterapia. LXVII:78-79.
Vimalraj TR, Kumar SS, Vadivel S, Ramesh S, Thejomoorthy P. 2009. Antibacterial effect of Cassia fistula extract on pathogenic bacteria of veterinary importance. J Veterinary & Animal Sci. 55(3):109-113.
Lampiran 1 Bagan alir penelitian
14
Lampiran 2 Metode uji fitokimia (Harborne 1996) 1. Uji alkaloid
Sebanyak 2 g ekstrak dilarutkan dalam kloroform, kemudian ditambahkan 10 mL kloroform-amonia dan disaring. Filtrat yang diperoleh ditetesi dengan H2SO4 2 M,
kemudian dikocok hingga terbentuk 2 lapisan. Lapisan asam (tidak berwarna) dipipet ke dalam tabung reaksi, kemudian larutan dibagi 3 untuk diuji dengan beberapa tetes reagen Dragendorf, Mayer, dan Wagner. Uji positif alkaloid berturut-turut ditunjukkan dengan munculnya endapan jingga, putih kekuningan, dan cokelat.
2. Uji triterpenoid dan steroid
Sebanyak 2 g ekstrak ditambahkan 25 mL etanol kemudian dipanaskan dan disaring. Filtrat diuapkan, lalu ditambahkan dietil eter. Lapisan eter dipipet dan diuji pada pelat tetes. Jika contoh berubah warna menjadi merah/ungu setelah penambahan 3 tetes pereaksi Lieberman-Buchard, maka contoh positif mengandung triterpenoid. Jika terbentuk warna hijau, maka contoh positif mengandung steroid.
3. Uji flavonoid dan fenolik
Sebanyak 2 g ekstrak ditambahkan beberapa mL metanol hingga terendam dan dipanaskan hingga mendidih, kemudian disaring. Filtrat yang diperoleh dibagi menjadi 2 bagian. Bagian pertama ditambahkan NaOH 10% dan bagian kedua ditambahkan H2SO4 pekat. Bila setelah penambahan NaOH 10% dihasilkan warna
merah berarti positif terdapat senyawa fenol hidrokuinon. 4. Uji saponin dan tanin
Sebanyak 2–4 g ekstrak ditambahkan akuades panas kemudian dipanaskan sampai mendidih dan disaring. Filtrat dibagi ke dalam 2 tabung reaksi. Uji saponin dilakukan dengan cara larutan didinginkan terlebih dahulu kemudian dikocok tegak. Timbulnya busa yang stabil setinggi lebih kurang 1 cm selama 10 menit menandakan positif terdapat saponin. Filtrat pada tabung reaksi kedua ditambahkan FeCl3 1% dan bila dihasilkan warna biru atau hijau tua, menandakan
Lampiran 3 Kadar air simplisia sampel kering
16
Lampiran 5 Spektrum 1H NMR fraksi E4-2
18
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 26 Agustus 1991 dari pasangan Adi Priyanto dan Henny Pusparini. Penulis merupakan anak pertama dari 4 bersaudara. Tahun 2009, penulis lulus dari SMA Negeri 1 Jakarta (Boedoet) dan pada tahun yang sama diterima di Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI).