ABSTRAK
UJI APLIKASI JAMURMETARIHZIUM ANISOPLIAETERHADAP
SYMPHYLIDPADA MEDIA HIDUP TANAH BERBAHAN
ORGANIK DAN TANPA BAHAN ORGANIK DI LABORATORIUM
Oleh
Candra Susiyanti
Dalam pengendalian hamasymphylidperlu dikembangkan upaya pengendalian yang ramah lingkungan dan menjamin hasil yang sehat. Oleh karena itu, saat ini
terus dilakukan penelitian pemanfaatan agensia hayati, contohnya jamur
Metarhizium anisopliae. Penelitian ini bertujuan untukmengetahui apakah cendawan entomopatogenMetarhizium anisopliaeyang diaplikasikan dapat menginfeksisymphylidyang hidup pada tanah berbahan organik dan tanpa bahan organik. PadaaplikasiM. anisopliaedilakukan dengan metode residu pakan dan residu media hidupsymphylid yaitu tanah berbahan organik dan tanpa bahan
organik. Hasil pengamatanmenunjukkan bahwa data mortalitassymphylidtidak berbeda nyata pada ketiga perlakuan. Mortalitassymphylidtertinggi hanya
pergerakanya. Hasil penelitian ini belum dapat membuktikan bahwaM anisopliaemampu menginfeksi dan menyebabkan kematiansymphylid.
UJI APLIKASI JAMUR
METARHIZIUM ANISOPLIAE
TERHADAP
SYMPHYLID
PADA MEDIA HIDUP TANAH
BERBAHAN ORGANIK DAN TANPA BAHAN ORGANIK DI
LABORATORIUM
Oleh
Candra Susiyanti
Skripsi
Sebagai Salah Satu Syarat Untuk Mencapai Gelar SARJANA PERTANIAN
Pada
Jurusan Agroteknologi
Fakultas Pertanian Universitas Lampung
FAKULTAS PERTANIAN
UNIVERSITAS LAMPUNG
UJI APLIKASI JAMUR
METARHIZIUM ANISOPLIAE
TERHADAP
SYMPHYLID
PADA MEDIA HIDUP TANAH
BERBAHAN ORGANIK DAN TANPA BAHAN ORGANIK DI
LABORATORIUM
(Skripsi)
Oleh
Candra Susiyanti
FAKULTAS PERTANIAN
UNIVERSITAS LAMPUNG
v DAFTAR GAMBAR
Gambar Halaman
1. Gejala serangan hamaSymphylidpada akar mengalami
gejalawitches broom.………... 10 2. Gejala merah yang muncul diikuti dengan mengecilnya
lebar daun... 10 3. Symphylid……….………......
DAFTAR TABEL
Tabel Halaman
1.Pengamatan mortalitas hamasymphylid... 20
2. Jumlah mortalitas hamasymphilydyang diamati pada laboratorium ... 28
3. Mortalitassymphylidpada perlakuan aplikasiM. anisopliae dengan metode residu residu pakan dan residu media hidup symphylid ... 21
4. Analisis mortalitassympilidpada 5 hsa ... 28
5. Analisis mortalitasSympilidpada 10 hsa ... 28
6. Analisis mortalitasSympilidpada 15 hsa...…. 28
`
Jika sudah tak bisa percaya pada siapapun setidaknya
masih bisa percaya pada diri sendiri namun jangan terlalu
percaya diri karna dapat menjadi senjata yang dapat
Alhamdu lillahhi robbil alamin
Dengan penuh rasa syukur kupersembahkan karya ini sebagai tanda terimakasihku kepada
Keluargaku Tercinta
Ayahanda dan Ibunda tercinta Saudaraku
Mbak Sri Darwati, Mas Edy Santoso, Mas Slamet, Mendiko
Suwandi, keponakan tercinta Singgih Nugraha, Sazkia Setia
Ningrum, dan Serli Ulia Ningrum. Terimakasih Telah memberikan
memberikan doa dan dukungan tak terbatas.
Dosen Pembimbing
Ibu Lestari Wibowo dan Bapak Afandi
Sahabat sahabatku tercinta siti jarlina, Susi, Septi, Rully, Eka, Dian oktaviani. Terimakasih atasbantuan, do a, nasehat, semangat, candaan, bantuan, dan kebersamaan selama ini.
Rekam rekan HPT 2010 (Astri, Eko andrianto, mbak Desye, Yudi, Galih) dan AGT D 2010 terimakasih atas canda, tawa, dan
kebersamaanya
Serta Almamater kebanggaan Fakultas Pertanian Universitas Lampung
Agroteknologi 2010
RIWAYAT HIDUP
Penulis dilahirkan di Pati, Jawa Tengah pada 28 September 1992, sebagai putri ke-3 dari 3 bersaudara dari pasangan Bapak Sarti dan Ibu Jasmi. Penulis
menyelesaikan pendidikan Sekolah Dasar di SD Negeri 02 Beketel Kec. Kayen, Pati pada tahun 2004; Sekolah Menengah Pertama di SMP Satya Dharma Sudjana, Gunung Madu Lampung Tengah pada tahun 2007; Sekolah Menengah Atas di SMA Negeri 1 Terusan Nunyai Lampung Tengah pada tahun 2010.
Penulis terdaftar sebagai mahasiswi Program Studi Agroteknologi Fakultas Pertanian, Universitas Lampung pada tahun 2010 melalui jalur Mandiri(UM). Selama menjadi mahasiswi, penulis aktif dalam Lembaga Mahasiswa Pertanian (LS-MATA) sebagai Anggota Bidang Hubungan Masyarakat (HUMAS) pada tahun 2012. Penulis pada semasa kuliah juga pernah menjadi asisten dosen Matakuliah Penyakit Penting Tumbuhan (2012/2013), Pengendalian Hama Tumbuhan (2012/ 2013), Hama Nir Serangga (2014), dan Matakuliah Pengendalian Hama Tanaman Kelapa sawit (2014)
Penulis melaksanakan Praktik Umum (PU) Pada tahun 2013 di Balai Penelitian Tanaman Hias (BALITHI). Pada tahun 2014 penulis melaksanakan Kuliah Kerja Nyata (KKN) di Desa Labuhan Ratu, Kecamatan Pasir Sakti, Kabupaten
SANWACANA
Puji syukur Penulis panjatkan kehadirat ALLAH SWT yang telah memberikan segala rahmat Nya, sehingga Penulis dapat menyelesaikan skripsi ini. Di dalam proses penulisan skripsi ini penulis telah menerima bantuan dan bimbingan dari banyak pihak. Oleh karena itu penulis mengucapkan terima kasih kepada:
1. Ibu Ir. Lestari Wibowo, M. P., selaku Pembimbing Utama yang telah
memberikan segala ide, bimbingan, motivasi, saran, perhatian serta pengertian kepada penulis selama penelitian dan penulisan skripsi hingga selesai;
2. Bapak Dr. Ir. Afandi, M. P., selaku Pembimbing Kedua atas segala saran, bimbingan dan kesabaran yang telah diberikan kepada penulis selama penelitian dan penulisan skripsi ini;
3. Bapak Prof. Dr. Ir. Hamim Sudarsono, M. Sc., selaku Dosen Penguji atas saran, kritik, bimbingan, dan pengarahan kepada penulis dalam menyelesaikan skripsi ini;
4. Ibu Dr. Ir. Suskandini Ratih, M. P., selaku Pembimbing Akademik atas saran, kritik, bimbingan, pengarahan dan motivasi kepada penulis selama berada di Perguruan Tinggi Universitas Lampung;
6. Bapak Dr. Ir. Kuswanta Futas Hidayat, M. P., Ketua Jurusan Agroteknologi, Fakultas Pertanian Universitas Lampung;
7. Bapak Prof. Dr. Ir. Wan Abbas Zakaria, M. S., Dekan Fakultas Pertanian Universitas Lampung;
8. Seluruh Dosen Fakultas Pertanian, khususnya Jurusan Agroteknologi, yang telah
memberikan ilmu pengetahuan dan bimbingan selama mengikuti perkuliahan;
9. Kedua orangtuaku Bapak Sarti dan Ibu Jasmi atas cinta, doa, dan dukungan yang tak terbatas. Keluarga besarku, Mbak Sri Darwati, Mendiko Suwandi, Mas Edy Santoso, Mas Slamet Riyad, Keponakan Tercinta, Singgih Nugraha, Sazkia Setya Ningrum, Serly Ulya Ningrum,dan Muhammad fatir atas segala cinta doa, dukungan baik secar moral maupun spiritual,
10. Teman dekatku Siti Jarlina, Susi Susanti, Septia Hasanah, Dian Oktaviani, dan Rully Pebriansyah atas segala cinta, doa, dan dukungan semoga persahabatan kita selalu teringat dan terkenang,
11. Teman-teman Agroteknologi 2010 atas persahabatan yang terjalin selama ini. Semoga ALLAH SWT membalas dan memberikan rahmat untuk semua kebaikan yang telah diberikan kepada penulis dan skripsi ini dapat bermanfaat bagi kita semua. Amin.
Bandar Lampung, 28 September 2015
DAFTAR ISI
3.4.2 Persiapan Hama symphylid... ... 17
3.4.3 Pengujian M. anisopliae pada Hama symphylid... 17
3.5 Pengamatan ... 20
3.6 Analisis data ... 20
IV. HASIL DAN PEMBAHASAN ... 21
V. KESIMPULAN DAN SARAN ... ... 24
5.1Kesimpulan... ... 24
5.2Saran... . 24
PUSTAKA ACUAN... .. 25
1
I. PENDAHULUAN
1.1 Latar belakang dan Masalah
Nanas (Ananas comosus[L.] Merr.) merupakan komoditas andalan yang sangat berpotensi dalam perdagangan buah tropik yang menempati urutan kedua terbesar
setelah pisang. Di Indonesia produsen nanas olahan terbesar adalah PT Great
Giant Pinaple (GGP) yang berlokasi di Provinsi Lampung. Nanas menjadi
prioritas tanaman yang dikembangkan di Indonesia karena memiliki potensi
ekspor, terutama bagi industri pengolahan buah. Produksi nanas di Indonesia
pada tahun 2013 mencapai 1.837.159 ton (BPS, 2014).
Salah satu kendala dalam budidaya pertanaman nanas adalah adanya organisme
pengganggu Tanaman (OPT). Akhir-akhir ini terdeteksisymphylidsebagai hama pada tanaman nanas. Hama ini memakan akar atau bagian lain yang terdapat
dibawah tanah dan dapat menyebabkan kematian tanaman nanas. Serangan hama symphylidtelah dirasakan oleh salah satu perusahaan swasta yang
membudidayakan nanas yaitu PT GGP. Bila populasisymphylidyang menyerang tanaman pada khususnya tanaman muda cukup tinggi, maka akan dapat
menimbulkan kerugian besar karena akar tanaman menjadi rusak sehingga
kemampuan akar untuk menyerap unsur hara dan air di dalam tanah menjadi
2
Symphylidtelah dilaporkan sebagai hama penting pada tanaman nanas oleh negara penghasil nanas. Hama ini memakan rambut akar dan ujung ajar (tudung akar).
Symphylidmenyukai tanah dengan bahan organik yang tinggi dan memiliki aerasi yang baik dan jugasymphylidmudah ditemukan pada tanah yang berpasir.
Symphylid merupakan hama yang bersifat kanibal jika tidak tersedianya cadangan makanan dan juga dapat bertahan hidup 4 bulan selama suhu dan kelembaban
lingkungan terjaga. Suhu tanah dapat mempengaruhi pergerakansymphylid sedangkan kelembaban tanah dapat mempengaruhisymphyliduntuk bermigrasi ke daerah yang lebih lembab (Pyet al.,1987).
Matasymphylidtidak berkembang dan tidak digunakan untuk indra pengelihatan, symphylidbergerak dengan mengandalkan antena. Tubuhsymphyliddapat menggali tanah untuk membuat jalan sendiri atau mendapatkan jalan melalui
pergerakan hewan lain untuk dapat berpindah di dalam tanah. Symphylidmampu bergerak secara vertikal ke dalam tanah sedalam 90 cm untuk menghindari
pengolahan tanah dan aplikasi herbisida (Alphonsine, 2010).
Serangansymphylidsmenyebabkan akar tanaman nanas nampak bercabang-cabang seperti sapu (gejalawitches broom)yaitu ujung akar terpotong, menumpul dan akar–akar serabut atau rambut akar umumnya habis dimakan. Akibatnya serapan akar terhadap nutrisi dan airpun berkurang, sehingga pertumbuhan tanaman terganggu dan tanaman menjadi kerdil. Seperti serangan hama
3
Serangan pada akar akan menyebabkan munculnya gejala daun berwarna merah
dan semakin lama tanaman akan menjadi kurus (tanaman kerdil). Hama symphylidshidup pada daerah perakaran tanaman nanas, populasi hama ini diperkirakan justru akan berkembang dengan baik ketika tanah memiliki kandungan bahan organik tinggi akibat dari penggunaan pupuk alami.Upaya pengendalian yang pernah dilakukan dalam mengendalikan hamasymphylidyaitu menggunakan fumigan dan pestisida kimia. Tetapi ternyata hasil yang didapatkan
tidak efektif dan memerlukan biaya yang mahal. Penggunaan pestisida sintesis
selain tidak efektif juga dapat menimbulkan resistensi dan residu yang dapat
membahayakan kesehatan para pelaksana budidaya tanaman nanas serta dapat
menimbulkan dampak negatif pada lingkungan sekitar.
Sesuai dengan konsep PHT penggunaan bahan kimia berangsur-angsur akan
dikurangi, karena telah menimbulkan masalah yang cukup serius bagi lingkungan.
Penggunaan pestisida yang tidak benar mengakibatkan munculnya hama yang
resisten terhadap bahan kimia tersebut. Untuk mengurangi digunakannya bahan
kimia telah banyak diupayakan penggunaan musuh alami hama, baik berupa
predator, parasitoid maupun patogen (Untung, 1993).
Salah satu alternatif untuk mengurangi penggunaan insektisida sintetik dalam
mengendalikan populasi hama adalah menggunakan agensia hayati yang berupa
entomopatogen yang bersifat patogen hanya pada serangga sasaran. Jamur
entomopatogen adalah salah satu agensia hayati yang banyak dimanfaatkan.
Jamur ini dapat menginfeksi dan menyebabkan penyakit pada serangga, sehingga
4
(Gopalakrishnan, 2001). Dalam pengendalian hamasymphylidperlu
dikembangkan upaya pengendalian yang ramah lingkungan dan menjamin hasil
yang sehat. Oleh karena itu, saat ini terus dilakukan penelitian dengan
memanfaatkan jamurMetharizium anisopliaesebagai agensia hayati.
M.anisopliaedapat menginfeksi dan menyebabkan kematian pada hewan Arthropoda seperti serangga. Mekanisme infeksi dimulai dengan adanya kontak
antara spora jamur dengan serangga. Spora jamur yang melekat pada permukaan
kutikula larva akan membentuk hifa yang memasuki jaringan internal larva
melalui interaksi biokimia yang kompleks antara inang dan jamur. Selanjutnya,
enzim yang dihasilkan jamur berfungsi mendegradasi kutikula larva serangga, hifa
jamur akan tumbuh ke dalam sel-sel tubuh serangga, dan menyerap cairan tubuh
serangga. Hal ini akan mengakibatkan serangga mati dalam keadaan tubuh yang
mengeras seperti mumi (Tanada dan Kaya,1993).
Serangga yang terinfeksi jamur entomopatogen ditandai dengan pertumbuhan hifa
berwarna putih pada permukaan kutikula tubuh, dan memasuki hemocoel. Di
dalam hemocoel, hifa akan membentuk “yeastlike hyphal bodies”(blastospora), yang memperbanyak diri dengan cara pembentukkan tunas. Blastopora tumbuh
dan berkembang di dalam hemocoel dengan menyerap cairan hemolimpf. Selain
itu infeksi jamur ini menghasilkan enzim dekstruksin yang bersifat toksik dan
menimbulkan kerusakan pada jaringan serangga (Kershawet al., 1999).
5
terutama pada stadia larvaOryctes rhinocerosyang hidup dalam tumpukan bahan organik.
Dari hasil pengamatan pendahuluan, aplikasi bahan organik mempengaruhi
keberadaan symphylid. Keberadaansymphylidlebih banyak dijumpai pada lahan berbahan organik. PemanfaatanM. anisopliaesebagai agensia hayati untuk mengendalikan hamasymphylidperlu dikaji lebih lanjut. Karena alasan tersebut maka perlu diadakan penelitian untuk mengetahuiM. anisopliae sebagai agensia hayati terhadap hamasymphylid.
1.2 Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui apakah cendawan entomopatogen
Metathizium anisopliaeyang diaplikasikan dapat menginfeksisymphylidyang hidup pada tanah berbahan organik dan tanpa bahan organik.
1.3 Kerangka Pemikiran
Jika lingkungan tanah yang menguntungkan atau pada tanah dengan bahan
organik yang cukupsymphyliddapat bermigrasi dari permukaan tanah sampai kedalaman lebih dari 3 meter. Profil tanah yang padat atau berpasir dan air yang
menggenang dapat menghambat gerakansymphylid. Waktu migrasi symphylid bergerak secara vertikal dan disebabkan oleh interaksi antara kelembaban, suhu,
6
Beberapa spesiessymphylidmemakan bahan organik mati atau membusuk. Spesies lain merupakan hama yang serius karena memakan tanaman hidup. Secara umum, pengolahan struktur tanah misalnya: penambahan bahan organik, mengurangi pengolahan tanah dapat meningkatkan kemampuansymphylid untuk bergerak melalui tanah, yang menyebabkan peningkatan populasi dan atau
peningkatan kerusakan akar tanaman. Akibatnya, populasisymphylidtinggi ditemukan di tanah bertekstur halus, lebih berat dengan struktur yang moderat atau lebih baik dan banyak pori makro , bukan di tanah berpasir (Edwards., 1958; Edwards., 1961 dalam Umbelet al., 2006).
Pada penelitian sebelumnya menunjukkan bahwa jamurM. anisopliaedapat menginfeksi hama tungau merah dan dapat mengakibatkan mortalitas tungau hingga 98% (Sanjayaet al.,2013). Secara taksonomi tungau memiliki kedekatan dengan hamasymphylid. Kemungkinan bahwasymphyliddapat terinfeksi oleh jamurM. anisopliaedan dikarenakan jamur ini dapat digunakan sebagai pengendalian alternatif.
7
1.4 Hipotesis
8
II.TINJAUAN PUSTAKA
2.1 Hama Symphilid
Symphylid memiliki bentuk yang menyerupai kelabang, namun lebih kecil, berwarna putih dan pergerakannya cepat. Dalam siklus hidupnya, symphylid bertelur dan telurnya menetas sekitar 25 – 40 hari. Perkembangan symphylid dipengaruhi oleh suhu lingkungan. Pada suhu 10 – 21o C, total waktu dari telur
hingga fase dewasa matang seksual yaitu sekitar 5 bulan. Rentang waktu semakin
menurun menjadi ± 3 bulan pada suhu 21o C dan terus menurun menjadi 2 bulan
pada suhu 25o C. Satu individu symphylid dapat berganti kulit hingga 52 kali (Berry and Robinson, 1974).
Symphylid berukuran kecil, memiliki panjang 3-7 mm, berwarna putih, dengan antena menonjol dengan 12 kaki (Carr, 2003), symphylid mereproduksi dari telur yang biasanya disimpan di cluster di berbagai kedalaman di dalam tanah
tergantung pada struktur tanah, suhu, dan kelembaban. Symphylid umumnya lebih putih dan lebih kecil dari lipan yang juga artropoda tanah dengan banyak pasang
kaki (satu pasang per segmen tubuh) dan gerakan cepat. Kaki seribu umumnya
lebih lambat bergerak, dengan dua pasang kaki pada setiap segmen tubuh.
9
bahkan spesies lain juga merupakan hama yang serius, karena memakan akar
tanaman (Umble and Fisher, 2003; Umble et al., 2006).
Secara sederhana klasifikasi hama symphylid sebagai berikut (Umble et al., 2006). Filum : Artropoda
Subfilum : Miriapoda Kelas : Symphyla
Ordo : Symphyla/ Cephalostigmata Famili : Scutigerellidae
Genus : Scutigerellidae & Hanseniella
Spesies : Scutigerellidae spp. dan Hanseniella spp.
Telur symphylid berbentuk seperti mutiara putih dan bulat dengan punggung berbentuk heksagonal. Telur menetaskan selama sekitar 25 sampai 40 hari ,
ketika suhu berkisar antara 50° sampai 70° F , tetapi penetasan terjadi pada sekitar
12 hari karena suhu mencapai 77° F (Berry., 1972 dalam Umble et al., 2006).
Larva symphylid instar pertama muncul dari telur dengan enam pasang kaki dan enam segmen antennal, tubuh mereka ditutupi dengan bulu-bulu halus. Gerakan
lambat dan posterior bengkak membuat instar pertama kali muncul dangkal lebih
seperti collembolan dari pada symphylid dewasa. Larva symphylid instar pertama jarang ditemukan di zona perakaran namun dalam beberapa hari dapat berubah ke
instar kedua yang kecil menyerupai symphylid dewasa (Michelbacher, 1938 dalam Umble et al., 2006).
Mendiagnosis gejala yang ditimbukan oleh symphylid kadang-kadang sulit karena kerusakan dapat diperlihatkan di sejumlah bentuk pada tanaman dan symphylid tidak selalu mudah untuk ditemukan, bahkan ketika kerusakan tanaman terlihat
10
akar dan umbi tanaman (Umble dan Fisher, 2003). Jika symphylid makan akar tanaman maka dapat mengurangi kemampuan tanaman untuk mengambil air dan nutrisi tanaman. Kerusakan akar juga dapat membuat tanaman lebih rentan terhadap beberapa patogen tanah (Berry dan Robinson, 1974).
Tanaman yang terserang symphylid memiliki gejala visual daun tanaman berwarna merah, warna yang ditunjukan berbeda dengan jenis nanas yang daunnya memang berwarna merah. Pada tahap serangan lanjut, gejala merah yang muncul diikuti dengan mengecilnya lebar daun (daun menjadi kurus) dan tanaman menjadi kerdil (Gambar 1 b.). Sedangkan akar tanaman yang terserang hama symphylid akan mengalami gejala witches broom yaitu ujung akar terpotong, menumpul, dan akar-akar serabut tidak ada lagi. Biasanya pada akar-akar yang menumpul akan tumbuh cabang akar yang baru dan pada akar yang menumpul tersebut terdapat lubang-lubang/luka ( Gambar 1a).
11
( a ) ( b )
Gambar 1. ( a ) Gejala serangan hama symphylid pada akar mengalami gejala witches broom, ( b ) gejala merah yang muncul diikuti dengan mengecilnya lebar daun.
4.3 Jamur Metarhizium anisopliae
Metarhizium anisopliae adalah jamur yang dikelompokkan ke dalam division
Amastigomycotina. Jamur ini merupakan jamur tanah bila dalam keadaan saprofit,
tetapi memiliki kemampuan sebagai pathogen pada beberapa ordo serangga (Tanada
dan Kaya, 1993 ; Alexopoulus, et al.,1996). Pada awal pertumbuhan koloni jamur
ini berwarna putih, kemudian akan berubah menjadi warna hijau gelap saat
konidia matang dan dilanjutkan dengan pembentukan spora. Spora yang berwarna hijau ini yang diberi istilah green muscardin fungus pada M. anisopliae (Tanada dan Kaya, 1993).
12
Taksonomi jamur Metarhizium anisopliae (Metschnikoff) Sorokin seperti berikut: Filum : Askomikota
Kelas :Hypomycetes Ordo : Moniliales Famili : Clavicipitaceae Genus : Metarhizium
Spesies : Metarhizium anisopliae (Metschnikoff) Sorokin
Jamur M. anisopliae memiliki kisaran inang yang sangat luas, meliputi ordo Lepidoptera, Coleoptera, Hemiptera, Diptera, Hymenoptera, Orthoptera, Dermaptera, Isoptera, Shiponaptera, bahkan arthopoda nir serangga seperti Simfilia, Acari, Malacosta`(Ampipoda) (Laird et al., 1990). M. anisopliae memiliki beberapa jenis enzim berbagai macam enzim untuk membantu dalam pelaksanaan penetrasi. Beberapa enzim yang dihasilkan jamur ini yang
mendukunng mekanisme tersebut misalnya khitinase, peptidase, dan endokhhitinase yang bersifat asam (Ahmad, 2004).
Mekanisme penetrasi jamur ini ke dalam tubuh serangga sangat dipengaruhi oleh struktur kutikula yaitu ketebalan, sklerotisasi, kandungan zat antijamur, dan substansi nutrisi. Larva yang baru mengalami penggantian kulit dan larva yang baru membentuk pupa lebih mudah diinfeksi dibandingkan dengan kutikula yang telah mengalami pengerasan.(Tanada dan Kaya, 1993).
Pada waktu serangga mati, fase perkembangan saprofit jamur dimulai dengan
penyerangan jaringan dan berakhir dengan pembentukan organ reproduksi. Pada
umumnya semua jaringan dan cairan tubuh serangga habis digunakan oleh jamur,
sehingga serangga mati dengan tubuh yang mengeras seperti mumi. Pertumbuhan
13
serangga dari serangan mikroorganisme lain terutama bakteri. Tidak selalu jamur
tumbuh ke luar menembus integumen serangga. Apabila keadaan kurang
mendukung, perkembangan saprofit hanya berlangsung di dalam jasad serangga
tanpa ke luar menembus integumen. Dalam hal ini jamur membentuk struktur
14
III. BAHAN DAN METODE
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Hama dan Penyakit Tanaman, Fakultas
Pertanian Unila. Hama symphylid diperoleh dari perkebunan nanas PT. Great Giant Pineapple Kecamatan Terbanggi Besar, Kabupaten Lampung Tengah. Penelitian ini dilakukan pada bulan November 2014 hingga bulan Januari 2015.
3.2 Bahan dan Alat Penelitian
Bahan yang digunakan dalam penelitian ini adalah media PDA (potato dextrose agar), menir jagung, isolat jamur Metathizium anisopliae, alkohol 70%, kertas tissu, dan daun pepaya.
Alat-alat yang digunakan dalam penelitian ini adalah alat tulis, cawan petri, jarum
ose, erlenmeyer, tabung reaksi, panci, sendok, bor gabus, bunsen, autoklaf,
kompor gas, kertas tissu, mikroskop, timbangan elektrik, toples kecil, kertas label,
dan lup.
Hewan uji dalam penelitian ini yaitu hama symphylid yang diperoleh dari perkebunan nanas PT. GGP Kecamatan Terbanggi Besar, Kabupaten Lampung
15
3.3 Metode Penelitian
Penelitian ini terdiri dari 3 perlakuan dan 10 ulangan. Sebagai perlakuan yaitu :
K = Kontrol
MO = Aplikasi M. anisopliae dengan metode residu terhadap symphylid yang hidup pada tanah berbahan organik di laboratorium
MT = Aplikasi M. anisopliae dengan metode residu terhadap symphylid yang hidup pada tanah tanpa bahan organik di laboratorium.
Percobaan ini disusun dalam RAL (Rancangan Acak Lengkap). Setiap unit
percobaan terdiri dari 10 g tanah sebagai media hidup symphylid yang diletakkan ke dalam toples kecil yang berdiameter 3 cm, tinggi 2 cm dan pada setiap toples
terdapat 5 ekor symphylid.
3.4 Pelaksanaan Penelitian
Pelaksanaan penelitian ini dilakukan tiga tahap yaitu tahap pertama perbanyakan
jamur M. anisopliae meliputi pembuatan kultur murni dan perbanyakan pada media jagung. Tahap kedua yaitu pencarian dan penangkapan symphylid dari kebun nanas dengan metode perangkap. Symphylid yang diperoleh dipelihara di laboratorium. Pada tahap ketiga yaitu pengujian jamur M. anisopliae pada symphylid, dan pengamatan.
3.4.1 Perbanyakan Jamur M. Anisopliae
Pembuatan Media Potato Dextrose Agar (PDA)
Dalam pembuatan 1 liter media PDAdiperlukan 1000 ml aquades, 200 g kentang,
16
ditimbang kemudian dipotong dadu. Kentang direbus sampai air mendidih dan air
rebusan kentang dimasukkan ke dalam labu erlenmeyer bersamaan dengan gula,
agar, dan dextrose. Kemudian diaduk hingga homogen. Dilakukan strerilisasi
basah menggunakan autoklaf selama 30 menit . Sebelum media digunakan dapat
diberi anti baktei agar tidak terjadi kontaminasi dapat menggunakan larutan asam
laktat atau streptomizin (tablet).
Isolasi M. anisopliae pada media PDA (pemurnian jamur)
Biakan jamur ini diperoleh UPTD Balai Perlintan Tegineneng, Lampung.
Selanjutnya M. anisopliae diinokulasi pada media PDA. Disiapkan media PDA 1000 ml steril dalam erlenmeyer dan dituangkan ke dalam 20 cawan petri steril.
Setelah media PDA dingin segera diinokulasi dengan M. anisopliae. Selanjutnya diinkubasi selama 14 hari dan dilakukan pengamatan.
Perbanyakan M. anisopliae pada media menir jagung
Disiapkan menir jagung sebanyak 1 kilogram, kemudian dikukus sampai matang
dan ditiriskan sampai dingin. Setelah dingin dimasukkan jagung sebanyak 100
gram ke dalam plastik tahan panas dan disterilisasikan ke dalam autoklaf selama
15 menit. Setelah menir jagung diangkat dari autoklaf dan dimasukkan ke dalam
17
3.4.2 Persiapan Hama Symphylid
Symphylid diambil pada lahan nanas secara manual. Pengambilan dilakukan dengan menggali tanah sedalam 10 cm di daerah perakaran tanaman nanas yang
tumbuh di daerah lembab yang mendapat naungan. Penggalian tanah
menggunakan sekop dan symphylid yang didapat dimasukkan ke dalam toples plastik dan diberi pakan media hidup symphylid yaitu daun pepaya dan kentang. Symphylid yang berada pada toples berukuran tinggi 20 cm dan diameter 6 cm berjumlah 500 ekor dan diletakkan di tempat yang lembab dan gelap.
3.4.3 Pengujian M. anisopliae pada Hama Symphylid
Pembuatan Suspensi M. anisopliae
Setelah 2 minggu masa inkubasi jamur M. anisopliae pada menir jagung dilakukan pemanenan. Diambil menir jagung yang telah ditumbuhi jamur M. anisopliae menggunakan sendok dan ditimbang sebanyak 10 g. Lalu diuukur aquades menggunakan gelas ukur sebanyak 100 ml. Setelah itu aquades dan
menir jagung berjamur yang telah ditimbang dimasukkan ke dalam labu
18
1. 500 g tanah diletakkan ke dalam nampan, lalu disemprotkan menggunakan 10 cc suspensi M. anisopliae
2. Tanah diaduk secara merata dan dikering anginkan.
3. Keesokan hari tanah yang telah diaplikasi suspensi M. anisopliae siap digunakan dalam penelitian.
Pada perlakuan kedua tanah yang digunakan adalah tanah humus yang
mengandung bahan organik sedangkan pada perlakuan ketiga tanah yang
digunakan adalah tanah berpasir.
Persiapan Unit Percobaan
Setiap unit percobaan terdiri dari toples kecil berukuran berdiameter 3 cm, tinggi
2 cm. Toples berisi 10 g tanah dan 0,2 g daun pepaya yang telah dipotong kecil –
kecil. Pada perlakuan pertama yaitu kontrol, potongan daun pepaya tanpa aplikasi
19
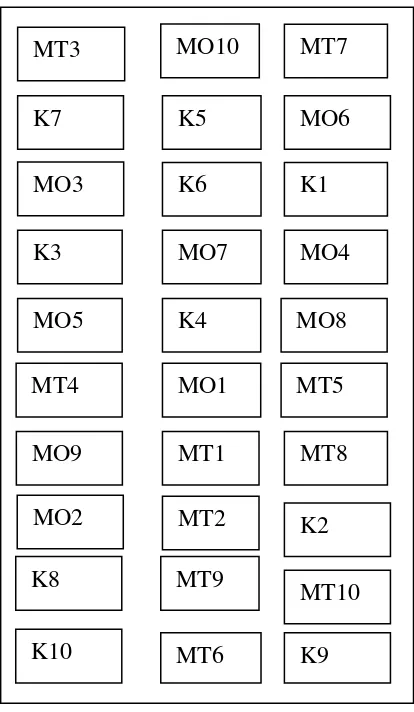
Gambar 1. Tata letak unit – unit percobaan
Keterangan : K = Kontrol
MO = Aplikasi M. anisopliae dengan metode residu terhadap symphylid yang hidup pada tanah berbahan organik di laboratorium.
MT = Aplikasi M. anisopliae dengan metode residu terhadap symphylid yang hidup pada tanah tanpa bahan organik di laboratorium.
Aplikasi M. anisopliae pada perlakuan kedua dan ketiga yaitu menggunakan metode residu yaitu M. anisopliae diaplikasikan pada tanah dan potongan daun pepaya sebagai pakan symphylid selanjutnya setiap 3 hari diberi pakan yang baru berupa potongan daun pepaya dan diberi perlakuan sesuai perlakuan masing –
20
3.5 Pengamatan
Pengamatan dilakukan setiap hari selama 20 (dua puluh) hari. Pengamatan
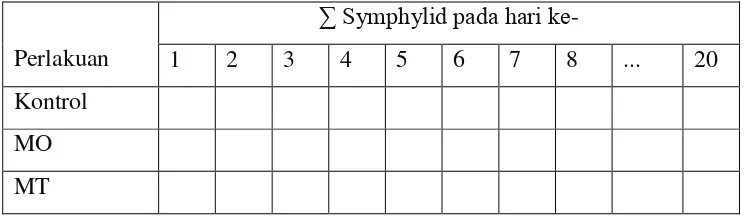
meliputi jumlah symphylid yang mati dan indikasi kematian symphylid. Indikasi kematian dilakukan dengan cara mengamati symphylid yang mati di bawah mikroskop, apakah pada tubuh serangga uji tumbuh cendawan M. anisopliae. Symphylid yang mati dideteksi penyebabnya dengan menginkubasi symphylid diatas media PDA. Data yang didapat dimasukkan ke dalam tabel seperti di
bawah ini:
Tabel 1. Pengamatan mortalitas hama symphylid
Perlakuan
Persentase kematian serangga dihitung dengan rumus sebagai berikut:
Seluruh data yang diperoleh diuji dengan analisis sidik ragam dan dilanjutkan
dengan pengujian BNT dengan taraf nyata 5%. Data yang diperoleh dianalisis
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
Perlakuan aplikasiM. anisopliaeterhadapsymphyliddengan metode residu pakan dan residu media hidupsymphylidpada tanah berbahan organik dan tanpa bahan organik tidak memberikan pengaruh yang nyata terhadap mortalitassymphylid sampai dengan pengamatan 20 hari. Motalitassymphylidtertinggi hanya sebesar 10% dan hasil penelitian ini belum dapat membuktikan bahwaM. anisopliae mampu menginfeksi dan menyebabkan kematiansymphylid.
5.2 Saran
Perlu penelitian lebih lanjut untuk mengerahuiM. anisopliaedengan asal isolat dari beberapa tempat apakah bersifat infektif hamaSimphyliddengan
PUSTAKA ACUAN
Ahmad, R. Z. 2004. Cendawan Metarhizium anisopliae sebagai Pengendalian Hayati Ektoparasit Caplak dan Tungau pada Ternak. Wartazoa 14(2):73-78
Alexopoulous, C.J., C.W. Mims, and M. Blackwel. 1996. Introductory Mycology. Jhon Willey & Sons Inc. New York.
Alphonsine, P. 2010. A Bait and Trap Method for Sampling Symphylid Populations in Pineaple. 7tnInternational Pinaple Symposium.
Anggraeni, S. 2015. Praktik Pengamatan Patogenesitas Jamur Beuveria dan Jamur Metarhizium terhadap Hama Symphiliddi Laboratorium PT. Great Gean Peanaple (GGP) Terbanggi Besar Lampung Tengah (Laporan Praktik Umum) Universitas Lampung. Bandar Lampung.
Badan Pusat Statistik. 2014. Horticulture Statistic.http://.bps.go.id/
Bartholomew, D. 2001.Newsletter of the Pineapple Working Group.International Society for Horticultural Science.
Berry,R.E. dan Robinson, R.R 1974.Biology and Control of the Garden Symplylans. Oregon State University. Extention Serve. Extention Circular 845.
Carr, P. 2003. Garden Symphlyd (Scutigerella immaculata). Departement of Primary Industries VegCheque Extention Program. The State of Victoria.
Darwis, M, 1989,Pengaruh Jenis Media Organik dan Kedalaman Inokulum Metarhizium anisopliae terhadap Mortalitas Larva Oryctes rhinoceros. Balai Penelitian Kelapa. Manado.
Edwards, C. A. 1990. Symphyla. dlm:Soil Biologi Guide. Dindal, D. L (ed.). A willey–Interscience Publication John Willey & Sains, USA.
Ferron, P. 1985. Fungal control. Comprehensive Insect Phisiology, Biochem. Pharmacol. (12): 313−346
Gopalakrishnan, C. 2001. Fungal Pathogens as Components in I ntegrated Pest Management of Horticultural Crops. Integrated Pest Management in Horticultural Ecosystems. Capital Publishing Company. New Delhi. Herlinda, S., E.M. Sari, Y. Pujiastuti, Suwandi, E. Nurnawati & A. Riyanta.
2005a. Variasi virulensi strain-strain Beauveria bassiana (Bals.) Vuill. terhadap larvaPlutella xylostella(L.) (Lepidoptera: Plutellidae). Agritrop24:52-57.
Kershaw, M. J., E. R. Moorhouse, R. Bateman, S. E. Reynolds, and A. K. Charnley. 1999. The Role of Destruxin in the Pathogenecity of Metarhizium anisopliarfor Three Species of Insect. Journal of Invertebrate Pathology 74 : 213–223.
Laird, M., Lacey, L. A., dan Davidson, E. W . 1990. Safety of Microbial Insecticide. CRC Press. Boca. Raton
Oviana,Tya. 2013. Hubungan Kondisi Visual Tanaman Dengan Populasi Symphylid Dan Gejala Witches Broom Pada Akar Tanaman Nanas [Ananas Comosus(L) Merr] Di Perkebunan PT Great Giant Pineapple. ( Laporan Praktik Umum ) Universitas Lampung. Bandar Lampung Prayogo, Y., W. Tengkano dan Marwoto. 2005. Prospek Cendawan
Entomopatogen Metarhizium anisopliae Untuk Mengendalikan Ulat Grayak Spodoptera litura Pada Kedelai. Jurnal Litbang Pertanian 24(1):19-26.
Py, C., Lacoeulilhe, J.J. and Teison, C. 1987. The Peanaple : Cultivation and Uses.G.P. Maisonneuve et Larose, Paris.
Roharbach, K.G. and M.W. Johnson.2003. Pest, Diseases and Weeds.InD.P Bartholomew, R.E Paull and K.G Rohrbach ( Eds.) The panaple Botani Production and Uses.University of Hawai at Manoa, Honolulu, USA. CABI Publishing.
Rustama, M., M. Melanie dan B. Irawan. 2008. Patogenisitas Jamur EntomopatogenMetarhizium anisopliaeterhadapCrocidolomia pavonanaFab. dalam Kegiatan Studi Pengendalian Hama Terpadu Tanaman Kubis dengan Menggunakan Agensia Hayati. (Laporan Akhir Penelitian Peneliti Muda). Universitas Padjajaran. 58 hlm
Soler, A., Gaude, J.M.,Alponsine, P. A. M Vinatier, F., Dole, B., Govidin, J.C., Fournier, P., dan Queneherve,P. 2011. Development and evaluation of a new method for sampling and monitoring the symphylid population in pineapple. Pest manage Sci 67:1169-1177
Tanada, Y. dan H. K. Kaya, 1993. Insect Pathology. Academic Press, Inc. California.
Umble, J. R., dan J R. Fisher. 2003. Influence of below-ground feeding by garden Symphylans (Cephalostigmata: Scutigerellidae) on plant healt. Environmental Entomology32 (5): 1251-1261.
Umble, J., Dufour, R.,Fisher, G., Fisher, J., Leap, J., dan Horn, M. V. 2006. Symphylans: Soil Pest Management Options. ATTRA. National Center for Approprivate Technology (NCAT). Butte.