Uji Fitokimia dan Aktivitas Antioksidan
Ekstrak Jantung Pisang Batu (Musa balbisiana Colla)
Diajukan untuk memenuhi syarat mata kuliah Praktikum Kimia Bahan AlamOleh: Fahri rachmat Anissa nurlely
Ameliani Sri suci mulyani
Program Studi Kimia
Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah
Jakarta
ii KATA PENGANTAR
Syukur Alhamdulillah penulis ucapkan kehadirat Allah subhanallahuwata’ala atas karunia yang tak terhingga dengan selesainya penyusunan makalah yang berjudul “
Uji
Fitokimia dan Aktivitas Antioksidan Ekstrak Jantung Pisang Batu (Musa
balbisiana Colla)
”. Melalui penelitian ini, penulis berharap dapat berpartisipasi dalam membangun kemajuan ilmu pengetahuan bangsa dan dapat bermanfaat bagi kehidupanmasyarakat Indonesia. Penyusunan makalah ini tidak terlepas dari dukungan dan bantuan
yang sangat berharga dari berbagai pihak. Oleh karena itu, penulis sangat berterima kasih,
terutama kepada :
1. Dosen Pembimbing kami Eka Rizky Amelia S.Si
2. Kepala Laboratorium Kimia yang telah mengizinkan kami melakukan penelitian ini.
3. Serta pihak-pihak yang tak sempat disebutkan yang telah membantu atas bantuan dan
dukungan yang tak terhingga, mohon maaf atas kekhilafan penulis.
Semoga makalah ini dapat bermanfaat bagi kemajuan riset di bidang pangan
khususnya dan bagi masyarakat Indonesia pada umumnya. Penulis menyadari akan
kekurangan yang tak dapat dihindari pada makalah ini, sehingga masukan kiritik dan saran
sangat diharapkan untuk menyempurnakan makalah ini.
Ciputat, 20 Oktober 2013
DAFTAR ISI
Kata Pengantar ... ii
Daftar Isi ... iii
BAB I PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 2
1.3 Hipotesis ... 2
1.4 Tujuan Penelitian ... 2
1.5 Manfaat Penelitian ... 2
BAB II TINJAUAN PUSTAKA 2.1 Botani Tanaman Pisang ... 4
2.2 Pisang Batu ... 6
2.3 Jantung Pisang ... 7
2.4 Ekstraksi ... 8
2.5 Metode Ekstraksi ... 9
2.5.1 Maserasi ... 9
2.5.2 Perkolasi ... 9
2.5.3 Sokletasi ... 10
2.6 Fitokimia ... 10
2.6.1 Alkaloid ... 11
2.6.2 Flavonoid ... 12
2.6.3 Terpenoid ... 12
2.6.4 Saponin ... 13
2.6.5 Kuinon ... 13
2.6.6 Tanin ... 14
2.6.7 Polifenol ... 14
iv BAB III METODELOGI PENELITIAN
3.1 Lokasi Penelitian ... 17
3.2 Bahan dan Alam ... 17
3.3 Metode Penelitian ... 17
BAB IV HASIL DAN PEMBAHASAN
4.1 Ekstraksi ... 23
4.2 Uji Fitokimia ... 24
4.3 Uji Aktivitas Antioksidan ... 27
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan ... 30
DAFTAR PUSTAKA ... 31
1 BAB I
PENDAHULUAN
1.1. Latar Belakang
Pisang (Musa balbisiana Colla) merupakan tanaman buah-buahan tropika yang berasal dari Asia Tenggara, Brazil dan India. Di Asia Tenggara, pisang diyakini
berasal dari Semenanjung Malaysia dan Filipina. Pisang telah lama berkembang di
India yaitu sejak 500 tahun sebelum masehi dan menyebar sampai ke daerah Pasifik.
Pisang memiliki peranan penting di Indonesia karena dikonsumsi oleh konsumen
tanpa memperhatikan tingkat sosial (Satuhu dan Supriadi, 2000). Indonesia
merupakan salah satu sentra primer keragaman pisang,baik pisang segar, olahan dan
pisang liar. Lebih dari 200 jenis pisang terdapat di Indonesia. Sentra produksi pisang
di Indonesia tersebar di 16 provinsi, 70 kabupaten. Provinsi tersebut antara lain NAD,
Sumatera Utara, Sumatera Barat, Sumatera Selatan, Lampung, Riau, Jawa Timur
,Jawa Barat, Jawa Tengah ,Banten, Bali, Kalimantan Barat, Kalimantan Selatan,
Kalimantan Timur, Sulawesi Selatan, dan Maluku Utara. Selama periode 1995 sampai
2002 luas panen pisang berfluktuasi, namun pada tahun 2003-2004 cenderung
meningkat (BPS, 2003).
Di Indonesia tanaman pisang adalah tanaman yang multiguna, selain buahnya
yang digunakan sebagai bahan konsumsi, daunya juga dapat digunakan sebagai
pembungkus dan bakal buahnya atau yang sering dikenal sebagai jantung pisang
digunakan sebagai sayur. Pisang memiliki kandungan gizi seperti karbohidrat,
vitamin, mineral, air, lemak dan protein(Direktor Jenderal Bina Reproduksi
Hortikultura, 2003).
Selain itu, pisang merupakan jenis buah yang mengandung banyak senyawa
kimia yang bersifat antioksidan. Penelitian terhadap pisang menunjukan bahwa pisang
tersebut banyak mengandung phenolik serta karotene (Fatemeh et al.,2012). Selain pada buah pisang, antioksidan juga terdapat pada kulit pisang. Antioksidan yang
terdapat pada kulit pisang memiliki aktivitas yang lebih tinggi dibandingan dengan
- 2 - Penelitian-penelitian mengenai aktivitas antioksidan pada buah maupun kulit
pisang sudah banyak dilakukan namun, penelitian-pennelitian tersebut belum banyak
menggunakan bakal buah atau jantung pisang khususnya jantung pisang batu (Musa balbisiana Colla). Selain itu pisang batu merupakan holtikultura asli Indonesia.Oleh karna itu, penelitian ini dilakukan guna mengetahui senyawa antioksidan pada
Jantung pisang (Musa balbisiana Colla) serta aktivitas antioksidan yang terdapat pada Jantung pisang (Musa balbisiana Colla). Diharapkan hasil penelitian ini dapat memberikan informasi serta manfaat yang berguna bagi dunia kesehatan maupun
dunia pendidikan.
1.2. Rumusan Masalah
Berdasarkan latar belakang timbul pertanyaan, senyawa antioksidan apa yang
terdapat pada Jantung Pisang (Musa balbisiana Colla) serta bagaimanakah aktifitas antioksidan dari ekstrak etil asetat dan etanol Jantung Pisang (Musa balbisiana Colla).
1.3. Hipotesis
Aktifitas jantung pisang (Musa balbisiana Colla). Memiliki aktivitas antioksidan yang baik. Senyawa antioksidan yang terdapat pada jantung pisang (Musa balbisiana Colla) yaitu flavonoid.
1.4. Tujuan Penelitian
Tujuan dari penelitian ini antara lain:
1.4.1. Mengetahui senyawa antioksidan yang terdapat pada Jantung Pisang (Musa balbisiana Colla).
1.4.2. Mengetahui aktifitas antioksidan dari ekstrak etil asetat dan kloroform Jantung
Pisang (Musa balbisiana Colla).
1.5. Manfaat Penelitian
Manfaat penelitian ini antara lain:
1.5.1. Hasil penelitian ini diharapkan dapat memberikan informasi mengenai
manfaat Jantung Pisang (Musa balbisiana Colla) sebagai sumber antioksidan kepada masyarakat dan sebagai dasar ilmiah dalam pengembangan dan
3 1.5.2. Hasil penelitian ini diharapkan dapat memberikan informasi mengenai
aktifitas antioksidan dari ekstrak Jantung Pisang (Musa balbisiana Colla) dengan pelarut etil asetat dan etanol sebagai dasar ilmiah dalam
- 4 - BAB II
TINJAUAN PUSTAKA
2.1 Botani Tanaman Pisang
Pisang adalah tanaman buah berupa herba yang berasal dari kawasan di Asia
Tenggara (termasuk Indonesia). Tanaman ini kemudian menyebar ke Afrika
(Madagaskar), Amerika Selatan dan Tengah. Menurut Ahli sejarah dan botani
mengambil kesimpulan, bahwa tanaman pisang berasal dari Asia Tenggara yang
disebarkan oleh para penyebar agama Islam (Satuhu dan Supriyadi, 2004). Di Jawa
Barat, pisang biasa disebut dengan Cau sedangkan di Jawa Tengah dan Jawa Timur
dinamakan sebagai gedang.
Menurut Astawan (2005) kata pisang berasal dari bahasa Arab, yaitu ”maus” yang oleh Linneus dimasukkan ke dalam keluarga Musaceae untuk memberikan
penghargaan kepada Antonius Musa, dokter pribadi kaisar Romawi (Octaviani
Agustinus) yang menganjurkan untuk memakan pisang. Itulah sebabnya dalam bahasa
Latin, pisang disebut Musa paradisiacal. Tanaman pisang termasuk dalam kingdom Plantae filum Spermatophyte, kelas Angiospermae, subkelas Monocotyledone, ordo Scitamineceae, family Musaceae (Anonim, 2005), Spesies Musa Spp dan terdiri dari dua genus yaitu Ensente dan Musa. Genus Musa dibagi menjadi empat golongan yaitu
Australimusa, Eumusa, Callimusa, Rodochlamys. Australimusa dan Eumusa adalah
golongan yang banyak dimanfaatkan sebagai buah konsumsi. Golongan Eumusa
adalah golongan yang saat ini paling banyak dibudidayakan. Kultivar pisang yang
dapat dimakan dan terkenal sekarang merupakan hasil persilangan dari dua spesies
liar anggota Eumusa yaitu Musa acuminata (AA) dan Musa balbisiana (BB) (Simmonds, 1959). Hasil persilangan pisang budidaya diploid tersebut menghasilkan
turunan hibrid steril baik diploid, triploid maupun tetrapolid dengan genom AB,
AAA, AAB, ABB dan seterusnya.
Menurut Satuhu dan Supriyadi (2004) pisang merupakan tanaman yang mudah
tumbuh di sembarang tempat. Namun, agar produktivitas tanaman optimal, sebaiknya
ditanam di dataran rendah. Dimana ketinggian tempat harus di bawah 1000 meter di
atas permukaan laut. Di atas itu, produksi pisang kurang optimum dan waktu berbuah
5 adalah iklim basah dengan curah hujan merata sepanjang tahun. Oleh karena itu,
pisang memberikan hasil yang baik pada musim hujan dan hasil yang kurang
memuaskan pada musim kemarau. Jenis tanah yang disukai tanaman pisang adalah
tanah liat yang mengandung kapur atau tanah alluvial dengan pH antara 4.5-7.5
(Satuhu dan Supriyadi, 2004).
Tanaman pisang sangat banyak membutuhkan zat mineral seperti kalium dan
fosfor untuk pertumbuhannya (Munadjim, 1983). Mineral ini banyak terdapat di
dalam tanaman yang telah membusuk seperti sampah, kompos dan lain-lain. Di
samping itu, mineral kalium dan fosfor banyak terdapat di dalam tanah yang
mengandung kapur. Tanaman pisang yang ditanam pada tanah biasa dapat tumbuh
dengan subur dan memiliki produktivitas yang tinggi jika dilakukan pemupukan yang
mengandung kalium dan fosfat (Rusmianto, 2007). Berikut adalah nilai kandungan
gizi pada buah psang per 100 gram bahan dalam tabel 1.
Pisang adalah bahan pangan yang bergizi merupakan sumber karbohidrat,
protein, vitamin, dan mineral. Komponen karbohidrat terbesar pada buah pisang
adalah pati pada daging buahnya, dan akan diubah menjadi sukrosa, glukosa dan
fruktosa pada saat pisang matang (15-20 %) (Bello et al., 2000). Berdasarkan jenisnya pisang di kelompokkan menjadi empat jenis yaitu (1) pisang yang dapat
dimakan langsung buahnya tanpa dimasak contohnya pisang kepok, susu, hijau,
- 6 - (diolah terlebih dahulu) contohnya pisang tanduk, oli dan kapas. (3) Pisang yang
diambil seratnya dimanfaatkan untuk keperluan tekstil dengan memanfaatkan serat
batangnya. Pisang ini disebut sebagai pisang manila karena di duga berasal dari
Manila., dan pisang berbiji yaitu pisang batu (pisang klutuk).
2.2 Pisang Batu
Berdasarkan jenisnya pisang batu termasuk ke dalam jenis pisang berbiji yaitu
M.usa brachycarpa Back yang di Indonesia daunnya sering dimanfaatkan (Hendro Sunaryono, 2003:41). Nama lain dari tanaman ini yaitu Musa balbisiana Colla atau pisang klutuk, pisang biji dan pisang bereng. Pisang batu merupakan tanaman yang
dijumpai sebagai tanaman liar atau dibudidayakan, dan diduga bahwa pisang yang
umumnya dibudidayakan sekarang merupakan turunan dari Musa balbisana Colla dan Musa acuminate Colla yang banyak memiliki keanekaragaman di Muangthai,
Malaysia, Indonesia, dan Papua Nugini (Anonim 1977). Tanaman budidaya biasanya
tidak diambil daging buahnya tetapi diambil bagian daunnya sebagai kemasan
pembungkus karena daunnya lebih tebal (banyak mengandung lapisang lilin)
dibandingkan daun pisang jenis lain sehingga tidak mudah sobek atau rusak ketika
diguna-kan (Irbi’ati 2002).
Tanaman pisang batu memiliki ciri-ciri pertumbuhan yaitu bersemak,
berumpun, tinggi tanaman 3 meter dengan lingkar batang 60-70 cm, memiliki batang
semu, berpelepah, berwarna hijau dengan atau tanpa coklat kehitaman, memiliki daun
tunggal yang panjangnya 60-200cm, bentuk lanset memanjang, mudah koyak, pada
permukaan bawah daun berlilin, tandan buah mencapai panjang 80-100 cm, jantung
berbetuk bulat telur memiliki daun pelindung (kelopak luar) berwarna ungu dan
sebelah berwarna merah, mudah rontok, mahkota bunga segitiga berwarna putih
kekuningan. Buah bulat memanjang tersusun seperti sisir dua baris, berwarna hijau.
Biji kecil bulat dan hitam, Daging buah putih atau kekuning-kuningan, rasa kurang
manis dan tekstur agak kasar (Anonim, 2006).
Bagian dari tanaman pisang batu yang banyak dimanfaatkan oleh masyarakat
yaitu bagian buah, akar dan daun. Buah pisang batu memiliki biji yang dapat
membedakan jenis pisang ini dari pisang lainnya. Selain memiliki biji, daun pisang
7 tradisional. Kandungan kimia yang dimiliki oleh pisang batu yaitu serotonin dan
norepinefrin yang berfungsi sebagai penenang bagi tubuh.
2.3 Jantung Pisang
Jantung pisang merupakan nama lain dari bunga pisang karena bentuknya
menyerupai jantung. Jantung pisang adalah salah satu bagian dari tanamanpisang
yang mempunyai warna merah keunguan. Menurut Simonds (1962, dalam
Pazmino-Duren et al,. 2001), variasi pada jantung pisang berhubungan dengan kandungan
antosianin yang terdapat di dalamnya. Dengan adanya antosianin tersebut pada
tanaman pisang menyebabkan tanaman pisang akan tumbuh sepanjang tahun dan
mudah dibudidayakan. Pada umumnya jantung pisang dimanfaatkan untuk dibuat
sayur karena memiliki kandungan gizi yaitu protein, lemak, karbohidrat, kalsium,
besi, fosfor, vitamin A, B dan vitamin C. Selain dibuat sayur, jantung pisang dapat
pula dibuat manisan, acar, maupun lalapan. Namun, jantung pisang belum
dimanfaatkan secara optimal, bahkan sering dibuang begitu saja. Menurut Satuhu dan
Supriyadi (2004), bunga jantung pisang berkelamin satu dan berumah satu dalam
tandan. Daun penumpu bunga berjejal rapat dan tersusun secara spiral. Daun
pelindung bunga atau seludang yang berada di luar berwarna merah tua dan di dalam
berwarna putih kekuningan, daun pelindung berlilin dan mudah rontok denganpanjang
10-25 cm. Bunga tersusun dalam dua baris melintang. Rangkaian bunga pada pangkal
merupakan bunga betina dan bisa menjadi buah. Rangkaian bunga bagian tengah
merupakan bunga sempurna dan dapat menjadi buah. Sedangkan bunga yang berada
di bagian pucuk adalah bunga jantan dan tidak bisa menjadi buah. Bunga betina
berada di bawah bunga jantan (jika ada). Lima daun tenda bunga melekat sampai
tinggi, panjangnya 6-7 cm. Benang sari 5 buah pada bunga betina tidak sempurna,
bakal buah persegi, sedangkan pada bunga jantan tidak ada benang sari (Rusmianto,
2007).
Menurut Putro dan Rosita (2006), jantung pisang terdiri dari empat rasa.
Keempat rasa tersebut yaitu :
a. Rasa gurih dan hambar, terdapat pada jantung pisang kepok, jantung pisang batu
(klutuk), dan jantung pisang hutan.
b. Rasa asam, terdapat pada jantung pisang marlin, jantung pisang kole dan jantung
- 8 - c. Rasa sepat, terdapat pada jantung pisang susu, tanduk dan jantung pisang raja.
d. Rasa pahit, terdapat pada jantung pisang ambon putih dan jantung pisang nangka.
Jantung pisang memiliki nilai gizi yang dapat dimanfaatkan oleh manusia.
Komposisi nilai gizi dari setiap jantung pisang berbeda-beda, hal ini dikarenakan jenis
dan tempat pertumbuhannya berbeda-beda pula. Komposisi gizi jantung pisang
disajikan pada Tabel 2
bermanfaat bagi tubuh manusia.Jantung pisang klutuk atau yang lebih dikenal dengan
jantung pisang batu merupakan jenis jantung pisang yang memiliki nilai gizi tertinggi
jika dibandingkan dengan jantung pisang lainnya. Jantung pisang batu memiliki warna
seludang merah hati sehingga jantung pisang batu dapat dibedakan dari jantung pisang
lainnya.
2.4 Ekstraksi
Ekstraksi adalah suatu proses pemisahan dari bahan padat maupun cair dengan
bantuan pelarut. Pelarut yang digunakan harus dapat mengekstrak substansi yang
diinginkan tanpa melarutkan material lainnya. Ekstraksi padat cair atau leaching
adalah transfer difusi komponen terlarut dari padatan inert ke dalam pelarutnya.
Proses ini merupakan proses yang bersifat fisik karena komponen terlarut kemudian
dikembalikan lagi ke keadaan semula tanpa mengalami perubahan kimiawi. Ekstraksi
dari bahan padat dapat dilakukan jika bahan yang diinginkan dapat larut dalam solven
pengekstraksi. Ekstraksi berkelanjutan diperlukan apabila padatan hanya sedikit larut
dalam pelarut. Namun sering juga digunakan pada padatan yang larut karena
9 kemampuan kelarutan yang berbeda dari komponen-komponen yang terdapat di
dalam campuran (Bernasconi, et al, 1987).
2.5 Metode Ekstraksi
Terdapat beberapa metode ekstraksi senyawa organik bahan alam yang sering
digunakan pada penelitian adalah sebagai berikut :
2.5.1 Maserasi
Menurut Guenther (1987), maserasi adalah proses perendaman sampel
dengan pelarut organic yang digunakan pada temperature ruang. Umumnya
perendaman dilakukan 24 jam dan selanjutnya pelarut diganti dengan pelarut
baru. Namun dari beberapa penelitian melakukan perendaman hingga 72 jam.
Selama proses perendaman, cairan akan menembus dinding sel dan masuk ke
dalam rongga sel yang mengandung zat aktif. Kemudian zat aktif akan larut
dan karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel
dengan yang di luar sel, maka larutan yang terpekat didesak keluar. Peristiwa
tersebut terus berulang hingga terjadi keseimbangan konsentrasi antara larutan
antara larutan di luar sel dengan larutan di dalam sel. Keuntungan cara
ekstraksi dengan maserasi adalah cara pengerjaan dan peralatan yang
sederhana. Namun metode ini juga memiliki kekurangan, yaitu cara
pengerjaannya yang lama dan ekstraksi yang kurang sempurna (Anonim
2013a).
2.5.2 Perkolasi
Perkolasi merupakan cara ekstraksi yang dilakukan dengan
mengalirkan pelarut melalui bahan sehingga komponen dalam bahan tersebut
tertarik ke dalam pelarut (Anonim 2013 a). Pada prinsipnya, serbuk sampel
ditempatkan di dalam suatu bejana silinder yang dibawahnya diberikan sekat
berpori. Kemudian cairan pelarut dialirkan dari atas ke bawah melalui serbuk
tersebut sehingga akan melarutkan zat aktif (Lestari, 2008).
Keutamaan yang berperan pada perkolasi antara lain: gaya berat,
kekentalan, daya larut, tegangan permukaan, difusi, osmosis, adesi, daya
kapiler dan daya geseran (friksi). Hasil perkolasi disebut perkolat. Perkolasi
- 10 - proses perkolasi, terjadi partisi komponen yang diekstraksi, antara bahan dan
pelarut. Dengan pengaliran pelarut secara berulang-ulang, maka semakin
banyak komponen yang tertarik.
Kelemahan dari metode ini yaitu diperlukan banyak pelarut dan waktu
yang lama, sedangkan komponen yang didapat relatif tidak banyak.
Keuntungannya adalah tidak memerlukan pemanasan sehingga teknik ini baik
untuk substansi termolabil (yang tidak tahan terhadap panas) (Anonim 2013 a).
2.5.3 Sokletasi
Sokletasi adalah proses ekstraksi dimana sampel yang akan diekstraksi
ditempatkan dalam suatu timbel yang permeabel (kertas saring) terhadap
pelarut dan diletakkan di atas tabung destilasi, dididihkan dan
dikondensaasikan di atas sampel. Kemudian kondesat akan jatuh ke dalam
timbel dan merendam sampel dan diakumulasi sekeliling timbel. Setelah
sampai batas tertentu, pelarut akan kembali masuk ke dalam tabung destilasi
secara otomastis. Proses ini berulang terus dengan sendirinya di dalam alat
sampai ekstraksi terjadi sempurna (Anonim, 2013a). Ekstraksi sempurna
ditandai apabila cairan di kertas saring tidak berwarna lagi, tidak tampak noda
jika di KLT, atau sirkulasi telah mencapai 20-25 kali (Sukandar et al., 2013).
2.6 Fitokimia
Fitokimia atau kadang disebut fitonutrien, sedangkan dalam arti luas fitokimia
adalah segala jenis zat kimia atau nutrient yang diturunkan dari tumbuhan. Menurut
Sukandar et al,. (2013), fitokimia berasal dari kata phytochemical. Phyto adalah
tumbuhan dan Chemical adalah zat kimia. Dengan demikian fitokimia merupakan zat
kimia alami yang terdapat di dalam tumbuhan dan dapat memberikan rasa, aroma atau
warna pada tumbuhan itu. Akan tetapi senyawa fitokimia tidak termasuk kedalam zat
gizi karena bukan berupa karbohidrat, protein, lemak, vitamin, mineral maupun air.
Fitokimia adalah salah satu ilmu yang mempelajari berbagai senyawa
organik yang dibentuk dan disimpan oleh tumbuhan, yaitu tentang struktur kimia,
biosintetis, perubahan dan metabolisme, serta penyebaran secara alami dan fungsi
biologis dari senyawa organik (Anonim, 2013 a). Sampai saat ini sudah sekitar
11 (Anonim, 2013 a). Secara garis besar, fitokimia terdiri dari alkaloid, flavonoid,
terpenoid, saponin, kuinon dan tannin.
2.7 Jenis-Jenis Senyawa Fitokimia
2.7.1 Alkaloid
Alkaloid adalah sebuah golongan senyawa basa bernitrogen yang
kebanyakan heterosiklik dan terdapat di tumbuhan (tetapi ini tidak
mengecualikan senyawa yang berasal dari hewan). Asam amino, peptida,
protein, nukleotid, asam nukleik, gula amino dan antibiotik biasanya tidak
digolongkan sebagai alkaloid. Dan dengan prinsip yang sama, senyawa netral
yang secara biogenetik berhubungan dengan alkaloid termasuk digolongan ini
(Anonim, 2013b).
Menurut Sastrohamidjojo (1995), sifat fisika dari senyawa alkaloid
yang telah diisolasi merupakan padatan Kristal dengan titik lebur yang tertentu
atau mempunyai kisaran dekomposisi. Sedikit alkaloid yang termasuk amorf
dan beberapa seperti nikotin (20) dan konini (21) berupa cairan. Kebanyakan
alkaloid tersebut tidak berwarna, tetapi beberapa senyawa yang kompleks,
spesies aromatic berwarna (contoh, berberin (22) berwarna kuning dan betanin
(23) merah). Pada umumnya basa bebas alkaloid hanya larut dalam pelarut
organic, meskipun pseudo dan protoalkaloid larut dalam air. Garam alkaloid
dan alkaloid quartener sangat larut dalam air.
Sedangkan sifat kimia dari alkaloid menurut Sastrohamidjojo (1995),
adalah bersifat basa. Sifat tersebut tergantung pada adanya pasangan electron
pada nitrogen. Jika gugus fungsional yang berdekatan dengan nitrogen bersifat
melepaskan electron, sebagai contoh gugus alkil, maka ketersediaan electron
pada nitrogen naik dan senyawa lebih bersifat basa. Sebaliknya apabila gugus
fungsional yang berdekatan bersifat menarik electron (contoh, gugus karbonil0
maka ketersediaan pasangan electron berkurang dan pengaruh alkaloid yang
ditimbulkan dapat bersifat netral atau sedikit asam. Contohnya adalah senyawa
- 12 - 2.7.2 Flavonoid
Flavonoid merupakan salah satu kelompok senyawa metabolit
sekunder yang paling banyak ditemukan di dalam jaringan tanaman
(Rajalakshmi dan S. Narasimhan, 1985). Flavonoid termasuk dalam golongan
senyawa phenolik dengan struktur kimia C6-C3-C6 (White dan Y. Xing, 1951;
Madhavi et al., 1985; Maslarova, 2001) (Gambar 1). Kerangka flavonoid
terdiri atas satu cincin aromatik A, satu cincin aromatik B, dan cincin tengah
berupa heterosiklik yang mengandung oksigen dan bentuk teroksidasi cincin
ini dijadikan dasar pembagian flavonoid ke dalam sub-sub kelompoknya
(Hess, tt). Sistem penomoran digunakan untuk membedakan posisi karbon di
sekitar molekulnya (Cook dan S. Samman, 1996).Berbagai jenis senyawa,
kandungan dan aktivitas antioksidatif flavonoid sebagai salah satu kelompok
antioksidan alami yang terdapat pada sereal, sayur-sayuran dan buah, telah
banyak dipublikasikan. Flavonoid berperan sebagai antioksidan dengan cara
mendonasikan atom hidrogennya atau melalui kemampuannya mengkelat
logam, berada dalam bentuk glukosida (mengandung rantai samping glukosa)
atau dalam bentuk bebas yang disebut aglikon (Cuppett et al.,1954).
2.7.3 Terpenoid
Terpenoid merupakan derivat dehidrogenasi dan oksigenasi dari
senyawa terpen. Terpen merupakan suatu golongan hidrokarbon yang banyak
dihasilkan oleh tumbuhan dan sebagian kelompok hewan. Rumus molekul
terpen adalah (C5H8)n. Terpenoid disebut juga dengan isoprenoid. Hal ini
disebabkan karena kerangka karbonnya sama seperti senyawa isopren. Secara
13 berupa rantai terbuka atau siklik, dapat mengandung ikatan rangkap, gugus
hidroksil, karbonil atau gugus fungsi lainnya (Anonim 2012).
2.7.4 Saponin
Saponin adalah suatu glikosida alamiah yang terikat dengan steroid
atau triterpena. Saponin mempunyai aktifitas farmakologi yang cukup luas
diantaranya meliputi: immunomodulator, anti tumor, anti inflamasi, antivirus,
anti jamur, dapat membunuh kerang-kerangan, hipoglikemik, dan efek
hypokholesterol. Saponin juga mempunyai sifat bermacam-macam, misalnya:
terasa manis, ada yang pahit, dapat berbentuk buih, dapat menstabilkan
emulsi, dapat menyebabkan hemolisis. Dalam pemakaiannya saponin bisa
dipakai untuk banyak keperluan, misalnya dipakai untuk membuat minuman
beralkohol, dalam industry pakaian, kosmetik, membuat obat-obatan, dan
dipakai sebagai obat tradisional. Biarpun saponin bisa diisolasi dari binatang
tingkat rendah, sebenarnya saponin ditemukan terutama dalam
tumbuh-tumbuhan. Namanya diambil dari Genus suatu tumbuhan yaitu Saponaria,
akar dari famili Caryophyllaceae dapat dibuat sabun. Saponin juga bisa
didapatkan dalam beberapa famili tumbuhan yang lain (Anonim, 2013c).
2.7.5 Kuinon
Kuinon adalah senyawa berwarna dan mempunyai kromofor dasar
seperti kromofor pada benzokuinon, yang terdiri atas dua gugus karbonil yang
berkonjugasi dengan dua ikatan rangkap karbo-karbon. Untuk tujuan
identifikasi kuinon dapat dibagi atas empat kelompok yaitu : benzokuinon,
naftokuinon, antrakuinon dan kuinon isoprenoid. Tiga kelompok pertama
biasanya terhidroksilasi dan bersifat fenol serta mungkin terdapat dalam
bentuk gabungan dengan gula sebagai glikosida ataudalam bentuk kuinol
(Harborne, 1987).
Senyawa-senyawa kuinon merupakan zat warna yang terdapat dalam
tumbuh-tumbuhan yang berasal dari turunan senyawa aromatik. Menurut Hart (1983: 273)“Kuinon merupakan golongan senyawa karbonil yang unik. Senyawa ini merupakandiketon terkonjugasi siklik. Contoh paling sederhana
- 14 - berupa pigmen alami yang digunakansebagai zat warna”.Warna pigmen kuinon alam beragam, mulai dari kuning pucat sampai kehampir hitam, dan
struktur yang telah dikenal jumlahnya lebih dari 450. Walaupun mereka
tersebar luas dan strukturnya sangat beragam, sumbangannya terhadap
warnatumbuhan tinggi nilai nisbi kecil. Jadi, pigmen ini sering terdapat dalam
kulit, galihatau akar, atau dalam jaringan lain (misalnya daun), tetapi pada
jaringan tersebutwarnanya tertutupi pigmen lain.
2.7.6 Tanin
Tanin adalah senyawa metabolit sekunder yang terdapat pada beberapa
tanaman. Tanin mampu mengikat protein, sehingga protein pada tanaman dapat
resisten terhadap degradasi oleh enzim protease di dalam silo ataupun rumen
(Kondo et al., 2004). Tanin selain mengikat protein juga bersifat melindungi
protein dari degradasi enzim mikroba maupun enzim protease pada tanaman
(Oliveira et al., 2009), sehingga tanin sangat bermanfaat dalam menjaga
kualitas silase. Tanin merupakan senyawa kimia yang tergolong dalam
senyawa polifenol (Deaville et al., 2010). Tanin mempunyai kemampuan
mengendapkan protein, karena tanin mengandung sejumlah kelompok ikatan
fungsional yang kuat dengan molekul protein yang selanjutnya
akanmenghasilkan ikatan silang yang besar dan komplek yaitu protein tanin.
Tanin mempunyai berat molekul 0,5-3 KD. Tanin alami larut dalam air dan
memberikan warna pada air, warna larutan tanin bervariasi dari warna terang
sampai warna merah gelap atau coklat, karena setiap tanin memiliki warna
yang khas tergantung sumbernya (Ahadi, 2003).
2.7.7 Polifenol
Senyawa yng termasuk kedalam polifenol ini adalah semua
senyawayang memiliki struktur dasar berupa fenol. Fenol sendiri merupkan
struktur yangterbentuk dari benzena tersubtitusi dengan gugus –OH. Gugus –
OH yang terkandungmerupakan aktivator yang kuat dalam reaksi subtitusi
15 Polifenol adalah kelompok zat kimia yang ditemukan pada
tumbuhan. Polifenol (polyphenol) merupakan senyawa kimia yang bersifat
antioksidan kuat. Zat ini memiliki tanda khas yakni memiliki banyak gugus
fenol dalam molekulnya. Polifenol berperan dalam memberi warna pada suatu
tumbuhanseperti warna daun saat musim gugur. Pada beberapa penelitian
disebutkan bahwa kelompok polifenol memiliki peran sebagai antioksidan yang
baik untuk kesehatan. Antioksidan polifenol dapat mengurangi risiko penyakit
jantung dan pembuluh darah dan kanker. Terdapat penelitian yang
menyimpulkan polifenol dapat mengurangi risiko penyakit Alzheimer.
2.8 Antioksidan
Antioksidan adalah senyawa kimia yang dapat menyumbangkan satu atau
lebih elektron kepada radikal bebas, sehingga radikal bebas tersebut dapat diredam
(Suhartono, 2002). Berdasarkan sumber perolehannya ada 2 macam antioksidan, yaitu
antioksidan alami dan antioksidan buatan (sintetik) (Dalimartha dan Soedibyo, 1999).
Tubuh manusia tidak mempunyai cadangan antioksidan dalam jumlah berlebih,
sehingga jika terjadi paparan radikal berlebih maka tubuh membutuhkan antioksidan
eksogen. Adanya kekhawatiran akan kemungkinan efek samping yang belum
diketahui dari antioksidan sintetik menyebabkan antioksidan alami menjadi alternatif
yang sangat dibutuhkan (Rohdiana, 2001; Sunarni, 2005). Antioksidan alami mampu
melindungi tubuh terhadap kerusakan yang disebabkan spesies oksigen reaktif,
mampu menghambat terjadinya penyakit degeneratif serta mampu menghambat
peroksidae lipid pada makanan. Meningkatnya minat untuk mendapatkan antioksidan
alami terjadi beberapa tahun terakhir ini. Antioksidan alami umumnya mempunyai
gugus hidroksi dalam struktur molekulnya (Sunarni, 2005).
Antioksidan adlah senyawa yang dapat menunda, memperlambat dan
mencegah terjadinya reaksi oksidasi. Winarno (2002) menyatakan bahwa antioksidan
adalah suatu zat yang dapat menghentikan reaksi pembentukan radikal bebas.
Mekanisme kerja dari antioksidan tersebut yaitu :
- 16 - atau mengubahnya kebentuk yang lebih stabil, sementara turunan dari
radikal antioksidan (A*) tersebut memilki keadaan lebih stabil
dibandingkan dengan radikal lipida.
b. Memperlambat laju antioksidasi dengan berbagai mekanisme diluar mekanisme pemutusan rantai autiiksidasi dengan pengubahan radikal
17 BAB III
METODOLOGI PENELITIAN
3.1. Lokasi Penelitian
Pada penelitian kali ini di lakukan di Pusat Laboratorium Terpadu (PLT)
Universitas Islam Negeri Jakarta (UIN) pada bulan September dan Oktober 2013.
3.2. Bahan Dan Alat
Bahan yang diperlukan dalam penelitian ini adalah jantung pisang batu kering
dan basah , pelarut teknis klroroform , pelarut teknis etil asetat, pelarut teknis etanol,
akuades, kertas saring , aluminium foil, metanol, DPPH,HCI 2%, FeCl3 1,%,NaOH 2
N, sebuk Mg, reagen lieberman-burchard, reagen mayer, reagen dragendorff. Alat
yang dibutuhkan dalam penelitian ini adalah blender, rotary evaporator, soklet, vorteks,serta alat-alat gelas.
3.3. Metode Penelitian
Metode penelitian di bagi menjadi dua yaitu penelitian pendahuluan dan
penelitian lanjutan Penelitian pendahuluan terdiri dari persiapan sampel melalui
proses ekstraksi bertingkat dan persiapan larutan hasil ekstraksi. Sedangkan penelitian
lanjutan terdiri dari aktivitas antioksidan dengan metode DPPH free radical
- 18 -
3.3.1. Persiapan sampel
3.3.1.1. Proses Ekstrasi
Pada penelitian pendahuluan dilakukan ekstraksi
jantung pisang yang sudah dikeringkan kemudian akan diuji
aktivitas antioksidannya. Ekstraksi dilakukan menggunakan
metode maserasi bertingkat dengan tiga pelarut yang berbeda
kepolarannya, yaitu kloroform, etil asetat, dan etanol. Pelarut
yang perbandingan pe;arut yang digunakan aalah sampai
pelarut merendam jantung pisang yang ingin dimaserasi dan
proses ekstraksi dilakukan selama 3 x 24 jam dengan
menngunakkan erlenmeyer yang ditutupi dengan alumunium
- 20 - 3.3.1.2. Pembuatan Konsentrasi Sampel
Ekstrak jantung pisang hasil pemekatan ditimbang
sebanyak 0,1 gram kemudian dilarutkan kedalam 20 mL pelarut
yang digunakan saat ekstraksi pada peelitian digunakan
kloroform, etanol, etil asetat, dan metanol (5000 ppm). Dari
5000 ppm larutan dibuat kedalam bebrbagai konsentrasi (100
ppm, 50 ppm, 25 ppm,12,5 ppm, 6,25 ppm, 3,175 ppm).
3.3.2. Penelitian Lanjutan
3.3.2.1. Uji Aktivitas Antioksidan Metode DPPH free radical
21 Pada tahap ini dilakukan uji aktivitas antioksidan
terhadap ekstrak jantung pisang .Pengujian aktivitas
antioksidan lanjut ini dengan menggunakan metode DPPH
(Hatano et al., 1988). Pengukuran aktivitas antioksidan dengan metode ini berdasarkan pada DPPH free radical scavanging activity. Sebanyak 2 mL larutan sampel yang sudah diukur dengan berbagai konsetrasi (100 ppm, 50 ppm, 25 ppm,12,5
ppm, 6,25 ppm, 3,175 ppm) dimasukkan kedalam tabung reaksi
kemudian ditambahkan dengan 2 mL DPPH 0,002% (dilakukan
dalam ruang gelap). Setiap konsentrasi dibuat duplo. Kemudian
dikocok dan diinkubasi pada suhu 37 selama 30 menit lalu
diukur dengan spektrofotometer UV-Vis (panjang gelombang
DPPH = 517 nm). Selanjutnya dihitung nilai presentase inhibisi
yang diwakili oleh IC50 dengan rumus sebagai berikut :
Persen inhibisi = x 100%
Dimana nilai persen inhibisi sebagai absis (x) dan konsentrasi
ekstrak sebagai ordinat (y)
3.3.3. Uji Fitokimia
3.3.3.1. Pengujian golongan terpenoid dan steroid
Ekstrak tanaman sebanyak 2 mL dimasukkan kedalam
tabung reaksi kemudian ditambahkan beberapa tetes reagen
Liberman-Burchard ke dalam tabung tersebut (positif
triterpenoid jika terbentuk cincin kecoklatan atau violet dan
positif steroid jika berwarna hijau).
- 22 - Ekstrak tanaman sebanyak 2mL dikocok dengan
menggunakan vortex ( positif jika terdapat busa yang stabil
selama ±10 menit).
3.3.3.3. Pengujian golongan alkaloid
Ekstrak tanaman sebanyak 4 mL dimasukkan kedalam
tabung reaksi kemudian ditambahkan dengan 0,5 mL HCl 2%
ke dalam tabung tersebut. Setelah itu divortex dan dibagi
kedalam 2 tabung. Tabung pertama ditambahkan 2-3 tetes
Reagen Dragendorf (positif alkaloid jika terdapat endapan
jingga), sedangkan tabung kedua ditambahkan 2-3 tetes Reagen
Meyer (positif alkaloid jika terdapat endapan kuning).
3.3.3.4. Pengujian golongan flavonoid
Ekstrak tanaman sebanyak 2 mL dimasukkan kedalam
tabng reaksi kemudian ditambahkan sedikit serbuk Mg kedalam
tabung tersebut dan 1 mL HCl 2% (positif flavonoid jika timbul
busa dan berwarna bening-oranye).
3.3.3.5. Pengujian golongan kuinon
Ekstrak tanaman sebanyak 2 mL dimasukkan kedalam
tabung reaksi kemudian ditambahkan NaOH 2 N 1 mL kedalam
tabung reaksi tersebut dan dikocok (positif jika berwarna
merah).
3.3.3.6. Pengujian golongan tanin
Ekstrak tanaman sebanyak 2 mL dimasukkan kedalam
tabung reaksi lalu ditambahkan 2-3 tetes FeCl3 1% kedalam
tabung tersebut dan dikocok (positif jika berwarna hjau
23 BAB IV
HASIL DAN PEMBAHASAN
4.1 Ekstraksi
Proses ekstraksi jatung pisang batu dilakukan dengan cara maserasi
bertingkat. Hal ini dilakukan dengan tujuan agar zat aktif dalam sampel bisa
diekstraksi secara maksimal. Selain itu perbedaan pelarut yang digunakan bertujuan
untuk mengekstraksi zat aktif yang berbeda polaritasnya sehingga bisa diekstraksi
dengan baik.
Sampel kering yang telah dipotong kecil-kecil ditimbang sebanyak 50 gram
yang kemudian dimaserasi menggunakan kloroform sebagai pelarut semi polar yang
akan mengekstraksi senyawa non polar dalam jaringan sampel. Maserasi dilakukan
selama 3x24 jam dalam suhu ruang. Kemuadian ekstrak tersebut di pekatkan dengan
rotary evaporator. Selanjutnya, dengan sampel yang sama maserasi dlanjutkan
dengan etil asetat dengan cara yang sama seperti maserasi menggunakan kloroform
dan maserat terakhir menggunakan etanol sebagai pelarut polar yang akan
mengekstraksi senyawa polar dari jaringan jantung pisang batu.Cara maserasi
bertingkat ini memaksimalkan ekstraksi senyawa aktif dari sampel.
Selanjutnya ekstraksi dilakukan dengan cara sokletasi menggunakan
pelarut methanol. Cara sokletasi ini memisahkan zat dari jaringan sampel jantung
pisang batu dengan cara melarutkan zat tersebut dengan pelarut yang diuapkan dan
diembunkan seolah pelarut yang digunakan selalu baru. Cara ini cukup efektif
mengingat pelarut yang digunakan dalam jumlah yang sama tetapi kemampuan
melarutkannya seperti pelarut baru dimana pelarut itu belum jenuh dengan senyawa
yang diekstrak. Hasil dari setiap ekstraksi dilanjutkan dengan uji fitokimia. Hasil
pekat ekstraksi dapat dilihat pada Tabel 4.1
Tabel 4. 1 Hasil pekat ekstrak jantung pisang batu
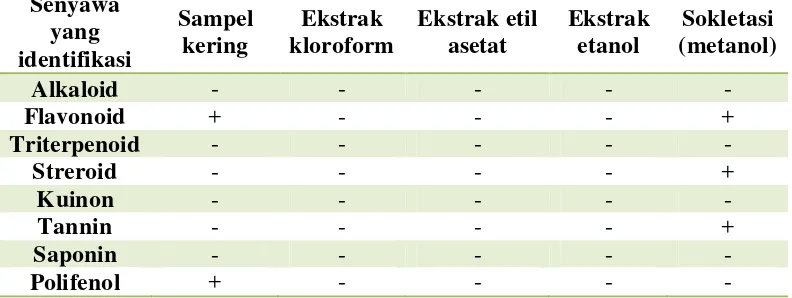
- 24 - 4.2 Uji Fitokimia
Uji fitokimia dilakukan dengan tujuan untuk mengetahui senyawa metabolit
sekunder dari sampel. Dalam hal ini senyawa-senyawa metabolit sekunder yang
terdapat dalam jantung pisang batu diuji secara kualitatif menggunakan berbagai
macam pereaksi. Hasil uji fitokimia dapat dilihat pada Tabel 4.2
Secara umum hasil uji fitokimia dari jantung pisang batu berhasil negatif.
Tetapi ada beberapa senyawa yang positif yaitu flavonoid, steroid, tannin dan
polifenol. Hasil uji fitokimia terhadap senyawa metabolit sekunder tersebut tidak
merata pada setiap ekstrak. Hal tersebut terjadi karena perbedaan karakteristik
pelarut yang sangat penting saat ekstraksi. Senyawa tertentu hanya bisa diekstraksi
oleh pelarut tertentu. Selain itu polaritas pelarut sangat berperan penting dalam
ekstraksi yang akan memepengaruhi hasil dari uji fitokimianya.
Tabel 4. 2 Hasil uji fitokimia ekstrak jantung pisang batu
Senyawa
Jantung pisang batu menunjukan reaksi positif terhadap uji flavonoid pada
sampel kering dan hasil sokletasi yang menggunakan methanol. Uji Flavonoid
positif jika menunjukan warna merah atau jingga. Hasil uji flavonoid pada sampel
kering dan hasil sokletasi menunjukan warna merah jambu. Warna merah atau
jingga yang menunjukan adanya flavonoid ini disebabkan terbentuknya garam
25
Perubahan warna pada identifikasi flavonoid adalah sifat alami flavonoid
sebagai indikator alami dimana penambahan HCl akan menyababkan larutan
bersuasana asam. Pada suasana ini yang diamati adalah perubahan warna jika
terdapat senyawa flavonoid pada sampel. Ditinjau dari reaksi yang terjadi pada
identifikasi senyawa flavonoid, penambahan serbuk Mg betujuan untuk mengikat
anion Cl yang merupakan hasil samping reaksi. Garam flavilium akan berwarna
merah pada suasana asam dan tidak berwarna pada suasana netral.
Berdasarkan penelitian yang dilakukan oleh Lydia et al., (2009) jantung pisang batu diketahui memiliki senyawa antosianin berupa delfinidin dan sianidin.
Kedua senyaa ini memiliki struktur yang tidak terlalu kompleks sehingga dapat
terekstrak dan teridentifikasi meski dalam jumlah yang kecil. Antosianin
menurapakan senyawa yang merupakan pewarna alami merah sampai biru pada
tanaman. Antosianin merupakan glikosida antosianidin yang merupan senyawa
flavonoid golongan flavon. Senyawa antosianin ini merupakan senyawa dengan
aktifitas sebagai antioksidan yang baik.
Jantung pisang batu bereaksi positi dengn pereaksi Liberman-Buchard yang
merupakan campuran asam asetan anhidrat dan asam sulat pekat. Pada sampel
kering dan ekstrak lain uji ini tidak berhasil positif tetapi pada hasi sokletasi uji ini
berhasil positif. Hal ini mungkin dikarenakan pada ekstraksi menggunakan metode
sokletasi pelarut yang digunkan seolah baru dehingga senyawa ini bisa terekstraksi.
Sedangkan jika menggunakan metode maserasi tidak bisa mengekstraksi steroid dari
jaringan jantung pisang batu karena jumlah steroidnya sedikit. Selain itu pada
metode maserasi pelarut dapat terbilang jenuh untuk mengekstraksi steroid yang
julmahnya sedikit karena telah mengekstraksi senyawa lain yang lebih dominan
terdapat pada sampel.
Selain itu untuk menunjukan keberadaan steroid dalam jantung pisang batu
- 26 - oleh Elly et al., dengan mengkonsumsi jantung pisang batu dapat meningkatkan produksi ASI sebesar 9,57 kali. Hal ini disebabkan karena jantung pisang batu
menandung steroid yang merupakan prekursor dari hormon-hormon seks yang
membantu hormo prolakton untuk merangsang pembentukan ASI.
Reaksi umum yang terjadi pada uji steroid adalah sebagai berikut:
HO H3CCOO
SO3H
1. Asam asetat anhidrat 2. H2SO4
Sterol berwarna hijau
Polifenol berhasil diidentifikasi pada sampel kering jantung pisang batu. Uji
ini menunjukan perubahan warna pada larutan sampel kering yang diberi larutan
FeCl3 dari warna kuning menjadi warna hijau sampai hitam. Polifenol merupakan
senyawa kompleks yang memiliki banyak gugus fenol. Gugus fenol bereaksi dengan
Fe membentuk Fe(OH)3 yang berwarna hijau kehitaman. Uji polifenol ini hanya
dilakukan pada sampel kering untuk menguji adanya senyawa antioksidan atau
tidak.
Reaksi yang umum terjadi pada uji polifenol adalah sebagai berikut:
OH
Uji tanin dilakukan pada ekstrak hasil maserasi bertingkat dan hasilnya
negatif. Uji tannin hanya positif pada hasil sokletasi kemungkin terjadi karena faktor
yang sama pada uji steroid. Jumlah tannin pada sampel yang sedikit tidak
terekstraksi oleh metode maserasi karena faktor kejenuhan. Tannin tetap terdeteks
27 tannin ini di dukung dengan positifnya uji polifenol pada sampe kering. Tannin
meripakan salah satu senyawa polifenol yang merupakan antioksidan.
4.3 Uji Aktivitas Antioksidan
Setelah semua sampel diuji kandngan fitokimianya, ekstrak pekat jantung
pisang diuji aktifitas antioksidannya dengan menggunakan DPPH
(1,1-difenil-2-pikrihidrazil). DPPH bersifat radikal bebas sehingga tidak stabil. DPPH yang radikal
berwarna ungu yang akan mengikat atom H dari senywa antioksidan dan menjadikan
dirinya stabil (1,1-difenil-2-pikrihidrazin) dan warnya berubah menjadi kekuningan.
Sifat DPPH ini dimanfaatkan untuk mengukur antioksidan dalam suatu sampel
secara kuantitatif.
Pengujian aktifitas antioksidan ini dapat dilakukan karena konsentrasi
antioksidan dalam sampel berbanding lurus dengan konsentrasi DPPH. Dengan
menghitung absorbansi dari DPPH sebagai standar pada panjang gelombang
maksimumnya yaitu 517 nm. Sampel ekstrak dari kloroform dilarutkan dalam
pelarut yang sama seperti pelarut DPPH yaitu metanol sedangkan pada ekstrak etil
asetat dilarutkan pada etanol agar pelarut yang digunakan sama dengan pelarut
DPPH. Perlakuan ini bertujuan agar DPPH tidak menyerang pelarut yang digunakan
pada ekstrak sehingga mengurangi akurasi dari pengujian kuantitatifnya. Setelah
ekstrak dilarutkan kemudian diencerkan dengan konsentrasi 100, 50, 25, 12.5, 6.25,
3.125 ppm.
Setiap variasi konsentrasi sampel ditambahkan DPPH (sampel : DPPH 1:1)
yang diinkubasi selama 30 menit dalam suhu ruang pada tempat yang gelap.
Perlakuan ini bertujuan agar DPPH yang bersifat radikal tidak menyerang pelarut
karena adanya cahaya. Setelah diinkubasi campuran diukur absorbansinya pada
panjag gelombang yang sama yaitu 517nm dan ditentukan persen inhibisinya.
- 28 - persen inhibisi yang telah ditentukan pada variasi konsentrasi dijadikan standar
untuk menghitung nilai IC50 yaitu konsentrasi antioksidan yang dibutuhka untuk
menginhibisi 50 persen radikal bebas.
Hasil dari uji aktivitas anti oksidan dari jantung pisang batu dapat dilihat
pada tabel 4.3
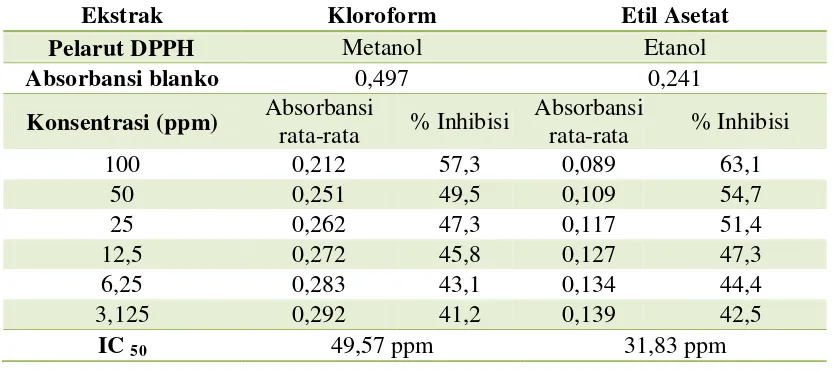
Tabel 4. 3 Hasil uji aktivitas antioksidan ekstrak jantung pisang batu
Ekstrak Kloroform Etil Asetat
Pelarut DPPH Metanol Etanol
Absorbansi blanko 0,497 0,241
Konsentrasi (ppm) Absorbansi
Hasil pengujian aktivitas antioksidan dari sampel jantung pisang batu
menunjukan aktivitas yang sangat tinggi. IC50 dari ekstrak kloroform sebesar 49,57
ppm sedangkan ekstrak etil asetat lebih tinggi aktivitas antioksidannya dari ekstrak
kloroform yang ditunjukan nilai IC50 ekstrak etil asetat sebesar 31,83 ppm.
Perbedaan ini menunjukan adanya pengaruh pelarut yang digunakan sangat
berpengauh pada aktivitas senyawa aktif. Artinya polaritas pelarut yang digunakan
sangat berarti. Dilihat dari nilai indeks polaritasnya etil asetat lebih polar dari
klorofom. Etil asetat memiliki nilai indeks polaritas 4,4 sedangkan kloroform
memiliki nilai indeks polaritas sebesar 4,1
(http://macro.lsu.edu/howto/solvents/Polarity%20index.htm, diakses pada 18
Oktober 2013).
Ditinjau dari hasil uji fitokimia yang menunjukan bahwa tannin terdapat dalam
jantung pisang batu hanya diperlihatkan oleh hasil sokletasi karena hasil ekstrak lain
tidak positif terhadap identifikasi tannin. Dalam hal ini yang lebih berperan aktif
29 Antosianin merupaka pigmen alami yang juga merupakan golongan polifenol.
Secara fisik dapat dilihat bahwa jantung pisang batu berwarna warna merah dimana
intersitas warna tersebut menunjukan kandungan antosianin sebagai pigmen warna
merah. Selain itu, penelitian Lydia et al., menunjukan bahwa kandungan antosianin pada jantung pisang batu sebesar 909,44 mg ± 225,97 mg/100 g berat
kering,meskipun hal ini dipengaruhi oleh kualits sampel yang memilki latar
belakang tempat dan kondisi lingkungan pohon sampel tumbuh. Tetapi dapat ditarik
kesimpulan bahwa semakin merah warna kelopak dari jantung pisang maka semakin
- 30 - BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hasil dari penelitian yang telah dilakukan dengan sampel jantung pisang batu ini
adalah sebagai berikut:
1. Ekstrak pekat yang didapatkan menggunakan pelarut kloroform seberat 3,99
gram, pelarut etil asetat seberat 0,96 gram, pelarut etanol 0,57 gram, pelarut
methanol seberat 0,64 gram.
2. Hasil uji fitokimia menunjukan bahwa jantung pisang mengandung senyawa
flavonoid, steroid, polifenol, tannin.
3. Ekstrak jantung pisang batu memiliki aktivitas antioksidan yang sangat tinggi.
4. Ekstrak jatung pisang batu dengan pelarut kloroform menghasilkan IC50
sebesar 49,57 pmm sedangkan dengan pelarut etil asetat didapatkan IC50
sebesar 31,83 ppm.
5. Aktifitas antioksidan dapat ekstrak jantung pisang batu sebagian besar berasal
dari senyawa antosinin yang termasuk golongan flavonoid sekaligus polifenol.
5.2 Saran
Adanya kekurangan dalam penelitian ini mengharuskan penelitian selanjutnya
di lakukan dengan tujuan memperjelas dan melengkapi kekurangan dari penelitian
ini. Adapun saran yang dapat diajukan sebagai rujukan untuk penelitian selanjutnya
adalah sebagai berikut:
1. Penelitian dilanjutkan ketingkat yang lebih sfesifik seperti karakterisasi
senyawa yang terdapat dalam setiap ekstrak seperti penentuan strukrur atau
isolasi dan uji aktivitas lainnya.
2. Dilakukan penelitian lebih lanjut mengenai jantung pisang batu agar
manfaatnya bisa diketahui dan dibuktikan secara ilmiah sehingga dapat
31 DAFTAR PUSTAKA
Agro inovasi. “Prospek dan Arah Pengembangan Agribisnis Pisang,” Diunduh dari: URL:
http://www.litbang.deptan.go.id/special/publikasi/doc_hortikultura/pisang/pisa ng-bagian-b.pdf. .[diunduh pada: 14 okrober 2013].
Ahadi, 2003. Dalam. Anonim. 2012a. “Tinjauan Pustaka Tanin,“ http://repository.ipb.ac.id/bitstream/handle/123456789/61538/BAB%20II%20 Tinjauan%20Pustaka.pdf?sequence=3 [19 Oktober 2013, pukul 15:01 WIB. Anonim. 1977. Buah-buahan. Bogor: Lembaga Biologi Nasional. hlm: 105.
Anonim. 2005. “Kandungan dan manfaat pisang,” Http://mydiarest.blogspot.com.[18 Oktober 2013, pukul 21.00].
Anonim. 2006. “Pisang,” Http://www.idionline.org [19 Oktober 2013, pukul 21.12 wib].
Anonim. 2012. “Biosintesis Terpenoid,”
zhttp://widyaistianichem.blogspot.com/2012/10/biosintesis-terpenoid.html . [19 Oktober 2013, pukul 14:24 wib].
Anonim. 2011.
http://repository.usu.ac.id/bitstream/123456789/16577/4/Chapter%20II.pdf Diunduh pada tanggal 18 Oktober 2013
Anonim. 2013a. “Ekstraksi,” http://ardydii.wordpress.com/2013/03/10/ekstraksi/ [18 Oktober 2013, pukul 22.00 wib].
Anonim. 2013 b. “Alkaloid,” http://hersipa.wordpress.com/alkaloid/ [19 Oktober 2013, pukul 13.19 wib].
Anonim. 2013c. “Saponin,” http://mhanafi123.files.wordpress.com/2012/11/saponin-makalah.pdf [19 Oktober 2013, pukul 14:32 wib].
Aspiatun. 2004. “Mutu dan Daya Terima Nugget Lele Dumbo (Clarias gariepinus)
dengan Penambahan Jantung Pisang.” Skripsi. Departemen Gizi Masyarakat
dan Sumber Daya Keluarga Fakultas Pertanian Institut Pertanian Bogor, Bogor.
Astawan, M. 2005. “Pisang Buah Kehidupan,” Http://www.kompas.com [30 November 2006]
Astawan, M., 2008. “Pisang. Sebagai Buah.” Kehidupan. www.edukasi.kompas.com Bello-Pérez, L.A. A. De Francisco, E.Agama-Acevedo, F. Gutierrez-Meraz, F. J.L.
García-Suarez. 2005.”Morphological and Molecular Studies of Banana Starch. SAGE Publications,” DOI: 10: 1177.
Bernasconi, Gester, Hauser, Stauble, Schneiner. 1987. Terjemah Lienda Handojo. Teknologi Kimia Bagian 2. PT Pradnya Pramita, Jakarta.
Cook, N. C. and S. Samman. (1996). Review Flavonoids-Chemistry, Metabolism, Cardioprotective Effect, And Dietary Sources, J. Nutr. Biochem (7): 66-76 Cuppett, S., M. Schrepf and C. Hall III. (1954). Natural Antioxidant – Are They
Reality. Dalam Foreidoon Shahidi: Natural Antioxidants, Chemistry, Health Effect and Applications, AOCS Press, Champaign, Illinois: 12-24.
Dalimartha, S. dan Soedibyo, M. (1999). Awet Muda Dengan Tumbuhan Obat dan Diet Supleme., Trubus Agriwidya, Jakarta. hal. 36-40.
- 32 - Endra, Yuli. 2006. “Analisis Proksimat Dan Komposisi Asam Amino Buah Pisang Batu (Musa balbisiana Colla),” [Skripsi]. Bogor : Fakultas Matematika Dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Fatemeh, S. R., Saifullah, R., Abbas, F. M. A. and Azhar, M. E. Total phenolics, flavonoids and antioxidant activity of banana pulp and peel flours: influence of variety and stage of ripeness. International Food Research Journal 19 (3): 1041-1046 (2012).
Guenther, E. 1987. Minyak Atsiri. UI Pres, Jakarta.
Harbone, J.B. 1987. Metode Fitokimia. Bandung: ITB. Dalam. Anonim. 2011. “ Antrakuinon,”http://repository.usu.ac.id/bitstream/123456789/24745/4/Chapte r%20II.pdf [19 Oktober 2013, pukul 14:40 wib].
Hart, H. 1983. Kimia Organik. Terjemahan Suminar, Jakarta: Erlangga. Dalam. Anonim.
2011.“Antrakuinon,”http://repository.usu.ac.id/bitstream/123456789/24745/4/ Chapter%20II.pdf [19 Oktober 2013, pukul 14:40 wib].
Irbi’ati HH. 2002. “Karakterisasi sifat fisikokimia dan mekanis daun pisang batu sebagai bahan kemasan,” [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Kondo et al., 2004. Dalam. Anonim. 2012a. “Tinjauan Pustaka Tanin ,“ http://repository.ipb.ac.id/bitstream/handle/123456789/61538/BAB%20II%20 Tinjauan%20Pustaka.pdf?sequence=3 [19 Oktober 2013, pukul 15:01 wib]. Lestari, E. 2008. Toksisitas Ekstrak Daun Pandan Wangi (Pandanusamaryllifolius
Roxb.) dengan Metode Brine Shrimp Lethality Test (BSLT). Artikel Karya Ilmiah. Semarang : Universitas Diponegoro.
Lestario, Lydia Ninan,. dkk. 2009. “Kandungan Antosianin Dan Antosianidin Dari Jantung Pisang Klutuk (Musa brachycarpa Back) Dan Pisang Ambon ( Musa
acuminata Colla),” J.Teknol. dan Industri Pangan, Vol. XX No. 2
Molyneux, P. 2003. The use of stable free radical diphenylpicrylhidrazyl (DPPH) for estimating antioxidant activity.
http://www.aseanbiodiversity.info/Abstract/53004092.pdf Diunduh pada tanggal 18 Oktober 2013
Musita, Nanti. 2009. “Kajian Kandungan Dan Karakterisik Pati Resisten Dari
Berbagai Varietas Pisang,” Jurnal Teknologi Industri dan Hasil Pertanian. Vol.14, No.1 : 68-79.
Nurhidayah bt. Pazil,Siti.2009.Perbandingan Aktivitas Antioksidan Ekstrak Pisang Raja (Musa AAB „Pisang Raja‟) dengan Vitamin A, Vitamin C dan Katekin Melalui Penghitungan Bilangan Peroksida.[SRIPSI]. Depok: FK UI
Oliveira et al., 2009. Dalam. Anonim. 2012a. “Tinjauan Pustaka Tanin ,“ http://repository.ipb.ac.id/bitstream/handle/123456789/61538/BAB%20II%20 Tinjauan%20Pustaka.pdf?sequence=3 [19 Oktober 2013, pukul 15:01 wib]. Pazmino-Duran, EA, Giusti MM, Wrolstad RE, Gloria MB. A. 2001. “Anthocyanins
from Banana Bracts (Musa X paradisiaca) as Potential Food Colorant,” Food Chemistry 73 : 321-332.
Rajalakshmi, D dan S. Narasimhan. (1985). “Food Antioxidants: Sources and Methods of Evaluation dalam D.L. Madhavi: Food Antioxidant, Technological, Toxilogical and Health Perspectives. Marcel Dekker Inc., Hongkong: 76-77. Redha, Abdi. 2010. “Flavonoid: Struktur, Sifat Antioksidatif Dan Peranannya Dalam
33 Rohdiana, D.(2001). Aktivitas Daya Tangkap Radikal Polifenol Dalam Daun Teh,
Majalah Jurnal Indonesia 12, (1), 53-58.
Rusmianto. 2007. “Penambahan Isolat Protein Kedelai Pada Pembuatan Dendeng Jantung Pisang Batu (Musa brachycarpa Back),” Skripsi. Institut Pertanian Bogor.
Samsu, H, Farid, Masruroh, Luluk,. 2008.“Perancangan Dan Pembuatan Otomatisasi Pada Alat Pengeringan Sale Pisang Berbasis Mikrokontroler Renesa
R8C/13,” Jurnal Neutrini. Vol.1 No, 1
Sastrohamidjojo, Hardjono. 1995. “Sintesis Bahan Alam,” Gadjah Mada University Press : Yogyakarta.
Satuhu, S., Ahmad Supriyadi. 2004. Budi daya, “Pengolahan dan Prospek Pasar
Pisang. Penebar Swadaya,” Jakarta.
Simmonds, N. W. 1959. “Bananas,” John Willey and Sons Inc. New York. 466p.\ Suhartono, E., Fujiati, Aflanie, I. (2002). Oxygen toxicity by radiation and effect of
glutamic piruvat transamine (GPT) activity rat plasma after vitamine C treatmen, Diajukan pada Internatinal seminar on Environmental Chemistry and Toxicology, Yogyakarta.
Sukandar, Dede et al,. 2013. “Petunjuk Praktikum Kimia Bahan Alam,” Pusat Laboratorium Terpadu (PLT) : UIN Jakarta.
Sunarni,T., (2005). Aktivitas Antioksidan Penangkap Radikal Bebas Beberapa kecambah Dari Biji Tanaman Familia Papilionaceae, Jurnal Farmasi Indonesia 2 (2), 2001, 53-61.
Sunaryono, Hendro. 2003. “Pengenalan Jenis Tanaman Buah-Buahan dan Bercocok Tanam Buah-Buahan Penting di Indonesia.” Bandung : Sinar Baru Algensindo
http://macro.lsu.edu/howto/solvents/Polarity%20index.htm diakses pada tanggal 19 Oktober 2013 pikul 21.35
Wattimena, M, Mulyani, Bintoro, S.V.P.”Kualitas Bakso Berbahan Dasar Daging
Ayam Dan Jantung Pisang Dengan Bahan Pengikat Tepung Sagu,” Jurnal Aplikasi Teknologi Pangan. Vol.2 No. 1 : 36-39.
White, P.J. and Y. Xing. (1954). Antioxidants from Cereals and Legumes dalam Foreidoon Shahidi : Natural Antioxidants, Chemistry, Health Effect and Applications. AOCS Press, Champaign, Illinois: 25-63.
- 34 - LAMPIRAN
Pelarut DPPH menggunakan methanol dan absorbansinya 0,497 pada panjang gelombang
517 nm
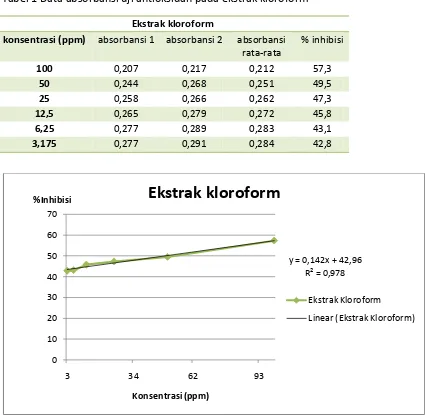
Tabel 1 Data absorbansi uji antioksidan pada ekstrak kloroform
Ekstrak kloroform
konsentrasi (ppm) absorbansi 1 absorbansi 2 absorbansi rata-rata
Grafik 1 Standard konsentrasi ekstrak terhadap % indihibisi uji antiokdsidan
35 DPPH yang digunakan menggukanan pelarut etanol dengan absorbansi 0,241 yang diukur
pada panjang gelombang 517 nm
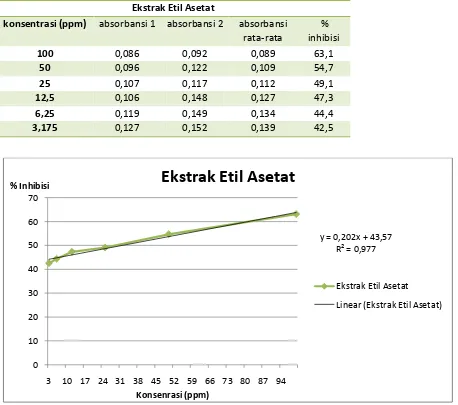
Tabel 2 Data absorbansi Uji Antioksidan ekstrak etil asetat
Ekstrak Etil Asetat
konsentrasi (ppm) absorbansi 1 absorbansi 2 absorbansi rata-rata
Grafik 2 Standard konsentrasi ekstrak etil aseta terhadap % indihibisi uji antiokdsidan
IC50 ekstrak etil asetat