BAGIAN IV
SIFAT DAN KARAKTERISTIK BAHAN KIMIA BERBAHAYA
1 UMUM
Penggunaan kimia dalam kebudayaan manusia sudah dimulai sejak zaman dahulu. Kimia merupakan salah satu ilmu pengetahuan alam, yang berkaitan dengan komposisi materi, termasuk juga perubahan yang terjadi di dalamnya, baik secara alamiah maupun sintetis. Senyawa-senyawa kimia sintetis inilah yang banyak dihasilkan oleh peradaban modern, namun materi ini pulalah yang dapat menimbulkan pencemaran lingkungan yang berbahaya. Dengan mengetahui komposisi dan memahami bagaimana perubahan terjadi, manusia dapat mengontrol dan
memanfaatkannya untuk kesejahteraan manusia.
Penggunaan bahan-bahan kimia di dunia telah berkembang pesat, yang sebagian besar merupakan bahan berbahaya. Ini ditunjukkan oleh hampir 11 juta jenis bahan kimia telah diidentifikasi pada tahun 1995, baik yang terdapat di alam maupun yang dibuat oleh manusia, dan hampir setiap tahun 1.000 jenis bahan kimia baru masuk ke perdagangan. Bahan kimia yang telah digunakan dan diperdagangkan secara umum sekitar 63.000 jenis, 50.000 jenis diantaranya digunakan sehari-hari, 1.500 jenis merupakan bahan aktif pestisida, sekitar 4.000 jenis sebagai bahan aktif obat-obatan, dan 2.500 jenis digunakan sebagai bahan tambahan makanan. Dari sekian banyak bahan kimia tersebut, baru beberapa ratus jenis saja yang telah dievaluasi
dampaknya tehadap kesehatan dan lingkungan. Perdagangan bahan kimia dunia pada tahun 1991 mencapai nilai 1,2 M US$, 40% berkaitan dengan petrokimia. Pemakaian bahan kimia di Indonesia (1991) sekitar 0,46% dari nilai perdagangan dunia. Proses penggunaan bahan yang berbahaya dalam kegiatan sehari-hari, terutama dari kegiatan industi khususnya penggunaan bahan kimia, akan menghasilkan limbah berbahaya.
Secara konvensional, terdapat 7 kelas bahan berbahaya, yaitu :
a. Materi mudah terbakar (flammable material) : padat, cair, uap,atau gas yang menyala dengan mudah dan terbakar secara cepat bila dipaparkan pada sumber nyala, misalnya pelarut (solvent) seperti benzene,
ethanol, debu aluminum, gas hidrogen dan metan.
b. Materi yang spontan terbakar
(spontaneously ignitable material) : padat atau cair yang dapat menyala secara spontan tanpa sumber nyala, misalnya karena perubahan panas, tekanan atau kegiatan oksidasi atau kegiatan lain seperti aktivitas mikrobiologis. Contoh materi ini misalnya fosfor putih.
c. Peledak (explosive) : materi kimia ini dapat meledak, biasanya karena adanya kejutan (shock), panas, atau mekanisme lainnya. Contoh materi ini misalnya dinamit dan trinitrotoluene (TNT).
d. Pengoksidasi (oxidizer) : Materi yang menghasilkan oksigen, baik dalam kondisi biasa atau bila terpapar dengan panas. Contoh materi ini adalah amonium nitrat dan benzoyl peroksida.
e. Materi korosif : padat atau cair seperti asam kuat atau basa kuat, yang dapat membakar dan merusak jaringan kulit bila berkontak dengannya.
f. Materi toksik : racun yang dalam dosis kecil dapat membunuh atau mengganggu kesehatan, seperti karbon monoksida dan hidrogen sianida.
g. Materi radioaktif : dicirikan dengan transformasi yang berlangsung dalam inti atom, misalnya uranium heksafluorida.
Materi tersebut kadangkala menjadi lebih berbahaya bila berada dalam kondisi tercampur dengan bahan lain. Kadangkala secara tidak sengaja terjadi pencampuran antara 2 materi yang asalnya tidak berbahaya. Pencampuran bahan berbahaya dapat menyebabkan:
o Timbulnya bahan toksik
o Timbulnya gas bakar yang dapat
menimbulkan kebakaran atau ledakan, atau
o Panas akibat reaksi kimia yang terjadi akan
dapat membakar bahan mudajh terbakar di sekitarnya.
Beberapa ilustrasi di bawah ini akan menggambarkan hal tersebut:
Interaksi bahan membentuk bahan toksik: Bila kita mencampur larutan asam yang banyak digunakan secara komersial untuk
renang. Reaksi yang terjadi akan berlangsung secara spontan, menghasilkan gas klorin yang sangat toksik melalui pernafasan. Tubuh manusia mentolerir konsentrasi bahan ini dengan konsentrasi tidak lebih dari 1 ppm di udara.
Interaksi bahan membentuk nyala atau bahan eksplosif:
Bahan logam natrium akan dapat terbakar dengan sendirinya bila terdapat uap air yang berkontak dengannya, karena reaksi yang terjadi akan menghasilkan gas hidrogen yang dapat terbakar tanpa adanya pemantik api. Misalnya gudang penyimpan logam natrium terbakar. Bila api yang dipadamkan dilakukan dengan air, maka kebakaran akan tambah besar, karena dihasilkan gas hidrogen.
Interaksi bahan membentuk panas: Bahan-bahan pengoksidasi adalah contoh bahan berbahaya yang siap bereaksi dengan bahan mudah terbakar, menyebabkan terjadinya swa-kebakaran. Bila larutan asam nitrat (oksidator) tercampur dengan tepung beras, akan memungkinkan bahan tepung tersebut secara spontan akan terbakar.
2 KELAS KEBAKARAN
Kebakaran biasanya dikaitkan dengan kecelakaan yang dipicu dari adanya bahan berbahaya, dan dapat dibagi menjadi 4 kelas, yaitu:
o Kebakaran kelas A: berasal dari bakaran
berbahan dasar sellulosa, seperti kayu, karton dan kertas, bahan-bahan sejenis baik alamiah maupun sintetis lainnya termasuk plastik dan karet. Kebakaran bahan ini akan meninggalkan bara api dan abu. Air dapat digunakan untuk
memadamkan jenis kebakaran ini
o Kebakaran kelas B: berasal dari bakaran
gas bakar (flammable gases) atau cairan yang mudah terbakar (flammable and combustible liquids), seperti LPG, hidrogen, propane, kerosen, methanol, ethyl ether. Karbon dioksida, dry chemical extinguisher, atau busa merupakan bahan yang cocok untuk memadamkannya. Jangan
dipadamkan dengan air.
o Kebakaran kelas C: berasal dari bakaran
bahan yang terjadi karena sirkuit tenaga listrik, seperti dari stop-kontak, sikring, kabel listrik, motor dan generator. Karbon dioksida atau dry chemical extinguisher, biasanya direkomendasikan untuk memadamkannya.
o Kebakaran kelas D: berasal dari bakaran
logam-logam yang mempunyai sifat reaktif yang spesifik terhadap air atau uap air, seperti logam titanium, magnesium, zirconium, aluminum, dan natrium. Kebakaran jenis ini mudah dipadamkan oleh baham spesifik sejenis graphite atau natrium klorida (garam dapur). Sangat berbahaya bila dipadamkan dengan menggunakan air.
3 INFORMASI TINGKAT BAHAYA
Tingkat bahaya suatu bahan berbahaya harus diinformasikan secara jelas kepada pemakai, khususnya dalam lingkungan kerja dimana bahan tersebut digunakan, melalui 2 jalan:
o Penggunaan label dan bentuk peringatan
lainnya: setiap produsen atau importir bahan kimia harus memastikan bahwa setiap kontainer atau pengemas produk B3-nya telah diberi label, papan-nama, atau tanda-tanda peringatan lain yang sesuai dengan jenis bahaya yang dikandung bahan tersebut, nama dan alamat
produsen, importir atau penanggung jawab lainnya. Label dapat menggunakan simbol, gambar atau kata-kata lainnya. Lihat contoh dalam Gambar 4.1
o
Informasi tentang Material Safety Data Sheets (MSDS): merupakan bulletin yang bersifat teknis yang mengandung informasi mendetail tentang bahaya dari bahan tersebut. Di Amerika Serikat, melalui OSHA, mewajibkan setiap produsen untuk menyiapkan MSDS ini bagi setiapproduknya. MSDS ini harus disertakan pada setiap sampel atau pengiriman ke sebuah tujuan untuk pertama kalinya.
Bila mengacu kepada Occupational Safety and Health Act (OSHA) yang berlaku di Amerika Serikat, maka:
a. MSDS harus dirancang sangat komprehensif dalam bentuk informasi tertulis untuk seluruh karyawan. b. Informasi minimum yang dibutuhkan
adalah:
o Identitas produk seperti tercantum dalam
container atau pengemasnya
o Nama umum dan nama kimia seluruh
Gambar 4.1: Contoh label untuk HCl
c. Informasi minimum yang dibutuhkan adalah:
o Identitas produk seperti tercantum
dalam container atau pengemasnya
o Nama umum dan nama kimia seluruh
komponen yang mempunyai konsentrasi >1%, yang diketahui berbahaya bagi kesehatan dan keselamatan, dan mempunyai konsentrasi ≥ 0,1% bagi bahan yang diketahui sebgai penyebab kanker
o Bahaya fisik dan kesehatan, termasuk
tanda-tanda dan simptom-nya bila terpapar
o Alur masuk ke tubuh manusia, kulit,
pernafasan, makanan atau minuman
o Batasan paparan yang diketahui o Apakah termasuk penyebab kanker
atau berpotensi-kanker
o Prosedur penanganan dan
penggunaan yang aman, penanggulangan tumpahan atau kebocoran
o Prosedur pertolongan pertama bila
terjadi kecelakaan
o Tanggal penyiapan bahan o Nama, alamat dan nomor telepon
perusahaan, atau yang bertanggung jawab yang mendistribusikan MSDS c. Training yang bersifat regular adalah
kegiatan yang dianggap penting, berbentuk program komunikasi, yang
4 DOKUMEN MATERIAL SAFETY DATA SHEETS
(MSDS)
Berikut ini adalah contoh MSDS yang
dikeluarkan oleh sebuah produsen bahan kimia di Amerika Serikat untuk produk HCl yang dihasilkan:
Informasi Umum (muncul di setiap lembar MSDS)
o J.T. Baker Chemical Co. 222 Red School
Lane, Phillipsburg, N.J. 08865, 24-Hour Emergency Telephone (201)859-2151, Chemtrec # (800) 424-9300, National Response Center # (800) 424-8802
o H3880-02 Hydrochloric Acid
o Effective: 08/07/86 Issued: 10/19/87
Seksi I: Identifikasi Produk
o Nama produk: Hydrochloric acid
o Formula: HCl o Formula Wt: 36, 46 o Cas No: 7647-01-0
o NIOSH/RTECS No: MW4025000
o Sinonim umum: Muriatic Acid; Chlorhydric
Acid, Hydrochloride
o Kode produk: 9543, 9539, 9535, 9534,
9544, 9529, 9542, 4800, 9549, 9530, 9548, 9540, 5537, 9547, 9546, 9537, 5367
Precautionary Labelling:
Baker SAF-T-DATATM System: (dengan label kode gambar)
o Kesehatan: Severe o Flammabilitas: None o Reactivitas: Moderate o Kontak: Severe
o Laboratory protective equipment: goggles &
shield, Lab coat & apron, vent hood, proper gloves
o Precautionary label statements:
RACUN! BAHAYA!
MENYEBABKAN LUKA BAKAR SERIUS MENJADI FATAL BILA TERTELAN ATAU TERHIRUP
Jangan berkontak dengan mata, kulit, dan baju.
Jangan terhirup uapnya. Penyebab kerusakan pada sistem pernafasan (paru-paru), mata dan kulit. Simpan dalam container yang tertutup rapat. Buka dengan hati-hati. Gunakan ventilasi yang
cukup. Cuci dengan cukup setelah penanganan. Bila terjadi tumpahan, netralisir dengan soda ash atau kapur dan tempatkan pada container kering.
Seksi II: Komponen Berbahaya
o Komponen: Hydrochloric Acid (23o Baume) o %: 35-40
o CAS No: 7647-01-0
Seksi III: Data Fisika
o Titik didih (boiling point): 110oC (230ºF) o Tekanan uap (mmHg): N/A
o Titik leleh (melting point): -25oC (-13oF) o Densitas uap (udara = 1): 1,3
o Specific gravity H2O = 1): 1,19
o Laju evaporasi (Butyl Acetate = 1): N/A o Kelarutan (H2O): sempurna dalam seluruh
proporsi
o % Volatil – volume: 100
o Tampilan dan bau: jernih, tidak berwarna
atau kuning muda, pungent, cairan berasap (fuming liuid)
Seksi IV: Data Bahaya Kebakaran dan Ledakan
o Flash point: N/A
o NFPA 704M Rating: 3-0-0
o Flammable limits: Upper – N/A % Lower –
N/A %
o Media pemadam kebakaran: gunakan
media pemadam kebakaran yang cocok untuk area sekitarnya
o Prosedur khusus pemadaman kebakaran:
anggota pemadam kebakaran harus mengenakan perlengkapan perlindungan yang memadai, dengan perlengkapan pernafasan yang dioperasikan pada tekanan positif. Pindahkan kontainer dari lokasi kebakaran bila dapat dilakukan tanpa resiko. Gunakan air. Jangan masukkan air ke dalam kontainer.
o Bahaya kebakaran dan ledakan yang tidak
biasa: dapat meng-emisikan gas hidrogen bila berkontak dengan logam
o Gas toksik yang dihasilkan: hydrogen
chlorida, gas hirogen
Seksi V: Data Bahaya Kesehatan
o PEL dan TLV dalam daftar menandakan
berada pada batas
o Treshold Limit Value (TLV/TWA): 7 mg/m3
(5 ppm)
o Permissible Exposure Limit (PEL) : 7 mg/m3
(5 ppm)
o Toksisitas :LD50 (oral-rabbit) (mg/kg) : 900
LD50 (inhl-rat-1H) (ppm) : 3124 o Carcinogenicity
NTP : No IARC : No Z List : No OSHA : No
o Pengaruh paparan yang berlebihan
(overexposure):
o Target organ: sistem pernafasan, mata,
kulit
o Kondisi medis yang biasanya diperparah
bila terpapar: tidak teridentifikasi
o Alur masuk: pencernaan, pernafasan,
kontak kulitm kontak mata
o Darurat dan pertolongan pertama
Seksi VI: Data Reaktivitas
o Stabilitas: stabil
o Bahaya polumerisasi: tidak akan terjadi o Kondisi yang dihindari: panas dan
kelembaban
o Tidak kompatibel: hampir semua logam, air,
amine, oksida logam, anhidrid acid, propiolakton, vinil asetat, murkuri sulfat, kalsium fosfida, formaldehid, alkali, karbonat, basa kuat, asam sulfat, asam klorosulfonik
o Produk dekomposisi: hidrogen klorida,
hidrogen, klorin
Seksi VII: Prosedur Penanganan Tumpahan dan Disposal
o Gunakan alat masker pernafasan (
self-contained breathing) dan baju pelindung
o Hentikan kebocoran bila dapat dilakukan
tanpa resiko
o Berikan ventilasi pada area tersebut o Netralisir tumpahan dengan abu soda atau
kapur
o Dengan skop yang bersih, tuang tumpahan
dengan hati-hati ke dalam kontainer bersih, kering dan tutup, dan pindahkan dari area tersebut
o Bilas area tumpahan dengan air o J.T. Baker NeutraorbR atau Penetralisir
asam NeutrasolR “Low Na” disarankan untuk digunakan untuk penanganan tumpahan
o Prosedur disposal: kubur atau timbun atau
singkirkan sesuai dengan peraturan yang berlaku
o EPA Hazardous Waste Number: D002
(Coorosive Waste)
Seksi VIII: Perlengkapan Perlindungan
o Ventilasi: gunakan exhaust ventilation
umum atau lokal untuk memenuhi standar TLV
o Perlindungan pernafasan: masker
pernafasan dibutuhkan bila konsentrasi di udara kerja melebihi TLV yang disyaratkan. Pada konsentrasi sampai dengan 100 ppm, disarankan menggunakan masker chemical cartridge respirator dengan acid cartridge. Di atas konsentrasi tersebut, alat bantu pernafasan disarankan untuk digunakan
o Perlindungan mata/kulit: sarung tangan
acid-resistant dan perlindungan muka (face shield), seragam, baju pelindung
direkomendasi untuk digunakan
Seksi IX: Penyimpanan dan Penanganan
o SAF-T-DATATM Storage Color Code: putih
(korosif)
o Syarat khusus: Kontainer selalu tertutup
rapat. Simpan di area anti korosi. Isolasi dari bahan-bahan yang tidak kompatibel. Dilarang disimpan berdekatan dengan bahan pengoksidasi
Seksi X: Data transportasi dan Informasi Tambahan
Domestik (DOT):
o Nama pengapalan (proper shipping name):
Hydrochloric acid
o Kelas bahaya: bahan korosif (cair) o UN/NA: UN1789
o Label: Korosif
o Kuantitas dilaporkan: 5000 Lbs
Internasional (IMO)
o Nama pengapalan (proper shipping name):
Hydrochloric acid, solution
o Kelas bahaya (hazard class): 8 o UN/NA: UN1789
o Labels: Corrosive
Info terakhir MSDS contoh di atas: The information publisher in this MSDS has been compiled from our experience and data presented in various technical publications, It is the user’s responsibility to determine the suitability of this information for the adoption of necessary safety precautions. We reserve the right to revise Material Safety Data Sheets periodically as new information becomes available. J.T. Baker makes no warranty or representation about the accuracy or completeness nor fitness for purpose of the information contained herein. COPYRIGHT 1987 J.T. BAKER INC.
5 BAHAN KIMIA KOROSIF
adanya oksigen di udara, yang menghasilkan oksida-oksida metalik. Namun korosi
sebetulnya tidak terbatas pada aktivitas oksigen terhadap sebuah logam. Korosi dapat pula disebabkan karena perusakan oleh bahan kimia (seperti asam atau basa kuat), baik terhadap logam dan mineral, juga terhadap jaringan kulit. Oleh karenanya US Department of
Transportation (USDOT) mendefinisikan bahan korosif sebagai : cairan atau padatan yang dapat menimbulkan kerusakan yang terlihat pada jaringan kulit manusia bila berkontak, atau cairan yang mempunyai laju korosi yang kuat terhadap baja alumunium dengan kriteria : - bila diuji terhadap kelinci albino, maka
struktur jaringan di lokasi kontak mengalami kerusakan atau tidak dapat pulih setelah pemaparan 4 jam atau kurang,
- bila sebuah cairan mempunyai laju korosi lebih besar dari 6,25 mm per tahun terhadap baja atau alumunium standar pada
temperatur pengujian 55 °C.
Beberapa bahan yang termasuk dalam kelompok ini adalah asam sulfat, asam nitrat, asam khlorida, asam perkhlorit, asam fluorida, asam fosfat, natrium hidroksida, kalium
hidroksida, yang akan dibahas secara umum di bawah ini.
Asam Sulfat (H2SO4):
Bahan ini banyak digunakan di industri,
sehingga dianggap banyaknya konsumsi bahan ini di suatu negara dapat menggambarkan status ekonomi dari negara tersebut. Asam ini merupakan cairan yang tidak berwarna, dengan densitas sekitar 2 kali air, dan sangat reaktif, dapat menimbulkan sifat toksik, nyala dan ledakan. Beberapa sifat asam sulfat pekat adalah :
- konsentrasinya dalam air: 98,33 % - gravitasi spesifik: 1,84
- titik didih: 338 o C - titik beku: 10 o C - sangat larut dalam air
Asam ini akan membebaskan panas bila diencerkan (sekitar 20 kcal per mole), dan dapat menimbulkan ledakan bila dicampur dengan bahan tertentu. Selalu diperhatikan bahwa pengenceran dilakukan dengan penuangan secara perlahan pada air yang teraduk perlahan. Bila ini dilakukan terbalik, akan menyebabkan terjadinya pendidihan lokal disertai percikan yang membahayakan. Bentuk bahaya yang kedua dari bahan ini adalah sifatnya yang dapat mengekstrak air dari bahan yang berkontak dengannya. Reaksi dehidrasi ini
sangat kuat, sehingga dapat menghancurkan sama sekali kertas dan tekstil. Gula misalnya akan menjadi arang bila bercampur dengan asam ini. Bahaya lain dari bahan ini adalah kemampuannya bereaksi dengan bahan lain, yang disertai akibat samping seperti timbulnya gas toksik, terjadinya bahan lain yang mudah terbakar atau terjadinya ledakan. Bila asam sulfat bercampur dengan NaCl, akan terbentuk uap HCl yang merupakan bahan toksik bagi pernafasan. Bahan ini juga akan menimbulkan ledakan bila bercampur dengan asam lain, seperti HClO4.
Beberapa reaksi di bawah ini akan memperjelas mekanisme yang terjadi:
a. Reaksi exotermis dengan gula : C12H22O11(s) ⇒ 12 C(s) + 11 H2O(g) b. Menimbulkan ledakan dengan asam
perkhlorit :
2HClO4 (l) ⇒ Cl2O7(g) + H7O(g)
c. Menghasilkan gas racun dengan asam oksalit :
H2C2O4(s) ⇒ H2O(g) + CO(g) + CO2(g)
d. Menghasilkan produk yang mudah terbakar dengan ethyl alkohol :
C2H5OH(l) ⇒ C2H4(g) + H2O(g)
e. Menghasilkan ledakan dan gas toksik dengan NaClO3:
NaClO3(s)+H2SO4(l)⇒NaHSO4(s)+HClO3(l) 3 HClO3(l)⇒HClO4+2ClO4+H2O
ClO2 bersifat toksik
f. Menghasilkan gas-gas racun dengan NaBr, NI dan NaCN atau NaSCN :
2NaBr(s)+2H2SO4(l)⇒
Br2(g)+SO2(g)+Na2SO4(l)+2H2O(l)
SO2 dan Br2 adalah gas toksik
g. Bahan ini juga tergolongkan sebagai oksidator, terutama pada kondisi panas, misalnya pada reaksi di bawah ini : Cu(s)+2H2SO4(pekat)⇒CuSO4(l)+SO2(g)+2 H2O(l) Pb(s)+3H2SO4(pekat)⇒
Pb(HSO4)2(s)+SO2(g)+2H2O(l)
Di lingkungan kerja, aturan di USA membatasi pemaparan maksimum terhadap manusia sebesar 1 mg/m3. Label bertuliskan 'korosif dan racun' dibutuhkan pada kontainer dan
kendaraan yang mengangkutnya.
Asam Nitrat (HNO3):
Asam nitrat merupakan cairan terpenting setelah H2SO4, digunakan misalnya dalam
Asam nitrat murni merupakan cairan yang tidak berwarna, namun sering dijumpai dengan warna kuning sampai merah-kecoklatan tergantung dari kandungan nitrogen dioksida yang terlarut. Kerapatannya sekitar 1,5 x air dan merupakan oksidator kuat. Beberapa sifat dari bahan ini pada kondisi pekat antara lain adalah :
- konsentrasi dalam air : 68 - 70 % - gravitasi spesifik: 1,5
- titik didih: 86 o C - titik beku: - 42 o C - sangat larut dalam air
Asam ini dapat merusak logam karena sifatnya sebagai oksidator kuat. Asam nitrat (pekat) direduksi menjadi nitrogen, atau nitrogen monoksida atau nitrogen dioksida atau dinitrogen monoksida atau ion amonium, tergantung pada konsentrasi asam tersebut, seperti reaksi di bawah ini :
5Zn(s)+12HNO3(l)⇒5Zn(NO3)2(l)+6H2O(l)+N2(g) 3Zn(s)+8HNO3(l)⇒3Zn(NO3)2(l)+4 H2O(l)+2NO(g) Zn(s)+4HNO3(l)⇒Zn(NO3)2(l)+2H2O(l)+2NO2 (g) 4Zn(s)+10HNO3(l)⇒4Zn(NO3)2(l)+5H2O(l)+N2O(g) 4 Zn(s)+10HNO3(l)⇒
4Zn(NO3)2(l)+3H2O(l) +NH4NO3(g)
Umumnya hanya satu reaksi yang terjadi. Nitrogen dioksida dapat terbentuk bila asam nitrat pekat yang digunakan, sedang monoksida terbentuk bila asam nitrat encer yang
digunakan. Bila logam yang dijumpainya adalah berupa serbuk maka reaksi akan disertai ledakan. Oksidasi logam alumunium pada temperatur kamar tidak dapat terjadi bila konsentrasi asam nitrat lebih tinggi dari 80%, dan korosi pada besi tidak terjadi bila
konsentrasi asam nitrat lebih tinggi dari 70%. Sedang logam khromium resistan terhadap asam ini.
Asam ini juga dapat merusak bahan non logam, seperti karbon dan sulfur. Asam ini juga
mengoksidasi senyawa-senyawa organik seperti aceton, nitrobenzene, ethyl alkohol, dan kadangkala disertai ledakan dan merupakan sumber nyala. Asam ini dapat menimbulkan swa-nyala bagi bahan sellulosa, terutama bila bahan ini dalam bentuk serbuk. Asam ini juga akan mengkorosi jaringan tubuh bereaksi dengan protein membentuk xanthroproteic acid berwarna kuning. Pemaparan maksimum yang diizinkan di Amerika Serikat adalah 2 ppm. Pengangkut dan kontainer yang digunakan mencantumkan label 'korosif, oksidator dan racun'.
Asam Khlorida (HCl):
Asam ini merupakan bahan kimia yang termasuk penting dalam kegiatan industri, misalnya pada industri pelapisan logam, minyak, atau untuk menghasilkan senyawa yang mengandung khlor seperti karet sintetis, atau produk yang banyak digunakan di rumah tangga, misalnya pembersih WC.
Bahan ini merupakan cairan yang tidak berwarna, membentuk asap, dan menyengat. Sifat-sifat asam khlorida pekat antara lain adalah :
- konsentrasi dalam air: 36 - 38 % - gravitasi spesifik: 1,20
- titik didih: - 85 °C - titik beku: - 115 °C
- kelarutan dalam air: 85 g/100 g air.
Bahan ini bukan termasuk oksidator, walaupun termasuk dalam kelompok asam kuat.
Klasifikasi bahaya dari bahan ini karena bersifat korosif dan toksik. Kerapatan gasnya sekitar 1/5 lebih ringan dari udara. Terhirupnya gas ini melalui pernafasan akan menyebabkan
degenerasi total sel bagian pernafasan, bahkan dapat merusaknya. Batas yang diperbolehkan di Amerika Serikat pada lingkungan kerja adalah 5 ppm. Label yang disyaratkat adalah 'korosif dan racun'.
Asam Perchlorit (HClO4):
Bahan ini termasuk asam mineral yang penting dalam perindustrian, misalnya pada industri kimia dan elektroplating. Asam ini, terutama pada kondisi panas, merupakan oksidator kuat khususnya terhadap senyawa organik. Materi sellulosa (seperti kertas, kayu) akan tebakar dengan sendirinya bila berkontak dengannya. Beberapa sifat (asam pekat) dari bahan ini adalah :
- konsentrasi dalam air: 72,4 % - gravitasi spesifik: 1,70 - titik didih: 203 o C - titik beku: - 18 o C
- kelarutan dalam air: sangat larut
Departemen Transportasi Amerika Serikat menentukan bahwa HClO4 dengan konsentrasi lebih kecil dari 50% sebagai 'korosif', sedang antara 50-72% sebagai 'oksidator' dan
pengangkutan dengan konsentrasi >72 % tidak diperkenankan. Label yang dipersyaratkan adalah : 'korosif dan oksidator'.
asam sulfat dapat menghidrasi asam perkhlorit, maka botol kedua jenis asam ini tidak
diperbolehkan diletakkan berdampingan.
Asam Fluorida (HF):
Penggunaan asam fluorida dalam industri adalah penting, baik digunakan secara langsung atau dicampur dengan H2SO4,
misalnya dalam pembuatan chip pada industri komputer, atau dalam industri perminyakan untuk menghasilkan bahan bakar beroktan tinggi.
Cairan ini tidak berwarna, mampu bereaksi dengan silikon dioksida (pasir) dan gelas membentuk silikon tetrafluorida, dan merupakan satu-satunya asam yang
mengkorosi gelas. Reaksi yang terjadi adalah : CaSiO3(s)+6HF(pekat)⇒CaF2(s)+SiF4(g)+ 3H2O(l)
Asam fluorida merupakan asam lemah, dapat mengkorosi bahan tetapi tidak sehebat asam-asam sebelumnya. Asam ini dalam kondisi pekat lebih berbahaya bila kontak dengan kulit karena tidak mendatangkan sakit pada saat kontak, namun beberapa jam kemudian terjadilah penetrasi dalam kulit.
Beberapa sifatnya (kondisi pekat) adalah : - konsentrasi biasa dijumpai: 48-60% - gravitasi spesifik: 1
- titik didih: 20 o C - titik beku: - 83 o C - sangat larut dalam air.
Aturan pengangkutan di Amerika Serikat adalah mensyaratkan label 'korosif dan toksik'.
Asam Fosfat (H3PO4):
Unsur fosfor paling tidak mempunyai 8 jenis asam, namun asam fosfat adalah yang paling umum digunakan dalam industri, seperti industri pupuk. Campuran kalsium dihidrogen fosfat dan kalsium fosfat dikenal sebagai superfosfat, yang merupakan pupuk sintetis yang penting.
Asam fosfat tidak berwarna dan tidak berbau. Beberapa sifat dari asam ini dalam keadaan pekat adalah :
- konsentrasi dalam air: 85 % - gravitasi spesifik: 1,69 - titik didih: 260 o C - titik beku: 42 o C - sangat larut dalam air.
larutan ini bereaksi dengan air secara keras, dan mengeluarkan panas. Disamping itu, larutan ini bersifat korosif pada bahan. Label
untuk pengangkutan dan kontainer mencantumkan sebagai 'korosif'. Batas
pemaparan yang diizinkan di ruang kerja adalah 1 mg/m3.
NaOH dan KOH:
NaOH merupakan kelompok alkalin korosif yang paling penting dan dikenal sebagai caustic soda. NaOH merupakan basa kuat, banyak digunakan di industri seperti: petroleum, tekstil, kertas, sabun; produk ini juga digunakan di rumah tangga, misalnya untuk menangani penyumbatan pipa plambing.
Pada temperatur kamar, NaOH adalah
berbentuk padat-putih, dapat mengkorosi logam seperti alumunium, seng, tembaga dan jaringan kulit dan melarutkan lemak; bila terjadi kontak yang lama, bahan ini dapat mengkorosi gelas, membentuk natrium silikat. Oleh karenanya, wadah yang digunakan sebaiknya bukan bahan gelas. Bahan ini reaktif dengan air dan
menghasilkan panas 10 kcal per mole sehingga dapat memicu kebakaran. Beberapa sifat penting dari bahan ini adalah :
- gravitasi spesifik: 2,13 - titik didih: 1390 o C - titik leleh: 315 o C
- kelarutan dalam air: 42 gr/100 gr H2O.
Pengangkutan bahan ini di Amerika Serikat mensyaratkan penulisan label sebagai 'korosif'. Batas pemaparan di ruang kerja adalah 2 mg/m3.
Kalium Hidroksida merupakan basa yang lebih kuat dibanding NaOH, tetapi dengan bahaya yang lebih kecil, dan dikenal dengan nama caustic potash. Bahan ini umumnya digunakan pada industri pupuk, fotografi, farmasi, sabun dan sebagainya. Reaksi yang terjadi umumnya seperti halnya NaOH, dan dikenal sebagai basa yang korosif. Sifat-sifat fisiknya antara lain: - gravitasi spesifik: 2,04
- titik didih: 1320 o C - titik leleh: 360 o C
- kelarutan dalam air: 107 gr/100 gr air.
6 BAHAN KIMIA YANG REAKTIF PADA AIR
Air dapat bereaksi dengan bahan berbahaya membentuk suatu produk yang dapat terbakar dengan sendirinya, menimbulkan ledakan, toksik atau bersifat korosif. Proses yang
menyebabkan air mendekomposisi suatu materi dikenal sebagai hidrolisis. Tetapi proses
- bereaksi dengan air secara kuat,
- membentuk campuran yang eksplosif bila bercampur air,
- menghasilkan gas, uap atau asap toksik. Disamping itu dikenal pula bahan yang higroskopik, yaitu bahan yang mampu untuk menyerap air di udara, seperti H2O4 dan NaOH,
sehingga bila bahan tersebut dibiarkan terbuka di udara lembab, maka wadahnya lama
kelamaan akan penuh. Beberapa bahan dikenal pula sebagai piroforik, yaitu bahan yang dapat terbakar secara spontan bila berada dalam keadaan udara kering atau lembab atau pada temperatur < 54,5 °C. Dalam uraian berikut ini dijelaskan secara umum kelompok bahan yang termasuk dalam katagori reaktif dalam air.
Logam-logam Alkali:
Beberapa jenis logam ini adalah lithium,
natrium, kalium, cesium, rubidium dan francium; namun yang paling sering digunakan adalah lithium, natrium dan kalium. Logam-logam alkali ini merupakan kelompok logam yang paling reaktif, terutama dalam kondisi lembab akan menghasilkan gas H2 dengan resiko kebakaran
yang tidak dapat dipadamkan dengan air, tetapi biasanya dengan dry powder yang
mengandung grafit. Pengangkutan bahan ini membutuhkan label yang menyatakan sebagai 'berbahaya bila lembab'. Beberapa sifat dari lithium, natrium dan kalim adalah seperti terlihat dalam tabel 4.1.
TABEL 4.1 : Sifat fisika logam-logam alkali
Lithium Natrium Kalium Kerapatan pada 20o C (g/ml) 0,534 0,972 0,819 Titik leleh (° C) 179 97,5 63,7 Titik didih (o C) 1317 833 760 Panas fusi (kcal/kg) 103,2 27,2 14,6 Panas penguapan (kcal/kg) 4680 1005 496
Lithium adalah logam yang lunak, merupakan unsur padat yang paling ringan dan dapat mengapung pada produk minyak bumi. Bahan ini digunakan dalam industri porselen, keramik, agen pemutih, farmasi. Bila bereaksi dengan air akan menghasilkan reaksi :
2 Li(s) + 2 H2O(l) ⇒ 2 LiOH(l) + H2(g)
Reaksi berlangsung lambat bila dibandingkan dengan reaksi alkali yang lain, sehingga tidak berbahaya dibandingkan logam alkali lainnya. Oleh karena titik didihnya lebih tinggi dari air, maka bila bereaksi dengan air akan tetap sebagai padatan, sedangkan logam alkali lainnya akan meleleh.
Natrium adalah unsur keenam yang paling banyak dijumpai dalam tanah dan lautan. Logam ini juga lunak, dan merupakan logam alkali yang paling umum digunakan. Bahan ini antara lain digunakan dalam produksi logam titanium, sebagai katalis dalam pembuatan karet sintetis, sebagai bahan baku dalam pembuatan senyawa-senyawa yang mengandung natrium yang bersifat reaktif, seperti natrium peroksida. Natrium dapat menyala secara spontan dalam udara bertemperatur kamar, berasap kuning dan membentuk natrium oksida sesuai dengan reaksi:
4 Na(s) + O2(g) ⇒ 2 Na2O(s)
Kalium merupakan unsur ketujuh yang paling banyak dijumpai di dalam tanah dan lautan. Sebagaian besar logam kalium digunakan untuk memproduksi logam campuran natrium-kalium sebagai penukar panas pada fluida. Dibandingkan dengan logam alkali yang lain, logam ini adalah yang paling reaktif. Bila terpapar dengan udara pada temperatur kamar, logam ini akan terbakar, berasap ungu dan membentuk kalium oksida.
Logam-logam lain:
Beberapa jenis logam lain yang mempunyai sifat reaktif terhadap air adalah magnesium, titanium, alumunium dan seng. Kelompok ini bila dalam bentuk bubuk akan secara spontan meledak sehingga dapat menimbulkan resiko kebakaran, karena bersifat piroforik. Kemurnian dari logam kelompok ini akan menentukan resiko tersebut di atas. Bila permukaan logam ini diselimuti oleh oksida, maka resiko tersebut dapat dikurangi. Faktor lain yang
mempengaruhinya adalah ukuran partikel, distribusi atau dispersi partikel, kelembaban dan jumlah oksigen yang terserap.
bagian-bagian mesin dan sebagainya. Bila logam ini terbakar di udara, hanya sekitar 75% diantaranya yang bereaksi dengan oksigen untuk membentuk magnesium oksida, sedang sisanya akan membentuk magnesium nitrida, seperti reaksi :
2 Mg(s) + O2(g) ⇒ 2 MgO(s)
3 Mg(s) + N2(g) ⇒ Mg3N2(s)
Cahaya yang ditimbulkan oleh terbakarnya magnesium adalah putih terang, yang dapat membahayakan retina mata. Asap dari magnesium oksida berbahaya bila terhisap karena bersifat reaktif terhadap lembab yang ada dalam saluran pernafasan dan membentuk magnesium hidroksida, yang dapat
menimbulkan luka pada paru-paru.
Pengangkutan bahan ini membutuhkan label yang bertuliskan 'berbahaya bila lembab'.
Titanium merupakan elemen ke sepuluh yang paling banyak dijumpai di dalam tanah dan lautan. Seperti halnya magnesium, logam ini termasuk yang mempunyai kerapatan kecil dibandingkan logam lainnya. Logam ini sekeras baja tetapi 45% lebih ringan. Oleh karena kombinasi keras dan ringan ini, maka logam ini banyak digunakan dalam industri pesawat terbang. Logam ini tahan terhadap sifat korosi air laut sehingga banyak digunakan dalam pembuatan kapal laut. Namun biaya untuk memproduksi logam ini adalah sangat tinggi sehingga membatasi penggunaannya. Seperti halnya magnesium, logam ini reaktif terhadap air dan berisiko terhadap terjadinya ledakan dan kebakaran.
Aluminum (alumunium) merupakan bahan yang paling populer diantara bahan-bahan
sebelumnya, dan merupakan unsur ketiga terbanyak di perut bumi dan lautan. Alumunium lebih ringan dibanding titanium. Bahan ini dapat dibentuk sebagai lembaran yang tipis dan banyak digunakan dalam kegiatan industri maupun non- industri. Alumunium murni termasuk salah satu logam yang paling reaktif. Namun dengan terbentuknya alumunium oksida yang berada di permukaan akan melindungi logam ini dari reaksi kimia. Adanya lapisan inilah yang menyebabkan alumunium dianggap sebagai logam yang tidak berbahaya. Seperti halnya yang lain, maka bila serbuk alumunium diangkut maka dibutuhkan label sebagai 'berbahaya bila lembab'.
Seng termasuk yang sering digunakan dalam kegiatan non-industri. Campurannya dengan tembaga menghasilkan logam campuran yang
dikenal sebagai kuningan. Seng juga digunakan untuk melindungi besi dari korosi (galvanis), atau sebagai pigmen dalam pembuatan cat. Transportasi bubuk seng membutuhkan label 'berbahaya bila lembab'.
Senyawa Organometalik:
Kelompok senyawa organometalik yang penting dalam industri adalah dalam bentuk atom-atom logam yang terikat secara langsung dengan atom-atom karbon, sehingga dekenal sebagai senyawa-senyawa organometalik. Senyawa ini biasanya digunakan sebagai katalis
polimerisasi. Tidak kurang dari 50 jenis senyawa organometalik tersedia secara
komersial, umumnya mengandung satu sampai sepuluh atom karbon pada setiap molekulnya, beberapa diantaranya adalah : diethylzinc (C2H5)2Zn, tetraethyllead (C2H5)5Pb,
trimethylaluminum Al(CH3)3, tri(isobutyl)
aluminum Al(C4H9)3, dimethylcadmium
Cd(CH3), tetramethyltin Sn(CH3)4.
Diethylzinc adalah organometalik yang biasanya digunakan dalam sintesa beberapa senyawa organik, terutama senyawa
organometalik yang lain, dan digunakan pula sebagai katalis dalam polimerisasi ethene. Senyawa ini bersifat piroforik, dapat terbakar secara spontan di udara, membentuk seng oksida, karbon dioksida dan air. Dalam air, senyawa ini akan bereaksi secara keras membentuk ethane, seperti reaksi: (C2H5)2Zn(l)+7O2(g)⇒ZnO(s)+4CO2(g)+ 5H2O(g) (C2H5)2Zn(l)+2H2O(l)⇒Zn(OH)2(s)+C2H6(g)
Tata cara pengangkutan di Amerika Serikat mensyaratkan label 'bahan bakar spontan'.
Diantara bahan organometalik yang mungkin paling terkenal adalah tetraethyllead yang digunakan dalam mengurangi ketuk (knock), yang ditambahkan pada bahan bakar
kendaraan bermotor. Bila terjadi pembakaran, akan dihasilkan cemaran timbal di udara, sehingga sangat tidak dianjurkan untuk digunakan. Berbeda dengan senyawa organometalik yang lain, senyawa ini
merupakan satu- satunya yang bukan termasuk piroforik, serta tidak reaktif terhadap air. Satu- satunya karakteristik bahaya yang
Kelompok organometalik yang juga penting dalam industri adalah senyawa- senyawa yang mengandung atom alumunium yang terikat pada atom karbon, dikenal sebagai senyawa aluminum alkyl, seperti trimethylaluminum dan tri(isobutyl) aluminum, yang digunakan
terutama untuk katalis polimerisasi. Seluruh senyawa kelompok ini merupakan senyawa yang piroforik, bereaksi secara keras dengan air dan sangat toksik.
Hidrida-hidrida Metalik:
Kelompok hidrida-hidrida metalik yang paling banyak digunakan secara komersial adalah yang tersusun dari atom hidrogen, atau logam alkali atau alumunium, atau kadangkala boron. Senyawa ini biasanya digunakan dalam industri sebagai pereduksi. Senyawa ini relatif stabil, namun bila bereaksi dengan air, termasuk kelembaban udara, akan menghasilkan gas H2
dan mudah terbakar. Kelompok ini juga
bereaksi secara hebat dengan bahan odsidator. Beberapa jenis hidrida metalik ini antara lain adalah lithium atau natrium hidrida (LiH), lithium atau natrium borohidrida, tetrahidridoaluminate (LiAlH4), lithium aluminium hidrida (LiAlH4),
aluminium tetrahidridoborate Al(BH4)3.
Departemen Transportasi Amerika Serikat mengatur pengangkutan lithium dan natrium hidrida, serta lithium dan natrium borohidrida sebagai 'berbahaya bila lembab.
Borane:
Senyawa-senyawa hidrogen dengan satu atau lebih unsur non-metal dikenal sebagai hidrida-hidrida molekular, karena berada sebagai satuan molekular. Molekular hidrida yang umum adalah air. Contoh lain adalah hidrogen sulfida (H2S), amonia (NH3), methane (CH4), hidrogen
khlorida (HCl) dan sebagainya. Molekular hidrida dari boron disebut borane, merupakan senyawa yang reaktif terhadap air, sangat toksik dan bila terbakar akan terbentuk oksida boron. Paling tidak dikenal 14 jenis borane, umumnya tidak stabil pada temperatur kamar. Hidrida-hidrida ini akan terdekomposisi menjadi boron dan hidrogen pada temperatur di atas 300oC.
Borane (BH3)pada tekanan atmosfer adalah
tidak stabil, dan berubah menjadi diborane (B2H6). Diborane ini termasuk gas yang mudah
terbakar. Dengan konsentrasi diborane sebesar 0,8% (volume) di udara, akan dapat
menyebabkan pembakaran spontan dan
berasap hijau. Dengan sifat panas
pembakarannya yang tinggi (527 kcal/mol), disertai dengan berat molekulnya yang rendah, menyebabkan diborane digunakan sebagai bahan bakar roket. Disamping itu, diborane tergolong toksik. Pemaparan maksimum dalam ruangan kerja adalah hanya 0,1 ppm.
Transportasi bahan ini membutuhkan label 'gas beracun dan mudah terbakar'.
Peroksida, Karbida, Fosfida dan Khlorida Metalik:
Senyawa-senyawa yang tersusun antara logam dengan ion peroksida (O2=) dikenal sebagai
peroksida metalik, yang umumnya berbahaya karena bersifat sebagai oksidator disamping reaktif terhadap air. Peroksida metalik yang penting dalam industri adalah yang tersusun dari logam alkali dan alkali tanah, terutama natrium peroksida dan barium peroksida. Senyawa ini tidak terbakar, namun dapat menimbulkan api. Barium peroksida disamping membutuhkan label 'oksidator', diperlukan juga label 'racun'.
Ion-ion karbon dalam bentuk C22-, C4- atau C3
4-dikenal sebagai karbida, dan senyawa yang mengandung logam dengan ion-ion karbida dikenal sebagai karbida-karbida metalik, seperti kalsium karbida CaC2 yang digunakan dalam
industri sebagai sumber acetylene dan pupuk kalsium cyanamida. Bila kalsium karbida bereaksi dengan air, gas acetylene (C2H2) akan
terbentuk sesuai dengan reaksi : CaC2(s)+2H2O(l)⇒Ca(OH)2(s)+C2H2(g)
Gas acetylene inilah yang berfungsi sebagai bahan bakar pada saat digunakan dalam pengelasan. Untuk menghindari bahaya kebakaran atau ledakan, maka kalsium karbida harus dijaga agar tetap kering dan bebas dari lembab udara.
Contoh fosfida metalik adalah kalsium fosfida, yang juga reaktif terhadap air. Bila kalsium fosfida bereaksi dengan air, akan terbentuk gas bakar fosfine, yang juga bersifat tosksik, dengani reaksi di bawah ini :
Ca3P2(s)+6H2O(l)⇒3Ca(OH)2(s)+2PH3(g)
Senyawa-senyawa yang mengandung khlor dengan metalik dan atau non-metalik
merupakan substansi yang reaktif terhadap air. Senyawa ini tergolong berbahaya, karena bereaksi secara keras dengan air,
berbentuk larutan akan bersifat korosif.
Beberapa jenis senyawa ini adalah : alumunium khlorida (AlCl3) yang bersifat korosif, antimoni
pentakhlorida (SbCl5) yang bersifat korosif,
boron trikhlorida (BCl3) yang menguap pada
18oC dan bersifat toksik, fosforus oksikhlorida (POCl3) yang bersifat korosif dan toksik.
7 BAHAN-BAHAN KIMIA TOKSIK
Terdapat berbagai cara agar sebuah bahan/substansi masuk ke dalam tubuh manusia; yang paling penting adalah melalui : mulut, kulit dan pernafasan. Bila sebuah substansi bersifat toksik, dia dapat merusak jaringan di lokasi kontaknya (efek lokal) atau berpengaruh negatif dengan jalan lain, yang mengakibatkan efek sistemis. Sebagai contoh, bila merkuri terserap oleh kulit maka akan dapat merusak ginjal atau pusat sistem syaraf.
Pengaruh racun dapat diklasifikasikan
berdasarkan waktu yang dibutuhkan terjadinya penyakit atau gangguan, yaitu:
- Bersifat akut : kerusakan yang terjadi biasanya akibat sejenis bahan dengan pemaparan singkat, seperti terhisapnya gas HCl beberapa detik yang akan menye-babkan kerusakan langsung pada paru-paru; bisa saja keterpaparan ini terjadi secara berulang-ulang sampai menimbulkan kerusakan.
- Bersifat kronis: suatu pengaruh atau keadaan sakit yang muncul sedikit demi sedikit dalam waktu yang agak lama setelah pemaparan pertama, misalnya timbulnya kanker liver angiosarcoma yang muncul beberapa tahun setelah menghirup vinyl khlorida.
- Bersifat laten: suatu pengaruh atau keadaan sakit yang baru berkembang setelah masa inkubasi terlampaui, misalnya benzene akan mengakibatkan aplastic anemia setelah sekitar 10 tahun sejak pertama kali terjadinya pemaparan.
Sebuah substansi yang masuk ke dalam tubuh melalui pernafasan dapat berakibat sebagai : - Asphyxiant : substansi kimia yang
menyebabkan kehilangan kesadaran karena kurangnya oksigen dalam darah, misalnya nitrogen, hidrogen, karbon monoksida. - Irritant : substansi kimia yang melukai
jaringan sistem pernafasan dan paru- paru, misalnya hidrogen khlorida yang merupakan bahan korosif.
Dalam toksikologi, untuk melihat pengaruh suatu substansi pada manusia, biasanya dilakukan percobaan melalui binatang, kemudian hasilnya di ekstrapolasi pada manusia. Cara ini biasanya cocok untuk toksik yang bersifat akut. Untuk toksik yang bersifat kronis atau laten, percobaan melalui binatang tidak selalu relevan karena faal manusia dan binatang tidak selalu sama. Oleh karenanya bila substansi tersebut menyebabkan kanker pada binatang dan belum terbukti pada manusia, maka bahan tersebut dikenal sebagai suspect human carcinogen, dan akan menjadi human carcinogen bila memang terbukti dapat menyebabkan kanker pada manusia.
Untuk mengkuantifikasi toksisitas akut, maka digunakan penelitian terhadap binatang percobaan, yaitu :
- Lethal dose-50 (LD50): konsentrasi bahan,
dengan satuan mg bahan per kg berat binatang, yang menyebabkan kematian binatang penelitian sebanyak 50% . - Lethal concentration-50 (LC50): konsentrasi
bahan, dalam satuan ppm (volume), yang dapat mematikan 50% binatang percobaan. - Threshold limit value (TLV): limit teratas dari
sebuah konsentrasi toxin yang tidak menimbulkan pengaruh kesehatan pada manusia yang terpapar secara rutin, dengan satuan ppm (gas) atau mg/m3 ( asap udara). - Immediately dangerous to life and health
(IDLH) : merupakan konsentrasi maksimum suatu substansi yang memungkinkan manusia menghindar dalam 30 menit tanpa masalah pada kesehatannya.
- Time weighted average threshold limit value (TWA-TLV) : konsentrasi rata- rata di ruang kerja yang dapat diterima oleh sebagian besar pekerja selama 40 jam per minggu atau 8 jam per hari tanpa menimbulkan gangguan.
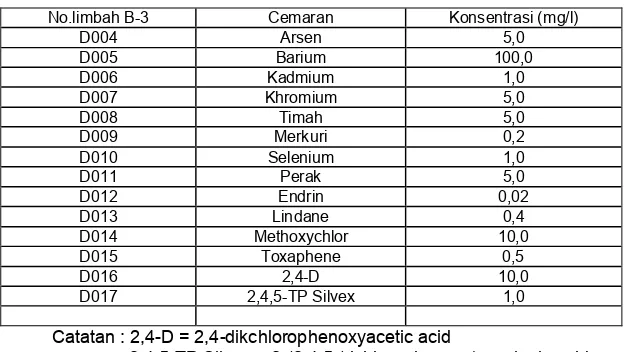
USEPA menggunakan tolak ukur yang bersifat praktis, yaitu dengan EP-toxicity ( extraction-procedure toxicity), yang mengatur beberapa cemaran logam toksik dan pestisida, dengan memberikan batasan konsentrasi maksimum cemaran yang diuji sesuai dengan protokol penelitian. Konsentrasi maksimum tersebut seperti terlihat dalam tabel 2.2.
Bila cemaran tersebut mengandung unsur berkonsentrasi lebih tinggi dari yang tertera dalam tabel, maka cemaran tersebut terkatagorikan sebagai toksik.
• Oksida-oksida karbon: seperti CO,CO2 • Hidrogen cyanida: HCN
• Senyawa sulfur: H2S, SO2
• Oksida-oksida nitrogen seperti N2O, NO2,
N2O4 – Amonia
• Logam-logam berat seperti: arsen, timah (Pb)
• Asbestos. Pestisida organik.
TABEL 2.2 : Konsentrasi maksimum bahan toksik dengan EP-toxicity
No.limbah B-3 Cemaran Konsentrasi (mg/l)
D004 Arsen 5,0
D005 Barium 100,0
D006 Kadmium 1,0
D007 Khromium 5,0
D008 Timah 5,0
D009 Merkuri 0,2
D010 Selenium 1,0
D011 Perak 5,0
D012 Endrin 0,02
D013 Lindane 0,4
D014 Methoxychlor 10,0
D015 Toxaphene 0,5
D016 2,4-D 10,0
D017 2,4,5-TP Silvex 1,0
Catatan : 2,4-D = 2,4-dikchlorophenoxyacetic acid
2,4,5-TP Silvex = 2-(2,4,5-trichlorophenoxy)propionic acid
Oksida-oksida Karbon:
Bila bahan mengandung karbon terbakar, maka akan terbentuk gas karbon dioksida (CO2). Bila
pembakaran tidak sempurna akan dihasilkan gas karbon monoksida (CO), yang tergolong gas berbahaya karena dapat menyebabkan kematian. Reaksi yang umum, misalnya dalam pembakaran gas methane, adalah :
2 CH4(g)+3O2(g)⇒ 2CO(g)+4H2O(g)
CH4(g)+O2(g)⇒ C(s)+2H2O(g)
Kedua jenis oksida tersebut adalah tidak berwarna dan tidak berbau. Beberapa sifat gas karbon monoksida adalah :
- titik didih: - 191,6 o C
- densitas cairan (pada titik didih):795 g/L - densitas gas (pada titik didih): 4,3 g/L - densitas gas (pada 20oC):1,25 g/L - densitas uap (udara=1): 0,97 - panas pembakaran: 67,64 kcal/mol - % batas bawah ledakan: 12,5 - % batas atas ledakan: 74 - rasio ekspansi cair ke gas: 700
Sedang beberapa sifat gas karbon dioksida adalah :
- titik beku (oC): - 56,55 oC
- titik sublimasi (pada 1 atm): 78,5 oC - panas fusi: 47,5 kcal/kg
- panas sublimasi: 36,2 kcal/kg
- densitas padat (pada 1 atm): 1,56 g/ml
- densitas gas (pada titik sublim): 2,8 g/L - densitas gas (pada 20oC): 1,98 g/L - densitas uap (udara=1): 1,529 - rasio ekspansi cair ke gás: 790
Karbonmonoksida merupakan gas toksik, yang dapat terserap oleh darah melalui pernafasan. Pada saat manusia bernafas, oksigen akan terbawa oleh aliran darah oleh komponen dalam darah yang disebut hemoglobin (Hb). Bila Hb ini menyerap oksigen akan terbentuk oksihemoglobin (O2Hb), dengan reaksi seperti :
Hb(l)+O2(g)⇒O2Hb(l)
Oksihemoglobin ini akan melepaskan oksigen pada jaringan atau organ lainnya. Bila
karbonmonoksida terhirup, akan terbentuk karboksihemoglobin (COHb) :
Hb(l)+CO(g)⇒COHb(l)
yang mempunyai afinitas kimia sebesar 300 kali lebih tinggi daripada pembentukan
oksihemoglobin.
Oksigen yang terikat dalam oksihemoglobin juga dapat dilepaskan sesuai dengan reaksi : O2Hb(l)+CO(g)⇒COHb(l)+O2
Karboksihemoglobin ini relatif stabil dan menghalangi penyerapan oksigen oleh darah sehingga penderita mengalami anoxia, yaitu kekurangan oksigen dalam darah.
Pada dasarnya tubuh manusia lebih toleran terhadap CO2, walaupun adanya CO2 akan
sehingga pekerjaan terasa menjadi lebih berat. TLV di udara untuk karbon monoksida adalah 100 ppm, sedangkan untuk CO2 adalah 5000
ppm (0,5 %); lebih dari konsentrasi tersebut akan menimbulkan gangguan pernafasan. Kontainer atau silinder gas karbon monoksida membutuhkan label 'gas beracun' dan ' gas mudah terbakar', sedang untuk gas karbon dioksida tergolongkan sebagai 'gas tidak terbakar'.
Hidrogen Sianida (HCN):
Pada temperatur kamar, hidrogen sianida adalah merupakan gas yang tidak berwarna, dengan sifat-sifat antara lain :
- titik beku (oC): - 14 oC - titik didih (oC): 26 oC
- kerapatan pada 20 oC: 1,2 g/L - kerapatan uap (udara = 1): 0,93 - % batas terendah ledakan: 6 - % batas tertinggi ledakan: 41 - titik nyala cairan: - 18 o C
Gas HCN larut dalam air membentuk asam hidrosianik. Hidrogen sianida anhidrous (cair) merupakan bentuk yang secara komersial sering dijumpai, merupakan bahan yang tidak stabil. HCN banyak digunakan dalam
pembuatan plastik seperti polyacrylonitrile yang mengandung grup -CN. Bila jenis plastik ini dipanaskan, maka akan terdekomposisi secara termal dan terbentuklah gas racun HCN. Bahan racun ini mempengaruhi transportasi oksigen dalam darah, karena dapat
mengganggu aktivitas enzim cyctochrome oxidase yang dibutuhkan untuk respirasi selluler dan pembentukan enersi. Bahan ini masuk ke dalam tubuh melalui pernafasan atau kulit.
Beberapa senyawa kimia dengan ion-ion metalik yang bergabung dengan ion- ion sianida, seperti natrium sianida, banyak
digunakan dalam industri elektroplating. Seperti halnya gas sianida, bahan ini juga bersifat racun bila terserap oleh manusia. Bahan ini juga akan bereaksi dengan asam membentuk gas HCN :
NaCN(s)+HCl(l)⇒NaCl(l)+HCN(g)
Beberapa besaran konsentrasi (dalam ppm) yang berkaitan dengan sifat toksikologi dari HCN adalah :
- batas bau: 0,2 - 5,0 - TLV: 10
- keluhan sakit kepala: 18-36
- bertahan selama 1/2 jam tanpa kesulitan: - kematian dalam 1 jam
Pengaturan pengangkutan dan pewadahan mensyaratkan label : racun' dan 'cairan mudah terbakar'.
Senyawa Sulfur:
Senyawa yang mengandung unsur sulfur dijumpai pada batu bara, gas alam, minyak mentah, wool, rambut, polimer-polimer sintetis dan sebagainya (lihat sub bab 2.2). Bila bahan ini terpapar dengan panas atau bila terbakar akan membentuk gas hidrogen sulfida (H2S) atau SO2. Hidrogen sulfida secara komersial banyak dijumpai dalam bentuk cairan, biasanya digunakan dalam industri yang memproduksi senyawa-senyawa mengandung sulfur. Bahan ini juga digunakan dalam industri metalurgi.
Gas H2S merupakan gas yang tidak berwarna, berbau seperti telur busuk. Secara alami dijumpai akibat proses dekomposisi senyawa organik dalam kondisi anaerob. Sifat-sifat dari gas ini adalah :
- titik didih: - 60 oC - titik beku: - 83 oC
- densitas pada 20 oC: 1,539 g/L - kerapatan uap (udara = 1): 1,2 - persen batas bawah ledakan: 4,3 - persen batas atas ledakan: 46 - panas fusi: 0,568 kcal/mol
- panas penguapan: 4,463 kcal/mol
TLV dari gas H2S dibatasi hanya 10 ppm. Bila
terus menerus menghirup udara yang mengandung gas ini, akan mengakibatkan pusing dan sakit kepala; bila terhirup dengan konsentrasi 600 ppm selama 30 menit akan berakibat fatal. Tetapi karena gas ini mempunyai bau khas, maka kehadirannya dapat diketahui sejak dini. Pengangkutan dan kontainer bahan ini membutuhkan label bertuliskan 'gan beracun' dan 'gas mudah terbakar'.
Sulfur dioksida merupakan gas tidak berwarna, berbau menyengat seperti karet terbakar. Gas ini terbentuk bila senyawa mengandung sulfur terbakar, misalnya pada pembakaran gas H2S
akan terjadi reaksi:
2H2S(g)+3O2(g) ⇒ 2H2(g)+2SO2(g)
Gas ini akan muncul misalnya karena pembakaran minyak bumi atau batu bara, karena kedua jenis bahan bakar ini
mengandung senyawa sulfur. Dalam emisinya di udara, gas ini secara lambat akan
lembab udara membentuk asam sulfat sebagai penyebab hujan asam, sesuai dengan reaksi : 2SO2(g)+O2(g)⇒2S O3(g)
SO3(g)+ H2O(g)⇒H2SO4 (l)
Masalah lingkungan yang ditimbulkan pada zone industri adalah adanya kabut sulfur (sulfurous smog), yang terbentuk akibat kumulasi asam sulfat di udara.
Beberapa sifat dari gas ini adalah : - titik didih: - 10 oC
- titik beku: - 76 oC
- densitas pada 20 oC: 2,93 g/l - Kerapatan uap (udara =1): 2,3 - panas difusi: 1,77 kcal/mol - panas vaporasi: 5,96 kcal/mol
Standar emisi yang dikeluarkan oleh USEPA adalah 0,03 ppm selama periode 24 jam, dan 0,14 ppm selama periode 3 jam. Standar kedua adalah konsentrasi tahunan sebesar 0,5 ppm. Dalam ruang kerja, TLV dari SO2 adalah 5 ppm.
Pada konsentrasi sebesar 10 ppm (volume) gas ini akan mengakibatkan iritasi pada mata. Konsentrasi melebihi 500 ppm akan
menyebabkan kematian seketika. Gas ini dalam pengangkutannya membutuhkan label
bertuliskan 'gas racun'.
Oksida Nitrogen (NOx):
Terdapat enam oksida-oksida nitrogen, yaitu dinitrogen monoksida (N2O), nitrogen
monoksida (NO), dinitrogen trioksida (N2O3),
nitrogen dioksida (NO2), dinitrogen tetroksida
(NO4) dan dinitrogen pentoksida (N2O5).
Diantara keenam oksida tersebut, maka N2O3
dan N2O5 yang tidak penting dalam industri.
Gas N2O merupakan gas tidak berwarna,
banyak digunakan sebagai anestesi oleh dokter gigi. Bahan ini merupakan agen pengoksidasi yang baik, sehingga sulfur, fosfor dan karbon dapat terbakar dalam atmosfer N2O seperti
halnya dalam atmosfer yang mengandung oksigen. Dengan adanya hidrogen atau amonia, dihasilkan campuran eksplosif. Label yang dibutuhkan dalam pengangkutannya adalah sebagai 'gas tidak terbakar' dan 'pengoksidasi'.
Gas NO merupakan agen pengoksida yang baik, tidak berwarna dan berbau tajam. Magnesium dan fosfor dapat terbakar dengan baik dalam atmosfer yang mengandung gas ini seperti halnya atmosfer yang mengandung oksigen. Gas ini dapat berkombinasi dengan hemoglobin dalam darah, seperti halnya karbon monoksida, membentuk metheglobin (NOHb),
sehingga dapat menimbulkan methemoglobine-mia dengan terhalangnya transportasi
hemoglobin. Oleh karenanya, gas ini tergolong toksik dengan batas TLV 25 ppm.
NO2 dan N2O4 merupakan agen pengoksida
yang lebih baik dibanding N2O atau NO,
sehingga digunakan sebagai agen pengoksida dalam roket; gas-gas ini juga toksik dan menyebabkan methemoglobinemia dengan batas TLV 5 ppm. Pengangkutan gas ini membutuhkan label bertuliskan 'gas beracun' dan 'pengoksidasi'.
Amonia (NH3):
Amonia merupakan gas yang tak berwarna dan berbau menyengat. Beberapa sifat dari gas ini adalah :
- titik didih: - 33 o C - titik beku: - 78 o C - densitas: 0,771 g/L
- kerapatan uap (udara = 1): 0,596 - swa-penyalaan: 651 o C
- batas bawah ledakan: 16 % - batas atas ledakan: 25 %
Gas ini mudah dicairkan dan dikenal sebagai anhydrous ammonia. Dengan sifatnya yang lebih ringan dari udara (densitas uap = 0,569), bila terlepas di udara akan cepat terdispersi apalagi bila terdapat angin. Walaupun tidak berwarna, bila bahan cairan ini tumpah akan terbentuk awan putih akibat kondensasi lembab udara, sehingga memudahkan pelacakan terjadinya kebocoran.
Gas ini berakibat seperti alkali terhadap kulit manusia, yaitu dari iritasi ringan sampai rusaknya jaringan, yang tergantung pada lamanya pemaparan. Mata dan paru-paru akan teritasi bila terpapar dengan bahan ini.
Pemaparan yang berlebihan menyebabkan kebutaan dan rusaknya jaringan pernafasan. Karena bahan ini sangat larut dalam air, maka air merupakan bahan yang efektif untuk penanggulangan masalah yang timbul. Limit pemaparan di ruang kerja = 50 ppm.
Gas amonia merupakan gas mudah terbakar, dengan rentang yang kecil, serta limit
bawahnya yang relatif besar (16%), maka bahaya kebakaran relatif kecil. Pengangkutan amonia cair (anhydrous) membutuhkan label 'gas racun'. Amonia yang dilarutkan dalam air merupakan larutan yang sering dijumpai secara komersial sebagai amonium hidroksida
Logam-logam Berat Toksik:
Yang dimaksud dengan logam berat dalam buku ini adalah setiap logam yang mempunyai berat atom lebih dari 50. Bila terserap dalam tubuh manusia, beberapa logam berat akan merupakan racun, apalagi bila dalam bentuk bubuk atau asap. Logam berat yang
digolongkan toksik oleh USEPA adalah : antimon, arsen, berillium, kadmiun, khromium, tembaga, timah, merkuri, nikel, selenium, perak, thallium dan seng.
Mekanisme keracunan dari logam berat ini tergantung jenisnya, tetapi umumnya ion-ion logam ini mempunyai affinitas yang sangat besar dengan sulfur. Bila logam ini terbawa darah maka akan bersenyawa dengan sulfur yang berada pada fluida sellular tubuh, dan mempengaruhi kerja enzimatik dalam tubuh.
Asbestos:
Absestos merupakan terminologi yang
digunakan dalam ilmu mineral untuk berbagai fiber silikat yang tersusun dari silicon, oxygen, hidrogen dan ion- ion metalik seperti natrium, magnesium, kalsium dan besi.
Bahan ini mempunyai titik leleh yang sangat tinggi, tidak terbakar dan digunakan sebagai penyekat panas. Bila dicampur dengan magnesium oksida, asbestos sangat baik digunakan sebagai bahan tahan api yang banyak digunakan. Namun disamping kegunaannya tersebut, pada kondisi khusus asbestos dapat membahayakan kesehatan manusia termasuk timbulnya karena kanker, terutama bila asbestos hadir dalam bentuk debu asbes sehingga mudah terhisap melalui pernafasan atau mulut.
Debu asbes ini sangat ringan dan dapat melayang di udara. Bila terhirup masuk ke dalam paru-paru, bahan ini akan terkumpul menyebabkan asbestosis. Namun bila tidak terkumpul di paru-paru, maka akan masuk pada kerongkongan dan dapat memnyebabkan kanker pada pencernaan. Bahan ini juga menyebabkan mesothelioma pada paru-paru atau saluran pernafasan, yang hanya dijumpai pada orang yang terpapar debu asbes. Debu asbes ini mempunyai efek sinergis, misalnya bila terhisap oleh perokok, akan mengakibatkan kemungkinan terserang kanker 50 kali lebih besar dibanding orang yang tidak merokok.
Kriteria yang diberlakukan di USA pada lingkungan kerja adalah dalam 1 cm3 udara tidak boleh terdapat lebih dari 10 fiber asbes yang lebih panjang dari 5 micrometer.
Pestisida Organik :
Pestisida adalah bahan kimia yang digunakan untuk membunuh insek, fungi, roden, atau tanaman. Sebagian besar pestisida yang sekarang digunakan adalah merupakan senyawa-senyawa organik. Telah dihasilkan ribuan jenis pestisida, beberapa diantaranya telah dilarang digunakan, karena terbukti berbahaya bagi manusia.
Didasarkan atas struktur molekulnya, maka pestisida organik dapat dikelompokkan menjadi beberapa grup, yang terpenting adalah
pestisida organochlorine, pestisida
organophosphorus, pestisida karbamate dan pestisida urea.
Pestisida organochlorine merupakan turunan hidrokarbon kompleks; paling tidak sebuah atom hidrogen dalam molekul hidrokarbon tersebut, digantikan oleh atom khlor. Sebagai contoh adalah Aldrin dengan formula C12H8Cl6,
yang berasal dari hidrokarbon dengan formula C12H14. Salah satu jenis kelompok ini yang
terkenal adalah DDT, yang banyak digunakan selama perang dunia ke dua, antara lain untuk mengontrol penyakit tifus dan malaria yang ditularkan melalui insek. Namun ternyata bahan ini menimbulkan masalah kesehatan bagi manusia, sehingga pembuatan dan
penjualannya dilarang. Mekanisme bagaimana pestisida ini memepengaruhi aktivitas biologi belumlah banyak diketahui. Hanya diketahui bahwa bahan ini merusak keseimbangan natrium dan kalium dalam sel-sel syaraf sehingga mempengaruhi impuls sel tersebut. Jenis organochlorine ini mempunyai efek biokumulasi terutama pada jaringan lemak, dan sangat stabil serta persisten; melalui rantai makananlah bahan ini akan sampai pada manusia.
Pestisida organophosphorus merupakan turunan dari asam fosfat, contohnya adalah Parathion dengan formula
(C2H5)2PSOC6H4NO2. Kelompok pestisida ini
juga bersifat toksik. Pada insek, pestisida ini mempunyai kemampuan untuk menghalangi kerja enzim, dikenal sebagai
acetylcholinesterase (ACHE). Enzim ini secara rutin berfungsi mempengaruhi impuls syaraf.
adalah Carbyl yang merupakan insektisida. Fungsinya pada insek atau vertebrata adalah mempengaruhi kerja enzim cholinistrase. Beberapa jenis pestisida carbamate juga berfungsi sebagai fungisida atau herbisida.
Pestisida urea merupakan turunan dari urea, yaitu dengan sebuah atom hidrogen (atau lebih) pada urea yang digantikan oleh atom-atom lain. Salah satu pestisida kelompok ini adalah Linuron. Umumnya pestisida ini digunakan sebagai herbisida yang dapat menghalangi proses fotosintesis.
8 SENYAWA PENGOKSIDASI
Terjadinya reaksi oksidasi-reduksi (redoks) yang terkontrol sangat bermanfaat bagi manusia, seperti pembakaran bahan bakar, khlorinasi air, peledakan dinamit. Enersi dari reaksi ini dapat disimpan, seperti pada batere. Bila reaksi tidak terkontrol, maka enersi yang terbentuk dapat menyebakan bahaya bagi manusia, seperti terjadinya kebakaran, ledakan. Bila misalnya gas alam dibakar, maka enersi yang ada dapat digunakan untuk berbagai keperluan. Tetapi panas yang ditimbulkan dari reaksi redoks tersebut dapat terserap oleh bahan yang dapat terbakar yang berada di dekatnya, sehingga bahan tersebut dapat terbakar dengan sendirinya. Kadangkala walapun agen pengoksidasi dijumpai dalam jumlah yang kecil, tetapi sudah cukup untuk memungkinkan terjadinya swa- pembakaran bahan semacam sulfur dan sebagainya.
Kemampuan agen pengoksidasi bervariasi. Ada oksidator yang mempunyai kemampuan lebih tinggi dibanding oksigen, ada yang berada di bawah kemampuan oksigen. Bahan
pengoksidasi yang mengandung oksigen dapat dikatakan tidak stabil waktu dipanaskan. Bahan tersebut akan memasok oksigen pada saat terjadinya kebakaran walaupun udara di
sekitarnya kekurangan oksigen. Beberapa agen pengoksidasi diuraikan di bawah ini secara umum.
Hidrogen Peroksida (H2O2):
Hidrogen peroksida merupakan peroksida yang paling sering dijumpai. Hidrogen peroksida murni mempunyai penampilan yang mirip air, tetapi mempunyai bau yang sedikit tajam. Bahan ini banyak digunakan dalam industri tekstil untuk pengelantang. Dalam industri kimia, bahan ini digunakan untuk memproduksi bahan peroksida metalik dan organik.
Hidrogen peroksida merupakan bahan yang relatif tidak stabil. Larutan dengan konsentrasi 8 % (massa) secara lambat akan terdekomposisi menjadi air dan oksigen setelah 9 bulan. Sinar matahari akan bertindak sebagai katalisator. Bila berada pada konsentrasi yang pekat (lebih besar dari 30 %), maka larutan ini aka
terdegradasi secara cepat yang disertai timbulnya panas sehingga akan dapat
teruapkan. Untuk menghindari bahaya ledakan, larutan ini distabilkan dengan sejumlah kecil natrium pirofosfat, yang akan bertindak sebagai katalis guna memperlama proses dekomposisi. Beberapa logam seperti besi, baja, timah, tembaga, khrom, seng, mangan dapat bertindak sebagai katalis guna terjadinya dekomposisi. Larutan yang mengandung hidrogen peroksida lebih dari 50% (volume) dapat menyebabkan timbulnya api secara spontan dari bahan yang dapat terbakar. Hidrogen peroksida selain dapat bertindak sebagi oksidator kuat, namun dapat pula berfungsi sebagai reduktor lemah. Pada saat bertindak sebagai reduktor, oksigen selalu dibebaskan.
Hidrogen peroksida dapat menimbulkan masalah kesehatan yang serius; pada konsentrasi larutan lebih besar dari 30 % (volume) larutan ini korosif terhadap kulit. Di lingkungan kerja batas pemaparan maksimum adalah 1 ppm. Transportasi hidrogen peroiksida dengan konsentrasi sampai 20 % diberi label : 'oksidator'. Bila di atas konsentrasi tersebut diberi label : 'oksidator dan korosif'.
Hipokhlorit, Khlorit, Khlorat dan Perkhlorat:
Bahan pengoksidasi yang juga banyak digunakan adalah natrium dan kalsium hipokhlorit, yang merupakan komponen aktif sebagai pemutih maupun untuk pembersih peralatan saniter. Hipokhlorit metal ini, dengan konsentrasi sekitar 3 sampai 5 %, biasanya digunakan sebagai pemutih pada pencucian pakaian karena kemampuannya bereaksi dengan karbon di udara akan memproduksi asam hipokhlor dan melepaskan oksigen, seperti reaksi di bawah ini :
2 NaClO(l)+H2O(l)+CO2⇒Na2CO3(l)+2HClO(l) 2 HClO(l)⇒2HCl(l)+O2(g)
Oksigen yang dibebaskan dari dekomposisi fotokimia ini akan memucatkan pakaian. Bahan ini digunakan pula dalam penyediaan air bersih atau pengolahan air limbah sebagai
Natrium khlorit merupakan agen
pemucat/pemutih yang banyak digunakan da-lam industri kertas dan tekstil. Secara komersial, bahan ini diperoleh dalam konsentrasi larutan sampai 80 %. Dalam pengangkutannya, bahan ini dianggap sebagai bahan pengoksidasi, sedangkan dalam kondisi sebagai larutan dianggap sebagai korosif.
Metal khlorat yang sering digunakan adalah natrium khlorat atau kalium khlorat, digunakan terutama sebagai komponen serbuk mesiu, herbisida dan sebagainya. Natrium khlorat sangat sensitif misalnya bila bergesekan dan dapat menimbulkan terjadinya api dengan mudah. Bahan ini merupakan pengoksidasi yang sangat kuat. Bila bereaksi dengan serbuk logam seperti alumunium, akan menimbulkan ledakan. Beberapa senyawa organik akan terbakar dengan sendirinya bila berkontak dengan bahan ini. Transportsai bahan ini membutuhkan label : 'pengoksidasi'.
Seperti halnya metal khlorat, maka metal-metal perkhlorat digunakan untuk kebutuhan yang hampir bersamaan, terutama yang berkaitan dengan penimbulan api dan ledakan. Namun bahan ini relatif lebih stabil dibanding bahan- bahan sebelumnya serta tidak menimbulkan reaksi yang prematur. Walaupun demikian, pengangkutan bahan ini pada kontainer pengangkutnya membutuhkan label : 'pengoksidasi'.
Senyawa-senyawa Amonium:
Pada dasarnya semua senyawa yang mengandung ion amonium (NH4+) secara
termal tidaklah stabil. Bila dipanaskan, senyawa ini akan terdekomposisi dengan dua jalan, yaitu :
- senyawa-senyawa amonium yang bukan agen-agen pengoksidasi terdekomposisi membentuk amonium, misalnya amonium khlorida yang secara termal terdekomposisi pada temperatur kurang dari 167 o C membentuk amonia dan hidrogen khlorida, - senyawa-senyawa amonium yang merupakan agen-agen pengoksidasi dapat juga
terdekomposisi membentuk amonia; tetapi lebih umum akan membentuk nitrogen, oksigen dan oksida-oksida metalik dan non metalik.
Senyawa-senyawa amonium merupakan senyawa yang sering dijumpai. Amonium sulfat merupakan pupuk yang paling sering digunakan dibanding senyawa amonium yang lain. Namun secara komersial, amonium nitrat dianggap sebagai yang paling penting diantara senyawa
amonium yang lain, baik sebagai pupuk maupun sebagai komponen bahan peledak.
Amonium nitrat berpotensi menimbulkan resiko ledakan. Pada temperatur 80o ke 93 o
amonium nitrat terdekomposisi membentuk amonia dan asan nitrat, yang berlangsung secara endotermis :
NH4NO3(s)⇒NH3(g)+HNO3
Pada temperatur sekitar 166 o C, amonium nitrat akan meleleh. Pada saat ini bahaya kebakaran dan ledakan akan besar bila senyawa ini tetap berada pada kondisi
temperatur tinggi. Bila temperatur di atas 212 o C, amonium nitrat akan terdekompiosisi membentuk dinitrogen oksida dan uap air yang berlangsung secara eksotermis :
NH4NO3(g)⇒N2O(g)+2N2O(g)
Bila pada saat pengangkutan bahan ini berada pada kontainer yang tertutup rapat, maka ledakan tidak dapat dihindari, api dapat berkobar yang didukung oleh adanya N2O
sebagai pengganti oksigen udara. Beberapa senyawa dikenal mempunyai peranan sebagai katalis dalam menaikkan laju dekopmposisi amonium ini, misalnya senyawa yang
mengandung tembaga, sulfur. Pengangkutan dan pewadahan bahan ini membutuhkan label : 'pengoksidasi'.
Oksidator Mengandung Khrom:
Khrom pada tingkat oksidasi +6 terdapat dalam bentuk senyawa logam khromat, logam
dikhromat, khrom trioksida dan khromilkhlorida. Pada kondisi sebagai ion-ion metalik tidak berwarna, sebagai khromat akan berwarna kuning dan sebagai dikhromat akan berwarna oranye.
Dikhromat metalik, seperti kalium dikhromat (K2Cr2O4) merupakan oksidator yang kuat,
terutama bila berada dalam larutan asam. Oksidator ini banyak digunakan dalam industri elektropalting khrom, pewarnaan dan
percetakan, komponen bahan peledak dan sebagainya.
Asam-asam yang berkaitan dengan khromat dan dikhromat hanya ada pada kondisi larutan. Bila air diuapkan darinya, maka yang tersisa adalah oksida khrom (VI) yang dikenal sebagai khromium trioksida, atau khromium anhidrid atau asam khromik dengan formula (CrO3).