STUDI PEMBUATAN TABLET ISONIAZID DENGAN PENGGUNAAN CORN STARCH®(SHIN DONG BANG) SEBAGAI BAHAN PENGIKAT
TABLET SECARA GRANULASI BASAH DAN EVALUASI TABLET
SKRIPSI
OLEH: THAHURA ALI
NIM 060824007
STUDI PEMBUATAN TABLET ISONIAZID DENGAN PENGGUNAAN CORN STARCH®(SHIN DONG BANG) SEBAGAI BAHAN PENGIKAT
TABLET SECARA GRANULASI BASAH DAN EVALUASI TABLET
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH: THAHURA ALI
NIM 060824007
FAKULTAS FARMASI
PENGESAHAN SKRIPSI
STUDI PEMBUATAN TABLET ISONIAZID DENGAN PENGGUNAAN CORN STARCH®(SHIN DONG BANG) SEBAGAI BAHAN PENGIKAT
TABLET SECARA GRANULASI BASAH DAN EVALUASI TABLET
OLEH: THAHURA ALI
NIM 060824007
Dipertahankan di hadapan Panitia Penguji Fakultas farmasi
Universitas Sumatera Utara Pada tanggal: Maret 2010
Pembimbing I, Panitia Penguji,
Drs.Agusmal Dalimunthe,Ms, Apt.
NIP 195406081983031005 NIP 130672239
Dra. Juanita Tanuwijaya, Apt
Pembimbing II, Drs.Agusmal Dalimunthe,Ms, Apt. NIP195406081983031005
NIP 194811111976031003 Drs.Syafrudin,Ms,Apt.
NIP 194810031987012001 Dra. Salbiah, MSi, Apt
NIP 196106191991031001 Drs. Suryanto, MSi, Apt.
Medan, Maret 2010 Fakultas Farmasi Universitas Sumatera Utara
ABSTRAK
Telah dilakukan penelitian pemanfaatan pati jagung cornstarch® sebagai bahan pengikat pada pembuatan tablet secara granulasi basah. pati jagung Corn starch® yang digunakan adalah pati jagung yang telah tersedia dipasaran dengan merek dagang Shin Dong Bang. Variasi corn starch yang digunakan sebagai bahan pengikat adalah 7.5%, 8.75%, 10%, 11.25%, 12.5%, dan 13.75%. Dan sebagai pembanding digunakan amilum manihot 11.25 % dan tepung jagung 11.25%.
ABSTRACT
Utilization of research has been done cornstarch® as a binder in the manufacture of tablets by wet granulation. Corn starch is used corn starch® has been available in the market come with a trademark Shin Dong Bang. Variations corn starch used as binder is 7.5%, 8.75%, 10%, 11.25%, 12.5%, and 13.75%.. And the comparison is used starch manihot 11.25% and 11.25% corn flour.
KATA PENGANTAR
Puji dan syukur kehadirat Allah S.W.T, atas nikmat dan karunia-Nya yang tak terhingga yang senantiasa dilimpahkan-Nya kepada penulis. Shalawat berangkaikan salam kepada junjungan Nabi Muhammad S.A.W. yang selalu
menjadi teladan bagi penulis untuk dapat melakukan amal dan perbuatan terbaik dalam hidup ini, sehingga penulis dapat menyelesaikan skripsi yang berjudul “
Studi pembuatan tablet isoniazid dengan penggunaan corn starch®(Shin Dong Bang) sebagai bahan pengikat tablet secara granulasi basah dan evaluasi tablet”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana
Farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Salah satu bahan pembuatan tablet adalah adalah bahan pengikat. Tujuan
penelitian ini adalah untuk mengetahui pati jagung (Corn Starch®) dapat digunakan sebagai bahan pengikat pada tablet . Ternyata pati jagung (Corn Starch®) dapat digunakan sebagai bahan pengikat pada tablet .
Pada kesempatan ini penulis menyampaikan terima kasih yang sebesar-besarnya kepada Bapak Drs.Agusmal Dalimunthe,Ms.Apt, serta Bapak Drs.
Syafrudin, Ms.Apt yang telah membimbing dengan penuh kesabaran, tulus dan ikhlas selama penelitian dan penulisan skripsi ini berlangsung. Ucapan terima kasih juga disampaikan kepada Dekan Fakultas Farmasi Universitas Sumatera
Utara, Prof. Dr. Sumadio Hadisahputra, Apt, yang telah memberikan bantuan dan fasilitas selama masa pendidikan.
jerman), abang (Budi, Latief), kakak (Ulfa, Lady), adik (Hidayah), dan keluarga
angkat penulis, atas doa, dorongan, dan pengorbanan baik moril maupun materil dalam penyelesaian skripsi ini, dan tidak lupa penulis ucapkan banyak terima kasih kepada Dra. Sudarmi. Msi, Apt selaku pembimbing akademik penulis,
Bapak dan Ibu dosen yang telah memberikan pengajaran kepada penulis, serta teman-teman (Bang Sidiq, yani, mak’drey, mak’cut, k’adek, sandra, mute, pasri,
bunga, eki, kak’wi, BR, pasri, timeh, mery dan teman-teman ekstensi farmasi 2006) yang telah membantu penulis dalam menyelesaikan skripsi ini.
Medan, Maret 2010 Penulis,
DAFTAR ISI
halaman
JUDUL ... i
HALAMAN PENGESAHAN ... i
KATA PENGANTAR ... ii
ABSTRAK ... iv
ABSTRACT ... v
DAFTAR ISI ... vi
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xii
Bab I. Pendahuluan ... 1
1.1. Latar belakang ... 1
1.2. Perumusan masalah ... 4
1.3. Hipotesis ... 4
1.4. Tujuan penelitian ... 4
Bab II. Tinjauan Pustaka 2.1. Uraian Pati jagung ... 6
2.2. Klasifikasi Tanaman Jagung ... 6
2.3. Pengertian Tablet ... 7
2.4. Komposisi Tablet ... 8
3.5. Disolusi ... 9
3.7. Isoniazid ... 10
Bab III. Metodologi Penelitian ... 11
3.1. Alat... 11
3.2. Bahan ... 11
3.3. Pembuatan pereaksi ... 11
3.3.1. Pembuatan HCl 0,1 N ... 11
3.4. Pembuatan tablet isoniazid ... 12
3.5. Pembuatan granul isoniazid... 14
3.6. Uji preformulasi ... 4
3.6.1. Sudut diam ... 14
3.6.2. Waktu alir ... 15
3.6.3. Indeks tap ... 15
3.7. Evaluasi tablet... 16
3.7.1. Pemeriksaan bentuk dan rupa ... 16
3.7.2. Pemeriksaan kekerasan tablet ... 16
3.7.3. Pemeriksaan friabilitas ... 16
3.7.4. Pengujian daya serap air (Water Uptake) dari tablet ... 17
3.7.5. Pemeriksaan waktu hancur ... 18
3.8. Penetapan kadar tablet Isoniazid ... 18
3.8.1. Pembuatan larutan induk baku ... 18
3.8.2. Pembuatan kurva serapan dalam air suling ... 18
3.8.5. Pemeriksaan keseragaman sediaan... 20
3.9. Uji disolusi……… 21
3.9.1. Pembuatan larutan induk baku ... 22
3.9.2. Pembuatan kurva serapan dalam HCl 0,1 N………… 23
3.9.3. Pembuatan kurva kalibrasi dalam HCl 0,1 N ... 24
3.9.4. Pengujian disolusi tablet isoniazid.. ... 25
Bab IV. Hasil dan Pembahasan ... 24
4.1. Hasil uji preformulasi terhadap massa granul ... 24
4.1.1. Uji waktu alir ... 25
4.1.2. Uji sudut diam ... 26
4.1.3. Uji indeks tap ... 27
4.2. Hasil evaluasi tablet ... 28
4.2.1. Hasil pembuatan kurva serapan dan kurva kalibrasi isoniazida BPFI serta Penetapan kadar isoniazida dalam tablet... ... 28
4.2.2. Keragaman bobot ... 30
4.2.3. Kekerasan tablet ... 31
4.2.4 Friabilitas... 32
4.2.5. Waktu hancur... 33
4.3. Uji daya serap Air (Water Uptake)... ... 35
4.4. Uji disolusi Tablet... 36
Bab V. Kesimpulan dan Saran ... 41
5.1. Kesimpulan... 41
5.2. Saran ... 41
DAFTAR TABEL
Tabel 1. Formula resep tablet isoniazid ... 13
Tabel 2. Kriteria penerimaan uji disolusi ... 23
Tabel 3. Data uji preformulasi massa granul ... 24
Tabel 4. Hasil penetapan kadar tablet isoniazid ... 29
Tabel 5. Data hasil evaluasi tablet ... 31
Tabel 6. Data uji daya serap air ( Water Uptake) dari tablet ... 35
DAFTAR GAMBAR
Gambar 1 Waktu alir ... 25
Gambar 2. Sudut diam ... 26
Gambar 3. Indeks tap ... 27
Gambar 4. Kurva serapan isoniazida BPFI dalam pelarut air suling ... 28
Gambar 5. kurva kalibrasi isoniazid BPFI dalam pelarut air suling ... 29
Gambar 6. Kekerasan tablet... 32
Gambar 7. Friabilitas ... 33
Gambar 8. Waktu hancur... 34
Gambar 9. Kurva serapan isoniazida BPFI dalam pelarut HCL 0,1 N ... 37
Gambar 10. Kurva kalibrasi isoniazid BPFI dalam pelarut HCL 0,1 N ... 31
DAFTAR LAMPIRAN
Lampiran 1. Contoh perhitungan pembuatan Tablet Isoniazid ... 44 Lampiran 2. Contoh perhitungan friabilitas Tablet ... 46 Lampiran 3. Hasil pembuatan kurva serapan isoniazid BPFI dalam
pelarut air suling ... 47 Lampiran 4. Hasil pembuatan kurva kalibrasi dan persamaan regresi
isoniazid BPFI dalam pelarut air suling ... 48 Lampiran 5 Contoh perhitungan kadar tablet isoniazid ... 50 Lampiran 6. Contoh perhitungan keragaman bobot ... 53
Lampiran 7. Hasil pembuatan kurva serapan isoniazid BPFI dalam
pelarut HCl 0.1 N ... 56
Lampiran 8. Hasil pembuatan kurva kalibrasi dan persamaan regresi
isoniazida BPFI dalam pelarut HCl 0,1 N ... 57 Lampiran 9. Contoh perhitungan hasil uji disolusi tablet ... 59
Lampiran 10. Hasil penetapan kadar tablet isoniazid pada berbagai
perbandingan formula tablet ... 60
Lampiran 11. Gambar modifikasi alat pengujian daya serap air
ABSTRAK
Telah dilakukan penelitian pemanfaatan pati jagung cornstarch® sebagai bahan pengikat pada pembuatan tablet secara granulasi basah. pati jagung Corn starch® yang digunakan adalah pati jagung yang telah tersedia dipasaran dengan merek dagang Shin Dong Bang. Variasi corn starch yang digunakan sebagai bahan pengikat adalah 7.5%, 8.75%, 10%, 11.25%, 12.5%, dan 13.75%. Dan sebagai pembanding digunakan amilum manihot 11.25 % dan tepung jagung 11.25%.
ABSTRACT
Utilization of research has been done cornstarch® as a binder in the manufacture of tablets by wet granulation. Corn starch is used corn starch® has been available in the market come with a trademark Shin Dong Bang. Variations corn starch used as binder is 7.5%, 8.75%, 10%, 11.25%, 12.5%, and 13.75%.. And the comparison is used starch manihot 11.25% and 11.25% corn flour.
BAB I PENDAHULUAN 1.1 Latar Belakang
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa
bahan pengisi. Berdasarkan metode pembuatan, dapat digolongkan sebagai tablet cetak dan kempa. Selain bahan pengisi digunakan juga zat tambahan lain yang
berfungsi sebagai zat pengembang, pengikat, pelicin, pembasah atau zat lain yang cocok (Ditjen POM,1995).
Dewasa ini, sediaan tablet semakin popular pemakaiannya dan merupakan
sediaan yang paling banyak diproduksi. Tablet merupakan salah satu sediaan yang banyak mengalami perkembangan dari segi formulasi. Beberapa keuntungan
sediaan tablet diantaranya adalah sediaan lebih kompak, biaya pembuatannya lebih murah, dosisnya tepat, mudah pengemasannya, sehingga penggunaannya lebih praktis jika dibandingkan dengan sediaan lain (Lachman et, al, 1994).
Beberapa keunggulan tablet adalah: Biaya produksinya paling murah, bentuk sediaan oral yang paling ringan dan paling kompak, mudah dan murah
untuk dikemas dan dikirim, mudah untuk diproduksi secara besar - besaran ,memiliki sifat pencampuran kimia, mekanik dan stabilitas mikrobiologi yang paling baik (Lachman et, al, 1994).
Tablet yang dinyatakan baik harus memenuhi syarat sebagai berikut : Harus merupakan produk menarik (bagus dilihat) yang mempunyai identitasnya
mempertahankan kelengkapan fisiknya sepanjang waktu. Dari segi lain tablet
harus dapat melepaskan zat aktifnya kedalam tubuh dengan cara yang dapat diramalkan serta tetap dapat diulang, stabil secara kimia sepanjang waktu sehingga tidak memungkinkan terjadinya penurunan mutu zat berkhasiatnya
(Lachman et al, 1994).
Isoniazid (piridina-4-karboksil-hidrazida) mempunyai berat molekul
137,14 merupakan hablur tidak berwarna atau serbuk hablur putih, tidak berbau dan mempunyai rasa yang agak pahit, dapat terurai perlahan-lahan dengan adanya udara dan cahaya. Kelarutannya mudah didalam air akan tetapi agak sukar larut di
dalam etanol, kloroform dan eter, yang berkhasiat sebagai anti -tuberkulosis (Ditjen POM, 1995).
Bahan pengikat dalam formulasi tablet adalah untuk mengikat komponen-komponen tablet untuk dijadikan granul dengan ukuran yang sama dan bentuk yang spheris setelah dipaksakan melewati ayakan. Dengan adanya
bahan pengikat, komponen tablet akan mudah dibentuk menjadi granul, sehingga akan memudahkan pencetakan. Pemilihan bahan pengikat
bergantung kepada sifat fisika dan kimia dari bahan obat, daya ikat yang diperlukan dan tujuan pemakaian obatnya (Soekemi, 1987).
Banyak peneliti melaporkan bahwa jenis pati dari berbagai tanaman dapat
dimanfaatkan sebagai substitusi bahan-bahan pembantu yang telah dikenal dalam formulasi tablet, pencarian bahan-bahan baru yang dapat digunakan sebagai bahan
Jagung relatif mudah di dapat karena tanaman jagung dibudidayakan di
daerah tropis seperti Indonesia. Jagung berperan penting dalam perekonomian nasional dengan berkembangnya industri pangan yang ditunjang oleh teknologi budi daya dan varietas unggul, untuk memenuhi kebutuhan dalam negeri yang
terus meningkat, Indonesia mengimpor jagung hampir setiap tahun. Pada tahun 2000, impor jagung mencapai 1,26 juta ton (BPS, 2005).
Selain untuk pengadaan pangan dan pakan, jagung juga banyak digunakan industri makanan, minuman, kimia, dan farmasi. Berdasarkan komposisi kimia dan kandungan nutrisi,pati jagung mempunyai prospek sebagai
pangan dan bahan baku industri. Pemanfaatan jagung sebagai bahan baku industri akan memberi nilai tambah bagi usaha tani komoditas tersebut (Suarni et al.
2005).
Oleh karena itu peneliti tertarik mencoba, apakah pati jagung merek Corn starch® ini dapat digunakan sebagai bahan pengikat pada pembuatan obat secara
1.2. Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut:
a. Apakah pati jagung (Corn starch®) dapat digunakan sebagai bahan
pengikat pada pembuatan tablet Isoniazid secara granulasi basah?
b. Berapakah rentang konsentrasi pati jagung (Cornstarch®) yang
dapat digunakan sebagai bahan pengikat pada pembuatan tablet secara granulasi basah.
1.3. Hipotesis
Berdasarkan perumusan masalah diatas, maka yang menjadi hipotesis dalam penelitian ini adalah :
a. Pati jagung (Corn starch®) dapat digunakan sebagai bahan pengikat dalam pembuatan tablet Isoniazid secara granulasi basah.
b. Konsentrasi pati jagung (Corn starch®) yang dapat digunakan sebagai bahan pengikat pada pembuatan tablet secara granulasi
basah adalah sekitar 7,5%-13,75%
1.4. Tujuan Penelitian.
Berdasarkan hipotesis diatas, maka yang menjadi tujuan dalam penelitian
ini adalah :
a. Untuk menggunakan pati jagung (Cornstarch®) sebagai bahan
b. Untuk mengetahui berapa konsentrasi optimum dari pati jagung
BAB II
TINJAUAN PUSTAKA 2.1. Uraian Pati Jagung
Pati adalah karbohidrat yang terjadi dari rangkaian molekul panjang yang
berbentuk butiran. Pati dapat diperoleh dari berbagai bagian tanaman seperti biji, umbi, batang, dan buah. Pati dalam jaringan mempunyai bentuk butir yang
berbeda-beda. Umumnya butir pati terdiri dari lapisan-lapisan yang mengelilingi suatu titik yang disebut hillum. Hillum dapat terletak ditengah atau dapat pula di pinggir (Fahn, 1992).
Biji jagung mengandung pati 54,1-71,7%. Karbohidrat pada jagung sebagian besar merupakan komponen pati, sedangkan komponen lainnya adalah
pentosa, dekstrin, sukrosa, dan gula pereduksi (Fahn, 1992).
Granul pati utuh tidak larut dalam air dingin. Granul pati dapat menyerap air dan membengkak, tetapi tidak dapat kembali seperti semula. Air yang terserap
dalam molekul menyebabkan granul mengembang. Apabila granul pati ditambahkan air panas atau dingin yang kemudian dipanaskan, maka pati dapat
mengalami gelatinasi, yaitu pati mengembang secara luar biasa(Winarno,1995)
2.2. Klasifikasi tanaman jagung Divisio : Spermatophyta Sub-divisio : Angiospermae Klass : Monocotyledoneae Ordo : Graminae
Famili : Graminaceae Genus : Zea
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa
bahan pengisi. Sebagian besar tablet dibuat dengan cara mengempaan dan merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan
cetakan baja. Tablet di buat dengan berbagai ukuran, bentuk dan penandaan permukaan tergantung pada desain cetakan (Ditjen POM, 1995).
Tablet dibuat dengan 3 cara umum yaitu : Granulasi basah, granulasi kering dan cetak langsung. Tujuan granulasi basah dan kering adalah untuk meningkatkan aliran campuran dan atau kemampuan kempa. Granulasi kering
dibuat dengan cara menekan massa serbuk pada tekanan tinggi sehingga menjadi tablet yang besar kemudian digiling dan diayak hingga diperoleh granul dengan
ukuran partikel yang diinginkan(Ditjen POM,1995).
2.4. Komposisi Tablet
Komposisi umum dalam tablet ádalah : 1. Zat berkhasiat.
2. Bahan pengisi : ditambahkan untuk mendapatkan berat yang diinginkan. 3. Bahan pengikat : ditambahkan untuk mengikat komponen-komponen
tablet untuk dijadikan granul dengan ukuran yang sama dan betuk spheris setelah dipaksakan melewati ayakan. Dengan adanya bahan pengikat, componen tablet akan mudah dibentuk menjadi granul, sehingga akan
memudahkan didalam pencetakkan.
4. Bahan pengembang : ditambahkan untuk memecahkan tablet menjadi
5. Bahan pelicin : ditambahkan dengan maksud untuk meningkatkan daya
alir granul-granul pada corong pengisi, mencegah melekatnya massa pada punch dan die, dan mengurangi gesekan antara batir-butir granul dan mempermudah pengeluaran tablet dari die.
6. Zat pewrna : ditambahkan dengan maksud untuk memperindah tablet, membedakan dosis, spesifikasi dari pabrik, serta untuk mempermudah
pengawasan.
7. Zat pewangi dan pemanis : ditambahkan untuk menutupi bau dan rasa yang tidak enak, memberikan bau tertentu.
8. Adjuvants : ditambahkan antara lain sebagai anti oksidan.
9. Absorban : ditambahkan untuk melindungi bahan berkhasiat dari
pengaruh lembab, menghomogenkan distribusi zat berkhasiat, menghindari kebasahan akibat sifat dan kombinasi zat berkhasiat.
10. Bahan pembasah : ditambahkan untuk mempercepat hancurnya tablet (Soekemi, 1987).
2.5. Disolusi.
Disolusi (pelarutan) adalah proses dalam suatu pelarut. Saat sekarang ini
disolusi dipandang seabagai salah satu uji pengawasan mutu yang paling penting dilakukan pada sediaan farmasi. Pada uji disolusi dapat diketahui bahan obat dalam larutan dengan kecepatan yang seharusnya. Cepatnya obat atau tablet
melarut menentukan beberapa kadar bahan berkhasiat terlepas didalam tubuh. Karena itu laju larut berhubungan langsung dengan kemanjuran dari tablet dan
perbedaan bioavaibilitas dari berbagai formula (Lachman,et al,1994)
Spektrofotometer UV adalah pengukuran panjang gelombang dan
intensitas sinar ultraviolet yang diabsorbsi oleh sampel. Sinar ultraviolet berada pada panjang gelombang 200 – 400 nm. Panjang gelombang adalah jarak antara satu lembah dan satu puncak, sebagai sumber cahaya biasanya digunakan lampu
hidrogen atau deutrum untuk pengukuran uv.
Spektrofotometer uv memiliki sumber cahaya tunggal, dimana sinyal
pelarut dihilangkan terlebih dahulu dengan mengukur pelarut tanpa sampel, setelah itu larutan sampel diukur (Dachriyanus, 2004)
2.7. Isoniazid
Isoniazid (piridina-4-karboksil-hidrazida) mempunyai berat molekul 137,14 merupakan hablur tidak berwarna atau serbuk hablur putih, tidak berbau dan mempunyai rasa yang agak pahit, dapat terurai perlahan-lahan dengan adanya udara
dan cahaya. Kelarutannya mudah didalam air akan tetapi larut di dalam etanol, kloroform dan eter, berkhasiat sebagai anti -tuberkulosis
.
Rumus Bangun Isonazida ( Ditjen POM, 1995)
BAB III
METODOLOGI PENELITIAN 3.1. Alat
Alat yang digunakan dalam penelitian ini adalah Neraca listrik
(Sartorius), timbangan dan anak timbangan, thermometer, stopwatch, mortir dan stemfer, lemari pengering, modifikasi alat sudut diam, modifikasi alat uji waktu
alir, modifikasi alat uji water uptake, mesin pencetak tablet single punch (Ateliers), strong cobb hardness tester (Erweka), Disentegration tester (Erweka), Disolution tester (Erweka), spetrofotometer Ultraviolet (UV mini
1240-SHIMADZU), Roche friabilator (Erweka), dan Alat-alat gelas laboratorium.
3.2. Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah Isoniazida (PT. Brataco Chemica), Isoniazida (BPFI), pati jagung (Corn starch® ) (Shin dong
bang) ,Tepung jagung maizena ( Maizenaku® ) , asam klorida p.a. (E.Merck), air suling, magnesium stearat (PT. Brataco Chemica), talkum (PT. Brataco Chemica),
amilum manihot (PT. Brataco Chemica) , laktosa (PT. Brataco Chemica).
3.3. Pembuatan pereaksi 3.3.1. Pembuatan HCl 0,1 N
Sebanyak 8,5 ml asam klorida p.a diencerkan dengan air suling dan dicukupkan hingga garis tanda dalam labu ukur 1000 ml (Ditjen POM, 1995).
Pati jagung (corn starch®) digunakan sebagai bahan pengikat dengan
konsentrasi 7,5%, 8,75%, 10%, 11,25%, 12,5%, dan 13,75% ( formula 1-6) sedangkan pembanding digunakan amilum manihot dengan konsentrasi 11,25% (formula 7) dan tepung jagung 11,25% (formula 8), Tablet dibuat dengan bobot
250 mg dan penampang 9 mm. Contoh perhitungan pembuatan tablet dapat dilihat pada lampiran 1 halaman 44.
R/ Isoniazida 100mg Amilum manihot 5%
Mucilago amili % bervariasi
Talkum 1%
Mg. Stearat 1%
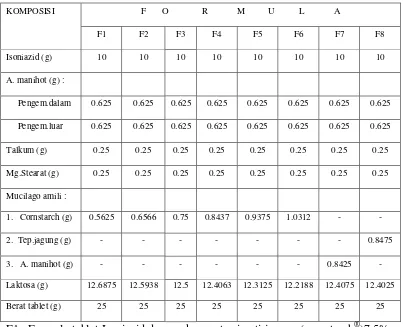
Tabel 1.Formula Resep Tablet Isoniazid Keterangan:
F1 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)7.5%
F2 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®) 8.75 %
F3 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)10 % F4 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)11.25%
F5 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)12.5%
F6 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)13.75%
F7 : Formula tablet Isoniazid dengan konsentrasi Amilum manihot 11.25 % F8 : Formula tablet Isoniazid dengan konsentrasi T.jagung (Maizenaku®)11.25 %
3.5. Pembuatan Granul isoniazid
KOMPOSISI F O R M U L A
F1 F2 F3 F4 F5 F6 F7 F8
Isoniazid (g) 10 10 10 10 10 10 10 10
A. manihot (g) :
Pengem.dalam 0.625 0.625 0.625 0.625 0.625 0.625 0.625 0.625
Pengem.luar 0.625 0.625 0.625 0.625 0.625 0.625 0.625 0.625
Talkum (g) 0.25 0.25 0.25 0.25 0.25 0.25 0.25 0.25
Mg.Stearat (g) 0.25 0.25 0.25 0.25 0.25 0.25 0.25 0.25
Mucilago amili :
1. Cornstarch (g) 0.5625 0.6566 0.75 0.8437 0.9375 1.0312 - -
2. Tep.jagung (g) - - - 0.8475
3. A. manihot (g) - - - 0.8425 -
Laktosa (g) 12.6875 12.5938 12.5 12.4063 12.3125 12.2188 12.4075 12.4025
Ditimbang semua bahan, Ditara cawan penguap dan batang pengaduk,
disuspensikan pati jagung dengan air dingin kemudian dipanaskan dengan api langsung sambil diaduk-aduk hingga diperoleh massa yang transparan. Mucilago yang terbentuk ditimbang kembali dan dicukupkan beratnya dengan menggunakan
air panas. Kedalam lumpang dimasukkan laktosa, amilum manihot(pengembang dalam), dan INH lalu digerus homogen. Dimasukkan mucilago amyli sedikit demi
sedikit sampai diperoleh massa yang kompak, dicatat berat mucilago yang terpakai, Massa diayak dengan ayakan mesh 12, dicatat berat granul basah, Granulat di tampung dan dikeringkan dalam lemari pengering pada suhu 40-60 C.
Setelah kering diayak pada ayakan mesh 14 dan ditimbang berat granulat kering , lalu ditambahkan Mg-Stearat, talkum dan pengembang luar, kemudian diaduk
sampai homogen, massa granul yang telah homogen diuji preformulasi, kemudian dicetak. Uji preformulasi yang dilakukan meliputi : sudut diam, waktu alir, dan
indeks tap.
3.6. Uji Preformulasi 3.6.1 Sudut Diam.
Granul sebanyak 100 gram dimasukkan kedalam corong yang telah dirangkai, permukaannya diratakan. Lalu penutup bawah corong dibuka, biarkan
granul mengalir sampai habis. Tinggi kerucut yang terbentuk diukur. Sudut diam diukur dengan rumus :
h = tinggi kerucut (cm)
Persyaratan : Uji dikatakan memenuhi syarat apabila berada pada 20° < O > 40°
(Cartensen, 1977).
3.6.2. Waktu Alir.
Uji waktu alir dilakukan menurut metode yang dibuat oleh Cartensen (1997). Granul sebanyak 100 gram dimasukkan kedalam corong yang telah dirangkai, kemudian permukaannya diratakan. Penutup bawah corong dibuka dan
secara serentak stopwatch dihidupkan. Stopwatch dihentikan saat granul telah habis melewati corong dan dicatat waktu alirnya. Menurut Guyot (1978), waktu
alir yang diperlukan oleh sejumlah serbuk untuk mengalir harus lebih singkat dari 10 detik.
3.6.3. Indeks Tap.
Kedalam gelas ukur 100ml, dimasukkan sejumlah granul hingga 100ml. Ditap dengan alat yang dimodifikasi sampai konstan. Setelah hentakan,
volumenya dihitung dengan rumus :
%
Dimana: VI = Volume sebelum hentakan
V2 = Volume setelah hentakan Granul akan mempunyai sifat alir yang baik jika mempunyai indeks tap <
20%.
3.7. Evaluasi Tablet.
Tablet diperiksa bentuk dan rupa secara visual. Tablet dinyatakan baik jika
permukaannya licin dan mengkilat.
3.7.2. Pemeriksaan Kekerasan Tablet.
Alat: Strong Cobb Hardness Tester (Erweka) Cara:
Sebuah tablet dimasukkan diantara anvil dan punch, tablet dijepit dengan cara memutar skrup pemutar sampai lampu stop menyala, ditekan knop tanda
panah kekanan sampai tablet pecah. Dan dicatat angka yang menunjukkan jarum penunjuk skala pada saat tablet pecah. Percobaan ini dilakukan untuk 5 tablet
Syarat: Kekerasan tablet antara 4-8 kg (Soekemi,dkk,1987).
3.7.3. Pemeriksaan Friabilitas.
Alat: Roche Friabiliator (Erweka).
Cara:
Ditimbang 20 tablet yang telah dibersihkan dari debu, dicatat beratnya (a gram), dimasukkan ke dalam alat (100 kali putaran), setelah batas waktu yang ditentukan tablet dkeluarkan dan dibersihkan dari debu, lalu ditimbang lagi (b
gram)
Friabilitas (F) = (a-b)/a xl00%.
Syarat: Kehilangan berat < 0,8% (Soekemi,dkk.1987).
3.7.4 Pengujian Daya serap Air (Water Uptake) dari Tablet.
Cara kerja:
1. Setelah alat dirangkai, dimasukkan air suling kedalam pipa U1, salah satu
ujung pipa U (yaituU2) disumbat dengan gabus, dimana ujung bawah dari
gabus empulur sejajar dengan permukaan ujung pipa U1.
2. Diletakkan kertas saring diatas gabus empulur yang ukurannya tepat sama dengan diameter. Setelah air merembes kedalam kertas saring,
ditambahkan air suling dari buret melalui ujung pipa U1 sehingga sejajar
dengan permukaan air pada ujung pipa U2 , dicatat skala penambahan air
suling tersebut.
3. Diletakkan tablet diatas ujung pipa U2 , diatasnya ditaburkan carmin.
4. Berkurangnya volume air suling dari garis tanda di cek setiap selang waktu
1 menit, dan pada saat tersebut ditambahkan air suling dari buret sampai garis tanda, dicatat skala penambahannya.
5. Pemeriksaan dilanjutkan sampai carmin menyebar pada permukaan tablet dan jumlah air suling yang terserap telah menjadi konstan ( kamp et al,
1986).
3.7.5. Pemeriksaan Waktu Hancur. Alat: Desintegration Tester (Erweka).
Dimasukkan 1 tablet pada dalam keranjang ,masukkan satu cakram pada tabung dan jalankan alat, digunakan air bersuhu 37º ± 2ºC. Sebagai media kecuali dinyatakan lain menggunakan cairan yang tercantum dalam masing-masing
keranjang dan amati semua tablet, semua tablet harus hancur sempurna. Bila 1 tablet
atau 2 tablet tidak hancur sempurna, ulangi pengujian dengan 12 tablet lainnya, tidak kurang 16 dari 18 tablet yang diuji harus hancur sempurna (Ditjen POM, 1995).
3.8. Penetapan kadar Tablet Isoniazida 3.8.1. Pembuatan larutan Induk Baku
Ditimbang 50 mg Isoniazida BPFI, dimasukkam ke dalam labu tentukur 100 ml, ditambahkan air suling, dikocok sampai larut dan ditambahkan air suling
sampai garis tanda konsentrasi teoritis adalah 500 mcg/ml ( LIB I ). Selanjutnya dipipet 10 ml dari LIB I, dimasukkan dalam labu tentukur 100 ml, dan dicukupkan dengan air suling sampai garis tanda, kemudian dikocok homogen
sehingga diperoleh larutan dengan konsentrasi teoritis 50 mcg/ml (LIB II).
3.8.2. Pembuatan kurva serapan
Dipipet sebanyak 6.5 ml dari ( LIB II ), lalu dimasukkan ke dalam labu
tentukur 25 ml, ditambahkan air suling sampai garis tanda kemudian dikocok homogen sehingga diperoleh larutan dengan konsentrasi teorotis 13 mcg/ml,
diukur serapannya pada panjang gelombang 200 – 400 nm.
3.8.3. Pembuatan Kurva kalibrasi
Dipipet LIB II sebanyak 3,5 ml; 5 ml; 6,5 ml; 8 ml; 9,5 ml; lalu
dimasukkan dalam labu tentukur 25 ml, dicukupkan dengan air suling sampai garis tanda. Dikocok homogen sehingga diperoleh larutan dengan konsentrasi teoritis 7 mcg/ml; 10 mcg/ml; 13 mcg/ml; 16 mcg/ml; 19 mcg/ml.Diukur
3.8.4. Penetapan kadar Isoniazida dalam tablet
Ditimbang 20 tablet, dicatat beratnya, kemudian digerus sampai homogen. Ditimbang sejumlah serbuk setara dengan 50 mg Isoniazid, kemudian dimasukkan ke dalam labu tentukur 100 ml, ditambahkan air suling, dikocok
homogen, dicukupkan dengan air suling sampai garis tanda, dihomogenkan dan disaring melalui kertas saring, filtrat pertama dibuang, filtrat selanjutnya
ditampung . Dari larutan dipipet 10 ml lalu dimasukkan kedalam labu tentukur 100 ml, dan diencerkan dengan air suling hingga garis tanda. Dari larutan ini, dipipet 6,5 ml kedalam labu tentukur 25 ml, ditambahkan air suling hingga
garis tanda. Lalu diukur serapan larutan pada panjang gelombang serapan maksimum yang diperoleh, dengan menggunakan air suling sebagai blanko,
pengerjaan ini dilakukan sebanyak 6 kali. Persyaratan: Menurut Farmakope Indonesia Edisi IV, tablet Isoniazid mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket (Ditjen POM,
1995).
3.8.5. Pemeriksaan Keseragaman Sediaan
Tablet yang dibuat adalah tablet Isoniazid dengan berat 1 tablet 250 mg
dan mengandung Isoniazida 100 mg. Menurut Farmakope Indonesia Edisi IV, bahwa kadar zat aktif 50 mg atau lebih besar dari 50 mg yang merupakan 50%
atau lebih dari bobot satuan sediaan maka uji keseragaman dilakukan dengan cara keragaman bobot.
Untuk penetapan keseragaman sediaan dengan cara keragaman bobot,
penetapan kadar, dihitung jumlah zat aktif dari masing-masing dari 10 tablet
dengan anggapan zat aktif terdistribusi homogen ( Ditjen POM, 1995).
Cara penetapan kadar:
Timbang 10 tablet, satu persatu, dan hitung bobot rata-rata. Penetapan kadar dilakukan dengan data: dari 10 tablet yang ditimbang. Di catat beratnya, kemudian digerus sampai homogen. Ditimbang seksama sejumlah serbuk setara
dengan lebih kurang 50 mg Isoniazid, kemudian dimasukkan dalam labu tentukur 100 ml, dicukupkan dengan air suling sampai garis tanda. Lalu dikocok hingga
homogen, disaring melalui kertas saring dan filtrat pertama dibuang, filtrate selanjutnya ditampung. Dari larutan ini dipipet sebanyak 10 ml larutan dan dimasukkan kedalam labu tentukur 100 ml, lalu dicukupkan dengan air suling
sampai garis tanda. Lalu dipipet kembali sebanyak 6,5 ml dan dimasukkan dalam labu tentukur 25 ml, kemudian dicukupkan dengan air suling sampai garis tanda.
Diukur serapannya pada panjang gelombang, dengan menggunakan air suling sebagai blanko, pengerjaan ini dilakukan sebanyak 6 kali.
Persyaratan : Tablet memenuhi syarat keseragaman sediaan jika jumlah zat
aktif dalam masing-masing dari 10 tablet tidak kurang dari 85,0% dan tidak lebih dari 115,0 % dari yang tertera pada etiket dan mempunyai simpangan
baku relatif kurang dari atau sama dengan 6,0% (Ditjen POM, 1995).
3.9. Uji Disolusi
3.9.1. Pembuatan Larutan Induk Baku dalam HCl 0,1 N
dicukupkan dengan HCl 0,1 N sampai garis tanda, konsentrasi teoritis
adalah 500 mcg/ml (LIB I). Selanjutnya dipipet sebanyak 10 ml dari LIB I lalu dimasukkan kedalam labu tentukur 100 ml lalu dicukupkan dengan HCl 0,1 N sampai garis tanda, kemudian dikocok hingga homgen sehingga diperoleh larutan
dengan konsentrasi teoritis 50 mcg/ ml ( LIB II ).
3.9.2. Pembuatan kurva serapan dalam HCI 0,1 N
Dipipet sebanyak 5,5 ml dari larutan baku lalu dimasukkan kedalam labu tentukur 25 ml dan ditambahkan medium disolusi hingga garis tanda, kemudian
dikocok homogen sehingga diperoleh larutan dengan konsentrasi teoritis 11 mcg/ml.Diukur pada panjang gelombang 200 – 400 nm dan sebagai blanko
digunakan HCI 0,1 N.
3.9.3. Pembuatan Kurva Kalibrasi
Dipipet LIB II sebanyak 3,5 ml, 4,5 ml, 5,5 ml, 6,5 ml, dan 7,5 ml, masing-masing dimasukkan kedalam labu tentukur 25 ml, dicukupkan dengan HCl 0,1 N sampai saris tanda. Dikocok homogen sehingga diperoleh
larutan dengan konsentrasi 7 mcg/ml, 9 mcg/ml, 11 mcg/ml, 13 mcg/ml, 15 mcg/ml.Diukur Serapannya pada panjang gelombang 267 nm.
3.9.4. Pengujian Disolusi Tablet Isoniazid
Medium : 900 ml larutan HCI 0,1 N
Alat : tipe –2
Kecepatan putaran : 100 rpm
Waktu : 45 menit prosedur:
disolusi, suhu 37° C ± 0,5° C. kemudian dayung diputar dengan kecepatan 100
rpm. Dalam interval waktu 5, 10, 15, 20, 25, 30, 35, 40, 45 menit, larutan dipipet
sebanyak 2,5 ml dan dimasukkan ke dalam labu tentukur 25 ml lalu diencerkan dengan HCI 0,1 N sampai garis tanda. Serapan diukur pada panjang gelombang maksimum dengan menggunakan HCI 0,1 N sebagai blanko. Volume
medium disolusi diusahakan tetap dengan menambahkan HCI 0,1 N dengan jumlah yang sama yang diambil. Syarat: Dalam waktu 45 menit harus larut tidak
kurang dari 80% (Q) C8H9NO2, dari jumlah yang tertera pada etiket. Interprestasi:
Persyaratan dipenuhi bila jumlah zat aktif yang terlarut dari sediaan yang diuji sesuai dengan tabel penerimaan. Lanjutkan pengujian sampai tiga tahap kecuali
bila hasil pengujian memenuhi tahap S1 atau S2. Harga Q adalah jumlah zat aktif yang terlarut seperti yang tertera dalam masing-masing monografi, dinyatakan
dalam persentase kadar pada etiket, angka 5% dan 15% dalam tabel adalah persentase kadar pada etiket, dengan demikian mempunyai arti yang sama dengan
Tabel 2. Kriteria Penerimaan Zat Aktif yang Larut dengan Disolusi
(Ditjen POM, 1995) S1 6 Tiap unit sediaan tidak kurang dari Q + 5%
S2 6 Rata-rata dari 12 unit (SI + S2) adalah sama dengan atau lebih besar dari Q dan tidak 1 unit sediaan yang lebih kecil dari Q – 15%.
S3 12
BAB IV
HASIL DAN PEMBAHASAN 4.1. Hasil uji Preformulasi Terhadap Massa Granul
Sebelum massa granul dicetak menjadi tablet umumnya harus melalui
serangkaian uji preformulasi. Hal penting dilakukan untuk mengetahui kelayakan pencetakan suatu tablet. Berikut tabel hasil uji preformulasi berbagai formula
yang dibuat.
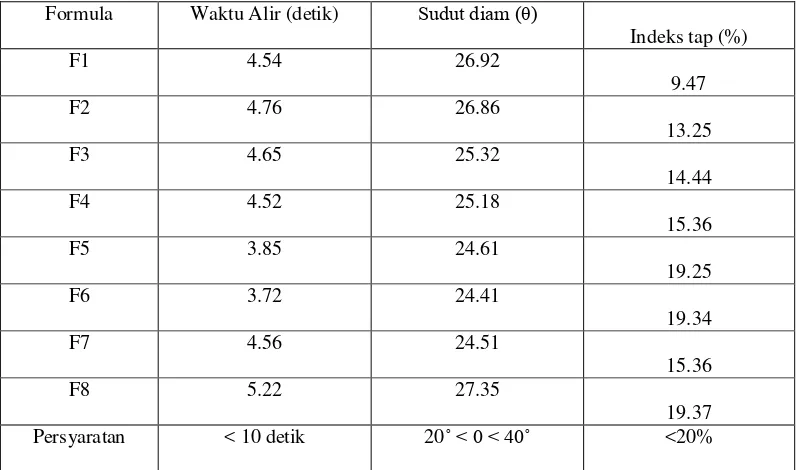
Tabel 3. Data Uji Preformulasi Massa Granul Formula Tablet Keterangan :
F1 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)7.5% F2 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®) 8.75 %
F3 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)10 %
F4 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)11.25% Formula Waktu Alir (detik) Sudut diam (θ)
F6 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)13.75%
F7 : Formula tablet Isoniazid dengan konsentrasi Amilum manihot 11.25 %
F8 : Formula tablet Isoniazid dengan konsentrasi T.jagung (Maizenaku®)11.25 %
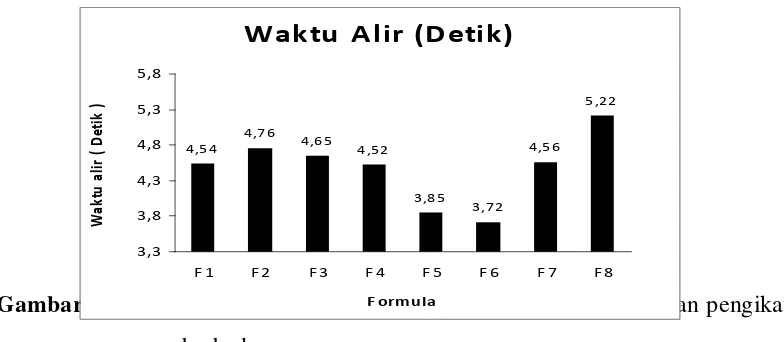
4.1.1 Uji Waktu Alir
Berdasarkan tabel 3 halaman 24, dapat dilihat bahwa waktu alir granul dengan bahan pengikat pati jagung (corn starch) dari formula F1 sampai
dengan formula F6 terjadi penurunan, mulai dari F1 = 4.54detik – F6 = 3,72 detik. Sedangkan pada formula pembanding amilum manihot menunjukkan
waktu alir 4,56 detik, sedangkan pati jagung 5,22 detik. Walaupun terjadi variasi waktu alir dari formula tersebut tetapi tetap masih berada dalam batas penerimaan. Granul dalam bentuk bulat dan permukaan halus akan lebih
mudah untuk mengalir (Cartensen, 1977).
Makin besar konsentrasi corn starch, maka makin cepat waktu alirnya. Hal ini disebabkan karena pati yang sudah berbentuk granul, massanya
semakin mudah mengalir yang menyebabkan waktu alir semakin cepat.
Gambar 1. Waktu alir massa granul dengan jenis dan persentase bahan pengikat yang berbeda.
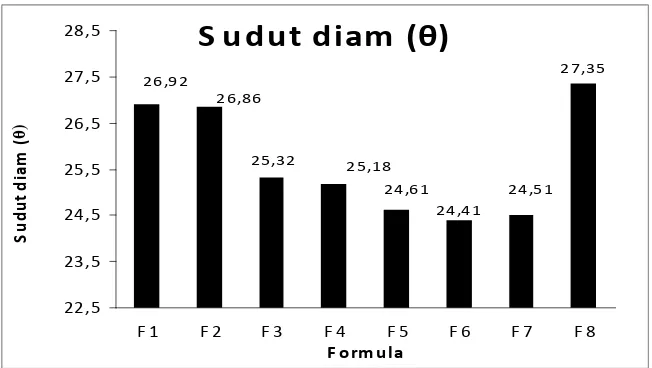
4.1.2 Uji Sudut Diam
S udut diam (θ)
Dari tabel 3 halaman 24, diatas juga menjelaskan bahwa penurunan sudut
diam dari formula F1 – formula F6 yaitu : 26,92-24,61. Sedangkan pada formula pembanding amilum manihot F7 menunjukkan sudut diam 24,51, sedangkan pada tepung jagung 27,35. Variasi sudut diam dari formula tersebut tidak jauh berbeda
dan masih berada dalam batas penerimaan. Hal ini merupakan suatu indikasi bahwa cornstarch memiliki efisiensi yang lebih baik dari pada tepung jagung.
Menurut (Cartensen, 1977), granul yang memiliki sifat free flowing mempunyai sudut diam yang lebih kecil dari 35. Partikel dengan bentuk yang lebih spheris
memberikan sudut diam yang lebih rendah (Lachman et al, 1989).
Hasil uji sudut diam memperlihatkan bahwa dengan penambahan konsentrasi pati jagung (corn strach) akan memperkecil sudut diam. Hal ini
disebabkan semakin banyak pati yang berbentuk granul akan mempunyai daya alir
yang baik.
In d eks T ap (%)
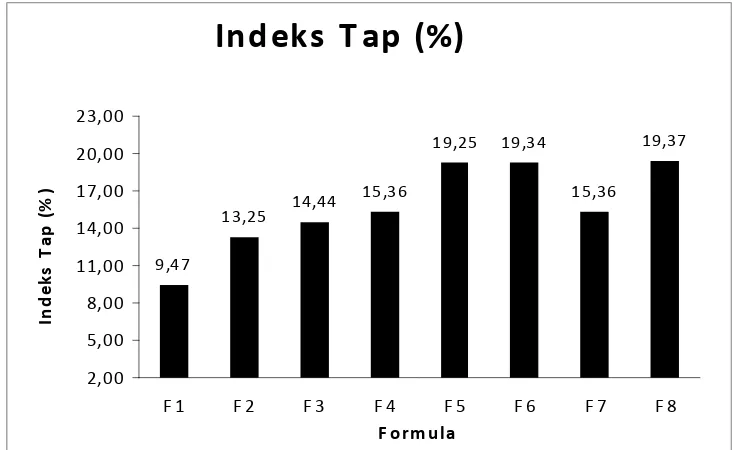
Dari tabel 3 halaman 24, Menjelaskan besarnya indeks tap dari
masing-masing formula F1 memiliki indeks tap sebesar 9,47%, formula F2 sebesar 13,25%, formula F3 sebesar 14,44%, formula F4 sebesar 15,36%, formula F5 sebesar 19,25%, formula F6 sebesar 19,34%, formula F7 sebesar 15.36%, formula
F8 sebesar 19,37%. Menurut (Guyot, 1978), granul yang bersifat mengalir bebas adalah partikel yang memiliki indeks tap < 20 %. Pengujian indeks tap memiliki
peran yang sangat penting dalam hal gambaran daya tahan granul terhadap daya kompressi yang diberikan oleh alat pencetak tablet. Semakin rendah persentase indeks tap menunjukkan kualitas yang lebih baik dari sifat fisis massa granul yang
akan di formulasikan kedalam bentuk tablet. Semakin tinggi konsentrasi pati jagung (Corn starch) yanh digunakan, maka indeks tap semakin tinggi juga, ini
dikarenakan semakin banyaknya pati yang berbentuk granul.
Gamba r 3. Indeks tap massa Granul dengan jenis dan persentase bahan pengikat yang berbeda.
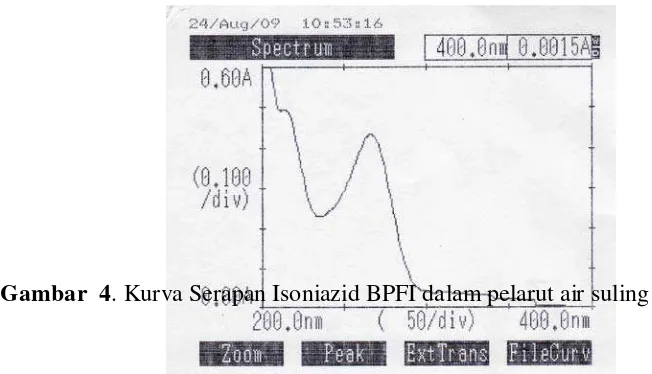
4.2.1 Hasil Pembuatan Kurva Serapan dan Kurva Kalibrasi Isoniazida BPF1 serta Penetapan kadar Isoniaid dalam Tablet.
Hasil pengukuran secara spektrofotometri ultraviolet BPFI dalam larutan. Dimana diperoleh serapan maksimum pada panjang gelombang 267 nm dengan
serapan 0.4300(Lampiran 3, halaman 47), ini sesuai dengan identifikasi spektrum Ultraviolet larutan Isoniazid BPFI dalam air pada panjang gelombang 200-400
nm diperoleh panjang gelombang maksimum yaitu 265 nm. Hal ini sesuai dengan pernyataan dalam Farmakope Indonesia Edisi IV yang menyatakan bahwa suatu penetapan atau pengujian mengenai panjang gelombang, serapan maksimum
mengandung implikasi bahwa maksimum tersebut tepat pada atau dalam batas 2 nm dari panjang gelombang yang ditentukan. Hasil pembuatan kurva serapan
dapat dilihat pada gambar 4.
NO FORMULA KADAR RATA - RATA (%)
1 F1 102.99 ±0.60
2 F2 102.78±0.52
3 F3 101.92±0.63
4 F4 101.60±0.68
5 F5 101.92±0.63
6 F6 100.35±0.82
7 F7 101.58±0.69
8 F8 102.97 ±0.61
Gambar 5. Kurva kalibrasi Isoniazida BPFI dalam pelarut air suling
Gambar 5 adalah gambar kurva kalibrasi Isoniazid dalam pelarut air suling pada panjang gelombang 267 nm. Pada penentuan kurva kalibrasi larutan,
Isoniazida BPFI dibuat konsentrasi berturut-turut ; 7 mcg/ml; 10 mcg/ml; 13 mcg ml; 16 mcg/ml; 19 mcg/ml, dapat dilihat pada lampiran 4 halaman 48 Diperoleh
persamaan regresi : Y = 0,032619X+0,001289 dengan nilai r = 0,9997
Tabel 4. Hasil penetapan Kadar Tablet Isoniazid
Keterangan :
F1 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)7.5%
F2 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®) 8.75 %
F3 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)10 %
F4 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)11.25% F5 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)12.5%
F6 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)13.75% F7 : Formula tablet Isoniazid dengan konsentrasi Amilum manihot 11.25 %
F8 : Formula tablet Isoniazid dengan konsentrasi T.jagung (Maizenaku®)11.25 %
Dari tabel 5 halaman 31, dapat dilihat bahwa keragaman bobot tablet
Isoniazid berkisar antara 99,54% hingga 101,57% dengan simpangan baku relatif antara 0,09% - 0,17%. Berdasarkan hal tersebut, maka keragaman bobot dari tablet Isoniazid memenuhi persyaratan yang ditetapkan oleh Farmakope
Indonesia edisi IV (1995) yaitu jika jumlah zat aktif dalam masing-masing dari 10 satuan sediaan terletak antara 85,0% hingga 115.0% dari yang tertera pada
etiket, atau jika simpangan baku relat if kurang dari atau sama dengan 6,0%. Dilihat berdasarkan hasil simpangan baku relatifnya, maka dapat
disimpulkan bahwa tablet yang tercetak memiliki keragaman bobot yang baik
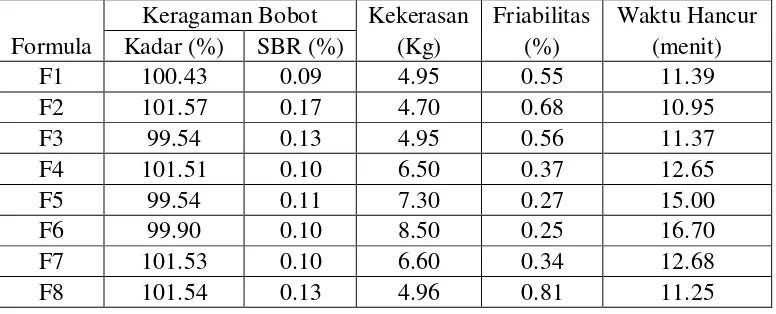
Tabel 5. Data Hasil Evaluasi Tablet
Keragaman Bobot Kekerasan Friabilitas Waktu Hancur Formula Kadar (%) SBR (%) (Kg) (%) (menit)
F1 100.43 0.09 4.95 0.55 11.39
F2 101.57 0.17 4.70 0.68 10.95
F3 99.54 0.13 4.95 0.56 11.37
F4 101.51 0.10 6.50 0.37 12.65
F5 99.54 0.11 7.30 0.27 15.00
Keterangan:
F1 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)7.5%
F2 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®) 8.75 % F3 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)10 %
F4 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)11.25% F5 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)12.5%
F6 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)13.75%
F7 : Formula tablet Isoniazid dengan konsentrasi Amilum manihot 11.25 %
F8 : Formula tablet Isoniazid dengan konsentrasi T.jagung (Maizenaku®)11.25 %
4.2.3 Kekerasan Tablet
Hasil uji kekerasan seperti yang terlihat pada tabel 5 halaman 31. menunjukkan bahwa kekerasan semakin menaik dengan meningkatnya konsentrasi cornstarch
yang ditambahkan pada tablet hingga pada konsentrasi 13,75%. yaitu FI<F2<F3<F4<F5<F6. Hal ini disebabkan karena kuatnya ikatan granul membentuk tablet sehingga tablet menjadi keras. Pada uji kekerasan yang
dilakukan pada F6, hasil yang diperoleh adalah 8.50 sehingga pada pengujian ini tablet pada F6 tidak memenuhi syarat, karena menurut Parrot (1971), kekerasan
tablet akan memenuhi syarat pada rentang 4-8 kg. Jika dibandingkan antara F4 (pati jagung cornstarch 11,25%) dengan F7 (amilum manihot 11,25%) dan F8 (tepung jagung Maizenaku 11,25%), kekerasan tablet yang
Grafik uji kekerasan (kg)
pati tetapi ia juga masih mengandung komposisi yang lain seperti lemak, sehingga
dapat mempengaruhi kekerasan pada tablet.
Gambar 6. Kekerasan Tablet dengan jenis dan Persentase Bahan pengikat yang berbeda.
4.2.4 Friabilitas
Friabilitas memberi gambaran terhadap ketahanan tablet terhadap benturan mekanis dalam masa pengangkutan dan pada saat
pengemasan.Nilai friabilitas yang besar menunjukkan kualitas tablet yang buruk. Menurut Voigt(1994), friabilitas (kehilangan bobot) dari
tablet yang diperbolehkan adalah≤ 0.8%.
Grafik Uji Friabilitas (%)
pada lampiran 2 halaman 49.
Gambar 7. Friabilitas Tablet dengan Jenis dan Persentase Bahan Pengembang yang Berbeda
4.2.5 Waktu Hancur
Berdasarkan data dari tabel 5 halaman 31, maka hasil pengujian waktu hancur terhadap tablet dapat diketahui di mana semakin menurun konsentrasi cornstarch yang digunakan maka semakin cepat waktu hancur tablet. Pada grafik
terlihat bahwa waktu hancur dari F4 dan F7 memiliki nilai yang hampir sama, F4 memiliki waktu hancur 12.65 dan F7 memiliki waktu hancur 12.68
dimana keduanya juga memiliki kekerasan yang hampir sama. Hal ini terjadi karena tablet dengan bahan pengikat cornstarch akan terkikis sedikit demi sedikit pada waktu pengujian, karena mengandung amilopektin yang sangat
besar dibandingkan amilosa, sedangkan tablet dengan bahan pengikat tepung jagung akan segera pecah menjadi partikel kasar hingga kemudian larut dalam
Grafik Waktu Hancur (menit)
Gambar 8. Waktu hancur Tablet dengan jenis dan persentase Bahan pengikat yang berbeda.
4.3. Uji Daya Serap Air (Water Uptake).
Tabel 6 Data Uji Daya Serap air (water uptake) dari tablet
Waktu Formula
18 0,20 0,20 0,22 0,26 0,25 0,25 0,25 0,22 19 0,22 0,24 0,26 0,25 0,23 0,25 0,22
20 0,26 0,25
21 0,26 0.26
22 0,26
Keterangan :
F1 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)7.5%
F2 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®) 8.75 %
F3 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)10 % F4 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)11.25%
F5 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)12.5%
F6 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)13.75% F7 : Formula tablet Isoniazid dengan konsentrasi Amilum manihot 11.25 %
F8 : Formula tablet Isoniazid dengan konsentrasi T.jagung (Maizenaku®)11.25 % Dari t abel 6 dapat dilihat bahwa konse nt rasi pati jagung
(cornstarch®) yang o pt imu m adalah pada konsentrasi 11,25%, yaitu dapat menyerap air sebanyak 0,26 ml ( jumlah ma k s imu m a ir ya ng d a p a t
d is e r a p t a b le t ) ha mp ir s a ma w a k t u n ya d e ng a n pembanding (amilum manihot 11,25%) Daya serap air juga dipengaruhi oleh kekerasan dimana dengan bertambahnya kekerasan tablet maka tablet memiliki daya serap
yang rendah sehingga waktu penyerapannya lama. Hal ini terjadi karena dengan meningkatnya kekerasan menyebabkan jumlah pori semakin
sedikit sehingga semakin sulit penetrasi air ke dalam tablet, makin lama waktu yang dibutuhkan untuk membasahi partikel. Daya serap air juga mempengaruhi waktu hancur, dimana dengan bertambahnya daya serap air
tablet menjadi semakin cepat.
4.4. Uji Disolusi tablet
3.4.1 Hasil pembuatan kurva serapan dan kurva kalibrasi Isoniazida BPFI dalam Pelarut HCL 0,1 N.
Isoniazid memberikan serapan maksimum pada panjang gelombang 266
dengan A
1
1 = 390a dalam pelarut asam (Moffat,1986). Oleh karena itu, isoniazid
dapat ditetapkan kadarnya dengan spektrofotometri ultraviolet.
Gambar 9. kurva serapan Isoniazida BPFI dalam pelarut HCl 0,1 N
Dari hasil identifikasi spectrum ultraviolet larutan Isoniazida BPFI dalam HCl 0.1 N diperoleh panjang gelombang 267 nm dengan serapan 0.4213,(
lampiran halaman 56) berdasarkan hal tersebut, nilai ini lebih tinggi sebesar 1 nm dibandingkan yang tertera pada Moffat (1986). Hal ini sesuai dengan pernyataan
0
Gambar 10. Kurva kalibrasi Isoniazid BPFI dalam pelarut HCL 0,1 N
4.4.2. Hasil Uji Disolusi isoniazida dalam sediaan tablet
Dari hasil uji disolusi tablet yang dapat dilihat pada tabel 7 halaman 39
dapat diketahui bahwa persen kumulatif Isoniazid yang terlarut pada menit ke-45 dari formula F1 104.48%, F2 sebesar 102.73%, F3 sebesar 100.31%, F4 sebesar 99,93%, F5 sebesar 88.50%, F6 sebesar 83,91%, F7 sebesar 99.87%,F8 sebesar
83,91%, ini menunjukkan bahwa formula pati jagung (cornstarch®) memenuhi persyaratan farmokope Indonesia edisi IV (1995), dimana dalam waktu 45 menit
harus larut tidak kurang dari 80% (Q) C8H9NO2, dari jumlah yang tertera pada
etiket.
Gambar 11. Persentase kumulatif Isoniazid yang terlepas Keterangan:
F3 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)10 %
F4 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)11.25%
F5 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)12.5%
F6 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)13.75%
F7 : Formula tablet Isoniazid dengan konsentrasi Amilum manihot 11.25 %
F8 : Formula tablet Isoniazid dengan konsentrasi T.jagung (Maizenaku®)11.25 %
Tabel 7 Hasil Uji Disolusi Tablet Isoniazida
Keterangan:
F1 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)7.5%
F2 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®) 8.75 % F3 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)10 %
F4 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)11.25%
F5 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)12.5%
F6 : Formula tablet Isoniazid dengan konsentrasi pati jagung (cornstarch®)13.75% F7 : Formula tablet Isoniazid dengan konsentrasi Amilum manihot 11.25 %
Waktu (Menit)
Persentase Kumulatif Isoniazida yang terlepas (%)
F1 F2 F3 F4 F5 F6 F7 F8
Dari tabel 7, dapat dilihat semakin tinggi konsentrasi corn starch yang digunakan
maka persentase kumulatif isoniazida yang terlepas (%), akan semakin kecil. Jika pati jagung corn starch 11, 25%, di bandingkan dengan tepung jagung dengan konsentrasi 11,25% dapat dilihat bahwa pati jagung (cornstarch®), isoniazid yang
terlepas lebih kecil dibandingkan tepung jagung, karena pati jagung (cornstarch®) komposisi seluruhnya adalah pati, yang amilopektin nya lebih besar, sehingga
pelepasan obatnya perlahan-lahan, sedangkan pada tepung jagung komposisi tidak seutuhnya pati, tapi juga mengandung komposisi lain seperti lemak, sehingga pelepasan obatnya lebih besar dibandingkan pati jagung (cornstarch®).
BAB V
KESIMPULAN DAN SARAN 5.1. Kesimpulan
a. Pati jagung (Cornstarch®) dapat digunakan sebagai bahan pengikat pada
pembuatan tablet dengan cara granulasi basah
b. Pati jagung (Cornstarch®) dapat digunakan sebagai bahan pengikat tablet
5.2. Saran
Disarankan pada peneliti selanjutnya untuk meneliti Pati jagung (Cornstarch®) yang dapat digunakan sebagai bahan pengembang tablet secara
granulasi basah, atau dengan memodifikasi pati jagung secara fisika kimia.
DAFTAR PUSTAKA
BPS (2005). Statistik Indonesia. Statistics Indonesia and Directorat General of Food crops. Jakarta Halaman 21-23.
Cartensen. J.T. (1977). Pharmaceutical of solid dosage form. New York : A.wiley Interscience Publication John Wiley and son. Page. 133-135,154-159, 216-218.
Ditjen POM (1979).Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Halaman 404, 748 dan 755.
Ditjen POM (1995). Farmakope Indonesia. Edisi IV.Jakarta: Departemen
Spektroskopi. Cetakan Pertama, Padang : Andalas University Press. Halaman 3.
Fahn.J. (1992). Teknologi pengolahan jagung untuk menunjang agroindustri pedesaan, Makalah Simposium Penelitian Tanaman Pangan III. Jakarta/Bogor, 23-25 Agustus 1993. Puslitbangtan,Bogor.
Guyot. J.G (1978). Critere Technology Des Choix Des Compression Direct. Dalam Dalimunte. A (1990). Tesis. Pengaruh Laktosa sebagai Pengisi Tablet Yang Dibuat Dengan Metode Cetak Langsung.
Hartono.S. (2007).Modifikasi pati jagung (Zea mays L.). Cetakan Pertama. Bogor: Institut Pertanian Bogor Press. Halaman 79.
Kamp.H.V, Bolhuis G.K, Lerk.C.F (1986). The Role of Water Uptake on Tablet Disintegration. Nedherland: State University of Gronigen. Pages 3-6.
Katzung, B.G (2004). Farmakologi Dasar dan klinik. Edisi Pertama, Jakarta : salemba Medika. Halaman 96.
Lachman.L Lieberman, H.A,Kanig.J.L (1994). Teori dan Praktek Farmasi Industri. Edisi Ketiga. Jakarta: UI Press. Halaman 654 dan 697
Moffat. A.C, et al (1971). Teknologi pengolahan Pati. Yogyakarta :UGM-Press. Halaman 45-47.
Mycek.J.M, Richard.A.H, dan Pamela.C.C (2001).Farmakologi Ulasan Bergambar. Edisi Kedua. Jakarta : Widya Medika. Halaman 336.
Parrot.E.L (1971). Pharmaceutical Technology Fundamental Pharmaceutical.
Minneapolis: Burgess Publishing Company. Pages 82-83.
Soekemi.R.A,dkk (1987). Tablet. Medan: Mayang Kencana.Halaman 13-17, 42.
meningkatkan nilai tambah dalam pengembangan agro industri.
Prosiding Seminar Nasional, BPTP Sulawesi Tengah.Halaman 1-5.
Voigt.R (1995). Buku Pelajaran Teknologi Farmasi. EdisiV. Yogyakarta: Gadjah Mada University Press. Halaman 200.
Wade. A dan Weller.P.J (1994). Handbook of pharmaceutical excipient. 2nd ed. Washington: American PharmaceuticalAssociation,.Hal: 151 - 153.
Winarno, F.G (1995). Kimia Pangan dan Gizi. Jakarta : PT.Gramedia Pustaka Utama Halaman 27-31.
Lampiran 1. Contoh Perhitungan Pembuatan Tablet Isoniazid
Sebagai contoh diambil tablet Isoniazid dengan konsentrasi 11.25% (Formula 4).
Dibuat formula untuk 100 tablet, dengan berat tablet 250 mg dan diameter tablet 9
mm.
Berat 100 tablet =100 x 0,250 g = 25 g
Berat Isoniazid dalam tablet =100x100mg=10000mg=10g a. Pengembang dalam = 2,5% x 25 g = 0,625 g b. Pengembang luar = 2,5% x 25 g = 0,625 g
c. Mg stearat = 1 % x 2 5 g = 0 , 2 5 g d. Talkum = 1 % x 2 5 g = 0 , 2 5 g e. Pengikat:
i. Bahan pengikat yang digunakan dalam formula adalah musilago amili (corn Starch) 11,25% yang dibuat sebanyak 30% = 30% x 25 g = 7,5 g
ii. Corn Starch yang ditimbang = 11,25% x 7,5 g = 0,8437 g
f. Laktosa = 25 g – ( 10 + 0,312 + 0,312 + 0,25 + 0,25 + 0,8437 )g
=12,4063g
Cara Kerja : metode granulasi basah
1. Isoniazid + laktosa +pengembang dalam, digerus homogen.
2. Ditambahkan musilago amili(corn starch) sedikit demi sedikit sampai
diperoleh massa yang kompak. Musilago amili 11,25% yang terpakai adalah 6,4815 g yang mengandung corn starch 0,6481 g
dengan ayakan mesh 14.
a. Berat massa secara teoritis :
= (bahan obat + pengembang dalam + pengikat + pengisi) =
(10 + 0,625 + 0,6481 + 12,4063)g = 23,6794 g
= 100% 94,71% 25
) 6794 , 23 (
=
x g
b. Granular kering ditimbang beratnya = 23,100 g c. Massa tablet seluruhnya = 100%/94,71% x 23,100 g
= 24,3902 g
d. Pengembang luar = 2,5/100 x 24,3902 g = 0,6097 g
e. Talkum = 1/100 x 24,3902 g = 0,2439 gr f. Mg stearat = 1/100 x 24,3902 g = 0,2439 g
6. Ditambahkan pengembang luar, talkum, Mg stearat lalu diaduk hingga homogen.
Lampiran 2. Contoh Perhitungan Friabilitas Tablet
A = Bobot tablet sebelum diputar dalam alat friabilator B = Bobot tablet setelah diputar dalam alat friabilator
Syarat Friabilator tablet :
Kehilangan bobot tidak boleh lebih dari 0,8% (F < 0,8%)
Sebagai contoh diambil tablet Isoniazid dengan konsentrasi cornstarch 11.25%
Bobot 20 tablet sebelum diputar = 5,034 g
Bobot 20 tablet setelah diputar = 5,015 g
Lampiran 4. Hasil pembuatan kurva kalibrasi dan persamaan regresi Isoniazida BPFI dalam pelarut Air suling.
Tabel data kurva kalibrasi
C (mcg /
ml) Abs (Y) XY X2 Y2
X
0.0000 0.0000 0.0000 0.0000 0.0000
7.0000 0.2320 1.6240 49.0000 0.0538
Lampiran 5. Contoh Perhitungan Kadar Tablet Isoniazid
Misalnya tablet Isoniazid dengan konsentrasi cornstarch 13,75% (Formula 6).
Berat 20 tablet = 4.8946 mg
Dilakukan sebanyak 6 kali perlakuan
a. Pengujian I
Serbuk ditimbang seksama sebanyak 122.2 mg, kemudian dilarutkan
sesuai prosedur yang telah disebutkan sebelumnya dan diukur serapan pada panjang gelombang maksimum.
Misalnya A(Y) = 0,4152dengan menggunakan persamaan regresi:
Y = 0,032619X + 0,001289 Diperoleh konsentrasi (X) larutan =
032619
Maka konsentrasi teoritis = 12.6647 mcg/ml
Konsentrasi larutan = 12.9893 mcg/ml Kadar Isoniazid = 99.30%
b. Pengujian III
Kadar Isoniazid = 100,33% c. Pengujian IV
Maka konsentrasi teoritis = 13,0106mcg/ml
Konsentrasi larutan = 12,8364mcg/ml
Kadar Isoniazid = 100,48% d. Pengujian V
Maka konsentrasi teoritis = 13,0106mcg/ml
Konsentrasi larutan = 12.8793mcg/ml
Kadar Isoniazid = 100,82% e.Pengujian VI
Maka konsentrasi teoritis = 13,0106 mcg/ml
Konsentrasi larutan = 12.9958 mcg/ml
Kadar Isoniazid = 101.73%
Dengan :
SD =
1 )
( 2
− −
∑
n X X
= (99.49−100.35)2 +...+(101.73−100.35)2. 6-1
Lampiran 6. Contoh Perhitungan Keragaman Bobot Contoh : Formula 4
Ditimbang masing-masing berat 10 tablet:
1. 248 6. 252
2. 250 7. 250
3. 248 8. 251
4. 252 9. 252
5. 249 10. 250
Berat rata-rata = mg
tablet
Ditimbang serbuk seksama dan dilakukan pengujian seperti pada penetapan
kadar. Maka diperoleh absorbansi (Y) = 0,4305
Konsentrasi Isoniazid dapat dihitung dengan memasukkan nilai absorbansi ke persamaan regresi :
Y = 0,032619X + 0,001289 Maka, X = 13.1583 mcg/ml
Diketahui konsentrasi teoritis = 12.9890 mcg/ml
Maka, kadar Isoniazid = 101,85% 103.17%
Kadar Isoniazid = 102.69% c. Pengujian 3
Kadar Isoniazid = 102.73% d. Pengujian 4
Kadar Isoniazid =102.40% f. Pengujian 6
Kadar Isoniazid =102.25%
Rata-rata hasil penetapan kadar = 102,62% x 100 mg
= 102.62 mg zat berkhasiat/tablet
Contoh: Berat tablet I = 248 mg
Maka kadar zat berkhasiatnya = 248 mg / 250,2 mg x 102,62 mg = 101,71 mg
Maka % penyimpangan berat terhadap berat rata-rata
(
)
2Dengan cara yang sama dihitung keragaman bobot untuk formula yang lain
Lampiran 9. Contoh perhitungan Hasil Uji Disolusi
Sebagai contoh adalah disolusi isoniazida dengan menggunakan cornstarch 7.5%. Untuk t = 5 menit, cuplikan diambil 2.5 ml, kemudian diencerkan ke labu tentukur 25 ml, diukur serapannya pada panjang gelombang 267 nm, diperoleh serapan
0.1976, maka konsentrasi isoniazida yang terlarut pada t = 5:
Dari persamaan regresi Y = 0,03878 X + 0.0018
03878
Jumlah isoniazida yang terlarut dalam 900 ml adalah:
= 900 x
x 5.0465 mcg/ml = 4541.85 mcg/ml
= 45.4185 mg
Pengambilan diteruskan untuk menit ke 10,15,20,25,30,35,40,45.
% kumulatif terlepas pada menit ke 5 adalah ;