Lampiran 2. Gambar tumbuhan, buah, dan simplisua buah stroberi (Fragaria vesca L. )
( A )
Lampiran 2 (lanjutan)
( C )
( D ) Keterangan :
A = Gambar tumbuhan buah stroberi (Fragaria vesca L.) B = Gambar buah stroberi (Fragaria vesca L.)
Lampiran 3. Flowsheet Pembuatan Ekstrak Stroberi
Dimasukkan ke dalam bejana Ditambah pelarut 4 liter etanol 70%
Dibiarkan selama 5 hari terlindung dari cahaya sambil sesekali di aduk
Diserkai, diperas
Dicuci dengan pelarut etanol 70% hingga diperoleh (100 bagian) Dipindahkan ke dalam bejana tertutup
Dibiarkan di tempat sejuk, terlindung dari cahaya selama 2 hari Dienap tuangkan dan di saring
Digabung
Dipekatkan dengan alat rotary evaporator 40oC Dikeringkan dengan waterbath
Buah stroberi (2000 g)
Ampas Maserat
Ampas Maserat
Lampiran 4. Perhitungan Bahan Tablet
R/ Parasetamol 0,250
Ekstrak buah stroberi 6% Pasta amylum manihot 7,5% b/b q.s
Talk 1%
Mg stearat 2%
Laktosa q.s ad 500 mg
m.f tab dtd No C I. Rencana kerja
1. Berat 1 tablet = 500 mg 2. Diameter tablet = 13 mm
3. Metode = granulasi basah 4. Bentuk tablet = bulat pipih II. Perhitungan Bahan
1. Parasetamol = 0,250 g x 100 = 25g 2. Ekstrak warna = 6/100 x 50 g = 3 g 3. Amilum manihot
• Pengembang luar = 2,5/100 x 50 g = 1,25 g
• Pengembang dalam = 2,5/100 x 50 g = 1,25 g 4. Talkum = 1/100 x 50 g = 0,5 g
5. Mg Stearat = 1/100 x 50 g = 1 g
6. Pastaamilum manihot 7,5%
Pasta amilum manihot terpakai 30% dari berat total maka :
30/100 x 50 g = 15 gram mengandung amylum manihot sebanyak: 7,5/100 x 15= 5,250 gram
Aquadest = 15- 5,250 = 9,750 gram
Lampiran 4 (Lanjutan)
Contoh Perhitungan Bahan Tablet
R/ Parasetamol 0,250
Ekstrak buah stroberi 8% Pasta amylum manihot 7,5% b/b q.s
Talk 1%
Mg stearat 2%
Laktosa q.s ad 500 mg
m.f tab dtd No C I. Rencana kerja
1. Berat 1 tablet = 500 mg 2. Diameter tablet = 13 mm
3. Metode = granulasi basah 4. Bentuk tablet = bulat pipih II. Perhitungan Bahan
8.Parasetamol = 0,250 g x 100 = 25g 9.Ekstrak warna = 8/100 x 50 g = 4 g
10.Amilum manihot
• Pengembang luar = 2,5/100 x 50 g = 1,25 g
• Pengembang dalam = 2,5/100 x 50 g = 1,25 g 11.Talkum = 1/100 x 50 g = 0,5 g 12.Mg Stearat = 1/100 x 50 g = 1 g 13.Pastaamylum manihot 71/2%
Suspensi pati singkong terpakai 30% dari berat total maka :
30/100 x 50 g = 15 gram mengandung amylum manihot sebanyak: 7 1/2/100 x 15= 5,250 gram
Aquades = 15 – 5,250 = 9,750 gram
Lampiran 4 (Lanjutan)
Contoh Perhitungan Bahan Tablet
R/ Parasetamol 0,250
Ekstrak buah stroberi 10% Pasta amylum manihot 7,5% b/b q.s
Talk 1%
Mg stearat 2%
Laktosa q.s ad 500 mg
m.f tab dtd No C I. Rencana kerja
1. Berat 1 tablet = 500 mg 2. Diameter tablet = 13 mm
3. Metode = granulasi basah 4. Bentuk tablet = bulat pipih II. Perhitungan Bahan
14.Parasetamol = 0,250 g x 100 = 25g 15.Ekstrak warna = 10/100 x 50 g = 5 g 16. Amilum manihot
• Pengembang luar = 2,5/100 x 50 g = 1,25 g
• Pengembang dalam = 2,5/100 x 50 g = 1,25 g 16.Talkum = 1/100 x 50 g = 0,5 g
17.Mg Stearat = 1/100 x 50 g = 1 g 18.Pastaamilum manihot 7,5%
Pasta amilum manihot terpakai 30% dari berat total maka :
30/100 x 50 g = 15 gram mengandung amylum manihot sebanyak: 7,5/100 x 15= 5,250 gram
Aquadest 15-5,250 = 9,750 gram
Lampiran 4 (Lanjutan)
Contoh Perhitungan Bahan Tablet
R/ Parasetamol 0,250
Ekstrak buah stroberi 12% Pasta amylum manihot 7,5% b/b q.s
Talk 1%
Mg stearat 2%
Laktosa q.s ad 500 mg
m.f tab dtd No C I. Rencana kerja
1. Berat 1 tablet = 500 mg 2. Diameter tablet = 13 mm
3. Metode = granulasi basah 4. Bentuk tablet = bulat pipih II. Perhitungan Bahan
21. Parasetamol = 0,250 g x 100 = 25g 22. ESB = 12/100 x 50 g = 6 g
23. Amilum manihot
• Pengembang luar = 2,5/100 x 50 g = 1,25 g
• Pengembang dalam = 2,5/100 x 50 g = 1,25 g 24. Talkum = 1/100 x 50 g = 0,5 g 25. Mg Stearat = 1/100 x 50 g = 1 g 26. Pastaamylum manihot 7,5%
Suspensi pati singkong terpakai 30% dari berat total maka :
30/100 x 50 g = 15 gram mengandung amylum manihot sebanyak: 7 1/2/100 x 15= 5,250 gram
Aquades = 15 – 5,250 = 9,750 gram
Lampiran 5. Gambar Tablet Parasetamol
Keterangan :
Lampiran 6. Gambar Warna Standart ( Standart Colour)
GAMBAR WARNA STANDART (STANDAR COLORS)
Gambar Tablet Parasetamol
Perbandingan warna tablet dengan warna standar (standart color)
Keterangan :
F1 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 6% F2 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 8% F3 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 10% F4 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 12%
Fodge Leather Brown Brown Autumn Brown Mirsty Red Brick Red
Fodge Leather Brown
Autu
Lampiran 8 (Lanjutan)
C (μg/ml)
(X)
Absorbansi
(Y) XY X
2
Y2
0,0000 0,000 0 0 0
3,200 0,180 0,576 10,240 0,0324
4,400 0,269 1,1836 19,36 0,72361
6,000 0,357 2,142 36 0,127449
7,200 0,440 3,168 51,48 19,36
8,800 0,532 4,6816 77,44 0,283024
ΣX =29,600 ΣY = 1,778 ΣXY = 11,7512
ΣX2 = 194,88 ΣY2 = 0,708834 X = 4,933333 Y = 0,
2963333
XY = 1,958533
X2 = 32,48 Y2 = 0,118139 a = = 6 / 2 ) 600 , 29 ( 880 , 194 6 / ) 778 , 1 )( 600 , 29 ( 7506 , 11 − − = 0,060981 Y = a X + b b = Y – a X
= 0,29633– (0,060981x 4,9333333) = 0,089148
Persamaan regresi : Y = 0,060981x + 0,089148 Dengan nilai r sebagai berikut :
r = ΣXY− (Σ�)(Σ�)/�
�(ΣX2−(ΣX)2/n (ΣY2− (ΣY)2/n)
Lampiran 9. Perhitungan keragaman bobot tablet parasetamol Contoh : Formula 1 ( 6 % )
Ditimbang masing-masing berat 10 tablet:
1. 500,0 6. 500,2
2. 499,0 7. 497,2
3. 495,0 8. 498,0
4. 498,0 9. 500,3
5. 497,0 10. 499,2
pBerat rata-rata 10 tablet : 497,1mg
Rata-rata hasil penetapan kadar = 94,70 % x 250 mg
= 236,75 mg (zat berkhasiat/tablet) Berat tablet 1 = 500 mg
Maka kadar zat berkhasiatnya = = x 236,75 mg = 119,065 mg
Maka % penyimpangan berat terhadap berat rata-rata :
= 236,75−119,065
236,75 x 100 %
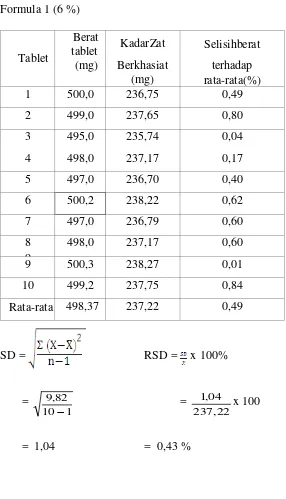
Lampiran 9 (Lanjutan) Formula 1 (6 %)
Tablet
Berat tablet
(mg)
KadarZat Berkhasiat
(mg)
Selisihberat terhadap rata-rata(%)
1 500,0 236,75 0,49
2 499,0 237,65 0,80
3 495,0 235,74 0,04
4 498,0 237,17 0,17
5 497,0 236,70 0,40
6 500,2 238,22 0,62
7 497,0 236,79 0,60
8 o
498,0 237,17 0,60
9 500,3 238,27 0,01
10 499,2 237,75 0,84
Rata-rata 498,37 237,22 0,49
SD = RSD = x 100%
=
1 10
82 , 9
− = 237,22
04 ,
1 x 100
= 1,04 = 0,43 %
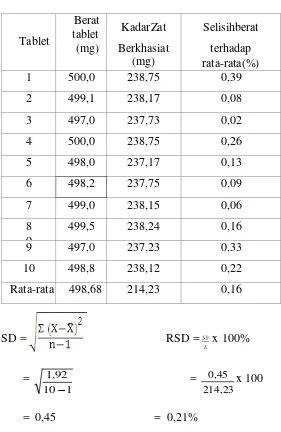
Formula 2 ( 8 % )
Tablet
Berat tablet
(mg)
KadarZat Berkhasiat
(mg)
Selisihberat terhadap rata-rata(%)
1 500,0 238,75 0,39
2 499,1 238,17 0,08
3 497,0 237,73 0,02
4 500,0 238,75 0,26
5 498,0 237,17 0,13
6 498,2 237,75 0,09
7 499,0 238,15 0,06
8 o
499,5 238,24 0,16
9 497,0 237,23 0,33
10 498,8 238,12 0,22
Rata-rata 498,68 214,23 0,16
SD = RSD = x 100%
=
1 10
92 , 1
− = 214,23 45 ,
0 x 100
= 0,45 = 0,21%
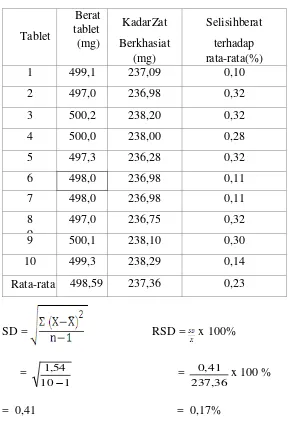
Formula 3 ( 10 % )
Tablet
Berat tablet
(mg)
KadarZat Berkhasiat
(mg)
Selisihberat terhadap rata-rata(%)
1 499,1 237,09 0,10
2 497,0 236,98 0,32
3 500,2 238,20 0,32
4 500,0 238,00 0,28
5 497,3 236,28 0,32
6 498,0 236,98 0,11
7 498,0 236,98 0,11
8 o
497,0 236,75 0,32
9 500,1 238,10 0,30
10 499,3 238,29 0,14
Rata-rata 498,59 237,36 0,23
SD = RSD = x 100%
=
1 10
54 , 1
− = 237,36 41 ,
0 x 100 %
= 0,41 = 0,17%
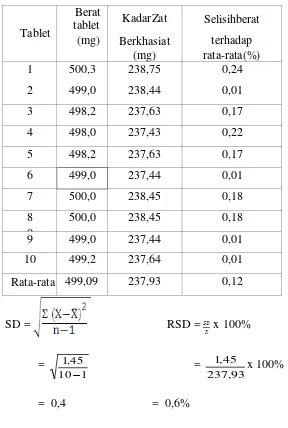
Tablet
Berat tablet
(mg)
KadarZat Berkhasiat
(mg)
Selisihberat terhadap rata-rata(%)
1 500,3 238,75 0,24
2 499,0 238,44 0,01
3 498,2 237,63 0,17
4 498,0 237,43 0,22
5 498,2 237,63 0,17
6 499,0 237,44 0,01
7 500,0 238,45 0,18
8 o
500,0 238,45 0,18
9 499,0 237,44 0,01
10 499,2 237,64 0,01
Rata-rata 499,09 237,93 0,12
SD = RSD = x 100%
=
1 10
45 , 1
− = 237,93 45 ,
1 x 100%
= 0,4 = 0,6%
• Pengujian I
1. Konsentrasi ( C )
Dengan persamaan regresi Y = 0,060981 + 0,089148 X = Konsentrasi
Y = Absorbansi
Pada t = 5 Menit, Y = 0,3945 2. Faktor Pengenceran
Fp = (pengenceran dalam labu 25 ml) / jumlah pemipetan aliquot = 25 / 1
Fp = 25
3. Konsentrasi dalam 1 ml (Cp x Fp) C = 9,5422mcg/ml x 25 = 238,55mcg/ml 4. konsentrasi dalam 900ml
C dalam 900ml = C dalam 1ml x 900 Contoh pada t = 5 menit
C = 238,55mcg/ml x 900 ml =214,6995 mcg/900 ml 5. Parasetamol yang terlepas
Parasetamol yang terlepas = 214699,50mcg + 0 = 214699,50mcg = 214,6995mg 6. Persen Kumulatif
% kumulatif =
Dosis parasetamol = 250 mg % kumulatif =
mg mg
250 6995 ,
214 = 85,87 %
T Y C (mcg/
ml)
Fp C 1 ml C 900 ml (mcg/ml) C yang terlepas (mcg)
% K % K
rata-rata
1 0,3945 9,5422 25 238,55 214699,50 214699,50 85,87 %
87,1 4% 2 0,4405 9,6354 25 240,88 21679,20 21679,20 86,71
%
3 0,4121 9,8154 25 245,38 220842,0 22084,20 88,33 %
4 0,4025 9,6664 25 241,60 217444,0 217444,0 86,97 %
5 0,4093 9,7719 25 244,19 219861,0 219861,0 87,94 %
6 0,4014 9,6493 25 241,23 217107,0 217107,0 86,84 %
SD = RSD = x 100%
= 1 6 9674 , 3
− = 522,66
89 ,
0 x 100
= 0,89 = 0,17
T Y C (mcg/
ml)
Fp C 1 ml C 900 ml (mcg/ml) C yang terlepas (mcg)
% K % K
rata-rata
1
0,3011 9,6447 25 241,11 216999.00 216999,00
86,79 %
87,12 % 2
0,3991 9,6136 25 240,37 216333,00 216333,00
86,53 %
3
0,4101 9,7844 25 244,61 220149,00 220149,00
88,05 %
4
0,4070 9,7362 25 243,40 219060,00 219060,00
87,62 %
5
0,4022 9,6617 25 241,54 217386,00 217386,00
86,95 %
6
0,4012 9,6462 25 241,15 217035,00 217035,00
86,81 %
SD = RSD = x 100%
= 1 6 2662 , 2
− = 522,75
67 ,
0 x 100
= 0,67 = 0,12
Formula F3 ( 10 %)
T Y C (mcg/ml
)
Fp C 1 ml C 900 ml (mcg/ml) C yang terlepas (mcg)
% K % K
rata-rata
1 0,3993 9,6167 25 240,41 216369,00 216369,00 86,54 %
86,9 2% 2 0,3989 9,6105 25 240,26 216234,00 216234,00 86,49
%
3 0,4050 9,7052 25 242,63 218367,00 218367,00 87,34 %
4 0,4008 9,6400 25 241,00 216900,00 216900,00 86,76 %
5 0,3995 9,6198 25 240,49 216441,00 216441,00 86,57 %
6 0,4088 9,7642 25 244,10 219690,00 219690,00 87,87 %
SD = RSD = x 100%
= 1 6 5563 , 1
− = 521,57
55 ,
0 x 100%
= 0,55 = 0,10
Formula F4 ( 12 %)
T Y C (mcg/
ml)
Fp C 1 ml
C 900 ml (mcg/ml)
C yang terlepas
(mcg)
% K % K
rata-rata
1 0,4101 9,7844 25 244,61 220149,00 220149,00 88,05%
87,1 0% 2 0,4078 9,7487 25 243,71 219339,00 219339,00 87,73%
3 0,4009 9,6416 25 241,04 216936,00 216936,00 86,77%
4 0,3990 9,6121 25 240.30 216270,00 216270,00 86,50%
5 0,3986 9,6059 25 240,14 216126,00 216126,00 86,45%
6 0,4034 9,6804 25 242,01 217809,00 217809,00 87,12%
SD = RSD = x 100%
=
1 6
1912 , 2
− = 522,62
66 ,
0 x 100%
= 0,66 = 0,12
Misalnya untuk formula F1 (6 % ) Berat 20 tablet = 10128 mg
Berat parasetamol dalam 20 tablet = 20 x 500mg = 10000 mg Berat setara 25 mg parasetamol=
mg mg
10000
25 x 10128mg = 25,3mg
- Pengujian 1 Serbuk ditimbang seksama sebanyak 25,3mg kemudian dilarutkan sesuai prosedur yang telah disebutkan sebelumnya dan diukur serapan pada panjang gelombang maksimum, Misalnya A(Y) = 0,4530 dengan menggunakan persamaan regresi :
Y = 0,060981 X + 0,089148 maka diperoleh konsentrasi larutan ( X ) : 0,4530 = 0,060981 X + 0,089148
X = 060981 , 0 089148 , 0 453 , 0 −
X = 5,9660
Diketahui konsentrasi teoritisnya
= x 6,3949
= mg mg 3 , 25 3 ,
25 x 6,3949
= 6,400
Kadar Parasetamol =
400 . 6 9660 , 5 x 100% = 93,29%
Berat 20 tablet = 10128 mg Berat setara 25 mg parasetamol ==
mg mg
10000
25 x 10128 mg = 25,3 mg
No Berat sampel yang ditimban g (mg) Kons, Teoritis (mcg/m l) Serapan Kons, Sampel (mcg/l) Kadar (%) Kadar rata-rata (%) Persyaratan
1 25,3 6,3949 0,453 5,9660 93,29
95,00 %
90,00% - 110,00% 2 25,3 6,3949 0,454 5,9830 95,35
3 25,3 6,3949 0,468 6,2126 97,14 4 25,3 6,3949 0,461 6,0978 95,35 5 25,3 6,3949 0,457 6,0322 94,32 6 25,3 6,3949 0,458 6,0486 94,58
SD = RSD = x 100%
= 1 6 3875 , 8
− = 95,00
2951 ,
1 x 100
= 1,2951 = 1,36
Berat 20 tablet = 10235mg Berat setara 25 mg parasetamol =
mg mg
10000
25 x10235mg = 25,5mg
N o Berat sampel yang ditimba ng (mg) Kons, Teoritis (mcg/m l) Serapan Kons, Sampel (mcg/m l) Kadar (%) Kadar rata-rata (%) Persyaratan
1 25,3 6,3949 0,471 6,4750 101,25
101,28 %
90,00% - 110,0% 2 25,4 6,3000 0,477 6,3602 100,95
3 25,3 6,3949 0,482 6,4422 100,73 4 25,4 6,3000 0,479 6,3930 101,47 5 25,5 6,3255 0,481 6,4258 101,58 6 25,4 6,3000 0,480 6,4094 101,73
SD = RSD = x 100%
= 1 6 5725 , 1
− = 101,28
5608 ,
0 x 100
= 0,5608 = 0,55
Berat 20 tablet =10268 mg Berat setara 25 mg parasetamo=
mg mg
10000
25 x l0268mg = 25,6 mg
N o Berat sampel yang ditimba ng (mg) Kons, Teoritis (mcg/m l) Serapan Kons, Sampel (mcg/m l) Kadar (%) Kadar rata-rata (%) Persyaratan
1 25,5 6,3750 0,480 6,4094 100,53
100,86 %
90,00% - 110,0% 2 25,3 6,3250 0,479 6,3930 101,07
3 25,4 6,3250 0,482 6,4422 101,45 4 25,3 6,3250 0,484 6,4750 101,07 5 25,5 6,3750 0,483 6,4422 100,53 6 25,5 6,3750 0,482 6,4586 100,53
SD = RSD = x 100%
= 1 6 763 , 0
− = 100,86
3906 ,
0 x 10
= 0,3906 = 0,38
Berat 20 tablet =10215mg Berat setara 25 mg parasetamol =
mg mg
10000
25 x10215mg = 25,5mg
N o Berat sampel yang ditimba ng (mg) Kons, Teoritis (mcg/m l) Serapan Kons, Sampel (mcg/m l) Kadar (%) Kadar rata-rata (%) Persyaratan
1 25,4 6,3749 0,4830 6,4422 100,28
101,04 %
90,00% - 110,0% 2 25,5 6,4000 0,4840 6,4750 101,17
3 25,3 6,3498 0,4851 6,4913 102,22 4 25,4 6,3749 0,4790 6,3930 100,28 5 25,5 6,4000 0,4811 6,4258 101,17 6 25,5 6,4000 0,4800 6,4094 101,17
SD = RSD = x 100%
= 1 6 5983 , 2
− = 101,04
1441 ,
0 x 100%
= 0,1441 = 0,14
Lampiran 13. Kuesioner Uji Akseptabilitas Tablet Parasetamol Dari Ekstrak Stroberi
Nama : Usia : Pekerjaan : Tanggal :
Petunjuk
1. Anda akan menerima 4 (empat) sampel tablet parasetamol ekstrak stroberi 2. Setelah menerima sampel, coba lihatlah warna daritablet parasetamol
tersebut dan seterusnya sampai formula 4
3. Berilah penilaian angka pada pernyataan yang sesuai dengan penilaian saudara.
No Penilaian Formula
F1 F2 F3 F4
1 Warna
Keterangan: 1. Tidak suka
2. Kurang suka 3. Suka
4. Sangat suka
Lampiran 14.Datadan Gambar Sukarelawan a. Data
( tahun )
1 Leni 30 IRT memiliki anak umur 10 tahun 2 Nining 26 IRT memiliki anak umur 3 tahun 3 Ledys diana 32 IRT memiliki anak umur 6 tahun 4 Sasmita 45 IRT memiliki anak umur 8 tahun 5 Kembariah 42 IRT memiliki anak umur 12 tahun 6 Pipit 36 IRT memiliki anak umur 10 tahun 7 Salamah 42 IRT memiliki anak umur 6 tahun 8 Rosiana 42 IRT memiliki anak umur 13 tahun 9 Bibah 38 IRT memiliki anak umur 5 tahun 10 Sri 36 IRT memiliki anak umur 2 tahun 11 Zakiyah 50 PNS memiliki anak umur 4 tahun 12 Asni siregar 47 PNS memiliki anak umur 10 tahun 13 Dawiyatul 42 PNS memiliki anak umur 3 tahun 14 Aini rahmah 53 PNS memiliki anak umur 6 tahun 15 Misni 45 IRT memiliki anak umur 8 tahun 16 Amah 36 IRT memiliki anak umur 10 tahun 17 Misnah 45 IRT memiliki anak umur 10 tahun 18 Widya 42 IRT memiliki anak umur 5 tahun 19 Irtha hanim 28 IRT memiliki anak umur 2 tahun 20 Devi
kesumawati
30 IRT memiliki anak umur 6 tahun
b. Gambar sukarelawan Lampiran 15. Hasil uji hedonik
Panelis I(6%) II(8%) III(10%) IV(12%) Total
1 1 3 1 2 7
3 1 4 3 3 11
4 2 3 2 1 8
5 1 2 4 3 10
6 2 4 4 1 11
7 2 4 3 1 10
8 1 3 3 2 9
9 4 3 3 1 11
10 3 4 2 1 10
11 1 4 2 2 9
12 1 4 4 2 11
13 1 4 3 2 10
14 1 3 3 2 9
15 3 2 4 2 11
16 3 1 4 1 9
17 3 1 2 2 8
18 2 2 3 2 9
19 3 4 4 1 12
20 2 4 4 4 15
Total 38 63 58 37 196
Rata-rata
1,9 3,15 2,9 1,85 2,45
( A )
( B )
( D )
Keterangan :
A = Gambar alat sudut diam dan waktu alir ( Flowmeter) B = Gambar alat mesin pencetak tablet (Erweka)
DAFTAR PUSTAKA
Agoes, G. (2008).Pengembangan Sediaan Farmasi.Bandung:: Penerbit ITB, Hal. 199-208.
Anief, (2003). Ilmu Meracik Obat, Teori dan Praktek. Gadjah Mada University Press: Yogyakarta. Hal. 161-162.
Ansel, H.C. (1989).Pengantar Bentuk Sediaan Farmasi.EdisiIV. UIPress Jakarta. Hal. 96.
Banker, G. S., Anderson N. R. (1994). Tablet. Edisi III, Jilid II. UI-Press. Jakarta.Hal. 643-703.
Budiman, S., dan Saraswati, D. (2005). Berkebun Stroberi secara Komersial. Jakarta: Penebar Swadaya. Hal. 8, 13-23.
Cartensen, J.T. (1977). Pharmaceutical of Solids and Dosage Forms. A Willey Interscience Publication. New York: John Willey and Sons. Hal. 133-135, 209-214, 216-218 dan 342.
Dalimartha, S., dan Felix, A. (2011). Khasiat Buah dan Sayur.Edisi II. Jakarta: Penebar Swadaya. Hal. 7-81.
Depkes RI. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Hal. 6-7.
Depkes RI. (1978). Materi Medika Indonesia. Jilid II. Jakarta: DepartemenKesehatanRI. Hal. 150-156,165-167.
DitjenPOM, (1995). Farmakope Indonesia. Edisi keempat.Jakarta: Departemen Kesehatan RI. Hal. 970-971, 999, 1083-1087.
DitjenPOM, (2000). Parameter Standar Umum Ekstrak Tanaman . Cetakan I.Jakarta: Departemen Kesehatan RI. Hal. 970-971, 999, 1083-1087. Ganiswarna, S.G. (editor). (1995), Farmakologi dan Terapi. Edisi 5. Bagian
Farmakologi Fakultas Kedokrteran Universitas Indonesia. Jakarta. Hal. 120-124.
Harbone, J.B. (1987). Metode Fitokimia, Penuntun Cara Modern Menganalisa Tumbuhan.. Terjemahan K.Padmawinata. Edisi II. Bandung: ITB Press. Hal. 259-260.
Lachman, L., Lieberman, H.A., Kanig, J.L. (1994). Teori dan Praktek Farmasi Industri. Edisi III.Jakarta: UI Press. Hal. 654.
Parmer, R.B., Baria, A.H.M., dan Faldus, D.(2009). Formulation and Evaluation of Domperidone Fast Dissolving Tablets. International journal of PharmaTech Research.1(3). Hal. 485-487.
Parrot, L. (1971). Pharmaceutical Technology. Burges PublishingCompany. United Stated of America. Hal. 82.
Saati, E.A. dan Hidayat, N. (2006). Membuat Pewarna Alami. Cetakan I. Trubus Argrisna. Hal. 5-10.
Sharma, R., Rajput, M., Prakash, P., Sharma, S. (2011). Fast Disolving Delivery System On review. International Journal of Pharmacy.2(10): 21-29. Silalahi, J. (2006). Makanan Fungsional. Yogyakarta: Kanisius. Hal. 40-51. Siregar, C.J.P., Wikarsa, S. (2010). Teknologi Farmasi Sediian Tablet
Dasar-Dasar Praktis. Cetakan II. Penerbit Buku Kedokteran EGC. Jakarta. Hal.1-2,8,416-418.
Soekarto, S.T. (1985). Penilaian Organoleptik untuk Industri Pangan dan Hasil Pertanian. Bhatara Aksara. Jakarta. Hal. 57.
Soekemi, R. A. Yanita, T. Fat Aminah, Salim Usman. (1987). Tablet. Mayang Kencana. Hal. 18-19.
Voigt, R. (1995). Buku Pelajaran Teknologi Farmasi. Cetakam II.Penerjemah: Soedani N. S. UGM-Press. Yogyakarta. Hal. 159.
BAB III
METODELOGI PENELITIAN
3.1 Tempat dan waktu penelitian
Penelitian ini dilangsungkan di laboratorium Teknologi Sediaan Farmasi II dan Laboratorium Farmakognosi Fakultas Farmasi Universitas Sumatera Utara. 3.2 Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas laboratorium, lemari pengering,rotary evaporator, penangas, corong pisah, cawan porselen berdasar rata, desikator, mesin cetak tablet single punch ((Erweka), hardness tester (Copley), Roche friabilator (Erweka), stopwatch, termometer, mortir, stamper, waterbath, dan ayakan mesh 14 dan mesh 20.
3.3 Bahan-bahan yang digunakan
Bahan-bahan yang digunakan pada penelitian ini adalah buah stroberi segar, parasetamol (derajat farmasetis), etanol 70%, akuades, pati jagung, pati manihot, talkum, magnesium stearat, dan laktosa.
3.4 Prosedur kerja
3.4.1 Pengumpulan sampel
Buah stroberi diambil secara purposif yaitu tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Tumbuhan yang digunakan adalah buah stroberi (Fragaria vescaL.) yang diperoleh dari pasar Kota Berastagi KabupatenKaro, Provinsi Sumatera Utara.
3.4.2 Identifikasi sampel
3.4.3 Uji Organoleptis dan Makroskopik
Pemeriksaan makroskopik dilakukan pada buah segar stroberi meliputi warna, bau, rasa, bentuk dan ukuran (Depkes RI., 1979).
3.5 Pembuatan EkstrakBuah Stroberi
Buah stroberi diekstraksi dengan cara maserasi dengan menggunakan pelarut etanol. Menurut Farmakope Indonesia Edisi III (1979) caranya adalah sebagai berikut :
Buah stroberi (Fragaria vesca L.) segar dibersihkan, dicuci. kemudian ditiriskan dan ditimbang beratnya, dihitung sebagai berat basah (2000g). Dipotong kecil kemudian ditimbang kembali sebagai berat yangsudah dipotong kecil-kecil sehingga beratnya (2200g). Lalu diekstraksi dengan etanol 70 %, ditutup dan dibiarkan selama 5 hari terlindung dari cahaya sambildiaduk,saring dengan kertas saring. Filtratnya pertama ditampung, kemudianampas diekstraksi kembali dengan etanol 70%, ditutup dan dibiarkanselama 2 hari terlindung dari cahaya sambil diaduk lalu disaring dengan kertas saring.
Hasil yang diperoleh dicampur dengan filtrat pertama lalu diuapkan dengan bantuan alat rotary evaporator pada temperatur kurang lebih ±50°C. Dikeringkan dengan penangasairsehingga didapatkan ekstrak buah stroberi kering (EBS) yang konsistensinya kental berwarna merah.
3.6 Skrining Fitokimia
3.6.1 Pemeriksaan Alkaloida
Sebanyak 0,5 g buah stroberi segar yang telah dihaluskan kemudian di tambahkan 1 mL HCl 2N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan dan disaring. Filtrat dipakai untuk percobaan berikut: a. Filtrat sebanyak 3 tetes di tambahkan 2 tetes pereaksi Meyer, akan terbentuk
endapan berwarna putih atau kuning jika mengandung alkaloida.
b. Filtrat sebanyak 3 tetes ditambahkan 2 tetes pereaksi Bourchardat, akan terbentuk endapan berwarna coklat sampai hitam jika mengandung alkaloida. c. Filtrat sebanyak 3 tetes ditambahkan 2 tetes pereaksi Dragendorff, akan
terbentuk endapan berwarna merah sampai coklat jika mengandung alkaloida. Tetapi jika reaksi 1 dan 2 hanya terjadi kekeruhan dilanjutkan pemeriksaan berikut:
Sebanyak 8 ml filtrat ditambahkan 2 mL ammonia pekat dan dikocok dengan 5 mL campuran eter-kloroform (3:1) dan dibiarkan memisah, diambil lapisan eter-kloroform, ditambahkan sedikit natrium sulfat anhidrat, disaring dan diuapkan filtrat di dalam gelas arloji di atas penangas air, dilarutkan residunya dengan sedikit HCl 2N. Alkaloid positif jika terjadi endapan atau kekeruhan paling banyak dua dari tiga percobaan di atas (Depkes RI., 1979).
3.6.2 Pemeriksaan flavonoid
lapisan metanol, lalu di uapakan pada suhu 400C, sisanya dilarutkan dalam 5 mL etil asetat, lalu disaring. Filtrat nya digunakan untuk uji flavonoid sebagai berikut: a. Sebanyak 1 ml filtrat di uapkan sampai kering, sisanya dilarutkan dalam 2
mL etanol 96% lalu ditambahkan 0,5 g serbuk Zn dan 2 ml asam klorida 2N, didiamkan selama 1 menit. Ditambahkan 10 tetes asam klorida pekat. Jika dalam waktu 2-5 menit terjadi warna merah intensif menunjukkan bahwa adanya flavonoida (glikosida-3-flavonol)
b. Sebanyak 1 mL filtrat diuapkan sampai kering, sisanya dilarutkan dalam 1mL etanol 96%, lalu ditambahkan 0,1 g serbuk magnesium dan 10 tetes asam klorida pekat. Jika terlihat warna merah jingga sampai merah ungu menunjukkan adanya flavonoid (Depkes RI., 1979).
3.6.3 Pemeriksaan Glikosida
Sebanyak 3 g buah stroberi segar disari dengan 30 mL campuran 7 bagian etanol 96% dan 3 bagian air, ditambahkan 10 mL asam sulfat 2N, lalu direfluks selama 10 menit, didinginkan dan disaring. Pada 20 mL filtrat tambahkan 25 mL air dan 25 mL larutan timbal (II) asetat 0,4 M, dikocok dan didiamkan selama 5 menit, saring. Filtrat disari 3 kali, tiap kali dengan 20 mL campuran 3 bagian kloroform dan 2 bagian isopropanol, pada kumpulan sari ditambahkan natrium sulfat anhidrat pekat lalu disaring dan diuapkan pada suhu tidak lebih dari 500C. Dilarutkan sisa dengan 2 mL metanol pekat. Larutan sisa digunakan untuk percobaan berikut:
dengan hati-hati 2 mL asam sulfat pekat hingga terbentuk cincin berwarna ungu pada batas cairan, menunjukkan adanya ikatan gula (Depkes RI., 1979).
3.6.4 Pemeriksaan Tanin
Sebanyak 500 mg buah stroberi segar,dipanaskan dengan 10 mL air, disaring, lalu diencerkan sampai hampir tidak berwarna. Pada 2 mL larutan sampel ditambahkan 1-2 tetes larutan FeCl3 10% dan diperhatikan warna yang
terjadi, warna biru atau hijau kehitaman menandakan adanya tanin (Depkes RI., 1979).
3.6.5 Pemeriksaan Saponin
Buah stroberi yang telah dihaluskan sebanyak 0,5 g dan dimasukkan ke dalam tabung reaksi, lalu ditambahkan 10 mL air panas, didinginkan dan kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1-10 cm yang stabil tidak kurang dari 10 menit dan pada penambahan asam klorida 2N buih tidak hilang, menunjukkan adanya saponin (Depkes RI., 1979).
3.6.6 Pemeriksaan Steroida/ Triterpenoida
Sebanyak 1 g buah stroberi segar di maserasi dengan 20 mL eter selama 2 jam kemudian disaring. Filtrat digunakan untuk reaksi berikut: 5 ml larutan eter diuapkan diatas penangas air, kemudian sisa ditambahkan 20 tetes asam asetat glasial dan 1 tetes asam sulfat pekat ( pereaksi Liebermann-Bourchard). Reaksi steroida / triterpenoida positif bila terjadi warna merah ungu atau biru hijau. (Harbone, 1987).
3.7Formula Sediaan Tablet
R/ Parasetamol 0,250 g Ekstrak Buah Stroberi (EBS) x (bervariasi) Pati jagung 5% Pasta amilum manihiot 7,5 % b/b q.s
Talk 1%
Magnesium stearat 2%
Laktosa ad 500mg
m.f tab dtd No C Keterangan x :
F1 = Formula tablet parasetamol dengan konsentrasi EBS 6% F2 = Formula tablet parasetamol dengan konsentrasi EBS 8% F3 = Formula tablet parasetamol dengan konsentrasi EBS 10% F4 = Formula tablet parasetamol dengan konsentrasi EBS 12% 3.8Pembuatan Sediaan tablet
Pembuatan tablet parasetamol dengan menggunakan zat warna ekstrak buah stroberi dilakukan dengan cara:
a. Ditimbang laktosa 16,25 gram dan ESB 3 g, pati jagung (pengembang dalam) 1,25 g, dan parasetamol 25 g, kemudian digerus sampai homogen. b. Pembuatan bahan pengikatpasta amilum manihot 7,5 % b/b
c. Tambahkan pasta amilum manihot sedikit demi sedikit ke massa a sambil digerus hingga diperoleh massa yang kompak, lalu digranulasi dengan ayakan mesh 14.
d. Granulat dikeringkan pada suhu 40-60 °C pada lemari pengering.
e. Granul kering, granulat diayak lagi dengan ayakan mesh 20 dan dicek kembali beratnya (berat kering = 28,96 g).
f. Ditimbang magnesium stearat1 g, talkum 0,5 g, pati jagung (pengembang luar) 1,25 g,kemudian ditambahkan pada granulat kering dan dihomogenkan.
g. Massa granul diuji preformulasi meliputi waktu alir, sudut diam, dan indeks tap.
h. Dicetak menjadi tablet dengan bobot tablet 500 mg dan diameter tablet 13 mm.
[image:42.595.118.512.525.740.2]i. Dilakukan uji evaluasi tablet meliputi kekereasan tablet, waktu hancur dan friabilitas.
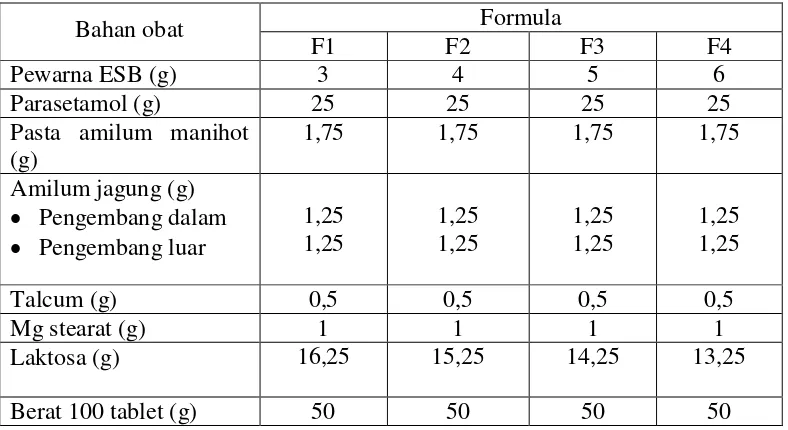
Tabel 3.1 Formula Sediaan Tablet
Bahan obat Formula
F1 F2 F3 F4
Pewarna ESB (g) 3 4 5 6
Parasetamol (g) 25 25 25 25
Pasta amilum manihot (g)
1,75 1,75 1,75 1,75
Amilum jagung (g) • Pengembang dalam • Pengembang luar
1,25 1,25
1,25 1,25
1,25 1,25
1,25 1,25
Talcum (g) 0,5 0,5 0,5 0,5
Mg stearat (g) 1 1 1 1
Laktosa (g) 16,25 15,25 14,25 13,25
Keterangan x :
F1 = Formula tablet parasetamol dengan konsentrasi EBS 6% F2 = Formula tablet parasetamol dengan konsentrasi EBS 8% F3 = Formula tablet parasetamol dengan konsentrasi EBS 10% F4 = Formula tablet parasetamol dengan konsentrasi EBS 12% 3.9 Uji Preformulasi
3.9.1 Sudut Diam Granul
Penentuan sudut diam granul dilakukan dengan cara:
Ditimbang 100 g granul kemudian dimasukkan ke dalam corong alir yang telah dirangkai, permukaan granul diratakan, lalu penutup corong dibuka, sehingga granul mengalir sampai habis. Tinggi tumpukan granul yang terbentuk diukur. Sudut diam dapat dihitung dengan menggunakan rumus:
���= 2�
�
θ = sudut diam
H = tinggi tumpukan granul (cm) D = diameter tumpukan granul (cm)
Granul yang mempunyai daya alir bebas akan mempunyai sudut diam antara 20° sampai 40° (Banker dan Anderson, 1994).
3.9.2 Waktu Alir Granul
Penentuan waktu granul dilakukan dengan cara:
3.9.3 Indeks Tap Granul
Penentuan indeks tap dilakukan dengan cara:
Dimasukkan granul ke dalam gelas ukur sampai garis tanda dan dinyatakan sebagai volume awalnya (V
1), kemudian gelas ukur dihentakkan
sebanyak 20 kali dengan alat yang dimodifikasi sehingga diperoleh volume akhir (V2). Indeks tap dapat dihitung dengan rumus :
���������= �1− �2
�2 � 100%
Syarat indeks tap lebih kecil dari 20 % (Voigt, 1995).
Evaluasi tablet yang dilakukan adalah homogenitas warna, kekerasan tablet, friabilitas, disolusidan waktu hancur.
3.10 Uji Evaluasi Tablet
3.10.1 Uji Homogenitas Warna Tablet
Penentuan homogenitas warna dilakukan dengan cara:
Dilihat permukaan tablet bagian atas, bawah dan sisi bulatan tablet apakah terdapat bintik-bintik warna selain warna coklat. Warna dibandingkan dengan warna standar.
3.10.2 Uji Kekerasan Tablet
3.10.3 Uji Friabilitas Tablet
Penetapan friabilitas tablet menggunakan alat Roche friabilator. Cara: ditimbang 20 tablet yang telah dibersihkan dari debu (A) dimasukkan ke dalam alat dan diputar selama 4 menit. Tablet dikeluarkan dan dibersihkan dari debu kemudian ditimbang (B), kehilangan bobot tidak lebih dari 0,8 % (Banker dan Anderson, 1994). Friabilitas dapat dihitung dengan rumus:
�����������= � − �
� � 100%
3.10.4 Uji Waktu Hancur
Penetapan waktu hancur tablet menggunakan alat Disintegration tester. Alat ini terdiri dari suatu rangkaian keranjang, gelas piala berukuran 1000 mL thermostat dengan suhu 36-38°C dan alat untuk menaik turunkan keranjang dengan frekuensi 30 kali per menit.
Cara : 5 tablet dimasukkan ke dalam keranjang,turun naikkan keranjang secara teratur 30 kali tiap menit. Tablet dinyatakan hancur jika tidak ada bahagian tablet yang tertinggal di atas kasa. Waktu yang diperlukan untuk menghancurkan kelima tablet tidak lebih dari 15 menit. Apabila tablet tidak memenuhi syarat ini, ulangi pengujian menggunakan tablet satu persatu kemudian ulangi percobaan menggunakan 5 tablet dengan cakram penuntun. Dengan cara ini harus dipenuhi persyaratan waktu hancur (DepkesRI.,1979).
3.10.5 Uji Penetapan Kadar Parasetamol
3.10.5.1 Pembuatan larutan induk baku dalam dapar fosfat pH 5,8
Dipipet sebanyak 1 mL larutan tersebut, dimasukkan kedalam labu tentukur 25 mL, dicukupkan dengan dapar fosfat pH 5,8 sampai garis tanda maka diperoleh larutan induk baku dengan konsentrasi 40,080 mcg/mL (LIB II).
3.10.5.2 Pembuatan Kurva Serapan
Dari LIB II Parasetamol, dipipet sebanyak 1,62 mL dan dimasukkan ke dalam labu tentukur 10 mL, diencerkan dengan dapar fosfat pH 5,8 sampai garis tanda. Dikocok homogen maka akan diperoleh konsentrasi 6,5 mcg/mL. Diukur serapannya pada panjang gelombang 200-400 nm dan sebagai blanko digunakan dapar fosfat pH 5,8.
3.10.5.3 Pembuatan Linieritas Kurva Kalibrasi
Dari LIB II dipipet 0,76; 1,12; 1,48; 1,84 dan 2,24 mL, dimasukkan ke dalam labu tentukur 10 mL, kemudian dicukupkan dengan dapar fosfat pH 5,8 sampai garis tanda, sehingga diperoleh konsentrasi 3,2 mcg/mL; 4,4 mcg/mL; 6 mcg/mL; 7,2 mcg/mL dan 8,8 mcg/mL. Diukur serapannya pada panjang gelombang maksimum.
3.10.5.4 Penetapan kadar Tablet Parasetamol
kemudian dicukupkan sampai garis tanda, maka diperoleh larutan dengan konsentrasi 6,4 mcg/mL. Diukur serapannya pada panjang gelombang 243,0 nm dengan menggunakan dapar fosfat pH 5,8 sebagai blanko.
3.10.6Uji Disolusi Tablet
Sejumlah volume media disolusi dimasukkan seperti yang tertera pada masing-masing monografi ke dalam wadah, pasang alat, biarkan media disolusi hingga suhu 37o ± 0,5o dan angkat thermometer. Masukkan satu tablet ke dalam alat, hilangkan gelembung udara dari permukaan sediaan yang diuji dan segera jalankan alat pada laju kecepatan seperti yang tertera pada masing-masing monografi. Dalam interval waktu yang ditetapkan atau pada tiap waktu yang dinyatakan, ambil cuplikan pada daerah pertengahan antara permukaan media disolusi dan bagian atas keranjang berputar atau daun dari alat dayung, tidak kurang 1cm dari dinding wadah. Lakukan penetapan seperti yang tertera dalam masing-masing monografi (Ditjen POM, 1995).
3.10.7 Uji Keragaman Bobot Tablet Parasetamol
Ditimbang saksama 10 tablet, satu persatu. Dan hitung bobot rata-rata. Dari hasil penetapan kadar, yang diperoleh seperti yang tertera dalam masing-masing monografi, hitung jumlah zat aktif dari masing-masing-masing-masing dari 10 tablet dengan anggapan zat aktif terdistribusi secara homogen. Persyaratan keseragaman bobot atau keseragaman kandungan terletak antara 85,0 hingga 115,0% dari yang tertera pada etiket dan simpangan baku relatif kurang dari atau sama dengan 6,0% (Ditjen POM, 1995).
3.11 Uji Hedonik
menggunakan 20 orang panelis yang disuguhi contoh tablet dengan 4 macam konsentrasi untuk diamati warnanya. Untuk melihat tingkat perbandingan warna, dilakukan skorsing pada tabel.
Tabel 3.2 Skala Uji Hedonik Untuk Penentuan Organoleptik Warna
Skala hedonik Skala numerik
Sangat suka suka Kurang suka
Tidak suka
4 3 2 1
Tabel 3.3 Perlakuan Konsentrasi Pewarna
Perlakuan Konsentrasi zat warna (%) I
II III IV
[image:48.595.114.503.321.391.2]BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Sampel
Hasil identifikasi tumbuhan yang dikirim ke Laboratorium Herbarium Medanese, Universitas Sumatera Utara, dinyatakan tumbuhan yang digunakan adalah buah stroberi (Fragaria vesca L.) dari famili Rosaceae.
4.2 Uji Organoleptis dan Makroskopik
Hasil uji organoleptis dan makroskopik buah stroberi (Fragaria vesca L.) Menunjukkan buah stoberi segar mempunyai kulit buah berwarna merah berbintik hitam, daging buah berwarna merah dan rasa asam sedikit manis, bentuk buah bulat melonjong ujungnya meruncing dan memiliki panjang 3-5 cm. Pada buah stroberi yang telah jadi ekstrak etanol berwarna merahkehitaman, ekstrak yang kental diperoleh sebanyak 86,3 g dengan rendemen 4,315%.
Rendemen = 86,3
2
x 100% = 4,315%
4.3 Skrining Fitokimia
Tabel 4.1Hasil Skrining Fitokimia buah Stroberi No. Golongan senyawa
kimia Buah stroberi segar 1. 2. 3. 4. 5. 6. Alkaloid Flavonoid Glikosida Tanin Saponin Steroid/triterpenoid – + + - + +
Keterangan : (+) = Mengandung senyawa (–) = Tidak mengandung senyawa
Hasil di atas menunjukkan buah stroberi yang telah dihaluskan mengandung golongan senyawa kimia yang sama yaitu flavonoid, glikosida, saponin dan steroid/ triterpenoid. Senyawa ini memiliki aktivitas sebagai antioksidan karena mengandung gugus hidroksil sebagai donor hidrogen atau memberi elektron dan bersifat reduktor terhadap radikal bebas (Silalahi, 2006). 4.4 Uji Preformulasi Granul
4.4.1 Sudut Diam Granul
[image:50.595.116.513.590.636.2]Hasil sudut diam granul dapat dilihat pada Tabel 4.2, berikut ini adalah hasil uji sudut diam dari berbagai variasi konsentrasi granul ekstrak buah stroberi pada formula yang dibuat.
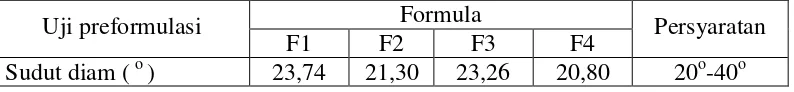
Tabel 4.2Hasil Uji Sudut Diam Granul
Uji preformulasi Formula Persyaratan
F1 F2 F3 F4
Gambar 4.1Histogram sudut diam massa granul
Dari Gambar4.1 diatas dapat dilihat sudut diam dari keempat formula tersebut memenuhi persyaratan sudut diam. Sudut diam lebih kecil sama dengan 20o biasanya bahwa bahan dapat mengalir bebas, bila sudut lebih besar atau sama dengan 40o biasanya daya mengalirnya kurang baik (Sharma, et al., 2011).
4.4.2 Waktu Alir Granul
Hasil waktu alir granul dapat dilihat pada Tabel 4.3 berikut ini adalah hasil uji waktu alir dari berbagai variasi konsentrasi granul ekstrak buah stroberi pada formula yang dibuat.
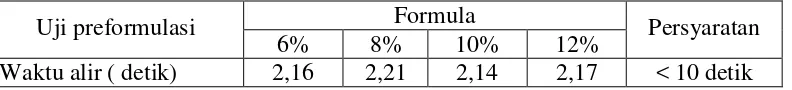
Tabel 4.3Hasil Uji Waktu Alir Granul
Uji preformulasi Formula Persyaratan
6% 8% 10% 12%
Waktu alir ( detik) 2,16 2,21 2,14 2,17 < 10 detik
23,74
21,3
23,26
20,8
19 20 21 22 23 24
F1 F2 F3 F4
(
°
)
[image:51.595.119.515.551.596.2]Gambar 4.2 Histogram waktu alir massa granul
Dari Gambar 4.2 diatas menunjukkan bahwa keempat formula memiliki waktu alir yang bervariasi akan tetapi masih memenuhi persyaratan waktu alir. Menurut (Voigt, 1995) syarat waktu alir granul lebih kecil dari 10 detik.
4.4.3 Indeks Tap Granul
Hasil indeks tap granul dapat dilihat pada Tabel 4.4 berikut ini adalah hasil uji indeks tap granul dari berbagai variasi konsentrasi granul ekstrak buah stroberi pada formula yang dibuat.
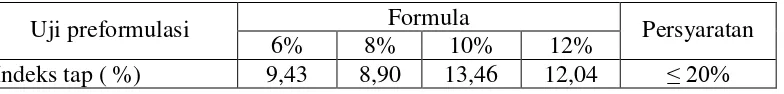
Tabel 4.4 Hasil Uji Indeks Tap Granul
Uji preformulasi Formula Persyaratan
6% 8% 10% 12%
Indeks tap ( %) 9,43 8,90 13,46 12,04 ≤ 20%
2,16
2,21
2,14
2,17
2,1 2,12 2,14 2,16 2,18 2,2 2,22
F1 F2 F3 F4
D
etik
[image:52.595.122.514.535.582.2]Gambar 4.3 Histogram indeks tap massa granul
Dari Gambar 4.3 diatas menunjukkan bahwa semakin kecil nilai dari indeks tap granul maka penyusutan volume yang terjadi akan tinggi. Diperoleh nilai indeks tap yang bervariasi, tetapi masih memenuhi persyaratan indeks tap yaitu lebih kecil dari 20% (Voigt, 1995).
4.5 Uji Evaluasi Tablet 4.5.1 Uji Homogenitas Warna
Tablet F1, F2, F3, dan F4 tidak terdapat bintik-bintik warna lain selain warna coklat setelah diamati pada permukaan atas, bawahdan sisi keliling tablet. Warna dibandingkan dengan warna standar (standart color).
4.5.2 Uji Kekerasan Tablet
Tabel 4.5 Hasil Uji Evaluasi Kekerasan Tablet
Uji evaluasi Formula Persyaratan
6% 8% 10% 12%
Kekerasan tablet (Kg) 5,75 5,43 4,77 4,49 4-8 Kg
Gambar 4.4 Histogram kekerasan tablet
Dari Gambar 4.4 diatas terlihat bahwa keempat formula tablet ini mempunyai kekerasan yang berbeda tetapi masih memenuhi persyaratan yaitu 4-8 kg. Menurut Siregar (2010). kekerasan tergantung pada bobot bahan dan celah antara punch atas dan punch bawah pada waktu pengempaan. Jika volume bahan atau jarak antara punch bervariasi, kekerasan juga bervariasi.
3.5.3Uji Friabilitas Tablet
Hasil friabilitas dapat dilihat pada Tabel 3.6, berikut ini adalah hasil uji friabilitas tablet dari berbagai variasi konsentrasi granul ekstrak buah stroberi pada formula yang dibuat.
Tabel 4.6Hasil Uji Evaluasi Friabilitas Tablet
Uji evaluasi Formula Persyaratan
6% 8% 10% 12%
Gambar 4.5 Histogram friabilitas tablet
Pada Gambar 4.5 diatas terlihat bahwa hasil friabilitas memenuhi persyaratan. Menurut Siregar (2010) menjelaskan bahwa persyaratan friabilitas yaitu maksimal 1% untuk tablet konvensional.
4.5.4 Uji Waktu Hancur Tablet
Hasil waktu hancur tablet dapat dilihat pada Tabel 3.7, berikut ini adalah hasil uji waktu hancur tablet dari berbagai variasi konsentrasi granul ekstrak buah stroberi pada formula yang dibuat.
Tabel 4.7 Hasil uji evaluasi waktu hancur tablet
Waktu Hancur Formula Persyaratan
6% 8% 10% 12%
[image:55.595.111.516.569.654.2]Gambar 4.6 Histogram waktu hancur tablet
Dari Gambar 4.6 diatas dapat dilihat bahwa keempat formula memenuhi persyaratan waktu hancur pada Farmakope Indonesia Edisi IV yaitu tidak lebih dari 15 menit.
4.5.5 Uji Keragaman Bobot
Uji keragaman bobot tablet parasetamol dapat dilihat pada Tabel 3.8 Tabel 4.8 Hasil Uji Keragaman Bobot
Formula Kadar rata – rata (%) Simpangan baku relatif (%)
F1 94,70 0,34
F2 100,35 0,16
F3 100,60 0,23
F4 100,69 0,12
Syarat 85,0% - 115,0% 6,0%
Keterangan
F1 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 6% F2 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 8% F3 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 10% F4 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 12%
[image:56.595.112.487.490.582.2]simpangan baku relatif kurang dari atau sama dengan 6,0% (Ditjen POM, 1995). 45.6 Uji Disolusi
[image:57.595.114.484.195.273.2]Uji disolusi tablet parasetamol dapat dilihat pada Tabel 4.9 Tabel 4.9 Hasil Uji Disolusi Tablet
No Formula Kadar (%)
1 F1 87,14± 0,17
2 F2 87,12± 0,12
3 F3 86,92± 0,10
4 F4 87,10 ± 0,12
Keterangan
F1 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 6% F2 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 8% F3 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 10% F4 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 12%
Berdasarkan Tabel 4.10 diatas hasil uji disolusi tablet dari keempat formula memenuhi persyaratan uji disolusi. Menurut Farmakope Indonesia Edisi IV (1995) persyaratan uji disolusi, kecuali dinyatakan lain dalam masing-masing monografi, persyaratan dipenuhi bila jumlah zat aktif yang terlarut dari sediaan yang diuji sesuai dengan tabel penerimaan. Harga Q adalah jumlah zat aktif yang terlarut seperti yang tertera dalam masing-masing monografi, dinyatakan dalam persentasi kadar pada etiket, angka 5% dan 15% dalam tabel adalah persentasi kadar pada etiket, dengan demikian mempunyai arti yang sama dengan Q. Toleransi dalam waktu 30 menit harus larut tidak kurang dari 80% (Q) parasetamol, dari jumlah yang tertera pada etiket (Ditjen POM, 1995) .
4.5.7 Uji Penetapan Kadar Parasetamol
Hasil Pembuatan Kurva Serapan Maksimum dan Kurva Kalibrasi
parasetamol BPFI dalam dapar fosfat pH 5,8 yang dilakukan diperoleh serapan maksimum pada panjang gelombang 243,0 nm dan serapan 0,433. Dengan demikian, panjang gelombang maksimum yang didapat sesuai dengan literatur.
Kurva Serapan Parasetamol BPFI dalam Dapar Fosfat pH 5,8 pada c = 6,5 mcg/mL
Data Panjang Gelombang Maksimum dan Absorbansi Parasetamol BPFI dalam Dapar Fosfat pH 5,8 pada c = 6,5 mcg/mL
Kurva Kalibrasi Parasetamol BPFI dalam Dapar Fosfat pH 5,8 secara Spektro Ultraviolet pada λ = 243,0 nm
Tabel 4.10Hasil Penetapan Kadar Tablet Parasetamol
No Formula Kadar (%)
1 F1 95,00 ± 1,36
2 F2 101,04 ± 0,55
3 F3 101,28 ± 0,38
4 F4 101,73 ± 0,14
Syarat: Kadar = 90,0%-110,0% Keterangan :
F1 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 6% F2 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 8% F3 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 10% F4 = Formula tablet parasetamol dengan konsentrasi ekstrak warna 12%
Indonesia Edisi IV. Kadar parasetamol dalam tablet berkisar antara 95,00% sampai 101,73%.
3.6 Uji Hedonik
[image:60.595.161.464.217.441.2]Data tentang nilai kesukaan warna terhadap keempat perlakuan dapat dilihat pada Gambar 4.7.
Gambar 4.7Histogram perlakuan terhadap nilai kesukaan warna
Dari Gambar 4.7 di atas dapat dilihat bahwa nilai kesukaan warna pada masing-masing konsentrasi adalah, F1 (konsentrasi 6%) memiliki nilai rata-rata sebesar 1,9 , F2 (konsentrasi 8%) memiliki nilai rata-rata sebesar 3,15 F3 (konsentrasi 10%) memiliki nilai rata-rata sebesar 2,9 dan F4 (konsentrasi 12%) memiliki nilai rata-rata sebesar 1,85. Dari histogram diatas menunjukkan bahwa F2 (konsentrasi 8%) menghasilkan nilai rata-rata paling tinggi yaitu 3,15.
Disimpulkan bahwa F2 (konsentrasi 8%) merupakan konsentrasi pewarna yang memberikan warna yang paling baik dan paling disukai panelis, sehingga konsentrasi ini dipilih sebagai pewarna tablet parasetamol anak-anak.
1,9
3,15
2,9
1,85
0 0,5 1 1,5 2 2,5 3 3,5
1 2 3 4
U
ju H
edo
ni
k
Formula
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Ekstrak buah stroberi (Fragaria vesca L.) dapatdigunakan sebagai pewarna tablet.
b. Konsentrasi ekstrak buah stroberi (Fragaria vesca L.) yang disukai sebagai pewarna tablet adalah8%.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Stroberi (Fragaria vesca L.) bukan merupakan tanaman asli Indonesia. Negara penghasil stroberi utama di dunia adalah Amerika Serikat. Negara produsen kedua setelah Amerika Serikat adalah Eropa, kemudian disusul oleh Jepang dan Meksiko. Di Amerika Serikat, terdapat 13 negara bagian penghasil stroberi. Negara bagian penghasil terbesar adalah California, kemudian menyebar ke Indonesia (Budiman dan Saraswati, 2005).
2.1.1 Sistematika tumbuhan
Sistematika buah stroberi (Fragaria vesca L.) sebagai berikut: Kingdom : Plantae
Divisi : Spermatophyta Kelas : Dicotyledoneae Bangsa : Rosales
Suku : Rosaceae Marga : Fragaria
Jenis : Fragaria vesca L. 2.1.2 Morfologi tumbuhan
Batang utama tanaman stroberi sangat pendek. Daun-daun terbentuk di setiap buku. Pada ketiak daun terdapat pucuk aksilar. Daun stroberi merupakan daun trifoliate dengan tepi bergerigi. Akar stroberi dewasa umumnya mempunyai 20- 35 akar primer dengan panjang akar sekitar 40 cm. Namun ada juga jenis stroberi yang mempunyai 100 akar primer. Akar primer dapat bertahan lebih dari satu tahun. Bunga tanaman stroberi mempunyai 5 kelopak, 5 daun mahkota, 20- 35 benang sari, dan ratusan pistil (putik) yang menempel pada dasar bunga dengan pola melingkar. Bunga tersusun dalam infloresens (malai) yang terletak di ujung tanaman. Pada kondisi pertumbuhan yang cocok, crown cabang yang muncul dari ketiak daun terakhir akan membentuk bunga pada ujungnya sehingga timbul kesan dua infloresens dalam satu tanaman. Buah stroberi berwarna merah merupakan buah semu yang sebenarnya merupakan receptacle yang membesar. Buah sejati yang berasal dari ovul yang telah diserbuki berkembang menjadi buah kering dengan biji keras. Bunga primer mempunyai jumlah pistil terbanyak, yaitu lebih dari 400 buah. Jumlah pistil pada bunga sekunder antara 200- 300 buah, sedangkan pada buah tersier hanya 50- 150 buah,oleh karena itu, ukuran buah terbesar adalah buah yang berasal dari bunga primer, kemudian disusul oleh bunga sekunder, tersier, kuartener, dan kuiner. Stolon adalah batang yang tumbuh horizontal sepanjang permukaan tanah (Budiman dan Saraswati, 2005).
2.1.3 Kandungan kimia dari stroberi
Tabel 2.1. Kandungan gizi buah stroberi segar (Depkes,RI.,1979).
Kandungan Gizi Nilai Satuan
Energi 37 kalori
Protein 0,8 g
Lemak 0,5 g
Karbohidrat 8,0 g
Kalsium 28 mg
Fosfat 27 mg
Besi 0,8 mg
Vitamin A 60 SI
Vitamin B 0,03 g
Vitamin C 60 mg
Air 89,9 g
2.1.4 Kegunaan tumbuhan
Buah stroberi pada zaman Yunani kuno diangkat sebagai lambang dewi Cinta ini mampu mencegah jantung koroner dan menekan darah tinggi. Stroberi juga bisa mengatasi masalah pencernaan, hati, rematik, radang, sendi dan encok. Buah stroberi berguna membantu penyerapan zat besi dari sayuran yang dikonsumsi. Selain itu, buah stroberi dapat membantu proses diet karena mengandung antikarsinogen Buah yang hanya sedikit mengandung gula ini juga sesuai untuk diet bagi penderita diabetes.
Buah stroberi dapat dimanfaatkan untuk kecantikan, diantaranya obat jerawat, mempercantik kulit, menjadikan gigi putih, serta meningkatkan kekuatan otak dan penglihatan (Budiman dan Saraswati, 2005).
2.1.5 Pewarna alami
Menurut Saati dan Hidayati, (2006) beberapa contoh pewarna alami yang biasa digunakan untuk mewarnai makanan yaitu :
1. Karoten, memberikan warna jingga sampai merah. Dapat diperoleh dari wortel, papaya dan sebagainya.
2. Kurkumin, berasal dari kunyit sebagai salah satu bumbu dapur dan memberikan warna kuning.
3. Antosianin, memberikan warna merah, oranye, ungu, dan biru. Banyak terdapat pada bunga dan buah-buahan seperti bunga mawar, pacar air, kembang sepatu, bunga tasbih, anggur, apel, stroberi, manggis dan lain-lain. 4. Karamel, memberikan coklat gelap dan merupakan hasil dari hidrolisis
pemecahan karbohidrat, gula pasir, laktosa dan sirup malt.
5. Klorofil, memberikan warna hijau dan diperoleh dari daun. Pigtmen klorofil banyak terdapat pada dedaunan seperti daun suji, daun pandan, daun katuk dan sebagainya. Dedauna tersebut sebagai penghasil warna hijau untuk berbagai jenis kue jajana pasar dan memiliki aroma yang khas (Saati dan Hidayati, 2006).
6. Biksin, memberikan warna kuning seperti mentega. Biksin diperoleh dari biji pohon Bixa orellana yang terdapat di daerah tropis.
7. Tanin, menghasilkan warna coklat, terdapat dalam getah. 2.16 Antosianin
Antosianin ditemukan di alam pada berbagai tumbuhan baik pada buah-bauhan maupun sauran, yang menyediakan berbagai warna ang bervariasi dari merah sampai ungu. Antosianin merupakan senyawa flavonoid yang memiliki kemampuan sebagai antioksidan. Umumnya senyawa flavonoid berfungsi sebagai antioksidan primer. Antosianin dalam bentuk aglikon lebih aktif daripada nentuk aglikosidanya. Dalam buah stroberi antosianin dapat meningkatkan kadar asam urat dalam tubuh, yang mana dapat berperan sebagai agen antioksidan dalam tubuh (Koswara, 2009).
2.2Ekstraksi
Ekstraksi adalah proses penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dalam pelarut. Simplisia yang diekstraksi mengandung senyawa aktif yang dapat larut dan senyawa yang tidak dapat larut seperti serat, karbohidrat, protein dan lain-lain (Ditjen POM, 2000). Beberapa metode ekstraksi yang sering digunakan dalam berbagai penelitian antara lain yaitu:
a.Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman menggunakan pelarut dengan sesekali pengadukan pada temperatur kamar. Maserasi yang dilakukan pengulangan penambahan pelarut setelah dilakukan penyarian terhadap maserat dan seterusnya disebut remaserasi.
b. Perkolasi
tahap pengembangan bahan, tahap maserasi antara, tahapan perkolasi sebenarnya (penetesan/penampungan ekstrak) terus-menerus sampai diperoleh perklorat.
c. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya dalam waktu tertentu pelarut akan terkondensasi menuju pendingin dan kembali ke labu.
d. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 900C selama 30 menit.
2.3 Parasetamol
2.3.1 Tinjauan umum Rumus bangun :
Rumus molekul : C8H9NO2
Nama kimia : 4-hidroksiasetanilida [ 103-90-2 ] Berat molekul : 151,16
Kandungan : Tidak kurang dari 98,0 % dan tidak lebih dari 101,0% C8H9NO2 dihitung terhadap zat anhidrat.
2.3.2 Farmakologi
Parasetamol merupakan metabolit fenasetin dengan efek antipiretik ditimbulkan oleh gugus aminobenzene. Asetaminofen di Indonesia lebih dikenal dengan nama parasetamol dan tersedia sebagai obat bebas (Wilmana, 1995).
Efek analgetik Parasetamol dapat menghilangkan atau mengurangi nyeri ringan sampai sedang. Parasetamol menghilangkan nyeri, baik secara sentral maupun secara perifer. Secara sentral diduga Parasetamol bekerja pada hipotalamus sedangkan secara perifer, menghambat pembentukan prostaglandin di tempat inflamasi, mencegah sensitisasi reseptor rasa sakit terhadap rangsangan mekanik atau kimiawi (Ganiswara, 1995).
2.4 Uraian Sediaan Tablet
Tablet adalah sediaan padat kompak, dibuat secara kempa cetak, yang mengandung satu jenis obat atau lebih, dengan atau tanpa bahan tambahan. Bahan tambahan yang dapat berfungsi sebagai bahan pengisi, bahan pengembang, bahan pengikat, bahan pelicin, bahan pembasah atau bahan lain yang cocok (Depkes RI., 1979).
Tablet dicetak dari serbuk kering, Kristal atau granulat, umumnya dengan penambahan bahan pembantu, pada mesin yang sesuai, dengan menggunakan tekanan tinggi. Tablet dapat memiliki bentuk silinder, kubus, batang atau cakram, serta bentuk seperti telur atau peluru. Garis tengah tablet pada umumnya 5-17 mm, sedangkan bobot tablet 0,1-1 g (Voigt, 1995).
Menurut Banker dan Anderson, (1994), tablet yang dinyatakan baik harus memenuhi syarat, yaitu:
2.Bebas dari kerusakan seperti pecah pada permukaan dan sisi-sisi tablet.
3.Dapat menjamin kestabilan fisik maupun kimia dari zat berkhasiat yang terkandung di dalamnya.
4.Dapat membebaskan zat berkhasiat dengan baik sehingga memberikan efek pengobatan seperti kehendaki.
Tablet dapat didefinisikan sebagai bentuk sediaan solid yang mengandung satu atau lebih zat aktif dengan satu atau tanpa berbagai eksipien (yang meningkatkan mutu sediaan tablet, kelancaran sifat aliran bebas, sifat kohesivitas, kecepatan disintegrasi, dan sifat antilekat) dan dibuat dengan mengempa campuran serbuk dalam mesin tablet (Siregar dan Wikarsa, 2010).
2.4.1 Bentuk tablet
Tablet terdapat dalam berbagai ragam bentuk, ukuran, bobot, kekerasan, ketebalan, sifat disolusi dan disintegrasi dan dalam aspek lain, tergantung pada pemggunaan yang dimaksudkan dan metode penggunaanya. Tablet biasanya berbentuk bundar dengan permukaan datar, atau konveks. Bentuk khusus seperti kaplet, segitiga, lonjong, empat segi dan segi enam dikembangkan oleh beberapa pabrik untuk membedakan produknya terhadap produk pabrik lainnya. Tablet dapat dihasilkan dalam berbagai bentuk, dengan membuat punch dan lubang kempa cetakan yang didesain secara khusus.
Tablet adalah sediaan solid mengandung zat aktif yang dapat diberikan secara oral dan ditelan, tablet yang hanya ditempatkan di dalam rongga mulut tanpa ditelan, tablet oral yang dikunyah dulu lalu ditelan, atau hanya dikulum/dihisap (Siregar dan Wikarsa, 2010).
2.4.2 Bahan pewarna tablet
membedakan dosis, spesifikasi dari pabrik, untuk memudahkan pengawasan misalnya warna yang pudar menunjukkan bahwa tablet tersebut telah rusak.
Zat warna yang dipakai harus memenuihi persyaratan Dirjen Pengawasan Obat dan Makanan Departemen Kesehatan Republik Indonesia (Koswara, 2009).
Ada 2 cara penambahan zat warna yaitu: 1. Cara basah
Bahan warna dilarutkan dalam larutan bahan pengikat kemudian ditambahkan kedalam serbuk yang akan digranulasi.
2. Cara kering
Bahan warna dicampurkan dalam keadaan kering ke dalam campuran serbuk kemudian baru ditambahkan larutan bahan pengikat. Konsentrasi zat warma yang biasa dipakai 0,33% (Soekemi, dkk., 1987).
2.4.3 Metode pembuatan sediaan tablet
Tablet dibuat dengan 3 cara umum, yaitu granulasi basah, granulasi kering dan kempa langsung. Tujuan granulasi basah dan kering adalah untuk meningkatkan aliran campuran dan atau kemampuan kempa (Depkes RI., 1995). Metode pembuatan tablet didasarkan pada sifat fisika kimia dari bahan obat, seperti stabilitas dari bahan aktif dalam panas atau terhadap air, bentuk partikel bahan aktif dan sebagiannya.
Metode pembuatan sediaan tablet yaitu a. Cetak langsung
Keuntungan utama dari cetak langsung ini adalah untuk bahan obat yang peka lembab dan panas, dimana stabilitasnya terganggu akibat pekerjaan granulasi, tetapi dapat dibuat menjadi tablet (Voigt, 1995).
b. Granulasi kering
Granulasi kering disebut juga slugging atau prekompresi. Cara ini sangat tepat untuk tabletasi zat-zat yang peka suhu atau bahan obat yang tidak stabil dengan adanya air.
Obat dan bahan pembantu pada mulanya dicetak dulu, artinya mula-mula dibua tablet yang cukup besar, yang massany tidak tertentu, selanjutnya terjadi penghancuran tablet yang dilakukan dalam mesin penggranul kering, atau dalam hal yang sederhana dilakukan diats sebuah ayakan. Granulat yang dihasilkan kemudian dicetak dengan takaran yang dikehendaki (Voigt, 1995).
Metode ini digunakan pada keadaan dosis efektif terlalu tinggi untuk pencetakan langsung, obatnya peka terhadap pemanasan, kelembaban atau keduanya (Lachman, dkk., 1994).
c. Granulasi basah
Pada teknik ini juga memerlukan langkah-langkah pengayakan, penyampuran dan pengeringan. Pada granulasi basah, granul dibentuk dengan suatu bahan pengikat. Teknik ini membutuhkan larutan, suspense atau bubur yang mengandung pengikat yang biasanya ditambahkan ke campuran serbuk.
Proses pengeringan diperlukan oleh seluruh cara granulasi basah untuk menghilangkan pelarut yang dipakai pada pembentukan gumpalan-gumpalan granul dan untuk mengurangi kelembaban sampai pada tingkat yang optimum (Banker dan Anderson, 1994).
2.4.4 Komposisi tablet
Tablet oral umumnya disamping zat aktif mengandung, pengisi, pengikat, penghancur dan pelicin.
Tablet tertentu mungkin pemacu aliran, zat warna, zat perasa dan pemanis (Lachman, dkk., 1994).
Komposisi umum dari tablet adalah zat berkhasiat, bahan pengisi, bahan pengikat atau perekat, bahan pengembang dan bahan pelicin. Kadang-kadang dapat ditambahkan bahan pewangi, bahan pewarna dan bahan-bahan lainnya (Ansel, 1989).
1. Pengisi
Digunakan agar telah memiliki ukuran dan massa yang dibutuhkan. Sifatnya harus netral secara kimia dan fisiologi, selain itu juga dapat dicerna dengan baik (Voigt, 1995).
2. Pengikat
3. Penghancur
Untuk memudahkan pecahnya tablet ketika terkontak dengan cairan saluran pencernaan dan mempermudah absorpsi (Lachman, dkk., 1994). Bahan ang digunakan sebagai pengembang yaitu: amilum, gom, derivate selulosa, alginate, dan clays (Lannie dan achmad., 2013).
4. Pelicin
Ditambahkan untuk meningkatkan daya alir granul-granul pada corong pengisi, mencegah melekatnya massa pada punch dan die, mengurangi pergesekan antara butir-butir granul, dan mempermudah pengeluaran tablet dari die. Bahan pelican yaitu : metalik stearat, talk, asam stearat, senyawa lilin dengan titik lebur tinggi, amilum maydis (Lannie dan Achmad., 2013).
2.5 Uji Preformulasi
Sebelum dicetak menjadi tablet, massa granul perlu diperiksa apakah memenuhi syarat untuk dapat dicetak. Preformulasi ini menggambarkan sifat massa sewaktu pencetakan tablet, meliputi waktu alir, sudut diam dan indeks tap 2.5.1 Waktu alir
Pengujian waktu alir dilakukan dengan mengalirkan massa granul melalui corong. Waktu yang diperlukan tidak lebih dari 10 detik, jika tidak maka akan dijumpai kesulitan dalam hal keseragaman bobot tablet (Cartensen, 1977).
2.5.2 Sudut diam
2.5.3 Indeks tap
Indeks tap adalah uji yang mengamati penurunan volume sejumlah serbuk atau granul akibat adanya gaya hentakan. Indeks tap dilakukan dengan alat volumenometer yang terdiri dari gelas ukur yang dapat bergerak secara teratur keatas dan kebawah. Serbuk atau granul yang baik mempunyai indeks tap kurang dari 20% (Cartensen, 1977).
2.6Evaluasi Tablet 2.6.1 Kekerasan tablet
Kekerasan tablet terhadap goncangan saat pengangkutan, pengemasan dan peredaran bergantung pada kekerasan tablet. Kekerasan yang lebih tinggi menghasilkan tablet yang bagus, tidak rapuh tetapi ini mengakibatkan berkurangna porositas dari tablet sehingga sukar dimasuki cairan ang mengakibatkan lamanya waktu hancur. Kekerasan dinyatakan dalam kg tenaga ang dibutuhkan untuk memecahkan tablet. Kekerasan untuk tablet secara umum yaitu 4-8 kg tablet hisap 10-20 kg, tablet kunyah 3 kg (Lannie dan Achmad., 2013).
Kekerasan tablet dipengaruhi oleh perbedaan massa granul yang mengisi die pada saat pencetakan tablet dan tekanan kompressi. Selain itu, berbedanya nilai kekerasan juga dapat diakibatkan oleh variasi jenis jumlah bahan tambahan yang digunakan pada formulasi. Bahan pengikat adalah contoh bahan tambahan yang bisa menyebabkan meningkatnya kekerasan tablet bila digunakan terlalu pekat (Lachman, dkk., 1994).
2.6.2 Friabilitas
tablet mengalami capping atau hancur akibat adanya goncangan dan gesekan, selain itu juga dapat menimbulkan variasi pada berat dan keseragaman isi tablet. Pengujian dilakukan pada kecepatan 25 rpm, menjatuhkan tablet sejauh 6 inchi pada setiap putaran, dijalankan sebanyak 100 putaran. Kehilangan berat yang dibenarkan yaitu lebih kecil dari 0,5 sampai 1% (Lachman, dkk., 1994).
Kerenyahan tablet dapat dipengaruhi oleh kandungan air dari granul dan produk akhir. Granul yang sangat kering dan hanya mengandung sedikit sekali persentase kelembapan, sering sekali menghasilkan tablet yang renyah daripada granul yang kadar kelembapannya 2 sampai 4% (Lachman, dkk., 1994).
2.6.3 Waktu hancur
Waktu hancur yaitu waktu yang dibutuhkan tablet pecah menjadi partikel-partikel kecil atau granul sebelum larut dan diabsorpsi. Menyatakan waktu yang diperlukan tablet untuk hancur di bawah kondisi yang ditetapkan dan lewatnya seluruh partikel melalui saringan mesh-10 (Lachman, dkk., 1994).
Hancurnya tablet tidak berat sempurna larutnya bahan obat dalam tablet. Tablet memenuhi syarat jika waktu hancur tablet tidak lebih dari 15 menit (Lannie dan Achmad., 2013).
Kebanyakan bahan pelican bersifat hidrofob, bahan pelican yang berlebihan akan memperlambat waktu hancur. Tablet dengan rongga-rongga yang besar akan mudah dimasuki air sehingga hancur lebih cepat daripada tablet yang keras dengan rongga-rongga yang kecil (Lannie dan Achmad., 2013).
2.6.4 Kadar zat berkhasiat
Untuk mengevaluasi kemanjuran suatu tablet, jumlah obat dalam tablet harus dipantau pada setiap tablet atau batch, begitu juga kemampuan tablet untuk melepaskan zat atau obat yang dibutuhkan harus diketahui (Lachman, dkk., 1994).
Persyaratan kadar berbeda-beda, dan tertera pada masing-masing monografi masing-masing bahan obat.
2.6.5 Keseragaman sediaan
Dapat ditentukan dengan salah satu dari dua metode :
a. Keseragaman bobot dilakukan terhadap tablet yang 50% bahan aktifnya lebih besar atau sama dengan 50 mg.
b. Keseragaman kandungan dilakukan terhadap tablet yang 50% bahan aktifnya kurang dari 50 mg (Depkes RI., 1995).
2.7 Uji Penilaian Organoleptik 2.7.1 Uji kesukaan
Uji kesukaan juga disebut uji hedonic. Dalam uji hedonic panelis dimintakan tanggapan pribadinya tentang kesukaan atau sebaliknya ketidaksukaan. Disamping panelis mengemukakan tanggapan senang, suka atau kebalikannya, mereka juga mengemukakan tingkat kesukaannya.
Tingkat-tingkat kesukaan ini disebut skala hedonik. Misalnya dalam hal “suka atau tidak suka”, dapat mempunyai skala hedonic seperti: sangat suka, suka, kurang suka, tidak suka. Skala hedonik dapat direntangkan atau diciutkan menurut rentangan skala yang dikehendaki.
2.7.2 Panel
Untuk melakukan suatu penilaian organoleptik diperlukan panel yang bertindak sebagai instrumen atau alat. Panel adalah satu atau kelompok orang bertugas untuk menilai sifat atau mutu benda berdasarkan kesan subjektif, yang menjadi anggota panel disebut panelis.
Dalam uji hedonik panelis dimintakan tanggapan pribadinya tentang kesukaan atau sebaliknya ketidaksukaan. Disamping panelis mengemukakan tanggapan senang, suka atau kebalikannya, mereka juga mengemukakan tingkat kesukaannya.
Dalam penilaian organoleptik dikenal ada macam-macam jenis panel. Penggunaan panel-panel ini dapat berbeda tergantung dari tujuan (Soekarto, 1985).
Menurut Soekarto (1985) ada 5 macam panel yang biasa digunakan dalam penilaian organoleptik yaitu:
1. panel pencicip perorangan (individual expert panel) 2. panel pencicip terbatas (small expert panel)