Informasi Dokumen
- Penulis:
- Ratih Dini Savitri
- Pengajar:
- Ir. Djoko Poernomo, B.Sc
- Dra. Pipih Suptijah, MBA
- Sekolah: Institut Pertanian Bogor
- Mata Pelajaran: Teknologi Hasil Perairan
- Topik: Aplikasi Proses Hidrolisis Enzimatis dan Fermentasi dalam Pengolahan Condiment Kupang Putih (Corbula faba H.)
- Tipe: Skripsi
- Tahun: 2011
- Kota: Bogor
Ringkasan Dokumen
I. PENDAHULUAN
Bagian ini membahas latar belakang dan tujuan penelitian. Latar belakang menjelaskan pentingnya kupang putih sebagai komoditas hasil perairan yang dapat diolah menjadi condiment. Penelitian ini bertujuan untuk menentukan rendemen kupang putih, kandungan logam berat, serta karakteristik proksimat condiment yang dihasilkan. Tujuan ini relevan dengan pendidikan tinggi dalam bidang teknologi hasil perairan dan memberikan wawasan tentang proses pengolahan makanan.
1.1 Latar Belakang
Kupang putih merupakan sumber pangan yang mudah rusak. Oleh karena itu, pengolahan yang tepat seperti fermentasi diperlukan untuk meningkatkan daya simpan dan kualitasnya. Penelitian ini bertujuan untuk mengeksplorasi metode pengolahan yang lebih efektif, yang merupakan bagian dari kurikulum pendidikan di bidang teknologi hasil perairan.
1.2 Tujuan
Penelitian ini bertujuan untuk menentukan rendemen, kandungan logam berat, dan kualitas condiment yang dihasilkan dari kupang putih. Tujuan ini memberikan kesempatan bagi mahasiswa untuk memahami dan menerapkan teknik analisis dan pengolahan makanan, sesuai dengan kompetensi yang diharapkan dalam pendidikan tinggi.
II. TINJAUAN PUSTAKA
Tinjauan pustaka mencakup deskripsi kupang putih, habitat, komposisi kimia, serta proses pembuatan condiment. Informasi ini penting untuk memberikan dasar teori yang kuat bagi mahasiswa dalam memahami karakteristik bahan baku dan proses pengolahan. Hal ini juga mencakup teknik fermentasi dan hidrolisis enzimatis yang relevan dalam konteks pengolahan makanan.
2.1 Deskripsi dan Klasifikasi Kupang Putih
Kupang putih adalah salah satu jenis kerang yang memiliki nilai gizi tinggi. Pengetahuan tentang klasifikasi dan morfologi penting untuk memahami potensi dan penggunaan kupang dalam industri makanan. Ini adalah bagian dari kurikulum yang dapat membantu mahasiswa dalam identifikasi spesies dan pemahaman biologi kelautan.
2.2 Habitat Kupang Putih
Habitat kupang putih yang spesifik di lingkungan perairan memberikan pemahaman tentang faktor-faktor yang mempengaruhi pertumbuhannya. Pengetahuan ini penting bagi mahasiswa dalam konteks pengelolaan sumber daya perairan dan konservasi.
2.3 Komposisi Kimia Kupang Putih
Mengetahui komposisi kimia kupang putih membantu mahasiswa memahami nilai gizi dan potensi pengolahan. Ini juga menjadi dasar untuk analisis proksimat yang dilakukan dalam penelitian, sehingga mahasiswa dapat menerapkan teori dalam praktik.
2.4 Condiment
Bagian ini membahas tentang condiment sebagai produk olahan dari kupang putih. Memahami proses pembuatan condiment dan kandungan gizinya sangat penting dalam pendidikan teknologi pangan, terutama dalam pengembangan produk baru.
2.5 Fermentasi
Proses fermentasi merupakan teknik pengolahan yang penting dalam industri makanan. Mahasiswa perlu memahami mekanisme fermentasi dan faktor-faktor yang mempengaruhinya untuk dapat mengaplikasikan dalam pengolahan makanan.
2.6 Enzim Bromelin
Enzim bromelin dari nenas digunakan dalam penelitian ini untuk meningkatkan efisiensi fermentasi. Pengetahuan tentang enzim dan aplikasinya dalam pengolahan pangan sangat relevan bagi mahasiswa di bidang bioteknologi dan teknologi pangan.
III. METODOLOGI
Metodologi penelitian mencakup desain percobaan, bahan, alat, dan prosedur yang digunakan. Ini penting untuk memberikan panduan kepada mahasiswa dalam melakukan penelitian dan eksperimen di laboratorium. Pemahaman tentang metodologi yang tepat sangat penting dalam pendidikan tinggi untuk memastikan validitas dan reliabilitas hasil penelitian.
3.1 Waktu dan Tempat Penelitian
Penelitian dilakukan di laboratorium yang sesuai, memberikan pengalaman praktis bagi mahasiswa dalam pengaturan penelitian. Ini juga menekankan pentingnya lingkungan laboratorium yang baik untuk menghasilkan data yang akurat.
3.2 Bahan dan Alat Penelitian
Daftar bahan dan alat yang digunakan memberikan pemahaman tentang persiapan yang diperlukan untuk eksperimen. Mahasiswa perlu memahami cara memilih dan menggunakan alat serta bahan yang tepat dalam penelitian.
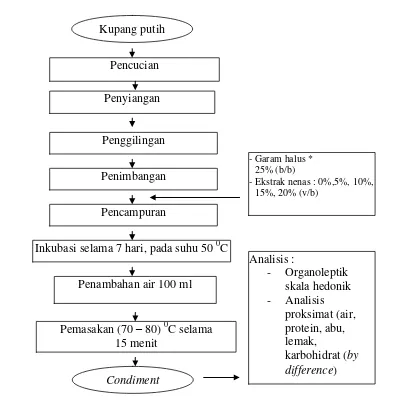
3.3 Metode Penelitian
Metode penelitian dibagi menjadi dua tahap, memberikan gambaran yang jelas tentang langkah-langkah yang harus diambil. Ini membantu mahasiswa dalam merencanakan dan melaksanakan penelitian mereka sendiri.
3.4 Prosedur Pengujian
Prosedur pengujian yang terperinci memberikan panduan bagi mahasiswa dalam melakukan analisis. Ini mencakup berbagai teknik yang relevan dalam penelitian pangan, meningkatkan keterampilan praktis mahasiswa.
IV. HASIL DAN PEMBAHASAN
Bagian ini menyajikan hasil penelitian dan analisis yang dilakukan. Memahami hasil dan interpretasinya adalah kunci dalam pendidikan penelitian. Mahasiswa belajar untuk menganalisis data dan menarik kesimpulan yang relevan dari penelitian yang dilakukan.
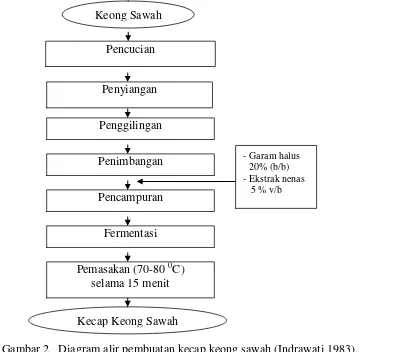
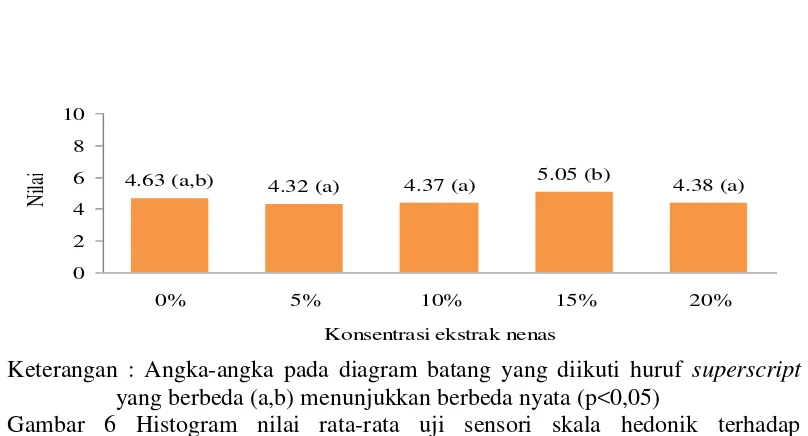
4.1 Penelitian Pendahuluan
Hasil dari penelitian pendahuluan memberikan dasar untuk penelitian utama. Ini menunjukkan bagaimana hasil awal dapat mempengaruhi desain penelitian selanjutnya, yang merupakan aspek penting dalam metodologi penelitian.
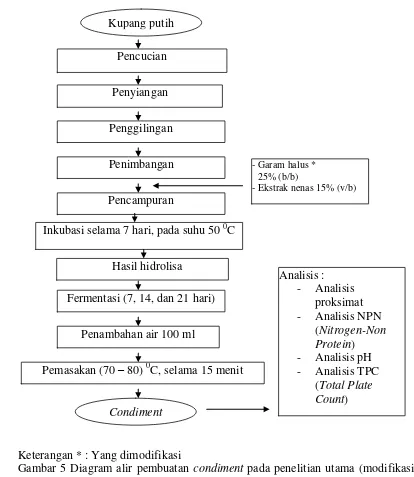
4.2 Penelitian Utama
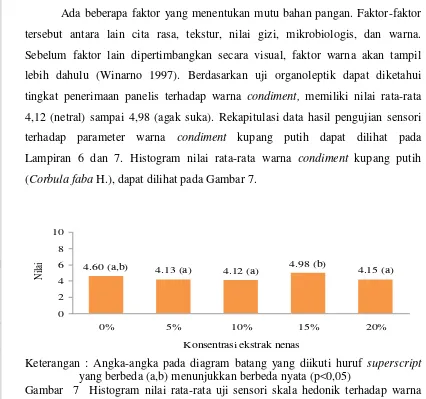
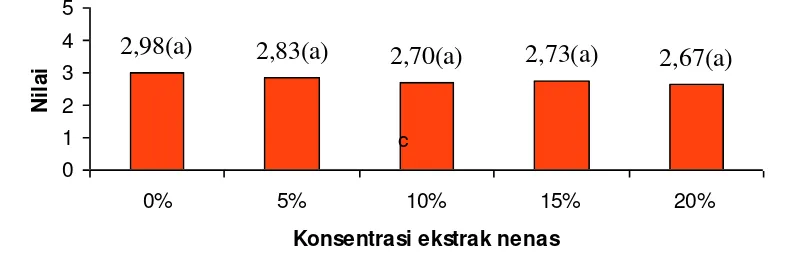
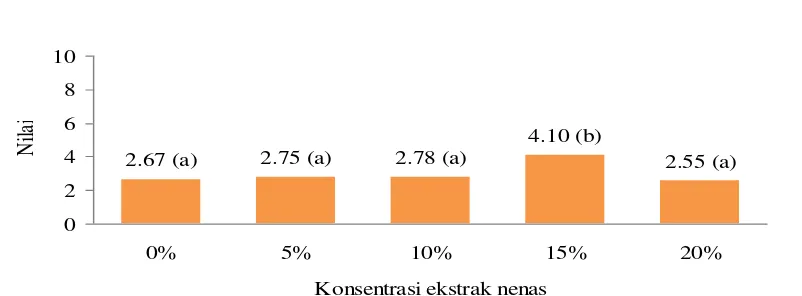
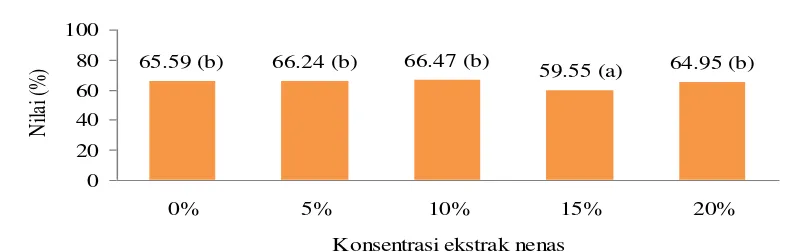
Analisis proksimat dan karakteristik lainnya dari condiment yang dihasilkan memberikan wawasan tentang kualitas produk. Ini relevan bagi mahasiswa dalam memahami hubungan antara proses pengolahan dan kualitas akhir produk.
V. KESIMPULAN DAN SARAN
Kesimpulan dari penelitian memberikan ringkasan temuan utama dan saran untuk penelitian selanjutnya. Ini penting untuk membangun keterampilan berpikir kritis mahasiswa dan memberikan arah untuk penelitian masa depan dalam bidang teknologi hasil perairan.
5.1 Kesimpulan
Kesimpulan mencakup temuan penting dari penelitian, memberikan pemahaman yang jelas tentang hasil yang diperoleh. Ini membantu mahasiswa dalam merangkum dan menyajikan hasil penelitian secara efektif.
5.2 Saran
Saran yang diberikan untuk penelitian selanjutnya menunjukkan pentingnya pengembangan berkelanjutan dalam bidang ini. Ini mendorong mahasiswa untuk terus mengeksplorasi dan berinovasi dalam penelitian mereka.