PROFIL FLAVONOID, TANIN, DAN ALKALOID DARI
EKSTRAK DAUN SIRIH MERAH (
Piper crocatum)
SUHERMANTO
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Profil Flavonoid, Tanin, dan Alkaloid dari Ekstrak Daun Sirih Merah (Piper crocatum) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini. Skripsi ini telah didanai oleh Yayasan Amanah IPB 2013 dan BPOPTN NO 231/IT3.41.2/SPK/2013.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
SUHERMANTO. Profil Flavonoid, Tanin, dan Alkaloid dari Ekstrak Daun Sirih Merah (Piper crocatum). Dibimbing oleh MEGA SAFITHRI dan SYAMSUL FALAH.
Sirih merah merupakan tanaman obat Indonesia yang telah terbukti memiliki aktivitas antihiperglikemik, antioksidan, dan antikanker. Oleh sebab itu, tujuan dari penelitian ini adalah menentukan kadar total dan menganalisis flavonoid, tanin, dan alkaloid dalam ekstrak air dan etanol 30 % daun sirih merah (Piper crocatum). Profil flavonoid, tanin dan alkaloid ditentukan dengan teknik spektofotometri, titrimetri, dan gravimetri, serta LC-MS. Identifikasi fitokimia telah membuktikan bahwa ekstrak air dan etanol 30 % mengandung flavonoid, tanin, dan alkaloid. Pengukuran flavonoid secara kuantitatif yang tertinggi terdapat pada ekstrak etanol 30 % yaitu 6.09 ± 0.26 mg QE/g. Kuantitatif tanin dan alkaloid tertinggi terdapat pada ekstrak air dengan nilai 3.97 ± 0.08 mg/g dan 543.75 ± 3.17 mg/g. Analisis LC-MS, senyawa flavonoid diduga banyak terdapat dalam ekstrak air. Senyawa tanin dan alkaloid diduga banyak terdapat dalam esktrak etanol 30 %.
Kata kunci: alkaloid, flavonoid, Piper crocatum, tanin.
ABSTRACT
SUHERMANTO. Flavonoid, Tannin, and Alkaloid Profiles of Piper crocatum leave Extract. Supervised by MEGA SAFITHRI and SYAMSUL FALAH.
Piper crocatum is Indonesia’s medicinal plant that has been proven to have anti-hyperglycemic, antioxidative, and anticancer activities. Hence, the aim of this study was to determine and analyze flavonoid, tannin, and alkaloid profiles of 30 % ethanol and water extracts of Piper crocatum leaves. Flavonoid, tannin, and alkaloid profiles were measured using spectrophotometry, titrimetry, gravimetry and LC-MS techniques. Phytochemical identification proved that both of extracts contain flanovoids, tannins, and alkaloids. Measurement of flavonoids quantitatively showed that the highest value was found in ethanol 30 % extract, 6.09 ± 0.26 mg QE/g. The highest quantitative tannin and alkaloid present in the water extract with a value of 3.97 ± 0.08 mg/g and 543.75 ± 3.17 mg/g. LC-MS analyze, the highest flavonoid compounds expected in water extract. The highest tannin and alkaloid compounds were expected in ethanol 30 % extract.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Biokimia
PROFIL FLAVONOID, TANIN, DAN ALKALOID DARI
EKSTRAK DAUN SIRIH MERAH (
Piper crocatum)
SUHERMANTO
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Profil Flavonoid, Tanin, dan Alkaloid dari Ekstrak Daun Sirih Merah (Piper crocatum)
Nama : Suhermanto NIM : G84090058
Disetujui oleh
Dr Mega Safithri, S.Si, M.Si Pembimbing I
Dr Syamsul Falah, S.Hut, M.Si Pembimbing II
Diketahui oleh
Dr Ir I Made Artika, M.App.Sc Ketua Departemen Biokimia
PRAKATA
Alhamdulillah, segala puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya. Shalawat dan salam semoga selalu tercurah kepada Nabi Muhammad SAW dan para pengikutnya sampai akhir zaman sehingga penulis dapat menyelesaikan penelitian ini. Penelitian ini berjudul “Profil Flavonoid, Tanin, dan Alkaloid dari Ekstrak Daun Sirih Merah (Piper crocatum)”. Kegiatan penelitian ini dilakukan dari bulan April hingga September 2013, bertempat di Laboratorium Biokimia IPB dan Laboratorium Kimia Fisik IPB, Laboratorium Pusat Studi Biofarmaka (PSB) IPB serta Laboratorium Balai Pengkajian Bioteknologi, Badan Pengkajian dan Penerapan Teknologi (BPPT).
Terima kasih penulis ucapkan kepada Ibu Dr. Mega Safithri, S.Si, M.Si dan Bapak Dr. Syamsul Falah, S.Hut, M.Si selaku pembimbing yang telah memberikan bimbingan dan saran. Di samping itu, penghargaan penulis sampaikan kepada Mbak Salinah dan Mas Endi beserta staf Pusat Studi Biofarmaka, serta staf Balai Pengkajian Bioteknologi, Badan Pengkajian dan Penerapan Teknologi, yang telah membantu selama proses anlisis data. Ungkapan terima kasih juga disampaikan kepada Bapak, Ibu (alm), Mimi, Supriwan, Surachman, Suhermim, sahabat Diah Ayu Lestari, Irma Handasari, Dhian, Yayuk, Nasrudin serta seluruh teman-teman Biokimia 46, atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
METODE 2
Bahan 2
Alat 2
Prosedur Percobaan 2
HASIL DAN PEMBAHASAN 6
Hasil 6
Pembahasan 10
SIMPULAN DAN SARAN 16
Simpulan 16
Saran 16
DAFTAR PUSTAKA 17
LAMPIRAN 20
DAFTAR TABEL
1 Komponen fitokimia ekstrak daun sirih merah 7
2 Hasil dugaan bobot molekul serta rumus molekul golongan flavonoid
ekstrak daun sirih merah hasil pengujian LC-MS 9
3 Hasil dugaan bobot molekul serta rumus molekul golongan tanin
ekstrak daun sirih merah hasil pengujian LC-MS 10
4 Hasil dugaan bobot molekul serta rumus molekul golongan alkaloid
ekstrak daun sirih merah hasil pengujian LC-MS 10
DAFTAR GAMBAR
1 Hasil rendemen ekstrak daun sirih merah 6
2 Hasil kadar total fenolik ekstrak daun sirih merah 7 3 Hasil kadar total flavonoid ekstrak daun sirih merah 8 4 Hasil kadar total tanin ekstrak daun sirih merah 8 5 Hasil kadar total alkaloid ekstrak daun sirih merah 9
DAFTAR LAMPIRAN
1 Bagan alir penelitian 20
2 Kadar air daun sirih merah 21
3 Contoh perhitungan rendemen ekstrak daun sirih merah 21
4 Hasil uji fitokimia 21
5 Kurva standar asam galat 22
6 Kandungan total fenolik ekstrak daun sirih merah 23
7 Kurva standar kuersetin 23
8 Kandungan total flavonoid ekstrak daun sirih merah 24 9 Kandungan total tanin ekstrak daun sirih merah 25 10 Kandungan total alkaloid ekstrak daun sirih merah 25 11 Kromatogram LC-MS golongan flavonoid ekstrak air daun sirih merah 26 12 Spektrum LC-MS golongan flavonoid ekstrak air daun sirih merah 26 13 Hasil analisis elemen puncak LC-MS golongan flavonoid ekstrak air
daun sirih merah 26
14 Kromatogram LC-MS golongan flavonoid ekstrak etanol 30 % daun
sirih merah 27
15 Spektrum LC-MS golongan flavonoid ekstrak etanol 30 % daun sirih
merah 27
16 Hasil analisis elemen puncak LC-MS golongan flavonoid ekstrak etanol
30 % daun sirih merah 27
17 Kromatogram LC-MS golongan tanin ekstrak air daun sirih merah 28 18 Spektrum LC-MS golongan tanin ekstrak air daun sirih merah 28 19 Hasil analisis elemen puncak LC-MS golongan tanin ekstrak air daun
sirih merah 28
20 Kromatogram LC-MS golongan tanin ekstrak etanol 30 % daun sirih
21 Spektrum LC-MS golongan tanin ekstrak etanol 30 % daun sirih merah 29 22 Hasil analisis elemen puncak LC-MS golongan tanin ekstrak etanol
30 % daun sirih merah 29
23 Kromatogram LC-MS golongan alkaloid ekstrak air daun sirih merah 30 24 Spektrum LC-MS golongan alkaloid ekstrak air daun sirih merah 30 25 Hasil analisis elemen puncak LC-MS golongan alkaloid ekstrak air
daun sirih merah 30
26 Kromatogram LC-MS golongan alkaloid ekstrak etanol 30 % daun sirih
merah 31
27 Spektrum LC-MS golongan alakloid ekstrak etanol 30 % daun sirih
merah 31
28 Hasil analisis elemen puncak LC-MS golongan alkaloid ekstrak etanol
PENDAHULUAN
Negara Indonesia kaya akan berbagai macam tumbuhan dengan jumlahnya yang mencapai 30.000 jenis (Rahmawati et al. 2012). Dari sekian banyak jumlah tumbuhan yang ada, sekitar 7.500 diantaranya adalah tanaman obat. Jumlah tersebut didukung dengan masyarakat Indonesia yang gemar mengonsumsi obat dari tanaman herbal (Deptan 2012). Salah satu tanaman obat yang ada di Indonesia adalah tanaman sirih merah (Piper crocatum). Daun sirih merah secara empiris memiliki banyak fungsi, diantaranya untuk mengobati diabetes melitus, asam urat, hipertensi, kanker payudara, peradangan (liver dan prostat), hepatitis, kadar kolesterol, mencegah stroke, dan lain-lain (Werdhany et al. 2008).
Fungsi tanaman sirih merah ternyata tidak hanya sebatas data empiris. Data ilmiah telah membuktikan bahwa daun sirih merah diantaranya memiliki fungsi empiris tersebut. Safithri dan Fahma (2008) adalah peneliti yang telah membuktikan bahwa air rebusan daun sirih merah memiliki fungsi antihiperglikemik yaitu dapat menurunkan kadar glukosa darah tikus sebesar 38%. Selain dengan air rebusan daun sirih merah, ekstrak etanol 70% dari daun sirih merah memiliki aktivitas antidiabetogenik melalui aktivitas antioksidasi (Alfarabi et al. 2010). Adapun fungsi lainnya yang telah dibuktikan melalui riset ilmiah diantaranya antikanker payudara (Wicaksono et al. 2009), aktivator enzim glukosa oksidase (Agustianti 2008), dan antiinflamasi (Fitriyani 2011).
Berbagai macam fungsi yang dimiliki oleh daun sirih merah disebabkan oleh metabolit sekunder yang terkandung didalamnya. Hasil penelitian yang dilakukan oleh Safithri dan Fahma (2005) serta Salim (2006) menunjukkan bahwa rebusan air dari daun sirih merah mengandung alkaloid, flavonoid dan tannin. Menurut Marlina (2008) ekstrak etanol 30 % dan rebusan air daun sirih merah mengandung senyawa flavonoid, alkaloid dan tanin. Kandungan flavonoid, tanin, dan alkaloid merupakan kandungan terbesar dari metabolit sekunder daun sirih merah. Data penelitian menyebutkan bahwa daun sirih merah selalu memiliki kandungan flavonoid, tanin dan alkaloid (Salim 2006; Marlina 2008; Agustianti 2008; Fitriyani 2011). Kandungan tersebut juga membuat daun sirih merah memiliki fungsi yang penting sebagai tanaman obat herbal dan menjadikannya terkenal dalam khasanah obat herbal.
Senyawa flavonoid, akaloid, dan tanin yang terdapat dalam daun sirih merah belum diketahui jenis golongannya dan hanya sebatas data fitokimia belum berdasarkan jumlah totalnya. Ada kemungkinan bahwa jika diekstraksi dengan dua pelarut yang berbeda yaitu air dan etanol 30 %, kemungkinan besar kandungan yang dimiliki keduanya berbeda. Kandungan metabolit sekunder terbanyak bisa jadi terdapat pada etanol 30 % atau bahkan sebaliknya. Oleh sebab itu perlu dilakukan pengkajian dan penelitian lebih lanjut untuk mengetahui kadar total senyawa flavonoid, alkaloid, dan tanin pada daun sirih merah (Piper crocatum).
2
menambah informasi ilmiah baru dalam beberapa jenis senyawa metabolit sekunder pada flavonoid, tanin dan alkaloid.
METODE
NH4OH pekat, NH4OH 1 %, asam asetat, aseton, asam askorbat, etil asetat, dietil eter, n-heksan, kloroform, metanol, n-butanol, asetonitril, 0.1 % asam format, FeCl3, pereaksi Dragendrof, Mayer, dan Wagner.Alat
Peralatan yang digunakan adalah alat refluks, kapas, alat freeze dry, rotary evaporator, sentrifuse, spektrofotometer UV-VIS, corong pisah, alat-alat gelas, alat titrasi, waterbath, kertas saring, timbangan, oven, dan alat LC-MS (UPLC-QToF-MS/MS System (Waters) dengan kolom yang digunakan yaitu Acquity UPLC BEH C18 1.7 µm, 2.1x50 mm. Biotek, BPPT Serpong, Tangerang).
Prosedur Percobaan
Pengeringan Bahan Uji
Daun sirih merah yang akan diteliti dikumpulkan. Setelah itu dilakukan pencucian dengan air yang mengalir dan ditiriskan. Selanjutnya tanaman dirajang dan dikeringkan dalam oven pada suhu 50 °C selama 5 hari. Daun sirih merah yang sudah kering dilakukan penggilingan untuk mendapatkan serbuk dengan ukuran 60 mesh.
Penentuan Kadar Air
Penentuan kadar air simplisia daun sirih merah menggunakan metode SNI 01-2891-1992 yang termodifikasi. Cawan porselin dikeringkan dalam oven 105 °C selama 3 jam, kemudian ditempatkan dalam desikator selama 1 jam. Setelah itu ditimbang dengan neraca sartorius (a). Lalu ke dalam cawan ditambahkan sebanyak 2.0-2.5 g sampel (b). Cawan yang berisi sampel ditempatkan dalam oven 105 °C selama 3 jam. Setelah itu ditempatkan dalam desikator selama 1 jam. Bobot cawan dan sampel ditimbang (c). Pengeringan dilakukan beberapa kali sampai bobot sampel yang diperoleh konstan. Analisis dilakukan 3 kali ulangan untuk masing-masing sampel.
% Bobot kering (BK) = c-a
3 Pembuatan Ekstrak Etanol 30% Daun Sirih Merah
Ekstraksi daun sirih merah menggunakan metode Depkes (2000) yang dimodifikasi. Serbuk kering daun sirih merah diekstraksi dengan metode refluks. Serbuk kering daun sirih merah sebanyak 100 g diekstraksi dengan 1 L etanol 30% selama 2 jam pada suhu 70 °C menggunakan alat refluks. Ekstrak yang diperoleh kemudian disaring dengan kertas saring. Ekstraksi diulang tiga kali. Hasil ekstrak dilakukan freeze dry sehingga diperoleh ekstrak kasar daun sirih merah.
Pembuatan Ekstrak Air Daun Sirih Merah
Ekstraksi daun sirih merah menggunakan metode Depkes (2000) yang dimodifikasi. Serbuk kering daun sirih merah diekstraksi dengan metode refluks. Serbuk kering daun sirih merah sebanyak 100 g diekstraksi dengan 1 L air selama 2 jam pada suhu 100 °C menggunakan alat refluks. Ekstrak yang diperoleh kemudian disaring dengan kertas saring. Ekstraksi diulang tiga kali. Hasil ekstrak dilakukan freeze dry sehingga diperoleh ekstrak kasar daun sirih merah.
Analisis Fitokimia
Uji flavonoid (Harbone 1987). Sebanyak 0.1 g ekstrak daun sirih merah dimasukkan ke dalam gelas piala kemudian ditambahkan 10 mL air panas dan didihkan selama 5 menit. Setelah itu, disaring dan filtratnya digunakan untuk pengujian. Filtrat dimasukkan ke dalam tabung reaksi lalu ditambahkan 0.5 g serbuk Mg, 1 mL HCl pekat, dan 1 mL amil alkohol kemudian dikocok dengan kuat. Positif flavonoid ditandai dengan terbentuknya warna merah, kuning, atau jingga pada lapisan amil alkohol.
Uji tanin (Harbone 2007). Sebanyak 1.0 g ekstrak daun sirih merah ditambahkan air kemudian didihkan selama beberapa menit. Setelah itu larutan ditambahkan FeCl3. Terbentuknya warna biru atau hijau kehitaman menunjukkan adanya tanin.
Uji alkaloid (Harbone 2007). Sebanyak 0.5 g ekstrak daun sirih merah dimasukkan ke dalam tabung reaksi dan ditambahkan 10 mL kloroform dan beberapa tetes amoniak. Fraksi kloroform dipisahkan dan diasamkan dengan H2SO4. Fraksi H2SO4 diambil kemudian ditambahkan pereaksi Dragendrof, Mayer, dan Wagner. Terdapatnya alkaloid ditandai dengan terbentuknya endapan putih pada pereaksi Mayer, endapan merah pada pereaksi Dragendrof, dan endapan cokelat pada pereaksi Wagner.
Penentuan Kadar Total Fenolik Ekstrak Daun Sirih Merah
4
Penentuan Kadar Total Flavonoid
Metode Chang et al. (2002) digunakan untuk penentuan kadar flavonoid. Sebanyak 0.5 ml ekstrak daun sirih merah (tiga kali ulangan) dengan konsentrasi 50000 mg/L, ditambahkan 1.5 mL metanol, setelah itu dimasukkan 0.1 AlCl3 10%, kemudian potasium asetat 1 M, dan terakhir tambahkan akuades 2.8 mL. Selanjutnya dilakukan inkubasi selama 30 menit, diukur pada panjang gelombang 415 nm. Total flavonoid ekstrak daun sirih merah diekspresikan sebagai miligram (mg) kuersetin per gram bobot ekstrak kering (mg QE/g ekstrak daun sirih merah). Sebagai standar digunakan kuersetin pada berbagai konsentrasi (0, 50, 100, 150, 200, 250, 300 mg/L).
Penentuan Kadar Total Tanin
Penentuan kadar total tanin menggunakan metode Depkes (1979). Ekstrak sebanyak 0.2 g dimasukkan dalam labu Erlenmeyer 250 mL yang sudah ditambahkan dengan air mendidih 5 mL. Setelah itu dipanaskan selama 30 menit di atas penangas air. Selanjutnya didiamkan selama beberapa menit dan dituang ke dalam labu takar 25 mL dengan menggunakan segumpal kapas sebagai penyaring. Residu yang tertinggal ditambahkan dengan air mendidih yang kemudian disaring lagi dengan kapas sampai esktrak tanin habis. Setelah selesai, cairan didinginkan dan ditambahkan dengan air sampai tanda tera. Pipet sebanyak 2.5 mL larutan ke dalam labu takar 100 mL, kemudian ditambahkan dengan 2.5 mL indigokarmin sulfonat LP dan air sampai tanda tera. Tahap akhir, titrasi dengan KMnO4 0.1 N hingga larutan berwarna kuning emas. Larutan blanko dibuat dengan prosedur yang sama tanpa sampel. Sebanyak 1 mL KMnO4 0.1 N setara dengan 0.004157 g tanin.
Kadar tanin (%) =
VKMnO4sampel- VKMnO4blankoX 0.0041571 mL
bobot sampel awal X 100 %
Penentuan Kadar Total Alkaloid
Penentuan kadar total alkaloid menggunakan metode Harbone (1987) yang dimodifikasi. Ekstrak kasar 6 g diasamkan dengan asam sulfat 2 M sampai pH 3. Setelah mencapai pH 3, diekstraksi dengan kloroform sebanyak 3 kali sampai lapisan kloroform menjadi tidak berwarna atau bening. Fase air-asam dibasakan dengan amonium hidroksida sampai pH 9 lalu diekstraksi dengan kloroform-metanol (3:1) sebanyak 2 kali. Tahap ini telah didapatkan residu kasar alkaloid total. Selanjutnya dipisahkan antara ekstrak kloroform-metanol dan ekstrak air-basa. Masing-masing diuji kualitatif terhadap alkaloid sebelum dikeringkan.
Ekstrak kloroform-metanol dikeringkan dengan natrium sulfat anhidrat kemudian dipekatkan dan setelah itu ekstrak ditimbang bobotnya (Y). Ekstrak air-basa diuapkan lalu diekstraksi dengan metanol dan diuapkan kembali. Setelah itu dipekatkan dan ditimbang (z). Jumlah alkaloid total yang terkandung di dalam daun sirih merah adalah:
Kadar total alkaloid (%) = Y+Z
5 Keterangan:
X = bobot simplisia yang diekstraksi. Y = bobot klorom : metanol.
Z = bobot air : basa. Fraksinasi Flavonoid
Ekstrak pekat etanol 30 % dan juga air dilarutkan dalam air, diaduk terus sampai encer dan homogen, kemudian dimasukkan dalam corong pisah yang berbeda (ekstrak air dan etanol 30 %). Setelah itu difraksinasi berturut-turut secara ekstraksi cair-cair dengan pelarut heksan, kloroform, dietileter, etilasetat, dan n-butanol. Langkah awal difraksinasi dengan pelarut n-heksan sebanyak 40 mL, diperoleh fraksi n-heksan dan fraksi air. Fraksi n-heksan dipisahkan, kemudian fraksi air difraksinasi dengan kloroform sebanyak 40 mL, diperoleh fraksi kloroform dan fraksi air. Fraksi kloroform dipisahkan, kemudian fraksi air difraksinasi dengan dietil eter, diperoleh fraksi dietil eter dan air. Fraksi air selanjutnya difraksinasi dengan etil asetat, diperoleh fraksi etil asetat dan fraksi air. Fraksi etil asetat dipisahkan, dan fraksi air ditambahkan dengan n-butanol. Fraksi terakhir dipekatkan. Fraksinasi dilakukan sebanyak tiga kali dengan menggunakan 40 mL pelarut untuk sekali fraksinasi (Modifikasi Budzianowski et al. 1985 dalam Heryani 2002).
Fraksinasi Tanin
Fraksinasi tanin menggunakan metode Makkar (1985). Ekstrak pekat etanol 30 % dan air dilarutkan dalam air panas pada dua tempat yang berbeda, diaduk sampai homogen kemudian disaring dan dimasukkan dalam corong pisah yang berbeda. Selanjutnya, diekstraksi dengan n-heksana, fraksi n-heksana dipisahkan. Fraksi air diekstraksi dengan aseton:air (70:30) dengan asam askorbat 0.1 %. Fraksi air:aseton dipisahkan dan fraksi air dicuci dengan kloroform, cucian dibuang. Fraksi air diekstrasi lagi dengan etil asetat, diperoleh fraksi etil asetat dan fraksi air. Fraksi etil asetat dipisahkan dan hasil akhir yaitu fraksi air dipekatkan dan didapatkan ekstrak tanin. Fraksinasi dilakukan sebanyak tiga kali dengan menggunakan 40 mL pelarut untuk sekali fraksinasi.
Fraksinasi Alkaloid
Fraksinasi alkaloid menggunakan metode Martono (1983). Ekstrak etanol 30 % dan air direndam dengan asam asetat 10 % dalam etanol (minimal 4 jam). Hasil rendaman disaring dan filtrat dipekatkan sampai ¼ volume awal. Setelah itu ditambahkan NH4OH pekat tetes demi tetes sampai terbentuk endapan. Endapan dipisahkan dengan sentrifuse. Hasilnya dicuci dengan NH4OH 1 %. Endapan dilarutkan dalam kloroform + HCL 10 % (kocok kuat). Hasilnya akan terbentuk dua fase, yaitu fase air dan kloroform. Fase kloroform ditambahkan dengan NH4OH 10 % sampai alkalis yang kemudian ditambahkan dengan kloroform. Fase air di buang dan fase kloroform dipekatkan.
Analisis Flavonoid, Tanin, dan Alkaloid
6
dipisahkan melalui HPLC atau UPLC, sampel akan masuk kedalam detektor massa. Selanjutnya sampel tersebut diubah menjadi fase gas, kemudian ion tersebut akan terionisasi dalam kondisi vakum. Ion-ion tersebut diakselerasi oleh medan elektrik atau magnetik, yang terukur sebagai rasio massa terhadap muatan (m/z), dan akan terdeteksi berdasarkan kelimpahan masing-masing ion (Rouessac dan Rouessac 2007). Hasil fraksinasi diinjeksikan ke dalam alat LC-MS. Spesifikasi LC-MS yang digunakan adalah sebagai berikut. Alat UPLC-QToF-MS/MS System (Waters). Kolom Acquity UPLC BEH C18 1.7 µm, 2.1x50 mm. Fase gerak yang digunakan berupa H2O + 0.1% formic acid, dan Acetonitrile + 0.1% formic acid. Suhu yang digunakan 40 °C. Laju alir yang digunakan sebesar 0.3 mL/min dengan volume yang diinjeksikan sebesar 5 µL.
HASIL DAN PEMBAHASAN
Hasil
Kadar Air Ekstrak Daun Sirih Merah
Kadar air daun sirih merah diperoleh melalui cara pengeringan. Pengeringan dilakukan menggunakan oven pada suhu 50 °C selama 5 hari. Hasil pengeringan dipastikan daun sudah berada dalam keadaan benar-benar kering. Kadar air yang didapatkan sebesar 6.52 ± 0.01 %.
Rendemen Ekstrak Daun Sirih Merah
Ekstraksi daun sirih merah dilakukan dengan metode refluks yang menggunakan perbedaan suhu. Ekstrak etanol 30 % dilakukan pada suhu 70 °C dan 100 °C untuk air. Hasilnya bahwa ekstrak etanol 30 % memiliki rendemen lebih besar daripada ekstrak air yaitu 14.83 % (Gambar 1).
Gambar 1 Hasil rendemen ekstrak daun sirih merah Komponen Fitokimia Ekstrak Daun Sirih Merah
7 Tabel 1 Komponen fitokimia ekstrak daun sirih merah
Keterangan:
(+) = mengandung senyawa (-) = tidak mengandung senyawa Total Fenolik Ekstrak Daun Sirih Merah
Hasil pengukuran kandungan fenolik pada ekstrak daun sirih merah menunjukkan perbedaan diantara ekstrak air dan etanol 30 %. Ekstrak etanol 30 % memiliki kandungan fenolik lebih banyak dibandingkan dengan ekstrak air. Kandungan fenolik pada ekstrak etanol 30 % yaitu 34.6 ± 4.90 mg GAE/g (Gambar 2).
Gambar 2 Hasil kadar total fenolik ekstrak daun sirih merah Total Flavonoid Ekstrak Daun Sirih Merah
8
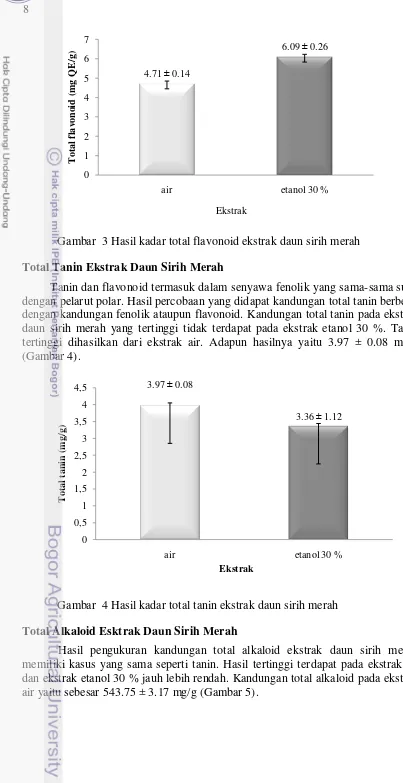
Gambar 3 Hasil kadar total flavonoid ekstrak daun sirih merah Total Tanin Ekstrak Daun Sirih Merah
Tanin dan flavonoid termasuk dalam senyawa fenolik yang sama-sama suka dengan pelarut polar. Hasil percobaan yang didapat kandungan total tanin berbeda dengan kandungan fenolik ataupun flavonoid. Kandungan total tanin pada ekstrak daun sirih merah yang tertinggi tidak terdapat pada ekstrak etanol 30 %. Tanin tertinggi dihasilkan dari ekstrak air. Adapun hasilnya yaitu 3.97 ± 0.08 mg/g (Gambar 4).
Gambar 4 Hasil kadar total tanin ekstrak daun sirih merah Total Alkaloid Esktrak Daun Sirih Merah
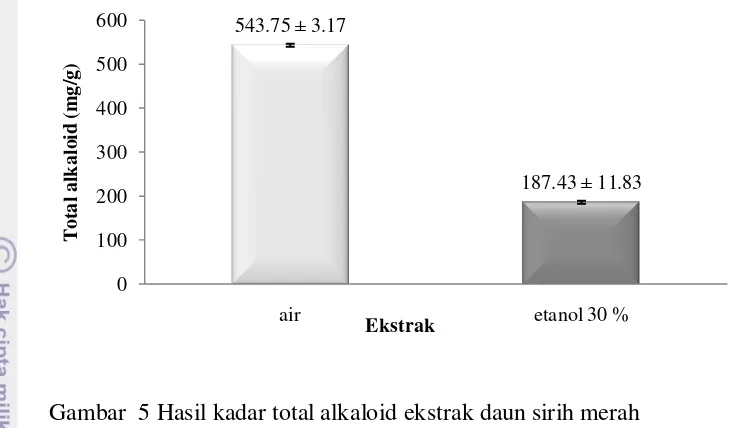
Hasil pengukuran kandungan total alkaloid ekstrak daun sirih merah memiliki kasus yang sama seperti tanin. Hasil tertinggi terdapat pada ekstrak air dan ekstrak etanol 30 % jauh lebih rendah. Kandungan total alkaloid pada ekstrak air yaitu sebesar 543.75 ± 3.17 mg/g (Gambar 5).
9
Gambar 5 Hasil kadar total alkaloid ekstrak daun sirih merah Hasil Analisis LC-MS Ekstrak Daun Sirih Merah
Hasil analisis LC-MS berdasarkan pada bobot molekul dari golongan senyawa yang ingin dianalisis. Golongan flavonoid pada ekstrak air diduga memiliki senyawa terbanyak yaitu sembilan jenis bobot molekul yang berarti diduga memiliki sembilan golongan flavonoid. Ekstrak etanol memiliki tujuh senyawa yang diduga sebagai golongan flavonoid (Tabel 2). Hasil kromatogram dari senyawa flavonoid pada masing-masing ekstrak mempunyai puncak tertinggi. Puncak tertinggi flavonoid pada ekstrak air mempunyai waktu retensi 4.47 (Lampiran 11) dengan bobot molekul 450.2034 (m/z). Puncak tersebut diduga memiliki rumus molekul C27H30O6. Ekstrak etanol 30 % memiliki puncak tertinggi yang terletak pada waktu retensi 2.54 (Lampiran 14) dan bobot molekul 578.1639 (m/z) serta rumus molekul C27H30O14.
Tabel 2 Hasil dugaan bobot molekul serta rumus molekul golongan flavonoid ekstrak daun sirih merah hasil pengujian LC-MS
Ekstrak Air Ekstrak Etanol
Bobot Molekul (m/z) Rumus Molekul Bobot Molekul (m/z) Rumus Molekul
10
Ekstrak air memiliki puncak tertinggi pada waktu retensi 4.21 (Lampiran 17) dengan bobot molekul 148.0152 (m/z), dan rumus molekul C8H4O3. Ekstrak etanol 30 % yaitu 2.54 (Lampiran 20) dengan bobot molekul 578.1639 (m/z), dan rumus molekul C27H30O14.
Tabel 3 Hasil dugaan bobot molekul serta rumus molekul golongan tanin ekstrak daun sirih merah hasil pengujian LC-MS
Ekstrak Air Ekstrak Etanol
Bobot Molekul (m/z) Rumus Molekul Bobot Molekul (m/z) Rumus Molekul
148.0152 C8H4O3 148.0158 C8H4O3
442.2209 C22H34O9
578.1639 C27H30O14
Hasil senyawa alkaloid sama dengan tanin bahwa pendugaan senyawa alkaloid banyak terdapat pada ekstrak etanol 30 % dibandingkan dengan ekstrak air yaitu sembilan (Tabel 4). Puncak tertinggi pada senyawa alkaloid memiliki waktu retensi yang hampir sama yaitu 4.48 untuk ekstrak air dan 4.42 untuk ekstrak etanol 30 %. Selain waktu retensi kesamaan juga terjadi pada bobot molekulnya yaitu 400.1879 (m/z), dan 400. 1870 (m/z). Pendugaan bobot molekul pada puncak tertinggi tidak dimasukkan kedalam hasil pada Tabel 4. Hal tersebut disebabkan bukan senyawa golongan alkaloid.
Tabel 4 Hasil dugaan bobot molekul serta rumus molekul golongan alkaloid ekstrak daun sirih merah hasil pengujian LC-MS
Ekstrak Air Ekstrak Etanol
Bobot Molekul
Kadar Air Simplisia Daun Sirih merah
11 akan menghasilkan mutu simplisia yang tahan lama dalam proses penyimpanan serta tidak merubah kandungan bahan aktif yang terdapat dalam simplisia (Manoi 2006).
Kadar air yang didapatkan sesuai dengan standar yang diberikan oleh Farmakope Herbal Indonesia (Depkes 2008) dibawah 10 % yaitu 6.52 ± 0.01 %. Selain Farmakope Herbal Indonesia, keputusan tersebut terdapat juga didalam Keputusan Menteri Kesehatan RI No. 661/Menkes/SK/VII/1994 tentang Persyaratan Obat Tradisional. Keputusan tersebut menyatakan bahwa standar maksimum simplisia adalah 10 %, dengan demikian keamanan dan kondisi bahan aktif pada simplisia daun sirih merah dapat terjaga dalam waktu yang lama.
Rendemen Ekstrak Daun Sirih Merah
Ekstraksi daun sirih merah menggunakan metode refluks. Metode refluks dilakukan karena ekstraksi daun sirih merah pernah dilakukan dengan cara direbus dan hasilnya masih mengandung metabolit sekunder (Safithri dan Fahma 2008; Salim 2006). Penjelasan tersebut dapat dikatakan bahwa prinsip metode refluks hampir sama dengan perebusan yaitu dengan menggunakan panas (Mawaddah 2008), oleh sebab itu dilakukan metode refluks. Adapun perbedaanya hanya terletak pada kondensor yang terdapat pada alat refluks.
Alasan lain menggunakan metode ini karena mempunyai beberapa kelebihan yaitu komponen terekstrak dengan sempurna, hemat, dan waktu yang dibutuhkan lebih cepat dan singkat karena adanya panas (Mawaddah 2008). Pelarut yang digunakan untuk ekstraksi yaitu air dan etanol 30 %. Kedua pelarut digunakan berdasarkan penelitian sebelumnya oleh Safithri dan Fahma (2008), Marlina (2008) serta Alfarabi (2010) yang menyatakan kedua pelarut memiliki senyawa aktif dalam daun sirih merah. selain itu juga didalam penggunaan aplikasi obat herbal, pelarut polar seperti etanol sering digunakan untuk pembuatan jamu dan obat-obatan fitofarmaka (Darusman et al. 2001).
Hasil ekstraksi daun sirih merah berupa gumpalan serbuk. Proses ekstraksi tersebut menghasilkan rendemen yang berbeda. Hasil Rendemen menunjukkan bahwa ekstrak etanol 30 % memiliki rendemen lebih besar dibandingkan dengan ekstrak air (Gambar 1). Perbedaan hasil rendemen salah satu kemungkinannya disebabkan oleh perbedaan pelarut. Kepolaran pelarut akan menentukan komponen bioaktif dan metabolit sekunder yang terkandung dalam sirih merah. Selain kepolaran, pemanasan atau suhu akan berpengaruh juga terhadap kelarutan ekstrak jika dibandingkan tanpa pemanasan (Pambayun et al. 2007). Hasil rendemen yang didapatkan menunjukkan kadar metabolit sekunder yang terbawa oleh pelarut dan tidak dapat menentukan jenis senyawanya (Ukieyanna 2012). Dengan demikian dapat diduga bahwa pelarut etanol 30 % dalam ekstrak daun sirih merah dapat menarik senyawa lebih banyak dari ekstrak air.
Komponen Fitokimia Ekstrak Daun Sirih Merah
12
Identifikasi fitokimia ekstrak air dan etanol 30 % ternyata terbukti memiliki kandungan flavonoid, tanin dan alkaloid (Tabel 1). Hasil yang didapatkan berdasarkan pembentukan warna yang terjadi akibat pereaksi yang digunakan. Senyawa flavonoid positif dengan ditunjukkannya warna kuning serta warna hijau untuk tanin. Senyawa alkaloid diuji dengan menggunakan tiga pereaksi alkaloid yaitu pereaksi Dragendrof (positif endapan merah), Mayer (positif endapan putih) dan Wagner (positif endapan cokelat) (Harbone 2007).
Selain itu berdasarkan penelitian sebelumnya telah dikatakan bahwa pelarut air dan etanol 30 % dapat menarik senyawa dengan hasil fitokimia yang sama (Agustianti 2008). Hasil tersebut telah terbukti seperti yang telah dilakukan oleh Salim (2006) dan Agustianti (2008) bahwa ekstrak air dan etanol sama-sama menghasilkan senyawa metabolit sekunder flavonoid, tanin, dan alkaloid. Dengan demikian bahwa pelarut air dan etanol 30 % dapat mengekstraksi tiga senyawa metabolit sekunder tersebut.
Total Fenolik Ekstrak Daun Sirih Merah
Pengujian fenolik dilakukan dengan tujuan untuk mengetahui keseluruhan dari golongan fenolik. Seperti yang telah diketahui bahwa flavonoid dan tanin termasuk dalam golongan fenolik. Senyawa fenolik juga menrut Deore et al. (2009) merupakan senyawa yang telah mempunyai banyak fungsi seperti antioksidan, antitumor, dan antiviral serta antibiotik. Sehingga sangat perlu untuk mengetahui kadar totalnya. Prinsip yang digunakan dalam penentuan kadar fenolik yaitu berdasarkan metode Folin-Ciocalteau.
Prinsipnya bahwa terjadinya reaksi antara senyawa fenol dengan reagen Folin-Ciocalteau. Reaksinya melibatkan transfer elektron dari senyawa fenolik dengan campuran asam fosfotungstat atau asam molibdat dalam reagen dan membentuk warna biru yang diukur absorbansinya (Kusumaningati 2009). Warna biru inilah yang bisa menandakan banyak atau tidaknya kandunggan fenolik. Hal itu terjadi pada saat pengukuran absorban. Warna biru yang lebih pekat akan menghasilkan absorbansi yang tinggi, degan kata lain sebanding antara warna dengan kandugan fenolik (Dai dan Mumper 2010). Selain itu asam galat digunakan sebagai standar karena asam galat termasuk dalam senyawa fenolik yang banyak terdapat pada tumbuhan. Asam galat juga termasuk senyawa yang lebih murni dan lebih stabil (Kusumaningati 2009).
Kandungan fenolik ekstrak etanol 30 % lebih tinggi dibandingkan dengan ekstrak air (Gambar 2). Hasil tersebut mempunyai kasus yang sama apabila dibandingkan dengan hasil kadar fenolik pada daun surian dengan pelarut etanol 70 % dan air. Pelarut etanol pada esktrak daun surian mempunyai kadar fenolik terbesar dibandingkan dengan air yaitu 500.30 mg/g GAE dan 465.30 mg/g GAE (Haryadi 2012). Apabila dibandingkan antara daun surian dan sirih merah, kadar fenolik daun surian memiliki kandungan yang lebih besar dari daun sirih merah.
13 Etanol dan air merupakan pelarut yang memiliki gugus hidroksil. Namun, gugus hidroksil pada etanol dapat berikatan dengan ikatan hidrogen intramolekuler pada gugus hidroksil senyawa fenolik. Hal tersebut menyebabkan peningkatan kelarutan senyawa fenolik dalam etanol (Murnah 2011). Menurut Tiwari et al. (2011) etanol merupakan pelarut yang efektif untuk senyawa fenolik karena tingkat kepolarannya yang rendah dibandingkan dengan air. Hal itu menyebabkan dinding sel pada tumbuhan yang kurang polar mudah terdegradasi dan senyawa fenol mudah keluar dari sel tanaman. Selain itu Septiana et al. (2002) menyatakan bahwa pelarut organik yang semipolar lebih mudah mengekstrak senyawa fenolik. Oleh sebab itu kandungan fenolik tertinggi ada pada ekstrak etanol 30 %.
Total Flavonoid Ekstrak Daun Sirih Merah
Kadar flavonoid ini ditentukan untuk mengetahui jumlah flavonoid pada ekstrak yang diduga berpotensi atau bahkan merupakan senyawa yang paling berperan pada daun sirih merah.Pengukuran kadar total flavonoid mengacu pada metode Chang et al. (2002) yang disebut juga metode AlCl3. Standar yang digunakan adalah kuersetin. Kuersetin digunakan karena akan memberikan kestabilan reaksi terhadap pereaksi yang digunakan yaitu AlCl3. Selain itu Chang et al. (2002) juga menyatakan bahwa flavonoid yang terukur adalah jenis flavon dan flavonol dan dua golongan tersebut merupakan senyawa yang akan membentuk kestabilan dengan AlCl3.
Total flavonoid yang dihasilkan dari percobaan menunjukkan bahwa ekstrak etanol 30 % memiliki total flavonoid tertinggi dibandingkan dengan ekstrak air (Gambar 3). Hasil tersebut sama halnya dengan total fenolik yang dipengaruhi oleh kepolaran senyawa terhadap pelarut. Stankovic et al. (2011) menyatakan bahwa kandungan flavonoid tertinggi terdapat pada pelarut dengan kepolaran sedang. Ekstrak etanol 30 % bersifat tidak terlalu polar jika dibandingkan dengan air. Flavonoid akan cenderung terlarut lebih banyak pada ekstrak etanol 30 %.
Kadar total flavonoid pada ekstrak daun sirih merah mempunyai kandungan yang sedikit apabila dibandingkan dengan tanaman herbal lain yang menggunakan kuersetin sebagai standar. Tanaman herbal lain seperti daun surian dengan pelarut etanol 70 % dan air memiliki kandungan flavonoid sebesar 62.96 mg/g QE dan 92.10 mg/g QE (Haryadi 2012). Selain daun surian, daun beluntas juga mempunyai kadar flavonoid yang besar yaitu 2163.59 mg/100g QE (Widyawati 2011).
Total Tanin Ekstrak Daun Sirih Merah
14
Ekstrak air memiliki kadar tanin yang tertinggi dibandingkan ekstrak etanol 30 %. Hasil tersebut tidak salah karena senyawa tanin suka terhadap pelarut polar seperti air. Alasan lain bahwa senyawa tanin yang salah satunya adalah tanin terhidrolisis termasuk senyawa yang hidrofilik. Senyawa hidrofilik adalah senyawa yang suka air. Peristiwa tersebut juga terjadi pada penelitian yang dilakukan oleh Marnoto et al. (2012) bahwa ekstrak etanol teknis yang lebih banyak mengandung air mempunyai kadar yang lebih tinggi dibandingkan dengan metanol. Kepolaran air yang membuat senyawa tanin lebih banyak terdapat pada ekstrak air.
Total Alkaloid Ekstrak Daun Sirih Merah
Senyawa alkaloid banyak ditemukan pada tumbuhan diberbagai bagian seperti biji, daun, ranting, dan kulit batang. Kandungan alkaloid salah satunya terdapat dalam daun sirih merah. Sifat alkaloid adalah bersifat basa, sehingga penentuan ekstraksi alkaloid lebih banyak menggunakan pelarut alkohol yang bersifat asam lemah (Harbone 1986). Proses penentuan total alkaloid menggunakan prinsip gavimetri yaitu penimbangan secara langsung yang sebelumnya telah diekstraksi dengan pelarut alkaloid.
Ada dua jenis pengukuran yang dilakukan dalam pengukuran alkaloid dalam satu prosedur. Pertama penimbangan total alkaloid berdasarkan fase kloroform-metanol dan kedua adalah fase air-basa. Kedua fase tersebut dipilih untuk penentuan alkaloid. Pemilihan kedua fase tersebut disebabkan senyawa alkaloid mempunyai sifat yang berbeda ketika diekstraksi. Alkaloid dapat larut dalam pelarut bersifat basa dan juga pelarut organik (kloroform). Alkaloid yang bersifat basa ada yang bersifat larut dan tidak larut dalam air (Besilla 1981 dalam Rolandani 2001). Hasil tertinggi kadar total alkaloid terdapat dalam ekstrak air. Dengan demikian alkaloid yang bersifat basa dan larut dalam air banyak terkandung dalam ekstrak air daun sirih merah.
Hasil Analisis LC-MS Ekstrak Daun Sirih Merah
Analisis flavonoid, tanin, dan alkaloid menggunakan Liquid Chromatography-Mass Spectroscopy (LC-MS). LC-MS digunakan untuk analisis metabolit sekunder karena mempunyai sensitivitas yang lebih tinggi. Alat ini juga dapat digunakan untuk analisis kuantitatif maupun analisis struktural sehingga senyawa akan lebih terdeteksi dengan baik. Analisis senyawa flavonoid dari tanaman juga sering dilakukan dengan LC-MS (Fabre et al. 2001). Theodoridis et al. (2008) juga menyatakan bahwa LC-MS sering digunakan dalam bidang bioanalisis serta dapat menentukan profil metabolit sekunder karena mampu memisahkan senyawa dengan resolusi yang tinggi.
15 bervariasi (Lampiran 11, Lampiran 14, Lampiran 17, Lampiran 20, lampiran 23, Lampiran 26).
Analisis yang dilakukan masih dalam tahap awal yaitu ekstrak secara kasar sehingga puncak yang bervariasi karena ekstrak yang diuji belum sepenuhnya murni. Namun demikian, dari hasil yang didapatkan masih bisa dianalisis senyawa dengan bobot molekul berapa saja yang termasuk kedalam golongan flavonoid, tanin, dan juga alkaloid. Analisis data dilakukan melalui beberapa tahapan dengan menggunakan program yang sesuai dan salah satunya yaitu software MassLynk versi 4.1 (dilakukan di Laboratorium Biotek, BPPT Serpong). Hasil analisis dugaan metabolit sekunder golongan flavonoid, tanin, dan alkaloid ditunjukkan pada Tabel 2, 3 dan 4. Berdasarkan hasil tersebut diketahui bahwa ekstrak air dan ekstrak etanol 30 % memiliki kandungan yang berbeda.
Perbedaan tersebut disebabkan oleh ketertarikan senyawa terhadap tingkat kepolaran suatu pelarut. Penelitian ini menggunakan pemisahan dengan tingkat kepolaran yang berbeda yaitu diantaranya n-heksan, kloroform, dietil eter, etil asetat, n-butanol, dan aseton. Semua larutan yang digunakan mempunyai tingkat kepolaran yang berbeda dari yang polar sampai dengan non polar. Pelarut n-heksan mempunyai sifat non-polar, sedangkan dietil eter, eteil asetat dan aseton pelarut yang semi polar. Dengan demikian senyawa yang mempunyai sifat kepolaran yang sama dengan pelarut akan tertarik pada pelarut yang sesuai (Markom et al. 2007).
Selain pelarut, senyawa flavonoid dan alkaloid juga memiliki perbedaan kepolaran. Seperti pada senyawa flavonoid, flavonoid mempunyai dua sifat kelarutan yaitu polar dan semi polar. Senyawa flavonoid yang bersifat polar mudah larut dalam pelarut polar seperti air. Senyawa yang semi polar akan sangat larut pada pelarut semi polar seperti dietil eter, dan etil asetat. Flavonoid yang polar karena berikatan dengan gula yang disebut glikon flavonoid, sedangkan flavonoid semi polar tidak berikatan dengan gula yang dikenal dengan aglikon flavonoid (Lenny 2006).
Sampel yang digunakan untuk analisis LC-MS adalah fraksi akhir dari proses fraksinasi baik ekstrak air maupun ekstrak etanol 30 %. Fraksinasi flavonoid memiliki fraksi akhir campuran air:butanol. Senyawa tanin pada proses fraksinasi memiliki fraksi akhir air. Sementara itu, senyawa alkaloid memiliki fraksi akhir kloroform. Oleh sebab itu memberikan hasil yang berbeda pada hasil analisis LC-MS.
Flavonoid fraksi air:butanol tertinggi pada ekstrak air dan diduga bahwa senyawa flavonoid yang tertarik merupakan senyawa yang bersifat polar yaitu termasuk dalam glikon flavonoid, sedangkan senyawa yang bersifat semi polar sebagian akan tertarik pada pelarut dietil eter serta etil asetat sehingga kandungannya sedikit pada ekstrak etanol 30 %. Hal tersebut juga terjadi pada senyawa alkaloid fraksi kloroform. Senyawa alkaloid sebagian larut dalam pelarut air dan banyak larut dalam pelarut organik. Hasil akhir dari pemisahan menggunakan pelarut organik yaitu kloroform. Selain kloroform etanol juga merupakan pelarut organik, sehingga gabungan kedua pelarut tersebut menyebabkan kandungan alkaloid hasil analisis LC-MS terbanyak pada ekstrak etanol 30 %.
16
tersebut tidak bisa dilakukan karena banyaknya senyawa yang terdeteksi dalam satu kromatogram. Seperti puncak tertinggi pada alkaloid, puncak tertinggi yang dihasilkan bukan termasuk golongan alkaloid karena tidak mengandung atom N pada rumus molekulnya. Hasil analisis hanya memiliki atom C, H dan O. Satu kromatogram LC-MS alkaloid tidak hanya mengandung senyawa alkaloid akan tetapi senyawa lain juga ikut terdeteksi.
Namun demikian, ada beberapa puncak tertinggi pada golongan flavonoid yang dapat ditentukan senyawanya melaului database. Puncak tertinggi pada flavonoid dengan bobot molekul 450.2034 dan 578.1639 yang memiliki rumus molekul C27H30O6 dan C27H30O14 dapat ditentukan melalui database pada buku Andersen dan Markham tentang senyawa flavonoid. Andersen (2006) dalam bukunya menyebutkan bahwa senyawa dengan bobot molekul 450.52 dengan rumus molekul C27H30O6, terdapat dua senyawa golongan isoflavonoid yaitu Flemiphilippinin B dan Glabrescione B. Bobot molekul 578.53 dengan rumus molekul C27H30O14 memiliki 7 senyawa isoflavonoid diantaranya Coromandelin, Biochanin A7-O-(6’’-apiosylglucoside), Biochanin A7-O-(6’’-xylosylglucoside), Genistein 7-O-neohesperidoside, Genistein 7-O-rutinoside, Tectorigenin 7
-O-(6’’-xylosylglucoside), Daidzein 7,4’-O-diglucoside. Hasil database menunjukkan bahwa dalam satu bobot molekul dan rumus molekul yang sama terdapat lebih dari satu senyawa. Oleh sebab itu masih belum bisa ditentukan senyawanya secara pasti. Selain itu menurut Sunaryanto (2011) LC-MS hanya bersifat memprediksi suatu senyawa dengan bobot molekul, sedangakan untuk memastikan secara akurat dibutuhkan analisis lanjut untuk elusidasi rumus molekul dengan alat analisis lain seperti NMR dan juga FTIR.
SIMPULAN DAN SARAN
Simpulan
Ekstrak air dan etanol 30 % daun sirih merah memiliki kandungan flavonoid, tanin dan alkloid. Kadar flavonoid tertinggi terdapat pada ekstrak etanol 30%, sedangkan ekstrak air lebih banyak mengandung tanin dan alkaloid. Analisis golongan senyawa flavonoid diduga lebih banyak terdapat pada ekstrak air, sedangkan golongan senyawa tanin dan alkaloid diduga banyak terdapat pada ekstrak etanol 30 %.
Saran
17
DAFTAR PUSTAKA
Agustianti L. 2008. Potensi daun sirih merah (Piper crocatum) sebagai aktivator enzim glukosa oksidase [skripsi]. Bogor (ID): Institut Pertanian Bogor. Alfarabi M, Bintang M, Suryani, Safithri M. 2010. The comparative ability of
antioxidant activity of Piper crocatum in inhibiting fatty acid oxidation and free radical scavenging. Hayati J. Biosci 17(4):201-204.
Andersen ØM, Markham KR. 2006. Flavonoids : Chemistry, Biochemistry, and Applications. New York (US): CRC Press.
Chang C, Yang M, Wen H, Chern J. 2002. Estimation of total flavonoid content in propolis by two complementary colorimetric methods. J Food Drug Analaysis 10: 178-182.
Dai J, Mumper RJ. 2010. Plant phenolic: extraction, analysis and their antioxidant and anticancer properties. Molecules 15 : 7313-7352.
Darusman LK, Rohaeti E, Sulistiyani. 2001. Kajian senyawa golongan flavonoid asal tanaman bangle sebagai senyawa peluruh lemak melalui aktivitas lipase [laporan penelitian]. Bogor (ID): Pusat Studi Biofarmaka Lembaga Penelitian, IPB.
Day RA, Underwood AL. 1999. Analisis Kimia Kuantitatif. Jakarta (ID): Erlangga. Deore SL, Khadabadi SS, Baviskar BA, Khangenbam RA, Koli US, Daga NP,
Gadbail PA, jain PA. 2009. Invitro antioxidant activity and phenolic conten of Croton caudatum. International Journal of Chemical Technology Research 1(2):174:176.
[Depkes] Departemen Kesehatan. 1979. Materia Medika Indonesia. Jakarta (ID): Depkes RI.
[Depkes] Departemen Kesehatan. 2000. Parameter standar umum ekstrak tumbuhan obat. Jakarta (ID): Depkes RI.
[Depkes] Departemen Kesehatan. 2008. Farmakope Herbal Indonesia. Edisi I. Jakarta (ID): DepKes RI.
[Deptan] Departemen Pertanian. 2012. Tanaman Obat Indonesia capai 7500 [internet]. [diacu 2013 agustus 18]. Tersedia dari: http://eksim.deptan. go.id/setjenew/berita-tanaman-obat-indonesia-capai-7500-spesies.html. Fabre N, Rustan I, De Hoffmann E, Quetin-Leclerq J. 2001. Determination of
flavone, flavonol, flavonone aglycones by negative ion liquid chromatography electrospry ion trap mass spectrometry. J AmSoc Mass Spectrum 12: 707-715.
Fitriyani A, Winarti L, Muslichah S, Nuri. 2011. Uji anti inflamasi ekstrak metanol daun sirih merah (Piper crocatum Ruiz & Pav) pada tikus putih. Majalah Obat Tradisional 16(1):34-42.
Harbone JB, Turner BI. 1986. Plant Chemosystematic. London (GB): Academic press.
Harbone JB. 1987. Metode Fitokimia Penuntun Cara Modern Menganalisa Tumbuhan Ed ke-3. Bandung (ID): ITB.
18
Haryadi D. 2012. Senyawa fitokimia dan sitotoksisitas ekstrak daun surian (Toona sinensis) terhadap Sel Vero dan MCF-7 [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Heryani H. 2002. Kajian fraksi aktif dan formulasi tabat barito (Ficus deltoida Jack) sebagai antimikroorganisme klinis [tesis]. Bogor (ID): Institut Pertanian Bogor.
Hagerman AE. 2002. Tannin Chemistry. Miami (US): Miami University.
Javanmardi J, Stushnoff C, Locke E, Vivanco JM. 2003. Antioxidant activity and total phenolic content of Iranian Ocimum accessions. J Food Chem 83: 547-550.
Kusumaningati RW. 2009. Analisis kandungan fenol total jahe (Zingiber officinale Roscoe) secara in vitro [skripsi]. Jakarta (ID): Universitas Indonesia.
Lenny S. 2006. Senyawa Flavonoid, Fenilpropanoida dan Alkaloida. Medan (ID): USU.
Makkar HPS, Bocker. 1985. Isolation of tannins from leaves of some trees and shurbs and their proper ties. J. Agric Food Chem 42.
Manoi F. 2006. Pengaruh pengeringan terhadap mutu simplisia sambiloto. Bul. Littro. 17(1):1-5.
Markom M, Hasan M, Daud WRW, Singh H, Jaim JM. 2007. Extraction of hydrolysable tannins from Phyllanthus niruri Linn:Effects of solvents and extraction methods. Separation and Purification Technology 52: 487-496. Marlina PWN. 2008. Konsentrasi flavonoid dan lethal concentration 50 (LC 50)
ekstrak daun sirih merah (Piper crocatum) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Marnoto T, Haryono G, Gustinah D, Putraa FA. 2012. Esktraksi tannin sebagai bahan pewarna alami dari tanaman putrimalu (Mimosa pudica) menggunakan pelarut organik. Reaktor 14(1):39-45.
Martono S. 1983. Isolasi dan identifikasi zat aktif berkhasiat analgetik pada daun Gendarussa vulgaris Nees [laporan penelitian]. Yogyakarta (ID): Universitas Gadjah Mada.
Mawaddah R. 2008. Kajian hasil riset potensi antimikroba alami dan aplikasinya dalam bahan pangan di pusat informasi teknologi pertanian fateta IPB [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Murnah. 2011. Pengaruh ekstrak etanol mengkudu (Morinda citrifolia L) terhadap diabetik nefropati pada tikus Sprague dawley yang diinduksi Streptozotocin (STZ) dengan kajian VEGF dan mikroalbuminuria (MAU) [tesisi]. Semarang (ID): Universitas Diponegoro.
Pambayun R, Gardjito M, Sudarmadji S, Kuswanto KR. 2007. Kandungan fenol dan sifat antibakteri dari berbagai jenis ekstrak produk gambir (Uncaria gambir Roxb). Majalah Farmasi Indonesia 3:141-146.
Rahmawati U, Suryani E, Mukhlason A. 2012. Pengembangan Repository Pengetahuan Berbasis Ontologi (Ontology-Driven Knowledge Repository)Untuk Tanaman Obat Indonesia. J Teknik Pomtis 1(1):1-6. Rolandani J. 2001. Pengaruh fiksasi nitrogen kacang tanah dan taraf nitrogen
19 Rouessac F, Rouessac A. 2007. Chemical Analysis: Modern Instrumentation
Methods and Techniques 2th ed. England (GB): John wiley & Sons.
Safithri M, Fahma F. 2005. Potensi rebusan daun sirih merah (Piper crocatum) sebagai senyawa antihiperglikemia pada tikus putih galur sparague dawley [laporan penelitian]. Bogor (ID): LPPM IPB.
Safithri M, Fahma F. 2008. Potency of Piper crocatum decoction as an antyhiperglycemia in rat strain Sparague dawley. Hayati J. Biosci 15(1):45-48.
Salim A. 2006. Potensi rebusan sirih merah (Piper crocatum) sebagai senyawa antihiperglikemia pada tikus putih galur Sprague-Dawley [skripsi]. Bogor (ID): Institut Pertanian Bogor
Septiana AT, Muchtadi D, Zakaria FR. 2002. Aktivitas antioksidan ekstrak diklorometana dan air jahe pada asam linoleat. Jurnal Teknol dan Industri Pangan 13(2):105-110.
[SNI] Standar Nasional Indonesia. 1992. SNI 01-2891-1992.Cara uji makanan dan minuman. Jakarta (ID): Dewan Standardisasi Nasional.
Stankovic MS, Niciforovic N, Topuzovic M, Solujic S. 2011. Total phenolic content, flavonoid noncentrations and antioxidant activity, of the whole plant and plant parts extracts from Teuchium montanum L. var. Montanum, F. supinum (L.) Reichenb [catatan penelitian]. Biotechnol. & Biotechnol. Eq 25(1):2222-2227.
Sunaryanto R. 2011. Isolasi, purifikasi, identifikasi, dan optimasi medium fermentasi antibiotik yang dihasilkan oleh aktinomisetes laut [disertasi]. Bogor (ID): Institut Pertanian Bogor.
Tiwari P, Kumar B, Kaur G, Kaur H, Kaur M. 2011. Phytochemical screening and extraction : A review. J Int Pharm Sci 1 : 98-106
Theodoridis G, Helen GG, Wilson ID. 2008. LC-MS-based methodology for global metabolite profilling in metabonomics/metabolomics. Trends in anal Chem 27:251-260.
Ukieyanna E. 2012. Aktivitas antioksidan, kadar fenolik, dan flavonoid total tumbuhan suruhan (Peperomia pellucida L. Kunth) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Werdhany I, Marton A, Setyorini W. 2008. Sirih Merah. Yogyakarta (ID): Balai Pengkajian Teknologi Pertanian Yogyakarta.
Wicaksono BD, Ayupriyanti Y, Handoko, Arung ET, Kusuma IW, Yulia D, Pancaputra AN, Sandra F. 2009. Antipoliferative effect of methanol extract of Piper crocatum Ruiz & Pav leaves on human breast (T47D) cells in-vitro. Trop J Pharm Res 8(4): 345-352.
20
LAMPIRAN
Lampiran 1 Bagan alir penelitian
Ekstraksi dengan metode refluks
Analisis senyawa (LC-MS) Pengeringan oven (50 °C selama 5 hari)
1. Flavonoid 2. Alkaloid 3. Tanin
Ekstrak air dan etanol
30 %
Flavonoid (ekstrak air dan ekstrak
etanol)
Tanin (ekstrak air dan ekstrak
etanol)
Alkaloid (ekstrak air dan ekstrak
etanol) 1. Fenolik 2. Flavonoid 3. Tanin 4. Alkaloid Fraksinasi
Analisis kadar total Uji fitokimia
21 Lampiran 2 Kadar air daun sirih merah
No Ulangan
Bobot simplisia X 100%
= 28.2347 g – 26.3612 g
Lampiran 3 Contoh perhitungan rendemen ekstrak daun sirih merah Bobot simplisisa terkoreksi = Bobot simplisia – kadar air
= 100 – 6.52 = 93.48
% Rendemen etanol 30 % = Bobot ekstrak
Bobot simplisia terkoreksi
x
100 %= 13.86
93.48
x
100 %= 14.83 % Lampiran 4 Hasil uji fitokimia
Uji Ekstrak
air Etanol 30 %
22
Lanjutan lampiran 4
Tanin
Alkaloid
Dagendrof
Mayer
Wagner
Lampiran 5 Kurva standar asam galat
Konsentrasi (ppm) Absorbansi (A)
0 0
20 0.161
40 0.2659
60 0.40025
80 0.5495
100 0.6505
y = 0.006x + 0.012 R² = 0.996
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7
0 20 40 60 80 100 120
Ab
sor
b
a
n
si
(
A)
23 Lampiran 6 Kandungan total fenolik ekstrak daun sirih merah
Contoh perhitungan: 1. Total fenolik ekstrak
Persamaan kurva standar asam galat :y = 0.006x + 0.012 Absorbansi rata-rata = 0.006x + 0.012 (total fenolik)
0.506 = 0.006x + 0.012 (total fenolik)
C = konsentrasi total fenolik dari kurva standar V = volume ekstrak
Lampiran 7 Kurva standar kuersetin
Konsentrasi (ppm) Absorbansi (A)
24
Lampiran 8 Kandungan total flavonoid ekstrak daun sirih merah Ulangan
Persamaan kurva standar kuersetin :y = 0.002x + 0.011 Absorbansi rata-rata = 0.002x + 0.011 (total flavonoid)
0.484 = 0.002x + 0.011 (total flavonoid) Total flavonoid = 0.484 - 0.011
0.002
= 236,67 mg/L
2. Total flavonoid GAE
Total felavonoid GAE (C) = c (V/m). FP Keterangan:
C = konsentrasi total flavonoid dari kurva standar V = volume ekstrak
m = berat ekstrak FP = faktor pengenceran
Diketahui:c = 236.67 mg/L, V = 10 ml = 0.01 L, m = 1.004 g Total flavonoid GAE (C) = 236.67 mg/L (0.01 L/1.004 g). 2
25 Lampiran 9 Kandungan total tanin ekstrak daun sirih merah
jenis ekstrak volume (mL)
VKmnO4sampel- VKmnO4blankoX
0.004157
Lampiran 10 Kandungan total alkaloid ekstrak daun sirih merah
Ekstrak Ulangan Bobot
1 1.1375 0.0026 1.1401 6.0109 18.96721 189.67
2 1.0527 0.0584 1.1111 6.0000 18.51833 185.18
Rerata 1.1256 6.0054 18.74277 187.43
SD 0.0205 0.0077 0.317403 3.1740
Air 1 2.9325 0.2838 3.2163 6.0074 53.53897 535.39
2 2.8785 0.4342 3.3127 6.0000 55.21167 552.12
26
Lampiran 11 Kromatogram LC-MS golongan flavonoid ekstrak air daun sirih merah
Lampiran 12 Spectrum LC-MS golongan flavonoid ekstrak air daun sirih merah
Lampiran 13 Hasil analisis elemen puncak LC-MS golongan flavonoid ekstrak air daun sirih merah
27 Lampiran 14 Kromatogram LC-MS golongan flavonoid ekstrak etanol 30 % daun
sirih merah
Lampiran 15 Spectrum LC-MS golongan flavonoid ekstrak etanol 30 % daun sirih merah
28
Lampiran 17 Kromatogram LC-MS golongan tanin ekstrak air daun sirih merah
Lampiran 18 Spectrum LC-MS golongan tanin ekstrak air daun sirih merah
29 Lampiran 20 Kromatogram LC-MS golongan tanin ekstrak etanol 30 % daun sirih
merah
Lampiran 21 Spectrum LC-MS golongan tanin ekstrak etanol 30 % daun sirih merah
30
Lampiran 23 Kromatogram LC-MS golongan alkloid ekstrak air daun sirih merah
Lampiran 24 Spectrum LC-MS golongan alkloid ekstrak air daun sirih merah
31 Lampiran 26 Kromatogram LC-MS golongan alkloid ekstrak etanol 30 % daun
sirih merah
Lampiran 27 Spectrum LC-MS golongan alkloid ekstrak etanol 30 % daun sirih merah
32
RIWAYAT HIDUP
Penulis dilahirkan di Indramayu pada tanggal 07 Oktober 1990 dari ayah Mista dan ibu Tarmi (alm). Penulis adalah putra keempat dari empat bersaudara. Tahun 2009 penulis lulus dari SMA Negeri 6 Cirebon dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB dan diterima di Departemen Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis menjadi asisten praktikum Struktur dan Fungsi Subseluler pada tahun ajaran 2012/2013, asisten Biokimia Klinis tahun ajaran 2012/2013, dan asisten AKBID tahun 2013. Penulis juga aktif dalam organisasi kampus sebagai Anggota Biro funrising Himpunan Keprofesian Mahasiswa Biokimia (CREBs) periode 2010-2011, Anggota UKM Gentra Kaheman 2010-2011, staf Profesi dan Keahlian UKM Gentra Kaheman 2011-2012, wakil ketua Profesi dan Keahlian UKM Gentra Kaheman 2012-2013.