KARAKTERISTIK MALTODEKSTRIN HASIL HIDROLISIS
PATI GADUNG (
Dioscorea hispida
Dennst)
SECARA ENZIMATIS
TESIS
Oleh
SYARIFAH ENITA SARI
127051010
PROGRAM STUDI MAGISTER ILMU PANGAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISTIK MALTODEKSTRIN HASIL HIDROLISIS
PATI GADUNG (
Dioscorea hispida
Dennst)
SECARA ENZIMATIS
TESIS
Oleh
SYARIFAH ENITA SARI
127051010
Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains Pada Program Studi Magister Ilmu Pangan Fakultas Pertanian Universitas Sumatera Utara
PROGRAM STUDI MAGISTER ILMU PANGAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
Judul Tesis : Karakteristik Maltodekstrin Hasil Hidrolisis Pati Gadung (Dioscorea hispida Dennst) Secara Enzimatis
Nama : Syarifah Enita Sari
NIM : 127051010
Program Studi : Magister Ilmu Pangan
Menyetujui Komisi Pembimbing,
(Prof. Dr. Ir. Zulkifli Lubis, M.App.Sc) (Dr.Ir. Herla Rusmarilin. MP) Ketua Anggota
Mengetahui :
Ketua Program Studi Dekan
(Dr. Ir. Elisa Julianti, M.Si) (Prof. Dr. Ir. Darma Bakti, MS)
PERNYATAAN
Dengan ini penulis menyatakan bahwa tesis dengan judul “Karakteristik Maltodekstrin Hasil Hidrolisis Pati Gadung (Dioscorea hispida Dennts) Secara
Enzimatis” adalah benar merupakan gagasan dan hasil penelitian saya sendiri,
dibawah arahan komisi pembimbing. Semua data dan sumber informasi yang digunakan dalam tesis ini telah dinyatakan secara jelas dan dicantumkan dalam daftar pustaka dibagian akhir tesis serta dapat diperiksa kebenarannya.
Tesis ini juga belum pernah diajukan untuk memperoleh gelar pada Program Studi sejenis di Perguruan Tinggi lain. Apabila di emudian hari ditemukan seluruh atau sebagian tesis ini bukan hasil karya penulis sendiri atau adanya plagiat dalam bagian-bagian tertentu, penulis bersedia menerima sanksi pencabutan gelar akademik yang penulis sandang dan sanksi-sanksi lainnya sesuai dengan peraturan perundangan yang berlaku .
Medan, April 2015
KARAKTRISTIK MALTODEKSTRIN HASIL DARI
HIDROLISIS PATI GADUNG (
Dioscorea hispida
Dennst)
SECARA ENZIMATIS
ABSTRAK
Beberapa jenis Dioscorea yang tumbuh di Indonesia belum dimanfaatkan secara maksimal, salah satunya umbi gadung. Gadung (Dioscorea hispida Dennst) adalah jenis umbi yang tumbuh liar di hutan dan tidak begitu sulit mendapatkannya. Memiliki potensi untuk dimanfaatkan sebagai sumber maltodekstrin. Maltodekstrin merupakan polimer dari glukosa dengan panjang ikatan rata-rata 5-10 unit rantai glukosa per molekul. Maltodekstrin adalah turunan pati yang dihasilkan dari degradasi rantai amilosa dan amilopektin secara kimia atau enzimatis menjadi dekstrin. Maltodekstrin memiliki DE dari 3-20. Penelitian ini bertujuan untuk mengetahui pengaruh pH dan waktu likuifikasi terhadap kualitas maltodesktrin dan hasil hidrolisis enzimatis pati umbi gadung.
Penelitian ini menggunakan metode enzimatis, dengan penambahan enzim amilase. Analisis data menggunakan Rancangan Acak Lengkap (2 faktor 3 ulangan). Hasil penelitian menunjukkan bahwa pH 5, 6 dan 7, waktu likuifikasi 60, 90 dan 120 menit dan interaksi pH dan waktu likuifikasi memberi pengaruh yang berbeda sangat nyata terhadap gula reduksi, dekstrosa equivalen, daya larut, viskositas, daya serap dan rendemen maltodesktrin. pH yang paling optimal adalah 6, waktu likuifikasi yang paling optimal adalah 90 dan 120 menit.
CHARACTERISTIC MALTODEKSTRIN HYDROLYSIS OF STARCH YAM (
Dioscorea hispida
Dennst) ENZYMATICALLY
ABSTRACT
Some of types Dioscorea that grows in Indonesia have not been fully utilized, one yam tubers. Yam (Dioscorea hispida Dennst) is a type of bulb that grows wild in the woods and not so difficult to get. Has the potential to be used as a source of maltodextrin. Maltodextrin is a polymer of glucose with an average bond length of 5-10 units per molecule of glucose chains. Maltodextrin is a starch derivative resulting from the degradation of amylose and amylopectin chains chemically or enzymatically into dextrin. Maltodextrin has a DE of 3-20. This study aimed to determine the effect of pH and liquefaction time to maltodesktrin quality and enzymatic hydrolysis of starch yam tubers.
This study uses the enzymatic method, with the addition of enzyme. Analysis of the data using a completely randomized design (2 factor 3 replications). The results showed that pH 5, 6 and 7, liquefaction time 60, 90 and 120 minutes and the interaction of pH and time likuifikasi gave highly significant effect on reducing sugar, dextrose equivalent, solubility, viscosity, absorption and yield maltodesktrin. The most optimal pH was 6, the most optimal liquefaction time was 90 and 120 minutes.
RIWAYAT HIDUP
Syarifah Enita Sari, dilahirkan di Aceh Barat, pada tanggal 27 Maret 1982
anak dari Bapak H. Said Razali dan Ibu Hj. Syarifah Rahmah.Penulis merupakan
anak ke enam dari enam bersaudara. Syarifah Enita Sari telah menikah dengan
Musriadi, ST, memiliki dua orang putra yakni Faisal Muntasir dan Rhaisan
Rahman.
Pendidikan formal yang pernah ditempuh penulis adalah sebagai berikut :
1. Tahun 1989 Madrasah Ibtidaiyah Negeri Drien Rampak
2. Tahun 1995 Madrasah Tsanawiyah Negeri 1 Meulaboh
3. Tahun 1998 masuk Sekolah Menengah Umum Negeri 1 Meulaboh
4. Tahun 2001 diterima di Program Studi Ilmu Teknologi Ternak (S1) di Institut
Pertanian Bogor
5. Tahun 2002 pindah ke Universitas Syiah Kuala Banda Aceh, Aceh pada
program studi Teknologi Hasil Pertanian Fakultas Pertanian.
6. Tahun 2012 melanjutkan pendidikan S2 di Program Studi Magister Ilmu
Pangan Universitas Sumatera Utara.
Saat ini penulis tercatat sebagai salah satu pengajar di Universitas Teuku
Umar, Meulaboh_Aceh pada program studi Budidaya Tanaman Pangan,
KATA PENGANTAR
Alhamdulillah, segala puji syukur saya panjatkan kehadirat Allah SWT,
atas segala karunia dan ridhaNya, sehingga tesis dengan judul “ Karakteristik
Maltodekstrin Hasil Hidrolisis Pati Gadung (Dioscorea hispida Dennst) Secara
Enzimatis ” ini dapat diselesaikan.
Tesis ini disusun untuk memenuhi salah satu persyaratan memperoleh
gelar Magister Sains di Program Studi Ilmu Pangan, Universitas Sumatera Utara.
Oleh karena itu pada kesempatan ini penulis menyampaikan rasa hormat dan
ucapan terima kasih yang sebesar-besarnya kepada:
1. Bapak Prof. Dr. Ir. Zulkifli Lubis, MApp.Sc selaku ketua komisi pembimbing
dan Ibu Dr. Ir. Herla Rusmarilin, MP selaku anggota komisi pembimbing serta
Ibu Dr. Ir. Elisa Julianti, M.Si dan Prof. Dr. Ir. Albiner Siagian, M.Si selaku
penguji yang telah membimbing dan membantu dalam penulisan tesis ini.
2. Teruntuk suami ku Musriadi, ST , kedua putra ku Faisal Muntasir dan Rhaisan
Rahman dan semua pihak yang telah membantu.
Dengan keterbatasan pengalaman, pengetahuan maupun pustaka yang
ditinjau, penulis menyadari bahwa tesis ini masih belum sempurna dan perlu
pengembangan lebih lanjut agar benar-benar bermanfaat. Oleh sebab itu, penulis
sangat mengharapkan kritik dan saran agar tesis ini lebih sempurna serta sebagai
masukan bagi penulis, sehingga tesis ini dapat bermanfaat untuk perkembangan
ilmu pengetahuan. Semoga tesis ini bermanfaat bagi kita semua.
Medan, Februari 2015
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PERSETUJUAN TESIS ... ii
SURAT PERNYATAAN ... iii
Hidrolisis Pati Secara Enzimatis ... 14
Faktor-faktor yang Berpengaruh pada Hidrolisis Pati Menjadi Glukosa ... 15
Enzim α-amilase dan Sifat-sifat Enzim α-amilase ... 16
Pembuatan Maltodekstrin dari Pati Umbi Gadung secara Enzimatis ... 17
Maltodekstrin ... 18
Hasil-hasil Penelitian Sebelumnya ... 19
METODOLOGI PENELITIAN ... 22
Analisis Produk Maltodekstrin ... 28
Penentuan % Kadar Gula Pereduksi Metode Luff Schroll ... 28
Penentuan DE ... 30
Hasil Analisis dan Pembahasan Maltodekstrin ... 35
Rendemen (%) ... 35
Hubungan Antara Perlakuan pH dengan Waktu Terhadap Rendemen ... 35
Gula Reduksi ... 37
Hubungan Antara Perlakuan pH dengan Waktu Terhadap Gula Reduksi ... 37
Dextrosa Equivalent ... 40
Hubungan Antara Perlakuan pH dengan Waktu Terhadap Dextrosa Equivalent ... 40
Viskositas (%) ... 44
Hubungan Antara Perlakuan pH dengan Waktu Terhadap Viskositas ... 44
Daya Serap (%) ... 46
Hubungan Antara Perlakuan pH dengan Waktu Terhadap Daya Serap ... 46
Daya Larut ... 48
DAFTAR TABEL
No. Halaman
1. Komposisi Kimia Gadung ... 8
2. Jenis Dekstrin dan Penggunaannya Berdasarkan Nilai DE ... 19
3. Syarat Mutu Dekstrin SNI ... 20
4. Karakteristik Pati Gadung ... 33
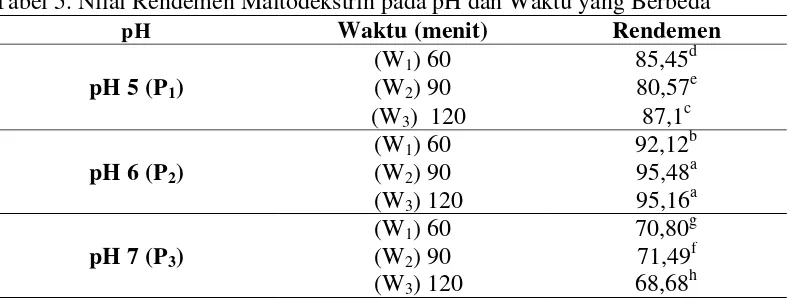
5. Nilai Rendemen Maltodekstrin... 35
6. Nilai Gula Reduksi Maltodekstrin... 37
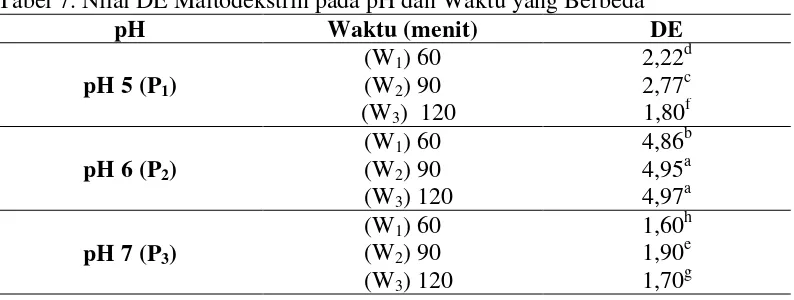
7. Nilai Dextrosa Equivalent... 40
8. Nilai Viskositas... 44
9. Nilai Daya Serap... 47
DAFTAR GAMBAR
No. Halaman
1. Proses Hidrolisis Pati Oleh Enzim α-amilase ... 3
2 Gadung ... 7
3 α-amilase yang Memotong Rantai Pati Pada Ikatan Alfa-1,4 ... 17
4 Hubungan Antara pH Proses dan Waktu Terhadap Rendemen ... 36
5 Hubungan Antara pH dan Waktu yang Berbeda Terhadap Gula Reduksi ... 38
6 Hubungan Antara pH dan Waktu yang Berbeda Terhadap DE ... 41
7 Hubungan Antara pH dan Waktu yang Berbeda Terhadap Viskositas ... 44
8 Hubungan Antara pH dan Waktu yang Berbeda Terhadap Daya Serap ... 47
DAFTAR LAMPIRAN
No. Halaman
1 Proses Pembuatan Pati Gadung ... 57
2. Proses Pembuatan Maltodekstrin ... 58
3. Rendemen ... 59
4. Gula Reduksi... 60
5. Dekstrosa Ekuivalen... 61
6. Viskositas ... 62
7. Daya Serap ... 63
8. Daya Larut ... 64
KARAKTRISTIK MALTODEKSTRIN HASIL DARI
HIDROLISIS PATI GADUNG (
Dioscorea hispida
Dennst)
SECARA ENZIMATIS
ABSTRAK
Beberapa jenis Dioscorea yang tumbuh di Indonesia belum dimanfaatkan secara maksimal, salah satunya umbi gadung. Gadung (Dioscorea hispida Dennst) adalah jenis umbi yang tumbuh liar di hutan dan tidak begitu sulit mendapatkannya. Memiliki potensi untuk dimanfaatkan sebagai sumber maltodekstrin. Maltodekstrin merupakan polimer dari glukosa dengan panjang ikatan rata-rata 5-10 unit rantai glukosa per molekul. Maltodekstrin adalah turunan pati yang dihasilkan dari degradasi rantai amilosa dan amilopektin secara kimia atau enzimatis menjadi dekstrin. Maltodekstrin memiliki DE dari 3-20. Penelitian ini bertujuan untuk mengetahui pengaruh pH dan waktu likuifikasi terhadap kualitas maltodesktrin dan hasil hidrolisis enzimatis pati umbi gadung.
Penelitian ini menggunakan metode enzimatis, dengan penambahan enzim amilase. Analisis data menggunakan Rancangan Acak Lengkap (2 faktor 3 ulangan). Hasil penelitian menunjukkan bahwa pH 5, 6 dan 7, waktu likuifikasi 60, 90 dan 120 menit dan interaksi pH dan waktu likuifikasi memberi pengaruh yang berbeda sangat nyata terhadap gula reduksi, dekstrosa equivalen, daya larut, viskositas, daya serap dan rendemen maltodesktrin. pH yang paling optimal adalah 6, waktu likuifikasi yang paling optimal adalah 90 dan 120 menit.
CHARACTERISTIC MALTODEKSTRIN HYDROLYSIS OF STARCH YAM (
Dioscorea hispida
Dennst) ENZYMATICALLY
ABSTRACT
Some of types Dioscorea that grows in Indonesia have not been fully utilized, one yam tubers. Yam (Dioscorea hispida Dennst) is a type of bulb that grows wild in the woods and not so difficult to get. Has the potential to be used as a source of maltodextrin. Maltodextrin is a polymer of glucose with an average bond length of 5-10 units per molecule of glucose chains. Maltodextrin is a starch derivative resulting from the degradation of amylose and amylopectin chains chemically or enzymatically into dextrin. Maltodextrin has a DE of 3-20. This study aimed to determine the effect of pH and liquefaction time to maltodesktrin quality and enzymatic hydrolysis of starch yam tubers.
This study uses the enzymatic method, with the addition of enzyme. Analysis of the data using a completely randomized design (2 factor 3 replications). The results showed that pH 5, 6 and 7, liquefaction time 60, 90 and 120 minutes and the interaction of pH and time likuifikasi gave highly significant effect on reducing sugar, dextrose equivalent, solubility, viscosity, absorption and yield maltodesktrin. The most optimal pH was 6, the most optimal liquefaction time was 90 and 120 minutes.
PENDAHULUAN
Latar Belakang
Gadung (Dioscorea hispida Dennst) merupakan salah satu jenis tanaman
umbi-umbian yang tergolong kedalam kelompok yam yang terdapat di Indonesia.
Tanaman ini awalnya ditemukan di India bagian barat, penyebarannya meluas ke
Asia Tenggara seperti Indonesia, Malaysia, serta kepulauan Karibia, Afrika Barat,
Amerika Selatan, Kepulauan Pasifik, dan seluruh daerah tropis. Di Indonesia
sendiri gadung ini banyak diusahakan sebagai tanaman pelarangan, tumbuh liar di
hutan-hutan dan berkembang secara luas di daerah tropis (Koswara, 2006).
Umbi gadung pada saat panen puncak dapat mencapai hingga 19,7 ton/ha.
Melalui pengusahaan yang intensif, kemungkinan besar tanaman ini dapat
menghasilkan umbi yang lebih banyak lagi, khususnya di Indonesia, karena
tanaman ini dapat tumbuh dan berkembang dengan baik di iklim tropis. Di
Indonesia tanaman ini tumbuh liar, sedangkan pembudidayaan gadung banyak
ditemukan di Jawa dan Madura (Deptan, 2005).
Menurut Webster et al., (1984), gadung merupakan umbi yang tergolong
beracun, namun beberapa daerah di Indonesia gadung ini digunakan untuk
makanan pokok setelah potongan umbi ini dicuci pada air yang mengalir selama
3-4 hari berturut-turut. Di beberapa daerah Indonesia bagian timur, pada musim
paceklik umbi gadung dimanfaatkan untuk bahan pangan.
Di dunia ini terdapat sekitar 3000 spesies tanaman dari 110 famili yang
dapat melepaskan hidrogen sianida memalui proses yang disebut cyanogenesis. Di
dalam sel tanaman asam sianida dalam bentuk bebas maupun terikat. Pada
dihasilkan sekitar 400mg sianida per kg, maka untuk dapat mengkosumsi gadung
diperlukan proses penghilangan HCN sebelum gadung diolah (Fitchner dan
Nasser, 1978).
Gadung merupakan golongan umbi yang kaya pati, sehingga dapat diolah
seperti umbi-umbi lain, misalnya seperti menjadi maltodekstrin merupakan salah
satu jenis pati termodifikasi dan telah banyak digunakan dalam industri makanan,
minuman, kimia dan farmasi. Di bidang industri pangan, maltodekstrin banyak
digunakan sebagai pengganti lemak susu pada minuman yogurt, produk roti, es
krim dan sebagai bahan tambahan pada produk margarine serta “cheese cakes
filling” (Anonim, 2008). Di bidang industri farmasi/kesehatan, dekstrin diyakini
dapat mengurangi kadar kolesterol, mencegah timbulnya racun dalam tubuh,
melancarkan buang air besar, meningkatkan nafsu makan dan mengurangi resiko
penyakit jantung koroner (Anonim, 2009).
Kebutuhan maltodekstrin di Indonesia cukup besar. Pada tahun 2002,
Indonesia mengimport 44.000-52.000 ton maltodekstrin dari total import 80.000
ton produk pati termodifikasi (Triyono, 2007) dan pada tahun 2006, import
produk pati termodifikasi meningkat hingga 283.046 ton (Deptan, 2005). Melihat
besarnya kebutuhan dan banyaknya industri pengguna maltodekstrin serta
ketersediaan bahan baku yang melimpah, maka usaha untuk menjadikan umbi
gadung sebagai maltodekstrin sangatlah tepat.
Reaksi hidrolisa pati merupakan reaksi pemecahan pati menjadi struktur
gula yang lebih sederhana. Maltodekstrin dapat dibuat dari hasil reaksi hidrolisis
pati tidak sempurna. Pati mengalami proses pemutusan rantai oleh asam atau
disebut maltodekstrin dengan dextrose equivalent, DE < 20, kemudian secara
bertahap menjadi maltodekstrin dengan DE 20-60, tahap akhir menjadi glukosa
dengan DE=100 (Othmer, 1984).
Reaksi pembentukan maltodekstrin berlangsung dalam fasa cair, bersifat
irreversible endotermis. Maltodekstrin terbentuk melalui dua tahapan yaitu
gelatinisasi dan liquifikasi. Proses gelatinisasi terjadi apabila pati mentah
dimasukkan kedalam air, granula patinya akan menyerap air dan membengkak,
tetapi jumlah air yang diserap dan pembengkakannya terbatas. Granula pati
membengkak dan tidak dapat kembali pada kondisi semula disebut gelatinisasi,
suhu pada saat granula pati pecah disebut suhu gelatinisasi (Winarno,2002).
Gelatinisasi merupakan faktor yang diharus diperhatikan terkait dengan
proses likuifikasi, dimana larutan pati harus sempurna, bila larutan pati terlalu
pekat maka akan sulit tersuspensi dengan baik selama proses gelatinisasi dan
mengakibatkan likuifikasi juga akan sulit terjadi secara sempurna. Adapun secara
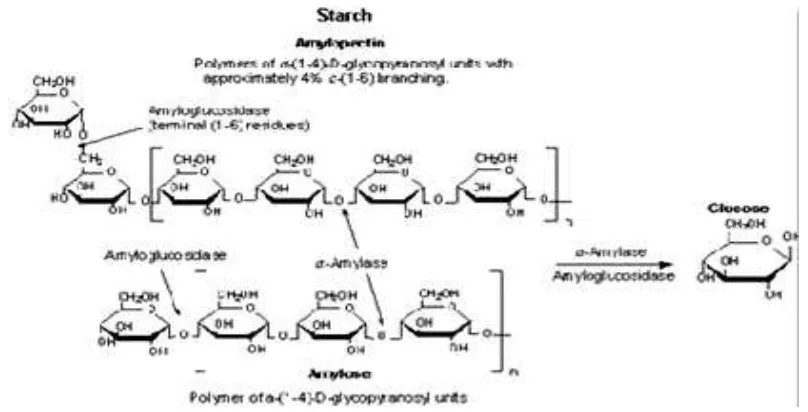
ringkas hidrolisis pati dapat digambarkan sebagai berikut:
Pati Dekstrin + maltosa + maltotresa + glukosa
Gambar 1. Proses Hidrolisis Pati Oleh Enzim α-amilase (Tjokroadikoesoemo, 1986).
Penelitian pembuatan maltodekstrin telah banyak dilakukan sebelumnya
dengan menggunakan enzim α-amilase, salah satunya dilakukan oleh Chafid, et
al., (2010) terhadap pati sagu. Hidrolisis secara enzimatik dilakukan pada pH
proses 7 dengan menggunakan waktu proses 60 menit, 90 dan 120 menit.
Didapatkan DE berkisar 4,79 – 9,57. Pada penelitian ini enzim yang digunakan
juga α-amilase dengan menggunakan bahan pati gadung, dengan variabel berubah
nya adalah pH dan waktu proses yang berbeda, sehingga nantinya didapatkan nilai
DE dan beberapa parameter lain dalam nilai yang bagus.
TujuanPenelitian
Tujuan penelitian yang dilakukan adalah sebagai berikut :
1. Untuk mengetahui kharakteristik maltodekstrin hasil hidrolisis enzimatik dari
pati umbi gadung (Dioscorea hispida Dennst).
2. Untuk mengetahui kombinasi perlakuan terbaik antara pengaruh pH dan waktu
proses yang berbeda untuk hasil maltodekstrin yang baik.
Hipotesis Penelitian
Hipotesis dari penelitian yang dilakukan adalah sebagai berikut :
1. Penggunaan pH dan waktu proses yang berbeda dan interaksinya pada
hidrolisis pati umbi gadung (Dioscorea hispida Dennst) secara enzimatis
berpengaruh terhadap nilai Dextrosa Equivalent maltodekstrin yang dihasilkan.
2. Maltodekstrin hasil hidrolisis pati umbi gadung secara enzimatis (Dioscorea
hispida Dennst) dengan pH dan waktu yang berbeda menghasilkan Dextrosa
Equivalent dengan nilai di bawah 10.
Manfaat Penelitian
Manfaat penelitian yang akan dilakukan adalah sebagai berikut :
1. Dapat memberikan informasi akan pengaruh penggunaan enzim dalam proses
hidrolisis terhadap kualitas maltodekstrin dari pati ubi gadung (Dioscorea
2. Dapat memberikan informasi tentang komposisi maltodekstrin dari pati ubi
gadung (Dioscorea hispida Dennst) dengan metode penambahan enzim dan
kondisi pHdan waktu yang berbeda.
3. Dapat memberikan informasi tentang penggunaan umbi gadung sebagai bahan
baku pembuat maltodekstrin, yang selama ini kurang dimanfaatkan secara baik.
4. Bagi perkembangan IPTEK, dapat mengetahui katalis biologi yang
TINJAUAN PUSTAKA
Tanaman Umbi Gadung (Dioscorea hispida Dennst)
Gadung (Dioscerea hispida Dennst., suku gadung-gadungan atau
dioscoreaceae) tergolong tanaman umbi-umbian yang cukup populer walaupun
kurang mendapat perhatian. Gadung menghasilkan umbi yang dapat dimakan,
namun mengandung racun yang dapat mengakibatkan pusing dan muntah apabila
kurang benar pengolahannya. Produk gadung yang paling dikenal adalah dalam
bentuk keripik meskipun rebusan gadung juga dapat dimakan. Di Indonesia,
tumbuhan ini memiliki nama seperti bitule (Gorontalo), gadu (Bima), gadung
(Bali, Jawa, Madura, Sunda), Iwi (Sumba), kapak (Sasak), salapa (Bugis), sikapa
(Makasar), (Anonim, 2014).
Taksonomi
Taksonomi umbi gadung sebagai berikut:
Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Liliopsida
Ordo : Dioscoreales
Famili : Dioscoreaceae
Genus : Dioscorea
Gambar 2. Umbi Gadung Hutan (Sibuea, 2002)
Gadung dapat menjadi sumber pangan alternatif selain sebagai sumber
pangan pokok seperti beras, jagung, singkong, gandum, dan lain-lain. Gadung
memang tidak sulit untuk didapatkan, tanaman ini tumbuh liar di hutan-hutan.
Selama masa pertumbuhan gadung ini tidak memerlukan perawatan khusus atau
penanganan khusus. Biasanya masyarakat yang mengkonsumsinya melakukan
pengolahan terhadap umbi gadung ini pada saat musim kemarau panjang tiba.
Ketika kemarau datang masyarakat pergi mencari umbi hutan dan kemudian
mengolahnya menjadi bahan makanan (Ode, 2007).
Morfologi
Gadung merupakan perdu memanjat yang tingginya dapat mencapai
5-10m. Batangnya bulat, berbentuk galah, berbulu, berduri yang tersebar sepanjang
batang dan tangkai daun. Umbinya bulat diliputi rambut akar yang besar dan
kaku. Kulit umbi berwarna gading atau coklat muda, daging umbinya berwarna
putih atau kuning. Umbinya muncul dekat permukaan tanah. Dapat dibedakan dari
jenis-jenis dioscorea lainnya karena daunnya merupakan daun majemuk terdiri
tipis lemas, bentuk lonjong, ujung meruncing, pangkal tumpul, permukaan kasar
(Ndaru, 2012).
Untuk membedakan antar spesies dalam gadung dapat dibedakan
berdasarkan arah lilitan batang, bentuk batang, ada atau tidaknya duri pada
batang, bentuk dan jumlah helaian daun, ada tidaknya buah di atas (Anonim,
2014). Ada beberapa varietasnya, diantaranya yang berumbi putih (yang besar
dikenal sebagai gadung punel atau gadung ketan, sementara yang kecil
berlekuk-lekuk disebut gadung suntil dan yang berumbi kuning antara lain gadung kuning,
gadung kunyit atau gadung padi. Gadung kuning umumnya lebih besar umbinya
bila dibandingkan gadung putih. Jumlah umbi dalam satu kelompok dapat
mencapai 30 umbi (Anonim, 2014).
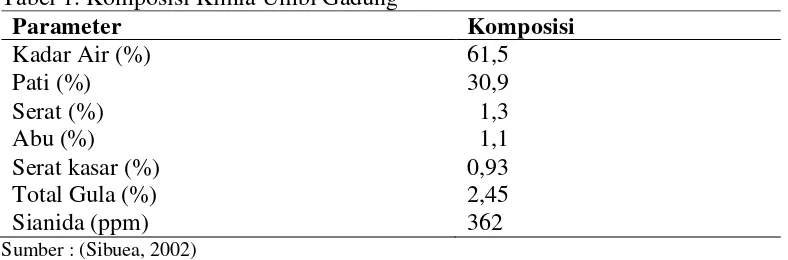
Komposisi Kimia Umbi Gadung
Umbi Gadung adalah jenis umbi-umbian yang dapat digunakan sebagai
alternatif sumber karbohidrat dan merupakan komoditi yang mempunyai prospek
yang sangat baik. Kandungan gizi gadung dapat dilihat pada Tabel 1.
Tabel 1. Komposisi Kimia Umbi Gadung
Parameter Komposisi
Umbi hutan nama lain dari gadung atau (Dioscorea hispida Dennst) dapat
menjadi sumber bahan pangan alternatif selain sebagai sumber bahan pokok
beberapa masyarakat yang pernah mengkosumsi umbi hutan ini apabila diolah
secara benar maka akan didapatkan makanan olahan yang enak dan bergizi,
(Sibuea, 2002).
Beberapa jenis nutrisi yang ditemukan didalam gadung ini ternyata juga
merupakan kandungan utama bahan pangan yang dijadikan masyarakat Indonesia
sebagai pokok selama ini, yaitu padi (Oryza sativa Linn) dan jagung (Zea mays
Linn). Disamping kandungan nutrisi tersebut, ternyata ubi hutan juga
mengandung zat yang bersifat toksik atau anti nutrisi, yakni glikosida sianogenik,
alkaloid dioscorin dan senyawa pahit yang terdiri dari saponin dan sapogenin
(Webster et al., 1984).
HCN dalam Gadung
Glikosida sianogenik yang dikandung umbi hutan (Dioscorea hispida
Dennst) dapat bersifat toksik karena dapat terhidrolisis sehingga terbentuk asam
sianida (HCN). Kandungan HCN dalam bahan makanan akan mengalami
pengurangan bahkan penghilangan apabila bahan makanan tersebut mendapat
perlakuan penghancuran atau pengirisan. Racun yang terdapat didalam umbi
gadung antara lain dioskorin, diosgenin, serta asam sianida (HCN).
Senyawa-senyawa ini memiliki efek hemolisis apabila masuk ke dalam tubuh manusia.
Senyawa ini juga memiliki efek paralisis pada susunan saraf sehingga dapat
menyebabkan kelumpuhan (Pambayun, 2008). Penghilangan racun-racun pada
umbi gadung yang biasa dilakukan oleh masyarakat umum adalah dengan
menggunakan cara tradisional yaitu perendaman irisan umbi gadung dalam air
Keracunan karena HCN pernah dilaporkan terjadi dia Mauritius tahun
1844 setelah mengkosumsi jenis kacangan yang disebut Phaseolus lunatus,
sedangkan keracunan karena mengkosumsi singkong ketela pohon dilaporkan
terjadi di Nigeria tahun 1965 dan di India tahun 1973. Juga pernah dilaporkan
keracunan karena mengkosumsi bambu muda (rebung), almond pahit, biji peach,
apricot dan chezzy. Di Indonesia, laporan tentang keracunan setelah mengkosumsi
umbi hutan terjadi di kabupaten Sikka, Nusa Tenggara timur, november 2006, dan
di Bengkulu tahun 2002.
Senyawa racun dalam gadung berupa senyawa glukosida sianogenik.
Senyawa ini dapat terpecah menjadi asam sianida apabila terhidrolisis oleh enzim
atau berada pada pH asam. Pada sistem pencernaan yang bersuasana asam
senyawa ini akan melepaskan HCN yang bisa meracuni tubuh. Oleh karena itu
detoksifikasi harus difokuskan pada pengurangan senyawa kompleks tersebut.
Menurut Damardjati dkk (1991), pengelompokan kadar sianida adalah < 50 ppm
tidak beracun, 50-80 ppm agak beracun, 80-100 ppm beracun dan > 100 ppm
sangat beracun.
Prinsip dasar metode detoksifikasi sianida pada umbi gadung adalah
menghambat terjadinya reaksi antara subtrat linamarin dan metal linamarin
dengan enzim linamarase. Perendaman irisan umbi dalam larutan 8 persen selama
tiga hari mampu mengurangi racun sianida dengan residu yang terbentuk relatif
rendah yaitu 7,32 ppm. Pemanasan irisan umbi gadung setebal 2 mm dalam air
mendidih selama 30 menit ternyata lebih efektif menurunkan kadar sianida bila
dibandingkan dengan metode perendaman dalam garam, yakni 4,12 ppm.
air mendidih selama 30 menit bisa mengakibatkan enzim linamarase dan
glukosidase tidak aktif dan pembentukan asam sianida pun menjadi terputus
(Pambayun, 2000).
Pati
Pati atau amilum adalah karbohidrat kompleks, tidak larut dalam air
dingin, berwujud bubuk, tawar dan tidak berbau. Pati merupakan bahan utama
yang dihasilkan oleh tumbuhan untuk menyimpan kelebihan glukosa (sebagai
produk fotosintesis) dalam jangka panjang. Hewan dan manusia juga menjadikan
pati sebagai sumber energi yang penting. Pati tersusun dari dua macam
karbohidrat, amilosa dan dan amilopektin dalam komposisi yang berbeda-beda.
Pati (starch) alami memiliki keterbatasan dalam kegunaannya untuk
aplikasi komersial. Sifat alami pati antara lain diantaranya tidak larut dalam air
dingin dan tidak dapat dicerna oleh tubuh manusia (Hay, 2002). Wurzburg (1989)
telah memberikan pengetahuan yang mendalam tentang sifat fisika dari pati alami
dibandingkan dengan pati modifikasi. Modifikasi pati memberikan perubahan dari
sifat fisika dan sifat kimia. Perubahan ini mempunyai sasaran utama untuk
aplikasi produk makanan lebih spesifik yang dapat memperbaiki sifat fungsional
produk terhadap viskositas, stabilitas, integritas, tekstur dan pengemulsi
sebagaimana keterbatasan dalam bentuk alaminya.
Dalam referensi lain, pati adalah salah satu yang paling banyak dan luas
terdapat dialam, sebagai karbohidrat cadangan pangan pada tanaman. Sebagian
besar pati di simpan dalam akar, umbi, akar, biji buah dan umbi lapis. Cadangan
tersebut berada dalam bentuk granula lebih besar disebut dengan pati cadangan.
sebagai pengental ataupun pembentukan gel hidrokoloid lainnya meliputi samping
itu banyak pati digunakan untuk pengikat lemak dan pembantu pembentukan
emulsi (Hawab, 2004). Perbedaan amilosa dengan amilopektin yaitu amilosa
memberikan sifat keras, sedangkan amilopektin menyebabkan sifat lengket.
Amilosa memberikan warna ungu pekat amilopektin tidak bereaksi. Secara
struktur amilosa dan amilopektin memiliki perbedaan. bahan penyusunan yang
granula-granula berukuran gum, pektin, gelatin, selulosa agar, dan lainnya.
Pati merupakan cadangan karbohidrat dalam tumbuh-tumbuhan dan
merupakan karbohidrat utama yang dikonsumsi manusia seluruh dunia.
Komposisi amilosa dan amilopektin pada setiap jenis berbeda. Amilopektin pada
umumnya terdapat dalam jumlah lebih besar. Sebagian besar pati mengandung
antara 15% dan 35% amilosa. Dalam butiran pati, rantai-rantai amilosa dan
amilopektin tersusun dalam bentuk semi kristal, yang menyebabkan tidak larut
dalam air dan memperlambat proses pencernaannya oleh amilase pankreas. Bila
dipanaskan dengan air, struktur kristal rusak dan rantai polisakarida akan
mengambil posisi acak. Hal inilah yang menyebabkan mengembang dan memadat
(gelatinisasi). Cabang-cabang yang terletak pada bagian amilopektin yang
terutama sebagai penyebab terbentuknya gel yang cukup stabil. Proses pemasakan
pati disamping menyebabkan terbentuknya gel juga dapat melunakkan dan
memecahkan sel, sehingga mempermudah pencernaan. Dalam proses pencernaan
semua bantuk pati akan terhidrolisa sebagian besar menghasilkan glukosa
(Afrianti, 2004).
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik.
serta lurus atau bercabangkah rantai molekulnya. Pati terdiri dari dua fraksi yang
dapat dipisahkan dengan air panas. Fraksi terlarut dinamakan amilosa dan fraksi
tidak terlarut dinamakan amilopektin. Amilosa menpunyai struktur lurus dangan
cabang ikatan α- (1,4) D-glukosa sebanyak 4,5 5 dari berat total (Winarno, 2004).
Peranan perbandingan amilosa dan amilopektin terlihat jelas pada serealia
contohnya pada beras, semakin kecil kandungan amilosa atau semakin tinggi
kandungan amilopektin semakin lekat nasi tersebut. Amilosa adalah molekul
berantai linier yang dihubungkan oleh ikatan α-1,4 dari sejumlah 500-5000 unit
glukosa. Amilosa bertindak sebagai pengisi amorf dalam granula, dalam
perdagangan dikenal dua macam pati, yaitu pati yang belum dimodifikasi dan pati
yang telah dimodifikasi. Pati yang tidak dimodifikasi atau pati biasa adalah semua
jenis pati yang dihasilkan di pabrik pengolahan dasar, misalnya tepung tapioka,
(Abu Bakar, 1986). Kandungan pati di dalam bahan cukup penting, sehingga
semakin tinggi kandungan pati semakin dikehendaki konsumen. Kandungan pati
didalam bahan bakunya akan dipengaruhi oleh umur tanaman dan lama
penyimpanan setelah panen. Oleh karena itu pada pembuatan tepung umbi
dikehendaki kandungan patinya maksimum, maka umbi hasil panen sebaiknya
segera diolah dan tidak dilakukan penyimpanan (Antarlina dan Utomo, 1999).
Berbagai proses kimia yang dapat diterapkan pada modifikasi pati
antaranya oksidasi, hidrolisa, cross linking atau cross bonding serta subsitusi
(Fleche, 1985). Maltodekstrin merupakan salah satu produk dari hasil hidrolisa
pati dengan menggunakan asam maupun enzim, yang terdiri dari campuran
Hidrolisis Pati Secara Enzimatis
Reaksi hidrolisa berlangsung lambat, untuk dapat mempercepat
digunakalah katalisator. Katalisator adalah zat yang dapat mempercepat reaksi
tetapi dia tidak ikut bereaksi pada prosesnya secara keseluruhan. Pada hidrolisa
pati katalisator yang digunakan adalah enzim. Enzim adalah zat organik yang
dihasilkan oleh sel hidup baik tanawan, hewan maupun mikroorganisme
(Sherman, 1962).
Enzim adalah biomolekul berupa protein yang berfungsi sebagai katalis
(senyawa yang mempercepat proses reaksi tanpa habis bereaksi) dalam suatu
reaksi kimia organik. Molekul awal yang dihasilkan disebut substrat akan
dipercepat perubahannya menjadi molekul lain disebut produk. Jenis produk yang
dihasilkan bergantung pada suatu kondisi zat, yang disebut promoter. Sebagian
besar enzim bekerja secara khas, artinya setiap enzim hanya akan bekerja pada
satu macam senyawa atau reaksi kimia. Hal ini disebabkan perbedaan struktur
kimia tiap enzim yang bersifat tetap. Sebagai contoh, enzim α-amilase hanya
dapat digunakan pada proses perombakan pati menjadi glukosa. Kerja enzim
dipengaruhi oleh beberapa faktor, terutama adalah substrat, suhu, keasaman,
kofaktor dan inhibitor (Februadi, 2011). Hidrolisis dengan enzim dapat
menghasilkan beberapa produk hidrolisat pati dengan sifat-sifat tertentu yang
didasarkan pada nilai DE (Ekuivalen dekstrosa). Beberapa jenis enzim yang
sering digunakan dalam menghidrolisis pati yaitu α-amilase, β-amilase, pullunase
Faktor – faktor yang berpengaruh pada hidrolisis pati menjadi glukosa : Suhu
Pengaruh suhu terhadap enzim ternyata agak kompleks, misalnya suhu
yang terlalu tinggi dapat mempercepat pemecahan atau perusakan enzim.
Sebaliknya semakin tinggi suhu (dalam batas tertentu) semain aktif enzim
tersebut. Bila suhu naik terus laju kerusakan enzim akan melampaui reaksi
katalisis enzim (Winarno, 1984). Reaksi paling cepat terjadi pada suhu optimum,
oleh karena penentuan suhu optimum aktivitas enzim sangat perlu karena apabila
suhu terlalu rendah maka kestabilan enzim akan naik namun aktitivitas menurun,
sedangkan pada suhu tinggi aktivitas enzim akan naik namun kestabilan menurun.
Kebanyakan enzim tidak aktif pada suhu 55ºC-60ºC (Rabyt dan White, 1987).
Waktu
Semakin lama waktu reaksi, maka kadar glukosa yang dihasilkan semakin
besar. Lamanya waktu reaksi juga dipengaruhi atau bergantung oleh banyaknya
substrat yang di hidrolisa dan jumlah enzim yang ditambahkan.
pH
Sebagian besar aktivitas enzim dipengaruhi derajat keasaman media
tempat enzim tersebut melakukan kegiatan katalitiknya. Derajat keasaman optimal
yang ditunjukan oleh enzim tertentu tidak selalu konstan. Masih ada berbagai
faktor lain yang memberikan pengaruh atas aktivitas enzim tersebut.
Kadar Suspensi Pati
Pada penggunaan kadar rendah, keseimbangan akan bergeser kekanan
dengan baik. Pada kadar suspensi tinggi mengakibatkan kekentalan campuran
meningkat. Hal ini mengakibatkan proses hidrolisa tidak dapat berjalan dengan
baik atau sempurna. Semakin tinggi kadar suspensi pati yang dihidrolisa, maka
waktu proses yang diperlukan untuk menghidrolisa pati tersebut akan semakin
lama. Jumlah enzim yang dibutuhkan juga semakin banyak.
Jumlah Penambahan Enzim
Semakin banyak jumlah enzim yang ditambahkan pada pati, akan
menghasilkan kadar glukosa yang semakin banyak pula. Keadaan ini juga
semakin mempercepat reaksi hidrolisa, untuk enzim α- amilase digunakan
perbandingan 2kg enzim untuk setiap ton pati, sedangkan untuk enzim
glukoamilase digunakan sebanyak 0,5-1,1 L untuk setiap ton pati.
Aktivator dan Inhibitor
Beberapa enzim memerlukan aktivator dalam reaksi katalisnya. Aktivator
adalah senyawa atau ion yang dapat menaikkan kecepatan reaksi enzimatis.
Komponen kimia yang membentuk aktivitas enzim disebut juga kofaktor.
Kofaktor tersebut dapat berupa ion anorganik seperti Zn2+, Fe2+, Ca2+ atau dapat
pula sebagai molekul organik komplek yang disebut koenzim. Pada umumnya
ikatan senyawa organik dengan protein enzim itu lemah apabila iktannya kuat.
Selain aktivator juga dipengaruhi oleh inhibitor, inhibitor adalah senyawa atau ion
yang dapat menghambat aktivitas enzim pada saat enzim bekerja pada substrat
(Lehninger, 1982).
Enzim α-amilase dan Sifat-Sifatnya
Hidrolisis amilosa oleh enzim α-amilase terjadi dalam dua tahap, pertama,
degradasi amilosa menjadi maltosa dan maltotriosa yang terjadi secara acak.
cepat pula. Kedua, relatif sangat lambat yaitu pembentukan glukosa dan maltosa
sebagai hasil akhirnya (Muchtadi dkk., 1992). Sebagian besar enzim bekerja khas
yaitu artinya setiap jenis enzim hanya dapat bekerja pada satu macam senyawa
atau reaksi kimia. Hal ini disebabkan perbedaan struktur kimia tiap enzim yang
bersifat tetap. Sebagai contoh, enzim α-amilase hanya dapat digunakan pada
proses perombakan pati menjadi glukosa.
Cara kerja α-amilase pada molekul amilosa akan menghasilkan glukosa,
maltosa dan berbagai jenis α-limit dekstrin. Jenis α-limit dekstrin yaitu
oligosakarida yang terdiri dari 4 atau lebih residu glukosa yang semuanya
mengandung ikatan α-1,6. Laju hidrolisis akan meningkat bila tingkat
polimersisasi menurun, dan laju hidrolisis akan lebih cepat pada rantai yang lurus
(Winarno,1995).
Gambar 3. α-amilase yang memotong rantai pati pada ikatan α-1,4 (Purba dan Elida, 2009).
Pembuatan Maltodekstrin dari Pati Umbi Gadung Secara Enzimatis
Proses hidrolisa pati secara enzimatis dilakukan melalui tahap liquifikasi.
Liquifikasi merupakan kombinasi dari dua proses, pertama yaitu hidrasi atau
gelatinisasi dari polimer pati, untuk mempermudah serangan-serangan hidrolitik,
yang kedua yaitu dekstrinasi, sehingga dapat mencegah terjadinya retrogradasi
untuk tahap selanjutnya (Muchtadi et al., 1992).
Maltodekstrin
Maltodekstrin merupakan polimer dari glukosa dengan panjang ikatan
rata-rata 5-10 unit rantai glukosa per molekul. Maltodekstrin banyak digunakan
dalam industri makanan sebagai pengisi, dan dalam industri farmasi sebagai
pengisi tablet, (Anwar, 2002). Maltodekstrin adalah turunan pati yang dihasilkan
dari degradasi rantai amilosa dan amilopektin secara kimia atau enzimatis menjadi
dekstrin, memiliki DE dari 2-30. Beberapa DE yang rendah telah dipatenkan
terbukti dapat digunakan sebagai pengganti lemak. Maltodekstrin 2-5 mempunyai
sifat fungsional membentuk gel dalam air panas pada konsentarsi diatas 15%.
Maltodekstrin dengan DE rendah sangat cocok sebagai bahan pengganti lemak
(Ingglet dan Grismore, 1991).
Maltodekstrin sebagai komponen bahan dalam industri pangan telah
banyak digunakan karena terbukti lebih aman dan terdaftar pada GRAS (Generaly
Recognized As Safe). Dalam aplikasinya maltodekstrin dapat memberikan
kekerasan dan tekstur dalam produk pangan, maltodekstrin yang mengandung
sakarida tinggi 95% dan Dextrose Equivalent rendah mempunyai sifat gel yang
dapat lumer dan bersifat thermoreversible, sehingga dapat diaplikasikan sebagai
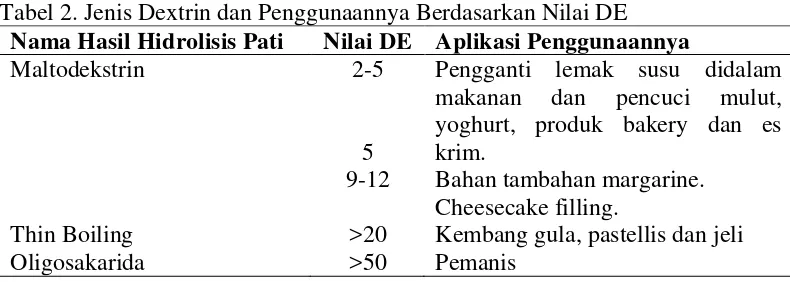
pengganti lemak dalam produk pangan (Roper, 1996). Pada Tabel. 2 dapat dilihat
Tabel 2. Jenis Dextrin dan Penggunaannya Berdasarkan Nilai DE
Nama Hasil Hidrolisis Pati Nilai DE Aplikasi Penggunaannya
Maltodekstrin 2-5
5 9-12
Pengganti lemak susu didalam makanan dan pencuci mulut, yoghurt, produk bakery dan es krim.
Bahan tambahan margarine. Cheesecake filling.
Thin Boiling >20 Kembang gula, pastellis dan jeli
Oligosakarida >50 Pemanis
Maltodekstrin memiliki kelarutan yang lebih tinggi, mampu membentuk
film, memiliki higroskopisitas rendah, mampu menghambat kristalisasi dan
memiliki daya ikat kuat, (Luthana, 2008). Maltodektrin tidak berasa dan dikenal
sebagai bahan tambahan makanan yang aman, (Blancard dan Katz, 1995).
Maltodektrin lebih mudah larut dari pada pati, maltodekstrin juga mempunyai rasa
yang enak dan lembut, (Sadeghi, et al., 2008). Maltodekstrin telah banyak
digunakan pada industri makanan, seperti pada minuman, susu bubuk, minuman
berenergi dan minuman prebiotik, (Blancard dan Katz, 1995).
Hasil-hasil Penelitian Sebelumnya
Triyono (2007) telah melakukan penelitian “Peningkatan Fungsional Pati
dari Ubi Jalar dengan Enzim α-Amilase Sebagai Bahan Subsitusi Pengolahan
Pangan”, diperoleh hasil terbaik pada konsentrasi enzim sebesar 0,5% dan pH
kondisi 6 dengan nilai DE sebesar 5-6 dan nilai kelarutan sebesar 98%.
Chafid et al (2010) membuktikan bahwa nilai DE terendah dari
maltodekstrin tepung sagu didapat pada kondisi konsentrasi enzim 0,09% selama
60 menit sebesar 4,69% dan DE tertinggi diperoleh pada konsentrasi enzim 0,09%
Anita et al (2009) telah melakukan penelitian berupa “Pembuatan
Maltodekstrin Dengan Proses Hidrolisa Pati Singkong Menggunakan Enzim α
-Amilase” didapatkan bahwa harga DE dipengaruhi oleh beberapa faktor,
diantaranya waktu dekstrinasi dan pH proses. Semakin lama waktu dekstrinasi
maka semakin besar pula harga DE. Perlakuan terbaik didapatkan pada kondisi
pH 6 dengan waktu 120 menit nilai DE 19,56 sedangkan pada pH 7 dengan waktu
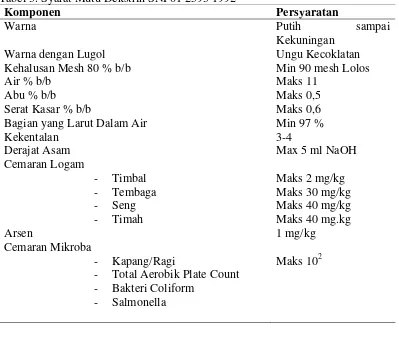
60 menit didapatkan DE sebesar 11,79. Syarat mutu Maltodekstrin secara umum
disajikan pada Tabel 3.
Tabel 3. Syarat Mutu Dekstrin SNI 01 2593 1992
Komponen Persyaratan
Warna Putih sampai
Kekuningan
Warna dengan Lugol Ungu Kecoklatan
Kehalusan Mesh 80 % b/b Min 90 mesh Lolos
Maltodekstrin memiliki kelarutan yang lebih tinggi, mampu
membentuk film, memiliki higroskopisitas rendah, mampu menghambat
berasa dan dikenal sebagai bahan tambahan makanan yang aman, (Blancard dan
Katz, 1995). Maltodektrin lebih mudah larut dari pada pati, maltodekstrin juga
mempunyai rasa yang enak dan lembut, (Sadeghi et al., 2008). Maltodekstrin
telah banyak digunakan pada industri makanan, seperti pada minuman, susu
bubuk, minuman berenergi dan minuman prebiotik, (Blancard dan Katz, 1995).
Proses Pembuatan Pati Gadung (Dioscorea hispida Dennst)
Bubur Umbi Gadung
Umbi gadung di kupas lalu dibersihkan Kemudian diiris tipis-tipis
Irisan umbi gadung direndam pada air yang mengalir selama 3 hari berturut-turut untuk selanjutnya dikeringkan selama 3 hari sehingga umbi gadung kering.
Kemudian irisan umbi gadung dihaluskan dan ditambah air dengan Disaring dengan kain saring untuk
memisahkan ampasnya lalu
diendapkan.
Endapan pati gadung dipisahkan dari supernatant dan dicuci dengan penambahan air 1:2 (b/v)
Diaduk, dan kembali diendapkan. Pencucian diulangi ±10 kali
METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Oktober sampai dengan Desember
2014 di Laboratorium Laboratorium Analisa Ilmu dan Teknologi Pangan Fakultas
Pertanian dan Laboratorium Biokimia Fakultas FMIPA Universitas Sumatera
Utara, Medan.
Bahan dan Alat Penelitian
Sampel yang digunakan dalam penelitian ini adalah umbi gadung
(Dioscorea hispida Dennst) yang termasuk dalam varietas gadung putih, kulit
umbinya berwarna gading atau coklat muda, daging umbinya berwarna putih
gading tau kuning serta memiliki ukuran umbi dengan panjang 20-25 cm serta
lebar 1-12 cm), yang diperoleh dari Lhokseumawe, Aceh. NaOH 1%, enzim
amylase (Merk Himedia), Na2HPO4 10 %, KI 30 %, H2SO4 25 %, Na2S2O3 0,1 N,
aquades, NaOH 30%, HCl 30%, karbon aktif, amilum 1%, larutan Luff Schrool.
Pisau, kain saring, stoples bening, labu takar 100 ml dan 250 ml (pyrex), pipet
tetes, magnetic stirrer, gelas ukur 10ml (pyrex), kertas saring, shaker incubator
(vision), autoclave, termometer, tabung reaksi, corong, beker glass 250ml, 500ml,
1000ml (pyrex), pipet volume 10ml dan 50ml, batang pengaduk dan alat titrasi,
neraca analitik, erlenmeyer 500 ml dan 250ml (pyrex), pH meter, oven
(Gallencamp), hot plate (PMC), gelas arloji, desikator, mafel, alat tulis dan alat
Metoda Penelitian
Penelitian ini dilakukan secara eksprimen dan menggunakan Rancangan
Acak Lengkap (RAL) dengan dua faktor, yang terdiri dari 9 (sembilan) perlakuan
dan 3 (tiga) kali ulangan sehingga diperoleh 27 unit. Perlakuan tersebut terdiri
dari
Faktor I : pH pada proses Likuifikasi (P) yang terdiri dari 3 taraf :
P1 = 5
P2 = 6
P3 = 7
Faktor II: Lama proses Likuifikasi (W) yang terdiri dari 3 taraf :
W1 = 60 menit
W2 = 90 menit
W3 = 120 menit
Model Rancangan Acak Lengkap (RAL) yang digunakan adalah sebagai berikut :
Yijk = μ + αi + βj + (αβ)ij + εijk
dimana :
Yijk = Hasil pengamatan faktor A pada taraf ke-i, dan faktor B pada taraf
ke-j dengan ulangan ke-k
μ = Efek nilai tengah atau rataan
αi = Pengaruh dari faktor A pada taraf ke-i
βj = Pengaruh dari faktor B pada taraf ke-j
(αβ)ij = Komponen interaksi dari faktor A dan faktor B
Apabila diperoleh hasil berbeda nyata dan sangat nyata maka uji dilanjutkan
dengan uji beda rataan dengan menggunakan uji Anova, program SPSS 20,00.
Pelaksanaan Penelitian
Analisis HCN dari Umbi Gadung (Dioscorea hispida Dennst)
Langkah-langkah penentuan kadar sianida dari umbi gadung adalah, bahan
uji yang telah dihaluskan ditimbang sebanyak 10 g. Lalu dimasukkan kedalam
labu erlenmeyer dan ditambahkan 100 ml air suling, direndam selama 2 jam lalu
dilakukan destilasi uap. Hasil destilat ditampung dalam labu erlenmeyer yang
berisi 20 ml larutan NaOH 2,5% telah mencapai 150 ml destilasi dihentikan.
Distilat yang diperoleh dititrasi dengan larutan AgNO3 0,02 N sampai timbul
kekeruhan. Penentuan kadar sianida memenuhi perhitungan 1 ml AgNO3 = 1,08
mg HCN, (Anonim, 2014).
Pembuatan Pati dari Umbi Gadung (Dioscorea hispida Dennst)
Proses pembuatan pati umbi gadung dimulai dengan proses pengupasan
dan membersihkan umbi, kemudian diiris tipis-tipis. Irisan umbi gadung direndam
pada air mengalir selama 3 hari, selanjutnya dikeringkan selama 3 hari dibawah
sinar matahari, selanjutnya umbi gadung yang telah kering tersebut dihaluskan
dan ditambah air dengan rasio 1:1. Bubur gadung disaring dengan kain saring
untuk memisahkan ampasnya lalu diendapkan.
Endapan pati gadung dipisahkan dari supernatant dan dicuci dengan
penambahan air 1:2 (b/v), diaduk, dan kembali diendapkan. Pencucian diulangi ±7
kali. Setelah itu dilanjutkan dengan pengeringan dengan oven pada suhu 55˚C
Pembuatan Maltodekstrin dari Umbi Gadung Liar dengan Hidrolisis Enzimatis
Pati umbi gadung ditimbang sesuai dengan kebutuhan proses, kemudian
dilarutkan menggunakan aquades dan diatur pHnya sesuai kebutuhan proses
menggunakan HCL atau NaOH. Setelah itu baru ditambahkan CaCL2 sebanyak 40
ppm dan enzim alpha amilase sebanyak konsentrasi yang diinginkan. Pengadukan
dilakukan pada suhu yang diinginkan dengan kecepatan putar 1080 rpm selama
waktu tertentu. Setelah proses pengadukan berakhir maka proses inaktivasi enzim
dihentikan dengan menambahkan HCL hingga pH nya mencapai 3,7-3,9. Setelah
selang waktu 30 menit, larutan yang diperoleh dinetralkan menggunakan NaOH
sampai pH 7. Kemudian larutan tersebut dikeringkan menggunakan oven, setelah
kering dihaluskan dengan blender dan dilakukan pengayakan dan hasilnya adalah
maltodekstrin yang halus, (Risnoyatiningsih, 2011).
Pengamatan dan Analisis Data
Analisis Proximat Umbi Gadung
Analisa Kadar Asam Sianida (Sudarmadji dkk., 1997)
Ditimbang sebanyak 20 g pati umbi gadung yang telah dihaluskan
kemudian ditambahkan 100 ml aquadest dalam erlenmeyer dan didiamkan selama
2 jam. Ditambahkan lagi 100 ml aquadest dan didestilasi dengan uap. Destilat
ditampung dalam erlenmeyer yang telah diisi dengan 20 ml NaOH 2,5%. Setelah
didestilasi (ditampung dalam erlenmeyer) mencapai volume 150 ml maka proses
NH4OH. Campuran destilat tersebut dititrasi dengan larutan AgNO3 0,02 N
sampai terjadi kekeruhan. Kemudian dihitung kadar asam sianida dengan rumus :
HCN =
Kadar Air (Sudarmadji dkk., 1989)
Ditimbang sampel sebanyak 2 g dalam cawan porselin yang tetah
diketahui beratnya. Dikeringkan dalam oven pada suhu 105 0C selama 4 jam.
Kemudian didinginkan dalam desikator selama 15 menit dan ditimbang.
Dipanaskan lagi dalam oven selama 30 menit, didinginkan lagi dalam desikator
dan ditimbang. Perlakuan ini diulangi sehingga didapat berat yang konstan.
Dihitung pengurangan berat yang merupakan banyaknya air dalam bahan dengan
% Kadar air = Berat awal – berat akhir x 100 % Berat awal
Kadar Abu (Sudarmadji dkk., 1989)
Ditimbang 2 g sampel dalam krus porselin yang kering dan telah diketahui
beratnya. Dipijarkan dalam muffle sampai diperoleh abu berwarna
keputih-putihan. Dimasukkan krus dan abu ke dalam desikator dan ditimbang berat abu
setelah dingin.
% Kadar Abu = Berat abu x 100 % Berat contoh
Kadar Pati (SNI 01-2892-1992)
Sebanyak 1 g sampel dilarutkan dalam 40 mL HCl 3%, dan di refluks
selama 3 jam dengan suhu sekitar 200-250˚C. Kemudian sampel didinginkan dan
kemudian dinetralkan dengan menambahkan beberapa tetes NaOH 3% dengan
bantuan indikator PP sampai berwarna merah muda dan diasamkan sedikit dengan
ditera dalam labu takar 100 mL dengan menggunakan akuades, kemudian
disaring. Sebanyak 5 mL filtrat dipipet ke dalam erlenmeyer asah dan
ditambahkan 25 mL larutan Luff Schrool dan 20 mL akuades dan direfluks
kembali selama 10 menit (dihitung pada saat mulai mendidih). Setelah mendidih,
kemudian didinginkan dalam es selama beberapa menit. Kemudian sampel yang
telah dingin ditambahkan 25 mL H2SO4 25% dan 15 mL larutan KI 20% lalu
segera dititrasi dengan Na2S2O3 0.1 N yang telah distandarisasi. Penambahan
indikator kanji 0.5% dilakukan pada saat titrasi berlangsung, titrasi dihentikan
pada saat larutan berubah warna dari ungu menjadi putih keruh.
Kadar pati diukur dengan cara sebagai berikut :
Kadar Pati =
x 100%
Dimana :
G = mg glukosa dari tabel (Vol Na2S2O3 Blanko - Vol Na2S2O3 contoh)
Fp = Faktor pengenceran
W = Bobot contoh (mg)
Kadar Amilosa (Apriyantono et al., 1989) dan Amilopektin
Sebanyak 100 mg sampel ditimbang dan dimasukkan dalam labu ukur 100
ml, kemudian 1 ml etanol 95% dan 9 ml NaOH 1 N ditambahkan ke dalam
sampel. Larutan dipanaskan dalam waterbath (air mendidih) selama 10 menit
(sampai pati tergelatinisasi. Setelah itu, labu ukur yang berisi sampel didinginkan
selama 1 jam dan ditambahkan akuades sampai tanda tera, kemudian dikocok.
Sebanyak 5 ml larutan sampel dipipet dan dimasukkan ke dalam labu ukur 100 ml
kemudian ditambahkan air sampai tanda tera. Larutan sampel dikocok dan
dibiarkan selama 20 menit. Larutan sampel diambil untuk dianalisa
spektrofotometer. Selain itu, dibuat juga larutan blanko dengan cara
mencampurkan semua bahan kecuali sampel. Kadar amilosa diukur dengan cara
sebagai berikut :
Kadar amilosa (%) =
x 100%
Dimana:
A = konsentrasi amilosa dari kurva standar (mg/ml)
Fp = faktor pengenceran
V = volume awal (ml)
W = bobot awal (mg)
Kadar amilopektin diperoleh dari selisih antara kadar pati dengan kadar
amilosa sampel.
Analisis Produk Maltodekstrin
1. Penentuan % kadar gula pereduksi metode Luff Schrool (SNI 01- 2891-1992 titrasi iodometri)
Sampel diambil sebanyak 5 g ditimbang dengan neraca analitik dan
dimasukkan ke dalam labu takar 250 ml serta ditambah air aquades hingga tanda
batas. Kemudian disaring dan dipipet 10 ml, filtratnya dimasukkan ke dalam labu
takar 250 ml. Ditambahkan 10 ml Pb asetat 5% kemudian dikocok. Larutan yang
didapat dites dengan tetesan larutan Na2HPO4 10 %, bila timbul endapan putih
dibiarkan sekitar 30 menit dan kemudian disaring. Sebelum terjadi inversi filtrat
sebanyak 10 ml dipipet ke dalam labu erlenmeyer 500 ml bertutup asah.
Kemudian ditambahkan 15 ml air, dan 25 ml larutan Luff Schoorll
dipanaskan selama 2 menit sampai mendidih dan dididihkan terus selama 10
menit dengan nyala kecil diangkat dan didinginkan cepat. Setelah dingin
ditambahkan 5 ml KI 20 % dan 5 ml H2SO4 25 % dengan pelan-pelan.
Selanjutnya dititrasi dengan larutan Natrium thiosulfat 0,1 N dan larutan kanji 1
% sebagai indikator titrasi sampai warna biru tua hilang. Dari selisih kedua
penitaran dapat dihitung jumlah glukosa fruktosa atau gula invert dengan
menggunakan daftar tabel Lehman.
Penentuan pada tabel Lehman (mg kesetaraan).
Kadar gula reduksi =
x
100%Dimana :
mg kesetaraan = volume blanko – volume sampel ( yang dikorelasikan
dengan tabel Luff Schroorl )
fP = faktor pengenceran yaitu bagian dari keseluruhan suatu
sampel yang diambil dari labu ukur
fN = faktor normalitas Na2S2O3 (0,1 N )
ml sampel total = volume sampel sebelum dianalisis
Ket : dari 100 ml larutan sampel diambil 10 ml untuk setiap kali titrasi, jadi factor
2. Penentuan DE (Dekstrosa Ekuivalen) (Shi dkk, 2000)
Nilai Dextrose Equivalen diawali dengan mencari nilai Fehling factor
dengan cara 2,5g glukosa dilarutkan dengan aquades sampain 1000 ml lalu
diambil 15 ml dan ditambahkan larutan Fehling A dan B masing-masing 5 ml.
Campuran di didihkan kemudian dititrasi dengan larutan glukosa sampai warna
cokelat kemerahan, kebutuhan titran dicatat lalu Fehling factor dihitung dengan
cara:
FF =
Setelah itu membuat maltodekstrin 10 gr dalam 200 ml aquades,
masukkan kedalam buret. Sedangkan kedalam elemeyer masukkan 50ml aquades,
ditambahkan masing-masing 5 ml Fehling A dan Fehling B dan indicator metilen
blue 3 tetes. Larutan di didihkan dan dititrasi dengan larutan sirup gula sampai
berwarna cokelat kemerahan. Titran yang dibutuhkan dicatat kemudian hitung
nilai DE.
DE = FF x
3. Penentuan Rendemen
Rendemen dihitung atas dasar rumus sebagai berikut :
%
4. Penentuan viskositas (Sukardjo, 2002)
Penentuan waktu alir zat pada viskosimeter oswald (t2) dilakukan dengan
cara yaitu diambil 10 ml sampel dan dimasukkan kedalam viskosimeter oswald.
Sampel diisap dengan bola bulb sampai batas tanda yang terdapat pada alat
viskometer. Sampel dibiarkan mengalir kebawah sampai batas tanda yang terdapat
pada alat. Dicatat waktu yang diperlukan dengan menggunakan stopwatch.
Penentuan massa jenis zat (ρ2) dilakukan dengan cara yaitu diambil 10 ml sampel
kemudian diukur beratnya. Massa jenis adalah hasil pembagian antara berat zat
dengan volum zat. Dilakukan penghitungan viskositas dengan menggunakan
rumus sebagai berikut:
η1/η2= ρ1 t1/ρ2 t2
5. Daya Larut Air (SNI 06-1451-1989)
Ditimbang teliti 2 g sampel, kemudian dimasukkan kedalam labu ukur 200
ml. Dibilas botol timbang dengan air aquadest sampai volume kira-kira 150 ml.
Kemudian dikocok dan dibiarkan beberapa jam sambil sesekali digoyangkan.
Ditambahkan air sampai tanda tera dan dibiarkan sampai 24 jam di dalam oven
pada suhu 37oC. Disaring dalam pipet 10 ml filtrate dimasukkan ke dalam krus
porselin 50 ml yang diketahui beratnya. Dipanas kan dalam oven selama 3 jam
hingga bobot tetap.
Daya Larut dalam Air = ( ) x100% C
B A
B = Berat akhir C = Berat sampel
6. Daya Serap (SNI 06-1451-1989)
Ditimbang teliti 2 g sampel, kemudian dimasukkan kedalam labu ukur 200
ml. Dibilas botol timbang dengan air aquadest sampai volume kira-kira 150 ml.
Kemudian dikocok dan dibiarkan beberapa jam sambil sesekali digoyangkan.
Ditambahkan air sampai tanda tera dan dibiarkan sampai 24 jam di dalam oven
pada suhu 37oC. Disaring dalam pipet 10 ml filtrate dimasukkan ke dalam krus
porselin 50 ml yang diketahui beratnya. Dipanas kan dalam oven selama 3 jam
hingga bobot tetap.
Daya Serap = ( ) x100% C
B A
HASIL DAN PEMBAHASAN Karakteristik Pati Gadung
Pati gadung yang dihasilkan dalam penelitian pendahuluan mempunyai
rendemen 20,09% terhadap umbi tanpa kulit, dengan komposisi kimia pati gadung
seperti pada Tabel 4 di bawah ini:
Tabel 4. Karakteristik pati gadung.
Keterangan : Analisis dilakukan dengan ulangan 3 kali, hasil rataan
Kadar air pati gadung adalah sebesar 8,3%. Menurut Syafi’i dkk. (2009)
kadar air pati rata-rata gadung berkisar antara 11,26% - 12,34%. Kadar air pati
gadung akan semakin turun dengan semakin meningkatnya lama pemanasan.
Winarno (2004) mengatakan bahwa semakin lama waktu pemanasan maka
molekul-molekul air yang terdapat pada jaringan, membran, ataupun kapiler pada
tanaman akan mudah keluar karena dinding jaringan akan mengalami
perenggangan atau pengembangan sehingga kekuatan ikatan molekul air akan
menurun.
Kadar abu pati gadung pada penelitian ini didapatkan sebesar 0,8%
menunjukkan bahwa tepung gadung telah melalui proses pengolahan yang baik.
Kadar abu pati gadung lebih rendah dibandingkan kadar abu maksimum untuk
terigu dan tepung beras berdasarkan SNI yaitu berturut-turut sebesar 0,70% dan
1%. Menurut Suismono (1998) penurunan kadar abu pati gadung disebabkan oleh
pengepresan akan menyebabkan mineral keluar bersama dengan air. Kadar abu
memiliki hubungan dengan mineral suatu bahan. Mineral yang terdapat dalam
suatu bahan dapat merupakan dua macam garam yaitu garam organik dan garam
anorganik. Kadar abu merupakan ukuran umum kualitas dan berguna bagi
identifikasi bahan makanan. Bila diperoleh nilai abu yang lebih besar maka di
dalam bahan makanan tersebut terkandung zat pengotor asing yang tinggi pula
(Triyono, 2007).
Pati merupakan unsur dengan jumlah terbesar yang terkandung dalam
tepung gadung. Pada hasil penelitian sebelumnya (Triyono, 2007) menunjukkan
rendemen pati ubi kayu berkisar antara 46,66 – 59,92%. Rendemen pati gadung
ditentukan dari pati gadung dengan kadar air 8,3% diperoleh hasilnya sekitar
70,63%.
Kadar HCN pada pati gadung didapatkan sebesar 14,95ppm. Hal ini
dapat tolerir karena pada penelitian yang dilakukan oleh Harijono, dkk (2008)
didapatkan kadar HCNnya yaitu 60,88ppm. Pati gadung telah mengalami
beberapa tahapan proses berupa pemanasan, pencucian dan pembilasan kembali
serta pengeringan pada saat pengolahan gadung menjadi pati gadung. Proses
pengeringan juga mampu menurunkan kandungan HCN dalam pati gadung.
Menurut Suryani dan Wesniati (2000) saat dikeringkan sianida yang terkandung
dalam bahan akan menguap sehingga kadar sianida pada pati pun menurun.
Gula Reduksi yang terkandung pada pati gadung hasil penelitian adalah
sebesar 1,02%. Mengindikasikan bahwa gula reduksi pati gadung cukup rendah
dibanding umbi lainnya.
Hasil penelitian menunjukkan bahwa perlakuan pH yang berbeda serta
waktu yang berbeda pada saat likuifikasi pati gadung menggunakan enzim α
-amilase yang hasilnya adalah maltodekstrin ternyata memberikan pengaruh yang
berbeda nyata (P< 0,05) terhadap parameter yang diamati yaitu : Dextrosa
equivalent, gula reduksi, viskositas, rendemen, daya serap dan daya larut.
Rendemen (%)
Perlakuan pH dengan Waktu Terhadap Rendemen
Dari daftar analisis sidik ragam (Lampiran 3) dapat dilihat bahwa
pengaruh perlakuan pH dan waktu memberikan pengaruh yang berbeda sangat
nyata (P < 0,01) terhadap rendemen yang dihasilkan, dapat dilihat pada Tabel 5.
Tabel 5. Nilai Rendemen Maltodekstrin pada pH dan Waktu yang Berbeda
pH Waktu (menit) Rendemen
sebesar 70,80%. Rendemen adalah persentase produk yang didapatkan dari
perbandingan berat awal bahan dengan berat akhirnya. Sehingga diketahui
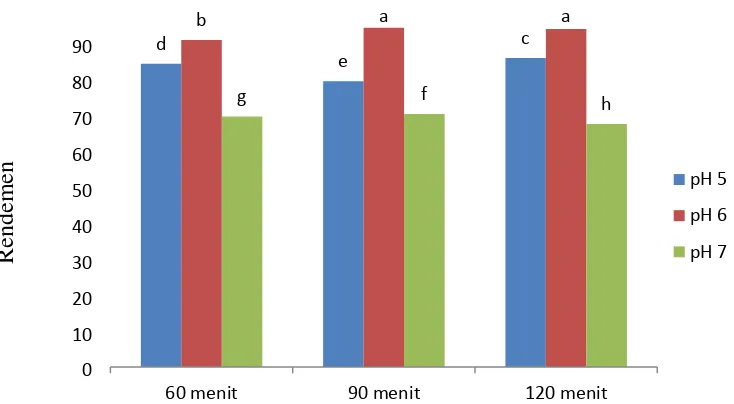
Gambar 4. Hubungan antara pH proses enzimatis dan waktu terhadap Rendemen maltodekstrin
Banyak faktor yang mempengaruhi tinggi rendahnya nilai rendemen yang
dihasilkan beberapa faktornya adalah susut bobot pada saat proses likuifikasi,
pengeringan, penggilingan dan pengayakan ( Triyono, 2007). Pada pH 6 dan
waktu likuifikasi 120 menit juga didapatkan nilai rendemen yang relatif baik, hal
ini menunjukkan bahwa aktivitas kerja enzim yang optimum cenderung terjadi
pada waktu proses 90 menit dan 120 menit dengan pH 6.
pH yang optimal dan stabil meningkatkan efektifitas enzim mengubah pati
menjadi glukosa, sehingga diperoleh rendemen sirup glukosa lebih banyak. pH
yang tidak tepat akan memperlambat atau menghambat kerja enzim, sehingga
enzim tidak dapat mengubah pati menjadi sirup glukosa. Hal ini sesuai dengan
pendapat Bastian (2012), tiap enzim memerlukan suhu dan pH (tingkat keasaman)
optimum yang berbeda-beda karena enzim adalah protein, yang dapat mengalami
perubahan bentuk jika suhu dan keasaman berubah. Di luar suhu atau pH yang
sesuai, enzim tidak dapat bekerja secara optimal atau strukturnya akan mengalami
Berdasarkan penelitian yang telah dilakukan oleh Anita (2009) nilai
rendemen maltodekstrin pada pH 6 paling optimum sebesar 77,49% sedangkan
pada pH 7 paling optimum sebesar 76,80%. Hal ini menunjukkan bahwa pada pH
6 lebih optimum dari pada pH 7 untuk mendapatkan nilai rendemen yang lebih
tinggi.
Gula Reduksi
Dari daftar analisis sidik ragam (Lampiran 4) dapat dilihat bahwa
pengaruh perlakuan pH dan waktu memberikan pengaruh yang berbeda sangat
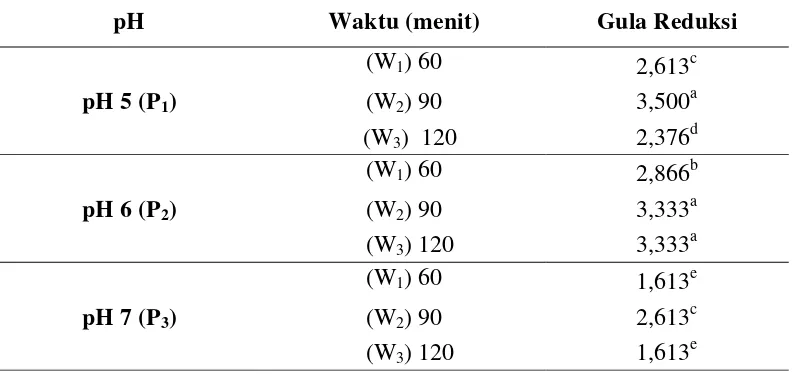
nyata (P < 0,01) terhadap gula reduksi yang dihasilkan, dapat dilihat pada Tabel 6.
Tabel 6. Nilai Gula Reduksi Maltodekstrin pada pH dan Waktu yang Berbeda
pH Waktu (menit) Gula Reduksi
pH 5 (P1)
(W1) 60 2,613c
(W2) 90 3,500a
(W3) 120 2,376d
pH 6 (P2)
(W1) 60 2,866b
(W2) 90 3,333a
(W3) 120 3,333a
pH 7 (P3)
(W1) 60 1,613e
(W2) 90 2,613c
(W3) 120 1,613e
Nilai gula reduksi yang tertinggi terdapat pada pH 5 dengan waktu
likuifikasi 90 menit yaitu 3,5% dan yang terendah terdapat pada pH 7 dengan
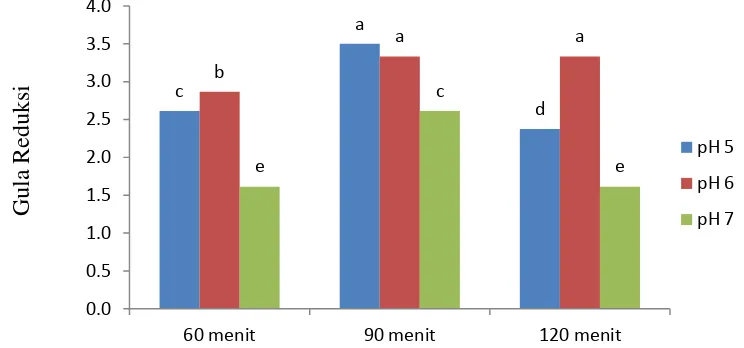
Gambar 5. Hubungan antara pH proses enzimatis dan waktu terhadap Gula Reduksi maltodekstrin
Data awal pada penelitian ini menunjukkan bahwa kadar gula reduksi pati
gadung adalah sekitar 1,02%. Secara kuantitatif lebih rendah dari nilai gula
reduksi yang didapat setelah dilakukan hidrolisis dengan penambahan enzim. Hal
ini disebabkan oleh granula pati gadung akan terhidrolisa secara sempurna saat
hidrolisis berlangsung, jika suhu medium substrat melewati suhu 84ºC (suhu
maksimum gelatinisasi pati gadung) maka seluruh bagian granula pati akan
tergelatinisasi secara keseluruhan (Parwiyanti, et al., 2011).
Kadar gula reduksi meningkat pada menit 90 dan menit ke 120, diduga
bahwa penggunaan enzim α- amilase dapat menghidrolisa substrat pati secara
sempurna pada pH 6 sehingga saat gelatinisasi terjadi menghasilkan amilosa dan
amilopektin dengan rantai yang lebih pendek. Suhu gelatinisasi pati gadung
berkisar antara 70ºC sampai dengan 84ºC (Satyatama, 2005). Hal ini juga
disebabkan semakin lama waktu hidrolisa maka kesempatan enzim untuk