KARAKTERISASI DAN UJI AKTIVITAS ANTIOKSIDAN
MINYAK HASIL EKSTRAKSI BIJI HONJE
(Etlingera elatior)
GUNTUR SETIAJI
PROGRAM STUDI KIMIA FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH JAKARTA
KARAKTERISASI DAN UJI AKTIVITAS ANTIOKSIDAN MINYAK HASIL EKSTRAKSI BIJI HONJE (Etlingera elatior)
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains
Program Studi Kimia
Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
Oleh:
GUNTUR SETIAJI 109096000031
PROGRAM STUDI KIMIA FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI (UIN) SYARIF HIDAYATULLAH JAKARTA
PERNYATAAN
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI ADALAH
HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI
SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU
LEMBAGA MANAPUN.
Jakarta, Oktober 2014
ABSTRAK
GUNTUR SETIAJI, Karakterisasi dan Uji Aktivitas Antioksidan Minyak Hasil Ekstraksi Biji Honje (Etlingera elatior) di bawah bimbingan DEDE SUKANDAR dan SITI NURBAYTI
Karakterisasi senyawa antioksidan dari minyak hasil ekstraksi biji honje
(Etlingera elatior) telah dilakukan. Biji honje yang berasal dari Pangandaran,
Jawa Barat, diekstraksi menggunakan metode sokletasi dengan pelarut n-heksan dan dietil eter, uji aktivitas antioksidan dengan metode TBA (Thiobarbituric acid) serta karakterisasi dengan GCMS, Spektrofotometer UV, dan FTIR. Sokletasi menggunakan pelarut n-heksan menghasilkan rendemen sebesar 2,75% sedangkan menggunakan pelarut dietil eter sebesar 1,94%. Hasil uji aktivitas antioksidan menunjukkan nilai IC50 dari minyak biji honje hasil sokletasi dengan pelarut
n-heksan adalah 92,11 ppm, sedangkan hasil sokletasi dengan pelarut dietil eter adalah 122,45 ppm. Karakterisasi menggunakan GCMS menunjukkan tiga senyawa dengan persen area tinggi yang diduga bersifat antioksidan yaitu, oktadek-9-asam enoat (31,25%), asam askorbat-2,6-diheksadekanoat (12,55%) dan eukaliptol (4,46%). Pemisahan minyak biji honje hasil sokletasi dengan pelarut n-heksan menggunakan KLT diperoleh 3 isolat, di mana isolat 2 memiliki % inhibisi tertinggi yaitu 33,89%. Karakterisasi isolat 2 menggunakan spektrofotometer UV-Vis menunjukkan adanya gugus kromofor C=O pada maks
272,73 nm serta analisis FTIR menunjukkan adanya gugus –CH2– alifatik
(2924,22 dan 2856,23 cm-1), gugus fungsi C=O (1746,67 dan 1715,89 cm-1), –CH3 alifatik (1459,64 dan 1377,53 cm-1), C–O alkohol (1239,96; 1163,46; dan
1119,39 cm-1), dan –CH2– (722,62 cm-1).
ABSTRACT
GUNTUR SETIAJI, Characterization and Antioxidant Activity Assay of Extracted Oil from Etlingera elatior under the guidance of DEDE SUKANDAR
and SITINURBAYTI
Characterization of antioxidant compound from Etlingera elatior seed oil has been studied. E. elatior seed which came from Pangandaran, West Java, was extracted using soxhlet method in hexane and diethyl ether, the antioxidant activity was investigated using TBA (Thiobarbituric acid) assay, and characterization was performed using GCMS, UV Spectrophotometre, and FTIR. Soxhletation using hexane as solvent produce 2.75% yields, while using diethyl ether produce 1.94% yields. The result of antioxydant assay showed IC50 value of
E. elatior seed oil that extracted by hexane is 92.11 ppm, while diethyl ether one
is 122.45 ppm. The result of GCMS analysis indicated three chemical compounds with high percent area were estimated as antioxidant with octadec-9-enoic acid (31.25%) constituting the bulk of the oil from Etlingera elatior, followed by ascorbic acid-2,6-dihexadecanoic (12.55%) and eucalyptol (4.46%). TLC result of
E. elatior seed oil that extracted by hexane showed 3 spot, which second spot has
highest % inhibition value, at 33.89%. UV characterization of second spot indicated chromophore group C=O conjugated at maks at 272.73 nm and FTIR
anlysis indicated –CH2– aliphatic (2924.22 and 2856.23 cm-1), C=O function
group (1746.67 and 1715.89 cm-1), –CH3 aliphatic (1459.64 and 1377.53 cm-1),
C–O alcohol (1239.96; 1163.46; and 1119.39 cm-1), and –CH2– (722.62 cm-1).
viii
KATA PENGANTAR
Alhamdulillahirabbil’alamin, puji dan syukur penulis panjatkan ke hadirat
Allah SWT yang telah melimpahkan rahmat dan hidayah-Nya sehingga penulis
dapat menyelesaikan penulisan dan penyusunan skripsi yang berjudul
“Karakterisasi dan Uji Aktivitas Antioksidan Minyak Hasil Ekstraksi Biji Honje
(Etlingera elatior)”. Shalawat dan salam semoga senantiasa tercurahkan kepada
Nabi Muhammad SAW beserta keluarga, para sahabatnya, dan para pengikutnya
yang selalu menjalankan Sunnahnya sampai hari kiamat.
Penulisan dan penyusunan skripsi ini dapat terselesaikan tidak lepas dari
bantuan berbagai pihak, maka pada kesempatan ini penulis menyampaikan terima
kasih kepada:
1. Bapak Drs. Dede Sukandar, M.Si selaku Pembimbing I yang telah
membimbing dan membantu penulis dalam penelitian serta penulisan skripsi
ini serta selaku Ketua Prodi Kimia Fakultas Sains dan Teknologi UIN Syarif
Hidayatullah Jakarta.
2. Ibu Siti Nurbayti, M.Si selaku Pembimbing II yang telah memberikan
bimbingannya dalam menyelesaikan penulisan dan penyusunan skripsi ini.
3. Bapak Dr. Agus Salim, M.Si selaku Dekan Fakultas Sains dan Teknologi
Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
4. Ibu Yusraini Dian Inayati Siregar, M.Si dan Bapak Adi Riyadhi, M.Si selaku
ix
5. Seluruh dosen Kimia FST UIN yang telah memberikan ilmu dan
pengetahuannya kepada penulis.
6. Seluruh Laboran di Laboratorium Kimia dan Pangan yang telah membantu
penulis selama penelitian berlangsung.
7. Kedua orang tua penulis, yang selalu mendoakan dan memberikan dukungan
baik secara moril maupun materil kepada penulis.
8. Teman-teman penelitian Kimia Bahan Alam yang telah memberikan
informasi dan sharing ilmu selama melakukan penelitian, penulisan dan
penyusunan skripsi ini.
9. Teman-teman Kimia angkatan 2009 yang telah memberikan motivasi kepada
penulis.
Penulis menyadari bahwa dalam penulisan dan penyusunan skripsi ini
masih banyak terdapat kesalahan dan kekurangan. Oleh karena itu, kritik dan
saran yang bermanfaat untuk kesempurnaan penulisan skripsi ini sangat penulis
harapkan. Semoga skripsi ini dapat memberikan manfaat bagi penulis secara
khusus dan bermanfaat serta dapat memberikan pengetahuan bagi para
pembacanya.
Jakarta, Oktober 2014
x
DAFTAR ISI
Halaman
KATA PENGANTAR ... viii
DAFTAR ISI ... x
DAFTAR GAMBAR ... xiii
DAFTAR TABEL ... xv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Rumusan Masalah ... 3
1.3. Hipotesis ... 4
1.4. Tujuan Penelitian ... 4
1.5. Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1. Honje (Etlingera elatior) ... 5
2.1.1. Taksonomi Honje ... 6
2.1.2. Morfologi Honje ... 6
2.1.3. Manfaat Honje ... 8
2.1.4. Kandungan Kimia ... 9
2.2. Ekstraksi ... 11
2.2.1. Ekstraksi Cara Panas ... 11
2.2.2. Ekstraksi Cara Dingin ... 13
xi
2.4. Antioksidan ... 18
2.4.1. Sumber-sumber Antioksidan ... 18
2.4.2. Mekanisme Kerja Antioksidan ... 20
2.4.3. Uji Antioksidan Metode Thiobarbituric Acid (TBA) ... 21
2.5. Kromatografi Lapis Tipis (KLT) ... 23
2.5.1. Fase diam KLT ... 24
2.5.2. Fase gerak KLT ... 25
2.6. Gas Chromatography Mass Spectrometry (GCMS) ... 26
2.6.1. Prinsip Kerja GCMS ... 26
2.6.2. Instrumentasi GCMS ... 27
2.7. Spektrofotometri UV-Vis (Ultraviolet-Visible) ... 30
2.8. Spektrofotometri Infrared (IR) ... 33
2.8.1. Gerak Molekul pada Infrared (IR) ... 34
2.8.2. Daerah Identifikasi pada Infrared (IR) ... 35
2.8.3. Instrumentasi FTIR ... 36
BAB III METODE PENELITIAN ... 38
3.1. Tempat dan Waktu Pelaksanaan ... 38
3.2. Bahan dan Alat ... 38
3.2.1. Bahan ... 38
3.2.2. Alat ... 39
3.3. Prosedur Kerja... 39
3.3.1. Ekstraksi Sokletasi ... 39
xii
3.3.3. Uji Fitokimia ... 40
3.3.4. Uji Aktivitas Antioksidan ... 41
3.3.5. Analisis GC-MS ... 42
3.3.6. Uji Kromatografi Lapis Tipis (KLT) ... 43
3.3.7. Analisis Spektrofotometri UV ... 44
3.3.8. Analisis FTIR ... 44
BAB IV HASIL DAN PEMBAHASAN ... 45
4.1. Hasil Determinasi ... 45
4.2. Hasil Ekstraksi Sampel ... 45
4.3. Hasil Uji Fitokimia... 46
4.4. Hasil Uji Antioksidan... 49
4.5. Hasil Analisis GC-MS ... 51
4.7. Hasil Analisis Spektrofotometri UV ... 60
4.8. Hasil Analisis FTIR ... 61
4.9. Mekanisme Reaksi Antioksidan... 63
BAB V KESIMPULAN DAN SARAN ... 65
5.1. Kesimpulan ... 65
5.2. Saran ... 66
DAFTAR PUSTAKA ... 67
xiii
DAFTAR GAMBAR
Halaman
Gambar 1. Peta Penyebaran Honje... 5
Gambar 2. (a) Pohon Honje (b) Buah Honjedan (c) Biji Honje... 7
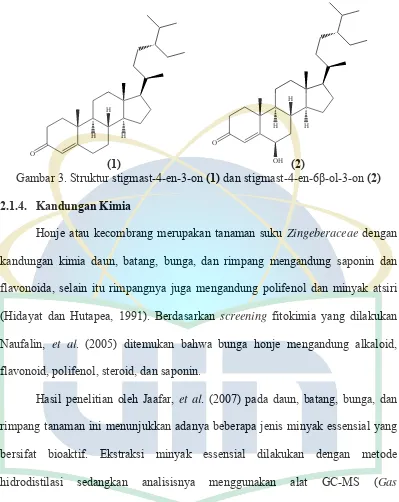
Gambar 3. Struktur stigmast-4-en-3-on (1) dan stigmast-4-en-6β-ol-3-on (2) ... 9
Gambar 4. Struktur(E)-ß-Farnesen (3), ß-Pinen (4), Kariofilen (5), 1,1-dodekanadiol diasetat (6), (E)-5-Dodekana (7), Siklododekana (8), Struktur 1-dodekanol (9), 1-tetradekena (10), dan 5-(3-Metil-but-1-eniloksi)-benzena-1,2,4-triol (11) ... 10
Gambar 5. Ekstraktor Soklet ... 12
Gambar 6. Ekstraktor Refluks ... 12
Gambar 7. Struktur vitamin C (12), katekin (13), resveratrol (14), flavonoid (15), β-karoten (16), vitamin E (17), polifenol (18), BHA (19), BHT (20), dan TBHQ (21) ... 19
Gambar 8. Reaksi antara Asam Linoleat dan Etanol untuk Pembentukan Lipid .. 22
Gambar 9. Reaksi Pembentukan Peroksidasi Lipid ... 23
Gambar 10. Reksi Pembentukan Kompleks MDA-TBA ... 23
Gambar 11. Skema GCMS ... 28
Gambar 12. Skema Spektrofotometer UV-Vis ... 30
Gambar 13. Reaksi Uji Terpenoid ... 47
Gambar 14. Reaksi Uji Mayer ... 48
Gambar 15. Reaksi Uji Dragendorff ... 48
Gambar 16. Penentuan Waktu Setimbang ... 49
xiv
Gambar 18. Struktur Senyawa eukaliptol (22), oktadek-9-asam enoat (23)
dan asam askorbat-2,6-diheksadekanoat (24) ... 53
Gambar 19. Hasil Analisis MS Senyawa Eukaliptol ... 53
Gambar 20. Prakiraan Pola Fragmentasi Senyawa Eukaliptol... 54
Gambar 21. Hasil Analisis MS Senyawa Asam Askorbat-2,6-diheksadekanoat .. 55
Gambar 22. Prakiraan Pola Fragmentasi Senyawa Asam Askorbat-2,6- diheksadekanoat ... 56
Gambar 23. Hasil Analisis MS Senyawa Oktadek-9-Asam Enoat ... 57
Gambar 24. Prakiraan Pola Fragmentasi Senyawa Oktadek-9-Asam Enoat ... 57
Gambar 25. Struktur Senyawa terpinen-4-ol (25), p-cimen (26), alfa terpineol (27), dan alfa selinen (28) ... 58
Gambar 26. Spot Minyak Biji Honje Ekstrak n-heksan pada KLT dengan Eluen n-heksan : kloroform (5:2) ... 59
Gambar 27. Spektrum UV Isolat 2 Minyak Biji Honje ... 61
Gambar 28. Spektrum FTIR Isolat 2 Minyak Biji Honje... 61
xv
DAFTAR TABEL
Halaman
Tabel 1. Ringkasan Data Transisi Elektronik ... 33
Tabel 2. Beberapa Frekuensi Gugus Fungsi pada Inframerah ... 36
Tabel 3. Hasil Uji Fitokimia ... 46
Tabel 4. Hasil Uji Aktivitas Antioksidan ... 50
Tabel 5. Senyawa-senyawa yang Memiliki Aktivitas Antioksidan ... 58
Tabel 6. Hasil Uji Antioksidan Isolat Hasil KLT ... 60
xvi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil Determinasi Tanaman Honje (Etlingera elatior) ... 74
Lampiran 2. Bagan Kerja Penelitian ... 75
Lampiran 3. Hasil Sokletasi Biji Honje ... 76
Lampiran 4. Hasil Uji Antioksidan ... 78
Lampiran 5. Optimasi GCMS ... 82
Lampiran 6. Komponen Senyawa Minyak Biji Honje HasilEkstraksi n-heksan ... 83
Lampiran7. Foto Hasil Pemisahan KLT ... 85
1
BAB I PENDAHULUAN
1.1.Latar Belakang
Radikal bebas adalah suatu senyawa yang mempunyai elektron tidak
berpasangan, sehingga senyawa ini bersifat sangat reaktif. Di dalam tubuh kita,
radikal bebas terbentuk secara terus menerus, baik melalui proses metabolisme sel
normal, peradangan, kekurangan gizi dan akibat respon terhadap pengaruh dari
luar tubuh, seperti polusi lingkungan yang disebabkan oleh asap rokok, asap
kendaraan bermotor, asap pembakaran pabrik, sinar ultraviolet (UV) dari cahaya
matahari, senyawa kimia, radiasi, dan lain-lain (Vimala, et al., 2003).
Pada keadaan normal, sejumlah kecil radikal bebas dihasilkan di dalam
tubuh untuk melawan peradangan, membunuh bakteri, dan memelihara fungsi
organ tubuh. Namun karena sifat radikal bebas yang sangat reaktif, jumlah radikal
bebas yang berlebihan dapat menggangu keseimbangan tubuh, serta dapat
berperan dalam terjadinya berbagai proses penyakit pada manusia (Arief, 2008).
Dampak reaktivitas senyawa radikal bebas bermacam-macam, mulai dari
kerusakan sel atau jaringan, penyakit autoimun, penyakit degeneratif, hingga
kanker. Namun reaktivitas radikal bebas itu dapat dihambat oleh sistem
antioksidan yang melengkapi sistem kekebalan tubuh. Secara kimiawi,
antioksidan merupakan senyawa pemberi elektron (electron donors) atau
reduktan. Senyawa ini mampu menginaktivasi berkembangnya reaksi oksidasi,
2 mendonorkan satu elektronnya kepada senyawa yang bersifat radikal sehingga
aktivitas senyawa tersebut dapat dihambat (Winarsi, 2007).
Antioksidan akan bertindak sebagai pemburu radikal bebas dan
menghambat peroksidasi lipid dan radikal bebas lain pada proses mediasi, oleh
karena itu antioksidan mampu melindungi tubuh manusia dari beberapa penyakit
yang disebabkan oleh reaksi radikal bebas (Arora dan Chandra, 2011)
Senyawa antioksidan yang sering digunakan dalam industri pengolahan
pangan adalah senyawa antioksidan sintetis seperti butylated hydroxyanisole
(BHA), butylated hydroxytoluene (BHT), propil galat (PG), ethoxyquin (EQ),dan
tert-butyl hydroquinone (TBHQ). Namun beberapa penelitian menemukan bahwa
penggunaan BHA dan BHT yang berlebihan dapat menjadi agen karsinogenik
penyebab penyakit kanker (Błaszczyk, et al., 2013).
Kondisi demikian mendorong penggunaan antioksidan alami yang aman
dikonsumsi bagi manusia. Beberapa jenis bahan pangan dapat menjadi sumber
antioksidan alami, misalnya rempah-rempah, teh, kakao, biji-bijian misalnya biji
atung (Parinarium glabemmum Hassk.) (Sarastani, et al., 2002), serealia,
umbi-umbian seperti umbi akar ginseng Jawa (Talinum trianguiare Wild.) (Estiasih dan
Kurniawan, 2006), sayur-sayuran dan daun-daunan seperti daun suji (Pleomele
angustifolia N.E. Brown) (Prangdimurti, et al., 2006). Menurut Pratt dan Hudson
(1990), antioksidan alami banyak terdapat dalam tanaman dan komponen tersebut
terkandung pada seluruh bagian tanaman seperti akar, daun, bunga, biji, batang,
3 Salah satu tanaman sumber antioksidan alami adalah tanaman honje
(Etlingera elatior). Menurut Antoro (1995), pada rimpang ditemukan senyawa
alkaloid, flavonoid dan minyak atsiri yang bertindak sebagai antioksidan.
Tampubolon, et al., (1983) menyebutkan bahwa honje mengandung senyawa
bioaktif seperti polifenol, alkaloid, flavonoid, steroid, dan saponin yang diduga
memiliki potensi sebagai antioksidan.
Hasil penelitian Jaafar, et al., (2007) menunjukkan adanya beberapa jenis
minyak atsiri pada daun, batang, bunga, dan rimpang tanaman ini masing-masing
0,0735%, 0,0029%, 0,0334%, dan 0,0021%. Ekstraksi dilakukan dengan metode
hidrodistilasi, dan dianalisis dengan menggunakan alat GCMS (Gas
Chromatography Mass Spectrometre). Hasil penelitian (Sukandar, et al., 2010)
menunjukan bahwa ekstrak air bunga honje memiliki aktivitas antioksidan dengan
nilai IC50 sebesar 61,6497 ppm.
Namun demikian penelitian mengenai karakterisasi minyak biji honje
belum pernah dilakukan. Hal inilah yang melatarbelakangi dilakukannya
penelitian ini, sebagai langkah untuk mengetahui potensi minyak biji honje
(Etlingera elatior) yang diduga memiliki aktivitas antioksidan.
1.2. Rumusan Masalah
1. Bagaimana aktivitas antioksidan minyak biji honje (Etlingera elatior) hasil
ekstraksi menggunakan pelarut n-heksan dan dietil eter dengan menggunakan
4 2. Bagaimanakah karakteristik senyawa antioksidan dari minyak biji honje
(Etlingera elatior) yang memiliki aktivitas antioksidan paling baik
berdasarkan analisis GCMS, Spektrofotometri UV, dan FTIR?
1.3. Hipotesis
1. Minyak biji honje (Etlingera elatior) hasil ekstraksi menggunakan pelarut
n-heksan dan dietil eter memiliki aktivitas antioksidan.
2. Senyawa yang memiliki aktivitas antioksidan dalam minyak biji honje
(Etlingera elatior) hasil ekstraksi menggunakan pelarut n-heksan dan dietil
eter adalah senyawa golongan terpenoid.
1.4. Tujuan Penelitian
1. Mengetahui aktivitas antioksidan minyak biji honje (Etlingera elatior) yang
diperoleh melalui proses sokletasi menggunakan pelarut n-heksan dan pelarut
dietil eter.
2. Mengidentifikasi senyawa yang yang memiliki aktivitas antioksidan yang
terkandung dalam minyak biji honje (Etlingera elatior).
1.5. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi bahwa minyak biji
honje (Etlingera elatior) hasil ekstraksi menggunakan pelarut n-heksan dan dietil
eter memiliki potensi sebagai antioksidan, serta pemanfaatannya sebagai
5
BAB II
TINJAUAN PUSTAKA
2.1.Honje (Etlingera elatior)
Honje atau kecombrang merupakan tanaman suku Zingeberaceae genus
Nicolaia atau Etlingera yang terdistribusi di Asia Tenggara sampai ke Asia
Selatan dan Australia. Honje umumnya tersebar secara alami di Malaysia dan
Indonesia (Jawa dan Sumatera) tetapi tanaman ini secara luas ditanam sebagai
tanaman tropis untuk tanaman hias dan aromatik (Ibrahim dan Setyowati, 1999).
Menurut Emonocot (2010), honje merupakan tumbuhan endemik di Indonesia
(Jawa, Sumatera, dan Kalimantan), Malaysia, Thailand, dan sudah disebarkan ke
berbagai daerah lain seperti Indonesia bagian timur (Sulawesi, Maluku, dan
Papua), Filipina, sebagian Tiongkok, Puerto Rico, Honduras, Trinidad dan
Tobago, serta daerah lainnya. Adapun peta penyebaran honje menurut Emonocot
(2010) dapat dilihat pada Gambar 1.
6 Honje mempunyai nama latin Etlingera elatior. Honje memiliki beberapa
nama latin yang lain, seperti Nicolaia speciosa Horan, Nicolaia elatior Horan,
Phaeomeria magnifica, speciosa, P. intermedia Valet (Tampubolon, et al., 1983).
Nama-nama lain di daerah tempat tanaman ini tumbuh yaitu kecombrang (Jawa
Tengah), honje (Sunda), kalo (Gayo), puwa kijung (Minangkabau), katinbung
(Makasar), salahawa (Seram), dan petikala (Ternate), (Hidayat dan Hutapea,
1991). Di Negara lain, dikenal dengan nama xiang bao jiang (Tiongkok),
gingembre aromatique (Perancis), boca de dragon (Spanyol), kantan (Malaysia),
kaa laa (Thailand), dan ginger bud/torch ginger (Inggris).
2.1.1. Taksonomi Honje
Menurut Hidayat dan Hutapea (1991), tanaman honje (E. elatior) memiliki
taksonomi sebagai berikut.
Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Liliopsida
Ordo : Zingiberales
Famili : Zingiberaceae
Genus : Etlingera
Spesies : Etlingera elatior
2.1.2. Morfologi Honje
Tanaman honje atau kecombrang merupakan tanaman tahunan yang
berbentuk semak dengan tinggi 1-3 m. Tanaman ini mempunyai batang semu,
7 lanset, ujung dan pangkal runcing tetapi rata, panjang daun sekitar 20-30 cm dan
lebar 5-15 cm, pertulangan daun menyirip, dan berwarna hijau (Gambar 2.a).
Bunga Honje merupakan bunga majemuk yang berbentuk bongkol dengan
panjang tangkai 40-80 cm, panjang benang sari ± 7, 5 cm dan berwarna kuning.
Putiknya kecil dan putih. Mahkota bunganya bertaju, berbulu jarang dan
warnanya merah jambu. Buah honje berbentuk kotak atau bulat telur dengan
warna kuning atau merah jambu (Gambar 2.b). Bijinya kecil dan berwarna coklat
(Gambar 2.c). Akarnya berbentuk serabut dan berwarna kuning gelap
(Syamsuhidayat, 1991).
(a)
(b) (c)
8
2.1.3. Manfaat Honje
Honje merupakan salah satu tanaman rempah yang sejak lama telah
dikenal dan dimanfaatkan manusia sebagai obat-obatan. Menurut Hidayat dan
Hutapea (1991), honje dapat dimanfaatkan sebagai pemberi citarasa pada
masakan, seperti urap, pecel, dan masakan lain. Honje juga dimanfaatkan sebagai
obat-obatan berkaitan dengan khasiatnya, yaitu sebagai penghilang bau badan dan
bau mulut. Penelitian pada rimpang honje telah mengungkapkan khasiat tanaman
ini sebagai antitumor dan antioksidan (Habsah, et al., 2005).
Menurut Sukandar et, al., (2010), ekstrak air bunga kecombrang memiliki
aktivitas antioksidan dengan nilai IC50 sebesar 61,65 g/mL dan memiliki
kemampuansebagai antibakteri terhadap S. aureus dan E. coli. Selain itu, hasil
analisis GCMS pada penelitian yang sama mengungkapkan senyawa yang bersifat
antioksidan dari ekstrak air bunga kecombrang adalah senyawa golongan fenolik.
Hasil studi lain menunjukkan fakta yang lebih mengejutkan karena
ternyata tanaman ini dapat dipakai untuk mengobati penyakit-penyakit yang
tergolong berat yaitu kanker dan tumor. Senyawa kimia stigmast-4-en-3-on (1)
dan stigmast-4-en-6β-ol-3-on (2) (Gambar 3) dari rimpang tanaman ini terbukti mempunyai sifat menghambat pertumbuhan tumor berdasarkan EBV-EA (Epstein
Barr Virus Early Antigens) assay. Senyawa-senyawa tersebut juga bersifat
sitotoksik terhadap kultur sel kanker CEM-SS (LC50 4 g/mL) dan MCF-7 (LC50
6,25 g/mL) berdasarkan MTT (Methyl Thiazole Tetrazolium) assay sehingga
direkomendasikan untuk dapat dipakai sebagai obat atau campuran obat anti
9
Gambar 3. Struktur stigmast-4-en-3-on (1) dan stigmast-4-en-6β-ol-3-on (2) 2.1.4. Kandungan Kimia
Honje atau kecombrang merupakan tanaman suku Zingeberaceae dengan
kandungan kimia daun, batang, bunga, dan rimpang mengandung saponin dan
flavonoida, selain itu rimpangnya juga mengandung polifenol dan minyak atsiri
(Hidayat dan Hutapea, 1991). Berdasarkan screening fitokimia yang dilakukan
Naufalin, et al. (2005) ditemukan bahwa bunga honje mengandung alkaloid,
flavonoid, polifenol, steroid, dan saponin.
Hasil penelitian oleh Jaafar, et al. (2007) pada daun, batang, bunga, dan
rimpang tanaman ini menunjukkan adanya beberapa jenis minyak essensial yang
bersifat bioaktif. Ekstraksi minyak essensial dilakukan dengan metode
hidrodistilasi sedangkan analisisnya menggunakan alat GC-MS (Gas
Chromatography Mass Spectrometer). Berdasarkan penelitian ini terungkap
bahwa terdapat kandungan minyak essensial pada daun sebesar 0,0735%, pada
bunga sebesar 0,0334%, pada batang sebesar 0,0029%, dan pada rimpang sebesar
0,0021%. Komponen utama minyak essensial pada daun adalah β-farnesen (3)
(27,9%), β-pinen (4) (19,7%), dan kariofilen (5) (15,36%), pada batang adalah 1,1-dodekanadiol diasetat (6) (34.26%) dan (E)-5-dodekana (7) (26.99%),
OH O
H H
10 sedangkan pada bunga dan akar adalah 1,1-dodekanadiol diasetat (6) (24.38% dan 40.37%) serta siklododekana (8) (47.28% dan 34.45%) (Gambar 4).
Sementara itu penelitian (Sukandar, et al., 2010) menunjukkan ekstrak air
bunga honje yang dianalisis dengan GC-MS memiliki tiga senyawa utama yaitu
1-dodekanol (9), 1-tetradekena (10), dan 5-(3-Metil-but-1-eniloksi)-benzena-1,2,4-triol (11) (Gambar 4). dodekanadiol diasetat (6), (E)-5-Dodekana (7), Siklododekana
11
2.2. Ekstraksi
Ekstraksi adalah proses pengambilan komponen kimia yang larut dalam
bahan atau sampel dengan menggunakan pelarut seperti air, alkohol, eter, dan
aseton (pelarut ekstraksi tidak boleh saling bercampur). Pemisahan komponen
terjadi atas dasar kemampuan kelarutan yang berbeda dari komponen-komponen
yang terdapat di dalam campuran (Harborne, 1987). Beberapa metode yang
digunakan untuk melakukan proses ekstraksi, yaitu:
2.2.1. Ekstraksi Cara Panas
1. Sokletasi
Sokletasi merupakan ekstraksi menggunakan pelarut yang selalu baru yang
umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi secara kontinu
dan jumlah pelarutnya terbatas dan relatif konstan dengan adanya pendingin balik
(Gambar 5) (Ditjen POM, 1997). Penarikan komponen kimia yang dilakukan
dengan cara serbuk simplisia ditempatkan dalam selongsong yang telah dilapisi
kertas saring sedemikian rupa. Cairan penyari dipanaskan dalam labu alas bulat
sehingga menguap dan dikondensasikan oleh kondensor bola menjadi
molekul-molekul cairan penyari yang jatuh ke dalam selongsong menyari zat aktif di dalam
simplisia dan jika cairan penyari telah mencapai permukaan sifon, seluruh cairan
akan turun kembali ke labu alas bulat melalui pipa kapiler hingga terjadi sirkulasi.
Ekstraksi sempurna ditandai bila cairan di sifon tidak berwarna. Ekstrak yang
diperoleh dikumpulkan dan dipekatkan (Sudjadi, 1986).
Kelebihan metode sokletasi yaitu, dapat mengekstraksi sampel dengan
13
2.2.2. Ekstraksi Cara Dingin
1. Maserasi
Maserasi merupakan cara penyarian yang sederhana. Maserasi dilakukan
dengan cara merendam serbuk simplisia dalam cairan penyari dan pada umumnya
dilakukan pada temperatur ruang. Cairan penyari akan menembus dinding sel atau
masuk ke dalam rongga sel yang mengandung zat aktif. Zat aktif tersebut akan
larut karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel
dengan di luar sel. Larutan yang lebih pekat (di dalam sel) didesak keluar sel,
masuk ke dalam larutan di luar sel. Peristiwa tersebut berulang sehingga terjadi
keseimbangan konsentrasi antara larutan di luar sel dan di dalam sel. Keuntungan
cara penyarian ini adalahcara pengerjaan dan peralatan yang diusahakan
sederhana dan mudah digunakan. Maserasi juga dapat digunakan untuk
mengekstrak senyawa-senyawa yang tidak tahan panas karena tidak dilakukan
pemanasan. Akan tetapi hal tersebut mengakibatkan proses ekstraksi yang kurang
sempurna (Ditjen POM, 1997) (Raaman, 2006).
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna yang umumnya dilakukan pada temperatur ruang. Prosesnya dilakukan
dengan mengalirkan cairan penyari melalui serbuk simplisia yang telah dibasahi
dalam bejana silinder yang bagian bawahnya diberi sekat berpori. Cairan penyari
dialirkan dari atas ke bawah melalui simplisia tersebut. Cairan penyari akan
melarutkan zat aktif dalam sel-sel simplisia yang dilalui sampai keadan jenuh.
14 atas dikurangi gaya kapiler yang menahan gerakan ke bawah. Aliran cairan
penyari menyebabkan adanya pergantian larutan sehingga ekstraksi berlangsung
lebih optimal dibandingkan dengan maserasi. Akan tetapi proses tersebut
membutuhkan waktu yang lama (Ditjen POM, 1997) (Raaman, 2006).
2.3. Radikal Bebas
Menurut Soeatmaji (1998), yang dimaksud radikal bebas (free radical)
adalah suatu senyawa atau molekul yang mengandung satu atau lebih elektron
tidak berpasangan pada orbital luarnya. Adanya elektron yang tidak berpasangan
menyebabkan senyawa tersebut sangat reaktif mencari pasangan, dengan cara
menyerang dan mengikat elektron molekul yang berada di sekitarnya. Radikal
bebas memiliki reaktivitas yang sangat tinggi. Hal ini ditunjukkan oleh sifatnya
yang segera menarik atau menyerang elektron di sekelilingnya. senyawa radikal
bebas juga dapat mengubah suatu molekul menjadi suatu radikal. Target utama
radikal bebas adalah protein, asam lemak tak jenuh dan lipoprotein, serta unsur
DNA termasuk karbohidrat. Serangan radikal bebas terhadap molekul
sekelilingnya akan menyebabkan terjadinya reaksi berantai, yang kemudian
menghasilkan senyawa radikal baru.
Menurut Winarsi (2007), tahapan reaksi pembentukan radikal bebas mirip
dengan rancidity oxidative, yaitu melalui 3 tahapan reaksi berikut.
1. Tahap inisiasi, yaitu awal pembentukan radikal bebas.
M++ + H2O → M+++ + OH- + •OH
15 2. Tahap propagasi, yaitu pemanjangan rantai radikal
R2-H + R1• → R2• + R1-H
R3-H + R2• → R3• + R2-H
3. Tahap terminasi, yaitu bereaksinya senyawa radikal dengan radikal lain atau
dengan penangkap radikal, sehingga potensi propagansinya rendah.
R1• + R1• → R1-R1
R2• + R1• → R2-R1
R2• + R2• → R2-R2
Zat radikal bebas yang terlalu banyak dapat menyebabkan terjadinya
tekanan oksidatif (oxidative stress) di dalam tubuh. Tekanan oksidatif adalah
suatu keadaan dimana tingkat reactive oxygen intermediate (ROI) yang toksik
melebihi pertahanan antioksidan endogen. Keadaan ini mengakibatkan kelebihan
radikal bebas, yang akan bereaksi dengan asam nukleat seluler, protein, dan
lemak, sehingga terjadi kerusakan lokal dan disfungsi organ tertentu. Lemak
merupakan biomolekul yang rentan terhadap serangan radikal bebas (Arief, 2006).
Beberapa akibat yang ditimbulkan oleh radikal bebas, antara lain:
1. Kerusakan DNA
Kerusakan sel akibat reaktivitas senyawa radikal mengawali timbulnya
berbagai penyakit degeneratif seperti kanker, infeksi, rheumatoid, liver, dan aging.
Keadaan ini terjadi karena interaksi senyawa oksigen reaktif dengan DNA
mengawali terbentuknya DNA adduct selama proses replikasi, yang berakibat
16 yang mudah teroksidasi sehingga menyebabkan degradasi dan hancurnya
single-strand (Winarsi, 2007).
2. Kerusakan protein
Protein dan asam nukleat lebih tahan terhadap radikal bebas dari pada
polyunsaturated fatty acid (PUFA), sehingga kecil kemungkinan dalam terjadinya
reaksi berantai yang cepat. Serangan radikal bebas terhadap protein sangat jarang
kecuali bila sangat ekstensif. Hal ini terjadi hanya jika radikal tersebut mampu
berakumulasi (jarang pada sel normal), atau bila kerusakannya terfokus pada
daerah tertentu dalam protein. Salah satu penyebab kerusakan terfokus adalah jika
protein berikatan dengan ion logam transisi (Droge, 2002).
3. Peroksidasi lemak
Membran sel kaya akan sumber polyunsaturated fatty acid, yang mudah
dirusak oleh bahan-bahan pengoksidasi, proses tersebut dinamakan peroksidasi
lemak. Hal ini sangat merusak karena merupakan suatu proses berkelanjutan. Dari
ketiga biomolekul ini, lemak merupakan biomolekul yang sangat rentan terhadap
serangan radikal bebas karena memiliki ikatan π (rangkap) yang terdelokalisasi.
Proses reaksi serangan radikal terhadap lemak berlangsung melalui beberapa
tahapan, yaitu secara inisiasi, propagasi, dan terminasi (Droge, 2002).
Salah satu hasil produk degradasi lemak adalah malondialdehid (MDA).
Malondialdehid (MDA) secara luas banyak digunakan sebagai salah satu indikator
peroksidasi lipid yang dapat ditentukan dalam suatu pengukuran dengan
17 Tidak selamanya radikal bebas berbahaya. Tubuh menghasilkan radikal
bebas karena radikal bebas juga memiliki manfaat bagi tubuh, yaitu untuk
membunuh patogen yang menginvasi tubuh. Radikal bebas menjadi berbahaya
jika jumlahnya berlebihan dan lebih banyak dari antioksidan yang berada di dalam
tubuh, hal ini akan menyebabkan kerusakan oksidatif. Tubuh dilengkapi dengan
sel-sel inflamasi seperti sel granulosit, monosit, dan makrofag, yang dapat
memproduksi senyawa-senyawa yang bersifat oksidan. (Winarsi, 2007).
Berikut beberapa contoh peranan radikal bebas sebagai senyawa oksigen
reaktif dan senyawa nitrogen reaktif yang secara fisiologis berperan sebagai
regulator dalam metabolisme.
1. Anion superoksida berperan dalam kemotaksis bakteri.
2. Senyawa oksigen reaktif berperan dalam proses bakterisidal dan bakteriolisis
normal. Seperti diketahui, senyawa oksigen reaktif jugfa disintesis sel fagosit
melalui jalur NADP oksidase, seperti radikal O2 dan H2O2 yang berperan
sebagai pembunuh bakteri (bakterisidal). Oleh sebab itu seseorang yang
kekurangan NADP oksidase akan mudah mengalami inflamasi berulang.
3. Radikal O2 memiliki sifat vasokonstriktor pada otot halus atau dalam
fibroblas.
4. Senyawa oksigen reaktif berperan dalam sintesis DNA karena aktivitas
ribonukleotida reduktase (yang mengubah ribosa menjadi doksiribosa) sangat
bergantung pada senyawa oksogen reaktif.
5. Senyawa oksigen reaktif berperan dalam kapasitasi spermatozoid sehingga
18
2.4. Antioksidan
Antioksidan merupakan senyawa yang dapat menghambat radikal bebas
sehingga antioksidan dapat mencegah penyakit-penyakit yang dihubungkan
dengan radikal bebas seperti karsinogenesis, kardiovaskular, dan penuaan
(Gutteridge dan Halliwell, 2000). Arti lainnya, antioksidan adalah senyawa yang
dapat melawan dan menetralisir radikal bebas dan memperbaiki kerusakan
oksidatif pada molekul biologis (Vimala, et al., 2003).
2.4.1. Sumber-sumber Antioksidan
a) Antioksidan alami
Antioksidan alami berasal dari tumbuhan yang sering dikonsumsi dan
telah diisolasi. Antioksidan yang terdapat dalam tumbuhan mengandung vitamin
C (12), katekin (13), resveratrol (14), flavonoid (15), β-karoten (16), vitamin E
(17), dan polifenol (18) (Gambar 7) (Hernani dan Rahardjo, 2006). b) Antioksidan sintetik
Antioksidan sintetik diizinkan penggunaannya dalam makanan untuk
menjaga mutu dan dari perubahan sifat kimia makanan akibat proses oksidasi
yang terjadi terutama pada waktu penyimpanan. Beberapa contoh antioksidan
sintetik yang diijinkan penggunaanya secara luas diseluruh dunia untuk digunakan
dalam makanan adalah Butylated Hidroxyanisol (BHA) (19), Butylated
Hidroxytoluene (BHT) (20), dan Tert-Butylated Hidroxyquinon (TBHQ) (21)
(Gambar 7). Antioksidan tersebut merupakan antioksidan yang telah diproduksi
secara sintetis untuk tujuan komersial (Buck, 1991).
20
2.4.2. Mekanisme Kerja Antioksidan
Antioksidan dalam menghambat jalannya reaksi oksidasi dapat melalui
beberapa cara, yaitu mekanisme donor proton, radical scavenger, oxygen
quencher, inhibisi dengan enzim, dan sinergis (Gordon, 1990).
Peranan antioksidan khususnya antioksidan fenolik dalam peroksida lipid
dapat digambarkan sebagai berikut:
ROO• + AH → ROOH + A•
RO• + AH → ROH + A•
R• + AH → RH + A•
HO• +AH → H2O + A•
Pada reaksi tersebut antioksidan (AH) bertindak sebagai donor hidrogen,
di mana hidrogen tersebut akan berikatan dengan radikal bebas (ROO•, RO•, R•,
dan HO•) dari lemak atau minyak sehingga membentuk senyawa yang stabil.
Pemberian atom hidrogen ini juga merupakan tahap awal dari mekanisme
antioksidan melalui radical scavenger (pemerangkap radikal). Radikal baru yang
terbentuk yaitu A• dapat langsung bergabung dengan radikal-radikal lain
membentuk senyawa yang tidak reaktif. Beberapa contoh radical scavenger
adalah Vitamin C (12), β-karoten (16), vitamin E (tokoferol) (17), BHA (19), dan BHT (20) (Winarsi, 2007).
Berdasarkan fungsinya, antioksidan dikelompokkan menjadi antioksidan
21 1. Antioksidan primer
Antioksidan primer yaitu antioksidan yang dapat bereaksi dengan radikal
lipid lalu mengubahnya ke bentuk yang lebih stabil. Antioksidan primer bekerja
untuk mencegah terbentuknya reaksi berantai radikal bebas dengan melepaskan
hidrogen sehingga tidak mampu lagi untuk bereaksi. Contohnya adalah enzim
SOD (Superoxide Dismutase) yang berfungsi sebagai pelindung sel dalam tubuh
serta mencegah proses peradangan karena radikal bebas. Antioksidan primer
seperti enzim SOD (Superoxide Dismutase), enzim katalase, dan enzim glutation
peroksidase. (Gordon, 1990).
2. Antioksidan sekunder
Antioksidan sekunder berfungsi menangkap senyawa radikal serta
mencegah terjadinya reaksi berantai. Antioksidan sekunder seperti vitamin C,
vitamin E, β-karoten, bilirubin, albumin, asam eritrobat (D-isomer asam askorbat)
dan garam sodiumnya, dilauril tiopropionat (Gordon, 1990).
2.4.3. Uji Antioksidan Metode Thiobarbituric Acid (TBA)
Metode TBA digunakan untuk mengetahui tingkat peroksidasi lipid. Pada
pH rendah dan suhu tinggi (100°C), ikatan malondialdehid–TBA akan berubah
menjadi kompleks MDA-TBA berwarna merah muda yang dapat diukur pada
panjang gelombang 532 nm (Naphade, et al., 2009). Senyawa tiga karbon
malondialdehid (MDA) adalah produk dekomposisi utama karbonil pada proses
autooksidasi dari lipid tak jenuh.
Menurut Jiun (2007), asam linoleat adalah suatu asam lemak yang
22 sampel akan membentuk ester (minyak atau lemak) yang dilakukan secara sintetik
dan berfungsi sebagai sampel lipid (Gambar 8).
CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH + C2H5OH
Asam linoleat Etanol
CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOC2H5 + H2O
Lipid Air
Gambar 8. Reaksi antara Asam Linoleat dan Etanol untuk Pembentukan Lipid (Jiun, 2007)
Asam linoleat yang bereaksi dengan etanol akan menghasilkan lipid.
Oksidasi lipid akan membentuk radikal peroksida (Gambar 9). Pada asam linoleat,
reaksi inisiasi terjadi pada C11, membentuk radikal karbon. Atom H diambil dari
asam linoleat menghasilkan radikal bebas. Jika radikal bebas sudah terbentuk,
radikal ini akan bereaksi dengan O2 membentuk radikal peroksil dan selanjutnya
dapat mengambil H dari molekul tak jenuh yang lain untuk menghasilkan peroksil
dan dan radikal bebas baru. Reaksi terjadi secara terus–menerus atau disebut pula
sebagai reaksi berantai (Deman, 1997). Reaksi terminasi terjadi ketika radikal
peroksil bereaksi dengan senyawa antioksidan. Produk yang dihasilkan berupa
23
LOO.
Rantai panjang asam lemak tak jenuh (LH)
R
Gambar 9. Reaksi Pembentukan Peroksidasi Lipid (Singh, et al., 2001)
Deteksi spektrofotometer dari senyawa kompleks MDA-TBA telah
digunakan secara luas pada oksidasi makanan dan jaringan biologi. Prinsip dasar
dari metode ini adalah reaksi yang terjadi antara 1 molekul MDA dengan 2
molekul TBA sehingga menghasilkan senyawa kompleks MDA-TBA berwarna
merah muda, yang dapat diukur dengan spektrofotometer (Tokur, et al., 2006).
Reaksi pembentukan kompleks MDA-TBA dapat dilihat pada Gambar 10.
N
Gambar 10. Reksi Pembentukan Kompleks MDA-TBA (Sugiman, 2000)
2.5. Kromatografi Lapis Tipis (KLT)
Kromatografi lapis tipis merupakan teknik pemisahan yang banyak
digunakan dalam proses pemurnian dan identifikasi senyawa kimia pada tanaman
24 fase diam dan fase gerak. Komponen yang memiliki interaksi lebih besar terhadap
fase diam akan tertahan lebih lama. Sebaliknya, komponen yang memiliki
interaksi lebih kecil terhadap fase diam akan bergerak lebih cepat. Fase diam yang
umum digunakan pada KLT adalah silika gel, alumina, kieselguhr, dan selulosa
(Adnan, 1997).
Fase gerak yang dikenal sebagai pelarut pengembang akan bergerak
sepanjang fase diam karena pengaruh kapiler pada pengembangan secara menaik
(ascending), atau karena pengaruh gravitasi pada pengembangan secara menurun
(descending). Kromatografi lapis tipis dalam pelaksanaannya lebih mudah dan
lebih murah dibandingkan dengan kromatografi kolom. Demikian juga peralatan
yang digunakan. Dalam kromatografi lapis tipis, peralatan yang digunakan lebih
sederhana dan dapat dikatakan bahwa hampir semua laboratorium dapat
melaksanakan setiap saat secara cepat (Gholib dan Rohman, 2007).
Beberapa keuntungan kromatografi lapis tipis antara lain: kromatografi
lapis tipis banyak digunakan untuk tujuan analisis; identifikasi pemisahan
komponen dapat dilakukan dengan pereaksi warna, fluoresensi, atau dengan
radiasi menggunakan sinar ultra violet; dapat dilakukan elusi secara menaik
(ascending), menurun (descending), atau dengan cara elusi 2 dimensi; dan
ketepatan penentuan kadar akan lebih baik karena komponen yang akan
ditentukan merupakan bercak yang tidak bergerak (Gholib dan Rohman, 2007).
2.5.1. Fase diam KLT
Fase diam yang digunakan dalam KLT merupakan penyerap berukuran
25 partikel fase diam dan semakin sempit kisaran ukuran fase diam, maka semakin
baik kinerja KLT dalam hal efisiensinya dan resolusinya. Penyerap yang paling
sering digunakan adalah silika dan serbuk selulosa, sementara mekanisme sorpsi
yang utama pada KLT adalah partisi dan adsorpsi. Lapisan tipis yang digunakan
sebagai penyerap juga dapat dibuat dari silika yang telah dimodifikasi, resin
penukar ion, gel ekslusi, dan siklodekstrin yang digunakan untuk pemisahan kiral.
Beberapa penyerap KLT serupa dengan penyerap yang digunakan pada KCKT
(Kromatografi Cair Kinerja Tinggi). Kebanyakan penyerap dikontrol keteraturan
ukuran partikel dan luas permukaannya (Gholib dan Rohman, 2007).
2.5.2. Fase gerak KLT
Fase gerak pada KLT dapat dipilih dari pustaka, tetapi lebih sering dengan
mencoba-coba karena waktu yang diperlukan hanya sebentar. Sistem yang paling
sederhana adalah campuran dua pelarut organik karena daya elusi campuran
kedua pelarut ini dapat mudah diatur sedemikian rupa sehingga pemisahan dapat
terjadi secara optimal Gholib dan Rohman, 2007). Berikut adalah beberapa
petunjuk dalam memilih dan mengoptimasi fase gerak:
1. Fase gerak harus mempunyai kemurnian yang sangat tinggi karena KLT
merupakan teknik yang sensitif.
2. Daya elusi fase gerak harus diatur sedemikian rupa sehingga harga Rf terletak
antara 0,2-0,8 untuk memaksimalkan pemisahan.
3. Untuk pemisahan dengan menggunakan fase diam polar seperti silika gel,
polaritas fase gerak akan menentukan kecepatan migrasi zat terlarut yang
26 polar seperti dietil eter ke dalam pelarut nonpolar seperti toluen akan
meningkatkan harga Rf secara signifikan.
4. Zat terlarut ionik dan zat terlarut polar lebih baik digunakan campuran pelarut
sebagai fase geraknya, seperti campuran air dan metanol dengan perbandingan
tertentu. Penambahan sedikit asam asetat atau amonia masing-masing akan
meningkatkan zat terlarut yang bersifat basa dan asam.
2.6. Gas Chromatography Mass Spectrometry (GCMS)
GCMS adalah teknik analisis yang menggabungkan dua metode analisis
yaitu kromatografi gas dan spektrometrimassa. Kromatografi gas adalah metode
analisis, di mana sampel terpisahkan secara fisik menjadi bentuk molekul-molekul
yang lebih kecil (hasil pemisahan berupa kromatogram). Sedangkan spektrometri
massa adalah metode analisis di mana sampel yang akan dianalisis diubah menjadi
ion-ionnya, dan massa dari ion-ion tersebut dapat diukur berupa spektrum massa
(Hermanto, 2008).
2.6.1. Prinsip Kerja GCMS
Pada GC hanya terjadi pemisahan untuk mendapatkan komponen yang
diinginkan, sedangkan bila dilengkapi dengan MS (berfungsi sebagai detektor)
akan dapat mengidentifikasi komponen tersebut, karena bisa mendapat spektrum
bobot molekul pada suatu komponen yang dapat dibandingkan langsung dengan
library (reference) pada software (Gritter, et al., 1991).
Proses pemisahan pada GC terjadi di dalam kolom (kapiler) melibatkan
dua fase, yaitu fase diam dan fase gerak. Fase diam adalah zat yang ada di dalam
27 kemurnian tinggi. Proses pemisahan terjadi karena terdapat perbedaan kecepatan
alir tiap molekul di dalam kolom. Perbedaan tersebut disebabkan olehperbedaan
afinitas antar molekul dengan fase diam yang ada di dalam kolom. Proses
pendeteksian sampel pada MS diawali dengan diubahnya sampel yang berasal dari
GC menjadi ion-ion gasnya terlebih dahulu. Kemudian ion-ion tersebut
dilewatkan melalui suatu penganalisis massa (mass analyzer) yang berfungsi
secara selektif untuk memisahkan ion dengan satuan massa atom yang berbeda.
Terakhir ion-ion tersebut dideteksi oleh electron multiplier detector (lebih peka
dari detektor biasa) (Lingga, 2004).
2.6.2. Instrumentasi GCMS
Instrumentasi GC yang menggunakan spektrometer massa (MS) sebagai
detektor dapat digunakan untuk memisahkan campuran komponen dalam suatu
sampel, sekaligus mengidentifikasi komponen-komponen tersebut pada tingkat
molekuler. Senyawa-senyawa yang terpisah dari analisis GC akan keluar dari
kolom dan mengalir ke dalam MS, kemudian senyawa-senyawa tersebut
teridentifikasi berdasarkan bobot molekul. Molekul-molekul analat yang bersifat
netral diubah menjdi ion-ion dalam fase gas. Ion-ion yang dihasilkan kemudian
dipisahkan menurut rasio massanya (m/e). Spektrum massa dari analat yang
muncul dibandingkan dengan spektrum pada library MS sehingga akan diketahui
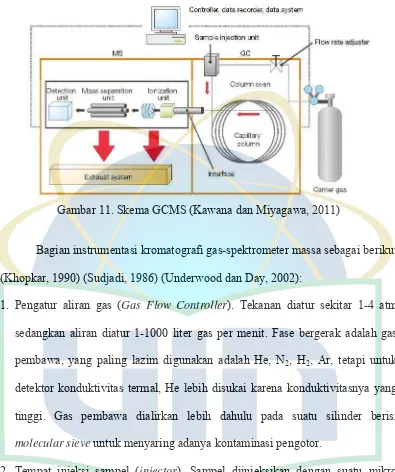
bobot molekul dari analat tersebut (Skoog et al., 2004). Skema GCMS dapat
28 Gambar 11. Skema GCMS (Kawana dan Miyagawa, 2011)
Bagian instrumentasi kromatografi gas-spektrometer massa sebagai berikut
(Khopkar, 1990) (Sudjadi, 1986) (Underwood dan Day, 2002):
1. Pengatur aliran gas (Gas Flow Controller). Tekanan diatur sekitar 1-4 atm
sedangkan aliran diatur 1-1000 liter gas per menit. Fase bergerak adalah gas
pembawa, yang paling lazim digunakan adalah He, N2, H2, Ar, tetapi untuk
detektor konduktivitas termal, He lebih disukai karena konduktivitasnya yang
tinggi. Gas pembawa dialirkan lebih dahulu pada suatu silinder berisi
molecular sieve untuk menyaring adanya kontaminasi pengotor.
2. Tempat injeksi sampel (injector). Sampel diinjeksikan dengan suatu mikro
syringe melalui suatu septum karte silikon ke dalam kotak logam yang panas.
Banyaknya sampel berkisar 0,5-10 L.
3. Kolom kromatografi. tempat berlangsungnya proses kromatografi, kolom
memiliki variasi dalam ukuran dan bahan isian. Ukuran yang umum sepanjang
6 kaki dan berdiameter dalam ¼ inci, terbuat dari tabung tembaga atau baja
29 dengan luas permukaan besar yang relatif inert. Padatan tersebut adalah sebuah
penyangga mekanik untuk cairan. Sebelum diisi padatan tersebut diimpregnasi
dengan cairan yang diinginkan yang berperan sebagai fase stasioner. Cairan ini
harus stabil dan tidak mudah menguap pada temperatur ruang dan harus sesuai
untuk pemisahan tertentu.
4. Interface, Berfungsi untuk mengirimkan sampel dari GC ke MS dengan
meminimalkan kehilangan sampel saat pengiriman.
5. Sumber ion (ion source), tempat terjadinya proses ionisasi dari molekul yang
berupa uap. Molekul tersebut akan kehilangan satu elektron dan terbentuk ion
molekul bermuatan positif. Proses lain, molekul menangkap satu elektron
bermuatan negatif.
6. Pompa vakum (vacuum pump). Pompa vakum tinggi untuk mengurangi dan
mempertahankan tekanan pada MS saat analisis dan pompa vakum rendah
untuk mengurangi tekanan udara luar MS.
7. Penganalisis massa (mass analyzer). Susunan alat untuk memisahkan ion-ion
dengan perbandingan massa terhadap muatan yang berbeda. Penganalisis
massa harus dapat membedakan selisih massa yang kecil serta dapat
menghasilkan arus ion yang tinggi.
8. Detektor. Peka terhadap komponen-komponen yang terpisahkan di dalam
kolom serta mengubah kepekaannya menjadi sinyal listrik. Kuat lemahnya
sinyal bergantung pada laju aliran massa sampel dan bukan pada konsentrasi
30
2.7. Spektrofotometri UV-Vis (Ultraviolet-Visible)
Spektrofotometer UV-Vis bermanfaat untuk penentuan konsentrasi
senyawa-senyawa yang dapat menyerap radiasi pada daerah ultraviolet (200-400
nm) atau daerah sinar tampak (400-800 nm). Biasanya cahaya terlihat merupakan
campuran dari cahaya yang mempunyai berbagai panjang gelombang ( ), dari
400-800 nm (Tahir, 2008).
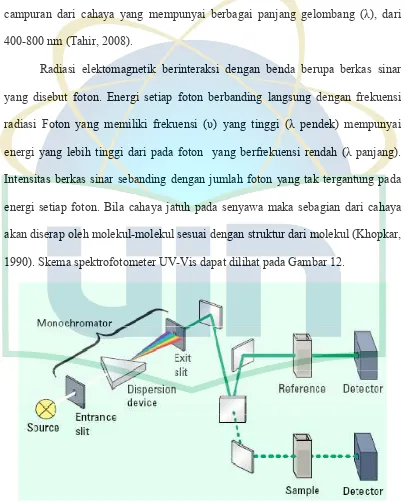
Radiasi elektomagnetik berinteraksi dengan benda berupa berkas sinar
yang disebut foton. Energi setiap foton berbanding langsung dengan frekuensi
radiasi Foton yang memiliki frekuensi (υ) yang tinggi ( pendek) mempunyai
energi yang lebih tinggi dari pada foton yang berfrekuensi rendah ( panjang).
Intensitas berkas sinar sebanding dengan jumlah foton yang tak tergantung pada
energi setiap foton. Bila cahaya jatuh pada senyawa maka sebagian dari cahaya
akan diserap oleh molekul-molekul sesuai dengan struktur dari molekul (Khopkar,
1990). Skema spektrofotometer UV-Vis dapat dilihat pada Gambar 12.
31 Setiap senyawa mempunyai tingkatan energi yang spesifik. Bila cahaya
yang mempunyai energi yang sama dengan perbedaan energi tereksitasi jatuh
pada senyawa, maka elektron-elektron pada tingkatan dasar dieksitasi ke tingkatan
tereksitasi dan sebagian energi cahaya yang sesuai dengan panjang gelombang
yang diserap. Elektron yang tereksitasikan melepaskan energi dengan proses
radiasi panas dan kembali ketingkatan dasar asal. Karena perbedaan energi antara
tingkat dasar dan tingkat tereksitasi spesifik untuk tiap-tiap bahan atau senyawa,
maka frekuensi yang diserap juga tertentu. Jika foton yang mengenai cuplikan
memiliki energi yang sama dengan yang dibutuhkan untuk menyebabkan
terjadinya perubahan energi, maka serapan dapat terjadi. Kekuatan radiasi juga
diturunkan dengan adanya penghamburan dan pemantulan, namun demikian
pengurangan-pengurangan ini sangat kecil bila dibandingkan dengan serapan
(Sastrohamidjojo, 2001).
Menurut Gholib dan Rohman (2007), penyerapan (absorpsi) sinar UV dan
sinar tampak pada umumnya dihasilkan oleh eksitasi elektron-elektron ikatan,
akibatnya panjang gelombang pita yang mengabsorpsi dapat dihubungkan dengan
ikatan yang mungkin ada dalam suatu molekul. Ada tiga macam proses
penyerapan energi ultraviolet dan sinar tampak, yaitu: (1) penyerapan oleh transisi
elektron ikatan dan elektron anti ikatan; (2) penyerapan oleh transisi elektron d
dan f dari molekul kompleks; dan (3) penyerapan oleh perpindahan muatan.
Transisi-transisi elektronik yang terjadi di antara tingkat-tingkat energi di dalam
suatu molekul ada 4, yaitu transisi sigma – sigma anti ikatan (σ→σ*); transisi n –
sigma anti ikatan (n→σ*); transisi n – phi anti ikatan (n→π*); dan transisi phi –
32 1. Transisi σ→σ*
Energi yang diperlukan untuk transisi ini besarnya sesuai dengan energi
sinar yang frekuensinya terletak di antara UV vakum (kurang dari 180 nm),
contoh: Metana, yang hanya mempunyai jenis ikatan -C-H, mempunyai pita
serapan elektron sigma pada panjang gelombang 125 nm.Jenis transisi ini (σ→σ*)
terjadi pada daerah ultraviolet vakum sehingga kurang begitu bermanfaat untuk
analisis dengan cara spektrofotometri UV-Vis.
2. Transisi n→σ*
Jenis transisi ini terjadi pada senyawa organik jenuh yang mengandung
atom-atom yang memiliki elektron bukan ikatan (elektron n). Energi yang
diperlukan untuk transisi jenis ini lebih kecil dibanding transisi σ→σ* sehingga
sinar yang diserapun mempunyai panjang gelombang lebih panjang, yakni sekitar
150-250 nm. Kebanyakan transisi ini terjadi pada panjang gelombang kurang dari
200 nm.
3. Transisi n→π* dan transisi π→π*
Untuk kemungkinan terjadinya jenis transisi ini, maka molekul organik
harus mempunyai gugus fungsional yang tidak jenuh sehingga ikatan rangkap
dalam gugus tersebut memberikan orbital phi yang diperlukan. Jenis transisi ini
merupakan transisi yang paling cocok untuk analisis sebab sesuai dengan panjang
gelombang antara 200-700 nm, dan panjang gelombang ini secara teknis dapat
diaplikasikan pada spektrofotometer.
Beberapa gugus kromofor dan panjang gelombang maksimum telah
33 Tabel 1. Ringkasan Data Transisi Elektronik (Supratman, 2010)
Contoh Transisi Elektronik λmax (nm) ɛmax
Asetofenon Aromatik π→π* 240 13000
Aromatik π→π* 278 1110
n→π* 319 50
Fenol Aromatik π→π* 210 6200
Aromatik π→π* 270 1450
2.8. Spektrofotometri Infrared (IR)
Spektrofotometer infrared atau inframerah merupakan suatu metode yang
mengamati interaksi molekul dengan radiasi elektromagnetik yang berada pada
daerah panjang gelombang 0,75-1,000 m atau pada bilangan gelombang
13.000-10 cm-1. Berdasarkan pembagian daerah panjang gelombang, maka daerah
34 pertengahan, dan daerah inframerah jauh. Berdasarkan pembagian daerah
spektrum elektromagnetik tersebut di atas, daerah panjang gelombang yang
digunakan pada alat spektrofotometer inframerah adalah pada daerah inframerah
pertengahan, yaitu pada panjang gelombang 2,5-50 m atau pada bilangan
gelombang 4.000-200 cm-1 (Khopkar, 1990).
2.8.1. Gerak Molekul pada Infrared (IR)
Menurut Taufiq (2007), setiap senyawa pada keadaan tertentu mempunyai
tiga macam gerak, yaitu gerak translasi (perpindahan dari satu titik ke titik lain),
gerak rotasi (berputar pada porosnya) dan gerak vibrasi (bergetar pada
tempatnya). Selain gerak, setiap molekul juga memiliki harga energi tertentu. Bila
suatu senyawa menyerap energi dari sinar inframerah, maka tingkatan energi di
dalam molekul itu akan tereksitasi ke tingkatan energi yang lebih tinggi. Sesuai
dengan tingkatan energi yang diserap, maka yang akan terjadi pada molekul itu
adalah perubahan energi vibrasi yang diikuti dengan perubahan energi rotasi.
Suatu ikatan dalam sebuah molekul dapat mengalami berbagai vibrasi
molekul. Secara umum terdapat dua tipe vibrasi molekul:
1. Streching (vibrasi regang/ulur): vibrasi sepanjang ikatan sehingga terjadi
perpanjangan atau pemendekan ikatan.
2. Bending (vibrasi lentur/tekuk): vibrasi yang disebabkan oleh sudut ikatan
sehingga terjadi pembesaran atau pengecilan sudut ikatan.
Bending juga ada dua macam yaitu in plane bending (tekuk pada bidang)
dan out of plane bending (tekuk tidak pada bidang). In plane bending dibagi
35 goyang). Out of plane bending juga dibagi menjadi dua yaitu wagging (bergoyang
ke depan dan ke belakang) dan twisting (memutar) (Panji, 2011).
2.8.2. Daerah Identifikasi pada Infrared (IR)
Harborne (1987), menyebutkan bahwa daerah pada spektrum inframerah
di atas 1200 cm-1 menunjukkan pita spektrum atau puncak yang disebabkan oleh
getaran (vibrasi) ikatan kimia atau gugus fungsi dalam molekul yang dianalisis,
sedangkan daerah di bawah 1200 cm-1 menunjukkan pita yang disebabkan oleh
getaran seluruh molekul, dan karena kerumitannya dikenal sebagai daerah sidik
jari.
Vibrasi yang digunakan untuk identifikasi adalah vibrasi bengkokan,
khususnya goyangan (rocking), yaitu yang berada di daerah bilangan gelombang
2000-400 cm-1, karena di daerah antara 4000-2000 cm-1 merupakan daerah khusus
berguna untuk identifikasi gugus fungsional. Daerah ini menunjukkan absorbsi
yang disebabkan oleh vibrasi regangan, sedangkan daerah antara 2000-400 cm-1
seringkali sangat rumit, karena vibrasi regangan maupun bengkokan
mengakibatkan absobrsi pada daerah tersebut. Pada daerah 2000-400 cm-1 tiap
senyawa organik mempunyai absorbsi yang unik, sehingga daerah tersebut sering
juga sebut sebagai daerah sidik jari (fingerprint region). Meskipun pada daerah
2000-400 cm-1 menunjukkan absorbsi yang sama, pada daerah 2000-400 cm-1 juga
harus menunjukkan pola yang sama sehingga dapat disimpulkan bahwa dua
senyawa adalah sama (Underwood dan Day, 2002).
Beberapa gugus fungsi dan bilangan gelombang (cm-1) telah diungkapkan
36 Tabel 2. Beberapa Frekuensi Gugus Fungsi pada Inframerah (Underwood dan Day,
2002)
Gugus Fungsi Nama Gugus Fungsi Daerah Serapan (cm-1)
OH Alkohol 3580-3650
Ikatan-H 3210-3550
Asam 2500-2700
NH Amina 3300-3700
CH Alkana 2850-2960
Alkena 3010-3095
Alkuna 3300
Aromatik ~3030
C≡C Alkuna 2140-2260
C=C Alkena 1620-1680
Aromatik ~1600
C=O Aldehida 1720-1740
Keton 1675-1725
Asam 1700-1725
Ester 1720-1750
C≡N Nitril 2000-2300
NO2 Nitro 1500-1650
2.8.3. Instrumentasi FTIR
Menurut Supratman (2010), spektrometer inframerah umumnya
merupakan spektrometer double-beam (berkas ganda) dan terdiri dari lima bagian
utama: sumber radiasi, daerah cuplikan, fotometer, kisi difraksi (monokromator),
dan detektor.
1. Sumber radiasi
Biasanya dihasilkan oleh pemijar Nerst dan Globar. Pemijar Nerst
merupakan batang cekungan dari Zirkonium dan Ytrium oksida yang dipanasi
hingga 1500oC dengan arus listrik. Pemijar Globar merupakan batang silikon
karbida yang dipanasi hingga 1200oC, sehingga memancarkan radiasi kontinu
37 2. Monokromator
Terdiri dari celah masuk dan celah keluar, alat pendespresi yang berupa
kisi difraksi atau prisma, dan cermin untuk memantulkan dan memfokuskan sinar.
Bahan prisma adalah natrium klorida, kalium bromida, sesium bromida dan litium
fluorida. Prisma natrium klorida paling banyak digunakan, karena dispersinya
tinggi untuk daerah 5,0-16 µm, tetapi kurang baik untuk daerah antara 1,0-5,0 µm.
3. Detektor
Sebagian besar alat modern menggunakan detektor panas. Detektor
fotolistrik tidak dapat digunakan untuk mendeteksi sinar inframerah, karena
energi foton inframerah tidak cukup besar untuk membebaskan elektron dari
38
BAB III
METODE PENELITIAN
3.1. Tempat dan Waktu Pelaksanaan
Penelitian ini dilaksanakan di Pusat Laboratorium Terpadu Universitas
Islam Negeri (UIN) Syarif Hidayatullah Jakarta, dimulai pada bulan Maret 2013
sampai bulan Februari 2014.
3.2. Bahan dan Alat 3.2.1. Bahan
Bahan-bahan yang digunakan dalam penelitian ini terdiri dari bahan
tumbuhan dan bahan kimia.
a. Bahan tumbuhan
Bahan tumbuhan yang digunakan sebagai sampel dalam penelitian ini
adalah biji honje (E. elatior) yang diperoleh dari Desa Cintaratu, Kecamatan
Parigi, Kabupaten Pangandaran, Jawa Barat. Biji honje diambil pada musim hujan
bulan Oktober 2012. Sampel telah dilakukan determinasi tumbuhan di Herbarium
Bogoriense, Bidang Botani Pusat Penelitian Biologi LIPI Cibinong, Bogor.
b. Bahan kimia
Bahan kimia yang digunakan adalah n-heksan, dietil eter, etanol (teknis
dan p.a), kloroform, Vitamin E (Alpha-Tocopherol) (CLR Fostpach), Vitamin C
(Ascorbic Acid) (Merck), DMSO, Asam Linoleat 75% (CLR Fostpach), TBA
39
3.2.2. Alat
Alat yang digunakan dalam penelitian ini terdiri dari alat-alat gelas,
timbangan analitik, ekstraktor soklet, rotary evaporator Heidolph Laborota
4000-Efficient, inkubator Memmert, Centrifuge Hettich EBA 20, plat aluminium TLC
(Thin Layer Chromatography), GC-MS Shimadzu QP-2010, Spektrofotometer
UV Perkin Elmer Lambda 25, Spektrofotometer FTIR (Fourier Transform Infra
Red) Spectrum One Perkin Elmer.
3.3. Prosedur Kerja
3.3.1. Ekstraksi Sokletasi
Biji honje yang telah dikeringkan dan dihaluskan ditimbang, lalu dibungkus
dengan kertas saring dan diikat dengan tali dan dimasukkan dalam tabung
(ekstraktor) soklet. Kemudian dituangkan pelarut ke dalam labu soklet dan
dilakukan ekstraksi sampai warna pelarut di dalam tabung ekstraktor kembali
menjadi jernih. Pelarut yang digunakan adalah n-heksan dan dietil eter.
Temperatur disesuaikan dengan titik didih pelarut. Setelah selesai, sampel diambil
dari tabung soklet dengan pinset. Hasil sokletasi dipisahkan dari pelarut dengan
cara diuapkan dengan menggunakan rotary evaporator. Setelah diperoleh minyak,
kemudian dicari massa jenis dan dihitung rendemennya.
% Rendemen = x 100%
3.3.2. Penentuan Massa Jenis (Densitas)
Penentuanmassa jenis dilakukan menggunakan alat piknometer.
Piknometer yang akan digunakan dicuci dengan akuades, dibilas dengan etanol Massa minyak
40 dan dietil eter serta dikeringkan bagian dalam piknometer. Setelah kering,
piknometer ditimbang dan dicatat nilainya. Selanjutnya piknometer diisi dengan
akuades hingga penuh kemudian piknometer berisi akuades tersebut dicelupkan
dalam penangas air pada suhu 25oC ± 0,2oC dan ditimbang. Piknometer yang
sudah berisi akuades dibilas kembali dengan etanol dan dietil eter, dan
dikeringkan. Piknometer yang sudah kering diisi dengan minyak biji honje hingga
penuh kemudian piknometer berisi minyak tersebut dicelupkan dalam penangas
air pada suhu 25oC ± 0,2oC dan ditimbang.Dihitung nilai massa jenisnya.
3.3.3. Uji Fitokimia
a. Identifikasi Alkaloid dengan metode Culvenor-Fitzgerald (Harborne, 1987)
Sampel dicampur dengan 5 mL kloroform dan 5 mL amoniak kemudian
dipanaskan, dikocok dan disaring. Ditambahkan 5 tetes asam sulfat 2 N pada
masing filtrat, kemudian kocok dan didiamkan. Bagian atas dari
masing-masing filtrat diambil dan diuji dengan pereaksi Mayer, bourchardat, dan
Dragendorf. Terbentuknya endapan jingga, cokelat, dan putih menunjukkan
adanya alkaloid.
b. Identifikasi Flavonoid (Harborne, 1987)
Sampel dicampur dengan 5 mL etanol, dikocok, dipanaskan, dan dikocok
lagi kemudian disaring. Kemudian ditambahkan Mg 0,2 g dan 3 tetes HCl pekat
pada masing-masing filtrat. Terbentuknya warna merah pada lapisan etanol
41 c. Identifikasi Saponin (Harborne, 1987)
Sampel dididihkan dengan 20 mL air dalam penangas air. Filtrat dikocokdan
didiamkan selama 15 menit. Terbentuknya busa yang stabil berarti positif terdapat
saponin.
d. Identifikasi Steroid (Harborne, 1987)
Sampel diekstrak dengan etanol dan ditambah 2 mL asam sulfat pekat dan 2
mL asam asetat anhidrat. Perubahan warna dari ungu ke biru atau hijau
menunjukkan adanya steroid.
e. Identifikasi Terpenoid (Harborne, 1987)
Sampel dicampur dengan 2 mL kloroform dan 3 mL asam sulfat pekat.
Terbentuknya warna merah kecoklatan pada antar permukaan menunjukkan
adanya terpenoid.
f. Identifikasi Tanin (Edeoga, et al., 2005)
Sampel didihkan dengan 20 mL air lalu disaring. Ditambahkan beberapa
tetes feriklorida 1% dan terbentuknya warna coklat kehijauan atau biru kehitaman
menunjukkan adanya tanin.
3.3.4. Uji Aktivitas Antioksidan (Bakr, et al., 2013)
Sebanyak 10 mg sampel ditimbang kemudian dilarutkan dalam 10 mL
etanol p.a. dan beberapa tetes DMSO. Dari larutan ini kemudian dibuat larutan
dengan konsentrasi 10, 25, 50, 75, dan 100 ppm. Larutan sampel diambil
sebanyak 4 mL dan dimasukkan dalam tabung tertutup. Kemudian ditambahkan
asam linoleat 2,31% (dalam etanol) sebanyak 4,1 mL, larutan buffer fosfat pH 7
42 tersebut diinkubasi pada suhu 40oC selama 8 hari. Pada hari ke-4 sampai hari ke-8
dilakukan pengukuran absorbansi terhadap kontrol negatif untuk menentukan
waktu setimbang.
Pengujian aktivitas antioksidan metode Thiobarbituric Acid (TBA)
dilakukan pada saat waktu setimbang, yaitu ketika absorbansi kontrol negatif
mencapai titik optimum. Pengukuran dilakukan dengan cara diambil 1 mL larutan
sampel yang telah diinkubasi, ditambahkan 2 mL asam trikloroasetat 20% dan 2
mL larutan TBA 0.67%. Campuran dididihkan dalam penangas air selama 10
menit, kemudian didinginkan dan disentrifugasi pada 3000 rpm selama 20 menit.
Supernatan diukur pada panjang gelombang 532 nm. Sebagai kontrol adalah
perlakuan tanpa penambahan sampel dan sebagai pambanding terhadap sampel
digunakan Vitamin E dan Vitamin C.
Nilai serapan yang diperoleh dihitung sebagai % inhibisi dengan rumus
sebagai berikut:
% inhibisi =
3.3.5. Analisis GC-MS
Analisis GC-MS dilakukan untuk mengetahui komponen minyak biji honje
hasil sokletasimenggunakan pelarut n-heksan.Minyak biji honje dilarutkan dengan
n-heksan kemudian dimasukkan ke dalam vial, lalu sebanyak 1µL sampel
diinjeksikan ke dalam kolom RTx-MS Restech Polymethyl xyloxan, menggunakan
helium sebagai gas pembawa dan split rasio 1 : 200. Temperatur oven diatur pada
suhu 70°C selama 3 menit, perlahan-lahan temperatur ditingkatkan rata-rata 5°C Akontrol – Asampel
43 permenit sampai 280°C dan suhu 280°C dipertahankan selama 5 menit.
Temperatur saat sampel diinjeksi pada suhu 230°C. Senyawa yang terdapat dalam
sampel diidentifikasi dengan membandingkan spektrum tersebut dengan senyawa
yang terdapat di dalam library. Cairan sampel yang dibawa dari GC diteruskan
sebagai sampel inlet MS, sumber ion pada suhu 250°C, fragmentasi ion yang
terbentuk dideteksi oleh analyzer berdasarkan rasio massa.
3.3.6. Uji Kromatografi Lapis Tipis (KLT)
Plat KLT yang akan digunakan terlebih dulu diberi tanda batas atas dan
bawah, kemudian dimasukkan ke dalam oven selama 30 menit untuk mengurangi
kadar air pada plat KLT. Setelah selesai minyak ditotolkan pada garis dasar plat
KLT, lalu ditempatkan dalam chamber yang berisi eluen berupa campuran
n-heksan dan kloroform dengan perbandingan 5 : 2. Ketika pelarut mulai
membasahi plat KLT, pelarut akan melarutkan senyawa dalam bercak yang telah
ditempatkan pada dasar. Bila bercak-bercak pada plat KLT tidak tampak, dapat
digunakan penyinaran di bawah sinar UV. Selanjutnya dimasukkan lagi ke dalam
oven selama 30 menit. Bercak-bercak senyawa pada plat KLT yang telah terpisah
namun tidak terlihat jelas dapat dibantu dengan menyemprotkan pelarut H2SO4
1M. Selanjutnya dimasukkan ke dalam oven selama 30 menit dan hasilnya