Lampiran 5. Contoh perhitungan dosis
Berat badan mencit 25 g dengan dosis EESA 200 mg/kg bb Dosis = 200 mg/kg bb
= 200 mg/1000 g x 25 g = 5 mg
Konsentrasi ekstrak yang dibuat = 200 mg/10 ml = 20 mg/ml Jumlah obat yang dioral = 1% x BB
= 1% x 25 g = 0.25ml atau
Lampiran 8. Skema proedur pembuatan preparat histopatologi
Skema langkah-langkah pengujian histologi secara garis besar adalah sebagai berikut:
Pengambilan organ
Fiksasi
Pemotongan organ
Washing
Dehidrasi
Clearing
Infiltrasi parrafin
Embedding parrafin
Pembuatan sayatan
Pewarnaan
Lampiran 9. Gambar alat dan objek yang digunakan
Oral sonde
Lampiran 10. Hasil analisis spss ALT
Descriptive Statistics Dependent Variable:kadar ALT
jenis
kelamin dosis ekstrak Mean
Std.
Intercept 136305.625 1 136305.625 4469.037 .000
gender 342.225 1 342.225 11.220 .002
dosis 7882.475 3 2627.492 86.147 .000
gender * dosis 152.675 3 50.892 1.669 .193
Error 976.000 32 30.500
Total 145659.000 40 Corrected Total 9353.375 39
Multiple Comparisons
Lampiran 11. Hasil analisissSpss AST
Descriptive Statistics Dependent Variable:kadar AST jenis kelamin dosis ekstrak Mean Std.
Deviation N
Intercept 106812.225 1 106812.225 996.034 .000
gender 207.025 1 207.025 1.931 .174
dosis 7164.475 3 2388.158 22.270 .000
gender * dosis 233.675 3 77.892 .726 .544
Error 3431.600 32 107.237
Total 117849.000 40
Multiple Comparisons
Lampiran 12. Signifikansi rata-rata berat badan mencit selama 90 hari
Hari
Rata-rata berat badan (g) ± SD K1
p K2 p K3 p K4 p
Jantan Betina Jantan Betina Jantan Betina Jantan Betina
Lampiran 13. Signifikansi rata-rata berat makanan yang dikonsumsi mencit selama 90 hari
Hari
DAFTAR PUSTAKA
Amalina, N. (2009). Uji Toksisitas Akut Ekstrak Valerian (Valeriana officinalis) Terhadap Hepar Mencit Balb/C.Skripsi. Semarang: Fakultas Kedokteran
Universitas Diponegoro. Halaman 28.
Anggraini, D.R. (2008). Gambaran Makroskopik dan Mikroskopik Hati dan Ginjal Mencit Akibat Pemberian Plumbum Asetat. Tesis. Medan: Sekolah
Pascasarjana Universitas Sumatera Utara. Halaman 52.
BPOM RI. (2004). Keputusan Kepala Badan Pengawas Obat Dan Makanan Tentang Ketentuan Pokok Pengelompokan Dan Penandaan Obat Bahan Alam Indonesia. Jakarta: BPOM RI. Halaman 2-3.
BPOM RI. (2014). Pedoman Uji Toksisitas Nonklinik Secara In Vivo. Jakarta:
BPOM RI. Halaman 3-5, 9-12, 28-38.
Bauer, J.D. (1982). Clinical Laboratory Methods. 9th edition. The C.V. Mosby
Company, London. halaman 578.
Boyd, L.A., Mark, J.M., Yumi, H., Richard, N.B., Chris, I.G., and Ian, R.R. (2006). Assessment of the Genotoxic, Proliferative, and Anti-Metastatic Potential of Crude Watercress Extract in Human Colon Cancer Cells. Nutrition and Cancer. 55(2): 232-241.
Brookes, M. (2005). Bengkel Ilmu Genetika. Jakarta: Erlangga. Halaman 134. Brzoska, M. M., Jakoniuk, J. M., Marcinkiewicz, B. P. and Sawicki, B. (2003).
Liver and Kidney Function and Histology in Rats Exposed to Cadmium and Ethanol. Alcohol Alcohol. 38 (1): 2-10.
Cahyono JBSB. 2009. Hepatitis A. Yogyakarta : Kanisius yogyakarta
Casaarett dan Doull. (2008). Toxicology the basic science of poisons seventh edition. Kansas: McCraw-Hill Medical Publishing Devision. Halaman
28,31, 32.
Cheville, N.F. (1999). Introduction to Veterinary Pathology. Edisi kedua. Iowa:
Iowa State University Press. Halaman 214.
Corona, M.R.C., Monica, A., Ramirez, C., Omar, G.S., Elvira, G.G., Isidoro, P.P., and Julieta, L.H. (2008). Activity Against Drug Resistant-Tuberculosis Strains of Plants Used in Mexican Traditional Medicine to Treat Tuberculosis and Other Respiratory Diseases. Phytotherapy Research. 22:
82-85.
Dalimartha, S. (2000). Atlas Tumbuhan Obat Indonesia. Jilid 2 Jakarta: Pustaka
Bunda. Halaman 146-148.
Plumbum. Tesis. Medan: Sekolah Pascasarjana Universitas Sumatera
Utara. Halamanaman 42-43.
Donatus, A.I. (2001). Toksikologi Dasar. Yogyakarta: Fakultas Biofarmasi Universitas Gajahmada. Halamanaman 67-79.
Elisma, Arifin, H., dan Handayani, D. (2009). Pengaruh Fraksi Daun Sidaguri (Sida Rhombifolia L.) Terhadap Kadar Asam Urat Dan Uji Toksisitas Sub Akutnya pada Mencit Putih Jantan. Jurnal Cermin Dunia Kedokteran.
32(1): 15-19.
Ginting, H., Aminah, F., Dalimunthe, A. (2014). Ekstrak Etanol Selada Air (Nasturtium officinale R.Br.) Sebagai Bahan Baku Pembuatan Tablet Diuretika. Penelitian Hibah Bersaing. Universitas Sumatera Utara.
Gruenwald, J., Thomas, B., and Christof, J. (2000). PDR for Herbal Medicine.
Montvale: Medical Economics Company, Inc. Halaman 798.
Hadi, S. (1995). Gastroenterologi. Edisi keenam. Bandung: Alumni. Halaman
400-12 ; 644-50.
Handoko, I.S. (2003). Tes Fungsi Hati. http:/ www. klinikku.com/ pustaka/ labhati /tes_f_hati. html.(diakses: 29 februari 2015)
Harmita, Radji. M. (2006). Buku Ajar Analisis Hayati edisi ketiga. Jakarta: Buku
Kedokteran EGC. Halaman 58-59, 63.
Hendriani, R. (2007). Uji Toksisitas Subkronis Kombinasi Ekstrak Etanol Buah Mengkudu (Morinda citrifolia Linn.) dan Rimpang Jahe Gajah (Zingiber officinale rosc.) pada Tikus Wistar. Jurnal Farmasi Indonesia. 11(4):
312-316. Rats. Pharmacologyonline. 3: 866-871.
Irianto, K. (2004). Struktur dan Fungsi Tubuh Manusia untuk Paramedis.
Bandung: Yrama Widya. Halaman 225.
Jones, T.C., Ronald, D.H., and Norval, W.K. (1997). Veterinary Pathology. Sixth
Edition. USA: Wiliam and Wilkins. Baltimore. Halaman 543.
Joseph, A.J, Nadeau, A.D, Underwood, A. (2002). Diet Sehat Dengan Kode Warna Makanan Diterjemahkan Dari Color Code : A Revolusionary Eating Plan For Optimum Health. New York: Hyperion. Halaman 170-171.
Junqueira, L.C., dan Corneiro, J. (2007). Histologi Dasar. Editor Dany, F. Edisi
Katzung BG. (2007). Farmakologi Dasar dan Klinik. Sjabana D, Isbadianti SE,
Basori A, Soedjak NM, uno I, Rhamadani, Zakaria PS, penerjemah dan penyunting. Jakarta Salemba Medika. Terjemahan dari: Basic dan Clinical Pharmacology Edisi kelima. Jakarta: Balai penerbit FKUI. Halaman 820-842
Klasseen, H. (2001). Casarett and Doull’s Toxicology. The Basic Science of Poison. Edisi keennam. New York: McGraw-Hill. United States of
America. Halaman 87.
Lee, S.S.T., Butter, J.T.M., Pinaeu, T., Fernandez, S.P., and Gonzalez, F.J. (1997). Role of CYP2E1 in the hepatotoxicity of acetaminophen. Journal Biology Chemical. 27(1): 12063–12067.
Lingga, L. (2012). The Healing Power of Anti-oxidant. Jakarta: PT Elex Media Komputindo. Halaman 3, 160.
Lu FC. (1995). Toksikologi Dasar. Edisi kedua. Jakarta: Universitas Indonesia
Press. Halaman 206-223.
Lubis, Z., Ginting, H., Nasution, M.P. (2013). Uji aktivitas Antioksidan Fraksi Etilsetat dan Kloroform Selada Air. Seminar Nasional Herbal Fakultas Farmasi dan IAI Sumut. Halaman 7.
Maya, V. H.( 2012). Selada Air Sayuran Super Pembasmi Kanker Dan Berbagai Macam Penyakit. Diakses pada hari kamis tanggal 26 Februari 2015.pukul
08.45 WIB.
Macfarlane, P.S., Reid, R., and Callander. (2000). Pathology Illustrated. Toronto:
Huerchill Livingstone. Halaman 342.
Muhlisah, F. Hening, S. (2009). Sayuran dan Bumbu Dapur Berkhasiat Obat.
Jakarta: Elex media Komputindo. Halaman 67-68.
Murray, R.K., Granner, D.K., Mayes, P.A., and Rodwell, V.W. (1995). Biokimia Harper. Edisi 22. Diterjemahkan oleh Andry, H. Penerbit buku kedokteran
EGC, Jakarta. Halaman 706–707.
Murtini, J. T., Triwibowo, R., Indriatri, N., dan Ariyani, F. (2010). Uji Toksisitas Sub Kronik Spirulina Platensis Secara In-Vivo. Jurnal Pascapanen dan Bioteknologi Kelautan dan Perikanan. 5(2):125.
Nisa, L.C., Wahyuningsih, S.P.A., dan Husen, S.A. (2012). Uji Toksisitas Subkronik Polisakarida Krestin Dari Ekstrak Coriolus versicolor Terhadap Kadar Kreatinin Mus musculus. Jurnal Bioscientiae. 31(2): 2-9.
Novia, J. (2014). Karakterisasi Simplisia dan Skrining Fitokimia Serta Uji Aktivitas Antioksidan Ekstrak N-Heksan Etil Asetat dan Metanol Selada Air (Nasturtium Offinale, W. T. Aiton). Skripsi, Fakultas Farmasi
OECD. (2001). Acute Oral Toxicity. OECD Guidelines for the Testing of Chemicals. TG 401. 432(1): 1-6.
OECD. (1998). Organization for Economic Cooperation and Development Guidelines for The Testing of Chemicals TG 408. 132(1): 4-13.
Özen, T. (2009). Investigation of Antioxidant Properties of Nasturtium officinale (watercress) Leaf Extracts. Acta Poloniae Pharmaceutica Drug Research.
66(2): 187-193.
Price, A.S. dan Wilson, M.L., (1995), Patofisiologi Konsep Klinik Proses-Proses Penyakit, Jakarta: EGC. Halaman 251.
Priyanto. (2009). Toksikologi Mekanisme, Terapi Antidotum, dan Penilaian Resiko. Jakarta: Lembaga Studi dan Konsultasi Farmakologi Indonesia
(LESKONFI). Halaman 1-7.
Robbins, S. L., Cotran, R. S., & Kumar, V. (2007). Jejas, Adaptasi, dan Kematian Sel. Dalam: Buku Ajar Patologi I, vol 1. EGC, Jakarta. Halaman 9, 26-27.
Sacher, R.A., dan Richard, A.M. (2004). Tinjauan Klinis Hasil Pemeriksaan Laboratorium. Edisi 11. Jakarta: Kedokteran EGC. Halaman 369.
Sagita, A. A., Wahyuningsih, S. P. A. dan Husen, S. A. (2012). Uji Toksisitas Subkronik Polisakarida Krestin dari Ekstrak Coriolus versicolor Terhadap Kadar ALT Mus musculus L. Jurnal Farmasi Indonesia. 87(3): 412-419. Schumann, Bonora, Ceriotti, Ferard. (2002). IFCC primary reference procedure
for themeasurement of catalytic activity concentration of aspartate aminotransferase. Clin Chem Lab Med. 40: 725 – 733.
Sherlock, S. (1981). Diseases of Liver and Billiary System. 7th edition. Blackwell
Scientific Publication, London. Halaman 125–126.
Supriningrum, R., Jubaidah, S., Sapri. (2014). Uji Toksisitas Akut Ekstrak Akar Tabar Kedayan (Aristolochia foveolata Merr). Media Sains. 7 (2): 247-251.
Tenggara, J.B. (2012). Liver: Struktur, Anatomi dan Fungsi. Diakses tanggal 18 November 2015. Http://ruh4dian.blogspot.com/2015/18/gangguan-pada-hati manusia_1.html
Underwood, J.C.E. (1994). Cedera Hepar Akibat Obat. Editor: Sarjadi. Edisi Patologi
Umum dan Sistemik Volume 2. Edisi II. Jakarta: EGC. Halaman 483.
Wicaksono, S. (2002). Efek Toksik dan Cara Menentukan Toksisitas Bahan Kimia. Jakarta: Departemen Kesehatan RI. Jurnal Cermin Dunia Kesehatan. 135(3): 32-36.
Widyastuti, S. (2008). Uji Toksikologi Daun Iprih (Ficus glabella Blume) terhadap Artemia salina Leach dan Profil Kromatografi Lapis Tipis. Skripsi. Surakarta: Fakultas Farmasi Universitas Muhammadiyah Surakarta. Halaman 6.
Wilson Nelson, Hardisty Jerry F, Hayes Johnnie R. (2001). Short-term, Subchronic and Chronic Toxicology Studies. Dalam:Taylor & Francis, penyunting. Principles and Methods of Toxicology. Edisi ke-4.
BAB III
METODE PENELITIAN
3.1 Jenis Penelitian
Penelitian ini menggunakan metode eksperimental dengan tahapan penelitian meliputi penyiapan bahan, penyiapan hewan percobaan, pengamatan gejala klinis, berat badan, jumlah makanan, kematian, pengukuran kadar ALT dan AST, serta histopatologi organ hati dan analisis data menggunakan statistik metode two-way analysis of variance (ANOVA). Penelitian ini dilakukan di laboratorium Farmakologi Fakultas Farmasi USU, laboratorium Kesehatan Daerah Dinas Kesehatan Provinsi Sumatera Utara dan laboratorium Rumah Sakit Murni Teguh Medan.
3.2 Alat
Alat-alat yang digunakan terdiri dari neraca hewan (GW-1500), neraca listrik (Mettler Toledo), alat-alat gelas laboratorium, mortir dan stamfer, alat
bedah (Wells spencer), kaca objek, kaca penutup, kertas perkamen, kaca arloji,
oral sonde, pipet tetes dan spuit 1 ml (Terumo), mikrotube, sentrifuse (Velocity 18-R) dan mikroskop (Olympus).
3.3 Bahan
Bahan-bahan yang digunakan dalam penelitian ini meliputi bahan tumbuhan, hewan dan bahan kimia. Bahan tumbuhan yang digunakan yaitu selada air (Nasturtium officinale, R.Br.). Bahan kimia yang digunakan yaitu
Na-CMC (natrium carboxy methyl cellulose), akuades, formalin 10%, natrium
3.4 Tahap Penelitian
3.4.1 Penyiapan ekstrak etanol herba selada air (EEHSA)
Ekstrak etanol herba selada air (EEHSA) diperoleh dari penelitian sebelumnya yang berjudul Ekstrak Etanol Selada Air (Nasturtium officinale R.Br)
Sebagai Bahan Baku Pembuatan Tablet Diuretika (Ginting, dkk., 2014)
3.5 Penyiapan Hewan Percobaan
Hewan percobaan yang digunakan dalam penelitian adalah mencit putih jantan dan betina dengan berat badan 15–25 g berumur sekitar 4 minggu, sebanyak 40 ekor mencit dibagi dalam 4 kelompok. Mencit diaklimatisasi terlebih dahulu dalam sebuah kandang untuk tiap kelompok dan dipisahkan berdasarkan jenis kelaminnya, diberi makan pelet dan minum air suling selama 7-14 hari.
3.6 Pembuatan Pereaksi
Pembuatan pereaksi mencakup pembuatan suspensi Na-CMC 0,5% b/v, pembuatan suspensi EEHSA dengan dosis 25 mg/kgbb, 50 mg/kgbb dan 200 mg/kgbb.
3.6.1 Pembuatan suspensi Na-CMC 0,5% b/v
Sebanyak 0,5 g Na-CMC ditaburkan dalam lumpang yang berisi 10 ml air suling panas. Didiamkan selama 15 menit lalu digerus hingga diperoleh massa yang transparan, kemudian digerus sampai homogen, diencerkan dengan air suling dan dimasukkan ke labu tentukur 100 ml, dicukupkan volumenya dengan air suling hingga 100 ml.
3.6.2 Pembuatan suspensi ekstrak etanol herba selada air (EEHSA)
Na-CMC 0,5% b/v sedikit demi sedikit sambil digerus sampai homogen kemudian dicukupkan hingga 10 ml.
3.7 Pengujian Efek Toksisitas
Pengujian efek toksisitas meliputi pembuatan suspensi ekstrak etanol herba selada air, pengujian toksisitas subkronik meliputi gejala-gejala klinis, perubahan berat badan, kematian hewan, pengukuran kadar ALT dan AST serta histopatologi organ hati.
3.7.1 Pengujian toksisitas subkronik
Hewan percobaan dikelompokkan menjadi 4 kelompok, masing-masing kelompok terdiri dari 10 ekor yaitu 5 jantan dan 5 betina. Dosis dalam penelitian ini berdasarkan dosis efektif untuk indikasi diuresis yaitu 50 mg/kgbb (Ginting, 2014). Kelompok tersebut adalah:
Kelompok 1 (K1) : Kelompok kontrol, diberi CMC Na 0,5% b/v
Kelompok 2 (K2) : Kelompok perlakuan, diberi EEHSA dosis 25 mg/kgbb Kelompok 3 (K3) : Kelompok perlakuan, diberi EEHSA dosis 50 mg/kgbb Kelompok 4 (K4) : Kelompok perlakuan, diberi EEHSA dosis 200 mg/kgbb
Hari ke-1 mulai dilakukan penimbangan pada mencit, kemudian diberikan sediaan uji dan diamati aktivitasnya. Sediaan uji tersebut diberikan secara oral setiap hari selama 90 hari dan dilakukan pengamatan.
3.8 Pengamatan 3.8.1 Gejala toksik
90 hari, meliputi adanya tremor, salivasi, diare, lemas, perubahan bulu, gerak-gerik hewan seperti berjalan mundur dan berjalan dengan perut (OECD, 1998). Adapun cara pengamatannya, yaitu:
a. Salivasi
Pengeluaran salivasi mencit yang telah diberi ekstrak etanol herba selada air dibandingkan dengan kontrol, menggunakan kertas saring.
b. Diare
Pengeluaran tinja mencit yang telah diberi ekstrak etanol herba selada air dibandingkan dengan kontrol, menggunakan kertas saring.
c. Tremor
Hewan yang telah diberi ekstrak etanol herba selada air, diamati tremor atau tubuh hewan bergetar.
d. Lemas
Hewan yang telah diberi ekstrak etanol herba selada air diamati aktivitasnya secara umum.
e. Gerak-gerik hewan
Hewan yang telah diberi ekstrak etanol herba selada air diamati gerak-geriknya seperti berjalan mundur dan berjalan menggunakan perut (Supriningrum, dkk., 2014).
3.8.2 Berat badan
2.8.3 Jumlah makanan
Makanan diberikan setiap hari sebanyak 25-30 g untuk tiap kelompoknya. Makanan yang tersisa pada hari berikutnya ditimbang sehingga diperoleh jumlah makanan yang dikonsumsi mencit. Data jumlah makanan dianalisis setiap dua minggu sekali (BPOM RI, 2014).
3.8.4 Kematian hewan
Mencit diamati kematiannya dari hari pertama sampai hari terakhir. Mencit yang mati selama waktu pemberian sediaan uji segera diotopsi dan organ diamati secara histopatologi (BPOM RI, 2014).
3.8.5 Penimbangan organ
Organ yang akan ditimbang (bobot absolut) harus dikeringkan terlebih dahulu dengan kertas penyerap, kemudian segera ditimbang, sedangkan yang dianalisis adalah bobot relatif, yaitu bobot organ absolut dibagi bobot badan dikali 100% (BPOM RI, 2014).
3.8.6 Pengukuran kadar ALT dan AST
Akhir periode pemberian sediaan uji, semua mencit yang masih hidup diotopsi. Pengukuran kadar ALT (Alanin Transferase) dan AST (Aspartat Transferase) dilakukan dengan cara mengambil darah menggunakan alat suntik steril. ALT dan AST adalah dua parameter yang digunakan untuk mendekeksi kerusakan hati. Darah diambil melalui jantung (intra cardiac) secara
3.8.7 Makropatologi
Mencit yang mati segera diotopsi dan dilakukan pengamatan (BPOM RI, 2014). Pengamatan meliputi warna, permukaan dan konsistensi organ hati secara visual (Anggraini, 2008).
3.8.8 Histopatologi organ hati
Mencit yang mati segera diambil organnya. Akhir periode pemberian sediaan uji, semua mencit yang masih hidup diotopsi, selanjutnya diambil organ hati dicuci dengan natrium klorida kemudian dimasukkan dalam larutan dapar formaldehida 10% dan dibuat preparat histopatologi selanjutnya dilihat di bawah mikroskop (BPOM RI, 2014; Hendriani, 2007).
3.8.9 Analisis statistik
BAB IV
HASIL DAN PEMBAHASAN
4.1 Bahan Baku Ekstrak
Penelitian ini digunakan ekstrak etanol herba selada air (EEHSA) yang sama dengan ekstrak dari penelitian sebelumnya yang berjudul Ekstrak Etanol Selada Air (Nasturtium officinale R.Br) Sebagai Bahan Baku Pembuatan Tablet
Diuretika (Ginting, dkk., 2014) oleh karena itu identifikasi tumbuhan tidak dilakukan lagi.
EEHSA disimpan di lemari pendingin dalam wadah tertutup rapat sehingga EEHSA terhindar dari kontaminasi zat-zat asing. Penyimpanaan di lemari pendingin bertujuan untuk mencegah tumbuhnya jamur, mencegah ekstrak terkena sinar matahari langsung. Secara organoleptik, EEHSA yang disimpan tidak ada ditumbuhi kapang dan jamur.
4.2 Hasil Pengujian Toksisitas Subkronik
Pengujian efek toksik ekstrak etanol herba selada air (Nasturtium officinalle
R.Br,), dilakukan terhadap mencit jantan dan betina. Dosis ekstrak etanol herba
selada air yang digunakan: 25, 50, dan 200 mg/kgbb. Pengamatan dilakukan selama 90 hari meliputi gejala klinis, berat badan, jumlah makanan, kematian hewan, kadar ALT, kadar AST dan histopatologi organ hati.
4.2.1 Hasil pengamatan gejala klinis
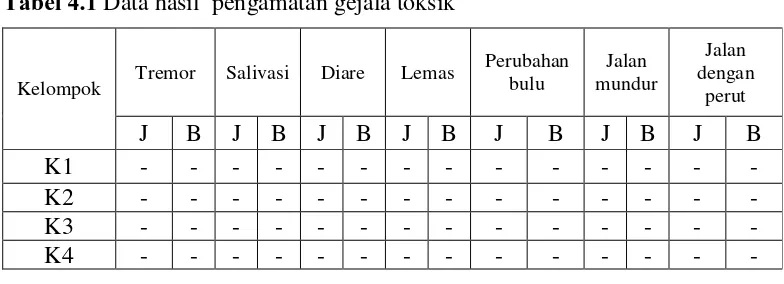
Tabel 4.1 Data hasil pengamatan gejala toksik
Kelompok Tremor Salivasi Diare Lemas
Perubahan
Keterangan : K1= kontrol CMC-Na 0.5%, K2= dosis 25 mg/kgbb, K3= dosis 50 mg/kgbb, K4= dosis 200 mg/kgbb, (-) = menunjukkan tidak adanya gejala, (+) = menunjukkan adanya gejala, j= jantan, B= betina
Berdasarkan Tabel 4.1 diketahui bahwa ekstrak etanol herba selada air yang diberikan secara oral pada mencit selama 90 hari pada kelompok kontrol dan kelompok dosis 25, 50 dan 200 mg/kgbb tidak terdapat gejala toksik. Konsep utama toksikologi adalah tergantung pada dosis. Suatu zat dapat menimbulkan efek yang tidak diinginkan berkaitan dengan dosis yang diberikan yaitu efek samping, efek merugikan dan efek toksik yang dapat diamati dengan parameter gejala toksik (Priyanto, 2009).
4.2.2 Hasil pengamatan berat badan
Penimbangan berat badan dilakukan setiap hari dari hari ke 0 sampai hari ke 90 untuk menentukan volume sediaan uji yang diberikan, sedangkan data berat badan yang dianalisis secara statistik menggunakan two way anova dilakukan tiap
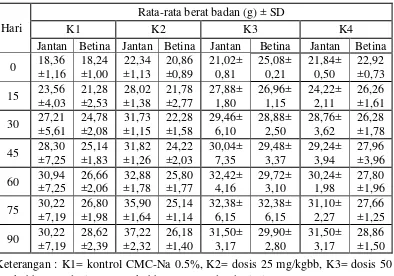
Tabel 4.2 Data rata-rata berat badan
Hari
Rata-rata berat badan (g) ± SD
K1 K2 K3 K4
Jantan Betina Jantan Betina Jantan Betina Jantan Betina 0 18,36 Keterangan : K1= kontrol CMC-Na 0.5%, K2= dosis 25 mg/kgbb, K3= dosis 50 mg/kgbb, K4= dosis 200 mg/kgbb, SD = standar deviasi
Berdasarkan Tabel 4.2 di atas yang dianalisis secara statistik menggunakan
two way anova menunjukkan tidak ada perbedaan yang signifikan antara kenaikan
berat badan kelompok kontrol dengan kelompok perlakuan yang diberi ekstrak etanol herba selada air.
Hal ini dapat ditunjukkan dengan tingkat signifikansi p≥0,05 dengan
4.2.3 Hasil pengamatan jumlah makanan
Jumlah makanan yang dikonsumsi ditimbang setiap 2 minggu sekali. Penghitungan secara statistik dilakukan setelah akhir periode perlakuan. Rata-rata jumlah makanan yang dikonsumsi dapat dilihat pada Tabel 4.3
Tabel 4.3 Data rata-rata jumlah makanan
Hari
Rata-rata jumlah makanan (g) ± SD
K1 K2 K3 K4
Jantan Betina Jantan Betina Jantan Betina Jantan Betina 0 22,32±7,00 16,56±3,36 23,66±6,18 20,16±9,00 24,02±6,80 25,46±5,01 ±4,73 24,64 22,66±3,04
Berdasarkan Tabel 4.3 di atas yang dianalisis secara statistik menggunakan
4.2.4 Hasil pengamatan kematian
Mencit diamati kematiannya dari hari pertama sampai hari terakhir. Mencit yang mati selama waktu pemberian sediaan uji segera diotopsi dan organ diamati secara histopatologi. Pengamatan kematian hewan dapat dilihat pada Tabel 4.4 Tabel 4.4 Data pengamatan kematian hewan
Kelompok Jumlah mencit Dosis (mg/kgbb) Jumlah kematian Jantan Betina keracunan terjadi akibat reaksi antara zat beracun dengan reseptor dalam tubuh (Katzung, 2002).
3.4.5 Hasil berat organ relatif
Semua mencit diotopsi dan ditimbang berat organ hatinya. Hasil berat organ relatif yang didata pada akhir perlakuan ditunjukkan pada Tabel 4.5.
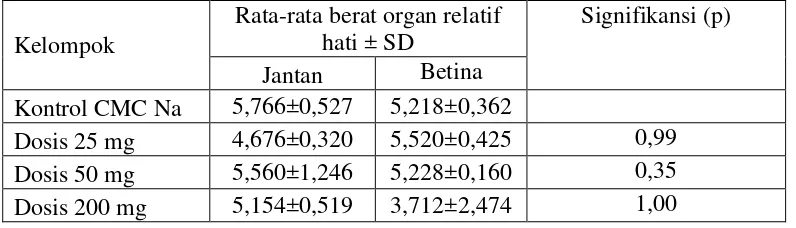
Tabel 4.5 Data berat organ relatif mencit
Kelompok
Rata-rata berat organ relatif hati ± SD
Signifikansi (p) Jantan Betina
Kontrol CMC Na 5,766±0,527 5,218±0,362
Dosis 25 mg 4,676±0,320 5,520±0,425 0,99
Dosis 50 mg 5,560±1,246 5,228±0,160 0,35
Dosis 200 mg 5,154±0,519 3,712±2,474 1,00 Keterangan : SD = Standar Deviasi
Berdasarkan hasil berat organ relatif mencit pada Tabel 4.5 yang dianalisis secara statistik menggunakan two way anova menunjukkan tidak ada perbedaan
adanya pengaruh berat organ relatif mencit yang diberi ektrak etanol herba selada air dengan mencit yang normal. Berat organ relatif yang diukur pada penelitian ini yaitu organ hati. Organ tersebut dipilih karena merupakan organ penting dalam metabolisme, detoksifikasi, penyimpanan dan ekskresi xenobiotik dan metabolitnya, serta organ ini rentan terhadap kerusakan akibat metabolit yang bersifat toksik (Brzoska, dkk., 2003).
4.2.6 Hasil pengukuran kadar ALT
Pada akhir periode pemberian sediaan uji, semua mencit diotopsi. Pengukuran kadar ALT (Alanin Transferase) dilakukan pada hari ke 91.
Pemeriksaan ALT adalah indikator yang lebih sensitif terhadap kerusakan hati dibanding AST. Enzim ALT sumber utamanya di hati, sedangkan enzim AST banyak terdapat pada jaringan terutama jantung, otot rangka, ginjal dan otak (Cahyono, 2009).
Hati membuat beberapa produk, termasuk jenis protein yang disebut sebagai enzim. Produk ini dapat keluar dari hati dan masuk ke aliran darah. Tingkat produk tersebut dapat diukur dalam darah. Kerusakan pada hati yang disebabkan oleh zat toksik dapat memungkinkan produk tersebut masuk ke aliran darah dalam tingkat yang lebih tinggi. Jadi, tes ini dapat menunjukkan tingkat kerusakan pada hati. Rata-rata kadar ALT dapat dilihat pada Tabel 4.6.
Tabel 4.6 Data pengukuran kadar ALT
Kelompok (mg/kgbb) Dosis Rata-rata ± SD Signifikansi (p)
Jantan Betina
K1 - 42,20±4,20 32,00±4,69
K2 25 58,60±4,77 52,60±4,56 0,00
K3 50 65,80±7,69 66,20±4,81 0,00
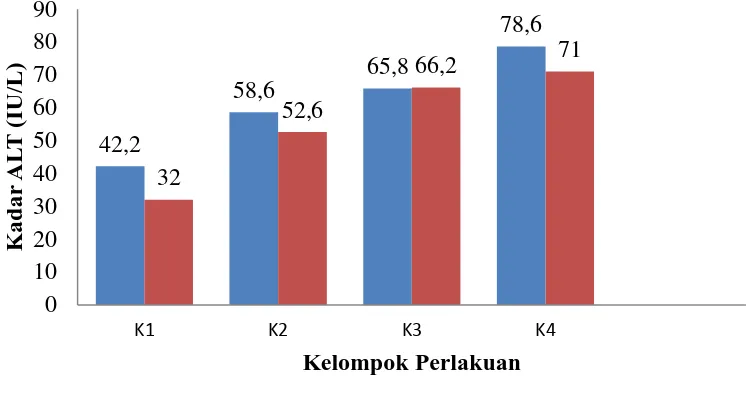
Gambar 4.1 Grafik rata-rata hasil pengukuran kadar ALT
Berdasarkan Tabel 4.6 di atas yang dianalisis secara statistik dengan menggunakan Two way anova, kemudian dilanjutkan dengan Post Hoc Test
berupa uji Tukey HSD memberikan hasil bahwa terdapat perbedaan yang signifikan antara semua kelompok perlakuan. Hal ini dapat ditunjukkan dengan tingkat signifikansi p<0,05. Kelompok kontrol rata-rata kadar ALT (Serum Glutamic piruvic Transminase) jantan (42,20UI/l) betina (32,00UI/l), dosis 25 mg/kgbb jantan (58,60UI/l) betina (52,60UI/l), dosis 50 mg/kgbb jantan (65,80UI/l) betina (66,20UI/l), dosis 200 mg/kgbb jantan (78,60UI/l) betina (71,00UI/l). Rata-rata kadar ALT dari tiap kelompok tersebut masih dalam batas normal. Kadar ALT darah mencit normal adalah 17–77 IU/L (Murtini, dkk., 2010).
Pengamatan fungsi hati adalah dengan mengamati aktivitas enzim ALT. Hati sering menjadi organ sasaran karena sebagian toksikan memasuki tubuh melalui sistem gastrointestinal dan setelah diserap toksikan dibawa oleh vena porta ke hati. Toksikan kemudian akan dimetabolisme menjadi radikal bebas yang
akan memecah sel hati (Lu, 1995). Sel hati jika mengalami nekrosis dapat segera dideteksi melalui peningkatan aktivitas enzim. Salah satu enzim yang dihasilkan oleh hati dan peka terhadap kelainan fungsi hati adalah enzim ALT. Enzim ALT ini lebih spesifik terhadap kerusakan hati dan merupakan enzim yang banyak terdapat di sitosol dalam hati dibandingkan pada jantung dan otot tubuh (Cahyono, 2009).
4.2.7 Hasil pengukuran kadar AST
Akhir periode pemberian sediaan uji, semua mencit diotopsi. Pengukuran kadar AST dilakukan diliakukan pada hari ke 91. AST atau juga dinamakan SGOT (Serum Glutamat Oxaloacetat Transminase) merupakan enzim yang dijumpai dalam otot jantung dan hati, sementara dalam konsentrasi sedang dijumpai pada otot rangka, ginjal dan pankreas. Konsentrasi rendah dijumpai dalam darah, kecuali jika terjadi cedera seluler, kemudian dalam jumlah banyak dilepaskan ke dalam sirkulasi. Hati dalam tubuh mempunyai multifungsi maka tes faal hati pun beraneka ragam sesuai dengan apa yang hendak dinilai. Dan ketika sel-sel atau jaringan hati mengalami kerusakan dapat dilakukan pemeriksaan AST dan ALT
Kadar AST akan meningkat apabila terjadi kerusakan sel yang akut seperti nekrosis hepatoseluler seperti gangguan fungsi hati dan saluran empedu, penyakit jantung dan pembuluh darah, serta gangguan fungsi ginjal dan pankreas (Price & Wilson,1995). Rata-rata kadar AST dapat dilihat pada Tabel 4.7
Tabel 4.7 Data hasil pengukuran AST
Kelompok (mg/kgbb) Dosis Rata-rata ± SD Signifikansi (p) Jantan Betina
K1 - 32,80±2,94 29,40±5,63
K2 25 48,40±10,72 49,60±7,23 0,03
K3 50 62,40±12,44 58,60±13,74 0,00
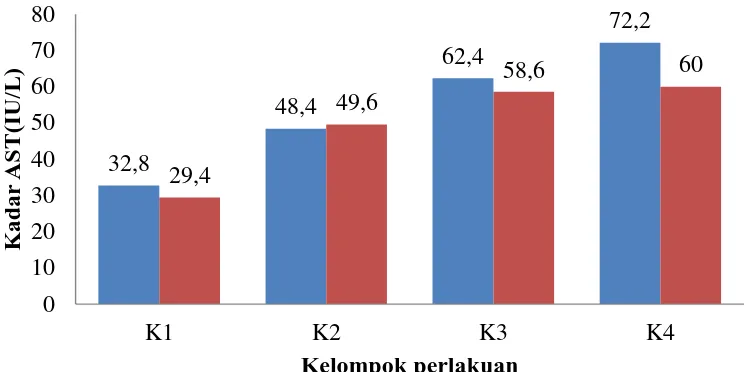
Gambar 4.2 Grafik rata-rata hasil pengukuran kadar AST
Berdasarkan Tabel 4.7 di atas yang dianalisis secara statistik dengan menggunakan two way anova, kemudian dilanjutkan dengan Post Hoc Test berupa
uji Tukey HSD memberikan hasil bahwa terdapat perbedaan yang signifikan antara semua kelompok perlakuan. Hal ini dapat ditunjukkan dengan tingkat signifikansi p<0,05. Kelompok kontrol rata-rata kadar AST jantan (32,80UI/l) betina (29,40UI/l), dosis 25 mg/kgbb jantan (48,40UI/l), betina (49,60UI/l), dosis 50 mg/kgbb jantan (62,40UI/l) betina (58,60UI/l), dosis 200 mg/kgbb jantan (72,20UI/l) betina (60,00UI/l). Rata-rata kadar AST dari tiap kelompok tersebut dalam batas normal. Kadar AST normal dalam darah mencit adalah 54-298 IU/L (Murtini, dkk., 2010).
AST merupakan enzim yang banyak ditemukan pada organ hati terutama pada sitosol. Peranan yang cukup penting dari jenis enzim ini utamanya dalam organ hati, maka kemudian digunakan dalam pemeriksaan laboratorium untuk mendeteksi adanya kelainan fungsi hati. Peningkatan Serum Glutamic
terjadi kelainan pada hati (Handoko, 2003). Ketika terjadi kerusakan pada hati, maka sel-sel hepatositnya akan lebih permeabel sehingga enzim ini bocor ke dalam pembuluh darah sehingga menyebabkan kadarnya meningkat pada serum. Enzim aspartat aminotransferase (AST) disebut juga serum glutamat oksaloasetat transaminase (SGOT) merupakan enzim mitokondria yang berfungsi mengkatalisis pemindahan bolak-balik gugus amino dari asam aspartat ke asam α -oksaloasetat membentuk asam glutamat dan -oksaloasetat. Enzim AST dan ALT mencerminkan keutuhan atau intergrasi sel-sel hati. Peningkatan enzim hati tersebut dapat mencerminkan tingkat kerusakan sel-sel hati (Schumann, dkk., 2002).
4.2.8 Hasil pengamatan makropatologi
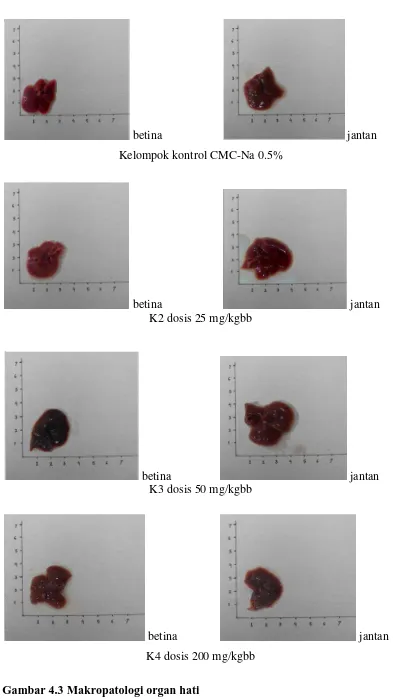
Organ hati pada mencit yang mati segera diambil dan pada akhir periode pemberian sediaan uji, semua mencit yang masih hidup diotopsi. Tujuan pengamataan ini adalah untuk melihat gambaran langsung keadaan hati setelah perlakuan pemberian ekstrak etanol herba selada air secara oral selama 90 hari sebagai salah satu parameter sensitif yang bisa dijadikan salah satu faktor penentu efek gejala toksik yang ditimbulkan secara.
Hasil pengamatan makropatologi meliputi pengamatan warna, permukaan dan konsistensi organ hati dapat dilihat pada Tabel 4.8 dan Gambar 4.3.
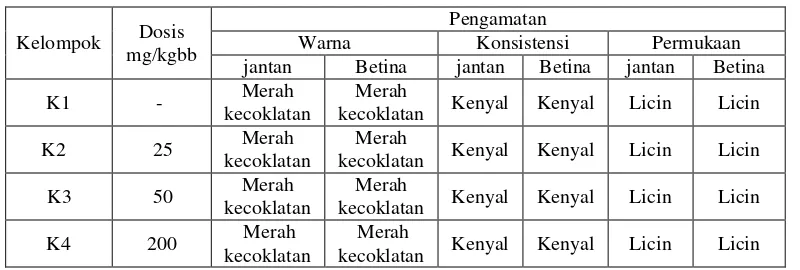
Tabel 4.8 Data pengamatan makropatologi organ hati
Kelompok mg/kgbb Dosis
Pengamatan
Warna Konsistensi Permukaan
jantan Betina jantan Betina jantan Betina
K1 - Merah
kecoklatan
Merah
kecoklatan Kenyal Kenyal Licin Licin
K2 25 kecoklatan Merah kecoklatan Merah Kenyal Kenyal Licin Licin
K3 50 kecoklatan Merah kecoklatan Merah Kenyal Kenyal Licin Licin
K4 200 Merah
kecoklatan
Merah
kecoklatan Kenyal Kenyal Licin Licin
betina jantan Kelompok kontrol CMC-Na 0.5%
betina jantan
K2 dosis 25 mg/kgbb
betina jantan
K3 dosis 50 mg/kgbb
betina jantan
Berdasarkan Tabel 4.8 terlihat pada kelompok kontrol dan dosis 25, 50 dan 200 mg/kgbb organ hati masih dalam keadaan normal yang berwarna merah kecoklatan, permukaannya licin dan konsistensinya kenyal. Kriteria normal pada organ hati bila tidak ditemukan perubahan warna, perubahan struktur permukaan dan perubahan konsistensi (Anggraini, 2008). Perubahan warna menjadi salah satu parameter terjadinya efek toksik yang bertujuan mendapatkan informasi mengenai toksisitas zat uji yang berkaitan dengan organ sasaran dan efek terhadap organ tersebut (Lu, 1995).
4.5.9 Hasil histopatologi organ hati
Pada akhir periode pemberian sediaan uji, semua mencit diotopsi. Organ hati kemudian diambil lalu organ tersebut dibuat preparat histopatologi lalu dilihat dibawah mikroskop pada perbesaran (10 x 40), hasil kerusakan dapat dilihat pada Tabel 4.9.
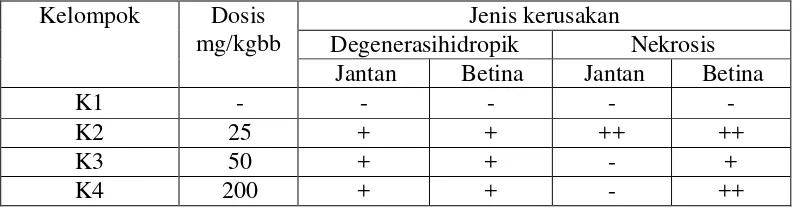
Tabel 4.9 Hasil histopatologi berdasarkan kerusakan hepatosit Kelompok Dosis
mg/kgbb
Jenis kerusakan
Degenerasihidropik Nekrosis Jantan Betina Jantan Betina
kolestasis, atau timbulnya disfungsi hati secara perlahan-lahan (Amalina, 2009). kerusakan pada sel hati dapat bersifat sementara (reversible) atau tetap (irreversible) (Wicaksono, 2002).
Gambaran histopatologi organ hati sesuai dengan pengamatan hematologi AST dan ALT dimana pada kelompok perlakuan dosis 25, 50 dan 200 mg/kgbb mulai terjadi peningkatan dibanding kelompok kontrol meskipun masih dalam rentang normal. Kerusakan pada gambaran histopatologi juga mulai terjadi pada dosis 25, 50 dan 200 mg/kgbb namun masih dalam kategori ringan hingga sedang artinya sudah mulai terjadinya gejala toksik pada kelompok dosis perlakuan ditandai mulai terjadinya kerusakan hepatoit dan kadar hematologi AST dan ALT meningkat namun hati masih dapat mengatasinya dengan kemampuan regenerasi sel hati sehingga gejala toksik belum terlihat parah. Sel hati mengalami nekrosis dapat segera dideteksi melalui peningkatan aktivitas enzim. Kerusakan membran sel menyebabkan enzim AST keluar dari sitoplasma sel yang rusak, dan jumlahnya meningkat di dalam darah. Sehingga dapat dijadikan indikator kerusakan hati. Salah satu enzim yang dihasilkan oleh hati dan peka terhadap kelainan fungsi hati adalah enzim ALT ddan AST (Elisma, dkk., 2009).
Betina
Jantan
Gambar 4.4 Gambar histoptologi organ hati perlakuan kontrol Na-CMC 0.5% Keterangan : Perlakuan kontrol Na-CMC 0.5%
1 = Vena central; 2 = Sinusoid; 3 = Hepatosit
1
2 3
2
Betina
jantan
Gambar 4.5 Gambar histopatologi organ hati perlaakuan dosis 25 mg/kgbb Keterangan : Perlakuan dosis 25 Mg/kgbb
1 = Degenerasi hidropik; 2 = Karioreksis; 3 = Vena central; 4 = Kariolisis; 5. Kariopiknosis; 6 =Sinusoid
3 1
2 3
6 5 4
2
5 4
Betina
Jantan Gambar 4.6 Gambar histopatologi organ hati perlakuan dosis 50 mg/kgbb Keterangan : Perlakuan dosis 50 Mg/kgbb
1 = Degenerasi hidropik; 2 = Karioreksis; 3 = Vena central; 4 = Kariopiknosis 5 = Sinusoid; 6 = Kariolisis
2
3
5 4 1
2
3 1
5
Betina
Jantan
Gambar 4.7 Gambar histopatologi organ hati perlakuan dosis 200 mg/kgbb Keterangan : Perlakuan dosis 200 Mg/kgbb
1 = Degenasi hidropik; 2 = Karioreksis; 3 = Vena central; 4 = Kariopiknisis; 5 =. Kariolisis; 6 = Sinusoid.
2
3
5 1 6
4
2
3 1
4 5
Berdasarkan dari gambar-gambar di atas dapat dilihat bahwa pada kelompok kontrol menunjukkan bahwa gambaran histologi tersebut masih dalam keadaan normal yaitu dengan menunjukkan hepatosit tersusun secara radial dalam lobulus hati dan belum ada terlihat terjadinya degenerasi hidropik, sedangkan pada kelompok dosis 25, 50 dan 200 mg/kgbb sebagian dari hepatosit sudah mengalami degenerasi hidropik hal ini terjadi karena adanya gangguan membran sel sehingga cairan masuk ke dalam sitoplasma, sinusoid sudah tidak teratur, hepatosit mengalami degenerasi hidropik dan sudah terjadi nekrosis. Kerusakan hati akibat senyawa kimia ditandai dengan lesi biokimiawi yang memberikan rangkaian perubahan fungsi dan struktur.
` Degenerasi hidropik, terjadi karena adanya gangguan membran sel sehingga cairan masuk ke dalam sitoplasma, menimbulkan vakuola-vakuola kecil sampai besar. Terjadi akumulasi cairan karena sel yang sakit tidak dapat menyingkirkan cairan yang masuk (Underwood, 1994). Hal ini disebabkan karena gangguan transpor aktif yang menyebabkan sel tidak mampu memompa ion Na+ keluar sehingga konsentrasi ion Na+ di dalam sel naik. Pengaruh osmosis menyebabkan influks air ke dalam sel sehingga terjadi perubahan morfologis yaitu sel menjadi bengkak (Robbins, dkk,. 2007).
BAB V
KESIMPULAN DAN SARAN
4.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat diambil kesimpulaan bahwa ekstrak etanol herba selada air berpotensi menimbulkaan gejala toksik, namun pada pemberian 90 hari pada dosis 25, 50 dan 200 mg/kgbb masih dalam kategori aman digunakan.
4.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Tanaman selada air (Nasturtium officinale R.Br) tidak terlalu mirip dengan
selada dari genus lactuce. Tanaman ini berupa herba aquatik menjalar atau tegak,
bisa mencapai ketinggiaan 1m, mempunyai akar tunjang dan sering menghasilkan akar pada buku. Tanaman ini memiliki banyak cabang dan berbatang licin, banyak
cairan serta berongga dalam batang (Muhlisah dan Sapta, 2009).
Daun selada air adalah jenis majemuk ganda dua bentuknya agak bulat dengan diameter 1,5-3 cm. Selada air sangat mudah tumbuh dan sering ditemukan tumbuh liar di aliran sungai kecil, kolam, rawa, atau bagian danau yang dangkal, oleh karena itu, tanaman ini sangat jarang dibudidayakan secara khusus oleh petani. Biasanya selada air yang dijual masih diandalkan dari hasil tanaman yang tumbuh liar di perairan sekitar rumah penduduk (Muhlisah dan Sapta, 2009). 2.1.1 Sistematika tumbuhan
Tumbuhan selada air memiliki sistematika sebagai berikut (Lubis, et al., 2013)
Kingdom : Plantae
Devisi : Spermatophyta Sub devisi : Angiospermae Kelas : Dicotyledoneae Suku : Brassicaceae Marga : Nasturtium
2.1.2 Sinonim tumbuhan
Sinonim Rorippa nasturtium aquaticum (Linn.) Hayek (Novia, 2014). 2.1.3 Nama daerah
Indonesia : selada air 2.1.4 Nama asing
Watercress (Inggris), sal yeung ts’ol (China) (Novia, 2014).
2.1.5 Daerah tumbuhan
Selada air sangat mudah tumbuh dan sering ditemukan tumbuh liar di aliran sungai kecil, kolam, rawa, atau bagian danau yang dangkal (Muhlisah dan Sapta, 2009).
2.1.6 Kegunaan
Selada air memiliki aktivitas antibiotika, antitumor dan diuretik. Sebagai obat selada air meningkatkan selera makan dan pencernaan. Selada air digunakan untuk mengobati iritasi dari saluran urin efferen (Gruenwald, dkk., 2000), antikanker (Boyd, dkk., 2006). Selada air juga telah diteliti aktivitasnya sebagai obat tuberculosis (Corona, dkk., 2008) dan antidiabetes (Hoseini, dkk., 2009). Penelitian Özen (2009) menunjukkan aktivitas ekstrak selada air dapat melawan dan mengurangi peroksidasi lipid pada hati, otak dan ginjal.
selada air, sama dengan memanen kangkung air. Pertama-tama, gulma yang tumbuh di sela-sela selada air diambil dan dibuang, kemudian selada air itu dipotong dengan menggunakan sabit yang tajam. Tinggi tanaman yang layak dipotong sekitar 20 cm (Muhlisah dan Sapta, 2009).
Bangsa Yunani Kuno dan Romawi menganggap selada air dapat memberikan kekuatan, keberanian, karakter dan bahkan kecerdasan. Selada air di abad pertengahan dipercaya dapat mencegah kebotakan, menyembuhkan sakit gigi, serta membersihkan darah dan kulit. Selada air memang banyak mengandung vitamin A dan C yang menyehatkan ditambah pula dengan sejumlah kalori yang sedikit. Seporsi 10 batang hanya mengandung 5g kalori (Joseph, dkk., 2002).
Selada air dikenal sebagai selada hijau yang “menggigit balik” dan
sekarang seharusnya bukan suatu kejutan bahwa rasa pahit dalam selada air merupakan akibat dari isothiocyanates. Selada air memiliki isothiocyanate yang berbeda bernama phenethyl isothiocyanate atau singkatnya PEITC. PEITC dapat
ditemukan di dalam lobak, lobak hijau, namun sejauh ini sumber terbaiknya adalah selada air (Joseph, dkk., 2002).
2.2 Toksisitas
Toksisitas adalah kemampuan suatu xenobiotik (zat yang berasal dari luar tubuh organisme) dalam menimbulkan kerusakan pada organisme baik saat digunakan atau saat berada dalam lingkungan (Priyanto, 2009)
Paracelcus yang dianggap sebagai bapak toksikologi tidak membedakan antara obat dengan zat beracun berdasarkan toksisitasnya. Paracelcus berpendapat, yang membedakan antara obat dengan racun atau zat yang bukan racun dengan racun adalah dosisnya. Paracelcus menyimpulkan bahwa obat bukan racun sebagaimana anggapan banyak pihak, karena penggunaan obat diberikan berdasarkan aturan dosis tertentu. Obat dapat menimbulkan efek yang tidak diinginkan yang berkaitan dengan dosis yang diberikan yaitu efek toksik (toxic effet) (Priyanto, 2009)
paparan zat kimia meliputi: jalur paparan (intravaskuler atau ekstravaskuler), lama dan kekerapan paparan, dosis paparan, paparan akut atau kronis. Kondisi makhluk hidup meliputi: keadaan fisiologi (berat badan, jenis kelamin, dll), keadaan patologi (penyakit saluran pencernaan, kardiovaskuler, hati, dan ginjal (Priyanto, 2009).
2.2.1 Toksisitas umum 2.2.1.1 Toksisitas akut
Uji toksisitas akut adalah suatu pengujian untuk mendeteksi efek toksik yang muncul dalam waktu singkat setelah pemberian sediaan uji secara oral dalam dosis tunggal yang diberikan dalam waktu 24 jam (Lu, 1995). Tujuan dilakukannya uji toksisitas akut adalah untuk menentukan LD50 (potensi ketoksikan) akut dari suatu senyawa. Semakin kecil harga LD50 maka semakin besar potensi ketoksikannya (Priyanto, 2009).
Prinsip uji toksisitas akut oral yaitu, sediaan uji dalam beberapa tingkat dosis yang diberikan pada beberapa kelompok hewan uji dengan satu dosis per kelompok, kemudian dilakukan pengamatan terhadap adanya efek toksik dan kematian (OECD, 2001).
2.2.1.2 Toksisitas subkronik
Uji toksisitas subkronik merupakan suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji dengan dosis berulang yang diberikan secara oral pada hewan uji (BPOM, RI., 2014).
dan mempelajari adanya efek kumulatif dan efek reversibilitas zat tersebut (OECD, 1998). Tujuan lain dari uji toksisitas oral adalah untuk menentukan organ sasaran yang menjadi target zat toksik (Priyanto, 2009).
Prinsip uji toksisitas subkronik oral adalah sediaan uji dalam beberapa tingkat dosis diberikan setiap hari pada beberapa kelompok hewan uji dengan satu dosis per kelompok selama 28 atau 90 hari. Selama pemberian sediaan uji, hewan harus diamati setiap hari untuk menentukan adanya toksisitas. Selama waktu dan pada akhir periode pemberian sediaan uji, hewan yang mati dan masih hidup diotopsi selanjutnya dilakukan pengamatan secara makropatologi pada setiap organ dan jaringan. Pemeriksaan hematologi, biokimia klinis dan histopatologi juga dilakukan untuk mendukung hasil uji (BPOM, RI., 2014).
Dosis uji pada uji toksisitas subkronik sekurang-kurangnya digunakan tiga kelompok dosis dan satu kelompok kontrol untuk setiap jenis kelamin. Dosis toksik harus menyebabkan gejala toksik pada beberpa hewan uji dan terjadinya kematian tidak boleh lebih dari 10%, sedangkan dosis tidak berefek tidak boleh menyebabkan gejala toksik. Uji pendahuluan yang diperoleh perlu dipertimbangkan hasilnya. Tingkat dosis lain ditetapkan dengan faktor perkalian tetap 2 sampai 10 (Harmita, 2006).
2.2.1.3 Toksisitas kronik
biokimia klinis, makropatologi, penimbangan organ dan histopatologi (BPOM, RI., 2014).
2.3 Biologi Mencit
Mencit merupakan salah satu hewan percobaan yang sering digunakan dalam penelitian. Tujuan penggunaan hewan percobaan adalah untuk mempelajari dan mengembangkan berbagai macam bidang ilmu dan serta penelitian laboratorium. Hewan percobaan harus mempunyai persyaratan tertentu antara lain persyaratan genetis dan lingkungan yang memadai (Dolokasaribu, 2008).
Mencit termasuk hewan pengerat yang cepat berkembangbiak, mudah dipelihara dalam jumlah banyak dan variasi genetiknya cukup besar. Mencit merupakan hewan percobaan yang efisien karena mudah dipelihara, tidak memerlukan tempat yang luas, waktu kebuntingan yang singkat dan banyak memiliki anak. Mencit dan tikus putih memiliki banyak data toksikologi, sehingga mempermudah membandingkan toksisitas zat-zat kimia (Lu, 1995). Sistem taksonomi mencit termasuk golongan
Kingdom : Animalia Filum : Chordata Subfilum : Vertebrata Kelas : Mamalia Bangsa : Rodentia Marga : Mus
Jenis : Mus musculus
musculus. Berbeda dengan hewan-hewan lainnya, mencit tidak memiliki kelenjar
keringat (Dolokasaribu, 2008).
Umur empat minggu berat badannya mencapai 18-20 g. Jantung terdiri dari empat ruang dengan dinding atrium yang tipis dan dinding ventrikel yang lebih tebal. Peningkatan temperatur tubuh tidak dipengaruhi tekanan darah, sedangkan frekuensi jantung, cardiac output berkaitan dengan ukuran tubuhnya.
Hewan ini memiliki karakter lebih aktif pada malam hari dibanding siang hari (nokturnal). Mencit adalah hewan yang paling banyak digunakan untuk penelitian medis (60-80%) karena murah dan mudah berkembang biak (Dolokasaribu, 2008).
Kondisi ruangan dan pemeliharaan hewan uji untuk hewan pengerat digunakan ruangan dengan suhu 220C (±30C), kelembapan relatif 30-70% dan penerangan 12 jam terang dan 12 jam gelap. Hewan dikelompokkan dalam kandang berdasarkan jenis kelamin. Ukuran kandang yang digunakan sesuai dengan jumlah hewan per kandang. Hewan diberi makanan hewan laboratorium yang sesuai, makanan dan minuman diberikan tanpa batas (Harmita, 2006).
cenderung berkumpul sesamanya dan lebih aktif pada malam hari dibandingkan siang hari (nokturnal) (Harmita, 2006).\
2.4 Hati
Salah satu organ yang sering menderita karena adanya zat-zat toksik adalah hati. Bahan kimia kebanyakan mengalami metabolisme dalam hati oleh karenanya berpotensi merusak sel-sel hati (Wicaksono, 2002).
2.4.1 Anatomi hati
Hati merupakan organ tubuh terbesar kedua di dalam tubuh, dengan berat rata-rata sekitar 1,5 kg. Organ ini terletak dalam rongga perut sebelah kanan di bawah diafragma (Junqueira and Carneiro, 2007). Hati terbagi dalam dua belahan utama kanan dan kiri yang dipisahkan oleh fisura longitudinal (Irianto, 2004). Warnanya dalam keadaan segar merah kecoklatan, warna tersebut terutama disebabkan oleh adanya darah yang amat banyak (Lee, et al., 1997). Gambar anatomi hati dapat dilihat pada Gambar 2.1 berikut
Secara anatomi hati terdiri dari beberapa lobus tergantung pada spesiesnya, untuk mencit terdapat empat lobus (lobus medial, kaudal, lateral kiri dan lateral kanan). Setiap lobus hati terdiri dari beberapa lobulus yang terdiri dari berbagai komponen, yaitu sel-sel hati (hepatosit), vena sentralis, sinusoid, cabang-cabang vena porta, cabang-cabang-cabang-cabang arteri hepatika, sel kupffer dan kanalikuli biliaris (Junqueira and Carneiro, 2007).
2.4.2 Fisiologi hati
Organ hati terlibat dalam metabolisme zat makanan serta sebagian besar obat dan toksikan (Lu, 1995). Berdasarkan fungsinya, hati juga termasuk sebagai alat ekskresi. Hati membantu fungsi ginjal dengan cara memecah beberapa senyawa yang bersifat racun. Hati mempunyai fungsi yang sangat banyak dan kompleks yang penting untuk mempertahankan hidup (Husadha, 1996) yaitu : a. Fungsi pembentukan dan ekskresi empedu
Hal ini merupakan fungsi utama hati yaitu mengekskresikan sekitar satu liter empedu setiap hari. Garam empedu penting untuk pencernaan dan absorbsi lemak dalam usus halus.
b. Fungsi metabolik
Hati berperaan penting dalam metabolisme karbohidrat, lemak, protein, vitamin dan juga memproduksi energi. Hati mengubah ammonia menjadi urea, untuk dikeluarkan melalui ginjal dan usus.
c. Fungsi pertahanan tubuh
membahayakan dan mengubahnya menjadi zat yang secara fisiologis tidak aktif. Fungsi perlindungan dilakukan oleh sel kupffer yang terdapat di dinding sinusoid hati.
2.4.3 Histologi hati
Hati terdiri atas unit-unit heksagonal yaitu lobulus hati. Bagian tengah setiap lobulus hati terdapat sebuah vena sentralis yang dikelilingi secara radial oleh sel-sel hati (hepatosit). Sel hati memiliki kemampuan regenerasi yang cukup tinggi. Sel parenkim pada hati disebut hepatosit, menempati sekitar 80% volume hati dan melakukan berbagai fungsi utama hati. 40% sel hati terdapat pada lobus sinusoid. Sel non-parenkimal menempati sekitar 6,5% volume hati dan memproduksi berbagai substansi yang mengendalikan banyak fungsi hepatosit (Junqueira dan Corneiro, 2007)
Sel hati berbentuk polihedral dengan inti bulat yang terletak di tengah dan kadang tampak lebih dari satu inti akibat pembelahan sitoplasma yang tidak sempurna. Sel tersebut terletak di antara sinusoid yang berisi darah dan saluran empedu (Lu, 1995). Darah yang mengandung toksin dibawa dari usus kemudian masuk ke hati melalui vena porta kemudian melewati sinusoid menuju vena sentralis (Macfarlane, et al., 2000).
2.4.4 Intoksikasi hati
Metabolisme umumnya berlangsung di hati karena di hati banyak terdapat enzim pemetabolisme. Tujuannya adalah membuat senyawa menjadi lebih polar sehingga mudah dieksresikan dan menjadi kurang toksik, namun ada senyawa tertentu yang setelah mengalami metabolisme menjadi lebih toksik, misalnya fenasetin menjadi paracetamol, faration menjadi paraokson dan protonsil menjadi silfa. Hati adalah tempat banyak proses metabolisme penting, termasuk sintesis protein, detoksifikasi, dan produksi bahan kimia pencernaan. Metabolisme hati adalah sumber dari banyak zat penting untuk kesehatan lanjutan dan kelangsungan hidup (Priyanto, 2009).
Kerusakan pada hati dapat terjadi oleh beberapa faktor yaitu onset pemaparan yang terlalu lama, durasi pemaparan, dosis dan sel inang yang rentan. Kerusakan yang terjadi pada sel hati dapat bersifat sementara (reversible) dan tetap atau tidak bisa kembali pulih (irreversible) (Wicaksono, 2002). Sel akan mengalami perubahan untuk beradaptasi mempertahankan hidupnya, perubahan ini biasa disebut degenerasi. Degenerasi terjadi karena adanya gangguan biokimiawi yang disebabkan oleh iskemia, anemia, metabolisme abnormal dan zat kimia yang bersifat toksik (Cheville, 1999).
oleh pompa Na+ yang memerlukan ATP, jika ATP berkurang maka akan mengakibatkan masuknya Na+ ke intrasel melebihi jumlah normalnya (Priyanto, 2009).
Kerusakan sel secara terus-menerus akan mencapai suatu titik sehingga terjadi kematian sel (Lu, 1995). Paparan zat toksik pada sel apabila cukup hebat atau berlangsung cukup lama, maka sel tidak dapat lagi mengkompensasi dan tidak dapat melanjutkan metabolisme (Priyanto, 2009). Inti sel yang mati dapat terlihat lebih kecil dan menjadi lebih padat (kariopiknosis), setelah itu menjadi hancur bersegmen-segmen (karioreksis) dan kemudian inti sel menghilang (kariolisis) (Underwood, 1994). Nekrosis hati dapat bersifat reversible maupun irreversible. Nekrosis hati adalah kematian hepatosit yang umumnya merupakan kerusakan akut (Lu, 1995).
2.5 ALT (Alanine Aminotransferase)
Tes fungsi hati yang umum untuk mengetahui adanya gangguan dalam organ hati adalah dengan mengukur serum aminotransferase yaitu ALT (Alanine Aminotransferase) atau SGPT (Serum Glutamic Pyruvic Transaminase) (Wibowo,
dkk., 2005). ALT memindahkan satu gugus amino antara alanin dan asam alfa keto-glutamat, fungsi ini penting untuk pembentukan asam-asam amino yang dibutuhkan untuk menyusun protein di hati (Sacher dan Richard, 2004).
kerusakan dalam hati dibandingkan dengan AST (Hadi, 1995). ALT darah mencit normal adalah 17-77 IU/L (Murtini, dkk., 2010).
2.6 AST (Aspartat Aminotransferase)
AST (Aspartat Aminotransferase) atau juga dinamakan SGOT (Serum Glutamic Oxaloacetic Transaminase) merupakan enzim yang dijumpai dalam otot
jantung dan hati, sementara dalam konsentrasi sedang dijumpai pada otot rangka, ginjal dan pankreas. Konsentrasi rendah dijumpai dalam darah, kecuali jika terjadi cedera seluler, kemudian dalam jumlah banyak dilepaskan ke dalam sirkulasi. Kadar AST/AST biasanya dibandingkan dengan kadar enzim jantung lainnya, seperti CK (creatin kinase), LDH (lactat dehydrogenase). Pada penyakit hati, kadarnya akan meningkat 10 kali lebih dan akan tetap demikian dalam waktu yang lama (Wibowo, dkk., 2005). Saat terjadi kerusakan hati akut, jumlah enzim transaminase alanin (ALT) dan transaminase aspartat (AST) meningkat
BAB I PENDAHULUAN
1.1Latar Belakang
Toksisitas adalah kemampuan suatu zat kimia dalam menimbulkan kerusakan pada organisme baik saat digunakan atau saat berada dalam lingkungan. Secara umum toksisitas dibedakan menjadi toksisitas akut, toksisitas subkronik dan toksisitas kronik. Uji toksisitas subkronis adalah uji ketoksikan suatu senyawa yang diberikan dengan dosis berulang pada hewan uji tertentu, selama kurang dari tiga bulan (Priyanto, 2009). Uji toksisitas bertujuan untuk mengetahui efek toksik dan menentukan batas keamanan suatu senyawa yang terdapat dalam zat-zat kimia, termasuk dalam tumbuh-tumbuhan (Widyastuti, 2008).
Uji toksisitas subkronik adalah salah satu uji praklinik untuk mengidentifikasi ciri fisik maupun organ yang diberikan senyawa uji secara berulang dalam waktu tertentu yaitu selama 28 atau 90 hari (Casarett dan Doull, 2008). Prinsip uji toksisitas subkronik yaitu, sediaan uji dalam beberapa tingkat dosis diberikan setiap hari pada beberapa kelompok hewan uji. Tujuan uji toksisitas subkronik adalah untuk memperoleh informasi adanya efek toksik zat yang tidak terdeteksi pada uji toksisitas akut (OECD, 1998).
resiko efek sampingnya sedikit dibandingkan obat-obatan kimia. Pemakaian obat tidak dapat dihindarkan dari efek samping yang ditimbulkan. Obat-obatan kimia biasanya mempunyai kontra indikasi dengan efek samping yang tidak diharapkan begitu juga dengan obat yang berasal dari alam namun hal itu jarang dipublikasikan (Dalimartha, 2002). Informasi adanya ketoksikan dari suatu bahan alam yang biasa digunakan untuk pengobatan sangat dibutuhkan.
Salah satu tanaman yang dapat digunakan sebagai bahan obat adalah tanaman selada air (Nasturtium officinale R.Br). Sayuran ini telah diuji aktivitas
antikankernya yakni untuk kanker kolon dengan menggunakan jus selada air
dengan konsentrasi paling efektif 50 μl/ml terhadap kerusakan DNA pada sel
HT29 (Boyd, dkk., 2006). Herba selada air digunakan untuk pengobatan tuberkulosis (Corona, dkk., 2008), antidiabetes (Hoseini, dkk., 2009), antialergi (Lingga, 2012) dan obat diuretik (Ginting, dkk., 2014).
Selada air adalah salah satu tanaman sayur dari suku Brassicaceae banyak
dijumpai dikawasan beriklim sederhana dan di dataran tinggi kawasan iklim tropik termasuk Indonesia. Obat tradisional dalam bentuk bahan baku ekstrak agar dapat menjadi obat herbal terstandar, maka harus dilakukan uji praklinik termasuk uji keamanan yaitu uji toksisitas akut, subkronik dan kronik (BPOM RI, 2004).
Penelitian sebelumnya mengenai uji toksisitas akut diketahui bahwa ekstrak etanol herba selada air memiliki nilai dosis aman tertinggi adalah 4000 mg/kgbb (Ginting, dkk., 2014). Berdasarkan informasi tersebut maka peneliti tertarik melakukan penelitian lanjutan untuk mengetahui toksisitas subkronik dari pemberian ekstrak etanol herba selada air (Nasturtium officinale R.Br) dengan
betina. Selama waktu pemberian sediaan uji, hewan harus diamati setiap hari untuk menentukan adanya toksisitas.
1.2Perumusan Masalah
Berdasarkan uraian di atas, maka rumusan masalah dalam penelitian ini adalah apakah ekstrak etanol herba selada air (EEHSA) dapat menimbulkan gejala toksik pada mencit selama pemberian 90 hari?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis pada penelitian ini diduga EEHSA menimbulkan gejala toksik pada mencit selama pemberian 90 hari.
1.4 Tujuan Penelitian
Adapun tujuan penelitian ini adalah untuk mengetahui EEHSA dapat menimbulkan gejala toksik mencit selama pemberian 90 hari.
1.5 Manfaat Penelitian
1.5Kerangka Pikir Penelitian
Adapun kerangka pikir penelitian ini dapat dilihat pada Gambar 1.1
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Kerangka pikir penelitian Simplisia herba
organ hati 1. Warna 2. Konsistensi
UJI TOKSISITAS SUBKRONIK EKSTRAK ETANOL HERBA SELADA AIR (Nasturtium officinale R.Br)
PADA ORGAN HATI MENCIT ABSTRAK
Uji toksisitas subkronik merupakan suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji dengan dosis berulang yang diberikan secara oral pada hewan uji selama 28 atau 90 hari. Selada air (Nasturtium officinale R.Br) merupakan salah satu tanaman sayur dari suku Brassicaceae. Selada air memiliki efek sebagai antialergi, antidiabetes,
pengobatan tuberkulosis dan antikanker. Tujuan penelitian ini adalah untuk mengetahui efek toksik dan mengetahui batas keamanan dosis ekstrak etanol herba selada air (EEHSA) selama 90 hari.
Ekstrak diuji toksisitas subkroniknya menggunakan mencit sebanyak 40 ekor dibagi dalam 4 kelompok terdiri dari jantan dan betina. kelompok kontrol diberi suspensi CMC-Na 0,5%, perlakuan diberi EEHSA dosis 25, 50, 200 mg/kgbb yang diberi secara oral setiap 6 hari dalam seminggu selama 90 hari. Pengamatan dilakukan setiap hari meliputi gejala toksik, berat badan, kematian, pengukuran kadar AST, ALT, makropatologi dan histopatologi organ hati, kemudian dianalisis statistik dengan ANOVA menggunakan statistical program service solution (SPSS) versi 17.
Hasil pengamatan tidak ditemukan gejala toksik pada kelompok kontrol maupun pada kelompok dosis perlakuan. Hasil uji statistik tidak ada perbedaan yang signifikan antara kenaikan berat badan dengan pemberian EEHSA (p≥0,05). Selama perlakuan tidak ada kematian mencit. Hasil rata-rata kadar ALT terdapat
perbedaan signifikan pada tiap kelompok perlakuan (p<0,05). Rata-rata kadar ALT dari tiap kelompok tersebut masih dalam batas normal. Hasil rata-rata kadar AST terdapat perbedaan signifikan pada tiap kelompok perlakuan (p<0,05). Rata-rata kadar AST dari tiap kelompok tersebut masih dalam batas normal. Hasil makropatologi dan histopatologi pada dosis 25, 50 dan 200 mg/kgbb terjadi perubahan inti sel dan nekrosis. Tidak ada perbedaan signifikan antara kelompok jantan dengan kelompok betina. Hal ini dapat disimpulkan bahwa EEHSA berpotensi menimbulkan gejala toksik, namun pada pemberian 90 hari pada dosis 25, 50 dan 200 mg/kgbb masih dikategorikan aman digunakan.
SUBCHRONIC TOXICITY TEST OF WATERCRESS HERB ETHANOLIC EXTRACT (Nasturtium offinale R.Br)
ON THE MICE LIVER ABSTRACT
Subcronic toxicity test is a test to detect the toxic effects that arise after the administration of the test preparation with repeated doses were given orally to the tested animals for 28 or 90 days. Watercress (Nasturtium Officinalle R.Br) is one
of the vegetable plants of the Brassicaceae family. Watercress has the abilities such as hypo-allergenic, anti-diabetes, tuberculosis, and anticancer treatment. The purpose of this study was to determine the toxic effects and determine the safety limit dose of ethanol extract of watercress herb (EEHSA) for 90 days.
Fourty mice were divided into 4 groups: control group were given CMC-Na suspension 0.5%, the treatments were given EEHSA dose of 25, 50, 200 mg/kgbw orally every 6 days in every week for 90 days. Observations have been done every day included toxic symptoms, weight loss, mortality, measurement of the levels of AST, ALT, macropathology and liver histopathology, then statistically analyzed by ANOVA using the statistical program service solution (SPSS) version 17.
The observations found that there’s no toxic symptoms in the control group and the treatment dose groups. The statistic test results shows that there’s no significant difference on weight gain by administering the EEHSA (p≥0.05) The test results were not statistically . During the treatments there were no death mice. There’s difference on the average yield ALT levels results in each treatment group (p<0.05). The average of each group ALT levels are still within normal limits. The average yield AST significant difference in each treatment group (p<0.05). The average of AST of each group is still within normal limits. Macropathology and histopathology result at doses of 25, 50 and 200 mg/kg bw changes in the nucleus of cells and necrosis. No significant differences between groups of males with a group of females. It can be concluded that EEHSA potential to cause toxic symptoms, but on giving 90 days at doses of 25, 50 and 200 mg/kgbw is still considered safe to use.
UJI TOKSISITAS SUBKRONIK EKSTRAK ETANOL
HERBA SELADA AIR (Nasturtium officinale R.Br)
PADA ORGAN HATI MENCIT
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
SITI KHOLIJAH
NIM 111501026
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI TOKSISITAS SUBKRONIK EKSTRAK ETANOL
HERBA SELADA AIR (Nasturtium officinale R.Br)
PADA ORGAN HATI MENCIT
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
SITI KHOLIJAH
NIM 111501026
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI TOKSISITAS SUBKRONIK EKSTRAK ETANOL HERBA SELADA AIR (Nasturtium officinale R.Br)
PADA ORGAN HATI MENCIT OLEH:
SITI KHOLIJAH NIM 111501026
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: 18 Desember 2015
Disetujui oleh:
Pembimbing I, Panitia Penguji,
Dra. Herawaty Ginting, M.Si., Apt. Prof. Dr. Urip Harahap, Apt. NIP 195112231980032002 NIP 195301011983031004
Pembimbing II, Dra. Herawaty Ginting, M.Si., Apt. NIP 195112231980032002
Aminah Dalimunthe, M.Si., Apt. Marianne, S.Si., M.Si., Apt. NIP 197806032005012004 NIP 198005202005012006
Hari Ronaldo Tanjung, M.Si., Apt. NIP 197803142005011002
Medan, Januari 2016 Fakultas Farmasi
Universitas Sumatera Utara Pejabat Dekan,
Dr. Masfria, M.S., Apt.
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan karunia yang berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi yang berjudul Uji Toksisitas Subkronik Herba Selada Air (Nasturtium officinale,
R.Br) pada Organ Hati Mencit. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada Ibu Dr. Masfria, M.S., Apt., selaku Pejabat Dekan Fakultas Farmasi yang telah menyediakan fasilitas kepada penulis selama perkuliahan di Fakultas Farmasi. Penulis juga mengucapkan terima kasih kepada Ibu Dra. Herawaty Ginting, M.Si., Apt., dan Ibu Aminah Dalimunthe, M.Si., Apt., yang telah meluangkan waktu dan tenaga dalam membimbing penulis dengan penuh kesabaran dan tanggung jawab, memberikan petunjuk dan saran-saran selama penelitian hingga selesainya skripsi ini. Ucapan terima kasih juga penulis sampaikan kepada Bapak Prof. Dr. Urip Harahap, Apt., selaku ketua penguji, Ibu Marianne, S.Si., M.Si., Apt., dan Bapak Hari Ronaldo Tanjung, M.Si., Apt., selaku anggota penguji yang telah memberikan saran untuk menyempurnakan skripsi ini, dan Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku dosen pembimbing akademik serta Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah banyak membimbing penulis selama masa perkuliahan hingga selesai.
kakak-kakak dan adik-adikku atas limpahan kasih sayang, semangat dan doa yang tak ternilai dengan apa pun. Penulis juga mengucapkan terima kasih kepada sahabat-sahabat terdekat terutama Fitri Falah, Ananda Paradita, Afina Faza, Eka Dharma Isni, Annisa Mulia Hapsari, Laili Safitri, teman-teman Asisten Farmakologi Fakultas Farmasi USU yang telah banyak membantu serta teman-teman mahasiswa/i Farmasi Stambuk 2011 yang selalu mendoakan dan memberi semangat yang tiada henti.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, 18 Desember 2015 Penulis,