Lampiran 3. Gambar mikroskopik simplisia teripang Pearsonothuria graeffei
perbesaran 10x40
Keterangan :
1. spikula bentuk kancing(buttons)
2. spikula bentuk meja semu (pseudo-tables) 3. spikula bentuk batang (rods)
1
2
Lampiran 4. Perhitungan hasil penetapan kadar air serbuk simplisia teripang
Kadar air = e a
be a a e g
1. Kadar air 1
Berat sampel = 5,010 g Volume air = 0,5 ml
Kadar air =
= 9,98 % 2. Kadar air II
Berat sampel = 5,003 g Volume air = 0,45 ml
Kadar air =
3 = 8,99 % 3. Kadar air III
Berat sampel = 5,026 g Volume air = 0,65 ml
Kadar air =
= 9,45 %
Kadar air rata – rata = 3
Lampiran 5. Perhitungan hasil penetapan kadar sari larut air serbuk simplisia 3. Kadar sari larut air III
Lampiran 6. Perhitungan hasil penetapan kadar sari larut etanol serbuk simplisia 3. Kadar sari larut etanol III
Lampiran 8. Perhitungan hasil penetapan kadar abu tidak larut asam serbuk simplisia teripang
1. Kadar abu tidak larut asam I
Berat sampel = 2,016 g
Berat abu tak larut asam = 0,06 g Kadar abu tidak larut asam =
gx 100% = 2,98%
2. Kadar abu tidak larut asam II
Berat sampel = 2,007 g
Berat abu tak larut asam = 0,091 g Kadar abu tidak larut asam = g
gx 100% = 4,53%
3. Kadar abu tidak larut asam III
Lampiran 9. Bagan alur pembuatan ekstrak teripang
Teripang
Simplisia Teripang
Dibersihkan isi perutnya
Lampiran 10. Bagan alur ekstraksi cair-cair ekstrak etanol dengan pelarut
n-heksana 10 g Ekstrak Etanol
Dilarutkan dengan 10 ml etanol Ditambah 50 ml air suling Dimasukkan ke dalam corong pisah
Ditambahkan 50 ml n-heksana Didiamkan hingga memisah
Diuapkan dengan rotary evaporator Lapisan bawah
(etanol)
Lapisan atas (n-heksana)
Ekstrak n-heksana
TP BP
a b c d e f g
Lampiran 11. Kromatogram KLT analisis ekstrak teripang Pearsonothuria
graeffei
KLT Preparatif
Fase diam : silika gel 60 F254 F Fase gerak : n-heksana-
etilasetat (70:30)
Lampiran 12. Bagan isolasi steroid/triterpenoid dari teripang
Ekstrak n-heksana
Kromatogram
Isolat
Isolat murni
Spektrum
KLT 2 arah
Identifikasi secara spektrofotometri UV, spektrofotometri IR dan spektrofotometri MS
KLT Analisis
Lampiran 13. Kromatogram KLT preparatif teripang Pearsonothuria graeffei
Keterangan : Fase gerak n-heksana-etilasetat (70:30), fase diam silika gel 60 F254, penampak noda Liebermann-Burchard (LB), tp = titik penotolan, bp= batas penotolan
Bp
Lampiran 14. Kromatogram KLT dua arah isolat teripang Pearsonothuria
graeffei
Keterangan : Fase gerak I = n-heksana-etilasetat (70:30), fase gerak II = toluen-etilasetat (80:20), fase diam silika gel 60 F254, penampak noda Liebermann-Burchard (LB), M= merah ungu, tp = titik penotolan, bp1= batas penotolan 1, bp2 = batas penotolan 2
Bp 1
Bp 2
Lampiran 15. Spektrum UV isolat teripang Pearsonothuria graeffei
Lampiran 16. Spektrum IR Isolat teripang Pearsonothuria graeffei
Lampiran 17. Spektrum MS teripang isolat Pearsonothuria graeffei
Mariner Spec /90:92 (T /3.46:3.53) -82:84 (T -3.46:3.53) ASC= > NR(2.00)[BP = 337.3, 208]
DAFTAR PUSTAKA
Anonima. (2009). Estrone, Hexanoat. http://webbook.nist.gov/cgi/cbookcgi?ID= U368356&Units=SI. Diakses pada tanggal 29 November 2015.
Anonimb. (2009). 3 alpha, 11 beta, 17, 20 alpha, 21-Pentahidroxy. http://webbook.nist.gov/cgi/cbook.cgi?ID =C516381&Units=SI. Diakses pada tanggal 29 November 2015.
Basset, J., Denny, R.C., Jeffery, G. H., dan Mendham, J. (1994). Buku Ajar Vogel: Kimia Analisis Kuantitatif Anorganik. Jakarta: Buku Kedokteran EGC. Halaman 165.
Bintang, M. (2010). Biokimia Teknik Penelitian. Jakarta: Erlangga. Halaman 125, 148-149. 197-198.
Bordbar, S., Anwar. F., dan Saari, N., (2011) High-Value Components and Bioactive from Sea Cucumbers for Functional Food. Journal Marine
drugs. 9(1): 1761.
Day, R. A., dan Underwood, A. L. (1986). Analisis Kimia Kualitatif. Edisi Keenam. Jakarta: Penerbit Erlangga. Halaman 382.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Departemen Kesehatan RI. Halaman 300-304, 306, 321-325, 336.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Cetakan I. Jakarta: Departemen Kesehatan RI. Halaman 10-11, 14, 17.
Dharmananda. (2003). Sea Cucumber: Food and Medicine. Institute for Traditional Medicine. Oregon: Portland.
Stahl, E. (1985). Analisis Obat secara Kromatografi dan Mikroskopik. Bandung: Penerbit ITB. Halaman 6.
Fitrya., Muharni., dan Kobaywan, M., (2012). Senyawa Fenolat Dari Fraksi Etil Asetat Buah Tumbuhan Mempelas (Tetracera Indica Merr.). Jurnal
Penelitian Sains. Palembang: Universitas Sriwijaya. 15(3): 107-110.
Gusnanto A, Nugroho S G., dan Sri M. (2013). Maskulinisasi Lobster Air Tawar (Cherax Quadricarinatus) dengan Ekstrak Steroid Teripang Pasir (Holothuria Scabra) Pada Umur Larva Yang Berbeda. Seminar Nasional
Sains & Teknologi V Lembaga Penelitian. Lampung: Universitas
Lampung.
Ghufran M. H., dan Kordi K. (2010). A to Z Budi Daya Akuatik untuk Pangan,
Kosmetik dan Obat-Obatan. Yogyakarta: Lily Publisher. Halaman
Gritter, R.J., Bobbit, J.M., dan Schwirting, A.E. (1991). Pengantar Kromatografi. Edisi II. Bandung: Penerbit ITB. Halaman 14, 109, 114 – 115, 130-131. Harbourne (1987). Metode Fitokimia. Bandung: Penerbit ITB. Halaman 11,
147-149, 151.
Harmita. (2015). Analisis Fisikokimia Potensiometri dan Spektroskopi. Volume 1. Jakarta: Penerbit EGC. Halaman 76-79.
Hostettmann, K., Hostettmann, M., dan Marston, A. (1995). Cara Kromatografi
Preparatif: Penggunaan pada Isolasi Senyawa Alam. Bandung: ITB.
Halaman 9 – 11.
Hostettman, K., dan Marston, A. (1995). Saponins. UK: Cambridge University Press. Halaman 2.
Kazakevich, Y., dan Rosario L. (2007). HPLC for Pharmaceutical Scientist. New Jersey: John Willey & Sons, Inc. Halaman 289, 306-307.
Kurnia, D.H, Devi, S., Laili, S., Masturah, M., dan Evi, N.Y. (2010). Pengaruh Kecepatan Sentrifugasi Pada Proses Pemisahan Hasil Ekstrak Teripang Pasir (Holothuria Scabra) Sebagai Sumber Testosteron Alami Dan Antigen. Prosiding Seminar Nasional Teknik Kimia. Yogyakarta. Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Jakarta: UI Press. Halaman
85.
Martoyo, J.N., Aji, dan Winanto, T. (2006). Budidaya Teripang. Jakarta: Penebar Swadaya. Halaman 6-7, 9.
Meydia. (2006). Isolasi Senyawa Steroid dari Teripang Gama (Stichopus variegatus) dengan Berbagai Jenis Pelarut. Skripsi. Bogor: Institut Pertanian Bogor.
Nurjanah S., Said E.G., Syamsu K., Suprihatin., dan Riani E. (2009). Pengaruh Ekstrak Steroid Teripang Pasir (Holothuria Scabra) Terhadap Perilaku Seksual Dan Kadar Testosteron Darah Mencit (Mus musculus). Tesis. Bandung: Universitas Padjajaran.
Pavia, D.L., Lampman, G.M., dan Kriz, K.S. (2001). Introduction to
Spectroscopy: A Guide for Students of Organic Chemistry. Edisi III.
United States of America: Thomson Learning, Inc. Halaman 28 – 29. Purcell, S.W., Samyn, Y., dan Conand, C. (2012). Commercially Important Sea
Remy, M.E.P., dan Losung, F. (2013). Aktivitas Hemolitik Teripang (Bohadschia
Graeffei) dari Pantai Malalayang, Sulawesi Utara Pada Beberapa Suhu
Dan PH. Jurnal Ilmiah Sains . 13(1): 29-32.
Robinson, T. (1995). Kandungan Oganik Tumbuhan Tingkat Tinggi. Bandung: Penerbit ITB. Halaman 154.
Rohman, A., dan Ibnu, G.G. (2012). Analisis Obat secara Spektrofotometri dan
Kromatografi. Jakarta: Pustaka Pelajar. Halaman 349.
Silverstein, R.M., Bassler, G.C., dan Morrill, T.C. (1981). Spectrometric
Identification of Organic Compounds. Edisi IV. Singapore: John Wiley
& Sons. Halaman 96.
Supriyatna., Mulyono. M.W., Yoppi. I., dan Maya F.R. (2010). Prinsip Obat
Herbal: Sebuah Pengantar untuk Fitoterapi. Yogyakarta: Deepublish.
Halaman 31.
Tobing, C. N. (2015). Karakterisasi dan Uji Efek Ekstrak Etanol Teripang Jenis
Pearsonothuria graeffei (Semper) Terhadap Penurunan Kadar Glukosa
Darah Mencit yang Diinduksi Aloksan. Skripsi. Medan: Universitas Sumatera Utara.
William, H. D., dan Flemming, I. (2014). Metode Spektroskopi Dalam Kimia
Organik. Edisi 6. Jakarta: Penerbit EGC. Halaman 1-10, 33.
BAB III
METODE PENELITIAN
Metode yang digunakan adalah metode eksperimental meliputi pengumpulan hewan, identifikasi hewan, pembuatan simplisia, pemeriksaan karakterisasi simplisia, pemeriksaan golongan senyawa, pembuatan ekstrak etanol, fraksinasi n-heksana dengan metode ekstraksi cair-cair, analisis senyawa steroid/triterpenoid secara kromatografi lapis tipis (KLT) dan dilanjutkan isolasi secara KLT preparatif, isolat yang diperoleh diuji kemurniannya dengan KLT dua arah, selanjutnya terhadap isolat yang telah murni dikarakterisasi dengan menggunakan spektrofotometri ultraviolet (UV), spektrofotometri inframerah (IR) dan spektrofotometri massa (MS). Penelitian dilakukan di Laboratorium Farmakognosi dan Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara.
3.1 Alat dan Bahan
3.1.1 Alat-alat
Alat-alat yang digunakan pada penelitian ini adalah: alat-alat gelas
laboratorium, blender (Philips), botol penyemprot, cawan penguap, cawan datar,
chamber, deck glass, krus porselin, lemari pengering, mikroskop, neraca kasar (Ohaus), neraca analitik (Mettler Toledo), oven listrik (Fischer Scientific), object
glass, pipet tetes, penangas air (Yenaco), tanur, rotary evaporator, spatula,
seperangkat alat kromatografi lapis tipis, seperangkat alat destilasi, seperangkat alat
perkolasi, spektrofotometri ultraviolet (Shimadzu QP 5000), spektrofotometri
3.1.2 Bahan-bahan
Bahan-bahan yang digunakan pada penelitian ini adalah teripang. Semua bahan yang digunakan kecuali dinyatakan lain adalah berkualitas proanalisa yaitu air suling, asam asetat anhidrida, asam sulfat pekat, asam klorida pekat, etilasetat, etanol destilasi, kalium bromida, kloralhidrat, kloroform, metanol, n-heksana, plat pra lapis silika gel 60 F254 dan toluen.
3.2 Pengumpulan dan Pengolahan Teripang
3.2.1 Pengumpulan teripang
Metode pengumpulan bahan teripang dilakukan secara purposif yaitu tanpa membandingkan dengan bahan teripang yang sama dari daerah lain. Bahan yang digunakan adalah teripang yang diambil dari perairan daerah sekitar Makassar, Pulau Barrang Lompo, kota Makassar, Provinsi Sulawesi Selatan. 3.2.2 Identifikasi teripang
Identifikasi teripang dilakukan di Lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian Oseanografi Jakarta. Teripang yang digunakan sama dengan teripang yang diidentifikasi atas nama Tobing (2015). Hasil identifikasi dapat dilihat pada Lampiran 1, halaman 42.
3.2.3 Pengolahan teripang
Serbuk simplisia disimpan dalam kantung plastik untuk mencegah pengaruh lembab dan pengotoran lainnya.
3.3 Pembuatan Pereaksi
3.3.1 Pereaksi Molish
Sebanyak 3 g α-naftol P, dilarutkan dalam asam nitrat 0,5 N hingga
diperoleh larutan 100 ml (Depkes RI, 1995). 3.3.2 Larutan asam klorida 2 N
Larutan asam klorida pekat sebanyak 17 ml ditambahkan air suling
sampai 100 ml (Depkes RI, 1995). 3.3.3 Larutan asam nitrat 0,5 N
Sebanyak 3,4 ml asam nitrat pekat diencerkan dengan air suling hingga volume 100 ml (Depkes RI, 1995).
3.3.4 Larutan timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat P dilarutkan dalam air bebas karbon dioksida hingga 100 ml (Depkes RI, 1995).
3.3.5 Larutan pereaksi kloralhidrat
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 20 ml air suling (Depkes RI, 1995).
3.4 Pemeriksaan Karakteristik Simplisia
Hewan yang dikarakterisasi adalah hewan yang diambil pada waktu dan tempat yang sama, memiliki jenis yang sama serta waktu pengerjaan karakterisasi dilakukan secara bersamaan dengan Tobing, (2015). Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, pemeriksaan mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air, penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total dan penetapan kadar abu yang tidak larut dalam asam (Depkes RI, 1995).
3.4.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik terhadap teripang dilakukan dengan cara mengamati bentuk, ketebalan, diameter, permukaan tubuh. Pemeriksaan organoleptis meliputi warna, bau dan rasa dari teripang. Gambar makroskopik teripang dapat dilihat pada Lampiran 2, halaman 43.
3.4.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik terhadap serbuk simplisia teripang dilakukan dengan cara serbuk simplisia diletakkan di atas kaca objek yang telah diteteskan dengan larutan kloralhidrat dan ditutup dengan kaca penutup kemudian diamati dibawah mikroskop. Gambar mikroskopik serbuk teripang dapat dilihat pada Lampiran 3, halaman 45.
3.4.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Prosedur kerja:
1. Penjenuhan toluen
menit dan volume air pada tabung penerima dibaca dengan ketelitian 0,05 ml (WHO, 1998).
2. Penetapan kadar air simplisia
Sebanyak 5 g serbuk simplisia yang telah ditimbang seksama dimasukkan ke dalam labu alas bulat berisi toluen yang telah dijenuhkan, lalu dipanaskan hati-hati selama 15 menit, setelah toluen mendidih kecepatan tetesan diatur lebih kurang 2 tetes per detik sampai sebagian besar air terdestilasi. Kecepatan destilasi dinaikkan sampai 4 tetes per detik, setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit kemudian tabung penerima dibiarkan mendingin sampai suhu kamar, setelah air dan toluen memisah sempurna, lalu volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air. Kadar air dihitung dalam persen (WHO, 1998). Hasil perhitungan kadar air dapat dilihat pada Lampiran 4, halaman 46.
3.4.4 Penetapan kadar sari larut air
3.4.5 Penetapan kadar sari larut etanol
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu tersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam, kemudian disaring cepat untuk menghindari penguapan etanol, 20 ml filtrat diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara dan dipanaskan pada suhu 105℃ sampai bobot tetap. Kadar sari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995). Perhitungan kadar sari larut etanol dapat dilihat pada Lampiran 6, halaman 48.
3.4.6 Penetapan kadar abu total
Sebanyak 2 g serbuk simplisia yang telah digerus dan ditimbang seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus porselin kemudian dipijarkan perlahan-lahan hingga arang habis, pijaran dilakukan pada suhu 600℃, kemudian didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (WHO, 1998). Hasil perhitungan kadar abu total dapat dilihat pada Lampiran 7, halaman 49.
3.4.7 Penetapan kadar abu tidak larut asam
3.5 Pemeriksaan Senyawa pada Teripang
3.5.1 Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisia dimasukan ke dalam tabung reaksi dan ditambahkan 10 ml air suling panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik, terbentuk buih atau busa tidak kurang dari 10 menit setinggi 1-10 cm, pada penambahan 1 tetes larutan asam klorida 2 N apabila buih tidak hilang menunjukkan adanya saponin (Depkes RI, 1995).
3.5.2 Pemeriksaan steroid/triterpenoid
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml n-heksana selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap, pada sisa ditambahkan 2 tetes asam asetat anhidrida dan 1 tetes asam sulfat pekat, timbul warna ungu atau merah kemudian berubah menjadi hijau biru menunjukkan adanya steroid/triterpenoid (Harborne, 1987).
3.5.3 Pemeriksaan glikosida
3.6 Pembuatan Ekstrak
3.6.1 Pembuatan ekstrak etanol
Pembuatan ekstrak dilakukan secara perkolasi dengan menggunakan pelarut etanol 96%.
Cara kerja :
Sebanyak 350 g serbuk simplisia dimasukkan ke dalam bejana tertutup, lalu direndam dengan cairan penyari etanol selama 3 jam. Massa dimasukkan ke dalam perkolator, lalu pelarut etanol dituang secukupnya sampai terdapat selapis larutan penyari di atas serbuk sumplisia, mulut perkolator ditutup dengan plastik dan aluminium foil dan dibiarkan selama 24 jam. Kran perkolator dibuka setelah 24 jam dan cairan perkolat dibiarkan menetes 1 ml/menit. Perkolasi dihentikan apabila sebanyak 500 mg cairan perkolat diuapkan di atas penangas air tidak meninggalkan sisa. Perkolat diuapkan dengan menggunakan rotary evaporator pada suhu tidak lebih dari 40o C. Bagan alur pembuatan ekstrak teripang dapat dilihat pada Lampiran 9, halaman 51.
3.6.2 Fraksinasi dengan n-heksana
Dilakukan dengan metode ekstraksi cair-cair (ECC) ekstrak etanol dengan pelarut n-heksana.
Cara kerja:
3.7 Analisis Ekstrak Teripang secara Kromatografi Lapis Tipis (KLT)
Ekstrak n-heksana dianalisis secara KLT menggunakan plat pra lapis tipis silika gel 60 F
254, dan sebagai fase gerak digunakan campuran n-heksana-etilasetat dengan perbandingan (100:0), (90:10), (80:20), (70:30), (60:40), (50:50) dan (40:60) serta sebagai penampak bercak digunakan pereaksi Libermann-Burchard. Cara kerja :
Ekstrak diencerkan dengan n-heksana, ditotolkan pada plat pra lapis tipis silika gel 60 F
254, dimasukkan ke dalam bejana yang telah jenuh dengan uap fase gerak dan ditutup rapat. Plat dikeluarkan dari bejana setelah elusi selesai dan diamati secara visual, lalu disemprot dengan pereaksi Libermann-Burchard, plat dipanaskan di oven pada suhu 1050 C selama 10 menit, diamati kembali warna bercak dan dihitung harga Rf. Hasil analisis KLT senyawa steroid/triterpenoid ekstrak n-heksana dapat dilihat pada Lampiran 11, halaman 53.
3.8 Isolasi Senyawa Steroid/Triterpenoid secara KLT Preparatif
Ekstrak n-heksana teripang diisolasi secara KLT preparatif, sebagai
penampak bercak digunakan pereaksi Liebermann-Burchard dan sebagai fase gerak
digunakan n-heksana-etilasetat (70:30) dan fase diam silika gel 60 F254.
Cara kerja:
Ekstrak diencerkan dengan n-heksana, ditotolkan berupa pita pada jarak 2 cm dari tepi bawah plat KLT berukuran 20x20 cm yang telah diaktifkan, setelah
kering plat KLT dimasukkan ke dalam bejana yang telah jenuh dengan uap fase
gerak, pengembang dibiarkan naik membawa komponen yang ada, setelah mencapai
batas pengembangan plat dikeluarkan dari bejana lalu dikeringkan. Bagian tengah
disemprot dengan penampak bercak Liebermann-Burchard kemudian dikeringkan
dalam oven pada suhu 105℃. Bagian tengah plat yang sejajar dengan bercak
berwarna merah ungu dikerok dan dikumpulkan, direndam dengan metanol satu
malam lalu disaring kemudian pelarutnya diuapkan, dilakukan uji kemurnian dengan
KLT terhadap isolat yang diperoleh. Bagan isolasi steroid/triterpenoid secara KLT
preparatif dapat dilihat pada Lampiran 12, halaman 54. Gambar hasil KLT preparatif
dapat dilihat pada Lampiran 13, halaman 55.
3.9 Uji Kemurnian Isolat secara KLT Dua Arah
Isolat hasil isolasi dilakukan uji kemurnian secara KLT dua arah menggunakan dua sistem pengembang yang berbeda kepolaran. Fase gerak I n-heksana-etilasetat (70:30) dan fase gerak II toluen-etilasetat (80:20).
Cara kerja:
Isolat ditotolkan pada plat pra lapis silika gel 60 F254 lalu dielusi memakai fase gerak I yaitu n-heksana-etilasetat (70:30) hingga mencapai batas pengembangan, kemudian plat dikeluarkan dari dalam bejana dan dikeringkan, setelah plat kering dielusi kembali dengan arah yang berbeda 90℃ memakai fase gerak II yaitu toluen-etilasetat (80:20), disemprot dengan memakai penampak bercak Liebermann-Burchard, setelah itu plat dipanaskan pada suhu 105℃ selama 10 menit lalu diamati warna yang terbentuk. Hasil uji kemurnian isolat dapat dilihat pada Lampiran 14, halaman 56.
3.10 Karakterisasi Isolat
Lembaga Ilmu Pengetahuan Indonesia (LIPI) Kimia, Serpong, Provinsi Banten. 3.10.1 Karakterisasi isolat secara spektrofotometri UV
Cara kerja:
Karakterisasi isolat secara spektrofotometri UV dilakukan dengan cara
melarutkan isolat dengan metanol kemudian dimasukkan kedalam kuvet yang telah
dibilas dengan larutan sampel dan diukur panjang gelombang maksimumnya pada
panjang gelombang 200–400 nm. Hasil karakterisasi isolat dengan spektrofotometri UV dapat dilihat pada Lampiran 15, halaman 57.
3.10.2 Karakterisasi isolat secara spektrofotometri IR
Cara kerja:
Karakterisasi isolat secara spektrofotometri IR dilakukan dengan cara mencampurkan isolat dengan 100 mg kalium bromida kemudian dimasukkan ke dalam cell holder spektrofotometri inframerah serta diukur pada bilangan gelombang 400-4000 cm-1. Hasil karakterisasi isolat dengan spektrofotometri IR dapat dilihat pada Lampiran 16, halaman 58.
3.10.3 Karakterisasi isolat secara spektrofotometer massa (MS)
Cara kerja:
Karakterisasi isolat dilakukan secara kromatografi cair-spektrofotometri massa dengan cara melarut isolat dengan metanol kemudian diinjeksikan ke dalam alat mass spectra (Lc-Ms). Analisis dilakukan dengan sistem electrospray
ionization, kemudian dibaca hasil dari Lc-MS. Hasil spektrofotomer massa dapat
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Teripang
Hasil identifikasi teripang yang dilakukan di Lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian Oseanografi Jakarta adalah teripang jenis
Pearsonothuria graffei (Semper, 1868), marga Pearsonothuria, suku Holothuriidae, bangsa Aspidochirotida, kelas Holothuroidea dan filum Echinodermata (Tobing, 2015).
4.2 Hasil Karakterisasi Simplisia
Secara makroskopis, tubuh teripang segar berbentuk lonjong menyerupai bentuk timun dengan panjang sekitar 65 cm dengan lebar 10 cm, dengan mulut pada salah satu ujungnya dan anus pada ujung lainnya. Tubuhnya lunak dan berlendir, permukaan tubuhnya berwarna coklat dengan bintik-bintik berwarna hitam. Diameter tubuh bagian tengah lebih besar dari bagian ujungnya, yaitu bagian mulut dan anus.
Pemeriksaan makroskopis terhadap simplisia yaitu simplisia berwarna lebih pucat dan mengkerut. Pemeriksaan organoleptis terhadap teripang segar yaitu berbau spesifik sedangkan serbuk simplisia berwarna cream, rasa asin, dan berbau spesifik.
(pseudo-tables) yang berasal dari dinding tubuh.
Hasil pemeriksaan karakteristik teripang yang diperoleh dari hasil pemeriksaan yang dilakukan oleh Tobing, (2015) dapat dilihat pada Tabel 4.1 berikut ini:
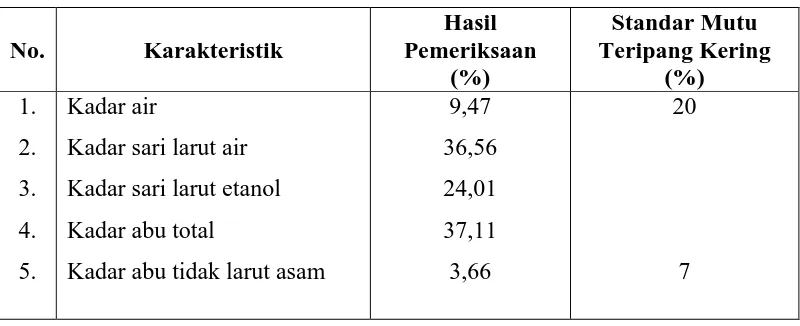
Tabel 4.1 Hasil pemeriksaan karakteristik simplisia Pearsonothuria graffei
No. Karakteristik
Penetapan kadar air dilakukan dengan metode azeotropi (destilasi toluen), penetapan kadar sari larut air dan kadar sari larut etanol, kadar abu total dan abu tidak larut asam dilakukan menggunakan metode gravimetri. Tabel 4.1 menunjukkan kadar air simplisia teripang sebesar 9,47%. Berdasarkan standar mutu teripang kering yaitu (SPI-KAN/02/29/1987) sesuai surat Keputusan Menteri RI no.701/Kpts/TP.830/10/1987 yang tercantum pada Tabel 4.1 kadar air dari teripang kering tidak lebih dari 20%, sehingga kadar air dari simplisia
Pearsonothuria graeffei (Semper, 1868) memenuhi persyaratan.
Kadar air yang lebih besar dari 10% dapat menjadi media pertumbuhan kapang dan jasad renik lainnya. Tujuan dari penetapan kadar air adalah untuk memberikan batasan minimal atau rentang tentang besarnya kandungan air di dalam bahan (Depkes RI, 2000).
Kadar sari larut air yaitu 36,56% hal ini menunjukkan bahwa teripang
seperti saponin dan garam. Kadar sari larut etanol yaitu 24,01% menunjukkan adanya senyawa yang dapat larut etanol seperti steroid/triterpenoid, gikosida, lemak dan kolagen.
Kadar abu total yaitu 28,75% menunjukkan bahwa kadar abu teripang tinggi, disebabkan karena teripang mengandung berbagai mineral seperti garam dan kalsium karbonat dari spikula (Bodrbar, dkk., 2011). Tujuan dari penetapan kadar abu total adalah memberikan gambaran kandungan mineral internal dan eksternal yang berasal dari proses awal sampai terbentuknya ekstrak (Depkes RI, 2000). Kadar abu tidak larut asam yaitu 3,66% yang termasuk dalam abu tidak larut asam adalah silikat. Kadar abu tidak larut asam juga memenuhi persyaratan mutu teripang kering yaitu (SPI-KAN/ 02/29/1987) sesuai surat Keputusan Menteri Pertanian RI No. 701/Kpts/TP.830/10/1987.
4.3 Hasil Pemeriksaan Golongan Senyawa
Hasil pemeriksaan golongan senyawa terhadap serbuk simplisia teripang dapat dilihat pada Tabel 4.2 sebagai berikut:
Tabel 4.2 Hasil pemeriksaan golongan senyawa teripang Pearsonothuria graeffei
Keterangan: (+) Positif : mengandung golongan senyawa () Negatif : tidak mengandung golongan senyawa
Hasil pemeriksaan golongan senyawa terhadap serbuk simplisia, ekstrak etanol dan fraksi n-heksana teripang Pearsonothuria graeffei diperoleh pada
Tabel 4.2 menunjukkan bahwa serbuk simplisia dan ekstrak etanol mengandung saponin, karena pada uji busa terbentuk busa yang stabil melalui pengocokkan dengan air panas dan tidak hilang dengan penambahan HCl 2 N. Serbuk simplisia dan esktrak etanol teripang positif mengandung glikosida, pada penambahan pereaksi Molish dan asam sulfat pekat terbentuk cincin ungu (Depkes RI, 1995). Ketiganya positif mengandung steroid/triterpenoid yang berwarna biru-hijau hingga merah ungu setelah penambahan pereaksi Liebermann-Burchard (Robinson, 1995).
4.4 Ekstraksi
Sejumlah 350 g serbuk simplisia diekstrasi dengan cara perkolasi menggunakan pelarut etanol 96% sehingga diperoleh ekstrak etanol sebanyak 22,4 g. Fraksinasi ekstrak etanol dilakukan menggunakan metode ekstraksi cair-cair dengan pelarut n-heksana sehingga diperoleh ekstrak n-heksana sebanyak 2,06 g.
4.5 Isolasi Senyawa Steroid/Triterpenoid
Analisis KLT dari ekstrak heksana dilakukan dengan fase gerak n-heksana:etilasetat dengan perbandingan (100:0), (90:10), (80:20), (70:30), (60:40), (50:50), (40:60) menunjukkan bahwa fase gerak yang paling baik adalah
n-heksana-etilasetat (70:30) karena menghasilkan pemisahan noda yang paling
baik yaitu diperoleh dua noda yang berwarna merah ungu dengan penampak noda Liebermann-Burchard.
pada kedua sisi plat memberikan dua bercak berwarna merah ungu kemudian keduanya dikerok pada bagian plat yang tidak disemprot lalu direndam dengan metanol dingin selama satu malam kemudian disaring sehingga diperoleh filtrat.
Filtrat yang diperoleh dari kedua bercak diuapkan hingga kering, setelah itu ditambahkan metanol dan dimasukkan ke dalam lemari pendingin selama satu malam. Filtrat dikeluarkan dari lemari pendingin setelah satu malam dan dibiarkan menguap. Perlakuan diulangi beberapa kali sampai terbentuk kristal. Kristal yang terbentuk dari kedua filtrat yaitu isolat 1 berupa kristal amorf berwarna putih kekuningan sebanyak 11,56 mg sedangkan pada isolat 2 kristal yang terbentuk sangat sedikit sehingga tidak dilakukan uji selanjutnya.
Uji kemurnian isolat dilakukan secara KLT dua arah menggunakan dua sistem pengembang yang berbeda kepolaran. Fase gerak pertama yang digunakan adalah n-heksana-etilasetat (70:30) yang bersifat lebih non-polar dari fase gerak kedua yaitu toluen-etilasetat (80:20). Hasil KLT dua arah menunjukkan isolat memiliki satu noda dengan harga Rf 0,51. Hasil ini menunjukkan bahwa senyawa steroid/triterpenoid yang diperoleh dianggap murni.
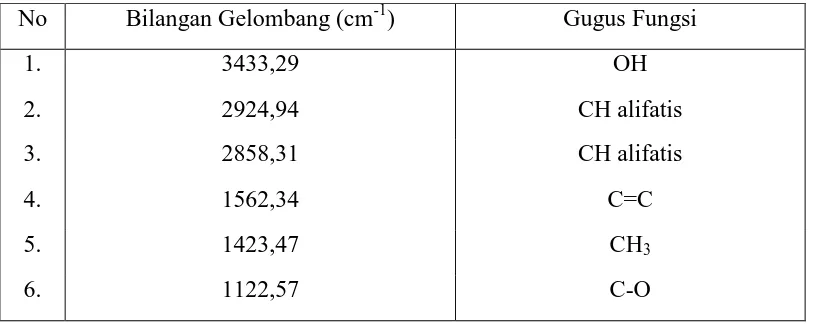
cm-1 dan 2858,51 cm-1 menunjukkan adanya gugus C–H alifatis, yang diperkuat oleh pita serapan pada bilangan gelombang 1423,47 cm-1 yang menunjukkan adanya gugus metil (–CH3). Pita serapan pada bilangan gelombang 1562,34 cm-1 menunjukkan adanya ikatan rangkap dua C=C (Harmita, 2015). Hasil identifikasi dengan spektrofotometer dapat dilihat pada Tabel 4.3 di bawah ini.
Tabel 4.3 Hasil identifikasi spektrum inframerah isolat
No Bilangan Gelombang (cm-1) Gugus Fungsi
1. 3433,29 OH
1. Estrone, Hexanoat
Gambar 4.1 Struktur Estrone, Hexanoat (Anonima, 2009)
2. 3 alpha, 11 beta, 17, 20 alpha, 21-Pentahydroxypregnane
Gambar 4.2 Struktur 3 alpha, 11 beta, 17, 20 alpha, 21-Pentahydroxypregnane
(Anonimb, 2009)
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Hasil pemeriksaan makroskopis menunjukkan teripang segar memiliki bentuk tubuh lonjong dengan panjang sekitar 65 cm, lebar 10 cm, lunak dan berlendir, warna permukaan tubuhnya coklat dengan bintik-bintik berwarna hitam, sedangkan pada simplisia berwarna lebih pucat dan mengkerut. Hasil mikroskopis menunjukkan teripang terdiri dari spikula bentuk kancing (button), meja semu (pseudo table), dan batang (rods). Karakteristik simplisia hewan yaitu kadar air 9,47%, kadar sari larut air 36,56%, kadar sari larut etanol 24,01%, kadar abu total 28,75%, kadar abu tidak larut asam 3,66%.
b. Senyawa steroid/triterpenoid teripang Pearsonothuria graeffei (Semper, 1868) terpisah dengan baik menggunakan metode ekstraksi cair-cair dan KLT preparatif.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Hewan
Teripang adalah salah satu hewan berkulit duri atau berbintil (Echinodermata). Tidak semua teripang memiliki duri atau bintil pada permukaan tubuhnya. Tubuh teripang umumnya berbentuk bulat panjang atau silindris sekitar 10-30 cm dengan mulut pada salah satu ujungnya dan anus pada ujung yang lainnya. Bentuk umum teripang tersebut menyerupai mentimun sehingga teripang dikenal dengan nama sea cucumber atau ketimun laut. Warna tubuh teripang bermacam-macam, ada yang hitam pekat, cokelat, bergaris-garis dan mempunyai bercak-bercak pada permukaan tubuhnya. Gerakan teripang sangat lamban sehingga hampir seluruh hidupnya berada di dasar laut. Sebagai bentuk perlindungan diri dari pemangsa, teripang dapat mengeluarkan lendir yang beracun dari tubuhnya seperti pada jenis teripang getah (Holothuria vacabunda) (Ghufran dan Kordi, 2010).
2.1.1 Sistematika hewan
Identifikasi sampel teripang dilakukan di Lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian Oseanografi dengan hasil sebagai berikut: Filum : Echinodermata
Kelas : Holothuroidea Bangsa : Aspidochirotida Suku : Holothuriidae Marga : Pearsonothuria
2.1.2 Habitat
Teripang ditemukan hampir diseluruh perairan, dari daerah perairan yang dangkal hingga bagian yang dalam. Teripang yang telah dewasa biasanya berada di daerah dasar laut atau bisa juga ditemukan hidup daerah bebatuan dan terumbu karang (Purcell, dkk., 2012).
Umumnya masing-masing jenis teripang memiliki habitat yang spesifik, misalnya teripang putih banyak ditemukan di daerah yang berpasir atau pasir bercampur lumpur dengan kedalaman 1-40 m. Teripang putih juga sering ditemukan di perairan yang dangkal dan banyak ditumbuhi rumput laut. Teripang kapuk dan teripang pasir banyak ditemukan di daerah terumbu karang, sementara teripang koro dan teripang pandan banyak ditemukan di perairan yang lebih dalam. Hewan ini dalam habitatnya teripang hidup secara berkelompok dengan cara membentuk kelompok yang terdiri dari 3-30 ekor teripang dan ada pula yang hidup sendiri (Martoyo, dkk., 2006).
2.1.3 Morfologi
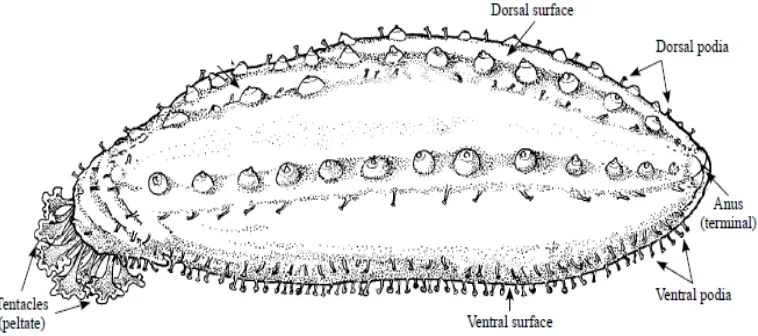
dengan tentakel atau dengan menelan pasir dan kemudian menangkap sumber makanannya yang terkandung di dalamnya. Bentuk tubuh teripang dapat dilihat pada Gambar 2.1 dibawah ini:
Gambar 2.1 Morfologi tubuh teripang (Purcell, dkk., 2012)
Teripang mempunyai tulang-tulang berukuran mikroskopis yang dikenal sebagai "spikula". Bentuk spikula bervariasi dan karakteristik untuk setiap jenis (spesies), sehingga spikula sangat penting dan menentukan dalam klasifikasi maupun identifikasi. Variasi bentuk spikula bermacam-macam, seperti bentuk batang, kancing, roset, jangkar dan meja (Purcell, dkk., 2012).
2.2 Uraian Kandungan Kimia Hewan
2.2.1. Saponin
Saponin adalah senyawa aktif permukaan yang kuat dan bersifat sepeti sabun, memiliki kemampuan menimbulkan busa jika dikocok dalam air dan pada konsentrasi yang rendah sering menyebabkan hemolisis sel darah merah (Harborne, 1987).
genin atau sapogenin. Berdasarkan aglikonnya saponin dibagi menjadi tiga kelas utama, yaitu:
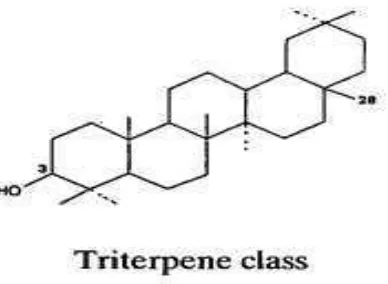
a. aglikon triterpenoid
Gambar 2.2 Struktur aglikon triterpenoid
b. aglikon steroid
Gambar 2.3 Struktur aglikon steroid
c. aglikon steroid alkaloid
2.2.2. Glikosida
Glikosida merupakan senyawa terdiri atas dua bagian yaitu molekul gula (glikon) dan aglikon. Gugus gula bisa berikatan dengan aglikon dengan berbagai cara. Paling umum dijembatani oleh atom oksigen (O-glikosida), tetapi bisa juga dijembatani oleh sulfur (S-glikosida), juga oleh atom nitrogen (N-glikosida) dan atom karbon (C-glikosida). Glikosida umumnya cukup larut dalam air dan alkohol tetapi sedikit larut dalam eter. Ikatan glikosidik resisten terhadap hidrolisis oleh alkali tetapi mudah pecah oleh asam mineral encer seperti asam sulfat encer (Supriyatna, dkk., 2015).
2.2.3. Steroid/triterpenoid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam satuan isoprena dan secara biosintesis masuk jalur asam mevalonat diturunkan dari hidrokarbon C30 asiklik, yaitu skualena. Triterpenoid berupa senyawa tanpa warna berbentuk kristal, sering kali bertitik leleh tinggi. Triterpenoid dibagi menjadi empat golongan, yaitu triterpen, steroid, saponin dan glikosida jantung. Uji yang banyak dilakukan untuk identifikasi triterpenoid dan steroid adalah reaksi Liebermann-Burchard yang biasanya menghasilkan warna merah ungu hingga biru-hijau. Triterpenoid memiliki aktivitas sebagai antibakteri, antifungi (Harborne, 1987).
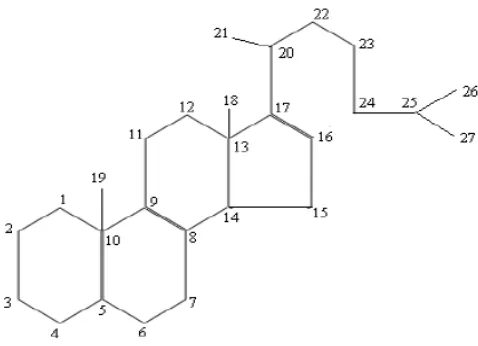
Kerangka dasar dan sistem penomoran steroid menurut Robinson (1995), dapat dilihat pada Gambar 2.5 dibawah ini:
Gambar 2.5 Sistem penomoran steroid
2.3 Ekstraksi
Ekstraksi adalah suatu proses pemisahan satu atau lebih zat dari bahan asal dengan menggunakan pelarut. Umumnya zat berkhasiat tersebut dapat ditarik, namun khasiatnya tidak berubah. Tujuan utama ekstraksi adalah mendapatkan atau memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan dari zat-zat yang tidak dibutuhkan, agar lebih mudah digunakan (kemudahan diabsorpsi, rasa dan pemakaian) dan disimpan dibandingkan simplisia asal dan tujuan pengobatannya terjamin (Depkes RI, 1995).
Ekstraksi dengan menggunakan pelarut dapat dilakukan dengan beberapa cara yaitu:
a. Cara dingin 1. Maserasi
pengadukkan pada temperatur kamar. Maserasi yang dilakukan pengadukan secara terus-menerus disebut maserasi kinetik sedangkan penambahan ulang pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi (Depkes RI, 2000).
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar (Depkes RI, 2000).
b. Cara panas 1. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik (Depkes RI, 2000).
2. Sokletasi
Sokletasi adalah ekstraksi dengan pelarut yang umumnya menggunakan alat khusus (soklet) sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dan dengan adanya pendingin balik (Depkes RI, 2000).
3. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur yang lebih tinggi dari temperatur ruangan yaitu secara umum dilakukan pada temperatur 40-50o C (Depkes RI, 2000).
4. Infundasi
5. Dekoktasi
Dekoksi adalah ekstraksi dengan pelarut air pada temperatur 90o C selama 30 menit (Depkes RI, 2000).
2.4 Ekstraksi Cair-Cair
Ekstraksi cairan-cairan merupakan suatu teknik pemisahan atau pengambilan zat dalam suatu larutan menggunakan pelarut lain (biasanya pelarut organik) yang tidak tercampurkan. Pemisahan yang dilakukan, bersifat sederhana, bersih, cepat dan mudah. Pemisahan dapat dilakukan dengan mengocok-ngocok dalam sebuah corong pemisah selama beberapa waktu hingga terbentuk dua lapisan (Basset, dkk., 1994).
Prinsip metode ini didasarkan pada distribusi zat terlarut dengan perbandingan tertentu antara dua pelarut yang tidak saling bercampur seperti benzena, karbon tetraklorida atau kloroform. Teknik ini dapat digunakan untuk kegunaan preparatif, pemurnian, memperkaya, pemisahan serta analisis (Khopkar, 1990).
2.5 Kromatografi
Kromatografi merupakan suatu untuk memisahkan suatu senyawa yang terdistribusi antara dua fase, yaitu fase gerak yang membawa sampel dan fase diam yang menahan sampel. Pemisahan dan pemurnian suatu bahan dapat dilakukan menggunakan salah satu dari teknik kromatografi yang ada. Pemilihan teknik kromatografi sebagian besar tergantung pada sifat kelarutan dan keatsirian senyawa yang akan dipisah (Bintang, 2010).
dengan senyawa murni. Kromatografi juga dapat menunjukkan jumlah minimum komponen yang ada dalam campuran (Gritter, dkk., 1991).
2.5.1 Kromatografi lapis tipis
Kromatografi lapis tipis termasuk kromatografi adsorpsi. Fase diam pada kromatografi lapis tipis berupa lapisan tipis yang terdiri dari bahan padat yang dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca atau logam. Fase gerak pada kromatografi lapis tipis adalah zat cair yang disebut larutan pengembang (Gritter, dkk., 1991).
Campuran yang akan dikromatografi harus dilarutkan terlebih dahulu dalam pelarut yang sesuai. Hampir segala macam pelarut dapat dipakai, tetapi yang terbaik adalah yang bertitik didih antara 50o hingga 100o C agar mudah menguap dari lapisan (Gritter, dkk., 1991). Cuplikan ditotolkan berupa pita yang harus sesempit mungkin karena pemisahan berdasarkan pita. Penotolan dapat dilakukan dengan kapiler halus atau dengan penotol otomatis. Plat dielusi dengan pelarut yang diinginkan dan setelah elusi selesai disemprot dengan penampak bercak (Hostettman, dkk., 1995).
a. Fase diam
untuk mengikat lapisan pada lempeng (Bintang, 2010). b. Fase gerak
Fase gerak ialah medium angkut dan terdiri dari satu atau beberapa pelarut. Pemilihan sistem pelarut yang dipakai didasarkan atas prinsip like
dissolves like yaitu untuk memisahkan sampel yang bersifat non polar digunakan
sistem pelarut yang bersifat non polar dan untuk memisahkan pelarut sampel yang bersifat polar digunakan sistem pelarut yang bersifat polar (Stahl, 1985).
c. Harga Rf
Identifikasi bercak komponen dilakukan dengan menghitung harga
Retardation Factor (Rf) sebagai derajat retensi, yang didefinisikan sebagai jarak
yang ditempuh senyawa pada kromatografi dari tempat totolan terhadap jarak tempuh pelarut atau dapat dituliskan sebagai berikut:
Faktor yang mempengaruhi harga Rf antara lain adalah suhu, pelarut, sifat penjerap dan jumlah cuplikan (Bintang, 2010).
2.5.2 Kromatografi lapis tipis preparatif
dengan cara menutup plat dengan sepotong kaca lalu menyemprot kedua sisi dengan pereaksi semprot (Hostettman, dkk., 1995).
2.5.3 Kromatografi lapis tipis dua arah
Kromatografi lapis tipis (KLT) dua arah bertujuan untuk meningkatkan resolusi sampel ketika komponen-komponen mempunyai karakteristik kimia yang hampir sama, karena nilai Rf juga hampir sama. Dua sistem fase gerak yang sangat berbeda dapat digunakan secara berurutan pada suatu campuran tertentu, sehingga memungkinkan untuk melakukan pemisahan analit yang mempunyai tingkat polaritas yang hampir sama, sehingga KLT dua arah dapat dipakai untuk memeriksa kemurnian isolat (Rohman dan Ibnu, 2012).
KLT dua dimensi dilakukan dengan menotolkan sampel pada satu sudut lapisan berbentuk bujur sangkar dan dikembang dengan satu sistem pelarut sehingga campuran terpisah menurut jalur yang sejajar dengan salah satu sisi. Plat diangkat, dikeringkan, diputar 90 derajat, lalu diletakkan di dalam sistem pelarut kedua (Gritter, dkk., 1991).
2.6 Spektrofotometri
2.6.1. Spektrofotometri sinar ultraviolet
Spektrofotometri dapat dianggap sebagai perluasan pemeriksaan visual, yaitu dengan menggunakan alat untuk mengukur absorbsi energi radiasi macam-macam zat kimia dan memungkinkan dilakukannya pengukuran kualitatif dari suatu zat dengan ketelitian yang lebih besar (Day dan Underwood, 1986).
gelombang. Panjang gelombang serapan merupakan suatu ukuran perbedaan tingkat-tingkat energi pada orbital-orbital yang tereksitasi (William dan Flemming, 2014).
2.6.2 Spektrofotometri sinar inframerah
Spektrofotometri sinar inframerah digunakan untuk mengidentifikasi senyawa organik. Pengukuran spektrum inframerah paling banyak dilakukan pada daerah bilangan gelombang 4000-400 cm-1 (Bintang, 2010). Spektrum inframerah terjadi akibat adanya berbagai transisi antara tingkat-tingkat energi vibrasi yang dihasilkan oleh gugus fungsional (William dan Flemming, 2014).
Langkah-langkah umum untuk memeriksa spektrum inframerah menurut Pavia, dkk (2001) adalah:
1. apakah terdapat gugus karbonil?
Gugus C=O memberikan puncak pada daerah 1660-1820 cm-1. Puncak ini biasanya memiliki puncak yang lebar pada spektrum.
2. jika gugus C=O ada, periksalah gugus-gugus berikut: a. Asam: memiliki serapan melebar pada 2500-3000 cm-1.
b. Amida: memiliki serapan medium di dekat 3500 cm-1. Kadang-kadang puncak rangkap
c. Ester: memiliki serapan medium di daerah 1000-1300 cm-1.
d. Anhidrida: mempunyai dua serapan C=O di daerah 1810 dan 1760 cm-1. e. Aldehida: mempunyai dua serapan lemah di dekat 2850-275- cm-1. f. Keton: jika kelima kemungkinan di atas tidak ada.
3. jika gugus C=O tidak ada
b. Amina: memiliki gugus N-H, yaitu serapan medium di daerah 3500cm-1 c. Eter: memiliki gugus C-O (tidak ada -OH), yaitu serapan medium di daerah
1000-1300 cm-1.
4. Ikatan rangkap dua atau cincin aromatik
a. Ikatan C=C mempunyai serapan lemah di daerah 1650 cm-1.
b. Serapan medium sampai kuat pada daerah 1450-1650 cm-1 sering menunjukkan adanya cincin aromatik.
5. Ikatan rangkap tiga
a. C N mempunyai serapan lemah di daerah 1650 cm-1. b. C C mempunyai serapan tapi tajam di daerah 2150 cm-1. 6. Hidrokarbon
a. Kelima kemungkinan diatas tidak ada.
b. Serapan utama di daerah CH dekat 3000 cm-1. c. Serapan lain di daerah 1375-1450 cm-1. 2.6.3 Spektrofotometri massa
Spektrofotometer massa merupakan perangkat untuk menghasilkan dan menghitung berat ion suatu senyawa yang berat molekul dan informasi struktur yang ingin diketahui. Semua spektrofotometri massa menggunakan tiga tahapan dasar, yaitu molekul dibuat menjadi fase gas, lalu ditembakkan berkas elektron dan menghasilkan ion bermuatan positif seperti kation M.+ kemudian ion-ion dipisahkan berdasarkan rasio massa terhadap muatannya (m/z) (William dan Fleming, 2014).
Salah satu sistem dari spektrofotometri massa yaitu Electrospray Mass
Spectrometry (ESI). Istilah electrospray adalah istilah yang diterapkan untuk
meninggalkan kapiler berupa kabut halus dan terdiri dari tetesan cairan bermuatan tinggi, yang dapat ditentukan sebagai muatan positif atau negatif sesuai dengan tegangan yang diterapkan pada pipa kapiler (William dan Fleming, 2014).
Keuntungan utama spektrofotometri massa yaitu metode ini lebih spesifik dan sensitif untuk identifikasi senyawa yang tidak diketahui atau untuk menetapkan keberadaan senyawa tertentu. Hal ini karena spektrofotometri massa dapat memberikan informasi mengenai bobot molekul dan rumus molekul berdasarkan pola fragmentasi. Puncak ion molekul penting dikenali karena memberikan bobot molekul senyawa yang diperiksa (Silverstain, dkk., 1981).
BAB I
PENDAHULUAN
1.1Latar Belakang
Teripang atau timun laut termasuk dalam filum Echinodermata merupakan
salah satu komoditas laut yang banyak ditemukan di perairan Indonesia. Hal ini karena kondisi alam dan iklim Indonesia tidak banyak mengalami perubahan sepanjang tahun sehingga sangat memungkinkan memiliki banyak jenis biota akuatik. Komoditas ini memiliki prospek yang cukup baik dan bernilai tinggi, baik di pasar lokal maupun internasional karena memiliki kandungan nutrisi yang tinggi. Hewan ini dikenal pula dengan nama ketimun laut (holothuria) sea
cucumber (Inggris), bech-de-mer (Prancis), atau dalam istilah pasar internasional
dikenal dengan nama teat fish (Ghufran dan Kordi, 2010).
Daerah penyebaran teripang yaitu perairan Madura, Bali, Lombok, Aceh, Bengkulu, Bangka, Kalimantan, Sulawesi, NTT, NTB, dan kepulauan Seribu dan umumnya ditemukan pada daerah dangkal hingga 40 m. Teripang dipasarkan dalam bentuk produk yang bermacam-macam, misalnya teripang kering
(beche-de-mer), teripang kaleng dan kerupuk teripang. Teripang selain dikonsumsi juga
digunakan sebagai obat tradisional seperti untuk menyembuhkan luka dan mengatasi gangguan pencernaan oleh masyarakat yang tinggal di daerah pantai (Martoyo, dkk., 2006).
kolagen. Teripang juga mengandung beberapa senyawa metabolit sekunder yaitu saponin, steroid/triterpenoid, dan glikosida (Meydia, 2006). Senyawa metabolit sekunder yang menjadi objek utama dalam penelitian ini adalah steroid/triterpenoid yang memiliki efek sebagai aprodisiaka alami, antibakteri dan antifungi (Kurnia, dkk., 2010).
Penelitian yang telah dilakukan membuktikan bahwa teripang memiliki beberapa zat aktif yang bermanfaat bagi kesehatan. Dharmananda mengatakan teripang kaya akan saponin, terutama triterpenoid glikosida. Senyawa ini mempunyai aktivitas sebagaimana tonik yang berasal dari ginseng, ganoderma dan tumbuhan. Secara farmakologis, saponin menunjukkan aktivitas sebagai anti-inflamasi dan antikanker (Dharmananda, 2003). Penelitian Nurjanah melaporkan adanya tepung teripang memiliki efek aprodisiaka yang diuji coba pada mencit (Nurjanah, dkk., 2009).
Gusnanto melaporkan ekstrak teripang dapat digunakan untuk maskulinasi lobster air tawar dengan teknik sex reversal. Sex reversal merupakan teknik pembalikan arah perkembangan kelamin yang seharusnya berkelamin betina menjadi jantan atau sebaliknya (Gusnanto, 2013). Penelitian Remy dkk, melaporkan teripang jenis Bohadschia graffei memiliki aktivitas hemolitik (Remy, dkk., 2013).
Hewan yang digunakan untuk penelitian ini adalah teripang yang diperoleh di perairan pulau Barrang Lompo, kota Makassar, provinsi Sulawesi Selatan. Hal ini karena perairan Makassar terdapat banyak jenis teripang alami maupun budidaya serta memiliki harga yang lebih ekonomis.
1.2Perumusan Masalah
Berdasarkan uraian di atas, maka perumusan masalah dalam penelitian ini
dapat dirumuskan sebagai berikut :
a. apakah karakteristik serbuk simplisia teripang Pearsonothuria graeffei (Semper, 1868) memenuhi persyaratan mutu secara umum?
b. apakah senyawa steroid/triterpenoid teripang Pearsonothuria graeffei (Semper, 1868) dapat dipisahkan dengan baik melalui metode ekstraksi cair-cair dan dilanjutkan dengan KLT preparatif?
c. apakah isolat mempunyai panjang gelombang dan gugus fungsi yang mendukung adanya senyawa steroid/triterpenoid setelah dianalisis secara spektrofotometri ultraviolet (UV), spektrofotometri inframerah (IR) dan spektrofotometri massa?
1.3Hipotesis
Berdasarkan rumusan masalah di atas, maka hipotesis dari penelitian ini
sebagai berikut :
a. karakteristik simplisia teripang Pearsonothuria graeffei (Semper, 1868) memenuhi persyaratan mutu secara umum.
b. senyawa steroid/triterpenoid teripang Pearsnothuria graeffei (Semper, 1868) dapat dipisahkan dengan baik menggunakan metode ekstraksi cair-cair dan dilanjutkan secara KLT preparatif.
1.4Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah :
a. untuk mengetahui karakteristik simplisia teripang Pearsonothuria graeffei (Semper, 1868) memenuhi persyaratan mutu secara umum.
b. untuk mengetahui hasil pemisahan senyawa steroid/triterpenoid teripang
Pearsonothuria graeffei (Semper, 1868) dengan ekstraksi cair-cair dan KLT preparatif.
c. untuk mengetahui panjang gelombang dan gugus fungsi senyawa steroid/triterpenoid hasil isolasi secara spektrofotometri ultraviolet (UV), spektrofotometri inframerah (IR) dan spektrofotometri massa.
1.5Manfaat Penelitian.
ISOLASI SENYAWA STEROID/TRITERPENOID DARI EKSTRAK ETANOL FRAKSI n-HEKSANA TERIPANG
Pearsonothuria graeffei
ABSTRAK
Teripang adalah salah satu komoditas hasil laut yang banyak terdapat di perairan Indonesia tetapi belum banyak dieksplorasi manfaat kandungannya. Kandungan metabolit sekunder utama dari teripang adalah steroid/triterpenoid, saponin, dan glikosida yang memiliki aktivitas biologi yang baik sehingga dapat dikembangkan dalam berbagai bidang pengobatan. Penelitian ini bertujuan untuk mengetahui karakterisasi simplisia dan isolasi steroid/triterpenoid dari teripang.
Pemeriksaan karakteristik simplisia hewan meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari larut air, penetapan kadar sari larut etanol, penetapan kadar abu total, dan penetapan kadar abu tidak larut asam. Pemeriksaan golongan senyawa terhadap serbuk simplisia hewan meliputi pemeriksaan glikosida, saponin dan steroid/triterpenoid. Ekstraksi dilakukan dengan metode perkolasi dan fraksinasi dilakukan dengan metode ekstraksi cair-cair, isolasi senyawa steroid/triterpenoid dilakukan secara kromatografi lapis tipis, lalu diuji kemurnian isolat menggunakan kromatografi lapis tipis dua arah serta analisis isolat dengan spektrofotometri UV, IR dan spektrofotometer massa. Hasil karakteristik simplisia teripang yaitu kadar air 9,47 %, kadar sari larut air 36,56% , kadar sari larut etanol 24,01 % , kadar abu total 28,75 %, dan kadar abu tidak larut asam 3,66 %. Hasil mikroskopik serbuk simplisia teripang mempunyai spikula bentuk kancing (buttons), spikula bentuk batang (rods) dari tentakel dan spikula bentuk meja semu (pseudo-tables) dari dinding tubuh. Hasil pemeriksaan golongan senyawa kimia simplisia teripang mengandung glikosida, saponin dan steroid/triterpenoid. Hasil analisis isolat secara kromatografi lapis tipis diperoleh senyawa golongan steroid/triterpenoid yang memberikan noda berwarna merah ungu dengan penampak bercak Liebermann-Burchard. Hasil uji kemurnian isolat secara kromatografi lapis tipis dua arah memberikan noda tunggal yang dapat dianggap murni. Hasil analisis isolat secara spektrofotometri ultraviolet diperoleh absorbansi maksimum pada panjang gelombang 202 nm yang menunjukkan adanya gugus kromofor serta secara spektrofotometri inframerah isolat menunjukkan adanya gugus O–H, C–H, C=C, –CH3, C=O dan C–O spektrofotometri massa menunjukkan berat molekul 368,5. Hasil analisis diduga adalah senyawa 3 alpha, 11 beta, 17, 20 alpha, 21-Pentahydroxypregnane.
ISOLATION STEROID/TRITERPENOID FROM ETHANOL EXTRACT n-HEXANE FRACTION OF SEA
CUCUMBER Pearsonothuria graeffei
ABSTRACT
Sea cucumbers are one of marine commodities that widely spread in Indonesia but its content has not been explored further. The main secondary metabolites of sea cucumber are steroids/triterpenoids, saponins, and glycosides that have good biological activity that can be developed in various medical fields. The purpose of this study was to determine the simplex characterization and isolated steroids/triterpenoids from sea cucumber.
Simplex characterization including moisture content, water-soluble extract, ethanol-soluble extract, total ash content and acid insoluble ash content. Examination of secondary metabolites of simplex powder including determination glycoside, saponin and steroid/triterpenoid. Extraction was held using percolation method and fraction was held by using liquid-liquid extraction method. Isolating steroid/triterpenoid compounds using preparative thin-layer chromatography and the isolated was tested for its purity with two-dimentional thin layer chromatography and identification of isolates with ultraviolet spectrophotometry, infrared spectrophotometry and mass spectrofotometry.
Simplex characteristics of sea cucumbers result are 9.47% of water content, water soluble extract content of 36.56%, soluble extract ethanol content of 24.01%, 28.75% total ash content and acid insoluble ash content of 3.66%. Microscopic of the simplex powder are spicules form buttons (buttons), spicules form rods (rods) from the tentacles and the spicules form a pseudo table (pseudo-tables) from its body wall. Result test secondary metabolites of sea cucumber are glycosides, saponins and steroid/triterpenoid. Results of analysis by thin-layer chromatography isolates obtained triterpenoids class of compounds which give one red stain purple with Liebermann-Burchard. Purity test of isolates was held by using thin layer chromatography two phases prove the isolates is considered pure. Results of identification of isolates obtained ultraviolet spectrophotometry maximum absorbance at 202 nm wavelength indicating chromophor group and the infrared spectrophotometry isolates showed OH group, aliphatic CH, C=C, -CH3, C=O and C-O result of mass spectrophotometer showed a molecular weight of 368,5. Based of the results assumption of the the identification isolated compound is 3 alpha, 11 beta, 17, 20 alpha, 21-Pentahydroxypregnane.
ISOLASI SENYAWA STEROID/TRITERPENOID DARI
EKSTRAK ETANOL FRAKSI n-HEKSANA TERIPANG
Pearsonothuria graeffei
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
FITRI FALAH
NIM 111501020
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ISOLASI SENYAWA STEROID/TRITERPENOID DARI
EKSTRAK ETANOL FRAKSI n-HEKSANA TERIPANG
Pearsonothuria graeffei
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
FITRI FALAH
NIM 111501020
PENGESAHAN SKRIPSI
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ISOLASI SENYAWA STEROID/TRITERPENOID DARI EKSTRAK
ETANOL FRAKSI n-HEKSANA TERIPANG
Pearsonothuria graeffei
OLEH: FITRI FALAH NIM 111501020
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: 24 November 2015
Pembimbing I, Panitia Penguji,
Dra. Suwarti Aris, M.Si., Apt. Dr. Panal Sitorus, M.Si., Apt. NIP 195107231982032001 NIP 195310301980031002
Dra. Suwarti Aris, M.Si., Apt.
Pembimbing II, NIP 195107231982032001
Dra. Aswita Hafni Lubis, M.Si., Apt. Drs. Suryadi Achmad., M.Sc., Apt. NIP 195304031983032001 NIP 195109081985031002
Dra. Herawaty Ginting., M.Si., Apt. NIP 195112231980032002
Medan, Januari 2016 Fakultas Farmasi
Universitas Sumatera Utara Pejabat Dekan
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan
karunia yang berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi yang berjudul Isolasi Senyawa Steroid/Triterpenoid dari Ekstrak Etanol Fraksi n-Heksana Teripang Pearsonothuria graeffei. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada Ibu Dr. Masfria, M.S., Apt. selaku Pejabat Dekan Fakultas Farmasi, kepada Ibu Dra. Suwarti Aris, M.Si., Apt., Alm. Ibu Dra. Aswita Hafni Lubis, M.Si., Apt., dan Ibu Prof. Dr. Julia Reveny, M.Si., Apt selaku dosen pembimbing, kepada Bapak Dr. Panal Sitorus, M.Si., Apt., Bapak Drs. Suryadi Achmad., M.Sc., Apt dan Ibu Dra. Herawaty Ginting., M.Si., Apt., selaku dosen penguji serta Bapak Prof. Dr. Jansen Silalahi, M.App., Sc., Apt., selaku dosen pembimbing akademik serta Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah menyediakan fasilitas kepada penulis selama perkuliahan di Fakultas Farmasi dan telah meluangkan waktu dan tenaga dalam membimbing penulis dengan penuh kesabaran dan tanggung jawab serta memberikan petunjuk dan saran-saran selama penelitian hingga selesainya skripsi ini.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, Januari 2016 Penulis,
ISOLASI SENYAWA STEROID/TRITERPENOID DARI EKSTRAK ETANOL FRAKSI n-HEKSANA TERIPANG
Pearsonothuria graeffei
ABSTRAK
Teripang adalah salah satu komoditas hasil laut yang banyak terdapat di perairan Indonesia tetapi belum banyak dieksplorasi manfaat kandungannya. Kandungan metabolit sekunder utama dari teripang adalah steroid/triterpenoid, saponin, dan glikosida yang memiliki aktivitas biologi yang baik sehingga dapat dikembangkan dalam berbagai bidang pengobatan. Penelitian ini bertujuan untuk mengetahui karakterisasi simplisia dan isolasi steroid/triterpenoid dari teripang.
Pemeriksaan karakteristik simplisia hewan meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari larut air, penetapan kadar sari larut etanol, penetapan kadar abu total, dan penetapan kadar abu tidak larut asam. Pemeriksaan golongan senyawa terhadap serbuk simplisia hewan meliputi pemeriksaan glikosida, saponin dan steroid/triterpenoid. Ekstraksi dilakukan dengan metode perkolasi dan fraksinasi dilakukan dengan metode ekstraksi cair-cair, isolasi senyawa steroid/triterpenoid dilakukan secara kromatografi lapis tipis, lalu diuji kemurnian isolat menggunakan kromatografi lapis tipis dua arah serta analisis isolat dengan spektrofotometri UV, IR dan spektrofotometer massa. Hasil karakteristik simplisia teripang yaitu kadar air 9,47 %, kadar sari larut air 36,56% , kadar sari larut etanol 24,01 % , kadar abu total 28,75 %, dan kadar abu tidak larut asam 3,66 %. Hasil mikroskopik serbuk simplisia teripang mempunyai spikula bentuk kancing (buttons), spikula bentuk batang (rods) dari tentakel dan spikula bentuk meja semu (pseudo-tables) dari dinding tubuh. Hasil pemeriksaan golongan senyawa kimia simplisia teripang mengandung glikosida, saponin dan steroid/triterpenoid. Hasil analisis isolat secara kromatografi lapis tipis diperoleh senyawa golongan steroid/triterpenoid yang memberikan noda berwarna merah ungu dengan penampak bercak Liebermann-Burchard. Hasil uji kemurnian isolat secara kromatografi lapis tipis dua arah memberikan noda tunggal yang dapat dianggap murni. Hasil analisis isolat secara spektrofotometri ultraviolet diperoleh absorbansi maksimum pada panjang gelombang 202 nm yang menunjukkan adanya gugus kromofor serta secara spektrofotometri inframerah isolat menunjukkan adanya gugus O–H, C–H, C=C, –CH3, C=O dan C–O spektrofotometri massa menunjukkan berat molekul 368,5. Hasil analisis diduga adalah senyawa 3 alpha, 11 beta, 17, 20 alpha, 21-Pentahydroxypregnane.
ISOLATION STEROID/TRITERPENOID FROM ETHANOL EXTRACT n-HEXANE FRACTION OF SEA
CUCUMBER Pearsonothuria graeffei
ABSTRACT
Sea cucumbers are one of marine commodities that widely spread in Indonesia but its content has not been explored further. The main secondary metabolites of sea cucumber are steroids/triterpenoids, saponins, and glycosides that have good biological activity that can be developed in various medical fields. The purpose of this study was to determine the simplex characterization and isolated steroids/triterpenoids from sea cucumber.
Simplex characterization including moisture content, water-soluble extract, ethanol-soluble extract, total ash content and acid insoluble ash content. Examination of secondary metabolites of simplex powder including determination glycoside, saponin and steroid/triterpenoid. Extraction was held using percolation method and fraction was held by using liquid-liquid extraction method. Isolating steroid/triterpenoid compounds using preparative thin-layer chromatography and the isolated was tested for its purity with two-dimentional thin layer chromatography and identification of isolates with ultraviolet spectrophotometry, infrared spectrophotometry and mass spectrofotometry.
Simplex characteristics of sea cucumbers result are 9.47% of water content, water soluble extract content of 36.56%, soluble extract ethanol content of 24.01%, 28.75% total ash content and acid insoluble ash content of 3.66%. Microscopic of the simplex powder are spicules form buttons (buttons), spicules form rods (rods) from the tentacles and the spicules form a pseudo table (pseudo-tables) from its body wall. Result test secondary metabolites of sea cucumber are glycosides, saponins and steroid/triterpenoid. Results of analysis by thin-layer chromatography isolates obtained triterpenoids class of compounds which give one red stain purple with Liebermann-Burchard. Purity test of isolates was held by using thin layer chromatography two phases prove the isolates is considered pure. Results of identification of isolates obtained ultraviolet spectrophotometry maximum absorbance at 202 nm wavelength indicating chromophor group and the infrared spectrophotometry isolates showed OH group, aliphatic CH, C=C, -CH3, C=O and C-O result of mass spectrophotometer showed a molecular weight of 368,5. Based of the results assumption of the the identification isolated compound is 3 alpha, 11 beta, 17, 20 alpha, 21-Pentahydroxypregnane.
2.2.2 Glikosida ... 7
2.5.2 Kromatografi lapis tipis preparatif ... 15
2.5.3 Kromatografi lapis tipis dua arah ... 15
2.6 Spektrofotometri ... 15
2.6.1 Spektrofotometri sinar ultraviolet ... 15
2.6.2 Spektrofotometri sinar inframerah ... 16
2.6.3 Spektrfotometri massa ... 17
BAB III METODE PENELITIAN ... 19
3.1 Alat dan Bahan ... 19
3.1.1 Alat-alat ... 19
3.1.2 Bahan-bahan ... 20
3.2 Pengumpulan dan Pengolahan Teripang .. ... 20
3.3.5 Larutan pereaksi kloraljidrat ... 21
3.3.6 Larutan pereaksi Liebermann-Bourchard ... 21
3.3.6 Larutan asam sulfat 2 N ... 21
3.4 Pemeriksaan Karakteristik Simplisia ... 22
3.4.1 Pemeriksaan makroskopik ... 22
3.4.2 Pemeriksaan mikroskopik ... 22
3.4.3 Penetapan kadar air ... 22
3.4.4 Penetapan kadar sari larut air ... 23
3.4.5 Penetapan kadar sari larut etanol ... 24
3.4.6 Penetapan kadar abu total ... 24
3.4.7 Penetapan kadar abu tidak larut asam ... 24
3.5 Pemeriksaan Senyawa pada Teripang ... 25
3.5.1 Pemeriksaan saponin ... 25
3.5.2 Pemeriksaan steroid/triterpenoid ... 25
3.5.3 Pemeriksaan glikosida ... 25
3.6 Pembuatan ekstrak ... 26
3.6.1 Pembuatan ekstrak etanol ... 26
3.6.2 Fraksinasi dengan n-heksana ... 26
3.7 Analisis Ekstrak Teripang secara KLT ... 27
3.8 Isolasi Senyawa Steroid/Triterpenoid secara KLT Preparatif ... 27
3.9 Uji Kemurnian Isolat secara KLT Dua Arah ... 28
3.10 Karakterisasi Isolat ... 28
3.10.1 Karakterisasi isolat dengan spektrofotometri UV ... 29
3.10.2 Karakterisasi isolat dengan spektrofotometri IR ... 29