PRARANCANGAN PABRIK UREA FORMALDEHID DARI
METANOL,UDARA DAN UREA KAPASITAS
28000 TON/TAHUN
(Tugas Khusus Perancangan Reaktor 202 (RE-202))
Oleh
SEDNY ANTONI
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA TEKNIK
Pada
Jurusan Teknik Kimia
Fakultas Teknik Universitas Lampung
FAKULTAS TEKNIK UNIVERSITAS LAMPUNG
PRARANCANGAN PABRIK UREA FORMALDEHID DARI METANOL,UDARA DAN UREA KAPASITAS
28000 TON/TAHUN
O l e h Sedny Antoni
Kebutuhan indonesia akan urea formaldehid yang banyak dimanfaatkan pada industri perekatan semakin bertambah dari tahun ke tahun, sedangkan industri yang memproduksi urea formaldehid relatif tetap sehingga kebutuhan industri tersebut masih dipenuhi dari produsen luar negeri.
Bahan baku metanol sebanyak 1382,75 kg/jam diperoleh dari PT. Kaltim Methanol Industri dan urea sebesar 1722,94 kg/jam dari PT. Pupuk Kalimantan Timur, sedangkan bahan baku oksigen sebanyak 1534,47 kg/jam dapat diperoleh dari udara lingkungan. Proses produksi urea formaldehid terbagi menjadi dua tahap proses yaitu proses pembuatan formaldehid dan proses pembentukan urea formaldehid. Formaldehid dibentuk dengan mereaksikan metanol fasa gas dan oksigen pada temperatur 240 oC dan tekanan 1,4 atm . Selanjutnya gas formaldehid yang terbentuk direaksikan dengan larutan urea pada temperatur 70oC dan tekanan 1,2 atm untuk membentuk produk urea formaldehid 3535,35 kg/jam.
.Analisa kelayakan prarancangan pabrik urea formaldehid sebagai berikut : Fixed Capital Investment (FCI) = Rp. 177.102.551.742,13
Working Capital Investment (WCI) = Rp. 31.253.391483,91 Total Capital Investment (TCI) = Rp. 208.355.943.226,04
Break Even Point (BEP) = 45,92 %
Pay Out Time before Taxes (POT) = 1,98 tahun Pay Out Time after Taxes (POT)a = 2,36 tahun Return on Investment before Taxes (ROI)b = 34,34 % Return on Investment after Taxes (ROI)a = 27,47 %
Discounted Cash Flow (DCF) = 31,42 %
Shut Down Point (SDP) = 27,19 %
DAFTAR ISI
Halaman DAFTAR ISI
DAFTAR TABEL DAFTAR GAMBAR
I. PENDAHULUAN
A. Latar Belakang Pendirian Pabrik ………. 1
B. Kegunaan Produk ……… 2
C. Ketersedian Bahan Baku ………. 3
D. Analisis Pasar ………... 3
E. Kapasitas Pabrik ………... 4
F. Penentuan Lokasi Pabrik ……… 6
II. DESKRIPSI PROSES A. Konsep Proses ………..……. 8
B. Tinjauan Proses ………..…….… 10
C. Uraian Proses ……….. 14
III. SPESIFIKASI BAHAN A. Bahan Baku ………18
B. Bahan Pembantu ………20
C. Produk ………20
IV. NERACA MASSA DAN NERACA ENERGI A. Neraca Massa ………....21
B. Neraca Energi ………22
V. SESIFIKASI PERALATAN A. Peralatan Proses ………26
B. Peralatan Utilitas ………39
VI. UTILITAS A. Unit Pendukung Proses ………...68
B. Unit Pengolahan Limbah ………..….. 91
C. Laboratorium ………..…………..93
VII. TATA LETAK PABRIK
A. Lokasi Pabrik ………..…………..98
B. Tata Letak Pabrik Keseluruhan ……….101
C. Tata Letak Peralatan Proses ……….102
VIII. SISTEM MANAJEMEN DAN ORGANISASI PERUSAHAAN A. Bentuk Perusahaan ………..105
B. Struktur Organisasi Perusahaan ………..108
C. Tugas dan Wewenang ………..111
D. Status Karyawan dan Sistem Penggajian …….……….119
E. Pembagian Jam Kerja Karyawan ………..119
F. Penggolongan Jabatan dan Jumlah Karyawan ………..122
G. Kesejahteraan Karyawan ………..125
IX. INVESTASI DAN EVALUASI EKONOMI A. Investasi ………..128
B. Evaluasi Ekonomi ………..132
C. Angsuran Pinjaman ………..134
D. Discounted Cash Flow ………..135
X. KESIMPULAN DAN SARAN A. Kesimpulan ………..136
B. Saran ………..136
I.
PENDAHULUAN
A.Latar Belakang Pendirian Pabrik
Industri plywood awalnya menggunakan phenol formaldehid sebagai perekat.
Tetapi ketika urea formaldehid telah digunakan secara komersil, maka
pemakaian phenol formaldehid semakin berkurang dan fungsinya digantikan
oleh urea formaldehid. Hal tersebut disebabkan harga urea formaldehid lebih
murah jika dibandingkan dengan phenol formaldehid. Selain harga yang lebih
murah, urea formaldehid memiliki beberapa keunggulan lain, seperti : kualitas
produk yang dihasilkan lebih baik, mudah dalam penuangan dan proses
pemotongan cepat serta tidak meninggalkan bekas warna pada papan yang
dihasilkan (Meyer, 1979).
Dalam penggunaannya secara luas, resin urea formaldehid lebih banyak
dimanfaatkan dalam industri perekatan yaitu sekitar 82 %. Pada industri
perekatan, urea formaldehid dikehendaki dalam bentuk resin, yaitu suatu
polimer yang masih memiliki bobot molekul rendah. Hal ini dimaksudkan agar
proses penetrasi selama perekatan dapat berlangsung lebih sempurna
(Pizzi,1996).
Kebutuhan industri akan urea formaldehid sebagai bahan baku utama maupun
bahan pendukung semakin bertambah dari tahun ke tahun sedangkan industri
tersebut masih dipenuhi dari produsen luar negeri. Oleh karena itu,
pembangunan pabrik urea formaldehid ini dapat memberikan dampak positif
terhadap pemenuhan kebutuhan dalam negeri.
B.Kegunaan Produk
Industri-industri yang memanfaatkan urea formaldehid, antara lain :
1. Industri tekstil
Penambahan 7-10 % urea formaldehid dapat mencegah kekerutan dan
kusutnya kain katun (Rukaesih,2000).
2. Industri kertas
Urea formaldehid sebagai perekat dan pelapis kertas untuk meningkatkan
mutu dan kekuatan kertas karena penambahan 2 - 4 % urea formaldehid
pada pH 4,5 dapat memperkuat kertas (Cucu dkk,2011).
3. Industri kayu lapis dan meubel
Urea formaldehid digunakan sebagai perekat (glue) dan pelapis kayu,
menginsulasi busa, perekat untuk pembuatan chipboard dengan
menambahkan 10 % larutan urea formaldehid. Selain itu urea formaldehid
memiliki warna terang sehingga cocok untuk pemakaian dekoratif. Industri
kayu lapis dan meubel merupakan konsumen urea formaldehid terbesar
(Cucu dkk,2011).
4. Industri pembuatan kapal
Urea formaldehid mempunyai sifat dapat dicetak tekan sehingga
mempunyai permukaan keras yang cocok sebagai bahan pelapis pada
badan kapal. Warnanya yang terang memudahkan pemberian berbagai
C.Ketersediaan bahan baku
Metanol dapat diperoleh dari PT. Kaltim Methanol Industri yang mempunyai
kapasitas 660.000 ton/tahun dan urea dapat diperoleh dari PT. Pupuk
Kalimantan Timur yang mempunyai kapasitas 2.980.000 ton/tahun. Sedangkan
bahan baku oksigen dapat diperoleh dari udara lingkungan sekitar sehingga
dapat disimpulkan bahwa kebutuhan bahan baku untuk pembuatan urea
formaldehid dapat menjamin kelangsungan hidup pabrik yang akan dirancang.
D.Analisa Pasar
1. Prediksi kebutuhan pasar
Indonesia masih mengimpor urea formaldehid dari negara lain.
Perkembangan impor urea formaldehid disajikan pada Tabel 1.1 (Badan Pusat Statistik, 2012).
Tabel 1.1 Data Impor Urea Formaldehid Indonesia Tahun Jumlah (ton)
1 = 2003 2 = 2004 3 = 2005 4 = 2006 5 = 2007 6 = 2008 7 = 2009 8 = 2010
3.806 4.124 7.477 8.092 9.568 12.810 14.359 15.908
2. Harga Bahan Baku dan Produk
Tabel. 1.2. Harga bahan baku dan produk
No Bahan Harga
1 Metanol US$ 0,41/kg
2 Urea US$ 0,46/kg
E.Kapasitas Pabrik
Untuk memprediksi kebutuhan impor urea formaldehid pada tahun 2017 atau
tahun ke 15 dilakukan dengan memplotkan data impor pada tabel 1.1 dalam
grafik dan dilakukan pendekatan berupa garis lurus.
Gambar 1.1 Grafik Impor Urea Formaldehid Indonesia
Dari Gambar 1.1 dapat diperkirakan kebutuhan impor urea formaldehid terus
meningkat dari tahun ke tahun. Untuk dapat memperkirakan kebutuhan impor
urea formaldehid pada tahun berikutnya dapat menggunakan persamaan garis
lurus :
y = ax + b
Keterangan : y = kebutuhan imporurea formaldehid, ton/tahun
x = tahun ke- i
b = intercept
a = gradien garis miring
y = 1825.76x + 1302.07
0 2000 4000 6000 8000 10000 12000 14000 16000 18000
0 2 4 6 8 10
im
p
o
r
Diperoleh persamaan garis lurus : y = 1825,76x + 1302,07
Dari persamaan di atas diketahui bahwa kebutuhan impor urea formaldehid di
Indonesia pada tahun ke 15 adalah :
y = 1825,76 (15) + 1302,07
y = 28688,47 ton/tahun
Dengan demikian dapat diperkirakan bahwa pada tahun 2017 impor urea
formaldehid sebesar 28.000 ton.
Produsen urea formaldehid di Indonesia (http://kemenperin.go.id) dapat dilihat
pada Tabel 1.2 sebagai berikut :
Tabel 1.2 Produsen Urea Formaldehid di Indonesia
Pabrik Kapasitas (ton/tahun)
PT. Pamolite Adhesive Industry PT. Arjuna Utama Kimia PT. Benua Multi Lestari PT. Binajaya Rodakarya PT. Cakram Utama Jaya PT. Gelora Citra Kimia Abadi PT. Giat Ultra Chemical Industry PT. Kayu lapis Indonesia
PT. Korindo Abadi PT. Kurnia Kapuas Utama PT. Lakosta Indah
PT. Prima Adhesnas PT. Susel Prima Permai PT. Tecwin Jaya Development PT. Wiranusa Trisatya
PT. Korindo Ariabimasari PT. Dyno Mugi Indonesia PT. Superin
PT. Intanwijaya Internasional PT. Batu Penggal
PT. Sabak Indah Jambi PT. Nusa Prima Pratama PT. Uforin prajen
PT. Duta Pertiwi Nusantara
45.000 35.900 55.000 32.000 11.800 72.000 40.000 56.000 21.000 40.000 40.000 50.000 49.000 20.000 106.000 24.000 37.000 48.000 65.000 40.000 48.000 40.000 45.000 84.000
(sumber: http://kemenperin.go.id, 2012)
Dengan menganggap bahwa kapasitas pabrik-pabrik di atas tetap pada tahun
kekurangan sebesar 28.000 ton pada tahun 2017. Untuk itu pendirian pabrik
yang baru sangat diharapkan untuk memenuhi kekurangan kebutuhan urea
formaldehid dalam negeri pada tahun 2017.
F. Penentuan Lokasi Pabrik
Pemilihan lokasi pabrik merupakan hal yang penting dalam suatu perancangan
pabrik, karena berkaitan dengan nilai ekonomis. Bahan baku yang diperlukan
adalah metanol dan urea yang didapat dari dalam negeri. Pabrik metanol di
Indonesia adalah PT. Kaltim Methanol Industri dan PT. Pertamina Pulau
Bunyu yang berlokasi di Kalimantan Timur. Sedangkan pabrik urea di
Indonesia adalah PT. Pupuk Iskandar Muda yang berada di Nangro Aceh
Darussalam, PT. Pupuk Sriwidjaja (Sumatera Selatan), PT. Pupuk Kujang
(Jawa Barat), PT. Petrokimia Gresik (Jawa Timur) dan PT. Pupuk Kaltim
(Kalimantan Timur).
Produk urea formaldehid mayoritas digunakan oleh industri plywood, particle
board dan industri perekatan lainnya dimana lokasi pabrik-pabrik tersebut
dapat dilihat pada Tabel 1.4. dan 1.5. berikut ini :
Tabel 1.4 Perusahaan Perekatan di Indonesia dengan Jenis Industri Particle Board
Nama Perusahaan Lokasi Kapasitas(ton/tahun) - PT Asia Forestama Raya
- PT Nuvopan Indotama - PT Sari Bumi Kusuma - PT Akhates
- PT Barito Pacific Timber
Sumatera Utara Kalimantan Barat Kalimantan Barat KalimantanTengah Kalimantan Selatan
30.000 121.250 74.000 45.000 200.000
(sumber: http://kemenperin.go.id, 2012)
Pertimbangan lain dalam memilih lokasi pabrik adalah sifat bahan baku dan
sebaiknya berada di dekat sumber bahan baku, sementara jika produk yang
berbahaya, maka lokasi pabrik seharusnya berada di dekat pasar.
Tabel 1.5 Perusahaan Perekatan di Indonesia dengan Jenis Industri Plywood
(sumber: http://kemenperin.go.id, 2012)
Alternatif lokasi yang memenuhi faktor-faktor tersebut di atas, yaitu di daerah
Bontang. Bontang memenuhi kriteria dekat dengan sumber kedua bahan baku,
yaitu metanol dari PT. KMI dan urea dari PT. Pupuk Kaltim serta dekat dengan
pasar urea formaldehid. Bontang merupakan kawasan industri sehingga pajak,
karakter tanah, pengolahan limbah, pengadaan energi telah diperhitungkan dan
tersedia.
Nama Perusahaan Lokasi Kapasitas
(ton/tahun)
- PT Panca Eka Bina Plywood Industri - PT Kampari Wood
- PT Olympia Veneer Product - PT Sola Gratia Plywood
- PT Putra Sumber Utama Timber - PT Andatu Lestari Plywood - PT Kayu Lapis Indonesia - PT Sumber Mas Indah Plywood - PT Wana Bangun Agung - PT Erna Djuliawati
- PT Kurnia Kapuas Plywood - PT Antang Cahaya Baru - PT Meranti Mustika
- PT IDEC Abadi Wood Industries - PT Intracowood Manufacturing - PT Meranti Sakti Indah plywood - PT Tirta Mahakam Plywood Industry - PT Daya Sakti Unggul Corporindo, Tbk - PT Hendratna Plywood
- PT Tanjung Raya Plywood - PT Katingan Timber Celebes - PT Jati Dharma Indah Plywood - PT Waenebi Wood
- PT Wapoga Mutiara Timber
X. KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil analisis ekonomi yang telah dilakukan terhadap
Prarancangan Pabrik Urea Formaldehid dari Metanol, Udara dan Urea dengan
kapasitas 28.000 ton/tahun dapat ditarik simpulan sebagai berikut :
1. Percent Return on Investment (ROI) sesudah pajak adalah 27,47 %.
2. Pay Out Time (POT) sesudah pajak adalah 2,36 tahun.
3. Break Even Point (BEP) sebesar 45,92 % dimana syarat umum pabrik di
Indonesia adalah 30 – 60 % kapasitas produksi. Shut Down Point (SDP)
sebesar 27,19 %, yakni batasan kapasitas produksi sehingga pabrik harus
berhenti berproduksi karena merugi.
4. Discounted Cash Flow Rate of Return (DCF) sebesar 31,42 %, lebih besar
dari suku bunga bank sekarang sehingga investor akan lebih memilih
untuk berinvestasi ke pabrik ini dari pada ke bank.
B. Saran
Pabrik Urea Formaldehid dari Metanol, Udara dan Urea dengan kapasitas
28.000 ton/tahun sebaiknya dikaji lebih lanjut baik dari segi proses maupun
DAFTAR PUSTAKA
Adang. P., 2001, Technical Training Proses Pembentukan Steam. ITB : Bandung
A.M.Estevez S .1989. Oxidation Of Methanol To Formaldehyde On Iron-Molybdenum Oxide Catalysts, With And Without Chromium As A
Promoter. Reaction Kinetics and Catalysis Letters 1989, Volume 38, Issue 1, pp 193-198
Anonim.2012. http://www.o-fish.com/Filter/filter_ro.php , diakses 10 Desember 2013)
Anonim. 2013. (http://www.batan.go.id/ptrkn/file/Epsilon/Vol_12_03/2.Itjeu.pdf. diakses16 Januari 2013, Pukul 17.30 WIB)
Anonim. 1988.(http://google.com/Bab II 1988psu.pdf , diakses tanggal 10 Desember 2013)
Anonim.2011.http://dardel.info/IX/processes/processes.html, Basic ion exchange processes in water treatment, diakses 07 Desember 2013)
Anonim.2012.(http://bps.go.id, diakses September 2012)
Anonim.2013.(http://4funjava.blogspot.com/2010/04/proses-pengolahan-air.html. diakses September Pukul 16.47 WIB)
Anonim.2013.( http://aplikasiteknikkimia.blogspot.com/2009/04/pengolahan-air-umpan-boiler.html, diakses 16 Januari 2013 Pukul 16.53 WIB.)
Anonim.2013.(http://fisika-utility.blogspot.com/. 16 Januari 2013, Pukul 19.47 WIB.)
Anonim.2012.(http://www.alibaba.com,diakses oktober 2012)
Anonim.2012.http://www.che.com/pci (as Published in Chemical Engineering Magazine, diakses Februari 2013)
Anonim.2012.(http://www.dbwestern.com, diakses Agustus 2012)
Anonim.2012.(http://www.pupukkaltim.com, diakses Agustus 2012)
Anonim.2013.(http://www.matches.com, diakses September 2013)
Anonim.2012.(http://x.kemenperin.go.id/IND/Link/KIP.pdf. diakses 15 Agustus 2012.)
A.Pizzi. 1996.Urea-formaldehyde adhesives.universite de nancy,epinal,france Esterino C dan Rubini. 2005.catalysts for oxidation of methanol to
formaldehyde ( US Patent No,7468341). USA
Anthony H.C.1996. urea-formaldehyde adhesive resins. university of Massachusetts: USA
B.Raveendran dan D.J.Francis. 1982. Kinetics and Mechanism of urea formaldehyde reaction. Jurnal department of applied chemistry,university of cochin 682002,india ,received 29 march 1982)
Brown.G.G. 1950, Unit Operation 6ed, Wiley&Sons, USA.
Brownell.L.E. and Young.E.H., 1959, Process Equipment Design 3ed, John Wiley & Sons, New York.
Coulson.J.M. and Ricardson.J.F., 1983, Chemical Engineering vol 6, Pergamon Press Inc, New York.
Cucu dkk. 2011. Kajian Awal Pembuatan Adhesif Untuk Kertas Dekoratif Pada Pembuatan Furnitur.Balai Besar Pulp dan Kertas: Bandung
Ferreira.A, dkk, 2007, Jurnal Research and Design Trans IChemE, Portugal
Fogler.A.H.Scott, 1999, Elements of Chemical Reaction Engineering, Prentice Hall International Inc, New Jersey.
Geankoplis.Christie.J., 1993, Transport Processes and unit Operation 3th ed, Allyn & Bacon Inc, New Jersey.
Himmeblau.David., 1996, Basic Principles and Calculation in Chemical Engineering, Prentice Hall Inc, New Jersey.
Jane,K. 2010. Reverse Osmosis: Design, Processes, and Applications for Engineers. John Wiley and Sons Inc., New York.
Malik dkk.Characteristics Of Laminated Wood Of Logging Waste Three Natural Forest Wood Species (Journal of Forestry Research Vol. 2 No. 1, March 2005: 37 – 48)
McCabe.W.L. dan Smith.J.C., 1985, Operasi Teknik Kimia, Erlangga, Jakarta.
McKetta,J.J. 1988.Encyclopedia Of Chemical Processing And Design. Marcel dekker inc: USA
Megyesy.E.F., 1983, Pressure Vessel Handbook, Pressure Vessel Handbook Publishing Inc, USA.
Meyer, Beat, 1979, Urea Formaldehyde Resins, Addison Wesley Publishing, Canada.
Perry.R.H. and Green.D., 1997, Perry’s Chemical Engineer Handbook 7th ed, McGraw-Hill Book Company, New York.
Peter.M.S. and Timmerhaus.K.D., 1991, Plant Design an Economic for Chemical Engineering 3ed, McGraww-Hill Book Company, New York.
Powell, S.T., 1954, Water Conditioning for Industry, Mc Graw Hill Book Company, New York.
Rukaesih,Okay.2000.Pengaruh Senyawa Silikon Sebagai Pelemas Dalam Proses Penyempurnaan Anti Kusut Kain Polyester Kapas.Balai Besar
Pengembangan Dan Penelitian Tekstil:Bandung
Smith.J.M. and Van Ness.H.C., 1975, Introduction to Chemical Engineering Thermodynamics 3ed, McGraww-Hill Inc, New York.
Treyball.R.E., 1983, Mass Transfer Operation 3ed, McGraw-Hill Book Company, New York.
Ulmann, 2007. Ulmann’s Encyclopedia of Industrial Chemistry. VCH Verlagsgesell Scahft, Wanheim, Germany.
Ulrich.G.D., 1984, A Guide to Chemical Engineering Process Design and Economics. John Wiley & Sons Inc, New York.
Wallas. S.M., 1988, Chemical Process Equipment, Butterworth Publishers, Stoneham USA.
LAMPIRAN A
PERHITUNGAN NERACA MASSA
I. Kapasitas Prarancangan
Kapasitas per tahun = 28.000 Ton/Tahun
1 tahun operasi = 330 hari
Kapasitas prarancangan =
ton 1
kg 1000 jam
24 hari 1 hari 330
tahun 1 tahun 1
ton 000 . 28
x x
x
= 3535,35 kg/jam
II. Komposisi Bahan Baku dan Produk
1. Metanol
Metanol = 99,90 % berat
Air = 0,10 % berat
2. Udara
Nitrogen = 79 % mol
Oksigen = 21 % mol
3. Urea
Urea = 99,27 % berat
Air = 0,73 % berat
4. Urea Formaldehid
Urea Formaldehid = 80,00 % berat
Air = maks 20,00 % berat
II. Reaksi
a. Reaksi di Reaktor 01 (Sintesa Formaldehid)
Umpan yang masuk = Mol Metanol : Mol Oksigen = 9 : 10
Konversi metanol = 99 %
Selektivitas = 94 %
Reaksi utama :
CH3OH(g) + ½ O2(g) HCHO(g) + H2O(g) …(1)
Reaksi samping :
HCHO(g) + ½ O2(g) CO(g) + H2O(g) …(2)
b. Reaksi di Reaktor 02 (Sintesa Urea Formaldehid)
Perbandingan mol umpan = Urea : Formaldehid = 1 : 1,4
Konversi = 97 %
Reaksi yang terjadi :
13 CO(NH2)2 (l) + 18 CH2O (g) 9 HOCH2NHCONH2(l) +
3NHCONH(CH2OH)2(l)+
NHCON(CH2OH)3(l)
III. Notasi
CH3OH = Metanol
H2O = Air
O2 = Oksigen
CO2 = Karbondioksida
N2 = Nitrogen
U rea = CO(NH2)2
Formaldehid = HCHO
UF1 = HOCH2NHCONH2
UF2 = NHCONH (CH2OH)2
UF3 = NHCON(CH2OH)3
IV. Berat Molekul
Metanol = 32,04 kg/kgmol
Air = 18,01 kg/kgmol
Oksigen = 32,00 kg/kgmol
Karbonmonoksida = 28,01 kg/kgmol
Karbondioksida = 44,01 kg/kgmol
Nitrogen = 28,01 kg/kgmol
Urea = 60,06 kg/kgmol
Formaldehid = 30,03 kg/kgmol
UF1 = 90,09 kg/kgmol
UF2 = 120,12 kg/kgmol
UF3 = 150,15 kg/kgmol
V. Basis Perhitungan
VI. Neraca Massa Tiap Alat
1. REAKTOR 202 (RE-202)
Fungsi : Tempat mereaksikan larutan urea dan gas formaldehid untuk
menghasilkan produk urea formaldehid.
Gambar :
Massa total produk = 3535,35 kg/jam
Kandungan Urea formaldehid dalam produk = 80 %
Berat urea formaldehid total dalam produk = 3535,35 kg/ jam
100 80
= 2828,28 kg/jam
BM rata-rata urea formaldehid =
13
1 3
9BMUF1 BMUF2 BMUF3
=
13
15 , 150 1 12 , 120 3 09 , 90
9
= 101,64 kg/kmol
Mol Urea formaldehid total =
kmol kg
jam kg
/ 64 , 101
/ 28 , 2828
Mol UF1 = 27,83kmol/ jam 13
9
= 19,26 kmol/jam
Massa UF1 = 19,26 kmol/jam x 90,09 kg/kmol
= 1735,54 kg/jam
Mol UF2 = 27,83kmol/ jam 13
3
= 6,42 kmol/jam
Massa UF2 = 6,42 kmol/jam x 120,12 kg/kmol
= 771,35 kg/jam
Mol UF3 = 27,83kmol/ jam 13
1
= 2,14 kmol/jam
Massa UF3 = 2,14 kmol/jam x 150,15 kg/kmol
= 321,40 kg/jam
Reaksi yang terjadi di Reaktor 202
13 CO(NH)2 + 18 HCHO 9 UF1 + 3 UF2 + UF3
M 28,69 40,16
R 27,83 38,53 19,26 6,42 2,14
S 0,86 1,63 19,26 6,42 2,14
Massa Umpan HCHO = 40,16 kmol/jam x 30,03 kg/kmol
Massa Umpan Urea = 28,69 kmol/jam x 60,06 kg/kmol
= 1722,94 kg/jam
Kelarutan urea pada temperatur 70oC = 268,04 gr/100 ml
Jumlah air yang dibutuhkan untuk melarutkan umpan urea :
x gr x ml
gr 1722,94 103 100
04 ,
268
x = 642,80 L = 642,80 kg
Jumlah kandungan air dalam urea = x1722,94kg/ jam %
100 % 73 , 0
= 12,58 kg/jam
Jumlah total air = 642,80 kg/jam + 12,58 kg/jam
= 655,38 kg/jam
Massa urea sisa = 0,86 kmol/jam x 60,06 kg/kmol
= 51,69 kg/jam
Tabel A.1. Neraca massa pada reaktor 202
Komponen Massa Masuk (kg/jam)
Massa Keluar (kg/jam)
Urea 1722,94 51,69
HCHO 1206,06 49,04
H2O 655,38 655,38
UF1 0 1735,54
UF2 0 771,35
UF3 0 321,40
2. REAKTOR2 201 (RE-201)
Fungsi : Tempat mereaksikan uap metanol dan oksigen untuk membentuk gas
formaldehid sebagai umpan reaktor 02 (sintesa urea formaldehid).
Gambar :
HCHO yang dihasilkan pada reaksi 1 = 40,16kmol/ jam %
94 % 100
= 42,73 kmol/jam
HCHO yang bereaksi pada reaksi 2 = 42,73kmol/ jam
100
6
= 2,56 kmol/jam
Reaksi 1 CH3OH + ½ O2 HCHO + H2O
M 43,16 47,95
R 42,73 21,35 42,73 42,73
S 0,43 26,59 42,73 42,73
Reaksi 2 HCHO + ½ O
2 CO + H2O
2,56 1,28 2,56 2,56
Massa CH3OH Umpan = 43,16 kmol/jam x 32,04 kg/kmol
Kandungan air dalam CH3OH = 0,1 %
Massa H2O dalam CH3OH = 1382,75kg/ jam
% 9 , 99
% 1 , 0
= 1,38 kg/jam
Massa O2 Umpan = 47,95 kmol/jam x 32 kg/kmol
= 1534,47 kg/jam
Massa N2 Umpan = 47,95kmol/ jamx28,01kg/kmol
% 21
% 79
= 5052,77 kg/jam
Massa HCHO terbentuk = (42,73– 2,56) kmol/jam x 30,03 kg/kmol
= 1206,06 kg/jam
Massa CH3OH sisa = 0,43 kmol/jam x 32,04 kg/kmol
= 13,83 kg/jam
Massa O2 sisa = (26,59– 1,28) kmol/jam x 32 kg/kmol
= 809,85 kg/jam
Massa H2O terbentuk = (42,73+ 2,56) kmol/jam x 18,01 kg/kmol
= 815,65 kg/jam
Massa total H2O keluar = ( 815,65 + 1,38 ) kg/jam
= 817,04 kg/jam
Massa CO terbentuk = 2,56 kmol/jam x 28,01 kg/kmol
= 71,80 kg/jam
Tabel A.2. Neraca massa pada reaktor 201
Komponen Massa Masuk (kg/jam)
Massa Keluar (kg/jam)
CH3OH 1382,75 13,83
O2 1534,47 809,85
HCHO 0 1206,06
CO 0 71,80
H2O 1,38 817,04
N2 5052,77 5052,77
Total 7971,37 7971,37
3. MIXING TANK (MT-101)
Fungsi : Tempat pencampuran urea dengan sejumlah air agar terbentuk larutan
urea untuk diumpankan ke reaktor 02 (sintesa urea formaldehid)
Gambar :
Massa urea = 1722,94 kg/jam
Komposisi urea : Urea = 99,27 % berat
H2O = 0,73 % berat
Jumlah kandungan air dalam urea = x1722,94kg/ jam %
100 % 73 , 0
= 12,58 kg/jam
Jumlah air yang dibutuhkan untuk melarutkan umpan urea :
x gr x ml
gr 1722,94 103 100
04 , 268
x = 642,80 L = 642,80 kg
Jumlah total air = 642,80 kg/jam + 12,58 kg/jam
= 655,38 kg/jam
Tabel A.3. Neraca massa pada Mixing tank
Komponen Massa Masuk (kg/jam) Massa Keluar (kg/jam) Input 1 Input 2
Urea 1722,94 0 1722,94
H2O 12,58 642,80 655,38
Total 1735,52 642,80 2378,33 2378,33
4. SEPARATOR (SE-201)
Fungsi : Memisahkan H2O liquid dari fraksi gas produk reaktor 201 (sintesa
formaldehid) setelah melewati cooler pada temperatur 70oC
Gambar :
Komponen yang masuk ke dalam separator sama seperti komponen yang
Pemisahan antara fasa gas dan cairan pada separator dapat dilihat dari perbedaan titik didihnya.
Tabel A.4. Titik didih produk reaktor 201 Komponen Titik didih (oC)
CH3OH 64,7
O2 -183
HCHO -21
CO -192
H2O 100
N2 -195,8
Berdasarkan data titik didih diatas maka H2O mempunyai fasa liquid karena titik
didihnya lebih besar dari temperatur separator 70oC, sedangkan yang lain masih dalam fasa gas.
Pemisahan campuran fasa gas dengan fasa cair di dalam separator juga dapat
dilakukan berdasarkan perbedaan tekanan uap. Tekanan uap komponen dapat
dihitung dengan menggunakan persamaan Antoine:
Keterangan : Pi = Tekanan uap komponen i, mmHg
T = Temperatur, K
A, B, dan C = Konstanta Antoine
Tabel A.5 Konstanta Antoine
Komponen A B C
CH3OH 18,5875 3626,55 -34,29
Oksigen 13,6835 780,26 -4,1758
HCHO 7,46432 1078,39 254,377
CO 6,72527 295,228 268,243
Air 16,5362 3985,44 -38,9974
N2 15,3768 1956,25 -2,1117
(Sumber : Reklaitis, 1983, yaws,himelblau)
ln�� = −
Untuk HCHO dan CO, persamaan Antoine yang digunakan :
Dengan : Pi = Tekanan uap komponen i, mmHg T = temperatur, oC
Diketahui temperatur keluaran dari cooler produk reaktor 01 adalah 70oC.
Sehingga diperoleh tekanan uap masing-masing komponen seperti yang tersaji
dalam tabel berikut.
Tabel A.6 Tekanan Uap pada T = 70 oC
Komponen Pi (bar)
CH3OH 1,229673517
O2 115,2767121
HCHO 18,15559674
CO 936,7599031
H2O 0,305650866
N2 129,3074302
Jika Pi > P, maka komponen tersebut dalam fasa gas. Dan sebaliknya, jika Pi < P,
maka komponen tersebut dalam fasa cair. Di mana P = 1bar, sehingga yang
merupakan fasa cair adalah H2O, sedangkan yang lainnya merupakan fasa gas.
Asumsi seluruh komponen fasa gas ke atas, dan seluruh fasa cair ke bawah.
Aliran Masuk :
Massa HCHO = 1206,06 kg/jam
Massa CH3OH = 13,83 kg/jam
Massa O2 = 809,85 kg/jam
Massa total H2O = 817,04 kg/jam
Massa CO = 71,80 kg/jam
Massa N2 = 5052,77 kg/jam
log�� = −
Aliran Keluar :
Bagian atas :
Massa HCHO = 1206,06 kg/jam
Massa CH3OH = 13,83 kg/jam
Massa O2 = 809,85 kg/jam
Massa CO = 71,80 kg/jam
Massa N2 = 5052,77 kg/jam
Bagian bawah :
[image:31.595.148.465.403.535.2]Massa total H2O = 817,04 kg/jam
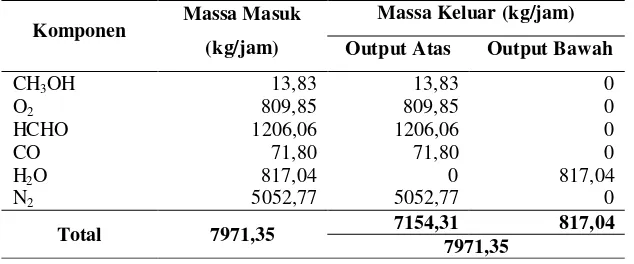
Tabel A.7. Neraca massa pada Separator
Komponen Massa Masuk (kg/jam)
Massa Keluar (kg/jam) Output Atas Output Bawah
CH3OH 13,83 13,83 0
O2 809,85 809,85 0
HCHO 1206,06 1206,06 0
CO 71,80 71,80 0
H2O 817,04 0 817,04
N2 5052,77 5052,77 0
LAMPIRAN B
PERHITUNGAN NERACA PANAS
Dari perhitungan neraca massa, selanjutnya dilakukan perhitungan neraca energi.
Perhitungan neraca energi didasarkan pada:
Basis waktu : Jam
Satuan panas : Kilo Joule (kJ)
Temperatur referensi : 25 oC (298,15 K)
Neraca energi:
{(Energi masuk) – (Energi keluar) + (Generasi energi) – (Konsumsi energi)} =
{Akumulasi energi} (Himmelblau,ed.6, 1996:400)
Energi secara umum yang terlibat berupa energi panas (Q) dan kerja (W).
Perhatikan Gambar B.1 dibawah ini.
Gambar B.1. Proses Secara Umum Perpindahan Energi Pada Suatu Sistem m1
U1 P1 K1 w1
m2 U2 P2 K2 w2 Sistem
W Q
-W -Q
1 2
Pada Gambar B.1 terlihat proses perpindahan energi secara pada suatu sistem.
Pada keadaan 1, suatu materi atau bahan memiliki empat buah energi yaitu energi
kinetik (K1), energi potensial (P1), energi dalam (U1), dan energi berupa kerja p1v1
(w1) serta memiliki laju alir massa m1. Materi atau bahan tersebut kemudian
melewati sebuah sistem tertentu, dimana materi atau bahan tersebut membutuhkan
energi dari luar berupa panas (-Q) dan kerja (-W) atau sebaliknya, dapat
menghasilkan energi berupa panas (Q) dan kerja (W). Setelah melewati sistem,
bahan atau materi tersebut berada pada keadaan 2, dimana materi tersebut
memiliki energi berupa energi kinetik (K2), energi potensial (P2), energi dalam
(U2), dan energi berupa kerja p2v2 (w2) serta memiliki laju alir massa m2.
Sehingga persamaan neraca energi secara umum menjadi :
(U1 + K1 + P1)m1 - (U2 + K2 + P2)m2 + Q + W + w1– w2= ∆E
(U1 + K1 + P1)m1 - (U2 + K2 + P2)m2 + Q + W + (p1v1)m1 - (p2v2)m2= ∆E
Jika tidak ada perubahan laju alir massa sebesar m1=m2=m dan tidak akumulasi
energi pada sistem, maka persamaan tersebut dapat disederhanakan menjadi,
{(U2-U1) + (K2-K1) + (P2-P1) + (p2v2) - (p1v1)}m = Q + W
{∆U + ∆Ek + ∆P + ∆pv }m = Q + W
Sistem berada pada tekanan tetap sehingga terdapat hubungan ∆H = ∆U + ∆pv
(Smith, J.M., Ed.6th, 2001, Pers.2.11., hal. 38) {∆H + ∆Ek + ∆P}m = Q + W
Jika pada sistem perubahan energi kinetik dan energi potensial sangat kecil dibandingkan energi yang timbul akibat adanya reaksi maka nilai ∆Ek dan ∆P
dapat diabaikan (bernilai nol) dan jika tidak ada kerja yang diberikan atau
dihasilkan ke dan dari sistem maka persamaan neraca energi tersebut menjadi,
Q = ∆H
Q = ∆H = Hproduk - Hreaktan
Jika tidak ada panas yang timbul akibat perubahan fasa materi pada suatu sistem
maka, Q = ∆H = (Σ n CP dT)keluar– (Σ n CP dT)masuk
Jika sistem yang ditinjau berada pada keadaan adiabatis maka,
0 = ∆H = (Σ n CP dT)keluar– (Σ n CP dT)masuk
(Σ n CP dT)keluar = (Σ n CP dT)masuk
Keterangan :
∆H = Perubahan Panas (kJ)
n = Kuantitas Materi (kmol)
CP = Kapasitas panas (kJ/kmol.K)
dT = Perbedaan temperatur (K)
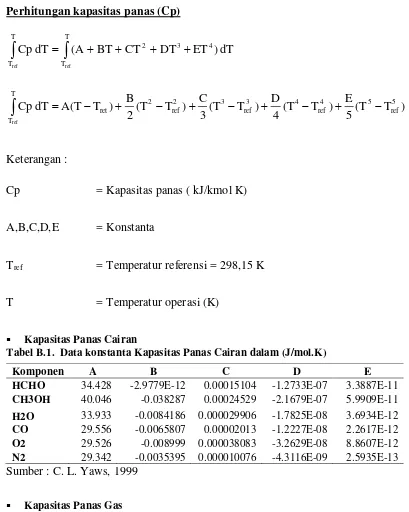
Perhitungan kapasitas panas (Cp)
T T
4 3 2
T
Tref ref
dT ) ET DT CT BT (A dT Cp ) T (T 5 E ) T (T 4 D ) T (T 3 C ) T (T 2 B ) T A(T dT
Cp ret 2 ref2 3 ref3 4 ref4 5 ref5
T Tref
Keterangan :Cp = Kapasitas panas ( kJ/kmol K)
A,B,C,D,E = Konstanta
Tref = Temperatur referensi = 298,15 K
T = Temperatur operasi (K)
Kapasitas Panas Cairan
Tabel B.1. Data konstanta Kapasitas Panas Cairan dalam (J/mol.K)
Sumber : C. L. Yaws, 1999
[image:35.595.107.516.81.593.2] Kapasitas Panas Gas
Tabel B.2. Data konstanta Kapasitas Panas Gas dalam (J/mol.K)
Komponen A B C D
CH3OH 40.152 0.31046 -0.0010291 1.4598E-06
H2O 92.053 -0.039953 -0.00021103 5.3469E-07
CO(NH)2 (urea) 24.856 0.14437 0.000038088 -1.1007E-07
Urea formaldehid -193.924 1.5238 0.0024738 Sumber : C. L. Yaws, 1999
Komponen A B C D E
HCHO 34.428 -2.9779E-12 0.00015104 -1.2733E-07 3.3887E-11
CH3OH 40.046 -0.038287 0.00024529 -2.1679E-07 5.9909E-11
H2O 33.933 -0.0084186 0.000029906 -1.7825E-08 3.6934E-12
CO 29.556 -0.0065807 0.00002013 -1.2227E-08 2.2617E-12
O2 29.526 -0.008999 0.000038083 -3.2629E-08 8.8607E-12
Berikut ini adalah perhitungan neraca panas pada masing-masing alat:
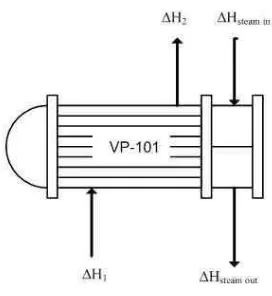
1. Neraca panas di sekitar Vaporizer
Fungsi : Menguapkan dan memanaskan campuran CH3OH fasa liquid
menjadi fasa uap pada temperatur 240oC sehingga siap diumpankan ke reaktor 201.
Gambar B.1 Aliran panas di sekitar Vaporizer
Dimana : ∆H1 = Laju alir panas CH3OH masuk vaporizer (kJ/jam)
∆H2 = Laju alir panas CH3OH keluar vaporizer (kJ/jam)
∆Hsteam in = Laju alir panas steam masuk (kJ/jam)
∆Hsteam out = Laju alir panas steam keluar (kJ/jam)
a. Panas masuk vaporizer (aliran 1)
T bahan = (273.15+30oC) = 303.15 K
[image:36.595.245.381.239.387.2]T ref = (273.15+25oC) = 298.15 K
Tabel B.3 Perhitungan ∆H masuk pada aliran 1
Komponen n (kmol) ſCP dT
(kJ/kmol) ∆
H 1
(kJ/jam)
CH3OH 43.15697532 400.7148235 17293.63975
H2O 0.076624098 377.4863816 28.92455339
b. Panas keluar vaporizer (aliran 2)
T out = (273.15+240oC) = 513.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.4 Perhitungan ∆H keluar pada aliran 2
c. Menghitung laju alir massa dan laju alir panas steam ∆Hsteam = ∆H1 - ∆H2
= 484798.7334 - 17322.5643
= 467476.1691 kJ/jam
Data steam pada T = (273.15+300oC) = 573.15 K dan P = 8581 kPa:
Hl = 1344 kJ/kg
Hv = 2749 kJ/kg
λs = Hv– Hl = 2749– 1344= 1405 kJ/kg
Maka massa steam:
= ∆�
� =
467476.1691 kJ/jam
1405 �/ = 332.723252 /
Panas steammasuk (∆Hsteam in)
∆Hsteam in = Ws x Hv = (332.723252 kg/jam) . (2749 kJ/kg)
= 914656.2198 kJ/jam
Panas steamkeluar (∆Hsteam out)
∆Hsteam out = Ws x Hl = (332.723252 kg/jam) . (1344 kJ/kg)
= 447180.0507 kJ/jam
Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 2
(kJ/jam)
CH3OH 43.15697532 11220.25118 484232.1031
H2O 0.076624098 7394.93588 566.6302895
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen
[image:38.595.248.389.378.509.2]maka dapat disusun tabel neraca panas komponen sebagai berikut:
Tabel B.5 Neraca panas di sekitar Vaporizer (VP-101)
Komponen Aliran Input (kJ/jam) Aliran Output (kJ/jam)
∆H1 ∆Hsteam in ∆H2 ∆Hsteam out
CH3OH 17293.63975 0,000 484232.1031 0,000
H2O 28.92455339 566.6302895
Steam 0,000 914656.2198 0,000 447180.0507
Sub Total 17322.5643 914656.2198 484798.7334 447180.0507
Total 931978.7841 931978.7841
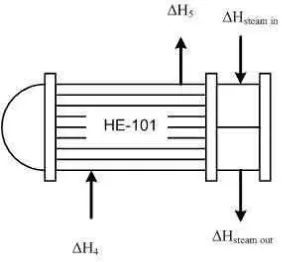
2. Neraca panas di sekitar Heater (HE-101)
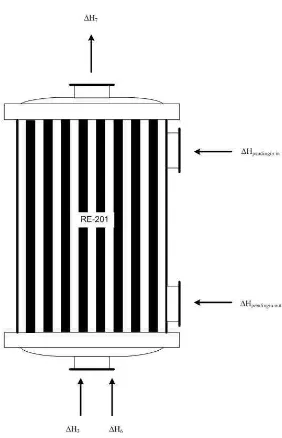
Fungsi : Memanaskan umpan udara pada temperatur 240oC sehingga siap diumpankan ke reaktor 201.
Gambar B.2 Aliran panas di sekitar Heater
Dimana : ∆H4 = Laju alir panas udara masuk (kJ/jam)
∆H5 = Laju alir panas udara keluar (kJ/jam)
∆Hsteam in = Laju alir panas steam masuk (kJ/jam)
a. Panas masuk heater (aliran 4)
T bahan = (273.15+30oC) = 303.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.6 Perhitungan ∆H keluar pada aliran 4
b. Panas keluar heater (aliran 5)
T out = (273.15+240oC) = 513.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.7 Perhitungan ∆H keluar pada aliran 5
c. Menghitung laju alir massa dan laju alir panas steam ∆Hsteam= ∆H5 - ∆H4
= (1448176.147- 33283.74901) kJ/jam
= 1414892.398 kJ/jam
Data steam pada T = (273.15+300oC) = 573.15 K dan P = 8581 kPa: Hl = 1344 kJ/kg
Hv = 2749 kJ/kg
λs = Hv– Hl = 2749– 1344= 1405 kJ/kg
Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 4
(kJ/jam)
O2 47.9521948 147.2424553 7060.598899
N2 180.39159 145.3679194 26223.15011
Total 228.3437847 33283.74901
Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 5
(kJ/jam)
O2 47.9521948 6499.833912 311681.3019
N2 180.39159 6300.154265 1136494.845
Maka massa steam:
= ∆�
� =
1414892.398 kJ/jam
1405 �/ = 1007.040852 /
Panas steammasuk (∆Hsteam in)
∆Hsteam in = Ws x Hv = (1007.040852 kg/jam) . (2749 kJ/kg)
= 2768355.304 kJ/jam
Panas steamkeluar (∆Hsteam out)
∆Hsteam out = Ws x Hl = (1007.040852 kg/jam). (1344 kJ/kg)
= 1353462.906 kJ/jam
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen
[image:40.595.131.521.456.552.2]maka dapat disusun tabel neraca panas komponen sebagai berikut:
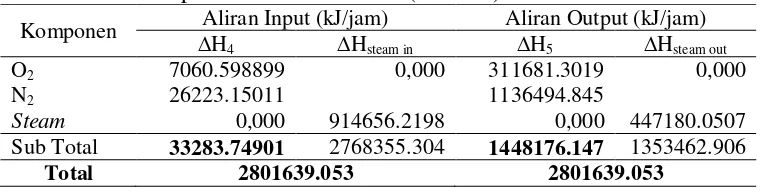
Tabel B.8. Neraca panas di sekitar Heater (HE-101)
Komponen ∆Aliran Input (kJ/jam) Aliran Output (kJ/jam)
H4 ∆Hsteam in ∆H5 ∆Hsteam out
O2 7060.598899 0,000 311681.3019 0,000
N2 26223.15011 1136494.845
Steam 0,000 914656.2198 0,000 447180.0507
Sub Total 33283.74901 2768355.304 1448176.147 1353462.906
3. Neraca panas di sekitar Reaktor (R-201)
Fungsi : Mereaksikan CH3OHfasa gas dengan gas O2sehingga akan terbentuk
[image:41.595.257.398.167.386.2]produk utama berupa HCHO
Gambar B.3 Aliran panas di sekitar Reaktor
Dimana : ∆H3 = Laju alir panas umpan CH3OH dari Vaporizer 101 (kJ/jam)
∆H6 = Laju alir panas umpan udara dari Heater 101 (kJ/jam)
∆H7 = Laju alir panas produk yang keluar Reaktor 201 (kJ/jam)
∆Hpendingin in = Laju alir panas air pendingin masuk (kJ/jam)
∆Hpendingin out = Laju alir panas air pendingin keluar (kJ/jam)
a. Panas masuk pada aliran 3
Panas masuk pada aliran 3 sama dengan panas keluar dari Vaporizer 101
yaitu 484798.7334 kJ/jam.
b. Panas masuk pada aliran 6
Panas masuk pada aliran 6 sama dengan panas keluar dari Heater 101
Iron Molybdenum
c. Panas keluar pada aliran 7
T in = (273.15+240oC) = 513.15 K T ref = (273.15+25oC) = 298.15 K
Tabel B.9 Perhitungan ∆H keluar pada aliran 7 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 7
(kJ/jam)
CH3OH 0.431569753 10220.03597 4410.658402
O2 25.30772985 5975.158224 151217.6901
HCHO 40.16188123 10148.24956 407572.7935
H2O 45.36578351 6799.57522 308468.0574
N2 180.39159 5800.479015 1046357.632
CO 2.563524334 5831.053867 14948.04848
Total 294.2220786 1932974.88
d. Menghitung panas reaksi
Reaksi yang terjadi di Reaktor:
CH3OH(g) + ½ O2(g) HCHO(g) + H2O(g)
Reaksi samping :
HCHO(g) + ½ O2(g) CO(g) + H2O(g) (Mc. Ketta, 1988)
Neraca panas umum di Reaktor:
� �
� �
� �
�
=
� ��
� ��
� �
� � −
� �
� �
�
+
� �
� � �
� � �
�
−
� �
�
� � �
� �
(Pers. 8.2, Fogler., H. Scott, 3rd Ed)
Diasumsikan steady state maka akumulasi = 0 sehingga,
0 = − + − � �
0 = − + �0 � �0− � =1
− ∆� (�) �0
Karena sangat kecil dibandingkan dengan ∆� (�) �0 maka dapat
Reaktor dioperasikan secara isotermal maka �0 =1� �0− � = 0
sehingga,
0 = − ∆� (�) �0
= ∆� (�) �0
dimana:
∆� � = ∆� � + �
�
�
− � �
�
�
Panas pembentukan standar (∆HoRx 298,15 K)
Data ∆Ho
Rx masing-masing komponen pada keadaan standar
(298,15 K):
ΔHfo CH3OH(g) = -48,08 kcal/mol
ΔHfo O2(g) = 0 kcal/mol
ΔHfo HCHO(g) = -28,29 kcal/mol
ΔHfo H2O(g) = -57,7979 kcal/mol
ΔHfo CO (g) = -26,216 kcal/mol
(Perry, 1997)
∆HoRx 298,15 K = ΔHfo CH3OH(g) x mol CH3OH(g)
= -20116.672 kj/kmol x 42.72 kmol
= -859492.9698 kj
Total ∆HoRx = ∆Hproduk - ∆Hreaktan
= ΔHfo (HCHO(g)+ H2O(g)+CO(g)) - ΔHfo (CH3OH(g) + O2(g))
Tabel B.10 Perhitungan ∆HoRx 298,15 K
Komponen ΔHf
o
(kJ/kmol)
∆HoRx 298,15 K (kJ) CH3OH -20116.672 -859492.9698
O2 0 0
HCHO -11836.536 -505720.8011
H2O -24179.336 -1033071.937
CO -10968.7744 -28118.72009
∆H reaktan
Perubahan entalpi reaktan dari 513.15 K ke 298,15 K dapat ditentukan
dengan menggunakan persamaan berikut :
∆� = � �
513 .15
298,15
Hasil perhitungan perubahan entalpi reaktan dapat dilihat pada tabel
berikut :
Tabel B.11 Perhitungan ∆Horeaktan
Komponen ∆H
o reaktan
(kJ/kmol)
n (kmol) ∆H reaktan
(kJ)
CH3OH 10220.03597 43.15697532 484232.1031
O2 5975.158224 47.9521948 311681.3019
Total 91.10917011 795913.405
∆H produk
Perubahan entalpi produk dari 298,15 K ke 513.15 K dapat ditentukan
dengan menggunakan persamaan berikut:
∆� = �
513 .15
298 ,15
Hasil perhitungan perubahan entalpi produk dapat dilihat pada tabel
berikut :
Tabel B.12 Perhitungan ∆Hoproduk
Komponen ∆H
o produk
(kJ/kmol)
n (kmol) ∆H produk
(kJ)
CH3OH 10220.03597 0.431569753 4410.658402
O2 5975.158224 26.58949201 158876.4219
HCHO 10148.24956 42.72540556 433588.0782
H2O 6799.57522 42.72540556 290514.6089
CO 5831.053867 2.563524334 14948.04848
Sehingga : ∆Hreaksi = (∆H
o
Rx 298,15 K + ∆Hoproduk - ∆Horeaktan)
= (-707418.4882 + 902337.8159 - 795913.405) = 600994.0773 kj/jam
e. Menghitung kebutuhan air pendingin
Panas yang harus diserap = ∆Hreaksi
Kondisi media pendingin :
Jenis pendingin : Air
T in = (273.15+30oC) = 303.15 K
T out = (273.15+60oC) = 333.15 K (Kern,594)
T ref = (273.15+25oC) = 298.15 K
Sehingga didapat,
ſCP dT = 2256.67 9 kj/kmol
mol pendingin =
(ſCP dT)
= 600994 .0774 �/
2256.67 9 kj/kmol
= 266.317 kmol/jam
massapendingin = mol pendingin x mr
= 266.317 kmol/jam x 18 kmol/kg
= 4793.72 kg/jam
Menghitung Q pendingin :
∆H pendingin in = n ſCP dT
= 100531.347 kj/jam ∆H pendingin out = n ſCP dT
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen
[image:46.595.106.563.154.311.2]maka dapat disusun tabel neraca panas komponen sebagai berikut:
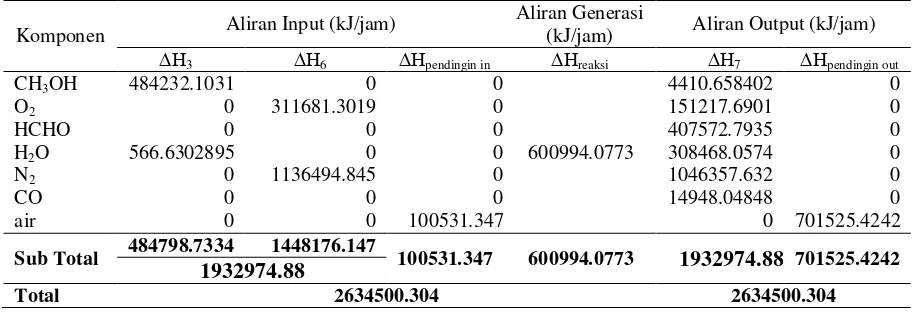
Tabel B.13 Neraca panas di sekitar Reaktor (RE-201)
Komponen Aliran Input (kJ/jam)
Aliran Generasi
(kJ/jam) Aliran Output (kJ/jam)
∆H3 ∆H6 ∆Hpendingin in ∆Hreaksi ∆H7 ∆Hpendingin out
CH3OH 484232.1031 0 0
600994.0773
4410.658402 0
O2 0 311681.3019 0 151217.6901 0
HCHO 0 0 0 407572.7935 0
H2O 566.6302895 0 0 308468.0574 0
N2 0 1136494.845 0 1046357.632 0
CO 0 0 0 14948.04848 0
air 0 0 100531.347 0 701525.4242
Sub Total 484798.7334 1448176.147 100531.347 600994.0773 1932974.88 701525.4242
1932974.88
Total 2634500.304 2634500.304
4. Neraca panas di sekitar cooler (CO-201)
Fungsi : Menurunkan temperatur keluaran reaktor 201 dari temperatur 240 oC menjadi 70oC
Gambar B.4 Aliran panas di sekitar cooler
Dimana : ∆H7 = Laju alir panas masuk cooler (kJ/jam)
∆H8 = Laju alir panas keluar cooler (kJ/jam)
∆Hpendingin in = Laju alir panas pendingin masuk (kJ/jam)
[image:46.595.243.399.429.561.2]a. Panas masuk cooler (aliran 7)
Panas masuk ke dalam cooler 201 adalah panas keluaran reaktor 201.
T bahan = (273.15+240oC) = 513.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.14.Perhitungan ∆H keluar pada aliran 7 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 7
(kJ/jam) CH3OH 0.431569753 10220.03597 4410.658402
O2 25.30772985 5975.158224 151217.6901
HCHO 40.16188123 10148.24956 407572.7935
H2O 45.36578351 6799.57522 308468.0574
N2 180.39159 5800.479015 1046357.632
CO 2.563524334 5831.053867 14948.04848
Total 294.2220786 1932974.88
b. Panas keluar cooler (aliran 8)
T out = (273.15+70oC) = 343.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.15 Perhitungan ∆H keluar pada aliran 8 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 8
(kJ/jam) CH3OH 0.431569753 2091.947151 902.8211158
O2 25.30772985 1330.921526 33682.60243
HCHO 40.16188123 2075.676344 83363.06679
H2O 45.36578351 3385.062502 153566.0127
N2 180.39159 1309.709767 236260.6272
CO 2.563524334 1311.212204 3361.324391
Total 294.2220786 511136.4546
c. Menghitung kebutuhan pendingin
Panas yang harus diserap = ∆H7 - ∆H8
= (1932974,88-511136,4546) kg/jam
Kondisi media pendingin :
Jenis pendingin : Air
T in = (273.15+30oC) = 303.15 K
T out = (273.15+45oC) = 323.15 K (Kern,594)
T ref = (273.15+25oC) = 298.15 K
Sehingga didapat,
ſCP dT = 1881,178293 kj/kmol
mol pendingin =
(ſCP dT)
= 1421838 ,43 �/
1881,1782 kj/kmol
= 755,8233 kmol/jam
massapendingin = mol pendingin x mr
= 755,8233 kmol/jam x 18 kmol/kg
= 13604,81973 kg/jam
Menghitung Q pendingin :
∆H pendingin in = n ſCP dT
= 302869,608 kj/jam ∆H pendingin out = n ſCP dT
Setelah dilakukan perhitungan neraca panas pada masing-masing
komponen maka dapat disusun tabel neraca panas komponen sebagai
[image:49.595.276.363.452.627.2]berikut:
Tabel B.16. Neraca panas di sekitar Cooler (CO-201)
Komponen Aliran Input (kJ/jam) ∆ Aliran Output (kJ/jam)
H7 ∆Hpendingin in ∆H8 ∆Hpendingin out
CH3OH 4410.658402 0,000 902.8211158 0,000
O2 151217.6901 33682.60243
HCHO 407572.7935 83363.06679
H2O 308468.0574 153566.0127
N2 1046357.632 236260.6272
CO 14948.04848 3361.324391
Air 0,000 302869,61 0,000 1707151,44
Sub Total 1932974.88 302869,61 511136.4546 1707151,44
Total 2235844,489 2235844,489
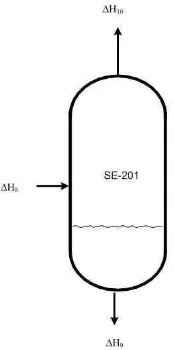
5. Neraca panas di sekitar separator (SE-201)
Fungsi : Memisahkan fasa liquid dan fasa gas produk keluaran cooler 201
Gambar B.5 Aliran panas di sekitar separator
Dimana : ∆H8 = Laju alir panas masuk separator (kJ/jam)
∆H9 = Laju alir panas keluar bagian bawah separator (kJ/jam)
a. Panas masuk separator (aliran 8)
Panas masuk ke dalam separator 201 adalah panas keluaran cooler
201.
T in = (273.15+70oC) = 343.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.17 Perhitungan ∆H keluar pada aliran 8 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 8
(kJ/jam) CH3OH 0.431569753 2091.947151 902.8211158
O2 25.30772985 1330.921526 33682.60243
HCHO 40.16188123 2075.676344 83363.06679
H2O 45.36578351 3385.062502 153566.0127
N2 180.39159 1309.709767 236260.6272
CO 2.563524334 1311.212204 3361.324391
Total 294.2220786 511136.4546
b. Panas keluar cooler (aliran 9)
T out (trial) = (273.15+70oC) = 343.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.18 Perhitungan ∆H keluar pada aliran 9 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 9
(kJ/jam)
H2O 45.36578351 3385.062502 153566.0127
Total 45.36578351 3385.062502 153566.0127
c. Panas keluar cooler (aliran 10)
T out (trial) = (273.15+70oC) = 343.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.19 Perhitungan ∆H keluar pada aliran 10 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 10
(kJ/jam)
CH3OH 0.431569753 2091.947151 902.8211158
O2 25.30772985 1330.921526 33682.60243
HCHO 40.16188123 2075.676344 83363.06679
N2 180.39159 1309.709767 236260.6272
CO 2.563524334 1311.212204 3361.324391
Setelah dilakukan perhitungan neraca panas pada masing-masing
komponen maka dapat disusun tabel neraca panas komponen sebagai
[image:51.595.175.477.181.327.2]berikut:
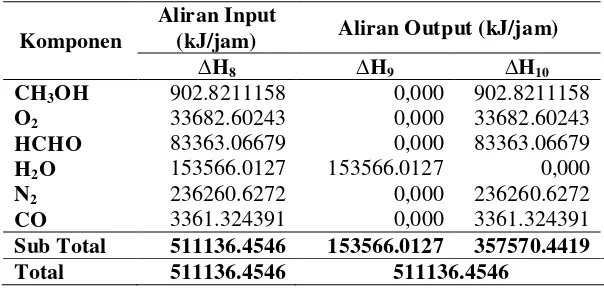
Tabel B.20. Neraca panas di sekitar Separator (SE-201)
Komponen
Aliran Input
(kJ/jam) Aliran Output (kJ/jam)
∆H8 ∆H9 ∆H10
CH3OH 902.8211158 0,000 902.8211158
O2 33682.60243 0,000 33682.60243
HCHO 83363.06679 0,000 83363.06679
H2O 153566.0127 153566.0127 0,000
N2 236260.6272 0,000 236260.6272
CO 3361.324391 0,000 3361.324391
Sub Total 511136.4546 153566.0127 357570.4419
Total 511136.4546 511136.4546
6. Neraca panas di sekitar Heater (HE-102)
Fungsi : Memanaskan air umpan untuk pelarut urea pada temperatur 42oC
Gambar B.6 Aliran panas di sekitar Heater
Dimana : ∆H13 = Laju alir panas air masuk (kJ/jam)
∆H14 = Laju alir panas air keluar (kJ/jam)
∆Hsteam in = Laju alir panas steam masuk (kJ/jam)
[image:51.595.241.387.447.575.2]a. Panas masuk heater (aliran 13)
T bahan = (273.15+30oC) = 303.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.21 Perhitungan ∆H keluar pada aliran 13
b. Panas keluar heater (aliran 14) T out = (273.15+42oC) = 315.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.22 Perhitungan ∆H keluar pada aliran 14
c. Menghitung laju alir massa dan laju alir panas steam ∆Hsteam= ∆H14 - ∆H13
= (45738.60543- 13473.06038) kJ/jam
= 32265.54505 kJ/jam
Data steam pada T = (273.15+300oC) = 573.15 K dan P = 8581 kPa:
Hl = 1344 kJ/kg
Hv = 2749 kJ/kg
λs = Hv– Hl = 2749– 1344= 1405 kJ/kg
Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 13
(kJ/jam)
H2O 35.69151374 377.4863816 13473.06038
Total 35.69151374 13473.06038
Komponen n (kmol) ſCP dT
(kJ/kmol) ∆
H 14
(kJ/jam)
H2O 35.69151374 1281.498055 45738.60543
Maka massa steam:
= ∆�
� =
32265.54505 kJ/jam
1405 �/ = 22.96480075 /
Panas steammasuk (∆Hsteam in)
∆Hsteam in = Ws x Hv = (22.96480075 kg/jam) . (2749 kJ/kg)
= 63130.23726 kJ/jam
Panas steamkeluar (∆Hsteam out)
∆Hsteam out = Ws x Hl = (22.96480075 kg/jam). (1344 kJ/kg)
= 30864.69221 kJ/jam
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen
[image:53.595.130.524.458.546.2]maka dapat disusun tabel neraca panas komponen sebagai berikut:
Tabel B.23. Neraca panas di sekitar Heater (HE-102)
Komponen ∆Aliran Input (kJ/jam) Aliran Output (kJ/jam)
H13 ∆Hsteam in ∆H14 ∆Hsteam out
H2O 13473.06038 0,000 45738.60543 0,000
Steam 0,000 63130.23726 0,000 30864.69221
Sub Total 13473.06038 63130.23726 45738.60543 30864.69221
7. Neraca panas di sekitar Mixing Tank (MT-101)
Fungsi : Melarutkan urea ( CO(NH)2 )menggunakan air sebagai umpan reaktor
202
Gambar B.7 Aliran panas di sekitar Mixing Tank
Dimana : ∆H12 = Laju alir panas CO(NH)2 (kJ/jam)
∆H14 = Laju alir panas air (kJ/jam)
∆H15 = Laju alir panas CO(NH)2solution (kJ/jam)
Neraca Energi di Mixing Tank:
{(∆H12+ ∆H14) –(∆H15) + (∆Hpengenceran) – (0)} = {0}
(∆H12+ ∆H14+ ∆Hpengenceran) –∆H3 = 0
[image:54.595.278.349.178.321.2]1) Panas masuk pada aliran 12 T in = (273.15+30oC) = 303.15 K T ref = (273.15+25oC) = 298.15 K
Tabel B.24 Perhitungan ∆H masuk pada aliran 12 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 12
(kJ/jam)
CO(NH)2 0.698361818 377.4863816 263.6220758
H2O 28.68705802 343.5612713 9855.762124
2) Panas masuk pada aliran 14
T in = (273.15+42oC) = 315.15 K T ref = (273.15+25oC) = 298.15 K
Tabel B.25 Perhitungan ∆H masuk pada aliran 14 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 14
(kJ/jam)
H2O 35.69151374 1281.498055 45738.60543
Total 35.69151374 45738.60543
3) Panas pengenceran
Diketahui : Panas pelarutan CO(NH)2 = 0.32 kkal/kgr.C (Sumber: Perry ed.8, Tabel 2-182)
Massa CO(NH)2 yang akan dilarutkan sebanyak = 1722.94 kg/jam
Maka panas pengenceran :
∆Hpengenceran = Panas pelarutan CO(NH)2 x massa CO(NH)2 x Temperatur
pelarutan
∆Hpengenceran = (0.32 kkal/kg.C).(1722.94 kg/jam).(70oC)
∆Hpengenceran = (39013.58135 kkal/jam . 4.184 ) = 163232.8244 kj/jam
4) Menghitung panas dan temperatur pada aliran 15
Untuk mendapatkan temperatur keluaran dari Mixing Tank maka perlu
dilakukan perhitungan trial and error dimana ∆Hhitung harus sama dengan
∆H15. Dengan bantuan solver Excel maka didapatkan hasil sebagai berikut:
Neraca energi:
(∆H12+ ∆H14+ ∆Hpengenceran) –∆H15 = 0
∆H15= ∆H12+ ∆H14+ ∆Hpengenceran
T in (trial) = (273.15+70oC) = 343.15 K T ref = (273.15+25oC) = 298.15 K
Tabel B.26 Perhitungan ∆H keluar pada aliran 15 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 12
(kJ/jam)
CO(NH)2 36.38987556 3442.220627 125261.9803
H2O 28.68705802 3270.772264 93828.83372
Total 65.07693358 219090.814
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen
maka dapat disusun tabel neraca panas komponen sebagai berikut:
Tabel B.27 Neraca panas di sekitar Mixing Tank (MT-101)
Komponen Aliran Input (kJ/jam)
Aliran Generasi (kJ/jam)
Aliran Output (kJ/jam)
∆H12 ∆H14 ∆H15
CO(NH)2 263.6220758 0,000 0,000 125261.9803
H2O 9855.762124 45738.60543 0,000 93828.83372
Qpengenceran 0,000 0,000 163232.8244 0,000
Sub Total 10119.3842 45738.60543 163232.8244 219090.814
Total 219090.814 219090.814
8. Neraca panas di sekitar Reaktor (R-202)
Fungsi : Mereaksikan gas HCHO dengan CO(NH)2 solution sehingga akan
terbentuk produk utama berupa urea formaldehid
[image:56.595.270.390.540.711.2]Dimana : ∆H11 = Laju alir panas umpan HCHO dari separator 101(kJ/jam)
∆H16= Laju alir panas umpan CO(NH)2 solution dari
mixing tank 101 (kJ/jam)
∆H17 = Laju alir panas gas buang yang keluar Reaktor 202 (kJ/jam)
∆H18 = Laju alir panas produk yang keluar Reaktor 202 (kJ/jam)
∆Hpendingin in = Laju alir panas air pendingin masuk (kJ/jam)
∆Hpendingin out = Laju alir panas air pendingin keluar (kJ/jam)
a. Panas masuk pada aliran 11
Panas masuk pada aliran 11 sama dengan panas keluar dari bagian atas
separator 101 yaitu 357570.4419 kJ/jam.
b. Panas masuk pada aliran 16
Panas masuk pada aliran 16 sama dengan panas keluar dari mixing tank
101 yaitu 219090.814 kJ/jam.
c. Panas keluar pada aliran 17
T out = (273.15+70oC) = 343.15 K T ref = (273.15+25oC) = 298.15 K
Tabel B.28 Perhitungan ∆H keluar pada aliran 17 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 17
(kJ/jam)
CH3OH 0.431569753 1131.895275 488.4917643
O2 25.30772985 728.0767291 18425.96917
HCHO 1.63295561 1122.476318 1832.954001
CO 2.563524334 718.1914824 1841.101342
N2 180.39159 717.6769064 129462.8782
d. Panas keluar pada aliran 18
T out = (273.15+70oC) = 343.15 K T ref = (273.15+25oC) = 298.15 K
Tabel B.29 Perhitungan ∆H keluar pada aliran 18 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 17
(kJ/jam)
H2O 36.38987556 1858.413618 67627.44028
CO(NH)2 0.860611741 1728.432663 1487.509443
UF1 19.26446281 12775.43342 246111.8619
UF2 6.421487603 12775.43342 82037.28731
UF3 2.140495868 12775.43342 27345.76244
Total 65.07693358 424609.8614
e. Menghitung panas reaksi
Reaksi yang terjadi di Reaktor:
) ( 2 2 (g) 2 ) ( 2
2) 18CH O 9HOCH NHCONH CO(NH
13 l l
3(l) 2 (l)
2
2OH) NHCON(CH OH)
NHCONH(CH 3
(Kirk – Othmer, 1955).
Neraca panas umum di Reaktor:
� � � � � � � = � �� � �� � � � � − � � � � � + � � � � � � � � � − � � � � � � � �
(Pers. 8.2, Fogler., H. Scott, 3rd Ed)
Diasumsikan steady state maka akumulasi = 0 sehingga,
0 = − + − � �
0 = − + �0 � �0− � =1
− ∆� (�) �0
Karena sangat kecil dibandingkan dengan ∆� (�) �0 maka dapat
diabaikan. Reaktor dioperasikan secara isotermal maka �0 =1� �0−
0 = − ∆� (�) �0
= ∆� (�) �0
dimana:
∆� � = ∆� � + �
�
�
− � �
�
�
Panas pembentukan standar (∆HoRx 298,15 K)
Data ∆Ho
Rx masing-masing komponen pada keadaan standar
(298,15K):
ΔHfo CO(NH2)2 = -26,0045 kcal/mol
ΔHfo CH2O(g) = -26,880 kcal/mol
ΔHfo UF 1 = -62,658 kcal/mol
ΔHfo UF 2 = -99,271 kcal/mol
ΔHfo UF 3 = -137,706 kcal/mol
(Perry, 1997)
∆HoRx 298,15 K = ΔHfo CO(NH2)2 (g) x mol CO(NH2)2 (g)
= -112465.92 kj/kmol x 27.82 kmol
= -4333191.066 kj
Total ∆HoRx = ∆Hproduk - ∆Hreaktan
= ΔHfo (UF 1+ UF 2 + UF 3) - ΔHfo (CO(NH2)2+ CH2O)
Tabel B.30 Perhitungan ∆HoRx 298,15 K
Komponen ΔHf
o
(kJ/kmol)
∆HoRx 298,15 K (kJ)
HCHO -112465.92 -4333191.066
CO(NH)2 -108802.828 -3027596.049
UF1 -262161.072 -5050392.222
UF2 -415349.864 -2667164.003
UF3 -576161.904 -1233272.175
∆H reaktan
Perubahan entalpi reaktan dari 343.15 K ke 298,15 K dapat ditentukan
dengan menggunakan persamaan berikut :
∆� = � �
343 .15
298,15
Hasil perhitungan perubahan entalpi reaktan dapat dilihat pada tabel
berikut :
Tabel B.31 Perhitungan ∆Horeaktan
Komponen ∆H
o reaktan
(kJ/kmol)
n (kmol) ∆H reaktan
(kJ)
HCHO 2075.676344 40.16188123 83363.06679
CO(NH)2 3214.083374 28.68705802 92202.59624
Total 68.84893925 175565.663
∆H produk
Perubahan entalpi produk dari 298,15 K ke 343.15 K dapat ditentukan
dengan menggunakan persamaan berikut:
∆� = �
343 .15
298 ,15
Hasil perhitungan perubahan entalpi produk dapat dilihat pada tabel
berikut :
Tabel B.32 Perhitungan ∆Hoproduk
Komponen ∆H
o produk
(kJ/kmol) n (kmol)
∆H produk
(kJ)
HCHO 1122.476318 1.63295561 1832.954001
CO(NH)2 1728.432663 0.860611741 1487.509443
UF1 12775.43342 19.26446281 246111.8619
UF2 12775.43342 6.421487603 82037.28731
UF3 12775.43342 2.140495868 27345.76244
Sehingga :
∆Hreaksi= ∆HoRx 298,15 K + ∆Hoproduk - ∆Horeaktan
= -1590041.284 + 358815.3751 - 175565.663
= 1406791.572 kj/jam
f. Menghitung kebutuhan pendingin
Panas yang harus diserap = ∆Hreaksi
Kondisi media pendingin :
Jenis pendingin : Air
T in = (273.15+30oC) = 303.15 K
T out = (273.15+60oC) = 333.15 K (Kern,594)
T ref = (273.15+25oC) = 298.15 K
Sehingga didapat,
ſCP dT = 2256.67 9 kj/kmol
mol pendingin =
(ſCP dT)
= 1406791 .572 �/
2256.67 9 kj/kmol
= 623.389 kmol/jam
massapendingin = mol pendingin x mr
= 623.389 kmol/jam x 18 kmol/kg
= 11221.018 kg/jam
Menghitung Q pendingin :
∆H pendingin in = n ſCP dT
= 235321.207 kj/jam ∆H pendingin out = n ſCP dT
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen
[image:62.595.55.574.179.380.2]maka dapat disusun tabel neraca panas komponen sebagai berikut:
Tabel B.33 Neraca panas di sekitar Reaktor (RE-202)
Komponen Aliran Input (kJ/jam)
Aliran Generasi
(kJ/jam) Aliran Output (kJ/jam)
∆H11 ∆H16 ∆Hpendingin in ∆Hreaksi ∆H17 ∆H18 ∆Hpendingin out
CH3OH 902.8211158 0 0
1406791.572
488.4917643 0 0
O2 33682.60243 0 0 18425.96917 0 0
HCHO 83363.06679 0 0 1832.954001 0 0
CO 3361.324391 0 0 1841.101342 0 0
N2 236260.6272 0 0 129462.8782 0 0
H2O 0 125261.9803 0 67627.44028
CO(NH)2 0 93828.83372 0 1487.509443
UF1 0 0 0 246111.8619
UF2 0 0 0 82037.28731
UF3 0 0 0 0 27345.76244 0
Amonia 0 0 235321.207 0 1642112.779
Sub Total 357570.4419 219090.814 235321.207 1406791.572 152051.3945 424609.8614 1642112.779
576661.2559 576661.2559
Total 2218774.035 2218774.035
9. Neraca panas di sekitar cooler (CO-301)
Fungsi : Menurunkan temperatur keluaran reaktor 202 dari temperatur 70 oC menjadi 30oC
Gambar B.9 Aliran panas di sekitar cooler
Dimana : ∆H18 = Laju alir panas keluaran reaktor 202 masuk (kJ/jam)
[image:62.595.231.408.513.661.2]∆Hpendingin in = Laju alir panas pendingin masuk (kJ/jam)
∆Hpendingin out = Laju alir panas pendingin keluar (kJ/jam)
a. Panas masuk cooler (aliran 18)
Panas masuk ke dalam cooler 301 adalah panas keluaran reaktor 202.
T in = (273.15+70oC) = 343.15 K
T ref = (273.15+25oC) = 298.15 K
Tabel B.34 Perhitungan ∆H keluar pada aliran 18 Komponen n (kmol) ſCP dT
(kJ/kmol)
∆H 18
<