ABSTRACT
HERITABILITY AND GENETIC PROGRESS OF RESISTANT CHARACTER IN SOYBEAN SECOND GENERATION (F2)
TANGGAMUS AND B3570CROSSING INFECTED BY SOYBEAN MOSAIC VIRUS
By
Tety Maryenti
The need of soybean (Glycine max[L.] Merrill) in Indonesia increases in line with
the growth of population. However , the need of soybean in Indonesia has not
been fulfilled yet, due to the lack of soybean yield. One of the reason is an
infection caused bysoybean mosaic virus(SMV). The aim of this study was to
determine (1) the estimation of broad sense heritability for disease severity and
agronomy characters, (2) predictive value of genetic advanced for disease severity
and agronomy characters, (3) expectation numbers of genotype which are resistant
to SMV and high yield . The study was conducted in September 2013 until
January 2014 at the Integrated Field Laboratory of the College of Agriculture and
Seed and Plant Breeding Laboratory , University of Lampung . The seed which
was used in this study from Tanggamus and B3570crossing (F2). Each plant was
inoculated by SMV , and disease severity and agronomy characters were observed
replications . The results indicated that (1) the estimation of broad-sense
heritability were high for disease severity character , plant height , number of pods
, number of filled pods , the number of seeds , the percentage of healthy seeds ,
the percentage of diseased seeds, seed weight per plant , and day of harvesting, (2)
predictive value of high genetic progress were high for disease severity character ,
plant height , number of pods , number of filled pods , number of seeds , the
percentage of healthy seeds , and seed weight per plant , (3) there were 19 selected
genotypes which were resistant and tolerans to SMV and high yield.
ABSTRAK
HERITABILITAS DAN KEMAJUAN GENETIK KARAKTER KETAHANAN KEDELAI GENERASI F2PERSILANGAN
TANGGAMUS x B3570TERHADAP SOYBEAN MOSAIC VIRUS
Oleh
Tety Maryenti
Kebutuhan kedelai (Glycine max [L.] Merrill) di Indonesia terus meningkat
seiring dengan pertambahan jumlah penduduk. Namun, kebutuhan kedelai dalam
negeri masih belum terpenuhi karena produksi kedelai yang rendah. Salah satu
penyebab rendahnya produktivitas kedelai yaitu infeksi penyakit mosaik kedelai
yang disebabkan olehsoybean mosaic virus(SMV). Penelitian ini bertujuan untuk
mengetahui (1) besaran nilai duga heritabilitas arti luas pada berbagai karakter
keparahan penyakit dan agronomi (2) nilai duga kemajuan genetik pada berbagai
karakter keparahan penyakit dan agronomi, (3) nomor-nomor harapan benih yang
memiliki ketahanan terhadap SMV dan berproduksi tinggi. Penelitian
dilaksanakan pada bulan September 2013 sampai dengan Januari 2014 di
Laboratorium Lapangan Terpadu Fakultas Pertanian Universitas Lampung,
kemudian pengamatan dilanjutkan Laboratorium Benih dan Pemuliaan Tanaman
Tanggamus x B3570 generasi F2. Setiap tanaman diinokulasi dengan SMV.
Kemudian diamati keparahan penyakit dan karakter agronominya. Rancangan
percobaan yang digunakan adalah rancangan percobaan tanpa ulangan. Hasil
penelitian menunjukkan (1) besaran nilai duga heritabilitas arti luas yang tinggi
terdapat pada karakter keparahan penyakit, tinggi tanaman, total jumlah polong,
jumlah polong bernas, total jumlah biji, persentase biji sehat, persentase biji sakit,
bobot biji pertanaman, dan umur panen, (2) nilai duga kemajuan genetik yang
tinggi terdapat pada karakter keparahan penyakit, tinggi tanaman, total jumlah
polong, jumlah polong bernas, total jumlah biji, persentase biji sehat, dan bobot
biji per tanaman, (3) terdapat 19 genotipe terpilih yang memiliki sifat tahan dan
tolerans terhadap SMV dan berproduksi tinggi.
HERITABILITAS DAN KEMAJUAN GENETIK KARAKTER KETAHANAN KEDELAI GENERASI F2PERSILANGAN
TANGGAMUS x B3570TERHADAP SOYBEAN MOSAIC VIRUS
Oleh
TETY MARYENTI
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA PERTANIAN
Pada
Jurusan Agroteknologi Fakultas Pertanian
UNIVERSITAS LAMPUNG BANDAR LAMPUNG
HERITABILITAS DAN KEMAJUAN GENETIK KARAKTER KETAHANAN KEDELAI GENERASI F2PERSILANGAN
TANGGAMUS x B3570TERHADAP SOYBEAN MOSAIC VIRUS
(Skripsi)
Oleh
TETY MARYENTI
FAKULTAS PERTANIAN UNIVERSITAS LAMPUNG
DAFTAR GAMBAR
Gambar Halaman
1. Tata letak penanaman benih kedelai hasil persilangan
Tanggamus x B3570dan kedua tetuanya...
37
2. Tahap-tahap inokulasisoybean mosaic virusdi lapangan... 38
iv DAFTAR ISI
Halaman
DAFTAR ISI ... iii
DAFTAR TABEL ... v
DAFTAR GAMBAR ... vi
I. PENDAHULUAN 1.1 Latar Belakang dan Masalah... 1
1.2 Tujuan Penelitian... 8
1.3 Kerangka Pemikiran... 9
1.4 Hipotesis... 12
II. TINJAUAN PUSTAKA 2.1 Tanaman Kedelai... 13
2.1.1 Sejarah tanaman kedelai... ... 13
2.1.2 Taksonomi tanaman kedelai... 13
2.1.3 Morfologi tanaman kedelai... 14
2.1.4 Syarat tumbuh tanaman kedelai... 20
2.2 Soybean Mosaic Virus (SMV) ... 20
2.2.1 Sejarah soybean mosaic virus... 20
2.2.2 Karakter soybean mosaic virus... 21
2.2.3 Penularan... 22
2.2.4 Gejala soybean mosaic virus... 22
2.2.5 Kisaran inang... 22
2.2.6 Pengendalian soybean mosaic virus... 23
2.3 Ketahanan Tanaman terhadap Penyakit... 23
2.3.1 Ketahanan horisontal... 23
2.3.2 Ketahanan vertikal... 24
2.3.3 Ketahanan tanaman terhadap infeksi virus... 25
2.4 Heritabilitas... ... 26
2.5 Kemajuan Genetik... 29
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian... 30
iv
3.3 Metode Penelitian... 31
3.4 Analisis Data... 32
3.5 Pelaksanaan Penelitian... 35
3.5.1 Pembuatan larutan buffer fosfat... 35
3.5.2 Perbanyakan inokulum soybean mosaic virus... 35
3.5.3 Persiapan lahan... 36
3.5.4 Penanaman... 36
3.5.5 Pemupukan... 37
3.5.6 Inokulasi soybean mosaic virus di lapangan... 38
3.5.7 Pelabelan... 38
3.5.8 Perawatan dan pemeliharaan tanaman... 38
3.5.9 Pemanenan... 39
3.5.10 Pengamatan... 39
IV. HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian... 42
4.2 Pembahasan... 46
V. KESIMPULAN DAN SARAN 5.1 Kesimpulan... 53
5.2 Saran... 53
DAFTAR TABEL
Tabel Halaman
1 Tabel intensitas seleksi pada kemajuan genetik... 34
2 Nilai tengah populasi F2hasil persilangan Tanggamus x B3570. 42 3 Nilai heritabilitas dalam arti luas populasi F2hasil persilangan Tanggamus dan B3570... 43 4 Nilai kemajuan genetik populasi F2hasil persilangan Tanggamus dan B3570... 44 5 Peringkat genotipe F2hasil persilangan Tanggamus dan B3570 berdasarkan keparahan penyakit (%), bobot biji sehat per tanaman (g), bobot biji sakit (g), dan persentase bobot biji sakit (%)…... 45 6 Persilangan Tanggamus x B3570... 62
7 Tetua Tanggamus... 66
8 Tetua B3570... 67
9 Keragaman dan heritabilitas... 68
Kebahagiaan tak selamanya terlahir dari apa yg kita miliki, melainkan juga dari
apa yg kita syukuri
(Anonim)
Bersyukur itu tidak berhenti pada menerima apa adanya saja, tapi terutama bekerja
keras untuk mendapatkan yang terbaik.
(Mario Teguh)
You are the person who chosen to live this life by God. Why God chose you?
Because you have the strength to cope with any difficulties that given
(Anonim)
The strength given to you, is the key for you to embrace and beatify the people
around you, so keep struggling for them.
Dengan menyebut nama Allah yang Maha Pengasih dan Maha Penyayang
Kupersembahkan buah karya kecilku kepada Ayahanda Firdaus dan Ibunda Martini sebagai perwujudan rasa sayang dan cintaku kepada mereka yang
senantiasa memanjatkan doa untukku di setiap sujudnya.
Serta kakakku Elvi Sumarni dan adikku tersayang Habibur Rahman Hakim yang senantiasa memberikan dorongan semangat dan mengharapkan keberhasilanku, serta adikku Alm. Eva Novita yang akan
selalu kusayangi. Terima kasih telah menjadi warna dalam hidupku.
Terima kasih untuk para Sahabat dan Teman-temanku atas semangat, kesabaran, doa, dan bantuannya serta Almamaterku Agroteknologi,
RIWAYAT HIDUP
Penulis dilahirkan di Kota Bandar Lampung pada 16 Agustus 1992, sebagai anak
kedua dari empat bersaudara dari pasangan Bapak Firdaus dan Ibu Martini.
Pendidikan Sekolah Dasar diselesaikan di SD Negeri 1 Beringin Raya, Kecamatan
Kemiling, Kota Bandar Lampung tahun 2004, Sekolah Menengah Pertama di SMP
Negeri 1 Bandar Lampung pada tahun 2007, dan Sekolah Menengah Atas di SMA
Negeri 2 Bandar Lampung pada tahun 2010.
Tahun 2010, penulis terdaftar sebagai mahasiswa pada Program Studi Agroteknologi,
Fakultas Pertanian, Universitas Lampung melalui jalur Seleksi Nasional Masuk
Perguruan Tinggi Negeri (SNMPTN). Selama menjadi mahasiswa penulis pernah
menjadi asisten praktikum Genetika Dasar, Pemuliaan Tanaman, Bahasa Inggris
untuk mahasiswa D3 dan S1, dan Aneka Tanaman Perkebunan. Tahun 2012/2013
penulis aktif sebagai Duta Fakultas Pertanian. Pada tahun 2013 penulis aktif pada
Lembaga Bahasa Jepang (Minna no Nihongo). Pada tahun 2014, penulis berperan
aktif dalam Organisasi Internasional AIESEC sebagaiExternal Relations Organizing
Lampung pada program pertukaran pelajar diTokyo University of Agriculture and
Technology.
Pada Januari sampai Februari 2013, penulis melaksanakan Kuliah Kerja Nyata di
Desa Madaraya, Kecamatan Pagelaran Utara, Kabupaten Pringsewu. Penulis
melaksanakan Praktik Umum di PT DuPont Pioneer Indonesia dari bulan Juli—
SANWACANA
Puji syukur penulis panjatkan kehadirat Allah SWT, karena atas rahmat dan
hidayah-Nya, penulis dapat menyelesaikan skripsi ini. Pada kesempatan ini penulis
menyampaikan rasa terima kasih yang tulus kepada :
1. Ibu Dr. Ir. Maimun Barmawi, M. S., selaku Pembimbing Utama yang telah
memberikan ilmu pengetahuan, saran, kritik, semangat dan bimbingan dalam
penelitian.
2. Bapak Joko Prasetyo, M. S., selaku Pembimbing Kedua dan Pembimbing
Akademik yang telah memberikan ilmu pengetahuan, saran, kritik, semangat dan
bimbingan dalam proses perkuliahan dan penelitian.
3. Ibu Dr. Ir. Nyimas Sa’diyah, M. P.,selaku Penguji atas saran, kritik, dan
bimbingan dalam penelitian ini.
4. Bapak Dr. Ir. Kuswanta Futas Hidayat, M.P., selaku Ketua Program Studi
Agroteknologi, Fakultas Pertanian, Universitas Lampung.
5. Bapak Prof. Dr. Ir. Wan Abbas Zakaria, M.S., selaku Dekan Fakultas Pertanian,
Universitas Lampung.
6. Dosen-dosen di Fakultas Pertanian Universitas Lampung atas segala ilmu dan
7. Keluarga tercinta, Ayahanda Firdaus, Ibunda Martini, Kakak dan Adik penulis
Elvi Sumarni dan Habibur Rahman Hakim yang telah memberikan dorongan
serta bantuan moril maupun materil kepada penulis selama menyelesaikan
skripsi.
8. Sahabat penulis Riza Aprianti dan Windi Eka Pratiwi, terima kasih atas semangat
dan dukungan yang selalu diberikan selama kuliah.
9. Teman-teman seperjuangan penelitian (Wanda, Nurrul Vias, Amey, Dimas, Jefri,
Raymon) atas bantuan, kerja sama, saran, dan kritik selama penelitian
berlangsung.
10. Teman-teman yang membantu dalam proses penelitian (Intan, Mesa, Agung,
Ruby, Roki, dan Miandri).
11. Teman-teman Agroteknologi 2010, khususnya kelas C, terima kasih atas waktu
yang telah dilewati bersama selama perkuliahan di Universitas Lampung.
12. Teman-teman AIESEC, khususnyaOC Youth Entrepreneurial Projectdan
Exchanges Participants, terima kasih atas pengalaman organisasi yang luar biasa.
13. Semua pihak yang telah membantu penulis dalam menyelesaikan skripsi ini yang
tidak dapat disebutkan satu per satu.
Semoga skripsi ini dapat bermanfaat.
Bandar Lampung, 03 Oktober 2015 Penulis,
iv DAFTAR ISI
Halaman
DAFTAR ISI ... iii
DAFTAR TABEL ... v
DAFTAR GAMBAR ... vi
I. PENDAHULUAN 1.1 Latar Belakang dan Masalah... 1
1.2 Tujuan Penelitian... 8
1.3 Kerangka Pemikiran... 9
1.4 Hipotesis... 12
II. TINJAUAN PUSTAKA 2.1 Tanaman Kedelai... 13
2.1.1 Sejarah tanaman kedelai... ... 13
2.1.2 Taksonomi tanaman kedelai... 13
2.1.3 Morfologi tanaman kedelai... 14
2.1.4 Syarat tumbuh tanaman kedelai... 20
2.2 Soybean Mosaic Virus (SMV) ... 20
2.2.1 Sejarah soybean mosaic virus... 20
2.2.2 Karakter soybean mosaic virus... 21
2.2.3 Penularan... 22
2.2.4 Gejala soybean mosaic virus... 22
2.2.5 Kisaran inang... 22
2.2.6 Pengendalian soybean mosaic virus... 23
2.3 Ketahanan Tanaman terhadap Penyakit... 23
2.3.1 Ketahanan horisontal... 23
2.3.2 Ketahanan vertikal... 24
2.3.3 Ketahanan tanaman terhadap infeksi virus... 25
2.4 Heritabilitas... ... 26
2.5 Kemajuan Genetik... 29
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian... 30
iv
3.3 Metode Penelitian... 31
3.4 Analisis Data... 32
3.5 Pelaksanaan Penelitian... 35
3.5.1 Pembuatan larutan buffer fosfat... 35
3.5.2 Perbanyakan inokulum soybean mosaic virus... 35
3.5.3 Persiapan lahan... 36
3.5.4 Penanaman... 36
3.5.5 Pemupukan... 37
3.5.6 Inokulasi soybean mosaic virus di lapangan... 38
3.5.7 Pelabelan... 38
3.5.8 Perawatan dan pemeliharaan tanaman... 38
3.5.9 Pemanenan... 39
3.5.10 Pengamatan... 39
IV. HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian... 42
4.2 Pembahasan... 46
V. KESIMPULAN DAN SARAN 5.1 Kesimpulan... 53
5.2 Saran... 53
1
I. PENDAHULUAN
1.1 Latar Belakang dan Masalah
Pertanian merupakan sektor yang memegang peranan penting dalam mendukung
pembangunan Indonesia. Pembangunan negara dapat didukung oleh sektor
pertanian karena sektor pertanian merupakan sumber devisa negara. Dewasa ini,
permintaan komoditas tanaman pangan semakin banyak, seiring dengan
bertambahnya penduduk Indonesia. Salah satu tanaman yang merupakan
komoditas tanaman pangan adalah tanaman kedelai.
Kedelai (Glycine max [L.] Merrill) merupakan tanaman pangan yang sangat
dibutuhkan masyarakat. Menurut Handayani et al. (2007), gizi yang dikandung
oleh biji kedelai sangat tinggi, terutama proteinnya (35—38%) yaitu hampir
mendekati protein susu sapi. Bahkan kandungan gizi hewani seperti daging, telur
dan ikan dapat digantikan oleh tahu dan tempe. Selain itu harganya terjangkau
dan rasanya enak (Haliza et al, 2010). Kedelai adalah jenis kacang-kacangan
yang sangat mudah dicerna oleh tubuh daripada jenis kacang-kacangan yang lain.
Kedelai mengandung senyawa fenolik dan asam lemak tak jenuh dan keduanya
berguna untuk menghalangi timbulnya senyawa nitrosamin yang menyebabkan
kanker. Oleh karena itu, kedelai menjadi salah satu tanaman pangan yang
2
Permintaan pasar terhadap kedelai terus meningkat sejalan dengan pertambahan
jumlah penduduk. Akan tetapi, permintaan tersebut tidak dapat dipenuhi karena
produksi kedelai di Indonesia masih rendah. Kebutuhan kedelai setiap tahun
diperkirakan sebanyak 2,5 juta ton/tahun, sedangkan produksi kedelai dalam
negeri hanya sekitar 800 ribu—900 ribu ton (Balai Penelitian Tanaman
Kacang-kacangan dan Umbi-Umbian, 2011).
Indonesia hanya dapat memenuhi kebutuhan kedelai sebesar 40%, sedangkan 60%
kebutuhan kedelai dipenuhi melalui impor. Pada tahun 2012 total produksi
kedelai di Indonesia sebanyak 851.647 ton, sedangkan pada tahun 2013 sebanyak
807.568 ton. Penurunan produksi kedelai pada tahun 2013 mencapai 4,22%,
sehingga untuk memenuhi kebutuhan kedelai, pemerintah membuat kebijakan
dengan mengimpor kedelai (Badan Pusat Statistik, 2013).
Rendahnya produksi kedelai di Indonesia disebabkan oleh beberapa faktor.
Faktor pertama perbedaan kondisi lingkungan seperti lama penyinaran. Kedelai
merupakan tanaman berhari pendek sehingga membutuhkan lama penyinaran
sebesar 13,5 jam/hari. Akan tetapi di Indonesia lama penyinaran yang terjadi
hanya 12 jam/hari. Keadaan ini menyebabkan tanaman kedelai memasuki fase
generatif lebih awal, sehingga pembentukan polong kedelai lebih sedikit yang
mempengaruhi produksi kedelai (Martin et al.,2006).
Faktor kedua yaitu kondisi tanah di Indonesia. Tanah di Indonesia kebanyakan
berjenis Ultisol. Tanah Ultisol merupakan tanah tua yang mengandung unsur hara
3
Faktor ketiga yaitu serangan hama dan penyakit tanaman. Faktor hama dan
penyakit tanaman adalah salah satu penyebab yang dapat menurunkan
produktivitas tanaman. Kondisi di Indonesia yang beriklim tropis memberikan
keuntungan bagi penyakit untuk berkembang dan menyebar. Salah satu penyakit
penting utama yang menjadi kendala dalam budidaya kedelai adalah penyakit
yang disebabkan oleh virus (Sumarno et al., 1990).
Virus merupakan salah satu patogen yang dapat menyebabkan rendahnya produksi
kedelai. Virus yang menyebabkan penyakit mosaik dan kerdil minimal ada lima
belas jenis yang mengancam produksi kacang-kacangan di Indonesia di antaranya
adalah soybean mosaic virus dan cowpea mild mottle virus (Saleh, 2007).
Serangan virus tersebut dapat menurunkan produksi dan kualitas biji khususnya
kandungan protein dan lemak.
Soybean mosaic virus merupakan virus yang secara umum telah diketahui
keberadaannya dan dikenal sebagai virus yang paling serius, serta bermasalah
dalam kurun waktu yang lama di area produksi kedelai di dunia (Wang, 2009).
Virus ini dapat menyebar dengan mudah dan infeksi yang ditimbulkan oleh SMV
menyebabkan kehilangan hasil yang drastis dan penurunan kualitas benih.
Penurunan hasil yang telah dilaporkan sekitar 8—50% dalam kondisi
sub-optimum (Hill, 1999; Arif dan Hassan, 2002) dan dapat mencapai 100% pada
kondisi lingkungan yang tidak mendukung (Liao et al., 2002). Infeksi virus yang
terjadi dalam sel akan mempengaruhi sintesis protein dan asam nukleat tanaman.
Infeksi virus juga akan mempengaruhi jumlah dan bentuk sel serta organel, seperti
4
tanaman inang menunjukkan gejala di seluruh bagian tanaman seperti tanaman
menjadi bantut, perubahan warna daun, ukuran dan bentuk buah yang dihasilkan
(Akin, 2006).
Salah satu cara pengendalian virus SMV yaitu dengan menggunakan varietas
tahan dan berproduksi tinggi. Menurut Akin dan Barmawi (2005), genotipe
B3570 memiliki keunggulan yaitu tahan terhadap SSV (soybean stunt virus), akan
tetapi berproduksi rendah. Menurut Putri (2013), populasi F1 Tanggamus x
Yellow bean, dan Tanggamus x B3570 merupakan populasi yang tahan terhadap
SMV. Apabila gen ketahanan terdapat dalam plasma nutfah, maka teknik
pemuliaan tanaman konvensional dapat dilaksanakan, akan tetapi jika tidak
terdapat, maka melalui teknik rekayasa genetika (Akin dan Barmawi, 2005).
Penelitian ini menggunakan benih generasi F2 hasil persilangan varietas
Tanggamus x B3570. Populasi F1 Tanggamus x B3570 dengan genotipe nomor satu
merupakan hasil persilangan dialel setengah yang dilakukan oleh Maimun
Barmawi. Pengujian F1 dilakukan oleh Putri dan Jamil (2013) untuk mengetahui
tingkat ketahanan tanaman kedelai terhadap soybean mosaic virus pada generasi
F1.
Populasi F2 genotipe nomor satu hasil persilangan Tanggamus x B3570 dipilih
dengan mempertimbangkan jumlah biji sehat sebanyak 778 butir, jumlah biji sakit
sebanyak 83 butir, dan persentase keparahan penyakit (KP) sebesar 22,5% yang
termasuk ke dalam kriteria tahan. Dari hasil penelitian Putri (2013) menunjukkan
bahwa nilai estimasi heritabilitas dalam arti sempit untuk KP tersebut sebesar
5
persilangan Tanggamus x B3570 untuk karakter KP sebesar -0,67. Keadaan ini
menunjukkan bahwa karakter KP dikendalikan oleh aksi gen dominan sebagian
negatif. Berarti populasi F1 hasil persilangan Tanggamus x B3570 akan
menghasilkan tingkat KP yang berada di antara kedua tetuanya, tetapi lebih
dipengaruhi oleh tetua yang paling tahan. Oleh karena itu, perlu dilakukan
penelitian untuk mengetahui ketahanan tanaman kedelai terhadap infeksi SMV
pada generasi F2.
Penelitian tentang karakter tanaman yang menggunakan benih generasi F2 telah
banyak dilakukan. Menurut Poespodarsono (1988), generasi F2 merupakan
generasi yang memiliki keragaman yang luas dan paling tinggi. Semakin luas
keragaman genetik, semakin besar pula peluang untuk keberhasilan seleksi dalam
meningkatkan frekuensi gen/alel yang diinginkan dan sebaliknya. Hal ini
berkaitan dengan besaran beberapa parameter genetik. Beberapa parameter
genetik yang dapat digunakan sebagai pertimbangan agar seleksi efektif dan
efisien adalah keragaman genetik dan heritabilitas (Poehlman, 1991).
Besarnya nilai heritabilitas dapat memberikan informasi kepada pemulia
mengenai mudah tidaknya suatu karakter diwariskan kepada keturunannya.
Heritabilitas memberikan petunjuk suatu sifat lebih dipengaruhi faktor genetik
atau faktor lingkungan. Heritabilitas dalam arti luas merupakan suatu parameter
genetik yang mengukur kemampuan suatu genotipe dalam mewariskan
karakteristik-karakteristik yang dimilikinya yang melibatkan aksi gen dominan,
6
membandingkan besarnya ragam genetik total terhadap ragam fenotipik
(Borojevic, 1990).
Menurut Dahlan dan Slamet (1992), heritabilitas menentukan kemajuan genetik,
semakin besar nilai heritabiltas, semakin besar nilai kemajuan genetik dan
sebaliknya. Besarnya peningkatan yang diperoleh dari karakter yang diseleksi
akan memberikan nilai duga kemajuan genetik. Peningkatan akan dipengaruhi
oleh intensitas seleksi yang ditetapkan, ragam suatu karakter, dan heritabilitas arti
luasnya. Jika ragam suatu karakter dan heritabilitas besar maka akan berkorelasi
positif dengan kemajuan genetik.
Beberapa hasil penelitian mengenai berbagai karakter agronomi tanaman, nilai
duga heritabilitas dan kemajuan genetik tanaman kedelai pada karakter tinggi
tanaman, jumlah polong per tanaman, dan bobot biji per tanaman adalah tinggi
(Yantama, 2012). Pada tanaman wijen (Sesamum indicum L.), karakter tinggi
tanaman, jumlah polong per tanaman, jumlah biji per polong, dan hasil biji per
hektar memiliki nilai keragaman genetik dan heritabilitas yang tinggi (Sudarmadji
et al., 2007). Pada tanaman lentil (Lens culinaris Medik), Younis et al. (2008)
melaporkan bahwa umur berbunga, tinggi tanaman, jumlah cabang utama, hasil
biologi, indeks panen, dan umur masak memiliki nilai heritabilitas dan kemajuan
genetik yang tinggi. Raffi dan Nath (2004) melaporkan dengan analisis jalur,
hasil kacang merah (Phaseolus vulgaris L.) dipengaruhi secara langsung oleh
jumlah polong per tanaman, panjang polong, jumlah biji per tanaman, dan bobot
20 biji. Keempat karakter tersebut memiliki nilai keragaman genetik, heritabilitas,
7
Sumarno dan Zuraida (2006) menyarankan bahwa karakter tinggi tanaman dan
jumlah polong isi pada tanaman kedelai merupakan kriteria seleksi yang mudah
dan cepat pada generasi awal, sedangkan Susanto dan Adie (2006), melaporkan
bahwa umur panen, jumlah polong, dan jumlah biji per tanaman kedelai
merupakan kriteria seleksi yang efektif.
Penelitian ini dilakukan untuk menjawab masalah yang dirumuskan dalam
pertanyaan sebagai berikut:
1. Berapa besaran nilai duga heritabilitas dalam arti luas berbagai karakter
agronomi dan ketahanan terhadap penyakit SMV pada tanaman kedelai
populasi F2, hasil persilangan Tanggamus dan B3570 yang terinfeksi SMV?
2. Berapa besaran nilai kemajuan genetik berbagai karakter agronomi tanaman
dan ketahanan terhadap penyakit SMV pada tanaman kedelai populasi F2,
hasil persilangan Tanggamus dan B3570 yang terinfeksi SMV?
3. Apakah terdapat nomor-nomor harapan tanaman populasi F hasil persilangan
Tanggamus dan B3570 yang memiliki ketahanan yang tinggi terhadap penyakit
8
1.2 Tujuan Penelitian
Berdasarkan rumusan masalah yang diungkapkan, dibuat tujuan penelitian sebagai
berikut:
1. Menduga besaran nilai heritabilitas dalam arti luas berbagai karakter agronomi
dan ketahanan terhadap penyakit SMV pada tanaman kedelai populasi F2 hasil
persilangan Tanggamus dan B3570 yang terinfeksi SMV.
2. Menduga besaran kemajuan seleksi berbagai karakter agronomi tanaman dan
ketahanan terhadap penyakit SMV pada tanaman kedelai populasi F2 hasil
persilangan Tanggamus dan B3570 yang terinfeksi SMV.
3. Mengetahui nomor-nomor harapan tanaman kedelai populasi F2 hasil
persilangan Tanggamus dan B3570 yang memiliki ketahanan terhadap SMV
9
1.3 Kerangka Pemikiran
Berdasarkan rumusan permasalahan dan tujuan yang telah dikemukakan, disusun
kerangka pemikiran untuk memberikan penjelasan terhadap perumusan masalah.
Indonesia merupakan negara penghasil kedelai dengan urutan keenam. Namun
ironisnya Indonesia kerap mengalami krisis pangan. Permintaan pasar akan
kedelai semakin meningkat seiring dengan bertambahnya penduduk. Akan tetapi
kebutuhan kedelai di dalam negeri tidak dapat dipenuhi oleh produksi lokal.
Akibatnya, Indonesia harus mengimpor kedelai dari negara lain contohnya
Amerika Serikat, Malaysia, Kanada, Ukraina, dan China.
Rendahnya produksi kedelai merupakan penyebab tidak terpenuhinya kebutuhan
kedelai di Indonesia. Penyebab rendahnya produksi kedelai di dalam negeri
disebabkan oleh beberapa faktor. Faktor pertama yaitu kondisi lingkungan yang
berbeda seperti lama penyinaran. Faktor kedua yaitu kondisi tanah di Indonesia
yang kesuburannya rendah. Pasokan unsur hara yang rendah membuat tanaman
kekurangan unsur hara baik makro maupun mikro. Faktor ketiga yaitu serangan
hama dan penyakit tanaman. Kondisi lingkungan Indonesia yang beriklim tropis
memberikan dampak positif bagi perkembangan hama dan penyakit tanaman.
Salah satu penyakit yang menyerang tanaman kedelai yaitu penyakit mosaik yang
disebabkan oleh virus. Penyakit yang ditimbulkan oleh virus dipengaruhi oleh
inang, virus dan lingkungan. Hal ini dapat terjadi apabila strain virus yang
menyerang bersifat virulen, tanaman yang diserang rentan, dan kondisi
10
Soybean mosaic virus adalah virus tanaman kedelai yang berbahaya karena dapat
mengurangi kualitas benih dan menurunkan produktivitas tanaman hingga 100%.
Infeksi virus yang terjadi dalam sel akan mempengaruhi sintesis protein dan asam
nukleat tanaman. Infeksi virus juga akan mempengaruhi jumlah dan bentuk sel
serta organel, seperti mitokhondria dan kloroplas. Tanaman inang yang terinfeksi
virus ini akan menunjukkan gejala seperti tanaman menjadi bantut, perubahan
warna daun, ukuran dan bentuk buah yang dihasilkan.
Pemuliaan tanaman merupakan suatu teknik yang dapat dilakukan dalam
mengembangkan varietas, sehingga dapat dirakit varietas yang tahan terhadap
SMV dan berproduksi tinggi. Langkah awal yang harus dilakukan dalam
pemuliaan tanaman adalah membuat persilangan antara tetua tahan tetapi
berproduksi rendah dengan tetua rentan namun berproduksi tinggi. Tujuan
dilakukan persilangan adalah menggabungkan sifat tetua yang disilangkan dan
meningkatkan keragaman genetik populasi yang bersangkutan.
Persilangan antara tetua-tetua kedelai telah dilakukan dengan menggunakan
persilangan dialel setengah. Penelitian tersebut melibatkan sebanyak 5 tetua
kedelai yaitu B3570 , Orba, Tanggamus, Taichung, dan Yellow Bean dan diperoleh
10 kombinasi persilangan. Benih kedelai generasi F2 hasil persilangan
Tanggamus x B3570 genotipe nomor satu memiliki tingkat KP sebesar 22,5%
(tahan), jumlah biji sehat 778 butir, dan biji sakit 83 butir. Genotipe tersebut
ditanam pada penelitian ini dan dipilih berdasarkan hasil penelitian sebelumnya.
Generasi F2 merupakan generasi yang bersegregasi paling tinggi. Pada generasi
11
nilai tengah yang luas akan berdampak pada tingginya keragaman genetik. Nilai
keragaman genetik yang tinggi akan mempengaruhi nilai estimasi heritabilitas.
Heritabilitas merupakan rasio ragam genotipe terhadap ragam fenotipe. Estimasi
nilai heritabilitas berfungsi dalam menentukan karakter yang dikendalikan oleh
faktor genetik atau faktor lingkungan dan dapat mengetahui apakah karakter
tersebut mudah diwariskan atau tidak kepada keturunannya. Apabila nilai duga
heritabilitas tinggi, faktor genetik lebih berperan dalam mengendalikan karakter
yang dipelajari, sedangkan faktor lingkungan kurang berperan dan sebaliknya.
Mengingat penelitian ini menggunakan benih generai F2 yang memiliki tingkat
segregrasi tertinggi, kisaran nilai tengah dan keragaman genetik yang luas, maka
keadaan ini sejalan dengan tingginya nilai heritabilitas arti luas yang muncul pada
berbagai karakter agronomi dan ketahanan terhadap penyakit SMV.
Heritabilitas akan mempengaruhi keefektifan seleksi yang dilakukan. Seleksi
merupakan bagian penting dari program pemuliaan tanaman untuk memperbesar
peluang mendapatkan genotipe unggul. Apabila nilai heritabilitas dalam arti luas
tinggi, seleksi atas karakter tersebut dapat dilakukan pada generasi awal,
sedangkan jika nilai heritabilitas dalam arti luas rendah maka seleksi dilakukan
pada generasi lanjut untuk memperoleh keragaman yang luas dan heritabilitas
yang tinggi.
Besaran keragaman genetik dan heritabilitas bermanfaat untuk menduga kemajuan
genetik yang didapat dari seleksi. Respons seleksi atau kemajuan genetik
merupakan suatu parameter yang menduga keberhasilan penerapan seleksi pada
12
pada intensitas seleksi tertentu. Besarnya peningkatan yang diperoleh dari
karakter yang diseleksi akan memberikan nilai duga kemajuan genetik.
Peningkatan akan dipengaruhi oleh intensitas seleksi yang ditetapkan, ragam suatu
karakter, dan heritabilitas arti luasnya. Apabila ragam suatu karakter luas dan
heritabilitas tinggi maka akan berkorelasi positif dengan kemajuan genetik. Oleh
karena itu, seleksi pada kedelai populasi F2 hasil persilangan Tanggamus dan
B3570 diharapkan akan menunjukkan kemajuan genetik yang tinggi untuk beberapa
karakter agronomi dan ketahanan terhadap penyakit SMV karena populasi yang
dilibatkan dalam seleksi memiliki keragaman genetik yang luas dan nilai
heritabilitas yang tinggi. Dengan demikian peluang diperoleh zuriat yang tahan
terhadap SMV dan berproduksi tinggi akan semakin besar.
1.4 Hipotesis
Hipotesis yang didapatkan adalah sebagai berikut:
1. Karakter agronomi dan ketahanan terhadap penyakit SMV generasi F2
persilangan Tanggamus x B3570 genotipe nomor satu mempunyai nilai
estimasi heritabilitas yang tinggi.
2. Karakter agronomi dan ketahanan terhadap penyakit SMV generasi F2
persilangan Tanggamus x B3570 genotipe nomor satu mempunyai nilai
kemajuan genetik yang tinggi.
3. Terdapat nomor-nomor harapan untuk karakter agronomi dan ketahanan
terhadap penyakit SMV generasi F2 hasil persilangan Tanggamus x B3570
13
II. TINJAUAN PUSTAKA
2.1 Tanaman Kedelai
2.1.1 Sejarah tanaman kedelai
Kedelai adalah salah satu tanaman polong-polongan yang menjadi bahan dasar
banyak makanan dari Asia Timur seperti kecap, tahu, dan tempe. Berdasarkan
peninggalan arkeologi, tanaman ini telah dibudidayakan sejak 3500 tahun yang
lalu di Asia Timur (Padjar, 2010). Menurut Sumarno et al. (1990) yang dikutip
oleh Cahyarini et al. (2004), tanaman kedelai (Glycine max (L.) Merill.)
merupakan tanaman yang banyak dibudidayakan di Indonesia. Namun tanaman
ini bukan merupakan tanaman asli dari Indonesia. Diperkirakan kedelai
diperkenalkan oleh pendatang Cina pada permulaan abad 18. Oleh karena itu,
keragaman genetik relatif sempit hanya terbatas karena adanya seleksi alami dan
adaptasi.
2.1.2 Taksonomi tanaman kedelai
Klasifikasi tanaman kedelai di dalam buku Rukmana (1996) dan Gembong (2005)
adalah sebagai berikut :
14
Ordo : Rosales
Sub ordo : Leguminosineae Family : Leguminoseae Sub family : Papiolionaceae Genus : Glycine
Spesies : Glycine max (L.) Merill.
2.1.3 Morfologi tanaman kedelai
Kedelai merupakan tanaman dikotil semusim dengan percabangan sedikit, sistem
perakaran akar tunggang, dan batang berkambium. Kedelai dapat berubah
penampilan menjadi tumbuhan setengah merambat dalam keadaan pencahayaan
rendah (Rukmana dan Yuniarsih,1996).
Para ahli botani mencatat suku kacang-kacangan (Papilionacae) yang tumbuh di
dunia diperkirakan mencapai 18.000 spesies. Tanaman kedelai yang ditanam
secara komersial di dunia diperkirakan keturunan atau kerabat jenis kedelai liar
G. soya atau G. usuriensis (AAK, 1989).
Tanaman kedelai terdiri atas dua organ yaitu organ vegetatif dan organ generatif.
Organ vegetatif meliputi akar, batang, dan daun yang berfungsi sebagai alat
pengambil, pengangkut, pengedar, dan penyimpan makanan. Organ generatif
meliputi bunga, buah, dan biji yang fungsinya sebagai alat perkembangbiakan
15
Adapun bagian-bagian organ vegetatif tanaman kedelai:
a. Akar
Akar kedelai mulai muncul dari belahan kulit biji yang muncul di sekitar misofil.
Calon akar tersebut kemudian tumbuh dengan cepat ke dalam tanah, sedangkan
kotiledon yang terdiri atas dua keping akan terangkat ke permukaan tanah akibat
pertumbuhan yang cepat dari hipokotil. Sistem perakaran kedelai terdiri atas dua
macam, yaitu akar tunggang dan akar sekunder (serabut) yang tumbuh dari akar
tunggang. Selain itu kedelai juga seringkali membentuk akar adventif yang
tumbuh dari bagian bawah hipokotil (Budidaya Tanaman Kedelai (Glycine max
[L.] Merril), 2009).
Tanaman kedelai dapat mengikat nitrogen (N2) di atmosfer melalui aktivitas
bakteri pengikat nitrogen, yaitu Rhizobium japonicum. Bakteri ini terbentuk di
dalam akar tanaman yang diberi nama nodul atau bintil akar. Keberadaan
Rhizobium japonicum di dalam tanah ada karena tanah tersebut telah ditanami
kedelai atau sebelumnya telah ditambahkan ke dalam tanah. Bintil akar tanaman
kedelai umumnya dapat mengikat nitrogen dari udara pada umur 10—12 hari
setelah tanam, tergantung pada kondisi lingkungan tanah dan suhu.
Pemupukan nitrogen sebagai starter pada awal pertumbuhan kedelai perlu
dilakukan untuk pertumbuhan dalam satu minggu pertama. Pada keadaan
tersebut, akar tanaman belum berfungsi sehingga tambahan nitrogen diharapkan
dapat merangsang pembentukan akar. Hal ini akan membuka kesempatan
pembentukan bintil akar (Budidaya Tanaman Kedelai (Glycine max [L.] Merril),
16
b. Batang
Tanaman kedelai berbatang pendek (30 cm—100 cm) memiliki 3—6
percabangan dan berbentuk tanaman perdu. Pada pertanaman yang rapat
seringkali tidak terbentuk percabangan atau hanya bercabang sedikit. Batang
tanaman kedelai berkayu, biasanya kaku dan tahan rebah, kecuali tanaman yang
dibudidayakan di musim hujan atau tanaman yang hidup di tempat yang ternaungi
(Pitojo, 2003).
Tipe pertumbuhan batang kedelai dapat dibedakan menjadi tiga macam,yakni
determinate (terbatas), indeterminate (tidak terbatas), dan semi determinate
(setengah terbatas) (Suprapto, 1999). Menurut Adisarwanto (2005), perbedaan
sistem pertumbuhan batang ini didasarkan atas keberadaan bunga pada pucuk
batang. Tipe terbatas memiliki ciri khas berbunga serentak dan mengakhiri
pertumbuhan meninggi. Pertumbuhan batang tipe ini ditunjukkan dengan
pertumbuhan batang yang tidak tumbuh lagi pada saat tanaman mulai berbunga.
Tanaman pendek sampai sedang, ujung batang hampir sama besar dengan batang
bagian tengah, daun teratas sama besar dengan daun batang tengah. Tipe tidak
terbatas memiliki ciri berbunga secara bertahap dari bawah ke atas dan tumbuhan
terus tumbuh. Pertumbuhan batang tipe ini dicirikan dengan pucuk batang
tanaman masih bisa tumbuh daun, walaupun tanaman sudah mulai berbunga.
Tanaman berpostur sedang sampai tinggi, ujung batang lebih kecil dari bagian
17
c. Daun
Bentuk daun kedelai ada dua macam, yaitu bulat (oval) dan lancip (lanceolate)
yang diistilahkan dengan berdaun lebar (broad leaf) dan berdaun sempit (narrow
leaf) (Adisarwanto, 2008). Kedua bentuk daun tersebut dipengaruhi oleh faktor
genetik. Bentuk daun diperkirakan mempunyai korelasi yang sangat erat dengan
potensi produksi biji. Umumnya daerah yang mempunyai tingkat kesuburan tanah
tinggi sangat cocok untuk varietas kedelai yang mempunyai bentuk daun lebar.
Daun mempunyai stomata, berjumlah 190—320/m2 (Adisarwanto, 2005).
Daun kedelai merupakan daun majemuk yang terdiri atas tiga helai anak daun dan
pada umumnya berwarna hijau muda atau hijau kekuning-kuningan. Bentuk daun
ada yang oval, juga ada yang segitiga. Warna dan bentuk daun kedelai ini
tergantung pada varietas masing-masing (AAK, 1989). Daun kedelai hampir
seluruhnya trifoliate (menjari tiga) dan jarang sekali mempunyai empat atau lima
daun.
Menurut Lamina (1990), daun pertama keluar dari buku sebelah atas kotiledon
(keping biji) yang disebut daun tunggal dengan bentuk sederhana dan letak
daunnya berseberangan. Daun ketiga pada daun profila terbentuk pada batang
utama dan cabang. Daun profila terbentuk pada batang utama dan cabang, dan
18
Adapun bagian-bagian organ generatif tanaman kedelai:
a. Bunga
Bunga kedelai berbentuk seperti kupu-kupu, terdiri atas kelopak, tajuk, benang
sari (anteredium) dan kepala putik (stigma). Warna mahkota bunga kedelai putih
atau ungu tergantung varietasnya. Bunga jantan pada kedelai terdiri atas sembilan
benang sari yang membentuk tabung benang sari. Bila bunga masih kuncup,
kedudukan kepala sari berada di bawah kepala putik, tetapi pada saat kepala sari
menjelang pecah, tangkai sari memanjang sehingga kepala sari menyentuh kepala
putik yang menyebabkan terjadi penyerbukan pada saat bunga masih tertutup
menjelang mekar (Kasno et al., 1992).
Bunga kedelai termasuk penyerbukan sendiri karena pembuahan telah terjadi
sebelum bunga mekar (kleistogami). Pada saat melakukan persilangan
(hibridisasi), mahkota daun dan benang sari dibuang atau dikastrasi, hanya
putiknya saja yang ditinggalkan. Jika mahkota dan benang sari tidak dibuang
maka akan tercampur benang sari dari tanaman lain sehingga proses persilangan
tidak berjalan dengan sempurna (AAK, 1989).
b. Buah (polong)
Buah kedelai berbentuk polong. Setiap tanaman mampu menghasilkan 100—250
polong, namun pertanaman yang rapat mampu menghasilkan sekitar 30 polong
(Pitojo, 2003). Biji kedelai berada dalam polong, setiap polong berisi satu sampai
empat biji. Polong kedelai mempunyai rambut, berwarna kuningkecoklatan atau
kuning muda. Polong yang sudah masak berwarna lebih tua,warna hijau berubah
19
Jumlah polong per tanaman bervariasi tergantung sifat genetika yang
terekspresikan dalam bentuk sifat dan ciri morfologi, kemungkinan juga
disebabkan oleh keragaman tanah dan iklim pada masing-masing lokasi
penanaman, kesuburan tanah dan jarak tanam (Suprapto, 1999).
Polong kedelai pertama kali terbentuk sekitar 7—10 hari setelah muncul bunga
pertama. Panjang polong muda sekitar 1 cm. Jumlah polong yang terbentuk pada
setiap ketiak tangkai daun sangat beragam, 1—10 buah dalam setiap kelompok.
Pada setiap tanaman, jumlah polong dapat mencapai lebih dari 50, bahkan ratusan.
Kecepatan pembentukan polong dan pembesaran biji akan semakin cepat setelah
proses pembentukan bunga berhenti. Ukuran dan bentuk polong menjadi
maksimal pada awal periode pemasakan biji. Hal ini kemudian diikuti dengan
perubahan warna polong, dari hijau menjadi kuning kecoklatan pada saat masak.
Di dalam polong terdapat biji yang berjumlah 2—3 biji (Adisarwanto, 2005).
c. Biji
Setiap biji kedelai mempunyai ukuran bervariasi, mulai dari kecil (sekitar 7—9
g/100 biji), sedang (10—13 g/100 biji), dan besar (>13 g/100 biji). Bentuk biji
bervariasi, tergantung pada varietas tanaman, yaitu bulat, agak gepeng, dan bulat
telur. Namun demikian, sebagian besar biji berbentuk bulat telur. Warna kulit
biji bervariasi, mulai dari kuning, hijau, coklat, hitam, atau kombinasi campuran
dari warna-warna tersebut. Biji kedelai tidak mengalami masa dormansi sehingga
setelah proses pembijian selesai, biji kedelai dapat langsung ditanam. Namun
20
2.1.4 Syarat tumbuh tanaman kedelai
Di Indonesia kedelai dapat tumbuh dan berproduksi dengan baik di dataran rendah
sampai ketinggian 900 meter di atas permukaan laut. Kondisi iklim yang paling
cocok yaitu daerah-daerah yang mempunyai suhu 25°—27°C, kelembaban udara
(RH) rata-rata 65%, penyinaran matahari 12 jam/hari atau minimal 10 jam/hari
dan curah hujan paling optimum 100—200 mm/bulan. Tanaman kedelai memilki
daya adaptasi yang luas pada berbagai jenis tanah. Hal yang paling penting dalam
pemilihan lokasi dan lahan untuk penanaman kedelai adalah tata air (drainase) dan
tata udara (aerasi) tanahnya baik, bebas dari kandungan wabah nematoda dan pH
tanah yang sesuai yaitu 5,0—7,0 (Rukmana dan Yuniarsih, 1996).
2.2 Soybean Mosaic Virus
2.2.1 Sejarah
Di antara 67 atau lebih virus yang dapat menginfeksi kedelai , 27 jenis virus
dianggap sebagai ancaman terhadap industri kedelai (Tolin dan Lacy, 2004;
Saghai et al., 2008). Virus mosaik kedelai adalah virus yang umum dan diakui
sebagai virus yang paling serius. Virus ini telah menjadi masalah lama di berbagai
daerah penghasil kedelai di dunia (Wang, 2009). Soybean mosaic virus adalah
anggota dari genus Potyvirus dalam keluarga Potyviridae. Penyakit yang
disebabkan oleh SMV pertama kali didokumentasikan di USA pada tahun 1915
oleh Clinton (1916) dan penamaan virus ini berasal dari Gardner dan Kendrick
(1921). Sejak saat itu, SMV kemudian ditemukan di China, Jepang, Korea
Selatan, Kanada, Brazil, Australia dan banyak negara lain di mana kedelai
21
penurunan kualitas benih. Telah dilaporkan bahwa kehilangan hasil berkisar
8—50% di bawah kondisi lapang alam ( Hill, 1999; Arif dan Hassan, 2002) dan
mencapai 100% pada kondisi lapang yang parah (Liao et al., 2002).
2.2.2 Karakter soybean mosaic virus
Menurut Sudjono et al. (1993) yang dikutip oleh Mulia (2008), soybean mosaic
virus termasuk genus potyvirus berbentuk batang lentur, rata-rata berukuran 750
nm dan lebar rata-rata 15—18 nm. Virion yang paling infektif berukuran panjang
lebih dari 656 nm. Infektifitas menurun bila terkena sinar ultraviolet atau berada
dalam larutan sangat asam (pH < 4) atau sangat basa (pH > 9). Pada suhu 26°C
translokasi dan replikasi virus cepat, tetapi pada suhu di bawah 10°C translokasi
virus terhenti.
Stabilitas SMV dalam cairan perasan antara lain suhu inaktivasi 55°C— 60 °C
(selama 10 menit). Titik batas pengenceran 1 : 1000 sampai 100.000 dan
ketahanannya dalam penyimpanan berkisar dua atau tiga hari pada suhu kamar
(Bos (1994), dikutip oleh Mulia, 2008). Menurut Matthews (1992) dikutip oleh
Mulia (2008), genom SMV terdiri atas RNA utas tunggal berukuran sekitar 10 kb
dan poli-A pada ujung tiganya. Tidak diperoleh subgenom RNA pada jaringan
tanaman terinfeksi. Genom SMV menyandikan delapan protein yang pada
awalnya merupakan satu protein besar yang kemudian mengalami pemotongan
22
2.2.3 Penularan soybean mosaic virus
Lebih dari 30% benih yang berasal dari tanaman kedelai yang terinfeksi SMV
membawa virus, tergantung pada kultivar dan waktu penularan sebelum
pembungaan. Benih yang terinfeksi SMV merupakan sumber inokulum utama,
akan tetapi gulma dan tanaman lainnya dapat juga sebagai sumber keberadaan
SMV. Penyebaran virus juga dapat disebabkan oleh kutu aphis. Kutu aphis
memiliki perbedaan spesies lebih dari 32 jenis dari 15 genus yang berbeda yang
juga memiliki perbedaan cara penularan (Arif dan Hassan, 2002; Steinlage et al.,
2002). Beberapa jenis aphis yang menjadi vektor soybean mosaic virus adalah
Acyrthosiphom pisum, Aphis craccivora, A. fabae, A. glycine, A gossypii, Myzus
persicae, Rhopalosiphum maidis dan R. padi.
2.2.4 Gejala soybean mosaic virus
Tanaman kedelai yang terinfeksi SMV pada awalnya menunjukkan gejala tulang
daun pada anak daun yang masih muda menjadi kuning jernih. Setelah itu daun
menjadi tidak rata (mengkerut) dan memiliki gambaran mosaik dengan warna
hijau gelap di sepanjang tulang daun dan tepi daun mengalami klorosis. Tanaman
sakit membentuk polong kecil, rata, kurang berbulu, dan lebih melengkung. Biji
lebih kecil dari biasanya dan daya kecambah menurun. Sebagian dari biji
tanaman sakit berbercak-bercak coklat, tetapi tergantung dari kultivar kedelai,
strain virus, dan umur tanaman pada waktu terjadi (Semangun, 1991).
2.2.5 Kisaran Inang
Perbedaan SMV dengan potyvirus lainnya yaitu SMV memiliki kisaran inang
23
Fabaceae (Leguminosae), Amaranthaceae, Chenopodiaceae, Passifloraceae,
Schropulariaceae dan Solanaceae. Tetapi yang paling sering terdapat pada famili
Leguminosae termasuk kedelai dan kedelai liar lainnya (Galvez, 1963; Hill,
1999).
2.2.6 Pengendalian soybean mosaic virus
Menurut Sudjono et al.(1983) yang dikutip oleh Semangun (1991), untuk
mengendalikan penyakit mosaik kedelai dapat dilakukan beberapa cara sebagai
berikut:
1. Menanam benih yang bebas virus.
2. Segera mencabut dan membinasakan kedelai yang terinfeksi.
3. Menanam varietas kedelai yang tahan terhadap infeksi virus.
4. Jika perlu gunakan insektisida untuk mengendalikan kutu daun yang menjadi
vektor virus.
5. Membasmi tumbuhan inang virus mosaik kedelai.
2.3 Ketahanan Tanaman Terhadap Penyakit
2.3.1 Ketahanan horisontal
Ketahanan yang dimiliki tanaman secara alamiah bersifat poligenik, yaitu
dikendalikan oleh banyak gen. Tanaman yang memiliki ketahanan yang
dikendalikan oleh banyak gen disebut juga tanaman yang memiliki ketahanan
24
Sifat ketahanan horisontal yaitu sebagai berikut (Nyoman, 1993):
1) Ketahananan yang dikendalikan oleh banyak gen;
2) Reaksinya tidak diferensial;
3) Tahan terhadap semua ras dari satu spesies patogen, terhadap spesies patogen
berbeda, atau genus;
4) Gen-gen tahan tidak dapat diidentifikasi;
5) Pewarisanya tidak mengikuti nisbah Mendel;
6) Ketahanannya relatif mantap.
2.3.2 Ketahanan vertikal
Ketahanan vertikal disebut juga ketahanan spesifik. Ketahanannya benar-benar
menghadapi gen virulen dari patogen itu. Jadi interaksinya adalah gen tahan
tanaman melawan gen virulen patogen.
Sifat-sifat ketahanan vertikal adalah sebagai berikut (Nyoman, 1993):
1) Ketahanannya dikendalikan oleh satu gen utama (mayor);
2) Reaksinya diferensial;
3) Tahan terhadap satu ras dari suatu spesies patogen,
4) Mengikuti nisbah Mendel;
5) Gennya dapat diidentifikasi;
6) Ketahanannya tidak mantap dalam menghadapi patogen yang bersifat
25
2.3.3. Ketahanan tanaman terhadap infeksi virus
Menurut Akin (2011), terdapat beberapa ketahanan tanaman terhadap infeksi virus
yaitu
1. Ketahanan melalui satelit RNA
Satelit RNA (satRNA) merupakan molekul kecil RNA, berukuran
200—1500 nt, yang berasosiasi dengan virus lain sebagai inang (helper) dan
berada bersama genom virus inang. Asosiasi satRNA dengan suatu virus
dapat menyebabkan ketidakmampuan isolat virus tersebut untuk menginduksi
gejala pada inangnya dan juga dapat menyebabkan isolate virus tersebut
bersifat antagonis terhadap isolat lainnya.
2. Ketahanan melalui proteksi silang
Proteksi silang merupakan hambatan super infeksi suatu virus akibat imbas
ketahanan dari infeksi virus sebelumnya.
3. Ketahanan melalui protein selubung virus
Mekanisme ketahanan ini dikenal dengan sebutan uncoating partikel virus
target dalam sitoplasma tanaman.
4. Ketahanan melalui antisense RNA
Antisense RNA adalah RNA yang ditranskripsi dari transgen yang urutan
nukleotida merupakan komplemen dari sebagian genom virus. Tanaman
transgen yang mengekspresikan antisense gen U1 RNA TMV mempunyai
ketahanan yang sangat tinggi terhadap strain- strain virus TMV.
5. Ketahananan virus melalui post transcriptional gene silencing
Penghentian atau supresi ekspresi gen dapat terjadi pada tahap transkripsi, dan
26
2.4 Heritabilitas
Terdapat dua tipe heritabilitas yaitu heritabilitas arti luas dan heritabilitas arti
sempit. Heritabilitas arti luas merupakan proporsi ragam genetik total terhadap
ragam fenotipe, sedangkan heritabilitas arti sempit merupakan proporsi ragam
aditif terhadap ragam fenotipe. Nilai heritabilitas dapat diduga secara langsung
melalui pendugaan komponen ragam dan secara tidak langsung melalui regresi
antara tetua dengan turunannya dan respon seleksi. Pendugaan komponen ragam
dapat dilakukan dengan menggunakan populasi dari berbagai rancangan
persilangan (Roy, 2000).
Seperti yang telah disinggung sebelumnya bahwa heritabilitas arti luas adalah
proporsi ragam genetik total yang mempengaruhi keragaman fenotipe. Ragam
genetik terdiri atas ragam aditif, ragam dominan, dan ragam epistasis yang
masing-masing disebabkan oleh aksi gen aditif, aksi gen dominan dan aksi gen
epistasis. Ragam aditif adalah ragam yang disebabkan oleh alel yang terdapat
dalam lokus, ragam dominan adalah ragam yang disebabkan oleh interaksi antara
alel dalam satu lokus, sedangkan ragam epistasis adalah ragam yang disebabkan
oleh interaksi antara alel dari lokus yang berbeda (Falconer dan Mackay, 1996).
Heritabilitas dapat dijadikan landasan dalam menentukan program seleksi.
Apabila nilai heritabilitas tinggi, maka seleksi dapat dilakukan pada generasi awal,
sebaliknya apabila heritabilitas rendah, maka seleksi baik dilakukan pada generasi
lanjut, karena peluang terjadi peningkatan keragaman dalam populasi akan
semakin besar (Falconer, 1970). Metode seleksi yang cocok diterapkan apabila
heritabilitas bernilai rendah adalah metode pedigri, metode penurunan satu biji
27
Apabila nilai heritabilitas tinggi, metode seleksi massa atau galur murni dapat
digunakan. Dahlan dan Slamet (1992) menyatakan bahwa heritabilitas
menentukan kemajuan genetik, semakin besar nilai heritabilitas arti luas, semakin
besar pula nilai kemajuan genetik, sehingga semakin cepat varietas unggul dilepas.
Sebaliknya semakin rendah nilai heritabilitas arti luas, semakin kecil nilai
kemajuan genetik, dan semakin lama varietas unggul baru dilepas.
Menurut Rachmadi (2000), besarnya nilai heritabilitas suatu karakter dalam
populasi tergantung kepada beberapa hal :
1. Karakteristik populasi
Pendugaan heritabilitas suatu karakter dipengaruhi oleh besarnya nilai keragaman
genetik yang ada di dalam populasi. Suatu populasi yang berasal dari turunan
tetua yang berkerabat jauh akan memberikan harapan keragaman genetik yang
lebih besar dibandingkan dengan penggunaan tetua yang berkerabat dekat.
Jumlah generasi menyerbuk sendiri juga mempengaruhi besarnya nilai keragaman
genetik dalam populasi.
2. Sampel genotipe yang dievaluasi
Jumlah segregasi gen yang mungkin timbul dalam suatu populasi sangat
tergantung kepada konstitusi gen yang mengendalikannya. Konstitusi gen
kuantitatif akan memberikan jumlah segregasi yang sangat besar sehingga akan
memberikan nilai duga keragaman genetik besar yang mengarah kepada
diperolehnya pendugaan nilai heritabilitas yang besar. Hal tersebut ada
28
terbatas, sehingga menyebabkan hilangnya beberapa komponen segregasi gen
(segregan) yang terlibat dalam analisis ini.
3. Metode penghitungan
Pendugaan nilai heritabilitas suatu karakter dapat diperoleh melalui beberapa
metode penghitungan yang memberikan nilai pendugaan yang berbeda.
Penggunaan metode disesuaikan dengan karakteristik populasinya, ketersediaan
materi genetiknya, atau tujuan pendugaannya.
4. Keluasan evaluasi genotipe
Seleksi di antara genotipe-genotipe tanaman pada suatu spesies didasarkan pada
penampilan masing-masing individu tanaman atau terhadap penampilan rata-rata
keturunan dari genotipe-genotipe yang dievaluasi dalam satu atau lebih ulangan,
lokasi, dan musim.
5. Ketidakseimbangan pautan
Dua alel pada suatu lokus dapat terpaut (linked) secara coupling (AB/ab) atau
secara repulsion (Ab/aB). Suatu populasi dikatakan berada dalam
ketidakseimbangan pautan apabila frekuensi pautan coupling dan repulsion tidak
seimbang.
6. Pelaksanaan percobaan
Dalam suatu desain percobaan, peranan faktor lingkungan ditunjukkan oleh
komponen galat percobaan. Besarnya nilai galat percobaan menyebabkan
menurunnya pendugaan keragaman genetik suatu karakter. Galat percobaan yang
29
pengujian ketidaktepatan pengukuran yang diamati, atau konstitusi genetik yang
masih bersegregasi.
2.5 Kemajuan Genetik
Besarnya kemajuan genetik dipengaruhi oleh keragaman, nilai duga heritabilitas,
dan intensitas seleksi yang dilakukan. Intensitas seleksi tergantung dari
banyaknya individu keturunan yang akan diseleksi. Nilai duga heritabilitas yang
tinggi dan intensitas seleksi yang tinggi diharapkan memberikan nilai kemajuan
genetik yang tinggi. Kemajuan genetik harapan dapat diukur dengan kemajuan
genetik (Suharsono et al., 2006). Kemajuan genetik merupakan suatu parameter
yang menduga penerapan seleksi suatu karakter diharapkan akan memberikan
pengaruh kepada perbaikan suatu genotipe tanaman pada intensitas seleksi
tertentu. Berdasarkan pengertian tersebut seleksi suatu karakter dalam populasi
tanaman yang diregenerasikan melalui biji dan populasi tanaman yang
bersegregasi bebas akan memperlihatkan kemajuan genetik yang diharapkan,
karena populasi F2 merupakan populasi yang memiliki tingkat keragaman yang
30
III. BAHAN DAN METODE
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Lapangan Terpadu Fakultas
Pertanian, Universitas Lampung dari bulan September 2013 sampai dengan
Januari 2014, sedangkan perbanyakan virus juga akan dilakukan di Laboratorium
Lapangan Terpadu Fakultas Pertanian. Pengamatan kemudian dilanjutkan di
Laboratorium Benih dan Pemuliaan Tanaman Universitas Lampung.
3.2 Bahan dan Alat
Bahan yang digunakan yaitu alkohol 70%, zeolit, air, Furadan 3G, fungisida
berbahan aktif mancozeb 80%, insektisida berbahan aktif delhtametrin 25 g/l
aquades, buffer fosfat, Urea 50 kg/ha, SP 36 100 kg/ha, KCl 100 kg/ha dan pupuk
kandang 10 ton/ha. Benih yang digunakan yaitu 100 butir dari satu populasi F2
hasil persilangan Tanggamus dan B3570 genotipe nomor satu dan 20 tetua kedelai
yang terdiri atas varietas Tanggamus dan B3570.
Alat yang digunakan yaitu mortal, korek api, alu, hand sprayer, mistar, gunting,
benang, kamera, cangkul, sabit, koret, golok, knapsack sprayer, polybag, cotton
bud, kertas label, botol aqua, gelas ukur, timbangan analitik, cangkul, patok,
31
Tanggamus dan B3570 merupakan hasil persilangan dengan metode dialel setengah
yang dilakukan oleh Maimun Barmawi dengan menggunakan lima tetua yaitu
B3570, Tanggamus, Orba, Taichung, dan Yellow Bean yang kemudian penelitian
tersebut dilanjutkan oleh Putri dan Jamil (2013) untuk mengetahui tingkat
ketahanan populasi F1 terhadap infeksi soybean mosaic virus. Dari 10 kombinasi
persilangan, dipilih satu kombinasi persilangan Tanggamus dan B3570 dengan
genotipe nomor satu. Persilangan ini memiliki persentase keparahan penyakit
rendah sebesar 22,5%, jumlah biji sehat sebanyak 778 butir, dan jumlah biji sakit
83 butir. Selanjutnya dari total keseluruhan biji, diambil 100 butir biji secara acak.
Pada generasi F2 rancangan percobaan yang digunakan tanpa ulangan karena
benih yang digunakan adalah benih F2 yang masih mengalami segregasi (Baihaki,
2000) dan benih belum homozigot secara genetik.
3.3 Metode Penelitian
Untuk menjawab pertanyaan dalam perumusan masalah dan untuk menguji
hipotesis maka rancangan perlakuan yang digunakan yaitu rancangan perlakuan
tunggal terstruktur bersarang, sedangkan rancangan percobaan yang digunakan
adalah rancangan percobaan tanpa ulangan. Dalam penelitian ini seluruh tanaman
32
3.4 Analisis Data
Menurut Suharsono et al.(2006 ), ragam fenotipe ( ) ditentukan dengan rumus:
σ2 f =
Keterangan:
σ2f = ragam fenotipe
Xi = nilai pengamatan tanaman ke –i µ = nilai tengah populasi
N = jumlah tanaman yang diamati
Ragam lingkungan ( ) ditentukan dengan rumus:
σ2 e =
Keterangan:
σp1 = simpangan baku tetua 1
σp2 = simpangan baku tetua 2
n1+n2 = jumlah tanaman tetua
Populasi tetua secara genetik adalah seragam sehingga ragam genotipe nol. Oleh
karena itu, ragam fenotipe yang diamati pada populasi tetua sama dengan ragam
lingkungan. Tetua dan populasi keturunannya ditanam pada lingkungan yang
sama, sehingga ragam lingkungan tetua sama dengan ragam lingkungan populasi
keturunan.
Dengan demikian ragam genetik (σ2g) dapat dihitung dengan rumus:
σ2
g= σ2p - σ2e
Keterangan : σ2
p = ragam fenotipe
σ2
33
Menurut Anderson dan Bancroft, 1952 dikutip Wahdah 1996, ragam fenotipe
dikatakan luas apabila ragam fenotipe lebih besar dua kali standar deviasi,
sedangkan ragam fenotipe dikatakan sempit apabila ragam fenotipe lebih kecil
dua kali standar deviasi.
Berdasarkan kriteria keragaman tersebut, untuk menghitung ragam lingkungan
maka diperlukan rumus penghitungan simpangan baku ( ), berdasarkan
Walpole (1992) yaitu sebagai berikut:
=
Keterangan:
= simpangan baku Xi = nilai pengamatan ke –i µ = nilai tengah populasi
N = jumlah tanaman yang diamati
Menurut Suharsono et al., 2006, pendugaan heritabilitas dalam arti luas (HL)
dengan menggunakan rumus:
HL =
Keterangan :
HL = heritabilitas arti luas
= ragam genotipe = ragam fenotipe
Penduga nilai heritabilitas menurut Mendez-Natera et al., 2012 yaitu
1. Heritabilitas tinggi apabila H ≥ 0,5
2. Heritabilitas sedang apabila 0,2 < H < 0,5
34
Menurut Suharsono et al. (2006), nilai duga kemajuan seleksi dapat dihitung
berdasarkan rumus:
R = i σx HL
Keterangan:
R = Respons terhadap seleksi
i = Intensitas seleksi yang diterapkan
HL = Pendugaan heritabilitas dalam arti luas suatu karakter
σx = Simpangan baku suatu karakter
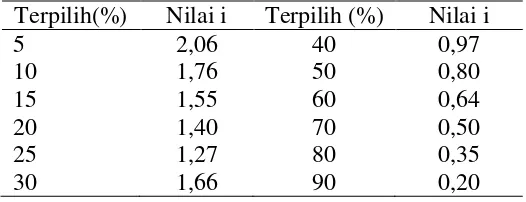
Intensitas seleksi yang diterapkan yaitu sebesar 20%, sehingga nilai i yang
[image:55.595.107.370.353.454.2]digunakan yaitu 1,40.
Tabel 1. Nilai intensitas seleksi (i) pada kemajuan genetik
Terpilih(%) Nilai i Terpilih (%) Nilai i
5 2,06 40 0,97
10 1,76 50 0,80
15 1,55 60 0,64
20 1,40 70 0,50
25 1,27 80 0,35
30 1,66 90 0,20
KGH (%) = R x 100% Nilai tengah
Kriteria nilai duga kemajuan genetik harapan berdasarkan Begun dan Sobhan
(1991) dikutip Hadiati et al. (2003) adalah
a. Tinggi apabila nilai KGH > 14%;
b. Sedang apabila nilai 7% ≤ KGH ≤ 14%
35
3.5 Pelaksanaan Penelitian
3.5.1. Pembuatan larutan buffer fosfat
Bahan pembuatan larutan buffer fosfat terdiri atas KH2PO4 (larutan A: 1,36 g),
Na2HPO4 . 2H2O (larutan B: 1,78 g) dan akuades sebanyak dua liter. Alat yang
digunakan adalah timbangan elektrik, dua buah gelas ukur berukuran 1000 ml dan
satu buah berukuran 500 ml, pengaduk, dan botol berukuran dua liter. Pembuatan
buffer fosfat dapat dilakukan dengan menimbang 1,36 g KH2PO4 dan 1,78 g
Na2HPO4.2H2O. Pembuatan larutan A dilakukan dengan menimbang 1,36 g
KH2PO4 dan dilarutkan ke dalam satu liter akuades. Pembuatan larutan B
dilakukan dengan menimbang 1,78 g Na2HPO4 . 2H2O, kemudian dilarutkan ke
dalam satu liter akuades. Satu liter buffer fosfat diperoleh dengan cara
mencampur 510 ml larutan A dan 490 ml larutan B, kemudian dimasukkan ke
dalam botol dan ditutup rapat.
3.5.2. Perbanyakan inokulum soybean mosaic virus
Benih kedelai yang digunakan untuk perbanyakan SMV yaitu benih varietas Orba
karena merupakan benih yang rentan terhadap infeksi virus. Kegiatan pertama
yang dilakukan untuk perbanyakan inokulum SMV yaitu pembuatan sap/ekstrak
daun. Sap dibuat dengan cara menggerus daun kedelai yang telah terinfeksi
sebanyak 5 g dengan menggunakan mortal dan alu yang diencerkan dengan buffer
fosfat pH 7 sebanyak 5 ml. Inokulasi secara mekanik (mechanical inoculation)
dilakukan sesuai dengan prosedur Akin (2006) yaitu setelah daun berjumlah lebih
dari 4 helai atau berumur 10 hari. Langkah pertama yaitu taburkan zeolit ke
36
daun mengalami luka mikro (sublethal wounding or abrasi) sehingga virus dapat
masuk. Kemudian sap (ekstrak daun) dioleskan pada permukaan daun tanaman
dengan menggunakan cotton bud. Setelah sap dioleskan, dilakukan pencucian
menggunakan aquades dengan cara disemprot menggunakan hand sprayer.
3.5.3. Persiapan lahan
Lahan diolah dengan menggunakan cangkul sedalam 20—25 cm. Tujuan
pengolahan lahan yaitu untuk memperbaiki sifat fisik tanah dan untuk
membersihkan gulma. Kemudian tanah tersebut dicampur dengan pupuk kandang
dengan dosis 10 ton/ha secara merata untuk meningkatkan kesuburan tanah.
3.5.4. Penanaman
Penelitian ini dilakukan dengan menanam 100 benih F2 hasil persilangan
Tanggamus dan B3570 pada petak percobaan berukuran 3 m x 4 m. Benih tersebut
ditanam pada petak percobaan dengan jarak tanam 20 cm x 50 cm. Jarak
antarbaris 50 cm dan jarak tanam dalam baris 20 cm. Pada setiap baris ditanam
15 benih yang sama yang dipilih secara acak, sedangkan tetua ditanam pada baris
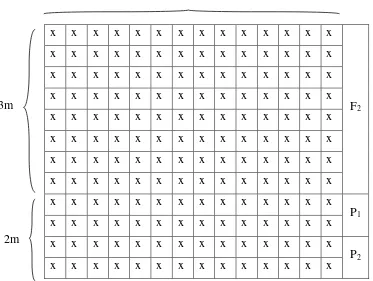
terluar. Tata letak penanaman kedelai F2 hasil persilangan Tanggamus dan B3570
37
x x x x x x x x x x x x x x
F2
x x x x x x x x x x x x x x
x x x x x x x x x x x x x x
x x x x x x x x x x x x x x
x x x x x x x x x x x x x x
x x x x x x x x x x x x x x
x x x x x x x x x x x x x x
x x x x x x x x x x x x x x
x x x x x x x x x x x x x x
P1
x x x x x x x x x x x x x x
x x x x x x x x x x x x x x
P2
[image:58.595.115.488.116.397.2]x x x x x x x x x x x x x x
Gambar 1. Tata letak penanaman benih kedelai hasil persilangan Tanggamus x B3570 dan kedua tetuanya.
Keterangan:
P1 = Tetua Tanggamus P2 = Tetua B3570
F2 = Persilangan Tanggamus x B3570
3.5.5. Pemupukan
Pemupukan dilakukan dua kali yaitu pada awal tanam dan pada fase generatif.
Pupuk yang diaplikasikan yaitu KCl 100 kg/ha, SP-36 100 kg/ha, dan Urea 50
kg/ha. Pupuk diaplikasikan dengan jarak 5 cm dari lubang tanam tanaman
kedelai. 2m 3m
38
3.5.6. Inokulasi soybean mosaic virus di lapangan
Tanaman kedelai yang sudah memiliki daun terbuka sempurna (7—10 HST) dapat
diinokulasi dengan sap SMV yang sebelumnya telah ditaburi zeolit. Setelah daun
dinokulasi, daun tersebut dicuci kembali dengan aquades secukupnya
menggunakan hand sprayer. Tahapan inokulasi soybean mosaic virus di lapangan
[image:59.595.116.510.271.479.2]dapat dilihat pada Gambar 2.
Gambar 2. Tahap-tahap inokulasi soybean mosaic virus di lapangan.
3.5.7 Pelabelan
Setiap tanaman yang telah diinokulasi masing-masing diberi label seperti waktu
penanaman dan tanggal inokulasi untuk mempermudah dalam pengamatan.
3.5.8 Perawatan dan pemeliharaan tanaman
Perawatan dan pemeliharaan tanaman meliputi penyulaman tanaman yang mati,
penyiangan gulma, penyiraman, pengendalian hama dan penyakit, perbaikan label
39
menggunakan koret. Penyemprotan dengan insektisida dan fungisida dilakukan
sesuai dengan kebutuhan. Insektisida yang digunakan yaitu Decis (Delmetrin)
dan fungisida yang digunakan yaitu Dithane (Mankozeb). Penyiraman dilakukan
setiap hari pada sore hari dengan menggunakan gembor dan selang.
3.5.9 Pemanenan
Ciri-ciri umum tanaman kedelai yang siap panen yaitu polong berwarna kuning
kecoklatan secara merata dan matang serta adanya degradasi klorofil pada daun
tanaman yang menyebabkan daun tanaman kedelai menguning. Pemanenan
dilakukan dengan memanen tanaman kedelai secara utuh dengan mencabut satu
per satu tanaman, kemudian dimasukkan ke dalam kantong panen yang telah
diberi label.
3.5.10 Pengamatan
Pengamatan yang dilakukan pada penelitian ini terdiri atas pengamatan sebelum
panen dan pengamatan setelah panen. Pengamatan sebelum panen meliputi:
1. Periode inkubasi, dihitung dari waktu inokulasi sampai dengan timbulnya
gejala (Mulia, 2008).
2. Keparahan penyakit, diamati minggu ke enam setelah tanam dan dilakukan
terhadap 10 daun tanaman trifoliate, serta dihitung menurut Campbell dan
Madden yang dikutip Mulia (2008). Pengamatan dilakukan pada 10 daun
trifoliate pada batang utama. Hal ini dilakukan karena 6 MST dianggap dapat
40
KP = x 100%
Keterangan:
KP =Keparahan penyakit
n =Jumlah sampel yang diamati Z =Nilai skor tertinggi
N =Jumlah sampel untuk kategori serangan V =Nilai skor untuk kategori serangan
Menurut Akin (2006), gejala serangan setiap jenis virus yang muncul memiliki
[image:61.595.112.510.308.517.2]rincian sebagai berikut:
Gambar 3. Skor gejala penyakit
Keterangan:
Tidak bergejala = 0 (A), klorosis dan tulang daun memucat = 1 (B), mosaik dengan klorosis pada tulang daun dan permukaan daun = 2 (C), mosaik berat, klorosis dan terjadi pembengkokan pada permukaan daun, daun melengkung ke bawah atau ke atas = 3 (D), dan malformasi daun = 4 (E).
A B C
41
Kategori keparahan penyakit (%):
1—10 = Sangat tahan 11—25 = Tahan 26—35 = Agak tahan 36—50 = Agak rentan 51—75 = Rentan 76—100 = Sangat rentan
Pengamatan yang dilakukan setelah panen meliputi:
1. Tinggi tanaman, diukur dari pangkal batang sampai titik tumbuh tanaman.
Pengukuran dilakukan setelah panen dalam satuan cm;
2. Jumlah cabang produktif, dihitung berdasarkan jumlah cabang yang dapat
m