SEL SURYA HIBRID NANOPARTIKEL ZnO/KLOROFIL
TERMODIFIKASI ION LOGAM (Zn
2+dan Cu
2+)
SUGIANTO
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Sel Surya Hibrid Nanopartikel ZnO/Klorofil termodifikasi Ion Logam (Zn2+ dan Cu2+) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Februari 2014
Sugianto
RINGKASAN
SUGIANTO. Sel Surya Hibrid Nanopartikel ZnO/Klorofil termodifikasi Ion Logam (Zn2+ dan Cu2+). Dibimbing oleh AKHIRUDDIN MADDU dan IRMANSYAH.
Zinc Oxide (ZnO) merupakan semikonduktor tipe-n dengan besar lebar pita
energi (Band Gap) adalah 3,37 eV pada suhu ruang dan 3,34 eV pada suhu rendah
dengan besar energi ikat eksitonnya adalah 60 meV. ZnO yang disintesis dengan menggunakan metode hidrotermal, telah menghasilkan penurunan ukuran partikel seiring penambahan durasi hidrotermal. Hasil uji sifat kristalografi dengan XRD telah memperlihatkan bentuk kristal pada semua puncak difraksi ZnO dengan struktur heksagonal wurtzite, dengan ukuran kristal yang meningkat terhadap
perubahan ukuran partikel. Perubahan ukuran partikel ini telah menyebabkan pula perubahan pada puncak serapan dari ZnO, sebagaimana yang diperlihatkan melalui uji sifat optik menggunakan spektrofotometer UV-Vis. Perubahan serapan ini juga telah menyebabkan perubahan pada energi band gap, dimana energi band gap nya meningkat terhadap ukuran partikelnya.
Dalam aplikasi sel surya, klorofil dianggap kurang efektif karena sifat alamiahnya yang mudah terdegradasi akibat dari beberapa reaksi diantaranya adalah asam, cahaya dan suhu. Hasil uji stabilitas dengan menggunakan lampu halogen 34 W/m2 selama 5 jam, bahwa subtitusi klorofil dengan ion logam Zn2+ dan Cu2+ telah memperlihatkan bentuk yang lebih stabil dari klorofil alamiahnya.
Hasil karakterisasi sifat optik memperlihatkan bahwa kombinasi ZnO/klorofil dalam bentuk film hibrid telah menyebabkan pergeseran daerah serapan dari ZnO menjadi lebih lebar dari UV ke Visibel. ZnO/klorofil memiliki rentang serapan 350-515 nm, ZnO/Zn-feofitin 332-401 nm dan 332-632 nm untuk Cu-feofitin. Hasil kombinasi ZnO/klorofil dan CuSCN dalam sel surya hibrid, klorofil yang termodifikasi dengan ion logam Zn2+ dan Cu2+, memperlihatkan bentuk kurva I-V yang lebih stabil. Ini ditandai dengan nilai fill factor nya yang lebih besar dari klorofil alami. Meskipun demikian, sel surya
dengan klorofil alami mampu menghasilkan nilai efisiensi yang lebih tinggi dari klorofil yang tersubtitusi. Ini dikarenakan kosentrasi yang menurun diperlihatkan oleh klorofil yang termodifikasi. Penurunan kosentrasi klorofil setelah subtitusi ion logam ini, ditandai dengan penurunan nilai absorbansinya.
SUMMARY
SUGIANTO. Hybrid Solar Cells of ZnO Nanoparticles/Chlorophyll was modified Metal Ions (Zn2+ and Cu2+ ). Supervised by AKHIRUDDIN MADDU and IRMANSYAH.
Zinc Oxide (ZnO) is a n-type semiconductor with a wide the energy band (Band Gap) is 3.37 eV at room temperature and 3.34 eV at low temperature with a large exiton binding energy is 60 meV. ZnO has been synthesized by hydrothermal method, resulting in a decrease in particle size over the duration of the hydrothermal changes. Crystallographic structure of ZnO were characterized using XRD, has shown the characteristic pattern of a hexagonal wurtzite structure, the crystallite size increases to changes in particle size. Changes in particle size has also led to a change in the absorption peak of ZnO as has been demonstrated posted under test using the optical properties of UV-Vis spectrophotometer. Changes of this uptake has also led to changes in the energy band gap, which increases its band gap energy of the particle size.
In electronic applications, especially in solar cells. Chlorophyll is considered less effective, because of their very nature are easily degraded as a result of several reactions which are acid, lighting and temperature. The results of the stability test using a halogen lamp 34 W/m2 for 5 hours, that the substitution of chlorophyll with metal ions Zn2+ and Cu2+ has been shown to form more stable than natural chlorophyll. The characterization of the optical properties, the combination of ZnO / chlorophyll in the form of hybrid films has led to a shift in the absorption region of ZnO becomes more widely from the UV to Visible. ZnO/chlorophyll has absorption range of 350-515 nm, ZnO / Zn-feofitin 332-401 nm and 332-632 nm for Cu-feofitin. The combination of ZnO/chlorophyll and CuSCN as a solid electrolite in hybrid solar cell, a modified chlorophyll with metal ions Zn2+ and Cu2+ has been shown to form a more stable I-V curve. It is characterized by its fill factor value greater than natural chlorophyll. Nevertheless, solar cells with natural chlorophyll has been able to produce higher efficiency values of chlorophyll were substituted.
© Hak Cipta Milik IPB, Tahun 2014
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Biofisika
SEL SURYA HIBRID NANOPARTIKEL ZnO/KLOROFIL
TERMODIFIKASI ION LOGAM (Zn
2+dan Cu
2+)
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
Judul Tesis : Sel Surya Hibrid Nanopartikel ZnO/Klorofil Termodifikasi Ion Logam (Zn2+ Dan Cu2+)
Nama : Sugianto NIM : G751110111
Disetujui oleh Komisi Pembimbing
Dr Akhiruddin Maddu, SSi MSi
Ketua Dr Ir Irmansyah, MSi Anggota
Diketahui oleh
Ketua Program Studi Biofisika
Dr Agus Kartono, SSi MSi
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
Tanggal Ujian:
PRAKATA
Puji syukuri bagi Allah SWT, karena atas limpahan rahmat, taufik dan hidayah-Nya hingga penulis dapat menyelesaikan karya ilmiah ini dengan baik. Judul dari penelitian ini adalah Sel Surya Hibrid Nanopartikel ZnO/Klorofil termodifikasi Ion Logam (Zn2+ dan Cu2+). Penelitian ini dilaksanakan sejak bulan Oktober 2012 sampai September 2013 di Laboratorium Biofisika IPB, Bogor.
Teristimewa penulis ungkapkan penghargaan dan ucapan terima kasih yang kepada ayahanda (ARJO), Ibunda (PONIYEM) yang telah mencurahkan segalanya atas kasih sayang, serta kakak (Ani Winarsih dan Siti Asiyah) dan Adikku (Rizky Reza Atfatur) yang telah memberikan semangat, do’a, perhatian dan pengorbanannya yang tak terhingga kepada penulis sehingga penulis mampu menyelesaikan studi. Karya ini pula tak lupa saya persembahkan buat seseorang yang unik RASDIANA, atas segala supportnya saya ucapkan terima kasih.
Penulis sadar sepenuhnya bahwa tugas akhir ini dapat dirampungkan berkat bantuan dari berbagai pihak. Oleh karena itu, dengan segala kerendahan hati, penulis mengucapkan terima kasih dan penghargaan yang sebesar-besarnya kepada Bapak Dr. Akhiruddin Maddu, SSi, MSi dan Bapak Dr. Ir. Irmansyah, MSi sebagai pembimbing yang telah meluangkan waktu dan memberikan bimbingan, arahan dan kritik yang sangat berharga bagi penulis selama pengerjaan karya ilmiah ini. Terima kasih kepada Bapak Dr. Agus Kartono, MSi yang telah bersedia sebagai Penguji Luar Komisi dalam ujian sidang tesis penulis. Terima kasih kepada Irna, Junaidi dan para Dosen dan Staf Fisika lainnya atas bantuannya selama ini. Tak luput pula ucapan terimakasih saya kepada Bapak Muhammad Nur Jaya, Ibu Titien Yusnita, Ibu Atira Maddu yang telah memberikan support baik moril maupun materil selama penulis menempuh studi. Teristimewa buat rekan-rekan sekalian khususnya angkatan 2011 SPS Biofisika kepada Endang Rancasa, Masrur, Otto Muzikarno, Farly T, Abd Wahidin, TB, Idawati, Suryanti, Nur’aisyah salam kompak selalu buat kalian.
Ucapan terima kasih juga penulis tujukan pada semua pihak yang telah memberikan dorongan, bimbingan dan kemudahan serta bantuan moril dan materil baik secara langsung maupun tidak langsung selama penulis hingga penyelesaian tugas akhir ini yang tak tersebutkan.
Dan akhirnya penulis mengucapkan semoga karya tulis ini dapat bermanfaat dan inspirasi bagi semua pihak khususnya Bangsa ini.
Bogor, Februari 2014
DAFTAR ISI
DAFTAR TABEL DAFTAR GAMBAR DAFTAR LAMPIRAN 1 PENDAHULUAN Latar Belakang Rumusan Masalah TujuanRuang Lingkup Penelitian
2 SINTESIS DAN KARAKTERISASI NANOSTRUKTUR ZnO Pendahuluan
Tujuan Metode
Hasil dan Pembahasan Simpulan
3 EKSTRAKSI, MODIFIKASI DAN KARAKTERISASI KLOROFIL Pendahuluan
Tujuan Metode
Hasil dan Pembahasan Simpulan
4 FABRIKASI DAN KARAKTERISASI SEL SURYA HIBRID ZnO-KLOROFIL
Pendahuluan Tujuan Metode
Hasil dan Pembahasan Simpulan
5 PEMBAHASAN UMUM
DAFTAR TABEL
1 Nilai parameter kisi ZnO pada durasi hidrotermal 2 Nilai parameter dalam sel surya
3 Perbandingan peforma sel surya hibrid
4 27 30
DAFTAR GAMBAR
1 Pola difraksi nanopartikel ZnO yang disintesis dengan menggunakan metode hidrotermal selama durasi 3 jam, 6 jam dan 12 jam
2 Foto SEM film permukaan morfologi ZnO a (3 jam), b (6 jam), c (12 jam)
3 Pengaruh durasi terhadap ukuran partikel dan kristal pada metode hidrotermal
4 Sifat optik transmitansi dari semikonduktor film ZnO yang diukur dengan spektrometer UV-Vis
5 Kurva hubungan Gärtner's pada transisi langsung dan tak langsung semikonduktor
6 Kurva hubungan nilai absorbansi (α) terhadap panjang gelombang (λ) 7 Plot (αhv)2 terhadap energi foton absorbansi (hv)
8 Perubahan energi gap terhadap ukuran partikel dan ukuran kristal 9 Skema pengukuran flouresensi dye klorofil
10 Reaksi klorofil terhadap asam
11 Kurva hasil subtitusi ion logam Zn2+ dan Cu2+ pada inti klorofil
12 Kurva perbandingan nilai maksimum antara absorbansi dan emisi dari
dye alam dalam etanol 96%. Klorofil (A), Zn-feofitin (B) dan Cu-feofitin(C)
13 Kurva absorbansi degradasi klorofil dan klorofil kompleks terhadap waktu: Klorofil (A), Zn-peofitin (B), Cu-peofitin (C).
14 Perubahan absorbansi maksimum pada daerah Q-band setelah penyinaran selama 5 jam pada klorofil, Zn-feofitin dan Cu-feofitin
15 Rangkaian pengukuran karakterisasi arus tegangan sel surya 16 Sifat optik film hibrid nanopartikel ZnO/klorofil
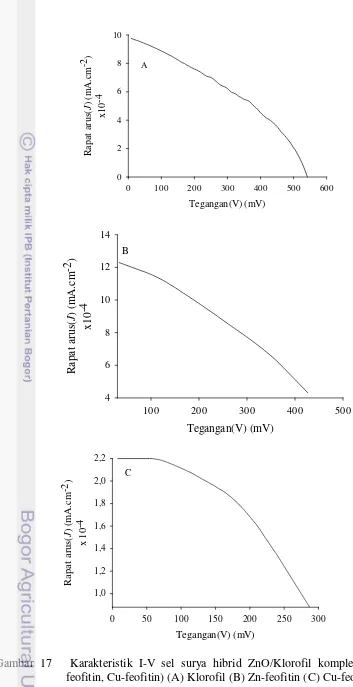
17 Karakteristik I-V sel surya hibrid ZnO/Klorofil kompleks (Zn-feofitin, Cu-feofitin) (A) Klorofil (B) Zn-feofitin (C) Cu-feofitin
18 Mekanisme transpor elektron pada sel srya hibrid
5 6 7 8 9 9 10 10 13 14 15 17 19 20 22 23 26 29
DAFTAR LAMPIRAN
1 Data JCPDS
2 PerhitunganNilai Parameter Kisi Kristal (a, c) 3 PerhitunganUkuran Kristal
4 PerhitungaNilai Celah Pita Energi (band gap)
5 Perhitungan Nilai Parameter dalam Sel Surya
1
1
PENDAHULUAN
.
Latar Belakang
Sel surya merupakan pengembangan teknologi yang memanfaatkan cahaya matahari untuk diubah menjadi energi listrik. Penelitian mengenai sel surya bukan suatu yang terbarukan, karena penelitian sel surya sendiri sudah sejak lama dikembangkan. Sel surya yang pertama kali dikembangkan adalah sel surya yang berbasiskan silikon berupa silikon kristal tunggal dan silikon polikristal yang efisiensinya mencapai 25±0,5% (Ozgur. 2005). Generasi kedua adalah sel surya yang berbasis film tipis, dimana sel surya ini dibuat dari semikonduktor seperti Tembaga Indium Galium diselenida (CIGS) dan kadmium telluride (CdTe) sebagai bahan penyerapnya. Efisiensi yang dicapai pada generasi ini mencapai 19,9% (CIGS) (Repins et al. 2008). Karena bahannya yang bersifat toksik,
sehingga sel surya bentuk ini dianggap tidak ramah lingkungan dan dapat membahayakan bagi peneliti. Generasi yang ketiga merupakan jenis sel surya berbasis semi konduktor organik seperti PCBM, C60, P3HT dan lain sebagainya. Sel surya jenis ini dianggap ramah lingkungan dan relatif lebih murah bila dibandingkan dengan generasi sebelumnya, tetapi efisiennya masih jauh dari generasi sebelumnya yang hanya mencapai 1,78% (Tong et al. 2012). Di tahun
1991 seorang ilmuan yang bernama Gratzel (Gratzel. 1991) telah memperkenalkan jenis sel surya baru yang dikenal sebagai dye-sensitised solar cell (DSSC), yang mana sel surya bentuk ini didasarkan pada kaidah proses
fotosintesis yang terjadi di alam bebas yang dilakukan oleh semua jenis tanaman. Selain sel surya organik dan anorganik ada pula jenis sel hibrid yaitu jenis sel surya yang merupakan perpaduan antara semikonduktor anorganik dan organik. Material organik dalam sel surya jenis ini berfungsi sebagai penyerap cahaya dan bagian anorganiknya adalah nanokristal semikonduktor biasanya material golongan II-IV. Secara umum lapisan foto aktif memiliki bentuk struktur bilayer dan struktur bulk heterojuction dengan memadukan bahan yang bersifat donor dan
akseptor yang didepositkan pada subtrat. Berbeda dengan bulk semikonduktor
anorganik, penyerapan foton oleh semikonduktor organik tidak menghasilkan pembawa muatan bebas tetapi terikat oleh pasangan elektron-hole yang selanjutnya disebut sebagai eksiton (Gledhil. 2005). Secara khusus prinsip kerja sel surya hibrid yaitu diawali dengan penyerapan foton oleh bahan absorban dari pita valensi (VB) ke pita konduksi (CB) dalam bentuk eksiton. Eksiton berdifusi ke interface donor/akseptor, dimana muatan yang ditransferkan mengarah pada
pemisahan eksiton mejadi elektron bebas dan hole dibawah pengaruh medan listrik internal yang ditransferkan oleh material donor atau akseptor yang dominan dan akhirnya dikumpulkan pada masing-masing elektroda. Singkatnya ada empat tahapan dalam sel surya hibrid yaitu penyerapan foton, difusi eksiton, pemisahan muatan serta transportasi pembawa muatan dan pengumpulan (Greenham. 2008).
2
Pada tanaman, semua pigmen memiliki karakteristik tersendiri dalam merespon cahaya. Klorofil merupakan bagian dari tanaman yang memiliki peran aktif dalam proses fotosintesis. Klorofil menyerap cahaya berupa gelombang elektromagnetik pada spektrum kasat mata (visible) dengan panjang gelombang
antara 400 sampai 700 nm.
Dalam beberapa dekade terakhir, klorofil dan turunannya telah dikembangkan untuk berbagai aplikasi elektronik, diantaranya adalah sebagai optoelektronik (Ohtani et al. 2011), fotosensitiser (Chand et al. 2012),
fototransistor (Chen et al. 2013) dan terapi fotodinamik untuk kanker (Park et al.
1989).
Secara umum klorofil merupakan pigmen yang mudah terdegradasi akibat berkurangnya atau menurunnya logam Mg di dalam inti cincin porfirin, Ini disebabkan oleh beberapa faktor yaitu panas (Erge et al. 2008) dan kosentrasi
asam (Koca et al.2003), sehingga beberapa penelitian telah melakukan modifikasi
terhadap logam inti pada klorofil (Mg) dengan unsur logam lainnya yaitu seng (Zn2+) dan tembaga (Cu2+).(Kupper et al. 1996), agar pigmen klorofil lebih stabil.
Pengembangan lebih lanjut dalam penelitian ini, akan memanfaatkan klorofil yang termodifikasi ion logam Zn2+ dan Cu2+ sebagai fotosensitiser sel surya hibrid nanopartikel ZnO.
Perumusan Masalah
Masalah utama dalam penelitian ini adalah bagaimana mengoptimalkan pembentukan nanopartikel ZnO dan klorofil kompleks (Zn2+ dan Cu2+) yang diambil dari tanaman tingkat tinggi serta menentukan bagaimana bentuk struktur divais yang baik untuk meningkatkan peforma sel surya hibrid.
Tujuan Penelitian
Memanfaatkan klorofil termodifikasi ion logam Zn2+ dan Cu2+ sebagai fotosensitiser pada sel surya hibrid nanopartikel ZnO
Ruang Lingkup Penelitian
Ruang lingkup penelitian dalam penelitian ini meliputi:
1. Membuat dan mengkarakterisasi material semikonduktor nanopartikel ZnO yang diperoleh dengan metode hidrotermal
2. Mensintesis dan mengkarakterisasi klorofil kompleks (Zn-feofitin dan Cu-feofitin).
3
2
SINTESIS DAN KARAKTERISASI NANOSTRUKTUR ZnO
Pendahuluan
ZnO merupakan bahan semikonduktor tipe-n yang memiliki lebar pita energi 3,37 eV pada suhu ruang dan 3,34 eV pada temperatur rendah dengan nilai energi ikat eksitonnya sebesar 60 meV (Takena et al. 2012). ZnO memiliki
struktur kristal wurtzite heksagonal, dengan nilai parameter kisinya a = 3249 Å
dan c = 5,206 Å (Wu et al.2007).
Beberapa aplikasi yang telah dikembangkan dari semikonduktor ZnO adalah sel surya (Xiaohui et al. 2008; Beek et al. 2005), sensor (Parviz et al. 2011,
Gupta et al. 2010, Chueh-Yang et al. 2009), optoelektronik, ZnO thin film transistor (ZnO-TFTs) dibuat dalam bentuk transparan dan fleksibel sebagai
lapisan selektif elektron pada sel surya organik yang fleksibel (Lee et al. 2010).
Beberapa metode yang telah dilakukan untuk membentuk struktur kristal ZnO diantaranya adalah metode sol gel (Hassan et al. 2011), hidrotermal
(Yong-hong et al, 2005; Sarika et al. 2012), chemical bath depotitions (CBD), (Ali et al.
2011; Wen-Yao et al. 2012). Dari metode yang telah disebutkan tersebut,
hidrotermal merupakan salah satu metode yang efektif dan efisien, karena dalam proses hidrotermal dapat dikontrol suhu dan tekanan yang sangat berpengaruh pada hasil yang diperoleh. Untuk metode hidrotermal yang telah dilakukan dalam mensintesis nanopartikel ZnO, dikaji berdasarkan pada variasi suhu (Aneesh et al.
2007; Meen et al. 2007). Dalam penelitian ini akan dikaji pengaruh durasi
hidrotermal terhadap struktur morfologi, ukuran partikel dan sifat optik dari nanopartikel ZnO.
Tujuan
Mensintesis dan mengkarakterisasi nanostruktur ZnO dengan menggunakan metode hidrotermal dengan durasi 3 jam, 6 jam dan 12 jam.
Metode
Sintesis nanopartikel ZnO
Penumbuhan nanopartikel ZnO dilakukan dengan cara melarutkan 8,75 gram CH3COO)2Zn.2H2O ke dalam 28 ml etanol (C2H5OH) dan 12 ml ethylen glycol (HOCH2CH2OH) dan diaduk selama 10 menit sampai terlarut sempurna. Kemudian larutan yang terbentuk dimasukkan ke dalam reaktor hidrotermal dengan durasi 3 jam, 6 jam dan 12 jam. Endapan yang diperoleh dari proses hidrotermal dicuci dengan akuades dan etanol secara bergantian sebanyak tiga kali lalu dikeringkan diatas hotplate pada suhu 100oC sampai mengering, kemudian
dikalsinasi selama dua jam pada suhu 300oC. Selanjutnya dilakukan uji karakterisasi X-ray diffraction (XRD) (GBC Emma) untuk menentukan struktur
4
Untuk pengukuran sifat optik dari film ZnO, dilakukan dengan menggunakan spektrometer Uv-Vis (Ocean Optics).
Fabrikasi dan karakterisasi film ZnO
Pertama, bubuk ZnO dibuat suspensi koloid yang di dispersikan dengan
ethylen glycol 5 wt% dan etanol (Ibrahem et al. 2013) kemudian diaduk dengan
magnetik stirrer selama 30 menit. Setelah itu dilapiskan pada kaca preparat dengan menggunakan metode casting. Sampel yang telah dilapiskan pada preparat
kemudian dipanaskan di atas hot plate selama 1 jam pada suhu 100oC, setelah itu
dilakukan uji karakterisasi dengan menggunakan spektrofotometer UV-Vis (Ocean Optics). Karakteristik film ZnO dipelajari berdasarkan spektrum
transmitansi, diantaranya untuk menentukan lebar celah energi (band gap).
Hasil dan Pembahasan
Struktur kristal Nanopartikel ZnO
Hasil sintesis nanopartikel ZnO dengan metode hidrotermal kemudian dilakukan beberapa uji karakterisasi yaitu XRD, SEM dan spektrofotometer UV-Vis. Dari hasil XRD memperlihatkan pola-pola difraksi menunjukkan karakteristik dari ZnO yang sesuai dengan data JCPDS no. 1314-13-2. Dari pola-pola tersebut memperlihatkan bentuk pola-pola dari polikristalin ZnO yang merupakan bentuk struktur wurtzite heksagonal (Wu et al. 2007, Maddu et al. 2006) dengan
nilai parameter kisi a dan c yang telah disesuaikan dengan data JCPDS No.1314-13-2 sebagaimana yang tercantum dalam lampiran 1. Hasil perhitungan ini juga tidak jauh berbeda dengan hasil yang diperoleh dari beberapa peneliti sebelumnya yaitu a= 3,620Å, c= 5,214Å (Khan et al. 2011), a= 3,248Å, c= 5,2Å (Hamedani
dan Farzaneh. 2006). Parameter kisi dihitung dengan menerapkan metode Cohen
untuk kristal ZnO heksagonal dengan persamaan (1). Hasil perhitungan ini dapat dilihat pada Tabel 1.
dimana d adalah jarak antar kisi kristal, a dan c adalah parameter kisi kristal.
Tabel 1. Nilai parameter kisi ZnO pada durasi hidrotermal
Sampel a (Å) JCPDS (Å) c (Å) JCPDS (Å) 3 jam 3,256
3,249
5,212
5,209
6 jam 3,256 5,215
12 jam 3,264 5,228
Nilai parameter kisi ZnO sebagaimana diperlihatkan pada Tabel 1, menunjukkan adanya peningkatan nilai parameter kisi meskipun tidak begitu signifikan. Menurut Samuel et al. (2009), meningkatnya nilai parameter kisi ini
5 dan 12 jam diperlihatkan pada Gambar 1. Pada Gambar 1 diperlihatkan bahwa bidang 101 memiliki nilai intensitas lebih tinggi dari lainnya. Ini menggambarkan bahwa bidang 101 lebih dominan pada struktur ZnO yang dihasilkan.
Ukuran kristal dari pola difraksi Gambar 1, didapatkan dengan menerapkan persamaan (2).
σ adalah ukuran kristal rata-rata, k adalah konstanta (0,9), λ adalah panjang
gelombang sumber sinar-X yaitu 1,54059 Å, adalah lebar puncak setengah maksimum (FWHM) masing-masing puncak, dan adalah sudut difraksi.
Ukuran kristal rata-rata yang didapatkna dari perhitungan berdasarkan durasi hidrotermal adalah 44,32 nm untuk durasi 3 jam, 50,56 nm untuk durasi 6 jam dan 54,37 nm untuk durasi 12 jam memperlihatkan ukuran dari nanokristal. Hasil ini mirip dengan metode hidrotermal lainnya yang meninjau ukuran partikel berdasarkan pada perubahan suhu dan kosentrasi (Aneesh at al.2007).
In
te
ns
ita
s (
a.u
)
2 Tetha (derajat)
30 40 50 60 70
100
201
112
200
103
110
102
101
002
3 Jam 6 Jam 12 Jam
6
Morfologi
Hasil karakterisasi SEM memperlihatkan bentuk morfologi ZnO tampak lebih homogen dengan ukuran partikelnya menurun bersamaan dengan pertambahan durasi hidrotermal. Dari analisis Gambar 2 (a, b dan c) dengan menggunakan CorelDraw, didapatkan ukuran partikel rata-rata untuk setiap durasi 3 jam yaitu 249 nm, 147 nm untuk durasi 6 jam dan 107 nm untuk durasi 12 jam. Menurunnya ukuran partikel ini ternyata menyebabkan meningkatnya ukuran kristal dengan nilai parameter kisinya juga meningkat (Samuel et al. 2009). Ini
kemungkinan disebabkan oleh menurunnya ukuran partikel, sehingga dalam pembentukan kristal akan lebih mudah dibandingkan dengan partikel yang lebih besar. Pada Gambar 2, juga memperlihatkan adanya pengaruh ukuran partikel terhadap suhu saat dilakukan kalsinasi. Dimana pada Gambar 2(c) memperlihatkan adanya proses algomerasi (penggumpalan) yang diakibatkan ukuran partikel lebih kecil yang lebih rentan terhadap suhu kalsinasi.
(a) (b)
(c)
7 Hubungan antara ukuran partikel dengan ukuran kristal terhadap perubahan waktu lebih jelasnya dapat dilihat pada Gambar 3. Gambar 3 memperlihatkan bahwa lama waktu hidrotermal yang digunakan menyebabkan ukuran partikel semakin menurun dan menghasilkan ukuran kristal yang meningkat. Meningkatnya ukuran kristal ini, dihasilkan dari ukuran partikel yang lebih kecil. Karena sifat dari suatu partikel, semakin kecil akan memiliki tingkat keteraturan struktur molekul yang baik.
Waktu (jam)
2 4 6 8 10 12
U ku ra n kr is ta l ( nm ) 42 44 46 48 50 52 54 56 U ku ra n pa rt ik el ( nm ) 80 100 120 140 160 180 200 220 240 260 Ukuran kristal Ukuran partikel
Gambar 4. Pengaruh durasi terhadap ukuran partikel dan kristal pada metode hidrotermal
Sifat optik dan lebar pita energi
Sifat optik ZnO nanopartikel ditentukan berdasarkan pengamatan spektrum transmitansi yang diperoleh dengan memakai alat spektrofotometer UV-Vis. Dari
hasil pengukuran ini didapatkan film ZnO menyerap spektrum UV pada panjang gelombang maksimum 361 nm untuk sampel 3 jam, 364 nm untuk sampel 6 jam dan 367 nm untuk sampel 12 jam.
Seperti yang telah diketahui, faktor durasi hidrotermal menyebabkan perbedaan ukuran partikel untuk setiap waktunya, sehingga ukuran partikel ini kemungkinan mempengaruhi terjadinya pergeseran pada daerah serapan meskipun tidak begitu signifikan. Bila merujuk pada hasil penelitian sebelumnya, dinyatakan bahwa pergeseran puncak serapan dari panjang gelombang yang rendah ke yang lebih tinggi disebabkan oleh ukuran partikel yang berbeda, sehingga Ini akan berpengaruh pada energi celah pita yang dihasilkan. Karena energi celah pita itu sendiri akan meningkat seiring dengan menurunnya ukuran partikel disebabkan oleh ukuran kuantum (Samuel et al. 2009).
8
(nm)
400 500 600 700 800 900
T
ra
nsm
ita
nsi
(%)
20 40 60 80 100
3 jam 6 jam 12 jam
Gambar 4. Sifat optik transmitansi dari semikonduktor film ZnO yang diukur dengan spektrometer UV-Vis
Untuk menentukan besarnya energi celah (Eg) dari film ZnO, dapat diestimasikan secara fundamental yang merupakan transisi dari absorbansi atau transmitansi. Untuk transisi secara langsung dan tak langsung dapat digunakan hubungan sebagai mana dalam persamaan (3) ( Altaf et al. 2003, Maddu et al.
2006).
⁄ ( )
dimana hv adalah energi foton, A adalah sebuah konstanta yang nilainya antara
107 sampai 108 m-1 (Samuel et al. 2009), sedangkan eksponen n bergantung pada
jenis transisi di dalam bahan. Untuk transisi langsung n = ½, untuk transisi tak
langsung n = 2, Eg adalah lebar celah pita optik bahan semikonduktor, α adalah
koefesien absorbansi yang dapat ditentukan dari kurva transmitansi atau absorbansi pada setiap panjang gelombang melalui hubungan Beer-Lambert, yang
ditunjukkan pada persamaan (4)
sedangkan untuk nilai α dapat ditentukan dengan :
( )
dengan I adalah intensitas cahaya yang ditransmisikan melalui sampel film, I0
adalah intensitas cahaya datang dan t adalah ketebalan film.
9 nilai koefesien absorbansi (α) terhadap nilai panjang gelombang (λ). Adapun kurva hubungan Gärtner's tersebut dapat dilihat pada Gambar 5.
.
Gambar 5 Kurva hubungan Gärtner's pada transisi langsung dan tak langsung semikonduktor
Plot nilai koefisien absorbansi (α) terhadap pajang gelombang (λ) untuk semua sampel ZnO ditunjukkan pada Gambar 6. Hasil plot ini memperlihatkan bentuk transisi langsung, sebagaimana mengacu pada kurva hubungan Gärtner's pada Gambar 5, sehingga nilai n yang digunakan adalah ½. Hasil plot ini dapat dilihat pada Gambar 6.
Panjang gelombang( (nm)
400 500 600 700 800 900
K
oe
fe
si
en a
bs
orba
ns
i (
)
x 10
6
0 1 2 3 4 5 6
3 Jam 6 Jam 12 Jam
Gambar 6 Kurva hubungan nilai absorbansi (α) terhadap panjang gelombang (λ)
Hasil Tonc plot antara terhadap dari tiga film ZnO sebagaimana
pada pada Gambar 7, masing-masing dari durasi hidrotermal 3 jam, 6 jam dan 12 jam. Nilai energi pita (Eg) ditentukan dari perpotongan bagian linier kurva dengan
10
eV dan 3,24 eV. Nilai energi pita ini tidak jauh berbeda dengan hasil peneliti sebelumnya dengan menggunakan metode sol gel yaitu 3,24 eV (Khan. 2011), 3,280 eV, 3,287 eV, dan 3,290 eV (Ilican et al. 2008), dan 3,20 eV, 3,19 eV dan
3,16 eV (Gupta et al. 2009).
hv (eV)
2,0 2,2 2,4 2,6 2,8 3,0 3,2 3,4
hv eV ) 0 10 20 30 3 jam 6 jam 12 jam
Gambar 7 Plot (αhv)2 terhadap energi foton absorbansi (hv)
Sebagaimana telah dijelaskan sebelumnya, bahwa perubahan energi gap ini
disebabkan oleh adanya perbedaan ukuran dari ukuran partikel, dan dari hasil penelitian telah di dapatkan bahwa faktor lamanya durasi menyebabkan ukuran partikel yang menurun dengan ukuran kristalnya meningkat, sehingga dapat dibuat suatu hubungan yaitu perubahan energi pita terhadap ukuran partikel dan ukuran kristal yang dapat dilihat pada Gambar 8.
Eg (eV)
3,17 3,18 3,19 3,20 3,21 3,22 3,23 3,24 3,25
U kura n pa rt ike l ( nm ) 80 100 120 140 160 180 200 220 240 260 U kura n kr is ta l ( nm ) 42 44 46 48 50 52 54 56 Ukuran partikel Ukuran kristal
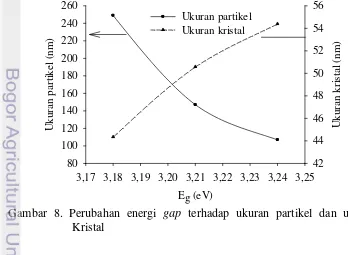
Gambar 8. Perubahan energi gap terhadap ukuran partikel dan ukuran
11 Gambar 8 memperlihatkan bahwa perubahan energi pita meningkat seiring dengan meningkatnya ukuran kristal dan menurun seiring dengan meningkatnya ukuran partikel. Artinya ukuran kristal yang besar memiliki energi pita yang besar dengan ukuran partikelnya lebih kecil dan sebaliknya.
Simpulan
Hasil sintesis nonostruktur ZnO dengan metode hidrotermal terhadap waktu 3 jam, 6 jam dan 12 jam telah didapatkan ukuran-ukuran partikel cenderung menurun yaitu 249 nm, 147 nm dan 107 nm dengan ukuran kristalnya juga meningkat seiring dengan perubahan ukuran partikel yaitu 44,32 nm, 50,65 nm, dan 54,37 nm dengan sebaran butiran partikelnya cenderung merata dan homogeny dengan masing-masing besarnya nilai energi pita adalah 3,18 eV, 3,21 eV dan 3,24 eV.
3
EKSTRAKSI, MODIFIKASI DAN KARAKTERISASI
KLOROFIL
Pendahuluan
Klorofil merupakan pigmen alam yang umumnya terdapat pada kelompok tumbuhan hijau yang terletak pada daun. Klorofil memiliki peranan sangat penting dalam proses fotosintesis. Cahaya matahari yang mengenai daun akan di serap oleh pigmen ini untuk mengubah gas karbon dioksida dan air menjadi glukosa dan oksigen. Secara khusus proses fotosintesis ini dapat digambarkan dengan reaksi sebagai berikut:
6 CO2 + H2O C6H12O6 + 6 O2
Penyerapan cahaya oleh klorofil ini disebabkan adanya peranan utama dari struktur porfirin yang mengikat ion magnesium (Mg2+), yang merupakan struktur utama klorofil. Saat menyerap cahaya, klorofil akan mentransferkan energinya untuk mengeksitasi elektron menuju ke pusat reaksi. Semakin lama tahapan eksitasi singlet klorofil, semakin besar konversi energi elektronik dari tingkat
dasar ke tingkatan tereksitasi triplet dapat terjadi (Schaber et al. 1984).
12
Untuk berbagai aplikasi, klorofil dianggap kurang efektif karena keberadaanya yang mudah terdegradasi. Menurunnya unsur Mg saat terdegradasi ini dapat disebabkan oleh reaksi langsung terhadap sifat asam (Budiyanto et al.
2008) dan panas (Erge et al. 2008).
Daun Katuk yang umumnya dimanfaatkan oleh masyarakat sebagai tanaman obat, akan dikembangkan lebih lanjaut dengan memanfaatkan kandungan klorofilnya untuk aplikasi lain. Dalam bagian penelitian ini akan dikaji tingkat stabilitas klorofil dari daun Katuk dengan mengganti unsur Mg nya dengan Zn2+ dan Cu2+, sebagaimana telah dilakukan oleh peneliti sebelumnya ( Kupper et al.
1996; Nurdin (2009); Nurhayati and Suendo. 2011; Zvezdanovic et al. 2012).
Hasil subtitusi selanjutnya akan dimanfaatkan sebagai fotosensitiser atau fotoaktif yang berfungsi sebagai pemanen cahaya dalam sel surya hibrid nanopartikel ZnO
bulk heterojunktion.
Tujuan
Melakukan ekstraksi dan modifikasi klorofil dengan ion Zn dan Cu serta menguji foto stabilitasnya.
Metode
Isolasi dan Modifikasi Klorofil
Ekstraksi
Klorofil diperoleh dari daun Katuk yang telah diekstraksi dengan menggunakan pelarut organik etanol 96%. Pertama-tama daun Katuk dibilas terlebih dahulu dengan menggunakan akuades sampai bersih, kemudian ditiriskan sampai airnya benar-benar mengering. Selanjutnya menimbang daun Katuk sebanyak 100 gram dan dihancurkan dengan menggunakan mortar hingga permukaan daun Katuk benar-benar memar seluruhnya. Hasil tumbukan daun Katuk dimasukkan ke dalam 500 ml etanol 96% dan didiamkan selama 24 jam, setelah itu dilakukan penyaringan dengan menggunakan corong Bruncher.
Penyaringan pertama dengan menggunakan kertas saring biasa. Residu dicuci dengan 500 ml atanol 96% dan disaring menggunakan kertas saring Whatman
ukuran 40 mess. Penyaringan dilakukan dengan menggunakan pompa vakum. Filtrat diambil sebagai ekstrak kasar klorofil (Nurdin, 2009). Hasil penyaringan kemudian ditambahkan dengan MgCO3 sebanyak 1 ml. Kemudian disimpan semalam ke dalam freezer (-20oC), setelah itu dilakukan uji spektroskopi
abasorbansi dan flouresensi dengan menggunakan spektrofotometer UV-Vis dan spektroflouresens (Ocean optics, Departemen Fisika, IPB). Semua proses
dilakukan dalam ruang gelap. Pengukuran absorbansi dilakukan dengan sumber lampu Halogen.
13 bentuk gambar dan data yang ditampilkan oleh monitor. Lebih jelasnya proses pengukuran flouresensi ini dapat dilihat pada Gambar 9.
Gambar 9. Skema pengukuran flouresensi dye klorofil
Subtitusi logam inti klorofil
Penggantian logam inti pada klorofil (Mg) dengan unsur Zn dan Cu, pertama-tama dilakukan pendegradasian terlebih dahulu yaitu dengan menambahkan larutan klorofil dengan HCl 1M tetes demi tetes hingga pH 4 sambil diaduk menggunakan pengadu dengan kecepatan putaran 400 rpm (Nurdin. 2009). Hasil pendegradasian ini disebut feofitin. Feofitin ini kemudian disimpan dalam inkubator selama 24 jam pada suhu 40oC (Zvezdanovic et al. 2012). Setelah itu dilakukan penambahan ion Zn2+ atau Cu2+ dengan melarutkan 0,1 g/ml
Zinc Acetat dihidrat ke dalam etanol atau 0,1 g/ml Cuprum chloride (Kupper et al. 1996) dan diaduk selama 30 menit sampai terjadi perubahan warna. Semua
proses dilakukan dalam ruang gelap. Setelah reaksi dilakukan, campuran dimasukkan ke dalam freezer (-20oC) dan didiamkan selama semalam setelah itu
dilakukan uji spektroskopi absorbansi, kemudian semua larutan (klorofil, Zn-feofitin dan Cu-Zn-feofitin) dikeringkan dengan menggunakan pengering (freezdryer,
PAU laboratorium mikrobiologi IPB).
Fotostabilitas
Uji stabilitas ini dilakukan melalui pengukuran spektroskopi absorbansi, dimana larutan klorofil dan klorofil kompleks didegradasi menggunakan lampu halogen yang berintensitas 34 W/m2. Penyinaran dilakukan selama 5 jam dan pengambilan data absorbansi dilakukan setiap 30 menit.
Laser
Sampel
Spektroflourometer (Fl) (Ocen Optics)
Monitor
PC
Fiber optik
14
Hasil dan Pembahasan
Sifat optik klorofil ekstrak daun Katuk menggunakan etanol 96% menghasilkan dua daerah serapan utama yaitu 436,53 nm (soret band) dan 664,00
nm (Q-band). Serapan pada daerah soret band lebih tinggi dari pada daerah Q-band. Ini menunjukkan bahwa pada klorofil tahapan eksitasi elektronnya ada
dua dari keadaan ground state (So), yaitu singlet pertama (S1) yang terjadi pada daerah merah dan singlet kedua (S2) yang terjadi pada daerah biru.
Hasil degradasi klorofil menggunakan HCl 1M memberikan perubahan warna terhadap klorofil alami menjadi warna kecokelatan yang disebut sebagai feofitin. Feofitin terbentuk dikarenakan hilangnya logam inti korofil pada cincin aromatik porfirin. Ikatan pada porfirin ini akan mengalami deformasi bila terjadi proses metalisasi, yaitu masuknya ion logam menggantikan atom hidrogen. Penambahan HCl menyebabkan cincin porfirin menerima atom H yang berikatan dengan N yang disebut sebagai ikatan imida pyrolle (=NH-) yang bersifat sangat
kuat. Proses terbentuknya feofitin ini dikenal sebagai proses katabolisme. Proses ini diawali dengan pembelahan cincin oxygenolytic dari pheophorbida yang
merupakan intermediet nyata pada magnesium dari inti cincin klorofil. Pada langkah selanjutnya dari katabolisme klorofil, klorofil katabolis fluoresens primer (pFCCs) terbentuk setelah terjadinya setengah penurunan. Setelah itu terjadi proses tautomerisasi dari pFCCs ke dalam bentuk non-katabolites klorofil fluoresens (NCC) (Kraeutler, 2003). Proses terbentuknya feofitin ini dapat dilihat pada Gambar 10 ( Dapic. 2012, Inanc. 2011)
15 Hasil karakterisasi optik feofitin menunjukkan daerah serapan utama untuk
soret band adalah 421,50 nm dan 657,28 nm untuk Q-band. Feofitin kemudian
dimetalisasi dengan ion logam Zn2+ dan Cu2+, dan menunjukkan adanya perubahan warna dan daerah serapan. Feofitin yang tersubtitusi dengan ion Zn2+ mengalami perubahan warna menjadi hijau muda dengan daerah puncak serapannya 428,82 nm untuk daerah soret band dan 658,41 nm untuk daerah Q-band. Sedangkan untuk yang termodifikasi ion Cu2+, memberikan perubahan
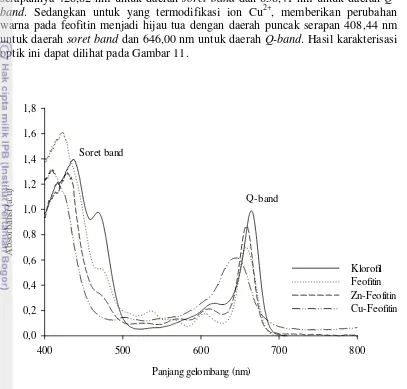
warna pada feofitin menjadi hijau tua dengan daerah puncak serapan 408,44 nm untuk daerah soret band dan 646,00 nm untuk daerah Q-band. Hasil karakterisasi
optik ini dapat dilihat pada Gambar 11.
soret band
Q-band
Panjang gelombang (nm)
400 500 600 700 800
A
bs
or
ba
ns
i (
a.u
)
0,0 0,2 0,4 0,6 0,8 1,0 1,2 1,4 1,6 1,8
Klorofil Feofitin Zn-Feofitin Cu-Feofitin Soret band
Q-band
Gambar 11. Hasil subtitusi ion logam Zn2+ dan Cu2+ pada inti klorofil Berdasarkan pengamatan pola spektrum pada Gambar 11 tampak bahwa penggantian unsur logam pada inti klorofil, menyebabkan terjadinya pergeseran baik daerah Soret band maupun Q-band yang bergeser ke daerah biru. Hasil ini
berbeda dengan hasil penelitian sebelumnya oleh Nurhayati et al (2009), dimana
daerah soret band bergeser ke arah merah dengan pelarut metanol. Namun, dari
hasil penelitian yang dilakukan Zvedanovic et al (2012), juga melakukan subtitusi
pada klorofil dengan unsur Zn2+ dan Cu2+ menggunakan pelarut etanol 96% dan didapatkan pergeseran ke daerah biru, baik daerah soret band maupun Q-band.
Dari hasil tersebut menunjukkan bahwa pelarut yang digunakan juga berpengaruh pada daerah serapan.
Pergeseran pada daerah Soret band dan Q-band maksimum ke panjang
16
mengindikasikan bahwa energi gap antara HOMO (Highest Occupied Molecular Orbital) dan LUMO (Lowest Unoccupied Molecular Orbital) pada Zn-feofitin
dan Cu-feofitin lebih besar dari klorofil. Perbedaan besarnya nilai energi ini, tentu saja akan berpengaruh pada tahapan tingkat eksitasi elektroniknya. Energi yang besar akan memberikan tahapan eksitasi yang lebih lama pada daerah singlet dan
memberikan peluang untuk tereksitasi pada daerah triplet. Kelebihan energi pada
daerah triplet, akan menyebabkan peluang terjadinya transfer energi ke molekul
oksigen yang bersifat merusak (Fiedor et al. 2002; Agostiano et al. 2003).
Pada Gambar 11 pula, dapat dilihat khususnya daerah Q-band, telah terjadi
penurunan tingkat absorbansi. Penurunan nilai absorbansi ini mengindikasikan besarnya kosentrasi pada masing-masing dye, sehingga pada Gambar 11 dapat
dilihat bahwa hasil subtitusi logam Zn dan Cu lebih rendah dari klorofil. Untuk klorofil yang tersubtitusi Cu memiliki daerah serapan yang lebih luas dari pada yang tersubtitusi Zn. Akan tetapi secara keseluruhan, klorofil yang tersubtitusi dengan ion logam, menyebabkan pelebaran pada daerah serapan klorofil. Pelebaran daerah serapan ini kemungkinan disebabkan oleh struktur baru yang terbentuk akibat proses metalisasi sehingga mengakibatkan perubahan energi pada level HOMO dan LUMO.
Pada daerah Q- band yang menyatakan absorbansi maksimum dari dye, dan
daerah flouresensi yang menyatakan tempat terjadinya emisi. Hubungan antara spektrum absorbansi dan emisi terhadap panjang gelombang yang dikonversi ke dalam bentuk energi (eV) memberikan gambaran yang dikenal sebagai pergeseran Stokes. Pergeseran ini disebabkan oleh perbedaan antara struktur
relaksasi pada keadaan ground dan keadaan eksitasi, sebagaimana pada
Gambar 12.
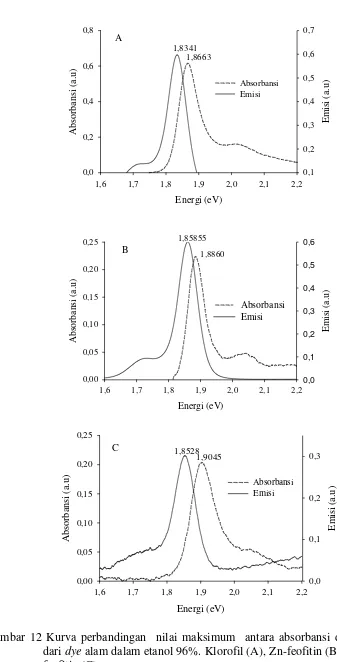
Pada Gambar 12 tampak bahwa pergeseran Stokes antara absorbansi
maksimum dan emisi maksimum yaitu 0,032 eV untuk korofil, 0,028 eV untuk Zn-feofitin dan 0,053 eV untuk Cu-feofitin. Hasil ini memperlihatkan bahwa pergeseran Stokes dari Cu-feofitin lebih besar dari pada klorofil dan Zn-feofitin.
Ini menunjukkan bahwa waktu yang dibutuhkan Cu-feofitin dalam relaksasi lebih lama, sedangkan untuk Zn-feofitin lebih singkat dari klorofil. Hasil ini berbeda dengan eksperimen sebelumnya yang dilakukan oleh Nurhayati et all (2011), yang
lebih mengkhususkan pada klorofil a, dimana Zn-feofitin membutuhkan waktu yang lebih lama dalam relaksasi yaitu dua kali dari klorofil a. Dalam kajian yang lain, telah dijelaskan bahwa pergeseran Stokes juga dipengaruhi oleh pelarut yang
17
Energi (eV)
1,6 1,7 1,8 1,9 2,0 2,1 2,2
A bs orba ns i (a .u) 0,0 0,2 0,4 0,6 0,8 E m is i (a .u) 0,1 0,2 0,3 0,4 0,5 0,6 0,7 Absorbansi Emisi 1,8341 1,8663 A Energi (eV)
1,6 1,7 1,8 1,9 2,0 2,1 2,2
A bs orba ns i (a .u) 0,00 0,05 0,10 0,15 0,20 0,25 E m is i (a .u) 0,0 0,1 0,2 0,3 0,4 0,5 0,6 Absorbansi Emisi 1,8860 1,85855 B Energi (eV)
1,6 1,7 1,8 1,9 2,0 2,1 2,2
A bs orba ns i (a .u) 0,00 0,05 0,10 0,15 0,20 0,25 E m is i (a .u) 0,0 0,1 0,2 0,3 Absorbansi Emisi 1,8528 1,9045 C
Gambar 12 Kurva perbandingan nilai maksimum antara absorbansi dan emisi dari dye alam dalam etanol 96%. Klorofil (A), Zn-feofitin (B) dan
18
Analisis fotostabilitasklorofil
Pengujian klorofil hasil ekstrak dan yang telah disubtitusi dengan ion logam Zn2+ dan Cu2+ dengan penyinaran lampu halogen dengan intensitas 34 W/m2. Dari hasil pengamatan yang diperoleh, klorofil yang terdegradasi mengalami pemudaran warna menjadi hijau kelabu (Zvezdanovic et al. 2008) yang disertai
dengan penurunan puncak absorbansi (proses hipokromik) pada daerah Q-band
(Erge et al. 2008). Selain penyinaran, pendegradasian warna klorofil juga
disebabkan oleh pengaruh asam yang menyebabkan proses pembentukan produk degradasi seperti pelepasan inti logam klorofil sehingga lebih cepat dalam pembentukan proses feofitinase (Gross. 1991; Jeffrey et al. 1997; Gaur et al.2006;
Budiyanti et al. 2008). Pada proses ini terjadi reaksi oksidasi pada ikatan metin
antara C4 dan C5 yang menyebabkan terjadinya tetrapirol linier, sehingga C5 membentuk gugusformil (HCO-) yang kelebihan atom O, sedangkan C4 membentuk gugus laktam (Matile et al.1999).
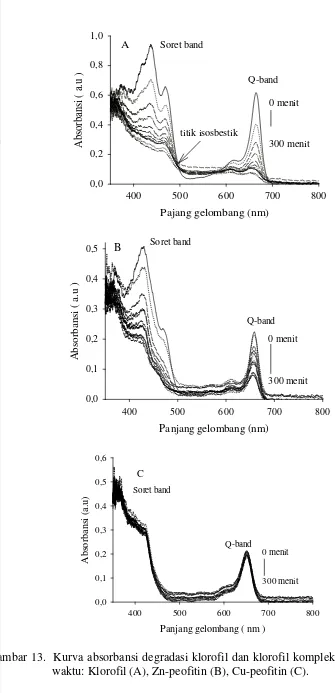
Gambar 13(A) dapat dilihat bahwa klorofil setelah dilakukan penyinaran mengalami kenaikan pada daerah panjang gelombang sekitar 500-600 nm dan akhirnya membentuk suatu kurva yang terikat secara bersama. Ini menunjukkan bahwa telah terjadi reaksi kesetimbangan dan memiliki koefisien serapan pola yang sama pada molekul yang berbeda (isosbestik) (Endo et al. 1984; Christina et al. 2008). Sedangkan pada Gambar 13(B) hampir tidak terlihat terjadinya
perubahan yang signifikan pada daerah isosbestik, Ini memperlihatkan bahwa klorofil yang tersubtitusi oleh ion Zn2+ (Zn-feofitin) cenderung lebih stabil dari klorofil, akan tetapi pada daerah Q-band terjadi penurunan puncak meskipun tidak
begitu signifikan. Ini menunjukan bahwa pada Zn-feofitin masih terjadi proses feofitinase dan pada daerah 500-600 nm terdapat sedikit puncak-puncak kecil yang mengindikasikan terjadinya eksitasi terendah dari spesis singlet (Budiyanto et al. 2008). Untuk klorofil yang tersubtitusi oleh ion Cu2+ (Gambar 13(C))
terlihat spektrum absorbansinya pada daerah Q-band hampir tidak terjadi
penurunan dan tidak terlihat terbentukya daerah isobestik, Ini menunjukkan bahwa molekul-molekul yang ada setelah penambahan ion Cu2+ cenderung tidak mengalami perubahan.
Perbedaan perubahan klorofil sebelum dan sesudah penambahan ion logam setelah penyinaran selama 5 jam dapat dilihat pada Gambar 14. Gambar 14 merupakan hasil plot antara nilai absorbansi maksimum pada daerah Q-band
terhadap perubahan waktu.
19
Pajang gelombang (nm)
400 500 600 700 800
A bs orba ns i ( a.u ) 0,0 0,2 0,4 0,6 0,8 1,0 A Q-band Soret band titik isosbestik 0 menit 300 menit
Panjang gelombang (nm)
400 500 600 700 800
A bs or ba ns i ( a .u ) 0,0 0,1 0,2 0,3 0,4 0,5 Q-band Soret band B 0 menit 300 menit
Panjang gelombang ( nm )
400 500 600 700 800
[image:31.595.125.460.71.764.2]A bs or ba ns i ( a.u ) 0,0 0,1 0,2 0,3 0,4 0,5 0,6 Q-band Soret band C 0 menit 300 menit
20
Waktu (menit)
0 100 200 300 400
A
bs
orba
ns
i (a
.u)
0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7
Klorofil Zn-Feofitin Cu-Feofitin
Gambar 14. Perubahan absorbansi maksimum pada daerah Q-band setelah
penyinaran selama 5 jam pada klorofil, Zn-feofitin dan Cu-feofitin Gambar 14 juga menunjukkan adanya nilai absorbansi yang sama khususnya untuk klorofil dan Zn-feofitin, yaitu pada menit ke 150. Ini menunjukkan bahwa klorofil dan Zn-feofitin telah mengalami perubahan struktur molekul menjadi bentuk yang baru, selama itu juga ditandai dengan adanya titik isobestik yang terbentuk, seperti yang dijelaskan pada Gambar 13.
Simpulan
[image:32.595.74.467.80.602.2]21
4
FABRIKASI DAN KARAKTERISASI SEL SURYA HIBRID
ZnO-KLOROFIL
Pendahuluan
Sel surya hibrid merupakan suatu bentuk sel surya yang memadukan antara semikonduktor anorganik dan organik. Dimana dalam bentuk ini material organiknya digunakan sebagai pemanen cahaya atau komponen fotoaktif. Pada sel surya hybrid, lapisan aktif memiliki beberapa bentuk yaitu bilayer, bulk heterojunction, dan interdigital. Dalam penelitian ini dibuat jenis sel surya hibrid
dengan struktur lapisan aktif bulk heterojunction, yang mana pada bentuk ini
material semikonduktor anorganik (ZnO) dicampur dengan bahan organik (dye),
dalam penelitian ini yang digunakan klorofil. Dipilihnya bentuk ini dikarenakan proses pembuatannya lebih mudah dibandingkan dengan bilayer dan interdigital.
Regenerasi dari molekul organik yang akan menginjeksikan hole ke dalam
elektrolit atau material transpor hole yang kemudian ditransferkan ke elektrodanya
untuk menerima elektronnya sehingga membentuk pasangan muatan bebas. Sehingga dalam proses ini dibutuhkan bentuk elektrolit yang lebih stabil, yang mampu meningkatkan peforma dari sel surya.
Beberapa kombinasi elektrolit pada sel surya hibrid yang telah dilakukan untuk meningkatkan peforma dari sel surya adalah ZnO/N3/CuSCN (O’Regan et al. 2002), TiO2/N3/CuI (Meng et al.2003), TiO2/C60/CuSCN (Senadeera dan Perera. 2005) dan ZnO/N719/CuSCN (Desai et al. 2012). Melihat kombinasi yang
akan dilakukan dalam penelitian ini yaitu ZnO/klorofil dalam bentuk bulk heterojunktion, maka elektrolit yang mungkin untuk digunakan adalah CuSCN
sebagai konduktor hole.
Tujuan
Memodifikasi dan mengkarakterisasi semikonduktor nanopartikel ZnO dan klorofil dalam bentuk sel surya hibrid bulk heterojunction
Metode
Fabrikasi film hibrid
Fabrikasi film hibrid ZnO/klorofildilakukan dengan melarutkan 0,005 gram ZnO ke dalam 5 ml etanol kemudian di stirrer 300 rpm sambil ditetesi 10 µl aethylen glycol kemudian memasukkan 0,005 gram dye klorofil. Reaksi dilakukan
selama 10 menit sampai semua komposisi terlihat tercampur sempurna. Pelapisan film ZnO/klorofil dilakukan dengan menggunakan metode spin coating (Ibrahem
22
Fabrikasi sel surya hibrid
Pembuatan sel surya hibrid bulk heterojunction dilakukan dengan cara
mencampurkan bahan semikonduktor bubuk ZnO dan bubuk klorofil dengan perbandingan 1:1 kemudian campuran ini digerus dengan menggunakan mortar dan ditambahkan etanol secukupnya sampai halus sempurna, setelah itu ditambahkan larutan asam asetat 1% 0,5 ml untuk campuran 0,1 gram ZnO dan 0,1 gram klorofil, setelah tercampur sempurna kemudian adonan diteteskan diatas kaca TCO yang telah diabuat pola terlebih dahulu dengan ukuran 1x1 cm. Pelapisan dilakukan dengan menerapkan metode Docter bladge. Sel yang telah
terbentuk dibiarkan pada temperatur ruang sampai mengering, kemudian sel ditetesi dengan larutan CuSCN secukupnya sampai merata. Larutan CuSCN dibuat dengan cara melarutkan 0,1 gram bubuk CuSCN ke dalam 12 ml acetonitril dan selanjutnya ditutup kembali dengan kaca TCO yang mana bagian konduktifnya menghadap kearah bagian dalam sel dan kemudian dijepit dan biarkan selama beberapa saat.
Sel surya yang tersusun atas lapisan TCO/CuSCN/ZnO-Klorofil/TCO dikarakterisasi dengan menggunakan rangkaian sebagaimana yang terlihat pada Gambar 15. Pengukuran dilakukan secara langsung menggunakan sinar matahari dengan intensiatas yang terukur adalah 117,401W/m2, dari pengukuran ini didapatkan kurva yang memperlihatkan hubungan antara tegangan (V) dan rapat arus (J) atau yang dikenal sebagai kurva I-V.
Gambar 15. Rangkaian pengukuran karakterisasi arus tegangan sel surya
Hasil dan Pembahasan
Hasil eksperimen didapatkan bahwa spektrum ZnO menyerap kuat pada daerah UV pada panjang gelombang 367 nm. Setelah dilakukan kombinasi antara ZnO dengan klorofil, Zn-feofitin dan Cu-feofitin, telah menyebabkan perubahan pada daerah serapan ZnO menjadi lebih lebar, dari spektrum UV ke visibel yaitu pada panjang gelombang 300 nm sampai 500 nm, sebagaimana yang terlihat pada Gambar 16.
23 penambahan klorofil. Untuk kombinasi antara ZnO dengan Cu-feofitin, terjadi pelebaran puncak yang sangat signifikan yaitu dari 300 nm sampai 600 nm.
Pelebaran spektrum setelah penambahan klorofil dan klorofil kompleks ini mengindikasikan banyakya jumlah spektrum yang terserap oleh kombinasi material ZnO dengan dye, sehingga sangat mendukung bila diaplikasikan sebagai
sel surya.
Panjang gelombang (nm)
300 400 500 600 700 800 900
[image:35.595.147.482.184.393.2]A bs orba ns i dye (a .u) 0,00 0,05 0,10 0,15 0,20 0,25 A bs orba ns i Z nO (a .u) 0,0 0,2 0,4 0,6 0,8 1,0 1,2 Klorofil Zn-feofitin Cu-feofitin ZnO 367
Gambar 16. Sifat optik film hibrid nanopartikel ZnO/klorofil
Karakteristik I-V
Karakteristik I-V menjelaskan bagaimana sel surya tersebut mampu bekerja di bawah cahaya langsung. Hal tersebut dapat terlihat pada kurva yang terdiri atas beberapa parameter seperti arus hubungan singkat Isc (short circuit) yaitu arus ketika potensial sama dengan nol, tegangan rangkaian terbuka Voc (open circuit voltage) yaitu tegangan ketika beban luar diberikan sangat besar, Vmax yaitu tegangan yang memberikan nilai daya maksimum, dan Imax arus yang memberikan nilai daya maksimum.
Saat tanpa cahaya sel surya memiliki karakteristik sebagaimana pada dioda ideal, sehigga hubungan antara arus dan tegangannya dapat dituliskan sebagaimana pada persamaan (6).
(
⁄
)
Saat sel surya disinari akan dihasilkan arus yang terjadi karena pembangkitan elektron oleh cahaya dengan energi tertentu (foton), sehingga rapat arus total yang mengalir pada rangkaian terbuka dapat dituliskan seperti pada persamaan (7), yaitu:
24
( ⁄ )
dimana kB adalah konstanta Bolztaman, T adalah J0 adalah rapat arus saturasi, Jsc
adalah rapat arus pada rangkaian terhubung singkat saat disinari ketika V= 0. Tegangan yang diukur pada rangkaian terbuka (open circuit) ketika J(V)= 0,
disebut tegangan rangkaian terbuka (Voc), yang dapat dituliskan seperti pada persamaan (8)
Efisiensi konversi merupakan kemampuan sebuah piranti sel surya untuk mengubah energi cahaya menjadi energi listrik dalam bentuk arus tegangan. Efisiensi konversi energi sebuah energi sebuah sel surya dapat dinyatakan melalui persamaan (9)
dengan Pmax adalah daya maksimum yang dihasilkan yaitu:
dari persamaan ini diperoleh nilai fill factor (FF) melalui persamaan (11)
Subtitusi persamaan (11) ke dalam persamaan (10), maka persamaan (9) dapat dituliskan sebagaimana dalam persamaan (13), yaitu:
Pinadalah daya energi cahaya yang tiba pada permukaan sel surya. Pin ditentukan
melalui persamaan (13)
dengan Iinadalah intensitas sumber cahaya dan A adalah luas permukaan sel surya
yang disinari. Bila persamaan (10) disubtitusikan kedalam persamaan (9), maka besar efisiensi dapat dituliskan sebagaimana dalam persamaan (14).
25 ZnO/Cu-feofitin. Pada kurva tersebut tampak bahwa adanya perbedaan pada nilai tegangan dan rapat arus yang berbeda-beda. Besar dan kecilnya tegangan yang dihasilkan pada masing-masing sel tergantung pada kombinasi antara semikonduktor (ZnO), dye dan elektrolit (CuSCN). Semakin banyak dye yang
terjerap atau menempel pada permukaan partikel ZnO akan semakin memicu untuk terjadinya beda potensial sebagai pembangkit tegangan, sehingga dengan penambahan elektrolit padat CuSCN yang merupakan sumber hole akan
meningkatkan tegangan yang ada. Dari beberapa studi literatur diketahui bahwa penambahan elektrolit CuSCN dapat meningkatkan peforma sel surya pada tegangan terbuka (Voc) (Desai et al. 2012; O’Regan et al. 2002).
Karakteristik I-V yang diperoleh dari masing-masing sel tampak adanya perbedaan bentuk kelengkungan kurva. Ini menggambarkan bagaimana mobilisasi elektron pada masing-masing sel yang berbeda. Gambar 17 (A) kombinasi ZnO/klorofil dan (B) kombinasi ZnO/Zn-feofitin memiliki bentuk kurva yang kurang ideal. Kurang idealnya kurva ini ditandai oleh kelengkungannya yang curam, disebabkan oleh kebocoran yang terjadi pada masing-masing sel kemungkinan disebabkan adanya rekombinasi prematur atau jatunya elektron sebelum sampai pada elektrodanya. Jatuhnya elektron ini kemungkinan disebabkan oleh stabilitas dari masing-masing dye. Sedangkan untuk sel
kombinasi ZnO/Cu-feofitin pada Gaambar 17(C) memperlihatkan bentuk karakteristik kurva I-V yang lebih ideal meskipun memiliki nilai tegangan Voc dan rapat arus (Jsc) yang lebih rendah. Idealnya bentuk kurva yang dihasilkan ini
kemungkinan disebabkan oleh stabilitas dari dye. Sebagaimana yang diperlihatkan
pada Gambar 15, tampak bahwa Cu-feofitin lebih stabil dari klorofil dan Zn-feofitin.
Perbedaan nilai tegangan Voc pada Gambar 17, kemungkinan disebabkan oleh jumlah muatan pada masing-masing dye yang berbeda. Perbedaan ini
ditandai dengan penurunan nilai absorbansi dari masing-masing dye seperti yang
ditujukkan pada Gambar 15. Jumlah muatan yang banyak memungkinkan untuk terjadinya pasangan muatan bebas (eksiton) yang lebih banyak ketika mendapat energi foton yang cukup, sehingga memicu timbulnya nilai tegangan yang lebih besar. Sedangkan untuk rapat arus Isc yaitu arus yang mengalir saat terjadi
hubungan singkat pada rangkaian uji, untuk analisis sel biasanya digunakan rapat arus (J) yaitu arus yang mengalir untuk setiap satuan luas. Disini didapatkan nilai
rapat arus (J) untuk masing-masing sel tampak bervariasi dan tergolong masih
sangat rendah. Rendahnya rapat arus ini disebabkan oleh berbagai faktor, semua komponen dalam sel sangat berpengaruh. Bila ditinjau secara khusus yaitu yang sangat berpengaruh dalam proses mobilitas elektron dari satu elektroda ke elektroda lainnya adalah ukuran partikel, dimana telah dilaporkan bahwa ukuran ideal diameter partikel dalam aplikasi sel surya adalah kurang dari 10 nm, semakin kecil ukuran suatu partikel akan memudahkan elektron menuju elektroda lainnya sehingga dapat mencegah terjadinya rekombinasi prematur elektron (Lee
26
Tegangan(V) (mV)
0 100 200 300 400 500 600
Ra pa t a ru s( J ) (m A .c m -2) x10 -4 0 2 4 6 8 10 A Tegangan(V) (mV)
100 200 300 400 500
Ra pa t a ru s( J ) (m A .c m -2 ) x10 -4 4 6 8 10 12 14 B Tegangan(V) (mV)
0 50 100 150 200 250 300
Ra pa t a rus ( J ) (m A .c m -2) x 10 -4 1,0 1,2 1,4 1,6 1,8 2,0 2,2 C
[image:38.595.90.443.71.758.2]27 Hasil karakteristik I-V pada Gambar 17, dapat dihitung beberapa nilai parameter dalam sel surya yang meliputi Tegangan terbuka (Voc), rapat Arus pendek (Jsc), tegangan maksimum (Vmax), rapat arus maksimum (Jmax), daya maksimum (Pmax), fill factor (FF) dan efisiensi (η) yang dapat dilihat pada Tabel 2.
Tabel 2. Nilai parameter dalam sel surya
Sel Voc Isc Vmax Imax Pmax FF η
(mV) (mA) (mV) (mA) (mWcm-2) (%) A 542 9,9x10-4 364 5,4x10-4 0,196 0,37 2,5 B 427 1,2x10-3 330 7,2x10-4 0.238 0,45 1,3 C 286,8 2,2x10-4 218,5 1,6x10-4 0,035 0,55 0,3
A : ZnO/Klorofil/CuSCN B : ZnO/Zn-feofitin/CuSCN C : ZnO/Cu-feofitin/CuSCN
Pada Tabel 2 tampak bahwa nilai parameter sel surya yang dihasilkan bervariasi. Bervariasinya hasil ini tergantung pada karakteristik I-V yang dibentuk dari masing-masing sel. Pada Tabel 2 tampak juga perbedaan antara nilai tegangan maksimum (Vmaks) dan arus maksimum (Imaks). Perbedaan nilai tegangan maksimum (Vmaks) kemungkinan disebabkan oleh penurunan jumlah muatan bebas (eksiton) yang dihasilkan ketika dye berinteraksi dengan foton secara terus
menerus. Dye yang baik akan menghasilkan muatan bebas yang besar, selanjutnya
dikonversi menjadi arus ketika sampai pada elektroda. Arus maksimum yang dihasilkan merupakan gambaran jumlah elektron yang sampai pada elektrodanya. Bila dilihat dari nilai Voc dan Vmaks untuk semua sampel tampak adanya penurunan yang signifikan yang tunjukkan oleh sel A dan sel B, ini menggambarkan adanya penurunan kualitas dye ketika berinteraksi dengan foton,
sehingga muatan yang dikonversi menjadi arus pun semakin berkurang. Peristiwa ini sebagaimana ditunjukkan oleh bentuk kurva I-V. Sedangkan untuk sampel C terlihat hanya sedikit perubahan yang terjadi dari Voc ke Vmaks, ini menggambarkan bahwa dye ketika berinteraksi dengan foton hanya sedikit
kehilangan muatan yang akan dikonversi menjadi arus. Sehingga tampak bahwa kelengkungan kurava I-V yang dihasilkan lebih ideal dari sel A dan B.
Kestabilan kurva I-V yang dihasilkan oleh masing-masing sampel juga ditunjukkan oleh hasil perhitungan fill factor (FF). Hasil perhitungan fiil factor
28
Simpulan
Hasil modifikasi dye yang menggantikan unsur logam inti klorofil (Mg)
dengan unsur ion logam Zn2+ dan Cu2+ yang kemudian dikombinasikan dengan nanopartikel ZnO mengubah daerah serapan ZnO menjadi lebih lebar dari daerah UV ke visibel. Untuk aplikasi sel surya yang dikombinasikan dengan elektrolit padat CuSCN ke dalam bentuk sel surya hibrid, didapatkan bahwa dye Cu-feofitin
menghasilkan nilai fill factor 55% lebih besar dari jenis dye klorofil dan
Zn-feofitin. Besarnya nilai Vmaks sangat dipengaruhi oleh kualitas dye yang digunakan yang terkait dengan stabilitas. Rendahnya nilai Voc sangat dipengaruhi oleh kosentrasi dari dye, mengakibatkan rendahnya daya maksimum yang dihasilkan
akibat penurunan rendahnya tegangan maksimum sehingga arus maksimumnyapun akan rendah.
5
PEMBAHASAN UMUM
Subtitusi ion logam Zn2+dan Cu2+ ke dalam pusat klorofil telah memberikan pengaruh terhadap posisi dan pola serapan serta memberikan tingkat stabilitas yang baik pada klorofil. Klorofil yang telah tersubtitusi dengan ion logam mengalami pergeseran ke daerah biru dengan daerah serapan yang lebih luas. Pergeseran pada daerah serapan ini tentu saja mengakibatkan terjadinya perbedaan dalam transfer muatan pada keadaan HOMO dan LUMO. Sesuai teori bahwa transfer elektron pada HOMO dan LUMO tergantung pada tingkat energi ionisasinya (Xu et al. 2010), Ini dikarenakan oleh muatan inti dalam klorofil yang
berbeda setelah subtitusi. Sedangkan pelebaran serapan yang dihasilkan setelah subtitusi mengindikasikan jumlah spektrum yang terserap masing-masing dye.
Banyaknya jumlah spektrum yang terserap ini akan mempercepat elektron untuk tereksitasi dari keadaan dasar ke keadaan yang lebih tinggi. Hasil subtitusi ion logam pada klorofil juga telah menyebabkan penurunan absorbansi yang mengindikasikan pada jumlah kosentrasi. Kosentrasi yang rendah mengakibatkan jumlah muatan yang terkandung di dalam dye telah berkurang.
Kombinasi antara ZnO/klorofil dalam bentuk film hibrid, telah menyebabkan perubahan pola serapan pada ZnO yang menjadi lebih lebar, sehingga lebih banyak spektrum yang terserap. Dalam kombinasi antara ZnO/klorofil-CuSCN pada bentuk sel surya hibrid telah membangkitkan tegangan terbuka (Voc) yang berbeda untuk setiap dye yang digunakan. Perbedaan nilai tegangan yang dihasilkan ini kemungkinan besar disebabkan oleh kosentrasi untuk masing-masing dye yang berbeda. Perbedaan nilai kosentrasi ini, telah
ditandai dengan menurunnya nilai absorbansi yang dihasilkan.
29 mengalami degradasi. Sedangkan untuk klorofil yang tersubtitusi dengan logam, tampak memperlihatkan bentuk kurva lebih stabil yang ditandai dengan nilai fill factor (FF) yang dihasilkan, meskipun nilai efisiensinya lebih rendah dari klorofil
modifikasi.
Secara khusus mekanisme terbentuknya arus dapat dilihat pada Gambar 18, yaitu diawali dengan penyerapan foton pada material organik sehingga menghasilkan pasangan muatan antara elektron dan hole bebas yang disebut
eksiton. Eksiton akan tereksitasi ke level yang lebih tinggi bila mendapat energi yang cukup, artinya enegi foton yang diberikan harus lebih besar atau sama dengan energi dalam eksiton. Eksiton yang tereksitasi akan berdifusi ke inter face
sehingga terjadi pemisahan muatan antara elektron dan hole akibat medan listrik
yang disebabkan oleh beda muatan. Selanjutnya elektron dan hole akan bergerak
menuju elektroda masing-masing. Dalam perjalanannya menuju elektroda, elektron harus terfasilitasi dengan baik, disinilah peranan elektrolit sangat dibutuhkan. Elektron yang telah mencapai elektrodanya akan siklus kembali menuju elektroda hole sehingga membentuk pasangan elektron hole atau eksiton.
Secara rinci proses ini dapat digambarkan pada diagram Gambar 18 dibawah ini.
[image:41.595.212.439.348.528.2](Desai et al. 2012)
Gambar 18. Mekanisme transpor elektron pada sel srya hibrid
Beberapa hasil penelitian yang telah dilakukan dalam bentuk sel surya hibrid, merupakan kombinasi dari ZnO dengan dye sintetis dapat dilihat pada
Tabel 3. Bila dibandingkan antara hasil eksperimen dengan penelitian sebelumnya, klorofil yang termodifikasi dengan logam sangat mungkin untuk dikembangkan lebih lanjut baik dari sisi stabilitas I-V maupun efisiensi. Khusus untuk klorofil yang termodifikasi dengan logam Cu memiliki nilai fill factor yang lebih tinggi
30
Tabel 3. Perbandingan tingkat stabilitas dalam sel surya hybrid
Struktur Sel Voc
(mV) FF (%) η Acuan
ZnO/klorofil/CuSCN 542 0,37 2,5 eksperimen
ZnO/Zn-feofitin/CuSCN 427 0,45 1,3 eksperimen ZnO/Cu-feofitin/CuSCN 286,8 0,55 0,3 eksperimen
TiO2/N3/CuI 590 0,37 0,4 Meng et al. (2003) ZnO/N719/CuSCN 570 0,37 1,7 Desai et al. 2012
ZnO/N3/CuSCN 600 0,44 2,1 O’regan et al. 2002
TiO2/C60/CuSCN 350 0,4 0,12 Senadeera dan Perera. 2005
6
SIMPULAN DAN SARAN
Simpulan
Klorofil yang termodifikasi dengan ion logam Zn2+ dan Cu2+ telah menyebabkan perubahan pada serapan klorofil alami. Korofil yang termodifikasi memiliki serapan yang lebih luas khususnya yang termodifikasi ion logam Cu2+. Kombinasi antara ZnO/klorofil dalam bentuk sel surya hibrid,telah memperlihatkan serapan yang lebih luas pada serapan ZnO ke daerah visibel, khususnya untuk klorofil yang termodifikasi. Sehingga dalam aplikasi sel suryanya klorofil yang termodifikasi menghasilkan nilai fill factor yang lebih
besar dari pada klorofil tanpa modifikasi.
Saran
1. Perlu dilakukan kembali sintesis ZnO dengan bentuk morfologi ZnO nanorod, nanofiber, nanoflower, dll
2. Karena klorfil a merupakan bagian yang sensitif cahaya, sebaiknya klorofil yang digunakan adalah klorofil a, sehingga perlu dilakukan pemisahan antara klorofil a dan b
31 DAFTAR PUSTAKA
Agostiano. A, Catucci. L, Cosma. P, and Fini. P,. 2003. Aggregation Prosses and Photophysical Poperties of Chlorophyll a in Aqueous Solution Modulated by Presence of Cyclodextrins. J.Phys. Chem. 5. 2122-2128
Agmon N. 1990. Dynamic Stikes shift in Coumarin: Is it only relaxation?. J. Phys. Chem. 94. 2959-2963
Ali. Mohammad M. 2011. Characterization of ZnO thin films grown by chemical bath deposition. Journal of Basrah Researches.Vol.37.No.3A
Altaf M, Chaudhry M. Ashraf, Zahid Maria. 2003. Study Of Optical Band Gap Of Zinc-Borate Glasses. J. res. Sci. 14(2). 253-259
Aneesh P. M., Vanaja K. A., Jayaraj M. K., 2007, Synthesis of ZnO nanoparticles by hydrothermal method, Nanophotonic Materials IV, Vol. 6639, 0277-786
Beek Waldo J. E., Wienk Martijn M., Kemerink Martijn, Yang Xiaoniu, and Janssen Ren A. J. 2005, Hybrid Zinc Oxide Conjugated Polymer Bulk Heterojunction Solar Cells, J. Phys. Chem. B, 109, 9505-9516
Budiyanto A.W., Notosudarmo S., dan Limantara L., 2008. Pengaruh pengasaman terhadap fotodegradasi Kloofil a. JMS. Vol. 13. No.3
Chand N, Hedaoo M, Gautam KKS and Khare PS. 2012. Optical Properties of Mango Leaf Dye Sensitized Zinc Oxide NanocrystallineThin Film for Solar Cell. Scholarly J. Biotechnol. Vol. 1(2), pp. 39-46
Christiana R, Kristopo H, Limantara L. 2008. Photodegradation and antioxidant activity of chlorophyll a from spirulina (spirulina sp.) Powder. Indo. J. Chem. (2), 236 - 241
Dapic N, 2012, Behaviour Of Fothergilla gardenii Chlorophyll Catabolite Under
Acidic Conditions, Kragujevac J. Sci. (34) 79-85.
Desai U.V, Xu Chengkun, Wu Jiamin, dan Gao Di, 2012, Solid-state-Dye Sensitized Solar Cell Based on Ordered ZnO nanowire arrays,
Nanotechnology, (23).205-401
Erge H.S, Karadenz F, Koca N, Soyer Y., 2008. Effect Of Heat Treatment On Chlorophyll Degradation And Color Loss In Green Peas. GIDA. 33 (5) : 225-233
Fiedor J, Fiedor L, Kammhuber N, Scherz. A, and Scher. H. 2002. Photodynamics of the Bacteriochlorophyll-Carotenoid System. 2. Influence of central Metal,
Solvent and β-Caroten on Photobleaching of Bacteriochlorophyll Derivatives.
J. Photochem. Photbiol. 76:2. 145-152.
Gupta S.K, Joshi A,Kaur M. 2010. Development of gas sensors using ZnO nanostructures. J. Chem. Sci. Vol. 122, No. 1.57–62
Gupta M, Sharma V, Shrivastav