PENGARUH PEMBERIAN EKSTRAK BUAH MAHKOTA DEWA(Phaleria macrocarpa) TERHADAP GAMBARAN
HISTOPATOLOGIS HEPAR TIKUS PUTIH (Rattus Norvegicus) GALUR Sprague dawley YANG
DIINDUKSI7,12-DYMETHYLBENZ(α)ANTHRACENE (DMBA)
Oleh
Desty Ariani 1018011050
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA KEDOKTERAN
Pada
Fakultas Kedokteran Universitas Lampung
FAKULTAS KEDOKTERAN UNIVERSITAS LAMPUNG
ABSTRACT
THE INFLUENCE OF GIVING MAHKOTA DEWA (Phaleria macrocarpa) EXTRACT AGAINST DYMETHYLBENZ(α)ANTHRACENE (DMBA)
INDUCED HEPAR HISTOPATHOLOGY APPEARANCE IN Sprague dawley RATS
By
DESTY ARIANI
Mahkota dewa (Phaleria macrocarpa) is one type of plant that originated from island of Papua but able to live well in other place. It reported to have various biological activities as hepatoprotector. Phaleria macrocarpa (PM) contain flavonoid and polifenol which are neutralize free radicals because of their antioxidant and antiinflammatory activity.
The aim of this research was to determine the influence of giving etanol 70% extract of Mahkota dewa fruit. In this study, twenty five rats (Rattus novergicus) Sprague dawley strain devided into five groups and given treatment for 14 days. G1 (only given aquadest), G2 (only given DMBA 30 mg/BW), G3 (given DMBA and PM extract 24 mg), G4 (given DMBA and PM extract 48 mg), G5 (given DMBA and PM extract 96 mg).
Result showed that total average of inflammation in G1 was 1,08; G2: 3,32; G3: 2,92; G4: 2,28; G5: 1,84. The conclusion of this research is that Mahkota dewa extract 24 mg, 48 mg, and 96 mg could act against DMBA-induced hepar inflammation in rats by mechanism related to its antioxidant and antiinflammatory properties.
ABSTRAK
PENGARUH PEMBERIAN EKSTRAK BUAH MAHKOTA DEWA (Phaleria macrocarpa) TERHADAP GAMBARAN HISTOPATOLOGIS HEPAR TIKUS PUTIH (Rattus Norvegicus) GALUR Sprague dawley YANG
DIINDUKSI 7,12-DYMETHYLBENZ(α)ANTHRACENE (DMBA)
Oleh
DESTY ARIANI
Mahkota dewa (Phaleria macrocarpa) merupakan salah satu tanaman yang berasal dari Pulau Papua namun dapat hidup dengan baik di tempat lainnya. Dia dilaporkan dilaporkan memiliki berbagai aktivitas biologi seperti hepatoprotektor. Phaleria macrocarpa (PM) mengandung flavonoid dan polifenol yang dapat menetralkan radikal bebas karena aktivitas antioksidan dan antiinflamasinyanya.
Tujuan dari penelitian ini adalah untuk mengetahui pengaruh pemberian ekstrak etanol 70% buah mahkota dewa. Pada penelitian ini, 25 tikus dibagi dalam 5 kelompok dan diberi perlakuan selama 14 hari. K1 (hanya diberi aquades), K2 (hanya diberi DMBA 30 mg/kgBB), K3 (diberi DMBA 30 mg/kgBB ekstrak PM 24 mg), K4 (diberi DMBA 30 mg/kgBB dan ekstrak PM 48 mg), dan K5 (diberi DMBA 30 mg/kgBB dan ekstrak PM 96 mg).
Hasil penelitian menunjukkan total rerata inflamasi pada K1 yaitu 1,08; K2: 3,32; K3: 2,92; K4: 2,28; K5: 1,84. Kesimpulan dari penelitian ini yaitu ekstrak mahkota dewa dapat bertindak melawan inflamasi hepar tikus yang diinduksi DMBA yang berkaitan dengan sifat antioksidan dan antiinflamasinya.
DAFTAR ISI
Halaman
DAFTAR TABEL ...iv
DAFTAR GAMBAR ... v
DAFTAR LAMPIRAN...vi
I. PENDAHULUAN ...1
A. Latar Belakang ...1
B. Perumusan Masalah...3
C. Tujuan Penelitian ...3
D. Manfaat Penelitian...3
E. Kerangka Teori ...4
F. Kerangka konsep...7
G. Hipotesis...9
II. TINJAUAN PUSTAKA ...10
A. Intoksikasi hepar ...10
B. Mahkota dewa ...13
1. Klasifikasi...13
2. Deskripsi tanaman mahkota dewa...14
ii
III. METODE PENELITIAN ...20
A. Desain Penelitian...20
B. Tempat dan Waktu ...20
C. Populasi dan Sampel ...21
D. Kriteria inklusi dan eksklusi...22
E. Alat dan bahan ...23
1. Bahan penelitian...23
2. Bahan kimia ...23
3. Alat penelitian ...23
4. Alat pembuatan preparat histopatologi...24
F. Prosedur Penelitian ...24
1. Prosedur pemberian ekstrak etanol 70% mahkota dewa...24
2. Prosedur pemberian dosis ekstrak etanol 70% mahkota dewa...25
3. Prosedur pemberian dosis DMBA ...26
4. Prosedur penelitian ...26
G. Identifikasi Variabel dan Definisi Operasional ...33
1. Identifikasi variabel ...33
2. Definisi operasional variabel...33
H. Analisis Data ...34
I. Etika penelitian ...35
IV. HASIL DAN PEMBAHASAN ...36
A. Hasil Penelitian ...36
1. Gambaran histopatologi hepar tikus...36
2. Analisis histopatologi kerusakan hepar tikus ...40
B. Pembahasan...42
V. KESIMPULAN DAN SARAN...50
A. Kesimpulan ...50
DAFTAR PUSTAKA ...52
DAFTAR GAMBAR
Gambar Halaman
1. Kerangka teori ...6
2. Kerangka konsep ...8
3. Peradangan pada hepatosit ...11
4. Perlemakan hepar ...12
5. Diagram alur penelitian ...32
6. Gambran histopatologi hepar ... 38
DAFTAR TABEL
Tabel Halaman
1. Skor penilaian derajat peradangan ...31
2. Definisi operasional variabel... 33
3. Hasil persentase rerata skor sel radang pada hepar tikus yang diberi
DAFTAR LAMPIRAN
Lampiran Halaman
A. Hasil persentase rerata skor sel radang pada hepar tikus yang diberi
ekstrak buah mahkota dewa... 58
B. Uji statistik ... 59
C. Foto gambaran histopatologi hepar tikus ... 67
I. PENDAHULUAN
A. Latar Belakang
Hati merupakan organ metabolisme terpenting dalam proses sintetis, penyimpanan,
metabolisme, dan klirens banyak senyawa endogen. Salah satu fungsi hati adalah
detoksikasi (menawarkan racun tubuh), sehingga hati mudah menjadi sasaran utama
ketoksikan. Penyakit hati tergolong sebagai salah satu penyakit yang merupakan
problem nasional di Indonesia dan negara berkembang pada umumnya, bahkan
merupakan masalah yang hangat di negara–negara maju. Berdasarkan laporan dari
Rumah Sakit Umum Pusat (RSUP) tipe A dan B di seluruh Indonesia, ternyata
penyakit hepar menempati urutan ketiga setelah penyakit infeksi dan penyakit paru,
bahkan penyakit hepar penyebab kematian tergolong tinggi (Akhirunnisa, 2010).
Hepatoprotektor yang saat ini digunakan, harganya tidak terjangkau bagi masyarakat
dan mengandung bahan kimia sehingga diperlukan hepatoprotektor yang aman dan
terjangkau bagi masyarakat. Salah satu kandungan yang diperlukan sebagai
hepatoprotektor adalah antioksidan yang banyak dikandung oleh berbagai macam
tanaman yang mudah didapat oleh masyarakat, murah, dan tidak mengandung bahan
kimia yang berbahaya (Situmorang, 2010). Selain itu, saat ini banyak penelitian
dilakukan untuk mencari alternatif pengobatan terutama menggunakan bahan–bahan
dan lebih ekonomis dibandingkan dengan obat sintetis. Di sisi lain pengembangan
obat bahan alam Indonesia yang potensial untuk obat masih harus dilakukan oleh
para peneliti/akademisi sehingga ketergantungan bahan baku dari negara lain dapat
dikurangi (Wahyunigsih, 2010).
Salah satu tumbuhan obat Indonesia yang sangat populer saat ini adalah mahkota
dewa (Phaleria macrocarpa) dari suku Thymelaceae yang mempunyai kandungan senyawa aktif yaitu flavonoid yang berpotensi sebagai antiinflamasi dan antioksidan
kuat. Mahkota dewa tergolong tanaman perdu yang tumbuh dari dataran rendah
hingga ketinggian 1200 meter di atas permukaan laut (Simanjuntak, 2008).
Penelitian sebelumnya yang dilakukan oleh Hamid dkk. (2009) menyatakan bahwa
kandungan flavonoid pada ekstrak daun sambung nyawa (Gynura procumbens) dapat berperan sebagai blocking agent dalam mencegah inisiasi tahap karsinogenesis hepar yang terinduksi 7,12 dimethylbenz(α)anthracene (DMBA). Selain itu, penelitian
lainnya dilakukan oleh Meiyanto dkk. (2011) yang menggunakan ekstrak etanolik
kulit jeruk keprok yang memiliki kandungan flavonoid dapat menghambat proliferasi
sel hepar tikus akibat pemberian DMBA melalui penekanan ekspresi c–Mcy sel hepar
tikus galur Sprague dawley. Namun, penelitian mengenai pengaruh ekstrak buah mahkota dewa terhadap histopatologi hepar tikus yang diinduksi DMBA masih jarang
dilakukan.
Berdasarkan uraian tersebut, peneliti tertarik untuk melakukan penelitian mengenai
pengaruh ekstrak daun mahkota dewa (Phaleria macrocarpa) terhadap tikus putih (Rattus norvegicus) galur Sprague dawley yang diinduksi DMBA. Parameter yang digunakan dalam penelitian ini adalah dilakukan pemeriksaan mikroskopis untuk
3 B. Perumusan Masalah
Apakah ada pengaruh pemberian ekstrak mahkota dewa (Phaleria macrocarpa) terhadap gambaran histopatologis hepar tikus putih (Rattus norvegicus) galurSprague dawleyyang diinduksi DMBA?
C. Tujuan
Adapun tujuan dari penelitian ini adalah:
1. Tujuan Umum
Mengetahui pengaruh ekstrak buah Mahkota Dewa (Phaleria macrocarpa) terhadap gambaran histopatologi hepar tikus putih (Rattus novergicus) galur Sprague dawley yang diinduksi DMBA.
2. Tujuan khusus
Mengetahui pengaruh pemberian peningkatan dosis ekstrak mahkota dewa
(Phaleria macrocarpa), 24 mg, 48 mg, dan 96 mg, terhadap gambaran histopatologis hepar tikus putih (Rattus norvegicus) galur Sprague dawley yang diinduksi oleh DMBA.
D. Manfaat Penelitian
1. Bagi ilmu pengetahuan
Hasil penelitian ini diharapkan dapat memberikan informasi ilmiah mengenai
2. Bagi Pembangunan
Hasil penelitian ini diharapkan dapat menjadi acuan yang akan mendukung upaya
pemeliharaan tanaman mahkota dewa (Phaleria macrocarpa) sebagai salah satu tanaman berkhasiat obat. Dengan demikian akan mendukung upaya pemerintah
untuk menyukseskan program tanaman obat atau obat herbal.
3. Bagi Fakultas Kedokteran Universitas Lampung (FK Unila)
Meningkatkan iklim penelitian dibidang agromedicinesehingga dapat menunjang pencapaian visi FK Unila 2015 sebagai Fakultas Kedokteran Sepuluh Terbaik di
Indonesia pada Tahun 2025 dengan kekhususanagromedicine. 4. Bagi Peneliti Lain
Dapat dijadikan bahan acuan untuk dilakukannya penelitian yang serupa yang
berkaitan dengan efek buah mahkota dewa (Phaleria macrocarpa).
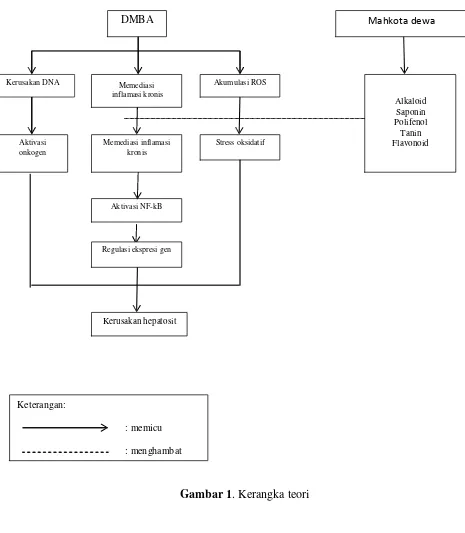
E. Kerangka Teori
7,12–dymethylbenz(α)anthracene (DMBA) merupakan karsinogen prototipe yang
secara luas digunakan dan poten di selektif area yaitu kelenjar mama, kulit, ginjal, dan
liver. Paparan DMBA menginduksi perubahan patologi klinik melalui toksisitas yang
terjadi pada kulit, hepar, kelenjar mammae, dan ginjal. Pada hepar ditandai dengan
adanya kerusakan parenkim hepatoseluler, lesi hati, tumor, dan kanker (Paliwal et al., 2011).
5 dan atau inaktivasi gen supresi tumor dan berbagai epigenetik yang menyebabkan
progresi dari tumor (He & Karin, 2011). DMBA terbukti dapat menginduksi produksi
ROS yang mengakibatkan peroksidasi lipid, kerusakan DNA, dan deplesi dari sel
sistem pertahanan antioksidan (Kasolo et al., 2010). Mediator inflamasi kronis yang dihasilkan oleh makrofag yang teraktivasi akibat induksi DMBA dapat
mengakibatkan nuclear factor kappa B (NF-kB) teraktivasi (Oktaviana dkk., 2012). NF-kB meregulasi ekspresi gen yang termasuk dalam beberapa proses yang
mempunyai peranan penting di dalam perkembangan dan progresi dari kanker, yaitu
proliferasi, migrasi, dan apoptosis (Dolcetet al., 2005).
Flavonoid adalah antioksidan yang kuat karena aktivitasnya sebagai antioksidan dan
antiinflamasi. Antioksidan di dalam mahkota dewa mempunyai aktivitas menetralkan
radikal bebas sehingga mencegah kerusakan oksidatif pada sebagian besar biomolekul
dan menghasilkan proteksi terhadap kerusakan oksidatif secara signifikan (Sreelatha
& Padma, 2009). Antioksidan menstabilkan radikal bebas dengan melengkapi
kekurangan elektron yang dimiliki radikal bebas, dan menghambat terjadinya reaksi
berantai dari pembentukan radikal bebas yang dapat menimbulkan stres oksidatif
DMBA Mahkota dewa
Kerusakan DNA Memediasi inflamasi kronis
Akumulasi ROS
Alkaloid Saponin Polifenol
Tanin Aktivasi
onkogen
Memediasi inflamasi kronis
Stress oksidatif Flavonoid
Aktivasi NF-kB
Regulasi ekspresi gen
Kerusakan hepatosit
Keterangan:
: memicu
: menghambat
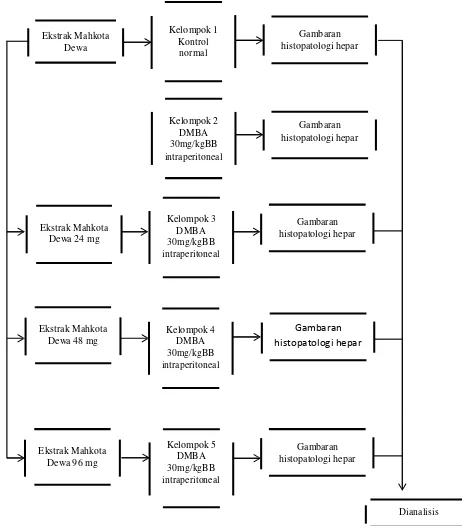
7 F. Kerangka Konsep
Tikus sebanyak 25 ekor, dikelompokkan dalam 5 kelompok. Kelompok I sebagai
kontrol normal, hanya yang diberi aquades dan pakan protein 14% untuk riset.
Kelompok II sebagai kontrol patologis, yang telah diinduksi DMBA dengan dosis 30
mg/kgBB. Kelompok III adalah kelompok yang telah diinduksi DMBA 30 mg/kgBB
dan diberikan ekstrak mahkota dewa dosis 24 mg, kelompok IV telah diinduksi dmba
30 mg/kgBB dan diberikan ekstrak mahkota dewa dengan dosis 48 mg, dan kelompok
V telah diinduksi DMBA dan diberikan ekstrak mahkota dewa dengan dosis 96 mg.
Masing–masing mahkota dewa diberikan secara peroral selama 15 hari. Setelah 15
hari, perlakuan diberhentikan. Selanjutnya tikus dilakukan dekapitasi dan dilakukan
pembedahan. Setelah dilakukan laparotomi untuk mengambil organ hepar tikus,
Ekstrak Mahkota Dewa Kelompok 1 Kontrol normal Gambaran histopatologi hepar Kelompok 2 DMBA 30mg/kgBB intraperitoneal Gambaran histopatologi hepar Ekstrak Mahkota Dewa 24 mg
Kelompok 3 DMBA 30mg/kgBB intraperitoneal Gambaran histopatologi hepar Ekstrak Mahkota Dewa 48 mg
Kelompok 4 DMBA 30mg/kgBB intraperitoneal Gambaran histopatologi hepar Ekstrak Mahkota Dewa 96 mg
Kelompok 5 DMBA 30mg/kgBB intraperitoneal Gambaran histopatologi hepar Dianalisis
9 G. Hipotesis
1. Pemberian ekstrak buah mahkota dewa (Phaleria macrocarpa) berpengaruh terhadap gambaran histopatologis hepar tikus putih (Rattus norvegicus) galur Sprague dawleyyang diinduksi DMBA.
2. Pemberian peningkatan dosis ekstrak buah mahkota dewa (Phaleria macrocarpa), 24 mg, 48 mg, dan 96 mg berpengaruh terhadap gambaran histopatologis hepar
II. TINJAUAN PUSTAKA
A. Intoksikasi Hepar
Hepar memiliki fungsi vital dalam detoksikasi bahan toksik. Hal ini
menyebabkan hepar menjadi sering terpapar dengan zat–zat toksik yang
mengakibatkan kerusakan sel hepar (Anshor dkk., 2013). Kerusakan hati
dapat meliputi struktur maupun gangguan fungsi hati. Kerusakan hati
dapat disebabkan oleh infeksi, virus, obat, trauma, atau karena bahan
kimia alami atau sintetik. Pemaparan oleh berbagai bahan toksik akan
mempertinggi kerusakan hati. Radikal bebas adalah salah satu produk
reaksi kimia dalam sel yang sangat reaktif karena mengandung elektron
yang tidak berpasangan dan dapat menyebabkan kerusakan hati yang
ditandai dengan peradangan akut pada sel–sel hati yaitu terjadinya
steatosis dan nekrosis (Xiaoyueet al., 2007).
Dari sudut pandang patologik, hepar adalah organ yang secara inheren
sederhana dengan berbagai respons yang terbatas terhadap cedera.
Apapun penyebabnya, ditemukan lima respon umum hepar terhadap
cedera, yaitu peradangan, degenerasi, nekrosis, fibrosis, dan sirosis
11 a. Peradangan
Cedera hepatosit yang menyebabkan influks sel radang akut atau
kronis ke hepar disebut hepatitis. Serangan terhadap hepatosit hidup
yang mengekspresikan antigen oleh sel T yang telah tersensitisasi
merupakan penyebab umum kerusakan hepar. Peradangan mungkin
terbatas di saluran porta atau mungkin meluas ke parenkim (Kumar
dkk., 2007).
Gambar 3.Peradangan pada hepatosit (Kumar dkk., 2007).
b. Degenerasi
Kerusakan akibat gangguan toksik atau imunologis dapat
menyebabkan hepatosit membengkak, tampak edematosa, dengan
sitoplasma iregular bergumpal dan rongga–rongga jernih yang lebar.
Selain itu, bahan empedu yang tertahan dapat menyebabkan hepatosit
tampak membengkak seperti berbusa degenerasi busa. Akumulasi
hati alkoholik, sindrom Reye, dan perlemakan hati akut pada
kehamilan (Kumar dkk., 2007).
Gambar 4.Perlemakan hepar (Kumar dkk, 2007).
c. Nekrosis
Pada nekrosis, tersisa hepatosit yang mengalami mumifikasi dan kurang
terwarnai, umumnya akibat iskemia atau nekrosis koagulasi. Kematian
sel yang bersifat toksik atau diperantarai oleh sistem imun terjadi melalui
apoptosis, yang hepatositnya menjadi ciut, piknotik, dan sangat
eosinofilik. Selain itu, hepatosit dapat mengalami pembengkakan
osmotik dan pecah yang disebut degenerasi hidropik atau nekrosis litik
(Kumar dkk., 2007).
d. Fibrosis
Jaringan fibrosis terbentuk sebagai respons terhadap peradangan atau
gangguan toksik langsung ke hepar. Pengendapan kolagen menimbulkan
dampak permanen pada pola aliran darah hepar dan perfusi hepatosit.
13 vena sentralis, atau mengendap langsung di dalam sinusoid. Lambat laun
jaringan fibrosa menghubungkan regio hepar dari ke-porta,
porta-ke-sentral, atau sentral-ke-sentral yang disebut bridging fibrosis (Kumar dkk., 2007).
e. Sirosis
Berlanjutnya fibrosis dan cedera parenkim menyebabkan hepar terbagi–
bagi menjadi nodus hepatosit yang mengalami regenerasi dan dikelilingi
oleh jaringan parut. Jaringan parut ini disebut sirosis (Kumar dkk., 2007).
B. Mahkota Dewa
1. Klasifikasi
Klasifikasi tumbuhan mahkota dewa menurut Kurniasih (2013) adalah
sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Dicotyledon
Kelas : Thymelaeacae
Marga : Phaleria
2. Deskripsi Tanaman Mahkota Dewa
Mahkota dewa (Phaleria macrocarpa) adalah jenis tanaman yang termasuk dalam famili Thymelaeaceae dan umumnya dikenal sebagai mahkota dewa (Hendra dkk., 2011). Tanaman ini berasal dari Pulau
Papua, Indonesia, tumbuh di daerah tropis dan merupakan salah satu
tanaman obat yang paling populer di Indonesia (Parhizkaret al., 2013). Ia berbunga pada April–Agustus. Bunga berbentuk terompet, putih, dan
harum. Panjang dari pangkal tangkai hingga ujung 3–4 cm. Buahnya
bulat, hijau ketika muda dan merah marun saat tua. Terdiri dari kulit,
daging, cangkang, dan biji. Besar buah umumnya seukuran bola
pingpong. Tebal kulit 0,5–1 mm. Penampilan menarik membuat mahkota
dewa banyak dipelihara sebagai tanaman hias (Wijayakusuma, 2008).
Mahkota dewa merupakan tanaman obat yang sudah dikenal dan saat ini
semakin diminati masyarakat. Tanaman yang berasal dari Papua berkhasiat
untuk mengobati luka, diabetes, lever, flu, alergi, sesak nafas, disentri,
penyakit kulit, diabetes, jantung, ginjal, kanker, darah tinggi, asam urat,
penambah stamina, ketergantungan narkoba, dan pemicu kontraksi rahim
(Rohyami, 2008).
Penelitian tentang uji aktivitas dan karakterisasi senyawa aktif terus
dikembangkan, terutama aktivitasnya sebagai antioksidan yang merupakan
senyawa polifenol, flavonoid, alkaloid, dan saponin. Salah satu senyawa
aktif yang ditemukan terdapat dalam ekstrak metanol daging buahnya yang
15 telah dilakukan menunjukkan aktivitas biologi antikanker pada bagian buah
tanaman lebih tinggi dibandingkan dengan bagian tanaman lain dari
mahkota dewa (Lisdawati, 2009).
Flavonoid termasuk senyawa fenolik alam yang potensial sebagai
antioksidan dan mempunyai bioaktivitas sebagai obat. Flavonoid
merupakan sekelompok besar antioksidan bernama polifenol yang terdiri
atas antosianidin, biflavon, katekin, flavanon, flavon, dan flavanolol.
Kuersetin adalah salah satu zat aktif kelas flavonoid yang secara biologis
amat kuat dan merupakan senyawa kelompok flavonolol terbesar, 60–75%
dari total flavonoid. Bila vitamin C mempunyai aktivitas antioksidan 1,
maka kuersetin memiliki antioksidan 4,7. Oleh karena itu, kuersetin dari
flavonoid diduga menjadi faktor penyebab radikal bebas menjadi netral
sehingga dapat menurunkan agen proinflamasi yang selanjutnya dapat
mempengaruhi aktivitas NF-B (Waji & Sugrani, 2009).
Penggunaan tanaman obat harus berdasarkan asas manfaat dan keamanan.
Jika bermanfaat untuk menyembuhkan penyakit, tetapi tidak aman karena
racun, harus dipikirkan kemungkinan timbulya keracunan akut maupun
keracunan kronis yang mungkin terjadi. Belum diketahui dosis efektif yang
aman dan bermanfaat. Untuk obat yang diminum, gunakan beberapa irisan
buah kering (tanpa biji). Selama beberapa hari baru dosis ditingkatkan
sedikit demi sedikit, sampai dirasakan manfaatnya. Untuk penyakit berat,
seperti kanker dan psoriasis, dosis pemakaian kadang harus lebih besar agar
C. Intoksikasi Hepar dan Ekstrak Mahkota Dewa
Kerusakan hepar karena zat toksik dipengaruhi oleh beberapa faktor, seperti
jenis zat kimia yang terlibat, dosis yang diberikan, dan lamanya paparan zat
tersebut. Kerusakan hepar dapat terjadi setelah beberapa minggu sampai
beberapa bulan. Kerusakan dapat berbentuk nekrosis hepatosit, kolestasis,
atau timbulnya disfungsi hepar secara perlahan. Radikal bebas merupakan
suatu molekul yang sangat reaktif karena mempunyai satu atau lebih elektron
yang tidak berpasangan. Radikal bebas sangat reaktif karena kehilangan satu
atau lebih elektron yang bermuatan listrik, dan untuk mengembalikan
keseimbangannya maka radikal bebas berusaha mendapatkan elektron dari
molekul lain atau melepas elektron yang tidak berpasangan tersebut
(Amalina, 2009).
Salah satu radikal bebas adalah senyawa 7,12–dimetilbenz(α)antrasen
(DMBA) yang banyak terdapat pada asap rokok, asap kendaraan bermtor, dan
asap dapur. DMBA merupakan karsinogen sekunder (prokarsinogen)
sehingga harus mengalami aktivasi metabolisme (biotransformasi) untuk
menghasilkan karsinogen aktif. Proses metabolisme menghasilkan DMBA
menjadi senyawa yang lebih toksik (Gao et al., 2007). Banyaknya paparan radikal bebas yang terdapat di lingkungan sehingga sangat besar
kemungkinan radikal bebas tersebut berikatan dengan sel di dalam tubuh.
DMBA dimetabolisme di hati dan akan menjadi senyawa yang reaktif setelah
mengalami metabolisme, hal ini memungkinkan dapat menyebabkan
17 Supaya dapat berpotensi sebagai karsinogen, DMBA semestinya
dimetabolisme di hepar tikus menjadi metabolit 7–hydoxy–DMBA oleh
karena metabolit tersebut yang bersifat reaktif oksidan terhadap DNA sel.
Beberapa studi memperlihatkan bahwa senyawa DMBA yang tidak
mengalami biotransformasi menjadi 7–hydoxy–DMBA gagal dalam
menyebabkan karsinoma (Nair & Varalakshmi, 2011). DMBA menurunkan
aktivitas enzim antioksidan yang bersifat kemoprotektif terhadap radikal
bebas seperti superoxide dismutase dan katalase pada hepar (Paliwal et al.,
2011). Stres oksidatif adalah mekanisme umum yang berkontribusi terhadap
inisiasi dan perkembangan kerusakan hati dalam berbagai gangguan hati.
Kadar Aspartate Transaminase (AST), Alanine Transaminase (ALT), dan Alkaline Phosphatase (ALP) yang terdapat dalam sel hati merupakan indikasi dari kerusakan hepatoseluler yang ditemukan menurun pada tikus yang
diinduksi DMBA (Sharmaet a.l, 2012).
Alur metabolisme DMBA melalui aktivasi enzim P450 menjadi intermediate
reaktif yang dapat merusak DNA. Enzim sitokrom P450 CYP1A1 atau
CYP1B1 dan enzim mikrosomal hidrolase pada metabolisme fase 1 merubah
DMBA menjadi DMBA–3,4–diol–1,2–epoksida (DMBA–DE). DMBA–DE
dan senyawa xenobiotic polisiklik aromatik hidrokarbon (PAH) lainnya mengakibatkan pembentukan radikal reaktif yang bersifat destruktif,
imunotoksik, dan hepatotoksik (Gao et al., 2007). Aktivasi enzim tersebut dapat dihambat oleh senyawa flavonoid yang terkandung di dalam mahkota
DMBA menyebabkan transformasi neoplastik melalui kerusakan DNA,
akumulasi ROS, dan memediasi inflamasi kronis (Manoharan et al., 2010). Kerusakan DNA menyebabkan pengaktifan onkogen dan atau inaktivasi gen
supresi tumor dan berbagai epigenetik yang menyebabkan progresi dari tumor
(He & Karin, 2011). DMBA terbukti dapat menginduksi produksi reactive
oxygen species (ROS) yang mengakibatkan peroksidasi lipid, kerusakan
DNA, dan deplesi dari sel sistem pertahanan antioksidan (Kasolo et al.,
2010). Mediator inflamasi kronis yang dihasilkan oleh makrofag yang
teraktivasi akibat induksi DMBA dapat mengakibatkan NF-kB teraktivasi
(Oktaviana dkk., 2012). NF-kB meregulasi ekspresi gen yang termasuk dalam
beberapa proses yang mempunyai peranan penting di dalam perkembangan
dan progresi dari kanker, yaitu proliferasi, migrasi, dan apoptosis (Dolcet et al., 2005).
Inflamasi merupakan suatu proses fisiologis dalam menanggapi kerusakan
jaringan akibat infeksi mikroba patogen, iritasi kimia, dan atau luka. Setelah
terjadi kerusakan jaringan, sinyal kimia akan menginisiasi dan
mempertahankan respon host yang dirancang untuk menyembuhkan jaringan yang rusak. Aktivasi dan migrasi leukosit ke lokasi kerusakan dan faktor
pertumbuhan, sitokin, oksigen reaktif, dan nitrogen species diketahui
memainkan peran penting dalam respon inflamasi. Proses inflamsi diperlukan
untuk menjaga kekebalan tubuh, perbaikan optimal, dan regenerasi setelah
19 Kandungan senyawa aktif yang terdapat pada tanaman mahkota dewa adalah
alkaloid, flavonoid, tanin, saponin, terpenoid, dan steroid. Golongan senyawa
dalam tanaman yang berkaitan dengan aktivitas antikanker dan antioksidan
antara lain adalah golongan alkaloid, terpenoid, polifenol, flavonoid dan juga
senyawa resin (Septiawati, 2008). Beberapa alkaloid yang diisolasi dari
tumbuhan alami menunjukkan efek antiproliferasi antimetastasis pada
berbagai jenis kanker baikin vitromaupunin vivo(Luet al., 2012).
Flavonoid adalah antioksidan yang kuat karena aktivitasnya sebagai
antioksidan dan antiinflamasi. Antioksidan di dalam mahkota dewa
mempunyai aktivitas menetralkan radikal bebas sehingga mencegah
kerusakan oksidatif pada sebagian besar biomolekul dan menghasilkan
proteksi terhadap kerusakan oksidatif secara signifikan (Sreelatha & Padma,
2009). Antioksidan menstabilkan radikal bebas dengan melengkapi
kekurangan elektron yang dimiliki radikal bebas, dan menghambat terjadinya
reaksi berantai dari pembentukan radikal bebas yang dapat menimbulkan stres
III. METODE PENELITIAN
A. Desain Penelitian
Penelitian ini merupakan penelitian eksperimental dengan metode acak
terkontrol dengan polapost test–only control group design. Sampel peneltitian menggunakan 20 ekor tikus putih yang telah diinduksi DMBA dan 5 ekor
tikus putih normal galur Sprague dawley berumur 5 minggu yang dipilih secararandomyang dibagi menjadi 5 kelompok.
B. Tempat dan Waktu
Penelitian dilakukan di Animal House Fakultas Kedokteran UNILA, sedangkan pembuatan preparat dan pengamatannya dilakukan di
Laboratorium Patologi Anatomi dan Histologi Fakultas Kedokteran
Universitas Lampung. Penelitian dilaksanakan selama 15 hari di bulan
✁ C. Populasi dan Sampel
Populasi penelitian ini adalah tikus putih (Rattus norvegicus) galur Sprague dawley berumur 5 minggu yang diperoleh dari laboratorium Balai Penelitian Veteriner (BALITVET) Bogor.
Tikus putih (Rattus norvegicus) galur Sprague Dawley merupakan tikus yang
paling sering digunakan untuk percobaan. Tikus ini memiliki temperamen
yang tenang sehingga mudah dalam penanganan. Tikus ini jarang hidup lebih
dari 3 tahun (Putra, 2009).
Sampel penelitian yang digunakan sebanyak 25 ekor tikus yang dipilih secara
acak dan dibagi dalam 5 kelompok dengan pengulangan sebanyak 5 kali
(n=5), sesuai dengan rumus Frederer. Menurut Frederer , rumus penentuan
sampel untuk uji eksperimental adalah:
(t–1) (r–1)>15
Dimana t merupakan jumlah kelompok percobaan dan n merupakan jumlah
pengulangan atau jumlah sampel tiap kelompok. Penelitian ini menggunakan
5 kelompok perlakuan sehingga perhitungan sampel menjadi:
(5–1) (r–1)>15
4n–4>15
4n>19
Jadi, sampel yang digunakan tiap kelompok percobaan sebanyak 5 ekor
(n>4,75) dan jumlah kelompok yang digunakan adalah 5 kelompok sehingga
penelitian ini menggunakan 25 ekor tikus putih dari populasi yang ada.
D. Kriteria Inklusi dan Ekslusi
1. Kriteria inklusi
a. Aktif bergerak
b. Memiliki berat badan 180–200 gram
c. Berusia 5 minggu
2. Kriteria ekslusi
1. Tampak sakit (penampakan rambut kusam, rontok, atau botak dan
aktivitas kurang atau tidak aktif, keluarnya eksudat yang tidak normal
dari mata, mulut, anus, genital)
2. Terdapat penurunan berat badan lebih dari 10% setelah masa adaptasi
di laboratorium
✄☎ E. Alat dan Bahan
1. Bahan Penelitian
Bahan penelitian yang digunakan ada dua yaitu DMBA dengan dosis 30
mg/kgBB dan ekstrak mahkota dewa (Phaleria macrocarfa) dengan dosis 24 mg, 48 mg, dan 96 mg.
2. Bahan Kimia
Bahan yang digunakan untuk pembuatan preparat histopatologi dengan
metode paraffin meliputi: larutan formalin 10% untuk fiksasi, alkohol
70%, alkohol 96%, alkohol absolut, etanol, xylol, pewarna hematoksilin
dan eosin, dan entelan.
3. Alat Penelitian
Alat penelitian yang digunakan dalam penelitian ini adalah:
a. Neraca analitik Metler Toledo dengan tingkat ketelitian 0,01 g, untuk menimbang berat tikus.
b. Spuit oral 1 cc
c. Minor setuntuk pembedahan tikus d. Kandang tikus
e. Botol minuman tikus
f. Mikroskop cahaya
4. Alat Pembuat Preparat Histopatologi
Alat pembuat preparat histopatologi yang digunakan adalah object glass, deck glass, tissue cassette, rotarymicrotome, oven, water bath, platening table, autochnicom processor, staining jar, staining rak, kertas saring, histoplast,danparafin dispenser.
F. Prosedur Penelitian
1. Prosedur Pemberian Ekstrak Etanol 70% Buah Mahkota Dewa Proses pembuatan ekstrak buah mahkota dewa dalam penelitian ini
menggunakan etanol sebagai pelarut. Ekstraksi dimulai dari penimbangan
daun mahkota dewa. Selanjutnya seluruh bagian tumbuhan dikeringkan
dalam almari pengering, dibuat serbuk dengan menggunakan blenderatau mesin penyerbuk. Etanol dengan kadar 70% ditambahkan untuk
melakukan ekstraksi dari serbuk ini selama kurang lebih 2 (dua) jam
kemudian dilanjutkan maserasi selama 24 jam. Setelah masuk ke tahap
filtrasi, akan diperoleh filtrat dan residu. Filtrat yang didapatkan akan
✞✟ 2. Prosedur Pemberian Dosis Ekstrak Etanol 70% Buah Mahkota Dewa
Dosis ekstrak buah mahkota dewa pada ekperimen ini adalah 120
mg/kgBB yang didapat dari dosis mencit pada penelitian sebelumnya
yang telah dikonversi ke dosis manusia terlebih dahulu (Rahmawati dkk.,
2006).
Dosis tikus (200g) = 120 mg/kgBB /1000
= 0,12 mg/gBB x 200
= 24 mg/200gBB
Dosis untuk 200g tikus adalah 24 mg/200gBB. Dalam penelitian ini
kelompok kontrol negatif dan kontrol positif tidak diberikan ekstrak
etanol 70% buah mahkota dewa. Dosis awal ekstrak etanol 70% buah
mahkota dewa diambil dari dosis normal tikus, sedangkan dosis kedua
diambil dari hasil pengalian 2x dosis pertama dan dosis ketiga diambil
dari hasil pengalian 4x dari dosis awal.
Jadi, dosis yang digunakan untuk tiap tikus pada kelompok III adalah
sebanyak 24 mg/200gBB, pada kelompok IV adalah 48 mg/200gBB, dan
pada kelompok V adalah 96 mg/gBB.
Volume ekstrak etanol 70% buah mahkota dewa diberikan secara oral
sebanyak 1 ml yang merupakan volume yang boleh diberikan berdasarkan
melebihi volume lambung, dapat berakibat dilatasi lambung secara akut
yang dapat menyebabkan robeknya saluran cerna (Ngatidjan, 2006).
3. Prosedur Pemberian Dosis DMBA
Dosis DMBA yang digunakan dalam penelitian ini adalah dosis tunggal
30mg/kgBB intraperitoneal. Dosis ini merupakan dosis karsinogenik pada
tikus.
4. Prosedur Penelitian
a. Tikus sebanyak 25 ekor, dikelompokkan dalam 5 kelompok.
Kelompok I sebagai kontrol normal, hanya yang diberi aquades dan
pakan protein 14% untuk riset. Kelompok II sebagai kontrol
patologis, diinduksi DMBA dengan dosis 30 mg/kgBB. Kelompok III
adalah kelompok yang telah diinduksi DMBA 30 mg/kgBB dan
diberikan ekstrak mahkota dewa dosis 24 mg, kelompok IV telah
diinduksi dmba 30 mg/kgBB dan diberikan ekstrak mahkota dewa
dengan dosis 48 mg, dan kelompok V telah diinduksi DMBA dan
diberikan ekstrak mahkota dewa dengan dosis 96 mg. Masing–masing
mahkota dewa diberikan secara peroral selama 15 hari
b. Setelah 15 hari, perlakuan dihentikan
c. Selanjutnya tikus dianastesi kemudian dilakukan dekapitasi dan
✡☛ d. Setelah dilakukan laparotomi untuk mengambil organ hepar tikus,
bangkai tikus dimusnahkan dengan cara pembakaran di tempat
khusus.
5. Dilakukan pemeriksaan morfologi hepar secara mikroskopis
a. Teknik pembuatan preparat:
1) Fixation
a) Memfiksasi spesimen berupa potongan organ hepar yang telah
dipilih segera dengan larutan pengawet formalin 10%
b) Mencuci dengan air mengalir
2) Trimming
a) Mengecilkan organ ±3 mm
b) Memasukkan potongan organ hepar tersebut ke dalam
embedding cassette 3) Dehidrasi
a) Menuntaskan air dengan meletakkan embedding cassette pada kertas tisu
b) Berturut–turut melakukan perendaman organ hepar dalam
alkohol bertingkat 70%, 96%, alkohol absolut I, II, III masing–
masing selama 1 jam
c) Clearing
4) Impregnasi
Impregnasi dengan menggunakan paraffin I dan II masing–masing selama 1 jam di dalam inkubator dengan suhu 65,10C
5) Embedding
a) Menuangkan paraffin cair dalam pan
b) Memindahkan satu persatu dari embedding cassette ke dasar pan
c) Melepaskan paraffin yang berisi potongan hepar dari pan
dengan memasukkan ke dalam suhu 4–60C beberapa saat
d) Memotong paraffin sesuai dengan letak jaringan yang ada
dengan menggunakan scalpel/pisau hangat
e) Meletakkan pada balok kayu, ratakan pinggirnya dan buat
ujungnya sedikit meruncing
f) Memblok paraffin siap dipotong dengan mikrotom
6) Cutting
a) Sebelum memotong, mendinginkan blok terlebih dahulu
b) Melakukan pemotongan kasar, dilanjutkan dengan
pemotongan halus dengan ketebalan 4–5 mikron
c) Memilih lembaran potongan yang paling baik, mengapungkan
pada air dan menghilangkan kerutannya dengan cara menekan
salah satu sisi lembaran jaringan tersebut dengan ujung jarum
✌✍ d) Memindahkan lembaran jaringan ke dalam water bath selama
beberapa detik sampai mengembang sempurna
e) Dengan gerakan menyendok mengambil lembaran jaringan
tersebut dengan slide bersih dan menempatkan di tengah atau pada sepertiga atas atau bawah, mencegah jangan sampai ada
gelembung udara di bawah jaringan
f) Mengeringkan slide. Jika sudah kering, slide dipanaskan untuk merekatkan jaringan dan sisa paraffin mencair sebelum
pewarnaan
g) Staining(pewarnaan) denganHarris Hematoxylin Eosin Setelah jaringan melekat sempurna pada slide, memilih slide yang terbaik selanjutnya secara berurutan memasukkan ke
dalam zat kimia di bawah ini dengan waktu sebagai berikut :
Untuk pewarnaan, zat kimia yang pertama digunakan xilol I,
II, III masing–masing selama 5 menit. Kedua, zat kimia yang
digunakan alkohol absolut I, II, III masing–masing selama 5
menit. Zat kimia yang ketiga aquades selama 1 menit.
Keempat, potongan organ di masukkan dalam zat warna
Harris Hematoxylinselama 20 menit.
Kemudian memasukkan potongan organ dalam Eosin selama
2 menit. Secara berurutan memasukkan potongan organ dalam
dan IV masing–masing selama 3 menit. Terakhir,
memasukkan dalam xilol IV dan V masing–masing 5 menit.
7) Mounting
Setelah pewarnaan selesai menempatkan slide diatas kertas tisu pada tempat datar, menetesi dengan bahan mounting yaitu kanada balsam dan tutup dengancover glasscegah jangan sampai terbentuk gelembung udara.
8) Membacaslidedengan mikroskop
Slide diperiksa di bawah mikroskop cahaya dengan perbesaran 400x. Preparat histopatologi dikirim ke laboratorium Patologi
Anatomi untuk dikonsultasikan dengan ahli patologi anatomi.
Gambaran kerusakan hepatosit tikus dilihat dengan melakukan
pengamatan sediaan histopatologi menggunakan mikroskop dengan
perbesaran 400x pada 5 lapangan pandang dimana setiap lapangan
pandang diamati berupa infiltrasi sel radang yang terjadi pada
hepatosit. Skala degenerasi bengkak keruh kemudian dihitung
✏1 Tabel 1.Skor penilaian derajat peradangan
Tingkat Perubahan Skor
Tidak ada hepatosit yang mengalami peradangan 0
<10% hepatosit yang mengalami peradangan 1
10–33% hepatosit yang mengalami peradangan 2
34–66% hepatosit yang mengalami peradangan 3
>66–100% hepatosit yang mengalami peradangan
K C
K K
C C
K K K K
Ekstrak B
K kstrak B Timbang berat badan tikus
K1 K2 K3 K4 K5
Tikus diberi perlakuan
1 K2 K3 4 5
ekok Cekok ekok` ekok Cekok
Aquades DMBA 30 mg/kgBB DMBA 30 mg/kgBB DMBA 30 mg/kgBB DMBA 30 mg/kgBB
Setelah 2 bulan
Timbang berat badan tikus
Adaptasi 7 hari
1 2 3 4 5
Aquades Aquades Ekstrak BMD 24 mg MD 48 mg E MD 96 mg
1x sehari 1x sehari 1x sehari 1x sehari 1x sehari
Tikus dianastesi kemudian dilakukan dekapitasi dan pembedahan
Lakukan laparotomi lalu hepar tikus diambil
Sampel hepar difiksasi dengan formalin 10%
Sampel hepar dikirim ke Laboratorium Patologi Anatomi Fakultas Kedokteran Universitas Lampung untuk pembuatan sediaan histopatologi
Pengamatan sediaan histopatologi dengan mikroskop
[image:46.612.95.508.87.642.2]Interpretasi hasil pengamatan
✓ ✓ G. Identifikasi Variabel dan Definisi Operasional Variabel
1. Identifikasi Variabel
a. Variabel independen adalah pemberian ekstrak mahkota dewa (Phaleria macrocarpa)
b. Variabel dependen adalah gambaran mikroskopis hepar
2. Definisi Operasional Variabel
Tabel 2.Definisi operasional variabel
Variabel Definisi Skala
Dosis ekstrak mahkota dewa
Gambar histopatologi hepar tikus
Dosis efektif mahkota dewa adalah 24 mg
• Kelompok I (kontrol negatif) = pemberian aquades
• Kelompok II (kontrol positif) = pemberian DMBA 30 mg/kgBB
• Kelompok III (perlakuan coba) = pemberian mahkota dewa dosis 24 mg + DMBA 30 mg/kgBB
• Kelompok IV (perlakuan coba) = pemberian mahkota dewa dosis 48 mg + DMBA 30 mg/kgBB
• Kelompok V (perlakuan coba) = pemberian mahkota dewa dosis 96 mg + DMBA 30 mg/kgBB
Gambaran kerusakan hepatosit tikus dilihat dengan melakukan pengamatan sediaan histopatologi menggunakan mikroskop dengan perbesaran 400x pada 5 lapangan pandang dimana setiap lapangan pandang diamati sel radang yang terjadi pada hepatosit
Kategorik
Numerik
H. Analisis Data
Analisis data penelitian diproses dengan program SPSS versi 20.0 for windows
1. Uji normalitas Data (p>0,05)
Pengujian normalitas data menggunakanShapiro Wilk test untuk mengetahui data berdistribusi normal atau tidak normal. Hasil uji normalitas ini untuk
menentukan analisis berikutnya, yaitu analisis parametrik bila data
berdistribusi normal atau non parametrik bila data tidak berdistribusi normal.
2. Uji Homogenitas data (p>0,05)
Pengujian homogenitas data menggunakan uji Levene’s untuk mengetahui
data homogen atau tidak homogen. Hasil uji homogenitas ini untuk
menentukan analisis berikutnya, yaitu analisis parametrik bila data homogen
atau non parametrik bila data tidak homogen.
3. Uji parametrik (One–Way ANOVA)
Untuk menguji perbedaan pengaruh kelompok I, kelompok II, kelompok III,
kelompok IV, kelompok V.
4. Uji non–parametrik (Kruskal Wallis)
Untuk menguji perbedaan pengaruh kelompok I, kelompok II, kelompok III,
kelompok IV, kelompok V dan merupakan uji alternatif dari One–Way ANOVA.
5. AnalisisPost Hoc
Bila pada ujiOne–Way ANOVAmenghasilkan nilai p<0,05. 6. UjiMann–Whitney Test
✖✗ I. Etika Penelitian
Implikasi etik pada hewan, pengelolaan binatang coba pada penelitian ini
mengikuti animal ethics. Hal yang perlu dilaksanakan sesuai dengan etik antara lain megikuti prinsip 3R dalam protokol penelitian, yaitu replacement, reduction, dan refinement (Ridwan, 2013). Replacement adalah keperluan memanfaatkan hewan percobaan sudah diperhitungkan secara seksama, baik dari pengalaman
terdahulu maupun literatur untuk menjawab pertanyaan penelitian dan tidak
dapat digantikan oleh mahluk hidup lain seperti sel atau biakan jaringan. Dalam
hal ini, peneliti tetap menggunakan hewan coba tikus putih (Rattus norvegicus) galur Spargue Dawley dan tidak digantikan dengan hewan coba lainnya. Reduction diartikan sebagai pemanfaatan hewan dalam penelitian sesedikit mungkin, tetapi tetap mendapatkan hasil yang optimal. Dalam penelitian ini,
peneliti menghitung jumlah minimum menggunakan rumus Frederer yaitu (n-1)
(t-1)>15, dengan n adalah jumlah hewan yang diperlukan dan t adalah jumlah
kelompok perlakuan. Refinement adalah memperlakukan hewan percobaan secara manusiawi (humane), memelihara hewan dengan baik, tidak menyakiti hewan, serta meminimalisasi perlakuan yang menyakitkan sehingga menjamin
kesejahteraan hewan coba sampai akhir penelitian. Pada dasarnya prinsip
refinement berarti membebaskan hewan coba dari beberapa kondisi. Yang pertama adalah bebas dari rasa lapar dan haus, dengan memberikan akses
makanan dan air minum yang sesuai dengan jumlah yang memadai baik jumlah
V. KESIMPULAN DAN SARAN
A. Kesimpulan
1. Pemberian ekstrak buah mahkota dewa (Phaleria macrocarpa) berpengaruh terhadap gambaran inflamasi hepar tikus putih yang diinduksi DMBA
2. Pemberian peningkatan dosis ekstrak buah mahkota dewa (Phaleria macrocarpa), 24 mg, 48 mg, dan 96 mg berpengaruh terhadap gambaran inflamasi hepar tikus putih yang diinduksi DMBA yaitu semakin
meningkatnya dosis dapat menghambat jumlah sel radang walaupun belum
bisa mencapai pada kondisi normal.
B. Saran
1. Peneliti lain disarankan untuk menguji lebih lanjut toksisitas dan efektivitas
pada ekstrak mahkota dewa
2. Peneliti lain disarankan untuk meneliti lebih lanjut tentang potensi zat–zat
✘ ✙ 3. Peneliti lain disarankan untuk meneliti lebih lanjut efek buah mahkota dewa
pada hepar dengan variabel lain, seperti makroskopis hepar
4. Peneliti lain disarankan untuk meneliti lebih lanjut efek buah mahkota dewa
DAFTAR PUSTAKA
Akhirunnisa DV. 2010. Efek hepatoprotektif ekstrak etanol 50% jamur lingzhi (Ganoderma lucidum) pada tikus jantan yang diinduksi parasetamol. Skripsi. Surakarta: Fakultas Farmasi Universitas Muhammadiyah Surakarta.
Amalina N. 2009.Uji toksisitas akut ekstrak valerian (Valeriana officinalis) terhadap hepar mencit BALB/C. Karya tulis ilmiah. Semarang: Fakultas Kedokteran Universitas Diponegoro.
Anshor T, dominius A, Irwanda, Imiawan MI. 2013. Supresi Ekspresi CYP1A1 dan CYP1A2 pada hepatocelluler carcinoma melalui potensi formula herbal terkombinasi Gynura procumbens dan kulit jeruk pontianak (Citrus nobilis var. Microcarpa) sebagai agen kemopreventif keganasan hepar. IMKU. 2(1): 1–11.
Arini S, Nurmawan D, Alfiani F, Hertiani T. 2003. Daya antioksidan dan kadar flavonoid hasil ekstraksi etanol–air daging buah mahkota dewa (Phaleria macrocarpa (Scheff.) Boerl.). Buletin Penalaran Mahasiswa UGM. 1(10): 2– 6.
Astuti S. 2008. Isoflavon kedelai dan potensinya sebagai penangkap radikal bebas. Jurnal Teknologi Industri dan Hasil Pertanian. 2(13): 126–36.
Cahyono JB. 2007. Obat inhibitor COX-2 dan penyakit kardiovaskuler. Deka Media. 1(20): 19–22.
Dahlan S. 2011. Statistik untuk kedokteran dan kesehatan. Jakarta: Salemba Medika. hlm. 102–11.
Dalimartha S. 2007. Atlas tumbuhan obat Jilid 3. Jakarta: Puspa Swara. hlm. 47-8.
Dewi MR. 2010. Pengaruh hepatoprotektor madu terhadap kerusakan histologis sel hepar mencit (Mus musculus) yang diberi perlakuan natrium siklamat. Skripsi. Surakarta: Universitas Sebelas Maret.
53 Ekawati RA. 2007. Potensi atioksidan daun salam (Eugenia polyantha Wight.) pada lingkungan agrobiofisik yang berbeda. Skripsi. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam IPB.
Fiqriyana MA. 2010. Pengaruh pemberian ekstrak Euchema spinom terhadap kadar glukosa dalam darah dan aktivitas superoksida dismutase (SOD) pada tikus terpapar multiple low doses streptozotocin (MLD-STZ). Skripsi. Malang: Fakultas Matematika dan Ilmu pengetahuan Alam Universitas Brawijaya.
Gao J, Lauer FT, Mitchaell LA, Burchiel SW. 2007. Microsomal epoxide hydralse is required for 7,12–dymethylbenz(a)anthracene (DMBA)–induced immunotoxicity in mice. Toxicol Science. 98(1):134–134.
Georgieva NV. 2005. Oxidative stress as a factor of disrupted ecological oxidative balance in biological systems–a review. Bulg.J.Vet.Med. 8(1): 1–11.
Hamid IS, Sugiyanto, Meiyanto E, Widyarini. 2009. Ekspresi CYP1A1 dan GSTµ hepatosit terinduksi 7,12-dimetilbenz(a)antrasena dan pengaruh pemberian ekstrak etanolik Gynura procumbers. Majalah Farmasi Indonesia. 20(4): 198–206.
He G, Karin M. 2011. NF-κB and STAT3 - key players in liver inflammation and cancer. Cell research. 21(1): 159-68.
Hendra R, Ahmad S, Sukari A, Shukor MY, Oskoueian E. 2011. Flavonoid analyses and antimicrobial activity of various parts of Phaleria macrocarpa (Scheff.) Boerl fruit. International Journal of Molecular Science. 12(6): 3422-31.
Hidayat A, Christijani W, Marianti A. 2013. Pengaruh vitamin E terhadap kadar SGPT dan SGOT tikus putih galur wistar yang dipapar timbal. Unnes Journal of Life Science. 2(1): 110–15.
Kasolo JN, Bimeya GS, Ojok L, Ochieng J, Okwal-okeng JW. 2010. Phytochemicals and uses of Moringa oleifera leaves in Ugandan rural communities. Journal of Medical Plant Research. 4(9): 753-7.
Kawasaki T, Igarashi K, Koeda T, Sugimoto K, Nakagawa K, Hayashi S, Yamaji R, Inui H, Fukusato T, Yamanouchi T. 2009. Rats fed fructosed enriched diets have charactheristies of non-alcoholic hepatic steatosis. The journal of nutrition. 11(139): 2067-71.
Kumar V, Cotran RS, Robbins SL. 2007. Robbins buku ajar patologi Edisi ke–7. Jakarta: EGC. hlm. 664-5.
Lavenia A. 2010. Penghambatan peroksidasi lipid oleh ekstrak kulit batang mahoni (Swietenia macrophylla King) pada tikus hiperurisemia. Skripsi. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam IPB.
Lisdawati V. 2009. Kajian terhadap prospek pengebangan bahan bioaktif buah mahkota dewa (Phaleria macrocarpa) sebagai kandidiat new chemical entity (NCE) untuk pengobatan kanker (sitostatiska). Buletin Penelitian Kesehatan. 1(37): 24-34.
Lu JJ, Bao JL, Chen XP, Huang M, Wang YT. 2012. Alkaloids isolated from natural herbs as the anticancer agents. Hindawi Publishing Corporation. 10(12): 1-12.
Manoharan S, Muneeswaran M, Baskaran N. 2010. Chemopreventive efficacy of berberine 7,12-dimethylbenz[a]anthracene (DMBA) induced skin carcinogenesis in Swiss albino mice. Pharmacope Foundation. 1(4): 521-9. Meiyanto E, Diah AP, Adhi, Darma AP, Ikawati M. 2011. Potensi kemopreventif
ekstrak etanolik kulit jeruk keprok (Citrus reticulata) pada karsinogenesis sel hepar tikus galur Sprague dawley terinduksi DMBA. Pharmacon. 1(12): 9-13.
Montano C, Moron BE, Guerrero P,Lazaro L. 2011. A review on the dietary flavonoid kaempferol. Bentham science.11(4): 298–344.
Muljono DH. 2004. Keterlibatan mitokondria pada penyakit hati. Jakarta: Lembaga Biologi Molekul Eijkman. hlm. 145–64.
Nair S, Varalakshmi KN. 2011. Anticancer, cytotoxic potential of Moringa oleifera extracts on HeLa cell line. Journal of Natural Pharmaceuticals. 2(3): 138-42.
Oktaviana KT. 2012. Pengaruh ekstrak metanol daun kelor (Moringa oleifera) tehadap penghambatan aktivasi NF-kB pada hepar tikus wistar model hepatocellular carcinoma (HCC) yang diinduksi DMBA. Faculty of Medicine Brawijaya University. 2(12): 14-21.
Paliwal R, Sharma V, Pracheta, Sharma SH. 2011. Hepatoprotective and antioxidant potential of Moringa oleifera pods against DMBA-induced hepatocarcinogenesis in male mice. International journal of drug development of research. 4(9): 753-7.
55 Parhizkar S, Zainudin CZ, Dollah MA. 2013. Effect of Phaleria macrocarpa on
sexual function of rats. Avicenna Journal of Phytomedicine: 4(3): 371-7. Rahayu WP. 2012. Aktivitas antiproliferatif jintan hitam (Nigell sativa) pada sel
paru yang diindksi 7,12–dimetilbenz[a]antrasena. Makara Kesehatan. 2(16): 51–56.
Reanmongkol W, Wattanapiromsakul C. 2007. Evaluation of the analgesic, antipyretic and anti-inflammatory activities of the extracts from the pericarp of Garcinia mangostana Linn. in experimental animals. Songklanakarin journal of science and technology. 30(6): 739-45.
Ridwan E. 2013. Etika pemanfaatan hewan percobaan dalam penelitian kesehatan. Artikel pengmbangan pendidikan keprofesian (P2KB). 63(3): 112–16.
Rohyami Y. 2008. Penentuan kandungan flavonoid dari ekstrak metanol daging buah mahkota dewa (Phaleria macrocarpa Scheff Boerl). Direktorat Penelitian dan Pengabdian Masyarakat (DPPM). 1(5): 1–16.
Sari W. 2008. Care yourself: hepatitis. Jakarta: Penebar plus. hlm. 27–28.
Septiawati T. 2008. Daya hambat ekstrak etanol buah mahkota dewa terhadap aktivitas α-glukosidase secara in vitro. Skripsi. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor.
Sharma V, Paliwal R, Janmeda P, Sharma S. 2012. Chemopreventive efficacy of Moringa oleifera pods against 7,12–dimethylbenz[a]anthracene induced hepatic carcinogenesis in mice. Asian Pacific Journal of Cancer Prevention. 13: 2563-9.
Simanjuntak P. 2008. Identifikasi senyawa kimia dalam buah mahkota dewa (Phaleria macrocarpa) thymelaceae. Jurnal Ilmu Kefarmasian Indonesia. 1(6): 23-8.
Situmorang TS. 2010. Pengaruh pemberian jus pepaya (Carica papaya L.) sebagai hepatoprotektor terhadap hepar mencit yang dipapar parasetamol. Skripsi. Surakarta: Fakultas Kedokteran Universitas Sebelas Maret.
Sreelatha S, Padma PR. 2009. Antioxidant activity and total phenolic content of Moringa oleifera leaves in two stages of maturity. Plant foods for human nutrition. 64(4): 303-11.
Wahyuningsih MHS. 2010. Potensi pengembangan obat bahan alam Indonesia untuk penyakit kanker: tantangan dan harapan. Yogyakarta: Universitas Gajah Mada. hlm. 5.
Wijayakusuma H. 2008. Atasi kanker dengan tanaman obat. Jakarta: Niaga Swadaya. hlm. 50.
Winarsi H. 2007. Antioksidan alami dan radikal bebas. Yogyakarta: Kanisius. hlm. 13–14.
Xiaoyue P, Hussain FN, Iqbal J, Feuerman M, Hussain MM. 2007. Inhibiting proteasomal degradation of microsomal trigliseride transfer protein prevents CCl4–induced steatosis. JBC papers. 282(23): 17078–89.