2
ABSTRAK
HERLIN EKA PRATIWI. Optimasi Kondisi Pengujian Kromatografi Cair Kinerja Tinggi pada Penetapan Kadar Bahan Aktif Obat Sakit Kepala. Dibimbing oleh RUDI HERYANTO dan YOANNE ECLEXIA N.S.
Optimasi kondisi pengujian kromatografi cair kinerja tinggi untuk penetapan kadar parasetamol dan kafein sebagai zat aktif dalam obat sakit kepala telah dilakukan dengan tujuan menetapkan kondisi optimum dan meningkatkan efisiensi waktu pengujian. Metode penelitian menggunakan metodologi permukaan respons dengan 2 peubah bebas, yaitu konsentrasi fase gerak dan laju alir, serta 3 taraf, yaitu 10, 15, dan 20% asetonitriluntuk konsentrasi fase gerak dan 0.5, 1.0, dan 1.5 mL/menit untuk laju alir. Kondisi optimum diperoleh pada konsentrasi asetonitril 15% dan laju alir 1.5 mL/menit namun kondisi yang terpilih adalah asetonitril 15% dan laju alir 1.0 mL/menit dengan pertimbangan ekonomis dan kesesuaian sistem. Hasil optimasi kemudian divalidasi untuk memastikan bahwa penetapan dengan metode tersebut dapat dipercaya. Parameter validasi meliputi uji plasebo, batas deteksi, batas kuantitasi, kecermatan, kesaksamaan, linearitas, ketangguhan, dan kekuatan metode. Dari hasil validasi dapat disimpulkan bahwa metode terpilih memenuhi kriteria untuk seluruh parameter dan dapat digunakan untuk analisis.
ABSTRACT
HERLIN EKA PRATIWI. Optimization of High Performance Liquid Chromatography Analysis Condition to Determine Active Substance in a Headache Medicine. Supervised by RUDY HERYANTO and YOANNE ECLEXIA NS.
Optimization of high performance liquid chromatography analysis condition for paracetamol and caffeine concentration determination as active substances in a headache medicine was performed to obtain the optimum condition and to increase the efficiency of analysis time. The research method used response surface methodology with 2 independent variables and 3 levels of analysis. The independent variables were concentrations of mobile phase and flow rate, the levels were 10, 15, and 20% of acetonitrile as the mobile phase and 0.5, 1.0, and 1.5 mL/min for the flow rate. Optimum condition was obtained in 15% concentration of acetonitrile and 1.5 mL/min of flow rate, but the selected condition is a 15% concentration of acetonitrile and 1.0 mL/min of flow rate because of the system suitability and economic reasons. The selected condition was then validated to ensure that the method could give reliable results. Validation parameters consist of placebo study, limit of detection and quantitation, accuracy, precision, linearity, ruggedness, and robustness. In conclusion, the selected method could fulfill the criteria for all parameters and could be used for analysis.
PENDAHULUAN
Obat pereda sakit kepala dengan 2 kandungan zat aktif, parasetamol dan kafein, telah diproduksi oleh perusahaan farmasi dengan memenuhi cara pembuatan obat yang baik (CPOB) yang dipersyaratkan oleh badan pengawasan obat dan makanan (BPOM). Parasetamol memiliki sifat analgesik yang efektif untuk menghilangkan rasa nyeri ringan dan mengobati sakit kepala, sedangkan kafein berfungsi sebagai stimulan (ASHSP 2001).
Obat pereda sakit kepala tablet diproduksi dalam jumlah yang semakin bertambah seiring dengan meningkatnya permintaan konsumen. Penambahan jumlah produksi berdampak terhadap penambahan jumlah analisis yang dilakukan sebagai jaminan kualitas produk. Oleh karena itu, diperlukan metode analisis yang cepat dan tepat untuk memenuhi keperluan tersebut. Metode penetapan kadar parasetamol dan kafein dalam obat sakit kepala menggunakan kromatografi cair kinerja tinggi (KCKT) hasil pengembangan in house oleh RnD menggunakan fase gerak asetonitril 10%, fase diam RP-18 125 × 4 mm 5µm, waktu alir 1.0 mL/menit dapat memisahkan parasetamol dan kafein dengan resolusi 13.2, waktu retensi parasetamol ±3.2 menit, kafein ±9.1 menit, dan lama waktu pengujian ±10 menit (Scientist 2003). Penelitian ini dimaksudkan untuk mengoptimasi kondisi pengujian tersebut sehingga dapat mempersingkat waktu analisis untuk mencapai efisiensi pengujian.
Modifikasi dengan melakukan perubahan komposisi fase gerak dan waktu alir. Kondisi optimum ditentukan menggunakan metodologi permukaan respons. Kondisi terpilih kemudian divalidasi untuk memastikan bahwa metode memberikan hasil uji yang terpercaya dan digunakan untuk analisis rutin. Parameter validasi meliputi batas deteksi, batas kuantitasi, kecermatan, kesaksamaan, linearitas, ketangguhan, dan kekuatan metode.
TINJAUAN PUSTAKA
Tablet Obat Sakit Kepala
Tablet adalah sediaan padat yang mengandung bahan obat dengan atau tanpa bahan pengisi. Berdasarkan metode pembuatannya, tablet dapat digolongkan sebagai tablet cetak dan kempa. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan baja. Tablet cetak dibuat dengan cara menekan
massa serbuk lembap pada tekanan rendah dalam lubang cetakan (Depkes RI 1995).
Bahan yang digunakan dalam pembuatan obat terdiri atas bahan utama (zat aktif) dan bahan tambahan (zat aditif). Bahan utama adalah zat kimia yang berfungsi menyembuhkan penyakit yang dialami oleh penderita, sedangkan bahan tambahan adalah zat kimia yang berfungsi menambah bobot yang diinginkan, mempermudah proses pencetakan, atau mempermudah proses pengikatan pada saat semua bahan obat tercampur. Obat sakit kepala tablet diproduksi dengan sediaan padat berbentuk tablet bundar berwarna putih, tidak berbau, berasa pahit, diameter 13 mm, dan memiliki kandungan bahan utama 500 mg parasetamol dan 30 mg kafein. Bahan tambahan terdiri atas larutan natrium benzoat sebagai pengikat pada proses granulasi basah sekaligus pengawet, bahan pengisi yang terdiri atas Primojel dan Kolidon, sedangkan fase luar terdiri atas Mgstearat dan Aerosil 200 yang berfungsi memudahkan proses pencetakan.
Parasetamol
Parasetamol atau dikenal sebagai asetaminofen(Gambar 1) merupakan zat aktif berbentuk serbuk hablur putih dan tidak berbau dengan rumus kimia C8H9NO2 dan bobot
molekul 151.16 g/mol. Parasetamol larut di dalam air mendidih dan NaOH 1 N, serta mudah larut dalam etanol. Suhu leburnya 168– 172 oC, sisa pijar ≤0.1%, kadar air ≤0.5%, dan logam berat ≤0.001% (Depkes RI 1995).
Parasetamol sangat stabil di dalam air dan memiliki kestabilan maksimum pada kisaran pH 5–7 (Connors et al. 1986). Parasetamol merupakan senyawa turunan dari p-aminofenol yang memiliki sifat analgesik dan antipiretik. Parasetamol memberi efek analgesik sementara, tidak memiliki efek antirematik, efektif menghilangkan rasa nyeri ringan, dan mengobati sakit kepala. Parasetamol ditemukan dapat dikombinasikan dengan kafein, aspirin, salisilamida, danopiat(ASHSP 2001).
PENDAHULUAN
Obat pereda sakit kepala dengan 2 kandungan zat aktif, parasetamol dan kafein, telah diproduksi oleh perusahaan farmasi dengan memenuhi cara pembuatan obat yang baik (CPOB) yang dipersyaratkan oleh badan pengawasan obat dan makanan (BPOM). Parasetamol memiliki sifat analgesik yang efektif untuk menghilangkan rasa nyeri ringan dan mengobati sakit kepala, sedangkan kafein berfungsi sebagai stimulan (ASHSP 2001).
Obat pereda sakit kepala tablet diproduksi dalam jumlah yang semakin bertambah seiring dengan meningkatnya permintaan konsumen. Penambahan jumlah produksi berdampak terhadap penambahan jumlah analisis yang dilakukan sebagai jaminan kualitas produk. Oleh karena itu, diperlukan metode analisis yang cepat dan tepat untuk memenuhi keperluan tersebut. Metode penetapan kadar parasetamol dan kafein dalam obat sakit kepala menggunakan kromatografi cair kinerja tinggi (KCKT) hasil pengembangan in house oleh RnD menggunakan fase gerak asetonitril 10%, fase diam RP-18 125 × 4 mm 5µm, waktu alir 1.0 mL/menit dapat memisahkan parasetamol dan kafein dengan resolusi 13.2, waktu retensi parasetamol ±3.2 menit, kafein ±9.1 menit, dan lama waktu pengujian ±10 menit (Scientist 2003). Penelitian ini dimaksudkan untuk mengoptimasi kondisi pengujian tersebut sehingga dapat mempersingkat waktu analisis untuk mencapai efisiensi pengujian.
Modifikasi dengan melakukan perubahan komposisi fase gerak dan waktu alir. Kondisi optimum ditentukan menggunakan metodologi permukaan respons. Kondisi terpilih kemudian divalidasi untuk memastikan bahwa metode memberikan hasil uji yang terpercaya dan digunakan untuk analisis rutin. Parameter validasi meliputi batas deteksi, batas kuantitasi, kecermatan, kesaksamaan, linearitas, ketangguhan, dan kekuatan metode.
TINJAUAN PUSTAKA
Tablet Obat Sakit Kepala
Tablet adalah sediaan padat yang mengandung bahan obat dengan atau tanpa bahan pengisi. Berdasarkan metode pembuatannya, tablet dapat digolongkan sebagai tablet cetak dan kempa. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan baja. Tablet cetak dibuat dengan cara menekan
massa serbuk lembap pada tekanan rendah dalam lubang cetakan (Depkes RI 1995).
Bahan yang digunakan dalam pembuatan obat terdiri atas bahan utama (zat aktif) dan bahan tambahan (zat aditif). Bahan utama adalah zat kimia yang berfungsi menyembuhkan penyakit yang dialami oleh penderita, sedangkan bahan tambahan adalah zat kimia yang berfungsi menambah bobot yang diinginkan, mempermudah proses pencetakan, atau mempermudah proses pengikatan pada saat semua bahan obat tercampur. Obat sakit kepala tablet diproduksi dengan sediaan padat berbentuk tablet bundar berwarna putih, tidak berbau, berasa pahit, diameter 13 mm, dan memiliki kandungan bahan utama 500 mg parasetamol dan 30 mg kafein. Bahan tambahan terdiri atas larutan natrium benzoat sebagai pengikat pada proses granulasi basah sekaligus pengawet, bahan pengisi yang terdiri atas Primojel dan Kolidon, sedangkan fase luar terdiri atas Mgstearat dan Aerosil 200 yang berfungsi memudahkan proses pencetakan.
Parasetamol
Parasetamol atau dikenal sebagai asetaminofen(Gambar 1) merupakan zat aktif berbentuk serbuk hablur putih dan tidak berbau dengan rumus kimia C8H9NO2 dan bobot
molekul 151.16 g/mol. Parasetamol larut di dalam air mendidih dan NaOH 1 N, serta mudah larut dalam etanol. Suhu leburnya 168– 172 oC, sisa pijar ≤0.1%, kadar air ≤0.5%, dan logam berat ≤0.001% (Depkes RI 1995).
Parasetamol sangat stabil di dalam air dan memiliki kestabilan maksimum pada kisaran pH 5–7 (Connors et al. 1986). Parasetamol merupakan senyawa turunan dari p-aminofenol yang memiliki sifat analgesik dan antipiretik. Parasetamol memberi efek analgesik sementara, tidak memiliki efek antirematik, efektif menghilangkan rasa nyeri ringan, dan mengobati sakit kepala. Parasetamol ditemukan dapat dikombinasikan dengan kafein, aspirin, salisilamida, danopiat(ASHSP 2001).
2
Kafein
Kafein (Gambar 2) berbentuk serbuk halus mengilat, biasanya menggumpal, tidak berbau, dan berasa pahit. Kafein agak sukar larut di dalam air dan sukar larut di dalam etanol. Kafein memiliki rumus kimia C8H10N4O2,
bobot molekul 194.19 g/mol, sisa pijar ≤0.1%, suhu lebur 235–239 oC, susut pengeringan
≤0.5%, dan logam berat ≤0.001% (Depkes RI 1995).
Gambar 2 Rumus struktur kafein.
Kromatografi Cair Kinerja Tinggi
Pada tahun 1903 Tswett menemukan teknik kromatografi, sebagai cara untuk menguraikan suatu campuran. Dalam kromatografi, komponen terdistribusi dalam 2 fase. Transfer massa antara fase gerak dan fase diam terjadi bila molekul-molekul campuran terjerap pada permukaan partikel atau terserap di dalam pori-pori partikel atau terbagi dalam sejumlah cairan yang terikat pada permukaan atau di dalam pori (Khopkar 2003).
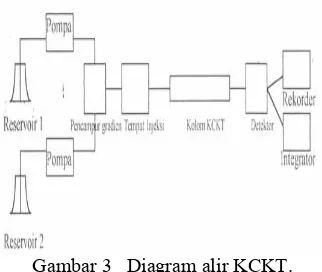
Komponen KCKT (Gambar 3) terdiri atas pompa bertekanan tinggi yang harus tahan terhadap semua jenis pelarut dan mampu mengantarkan aliran terukur 0.01–1.0 mL/menit (Zamri 2008). Injektor merupakan bagian untuk memasukkan contoh yang akan dianalisis melewati sistem. Kolom adalah jantung kromatografi, berhasil atau tidaknya analisis bergantung pada pemilihan kolom dan kondisi percobaan yang sesuai. Kolom dapat berupa kaca atau baja nir karat, pengisi kolom seperti partikel pellicular, yaitu butiran kaca yang dilapisi materi berpori seperti silika gel, alumina, atau penukar ion (Khopkar 2003). Detektor dibutuhkan untuk mendeteksi adanya komponen contoh dan menghitung kadarnya (Putra 2004). Detektor yang digunakan bergantung pada contoh yang dipisahkan, detektor UV lazim digunakan untuk analisis bahan organik bergugus fungsi.
Gambar 3 Diagram alir KCKT.
KCKT merupakan metode kromatografi cair yang paling banyak digunakan dalam analisis suatu senyawa, karena kompatibel untuk sebagian besar senyawa terutama senyawa dalam campuran yang konsentrasinya kecil dan tekanan uapnya rendah (Christinopa 2010). Menurut Khopkar (2003), penggunaan KCKT efisien, sangat selektif, memerlukan contoh dalam jumlah sedikit, serta dapat digunakan dalam analisis kuantitatif. Analisis didasarkan pada waktu retensi, yaitu waktu yang dibutuhkan untuk mengalirkan zat terlarut dari permulaan kolom sampai detektor.
Zat yang berinteraksi kuat dengan fase diam akan memiliki waktu retensi yang lama, demikian pula untuk sebaliknya. Waktu retensi tiap senyawa adalah khas pada kondisi kerja tertentu, sehingga dapat digunakan sebagai parameter kualitatif. Untuk kepentingan analisis kuantitatif, diperlukan data luas atau ketinggian puncak yang ditentukan oleh konsentrasi zat terlarut. Luas puncak pada kurva elusi dipengaruhi proses perpindahan massa, yaitu difusi Eddy, difusi longitudinal, dan transfer massa tidak seimbang. Parameter yang menunjukkan berlangsungnya proses adalah laju aliran, ukuran partikel, laju difusi, dan ketebalan stasioner (Khopkar 2003).
Metodologi Permukaan Respons
statistika yang digunakan untuk pemodelan dan analisis permasalahan pada respons yang dipengaruhi oleh beberapa peubah dan bertujuan memperoleh kondisi optimum.
Menurut Bezerra et al. (2009), untuk memperkirakan respons dari percobaan tidak dapat digunakan fungsi linear, tetapi kuadrat permukaan respons, seperti faktorial 3 tingkat, Box Behnken, komposit pusat, dan desain Doehlert. Kecocokan model orde dua central composite design (CCD) atau rancangan komposit pusat (RKP) banyak digunakan. RKP pertama kali diperkenalkan oleh Box dan Wilson.
Validasi Metode Analisis
Menurut Harmita (2004), ada beberapa parameter dalam validasi metode analisis yang dijelaskan di bawah ini :
Kecermatan
Kecermatan menunjukkan kedekatan hasil analisis dengan kadar analit sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan hasil analisis sangat bergantung pada sebaran galat sistematik di dalam keseluruhan tahapan analisis. Kecermatan ditentukan dengan 2 cara, yaitu metode simulasi (spiked-placebo recovery) dan metode penambahan baku (standard addition method). Dalam metode simulasi, sejumlah analit bahan murni sebagai senyawa pembanding kimia baku ditambahkan ke dalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan.
Dalam metode penambahan baku, contoh dianalisis lalu sejumlah tertentu analit yang diperiksa ditambahkan ke dalam contoh, dihomogenkan, kemudian dianalisis kembali. Selisih kedua hasil dibandingkan dengan kadar sebenarnya. Berdasarkan kedua metode tersebut, persen perolehan kembali dinyatakan sebagai nisbah antara hasil yang diperoleh dan hasil sebenarnya.
Kesaksamaan
Kesaksamaan menunjukkan kesesuaian antara hasil-hasil uji berdasarkan penyebaran hasil dari nilai rerata jika prosedur diterapkan secara berulang pada contoh yang diambil dari campuran yang homogen. Kriteria saksama diberikan jika metode memberikan simpangan baku relatif (SBR) atau koefisien variasi (KV) ≤2%. Akan tetapi, kriteria ini sangat fleksibel
bergantung pada konsentrasi analit yang diperiksa, jumlah contoh, dan kondisi laboratorium.
Percobaan kesaksamaan dilakukan terhadap sedikitnya 6 ulangan contoh yang diambil dari campuran contoh dengan matriks yang homogen. Sebaiknya kesaksamaan ditentukan terhadap contoh sebenarnya, yaitu berupa campuran dengan bahan pembawa sediaan farmasi (plasebo), untuk melihat pengaruh matriks pembawa terhadap kesaksamaan ini.
Selektivitas
Selektivitas adalah kemampuan metode untuk mengukur zat tertentusecara cermat dan saksama dengan adanya komponen lain yang mungkin ada dalam matriks contoh. Selektivitas sering kali dapat dinyatakan sebagai derajat penyimpangan(degree of bias).
Selektivitas metode ditentukan dengan membandingkan hasil analisis contoh yang mengandung cemaran, hasil urai, senyawa sejenis, senyawa asing, atau pembawa plasebo dengan hasil analisis contoh tanpa penambahan bahan. Penyimpangan hasil, jika ada, merupakan selisih dari hasil uji keduanya. Pada metode analisis yang melibatkan kromatografi, selektivitas ditentukan melalui perhitungan daya resolusinya (r).
Linearitas
Linearitas adalah kemampuan metode analisis memberikan respons secara langsung atau dengan bantuan transformasi matematika secaraa baik dan proporsional terhadap konsentrasi analit dalam contoh. Sebagai parameter adanya hubungan linear digunakan koefisien korelasi r pada analisis regresi linear
y = a + bx. Hubungan linear yang ideal dicapai jika nilai b = 0 dan r = +1 atau –1 bergantung pada arah garis, sedangkan nilai a
menunjukkan kepekaan analisis, terutama instrumen yang digunakan.
Batas Deteksi dan Batas Kuantitasi
4
Ketangguhan (Ruggedness)
Ketangguhan metode adalah tingkat ketertiruan hasil uji yang diperoleh dari analisis contoh yang sama dalam berbagai kondisi uji normal seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu, dan hari yang berbeda. Ketangguhan metode ditentukan dengan menganalisis contoh yang homogen dari laboratorium yang berbeda oleh analis yang berbeda menggunakan kondisi kerja dan lingkungan yang berbeda, tetapi dengan prosedur dan parameter uji yang sama.
Kekuatan (Robustness)
Kekuatan metode dapat divalidasi dengan perubahan metodologi yang kecil untuk mengevaluasi respons analitik dan efek presisi dan akurasi. Perubahan yang dibutuhkan untuk menunjukkan kekuatan prosedur KCKT mencakup perubahan komposisi organik fase gerak (1%), pH fase gerak (±0.2 unit), laju alir, dan suhu kolom (±2–3ºC).
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan selama penelitian adalah obat pereda sakit kepala tablet dengan kandungan zat aktif parasetamol 500 mg dan kafein 30 mg, standar parasetamol (Europe CW0910509, 99.622%), standar kafein (USA200910077, 100.7%), asetonitril Chrom AR®
(Mallinckrodt Chemical, 100%), dan air distilasi.
Peralatan yang digunakan selama penelitian adalah 3 macam KCKT (Waters 1525, Agilent 1200 series, dan Waters Aliance e2695) digunakan untuk parameter ketangguhan metode. Selain itu, digunakan perangkat lunak Design Expert 7.0, injektor Rheodyne 20 L
sample loop, kolom LichroCART RP–18 (125 × 4 mm, 5µm), neraca analitik (Mettler Toledo, MT XS205 DU), membran filter (millipore) 0.45 m, Ultrasonic (104H), labu takar Iwaki, pipet volumetrik, serta peralatan kaca lainnya.
Metode Penelitian
Metode penelitian ini dilakukan untuk memodifikasi metode pengujian KCKT pada penetapan kadar parasetamol dan kafein dalam obat sakit kepala (Lampiran 1). Parameter kondisi KCKT sebelum modifikasi diberikan pada Tabel 1. Modifikasi dilakukan terhadap
komposisi fase gerak dan laju alir, sedangkan parameter yang lainnya dibuat tetap.
Tabel 1 Parameter kondisi KCKT sebelum modifikasi
Parameter Sebelum optimasi Kolom Lichocart RP-18 (125 × 4
mm, 5µm) Detektor UV, 270 nm Laju alir 1.0 mL/mnt Loop injector 20 µL Pelarut dan fase gerak
Asetonitril:air(10:90)
Rancangan Percobaan
Metode RSM digunakan untuk menentukan kondisi optimum penetapan kadar parasetamol dan kafein dalam tablet sakit kepala dengan 2 faktor sebagai peubah bebas, yaitu konsentrasi fase gerak (%v/v) dan laju alir (mL/menit).Respons yang diamati adalah waktu retensi (menit) dan resolusi. Percobaan dirancang dalam bentuk RKP dan level terkode disajikan pada Tabel 2 dan 3.
Tabel 2 Perlakuan terkode penetapan kadar parasetamol dan kafein dalam obat sakit kepala
Perlakuan Perlakuan terkode
-1 0 1
Fase gerak (%) 10 15 20
Laju alir (mL/menit)
0.5 1.0 2.5
Tabel 3 Rancangan komposit pusat (RKP) dengan 2 peubah bebas
Metode tersebut digunakan untuk mengamati pengaruh konsentrasi fase gerak dan laju alir terhadap waktu retensi dan resolusi dari 2 zat aktif, yaitu parasetamol dan kafein. Untuk melihat pengaruh tersebut digunakan persamaan regresi
No. Konsentrasi Fase gerak (%)
Laju alir (mL/menit)
1 10 1.0
2 20 1.0
3 15 0.5
4 15 1.0
5 15 1.0
6 15 1.5
7 15 1.0
8 20 1.5
9 10 0.5
10 10 1.5
11 15 1.0
12 15 1.0
4
Ketangguhan (Ruggedness)
Ketangguhan metode adalah tingkat ketertiruan hasil uji yang diperoleh dari analisis contoh yang sama dalam berbagai kondisi uji normal seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu, dan hari yang berbeda. Ketangguhan metode ditentukan dengan menganalisis contoh yang homogen dari laboratorium yang berbeda oleh analis yang berbeda menggunakan kondisi kerja dan lingkungan yang berbeda, tetapi dengan prosedur dan parameter uji yang sama.
Kekuatan (Robustness)
Kekuatan metode dapat divalidasi dengan perubahan metodologi yang kecil untuk mengevaluasi respons analitik dan efek presisi dan akurasi. Perubahan yang dibutuhkan untuk menunjukkan kekuatan prosedur KCKT mencakup perubahan komposisi organik fase gerak (1%), pH fase gerak (±0.2 unit), laju alir, dan suhu kolom (±2–3ºC).
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan selama penelitian adalah obat pereda sakit kepala tablet dengan kandungan zat aktif parasetamol 500 mg dan kafein 30 mg, standar parasetamol (Europe CW0910509, 99.622%), standar kafein (USA200910077, 100.7%), asetonitril Chrom AR®
(Mallinckrodt Chemical, 100%), dan air distilasi.
Peralatan yang digunakan selama penelitian adalah 3 macam KCKT (Waters 1525, Agilent 1200 series, dan Waters Aliance e2695) digunakan untuk parameter ketangguhan metode. Selain itu, digunakan perangkat lunak Design Expert 7.0, injektor Rheodyne 20 L
sample loop, kolom LichroCART RP–18 (125 × 4 mm, 5µm), neraca analitik (Mettler Toledo, MT XS205 DU), membran filter (millipore) 0.45 m, Ultrasonic (104H), labu takar Iwaki, pipet volumetrik, serta peralatan kaca lainnya.
Metode Penelitian
Metode penelitian ini dilakukan untuk memodifikasi metode pengujian KCKT pada penetapan kadar parasetamol dan kafein dalam obat sakit kepala (Lampiran 1). Parameter kondisi KCKT sebelum modifikasi diberikan pada Tabel 1. Modifikasi dilakukan terhadap
komposisi fase gerak dan laju alir, sedangkan parameter yang lainnya dibuat tetap.
Tabel 1 Parameter kondisi KCKT sebelum modifikasi
Parameter Sebelum optimasi Kolom Lichocart RP-18 (125 × 4
mm, 5µm) Detektor UV, 270 nm Laju alir 1.0 mL/mnt Loop injector 20 µL Pelarut dan fase gerak
Asetonitril:air(10:90)
Rancangan Percobaan
Metode RSM digunakan untuk menentukan kondisi optimum penetapan kadar parasetamol dan kafein dalam tablet sakit kepala dengan 2 faktor sebagai peubah bebas, yaitu konsentrasi fase gerak (%v/v) dan laju alir (mL/menit).Respons yang diamati adalah waktu retensi (menit) dan resolusi. Percobaan dirancang dalam bentuk RKP dan level terkode disajikan pada Tabel 2 dan 3.
Tabel 2 Perlakuan terkode penetapan kadar parasetamol dan kafein dalam obat sakit kepala
Perlakuan Perlakuan terkode
-1 0 1
Fase gerak (%) 10 15 20
Laju alir (mL/menit)
0.5 1.0 2.5
Tabel 3 Rancangan komposit pusat (RKP) dengan 2 peubah bebas
Metode tersebut digunakan untuk mengamati pengaruh konsentrasi fase gerak dan laju alir terhadap waktu retensi dan resolusi dari 2 zat aktif, yaitu parasetamol dan kafein. Untuk melihat pengaruh tersebut digunakan persamaan regresi
No. Konsentrasi Fase gerak (%)
Laju alir (mL/menit)
1 10 1.0
2 20 1.0
3 15 0.5
4 15 1.0
5 15 1.0
6 15 1.5
7 15 1.0
8 20 1.5
9 10 0.5
10 10 1.5
11 15 1.0
12 15 1.0
Dengan y adalah peubah respons yang diukur, yaitu waktu retensi parasetamol, waktu retensi kafein, dan resolusi. β adalah tetapan linear kuadratik, x adalah peubah bebas, yaitu fase gerak dan laju alir, dan ε adalah sisa.
Preparasi Fase Gerak, Standar, dan Contoh
Pembuatan fase gerak dilakukan dengan cara mencampurkan pelarut asetonitril:air (sesuai nisbah yang diinginkan, yaitu asetonitril 10, 15, dan 20%). Campuran dihomogenkan dan disaring dengan membran filter PTFE (millipore) 0.45 m lalu dihilangkan gelembungnya.
Untuk pembuatan standar, sebanyak 500 mg standar parasetamol dan 30 mg kafein ditimbang saksama, dilarutkan dalam fase gerak dengan komposisi terpilih hingga 50 mL (A). Labu takar 10 mL disiapkan kemudian dipipet 1.0 mL larutan A dimasukkan ke dalam labu tersebut dan ditera dengan pelarut. Dipipet 1.0 mL lagi ke dalam labu takar 10 mL, diperoleh larutan parasetamol 100 ppm dan kafein 6 ppm.
Sebanyak 10 buah tablet ditimbang dan ditentukan nilai rerata bobotnya kemudian digerus hingga halus dan tercampur homogen. Ditimbang setara bobot 1 tablet (digunakan bobot rerata 10 tablet) kemudian dimasukkan ke dalam labu takar 100 mL dan dilarutkan dengan fase gerak komposisi terpilih (larutan B). Contoh diberi perlakuan seperti standar, yakni pengenceran 100 kali. Konsentrasi larutan contoh parasetamol 100 ppm dan kafein 6 ppm.
Uji Kesesuaian Sistem
Larutan standar parasetamol konsentrasi 100 ppm dan standar kafein 6 ppm diinjeksikan sejumlah 20 L melalui injektor ke dalam KCKT sebanyak 5 kali ulangan. Digunakan kecepatan alir hasil optimasi dan detektor diatur pada 270 nm. Diperoleh kromatogram untuk tiap injeksi yang akan digunakan untuk menentukan kadar keterulangan penyuntikan larutan baku, yang dinyatakan dalam SBR atau KV, waktu retensi, luas puncak, tinggi puncak, dan tailing factor.
Validasi Metode Penetapan Kadar
Studi Plasebo
Studi plasebo bertujuan melihat keberadaan gangguan yang berasal dari plasebo pada saat pengukuran kadar zat aktif dan dilakukan secara duplo. Plasebo dibuat dengan cara melarutkan gelatin E-200 dalam air panas hingga membentuk larutan. Kemudian ditambahkan Primogel, LHPC LH-11, natrium benzoat, dan diaduk hingga homogen lalu dikeringkan pada suhu 50 oC, dari plasebo tersebut ditimbang 120 mg ke dalam labu 50 mL dan selanjutnya diberikan perlakuan yang sama seperti preparasi contoh.
Batas Deteksi, Batas Kuantitasi, dan Linearitas
Parasetamol dan kafein masing-masing dibuat dengan konsentrasi 10, 20, 40, 70, 120, 160, 180, dan 200% kemudian diukur dengan KCKT. Diperoleh area contoh sebagai sinyal (S) kemudian dihitung nilai batas deteksi S/N = 3 dan batas kuantitasi S/N = 10. Area contoh yang diperoleh dialurkan terhadap konsentrasi lalu ditentukan nilai persamaan garis dan koefisien korelasi (r).
Kecermatan dan Ketangguhan
Preparasi contoh dilakukan dengan membuat larutan parasetamol dan kafein dengan konsentrasi 70, 100, dan 130%. Larutan dinjeksikan sebagai contoh dalam KCKT, diperoleh hasil kadar yang terukur dan dibandingkan hasil yang seharusnya, didapatkan nilai %perolehan kembali. Ketangguhan penetapan kadar parasetamoldan kafein ditetapkan melalui pengujian contoh yang sama, namun dikerjakan oleh analis, hari, dan instrumen KCKT yang berbeda.
Kesaksamaan dan Kekuatan
6
dibandingkan nilai SBRnya. Kesaksamaan dan kekuatan diterima apabila nilai SBR ≤2%.
HASIL DAN PEMBAHASAN
Modifikasi kondisi pengujian KCKT dilakukan dengan mengubah konsentrasi fase gerak dan laju alir untuk menentukan kondisi optimum dan efisiensi waktu pengujian. Optimasi dapat dilihat dari banyak kriteria seperti selektivitas, resolusi, ketangguhan, dan efisiensi. Menurut Andrade et al. (2008), beberapa parameter yang dapat memengaruhi kriteria tersebut ialah fase diam, suhu, komposisi fase gerak, dan tipe organik fase gerak. Modifikasi dalam penelitian ini menggunakan fase gerak campuran air dan pelarut organik asetonitril yang memiliki viskositas rendah sehingga diharapkan tidak menyebabkan tekanan yang tinggi di dalam kolom. Di awal penelitian, dilakukan usulan perubahan kolom dari LichoCART (RP-18 125× 4mm, 5µm) menjadi kolom yang lebih pendek X-Terra (RP-18 100×3.9mm, 5µm), namun setelah simulasi ternyata kolom pendek X-Terra tidak memberikan resolusi yang baik pada laju alir di atas 0.5 mL/menit dan memiliki tekanan yang tinggi. Karena itu, perubahan kolom tidak dilakukan.
Kolom fase terbalik (RP) sebagai fase diam bersifat non polar, sedangkan fase gerak yang digunakan bersifat polar. Parasetamol yang sifatnya lebih polar akan terelusi lebih dulu sehingga memiliki waktu retensi yang lebih singkat dibandingkan dengan kafein. Pemisahan parasetamol dan kafein dengan KCKT menggunakan kolom RP-18 pernah dilakukan sebelumnya dengan berbagai fase gerak campuran larutan pasangan ion: metanol:asetonitril = 25:57:18 (Qi et al. 2003), KH2PO4:metanol:asetonitril:2-propanol =
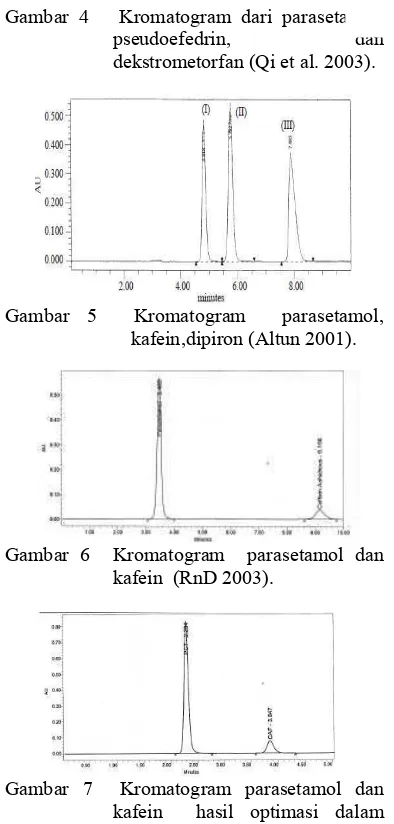
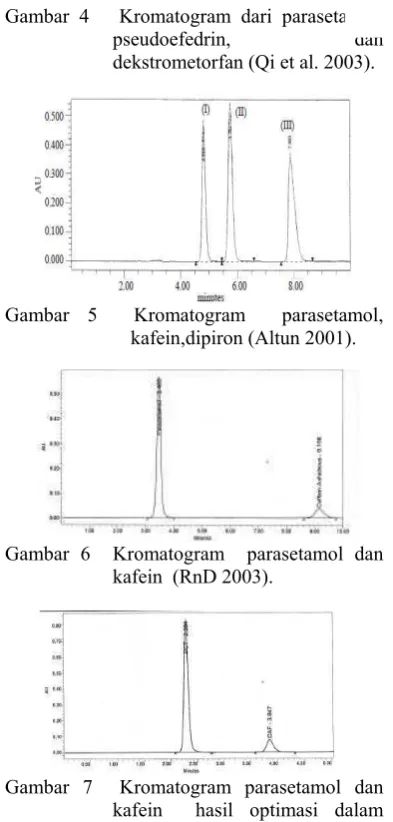
420:20:30:30 (Altun 2001), dan hasil pengembangan RnD (2003) dengan fase gerak asetonitril 10%. Kromatogram yang diperoleh dari ketiga penelitian tersebut ditunjukkan berturut-turut pada Gambar 4–6, sementara hasil optimasi penelitian ini dapat dilihat pada Gambar 7.
Gambar 4 Kromatogram dari parasetamol,
pseudoefedrin, dan dekstrometorfan (Qi et al. 2003).
Gambar 5 Kromatogram parasetamol, kafein,dipiron (Altun 2001).
Gambar 6 Kromatogram parasetamol dan kafein (RnD 2003).
Gambar 7 Kromatogram parasetamol dan kafein hasil optimasi dalam penelitian ini.
Berdasarkan hasil penelitian sebelumnya, waktu yang diperlukan untuk analisis parasetamol dan kafein dengan KCKT berkisar 10 menit sedangkan hasil modifikasi menunjukkan waktu yang relatif lebih singkat, yaitu 4 menit. Resolusi antarzat aktif (Gambar 6) diperoleh ±13, sedangkan hasil optimasi (Gambar 7) diperoleh ±6, namun keduanya masih memenuhi syarat uji kesesuaian sistem, yakni ≥2.
Optimasi Kondisi KCKT pada Penetapan Kadar Parasetamol dan Kafein
persamaan untuk respons waktu retensi parasetamol, waktu retensi kafein, dan resolusi berturut-turut
y = 17.29464 - 0.82260Xi - 12.12502Xj +
0.1888XiXj + 0.015083Xi2 + 3.09234 Xj2
y = 54.2840 - 3.81227Xi - 27.7280Xj + 0.7320
XiXj + 0.0788 Xi2 + 5.3640 Xj2
y = 45.91397 - 2.90793Xi - 15.98621Xj +
0.2800XiXj + 0.051931 Xi 2+ 4.59310 Xj2
Keterangan:
y = respons
Xi= konsentrasi fase gerak (%)
Xj= laju alir (mL/menit)
Dari Tabel 4 diketahui bahwa perubahan peubah konsentrasi fase gerak dan laju alir berpengaruh terhadap respons waktu retensi dan resolusi. Waktu retensi tersingkat dengan resolusi terkecil diperoleh pada konsentrasi asetonitril 20% dengan laju alir 1.5 mL/menit, sedangkan waktu retensi terlama dan resolusi terbesar diperoleh pada konsentrasi 10% dan laju alir 0.5 mL/menit. Hal ini disebabkan semakin tinggi konsentrasi pelarut organik dalam fase gerak, sifat kepolaran berkurang sehingga zat aktif parasetamol dan kafein berikatan lebih lama dengan fase gerak dan waktu retensinya lebih lama. Sementara laju alir mempengaruhi kecepatan fase gerak melewati kolom, semakin cepat laju alir, waktu retensi akan semakin pendek.
Tabel 4 Rancangan komposit pusat dan respons percobaan
Level terkode RKP
Faktor Respons Fase gerak (%) Laju alir (mL/menit) Wr PCT (menit) Wr KAF (menit) R
10 1.0 3.463 9.156 13.2
20 1.0 1.756 2.246 3.5
15 0.5 4.480 7.570 9.5
15 1.0 2.100 3.310 6.6
15 1.0 2.116 3.330 6.7
15 1.5 1.531 2.574 6.9
15 1.0 2.117 3.334 6.7
20 1.5 1.202 1.534 2.9
10 0.5 6.256 15.355 16.7
10 1.5 2.124 5.163 12.7
15 1.0 2..120 3.340 6.7
15 1.0 2.123 3.346 6.7
20 0.5 3.446 4.406 4.1
Keterangan:
Wr PCT = waktu retensi parasetamol Wr KAF= waktu retensi kafein R = resolusi
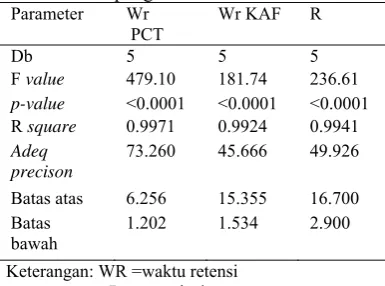
Hasil rancangan percobaan dengan RKP diolah datanya dengan Anova menggunakan perangkat lunak Design-Expert 7.0.0 hingga keseluruhan respons yang memilliki derajat bebas 5 memiliki nilai F yang lebih besar dari nilai p, Prob>F berarti semua respons secara signifikan dipengaruhi oleh peubah fase gerak dan laju alir. Nilai r2 untuk keseluruhan respons memenuhi ≥0.99. Nilai adeq precision
menunjukkan nilai nisbah antara sinyal dan derau yang diharapkan nilainya ≥4. Respons waktu retensi parasetamol, kafein, dan resolusi memberikan hasil berturut-turut 73.260; 45.666; dan, 49.926, menunjukkan sinyal berupa zat aktif yang dianalisis dapat dibedakan sempurna dengan derau (Tabel 5).
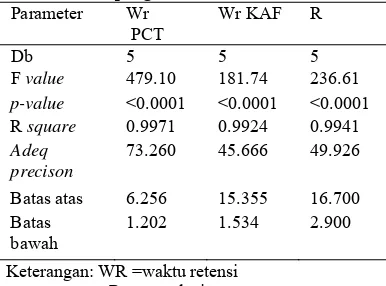
Tabel 5 Hasil pengolahan data Anova
Parameter Wr PCT
Wr KAF R
Db 5 5 5
F value 479.10 181.74 236.61
p-value <0.0001 <0.0001 <0.0001
R square 0.9971 0.9924 0.9941
Adeq precison
73.260 45.666 49.926
Batas atas 6.256 15.355 16.700 Batas
bawah
1.202 1.534 2.900
Keterangan: WR =waktu retensi R =resolusi
8
nilai-nilai yang merekomendasikan metode ketiga sebagai kondisi terpilih (Tabel 6).
Tabel 6, memperlihatkan bahwa total penggunaan fase gerak untuk asetonitril 15% dengan laju alir 1.0 mL/menit paling sedikit, yaitu 272 mL untuk 1 kali analisis. Penggunaan fase gerak yang lebih sedikit akan lebih ekonomis dan juga menghasilkan limbah lebih sedikit sehingga lebih ramah lingkungan. Komposisi fase gerak asetonitril 15% dengan laju alir 1.0 mL/menit ini juga hanya memerlukan 4.3 menit waktu pengujian, sementara pada metode terpilih dengan laju alir 1.5 mL/menit, meskipun hanya memerlukan waktu 3.5 menit tekanan tinggi yang diberikan dapat mempercepat rusaknya kolom.
Tabel 6 Perbandingan efisiensi dari 3 kondisi pengujian
Parameter Kondisi pengujian
A B C Wr PCT (menit) 3.5 1.5 2.1 Wr KAF (mnt) 9.2 2.6 3.3
Resolusi 13.2 6.9 6.6
Analisis (menit) 10 3.5 4.5 Fase gerak (mL) 402 327 272 Keterangan :
A= Fase gerak 10%, laju alir 1.0 mL/menit B= Fase gerak 15%, laju alir 1.5 mL/menit C= Fase gerak 15%, laju alir 1.0 mL/menit
Validasi Metode Hasil Optimasi
Kondisi terpilih hasil optimasi perlu divalidasi untuk memastikan bahwa metode tersebut memberikan hasil uji yang terpercaya dan selanjutnya dapat digunakan untuk analisis rutin di laboratorium. Validasi bertujuan melihat pengaruh kondisi peralatan yang digunakan, pereaksi, dan personel yang melakukan pemeriksaan. Parameter pengujian meliputi studi plasebo, linearitas, batas deteksi, dan kuantitasi, kesaksamaan, kecermatan, ketangguhan, dan kekuatan metode.
Sebelum dilakukan pengujian batas deteksi dan kuantitasi, terlebih dahulu dilakukan pengujian gangguan dengan menganalisis pengganggu yang terdapat di dalam plasebo. Pengujian gangguan ini bertujuan untuk mengetahui besarnya derau dan memastikan bahwa pada saat pengujian sinyal yang diberikan benar-benar hanya berasal dari analit. Berdasarkan percobaan yang dilakukan duplo, diperoleh nilai gangguan untuk parasetamol 1.36% dan kafein 0.63%. Nilai tersebut masih memenuhi
kriteria penerimaan batas gangguan ≤2.0%. (Lampiran 4).
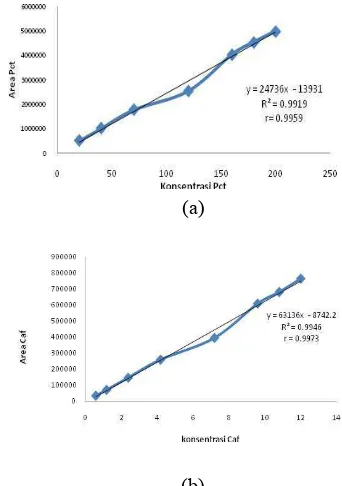
Linearitas menurut Zamri (2008) dapat menggambarkan kemampuan suatu alat untuk memperoleh hasil yang sebanding dengan kadar analit pada rentang kadar tertentu. Pengujian parameter linearitas memberikan nilai koefisien korelasi (r) 0.9959 untuk parasetamol dan 0.9973 untuk kafein (Lampiran 5).
(a)
(b)
Gambar 8 Kurva parasetamol (a) dan kafein (b).
Batas deteksi dan kuantitasi ditentukan dari persamaan regresi linear hasil penentuan linearitas. Berdasarkan persamaan y=24736x– 13931, diperoleh batas deteksi untuk parasetamol 0.5633 ppm dan batas kuantitasi 0.5636 ppm, untuk kafein, y= 63136x–8742.2, maka diperoleh batas deteksi 0.1385 ppm dan batas kuantisasi 0.1386 ppm (Lampiran 5). Batas deteksi digunakan untuk mengetahui konsentrasi analit terendah yang bisa dideteksi dengan masih dapat membedakan antara sinyal analit dan derau. Sementara batas kuantitasi digunakan untuk mengetahui konsentrasi terendah yang dapat ditentukan oleh suatu metode dengan tingkat ketepatan dan ketelitian yang tervalidasi.
≤2.0%. Berdasarkan hasil penelitian diperoleh nilai SBR untuk parasetamol adalah 0.3% dan kafein 0.2% (data dapat dilihat pada Lampiran 6). Nilai tersebut menunjukan bahwa metode hasil modifikasi memberikan hasil yang cukup tinggi dan sahih.
Kecermatan suatu metode ditentukan dengan studi perolehan kembali. Perolehan kembali merupakan jumlah analit yang dapat diperoleh kembali setelah diberikan perlakuan yang sama kemudian dilakukan perbandingan antara hasil yang diperoleh dan nilai
sebenarnya. Perolehan kembali kadar zat aktif yang dipersyaratkan dalam obat adalah 98.0– 102.0%. Berdasarkan percobaan yang dilakukan triplo untuk rentang kadar 70, 100, dan 130%, perolehan kembali untuk parasetamol 99.5% dan kafein 99.88%, memenuhi persyaratan (Lampiran 7). Secara keseluruhan, validasi metode hasil modifikasi pada Tabel 7.
Tabel 7 Validasi metode hasil modifikasi
Parameter Parasetamol Kafein Spesifikasi
USP 28 Metode lama Metode
baru
Metode lama
Metode baru
Studi plasebo Tidak terdeteksi
1.36% Tidak terdeteksi
0.63% ≤ 2.0%
Batas deteksi 0.049 ppm 0.563 ppm 0.033 ppm 0.139 ppm - Batas kuantitasi 0.048 ppm 0.564 ppm 0.035 ppm 0.139 ppm -
Linearitas 100.04% 0.9959 0.9997 0.9973% ≥0.98%
Kecermatan 0.7% 99.75% 99.90% 99.88% 98.0–102.0%
Kesakasamaan 1.08% 0.30% 0.7% 0.2% ≤ 2.0%
Ketangguhan - 0.65% 1.00% 0.83% ≤ 2.0%
kekuatan 0.50% - 0.70% ≤ 2.0%
Ketangguhan metode ditentukan dengan menetapkan kadar analit dengan menggunakan instrumen, analis, dan hari yang berbeda kemudian ditentukan nilai SBRnya. Ketangguhan metode ini akan menunjukkan kemampuan metode untuk digunakan pada kondisi instrumen, analis, dan hari berbeda dengan memberikan hasil yang tetap tepercaya. Pengujian ketangguhan ini menggunakan 3 instrumen KCKT yang berbeda, yakni Waters Pump 1525, Agilent 1200 series, dan Waters e2695 Alliance. Berdasarkan ketiga pengujian tersebut diperoleh hasil perolehan kembali yang memenuhi spesifikasi 98.0–102.0% dan nilai SBR ≤2.0% (Lampiran 8). Kekuatan metode ditentukan dengan menguji kadar zat aktif dengan variasi laju alir 0.8, 1.0, dan 1.2 mL/menit. Perubahan laju alir dimaksudkan untuk mengetahui sejauh mana metode masih bisa memberikan hasil yang sahih dengan adanya sedikit perubahan terhadap metode. Hasil pengujian menunjukkan SBR 0.5 untuk parasetamol dan 0.7% untuk kafein (Lampiran 9).
SIMPULAN DAN SARAN
Simpulan
Optimasi kondisi pengujian KCKT pada penetapan kadar parasetamol dan kafein dengan mengubah komposisi fase gerak menjadi asetonitril 15% dan laju alir 1.0 mL/menit telah berhasil mengefisienkan waktu pengujian dari ±10 menit menjadi ±4.5 menit dan menghemat jumlah fase gerak yang digunakan. Metode terpilih telah divalidasi dengan hasil memenuhi seluruh kriteria untuk parameter uji validasi.
Saran
≤2.0%. Berdasarkan hasil penelitian diperoleh nilai SBR untuk parasetamol adalah 0.3% dan kafein 0.2% (data dapat dilihat pada Lampiran 6). Nilai tersebut menunjukan bahwa metode hasil modifikasi memberikan hasil yang cukup tinggi dan sahih.
Kecermatan suatu metode ditentukan dengan studi perolehan kembali. Perolehan kembali merupakan jumlah analit yang dapat diperoleh kembali setelah diberikan perlakuan yang sama kemudian dilakukan perbandingan antara hasil yang diperoleh dan nilai
sebenarnya. Perolehan kembali kadar zat aktif yang dipersyaratkan dalam obat adalah 98.0– 102.0%. Berdasarkan percobaan yang dilakukan triplo untuk rentang kadar 70, 100, dan 130%, perolehan kembali untuk parasetamol 99.5% dan kafein 99.88%, memenuhi persyaratan (Lampiran 7). Secara keseluruhan, validasi metode hasil modifikasi pada Tabel 7.
Tabel 7 Validasi metode hasil modifikasi
Parameter Parasetamol Kafein Spesifikasi
USP 28 Metode lama Metode
baru
Metode lama
Metode baru
Studi plasebo Tidak terdeteksi
1.36% Tidak terdeteksi
0.63% ≤ 2.0%
Batas deteksi 0.049 ppm 0.563 ppm 0.033 ppm 0.139 ppm - Batas kuantitasi 0.048 ppm 0.564 ppm 0.035 ppm 0.139 ppm -
Linearitas 100.04% 0.9959 0.9997 0.9973% ≥0.98%
Kecermatan 0.7% 99.75% 99.90% 99.88% 98.0–102.0%
Kesakasamaan 1.08% 0.30% 0.7% 0.2% ≤ 2.0%
Ketangguhan - 0.65% 1.00% 0.83% ≤ 2.0%
kekuatan 0.50% - 0.70% ≤ 2.0%
Ketangguhan metode ditentukan dengan menetapkan kadar analit dengan menggunakan instrumen, analis, dan hari yang berbeda kemudian ditentukan nilai SBRnya. Ketangguhan metode ini akan menunjukkan kemampuan metode untuk digunakan pada kondisi instrumen, analis, dan hari berbeda dengan memberikan hasil yang tetap tepercaya. Pengujian ketangguhan ini menggunakan 3 instrumen KCKT yang berbeda, yakni Waters Pump 1525, Agilent 1200 series, dan Waters e2695 Alliance. Berdasarkan ketiga pengujian tersebut diperoleh hasil perolehan kembali yang memenuhi spesifikasi 98.0–102.0% dan nilai SBR ≤2.0% (Lampiran 8). Kekuatan metode ditentukan dengan menguji kadar zat aktif dengan variasi laju alir 0.8, 1.0, dan 1.2 mL/menit. Perubahan laju alir dimaksudkan untuk mengetahui sejauh mana metode masih bisa memberikan hasil yang sahih dengan adanya sedikit perubahan terhadap metode. Hasil pengujian menunjukkan SBR 0.5 untuk parasetamol dan 0.7% untuk kafein (Lampiran 9).
SIMPULAN DAN SARAN
Simpulan
Optimasi kondisi pengujian KCKT pada penetapan kadar parasetamol dan kafein dengan mengubah komposisi fase gerak menjadi asetonitril 15% dan laju alir 1.0 mL/menit telah berhasil mengefisienkan waktu pengujian dari ±10 menit menjadi ±4.5 menit dan menghemat jumlah fase gerak yang digunakan. Metode terpilih telah divalidasi dengan hasil memenuhi seluruh kriteria untuk parameter uji validasi.
Saran
OPTIMASI KONDISI PENGUJIAN
KROMATOGRAFI CAIR KINERJA TINGGI
PADA PENETAPAN KADAR BAHAN AKTIF
OBAT SAKIT KEPALA
HERLIN EKA PRATIWI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
10
DAFTAR PUSTAKA
Altun ML. 2001. HPLC method for the analysis of parasetamol, caffein, and dipyrone. Ankara University: Faculty of Pharmacy, Department of Pharmacognosy.
[ASHSP]. 2001. American Hospital Formulary Service (AHFS). New york: ASHSP. hlm 2046-2048.
[DepKes RI] 1995. Farmakope Indonesia. Ed ke-4. Jakarta:Depkes RI.
Andrade A, Dievart P, Dagaut P. 2009. Improve optimization of polycylic aromatic hydrocarbon (PAHs) mixtures resolution in reversed phase high performance liquid chromathography by using factorial design and responsse surface methodology. France: CNRS-ICARE IC, Avenua de la Recherche Scientifique.
Bezerra MA, Santelli RE, Oliveira EP, Villar LS, Escaleira LA. 2008. Response Surface Methodology as tool for optimization in analytical chemistry. Rua Jos´e Moreira: Departementode geouimica, Universidade Federal Fluminense.
Christinopa IL. 2010. Optimasi dan validasi metode kromatografi cair kinerja tinggi (KCKT) dan aplikasinya untuk penetapan kadar kurkumin dalam sediaan tablet salut gula [skripsi]. Yogyakarta: Fakultas MIPA, Universitas Gadjah Mada.
Connors KA, Gordon LA, Valentino JS. 1986. Chemical Stability of Pharmaceuticals Handbook for Pharmacist. Ed ke-2. New York: J Wiley. hlm 163-165.
Harahap H. 2008. Optimasi transesterifikasi
refined bleached deodorized palm oil
menjadi metil ester menggunakan katalis litium hidroksida [skripsi]. Medan: Universitas Sumatera Utara.
Harmita. 2004. Validasi metode analisis.
Maj Ilmu kefarmasian. I: 117-135.
Khopkar SM. 2003. Konsep Dasar Kimia Analitik. Saptorahardjo A, penerjemah; Jakarta : UI, Pr. Terjemahan dari Basic Concept of Analytical Chemistry.
Qi ML, Wang P, Leng XP, Gu JL, Fu RN. 2002. Simple HPLC methode simultaneous determination of acetaminophen, caffein, and chorpheniramine maleate in table formulation.
https://springerlink3.metapress.com/cont ent/h01584r07782n602/resourcesecured/ ?target=fulltext.pdf&sid=fhhx50nxor5f1 2o3cpo5crle&sh=www.springerlink.com [23 Jan 2011]
Qi ML, Wang P, Zhou L, Gu JL, Fu RN,. 2003. Simultaneous determination of acetaminophen, dextromethorphen hydrobromide, and pseudoephedrine hydrochloride in a new drug formulation for cold treatment by HPLC. http://www.springerlink.com/content/460 h7240w344mu18. [23 Jan 2011]
Putra ED. 2004. Kromatografi cair kinerja tinggi [artikel]. Medan : Jurusan Farmasi, Fakultas MIPA. Universitas Sumatera Utara.
Scientist AD. 2003. Analytical methode validation report for assay method of parasetamol and coffein in BOSKA 500 tablet. Palembang : Dexa Medica.
OPTIMASI KONDISI PENGUJIAN
KROMATOGRAFI CAIR KINERJA TINGGI
PADA PENETAPAN KADAR BAHAN AKTIF
OBAT SAKIT KEPALA
HERLIN EKA PRATIWI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
2
ABSTRAK
HERLIN EKA PRATIWI. Optimasi Kondisi Pengujian Kromatografi Cair Kinerja Tinggi pada Penetapan Kadar Bahan Aktif Obat Sakit Kepala. Dibimbing oleh RUDI HERYANTO dan YOANNE ECLEXIA N.S.
Optimasi kondisi pengujian kromatografi cair kinerja tinggi untuk penetapan kadar parasetamol dan kafein sebagai zat aktif dalam obat sakit kepala telah dilakukan dengan tujuan menetapkan kondisi optimum dan meningkatkan efisiensi waktu pengujian. Metode penelitian menggunakan metodologi permukaan respons dengan 2 peubah bebas, yaitu konsentrasi fase gerak dan laju alir, serta 3 taraf, yaitu 10, 15, dan 20% asetonitriluntuk konsentrasi fase gerak dan 0.5, 1.0, dan 1.5 mL/menit untuk laju alir. Kondisi optimum diperoleh pada konsentrasi asetonitril 15% dan laju alir 1.5 mL/menit namun kondisi yang terpilih adalah asetonitril 15% dan laju alir 1.0 mL/menit dengan pertimbangan ekonomis dan kesesuaian sistem. Hasil optimasi kemudian divalidasi untuk memastikan bahwa penetapan dengan metode tersebut dapat dipercaya. Parameter validasi meliputi uji plasebo, batas deteksi, batas kuantitasi, kecermatan, kesaksamaan, linearitas, ketangguhan, dan kekuatan metode. Dari hasil validasi dapat disimpulkan bahwa metode terpilih memenuhi kriteria untuk seluruh parameter dan dapat digunakan untuk analisis.
ABSTRACT
HERLIN EKA PRATIWI. Optimization of High Performance Liquid Chromatography Analysis Condition to Determine Active Substance in a Headache Medicine. Supervised by RUDY HERYANTO and YOANNE ECLEXIA NS.
Optimization of high performance liquid chromatography analysis condition for paracetamol and caffeine concentration determination as active substances in a headache medicine was performed to obtain the optimum condition and to increase the efficiency of analysis time. The research method used response surface methodology with 2 independent variables and 3 levels of analysis. The independent variables were concentrations of mobile phase and flow rate, the levels were 10, 15, and 20% of acetonitrile as the mobile phase and 0.5, 1.0, and 1.5 mL/min for the flow rate. Optimum condition was obtained in 15% concentration of acetonitrile and 1.5 mL/min of flow rate, but the selected condition is a 15% concentration of acetonitrile and 1.0 mL/min of flow rate because of the system suitability and economic reasons. The selected condition was then validated to ensure that the method could give reliable results. Validation parameters consist of placebo study, limit of detection and quantitation, accuracy, precision, linearity, ruggedness, and robustness. In conclusion, the selected method could fulfill the criteria for all parameters and could be used for analysis.
OPTIMASI KONDISI PENGUJIAN
KROMATOGRAFI CAIR KINERJA TINGGI
PADA PENETAPAN KADAR BAHAN AKTIF
OBAT SAKIT KEPALA
HERLIN EKA PRATIWI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
4
Judul : Optimasi Kondisi Pengujian Kromatografi Cair Kinerja Tinggi
pada Penetapan Kadar Bahan Aktif Obat Sakit Kepala
Nama
: Herlin Eka Pratiwi
NIM
: G44086013
Disetujui
Pembimbing I
Pembimbing II
Rudi Heryanto, S.Si M.Si
Yoanne Eclexia NS, S.Si Apt
NIP 19760428 200501 1 002
Diketahui
Ketua Departemen Kimia,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Bismillahirrahmanirrahim
Alhamdulillah, segala puji hanya bagi Allah SWT yang telah memberi
begitu banyak kemudahan bagi penulis dalam menyelesaikan karya ilmiah ini.
Shalawat serta salam semoga senantiasa terlimpahkan untuk Nabi Muhamad
SAW beserta keluarga, sahabat, dan pengikutnya hingga akhir zaman.
Skripsi ini disusun berdasarkan hasil penelitian yang dilaksanakan sejak
bulan Agustus hingga November 2010. Tema yang diambil adalah optimasi
metode dengan judul Optimasi Kondisi Pengujian Kromatografi Cair Kinerja
Tinggi pada Penetapan Kadar Bahan Aktif Obat Pereda Sakit Kepala.
Penulis
berharap hasil penelitian ini dapat memberikan manfaat bagi para pembaca
nantinya.
Akhirnya penulis menyampaikan terima kasih kepada Bapak Rudi
Heryanto S.Si, M.Si selaku pembimbing, Bapak Muhamad Rafi S.Si, M.Si
yang sebelumnya sempat menjadi pembimbing, Bapak Rahmat Budi Yuwono,
S.Si Apt dan Ibu Yoanne Eclexia NS, S.Si Apt yang telah memberi izin
penelitian di laboratorium
Quality Control
PT Ferron Par Pharmaceuticals,
kedua orang tua untuk doa tulus tak terputus, rekan-rekan QC laboratorium
dan staf, serta seluruh pihak yang telah membantu selama proses penyusunan
skripsi ini.
Cikarang, Maret 2011
6
RIWAYAT HIDUP
Penulis dilahirkan di kota Sukabumi pada tanggal 23 Mei 1986 sebagai
putri pertama dari pasangan H. Ujang Suardi dan Hj. Ipah Saripah. Tahun 2004
penulis lulus dari SMUN 3 Sukabumi dan pada tahun yang sama lulus seleksi
masuk Akademi Kimia Analisis (AKA) Bogor program Diploma III dan lulus
dengan gelar Ahli Madya (AMd) pada tahun 2007 dengan judul tugas akhir
Pengujian Kadar Logam Berat dalam Limbah Abu Batubara dengan
Metode
Toxicity Characteristic Leaching Procedure
(TCLP) secara Spektrofotometri
Serapan Atom.
Penulis telah bekerja sebagai analis QC di salah satu perusahaan farmasi
nasional pada tahun 2007 dan analis RnD di tahun 2011 di perusahaan milik
asing. Pada tahun 2008 penulis diberikan kesempatan untuk melanjutkan
pendidikan di Institut Pertanian Bogor (IPB) dengan mengikuti Program S1
Kimia dengan Penyelenggaraan Khusus Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ...
vii
DAFTAR TABEL ...
vii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ...
1
TINJAUAN PUSTAKA
Tablet Obat Sakit Kepala ...
1
Parasetamol ...
1
Kafein ...
2
Kromatografi Cair Kinerja Tinggi ...
2
Metodologi Permukaan Respons ...
2
Validasi Metode Analisis ...
3
Kecermatan ...
3
Kesaksamaan ...
3
Selektivitas ...
3
Linearitas ...
3
Batas Deteksi dan Batas Kuantitasi ...
3
Ketangguhan Metode (Ruggedness) ...
4
Kekuatan Metode (Robustness) ...
4
BAHAN DAN METODE
Bahan dan Alat ...
4
Metode Penelitian ...
4
Rancangan Percobaan ...
4
Preparasi Fase Gerak Standar dan Contoh ...
5
Uji Kesesuaian Sistem ...
5
Validasi Metode Penetapan Kadar ...
5
HASIL DAN PEMBAHASAN
Optimasi Kondisi KCKT pada Penetapan Kadar ...
6
Validasi Metode Hasil Optimasi ...
8
SIMPULAN DAN SARAN
Simpulan ...
9
Saran ...
9
DAFTAR PUSTAKA ...
10
vii
DAFTAR GAMBAR
Halaman
1 Rumus struktur parasetamol ...
1
2 Rumus struktur kafein ...
2
3 Diagram alir KCKT ...
2
4 Kromatogram dari parasetamol, pseudoefedrin, dekstrometorfan ...
6
5 Kromatogram parasetamol, kafein, dipiron………...…. ...
6
6 Kromatogram parasetamol dan kafein hasil RnD ...
6
7 Kromatogram parasetamol dan kafein hasil optimasi ...
6
8 Kurva linearitas parasetamol dan kafein ...
8
DAFTAR TABEL
Halaman
1 Parameter kondisi KCKT sebelum modifikasi ...
4
2
Perlakuan terkode penetapan kadar parasetamol dan kafein dalam
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ...
11
2 Permukaan respons peubah bebas fase gerak dan laju alir dengan
respons waktu retensi kafein (a), waktu retensi parasetamol (b), dan
resolusi (c )………..……… ...
12
3 Alur kontur peubah bebas fase gerak dan laju alir dengan respons
waktu retensi kafein (a), waktu retensi parasetamol (b), dan resolusi
(c )……… …………..………
13
4 Persentase gangguan dalam plasebo obat sakit kepala ... 14
5 Linearitas, batas deteksi, dan batas kuantitasi untuk parasetamol
dan kafein ...
14
6 Kesaksamaan parasetamol dan kafein ...
15
8 Nilai simpangan baku relatif ketangguhan metode ...
15
9 Kekuatan parasetamol dan kafein dengan variasi laju alir ...
15
7 Kecermatan parasetamol dan kafein ...
16
PENDAHULUAN
Obat pereda sakit kepala dengan 2 kandungan zat aktif, parasetamol dan kafein, telah diproduksi oleh perusahaan farmasi dengan memenuhi cara pembuatan obat yang baik (CPOB) yang dipersyaratkan oleh badan pengawasan obat dan makanan (BPOM). Parasetamol memiliki sifat analgesik yang efektif untuk menghilangkan rasa nyeri ringan dan mengobati sakit kepala, sedangkan kafein berfungsi sebagai stimulan (ASHSP 2001).
Obat pereda sakit kepala tablet diproduksi dalam jumlah yang semakin bertambah seiring dengan meningkatnya permintaan konsumen. Penambahan jumlah produksi berdampak terhadap penambahan jumlah analisis yang dilakukan sebagai jaminan kualitas produk. Oleh karena itu, diperlukan metode analisis yang cepat dan tepat untuk memenuhi keperluan tersebut. Metode penetapan kadar parasetamol dan kafein dalam obat sakit kepala menggunakan kromatografi cair kinerja tinggi (KCKT) hasil pengembangan in house oleh RnD menggunakan fase gerak asetonitril 10%, fase diam RP-18 125 × 4 mm 5µm, waktu alir 1.0 mL/menit dapat memisahkan parasetamol dan kafein dengan resolusi 13.2, waktu retensi parasetamol ±3.2 menit, kafein ±9.1 menit, dan lama waktu pengujian ±10 menit (Scientist 2003). Penelitian ini dimaksudkan untuk mengoptimasi kondisi pengujian tersebut sehingga dapat mempersingkat waktu analisis untuk mencapai efisiensi pengujian.
Modifikasi dengan melakukan perubahan komposisi fase gerak dan waktu alir. Kondisi optimum ditentukan menggunakan metodologi permukaan respons. Kondisi terpilih kemudian divalidasi untuk memastikan bahwa metode memberikan hasil uji yang terpercaya dan digunakan untuk analisis rutin. Parameter validasi meliputi batas deteksi, batas kuantitasi, kecermatan, kesaksamaan, linearitas, ketangguhan, dan kekuatan metode.
TINJAUAN PUSTAKA
Tablet Obat Sakit Kepala
Tablet adalah sediaan padat yang mengandung bahan obat dengan atau tanpa bahan pengisi. Berdasarkan metode pembuatannya, tablet dapat digolongkan sebagai tablet cetak dan kempa. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan baja. Tablet cetak dibuat dengan cara menekan
massa serbuk lembap pada tekanan rendah dalam lubang cetakan (Depkes RI 1995).
Bahan yang digunakan dalam pembuatan obat terdiri atas bahan utama (zat aktif) dan bahan tambahan (zat aditif). Bahan utama adalah zat kimia yang berfungsi menyembuhkan penyakit yang dialami oleh penderita, sedangkan bahan tambahan adalah zat kimia yang berfungsi menambah bobot yang diinginkan, mempermudah proses pencetakan, atau mempermudah proses pengikatan pada saat semua bahan obat tercampur. Obat sakit kepala tablet diproduksi dengan sediaan padat berbentuk tablet bundar berwarna putih, tidak berbau, berasa pahit, diameter 13 mm, dan memiliki kandungan bahan utama 500 mg parasetamol dan 30 mg kafein. Bahan tambahan terdiri atas larutan natrium benzoat sebagai pengikat pada proses granulasi basah sekaligus pengawet, bahan pengisi yang terdiri atas Primojel dan Kolidon, sedangkan fase luar terdiri atas Mgstearat dan Aerosil 200 yang berfungsi memudahkan proses pencetakan.
Parasetamol
Parasetamol atau dikenal sebagai asetaminofen(Gambar 1) merupakan zat aktif berbentuk serbuk hablur putih dan tidak berbau dengan rumus kimia C8H9NO2 dan bobot
molekul 151.16 g/mol. Parasetamol larut di dalam air mendidih dan NaOH 1 N, serta mudah larut dalam etanol. Suhu leburnya 168– 172 oC, sisa pijar ≤0.1%, kadar air ≤0.5%, dan logam berat ≤0.001% (Depkes RI 1995).
Parasetamol sangat stabil di dalam air dan memiliki kestabilan maksimum pada kisaran pH 5–7 (Connors et al. 1986). Parasetamol merupakan senyawa turunan dari p-aminofenol yang memiliki sifat analgesik dan antipiretik. Parasetamol memberi efek analgesik sementara, tidak memiliki efek antirematik, efektif menghilangkan rasa nyeri ringan, dan mengobati sakit kepala. Parasetamol ditemukan dapat dikombinasikan dengan kafein, aspirin, salisilamida, danopiat(ASHSP 2001).
2
Kafein
Kafein (Gambar 2) berbentuk serbuk halus mengilat, biasanya menggumpal, tidak berbau, dan berasa pahit. Kafein agak sukar larut di dalam air dan sukar larut di dalam etanol. Kafein memiliki rumus kimia C8H10N4O2,
bobot molekul 194.19 g/mol, sisa pijar ≤0.1%, suhu lebur 235–239 oC, susut pengeringan
≤0.5%, dan logam berat ≤0.001% (Depkes RI 1995).
Gambar 2 Rumus struktur kafein.
Kromatografi Cair Kinerja Tinggi
Pada tahun 1903 Tswett menemukan teknik kromatografi, sebagai cara untuk menguraikan suatu campuran. Dalam kromatografi, komponen terdistribusi dalam 2 fase. Transfer massa antara fase gerak dan fase diam terjadi bila molekul-molekul campuran terjerap pada permukaan partikel atau terserap di dalam pori-pori partikel atau terbagi dalam sejumlah cairan yang terikat pada permukaan atau di dalam pori (Khopkar 2003).
Komponen KCKT (Gambar 3) terdiri atas pompa bertekanan tinggi yang harus tahan terhadap semua jenis pelarut dan mampu mengantarkan aliran terukur 0.01–1.0 mL/menit (Zamri 2008). Injektor merupakan bagian untuk memasukkan contoh yang akan dianalisis melewati sistem. Kolom adalah jantung kromatografi, berhasil atau tidaknya analisis bergantung pada pemilihan kolom dan kondisi percobaan yang sesuai. Kolom dapat berupa kaca atau baja nir karat, pengisi kolom seperti partikel pellicular, yaitu butiran kaca yang dilapisi materi berpori seperti silika gel, alumina, atau penukar ion (Khopkar 2003). Detektor dibutuhkan untuk mendeteksi adanya komponen contoh dan menghitung kadarnya (Putra 2004). Detektor yang digunakan bergantung pada contoh yang dipisahkan, detektor UV lazim digunakan untuk analisis bahan organik bergugus fungsi.
Gambar 3 Diagram alir KCKT.
KCKT merupakan metode kromatografi cair yang paling banyak digunakan dalam analisis suatu senyawa, karena kompatibel untuk sebagian besar senyawa terutama senyawa dalam campuran yang konsentrasinya kecil dan tekanan uapnya rendah (Christinopa 2010). Menurut Khopkar (2003), penggunaan KCKT efisien, sangat selektif, memerlukan contoh dalam jumlah sedikit, serta dapat digunakan dalam analisis kuantitatif. Analisis didasarkan pada waktu retensi, yaitu waktu yang dibutuhkan untuk mengalirkan zat terlarut dari permulaan kolom sampai detektor.
Zat yang berinteraksi kuat dengan fase diam akan memiliki waktu retensi yang lama, demikian pula untuk sebaliknya. Waktu retensi tiap senyawa adalah khas pada kondisi kerja tertentu, sehingga dapat digunakan sebagai parameter kualitatif. Untuk kepentingan analisis kuantitatif, diperlukan data luas atau ketinggian puncak yang ditentukan oleh konsentrasi zat terlarut. Luas puncak pada kurva elusi dipengaruhi proses perpindahan massa, yaitu difusi Eddy, difusi longitudinal, dan transfer massa tidak seimbang. Parameter yang menunjukkan berlangsungnya proses adalah laju aliran, ukuran partikel, laju difusi, dan ketebalan stasioner (Khopkar 2003).
Metodologi Permukaan Respons
statistika yang digunakan untuk pemodelan dan analisis permasalahan pada respons yang dipengaruhi oleh beberapa peubah dan bertujuan memperoleh kondisi optimum.
Menurut Bezerra et al. (2009), untuk memperkirakan respons dari percobaan tidak dapat digunakan fungsi linear, tetapi kuadrat permukaan respons, seperti faktorial 3 tingkat, Box Behnken, komposit pusat, dan desain Doehlert. Kecocokan model orde dua central composite design (CCD) atau rancangan komposit pusat (RKP) banyak digunakan. RKP pertama kali diperkenalkan oleh Box dan Wilson.
Validasi Metode Analisis
Menurut Harmita (2004), ada beberapa parameter dalam validasi metode analisis yang dijelaskan di bawah ini :
Kecermatan
Kecermatan menunjukkan kedekatan hasil analisis dengan kadar analit sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan hasil analisis sangat bergantung pada sebaran galat sistematik di dalam keseluruhan tahapan analisis. Kecermatan ditentukan dengan 2 cara, yaitu metode simulasi (spiked-placebo recovery) dan metode penambahan baku (standard addition method). Dalam metode simulasi, sejumlah analit bahan murni sebagai senyawa pembanding kimia baku ditambahkan ke dalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan.
Dalam metode penambahan baku, contoh dianalisis lalu sejumlah tertentu analit yang diperiksa ditambahkan ke dalam contoh, dihomogenkan, kemudian dianalisis kembali. Selisih kedua hasil dibandingkan dengan kadar sebenarnya. Berdasarkan kedua metode tersebut, persen perolehan kembali dinyatakan sebagai nisbah antara hasil yang diperoleh dan hasil sebenarnya.
Kesaksamaan
Kesaksamaan menunjukkan kesesuaian antara hasil-hasil uji berdasarkan penyebaran hasil dari nilai rerata jika prosedur diterapkan secara berulang pada contoh yang diambil dari campuran yang homogen. Kriteria saksama diberikan jika metode memberikan simpangan baku relatif (SBR) atau koefisien variasi (KV) ≤2%. Akan tetapi, kriteria ini sangat fleksibel
bergantung pada konsentrasi analit yang diperiksa, jumlah contoh, dan kondisi laboratorium.
Percobaan kesaksamaan dilakukan terhadap sedikitnya 6 ulangan contoh yang diambil dari campuran contoh dengan matriks yang homogen. Sebaiknya kesaksamaan ditentukan terhadap contoh sebenarnya, yaitu berupa campuran dengan bahan pembawa sediaan farmasi (plasebo), untuk melihat pengaruh matriks pembawa terhadap kesaksamaan ini.
Selektivitas
Selektivitas adalah kemampuan metode untuk mengukur zat tertentusecara cermat dan saksama dengan adanya komponen lain yang mungkin ada dalam matriks contoh. Selektivitas sering kali dapat dinyatakan sebagai derajat penyimpangan(degree of bias).
Selektivitas metode ditentukan dengan membandingkan hasil analisis contoh yang mengandung cemaran, hasil urai, senyawa sejenis, senyawa asing, atau pembawa plasebo dengan hasil analisis contoh tanpa penambahan bahan. Penyimpangan hasil, jika ada, merupakan selisih dari hasil uji keduanya. Pada metode analisis yang melibatkan kromatografi, selektivitas ditentukan melalui perhitungan daya resolusinya (r).
Linearitas
Linearitas adalah kemampuan metode analisis memberikan respons secara langsung atau dengan bantuan transformasi matematika secaraa baik dan proporsional terhadap konsentrasi analit dalam contoh. Sebagai parameter adanya hubungan linear digunakan koefisien korelasi r pada analisis regresi linear
y = a + bx. Hubungan linear yang ideal dicapai jika nilai b = 0 dan r = +1 atau –1 bergantung pada arah garis, sedangkan nilai a
menunjukkan kepekaan analisis, terutama instrumen yang digunakan.
Batas Deteksi dan Batas Kuantitasi
4
Ketangguhan (Ruggedness)
Ketangguhan metode adalah tingkat ketertiruan hasil uji yang diperoleh dari analisis contoh yang sama dalam berbagai kondisi uji normal seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu, dan hari yang berbeda. Ketangguhan metode ditentukan dengan menganalisis contoh yang homogen dari laboratorium yang berbeda oleh analis yang berbeda menggunakan kondisi kerja dan lingkungan yang berbeda, tetapi dengan prosedur dan parameter uji yang sama.
Kekuatan (Robustness)
Kekuatan metode dapat divalidasi dengan perubahan metodologi yang kecil untuk mengevaluasi respons analitik dan efek presisi dan akurasi. Perubahan yang dibutuhkan untuk menunjukkan kekuatan prosedur KCKT mencakup perubahan komposisi organik fase gerak (1%), pH fase gerak (±0.2 unit), laju alir, dan suhu kolom (±2–3ºC).
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan selama penelitian adalah obat pereda sakit kepala tablet dengan kandungan zat aktif parasetamol 500 mg dan kafein 30 mg, standar parasetamol (Europe CW0910509, 99.622%), standar kafein (USA200910077, 100.7%), asetonitril Chrom AR®
(Mallinckrodt Chemical, 100%), dan air distilasi.
Peralatan yang digunakan selama penelitian adalah 3 macam KCKT (Waters 1525, Agilent 1200 series, dan Waters Aliance e2695) digunakan untuk parameter ketangguhan metode. Selain itu, digunakan perangkat lunak Design Expert 7.0, injektor Rheodyne 20 L
sample loop, kolom LichroCART RP–18 (125 × 4 mm, 5µm), neraca analitik (Mettler Toledo, MT XS205 DU), membran filter (millipore) 0.45 m, Ultrasonic (104H), labu takar Iwaki, pipet volumetrik, serta peralatan kaca lainnya.
Metode Penelitian
Metode penelitian ini dilakukan untuk memodifikasi metode pengujian KCKT pada penetapan kadar parasetamol dan kafein dalam obat sakit kepala (Lampiran 1). Parameter kondisi KCKT sebelum modifikasi diberikan pada Tabel 1. Modifikasi dilakukan terhadap
komposisi fase gerak dan laju alir, sedangkan parameter yang lainnya dibuat tetap.
Tabel 1 Parameter kondisi KCKT sebelum modifikasi
Parameter Sebelum optimasi Kolom Lichocart RP-18 (125 × 4
mm, 5µm) Detektor UV, 270 nm Laju alir 1.0 mL/mnt Loop injector 20 µL Pelarut dan fase gerak
Asetonitril:air(10:90)
Rancangan Percobaan
Metode RSM digunakan untuk menentukan kondisi optimum penetapan kadar parasetamol dan kafein dalam tablet sakit kepala dengan 2 faktor sebagai peubah bebas, yaitu konsentrasi fase gerak (%v/v) dan laju alir (mL/menit).Respons yang diamati adalah waktu retensi (menit) dan resolusi. Percobaan dirancang dalam bentuk RKP dan level terkode disajikan pada Tabel 2 dan 3.
Tabel 2 Perlakuan terkode penetapan kadar parasetamol dan kafein dalam obat sakit kepala
Perlakuan Perlakuan terkode
-1 0 1
Fase gerak (%) 10 15 20
Laju alir (mL/menit)
0.5 1.0 2.5
Tabel 3 Rancangan komposit pusat (RKP) dengan 2 peubah bebas
Metode tersebut digunakan untuk mengamati pengaruh konsentrasi fase gerak dan laju alir terhadap waktu retensi dan resolusi dari 2 zat aktif, yaitu parasetamol dan kafein. Untuk melihat pengaruh tersebut digunakan persamaan regresi
No. Konsentrasi Fase gerak (%)
Laju alir (mL/menit)
1 10 1.0
2 20 1.0
3 15 0.5
4 15 1.0
5 15 1.0
6 15 1.5
7 15 1.0
8 20 1.5
9 10 0.5
10 10 1.5
11 15 1.0
12 15 1.0
Dengan y adalah peubah respons yang diukur, yaitu waktu retensi parasetamol, waktu retensi kafein, dan resolusi. β adalah tetapan linear kuadratik, x adalah peubah bebas, yaitu fase gerak dan laju alir, dan ε adalah sisa.
Preparasi Fase Gerak, Standar, dan Contoh
Pembuatan fase gerak dilakukan dengan cara mencampurkan pelarut asetonitril:air (sesuai nisbah yang diinginkan, yaitu asetonitril 10, 15, dan 20%). Campuran dihomogenkan dan disaring dengan membran filter PTFE (millipore) 0.45 m lalu dihilangkan gelembungnya.
Untuk pembuatan standar, sebanyak 500 mg standar parasetamol dan 30 mg kafein ditimbang saksama, dilarutkan dalam fase gerak dengan komposisi terpilih hingga 50 mL (A). Labu takar 10 mL disiapkan kemudian dipipet 1.0 mL larutan A dimasukkan ke dalam labu tersebut dan ditera dengan pelarut. Dipipet 1.0 mL lagi ke dalam labu takar 10 mL, diperoleh larutan parasetamol 100 ppm dan kafein 6 ppm.
Sebanyak 10 buah tablet ditimbang dan ditentukan nilai rerata bobotnya kemudian digerus hingga halus dan tercampur homogen. Ditimbang setara bobot 1 tablet (digunakan bobot rerata 10 tablet) kemudian dimasukkan ke dalam labu takar 100 mL dan dilarutkan dengan fase gerak komposisi terpilih (larutan B). Contoh diberi perlakuan seperti standar, yakni pengenceran 100 kali. Konsentrasi larutan contoh parasetamol 100 ppm dan kafein 6 ppm.
Uji Kesesuaian Sistem
Larutan standar parasetamol konsentrasi 100 ppm dan standar kafein 6 ppm diinjeksikan sejumlah 20 L melalui injektor ke dalam KCKT sebanyak 5 kali ulangan. Digunakan kecepatan alir hasil optimasi dan detektor diatur pada 270 nm. Diperoleh kromatogram untuk tiap injeksi yang akan digunakan untuk menentukan kadar keterulangan penyuntikan larutan baku, yang dinyatakan dalam SBR atau KV, waktu retensi, luas puncak, tinggi puncak, dan tailing factor.
Validasi Metode Penetapan Kadar
Studi Plasebo
Studi plasebo bertujuan melihat keberadaan gangguan yang berasal dari plasebo pada saat pengukuran kadar zat aktif dan dilakukan secara duplo. Plasebo dibuat dengan cara melarutkan gelatin E-200 dalam air panas hingga membentuk larutan. Kemudian ditambahkan Primogel, LHPC LH-11, natrium benzoat, dan diaduk hingga homogen lalu dikeringkan pada suhu 50 oC, dari plasebo tersebut ditimbang 120 mg ke dalam labu 50 mL dan selanjutnya diberikan perlakuan yang sama seperti preparasi contoh.
Batas Deteksi, Batas Kuantitasi, dan Linearitas
Parasetamol dan kafein masing-masing dibuat dengan konsentrasi 10, 20, 40, 70, 120, 160, 180, dan 200% kemudian diukur dengan KCKT. Diperoleh area contoh sebagai sinyal (S) kemudia