CANGKANG UDANG VANNAMEI (Litopenaeus vannamei)
DENGAN METODE GELASI IONIK
DESIE RACHMANIA
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
DESIE RACHMANIA. C34070088. Karakteristik Nano Kitosan Cangkang Udang Vannamei (Litopenaeus vannamei) dengan Metode Gelasi Ionik. Dibimbing oleh PIPIH SUPTIJAH dan AGOES M. JACOEB.
Kemampuan kitosan yang diterapkan dalam berbagai bidang industri modern, misalnya farmasi, biokimia, kosmetika, industri pangan, dan industri tekstil mendorong untuk terus dikembangkannya berbagai penelitian yang menggunakan kitosan, termasuk melakukan modifikasi kitosan secara kimia atau fisik. Sejauh ini sistem pengahantar obat dengan menggunakan kitosan hanya terbatas pada modifikasi kima pada kitosan saja. Oleh karena itu, modifikasi fisik melalui pengaturan ukuran partikel kitosan menjadi hal yang sangat penting. Akan tetapi dalam pembuatan kitosan yang berstabilitas dan berkualitas tinggi, biasanya diperlukan metode yang cukup sulit. Pembuatan nanopartikel dipengaruhi oleh beberapa faktor, antara lain komposisi material dan metode yang digunakan.
Tujuan dari penelitian ini adalah mendapatkan rendemen kitosan tertinggi akibat pengaruh lama waktu perendaman HCl, menentukan proses gelasi ionik terbaik dengan berbagai perlakuan sizing, menentukan karakteristik nanopartikel yang meliputi morfologi, efisiensi, dan ukuran nanopartikel, menganalisa karakteristik partikel kitosan yang dilakukan dengan metode gelasi ionik menggunakan Fourier Transform InfraRed (FTIR) dan Scanning Electron Microscopy (SEM), menentukan metode pembuatan kitosan yang sederhana, dapat diterapkan dengan mudah di laboratorium. Pengujian yang dilakukan meliputi analisis proksimat, mutu kitosan, perhitungan rendemen kitosan dan nano kitosan, analisis Scanning Electron Miscroscopy (SEM), serta analisis Fourier Transform InfraRed (FTIR).
CANGKANG UDANG VANNAMEI (
Litopenaeus vannamei
)
DENGAN METODE GELASI IONIK
Skripsi
Sebagai salah satu syarat untuk mendapatkan gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
Oleh:
DESIE RACHMANIA C34070088
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
LEMBAR PENGESAHAN
Judul : Karakterisasi Nano Kitosan Cangkang Udang Vannamei
(Litopenaeus vannamei) dengan Metode Gelasi Ionik
Nama : Desie Rachmania
NIM : C34070088
Program Sarjana : Teknologi Hasil Perairan
Menyetujui:
Pembimbing I Pembimbing II
NIP. 19531020 1985 03 2 001 NIP. 19591127 1986 01 1 005
Dra. Pipih Suptijah, MBA Dr. Ir. Agoes M. Jacoeb, Dipl.-Biol
Mengetahui:
Ketua Departemen Teknologi Hasil Perairan
NIP. 19580511 1985 03 1 002 Dr. Ir. Ruddy Suwandi, MS., Mphil.
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi yang berjudul ” Karakteristik
Nano Kitosan Cangkang Udang Vannamei (Litopenaeus vannamei) dengan
metode gelasi ionik” adalah karya sendiri dan belum diajukan dalam bentuk
apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau
dikutip dari karya yang diterbitkan dari penulis lain telah disebutkan dalam teks
dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, Agustus 2011
Desie Rachmania
DAFTAR RIWAYAT HIDUP
Penulis dilahirkan di Jakarta, pada tanggal 18 Desember
1989. Penulis merupakan anak bungsu dari dua bersaudara
pasangan Bapak (Alm.) Momon Nurachman dan Ibu Sri
Handayani.
Penulis memulai jenjang formal pada pendidikan di
Sekolah Dasar Islam Pelita dan lulus pada tahun 2001.
Penulis melanjutkan Sekolah Menegah Pertama
di SMP Negeri 41 Jakarta dan lulus pada tahun 2004, selanjutnya penulis
melanjutkan Sekolah Menengah Atas di SMA Negeri 28 Jakarta dan lulus pada
tahun 2007.
Pada tahun 2007 penulis diterima di IPB melalui jalur Seleksi Penerimaan
Mahasiswa Baru (SPMB). Penulis diterima di Departemen Teknologi Hasil
Perairan, Fakultas Perikanan dan Ilmu Kelautan. Selama menjalani pendidikan
akademik di IPB penulis pernah aktif sebagai anggota Himpunan Mahasiswa
Teknologi Hasil Perikanan tahun 2009, Paguyuban Penerima Beasiswa Karya
Salemba Empat Institut Pertanian Bogor tahun 2010 - 2011, asisten praktikum
m.k. Pengembangan KitinKitosan dan m.k. Teknologi Pengolahan Hasil Perairan
tahun ajaran 2010-2011. Penulis juga aktif dalam kepanitiaan kegiatan mahasiswa
di Institut Pertanian Bogor.
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan,
Institut Pertanian Bogor, penulis melakukan penelitian dengan judul
Karakteristik Nano Kitosan Cangkang Udang Vannamei (Litopenaeus vannamei)
dengan Metode Gelasi Ionik dengan dosen pembimbing yaitu
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa, karena
berkat rahmat serta karunia-Nya penulis dapat menyelesaikan skripsi sebagai
tugas akhir yang berjudul Karakteristik Nano Kitosan Cangkang Udang Vannamei
(Litopenaeus vannamei) dengan Metode Gelasi Ionik dengan baik.
Penulis mengucapkan terima kasih kepada semua pihak yang telah
membantu dalam penulisan ini, terutama kepada:
1) Ibu Dr. Pipih Suptijah, MBA dan Bapak Dr. Ir. Agoes M. Jacoeb, Dipl.-Biol,
selaku dosen pembimbing yang telah memberikan bimbingan dan
pengarahannya kepada penulis.
2) Bapak Dr. Ir. Ruddy Suwandi MS., M.Phil selaku Ketua Departemen
Teknologi Hasil Perairan sekaligus dosen penguji yang telah memberikan
nasihat, kritik dan saran dalam penulisan skripsi.
3) Bapak Dr. Ir. Agoes Mardiono Jacoeb,-Dipl. Biol selaku Ketua Program Studi
Teknologi Hasil Perairan atas bimbingan kepada penulis.
4) Mama dan (Alm.) Papa yang selalu memberikan doa, semangat, cinta kasih
dan dukungan yang diberikan, baik moril maupun materil serta kasih sayang
kepada penulis.
5) Febri Ika Suseno, S.St.Pi yang selalu meberikan motivasi, semangat doa dan
perhatiannya kepada penulis.
6) Teman-teman seperjuangan ”Tim Nano ”(Nani, Icha dan Zahid). Terima
kasih atas kebersamaannya.
7) Sahabat - sahabat dan teman seperjuangan: Siska, Ria, Medal, Fasta atas
semangat, bantuan dan canda tawa selama ini.
8) Teman – teman ”Kost Tiara” : Mba Tatay, Fasta, Tatha, Aul, Ayu,dan Desti
atas semangat dan doa yang selalu diberikan.
9) Tim Nano Kitosan: Taufik (THP 45) dan Yunko atas kebersamaan,
kekompakan dan perjuangan menuju PIMNAS.
10)Teman-teman THP 44, 43 dan 45 yang telah mendukung dan memberikan
Penulis menyadari bahwa penulisan tugas akhir ini belum sempurna. Oleh
sebab itu penulis mengharapkan masukan berupa saran dan kritik yang bersifat
membangun dari pembaca dan semoga tulisa ini dapat bermanfaat bagi pihak yang
memerlukannya.
Bogor, Agustus 2011
Hal.
DAFTAR TABEL………. vii
DAFTAR GAMBAR………... viii
DAFTAR LAMPIRAN………. x
1 PENDAHULUAN………... 1
1.1Latar Belakang………... 1
1.2Tujuan Penelitian………... 3
2 TINJAUAN PUSTAKA... 4
2.1 Komposisi Kimia Kulit Udang………. 4
2.2 Karakteristik………... 5
2.2.1 Kitosan………... 5
2.2.2 Nano Kitosan………... 7
2.3 Gelasi Ionik………... 7
2.4 Tripolifosfat (TPP)……….... 8
2.5 Surfaktan………... 9
2.6 Sonikasi………... 9
2.7 Pengeringan Semprot (Spray Dryer)……….... 10
2.8 Scanning Electron Microscopy (SEM)………... 11
2.9 Fourier Transform Infrared (FTIR)………. 12
3 METODOLOGI………... 13
3.1 Waktu dan Tempat Penelitian……….. 13
3.2 Bahan dan Alat………. 13
3.3 Tahap penelitian………... 14
3.3.1 Penelitian Pendahuluan………... 14
3.3.2 Penelitian Utama………... 15
3.4.2.1 Tahapan pembuatan nano kitosan dengan metode gelasi ionik…….………... 15
3.4.1.2 Analisis kadar abu………. 17
3.4.1.3 Analisis kadar lemak………. 18
3.4.1.4 Analisis kadar protein……… 18
3.4.1.4 Analisis kadar karbohidrat (by difference)…...…………. 19
3.4.1 Rendemen Kitosan Cangkang Udang Vannamei (Litopenaeus vannamei)………... 19
3.4.2 Derajat Deasetilasi……….. 19
4 HASIL DAN PEMBAHASAN……… 21
4.1 Penelitian Pendahuluan……….... 21
4.2 Rendemen Kitosan……….. 22
4.3 Mutu Kitosan………... 23
4.4 Penelitian Utama………... 26
4.4.1 Rendemen Kitosan Nanopartikel………. 26
4.4.2 Hasil Analisis Scanning Electron Microscopy (SEM)………… 28
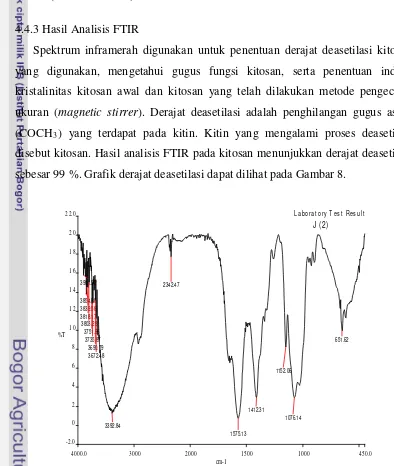
4.4.3 Hasil Analisis Fourier Transform Infrared (FTIR)………….... 35
5 KESIMPULAN DAN SARAN……… 37
5.1 Kesimpulan………... 37
5.2 Saran………. 37
DAFTAR PUSTAKA……….. 38
Nomor Teks Halaman
1 Komposisi kimia kulit udang (Litopenaeus vannamei).………... 4
2 Spesifikasi kitosan niaga……… 6
3 Komposisi kimia kulit udang hasil uji proksimat……….. 21
4 Rendemen kitosan dari cangkang udang terhadap lamanya
waktu perendaman HCl 1N……….. 22
5 Mutu kitosan dari rendemen hasil perendaman 72 jam HCl…….. 24
6 Rendemen kitosan nanopartikel dengan perbedaan perlakuan
alat penegcilan ukuran………. 27
1 Struktur kitosan………... 5
2 Kitosan nanopartikel dengan gelasi ionik……….... 8
3 Proses pembuatan kitosan……… 14
4 Diagram alir pengujian stabilitas nanopartikel kitosan dengan metode gelasi ionik………. 16
5 Grafik hasil rendemen kitosan terhadap pengaruh waktu perendaman HCl ………..………... 23
6 Grafik hasil rendemen kitosan nanopartikel dengan perbedaan perlakuan metode pengecilan ukuran………... 28
7 Hasil analisis uji SEM………... 34
7a. Morfologi partikel kitosan (magnetic stirrer)……….. 34
7b. Morfologi partikel kitosan (ultrasonik)………... 34
7c. Morfologi partikel kitosan (homogenizer)………... 34
Nomor Halaman
1. Analisis kadar air cangkang udang vannamei….………... 43
2. Analisis kadar abu cangkang udang vannamei.………. 43
3. Analisis kadar protein cangkang udang vannamei…….………... 44
4. Analisis kadar lemak cangkang udang vannamei……...………... 45
5. Analisis kadar karbohidrat cangkang udang vannamei secara by difference……….…. 45
6. Data rendemen kitosan udang vannamei………... 46
7. Analisis kadar air kitosan udang vannamei.……….. 46
8. Analisis kadar abu kitosan udang vannamei…….……… 47
9. Analisis kadar protein cangkang udang vannamei……… 48
10.Data hasil perhitungan derajat deasetilasi (DD)……… 48
I PENDAHULUAN
1.1Latar Belakang
Udang merupakan komoditas andalan dan bernilai ekonomis sebagai salah
satu hasil perikanan utama Indonesia. Pusat Data, Statistik dan Informasi
Departemen Kelautan dan Perikanan tahun 2008 menunjukkan ekspor udang
Indonesia meningkat selama periode tahun 2003 – 2007 sebesar 4,15 % yaitu dari
137.636 ton pada 2003 menjadi 160.797 ton pada tahun 2007. Peningkatan
volume ekspor tersebut mendorong peningkatan nilai produksi udang, yaitu dari
US$ 850,222 juta pada 2003 menjadi US$ 1,048 miliar tahun 2007. Nilai ekspor
udang ini mencapai hampir 50 % dari nilai ekspor perikanan sebesar
US$ 2,3 miliar. Selain itu produksi udang juga meningkat sebesar 16,9 % selama
periode 2003 – 2007 yaitu dari 192.926 ton pada 2003 menjadi 352.220 ton pada
tahun 2007.
Sekitar 80 – 90% ekspor udang dilakukan dalam bentuk udang beku tanpa
kepala dan kulit sehingga menghasilkan limbah yang bobotnya mencapai
25 – 30% dari bobot udang utuh (Sudibyo 1991 dalam Maulana 2009). Limbah
udang yang potensial ini mudah sekali rusak karena degradasi enzimatik
mikroorganisme sehingga menimbulkan masalah misalnya pencemaran
lingkungan bagi indutri pengolah dan membahaykan kesehatan. Selain itu limbah
ini sangat menyita ruang sehingga dibutuhkan tempat tertutup yang luas untuk
menampungnya. Disisi lain limbah ini dapat didayagunakan sebagai sumber
bahan mentah penghasil kitin, kitosan dan turunan keduanya yang berdaya guna
dan serta bernilai tinggi.
Kulit udang atau kepiting merupakan bahan baku penghasil kitin dan kitosan.
Kitosan adalah kitin yang telah diasetilasi. Kitosan merupakan polisakarida
dengan struktur yang mirip dengan selulosa (Savant et al. 2000 dalam
Kencana 2009). Terdapat 75% dari berat total udang merupakan bagian kulit dan
kepala. Kulit udang mengandung 15-20% kitin dan kitosan sebesar 50% dari
kandungan kitin, kadar abu sebesar 20% serta kadar protein sebesar 35% pada
basis kering (Kelly et al. 2005 dalam Rini 2010). Studi terhadap kitosan telah
Kemampuan kitosan yang diterapkan dalam berbagai bidang industri modern,
misalnya farmasi, biokimia, kosmetika, industri pangan, dan industri tekstil
mendorong untuk terus dikembangkannya berbagai penelitian yang menggunakan
kitosan, termasuk melakukan modifikasi kitosan secara kimia atau fisik.
Modifikasi kimia menghasilkan perbaikan stabilitas kitosan melalui
fungsionalisasi gugus fungsi yang ada, perbaikan ukuran pori kitosan dengan
menggunakan senyawa porogen, dan dapat menaikkan kapasitas adsorpsi kitosan
apabila kitosan dipadukan dengan polimer lain. Modifikasi fisik pada kitosan
mencakup perubahan ukuran partikel atau butir kitosan menjadi lebih kecil untuk
pemanfaatan yang lebih luas. Oleh karena itu, perkembangan modifikasi fisik
mengarah ke bentuk nanopartikel (Wahyono 2010).
Pembuatan nanopartikel dipengaruhi oleh beberapa faktor, antara lain
komposisi material dan metode yang digunakan. Untuk nanopartikel kitosan,
komposisi material yang digunakan adalah kitosan, TPP dan surfaktan (asam
oleeat). Metode pembuatan nanopartikel merupakan faktor lain yang menentukan
selain komposisi material. Banyak metode yang dikembangkan untuk
menghasilkan nanopartikel dan morfologi yang seragam (Wahyono 2010). Sampai
saat ini penelitian nanopartikel kitosan terus dikembangkan, baik dalam penentuan
komposisi maupun pencarian metode yang sesuai. Akan tetapi dalam pembuatan
kitosan yang berstabilitas dan berkualitas tinggi, biasanya diperlukan metode yang
cukup sulit. Untuk itu, dilakukan teknik atau metode yang prosesnya lebih efisien
dan sederhana untuk memudahkan dalam pembuatan nano kitosan.
Pengujian karakteristik nano kitosan dilakukan dengan proses gelasi ionik,
serta perlakuan pengecilan ukuran (sizing) dilakukan dengan metode magnetic
stirer, metode homogenizer ultrasonik dan metode sonokimia. Metode ini
bertujuan untuk mengetahui dan mendapatkan nano kitosan yang terbaik diantara
ketiga metode tersebut agar nano kitosan yang dihasilkan memiliki stabilitas
konstan, berukuran partikel terkecil, berkualitas baik, serta mendapatkan metode
yang paling sederhana dalam pembuatannya, sehingga dapat meningkatkan skala
1.2Tujuan
Penelitian ini bertujuan untuk
- Mendapatkan rendemen kitosan tertinggi akibat pengaruh lama waktu
perendaman HCl.
- Menentukan proses gelasi ionik terbaik dengan berbagai perlakuan sizing.
- Menentukan karakteristik nanopartikel yang meliputi morfologi, efisiensi,
dan ukuran nanopartikel dengan SEM.
- Menganalisis karakteristik partikel kitosan yang dilakukan dengan metode
gelasi ionik menggunakan Fourier Transform InfraRed (FTIR) dan
Scanning Electron Microscopy (SEM).
- Menentukan metode pembuatan kitosan yang sederhana, dapat diterapkan
2 TINJAUAN PUSTAKA
2.1 Komposisi Kimia Kulit Udang
Untuk kebutuhan ekspor udang beku, bagian tubuh udang yang dibekukan
adalah bagian badan (abdomen) hingga ekor (uropod). Bagian kepala dan dada
(cephaloporax) yang dibungkus oleh kulit udang keras merupakan bagian yang
dibuang oleh industri pembekuan udang. Kulit udang mengandung
25-40 % protein, 30-50% kalsium karbonat dan 15-20 % kitin serta komponen
lain sebagaimana tercantum pada Tabel 1.
Tabel 1 Komposisi kimia kulit udang Penaeus sp.
Komposisi Jumlah (%)
Air 12,86
Protein 32,75
Lemak 2,04
Abu 37,24
Karbohidrat 36,96
Kalsium 13,29
Magnesium 0,85
Fosfor 1,84
Besi 0,02
Mangan 0,0003
Kitin 18
Kalium 0,37
Tembaga 0,005
Natrium 0,436
Seng 0,005
Sulfur 0,419
Sumber: Arlius (1991) dalam Maulana (2007)
Limbah udang merupakan bahan yang mudah busuk karena adanya proses
menyebabkan menurunya mutu komponen yang terdapat dalam limbah, sehingga
apabila komponen tersebut rusak maka akan mengahsilkan produk yang bermutu
rendah. Oleh karena itu perlu diupayakan penanganan limbah yang baik agar tidak
cepat terdegradasi dengan tujuan untuk memperoleh produk yang lebih baik
(Suptijah et al. 1992 dalam Maulana 2007).
2.2 Karakteristik 2.2.1 Kitosan
Kitosan adalah jenis polimer alami yang dihasilkan dari proses deasetilasi
kitin. Kitosan mempunyai sifat yang khas yakni bioaktifis, biodegradasi dan tidak
beracun. Kitosan merupakan jenis polimer alam yang mempunyai rantai tidak
linier dan mempunyai rumus (C6H11NO4)n. Mempunyai sifat tidak
berbau,berwarna putih dan terdiri dari dua jenis polimer yaitu
poli (2-deoksi,2-asetilamin,2-glukosa) dan poli(2-deoksi,2- amino glukosa) yang
berikatan secara beta (1,4). Kitosan larut dalam pelarut organik, HCl encer, HNO3
encer, dan H3PO4 0,5%, tetapi tidak larut dalam basa kuat dan H2SO4. Sifat
kelarutan kitosan ini dipengaruhi oleh bobot molekul dan derajat deasetilasi.
Bobot molekul kitosan beragam, bergantung pada degradasi yang terjadi selama
proses deasetilasi (Sugita 2010). Struktur kitosan dapat dilihat pada Gambar 1.
Gambar 1. Struktur kitosan
(Sumber: Mardliyati 2010)
Parameter mutu kitosan biasanya dilihat dari nilai derajat deasetilsi, kadar air,
kadar abu, bobot molekul, dan viskositas. Viskositas kitosan dipengaruhi oleh
beberapa faktor seperti derajat deasetilasi, bobot molekul, konsentrasi pelarut, dan
suhu. Gel kitosan terjadi karena terbentuknya jaringan tiga dimensi antara molekul
kitosan yang terentang pada seluruh volume gel yang terbentuk dengan
menangkap sejumlah air di dalamnya. Sifat jaringan serta interaksi molekul yang
memperkuat jaringan di dalam gel biasanya digunakan molekul lain yang
berperan sebagai pembentuk ikatan silang (Keuteur 1996).
Penggunaan suhu yang terlalu tinggi (di atas 150 o
Derajat deasetilasi menyatakan banyaknya gugus amino bebas dalam
polisakarida. Kitosan merupakan kitin dengan derajat deasetilasi lebih dari 70%.
Deasetilasi adalah proses pengubahan gugus asetil (-NHCOCH
C) menyebabkan
pemecahan ikatan polimer (depolimerisasi) rantai molekul kitosan sehingga
menurunkan berat molekulnya. Kitosan dengan berat molekul rendah akan lebih
tepat diterapkan sebagai antibakteri, antifungi, antioksidan dan antitumor. Kitosan
menunjukkan sifat-sifat polimer biomedis misalnya nono-toksik, biokompatibel,
dan biodegradable. Struktur kitosan yang mirip dengan selulosa dan
kemampuanya membentuk gel dalam suasana asam, membuat kitosan memiliki
sifat-sifat sebagai matriks dalam sistem pengantar obat (Sutriyo et al. 2005).
Kitosan biasa dipakai sebagai pengantar obat berdasarkan kekuatan mekanik dan
keteruraian hayatinya yang lambat. Kitosan berbentuk gel atau lembaran telah
digunakan sebagai pengantar obat yang merupakan zat antikanker
(Dhanikula et al. 2004).
3) dan rantai
molecular kitin menjadi gugus amina lengkap (-NH2
Tabel 2 Spesifikasi kitosan niaga
) pada kitosan dengan
penambahan NaOH konsentrasi tinggi. Kemampuan kitosan bergantung pada
derajat kimia reaktif yang tinggi gugus aminonya(Kusumaningsih et al. 2004
dalam April 2008).
No Parameter Ciri
1 Ukuran partikel Serbuk sampai bubuk
2 Warna Putih kelabu
3 Kelarutan 97% dalam 1% asam asetat
4 Kadar abu (%) ≤ 2,0
5 Kadar air (%) ≤ 10,0
6 Warna Larutan Tak berwarna
7 N-deasetilasi (%) ≥70,0
2.2.2 Nano Kitosan
Nano kitosan yaitu kitosan yang memiliki pertikel yang berbentuk padat
dengan ukuran sekitar 10 – 1000 nm. Kitosan dalam bentuk nanopartikel ini pun
bersifat netral, tidak toksik, dan memiliki stabilitas yang konstan. Nanopartikel ini
digunakan dalam berbagai rute (aplikasi parental, mucosal misal oral, nasal, dan
ocular mucosa) yang sangat tidak invasive. Dalam sistem pengantaran obat,
nanopartikel berperan sebagai pembawa (carrier) dengan cara melarutkan,
menjebak, mengenkapsulasi, atau menempelkan obat di dalam matriksnya.
Baru-baru ini, nanopartikel yang berasal dari bahan polimer digunakan sebagai sistem
pengantaran obat yang potensial karena kemampuan penyebarannya di dalam
organ tubuh selama waktu tertentu, dan kemampuannya untuk mengantarkan
protein atau peptida (Mohanraj dan Chen 2006).
Nanopartikel dari bahan polimer yang biodegradable dan kompatibel
merupakan salah satu perkembangan baik untuk pembawa obat karena
nanopartikel diduga terserap secara utuh di dalam system pencernaan setelah
masuk ke dalam tubuh (Wu et al. 2005 dalam Wahyono 2010). Tujuan utama
dalam melakukan rancangan nanopartikel sebagai sistem pengantar obat adalah
untuk mengatur ukuran partikel, sifat-sifat permukaan, dan pelepasan zat aktif
pada tempat yang spesifik di dalam tubuh sebagi sasaran pengobatan. Aplikasi
nanoteknologi membuat revolusi baru dalam dunia industri dan diyakini
pemenang persaingan global di masa yang akan datang adalah negara-negara yang
dapat menguasai nanoteknologi. Ruang lingkup nanoteknologi meliputi usaha dan
konsep untuk menghasilkan material atau bahan berskala nanometer,
mengeksplorasi dan merekayasa karakteristik material atau bahan tersebut, serta
mendesain ulang material atau bahan tersebut ke dalam bentuk, ukuran dan fungsi
yang diinginkan.
2.3 Gelasi ionik
Gelasi atau pembentukan gel merupakan gejala penggabungan atau
pengikatan silang rantai-rantai polimer membentuk jaringan tiga dimensi yang
sinambung dan dapat memerangkap air di dalamnya menjadi suatu struktur yang
kompak dan kaku yang tahan terhadap aliran bertekanan (Fardiaz 1989 dalam
(Wang et al. 2004 dalam Napthaleni 2010). Hidrogel dapat diklasifikasikan
menjadi hidrogel kimia dan hidrogel fisika. Contoh hidrogel kimia adalah hidrogel
kitosan yang berikatan silang secara kovalen (Keuteur 1996). Larutan kitosan
pada batas konsentrasi tertentu dalam asam asetat 1% dapat membentuk gel. Gel
kitosan yang terbentuk dapat diperbaiki sifatnya (menurunnya waktu gelasi dan
meningkatnya kekuatan mekanik gel) dengan penambhan PVA (Wang et al. 2004
dalam Wahyono 2010).
Metode yang paling umum dalam pembuatan nanopartikel melalui proses
gelasi ionik yaitu metode magnetic stirer, metode homogenizer ultrasonik dan
metode high speed. Banyak penelitian difokuskan untuk membuat nanopartikel
dari polimer yang biodegradable: kitosan, gelatin, dan sodium alginat. Salah satu
contoh metode gelasi ionik ini adalah mencampurkan polimer kitosan dengan
polianion sodium tripoliposfat yang menghasilkan interaksi antara muatan positif
pada gugus amino kitosan dengan muatan tripolifosfat. Tripolifosfat dianggap
sebagai zat pengikat silang yang paling baik (Mohanraj dan Chen 2006).
Proses terbentuknya kitosan nanopartikel dengan gelasi ionik dapat dilihat pada
Gambar 2.
Sizing Gelasi Ionik
Chitosan solution chitosan nanoparticle
Gambar 2 Kitosan nanopartikel dengan gelasi ionik
2.4 Tripolifosfat (TPP)
Pembentukan ikatan silang ionik salah satunya dapat dilakukan dengan
menggunakan senyawa tripolifosfat. Tripolifosfat dianggap sebagai zat pengikat
silang yang paling baik. Shu dan Zhu (2002) melaporkan bahwa penggunaan
tripolifosfat untuk pembentukan gel kitosan dapat meningkatkan mekanik dari gel
yang terbentuk. Hal ini karena tripolifosfat memiliki rapatan muatan negatif yang
tinggi sehingga interaksi dengan polikationik kitosan akan lebih besar. Menurut
Yongmei dan Yumin (2003) dalam Wahyono (2010), pembentukan nanopartikel
pengikat silang akan memperkuat matriks nanopartikel kitosan. Dengan semakin
banyaknya ikatan silang yang terbentuk antara kitosan dan TPP maka kekuatan
mekanik matriks kitosan akan meningkat sehingga partikel kitosan menjadi
semakin kuat dan keras, serta semakin sulit untuk terpecah menjadi bagian -
bagian yang lebih kecil (Wahyono 2010).
2.5 Surfaktan
Penelitian nanopartikel kitosan termodifikasi menggunakan emulsifier yang
merupakan senyawa pengikat silang dan surfaktan. Berdasarkan penelitian
Silva et al. (2006) diketahui bahwa penambahan surfaktan dapat memperkecil
ukuran partikel kitosan. Zat pengikat silang yang sering digunakan adalah
glutaraldehida, sedangkan surfaktan yang banyak dipakai adalah surfaktan
nonionik (Tween 80 dan Span 80). Beberapa contoh surfaktan nonionik adalah
Tween 80 (polietilena sorbitan monooleat) dan Span 80 (sorbitan monooleat).
Tween 80 dan Span 80 bersifat nontoksik yang umumnya digunakan sebagai
emulsifier dan penstabil pada bidang pangan dan farmasi. Tarirai (2005) dalam
Wahyono (2010) telah melakukan penelitian tentang pembuatan gel kitosan
sebagai pembawa obat ibuprofen dengan menggunakan senyawa pengikat silang
tripolifosfat dan senyawa surfaktan yang sekaligus berfungsi sebagai pengikat
silang, yaitu asam oleat, sodium laurit sulfat (SLS) dan Tween 80.
2.6 Sonikasi
Gelombang ultrasonik merupakan gelombang mekanik longitudinal yang
memiliki frekuensi 20 KHz ke atas. Pada alat Ultrasonics Processor Cole-Parmer,
spesifikasi yang dapat diperoleh yaitu frekuensi yang tidak bisa diubah-ubah
sebesar 20 KHz dan daya sebesar 130 watt. Pada alat tersebut juga terdapat waktu
sonikasi, amplitude, dan pulsa gelombang yang dapat diatur sesuai kebutuhan.
Gelombang suara ultrasonik dapat didengar dan digunakan sebagai alat
komunikasi oleh pendengaran beberapa jenis binatang, seperti anjing, kelelawar
dan lumba - lumba (Tipler 1998).
Batas atas rentang ultrasonik mencapai 5 MHz untuk gas dan mencapai
500 Mhz untuk cairan dan padatan. Penggunaan ultrasonik berdasarkan
beramplitudo rendah (frekuensi lebih tinggi) dan berkaitan dengan efek fisik
medium pada gelombang dan biasanya disebut “gelombang energi rendah” atau
“ultrasonik frekuensi tinggi”. Biasanya, gelombang amplitudo rendah digunakan
dalam tujuan analisis untuk mengukur kecepatan dan koefisien absorpsi
gelombang dalam medium pada rentang 2 sampai 10 MHz. Yang kedua adalah
gelombang energi tinggi (frekuensi rendah), yang dikenal dengan “ultrasonik
energi tinggi” dan terletak antara 20 – 100 KHz. Jenis kedua ini digunakan untuk
pembersihan, pembentukan plastik, dan yang terbaru adalah untuk sonokimia
(Mason et al. 2002 dalam Komariah 2010).
Efek kimia dari gelombang ultrasonik, tidak secara langsung berinteraksi
dengan molekul – molekul untuk menginduksi suatu perubahan kimiawi. Ini
karena panjang gelombang ultrasonik yang terlalu panjang jika dibandingkan
dengan panjang gelombang molekul – molekul. Interaksi gelombang ultrasonik
dengan molekul – molekul terjadi melalui media perantara berupa cairan.
Gelombang yang dihasilkan oleh tenaga listrik (lewat tranduser) diteruskan oleh
media cair ke medan yang dituju melalui fenomena kavitasi akustik
(Wardiyati et al. 2004 dalam Wulandari 2010), yang menyebabkan terjadinya
temperatur dan tekanan lokal ektrem dalam cairan dimana reaksi terjadi.
2.7 Pengeringan Semprot (spray drying)
Metode pengerinagn semprot (spray drying) merupakan metode yang paling
mudah dan sederhana untuk mengenkapsulasi suatu bahan karena larutan suspensi
yang akan dinanoenkapsulasi cukup dimasukkan ke dalam alat pengering semprot
dengan serbuk nanokapsul sebagai produk. Metode ini dapat dilakukan melalui
beberapa tahap, yaitu (1) produk yang berupa cairan didispersikan dalam
penyemprot (sprayer), (2) kontak antara semprotan dengan udara panas, (3)
pengeringan semprotan, dan (4) pemisahan antara produk kering (aliran serbuk
bebas) dan udara.
Keuntungan nanoenkapsulasi dengan metode pengeringan semprot ini
diantaranya ialah (1) meningkatkan stabilitas serbuk, (2) teknik yang dapat
dipercaya, (3) biaya yang murah, (4) menghasilkan serbuk berupa mikrokapsul
dilakukan satu tahap, atau dengan kata lain prosesnya sinambung (continuous),
dan (7) merupakan metode yang fleksibel, dapat digunakan untuk enkapsulasi
polimer – polimer yang berbeda dan suhu berbeda (Yundhana 2008).
2.8 Scanning Electron Microscopy (SEM)
Mikroskop merupakan alat untuk melihat benda yang berukuran kecil (mm).
Salah satu jenis mikroskop adalah SEM (scanning electron microscopy). Scanning
Electron Microscopy (SEM) menggunakan elektron dan cahaya tampak sebagai
sumber cahayanya. Elektron menghasilkan gelombang yang lebih pendek
dibandingkan cahaya foton dengan ukuran 0,1 nm dan menghasilkan gambar
dengan resolusi yang lebih baik (Lee 1993 dalam Rini 2010).
Scanning electron microscopy (SEM) menghasilkan gambar dari suatu
permukaan spesimen dengan kedalaman fokus 500 kali lebih besar dibandingkan
mikroskop cahaya. Gambar yang dihasilkan memiliki fokus yang baik pada
kedalaman spesimen, sehingga gambar yang dihasilkan berupa bentuk tiga
dimensi spesimen. Hal ini disebabkan oleh ketajaman pancaran elektron yang
menyinari spesimen. Mikroskop SEM memiliki perbesaran hingga 50.000 kali
(Fujita et al. dalam Rini 2010).
Mikroskop SEM memiliki lensa yang berbeda dengan mikroskop cahaya.
Bagian electron gun berfungsi memancarkan elektron. Condensing lenses
berfungsi untuk memantulkan elektron. Lensa yang berdekatan dengan sampel
adalah lensa objek. Pancaran elektron yang mengenai permukaan sampel
diteruskan oleh detektor, sehingga penampakan permukaan sampel dapat terlihat
pada monitor (Chandler 1980 dalam Rini 2010).
Elektron bermuatan negatif sehingga untuk mengamati permukaan sampel,
diperlukan pelapis sampel yang bersifat konduktor. Pelapis yang umumnya
digunakan antara lain platina, emas, dan perak. Namun, platina relatif mahal
dibandingkan dengan emas dan perak. Perak memiliki harga yang relatif lebih
murah dibandingkan dengan platina dan emas, namun memiliki daya konduktor
yang kurang baik. Sehingga emas lebih banyak digunakan sebagai pelapis sampel
2.9 FTIR (Fourier Transform InfraRed)
FTIR (Fourier Transform InfraRed) merupakan suatu metode spektroskopi IR.
Spektroskopi InfraRed (IR) dapat mengidentifikasi kandungan gugus kompleks
dalam senyawa tetapi tidak dapat menentukan molekular unsur penyusunnya.
Pada spektroskopi IR, radiasi IR dilewatkan pada sampel. Sebagian dari radiasi IR
diserap oleh sampel dan sebagian lainnya diteruskan. Jika frekuensi dari suatu
fibrasi spesifik sama dari frekunsi radiasi IR yang langsung menuju molekul,
molekul akan menyerap radiasi tersebut. Spektrum yang dihasilkan
menggambarkan absoprsi dan transmisi molekular, membentuk sidik jari
molekular suatu sampel (Kencana 2009).
Sistem optik Spektrofotometer FTIR dilengkapi dengan cermin yang bergerak
tegak lurus dan cermin diam. Dengan demikian radiasi infra merah akan
menimbulkan perbedaan jarak yang ditempuh menuju cermin yang bergerak (M)
dan jarak cermin yang diam (F). Perbedaan jarak tempuh radiasi tersebut adalah 2
yang selanjutnya disebut sebagai retardasi (δ). Hubungan antara intensitas radiasi IR yang diterima detektor terhadap retardasi disebut sebagai interferogram.
Sedangkan sisitem optik dari Spektrofotometer IR yang didasarkan atas
bekerjanya interferometer disebut sebagai sistim optik Fourier Transform
Infra Red.
Pada sistim optik FTIR digunakan radiasi LASER (Light Amplification by
Stimulated Emmision of Radiation) yang berfungsi sebagai radiasi yang
diinterferensikan dengan radiasi infra merah agar sinyal radiasi infra merah yang
diterima oleh detector secara utuh dan lebih baik. Detektor yang digunakan dalam
Spektrofotometer FTIR adalah TGS (Tetra Glycerine Sulpahte) atau MCT
(Mercury Cadmium Telluride). Detektor MCT lebih banyak digunakan karena
memiliki beberapa kelebihan disbanding detector TGS, yaitu memberikan respon
yang lebih baik pada frekuensi modulasi tinggi, lebih sensitif, lebih cepat, tidak
dipengaruhi oleh temperatur, sangat selektif terhadap energi vibrasi yang diterima
dari radiasi infra merah.
3 METODOLOGI
3.1 Waktu dan Tempat Pelaksanaan
Penelitian ini dilaksanakan pada bulan Febuari 2011 sampai April 2011.
Pembutan kitosan dilakukan di Laboratorium Biokimia Hasil Perairan,
Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan,
Institut Pertanian Bogor. Pengujian analisis Proksimat Kitosan dilakukan di Pusat
Antar Universitas, Institut Pertanian Bogor. Pembuatan nano kitosan dilakukan
dengan gelasi ionik dan perlakuan pengecilan ukuran (sizing) dengan metode
magnetic stirer dilakukan di Laboratorium Biokimia Hasil Perairan, Departemen
Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut
Pertanian Bogor. Pembuatan nano kitosan menggunakan metode homogenizer
ultrasonik dilakukan di Laboratorium Kimia Fisik, Departemen Kimia, Fakultas
Matematikan dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Pembuatan
nano kitosan menggunakan metode sonikasi dilakukan di Laboratorium Biofisik,
Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut
Pertanian Bogor. Pengujian nano kitosan dengan SEM dilakukan di Pusat
Penelitian dan Pengembagan Kehutanan, Bogor dan Laboratorium Geologi
Kuarter, Institut Teknologi Bandung. Pengujian FTIR (Fourier Transform
InfraRed) dilakukan di Laboratorium Terpadu, Universitas Islam Negeri,
Tangerang.
3.2 Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah cangkang udang vannamei
(Litopenaeus vannamei), aquades, asam asetat 0,3%, dan tripoliphospat
(TPP) 0,1 %, dan surfaktan (Tween 80) 0,1 %.
Alat yang digunakan dalam penelitian ini adalah beaker glass, timbangan
digital, gelas ukur, kertas pH, kompor listrik, saringan, alat pengaduk, termometer,
magnetic stirer, homogenizer ultrasonik, Ultrasonics Processor (Cole-Parmer 20
3.3 Tahap Penelitian
Tahapan yang dilakukan dalam penelitian ini yaitu dimulai dari penelitian
pendahuluan dengan membuat kitosan dan pengujian proksimat kitosaan.
Penelitian utama membuat nano kitosan dengan perlakuan perbedaan pengecilan
ukuran menggunakan metode gelasi ionik, dan pengujian serta menganalisis
karakteristik nanopartikel. Adapun proses penelitian nano kitosan ini dapat dilihat
sebagai berikut.
3.3.1 Penelitian pendahuluan
Penelitian pendahuluan terdiri dari uji proksimat kitosan dari kulit udang
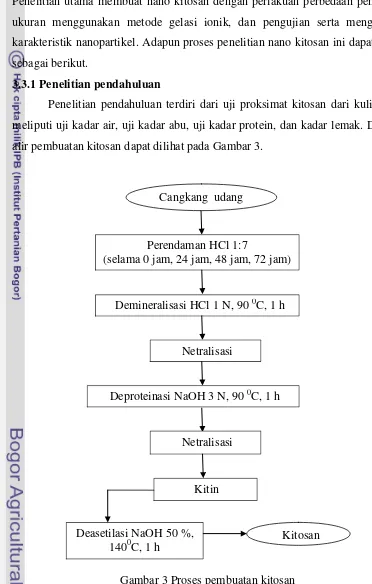
meliputi uji kadar air, uji kadar abu, uji kadar protein, dan kadar lemak. Diagram
alir pembuatan kitosan dapat dilihat pada Gambar 3.
Gambar 3 Proses pembuatan kitosan
(Sumber : Suptijah et al. 1992)
Cangkang udang
Demineralisasi HCl 1 N, 90 0C, 1 h
Netralisasi
Deproteinasi NaOH 3 N, 90 0C, 1 h
Netralisasi
Kitin
Deasetilasi NaOH 50 %, 1400C, 1 h
Kitosan Perendaman HCl 1:7
Pembuatan kitosan diawali dengan perendaman kulit udang dalam larutan
HCl 1 N dengan perlakuan waktu perendaman 0 jam, 24 jam, 48 jam dan 72 jam.
Setelah itu, dilakukan demineralisasi dengan HCl 1 N, pada suhu 90 °C selama 60
menit. Setelah 60 menit, dilakukan netralisasi menggunakan aquades sampai pH
netral. Kemudian dilakukan deproteinasi dengan NaOH 3 N, pada suhu 90 °C
selama 60 menit, dan dilakukan kembali netralisasi sampai pH netral untuk
mendapatkan kitin. Setelah itu, dilakukan deasetilasi dengan NaOH 50 %, pada
suhu 140 % selama 60 menit dan didapatkan kitosan.
3.3.2 Penelitian Utama
Perlakuan perendaman kulit udang yang menghasilkan rendemen kitosan
tertinggi dilanjutkan dalam penelitian utama. Penelitian utama meliputi tahapan
pembentukan gel yang lunak berantai panjang lurus dari 0,2 gr kitosan 0,2 % yang
dilarutkan dalam 100 ml asam asetat 0,3%. Hal ini bertujuan agar dengan mudah
memutuskan polimer tersebut. Kemudian dilakukan pencampuran bahan-bahan
dengan terlebih dahulu menentukan konsentrasi bahan (kitosan, asam oleat, dan
TPP) yang akan dibentuk menjadi emulsi cair.
3.3.2.1 Tahapan pembuatan nano kitosan dengan metode gelasi ionik
Kitosan yang telah dilarutkan dalam asam asetat, yang memiliki bentuk gel
lunak berantai panjang lurus, diambil sebanyak 50 ml. Setelah itu, dilakukan
pembuatan nanopartikel kitosan dengan gelasi ionik dan perlakuan pengecilan
ukuran (sizing) dengan metode magnetic stirer, metode homogenizer ultrasonik
dan metode sonikasi 60 menit. Kemudian ditambahkan 25 ml emulsifier (Tween
80) 0,2 % yang dapat memisahkan gel antara gel satu dengan gel lainnya.
Surfaktan (Tween 80) diberikan dengan cara tetes demi tetes ke dalam kitosan
yang telah mengalami pemotongan, dan didiamkan memutar selama 30 menit.
Setelah itu, ditambahkan 10 ml tripoliphospat 0,1 % yang bertujuan agar ukuran
partikel yang dihasilkan tetap stabil. Kemudian didiamkan selama 30 menit.
3.3.2.2 Tahapan pengujian dan analisis sifat karakteristik nano kitosan
Sampai tahap ini kemudian dilakukan analisis karakterisasi nanopartikel yang
dihasilkan dengan SEM untuk mengetahui karakteristik, ukturan dan morfologi
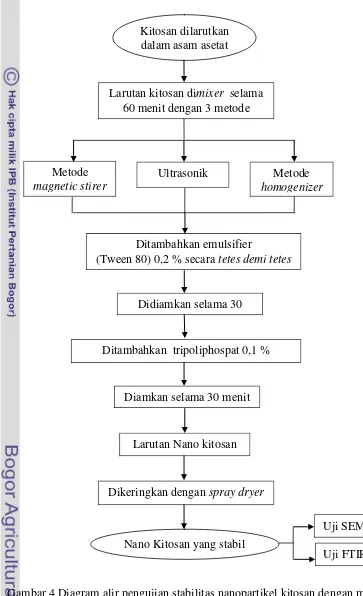
Diagram alir pengujian stabilitas nanopartikel kitosan dengan metode gelasi ionik
dapat dilihat pada Gambar 4.
Gambar 4 Diagram alir pengujian stabilitas nanopartikel kitosan dengan metode gelasi ionik
Kitosan dilarutkan dalam asam asetat
Larutan kitosan dimixer selama 60 menit dengan 3 metode
Metode
magnetic stirer
Ultrasonik
Ditambahkan emulsifier
(Tween 80) 0,2 % secara tetes demi tetes
Diamkan selama 30 menit Ditambahkan tripoliphospat 0,1 %
Didiamkan selama 30
Larutan Nano kitosan
Dikeringkan dengan spray dryer
Nano Kitosan yang stabil
Uji SEM Metode
homogenizer
3.4 Analisis Fisik dan Kimia Sampel
Analisis yang dilakukan untuk kitosan pada penelitian ini antara lain yaitu
analisis fisik dan kimia. Analisis fisik pada kitosan dilakukan perhitungan
rendemen kitosan dan nilai derajat deasetilasi. Analisis kimia yang dilakukan
yaitu analisa proksimat meliputi analisis kadar air, lemak, protein, abu, dan
karbohidrat (by difference).
3.4.1 Analisis Proksimat
Analisis proksimat merupakan suatu analisis yang dilakukan untuk
mengetahui komposisi kimia yang ada pada suatu bahan. Analisis proksimat yang
dilakukan meliputi:
3.4.1.1Analisis kadar air (AOAC 1995)
Tahap pertama yang dilakukan untuk menganalisis kadar air adalah
mengeringkan cawan porselen dalam oven pada suhu 105 oC selama 1 jam.
Cawan tersebut diletakkan ke dalam desikator (kurang lebih 15 menit) dan
dibiarkan sampai dingin kemudian ditimbang. Cawan tersebut ditimbang kembali
hingga beratnya konstan. Sebanyak 5 gram contoh dimasukkan ke dalam cawan
tersebut, kemudian dikeringkan dengan oven pada suhu 105 oC selama 5 jam,
kemudian cawan dimasukkan ke dalam desikator sampai dingin dan selanjutnya
ditimbang kembali.
Keterangan:
B = berat sampel (gram) B1
B
= berat (sampel+cawan) sebelum dikeringkan 2
3.4.1.2Analisis kadar abu (AOAC 1995)
= berat (sampel+cawan) setelah dikeringkan
Cawan pengabuan dikeringkan di dalam oven selama 1 jam pada
suhu 600 oC, kemudian didinginkan selama 15 menit di dalam desikator dan
ditimbang hingga didapatkan berat yang konstan. Sampel sebanyak 5 gram
dimasukkan ke dalam cawan pengabuan dan dipijarkan di atas nyala api hingga
tidak berasap lagi. Setelah itu dimasukkan ke dalam tanur pengabuan dengan suhu
Kadar abu ditentukan dengan rumus:
Kadar abu (berat basah)
3.4.1.3 Analisis kadar lemak (AOAC 1995)
Contoh seberat 5 gram (W1) dimasukkan ke dalam kertas saring pada kedua
ujung bungkus ditutup dengan kapas bebas lemak dan selanjutnya sampel yang
telah dibungkus dimasukkan ke dalam labu lemak yang sudah ditimbang
berat tetapnya (W2) dan disambungkan dengan tabung Soxhlet. Selongsong lemak
dimasukkan ke dalam ruang ekstraktor tabung Soxhlet dan disiram dengan
pelarut lemak (n-heksana), kemudian dilakukan refluks selama 6 jam. Pelarut
lemak yang ada dalam labu lemak didestilasi hingga semua pelarut lemak
menguap. Pada saat destilasi pelarut akan tertampung di ruang ekstraktor, pelarut
dikeluarkan sehingga tidak kembali ke dalam labu lemak, selanjutnya labu lemak
dikeringkan dalam oven pada suhu 105 oC, setelah itu labu didinginkan dalam
desikator sampai beratnya konstan (W3
Perhitungan kadar lemak : % Kadar lemak = ).
= Berat labu lemak kosong (gram) 3
3.4.1.4Analisis kadar protein (AOAC 1995)
= Berat labu lemak dengan lemak (gram)
Tahap-tahap yang dilakukan dalam analisis protein terdiri dari
tiga tahap, yaitu destruksi, destilasi, dan titrasi. Pengukuran kadar protein
dilakukan dengan metode mikro Kjeldahl. Sampel ditimbang sebanyak 0,25 gram,
kemudian dimasukkan ke dalam labu Kjeldahl 100 ml, lalu ditambahkan satu butir
kjeltab dan 3 ml H2SO4 pekat. Contoh didestruksi pada suhu 410 oC selama
kurang lebih 1 jam sampai larutan jernih lalu didinginkan. Setelah dingin,
ke dalam labu Kjeldahl ditambahkan 50 ml akuades dan 20 ml NaOH 40 %,
kemudian dilakukan proses destilasi dengan suhu destilator 100 oC. Hasil destilasi
ditampung dalam labu Erlenmeyer 125 ml yang berisi campuran 10 ml asam borat
(H3BO3) 2 % dan 2 tetes indicator bromcherosol green-methyl red yang berwarna
hijau kebiruan, maka proses destilasi dihentikan. Lalu destilat dititrasi dengan
HCl 0,1 N sampai terjadi perubahan warna merah muda. Volume titran dibaca dan
dicatat. Larutan blanko dianalisis seperti contoh.
Kadar protein dihitung dengan rumus sebagai berikut :
%N =
Keterangan : Fp = Faktor pengenceran fk = 6,25
3.4.1.5Analisis kadar karbohidrat (AOAC 1995)
Analisis karbohidrat dilakukan secara by difference, yaitu hasil pengurangan
dari 100 % dengan kadar air, kadar abu, kadar protein dan kadar lemak, sehingga
kadar karbohidrat tergantung pada faktor pengurangannya. Hal ini karena
karbohidrat sangat berpengaruh terhadap zat gizi lainnya. Analisis karbohidrat
dapat dihitung dengan menggunakan rumus:
% Karbohidrat = 100% - (kadar air + kadar abu + kadar lemak + kadar protein)
3.4.2 Rendemen Kitosan Cangkang Udang Vannamei (Litopenaeus vannamei)
Rendemen merupakan persentasi dari perbandingan serbuk kitosan terhadap
bobot kulit udang sebelum mengalami perlakuan. Perhitungan persentase
rendemen dengan rumus sebagai berikut:
3.4.3 Derajat Deasetilasi (Domsay 1985)
Kitosan sebanyak 0,2 gram digerus dengan KBr dalam mortar agate
sampai homogen, kemudian dimasukkan dalam cetakan pelet, dicetak dengan
dipadatkan dan divakum sampai optimum, selanjutnya pelet ditempatkan dalam
sel dan dimasukkan ke dalam tempat sel pada spektrofotometer inframerah
IR-408 yang sudah dinyalakan dan stabil, Kemudian tombol pendeteksian ditekan,
akan muncul histogram FTIR pada rekorder yang memunculkankan
puncak-puncak dari gugus fungsi yang terdapat pada sampel kitosan. Histogram yang
analisis kuantitatif derajat deasetilasi dari kitosan.
Pengukuran derajat deasetilasi berdasarkan kurva yang tergambar oleh
spektrofotometer. Puncak tertinggi (P0) dan puncak terendah (P) dicatat dan
diukur dengan garis dasar yang dipilih. Nisbah absorbansi dihitung dengan
rumus:
Keterangan:
P0
dengan panjang gelombang 1.655cm
= Jarak antara garis dasar dengan garis singgung antara dua puncak tertinggi -1
atau 3.450 cm-1
P = Jarak antara garis dasar dengan lembah terendah dengan panjang gelombang .
1.655cm-1 atau 3.450 cm-1
Perbandingan absorbansi pada 1.655cm .
-1 dengan absorbansi 3.450 cm-1
digandakan satu per standar N-deasetilasi kitosan (1,33). Dengan mengukuran
absorbansi pada puncak yang berhubungan, nilai persen N-deasetilasi dapat
dihitung dengan rumus:
Keterangan: A1.655 = Absorbansi pada panjang gelombang 1.655 cm-1
A
.
3.450 = Absorbansi pada panjang gelombang 3.450 cm-1
4 HASIL DAN PEMBAHASAN
4.1 Penelitian Pendahuluan
Pada penelitian pendahuluan dilakukan uji proksimat kulit udang. Uji
proksimat kulit udang yang dilakukan pada penelitian ini meliputi penentuan
kadar air, kadar lemak, kadar protein dan kadar abu. Berdasarkan uji proksimat,
kulit udang vanamei memiliki kadar air yakni 15,04 % (bb). Kadar air cangkang
udang Penaeus notabilis berdasarkan penelitian Emmanuel et al. (2008)
sebesar 13,3%. Perbedaan kadar air tersebut dipengaruhi oleh perbedaan jenis
udang dan tingkat kekeringan sampel yang digunakan pada penelitian.
Berdasarkan uji proksimat, kulit udang vanamei memiliki kadar lemak
sebesar 0,57% (bb), hal ini menunjukan bahwa kadar lemak pada kulit udang
tergolong rendah. Menurut literatur kadar lemak pada kulit udang yakni 9,8% (bk)
(Ravichandran et al. 2009). Perbedaan kadar lemak dipengaruhi oleh jenis udang
dan fase hidup udang saat panen. Udang pada fase molting mengandung
kadar lemak yang lebih tinggi (Cuzon dan Guillaume 2001 dalam Rini 2010).
Hasil analisis kadar protein dan kadar abu kulit udang vanamei menunjukkan
nilai yang relatif sama dengan hasil penelitian Ravichandran et al. 2009.
Komposisi kimia kulit udang vanamei hasil penelitian dapat dilihat pada Tabel 3.
Tabel 3 Komposisi kimia kulit udang hasil uji proksimat
Komposisi Jumlah (%)
Kadar protein kulit udang vanamei sebesar 34,69 % (bb). Menurut penelitain
yang dilakukan oleh Kim et al. (2011) kadar protein cangkang udang
Litopenaeus vannamei sebesar 40,35% (bb). Kadar abu pada kulit udang
kadar abu yang diteliti oleh Ravichandran et al. (2009) sebesar 21,5% (bk).
Perbedaan nilai kadar abu diduga dapat disebabkan oleh perbedaan hábitat dan
lingkungan hidup.
Hasil perhitungan kadar karbohidrat dengan metode by difference
menunjukkan bahwa cangkang udang vannamei mengandung karbohidrat sebesar
31,75%. Hasil perhitungan karbohidrat dengan metode by difference ini
merupakan metode penentuan kadar karbohidrat dalam bahan pangan secara
kasar, dimana serat kasar juga terhitung sebagai karbohidrat (Winarno 2008).
4.2 Rendemen Kitosan
Rendemen kitosan ditentukan berdasarkan persentase berat kitosan yang
dihasilkan terhadap bahan baku kulit udang kering dengan lamanya
waktu perendaman HCl. Rendemen kitosan dari kulit udang yang diperoleh
dengan perlakuan waktu perndaman HCl 1 N selama 0 jam, 24 jam, 48 jam, dan
72 jam tertera pada Tabel 4 dan Gambar 5.
Tabel 4 Rendemen kitosan dari cangkang udang terhadap lamanya waktu perendaman HCl 1 N
Rendemen yang diperoleh untuk setiap perlakuan 11,43% - 13,87%. Hasil
percobaan Suptijah et al. (1992) menunjukkan rendemen kitin kitosan yang
diperoleh dari limbah udang 20% - 30%.
Perlakuan waktu perendaman HCl 1 N yang berbeda memberikan
pengaruh terhadap rendemen kitosan tersebut. Perlakuan dengan perendaman
HCl 1 N (72 jam) menghasilkan rendemen tertinggi yakni sebesar 13,50%.
Perlakuan waktu perendaman HCl 1 N (0 jam) menghasilkan rendemen terendah
yakni sebesar 11,57 %. Hal ini dipengaruhi oleh kadar air pada kitosan tersebut
Lampiran 7. Grafik rendemen kitosan menurut waktu perendaman dengan HCl
dapat dilihat pada Gambar 5.
Gambar 5 Grafik rendemen kitosan terhadap pengaruh waktu perendaman HCl
Perlakuan perendaman dengan HCl 1 N yang berbeda memberikan pengaruh
terhadap rendemen kitosan. Mineral memiliki sifat larut asam, oleh karena itu
perendaman cangkang udang dengan HCl 1 N menyebebkan mengembangnya
matrik cangkang udang sehingga memudahkan pelarut masuk ke dalaam matriks.
Berdasarkan hal tersebut, waktu perendaman (retention time) kulit udang di dalam
larutan HCl 1 N akan mempengaruhi penurunan kadar mineral pada proses
pembuatan kitin. Semakin lama waktu perendaman, maka akan menghasilkan
semakin banyak rendemen dari kitosan. Hal ini dikarenakan, perendaman
menyebabkan terbukanya pori-pori cangkang udang yang maksimal, sehingga
ruang-ruang yang terbentuk memudahkan dicapai oleh pengestrak (HCl), dengan
demikian mineral mudah terlepas atau terekstrak dengan optimum (Suptijah 1992
dalam Ariesta 2008).
4.3 Mutu kitosan
Kitosan harus memiliki mutu yang baik, dan pengukurannya dapat dilihat dari
ukuran partikel, warna larutan, kadar air, kadar abu, dan kadar nitrogen. Setelah
dihasilkan rendemen kitosan terbanyak dan mutu yang memenuhi persyaratan
Protan Biopolimer (Suptijah et al. 1992). Berdasarkan hasil analisa terhadap
rendemen kitosan tertinggi, didapatkan mutu kitosan yang dapat dilihat pada
Tabel 5.
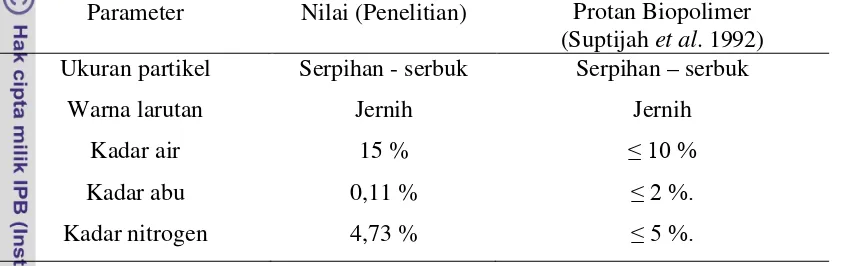
Tabel 5 Mutu kitosan dari rendemen hasil perendaman 72 jam HCl 1 N
Parameter Nilai (Penelitian) Protan Biopolimer
(Suptijah et al. 1992)
Ukuran partikel Serpihan - serbuk Serpihan – serbuk
Warna larutan Jernih Jernih
Kadar air 15 % ≤ 10 %
Kadar abu 0,11 % ≤ 2 %.
Kadar nitrogen 4,73 % ≤ 5 %.
Berdasarkan Tabel 5 dapat dilihat bahwa ukuran partikel pada kitosan dari
kulit udang berupa serpihan – serbuk. Hal ini sesuai dengan Suptijah et al. (1992)
yaitu ukuran partikel pada kitosan berupa serpihan – serbuk. Pada proses
pembuatan kitosan dengan ektraksi bahan baku terlihat hancur. Warna larutan
kitosan tersebut jernih, yang berarti tidak ada zat pengotor yang menempel pada
permukaan kitosan.
Kadar abu merupakan parameter untuk mengetahui mineral yang terkandung
dalam suatu bahan yang mencirikan keberhasilan proses demineralisasi yang
dilakukan. Kadar abu kitosan hasil penelitian ini yaitu 0,11%. Hal ini
menunjukkan bahwa kitosan yang dihasilkan telah memenuhi standar mutu sesuai
ketentuan Protan Biopolimer, yakni sebesar ≤ 2 %. Kadar abu ini dipengaruhi
proses pengadukan yang dilakukan selama proses pembuatan kitosan. Pada proses
tersebut dilakukan pengadukan yang cukup kostan sehingga kadar abu dari kedua
kitosan tersebut cukup rendah.
Kadar abu yang rendah menunjukan kandungan mineral yang rendah.
Semakin rendah kadar abu yang dihasilkan maka mutu dan tingkat kemurnian
kitosan akan semakin tinggi. Selain itu proses pencucian yang baik dan
diperolehnya pH netral, juga berpengaruh terhadap kadar abu. Dengan pencucian
terbuang dan larut bersama air (Angka dan Suhartono 2000). Pencucian yang
kurang sempurna akan mengakibatkan mineral yang sudah terlepas dapat melekat
kembali pada permukaan molekul kitin.
Kadar air merupakan salah satu parameter yang sangat penting untuk
menentukan mutu kitosan. Protan Biopolimer menetapkan standar mutu kadar air
kitosan adalah ≤ 10 % (Bastaman 1989). Dari Tabel 5 diketahui bahwa kadar air
kitosan sebesar 15 %. Kitosan yang dihasilkan memiliki kadar air yang masih
cukup tinggi dan melebihi batas maksimum standar mutu kadar air kitosan yang
telah ditetapkan. Kadar air yang terkandung pada kitosan dipengaruhi oleh proses
pengeringan, lama pengeringan yang dilakukan, jumlah kitosan yang dikeringkan
dan luas tempat permukaan tempat kitosan yang dikeringkan (Saleh et al. 1994).
Benjakula dan Sophanadora (1993) juga menyatakan bahwa kadar air kitosan
tidak dipengaruhi oleh jumlah bahan, nisbah bahan, dan waktu proses tetapi
dipengaruhi oleh waktu pengeringan yang dilakukan terhadap kitosan.
Kadar air yang tinggi dipengaruhi oleh kurang meratanya peletakan kitosan
pada tempat pengeringan, sehingga ada kitosan yang saling menggumpal dan akan
mempersulit proses pengeringan. Instensitas sinar matahari yang tidak stabil
(berubah-ubah) juga akan menyebabkan proses pengeringan berlangsung kurang
sempurna. Selain itu, kadar air kitosan sangat dipengaruhi oleh keadaan
lingkungan, khususnya kelembaban relatif dari tempat kitosan tersebut disimpan.
Pada umumnya kitosan disimpan di dalam ruangan. Hal yang harus diperhatikan
agar dihasilkan kitosan dengan kadar air yang memenuhi persyaratan adalah
dengan cara pengeringan, cara pengemasan dan cara penyimpanan yang baik.
Penyimpanan yang baik dengan penutupan yang sempurna merupakan upaya
untuk mempertahankan mutu kitosan, khususnya kadar airnya.
Kadar nitrogen merupakan salah satu parameter yang juga diukur untuk
menentukan mutu kitosan. Kadar nitrogen menentukan sifat kitosan yang
berinteraksi dengan gugus lainnya. Keberadaan senyawa lain dalam kitosan yaitu
bentuk gugus amin (NH2) menyebabkan kitosan memiliki reaktivitas kimia yang
cukup tinggi, sehingga kitosan mampu mengikat air dan larut dalam asam asetat.
Menurut Protan Biopolimer standar mutu kadar nitrogen kitosan yang telah
kitosan yang dihasilkan telah memenuhi standar yang ditetapkan yakni sebesar
4,73%.
Pada penelitian ini dilakukan proses deasetilasi yang sesuai dengan penelitian
Ariesta (2008), yaitu dengan konsentrasi NaOH 50 % dan suhu proses deasetilasi
140 °C. Hasil analisis kadar nitrogen menunjukkan nilai yang relatif sama dengan
hasil penelitian Ariesta (2008) yaitu ≤5 %. Konsentrasi NaOH dan suhu
deasetilasi yang semakin tinggi, menyebabkan kadar nitrogen cenderung semakin
kecil. Hal ini didukung oleh pernyataan Benjakula dan Sophanodora (1993)
bahwa kadar total nitrogen berupa protein yang dapat dihilangkan
(pada pembuatan kitin) sangat dipengaruhi oleh konsentrasi NaOH yang
digunakan, waktu ekstraksi dan suhu ekstraksi. Protein yang masih terikat setelah
proses deasetilasi dilakukan dengan suhu yang semakin meningkat dan
konsentrasi NaOH yang tinggi. Proses pengadukan yang konstan juga merupakan
salah satu faktor yang mempermudah panghilangan protein dari kulit udang
melalui reaksi antara larutan NaOH dengan bahan.
Menurut Saleh et al. (1994) kadar nitrogen dipengaruhi oleh konsentrasi
NaOH dan waktu proses deproteinasi. Semakin tinggi konsentrasi NaOH yang
digunakan dan semakin lama waktu deproteinasi yang digunkan maka reaksi
antara protein dengan larutan pembentuk ester (Na-proteinat) akan semakin
sempurna, sehingga protein yang dihilangkan akan semakin banyak.
4.4 Penelitian Utama
Pada penelitian utama dilakukan perhitungan rendemen kitosan nanopartikel
yang dihasilkan dari berbagai metode alat yang berbeda antara lain magnetic
stirrer, ultrasonik dan homogenizer. Tahap berikutnya, dari hasil rendemen yang
tertinggi dilakukan proses karakteristik fisik dari kitosan nanopartikel dengan
metode gelasi ionic menggunakan ketiga alat tersebut. Parameter yang diamati
pada penelitian utama meliputi ukuran partikel melalui analisis SEM (Scanning
Electron Microscopy)dan FTIR (Fourier Transform InfraRed).
4.4.1 Rendemen Kitosan Nanopartikel
Rendemen kitosan nanopartikel ditentukan berdasarkan persentase berat
digunakan. Rendemen yang diperoleh untuk setiap perlakuan adalah
38,5% - 85%. Hasil rendemen kitosan nanopartikel dengan perlakuan metode
yang berbeda dapat dilihat pada Tabel 6.
Tabel 6. Rendemen kitosan nanopartikel dengan perbedaan perlakuan alat pengecilan ukuran
Penggunaan alat ultrasonik atau mekanik dengan waktu sonikasi 60 menit dan
amplitudo 30% menghasilkan rendemen kitosan nano sebesar 46,88 %. Rendemen
kitosan nano menggunakan alat homogenizer dengan waktu homogenisasi
60 menit kecepatan 3000 rpm yaitu sebesar 40,00 %. Sedangkan rendemen
kitosan nano yang dihasilkan menggunakan alat magnetic stirrer dengan waktu 60
menit dan 6000 rpm yaitu sebesar 81,30 %. Tabel 6 menunjukkan rendemen
kitosan nanopartikel tertinggi terdapat pada perlakuan metode pengecilan ukuran
dengan alat magnetic stirer yaitu sebesar 81,30 %. Sedangkan rendemen terendah
ditunjukkan oleh kitosan nanopartikel dengan perlakuan menggunakan alat
homogenizer yaitu sebesar 40,00 %.
Rendemen yang rendah ini dapat disebabkan oleh proses yang digunakan. Alat
ultrasonik memiliki kelemahan yaitu memerlukan energi tinggi untuk
dekomposisi kimia. Selain itu, metode pemecahan menggunakan homogenizer
memiliki kelebihan antara lain cocok untuk senyawa yang kelarutannya rendah,
sedangkan kekurangan metode ini antara lain pemecahan partikel padatan
memerlukan energi dan waktu yang lebih besar, dapat menghasilkan panas, dan
ukuran partikel yang dihasilkan terbatas, yaitu lebih besar dari 1000 nm.
Berdasarkan hasil yang diperoleh, rendemen nano kitosan yang tertinggi yaitu
menggunakan magnetic stirrer, karena dengan alat magnetic stirrer memiliki
kelebihan yaitu proses homogenisasi antara kitosan serbuk awal dengan bahan
gelasi ionik, dapat dikendalikan secara merata dengan kecepatan yang tinggi,
nanopartikel dan dapat menghasilkan rendemen 81,30%, yang sesuai dengan
persentasi kitosan awal yang digunakan (Wahyono 2010).
Proses pengeringan semprot (spray drying) juga mempengaruhi rendemen
hasil nano kitosan yang dihasilkan. Pada pengeringan semprot terjadi kontak
antara semprotan dengan udara panas, pengeringan semprotan, dan pemisahan
antara produk kering (aliran serbuk bebas) dan udara (Yundhana 2008). Grafik
hasil rendemen kitosan nanopartikel dengan perbedaan pengecilan ukuran dapat
dilihat pada Gambar 6.
Gambar 6 Grafik hasil rendemen kitosan nanopartikel dengan perbedaan perlakuan metode pengecilan ukuran
4.4.2 Hasil Analisis Scanning Electron Microscopy (SEM)
SEM (Scanning Electron Microscopy) digunakan untuk mengamati morfologi
suatu bahan. Prinsip kerja mikroskop SEM adalah sifat gelombang dari elektron
berupa difraksi pada sudut yang sangat kecil. Elektron dapat dihamburkan oleh
sampel yang bermuatan karena memiliki sifat listrik (Samsiah 2009 dalam
Wulandari 2010). Hasil karakteristik SEM kitosan nanopartikel yang dibuat
dengan berbagai metode yaitu magnetic stirrer, ultrasonik, dan homogenizer
menunjukan partikel yang berupa bulatan menyerupai bola dan berkerut. Ukuran
partikel dapat ditentukan dengan mengukur diameter bola tersebut. Perbesaran
Setelah dilakukan pengukuran diameter berdasarkan foto SEM diperoleh data
yang ditunjukkan pada Tabel 7.
Tabel 7. Ukuran partikel nano kitosan hasil foto SEM
Perlakuan
Pada Tabel 7 terlihat bahwa dengan menggunakan magnetic stirrer dihasilkan
ukuran partikel terkecil dan lebih stabil yaitu sebesar 400 nm (H1) dan 450 nm
(H2). Sedangkan pada perlakuan ultrasonik dan homogenizer dihasilkan ukuran
pertikel yang lebih besar dan tidak stabil, yaitu dengan perlakuan ultrasonik
didapatkan ukuran partikel sebesar 1222 nm (H1) dan 1600 nm (H2). Dengan
perlakuan homogenizer dihasilkan ukuran partikel sebesar 1375 nm (H1) dan
2000 nm (H2). Hal ini sesuai dengan penelitian BPPT (2010) yaitu partikel
terkecil dan stabil didapatkan dengan perlakuan magnetic stirrer sebesar 25,9 nm
(H1) dan 28 nm (H2). Sedangkan partikel yang lebih besar serta tidak stabil
diperoleh dengan perlakuan ultrasonik dan homogenizer sebesar 1,2 nm (H1)
dan 25 nm (H2).
Berdasarkan Gambar 7, kerutan pada partikel semakin berkurang dengan
adanya pengaruh pemberian surfaktan, TPP dan perlakuan pengecilan ukuran.
Perbedaan metode pengecilan ukuran pada gelasi ionik ini, memperlihatkan
bahwa pengaruh alat homogenisasi cenderung mempengaruhi ukuran partikel dan
meningkatkan kehomogenan ukurannya. Karakteristik nanopartikel kitosan
dilakukan dengan menggunakan analisis SEM. Secara umum, nanopartikel
kitosan seluruh formula memiliki ukuran partikel tidak seragam. Hal ini diduga
karena dalam proses pembuatan nanopartikel, menggunakan perbedaan alat
pengecilan ukuran dengan kecepatan pengadukan yang berbeda- beda sehingga
pengendapan partikel-partikel berukuran besar menjadi kurang efektif. Akibatnya,
partikel yang dihasilkan masih berupa partikel yang berukuran mikro. Hasil
60 menit dan kecepatan maksimal, kisaran nanopartikel yang nanopartikel
dihasilkan adalah 400 - 450 nm.
Nanopartikel adalah butiran atau partikel padat dengan kisaran ukuran
10 - 1000 nm (Mohanraj dan Chen 2006). Nano partikel yang dihasilkan oleh
magnetic stirrer rata-rata berukuran sekitar 400 - 450 nm. Berdasarkan teori
kinetik molekul menyatakan bahwa molekul dapat bertumbukan satu dengan
lainnya. Jadi, reaksi kimia berlangsung sebagai akibat dari tumbukan antara
molekul-molekul satu dengan lainnya dalam reaksi. Dari segi teori tumbukan dari
kinetika kimia, maka laju reaksi akan berbanding lurus dengan banyaknya
tumbukan molekul per detik, atau berbanding lurus dengan frekuensi tumbukan
molekul. Semakin cepat putaran, memperbesar intensitas bersentuhan molekul
pelarut dengan kitosan, sehingga semakin besar intensitas kecepatan putaran dari
magnetic stirrer maka partikel yang dihasilkan semakin kecil (Chang 2005).
Pada alat ultrasonik, semakin tinggi persen amplitudo serta lama waktu
kontak, maka semakin kecil ukuran partikel dan seragam. Hasil dari ultrasonik
dan homogenizer masih berukuran lebih dari 1000 nm dan partikel masih
menempel satu sama lain. Hal ini dapat dipengaruhi oleh proses emulsi yang
kurang stabil sehingga saat proses ultrasonik dan homogenizer partikel yang
terpecah membentuk partikel yang lebih kecil tetapi mudah bergabung kembali.
Faktor pengeringan dengan menggunakan pengering semprot juga dapat
mempengaruhi ukuran partikel karena suhu yang terlibat di dalamnya cukup
tinggi (±180 °C). Selain itu, sifat surfaktan (Tween 80) juga mudah larut dalam
air, sehingga kemungkinan terjadi dalam proses difusi Tween 80 dalam air
menyebabkan penggabungan partikel proses penggumpalan kembali terjadi. Pada
dasarnya partikel yang dihasilkan melalui metode ultrasonik dan metode
homogenizer lebih kecil dibandingkan menggunakan magnetic stirrer. Partikel
yang lebih kecil mempunyai luas permukaan yang lebih besar. Konsentrasi
penstabil yang diberikan belum dapat mempertahankan partikel yang sudah
tersalut sehingga membutuhkan penstabil yang lebih kuat agar tidak bergabung
atau menyatu kembali (Latifah 2008).
Berbeda dengan sampel yang menggunkan alat magnetic stirrer, penyebaran
molekul larutan emulsi akan terpecah dengan ukuran yang sama serta distribusi
ukuran partikelnya cenderung labih homogen. Hal inilah yang menyebabkan
nanopartikel di dalamnya juga akan dapat terpisah satu sama lain sehingga
didapatkan nanosfer dengan ukuran terkecil. Selain itu, penggunaan tripolipospat
dalam proses gelasi juga besar pengaruhnya, yaitu dapat menstabilkan missel
(emulsi homogen dan sangat kecil) sehingga missel tersebut menjadi lebih stabil.
Hal ini sesuai dengan hasil penelitian BPPT yang dilakukan dengan uji PSA
(Particle Size Analyzer) (Tabel 7), bahwa ultrasonik dan homogenizer memiliki
kestabilan rendah. Sedangkan dengan magnetic stirrer menghasilkan kestabilan
tetap, yang bisa dilihat dalam waktu/hari. Magnetic stirrer lebih stabil dalam
waktu 24 jam, sementara pada ultrasonik dan homogenizer bisa berubah
kestabilannya mencapai 25 kali lebih meningkat (BPPT 2010).
Surfaktan yang digunakan untuk obat secara farmakologi harus nontoksik.
Oleh karena itu dalam penelitian ini digunakan surfaktan dari golongan nonionik
yang bersifat tidak toksik, yaitu Tween 80. Surfaktan merupakan molekul yang
diadsopsi oleh permukaan partikel untuk mencegah terjadinya gumpalan (Mustika
et al. 2006 dalam Latifah 2008). Pengaruh surfaktan dapat menurunkan tegangan
permukaan antar lapisan larutan bahan dengan kitosan semakin baik dengan
terbentuknya misel – misel, artinya bahan akan menyaluti permukaan matriks
kitosan atau berada pada inti matriks.
Penggunaan tripolipospat mengingat sifatnya yang nontoksik.
Menurut Mi et al. (1999) dalam Wahyono (2010), penambahan TPP bertujuan
untuk membentuk silang ionik antara molekul kitosan sehingga dapat digunakan
sebagai bahan penguat. Hal ini dapat disebabkan oleh peran TPP sebagai zat
pengikat silang yang akan memperkuat matriks nanopartikel kitosan. Dengan
semakin banyaknya ikatan silang yang terbentuk antara kitosan dan TPP maka
kekuatan mekanik matriks kitosan akan meningkat sehingga partikel kitosan
menjadi semakin kuat dan keras, serta semakin sulit untuk terpecah menjadi
bagian-bagian yang lebih kecil.
Pada penelitian ini, konsentrasi kitosan yang digunakan sebesar 0,2% (50 ml)
dan konsentrasi surfaktan sebesar 0,2% (25 ml), sesuai dengan penelitian