OPTIMALISASI REAKSI EPOKSIDASI METIL ESTER
JARAK PAGAR DENGAN KATALIS ZEOLIT SEBAGAI
PEMLASTIS ALTERNATIF
WAHYU DIANA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
WAHYU DIANA. Optimalisasi Reaksi Epoksidasi Metil Ester Jarak Pagar dengan Katalis Zeolit Sebagai Pemlastis Alternatif. Dibimbing oleh PURWANTININGSIH SUGITA dan AHMAD SJAHRIZA.
Pemlastis digunakan untuk pembuatan poli(vinilklorida) (PVC). Jenis pemlastis yang umum digunakan adalah pemlastis jenis ftalat yang berbahan dasar dari minyak bumi, namun dalam jangka waktu tertentu dapat membahayakan lingkungan. Oleh karena itu, perlu dicari pengganti pemlastis ftalat yang berbahan dasar bukan dari minyak bumi, salah satunya adalah minyak nabati. Dalam penelitian ini digunakan metil ester dari biji jarak pagar (Jatropha curcas L.)
Pencirian bahan baku metil ester jarak pagar (MEJP)menghasilkan bilangan iodin dan bilangan oksirana MEJP berturut-turut sebesar 97.00 g I/100 g MEJP dan 0.04 %. MEJP diepoksidasi dengan variasi waktu (12, 24, 36) jam, suhu (50, 60, 70) oC, dan konsentrasi katalis zeolit (1, 2, 3) % untuk memperoleh kondisi optimum menggunakan perangkat lunak Modde 5. Kondisi optimum diperoleh pada waktu 36 jam, suhu 70 oC, dan konsentrasi katalis 3% dengan bilangan oksirana maksimum sebesar 0.63%. Hasil validasi juga menunjukkan kondisi optimum yang sama, tetapi bilangan oksirananya sebesar 1.33% dan bilangan iodinnya sebesar 59.86 g I/100 g MEJP. Bilangan oksirana MEJP terepoksidasi (MEJPT) semakin tinggi dan bilangan iodinnya semakin rendah dibandingkan dengan MEJP awal. Hal ini menunjukkan reaksi epoksidasi telah terjadi. Spektrum FTIR MEJP dan MEJPT memperlihatkan bilangan gelombang yang hampir sama, yaitu adanya gugus C=O ester pada bilangan gelombang 1743.5 cm-1, C=C pada
bilangan gelombang 1654.8 cm-1, dan C–O pada bilangan gelombang 1018.3, 1118.6,
1168.8, 1195.8, dan 1245.9 cm-1.Perbedaannya terletak pada nilai %T gugus C=C, yaitu
ABSTRACT
WAHYU DIANA.Optimalization of Epoxidation Methyl Ester on Jatropha Using Zeolite Catalyst as An Alternative Plasticizer. Supervised by PURWANTININGSIH SUGITA dan AHMAD SJAHRIZA.
Plasticizer is used in poly(vinylchloride) (PVC) manufactures. The commonly utilized type of plasticizer is phtalate plasticizer which is petrochemical-based, but in a period of time may harm the environment. Therefore, it is important to find a substitute for phtalate plasticizer that is not petrochemical based, one of which is vegetable oil. In this research, methyl ester from kernel of jatropha was employed.
Characterization of jatropha methyl ester (MEJP) yielded an iodine and oxirane number of 97.00 g I/100 g MEJP and 0.04%, respectively. MEJP was epoxidized with variation of times (12, 24, 36) hours, temperatures (50, 60, 70) oC, and zeolite
concentrations (1, 2, 3) % to obtain the optimum condition using Modde 5 software. The optimum condition was achieved at time of 36 hours, temperature of 70 oC, and zeolite
concentration of 3% with maximum oxirane number of 0.63%. Validation result also showed a similar optimum condition, but its oxirane number was 1.33% and iodine number was 59.86 g I/100 g MEJP. The oxirane number of epoxidized MEJP (MEJPT) was higher and the iodine number was smaller than the initial MEJP. This fact showed that epoxidation reaction had occured. FTIR spectrum of MEJP and MEJPT showed similar wavenumbers of the presence of C=O ester group at 1743.5 cm-1, C=C at 1654.8 cm-1, and C–O at 1018.3, 1118.6, 1168.8, 1195.8, and 1245.9 cm-1.The difference was on %T value of C=C group, MEJP %T was smaller than MEJPT’s.
OPTIMALISASI REAKSI EPOKSIDASI METIL ESTER
JARAK PAGAR DENGAN KATALIS ZEOLIT SEBAGAI
PEMLASTIS ALTERNATIF
WAHYU DIANA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Optimalisasi Reaksi Epoksidasi Metil Ester Jarak Pagar dengan Katalis Zeolit Sebagai Pemlastis Alternatif.
Nama : Wahyu Diana NIM : G44202064
Disetujui:
Pembimbing I Pembimbing II
Dr. Purwantiningsih Sugita, MS Drs. Ahmad Sjahriza NIP 131 779 513 NIP 131 842 413
Diketahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, M. S. NIP 131473999
PRAKATA
Alhamdulillah, penulis panjatkan ke hadirat Allah SWT atas limpahan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini dilakukan selama bulan April 2006 – April 2007, tema yang dipilih yaitu optimalisasi reaksi epoksidasi metil ester jarak pagar dengan katalis zeolit sebagai pemlastis alternatif. Terima kasih penulis ucapkan kepada Ibu Dr. Purwantiningsih Sugita, MS dan Bapak Drs. Ahmad Sjahriza selaku pembimbing serta Kak Budi Arifin, S.Si atas segala saran, kritik, dorongan, dan bimbingannya selama penelitian dan dalam penyusunan karya ilmiah ini. Penulis juga mengucapkan terima kasih kepada PHK A2 sebagai penyandang dana. Selain itu penulis juga mengucapkan terima kasih kepada Pak Sabur, Bu Yenni, Bu Aah, dan seluruh staf Kimia Organik atas fasilitas dan kemudahan yang diberikan, serta kepada Joko, Teddy, Ade, Tria, Budi, Tesar, Ibu Lani, dan teman-teman seperjuangan di Laboratorium Kimia Organik atas saran selama penelitian.
Ucapan terima kasih yang tak terhingga penulis sampaikan kepada orang tua tercinta (Bapak dan Mama), adikku Yuni, dan seluruh keluarga di Bandung atas perhatian, dorongan dan doanya, kepada Amey atas dukungan dan kasih sayangnya, semua kawan-kawan khususnya Dias, Anna, Azhari, Steven, dan Dogar atas doa, dukungan, dan kebersamaannya, Mas Herry atas bantuannya, serta rekan-rekan kimia angkatan ’39.
Semoga karya ilmiah ini bermanfaat.
Bogor, Mei 2007
RIWAYAT HIDUP
Penulis dilahirkan di Bandung tanggal 29 Desember 1984 dari ayah Tatang Yuda dan ibu Enung Sariah, S. Pd. Penulis merupakan putra pertama dari dua bersaudara.
Pendidikan formal penulis sampai dengan tingkat SMU diselesaikan di Bandung, yaitu TK Sejahtera, SD Negeri Gunung Rahayu II, SLTP Negeri 1 Bandung, dan SMU Negeri 2 Bandung dari tahun 1988-2002. Penulis lulus dari SMU dan pada tahun yang sama lulus dari seleksi masuk IPB dengan pilihan Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, melalui jalur seleksi penerimaan mahasiswa baru (SPMB).
DAFTAR ISI
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
PENDAHULUAN . ... 1
TINJAUAN PUSTAKA Pemlastis ... 1
Jarak Pagar (Jatropha curcas L.) ... 1
Metil Ester ... 2
Epoksidasi ... 2
Zeolit ... 3
Optimalisasi Reaksi Epoksidasi ... 4
BAHAN DAN METODE Bahan dan Alat ... 4
Penelitian Pendahuluan ... 4
Penelitian Utama ... 4
HASIL DAN PEMBAHASAN Optimalisasi Reaksi Epoksidasi ... 5
Analisis FTIR ... 8
Validasi Kondisi Reaksi Epoksidasi ... 9
SIMPULAN DAN SARAN Simpulan ... 9
Saran ... 9
DAFTAR PUSTAKA ... 9
DAFTAR TABEL
Halaman
1 Kandungan asam lemak pada minyak jarak pagar ... 2
2 Sifat fisikokimia minyak jarak pagar ... ... 2
3 Jenis-jenis zeolit sintetik ... 3
4 Sifat-sifat mutu MEJP & MEJP Terepoksidasi ... 5
5 Kondisi optimum reaksi epoksidasi menggunakan Modde 5 ... 8
6 Bilangan oksirana dan bilangan iodin hasil validasi kondisi optimum ... 9
DAFTAR GAMBAR
Halaman 1 Tumbuhan Jarak pagar ... 2
2. Mekanisme reaksi epoksidasi ... 3
3 Ilustrasi stuktur 3 dimensi zeolit alam ... 3
4 Rangkaian alat sintesis ... ... 5
5 Pengaruh waktu dan konsentrasi zeolit pada suhu: (a) 50oC, (b) 60oC, dan (c) 70oC terhadap bilangan oksirana ... 6
6 Pengaruh waktu dan suhu pada konsentrasi zeolit: (a) 1%, (b) 2%, dan (c) 3% terhadap bilangan oksirana... 7
DAFTAR LAMPIRAN
Halaman
1 Skema pembentukan tapak asam BrÖnsted dan Lewis pada zeolit ... 12
2 Prosedur penentuan sifat-sifat bahan baku ... 13
3 Bagan alir reaksi epoksidasi ... 14
4 Data rendemen, bilangan iodin, dan bilangan oksirana ... 15
5 Spektrum FTIR MEJP awal ... 16
6 Spektum FTIR MEJPT dengan katalis zeolit ... 17
7 Pengaruh waktu dan suhu pada konsentrasi zeolit: (a) 1%, (b) 2%, dan (c) 3% terhadap bilangan iodin ... 18
8 Produk-produk pembukaan cincin oksirana ... 19
9 Grafik hubungan waktu Vs bilangan oksirana dan waktu Vs bilangan iodin hasil validasi ... 19
PENDAHULUAN
Pemlastis menguasai 65% dari 7.5 juta ton pasar zat aditif di dunia yang setara dengan US$7.6 miliar. Kegunaan utama zat aditif ini adalah untuk pembuatan poli(vinilklorida) (PVC), suatu polimer yang digunakan untuk berbagai aplikasi seperti pelapis, pipa, bahan konstruksi, dan botol plastik. Pasar untuk PVC terus berkembang dan diperkirakan mencapai 8% per tahun (Cavanaugh 1995).
Jenis pemlastis beraneka ragam; jenis yang
umum digunakan adalah kelompok ftalat,
yaitu dibutil ftalat (DBP), dimetoksietil ftalat (DMP), di-2-etilheksil ftalat (DEHP), dan dioktil ftalat (DOP), yang semuanya berbahan dasar minyak bumi (petrokimia). DOP digunakan secara besar-besaran untuk pembuatan PVC. Namun lama-kelamaan, ftalat dapat lepas ke lingkungan dan mengakibatkan plastik menjadi rapuh. Pelepasan ftalat sangat membahayakan
lingkungan, sehingga oleh EPA’s Toxic
Release Inventory telah diklasifikasikan sebagai bahan kimia yang toksik. Bahkan mulai tahun 2006, Uni Eropa telah mengeluarkan larangan penggunaan ester ftalat, termasuk DEHP yang paling banyak digunakan pada produk mainan anak dan kosmetik. Oleh karena itu, perlu dicari pengganti pemlastis ftalat yang bahan dasarnya bukan dari minyak bumi, salah satunya adalah menggunakan bahan baku dari minyak nabati.
Minyak nabati sebagai bahan baku pemlastis memiliki keunggulan seperti mudah diperbaharui, mudah terurai, dan ramah lingkungan. Saat ini minyak nabati yang banyak digunakan di dunia dalam industri pemlastis masih didominasi oleh minyak biji bunga matahari, minyak kelapa sawit, dan minyak kedelai (Chou & Lee 1997; Supriyadi 1992; Hazimah et al. 2000). Indonesia memiliki banyak sumber daya nabati yang dapat menghasilkan minyak, di antaranya kelapa sawit, kemiri, saga, kapuk, karet, dan jarak pagar. Dalam penelitian ini, digunakan minyak dari biji jarak pagar yang diubah menjadi metil esternya melalui proses esterifikasi dan transesterifikasi dengan metanol dan katalis asam (Jaya 2005). Biji jarak pagar dipilih karena komposisi asam lemaknya yang hampir sama dengan minyak kedelai.
Metil ester jarak pagar (MEJP) yang diperoleh diepoksidasi dengan bantuan katalis untuk memperoleh senyawa epoksida yang merupakan salah satu pemlastis. Pada
penelitian ini, suhu, waktu, dan konsentrasi katalis zeolit yang digunakan diragamkan untuk mencari kondisi optimum dari peubah-peubah tersebut yang dapat memenuhi tujuan, yaitu menghasilkan bahan baku pemlastis dengan kandungan epoksida yang tinggi.
TINJAUAN PUSTAKA
Pemlastis
Pemlastis merupakan bahan yang jika ditambahkan pada polimer akan mengurangi gaya antarmolekul dalam rantai polimer sehingga meningkatkan fleksibilitas dan pemanjangan plastik yang membuatnya lebih mudah dikerjakan. Pemlastis ada 10 jenis, yaitu pemlastis dari jenis ftalat, adipat, trimelitat, maleat, benzoat, minyak nabati terepoksidasi, sulfonamida, fosfat, glikol atau polieter, dan polimer.
Hal utama yang harus dipertimbangkan dalam memilih pemlastis adalah kompatibilitas (Ahmad et al. 1987). Untuk pemlastis jenis minyak nabati terepoksidasi, kompatibilitas berkaitan dengan kemampuan pemlastis untuk berikatan dengan polimer. Kompatibilitas dapat diperbaiki dengan meningkatkan kandungan epoksidanya. Mutu bahan baku juga dapat memengaruhi rendemen epoksida yang diperoleh dan sifat senyawa epoksi yang digunakan sebagai pemlastis (Kirk & Othmer 1965).
Jarak Pagar (Jatropha curcas L)
2
Gambar 1 Tumbuhan jarak pagar
Kandungan minyak yang besar dalam biji jarak pagar menjadikannya bahan baku yang potensial dalam pembuatan pelumas dan bahan bakar ramah lingkungan. Selain itu, minyak jarak pagar juga dapat digunakan sebagai obat pencahar, obat kulit, dan penghilang nyeri akibat rematik.
Setiap bagian tumbuhan jarak pagar mengandung senyawa kimia yang berbeda. Biji jarak pagar mengandung 35–45% trigliserida, yang komponen asam lemaknya meliputi asam linoleat, oleat, dan palmitat (Tabel 1). Sementara ciri fisikokimia minyak jarak pagar dapat dilihat pada Tabel 2.
Tabel 1 Kandungan asam lemak pada minyak jarak pagar
Asam lemak Komposisi (%)
Miristat (14:00) 0-0,1
Palmitat (16:00) 14,1-15,3
Stearat (18:00) 3,7-9,8
Arakidonat (20:00) 0–0.3
Beheniat (22:00) 0–0.2
Palmitoleat (16:01) 0–1.3
Oleat (18:01) 34,3–45.8
Linoleat (18:02) 29,0–44.2
Linolenat (18:03) 0–0.3
Sumber: Gubitz et al. 1999
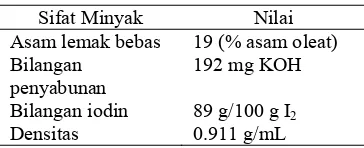
Tabel 2 Sifat fisikokimia minyak jarak pagar
Sifat Minyak Nilai
Asam lemak bebas 19 (% asam oleat) Bilangan
penyabunan
192 mg KOH
Bilangan iodin 89 g/100 g I2
Densitas 0.911 g/mL
Sumber: Heyne (1987)
Metil Ester
Asam lemak bebas dimetilasi dengan menggunakan metanol tanair berlebih dalam suasana asam, biasanya asam klorida. Menurut Paquot & Hautfene (1987), metil ester juga lazim diperoleh dari asam lemak dengan pereaksi BF3 dan NaOH. Jumlah BF3
dan NaOH bergantung pada berapa banyak contoh yang digunakan. Metil ester juga dapat dibuat secara langsung dari trigliserida, melalui reaksi transesterifikasi menggunakan metanol berlebih dan katalis asam (Paquot & Hautfene 1987).
Transesterifikasi minyak nabati dan lemak hewani merupakan proses paling efektif untuk mengubah molekul trigliserida menjadi ester asam lemak. Proses ini meliputi reaksi antara alkohol dan molekul trigliserida dengan adanya katalis basa atau asam. Beberapa peubah yang berpengaruh pada proses alkoholisis ini ialah waktu reaksi, suhu reaksi, jenis dan konsentrasi katalis, serta nisbah molar reaktan. Menurut Bernardini (1983), konsentrasi metanol yang digunakan pada proses transesterifikasi tidak boleh kurang dari 98% karena rendemen metil ester yang dihasilkan akan menurun dan sedangkan waktu reaksi menjadi lebih lama.
Transesterifikasi minyak nabati secara sinambung telah dilakukan oleh Noureddini et al. (1998) menggunakan pelarut metanol atau etanol pada suhu sekitar titik didih alkohol yang bersangkutan. Digunakan katalis NaOH atau KOH yang dilarutkan dalam alkohol 50% berlebih untuk waktu reaksi 1–2 jam. Boocock et al. (1998) menyatakan bahwa rendemen metil ester yang diperoleh dengan menggunakan katalis NaOH 1% mencapai sekitar 95%. Metil ester ini kemudian dapat diubah menjadi bahan dasar pemlastis melalui reaksi epoksidasi.
Epoksidasi
3
Menurut Rios (2003), pada dasarnya terdapat 4 metode epoksidasi, yaitu dengan asam perkarboksilat, dengan peroksida organik dan anorganik, dengan halohidrin, dan dengan molekul oksigen. Metode pertama umum digunakan di industri, dan dapat dikatalisis oleh asam atau enzim. Metode kedua meliputi epoksidasi alkali dan nitril oleh hidrogen peroksida serta epoksidasi berkatalis logam transisi. Metode ketiga menggunakan asam hipohalit (HOX) dan garamnya sebagai media untuk epoksidasi alkena dengan ikatan rangkap yang tuna elektron. Dari keempat metode tersebut, metode pertama dan kedua bersih dan efisien (Anonim 2006). Pada penelitian ini digunakan metode yang pertama, yaitu menggunakan asam peroksi.
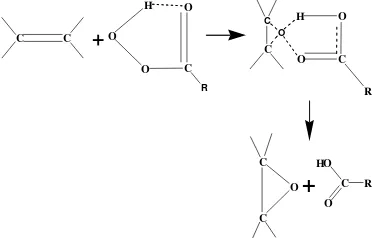
Asam peroksi dibentuk melalui interaksi antara asam karboksilat dan hidrogen peroksida. Reaksi ini dapat dipersingkat dengan menggunakan hidrogen peroksida yang berlebih (Gall & Greenspan 1953). Pembentukan asam peroksi dengan menggunakan hidrogen peroksida dapat dilakukan dengan 4 cara sebagaimana dikemukakan oleh Kirk dan Othmer (1965), yaitu asam peroksi asetat atau format yang dibentuk terlebih dahulu dan yang dibentuk secara in situ. Reaksi epoksidasi secara in situ memiliki beberapa keuntungan, antara lain mengurangi pemakaian hidrogen peroksida dan hemat biaya (Swern 1979). Mekanisme reaksi epoksidasi adalah sebagai berikut:
C C O
H O C O R + O O H O C R C C R C O HO O C C
+
Gambar 2 Mekanisme reaksi epoksidasi.
Wood & Termini (1958) mengatakan bahwa proses epoksidasi biasanya dilakukan pada suhu 65–75 oC. Suhu yang lebih rendah akan memperpanjang waktu epoksidasi dan menurunkan efisiensinya. Proses epoksidasi dapat dipersingkat dengan penggunaan katalis. Salah satunya ialah zeolit. Senyawa epoksida yang diperoleh dianalisis dengan melakukan uji bilangan iodin dan bilangan oksirana. Nilai bilangan iodin diperoleh dari banyaknya
ikatan rangkap pada metil ester jarak pagar (MEJP) yang diadisi oleh iodin. Bilangan oksirana menunjukkan banyaknya senyawa epoksida yang diperoleh dari pengikatan atom oksigen pada ikatan rangkap setelah proses adisi berlangsung.
Zeolit
Zeolit merupakan kristal aluminosilikat terhidrasi yang terdiri atas gugusan alumina dan gugusan silika-oksida, masing-masing berbentuk tetrahedral, yang saling dihubungkan oleh atom oksigen sedemikian rupa sehingga membentuk kerangka tiga dimensi (Handoko 2002). Hamdan (1992) mengemukakan bahwa mineral zeolit terdiri atas tiga komponen, yaitu kation yang dapat dipertukarkan, kerangka silika-alumina, dan air. Jumlah air yang terkandung dalam zeolit sesuai dengan banyaknya pori atau volume pori. Zeolit biasanya ditulis dengan rumus kimia Mx/n [(AlO2)x (SiO2)y].zH2O, dengan x
dan y adalah bilangan bulat, y/x sebanding atau lebih besar dari 1, dan n adalah valensi logam M (Tang 2003). Ilustrasi struktur 3 dimensi zeolit alam disajikan pada Gambar 2.
Keragaman nisbah antara atom Si dan Al akan menghasilkan berbagai jenis zeolit baik alami maupun sintetik. Pada saat ini telah ditemukan lebih dari 150 zeolit sintetik, di antaranya zeolit tipe A, X, Y, dan L (Tabel 3).
Gambar 3 Ilustrasi stuktur 3 dimensi zeolit alam
Tabel 3 Jenis-jenis zeolit sintetik
No. Nama Rumus Molekul
1 A Na12[(AlO2)12(SiO2)12]·27H2O
2 X Na86[(AlO2)86(SiO2)106]·264H2O
3 Y Na56[(AlO2)56(SiO2)136]·250H2O
4 L K9[(AlO2)9(SiO2)27]·22H2O
Sumber: Riberio (1984)
4
Keberadaan zeolit menjadi relatif penting dalam reaksi katalitik heterogen karena strukturnya yang berpori dan sifat alami dari Al3+, Si4+, dan O2- yang saling terikat dengan pola tertentu.
Zeolit yang digunakan secara luas sebagai katalis memiliki tapak asam BrÖnsted dan tapak asam Lewis di dalam pori-porinya (Smith 1992). Tapak asam BrÖnsted dapat dihasilkan dengan beberapa cara di antaranya dengan memanaskan bentuk amonium zeolit untuk menghilangkan amonia sehingga diperoleh bentuk H-Zeolit, dengan mendehidrasi kation multivalen pada zeolit yang diikuti terdisosiasinya air yang terkoordinasi dalam bentuk molekul sehingga membentuk ion H+ pada permukaan zeolit, atau dengan perlakuan asam terhadap zeolit yang stabil terhadap asam sehingga kation ditukar dengan proton. Tapak asam Lewis dapat diperoleh dari dehidroksilasi dua gugus hidroksil yang berdekatan dengan perlakuan panas (T>750 K) (Handoko 2002). Reaksi pembentukan tapak asam BrÖnsted dan tapak asam Lewis dapat dilihat pada Lampiran 1.
Zeolit perlu diaktivasi terlebih dahulu untuk menghilangkan pengotor (mineral pengganggu) yang berupa oksida logam yang menutupi rongga. Aktivasi zeolit dapat dilakukan dengan cara pemanasan, penambahan asam, atau penambahan basa. Pada penelitian ini dilakukan aktivasi dengan penambahan basa. Pada umumnya asam yang digunakan adalah H2SO4 dan HCl, sedangkan
basa yang digunakan adalah NaOH.
Optimalisasi
Secara umum, optimalisasi adalah serangkaian proses untuk mendapatkan kondisi yang diperlukan dalam mencapai hasil terbaik (bisa maksimum atau minimum) dalam keadaan tertentu. Dalam hal ini, pendekatan sistem memungkinkan untuk memberikan penanganan masalah dengan suatu metode yang logis sehingga dapat mengidentifikasi, menganalisis, dan mendesain sistem secara keseluruhan dari subsistem atau komponen yang saling berinteraksi.
Metode permukaan respons (response surface methodology) merupakan bentuk analisis yang digunakan pada respons yang dipengaruhi oleh beberapa faktor dan bertujuan menentukan kondisi optimum dari respon tersebut (Montgomery 1991). Pengertian yang lainnya yaitu suatu metode statistika yang menggunakan data kuantitatif
dari rancangan percobaan untuk menentukan dan menyelesaikan persamaan multipeubah. Persamaan tersebut dapat ditampilkan dalam bentuk grafik yang dapat menggambarkan bagaimana peubah uji memengaruhi respons; menentukan hubungan antara seluruh peubah uji; dan menggambarkan pengaruh gabungan dari seluruh peubah uji terhadap respons. RSM terdiri dari 4 tahap, yaitu penentuan dua atau lebih peubah kritis produk; penentuan kisaran taraf peubah; penentuan uji spesifik berdasarkan desain percobaan; dan analisis data. RSM digunakan untuk menentukan dan secara bersamaan menyelesaikan persamaan multipeubah.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah MEJP, katalis zeolit, NaOH 0.2 N, asam asetat glasial, toluena,
H2O2 35%, NaHCO3 jenuh, HCl 1 N,
kloroform, iodin murni, larutan bromin, asam asetat glasial-kloroform (3:2), KI, Na2S2O3 0.1
N, larutan HBr, indikator amilum 1%,dan indikator kristal ungu.
Alat-alat yang digunakan adalah lempeng pemanas, neraca analitik, neraca kasar, termometer, labu leher tiga, komputer dengan perangkat lunak Modde 5, FTIR tipe Shimadzu 8400, dan alat-alat kaca yang biasa dipakai di laboratorium.
Penelitian Pendahuluan
Pada penelitian pendahuluan dilakukan pencirian MEJP yang meliputi analisis bilangan iodin dan bilangan oksirana. Prosedur pencirian bahan baku dapat dilihat pada Lampiran 2.
Penelitian Utama
Pada penelitian utama ini dilakukan optimalisasi reaksi epoksidasi MEJP dengan menggunakan tiga peubah, yaitu suhu reaksi, konsentrasi katalis, dan waktu reaksi. Pertama-tama ditambahkan 0.80 mL asam asetat glasial, 2.90 mL toluena sebagai pelarut, dan 0.1–0.3% zeolit ke dalam 10 gram MEJP. Campuran ini dipanaskan pada suhu 50–70 oC. Setelah itu, 5.78 gram H2O2
5
pada 50–70 oC (± 5 oC) dengan terus diaduk kuat, dan direaksikan selama 12–36 jam. Rangkaian alatnya dapat dilihat pada Gambar 3.
Larutan hasil pencampuran kemudian dinetralkan dengan NaHCO3 jenuh. Lapisan
atas diambil dan kemudian dicuci berulang kali dengan akuades (Chou & Lee 1997; Gan et al. 1992; Rangrajan & Harey 1995). Pengamatan dilakukan dengan penimbangan untuk menghitung rendemen, penentuan bilangan iodin dan bilangan oksirana, serta analisis dengan FTIR (Parreira et al. 2002). Bagan alir optimalisasi reaksi epoksidasi dapat dilihat pada Lampiran 3.
* Larutan I : 10 g MEJP, 0.80 mL asam asetat glasial, 2.90 mL toluena, dan 1-3% zeolit.
* Larutan II : 5.78 g H2O2 35%
1 2 3
4567
8
9
1 10
2 3 4567
8 9 11 Larutan II termometer lempeng pemanas air keluar air masuk Larutan I Stirer
Gambar 4 Rangkaian alat sintesis
Data hasil penelitian diolah dengan menggunakan perangkat lunak Modde 5 dengan RSM. Metode tersebut digunakan untuk mengetahui kondisi optimum reaksi epoksidasi serta melihat pengaruh perubahan waktu, suhu, dan konsentrasi katalis zeolit terhadap bilangan oksirana. Bilangan oksirana ditunjukkan oleh garis warna pada gambar 3 dimensi. Kondisi optimum divalidasi dengan melakukan sintesis pada suhu dan konsentrasi katalis optimum dengan meragamkan waktu reaksi.
HASIL DAN PEMBAHASAN
Optimalisasi Reaksi Epoksidasi
Minyak jarak pagar terdiri dari trigliserida dan asam lemak bebas. Kedua penyusun minyak tersebut tidak dipisahkan terlebih dahulu untuk mendapatkan rendemen metil
ester yang besar. Baik trigliserida maupun asam lemak bebas sama-sama memiliki ikatan rangkap 2. Asam lemak bebas diestrifikasi, sedangkan trigliseridanya ditransesterifikasi membentuk metil ester jarak pagar, sehingga proses epoksidasi menghasilkan senyawa epoksida campuran.
Kondisi optimum untuk reaksi epoksidasi MEJP ditentukan dengan meragamkan peubah-peubah reaksi yang meliputi suhu, waktu, dan konsentrasi katalis zeolit. Produk epoksidasi dari masing-masing kondisi tersebut dianalisis parameter mutunya, yaitu rendemen, bilangan iodin dan bilangan oksirana. Data rendemen, bilangan iod dan bilangan oksirana tersebut selengkapnya ditunjukkan pada Lampiran 4. Seperti ditunjukkan pada Tabel 4, bilangan iodin produk yang optimum menurun dibandingkan dengan MEJP awal. Sebaliknya, bilangan oksirana meningkat. Hasil ini memperlihatkan bahwa telah berlangsung reaksi epoksidasi.
Tabel 4 Sifat-sifat mutu MEJP & MEJP Terepoksidasi
Parameter MEJP
awal
MEJP Terepoksidasi Bilangan iodin
(g I/100 g MEJP)
97.00 76.19
Bilangan oksirana (%)
0.04 0.65
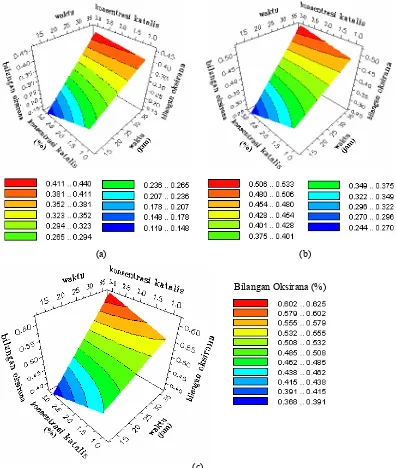
Gambar 5 menunjukkan pengaruh waktu dan konsentrasi zeolit pada suhu 50 oC [Gambar 5 (a)], 60 oC [Gambar 5 (b)], dan 70
o
C [Gambar 5 (c)] terhadap bilangan oksirana. Semakin tinggi konsentrasi zeolir dengan bertambahnya waktu epoksidasi menghasilkan bilangan oksirana yang semakin tinggi pula. Bilangan oksirana berturut-turut pada suhu 50, 60, dan 70 oC naik dari 0.21–0.24% menjadi 0.38–0.41%, 0.32–0.35% menjadi 0.48– 0.51%, dan 0.44–0.46% menjadi 0.58–0.60%. Suhu yang semakin tinggi cenderung menigkatkan bilangan oksirana. Suhu 70 oC menghasilkan bilangan oksirana maksimum (0.60– 0.63%) lebih tinggi daripada suhu 60
o
6
(a) (b)
Bilangan Oksirana (%)
(c)
Gambar 5 Pengaruh waktu dan konsentrasi zeolit pada suhu: (a) 50 oC, (b) 60 oC, dan (c) 70 oC terhadap bilangan oksirana.
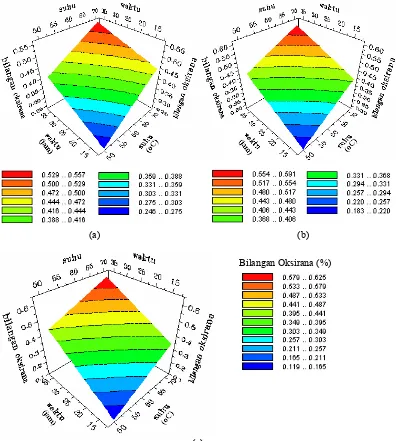
Gambar 6 menunjukkan pengaruh waktu dan suhu pada penggunaan konsentrasi zeolit 1% [Gambar 6 (a)], 2% [Gambar 6 (b)], dan 3% [Gambar 6 (c)] terhadap bilangan oksirana. Semakin tinggi suhu dan semakin lama waktu epoksidasi, bilangan oksirana yang dihasilkan semakin tinggi pula. Kenaikan bilangan oksirana pada konsentrasi zeolit 1, 2, dan 3% berturut-turut ialah dari 0.25–0.28% menjadi 0.50–0.53%, 018–0.22% menjadi 0.52–0.55%, dan 0.12–0.17% menjadi 0.53–0.58%. Bilangan oksirana cenderung meningkat dengan konsentrasi
7
(a) (b)
Bilangan Oksirana (%)
(c)
Gambar 6 Pengaruh waktu dan suhu pada konsentrasi zeolit: (a) 1%, (b) 2%, dan (c) 3% terhadap bilangan oksirana.
Gambar 7 menunjukkan pengaruh suhu dan konsentrasi zeolit pada waktu 12 jam [Gambar 7 (a)], 24 jam [Gambar 7 (b)], dan 36 jam [Gambar 7 (c)] terhadap bilangan oksirana. Semakin tinggi suhu dan semakin besar konsentrsasi zeolit yang digunakan, bilangan oksirana yang dihasilkan semakin tinggi pula. Bilangan oksirana naik dari 0.21– 0.24% menjadi 0.34–0.37%, 0.32–0.34% menjadi 0.47–0.49%, dan 0.41–0.43% berturut-turut pada waktu 12, 24 dan 36 jam. Semakin lama waktu epoksidasi, bilangan oksirana cenderung meningkat. Waktu 36 jam menghasilkan bilangan oksirana (0.61–0.63%) yang lebih tinggi dibandingkan dengan waktu
24 jam (0.49–0.51%) dan 12 jam (0.43– 0.46%). Kenaikan bilangan oksirana tersebut disebabkan dengan semakin lamanya waktu reaksi epoksidasi, maka semakin besar pula kesempatan pereaksi-pereaksi untuk bereaksi dengan MEJP membentuk senyawa epoksida.
8
.
(a) (b)
Bilangan Oksirana (%)
(c)
Gambar 7 Pengaruh suhu dan konsentrasi zeolit dengan waktu: (a) 12 jam, (b) 24 jam, dan (c) 36 jam terhadap bilangan oksirana.
Tabel 5 Kondisi optimum reaksi epoksidasi menggunakan Modde 5.
Analisis FTIR
Spektrum FTIR untuk bahan awal (MEJP) dan untuk produk optimum epoksidasi (MEJPT) memperlihatkan bilangan
gelombang yang hampir sama. Terlihat adanya gugus C=O ester pada bilangan gelombang 1743.5 cm-1, C=C pada bilangan
gelombang 1654.8 cm-1, dan C–O pada
bilangan gelombang 1018.3, 1118.6, 1168.8, 1195.8, dan 1245.9 cm-1 (Lampiran 5 & 6). Waktu suhu [katalis] bil. oksirana iter log[D]
9
tingkat ketidakjenuhan yang tinggi akan mengikat iodin dalam jumlah yang lebih besar. Bagaimanapun, penurunan bilangan iodin tidak sebanding dengan pertambahan bilangan oksirana. Hal tersebut dapat terjadi dikarenakan oksidasi dan atau pembukaan cincin oksirana (Lampiran 8). Pembukaan cincin dapat terjadi pada suasana asam dan serangan peroksida pada proses epoksidasi (Campanella & Baltanas 2005).
Validasi Kondisi Reaksi Epoksidasi
Validasi dilakukan dengan kondisi suhu dan konsentrasi katalis optimum selama 36 jam. Pengambilan sampel untuk dianalisis bilangan oksirana dan bilangan iodinnya dilakukan setiap 9 jam. Hasilnya ditunjukkan pada Tabel 6, sedangkan grafik hubungan waktu terhadap bilangan oksirana dan waktu terhadap bilangan iodin dapat dilihat pada Lampiran 9 Terlihat bahwa bilangan oksirana maksimum dan optimum terjadi pada jam ke-36, yaitu sebesar 1.33%. Dengan demikian prediksi kondisi optimum yang dihasilkan untuk memperoleh bilangan oksirana optimum dengan menggunakan perangkat lunak Modde 5 (Tabel 5) dapat dikatakan sahih.
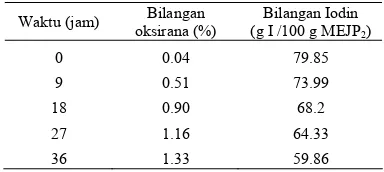
Tabel 6 Bilangan oksirana dan bilangan iodin hasil validasi kondisi optimum.
Waktu (jam) Bilangan oksirana (%)
Bilangan Iodin (g I /100 g MEJP2)
0 0.04 79.85
9 0.51 73.99
18 0.90 68.2
27 1.16 64.33
36 1.33 59.86
Hasil analisis keragaman atau ANOVA (Lampiran 10) menghasilkan persamaan pengaruh suhu reaksi, konsentrasi zeolit, dan waktu epoksidasi, serta interaksinya terhadap respons yang diukur, yaitu bilangan oksirana. Persamaan yang didapat adalah
Y= 0.402752 + 0.104094a + 0.100039b –
0.0146334c – 0.0157333ab +
0.0403583ac + 0.00856666bc. Keterangan:
a = waktu reaksi b = suhu reaksi
c = konsentrasi katalis zeolit
ab = interaksi waktu dengan suhu reaksi ac = interaksi waktu dengan konsentrasi katalis zeolit
bc = interaksi suhu reaksi dengan konsentrasi katalis zeolit
Persamaan tersebut memberikan pengaruh nyata terhadap bilangan oksirana dengan nilai peluang (P) 0.000, lebih kecil daripada taraf α (5%). Hal ini membuktikan bahwa perbedaan suhu, waktu, dan konsentrasi zeolit akan memengaruhi besarnya bilangan oksirana yang diperoleh.
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil penelitian dapat disimpulkan bahwa kondisi optimum reaksi epoksidasi MEJP menurut Modde 5 diperoleh
pada waktu 36 jam, suhu 70 oC, dan
konsentrasi katalis zeolit 3% dengan nilai bilangan oksirana sebesar 0.63%. Prediksi kondisi optimum ini sejalan dengan hasil validasi yang menghasilkan bilangan oksirana optimum sebesar 1.33% pada waktu 36 jam dengan suhu dan konsentrasi zeolit yang sama.
Saran
Suhu penyimpanan MEJP diperhatikan, karena kondisinya yang sangat tidak stabil. Selain itu, suhu, waktu, dan konsentrasi katalis yang lebih tinggi perlu diujikan. Aktivasi katalis juga perlu dioptimumkan terlebih dahulu agar diperoleh rendemen dan nilai bilangan oksirana yang lebih tinggi.
DAFTAR PUSTAKA
Ahmad S et al. 1987. Potential Application of Epoxydized Palm Oil in Plastic and Rubber Industries. Di dalam Palm Oil Conferences. Conferences II: Technolog; [tempat tidak diketahui], 29 Juni–1 Juli 1987.
Anonim. 2006. Preparation of Epoxides. [terhubung berkala]. http://www.mhhe .com/physsci/chemistry/carey/student/old/ graphics/carey04oc/ref/ch16prepareepoxid es.html [25 April 2006].
Bernardini E. 1983. Vegetable Oils and Fats
Processing. Volume ke-2. Rome:
10
Boocock R et al. 1998. Fast formation of high-purity methyl esters from vegetable oils. J Am Oil Chem Soc 75:1167-1172.
Campanella A, Baltanas MA. 2005. “Degradation of the oxirane ring of epoxidized vegetable oils in liquid-liquid system: I. hydrolysis and attack by H2O2”.
La. Am Appl Res 35: 205-210.
Cavanaugh T. 1995. Plastics Additives’95. Chemical Marketing Reporter p. SR. 10. [terhubung berkala]. http://www.carbo-hydrate economy.org/library/admin/ uploadedfiles/Biochemical Plasticizers. html [24 April 2006].
Chou TC, Lee V. 1997. Epoxidation of oleic acid in the present of benzaldehyde using cobalt (II) tetraphenylporpirin as catalyst. Indust Eng Res 36:1485-1490.
Gall RJ, Greenspan FP. 1953. Epoxy fatty acid ester plasticizer. Indust Eng Chem 45:2722-2726.
Gubitz GM, Mittelbatch M, Trabi M. 1999. Exploitation of the tropical oil seed plant Jatropha curcas L. Bioresource Tech 67:73-82.
Hamdan H. 1992. Introduction to zeolites: Synthesis, characterization, and modification [disertasi]. Malaysia: Malaysia Univ Teknol.
Handoko SD. 2002. Preparasi katalis Cr/Zeolit melalui modifikasi zeolit alam [tesis]. Jember: FMIPA Universitas Jember.
Hazimah AH, Salimah A, Ahmad I. 2000. Epoxidation palm oil creates exciting avenues for palm-based industrilisation. Forum Information Service ISSN 0218-5726.
Heyne K. 1987. Tumbuhan Berguna Indonesia. Jilid ke-2. Jakarta: Yayasan Sana Wana Jaya.
Jaya I. 2005. Optimasi sintesis biodiesel dari minyak jarak pagar (Jatropha curcas L.) melalui proses esterifikasi-transesterifikasi [skripsi]. Bogor: Departemen Kimia FMIPA IPB.
Kirk RE, Othmer DF. 1965. Encyclopedia of Chemical Technology. Volume ke-8. Ed ke-2. New York: J Wiley.
Montgomery DC. 1991. Design and Analysis of Experiments. New York: J Wiley.
Noureddini H, Harkey D, Medikonduru V. 1998. A continuous process for the conversion of vegetable oils into methyl esters of fatty acids. J Am Oil Chem Soc 75:1775-1783.
Paoletti R, Kritchevsky D. 1969. Advance in Lipid Research. Volume 77. New York: Academic Pr.
Paquot C, Hautfene A. 1987. Standard
Method for the Analysis of Oil, Fats, and
Derivatives of IUPAC. London:
Blackwell.
Rangrajan B, Harvey A. 1995. Kinetic parameter of a two-phase model for in-situ epoxidation of soybean oil. JAOAC 72: 10.
Riberio FR, Rodrigues AE, Deane RL, Claude N. 1984. Zeolite Science and Technology. Netherland: Martinus Nighoff.
Rios LA. 2003. Heterogeneously catalyzed reactions with vegetable oils: Epoxidation and nucleophilic epoxide ring-opening with alcohol [disertasi]. The Institute of Chemical Technology and Heterogenous Catalysis. University RWTH-Aachen.
Smith K. 1992. Solid Support and Catalyst in
Organic Synthesis. London: Ellis
Horwood.
Solomons TWG. 1980. Organic Chemistry. Ed ke-2. New York: J Wiley.
Sujatmaka. 1991. Prospek Pasar dan
Budidaya Jarak. Jakarta: Penebar
Swadaya.
Supriyadi S. 1992. Proses in-situ epoksidasi minyak sawit. Perkebunan 23:15-123.
Swern D, editor. 1979. Bailey’s Industrial Oil and Fat Products. Ed ke-4. Volume ke-2. New York: J Wiley.
Tang YR. 2003. Adsorbent Fundamental and Applications. Canada: J Wiley.
12
Lampiran 1 Skema pembentukan tapak asam BrÖnsted dan Lewis pada zeolit
O O O
O OO O
Al
- Si T
O O O
O OO O
Al
- Si
H+
+NH3
NH4+
(a)
O O O
O OO O
Al
- Si
Mn+(H2O)n
-Al
O O
O O O O
O OO O
Al
- Si
-Al
O O
O H+ MnOH+
-(H2O)n-1
(b)
O O O
O O O O
Al
- Si
H+
O O
O O O O
Al
Si
+
-OH
-(c)
(a) Perlakuan termal terhadap amonium-zeolit sehingga diperoleh bentuk H-Zeolit. (b) Dehidrasi terhadap kation multivalen pada zeolit menghasilkan tapak asam Bronsted. (c) Dehidroksilasi dua gugus yang berdekatan pada suhu lebih besar dari 4770C
13
Lampiran 2 Prosedur penentuan sifat-sifat bahan baku
Bilangan Oksirana
Sampel sebanyak (0.3–0.5) g (± 0.0001 g) ditimbang, lalu dimasukkan ke dalam labu Erlenmeyer 50 mL, kemudian dilarutkan dalam 10 mL asam asetat glasial. Setelah itu, ditambahkan indikator kristal ungu sebanyak 5 tetes (maksimum 0.1 mL), lalu dititrasi dengan larutan HBr 0.1 N sampai berwarna hijau kebiruan selama 30 detik.
contoh
bobot
60
1
oksirana
Bilangan
=
V
×
N
×
.
dengan:
V = volume HBr (mL)
N = normalitas HBr
Bilangan Iodin
Ditimbang ± 0.5 g contoh lemak/minyak ke dalam Erlenmeyer 250 mL lalu ditambahkan 10 mL kloroform dan 25 mL larutan Hanus (IBr), kemudian didiamkan selama 3 jam dalam ruang gelap. Setelah itu, ditambahkan 20 mL KI 10% dan Erlenmeyer segera ditutup. Dikocok sebentar lalu dititrasi dengan larutan Na2S2O3 0.1 N. Setelah titrat berwarna kuning muda, ditambahkan 5
tetes indikator amilum 1% dan dititrasi kembali sampai warna biru tepat hilang. Dikerjakan juga penetapan blangko.
Pembuatan larutan Hanus. Sebanyak 13.2 g iodium murni dilarutkan dalam 1 liter asam asetat glasial sambil dipanaskan sehingga iodium melarut sempurna (lakukan dengan hati-hati di ruang asam). Larutan tersebut dibiarkan sampai dingin. Setelah itu, ditambahkan 3 ml brom sehingga larutan berwarna kelabu tua. Larutan disimpan dalam botol berwarna gelap dan ditutup rapat. Bilangan iod dihitung sebagai berikut:
Bilangan iod =
M
)
V
(V
T
12.69
×
×
3−
4Dengan:
T : Normalitas larutan standar Na2S2O3 0.1 N
V3 : Volume larutan Na2S2O3 0.1 N yang diperlukan untuk mentitrasi larutan
blanko (mL).
V4 : Volume larutan Na2S2O3 0.1 N yang diperlukan untuk mentitrasi larutan
14
Lampiran 3 Bagan alir reaksi epoksidasi
NaHCO3
10 g MEJP 0.8 mL CH3COOH
2.9 mL Toluena Zeolit (1-3)%
Direaksikan pada: 1. Suhu: (50-70)0C
2. Waktu: 12-36 jam
Penyaringan
5.78 g H2O2 35%
Netralisasi (Pengukuran pH)
Pencucian berulang kali
Lapisan bawah Lapisan atas
Pengamatan:
1. Penentuan bilangan iodin 2. Penentuan bilangan oksirana
3. Analisis dengan FTIR Analisis Optimasi dengan metode MLR
Membuat kurva pengaruh variasi [katalis], suhu (T), dan waktu (r) terhadap bilangan oksirana.
15
Lampiran 4 Data rendemen, bilangan iodin, dan bilangan oksirana
Waktu (jam)
Kondisi Suhu
(oC) Konsentrasi katalis (%)
Bilangan Iodin (g I/100 g MEJP)
Bilangan
Oksirana (%) Rendemen (%)
50 88.26 0.20 89.00
60 1 85.84 0.29 90.15
70 83.63 0.41 92.46
50 81.40 0.18 99.54
12 60 2 80.80 0.28 79.16
70 80.61 0.43 78.67
50 82.79 0.12 96.28
60 3 82.60 0.25 94.85
70 81.52 0.33 92.27
50 87.84 0.37 82.98
60 1 86.00 0.47 79.63
70 83.24 0.61 89.78
50 88.91 0.37 87.00
24 60 2 85.84 0.55 94.18
70 85.21 0.55 72.28
50 80.13 0.24 96.19
60 3 79.81 0.37 95.04
70 78.67 0.49 91.04
50 79.60 0.33 92.93
60 1 78.30 0.57 96.09
70 76.44 0.57 89.11
50 78.99 0.45 97.15
36 60 2 77.55 0.53 76.28
70 76.95 0.57 73.79
50 78.73 0.4072 92.83
60 3 78.05 0.4925 92.17
16
Lampira
n 5
Spekt
rum
FT
IR MEJP
17
Lamp
iran
6
Sp
ek
tu
m FTIR
M
E
JPT d
eng
an
k
atalis
zeo
18
Lampiran 7 Pengaruh waktu dan suhu dengan konsentrasi zeolit: (a) 1%, (b) 2%, dan (c) 3% terhadap bilangan iod
Lampiran 7 Pengaruh waktu dan suhu dengan konsentrasi zeolit: (a) 1%, (b) 2%, dan (c) 3% terhadap bilangan iod
Bilangan Iodin (g I /100 g MEJP) Bilangan Iodin (g I /100 g MEJP)
Bilangan Iodin (g I /100 g MEJP)
Bilangan Iodin (g I /100 g MEJP)
(a)
(a)
18
Bilangan Iodin (g I /100 g MEJP)
Bilangan Iodin (g I /100 g MEJP)
(b)
19
.Lampiran 8 Produk-produk pembukaan cincin oksirana
Lampiran 9 Grafik hubungan waktu Vs bilangan oksirana dan waktu Vs bilangan iodin hasil validasi
waktu Vs bil.oksirana
y = 0.036x + 0.1411 R2 = 0.9653
0.00 0.30 0.60 0.90 1.20 1.50 1.80
0 6 12 18 24 30 36 42
w ak tu (jam )
b il. o k s ir a n a ( % )
waktu Vs bil.iodin
y = -0.5516x + 79.174 R2 = 0.9924
50 55 60 65 70 75 80
0 6 12 18 24 30 36 42
waktu (jam) b il.io d in (g I/1 0 0 g M E J P )
CH3COOH
R1 C
H
CH R2
O
H2O
H+
H2O2
R1 C
O
C H2
R2
R1 C
H C H
R2
OH OCOCH3
R1 C
H C H
R2
OH OH
R1 C
H C H
R2
20
Lampiran 10 Hasil uji ANOVA dan koefisien kuadratik
Uji ANOVA untuk bilangan oksirana
source DF SS MS F P SD
(variance)
Total 27 4.8643 0.180159
Constant 1 4.37964 4.37964
Total Corrected 26 0.484657 0.0186406 0.136531
Regression 6 0.402434 0.0670724 16.3148 0.000 0.258983 Residual 20 0.0822225 0.00411113 0.0641181
Lack of Fit -- -- -- -- -- --
(Model Error)
Pure Error -- -- -- --
(Replicate Error)
N = 27 Q2 = 0.681 Cond. no. = 1.5 DF = 20 R2 = 0.83 Y-miss = 0
R2 Adj.
= 0.779 RSD = 0.0641
Uji koefisien kuadratik untuk bilangan oksirana
source Coeff. SC Std. Err. P
Conf. int(±)
Constant 0.402752 0.0123395 8.02E-19 0.0257399 Wak 0.104094 0.0151128 1.08E-06 0.0315248
Suh 0.100039 0.0151128 1.91E-06 0.0315248
Kon -0.0146334 0.0151128 0.34447 0.0315248 wak*suh -0.0157333 0.0185093 0.405373 0.0386098 wak*kon 0.0403583 0.0185093 0.041341 0.0386098 suh*kon 0.00856666 0.0185093 0.648482 0.0386098
N = 27 Q2 = 0.681
Cond. no.
= 1.5
DF = 20 R2 = 0.83 Y-miss = 0
R2 Adj. = 0.779 RSD = 0.0641
Conf. lev.