PENGARUH NISBAH BAHAN BAKU – PELARUT DAN SUHU EKSTRAKSI TERHADAP KANDUNGAN XANTHORRHIZOL DALAM OLEORESIN
TEMULAWAK (Curcuma xanthorrhiza ROXB.)
Oleh:
NOVI PUSPITA YULIANTI F34050988
2010
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
PENGARUH NISBAH BAHAN BAKU – PELARUT DAN SUHU EKSTRAKSI TERHADAP KANDUNGAN XANTHORRHIZOL DALAM OLEORESIN
TEMULAWAK (Curcuma xanthorrhiza ROXB.)
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh:
NOVI PUSPITA YULIANTI F34050988
2010
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
Judul Skripsi : PENGARUH NISBAH BAHAN BAKU – PELARUT DAN SUHU EKSTRAKSI TERHADAP KANDUNGAN
XANTHORRHIZOL DALAM OLEORESIN TEMULAWAK (Curcuma Xanthorrhiza Roxb.) Nama : Novi Puspita Yulianti
NRP : F43050988
Menyetujui,
Bogor, Agustus 2010
Dosen Pembimbing I Dosen Pembimbing II
Dr. Ir. Meika Syahbana Rusli, MSc Ir. Wahyu Purwanto, MSc NIP : 19620505 198903 1 027 NIP : 19631005 198903 1 005
Mengetahui,
Ketua Departemen Teknologi Industri Pertanian
Prof. Dr. Ir. Nastiti Siswi Indrasti NIP : 19621009 198903 2 001
Novi Puspita Yulianti. F34050988. Pengaruh Nisbah Bahan Baku – Pelarut dan Suhu Ekstraksi terhadap Kandungan Xanthorrhizol dalam Oleoresin Temulawak (Curcuma xanthorhiza roxb.). Di bawah bimbingan Meika Syahbana Rusli dan Wahyu Purwanto. 2010.
RINGKASAN
Temulawak (Curcuma xanthorrhiza Roxb.) merupakan salah satu tanaman dalam suku temu – temuan (Zingiberaceae) yang memiliki berbagai khasiat. Menurut Sidik at all (1995), temulawak berkhasiat sebagai anti inflamasi, antitumor, mengobati penyakit hipokolesterolemia, mengobati gangguan fungsi hati, memperbaiki fungsi saluran cerna, bersifat antibakteri dan antijamur, dan sebagai antijerawat. Khasiat yang dimiliki oleh temulawak ini tidak lepas dari komponen yang terkandung di dalam rimpang temulawak. Kurkuminoid dan xanthorrhizol diduga sebagai komponen yang memberikan efek farmakologis dari rimpang temulawak. Kurkuminoid merupakan pigmen yang memberikan warna kuning terhadap temulawak, sedangkan xanthorrhizol merupakan salah satu komponen minyak atsiri temulawak.
Sejauh ini, temulawak diperdagangkan dalam beberapa bentuk yaitu bentuk rimpang temulawak yang utuh, serbuk temulawak, oleoresin temulawak, dan minyak atsiri temulawak. Penggunaan bahan baku temulawak dalam bentuk rimpang utuh maupun serbuk memiliki beberapa kelemahan, diantaranya adalah bersifat kamba, mudah mengalami perubahan warna dan aroma yang diakibatkan oleh perubahan iklim, mudah terkontaminasi oleh bahan asing, mudah terkontaminasi mikroorganisme, pada tahap aplikasi komponen aktif dihasilkan secara lambat dan tidak terekstrak secara sempurna, dan partikel rimpang mengakibatkan adanya bintik atau noda pada produk akhir (Ravindran at all, 2007). Untuk menutupi kelemahan – kelemahan tersebut, temulawak dapat dimanfaatkan dalam bentuk oleoresin. Oleoresin didefinisikan oleh Glibertson (1971) sebagai campuran antara resin dan minyak atsiri yang diekstrak dari berbagai jenis rempah, baik rempah yang berasal dari buah, biji, daun, kulit, maupun rimpang dengan menggunakan pelarut organik. Pada proses ekstraksi dengan menggunakan pelarut ini, terdapat beberapa faktor yang dapat mempengaruhi efisiensi dan efektifitas ekstraksi. Faktor tersebut diantaranya adalah jenis dan konsentasi pelarut yang digunakan, volume pelarut, suhu ekstraksi, dan ukuran bahan yang diekstrak.
Pada penelitian ini, faktor suhu ekstraksi dan volume pelarut diamati guna mengetahui pengaruhnya terhadap kadar xanthorrhizol yang terdapat dalam oleoresin temulawak. Pengaruh kedua faktor tersebut juga diamati terhadap rendemen oleoresin, kadar kurkumin, kadar minyak atsiri, kadar sisa pelarut dan indeks bias oleoresin temulawak. Suhu ekstraksi yang diamati pada penelitian ini terdiri dari tiga taraf, yaitu 30oC, 40oC dan 50oC. Faktor volume pelarut ditunjukkan dengan nisbah bahan baku - pelarut. Nisbah yang digunakan juga terdiri dari tiga taraf, yaitu 1:4, 1:6, dan 1:8 dengan menggunakan 100 gram serbuk temulawak sebagai dasar perbandingan.
mencapai ukuran 60 mesh. Selanjutnya, temulawak yang telah berbentuk serbuk tersebut diekstrak dengan menggunakan pelarut etanol 96% selama empat jam dan dibiarkan pada suhu ruang selama 24 jam. Kemudian dilakukan proses pemisahan ekstrak dengan ampas temulawak. Untuk menghilangkan pelarut dari oleoresin temulawak, maka dilakukan proses penguapan dengan menggunakan vacuum rotary evaporator pada suhu 50oC.
Rendemen oleoresin temulawak yang dihasilkan berkisar antara 9,40% - 17,77% (b/b). Hasil analisis menunjukkan bahwa kadar kurkumin yang terdapat dalam oleoresin temulawak berkisar antara 1,11 – 3,88 %, kadar minyak atsiri berkisar antara 3,64 – 11,43 %, persen area xanthorrhizol dalam bahan volatile pada oleoresin temulawak berkisar antara 1.26 - 42,82 %, kadar sisa pelarut dalam oleoresin berkisar antara 40.950 – 63.750 ppm, dan nilai indeks bias oleoresin temulawak (20/200C) berkisar antara 1,4817 – 1,5198.
Analisis keragaman dilakukan dengan menggunakan software SPSS dengan menggunakan tingkat kepercayaan 95% untuk mengetahui pengaruh faktor suhu ekstraksi dan pengaruh nisbah bahan baku - pelarut terhadap rendemen dan analisa lainnya yang dilakukan terhadap oleoresin temulawak. Hasil analisis keragaman menunjukkan bahwa faktor suhu ekstraksi dan nisbah bahan baku berpengaruh secara nyata terhadap kadar minyak atsiri. Peningkatan suhu mengakibatkan terjadinya kenaikan kadar minyak atsiri yang terdapat di dalam oleoresin temulawak. Hasil uji lanjut Duncan menunjukkan bahwa suhu 50°C memberikan pengaruh yang berbeda nyata dibandingkan suhu 30°C dan 40°C. Kenaikan nisbah bahan baku - pelarut mengakibatkan terjadinya penurunan kadar minyak atsiri. Hasil uji lanjut Duncan menunjukkan bahwa ekstraksi dengan menggunakan nisbah 1:8 menghasilkan kadar minyak atsiri yang paling rendah dibandingkan nisbah 1:4 dan 1:6.
Persen area xanthorrhizol hanya dipengaruhi oleh faktor suhu ekstraksi, sedangkan nisbah bahan baku - pelarut tidak memberikan pengaruh yang signifikan. Peningkatan suhu ekstraksi mengakibatkan penurunan persen area xanthorrhizol. Suhu ekstraksi 50°C menghasilkan persen area xanthorrhizol yang paling rendah. Hal tersebut diakibatkan oleh terjadinya kerusakan komponen minyak atsiri yang disebabkan oleh penggunaan suhu yang terlalu tinggi.
Faktor nisbah bahan baku - pelarut berpengaruh secara nyata terhadap nilai rendemen dan indeks bias oleoresin temulawak, sedangkan faktor suhu tidak memberikan pengaruh yang nyata terhadap kedua parameter tersebut. Peningkatan volume perlarut mengakibatkan terjadinya kenaikan jumlah oleoresin yang terekstrak, sehingga meningkatkan nilai rendemen ekstraksi. Namun peningkatan nisbah tersebut mengakibatkan terjadinya penurunan nilai indeks bias oleoresin. Hasil uji lanjut Duncan untuk kedua parameter tersebut menunjukkan bahwa nisbah 1:8 memberikan hasil yang berbeda nyata dibandingkan nisbah 1:4 dan1:6.
Novi Puspita Yulianti. F34050988. Influence of Raw Material-Solvent Ratio and Extraction Temperature to the Xanthorrhizol Content of Temulawak (Curcuma xanthorhiza Roxb.) Oleoresin. Supervised by Meika Syahbana Rusli and Wahyu Purwanto. 2010.
SUMMARY
Temulawak (Curcuma xanthorrhiza Roxb.) belongs to the plant family Zingiberaceae which have various benefits. Sidik et al (1995) described that temulawak can be used as anti-inflammatory, anti-cancer, medicine for many disease like hipokolesterolemia, disorders of liver function, improved gastrointestinal function, for anti-bacterial and anti-fungal, and as anti-acne. Those benefits are related to active components of temulawak rhizhome. Curcuminoids and xanthorrhizol are predicted as components that provides pharmacological effects of temulawak rhizomes. Curcuminoids is the pigment that gives yellow color to temulawak, while xanthorrhizol is one component of the essential oil of temulawak.
Temulawak is usually prepared as rhizome slices, powder, oleoresin, and essential oil. Temulawak in form of rhizome slices or powder has some weaknesses, such as bulky, easily to have color and flavor defect caused by climate change, easily contaminated by foreign material and microorganism, slowly produce of active component in the stage application and not completely extracted, and the final product have spots or strain that caused by the rhizome particles (Ravindran et al, 2007). To avoid these weaknesses, temulawak can be processed into temulawak oleoresin. Oleoresin is defined as a mixture of resin and volatile oil extracted from various kinds of herbs, either from the fruit, seeds, leaves, bark, and rhizomes by using organic solvents (Glibertson, 1971). In the process of extraction using this solvent, there are several factors that can affect the extraction efficiency and effectiveness. These factors include the type and concentration of solvent, solvent volume, extraction temperature, and size of the extracted material
In this research, extraction temperature and solvent volume were observed to determine their effect on xanthorrhizol content of temulawak oleoresin. The effects of these factors were measured on yield of oleoresin, curcumin content, volatile oil content, solvent residu and the refractive index of the oleoresin. Extraction temperature applied in the experiments were three levels, 30 oC, 40 oC and 50 oC. The solvent volume factor is indicated by the ratio of raw materials to solvent. This study observed three levels of ratio, 1:4, 1:6, and 1:8 using 100 grams of temulawak powder as the ratio basis.
Preparation prior to extraction process includes rhizome slicing, drying, and grinding to the size of 60 mesh. Temulawak powder was extracted by stirred maceration using ethanol 96% for four hours, followed by conditioning in room temperature for 24 hours. Temulawak extract was then separated from the solid waste by filtration. The evaporation to remove the solvent from the oleoresin finally conducted using a rotary vacuum evaporator at temperature of 50oC.
residu in the oleoresin is 40.950 – 63.750 ppm, and the refractive index value (20/20oC) is ranged from 1.4817 to 1.5198.
Statistical analysis of variance at 95% confidence level was used to determine the influence of extraction temperature and raw material-solvent ratio on yield and other experiments parameters. The result showed that extraction temperature and raw material-solvent ratio significantly influenced the concentration of essential oil. Increasing temperature resulted in increasing levels of essential oil contained in temulawak oleoresin. Duncan's test results further showed that the temperature of 50 °C gives a significantly different effect than the temperature of 30 °C and 40 °C. The increase in raw material-solvent ratio resulted in decreased content of essential oil. Duncan's test results further showed that the extraction using the ratio of 1:8 produces the essential oil content lower than 1:4 and 1:6 ratios.
Peak percentage area of Xanthorrhizol is only influenced by extraction temperature, while the ratio of raw material to solvent does not have a significant influence. Increasing extraction temperature resulted in decreased peak percentage area of xanthorrhizol. At extraction temperature of 50°C the xanthorrhizol peak percentage area is extremely low. The xanthorrhizol is presumed to be destructed at this temperature.
Raw material-solvent ratio affected significantly the yield and value of the refractive index of temulawak oleoresin, while the extraction temperature has no effect on that parameters. Increasing the volume of solvent resulted in increasing oleoresin yield. However, increasing the raw material-solvent ratio resulted in a decline of the refractive index of oleoresin. Duncan further test results for these parameters indicate that the ratio of 1:8 gave significantly different results than the ratio of 1:4 and 1:6.
SURAT PERNYATAAN
Saya yang bertanda tangan di bawah ini, Nama : Novi Puspita Yulianti NRP : F34050988
Departemen : Teknologi Industri Pertanian Fakultas : Teknologi Pertanian
Universitas : Institut Pertanian Bogor
menyatakan dengan sesungguhnya bahwa Skripsi dengan judul “Pengaruh Nisbah Bahan Baku – Pelarut dan Suhu Ekstraksi terhadap Kandungan Xanthorrhizol dalam Oleoresin Temulawak (Curcuma Xanthorrhiza Roxb.) “ merupakan karya tulis saya dengan bimbingan dan arahan dari dosen pembimbing, kecuali yang dengan jelas disebutkan rujukannya.
Demikian surat pernyataan ini saya buat dengan sebenar-benarnya tanpa tekanan dari siapapun.
Bogor, Agustus 2010 Penulis,
RIWAYAT HIDUP
Penulis bernama Novi Puspita Yulianti, merupakan anak pertama dari tiga bersaudara dari pasangan Yoyo Sunaryo dan Ede Komariah SPd, dilahirkan di Tasikmalaya pada tanggal 11 Juli 1987. Pada tahun 1999 penulis menyelesaikan pendidikan tingkat dasar di SDN Margajaya dan melanjutkan ke MTsN Cilendek sampai dengan tahun 2002. Pada tahun 2005 penulis menyelesaikan pendidikan di SMAN 2 Tasikmalaya.
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Allah SWT yang telah memberikan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi ini. Skripsi ini disusun sebagai bagian dari tugas akhir untuk memperoleh gelar sarjana Teknologi Industri Pertanian Fakultas Teknologi Pertanian Institut Pertanian Bogor.
Penulis menyadari bahwa bantuan dari berbagai pihak cukup berarti bagi penulis sehingga skripsi ini dapat diselesaikan. Untuk itu penulis mengucapkan terima kasih kepada :
1. Bapak Dr. Ir. Meika Syahbana Rusli, MSc selaku dosen pembimbing I yang telah memberikan banyak saran, bimbingan, serta arahan kepada penulis sampai terselesaikannya skripsi ini.
2. Bapak Ir. Wahyu Purwanto, MSc selaku pembimbing II yang telah memberikan bimbingan dan perhatian kepada penulis sampai terselesaikannya skripsi ini. 3. Ibu Dr. Ir. Dwi Setyaningsih, MSi selaku dosen penguji yang telah memberikan
waktu dan sarannya dalam perbaikan skripsi ini.
4. Orang tua dan keluarga tercinta yang selalu memberikan dukungan kepada penulis.
5. Ibu Suryatmi, Mas Nashori, Ibu Ega, Ibu Sri, Ibu Rini, Pak Sugihardi, dan Pak Edi yang telah memberikan bantuan selama penulis melakukan analisa di laboratorium.
6. Shafik Ahmeed dan Saiful Rizal atas kebersamaannya dalam menjalani proses pembelajaran selama di TIN.
7. Nunung, Ai, Dewi, Yeni, Alin, serta teman-teman TIN 42 atas canda dan tawa, kisah, kebersamaan dan persahabatan selama 4 tahun.
8. Aa Buldhan atas perhatian dan dukungannya selama ini.
Kritik dan saran yang membangun sangat penulis harapkan. Semoga skripsi ini dapat bermanfaat baik bagi penulis maupun pembacanya. Amin.
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
DAFTAR ISI ... ii
DAFTAR TABEL ... iv
DAFTAR GAMBAR ... v
DAFTAR LAMPIRAN ... vi
I. PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Tujuan. ... .. 3
II. TINJAUAN PUSTAKA. ... 4
A. Temulawak . ... 4
B. Oleoresin Temulawak ... . 11
C. Ekstraksi Oleoresin … ... . 12
D. Pemisahan Pelarut . ... . 16
III.METODOLOGI PENELITIAN. ... . 18
A. Bahan dan Alat. ... . 18
B. Perlakuan. ... . 18
C. Prosedur Penelitian... . 18
D. Analisa Oleoresin Temulawak... . 20
E. Rancangan Percobaan. ... . 21
IV. HASIL DAN PEMBAHASAN. ... . 22
A. Persiapan Bahan Baku. ... . 22
B. Proses Ekstraksi Oleoresin Temulawak. ... . 23
1. Rendemen Oleoresin. ... . 25
2. Kadar Kurkumin. ... . 26
3. Kadar Minyak Atsiri. ... . 28
4. Kadar Kadar Xanthorrhizol dalam Bahan Volatil pada Oleoresin Temulawak ………... . 30
5. Kadar Sisa Pelarut ... . 32
V. KESIMPULAN DAN SARAN... . 35
A. Kesimpulan. ... . 35
B. Saran. ... . 36
DAFTAR PUSTAKA. ... . 37
DAFTAR TABEL
DAFTAR GAMBAR
Halaman
Gambar 1. Bunga tanaman temulawak ... 5
Gambar 2. Rimpang temulawak……… .... 6
Gambar 3. Rumus bangun xanthorrizol... 9
Gambar 4. Proses ekstraksi temulawak dengan menggunakan shaker waterbath ... 20
Gambar 5. Rimpang temulawak (Curcuma xanthorriza Roxb) ... 22
Gambar 6. Irisan temulawak (Curcuma xanthorriza Roxb) Kering. ... 23
Gambar 7. Oleoresin temulawak (Curcuma xanthorriza Roxb) ... 25
Gambar 8. Histogram pengaruh suhu ekstraksi dan nisbah bahan baku – pelarut terhadap rendemen oleoresin yang dihasilkan ... 24
Gambar 9. Histogram pengaruh suhu ekstraksi dan nisbah bahan baku – pelarut terhadap kadar kurkumin dalam oleoresin temulawak... 27
Gambar 10. Histogram pengaruh suhu ekstraksi dan nisbah bahan baku – pelarut terhadap kadar minyak atsiri dalam oleoresin temulawak... 29
Gambar 11. Histogram pengaruh suhu ekstraksi dan nisbah bahan baku – pelarut terhadap persentase luas area xanthorrhizol komparatif terhadap bahan volatile dalam oleoresin temulawak ... 31
Gambar 12. Histogram pengaruh suhu ekstraksi dan nisbah bahan baku – pelarut terhadap kadar sisa pelarut dalam oleoresin temulawak... 32
DAFTAR LAMPIRAN
Halaman Lampiran 1. Diagram alir proses ekstraksi temulawak. ... 41 Lampiran 2. Prosedur analisis oloeresin temulawak... 43 Lampiran 3a. Hasil analisis keragaman rendemen oleoresin temulawak. .... 47 Lampiran 3b. Uji lanjut duncan nisbah bahan baku dengan pelarut
terhadap rendemen oleoresion ... 48 Lampiran 4. Analisis keragaman kadar kurkumin dalam oleoresin
temulawak ... 49 Lampiran 5a. Analisis keragaman kadar minyak atsiri dalam oleoresin
temulawak ... 50 Lampiran 5b. Uji lanjut duncan suhu dan nisbah bahan baku dengan
pelarut terhadap kadar minyak atsiri
oleoresin temulawak ... 51 Lampiran 6a. Analisis keragaman persen area xanthorrizol dalam
bahan volatile pada oleoresin temulawak ... 52 Lampiran 6b. Uji lanjut duncan suhu terhadap kadar xanthorrhizol
oleoresin temulawak ... 53 Lampiran 7. Analisis keragaman kadar sisa pelarut dalam
oleoresin temulawak. ... 54 Lampiran 8a. Analisis keragaman indeks bias oleoresin temulawak ... 55 Lampiran 8b. Uji lanjut duncan nisbah bahan baku dengan pelarut
terhadap indeks bias oleoresin oleoresion ... 56 Lampiran 9. Kromatogram hasil analisis gas Kromatografi (GC)
I. PENDAHULUAN
A. Latar Belakang
Perubahan gaya hidup ke arah lebih sehat cenderung menuntut adanya perubahan pemenuhan kebutuhan hidup dengan bahan alami atau yang lebih dikenal dengan back to nature. Begitu pula dalam hal penggunaan obat-obatan, terdapat kecenderungan untuk mengkonsumsi obat-obatan yang bersumber dari bahan alami. Bahan yang secara alami memiliki kemampuan untuk mengobati suatu penyakit dikenal sebagai bahan herbal. Indonesia memiliki berbagai macam tanaman yang memiliki kemampuan untuk mengobati berbagai penyakit maupun untuk menjaga kesehatan. Menurut Gabungan Pengusaha Jamu dan Obat Tradisional Indonesia, terdapat lima bahan herbal yang termasuk sebagai produk unggulan untuk dikembangkan. Kelima komoditas tersebut adalah temulawak, jahe, sambiloto, kencur dan pegagan (Republika, 2009).
Temulawak (Curcuma xanthorrhiza Roxb.) merupakan salah satu tanaman temu – temuan (Zingiberaceae) yang memiliki berbagai khasiat dan kegunaan. Menurut Ramlan (1985) di dalam Sidik et al (1995), temulawak dapat digunakan secara luas baik sebagai rempah, bahan baku obat tradisional, bahan baku makanan maupun minuman. Sebagai tanaman obat, temulawak memiliki berbagai khasiat. Menurut Sidik et al (1995), temulawak berkhasiat sebagai anti inflamasi, antitumor, mengobati penyakit hipokolesterolemia, mengobati gangguan fungsi hati, memperbaiki fungsi saluran cerna, bersifat antibakteri dan antijamur, dan antijerawat.
Efek farmakologis yang diberikan oleh temulawak tidak lepas dari peran senyawa aktif yang terdapat dalam rimpang temulawak. Senyawa aktif yang terdapat dalam temulawak terdiri dari dua fraksi utama yaitu zat warna kurkuminoid dan minyak atsiri. Salah satu komponen minyak atsiri temulawak adalah xanthorrhizol. Menurut Taryono et al (1987), Gabungan senyawa kurkumin dengan xanthorrhizol diduga sebagai penyebab berkhasiatnya temulawak.
hepototoksik (anti keracunan empedu). Xanthorrhizol merupakan salah satu komponen minyak atsiri temulawak. Menurut Hwang (2006) xanthorrhizol merupakan antibakteri potensial yang memiliki spektrum luas terhadap aktifitas bakteri, stabil terhadap panas, dan aman terhadap manusia.
Sejauh ini, temulawak diperdagangkan dalam beberapa bentuk yaitu bentuk rimpang temulawak yang utuh, serbuk temulawak, oleoresin temulawak, dan minyak atsiri temulawak. Penggunaan bahan baku temulawak dalam bentuk rimpang utuh maupun serbuk memiliki beberapa kelemahan, diantaranya adalah bersifat kamba, mudah mengalami perubahan warna dan aroma yang diakibatkan oleh perubahan iklim, mudah terkontaminasi oleh bahan asing, mudah terkontaminasi mikroorganisme, pada tahap aplikasi komponen aktif dihasilkan secara lambat dan tidak terekstrak secara sempurna, dan partikel rimpang mengakibatkan adanya bintik atau noda pada produk akhir (Ravindran et al, 2007).
Untuk menghindari hal-hal tersebut, maka penggunaan temulawak dapat dilakukan dalam bentuk oleoresin temulawak. Menurut Glibertson (1971), oleoresin merupakan campuran antara resin dan minyak atsiri yang diekstrak dari berbagai jenis rempah, baik rempah yang berasal dari buah, biji, daun, kulit, maupun rimpang dengan menggunakan pelarut organik. Selain untuk menutupi kekurangan penggunaan temulawak dalam bentuk rimpang dan sebuk, penggunaannya dalam bentuk oleoresin dapat meningkatkan nilai jual temulawak.
Dalam proses ekstraksi oleoresin temulawak, terdapat beberapa faktor yang berpengaruh terhadap mutu oleoresin yang dihasilkan. Ravindran et al (2007) menjelaskan bahwa faktor yang mempengaruhi proses ekstraksi oleoresin diantaranya adalah jenis dan konsentasi pelarut yang digunakan, suhu ekstraksi, dan ukuran bahan yang diekstrak. Selain itu, faktor volume dan lama ekstraksi juga dapat mempengaruhi proses ekstraksi oleoresin.
diamati terdiri dari tiga taraf, yaitu 4, 6 dan 8 jam dan tingkat kehalusan bahan terdiri dari dua taraf, yaitu 40 dan 60 mesh.
Hasil pengamatan Sembiring et al (2006) menunjukkan bahwa kehalusan bahan dan lama ekstraksi berpengaruh terhadap rendemen ekstraksi. Rendemen tertinggi dihasilkan pada tingkat kehalusan 60 mesh dan lama ekstraksi 6 jam, yaitu sebesar 32,49 %. Kehalusan bahan berpengaruh terhadap kadar minyak atsiri dan kadar xanthorrhizol, sedangkan lama ekstraksi tidak berpengaruh. Kadar kurkumin tidak dipengaruhi oleh faktor kehalusan bahan dan lama ekstraksi. Kadar minyak atsiri dan kadar kurkumin tertinggi dihasilkan pada kehalusan bahan 40 mesh dan lama ekstraksi 4 jam, yaitu secara berurutan sebesar 33,03 % dan 2,88%. Tingkat kehalusan 60 mesh dan lama ekstraksi 4 jam menghasilkan kadar xanthorrhizol terpilih, yaitu sebesar 14,21 %.
Faktor lain yang berpengaruh terhadap proses ekstraksi oleoresin temulawak adalah suhu ekstraksi dan volume pelarut yang digunakan. Peningkatan penggunaan suhu dan volume pelarut yang digunakan dalam proses ekstraksi diharapkan mampu meningkatkan mutu oleoresin yang dihasilkan, terutama terjadinya peningkatan kadar xanthorrhizol didalam oleoresin tersebut. Oleh karena itu, diperlukan kombinasi yang tepat diantara kedua faktor tersebut untuk menghasilkan rendemen oleoresin optimal dengan kandungan xanthorrhizol yang paling tinggi.
B. Tujuan Penelitian
II. TINJAUAN PUSTAKA
A. Temulawak
1. Botani Tanaman Temulawak
Temulawak (Curcuma xanthorriza Roxb) merupakan salah satu tanaman obat dari suku temu-temuan (Zingiberaceae). Tanaman ini termasuk ke dalam tanaman tahunan dan tumbuh secara liar di beberapa pulau Indonesia, antara lain Jawa, Maluku, dan Kalimantan. Selain dikenal dengan nama temulawak, tanaman ini memiliki beberapa nama daerah seperti koneng gede (Sunda), temo lobak (Madura) (Hyne, 1950 di dalam Sidik et al, 1995), tommo (Bali), tommon (Sulawesi Selatan), dan di Ternate dengan nama karbanga (Gunster, 1943 di dalam Sidik et al, 1995). Menurut Rukmana (1995) kedudukan tanaman temulawak dalam sistematika tumbuhan adalah sebagai berikut.
kingdom divisi sub divisi kelas ordo family genus spesies : : : : : : : : Plantae Spermatophyta Angiospermae Monocotyledonae Zingiberales Zingiberaceae Curcuma
Curcuma xanthorriza ROXB
Secara lebih lanjut Rukmana (1995) menjelaskan bahwa temulawak termasuk tanaman tahunan yang tumbuh merumpun. Batang tanaman temulawak adalah batang semu yang merupakan metamorphosis atau penjelmaan dari daun tanaman dengan tinggi mencapai 2 – 2,5 meter. Tiap rumpun tanaman terdiri atas beberapa tanaman (anakan), dan tiap tanaman memiliki 2 – 9 helai daun. Daun tanaman berbentuk panjang dan agak lebar. Lamina daun dan seluruh ibu tulang daun bergaris hitam. Lebar helaian daun temulawak adalah ±18 cm dengan panjang daunnya 50-55 cm, tiap helaian daun melekat pada tangkai daun yang posisinya saling menutupi secara teratur
panjangnya dapat mencapai 23 cm. Bunga tanaman ini memiliki banyak daun pelindung yang panjangnya melebihi atau terkadang sebanding dengan panjang mahkota bunga. Mahkota bunga berwarna putih sampai kuning dan bagian ujungnya berwarna merah dadu atau merah. Bunga temulawak memiliki benang sari dan putik sehingga setelah terjadi fruitset maka akan terbentuk buah. Buah yang terbentuk merupakan buah yang berbulu dengan panjang 2 cm (Anonim, 2002). Bunga temulawak dapat dilihat pada Gambar 1.
Gambar 1. Bunga Tanaman Temulawak
Gambar 2. Rimpang Temulawak
2. Kandungan Kimia Rimpang Temulawak
Menurut Sidik et al (1995), kandungan kimia rimpang temulawak yang memberi arti pada penggunaanya sebagai bahan baku pangan, bahan baku industri, dan sebagai bahan baku obat terbagi menjadi beberapa fraksi, yaitu fraksi pati, fraksi kurkuminoid, dan fraksi minyak atsiri. Kandungan kimia rimpang temulawak dapat dilihat pada Tabel 2.
Tabel 1. Komposisi Kimia Rimpang Temulawak
Komponen Jumlah (% BK)
Pati 58,24
Lemak (fixes oil) 12,10
Kurkumin 1,55
Serat Kasar 4,20
Abu 4,92
Protein 2,90
Mineral (N, P, K, Na) 4,29
Minyak Atsiri 4,90
Sumber : Roeslan (1980) di dalam Ketaren (1988)
2.1Fraksi Pati
Pati temulawak memiliki bentuk bulat telur sampai lonjong dengan salah
satu ujungnya persegi dengan ukuran rerata 60 µm. Bentuk pati temulawak
ini sangat khas sehingga digunakan sebagai salah satu unsur pengenal untuk mengidentifikasi simplisia rimpang temulawak. Bentuk pati temulawak murni adalah berupa serbuk dan berwarna putih kekuningan. Warna kuning diakibatkan oleh adanya spora kurkuminoid.
Pati temulawak berpotensi untuk dikembangkan sebagai bahan makanan, campuran bahan makanan, atau sebagai sumber karbohidrat. Herman (1985) di dalam Sidik et al (1995) memberikan contoh pemanfaatan pati temulawak, yaitu sebagai pencampur pati “sereal” untuk mengurangi sifat “basi” pada produk semacam roti atau digunakan sebagai pengental pada produk sediaan sirup.
2.2Fraksi Kurkuminoid
Kurkuminoid rimpang temulawak adalah suatu zat yang terdiri dari campuran komponen senyawa kurkumin dan desmetoksikurkumin. Komponen ini berwarna kuning atau kuning jingga, berbentuk serbuk dengan rasa sedikit pahit, memiliki aroma yang khas dan tidak bersifat toksik. Kurkuminoid dapat larut dalam aseton, alkohol, asam asetat glasial, dan alkali hidroksida dan tidak dapat larut dalam air dan dietileter (Sidik et al, 1995).
Kurkumin mempunyai rumus molekul C21H20O6 dengan bobot molekul
sebesar 368, sedangkan desmetoksikurkumin memiliki rumus molekul C20H18O5 dengan bobot molekul 338. Sifat kurkuminoid yang menarik adalah
perubahan warna akibat perubahan nilai pH lingkungan. Dalan suasana asam, kurkuminoid berwarna kuning atau kuning jingga, sedangkan dalam suasana basa berwarna merah.
2.3Fraksi Minyak Atsiri
Menurut Krisnamurthy (1976) di dalam Sidik et al (1995) minyak atsiri temulawak merupakan cairan berwarna kuning atau kuning jingga yang mempunyai rasa tajam dengan bau khas aromatik. Minyak atsiri temulawak ini memiliki indeks bias 1,5130 (24°C), bobot jenis 0,9423, dan rotasi optik -140 pada 24°C. Komposisi minyak atsiri tidak selalu sama, hal tersebut dipengaruhi beberapa faktor diantaranya adalah umur rimpang, tempat tumbuh, teknik isolasi, dan teknik analisis. Pada tahun 1985, Oei Ban Liang melakukan analisis terhadap minyak atsiri temulawak dengan menggunakan kromatografi gas dan mendeteksi adanya 31 komponen penyusun minyak atsiri. Komponen minyak atsiri tersebut dapat dilihat pada Tabel 3.
Tabel 2. Komponen dalam Minyak Atsiri Temulawak
No Komponen No Komponen No Komponen
1 2 3 4 5 6 7 8 9 10 Trisiklin α-Pinen Kamfen Sabinen Mirsen -Pinen α-Felandren Limonen 1,8 Sineol -Terpinen 11 12 13 14 15 16 17 18 19 20 p-Simen Terpinolen δ-Elemen Kamfora α-Bergamoten –Elemen allo-Aroma-dendren trans- -Farnesen Borneol Germakrene 21 22 23 24 25 26 27 28 29 30 31 Zingiberen -Bisabolen -Kurkumen -Kadinen -Seskuifelandren ar-Kurkumen Isofuarano-germaken Turmeron Turmerol Ar-Turmeron Xanthorrhizol Sumber : Liang (1985) di dalam Sidik et al (1995)
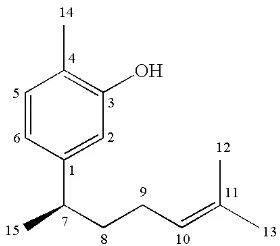
Fraksi murni xanthorrhizol berupa minyak tidak berwarna, memiliki rumus molekul C12H22O dengan bobot molekul sebesar 218,335 g/mol. Nama
IUPAC Xanthorrhizol adalah 5-(1,5-dimetilhex 4-enyl)-2-metil-phenol. Struktur xanthorrizol dapat dilihat pada Gambar 3 berikut ini.
Gambar 3. Rumus Bangun Xanthorrizol
Analisis kuantitatif miyak atsiri rimpang temulawak dapat dilakukan dengan cara distilasi clavenger atau cara distilasi stahl. Analisis kuantitatif komponen minyak atsiri dapat dilakukan melalui kromatografi lapis tipis yang digabung dengan densitometri atau melalui analisis kromatografi gas (Toussaint, 1982 di dalam Sidik et al, 1995).
3. Khasiat Farmakologi Rimpang Temulawak
oedema yang telah melakukan operasi. Oedema atau edema merupakan pembengkakan atau sembab yang disebabkan oleh penimbunan cairan abnormal dalam sela-sela jaringan dan rongga-rongga badan sebagai akibat adanya peningkatan volume cairan ekstraseluler dan ekstravaskuler.
Selain sebagai antiinflamasi, temulawak juga mempunyai aktivitas hipokolesterolemik. Rio (1970) di dalam Sidik (1995) melaporkan bahwa pemberian kurkuminoid kepada hewan percobaan yang mengalami hipokolesterolemia mampu menurunkan kadar kolesterol total dan mempunyai indikasi meningkatkan kadar lipoprotein densitas tinggi (HDL) kolesterol.
Temulawak juga memiliki aktivitas antijamur atau fungistatik terhadap beberapa jamur golongan dermatophyta. Selain itu, temulawak juga bersifat bakteriostatik atau antibakteri pada mikroba jenis staphylococcus dan salmonella. Pada dunia kosmetika, temulawak digunakan sebagai antijerawat. Hal ini disebabkan temulawak bersifat astringen (Afifah, 2003).
B. Oleoresin Temulawak
Ravindran et al (2007) menjelaskan bahwa penggunaan bahan-bahan rempah dalam bentuk rimpang utuh maupun bentuk serbuk memiliki beberapa kelemahan. Kelemahan-kelemahan tersebut diantaranya adalah sebagai berikut.
1. Bersifat kamba, sehingga memerlukan biaya transportasi yang tinggi dan memerlukan fasilitas gudang penyimpanan yang lebih besar.
2. Mudah mengalami perubahan warna dan aroma yang diakibatkan oleh perubahan iklim.
3. Mudah terkontaminasi oleh bahan asing, baik yang berasal dari proses pemanenan, penanganan pasca panen, penyimpanan, maupun dari transportasi.
4. Mudah terkontaminasi mikroorganisme yang mengakibatkan pendeknya daya simpan rimpang.
5. Pada tahap aplikasi, komponen aktif dihasilkan secara lambat dan tidak terekstrak secara sempurna.
6. Partikel rimpang mengakibatkan adanya bintik/noda pada produk akhir.
Untuk mengatasi kelemahan-kelemahan tersebut, rempah dapat digunakan dalam bentuk oleoresin. Rismunandar (1988) mendefinisikan oleoresin sebagai benda semi padat berbentuk pasta yang merupakan campuran dari minyak atsiri pembawa aroma dan sejenis dammar sebagai pembawa rasa. Menurut Gilbertson (1971) oleoresin dapat diekstrak dari berbagai jenis rempah, baik rempah yang berasal dari buah, biji, daun, kulit, maupun rimpang. Menurut Stanforth (1973) oleoresin dapat diperoleh melalui ekstraksi dengan menggunakan pelarut organik, sehingga selain mengandung minyak atsiri juga mengandung resin yang tidak dapat menguap dan menentukan rasa khas rempah.
pelarut yang dapat digunakan adalah alkohol, heksan, etil asetat, etil alkohol, isopropil alkohol, aseton, dan gliserol. Diantara bahan-bahan tersebut, alkohol banyak dipakai karena relatif aman untuk makanan, sifat polarnya banyak membantu dalam mendapatkan emulsi oleresin yang baik, dan mempermudah kelarutannya dalam air.
Selain menutupi kelemahan penggunaan rempah dalam bentuk rimpang dan serbuk, oleoresin juga memiliki keunggulan. Menurut Somaatmadja (1981), kelebihan penggunaan oleoresin untuk suatu industri terutama industri pangan adalah oleoresin yang diekstrak dengan menggunakan pelarut organik bersifat steril, dapat menghasilkan produk dengan mutu yang terjamin, dan penggunaan rempah akan lebih ekonomis dan efisien. Cripps (1973) menyatakan keuntungan penggunaan oleoresin dibandingkan dengan bentuk aslinya adalah higienis, kekuatan flavornya dapat distandarisasi, mengandung antioksidan alami, bebas dari enzim, dan memiliki waktu simpan yang lebih lama pada kondisi yang ideal.
Enzim dalam bahan pertanian dapat menyebabkan terjadinya kerusakan kimiawi terhadap bahan tersebut. Kerusakan bahan dapat ditandai dengan terjadinya perubahan warna sebagai akibat terjadinya reaksi pencoklatan enzimatis dan timbulnya ketengikan. Ketengikan dapat timbul dengan adanya kerusakan lemak oleh reaksi oksidasi yang dipercepat oleh adanya enzim lipoksidase (Syarief, 1993).
Sedangkan kekurangan oleoresin menurut Koswara (2009) antara lain sangat pekat dan kadang-kadang lengket sehingga sulit ditimbang dengan tepat, flavor oleoresin dipengaruhi oleh asal dan kualitas bahan mentah yang mungkin asalnya tidak sama, sejumlah tannin masih terdapat di dalamnya sehingga dapat menyebabkan terjadinya perubahan warna, dan kemungkinan masih terkandung residu atau sisa pelarut dalam jumlah yang melebihi batas yang ditentukan jika tidak dilakukan kontrol yang baik dalam proses ekstraksinya.
C. Ekstraksi Oleoresin
dengan pelarut sehingga terjadi perpindahan komponen aktif dari bahan baku ke dalam pelarut. Tahap selanjutnya adalah pemisahan larutan dengan bahan baku, sehingga dihasilkan larutan ekstrak dan ampas. Tahap terakhir adalah proses distilasi pelarut, sehingga dihasilkan oleoresin.
Proses kontak bahan baku dengan pelarut dapat dilakukan dengan beberapa metode. Menurut Afifah (2003) secara umum dikenal beberapa metode yang bisa diterapkan untuk proses ekstraksi bahan aktif temulawak. Metode tersebut diantaranya adalah sebagai berikut.
Maserasi, yakni merendam bahan di dalam pelarut. Cara ini sangat sederhana,
tetapi membutuhkan waktu sangat lama. Proses ektraksi dengan cara ini hasilnya kurang sempurna.
Digesti, yakni ekstraksi dengan cara maserasi yang dikombinasikan dengan pemanasan. Cara ini tidak cocok untuk bahan aktif yang tidak tahan panas.
Perkolasi, yakni ekstraksi dengan cara mengalirkan pelarut melalui serbuk
simplisia, cara ini membutuhkan waktu sangat lama.
Sokletasi, yakni cara ekstraksi yang digunakan di laboratorium. Cara ini juga
tidak cocok untuk bahan aktif yang tidak bahan panas.
Maserasi dengan pengadukan. Cara ini merupakan cara yang paling
representatif dari cara-cara diatas. Ekstraksi dengan cara ini dapat mempercepat waktu yang dibutuhkan menjadi 6-24 jam. Djubaedah (1978) menyatakan pengadukan yang dilakukan bertujuan untuk mempercepat pelarutan dan ekstraksi padatan dengan jalan membentuk suspensi serta melarutkan partikel-partikel ke dalam media pelarut.
Menurut Balakrishnan (2005) di dalam Ravindran et al (2007), efesiensi proses ekstraksi oleoresin dipengaruhi oleh beberapa faktor. Faktor-faktor tersebut adalah sebagai berikut.
1. Ukuran partikel simplisia temulawak
itu, partikel yang sangat halus akan melewati lubang saringan dan berkumpul dengan hasil saringan. Selain ukuran partikel, keseragaman ukuran partikel juga harus diperhatikan. Partikel yang bervariasi ukurannya akan mengurangi kontak antara bahan dengan pelarut, karena partikel yang berukuran lebih kecil akan masuk ke dalam celah-celah partikel yang lebih besar.
Menurut Purseglove (1981), ukuran yang lazim digunakan adalah 40 mesh. Ukuran partikel terbesar yang telah digunakan pada pengujian di laboratorium adalah 30 mesh dan yang paling halus adalah 60 mesh. Menurut Heath dan Reineocius (1986) di dalam Sembiring et al (2006), semakin kecil ukuran bahan yang digunakan maka semakin luas bidang kontak antara bahan dengan pelarut dan semakin besar kecepatan mencapai kesetimbangan sistem. Ukuran bahan yang sesuai akan menjadikan proses ekstraksi berlangsung dengan baik dan tidak memakan waktu yang lama.
2. Pelarut
Pelarut merupakan faktor yang sangat penting dalam proses ekstraksi. Menurut Purseglove (1981) pemilihan pelarut mempengaruhi komposisi oleoresin dan jumlah ekstrak yang dihasilkan. Ekstraksi dengan menggunakan pelarut non polar akan menghasilkan oleoresin dengan kandungan lemak yang tinggi, sedangkan ekstraksi dengan menggunakan pelarut polar akan menghasilkan oleoresin dengan kandungan lemak yang rendah. Hal tersebut disebabkan oleh karakteristik lemak yang bersifat non polar, sehingga lemak akan larut dalam pelarut non polar.
Pelarut yang digunakan harus memenuhi beberapa syarat. Menurut Ravindran et al (2007), syarat pelarut yang dapat digunakan untuk proses ekstraksi oleoresin adalah sebagai berikut.
Pelarut harus dapat melarutkan semua komponen aktif yang diinginkan, dan
sedikit mungkin melarutkan komponen yang tidak diinginkan.
Pelarut mempunyai titik didih yang cukup rendah, agar pelarut mudah
diuapkan tanpa memerlukan suhu yang tinggi. Namun jangan pula terlalu rendah karena akan mengakibatkan hilangnya pelarut selama proses ekstraksi.
Pelarut memiliki titik didih yang seragam, sehingga tidak ada pelarut yang
tertinggal dalam oleoresin.
Pelarut panas spesifik dan panas laten yang rendah.
Pelarut tidak bersifat racun dan tidak membahayakan kesehatan.
Pelarut tidak mudah terbakar dan meledak.
Pelarut dijual dengan harga yang sesuai dan masuk akal.
Pelarut diperbolehkan secara hukum untuk digunakan. Beberapa jenis pelarut
yang banyak digunakan pada proses ekstraksi flavor makanan disajikan pada Tabel 3.
Tabel 3. Pelarut yang Digunakan dalam Flavor Makanan
Pelarut Titik Didih 760 mmHg (0C) Spesifik Gravity (20/20 0C)
Etil Alkohol (Etanol) 78,4 0,7905
Isopropil Alkohol 82,3 0,7862
Etil Asetat 77,1 0,8990
Dietil Eter 34,4 0,7140
Gliserol 290 1,2600
Gliseril Monoasetat 158 1,2210
Gliseri diasetat 280 1,1780
Gliseril Triasetat 260 1,1590
Propilen Glikol 185 1,0380
Sumber : Scheflan and Jacobs (1953) di dalam Heath and Pharm (1978).
Volume pelarut yang digunakan memberikan pengaruh terhadap mutu dan rendemen oleoresin yang dihasilkan. Menurut Suryandari (1981), penggunaan pelarut dalam jumlah yang berbeda dapat menghasilkan oleoresin dalam jumlah yang berbeda pula. Semakin besar volume pelarut yang digunakan, maka jumlah oleoresin yang terekstrak juga semakin besar sampai larutan menjadi jenuh oleh pelarut. Menurut Purseglove et al (1981), jumlah pelarut yang baik digunakan untuk mengekstrak oleoresin adalah sebanyak tiga kali jumlah bahan yang diekstrak.
Etanol atau etil alkohol yaitu cairan bening tidak berwarna, mudah menguap, berbau merangsang dan mudah larut dalam air. Etanol mempunyai polaritas tinggi sehingga dapat mengekstrak oleoresin lebih banyak dibandingkan pelarut organik lainnya seperti heksan. Etanol mudah melarutkan senyawa resin, lemak, minyak, asam lemak, sebagian karbohidrat dan senyawa organik lainnya (Anonim, 1962).
Etanol (disebut juga etil-alkohol atau alkohol saja), adalah alkohol yang paling sering digunakan dalam kehidupan sehari-hari. Karena sifatnya yang tidak beracun bahan ini banyak dipakai sebagai pelarut dalam dunia farmasi dan industri makanan dan minuman. Etanol tidak berwarna dan tidak berasa tapi memilki bau yang khas. Bahan ini dapat memabukkan jika diminum. Etanol sering ditulis dengan rumus EtOH. Rumus molekul etanol adalah C2H5OH atau
rumus empiris C2H6O (Anonim, 2009).
3. Suhu proses ekstraksi
Menurut Moestafa (1981), ekstraksi akan lebih cepat jika dilakukan pada suhu tinggi, tetapi pada ekstraksi oleoresin seperti ini akan menyebabkan beberapa komponen yang terdapat dalam bahan akan mengalami kerusakan. Sabel dan Warren (1973) menjelaskan, suhu ekstraksi yang terlalu tinggi harus dihindarkan, karena akan menyebabkan oleoresin menjadi rusak.
D. Pemisahan Pelarut
untuk kesehatan. Sisa pelarut yang melebihi dosis yang telah ditetapkan dapat mengakibatkan terjadinya gangguan kesehatan. Menurut Somaatmadja (1981), proses pemisahan pelarut (solvent stripping) merupakan bagian terpenting untuk memperoleh oleoresin yang memenuhi persyaratan mutu. FDA (Food and Drug Administration) USA, membuat persyaratan batas sisa pelarut yang diijinkan dalam oleoresin. Batas sisa pelarut tersebut dapat dilihat pada Tabel 5.
Tabel 4. Batas sisa pelarut yang diijinkan dalam oleoresin menurut FDA
Jenis Pelarut Batas Sisa (ppm)
Aseton 30
Etilen dikhlorida 30
Methanol 50
Etanol 30
Heksana 25
Metilen dikhlorida 30
Isopropyl alkohol 50
Pelarut yang mengandung khlor 30
Sumber : FDA di dalam Ferrel (1985)
III. METODOLOGI
A. Alat dan Bahan
Alat yang digunakan pada persiapan bahan baku dan proses ekstraksi adalah slicer, oven, disc mill, neraca analitik, Erlenmeyer 1000 ml, shaker waterbath, penyaring vakum, dan vacuum rotary evaporator. Alat yang digunakan pada tahap analisa mutu oleoresin temulawak adalah refraktometer, spektrofotometer, dan gas kromatografi.
Bahan yang digunakan pada tahap ini adalah rimpang temulawak yang berasal dari Cicurug Sukabumi dengan umur panen 12 bulan, etanol 96% sebagai pelarut, asam asetat, asam oksalat, dan asam borat.
B. Perlakuan
Faktor yang diamati pada penelitian ini terdiri dari dua faktor, yaitu faktor suhu ekstraksi dan faktor volume pelarut yang digunakan. Faktor suhu ekstraksi yang digunakan terdiri dari tiga taraf, yaitu 30 °C, 40 °C, dan 50 °C. Faktor volume pelarut digambarkan dalam bentuk nisbah bahan baku - pelarut. Nisbah bahan baku - pelarut terdiri dari tiga taraf, yaitu 1:4, 1:6, dan 1:8. Nisbah yang digunakan adalah nisbah bobot bahan baku yang diekstrak terhadap volume pelarut yang digunakan. Dasar nisbah bahan baku - pelarut adalah 100 gram bahan baku. Dengan demikian, pada nisbah 1:4 menggambarkan penggunaan 100 gram bahan baku dan 400 ml etanol 96%, pada 1:6 menggambarkan 100 gram bahan baku dan 600 ml etanol 96%, dan pada 1:8 menggambarkan 100 gram bahan baku dan 800 ml etanol 96%.
C. Prosedur Penelitian 1. Persiapan Bahan Baku
jam. Rimpang kering tersebut selanjutnya dihaluskan dengan menggunakan disc mill yang telah dipasang saringan yang berukuran 60 mesh. Bubuk rimpang temulawak selanjutnya dimasukkan ke dalam plastik dan disimpan ditempat yang sejuk dan kering. Diagram alir proses persiapan bahan baku dapat dilihat pada Lampiran 1.
2. Proses Ekstraksi
Ekstraksi dilakukan dengan menggunakan variasi suhu dan nisbah bahan baku - pelarut sebagai faktor perlakuan penelitian. Suhu dan nisbah bahan baku - pelarut yang digunakan sesuai dengan perlakuan ekstraksi. Proses ekstraksi dimulai dengan menyiapkan serbuk temulawak dengan berat 100 gram, selanjutnya dimasukkan ke dalam Erlenmeyer 1000 ml. Pelarut ditambahkan sesuai dengan perbandingan nisbah bahan baku - pelarut yang digunakan. Erlenmeyer yang telah berisi serbuk temulawak dan pelarut ditutup dengan menggunakan aluminium foil, selanjutnya diletakkan ke dalam shaker waterbath yang telah disesuaikan suhunya. Proses ini dapat dilihat pada Gambar 1. Proses ekstraksi berlangsung selama 4 jam, dan selanjutnya bahan dibiarkan selama 24 jam.
Gambar 4. Proses ekstraksi temulawak dengan menggunakan shaker waterbath
D. Analisa Oleoresin Temulawak
Terdapat beberapa analisa yang dilakukan terhadap oleoresin temulawak yang dihasilkan. Analisa tersebut adalah sebagai berikut. Prosedur analisa-analisa tersebut secara lengkap terdapat pada lampiran 2.
a. Rendemen oleoresin
Rendemen oleoresin ditentukan berdasarkan perbandingan berat oleoresin yang diperoleh terhadap berat bahan yang diekstrak.
b. Kadar kurkumin (Tonnasen, 1986 dalam Siddik et al., 1995)
Analisis kadar kurkumin dilakukan berdasarkan reaksi perubahan warna yang diamati dengan menggunakan spektrofotometer pada panjang gelombang tertentu.
c. Kadar minyak atsiri (metode hidrodestilasi Clevenger dalam Rennecius et al., 1988)
Analisis kadar minyak atsiri ini pada dasarnya adalah penyulingan minyak atsiri dari oleoresin yang dihasilkan.
d. Kadar xanthorrhizol (gas kromatografi-spektometri massa)
Kromatografi gas merupakan metode umum yang digunakan untuk pemisahan, deteksi, dan perhitungan kuantitatif dari komponen yang tercampur dalam sample uji.
e. Kadar sisa pelarut (Ketaren, 1988)
Analisis ini menggambarkan kadar pelarut yang tertinggal dalam oleoresin. Perhitungannya didasarkan kepada berat pelarut yang menguap dari setiap berat bahan yang diuapkan.
f. Indeks bias oleoresin (AOAC, 2000 dalam SNI 06-2385-2006)
Metoda ini didasarkan pada pengukuran langsung sudut bias minyak yang dipertahankan pada kondisi suhu yang tetap.
E. Rancangan Percobaan
Rancangan percobaan yang digunakan adalah rancangan acak lengkap dua faktor dengan menggunakan tiga taraf. Faktor pertama adalah nisbah bahan baku - pelarut yang terdiri dari tiga taraf, yaitu 1:4, 1:6, dan 1:8. Faktor kedua adalah suhu ekstraksi yang terdiri dari tiga taraf, yaitu 30 °C, 40 °C, dan 50 °C. Penelitian dilakukan dalam dua kali ulangan.
Model rancangan tersebut adalah sebagai berikut. Yijk = U + Ai + Bj + (AB)ij + Errorijk
Yijk = rendemen oleoresin dengan nisbah bahan baku - pelarut ke-i dengan menggunakan suhu ekstraksi ke-j pada ekstraksi ke-k U = pengaruh rata-rata sebenarnya
Ai = pengaruh pelakuan nisbah bahan baku - pelarut ke i (i=1,2,3)
Bj = pengaruh pelakuan suhu ekstraksi ke j (j=1,2,3)
(AB)ij = pengaruh interaksi perlakuan nisbah bahan baku - pelarut ke i dengan
suhu ekstraksi ke j
IV. HASIL DAN PEMBAHASAN
A. Persiapan Bahan Baku
Rimpang temulawak yang digunakan pada penelitian ini diperoleh dari daerah Cicurug Sukabumi dengan umur panen 12 bulan. Gambar rimpang temulawak tersebut dapat dilihat pada Gambar 5. Sebelum diekstrak, rimpang segar temulawak tersebut harus dipersiapkan terlebih dahulu. Menurut Sabel dan Warren (1973), persiapan bahan merupakan salah satu tahapan penting dalam proses ekstraksi oleoresin.
Gambar 5. Rimpang Temulawak (Curcuma Xanthorriza Roxb)
Persiapan bahan baku meliputi proses pengirisan, pengeringan, dan penghalusan. Sebelum memasuki proses pengirisan, dilakukan pencucian dan sortasi terhadap rimpang temulawak yang akan digunakan. Hal ini bertujuan untuk menghilangkan benda asing yang tidak dikehendaki. Proses pengirisan ini bertujuan untuk mempercepat lama proses pengeringan. Tahapan pengirisan dilakukan dengan menggunakan slicer pada ketebalan 1-3 mm. Irisan temulawak tersebut segera dikeringkan dengan menggunakan pengering yang diatur pada suhu 50oC selama 20 jam. Menurut Purseglove (1981), pengeringan rimpang segar dapat dilakukan dengan menggunakan aliran udara panas dengan suhu maksimum 65°C. Pengeringan dengan menggunakan cara ini akan menghasilkan simplisia kering yang lebih higienis dan berwarna lebih cerah dibandingkan dengan hasil pengeringan dengan menggunakan cahaya matahari.
Gambar 6. Irisan Temulawak (Curcuma Xanthorriza Roxb) Kering
Persiapan bahan baku selanjutnya adalah proses penghancuran. Menurut Syarief dan Nugroho (1992), penghancuran merupakan salah satu jenis satuan operasi pengecilan ukuran. Pengecilan ukuran sampai halus disebut dengan proses penghancuran. Proses ini bertujuan untuk memperoleh serbuk temulawak dengan ukuran dan bentuk yang seragam. Serbuk temulawak dengan ukuran dan bentuk yang seragam akan mempermudah kontak antara bahan dengan pelarut sehingga akan meningkatkan efektifitas ekstraksi.
Penghancuran simplisia temulawak dilakukan dengan menggunakan alat discmill. Untuk mengatur ukuran serbuk temulawak agar sesuai dengan yang dikehendaki, alat penggiling dilengkapi dengan saringan. Pada penelitian ini digunakan saringan yang berukuran 60 mesh. Menurut Sembiring et al. (2006), dalam proses ekstraksi oleoresin temulawak, ukuran serbuk 60 mesh menghasilkan kadar xanthorrizhol lebih tinggi dibandingkan ukuran 40 mesh.
B. Proses Ekstraksi Oleoresin Temulawak
Penelitian ekstraksi oleoresin ini menggunakan percobaan acak lengkap faktorial dengan dua faktor percobaan dengan masing-masing tiga taraf dan dua ulangan. Faktor pertama yang digunakan adalah suhu ekstraksi dengan taraf 30, 40 dan 50 °C. faktor kedua adalah nisbah bahan baku-pelarut. Nisbah ini menunjukkan besarnya volume pelarut yang ditambahkan ke dalam proses ekstraksi. Taraf nisbah yang digunakan adalah 1:4, 1:6, 1:8 dengan menggunakan 100 gram serbuk temulawak sebagai basis untuk perbandingan.
berlangsung selama 4 jam dan selanjutnya dibiarkan selama 24 jam. Pemilihan lama waktu ekstraksi didasarkan kepada hasil penelitian Sembiring et al. (2006) yang menunjukkan bahwa lama ekstraksi berpengaruh terhadap rendemen oleoresin, namun tidak berpengaruh secara nyata terhadap kadar kurkumin, kadar minyak atsiri, dan kadar xanthorhizol. Ekstraksi serbuk temulawak yang berukuran 60 mesh selama 4 jam selanjutnya dibiarkan selama 24 jam, menghasilkan oleoresin temulawak dengan kadar xanthorhizol yang tidak berbeda nyata dengan lama ekstraksi 6 dan 8 jam. Selain itu, lama ekstraksi 4 jam mampu menghasilkan oleoresin dengan kandungan kurkumin yang lebih tinggi dibandingkan 6 dan 8 jam.
Pelarut yang digunakan dalam ekstraksi oleoresin temulawak ini adalah etanol 96%. Etanol merupakan salah satu pelarut yang digunakan dalam flavor makanan. Etanol atau etil alkohol yaitu cairan bening tidak berwarna, mudah menguap, berbau merangsang dan mudah larut dalam air. Etanol mempunyai polaritas tinggi sehingga dapat mengekstrak oleoresin lebih banyak dibandingkan pelarut organik lainnya seperti heksan. Etanol mudah melarutkan senyawa resin, lemak, minyak, asam lemak, sebagian karbohidrat dan senyawa organik lainnya (Anonim, 1962). Ria (1985) juga menyatakan, ekstraksi oleoresin temulawak dengan menggunakan pelarut etanol menghasilkan rendemen lebih tinggi dibandingkan dengan menggunakan pelarut aseton dan heksan.
[image:39.595.252.403.562.686.2]Oleoresin temulawak yang dihasilkan merupakan cairan kental, memiliki aroma khas temulawak yang tajam dan berwarna coklat gelap kekuningan. Produk oleoresin yang dihasilkan dapat dilihat paga Gambar 7.
1. Rendemen Oleoresin
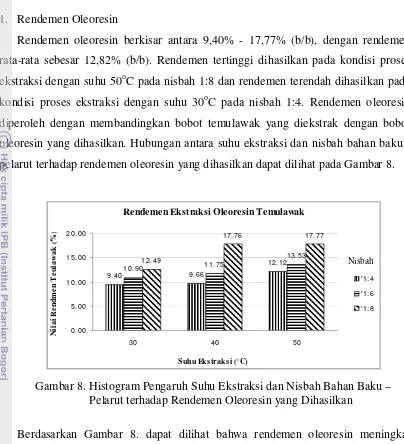
[image:40.595.114.518.73.517.2]Rendemen oleoresin berkisar antara 9,40% - 17,77% (b/b), dengan rendemen rata-rata sebesar 12,82% (b/b). Rendemen tertinggi dihasilkan pada kondisi proses ekstraksi dengan suhu 50oC pada nisbah 1:8 dan rendemen terendah dihasilkan pada kondisi proses ekstraksi dengan suhu 30oC pada nisbah 1:4. Rendemen oleoresin diperoleh dengan membandingkan bobot temulawak yang diekstrak dengan bobot oleoresin yang dihasilkan. Hubungan antara suhu ekstraksi dan nisbah bahan baku -pelarut terhadap rendemen oleoresin yang dihasilkan dapat dilihat pada Gambar 8.
Gambar 8. Histogram Pengaruh Suhu Ekstraksi dan Nisbah Bahan Baku – Pelarut terhadap Rendemen Oleoresin yang Dihasilkan
Berdasarkan Gambar 8. dapat dilihat bahwa rendemen oleoresin meningkat seiring dengan peningkatan suhu dan nisbah yang digunakan pada proses ekstraksi. Untuk mengetahui pengaruh faktor perlakuan terhadap nilai rendemen oleoresin, maka dilakukan analisis keragaman rendemen oleoresin dengan menggunakan
software SPSS pada tingkat kepercayaan 95% (α = 0,05). Hasil analisis keragaman
menunjukkan bahwa nisbah bahan baku – pelarut memberikan pengaruh secara nyata terhadap rendemen oleoresin temulawak, sedangkan suhu dan interaksi antara suhu dengan nisbah bahan baku – pelarut tidak berpengaruh secara nyata terhadap rendemen oleoresin. Hasil analisis dapat dilihat pada Lampiran 3a.
Uji lanjut Duncan memberikan informasi bahwa taraf nisbah bahan baku – pelarut 1:8 memberikan pengaruh yang berbeda nyata terhadap nilai rendemen dibandingkan taraf 1:4 dan 1:6. Hal tersebut menunjukkan pada lama ekstraksi yang
Rendemen Ekstraksi Oleoresin Temulawak
9.40 9.66 12.12 10.90 11.75 13.53 12.49 17.76 17.77 0.00 5.00 10.00 15.00 20.00
30 40 50
Suhu Ekstraksi (°C)
sama, penambahan volume etanol dapat meningkatkan nilai rendemen secara nyata. Perpindahan komponen dari bahan baku ke dalam pelarut dipengaruhi oleh perbedaan konsentrasi komponen tersebut dalam bahan dan dalam pelarut. Semakin besar perbedaan konsentrasi, maka semakin mudah dan cepat proses terjadinya perpindahan komponen. Peningkatan penggunaan volume pelarut dapat menyebabkan semakin menurunnya konsentrasi komponen tersebut dalam pelarut. Dengan demikian, peningkatan volume pelarut yang digunakan mengakibatkan semakin banyaknya komponen temulawak yang berdifusi ke dalam pelarut, sehingga meningkatkan rendemen ekstraksi. Hal ini selaras dengan hasil penelitian Suryandari (1981) yang menyatakan bahwa semakin besar volume pelarut yang digunakan, maka jumlah oleoresin yang terekstrak juga semakin besar sampai larutan menjadi jenuh oleh pelarut. Hasil uji lanjut Duncan dapat dilihat pada Lampiran 3b.
Hasil analisis keragaman menunjukkan bahwa peningkatan suhu tidak berpengaruh secara nyata terhadap nilai rendemen. Meskipun demikian, berdasarkan Gambar 4 dapat dilihat terjadi kecenderungan kenaikan rendemen dengan meningkatnya suhu ekstraksi. Peningkatan suhu ekstraksi ini diharapkan mampu mempercepat proses ekstraksi sehingga akan meningkatkan nilai rendemen pada lama ekstraksi yang sama. Menurut Moestafa (1981), ekstraksi akan lebih cepat jika dilakukan pada suhu tinggi. Peningkatan suhu ekstraksi mengakibatkan kinetika ekstraksi meningkat, sehingga pelarut bergerak lebih cepat dan acak pada saat kontak dengan serbuk temulawak. Selain itu, peningkatan suhu mengakibatkan pembesaran pori-pori dari serbuk temulawak sehingga lebih memudahkan komponen yang terdapat dalam bahan terlepas ke dalam pelarut. Dengan adanya dua hal tersebut, maka peningkatan suhu dapat meningkatkan rendemen ekstraksi. Namun penggunaan suhu yang terlalu tinggi, dapat menyebabkan rusaknya beberapa komponen yang terdapat dalam bahan.
2. Kadar Kurkumin
menjelaskan bahwa kurkuminoid dalam temulawak terdiri dari kurkumin dan desmetoksikurkumin. Jumlah kurkumin dalam kurkuminoid temulawak terdapat lebih banyak dibandingkan dengan jumlah desmetoksikurkumin dengan perbandingan kurkumin mencapai 71% dan desmetoksikurkumin sebesar 29%. Kurkuminoid bersifat larut dalam aseton, alkohol, asam asetat glasial, dan alkali hidroksida dan tidak dapat larut dalam air dan dietileter. Oleh karena itu, pada ekstraksi oleoresin temulawak ini digunakan pelarut etanol.
Pada penelitian ini, pengujian kadar kurkumin dalam oleoresin dilakukan dengan menggunakan spektroskopi sinar tampak pada panjang gelombang 530 nm. Hasil pengujian menunjukkan kadar kurkumin dalam oleoresin berkisar antara 1,11 – 3,88 %, dengan kadar rata-rata 2,68 %. Kadar kurkumin yang dihasilkan pada penelitian ini memiliki nilai rata-rata yang lebih tinggi dibandingkan hasil pengamatan Ria (1989) dengan nilai rata-rata 2,51%. Kadar kurkumin yang terdapat dalam oleoresin temulawak memiliki kadar yang lebih tinggi dibandingkan kadar kurkumin dalam rimpang temulawak. Kadar kurkumin dalam rimpang temulawak adalah sebesar 1,36 % (BK) (Sembiring, et al.,2006).
Kadar kurkumin tertinggi dihasilkan dari suhu 50°C dengan nisbah bahan baku – pelarut 1:8, sedangkan nilai terendah dihasilkan dari suhu 30°C dengan nisbah bahan baku – pelarut 1:6. Hubungan kombinasi perlakuan ekstraksi dengan kadar kurkumin dalam oleoresin temulawak dapat dilihat pada Gambar 9.
Gambar 9. Histogram Pengaruh Suhu Ekstraksi dan Nisbah Bahan Baku - Pelarut terhadap Kadar Kurkumin dalam Oleoresin Temulawak
K ad ar K u rk u m in d a la m Oleo re s in T e m u la w ak
3.20 2.38 3.49 1.11 2.63 2.88 3.19 2.98 3.88 0.00 0.50 1.00 1.50 2.00 2.50 3.00 3.50 4.00 4.50
30 40 50
S u h u Ekstra ksi (°C )
Hasil analisis keragaman menunjukkan bahwa suhu, nisbah bahan baku – pelarut, serta interaksi diantara keduanya tidak berpengaruh secara nyata terhadap kandungan kurkumin dalam oleoresin temulawak. Hal ini dapat disebabkan oleh tingginya sifat kelarutan kurkumin dalam etanol, sehingga kurkumin sudah dapat terekstrak dengan baik pada suhu 30oC dan nisbah 1:4 dari serbuk temulawak. Hasil analisis ragam dapat dilihat pada Lampiran 4.
3. Kadar Minyak Atsiri
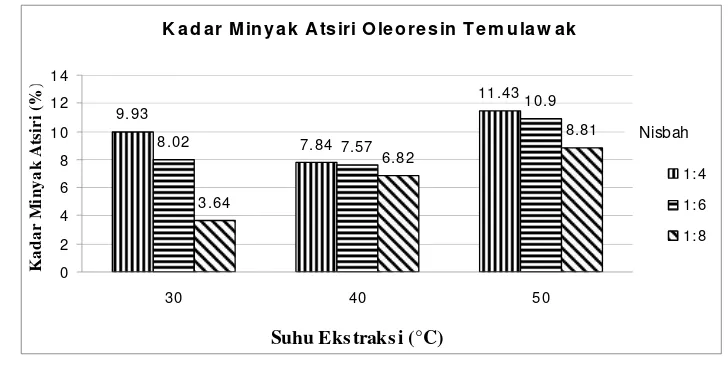
Oleoresin temulawak merupakan campuran antara minyak atsiri dan resin. Minyak atsiri tersebut berfungsi sebagai pemberi aroma khas temulawak pada oleoresin temulawak yang terekstrak. Kadar minyak atsiri dalam oleoresin diketahui melalui proses distilasi. Hasil pengujian menunjukkan kadar minyak atsiri dalam oleoresin temulawak berkisar antara 3,64 – 11,43 %. Kadar minyak atsiri tertinggi dihasilkan pada kondisi proses ekstraksi yang berlangsung pada suhu 50 oC dengan nisbah jumlah pelarut dengan bahan sebesar 1:4, sedangkan kadar minyak atsiri terendah dihasilkan pada kondisi proses esktraksi yang berlangsung pada suhu 30 oC dengan nisbah jumlah pelarut dengan bahan sebesar 1:8.
Gambar 10. Histogram Pengaruh Suhu Ekstraksi dan Nisbah Bahan Baku – Pelarut terhadap Kadar Minyak Atsiri dalam Oleoresin
Temulawak
Uji lanjut Duncan terhadap suhu menunjukkan bahwa suhu 50 oC memberikan pengaruh yang berbeda nyata terhadap kadar minyak atsiri dibandingkan suhu 30 oC dan 40 oC. Peningkatan suhu ekstraksi meningkatkan energi dan kecepatan molekul etanol, sehingga kontak etanol dengan serbuk temulawak semakin intensif. Dengan demikian semakin tinggi suhu ekstraksi, maka semakin besar pula jumlah komponen minyak atsiri yang terlarut dalam etanol.
Uji lanjut Duncan terhadap nisbah bahan baku - pelarut menunjukkan bahwa nisbah 1:8 memiliki pengaruh yang berbeda nyata terhadap kadar minyak atsiri dibandingkan nisbah 1:4 dan 1:6. Nisbah 1:8 memiliki kadar yang paling kecil dibandingkan dengan kedua nisbah lainnnya. Penurunan kadar minyak atsiri pada nisbah bahan baku - pelarut yang semakin besar terjadi seiring dengan peningkatan nilai rendemen oleoresin temulawak. Dengan meningkatnya rendemen ekstraksi menunjukkan terjadinya peningkatan komponen yang terdapat dalam oleoresin temulawak. Dengan demikian, terjadi penurunan kadar minyak atsiri relatif terhadap komponen-komponen yang terdapat dalam oleoresin temulawak. Selain itu, penurunan kadar minyak atsiri tersebut dapat disebabkan oleh hilangnya minyak atsiri pada saat penguapan pelarut. Semakian besar volume pelarut yang digunakan, semakin lama waktu penyaringan yang diperlukan. Selama proses pemisahan larutan dari ampas, besar kemungkinan terjadinya hilangnya minyak atsiri dari larutan tersebut.
K a d ar M in y a k Atsiri O le o res in T e m u la w ak
9.93 7.84 11.43 8.02 7.57 10.9 3.64 6.82 8.81 0 2 4 6 8 10 12 14
30 40 50
Suhu Eks traksi (°C)
Kehilangan kadar minyak atsiri pada volume pelarut yang lebih besar juga dapat terjadi pada proses ekstraksi. Proses ekstraksi berlangsung dengan menggunakan alat yang memiliki kapasitas yang sama. Jumlah volume pelarut yang berbeda, menyebabkan terjadinya perbedaan tinggi pelarut dalam wadah tersebut. Semakin banyak pelarut yang digunakan, semakin besar ketinggian pelarut dalam wadah. Hal ini menyebabkan proses penguapan minyak atsiri berlangsung lebih mudah, sehingga pada volume pelarut dengan nisbah 1:8 kadar minyak atsirinya paling rendah. Hasil uji lanjut Duncan pengaruh suhu dan nisbah bahan baku dengan pelarut dapat dilihat pada Lampiran 5b.
4. Kadar Xanthorrhizol dalam Bahan Volatil pada Oleoresin Temulawak
Identifikasi komponen minyak atsiri yang terdapat didalam oloeresin temulawak dilakukan dengan menggunakan kromatografi gas. Menurut Gritter et al. (1991), kromatografi gas merupakan metode yang cepat dan tepat untuk memisahkan campuran yang sangat rumit. Komponen campuran dapat diketahui dengan menggunakan waktu tambat (waktu retensi) yang khas pada kondisi yang tepat.
Berdasarkan hasil analisis kromatografi gas dapat diketahui bahwa terdapat 12 – 21 komponen yang terdapat dalam minyak atsiri temulawak. Terdapat perbedaan jenis dan kadar komponen minyak atsiri pada setiap sampel yang diuji. Perbedaan jumlah dan jenis komponen minyak atsiri ini dapat disebabkan oleh perbedaan kondisi sampel tersebut diperoleh.
Salah satu komponen minyak atsiri temulawak yang berperan penting adalam memberikan efek farmakologis adalah xanthorrhizol. Hal ini selaras dengan pernyataan dari Taryono et al.l (1987) yang menyatakan bahwa gabungan senyawa kurkumin dengan xanthorrhizol diduga sebagai penyebabnya berkhasiatnya temulawak. Senyawa ini menurut Maiwald dan schawantes (1991) didalam Sidik et al. (1995), digolongkan sebagai senyawa sesquiterpen.
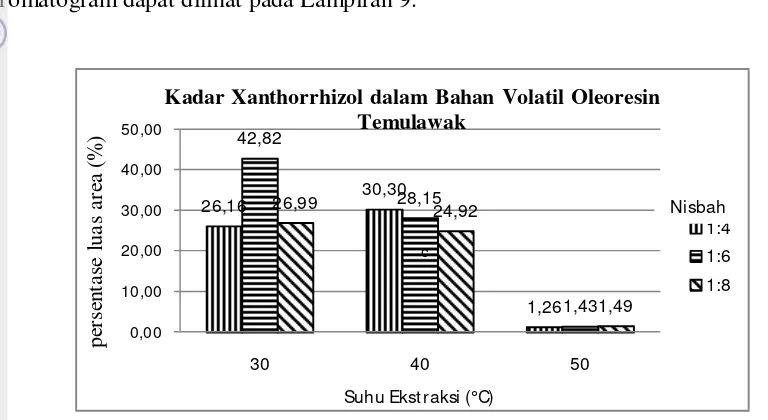
dalam oleoresin temulawak berkisar antara 1.26-42,82 %. Persentase luas area xanthorrhizol tertinggi terdapat di dalam oleoresin dengan menggunakan suhu ekstraksi 30 oC dan nisbah bahan baku - pelarut sebesar 1:6. Hubungan antara kombinasi faktor percobaan dengan persentase luas area xanthorrhizol yang terdapat dalam bahan volatil pada oleoresin temulawak dapat dilihat pada Gambar 11. Kromatogram dapat dilihat pada Lampiran 9.
Gambar 11. Histogram Pengaruh Suhu Ekstraksi dan Nisbah Bahan Baku – Pelarut terhadap Persentase Luas Area Xanthorrhizol
Komparatif terhadap Bahan Volatil dalam Oleoresin Temulawak
Berdasarkan gambar 11. dapat diketahui bahwa peningkatan suhu ekstraksi mengakibatkan penurunan persentase luas area xanthorrhizol. Hal ini selaras dengan hasil analisis keragaman terhadap persentase luas area xanthorrhizol yang memberikan informasi bahwa faktor suhu ekstraksi berpengaruh secara nyata terhadap persentase luas area xanthorrhizol, sedangkan nisbah bahan baku - pelarut tidak memiliki pengaruh yang nyata terhadap persentase luas area xanthorrhizol. Hasil uji lanjut Duncan menunjukkan bahwa suhu 50 oC menyebabkan rendahnya persentase luas area xanthorrhizol yang berbeda nyata dibandingkan persentase luas area xanthorrhizol yang terdapat dalam oleoresin dengan suhu ekstraksi 30 dan 40
o
C. Hasil analisis keragaman dapat dilihat pada Lampiran 6.
Xanthorrhizol merupakan salah satu komponen minyak atsiri temulawak. Seperti minyak atsiri lainnya, minyak atsiri temulawak bersifat sensitif terhadap panas. Peningkatan suhu proses untuk memperoleh minyak atsiri dapat mengakibatkan terjadinya kerusakan komponen minyak atsiri tersebut. Peningkatan suhu ekstraksi
26,16 30,30 1,26 42,82 28,15 1,43 26,99 24,92 1,49 0,00 10,00 20,00 30,00 40,00 50,00
30 40 50
pe rs en ta se l ua s a re a ( % )
Suhu Ekst raksi (°C)
oleoresin yang digunakan pada penelitian ini juga mengakibatkan terjadinya kerusakan komponen, salah satunya kerusakan pada komponen xanthorrhizol.
5. Kadar Sisa Pelarut dalam Oleoresin
Kadar sisa pelarut adalah kandungan pelarut etanol yang tertinggal dalam oleoresin. Menurut FDA dalam Ferrel (1985) kadar etanol yang tertinggal dalam oleoresin yang diperbolehkan adalah sebanyak 30 ppm. Hasil pengujian menunjukkan, kadar sisa pelarut dalam oleoresin berkisar antara 40.950 – 63.750 ppm, dengan kadar sisa pelarut rata-rata sebesar 52.961 ppm. Hubungan antara sisa pelarut dengan kombinasi perlakuan ekstraksi dapat dilihat pada Gambar 12.
Gambar 12. Histogram Pengaruh Suhu Ekstraksi dan Nisbah Bahan Baku - Pelarut terhadap Kadar Sisa Pelarut dalam Oleoresin
Temulawak.
Hasil analisis keragaman menunjukkan bahwa suhu, nisbah bahan baku - pelarut, serta interaksi antara suhu dengan nisbah bahan baku - pelarut tidak berpengaruh secara nyata terhadap sisa pelarut dalam oleoresin. Hal tersebut dikarenakan sisa pelarut dipengaruhi oleh proses penguapan bukan dipengaruhi oleh kondisi proses ekstraksi. Hasil analisis keragaman dapat dilihat pada Lampiran 7.
Tingginya kadar sisa pelarut dalam oleoresin temulawak disebabkan oleh tidak sempurnanya proses penguapan etanol dari oleoresin. Etanol adalah sejenis cairan yang memiliki titik didih 78,4°C pada tekanan 1 atm (Anonim, 2009). Proses penguapan etanol dari oleoresin temulawak dilakukan dengan menggunakan vacuum rotary evaporator pada suhu 50°C. Suhu penguapan ini berada di bawah titik didih
U ji S is a P e laru t
53,60 0
53,10 0
51,30 0 40,950 55,750 50,100 60,800 47,300 63, 750 -10,000 20,000 30,000 40,000 50,000 60,000 70,000
30 40 50
S u h u Ek stra k si (°C)
etanol, namun dengan adanya penurunan tekanan maka akan terjadi penurunan titik didih etanol. Dengan demikian etanol yang terdapat di dalam oleoresin belum sepenuhnya menguap suhu 50°C tersebut. Penggunaan suhu 50°C tersebut bertujuan untuk menghindari terjadinya kerusakan dan kehilangan komponen oleoresin, terutama komponen minyak atsiri.
Selain disebabkan oleh proses evaporasi etanol yang tidak sempurna, kadar sisa pelarut yang masih tinggi juga dapat disebabkan oleh masih adanya air di dalam oleoresin. Air dalam oleoresin berasal dari bahan baku yang mengandung kadar air sebesar 8,15%. Air juga berasal dari pelarut etanol yang tidak murni karena masih menggandung air sebesar 4%. Karakteristik etanol yang bersifat larut dalam air mengakibatkan terjadinya ikatan antara air dan etanol.
6. Indeks Bias
Indeks bias merupakan perbandingan antara kecepatan cahaya di dalam udara dengan kecepatan cahaya didalam oleoresin pada suhu 20°C. Pengukuran indeks bias dilakukan dengan menggunakan alat refraktometer. Indeks bias ini erat kaitannya dengan komponen yang terdapat dalam oleoresin. Semakin panjang ikatan komponen dalam oleoresin, maka nilai indeks bias akan semakin besar. Perubahan nilai indeks bias dapat dijadikan sebagai dugaan awal telah terjadinya perubahan komponen oleoresin, baik yang disebabkan oleh kerusakan maupun disebabkan oleh adanya campuran dari bahan lain.
Gambar 13. Histogram Pengaruh Suhu Ekstraksi dan Nisbah Bahan Baku – Pelarut terhadap Indeks Bias Oleoresin Temulawak
Berdasarkan Gambar 13 dapat dilihat bahwa indeks