PEMBUATAN ANGGUR PEPAYA DENGAN PROSES FERMENTASI
urung
kulta s Te knik USU – Me d a n
kukan melalui proses fermentasi alkohol dari sari buah
pepay antuan mikroba yang mengubah karbohidrat atau gula
menja elitian ini adalah mikroba saccharomyces cerevisiae.
e ukan secara anaerobik, yaitu mula-mula dengan inokulasi ragi roti dengan nutrien
a dalam proses pembuatan starter. Setelah diperoleh
buah pepaya steril yang telah mengandung (NH4)2SO4
dan (N ai 4,5 digunakan HCl2N yang diteteskan ke dalam sari
h p
, 3, 4, 5, 6, dan 7 hari, suhu fermentasi 250C, 300C, diperoleh anggur buah pepaya dilakukan analisis kadar
til al asam asetat. Dari hasil penelitian diperoleh lama fermentasi buah pepaya yang
inuman anggur adalah 3 hari dan dengan penambahan ohol sebesar 320%. Minuman anggur buah pepaya yang
ihasil asuk golangan B (kadar alkohol antara 5-20%) dan yang
alkohol 1-5%).
Kata k
tr ion of papaya wine by fermentation has been studied. The fermentation process was arried out in anaerobic condition by using saccharomyces cerevisiae and (NH4)2SO4 , (NH4)3PO4 as utrient. Initially, making starter from papaya concentrate followed by fermentation process. HCl 2N is used to get pH 4,0 up to 4,5.
The variation of time are 1, 2, 3 , 4, 5, 6 and 7 days with variable of temperature which is conducted with variation are 25oC, 30oC anf 35oC. Meanwhile concentration of leavened which used are 1%, 2% and 4%. The best condition for the largest product were found as result of this research. They are duration of process: 3 days, sugar added: 16% step up production of papaya wine about 320%. Papaya wine which was obtained classified in class B with concentration of alcohol about 5 to 20%.
Key words: Papaya Wine, fermentation process, starter.
I. PENDAHULUAN
1.1 Latar Belakang Penelitian
Tanaman pepaya tergolong tanaman yang banyak diusahakan oleh petani Indonesia. Indonesia
termasuk penghasil pepaya (carica papaya) kedua
terbesar di Asia. Perlakuan yang teliti akan diproduksi hasil berkisar antara 6-12 ton/hektar (Baga Kalie, 1994). Kehilangan hasil buah pepaya selama penyimpanan dan transportasi setelah panen tergolong masih tinggi mencapai 45,6-100 %. Kondisi ini disebabkan oleh daya kesegaran buah yang rendah (3-4 hari setelah panen). Buah makin cepat rusak dan tidak layak dikonsumsi jika indeks panennya makin rendah. Disamping itu varietas-varietas yang pupoler di masyarakat menunjukkan ciri tidak terus menerus berbuah, sehingga ditemukan panen raya yang menyebabkan pasokan buah melebihi permintaan (Efendy, 2002) sehingga banyak buah pepaya terlalu matang dan rusak. Salah
satu alternatif teknologi pengolahan buah pepaya yang terlalu matang atau rusak yang potensial untuk dikembangkan adalah pembuatan anggur dari buah pepaya yang diperoleh dengan cara fermentasi.
Produksi minuman anggur buah pepaya dapat dilakukan melalui proses fermentasi alkohol dari sari buah pepaya. Proses fermentasi ini dapat berjalan dengan bantuan mikroba yang mengubah karbohidrat atau gula menjadi alkohol. Mikroba yang digunakan dalam penelitian ini adalah mikroba
saccharomyces cerevisiae. Fermentasi alkohol ini dilakukan secara anaerobik yaitu mula-mula dengan inokulasi ragi roti dengan nutrien (NH4)2SO4, (NH4)3PO4, dan bahan baku sari buah pepaya dalam
proses pembuatan starter. Setelah diperoleh starter
maka dilakukan proses fermentasi terhadap sari buah pepaya steril yang telah mengandung (NH4)2SO4 dan (NH4)3PO4. Untuk mempertahankan pH 4,0 sampai 4,5 digunakan HCl 2 N yang diteteskan ke dalam sari buah pepaya.
Re nita Ma n
Pro g ra m Stud i Te knik Kim ia Fa
Abstrak: Produksi minuman anggur pepaya dapat dila a. Proses fermentasi ini dapat berjalan dengan b di alkohol. Mikroba yang digunakan dalam pen ntasi alkohol ini dilak
Ferm
(NH4)2SO4, (NH4)3PO4, dan bahan baku sari buah pepay
starter maka dilakukan proses fermentasi terhadap sari H4)3PO4. Untuk mempertahankan pH 4,0 samp epaya.
bua
Lingkup penelitiannya adalah dengan waktu fermentasi 1, 2 dan 350C, konsentrasi khamir 1%, 2%, dan 4%. Setelah
kohol, metil alkohol, dan e
baik untuk setiap variasi khamir dalam menghasilkan m gula sampai 16% dapat meningkatkan produksi etil alk
kan dengan penambahan gula sampai 16% term d
tidak ditambahkan gula sampai 16% golongan A (kadar
unci: Anggur pepaya, proses fermentasi, starter.
act: The product
Abs
1.2. Per
mana sari buah pepaya dapat dimanfaatkan menjadi bahan dasar minuman anggur dengan m
variasi terhadap lamanya waktu ferment dan konsentrasi ragi y
uah untuk memperoleh
.3. Ruang Lingkup Penelitian
1. Sebagai informasi awal bagi peneliti pengembangan inuman anggur.
si pada masyarakat
rusak)
Aquadest
um phosphat um sulfat
Larutan Gula 12 % KOH 30 %
• Beaker glass
saring
• pH meter
• Piknometer
Labu suling
Pembuatan starter
Starter dibuat berdasarkan yang telah dilakukan oleh Muljohardjo (1984) yaitu ke dalam 1000 ml sari buah ditambahkan 1%, 2%, dan 4% ragi roti (sesuai dengan perlakuan masing-masing),
nkee, Ough, 1
hemositometer dan ditutup
umusan Masalah
Yang menjadi permasalahan adalah sejauh
Bahan baku (buah pepaya matang atau
Ragi roti (yeast instant)
elakukan asi, suhu,
Amoni Amoni
ang ditambahkan ke dalam sari kualitas anggur yang baik.
HCl 2N NaOH 0,2 N b
1
Penelitian ini dilakukan di Fakultas Teknik Universitas Sumatera Utara.
Adapun variabel yang akan digunakan dalam penelitian ini adalah:
1. Variasi waktu fermentasi: 1, 2, 3, 4, 5, 6, 7 hari
2. Variasi suhu: 25 0C, 30 0C, 35 0C 3. Konsentrasi khamir: 1%, 2%, 4%
2.2.2. Peralatan
Peralatan pada penelitian ini adalah:
• Pisau
• Timbangan
• Blender
• Labu erlenmeyer
1.4. Parameter Uji
1.4.1. Secara Kimia
Uji Kuantitatif
• Kadar etil alkohol: Perbandingan berat jenis destilat.
• Kadar metil alkohol: Dengan
spektrofotometri
• Batang pengaduk
• Pipet tetes
• Timbangan digital
• Oven
• Termometer
• Gabus, lilin
• Kain • Kadar asam asetat: Dengan metode titrasi
1.5. Tujuan Penelitian
1. Untuk mengetahui lamanya waktu
fermentasi yang optimum pada pembuatan anggur buah pepaya.
• Biuret
• Gelas ukur
• Corong
•
2. Untuk mengetahui suhu fermentasi yang optimum pada pembuatan anggur buah pepaya.
3. Untuk mengetahui konsentrasi khamir yang optimum dalam proses fermentasi buah pepaya.
• Spektrofotometer
2.3 Prosedur Percobaan Penelitian
2.3.1.
.6. Manfaat Penelitian 1
selanjutnya dalam pembuatan m
2. Memberikan informa
tentang penggunaan buah pepaya busuk atau rusak agar dapat bernilai lebih ekonomis.
I. METODOLOGI PENELITIAN 2.1. Lokasi
Penelitian ini dilaksanakan di Laboratorium Penelitian Program Studi Teknik Kimia, Fakultas Teknik Universitas Sumatera Utara, Medan. Sedangkan sumber bahan baku yang digunakan dalam penelitian ini diperoleh dari pasar Sei Sikambing dengan pengambilan sampel secara
random (sembarang).
2.2. Bahan dan Peralatan
2.2.1. Bahan
Bahan-bahan yang digunakan pada penelitian ini adalah:
kemudian dimasukkan aktivator 0,33 gram (NH4)SO4 dan 0,05 gram (NH4)3PO4. Setelah itu diinkubasi selama 24 jam atau kalau jumlah selnya sudah
mencapai 106-108 / ml (Amerine, Berg, Ku
982).
2.3.2. Penentuan berat ragi (Saccharomyces
cerevisiae) yang digunakan.
Berat ragi yang dibutuhkan dalam tiap variasi konsentrasi ditentukan dengan cara:
Berat ragi roti = % ragi roti x berat sampel 100% - % ragi roti
2.3.3. Pengamatan jumlah sel khamir
Jumlah sel khamir ditentukan pada awal dan setiap hari fermentasi dengan menggunakan hemositometer. Sebelum sel-sel khamir dihitung, maka terlebih dahulu dilakukan pengenceran sampai
konsentrasi 10-4. Suspensi dengan konsentrasi 10-4
dengan gelas penutup, kemudian diamati di bawah
disaring dan diambil sarinya.
dipaste
ri sesuai dengan perlakuan.
2.4. P
2.4.1. K
distilasi 10
Campuran si. Distilat, ditampung dengan
pikno piknomete
menit, m sampai garis tanda dan
iangkat lalu didiamkan selama 15 menit kemudian rat kosong piknometer dan berat
BJ etil alk
2.4.2. A
H n sebanyak 50 ml ditambahak
ai indikator). 0,1 N sampai i
p. Untuk menentukan jumlah sel khamir
saccharomyces cerevisiae dalam 1 ml sampel dipakai rumus seperti yang dikemukakan oleh Hadioetomo (1985) yaitu:
Y = X * 50 * p * 103
Y = Jumlah sel kha
sampel.
X = Jumlah sel khamir yang dihitung pada lima buah petak ruang kecil.
P = Pengenceran.
Penyediaan sampel untuk fermentasi Buah pepaya dipilih yang sudah
pa g/ru ak atau hampir busuk, lalu diku
urkan (diblender) dengan penambah d
sebanyak 40 %, lalu
Kemudian diatur pHnya 4,0-4,5 lalu ditambahkan
amonium fosfat sebanyak 0,25 g/l, terus
urisasi pada suhu 80 0C selama 15 menit.
dian didinginkan (suhu sekitar 20 0C-25 0C)
ecara aseptis dimasukkan ke dalam botol tasi sebanyak 100 ml. Lalu ditambahkan
saccharomyces cerevisiae sebanyak 10 m masing-masing botol fermentasi. Fermenta p
dilakukan sampai tujuh ha
rosedur Analisis Hasil
adar etil alkohol
Dimasukkan 100 ml sampel ke dalam labu 00 ml, lalu ditambahkan 150 ml air suling. didistila
meter sampai garis tanda. Kemudian
r didinginkan pada suhu 20 0C selama 15
iniskus diatur d
ditimbang. Lalu hitung be
air pada 20 0C (sebagai pembanding).
ohol 20/200C =
Berat etil alkohol (sulingan) pada 20 0C Berat air pada 20 0C
nalisis Kadar Asam Asetat
asil sulinga n
phenolfthalen 2-3 tetes (sebag udian dititrasi dengan NaOH Kem
terjad perubahan warna menjadi merah jambu
(pink).
Kadar Asam Asetat dihitung dengan menggunakan rumus:
% Asam Asetat =
2.4.3.1 (panjang gelombang)
ml metanol absolut 99%
kemud n ke dalam kotak kuvet sampai
garis resapannya (absorbansi)
pada 250-300 nm dan dibuat
kurv r da (λ) maksimum adalah nilai
ari metanol absolut 99% yang
2.4.3.2 kurva kalibrasi metanol
ml metanol absolut 99% lam labu ukur 100 ml
standar dengan aquadest
aka diperoleh metanol
baku induk II dipipet sebanyak ke dalam labu ukur 100 kan sampai garis standar dengan
sampai larut. Maka diperoleh duk III).
ku induk III dipipet sebanyak asukkan ke dalam labu ukur 100 sampai garis standar dengan kocok sampai larut. Maka diperoleh
duk IV).
rutan baku induk IV masing-4, 5, 6, 7, 8, 9, dan 10 ml
dalam labu ukur 100 ml
standar dengan aquadest
. Maka akan
.1. Fase permula
cerevisiae
*NNaO
NaOH Volume
pel Volume
Kadar metanol dengan menggunakan metode Spektrofotome standar lalu diukur
ombang panjang gel
esapannya. Lam a
puncak resapan d paling tinggi.
. Pembuatan
50,5 Dipipet
kemudian dimasukkan ke da lalu di ad-kan sampai garis dan dikocok sampai larut. M 50 % (baku induk II).
Dari larutan 20 ml kemudian dimasukkan ml lalu di
ad-aquadest dan dikocok metanol 10 % (baku in Dari larutan ba 10 ml kemudian dim ml lalu di ad-kan
aquadest dan di metanol 1 % (baku in
ari la Dipipet d
masing 0,5, 1, 2, 3,
kemudian dimasukkan ke
a i ad-kan sampai garis
l lu d
dan masing-masing dikocok sampai larut iperoleh metanol dengan konsentrasi 0, d
%, 0,02 %, 0,03 %, 0,04 %, 0,08 % 0,09 %, dan 0,1 %.
Metanol dengan konsentrasi masing-masing 0,005 %, 0,01 %, 0,02 %, 0,03 %, 0,04 %, 0,05 %, 0,06 %, 0,07 %, 0,08 %, 0,09 %, dan 0,1 % kemudian diukur resapannya (absorbansi) pada
panjang gelombang (λ) maksimum.
Pembuatan kurva kalibrasi antara absorbansi (Abs) VS konsentrasi (%) agar diperoleh persamaan garis regresi standar metanol.
III. HASIL DAN PEMBAHASAN
Dari grafik 3.1 sampai 3.7 terlihat bahwa
fase pertumbuhan saccharomyces c
terhadap lamanya fermentasi yang dilakukan adala
3 an
Pada fase ini saccharomyces
masih sedikit menggunakan substrat yang ada pada sari buah pepaya, sehingga larutan gula yang dikonversi menjadi minuman anggur masih sedikit. Fase permulaan pada khamir dengan konsentarasi
4% terjadi beberapa jam setelah pencampuran starter
yang lebih tinggi dibandingkan khamir 1% dan 2%. Hal ini terjadi karena lebih banyaknya sel
saccharomyces cerevisiae/ml pada khamir 4% yaitu 493,7 x 105/ml dibandingkan jumlah sel khamir 1 % yaitu 90,1 x 105/ml dan 2% yaitu 264,2 x 105/ml.
logaritma
bahwa f pertama kecepata
melakuk e aan
berlangs e ah satu atau beberapa
h
hasil-kskresi khamir atau berkurangnya nutrien sehingga tersebut. gula membentuk alkohol (etanol
khamir us-menerus sedangkan
menjadi n
konversi g ol dan metanol)
e ehingga dapat
a
uhan optimum 300C (Desrosier, 1998) akan
meningk
dar alkohol yang dihasilkan. dapat dilihat bahwa dengan 4 %, penambahan gula sampai
16% suhu 300C, lama fermentasi tiga hari diperoleh
tingkat produksi etanol maksimum 12,81 %. Dari
grafik 3.2 dengan konsentrasi khamir 4 % suhu 300C
lama fermentasi tiga hari dan tanpa penambahan gula diperoleh tingkat produksi etanol maksimum 3,05 %.
a
%, kons 30
3.2. Fase pertumbuhan
Dari grafik 3.1 sampai 3.7 dapat dilihat ase pertumbuhan logaritma terjadi pada hari
sampai kedua, di mana pada fase ini n pembelahan paling tinggi dan khamir
at pesat. Kead an m tabolisme sang
ng t rus sampai sal
ini ko
u
nutrien abis atau sampai terjadi penimbunan
hasil metabolisme yang bersifat racun yang menyebabkan terhambatnya pertumbuhan dan
perkembangbiakan saccharomyces cerevisiae
(Jutono dkk, 1980). Sedangkan hari ketiga merupakan kondisi konversi (penguraian) substrat maksimum.
3.3. Fase pertumbuhan yang terhambat
Setelah melalui fase pertumbuhan logaritma, kecepatan pembelahan khamir akan berkurang. Hal ini dapat dilihat pada grafik 3.1 sampai 3.7 yang mengalami fase pertumbuhan terhambat pada selang hari kedua sampai ketiga. Hal ini mungkin disebabkan oleh penimbunan hasil e
mengganggu pertumbuhan khamir Akibatnya konversi larutan
dan metanol) akan menurun dibandingkan fase sebelumnya.
3.4. Fase kematian
Pada fase ini jumlah khamir yang mati akan semakin banyak dan melebihi jumlah yang membelah diri. Hal ini dapat dilihat pada grafik 3.1 sampai 3.7 yang mengalami fase kematian pada hari ketiga sampai ketujuh. Kecepatan kematian
meningkat secara ter
perkembangbiakannya semakin berkurang dan an khamir meng-ol sehingga kemampu
ula me jadi alkohol (etann
akan m nurun dan semakin sedikit s diabaik n.
Dari grafik 3.1 sampai 3.7 terlihat bahwa masing-masing perlakuan memperlihatkan perbedaan yang nyata untuk jumlah kadar etanol dan metanol. Pengaturan suhu fermentasi ke arah suhu pertumb
atkan pertumbuhan khamir yang diikuti pula dengan peningkatan ka
Dari grafik 3.5 konsentrasi khamir
Dari gr fik 3.1 dengan penambahan gula sampai 16
entrasi khamir 2 %, suhu 0
C, dan lama er
0
n demikian alkohol yang dihasilkan keluar k
fermentasi 3 hari dip oleh tingkat produksi metanol maksimum 0,07826241 %. Dari grafik 3.7 dengan
nsentrasi khamir 4 %, suhu 30 C, lama fermentasi tiga hari dan tanpa penambahan gula diperoleh tingkat produksi metanol maksimum 0,05955322 %.
Dengan meningkatnya pertumbuhan khamir dan pembentukan produk diikuti pula dengan meningkatnya evolusi panas (reaksi eksoterm), sehingga suhu medium dapat mencapai 37 0C. Dalam keadaa
dapat hilang melalui penguapan dan terikut
dengan eluarnya CO2 (Ayres, 1980). Penurunan
alkohol juga terjadi karena etanol dan metanol yang dihasilkan teroksidasi menjadi asetaldehid dan oksidasi lanjut akan menghasilkan asam asetat (Buckle, K. A, 1987). Oksidasi ini dapat terjadi karena kondisi fakultatif anaerob. Asam asetat yang dihasilkan akan menambah keasaman medium yang berakibat tidak baik bagi kehidupan khamir
saccharomyces cerevisiae. Jika kondisi ini berlangsung lebih lama maka akan semakin banyak etanol dan metanol yang terkonversi menjadi asetaldehid yang dengan demikian persentasi alkohol (etanol dan metanol) semakin menurun dan konsentrasi asam asetat meningkat.
0 1
1 2 3 4 5 6 7
Lama Fermentasi (hari)
Kons
Grafik 3.1. Hubungan lama fermentasi terhadap konsentrasi metanol dengan penambahan gula 16%
pada suhu 350C.
0
1 2 3 4 5 6 7
Lama Fermentasi (hari) 0,005
Konsentrasi Asam
0,01 0,015 0,02
Asetat (x10-2 %) Khamir 1%
Khamir 2% Khamir 4%
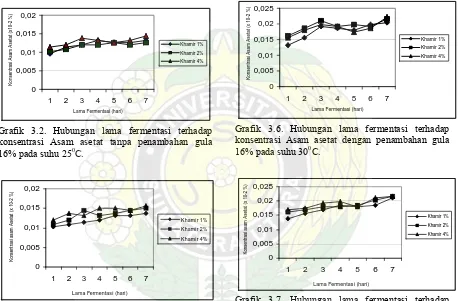
Grafik 3.2. Hubungan lama fermentasi terhadap konsentrasi Asam asetat tanpa penambahan gula
16% pada suhu 250C.
0 0,005 1
1 2 3 4 5 6 7
Lama Fermentasi (hari)
K
Grafik 3.3. Hubungan lama fermentasi terhadap konsentrasi Asam asetat tanpa penambahan gula
16% pada suhu 300C.
Lama Fermentasi (hari)
K
Grafik 3.4. Hubungan lama fermentasi terhadap konsentrasi Asam asetat tanpa penambahan gula
16% pada suhu 350C.
0
1 2 3 4 5 6 7 Lama Fermentasi (hari) 0,005
0,01 0,015 0,02 0,025
Konsentrasi Asam Asetat ( x 10-2 %)
Khamir 1% Khamir 2% Khamir 4%
Grafik 3.5. Hubungan lama fermentasi terhadap konsentrasi Asam asetat dengan penambahan gula
16% pada suhu 250C.
Lama Fermentasi (hari)
Konsentrasi Asam Asetat (x 10-2 %)
Khamir 1% Khamir 2% Khamir 4%
Grafik 3.6. Hubungan lama fermentasi terhadap asi Asam asetat dengan penambahan gula
16% pada suhu 300C.
Lama Fermentasi (hari)
Khamir 1% Khamir 2% Khamir 4%
Grafik 7. Hubungan lama fermentasi terhadap konsentrasi Asam asetat dengan penambahan gula
16% pad 0C.
3.
IV. KESIMPULAN DAN SARAN
4.1. Kesimpulan
1. Lama fermentasi sari buah pepaya yang baik untuk setiap variasi khamir dalam menghasilkan minuman anggur adalah tiga hari.
2. Penambahan gula sampai dengan 16% pada sari buah pepaya dapat meningkatkan produksi etanol sebesar 320%.
3. Penambahan gula sampai dengan 16% pada
ah pepaya dapat meningkatkan produksi asam asetat sebesar 42,31 %. 5. Kadar metanol dan asam asetat yang
diperoleh masih memenuhi standar nasional Indonesia 1993 (Anggur).
6. Berdasarkan surat keputusan Menteri Kesehatan No. 86 tahun 1977, minuman anggur yang dihasilkan dengan panambahan gula sampai 16% termasuk golongan B (kadar alkohol antara 5-20 %) sedangkan minuman anggur yang dihasilkan dengan tidak menambahkan gula ke dalam sari buah
Untuk mendapatkan minuman anggur dari sari buah pepaya yang siap untuk dikonsumsi perlu dilakukan analisis terhadap kandungan mikroba bahan dasar minuman anggur.
4.3. Ucapan Terima Kasih
Penulis mengucapkan terima kasih kepada Dedy N. dkk. (Mahasiswa Program Studi Teknik Kimia/Program Ekstension) yang telah membantu dalam pelaksanaan penelitian ini.
ugh, C.S. 1980. Methods For
Analysis of Must and Wine. New York: John Wiley & Sons.
Amerine, M. A. Berg, H. Kunkee, R.E., Ough, C.S., Singleton, V.L., and Webb, A.D.1982.
Technology of Wine Making. 4 th ed. Wesport, Connecticut: The AVI Publishing Company Inc.
Anonymous, 1977. The Preparation of Pried of
Pried Ginger. London: Mc. Compile by TPI.
Aries, R. S. 1947. Encyclopedia of Chemichal
Technology I. New York: The
Baga Kalie. M. 1989. Bertanam Pepaya. Jakarta:
Penerbit Penebar Swadaya.
Baga Kalie, M. 2000. Bertanam Pepaya (Revisi).
Jakarta: Penerbit Penebar Swadaya.
Bilford, H. R., Sclaf, R.E., Stark, and Kolachov,P.J.
1942. Alcoholic Fermentation of
Mollase. New York: Rapid Continous Fermentation Process Inc, Eng, Chem.
Buckle, K.A., Edwards, R.A., Fleet, G.H., and
Penerbit Universitas
rtemen Perindustrian. 1993. Mutu dan Cara Uji
Minuman Beralkohol. Jakarta: Standar Industri-Industri.
Direktorat Gizi Departemen Kesehatan RI. 1981.
Daftar Komposisi Bahan Makanan. Bharata Karya Aksara.
Desrosier, N.W. 1988. Teknologi Pengawetan
Pangan. Terjemahan oleh Muchji
Muljohardjo. Jakarta: Penerbit Universitas Indonesia.
oetomo, R.S. 1985. Mikrobiologi Dasar Dalam
Praktek. Teknik dan Prosedur Dasar Laboratorium. Jakarta: PT Gramedia.
Judoamidjojo, M. Darwis, A.A., Sa”id, E.G. 1992.
Teknologi Fermentasi. Jakarta: Penerbit Rajawali Pers.
Muljohardjo, M. 1984. Nenas dan Teknologi pengolahannya. Yogyakarta Liberty.
Pelczar, M. Z. Reid, and Chan. 1983. Microbiology,
4 th edition. New Delhi: ta Mc Graw
hird Edition. New York: Mc Graw Hill Book Company Inc.
a”id, G.A. 1987. Bio Industri, Penerapan Teknologi
Fermentasi. PAU Bioteknologi, IPB. Jakarta: Mediyatama Sarana Perkasa.
etyohadi. 1982. Pengaruh Lama Fermentasi
Terhadap Kadar Alkohol dari Bahan Air Kelapa Segar. Medan: Fakultas Pertanian, USU.
inarno, F.G. dan Fardiaz, S. 1992. Biofermentasi
dan Biosintesa Protein. Bandung: Penerbit Angkasa.
sari buah pepaya dapat meningkatkan produksi metanol sebesar 31,42 %.
4. Penambahan gula sampai dengan 16% pada sari bu
pepaya termasuk golongan A (kadar alkohol 1-5%).
4.2. Saran
DAFTAR PUSTAKA
Amerine, M.A. and O
Interscience Encyclopedia Inc.
Wootton, M. 1987. Ilmu Pangan.
Terjemahan oleh Purnomo, H. dan Adiono. Jakarta:
Indonesia.
Depa
Efendi, K. 2002. Pusat Penelitian Holtikultura dan
Aneka Tanaman. Jakarta.
Hadi
Hill Publishing Co. Ltd.
Prescott, S.C. and Dunn, C.G. 1959. Industrial
Microbiology, T
S
S