SELULOSA ASETAT DARI SELULOSA MIKROBIAL
UNTUK MEMBRAN ULTRAFILTRASI
Oleh :
DESIYARNI
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
PERANCANGAN PROSES PEMBUATAN
SELULOSA ASETAT DARI SELULOSA MIKROBIAL
UNTUK MEMBRAN ULTRAFILTRASI
Oleh
DESIYARNI
P. 25600001
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar Doktor
pada Program Studi Teknologi Industri Pertanian
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Nama
: Desiyarni
Nrp
: P. 256.00001
Program studi
: Teknologi Industri Pertanian
Menyetujui,
1.
Komisi pembimbing
Prof. Dr. Ir. H. Abdul Aziz Darwis, MSc
Ketua
Prof. Dr. Ir.Hj. Tun Tedja Irawadi, MS Dr. Ir.Hj. Erliza Noor
Anggota Anggota
Dr. Ir. Ani Suryani, DEA Dr. Ir. Kaseno, M.Eng
Anggota Anggota
Mengetahui,
2.
Ketua Program Studi 3. Dekan Pascasarjana
Teknologi Industri Pertanian
===========================================================
ABSTRAK
Selulosa asetat merupakan salah satu jenis polimer yang banyak digunakan untuk industri, salah satunya sebagai polimer pada pembuatan membran ultrafiltrasi. Selulosa asetat secara umum dibedakan atas dua jenis yaitu selulosa triasetat (selulosa asetat primer) dan selulosa diasetat (selulosa asetat sekunder). Selulosa asetat primer dibuat melalui reaksi esterifikasi (asetilasi) selulosa dengan pereaksi anhidrida asetat, sedangkan selulosa asetat sekunder dibuat dengan cara menghidrolisis selulosa asetat primer.
Secara komersial selulosa asetat dibuat dengan menggunakan bahan baku pulp kayu berkualitas tinggi. Salah satu masalah dalam produksi selulosa asetat dari pulp kayu adalah rendahnya kualitas dan kemurnian selulosa kayu karena pulp kayu masih mengandung hemiselulosa dan lignin. Selulosa mikrobial adalah jenis selulosa yang dihasilkan oleh mikroorganisme. Selulosa mikrobial bersifat renewable (dapat diperbarui), mempunyai karakteristik yang unik dan relatif lebih murni dibandingkan dengan selulosa kayu. Selulosa mikrobial merupakan salah satu alternatif sebagai sumber selulosa pada pembuatan selulosa asetat.
Membran ultrafiltrasi (UF) selulosa asetat merupakan salah satu jenis membran yang banyak digunakan pada proses pemisahan makromolekul. Membran UF mempunyai ukuran pori berkisar 0,1 – 0,001µm. Membran UF selulosa asetat umumnya dibuat dengan metoda inversi fasa menggunakan pelarut yang sesuai dengan jenis selulosa asetat yang digunakan
Penelitian ini bertujuan untuk (1) mendapatkan kondisi proses (konsentrasi asam sulfat, rasio anhidrida asetat dengan selulosa, waktu dan suhu reaksi) yang optimum pada proses asetilasi selulosa mikrobial menjadi selulosa triasetat (2) mendapatkan kondisi proses (rasio air terhadap selulosa mikrobial, konsentrasi
asam sulfat, waktu dan suhu reaksi) yang optimum pada proses hidrolisis selulosa triasetat menjadi selulosa diasetat kadar asetil 37-42 % dan (3) mendapatkan karakteristik (MWCO) membran ultrafiltrasi yang dihasilkan.
Penelitian ini dilakukan secara bertahap yang terdiri atas 3 tahap yaitu (1) optimasi proses asetilasi pada pembuatan selulosa triasetat dari selulosa mikrobial (2) optimasi proses hidrolisis selulosa triasetat menjadi selulosa diasetat dan (3) pembuatan dan karakterisasi membran ultrafiltrasi dari selulosa diasetat mikrobial. Penentuan kondisi optimum proses asetilasi dan hidrolisis dilakukan dengan menggunakan Metoda Permukaan Respon-Rancangan Komposit Pusat (Response Surface Methodology-Central Composite Design. Pembuatan membran UF dilakukan dengan dengan metode inversi fasa–presipitasi immersi, dengan pelarut dimetilformamida dan non pelarut berupa air. Selulosa diasetat mikrobial yang digunakan mempunyai kadar asetil berkisar 37% – 40 %, konsentrasi selulosa diasetat dalam larutan cetak berkisar 12-20% dan suhu air koagulasi berkisar 2-26
o
suhu 50 oC, dan waktu asetilasi 323 menit dengan hasil perolehan maksimum selulosa triasetat sebesar 1,79 (b/b) dan kadar asetil selulosa triasetat sebesar 45,78 %. Perlakuan rasio anhidrida asetat terhadap selulosa mikrobial dan waktu asetilasi berpengaruh nyata terhadap terhadap perolehan dan kadar asetil selulosa triasetat yang dihasilkan sedangkan konsentrasi asam sulfat dan suhu asetilasi tidak berpengaruh nyata. Pengaruh rasio anhidrida asetat terhadap selulosa mikrobial (X1) dan waktu asetilasi (X2) terhadap perolehan (Yper STA) dan kadar asetil selulosa
triasetat (Ykasetil STA) pada proses asetilasi selulosa mikrobial dapat dinyatakan
seperti persamaan berikut:
Y per STA =1,7425 + 0,1659 X1 + 0,0773X2 – 0,1230 X1 2
– 0,0200 X1X2 – 0,1205 X 2
2
Y kasetil STA = 45,7950 + 0,2321X1 + 0,2147X2 – 0,2777X12 –0,0508X1X2 – 0,3528 X22
Hasil optimasi proses hidrolisis selulosa triasetat menjadi selulosa diasetat menunjukkan kondisi optimum hidrolisis terjadi pada konsentrasi asam sulfat 1% (v/b), rasio air terhadap selulosa mikrobial 1,066 dan suhu 50 oC. Perlakuan rasio air terhadap selulosa mikrobial, konsentrasi asam sulfat, waktu dan suhu hidrolisis berpengaruh nyata terhadap kadar asetil selulosa diasetat. Pengaruh faktor rasio air terhadap selulosa mikrobial (X1), waktu (X2), konsentrasi asam sulfat (X3) dan
suhu (X4) terhadap kadar asetil selulosa diasetat (
Y
ka SDA) yang dihasilkan pada proses hidrolisis selulosa triasetat menjadi selulosa diasetat dapat dinyatakan seperti persamaan berikut:
Y
ka SDA = 41,5200- 0,2198X1 - 1,5915X2 - 0,6582X3 - 1,6582X4 - 0,6255X12 -0,1330X32-0,2940X2X3 - 0,2040X1X4 - 0,7028X2X4 - 0,1760X3X4
Puji syukur penulis panjatkan kehadirat Allah SWT atas limpahan rahmat dan
hidayah-Nya penulis dapat menyelesaikan penelitian dan menuliskan hasilnya dalam
disertasi yang berjudul Perancangan Proses Pembuatan Selulosa Asetat dari Selulosa
Mikrobial untuk Membran Ultrafiltrasi. Disertasi ini dibuat sebagai salah satu syarat
untuk memperoleh gelar Doktor pada program studi Teknologi Industri Pertanian
(TIP) pada Sekolah Pascasarjana Institut Pertanian Bogor.
Penulis menyampaikan ucapan terima kasih yang sangat tulus dan mendalam
kepada yang terhormat Prof. Dr. Ir. H. Abdul Aziz Darwis, MSc sebagai ketua
komisi pembimbing dan Prof. Dr. Ir. Hj. Tun Tedja Irawadi, MS, Dr. Ir. Hj. Erliza
Noor, Dr. Ir. Ani Suryani, DEA dan Dr. Ir. Kaseno, M.Eng masing-masing sebagai
anggota komisi pembimbing yang dengan tulus ikhlas telah membimbing penulis
hingga disertasi ini terwujud. Penghargaan dan ucapan terima kasih juga penulis
sampaikan kepada Dr. Ir. Hj. Liesbetini Hartato, MS dan Dr. Ir. H. Amril Aman atas
kesediaannya menjadi dosen penguji luar komisi pada ujian tertutup penulis.
Penghargaan dan ucapan terima kasih juga penulis sampaikan kepada
Direktur Akademi Teknologi Industri Padang – Departemen Perindustrian yang telah
memberikan kesempatan kepada penulis untuk melanjutkan pendidikan di Sekolah
Pascasarjana Institut Pertanian Bogor.
Terima kasih juga penulis sampaikan kepada Dekan Sekolah Pascasarjana
Institut Pertanian Bogor, Dekan Fakultas Teknologi Industri Pertanian, Ketua
Program Studi Teknologi Industri Pertanian dan seluruh staf pengajar Sekolah
Pascasarjana IPB khususnya Pogram Studi Teknologi Industri Pertanian (TIP) yang
telah memberi ilmu pengetahuan dan bimbingan kepada penulis selama menimba
Pendidikan Tinggi, Departemen Pendidikan Nasional Republik Indonesia yang telah
memberikan dukungan finasia l bagi pelaksanaan penelitian melalui Penelitian Hibah
Bersaing IX. Terima kasih juga penulis sampaikan kepada Ibu Rini Purnawati atas
bantuannya selama melaksanakan penelitian.
Kepada yang mulia Ayahanda H. Ahmad dan Ibunda Hj. Rosni, Ayah Mertua
H. Bahar (alm) dan Ibu mertua Hj. Ratna penulis persembahkan terima kasih tak
terhingga atas segala doa , dukungan, bimbingan dan nasehat yang tiada
henti-hentinya diberikan kepada penulis. Kepada suami tercinta M. Arifin SE, MM dan
anak-anakku tersayang Faiz Rahman Arifin, Hanif Rahman Arifin dan Azzahra
Arifin penulis ucapkan terima kasih tak terhingga atas dukungan, kesabaran,
pengorbanan dan iringan doa yang tulus ikhlas. Kepada kakanda Afrizal dan
Ardiamsyah, adinda Novi Erni, Susi, Mayesti, Arsil, Yosi Septriani, dan Aulia Rahim
penulis ucapkan terima kasih tak terhingga atas doa dan dukungannya.
Akhir kata, kepada semua pihak yang telah membantu penulis yang tidak
dapat penulis sebutkan satu persatu, penulis ucapkan terima kaih. Semoga Allah
SWT membalasnya berlipat ganda.
Bogor, Agustus 2006
Latar belakang
Selulosa asetat merupakan salah satu jenis polimer yang penting dan banyak
digunakan pada industri antara lain sebagai polimer pada industri plastik cetakan
(
moulding
), film fotografi dan membran. Selulosa asetat secara umum dibedakan atas
dua jenis yaitu selulosa triasetat (selulosa asetat primer) dan selulosa diasetat
(selulosa asetat sekunder). Selulosa asetat primer dibuat melalui reaksi esterifikasi
(asetilasi) selulosa dengan pereaksi anhidrida asetat, sedangkan selulosa asetat
sekunder dibuat dengan cara menghidrolisis selulosa asetat primer.
Secara komersial selulosa asetat dibuat dengan menggunakan bahan baku
berupa kapas dan pulp kayu berkualitas tinggi. Salah satu masalah dalam produksi
selulosa asetat dari pulp kayu adalah rendahnya kualitas dan kemurnian selulosa kayu
karena pulp kayu masih mengandung hemiselulosa dan lignin. Hemiselulosa dan
lignin merupakan senyawa yang tidak diinginkan terdapat dalam bahan baku
produksi selulosa asetat. Hemiselulosa yang terdapat dalam pulp kayu seperti
xylan
dan glukomanan akan berubah menjadi
xylan
asetat dan glukomanan asetat selama
reaksi esterifikasi. Kedua senyawa ini akan menyebabkan kekeruhan dan viskositas
palsu pada selulosa asetat yang dihasilkan.
sedang dikembangkan antara lain untuk diafragma speaker mutu tinggi (
high fidelity
audio speaker diaphragma)
, bahan pembuatan kertas sangat kuat (
ultrahigh strength
paper
), campuran pada produk perawat luka (
wound care products
), sumber selulosa
pada pembuatan mikrokristalin selulosa (MCC) dan sebagai bahan penyerap
(diaper). Selulosa jenis ini bersifat dapat diperbarui (
renewable
). Disamping itu
selulosa mikrobial mempunyai beberapa keunggulan antara lain (1) relatif murni
sehingga tidak membutuhkan proses delignifikasi , (2) sifat hidrofilik yang sangat
tinggi dan (3) dapat diproduksi dari berbagai macam substrat yang relatif mudah dan
murah. Berdasarkan keunggulan yang dimiliki tersebut maka selulosa jenis ini
merupakan alternatif sebagai sumber selulosa yang relatif murni pada produksi
selulosa asetat.
mikrobial telah berhasil dilakukan namun kondisi optimum pembuatannya belum
diketahui.
Tahapan yang paling penting pada proses pembuatan selulosa triasetat adalah
asetilasi. Pada pembuatan selulosa triasetat secara komersial terdapat beberapa faktor
penting yang mempengaruhi kecepatan reaksi asetilasi dan kualitas selulosa triasetat
yang dihasilkan antara lain karakteristik bahan baku, rasio anhidrida asetat dengan
selulosa, jenis dan konsentrasi katalis serta suhu dan lama asetilasi. Kondisi proses
asetilasi dan karakteristik selulosa asetat primer yang dihasilkan oleh Tabuchi
et al.
(1998), Safriani (2000) dan Darwis
et al.
(2003) berbeda-beda dan belum diketahui
kondisi optimumnya. Agar dapat dihasilkan selulosa triasetat yang berkualitas baik
dari selulosa mikrobial maka perlu dilakukan optimasi proses pembuatannya
sehingga dapat diperoleh informasi faktor- faktor yang berpengaruh pada proses
asetilasi selulosa mikrobial dan kondisi optimumnya.
menggunakan katalis. Proses hidrolisis dilakukan selama waktu tertentu hingga
diperoleh selulosa diasetat sesuai kadar asetil yang diinginkan.
Salah satu masalah pada proses hidrolisis adalah penentuan kondisi hidrolisis
dan lama hidrolisis yang tepat untuk bisa menghasilkan selulosa diasetat sesua i kadar
asetil yang diinginkan. Pada pembuatan selulosa diasetat secara komersial, penentuan
lama proses hidrolisis dilakukan dengan cara pengambilan contoh pada selang
waktu tertentu untuk mengetahui kelarutan atau kadar asetil selulosa asetat yang
telah dicapai. Pengukuran kadar asetil selulosa asetat yang dihasilkan pada proses
hidrolisis dengan metoda titrasi (ASTM D 871-96) membutuhkan waktu yang relatif
lama yaitu sekitar 3 – 4 hari. Hal ini menyebabkan pengambilan keputusan untuk
menentukan lama hidrolisis relatif sulit.
Penelitian tentang faktor-faktor yang berpengaruh dan penentuan kondisi
optimum hidrolisis pada proses pembuatan selulosa diasetat dari selulosa triasetat
mikrobial hingga saat ini belum pernah dilakukan. Diharapkan dari penelitian ini
dapat diperoleh informasi tentang faktor-faktor yang berpengaruh pada proses
hidrolisis dan kondisi optimum proses pembuatan selulosa diasetat dari selulosa
triasetat mikrobial.
antara lain pembuatan membran relatif lebih mudah, bahan dasarnya dapat diperbarui
(
renewable
) dan memiliki sifat hidrofilik serta dapat digunakan untuk membuat
berbagai jenis membran. Meskipun demikian terdapat juga kekurangannya yaitu
penggunaan membran yang dihasilkan terbatas pada suhu sekitar 30
oC, pH antara
2- 8 dan tidak tahan terhadap serangan mikroorganisme. Membran berbasis selulosa
merupakan tipe membran yang relatif murah.
Membran ultrafiltrasi selulosa asetat merupakan salah satu jenis membran
yang dewasa ini banyak digunakan pada proses pemisahan makromolekul.
Pembuatan membran ultrafiltrasi selulosa asetat umumnya dilakukan dengan metoda
inversi fasa. Pada pembuatan membran polimer dengan metoda inversi fasa terdapat
beberapa faktor yang mempengaruhi morfologi membran yang dihasilkan antara lain
jenis polimer, pelarut dan non pelarut yang digunakan, konsentrasi polimer dalam
larutan cetak, komposisi cairan dalam bak koagulasi.
Tujuan Penelitian
Penelitian ini bertujuan untuk (1) me ndapatkan kondisi proses (konsentrasi
asam sulfat, rasio anhidrida asetat dengan selulosa, waktu dan suhu reaksi) yang
optimum pada proses asetilasi selulosa mikrobial menjadi selulosa triasetat dan
mengetahui pengaruh konsentrasi asam sulfat, rasio anhidrida asetat dengan selulosa,
waktu dan suhu asetilasi terhadap perolehan dan kadar asetil selulosa triasetat yang
dihasilkan, (2) mendapatkan kondisi proses (
rasio air terhadap selulosa mikrobial,
konsentrasi
asam sulfat
, waktu dan suhu reaksi) yang optimum pada proses
hidrolisis selulosa triasetat menjadi selulosa diasetat kadar asetil 37-42 % dan
mengetahui pengaruh
rasio air dengan selulosa mikrobial, konsentrasi
asam sulfat
,
waktu dan suhu hidrolisis
terhadap kadar asetil selulosa diasetat yang dihasilkan
dan (3) mendapatkan karakteristik (
MWCO
) membran ultrafiltrasi yang dihasilkan.
Hipotesis
Rasio anhidrida asetat dengan selulosa mikrobial, konsentrasi asam sulfat,
waktu dan suhu asetilasi diduga berpengaruh nyata terhadap perolehan dan kadar
asetil selulosa triasetat yang dihasilkan karena semakin tinggi rasio anhidrida asetat
terhadap selulosa mikrobial, konsentrasi asam sulfat, waktu dan suhu asetilasi akan
meningkatkan perolehan dan kadar asetil selulosa triasetat yang dihasilkan.
dihasilkan karena semakin tinggi rasio air terhadap selulosa mikrobial, konsentrasi
asam sulfat, waktu dan suhu hidrolisis akan menurunkan kadar asetil selulosa diasetat
yang dihasilkan.
Terdapat perbedaan karakteristik membran ultrafiltrasi yang dibuat dari
selulosa diasetat kadar asetil 37 – 40 % pada konsentrasi selulosa diasetat dalam
larutan cetak (dope) berkisar 12 – 20 % dan suhu air koagulasi 2-26
oC karena
diduga peningkatan kadar asetil selulosa diasetat dan konsentrasi selulosa diasetat
dalam larutan cetak serta peningkatan suhu air koagulasi akan menyebabkan ukuran
pori membran semakin kecil.
Ruang Lingkup Penelitian
Pembuatan selulosa triasetat dari selulosa mikrobial (nata de coco) dilakukan
secara heterogen, dengan media asetilasi asam asetat, pereaksi anhidrida asetat dan
katalis asam sulfat. Penentuan kondisi optimum proses asetilasi (respon perolehan
dan kadar asetil selulosa triasetat) dilakukan dengan menggunakan Metoda
Permukaan Respon-Rancangan Komposit Pusat
(
Response Surface
Methodology-Central Composite Design).
Pembuatan selulosa triasetat dari selulosa diasetat mikrobial (hidrolisis)
dilakukan secara homogen dengan pereaksi air dan katalis asam sulfat. Penentuan
kondisi optimum proses hidrolisis (respon kadar asetil selulosa diasetat) dilakukan
dengan menggunakan Metoda Permukaan Respon-Rancangan Komposit Pusat
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan mulai Desember 2003 hingga Juni 2005.
Penelitian dilaksanakan di Laboratorium Teknologi Kimia dan Laboratorium
Pengawasan Mutu Departemen TIN - FATETA IPB, Laboratorium Kimia dan
Fisika T erapan LIPI Bandung.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini terdiri atas (1) bahan untuk
pembuatan selulosa triasetat (STA) dan selulosa diasetat (SDA) dan (2) bahan
untuk pembuatan membran ultrafiltrasi selulosa diasetat mikrobial. Bahan untuk
pembuatan selulosa triasetat dan selulosa diasetat terdiri atas lembaran selulosa
mikrobial (nata de coco), NaOH, asam asetat (CH3COOH) (Merck), anhidrida
asetat (J.T Baker), asam sulfat (H2SO4) (Merck), HCl, alkohol dan magnesium
karbonat (MgCO3). Bahan-bahan untuk analisis selulosa asetat terdiri atas etanol
75%, HCl 0,5 N, NaOH 0,5 N, aseton, indikator fenolftalein dan metil merah.
Bahan untuk pembuatan membran ultrafiltrasi adalah selulosa diasetat
mikrobial dan selulosa asetat komersial, dimetil formamida (DMF), aseton, Bovin
Serum Albumin dengan bobot molekul 67 kDa, dekstran dengan bobot molekul
37 kDa. Bahan-bahan untuk analisis membran terdiri atas H2SO4, fenol,
Alat-alat untuk pembuatan selulosa asetat yang digunakan adalah alat-alat
gelas, mesin penghancur (grinder), penekan hidrolik (hydraulic press), pengaduk
bermagnetik, termometer, penangas air bergoyang, oven dan sentrifus.
Alat-alat untuk pembua tan membran yang digunakan adalah alat-alat
gelas, pengaduk bermagnet, lembaran kaca, aplikator, termometer dan bak
koagulasi. Alat-alat untuk karakterisasi membran terdiri atas alat-alat gelas,
modul penyaringan aliran silang (crossflow filtration), spektrofotometer dan
Scanning Electron Microscope.
Metode Penelitian
Penelitian ini dilakukan secara bertahap yang terdiri atas 3 tahap yaitu:
1. Optimasi proses asetilasi pada pembuatan selulosa triasetat (STA) dari
selulosa mikrobial (penentuan kondisi aktivasi selulosa mikrobial,
penentuan faktor -faktor yang berpengaruh pada asetilasi, pembentukan
dan pengujian persamaan regresi perolehan dan kadar asetil STA dan
penentuan kondisi optimum asetilasi).
2. Optimasi proses hidrolisis selulosa triasetat menjadi selulosa diasetat
(SDA) (penentuan faktor-faktor yang berpengaruh pada hidrolisis,
pembentukan dan pengujian persamaan regresi kadar asetil selulosa
diasetat dan penentuan kondisi optimum hidrolisis).
3. Pembuatan dan karakterisasi membran ultrafiltrasi dari selulosa diasetat
(pengaruh kadar asetil selulosa diasetat berkisar 37,21% – 40,22% dan
konsentrasi selulosa diasetat dalam larutan cetak berkisar 12% – 20 %
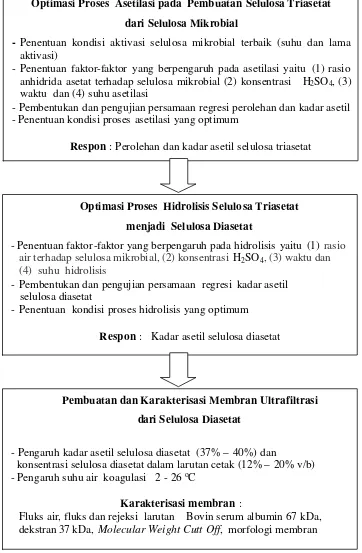
Gambar 4 . Skema tahapan penelitian
Optimasi Proses Asetilasi pada Pembuatan Selulosa Triasetat dari Selulosa Mikrobial
- Penentuan kondisi aktivasi selulosa mikrobial terbaik (suhu dan lama aktivasi)
- Penentuan faktor-faktor yang berpengaruh pada asetilasi yaitu (1) rasio anhidrida asetat terhadap selulosa mikrobial (2) konsentrasi H2SO4, (3)
waktu dan (4) suhu asetilasi
- Pembentukan dan pengujian persamaan regresi perolehan dan kadar asetil - Penentuan kondisi proses asetilasi yang optimum
Respon : Perolehan dan kadar asetil selulosa triasetat
Optimasi Proses Hidrolisis Selulosa Triasetat menjadi Selulosa Diasetat
- Penentuan faktor -faktor yang berpengaruh pada hidrolisis yaitu (1) rasio air terhadap selulosa mikrobial, (2) konsentrasi H2SO4, (3) waktu dan
(4) suhu hidrolisis
- Pembentukan dan pengujian persamaan regresi kadar asetil selulosa diasetat
- Penentuan kondisi proses hidrolisis yang optimum
Respon : Kadar asetil selulosa diasetat
Pembuatan dan Karakterisasi Membran Ultrafiltrasi dari Selulosa Diasetat
- Pengaruh kadar asetil selulosa diasetat (37% – 40%) dan
konsentrasi selulosa diasetat dalam larutan cetak (12% – 20% v/b) - Pengaruh suhu air koagulasi 2 - 26 oC
Karakterisasi membran :
Penelitian I. Optimasi Proses Asetilasi pada Pembuatan Selulosa Triasetat dari Selulosa Mikrobial
Selulosa mikrobial yang digunakan sebagai sumber selulosa pada
penelitian optimasi proses asetilasi ini adalah serbuk selulosa mikrobial kering
berukuran 10 mesh. Pembuatan selulosa mikrobial kering dari lembaran selulosa
mikrobial basah dilakukan dengan cara membersihkan selulosa mikrobial basah
dari sisa media kultivasi dan bakteri (modifikasi Yamanaka et al., 1989). Kondisi
aktivasi selulosa mikrobial yang digunakan pada penelitian pembuatan selulosa
triasetat ini adalah kondisi aktivasi terbaik yang diperoleh pada tahap penentuan
kondisi aktivasi selulosa mikrobial (modifikasi Malm dan Tanghe, 1953). Proses
asetilasi selulosa mikrobial dilakukan secara heterogen dengan menggunakan
anhidrida asetat sebagai pereaksi, asam sulfat pekat sebagai katalis dan asam
asetat sebagai media asetilasi (Malm dan Tanghe, 1953). Penelitian optimasi
proses asetilasi dilakukan dengan menggunakan Metoda Permukaan
Respon-Rancangan Komposit Pusat (Response Surface Methodology-Central Composite Design). Pengolahan data yang dihasilkan dilakukan dengan menggunakan perangkat lunak SAS dan Statistica .
Pembuatan Selulosa Mikrobial Kering (modifikasi Yamanaka et al., 1989)
Selulosa mikrobial yang digunakan pada penelitian ini dibuat dari
lembaran basah selulosa mikrobial hasil kultivasi diam selama 7 hari dengan
media utama air kelapa, isolat bakteri Acetobacter campuran. Lembaran basah
selulosa mikrobial dipotong-potong dan dicuci. Setelah itu direndam dalam
perendaman dalam larutan asam asetat 1%. Selanjutnya potongan nata dicuci
bersih dengan air, dikempa dengan penekan hidrolik dan dikeringkan pada suhu
sekitar 40 oC selama 6 jam. Lembaran selulosa mikrobial kering yang diperoleh dihancurkan dengan menggunakan mesin penghancur (grin der) dan disaring
dengan penyaring berukuran 10 mesh. Diagram alir pembuatan serbuk selulosa
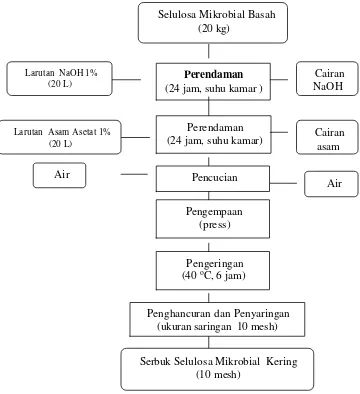
mikrobial kering (modifikasi Yamanaka et al., 1989) dapat dilihat pada Gambar 5.
Gambar 5. Diagram alir pembuatan serbuk selulosa mikrobial kering (modifikasi Yamanaka et al., 1989)
Perendaman
(24 jam, suhu kamar )
Perendaman (24 jam, suhu kamar)
Pengempaan (press)
Pengeringan (40 oC, 6 jam)
Pencucian
Penghancuran dan Penyaringan (ukuran saringan 10 mesh) Selulosa Mikrobial Basah
(20 kg)
Cairan asam
Air
Serbuk Selulosa Mikrobial Kering (10 mesh)
Cairan NaOH
Larutan NaOH 1% (20 L)
Larutan Asam Asetat 1% (20 L)
Penentuan Kondisi Aktivasi Selulosa Mikrobial Terbaik (modifikasi Malm dan Tanghe, 1953)
Penelitian penentuan kondisi aktivasi selulosa mikrobial bertujuan untuk
mendapatkan kondisi aktivasi selulosa mikrobial terbaik yang selanjutnya akan
digunakan pada tahap asetilasi selulosa mikrobial. Kondisi aktivasi yang terbaik
adalah kondisi aktivasi yang dapat menghasilkan perolehan selulosa triasetat
tertinggi pada proses asetilasi selulosa mikrobial. Perolehan selulosa triasetat
dihitung sebagai perbandingan antara bobot kering selulosa triasetat dengan bobot
kering selulosa mikrobial yang digunakan.
Media aktivasi yang digunakan adalah asam asetat glasial dengan rasio
asam asetat terhadap selulosa mikrobial yang digunakan adalah 8:1 (v/bk).
Proses aktivasi dilakukan dengan cara sebanyak 5 gram serbuk selulosa mikrobial
kering dan 40 ml asam asetat glasial dimasukkan kedalam labu erlenmeyer.
Aktivasi dilakukan dengan menggunakan penangas air (water bath) pada suhu air
50 oC selama 0, 2, 4, 6, 8 jam dan suhu kamar selama 4, 8, 12, 16 jam. Setelah proses aktivasi selesai selanjutnya dilakukan proses asetilasi selulosa mikrobial
menjadi selulosa triasetat (modifikasi Malm dan Tanghe, 1953).
Proses asetilasi dilakukan dengan rasio anhidrida asetat terhadap selulosa
mikrobial kering yang digunakan sebesar 3 : 1. Sebanyak 15 ml anhidrida
asetat, 22,5 ml asam asetat glasial dan 0,05 ml asam sulfat ditambahkan kedalam
labu erlenmeyer yang berisi selulosa mikrobial yang sudah diaktivasi. Campuran
diaduk hingga rata dengan menggunakan pengaduk bermagnet . Setelah diperoleh
campuran yang rata dilanjutkan proses asetilasi di dalam penangas air bergoyang
Selama proses asetilasi akan terjadi reaksi antara selulosa mikrobial
dengan anhidrida asetat sehingga terbentuk selulosa triasetat. Selulosa triasetat
yang terbentuk akan larut dalam media asetilasi sedangkan serbuk selulosa
mikrobial yang tidak bereaksi akan mengendap. Setelah proses asetilasi selesai
dilakukan pemisahan selulosa mikrobial yang tidak terkonversi dari media
asetilasi. Pemisahan selulosa mikrobial yang tidak terasetilasi dilakukan dengan
cara sentrifugasi. Sisa serbuk selulosa mikrobial akan mengendap sedangkan
selulosa triasetat terdapat dalam supernatan. Campuran hasil asetilasi disentrifus
pada suhu 20 oC selama 15 menit dengan kecepatan 3000 rpm.
Selulosa triasetat yang larut dalam supernatan selanjutnya dipisahkan
dengan cara menuangkannya kedalam larutan asam asetat 10%. Endapan selulosa
triasetat yang diperoleh disaring dan direndam dalam larutan magnesium karbonat
1% selama 2 jam untuk menghilangkan sisa asam. Selanjutnya endapan selulosa
triasetat dicuci bersih dengan air , dan dikeringkan dengan oven pada suhu 50 oC selama 6 jam. Selulosa triasetat kering yang diperoleh selanjutnya ditimbang dan
diukur kadar airnya. Perolehan selulosa triasetat dihitung sebagai perbandingan
antara bobot kering selulosa triasetat dengan bobot kering selulosa mikrobial yang
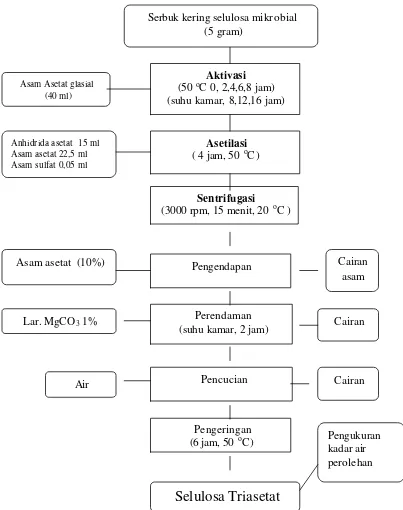
digunakan (Lampiran 1g). Diagram alir proses aktivasi dan proses asetilasi pada
tahap penentuan kondisi aktivasi selulosa mikrobial terbaik dapat dilihat pada
Gambar 6. Diagram alir penentuan kondisi aktivasi selulosa mikrobial terbaik pada pembuatan selulosa triasetat (modifikasi Malm dan Tanghe, 1953)
Selulosa Triasetat
Aktivasi(50 oC 0, 2,4,6,8 jam) (suhu kamar, 8,12,16 jam)
Asam asetat (10%)
Cairan
Anhidrida asetat 15 ml Asam asetat 22,5 ml Asam sulfat 0,05 ml
Asam Asetat glasial (40 ml)
Pengendapan
Pengeringan (6 jam, 50 oC)
Perendaman (suhu kamar, 2 jam)
Sentrifugasi
(3000 rpm, 15 menit, 20 oC )
Asetilasi
( 4 jam, 50 oC )
Serbuk kering selulosa mikr obial (5 gram)
Lar. MgCO3 1%
Cairan asam
Pencucian
Air Cairan
Penentuan Faktor yang Berpengaruh pada Proses Asetilasi
Proses asetilasi selulosa mikrobial dilakukan secara heterogen dengan
menggunakan anhidrida asetat sebagai pereaksi, asam sulfat pekat sebagai katalis
dan asam asetat sebagai media asetilasi (Malm dan Tanghe, 1953). Terdapat 4
variabel bebas yang diujikan pada tahap asetilasi selulosa mikrobial yaitu (1)
rasio anhidrida asetat terhadap selulosa mikrobial yang digunakan (2)
konsentrasi katalis H2SO4, (3) waktu reaksi dan (4) suhu asetilasi. Variabel
respon yang diamati adalah perolehan dan kadar asetil selulosa triasetat yang
dihasilkan.
Sebelum dilakukan proses asetilasi terlebih dahulu dilakukan proses
aktivasi selulosa mikrobial. Aktivasi selulosa mikrobial dilakukan berdasarkan
kondisi aktivasi terbaik yang diperoleh pada tahap penentuan kondisi aktivasi
selulosa mikrobial yaitu sebanyak 5 gram selulosa mikrobial kering (ukuran 10
mesh) dimasukkan kedalam labu erlenmeyer. Kemudian ditambahkan 40 ml asam
asetat glasial dan dibiarkan selama 6 jam pada suhu 50 oC. Selanjutnya dilakukan proses asetilasi.
Asetilasi dilakukan dengan cara menambahkan anhidrida asetat, asam
asetat dan asam sulfat kedalam selulosa mirobial teraktivasi. Anhidrida asetat
ditambahkan sebanyak 2, 3, dan 4 kali jumlah selulosa mikrobial yang digunakan
atau 10 ml, 15 ml dan 20 ml untuk setiap 5 g selulosa mikrobial kering yang
digunakan. Asam asetat glasial ditambahkan sebanyak 22,5 ml. Katalis asam
sulfat ditambahkan sebanyak 0,025 ml, 0,050 ml dan 0,075 ml atau 0,5%, 1%, dan
1,5%. Proses pencampuran anhidrida asetat, asam sulfat dan asam asetat dengan
bermagnet. Setelah diperoleh campuran yang rata dilanjutkan proses asetilasi di
dalam penangas air bergoyang dengan kecepatan 150 rpm pada suhu 40, 50, dan
60 oC selama 240, 300, dan 360 menit. Setelah proses asetilasi selesai, campuran selulosa triasetat yang diperoleh segera didinginkan dan disentrifus pada suhu 20
oC selama 15 menit dengan kecepatan 3000 rpm. Selulosa mikrobial yang tidak
bereaksi akan terdapat pada bagian endapan sedangkan selulosa triasetat yang
terbentuk terdapat pada supernatan.
Pemisahan selulosa triasetat yang larut dalam supernatan dilakukan
dengan cara pengendapan. Pengendapan selulosa triasetat dilakukan dengan cara
menuangkan supernatan kedalam larutan asam asetat 10%. Endapan selulosa
triasetat yang diperoleh selanjutnya disaring dan direndam dalam larutan
magnesium karbonat 1% untuk menghilangkan sisa asam. Selanjutnya selulosa
triasetat dicuci bersih dengan air , dan dikeringkan dengan oven pada suhu 50 oC selama 6 jam. Selulosa triasetat kering yang diperoleh selanjutnya ditimbang dan
diukur kadar airnya untuk mengetahui bobot kering selulosa triasetat yang
dihasilkan. Perolehan selulosa triasetat dihitung sebagai perbandingan antara
bobot kering selulosa triasetat dengan bobot kering selulosa mikrobial yang
digunakan (Lampiran 1g). Selanjutnya dilakukan pengukuran kadar asetil selulosa
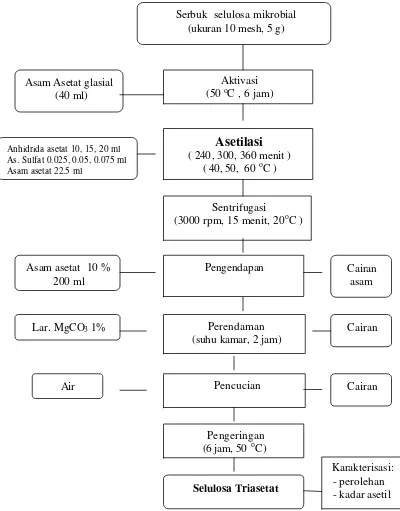
triasetat. Kadar asetil selulosa triasetat yang dihasilkan dihitung dengan metoda
Gambar 7. D iagram alir proses pembuatan selulosa triasetat dari selulosa mikrobial (modifikasi Malm dan Tanghe, 1953)
Selulosa Triasetat
Aktivasi (50 oC , 6 jam)
Asam asetat 10 % 200 ml
Cairan
Anhidrida asetat 10, 15, 20 ml As. Sulfat 0.025, 0.05, 0.075 ml Asam asetat 22.5 ml
Asam Asetat glasial (40 ml)
Pengendapan
Pengeringan (6 jam, 50 oC)
Perendaman (suhu kamar, 2 jam)
Sentrifugasi
(3000 rpm, 15 menit, 20 oC )
Asetilasi
( 240, 300, 360 menit ) ( 40, 50, 60 oC ) Serbuk selulosa mikrobial
(ukuran 10 mesh, 5 g)
Lar. MgCO3 1%
Cairan asam
Pencucian
Air Cairan
Selanjutnya dilakukan penentuan pengaruh variabel bebas terhadap respon
perolehan dan kadar asetil. Penentuan faktor-faktor yang berpengaruh dilakukan
dengan menggunakan uji analisis keragaman untuk masing-masing respon yang
diamati. Variabel yang berpengaruh nyata selanjutnya digunakan sebagai
variabel bebas pada tahap pembentukan model.
Pembentukan dan Pengujian Model
Model yang dibuat dalam penelitian ini adalah model empiris berupa model regresi. Terdapat dua model regresi yang dibuat pada penelitian ini yaitu model regresi perolehan selulosa triasetat dan model regresi kadar asetil selulosa triasetat yang dihasilkan pada proses asetilasi. Pengujian terhadap model regresi yang dihasilkan meliputi uji penyimpangan model atau lack of fit, uji determinan (R2 ), uji signifikansi model, dan uji asumsi residual (Box et al., 1978; Box dan Draper, 1987 ; Gaspersz, 1995).
Penentuan Kondisi Optimum Proses Asetilasi
Penentuan kondisi optimum proses asetilasi pada pembuatan selulosa triasetat dari selulosa mikrobial dilakukan dengan menggunakan analisis kanonik, analisis permukaan respon, analisis plot kontur dan ridge analysis. Kondisi proses optimum yang diperoleh selanjutnya diverifikasi di laboratorium.
Rancangan Percobaan
proses asetilasi yaitu (1) konsentrasi H2SO4 pekat (katalis) yang dikodekan
sebagai X1, (2) rasio anhidrida asetat terhadap selulosa mikrobial yang digunakan
yang dikodekan sebagai X2, (3) waktu asetilasi yang dikodekan sebagai X3, dan
(4) suhu asetilasi yang dikodeka n sebagai X4. Faktor, kode dan taraf kode yang
dicobakan pada proses asetilasi dapat dilihat pada Tabel 4.
Tabel 4. Faktor, kode dan taraf kode pada percobaan asetilasi Taraf kode
No Faktor Kode
rendah -1
tengah 0
tinggi +1
1 Katalis H2SO4 pekat (% v/bk) (K) X1 0.5 1 1.5
2 Rasio anhidrida asetat terhadap selulosa mikrobial (%v/bk) (P)
X2 2 3 4
3 Waktu ,menit (W) X3 240 300 360
4 Suhu (oC) (S) X4 40 50 60
Nilai faktor yang dikodekan dihitung dengan cara seperti be rikut :
X1 = (K – 1,5) X2 = (P - 3) X3 = (W- 300) X4 = (W-50)
0,5 1 60 10
X1 = nilai kode konsentrasi katalis K = nilai konsentrasi katalis aktual (%v/bk)
X2 = nilai kode rasio pereaksi P = nilai rasio pereaksi aktual (%v/bk)
X3 = nilai kode waktu reaksi W = nilai waktu reaksi aktual (menit)
X4 = nilai kode suhu reaksi S = nilai suhu reaksi aktual (oC)
faktorial dan 4 unit percobaan titik pusat. Pembuatan model regresi linier perolehan dan kadar asetil selulosa triasetat dilakukan dengan menggunakan respon pada percobaan faktorial dan titik pusat. Matriks rancangan percobaan dengan 4 faktor ini dapat dilihat pada Tabel 5.
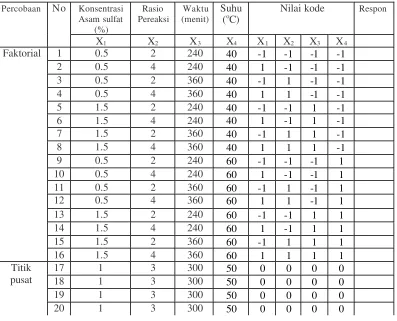
Tabel 5 . Matriks rancangan percobaan 4 faktor proses asetilasi
Konsentrasi Asam sulfat (%) Rasio Pereaksi Waktu (menit) Suhu
(oC)
Nilai kode Respon
Percobaan No
X1 X2 X3 X4 X1 X2 X3 X4
1 0.5 2 240 40 -1 -1 -1 -1
2 0.5 4 240 40 1 -1 -1 -1
3 0.5 2 360 40 -1 1 -1 -1
4 0.5 4 360 40 1 1 -1 -1
5 1.5 2 240 40 -1 -1 1 -1
6 1.5 4 240 40 1 -1 1 -1
7 1.5 2 360 40 -1 1 1 -1
8 1.5 4 360 40 1 1 1 -1
9 0.5 2 240 60 -1 -1 -1 1
10 0.5 4 240 60 1 -1 -1 1
11 0.5 2 360 60 -1 1 -1 1
12 0.5 4 360 60 1 1 -1 1
13 1.5 2 240 60 -1 -1 1 1
14 1.5 4 240 60 1 -1 1 1
15 1.5 2 360 60 -1 1 1 1
Faktorial
16 1.5 4 360 60 1 1 1 1
17 1 3 300 50 0 0 0 0
18 1 3 300 50 0 0 0 0
19 1 3 300 50 0 0 0 0
Titik pusat
20 1 3 300 50 0 0 0 0
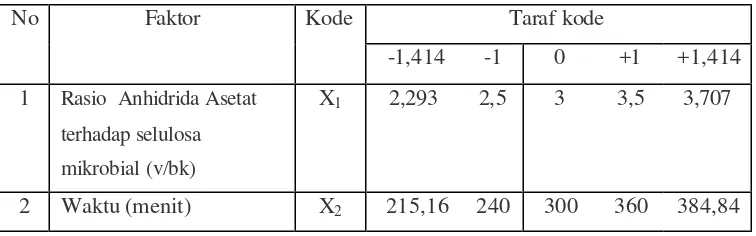
taraf kode pada percobaan asetilasi dengan 2 faktor dapat dilihat pada Tabel 6, sedangkan matriks percobaannya dapat dilihat pada Tabel 7.
Tabel 6 . Faktor , kode dan taraf kode pada proses asetilasi dengan 2 faktor Taraf kode
No Faktor Kode
-1,414 -1 0 +1 +1,414
1 Rasio Anhidrida Asetat
terhadap selulosa
mikrobial (v/bk)
X1 2,293 2,5 3 3,5 3,707
2 Waktu (menit) X2 215,16 240 300 360 384,84
Tabel 7 . Matriks rancangan percobaan 2 faktor proses asetilasi
Taraf faktor aktual Taraf fraktor yang dikodekan No
Rasio pereaksi X1
Waktu(menit) X2
X1 X2
Respon
1 2,5 240 -1 -1
2 3,5 240 1 -1
3 2,5 360 -1 1
4 3,5 360 1 1
5 3,0 300 0 0
6 3,0 300 0 0
7 3,0 300 0 0
8 3,0 300 0 0
5 2,293 300 -1.414 0
6 3,707 300 1.414 0
7 3,0 215.16 0 -1.414
[image:30.612.138.500.335.631.2]Penelitian II. Optimasi P roses Hidrolisis Selulosa Triasetat menjadi Selulosa Diasetat
Penelitian optimasi proses hidrolisis selulosa triasetat menjadi selulosa
diasetat dilakukan dengan menggunakan Metoda Permukaan Respon - Rancangan
Komposit Pusat. Pengolahan data yang dihasilkan dilakukan dengan menggunakan perangkat lunak SAS dan Statistica. Proses hidrolisis selulosa triasetat dilakukan dengan menggunakan air sebagai pereaksi dan asam sulfat
sebagai katalis (modifikasi Malm dan Tanghe, 1953). Terdapat 4 variabel bebas
yang dicobakan pada tahap hidrolisis yaitu rasio air terhadap selulosa mikrobial, konsentrasi asam sulfat (katalis), waktu dan suhu proses hidrolisis. Variabel respon yang diamati adalah kadar asetil selulosa diasetat yang dihasilkan.
Larutan selulosa triasetat yang akan dihidrolisis dibuat berdasarkan
kondisi optimum proses pembuatan selulosa triasetat yang diperoleh pada
penelitian tahap pertama yaitu sebanyak 5 gram serbuk selulosa mikrobial
direndam dalam 40 ml asam asetat pada suhu 50 oC selama 6 jam. Selanjutnya ditambahkan anhidrida asetat sebanyak 16,75 ml, asam asetat 22,5 ml dan asam
sulfat 0,075 ml. Proses asetilasi dilakukan pada suhu 50 oC selama 323 menit.
Penentuan Taraf Faktor Suhu dan Waktu Hidrolisis
Sebelum dilakukan optimasi proses hidrolisis dengan menggunakan
Metoda Permukaan Respon - Rancangan Komposit Pusat terlebih dahulu dilakukan percobaan untuk menentukan nilai taraf rendah, tengah dan tinggi untuk faktor suhu dan waktu hidrolisis. Percobaan dilakukan dengan cara
dan 10 jam. Katalis asam sulfat ditambahkan sebanyak 0,075 ml (1,5 % dari
bobot kering selulosa mikrobial yang digunakan) sedangkan air ditambahkan
sebanyak 5 ml (rasio air terhadap selulosa mikrobial sebesar 1). Pengukuran kadar
asetil selulosa diasetat yang dihasilkan dilakukan dengan metoda ASTM D
871-96 (Lampiran 1g). Selulosa diasetat yang diharapkan dapat diperoleh pada
penelitian ini adalah selulosa diasetat yang mempunyai kadar asetil berkisar 37 –
42%. Penentuan nilai taraf rendah dan tinggi dilakukan berdasarkan nilai kadar
asetil selulosa diasetat yang diperoleh yaitu kondisi hidrolisis yang dapat
menghasilkan selulosa diasetat de ngan kadar asetil berkisar 37 – 42%.
Proses Hidrolisis Selulosa Triasetat (modifikasi Malm dan Tanghe, 1953)
Sebanyak 5 g serbuk selulosa mikrobial direndam dalam 40 ml asam
asetat glasial pada suhu 50 oC selama 6 jam. Selanjutnya ditambahkan anhidrida asetat sebanyak 16,75 ml (rasio anhidrida asetat terhadap selulosa mikrobial
sebesar 3,35), asam asetat 22,5 ml dan asam sulfat 0,075 ml (konsentrasi katalis
1,5%). Proses asetilasi dilakukan pada suhu 50 oC selama 323 menit. Larutan selulosa tr iasetat yang diperoleh selanjutnya dihidrolisis.
Proses hidrolisis selulosa triasetat dilakukan dengan cara menambahkan
air sebanyak 1,70, 3,35, 5, 6,65, 8,30 ml (rasio air dengan selulosa mikrobial
sebesar 0,34, 0,67, 1, 1,33, 1.66). Pencampuran air de ngan larutan selulosa
triasetat tidak dapat dilakukan secara langsung tetapi dilakukan setelah terlebih
dahulu air dicampur dengan asam asetat dengan perbandingan antara air dengan
asam asetat sebesar 1:2 atau hingga diperoleh larutan asam asetat 66,67%. Katalis
1%, 1,5%, 2%, 2,5%). Pencampuran air dan katalis dengan larutan selulosa
triasetat dilakukan dengan menggunakan pengaduk bermagnet. Selanjutnya proses
hidrolisis selulosa triasetat dilakukan dalam penangas air bergoyang pada suhu
30, 40, 50, 60, dan 70 oC selama 120, 360, 600, 840 dan 1080 menit. Penghentian proses hidrolisis dilakukan dengan menambahkan 20 ml larutan MgCO3 1%
dalam asam asetat. Selanjutnya dilakukan sentrifugasi terhadap cairan hasil
hidrolisis pada kecepatan 3000 rpm selama 15 menit pada suhu 20 oC. Untuk memisahkan selulosa diasetat dari larutannya dilakukan proses pengendapan
dengan cara menuangkan larutan hasil hidrolisis kedalam larutan asam asetat 10
% diatas pengaduk bermagnet. Gumpalan selulosa diasetat yang diperoleh
selanjutnya direndam dalam larutan MgCO3 1%. Perendaman dilakukan selama 2
jam pada suhu kamar. Selanjutnya selulosa diasetat dicuci dengan air hingga
bersih dan dikeringkan pada suhu 50 oC selama 6 jam. Selulosa diasetat kering yang diperoleh disimpan dalam wadah yang tertutup rapat. Pengukuran kadar
asetil selulosa diasetat hasil hidrolisis dilakukan dengan metoda ASTM D 871-96
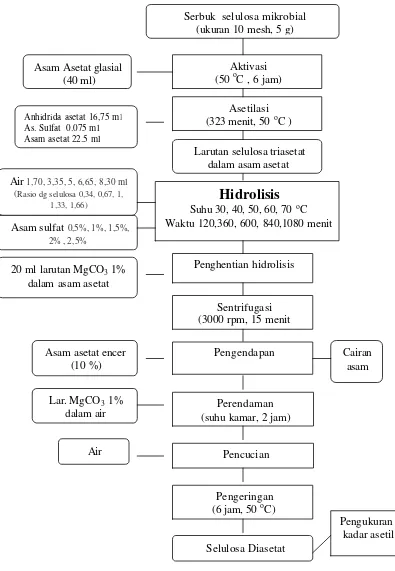
(Lampiran 1g). Diagram alir proses pembuatan selulosa diasetat dapat dilihat pada
Gambar 8.
Penentuan Faktor yang Berpengaruh
Terdapat 4 variabel bebas yang dicobakan pada tahap hidrolisis ini yaitu 1. Rasio air terhadap selulosa mikrobial dengan taraf 0,34 , 0,67 , 1 , 1,33 , 1,66 2. Konsentrasi asam sulfat (katalis) dengan taraf 0,5%, 1%, 1,5%, 2% , 2,5% 3. Waktu hidrolisis dengan taraf 120, 360, 600, 840, 1080 menit
4. Suhu hidrolisis dengan taraf 30, 40, 50, 60, 70 oC.
Gambar 8. Diagram alir penelitian pembuatan selulosa diasetat (modifikasi Malm dan Tanghe, 1953)
Selulosa Diasetat
Hidrolisis
Suhu 30, 40, 50, 60, 70 oC Waktu 120,360, 600, 840,1080 menit
Asam asetat encer (10 %) 20 ml larutan MgCO3 1%
dalam asam asetat Asam sulfat 0,5%, 1%, 1,5%,
2% , 2,5%
Pengendapan
Pengeringan (6 jam, 50 oC)
Perendaman (suhu kamar, 2 jam)
Sentrifugasi (3000 rpm, 15 menit Penghentian hidrolisis Larutan selulosa triasetat
dalam asam asetat
Lar. MgCO3 1%
dalam air Cairan asam Pencucian Air Pengukuran kadar asetil Air1,70, 3,35, 5, 6,65, 8,30 ml
(Rasio dg selulosa 0,34, 0,67, 1,
1,33, 1,66)
Aktivasi (50 oC , 6 jam)
Anhidrida asetat 16,75 ml As. Sulfat 0.075 ml Asam asetat 22.5 ml
Asam Asetat glasial (40 ml)
Asetilasi (323 menit, 50 oC ) Serbuk selulosa mikrobial
Pembentukan dan Pengujian Model
Model regresi kadar asetil selulosa diasetat dibuat berdasarkan data kadar asetil selulosa diasetat yang dihasilkan pada proses hidrolisis. Pada tahap pertama dilakukan pembentukan model linier dengan menggunakan data kadar asetil hasil hidrolisis pada rancangan titik faktoria l dan titik pusat. Tahap kedua dilakukan pembentukan model kuadratik dengan menggunakan tambahan data pada titik bintang. Pengujian terhadap model regresi yang dihasilkan meliputi uji penyimpangan model (lack of fit), uji R2 , uji signifikan model, da n uji asumsi residual (Box et al., 1978 ; Box dan Draper, 1987 ; Gaspersz, 1995 ; Montgomery
et al., 2001 ; Edgar et al., 2001) .
Penentuan Kondisi Optimum Proses Hidrolisis
Penentuan kondisi optimum proses hidrolisis dilakukan dengan menggunakan analisis kanonik dan analisis plot kontur permukaan respon. Kondisi optimum proses hidrolisis selulosa triasetat yang diperoleh selanjutnya diverifikasi di laboratorium.
Rancangan Percobaan
Percobaan hidrolisis dilakukan dengan menggunakan Metoda Permukaan Respons – Rancangan Komposit Pusat. Terdapat 4 variabel bebas yang dicobakan yaitu (1) rasio air terhadap selulosa mikrobial yang dikodekan sebagai X1, (2) waktu hidrolisis yang dikodekan sebagai X2, (3) jumlah H2SO4
dikodekan sebagai X4. Faktor, kode dan taraf kode yang dicobakan dapat dilihat
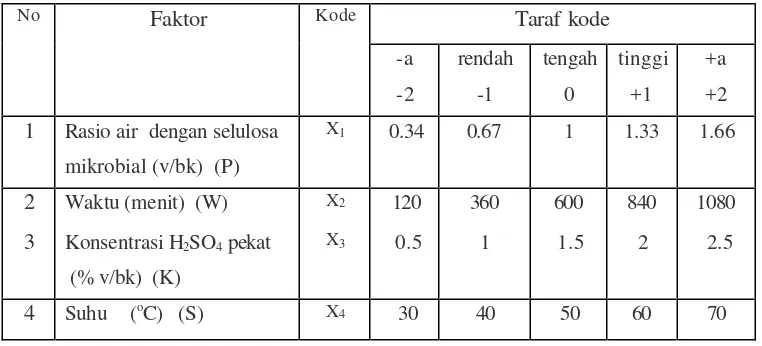
[image:36.612.123.504.180.353.2]pada Tabel 8.
Tabel 8. Faktor, kode dan taraf kode pada proses hidrolisis Taraf kode
No Faktor Kode
-a -2 rendah -1 tengah 0 tinggi +1 +a +2
1 Rasio air dengan selulosa
mikrobial (v/bk) (P)
X1 0.34 0.67 1 1.33 1.66
2 Waktu (menit) (W) X2 120 360 600 840 1080
3 Konsentrasi H2SO4 pekat
(% v/bk) (K)
X3 0.5 1 1.5 2 2.5
4 Suhu (oC) (S) X4 30 40 50 60 70
Konversi nilai taraf aktual menjadi nilai taraf kode dilakukan dengan cara seperti berikut :
X1 = (P -1) X2 = (W-600) X3 = (K- 1.5) X4 = (S-50)
0.33 240 0,5 10
X1 = nilai kode rasio pereaksi P = rasio air aktual (v/bk)
X2 = nilai kode waktu reaksi W = waktu reaksi aktual (menit)
X3 = nilai kode konsentrasi katalis K = konsentrasi katalis aktual (%v/bk)
X4 = nilai kode suhu reaksi S = suhu reaksi aktual (oC)
point) dengan faktor dapat putar (a) sebesar ±2 k/4 dimana k adalah jumlah faktor. Matriks rancangan percobaan dengan 4 faktor ini dapat dilihat pada Tabel 9.
Tabel 9. Matriks rancangan percobaan 4 faktor pada proses hidrolisis
Rasio air terhadap selulosa (v/bk) Waktu (menit) Kons. Asam sulfat (%v/bk) Suhu ( oC)
Nilai kode Kadar asetil Selulosa Disetat Rancangan percobaan
No X1 X2 X3 X4 X1 X2 X3 X4 (%)
1 0.67 360 1 40 -1 -1 -1 -1
2 1.33 360 1 40 1 -1 -1 -1
3 0.67 840 1 40 -1 1 -1 -1
4 1.33 840 1 40 1 1 -1 -1
5 0.67 360 2 40 -1 -1 1 -1
6 1.33 360 2 40 1 -1 1 -1
7 0.67 840 2 40 -1 1 1 -1
8 1.33 840 2 40 1 1 1 -1
9 0.67 360 1 60 -1 -1 -1 1
10 1.33 360 1 60 1 -1 -1 1
11 0.67 840 1 60 -1 1 -1 1
12 1.33 840 1 60 1 1 -1 1
13 0.67 360 2 60 -1 -1 1 1
14 1.33 360 2 60 1 -1 1 1
15 0.67 840 2 60 -1 1 1 1
Titik Faktorial
16 1.33 840 2 60 1 1 1 1
17 1 600 1.5 50 0 0 0 0
18 1 600 1.5 50 0 0 0 0
19 1 600 1.5 50 0 0 0 0
20 1 600 1.5 50 0 0 0 0
21 1 600 1.5 50 0 0 0 0
Titik pusat
22 1 600 1.5 50 0 0 0 0
23 0.34 600 1.5 50 -2 0 0 0
24 1.66 600 1.5 50 +2 0 0 0
25 1 120 1.5 50 0 -2 0 0
26 1 1080 1.5 50 0 +2 0 0
27 1 600 0.5 50 0 0 -2 0
28 1 600 2.5 50 0 0 +2 0
29 1 600 1.5 30 0 0 0 -2
Titik Bintang
Penelitian III. Pembuatan dan Karakterisasi Membran Ultrafiltrasi dari Selulosa Diasetat Mikrobial
Selulosa Diasetat Mikrobial (SDM) yang digunakan sebagai polimer pada
pembuatan membran ultrafiltrasi (UF) adalah selulosa diasetat yang dibuat pada
penelitian tahap kedua dan sebagai pembanding digunakan selulosa diasetat
komersial. Pembuatan membran ultrafiltrasi dilakukan dengan metoda inversi
fasa presipitasi imersi, menggunakan dimetil formamida seba gai pelarut dan air
sebagai non pelarut (Sivakumar et al., 1998). Selulosa diasetat mikrobial yang
digunakan mempunyai kadar asetil 37,14%, 38,11%, 39,19% dan 40,22%.
Konsentrasi selulosa diasetat dalam larutan cetak berkisar 12% – 20 %. Suhu air
koagulasi yang digunakan berkisar 2 – 26 oC. Penelitian pembuatan membran UF dari selulosa diasetat mikrobial ini dilakukan dalam dua tahap yaitu (1) pengaruh
kadar asetil selulosa diasetat dan konsentrasi selulosa diasetat dalam larutan cetak
terhadap karakteristik membran UF dan (2) pengaruh suhu air koagulasi terhadap
karakteristik membran UF yang dihasilkan.
Pembuatan Membran Ultrafiltrasi (Sivakumar et al., 1998)
Pembuatan membran dilakukan dengan menggunakan metoda inversi fasa-
presipitasi imersi. Jumlah selulosa diasetat dan dimetil formamida yang
digunakan pada setiap percobaan adalah 30 gram. Selulosa diasetat mikrobial
ditimbang sesuai konsentrasi yang ditetapkan (12% , 14%, 16%, 18% dan 20%)
kemudian dimasukkan kedalam labu erlenmeyer. Selanjutnya ditambahkan pelarut
campuran diaduk dengan menggunakan pengaduk bermagnet pada suhu kamar
selama satu hari hingga semua selulosa diasetat larut dalam DMF. Larutan
selulosa diasetat selanjutnya disimpan selama 2 hari untuk mengeluarkan
gelembung-gelembung udara. Larutan yang diperoleh disebut dope atau larutan
cetak.
Pencetakan membran dilakukan dengan cara menuangkan larutan dope di
atas plat kaca yang dilengkapi pisau casting (aplikator), lalu aplikator ditarik
hingga membentuk lapisan tipis dan dibiarkan selama 30 detik. Ketinggian pisau
aplikator diatur pada ketinggian 0,2 mm. Setelah dibiarkan selama 30 detik,
lembaran kaca dimasukkan kedalam bak koagulasi yang berisi air aquades suhu
10 oC . Selanjutnya lembaran tipis yang terbentuk direndam dalam air aquades selama satu hari untuk menghilangkan sisa DMF. Lembaran membran yang
diperoleh dipotong sesuai ukuran cetakan (modul) filtrasi yang tersedia.
Membran yang sudah dipotong disimpan dalam larutan formalin 1%. Diagram alir
pembuatan membran ultrafiltrasi dapat dilihat pada Gambar 9.
Pengujian terhadap karakteristik membran yang dihasilkan meliputi
pengukuran permeabilitas (fluk air, fluks albumin, fluks dekstran) dan selektifitas
(rejeksi albumin dan dekstran). Umpan yang digunakan adalah larutan bovin
serum albumin dengan bobot molekul 67 kDa dan larutan dekstran dengan bobot
molekul 37 kDa. Prosedur pengukuran fluks air, fluks dan rejeksi membran
terhadap umpan dapat dilihat pada Lampiran 1h dan 1i. Pengujian dilakukan
dengan metoda penyaringan aliran silang (cross-flow filtration). Pengamatan
terhadap morfologi dan ukuran pori membran dilakukan dengan menggunakan
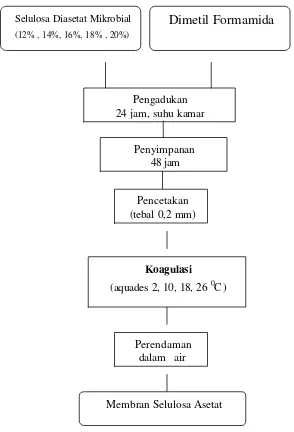
Gambar 9. Diagram alir proses pembuatan membran selulosa diasetat
(Modifikasi Sivakumar et al., 1998) Pengadukan 24 jam, suhu kamar
Penyimpanan 48 jam
Pencetakan (tebal 0,2 mm)
Perendaman dalam air
Koagulasi
(aquades 2, 10, 18, 26 0C) Selulosa Diasetat Mikrobial
(12% , 14%, 16%, 18% , 20%)
Dimetil Formamida
Rancangan Percobaan
Percobaan pembuatan membran ini dilakukan dua tahap. Tahap pertama
dilakukan pembuatan membran dari selulosa diasetat dengan kadar asetil berbeda
yaitu 37,21%, 38,11%, 39,19%, 40,22% dengan konsentrasi selulosa diasetat
dalam larutan cetak sebesar 12%, 14%, 16%, 18%, 20%. Pembuatan membran
dilakukan pada suhu air koagulasi tetap (10 oC). Tahap kedua dilakukan pembuatan membran pada suhu air koagulasi berbeda yaitu 2, 10, 18 dan 26 oC menggunakan selulosa diasetat kadar asetil 39,19 % dan konsentrasi selulosa
diasetat dalam larutan cetak tetap yaitu 18%.
Rancangan percobaan yang digunakan pada penelitian pembuatan membran
ultrafiltrasi tahap pertama adalah Rancangan Acak Lengkap Faktorial. yang terdiri
dari dua faktor dan dua kali ulangan. Faktor pertama (A) adalah kadar asetil
selulosa diasetat mikrobial (SDM) terdiri atas 4 taraf yaitu 37,21 %, 38,11 %,
39,19 % dan 40,22 %. Faktor kedua (B) adalah konsentrasi selulosa diasetat
mikrobial terdiri atas 5 taraf yaitu 12% , 14%, 16%, 18% dan 20%. Komposisi
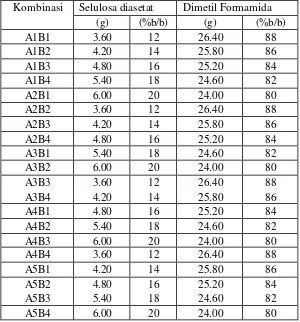
Tabel 10. Komposisi larutan cetak pada pembuatan membran
Kombinasi Selulosa diasetat Dimetil Formamida
(g) (%b/b) (g) (%b/b)
A1B1 3.60 12 26.40 88
A1B2 4.20 14 25.80 86
A1B3 4.80 16 25.20 84
A1B4 5.40 18 24.60 82
A2B1 6.00 20 24.00 80
A2B2 3.60 12 26.40 88
A2B3 4.20 14 25.80 86
A2B4 4.80 16 25.20 84
A3B1 5.40 18 24.60 82
A3B2 6.00 20 24.00 80
A3B3 3.60 12 26.40 88
A3B4 4.20 14 25.80 86
A4B1 4.80 16 25.20 84
A4B2 5.40 18 24.60 82
A4B3 6.00 20 24.00 80
A4B4 3.60 12 26.40 88
A5B1 4.20 14 25.80 86
A5B2 4.80 16 25.20 84
A5B3 5.40 18 24.60 82
A5B4 6.00 20 24.00 80
A1= Selulosa diasetat kadar asetil 37,21%
A2= Selulosa diasetat kadar asetil 38,11%
A3= Selulosa diasetat kadar asetil 39,19%
A4= Selulosa diasetat kadar asetil 40,22%
A5= Selulosa diasetat komersial
B1= konsentrasi selulosa diasetat dalam larutan cetak 12%
B2= konsentrasi selulosa diasetat dalam larutan cetak 14%
B3= konsentrasi selulosa diasetat dalam larutan cetak 16%
B4= konsentrasi selulosa diasetat dalam larutan cetak 18%
Model matematika untuk rancangan acak lengkap faktorial 2 faktor adalah
sebagai berikut (Sudjana, 1994) :
Y ijk = µ + Ai + Bj + ABij + Ek(ij)
Y ijk = hasil percobaan akibat peubah kadar asetil ke-i dan
konsentrasi selulosa diasetat ke-j
µ = nilai rata-rata sebenarnya
Ai = pengaruh peubah kadar asetil ke-i (i = 1, 2, 3, 4)
Bj = pengaruh peubah konsentrasi selulosa diasetat ke -j (j = 1, 2, 3,4,5)
ABij = pengaruh interaksi peubah kadar asetil ke -i dengan
konsentrasi selulosa diasetat ke-j
Ek(ij) = galat percobaan ke-k
Rancangan percobaan yang digunakan pada penelitian pembuatan
membran ultrafiltrasi tahap kedua adalah Rancangan Acak Lengkap Faktorial
yang terdiri dari satu faktor dengan dua kali ulangan. Faktor suhu air koagulasi
(A) terdiri atas 4 taraf yaitu 2, 10, 18 dan 26 oC.
Model matematika untuk Rancangan Acak Lengkap Faktorial satu faktor
adalah sebagai berikut (Sudjana, 1994) :
Y ijk = µ + Ai + Ek(ij)
Y ijk = hasil percobaan akibat peubah suhu air koagulasi ke-i
µ = nilai rata-rata sebenarnya
Ai = pengaruh peubah suhu air koagulasi ke -i (i = 1, 2, 3, 4)
Penelitian I.
Optimasi Proses Asetilasi pada Pembuatan Selulosa Triasetat dari Selulosa Mikrobial
Selulosa mikrobial kering yang digunakan pada penelitian ini berukuran
10 mesh dan berwarna putih kekuningan. Rasio bobot selulo sa mikrobial kering
terhadap selulosa mikrobial basah adalah sekitar 0,0984 – 0.1113. Hasil analisis
[image:44.612.178.460.355.478.2]proksimat serbuk selulosa mikrobial yang digunakan dapat dilihat pada Tabel 11.
Tabel 11. Hasil analisis proksimat serbuk selulosa mikrobial kering
Parameter analisis Nilai (%)
Kadar air 3,50
Kadar abu 0,23
Kadar protein (bk) 3,50
Kadar lemak (bk) 1,14
Kadar selulosa (bk) 92,53
Serbuk selulosa mikrobial yang digunakan pada penelitian ini mempunyai
kandungan selulosa yang relatif tinggi yaitu le bih dari 90% sehingga baik untuk
digunakan sebagai sumber selulosa pada pembuatan selulosa triasetat.
Dibandingkan dengan selulosa kayu, penggunaan selulosa mikrobial sebagai
sumber selulosa relatif lebih menguntungkan karena selain selulosa mikrobial
mempunyai kandungan selulosa yang relatif tinggi juga karena tidak terdapat
Menurut Fengel dan Wegener (1984) pada pulp kayu terdapat senyawa
yang bukan selulosa seperti lignin dan hemiselulosa. Hemiselulosa merupakan
heteropolimer sedangkan selulosa merupakan homopolimer. Pada proses
asetilasi akan terjadi reaksi antara senyawa-senyawa kelompok hemiselulosa
dengan anhidrida asetat. Hal ini akan mengakibatkan selulosa triasetat yang
dihasilkan tidak murni karena tercampur dengan hemiselulosa asetat seperti
glukomanan asetat.
Serbuk selulosa mikrobial yang digunakan sebagai sumber selulosa pada
proses pembuatan selulosa triasetat ini mempunyai kadar air yang relatif rendah
yaitu 3,50%, seperti terlihat pada Tabel 11. Kandungan air yang tinggi pada
selulosa yang akan diasetilasi tidak diinginkan. Pada proses asetilasi air yang
terdapat dalam selulosa akan bereaksi dengan anhidrida asetat membentuk asam
asetat. Hal ini akan menyebabkan jumlah anhidrida asetat yang akan bereaksi
dengan selulosa menjadi lebih sedikit. Menurut Pine et al. (1980) secara teoritis 1 mol air akan bereaksi dengan 1 mol anhidrida asetat menghasilkan 2 mol asam asetat. Rendahnya kadar air pada selulosa mikrobial yang digunakan pada penelitian ini relatif menguntungkan karena kadar air yang rendah akan
mengurangi jumlah anhidrida asetat yang dibutuhkan pada proses asetilasi
selulosa menjadi selulosa triasetat.
Selulosa mikrobial yang digunakan pada penelitian ini juga mempunyai
kadar abu yang relatif rendah yaitu 0,23%. Hal ini juga menguntungkan karena
dengan mengendalikan proses pembuatannya seperti tidak menggunakan peralatan
dari logam maka selulosa triasetat yang akan dihasilkan pada proses asetilasi
Penentuan Kondisi Aktivasi Selulosa Mikrobial
Proses aktivasi selulosa bertujuan untuk menggembungkan selulosa
sehingga dapat meningkatkan reaktifitas dan aksesibilitas selulosa. Proses
aktivasi dapat mempercepat terjadinya pertukaran gugus hidroksil molekul
selulosa dengan gugus asetil dari anhidrida asetat. Hasil perolehan selulosa
triasetat (STA) pada berbagai kondisi aktivasi yang dicobakan dapat dilihat pada
[image:46.612.192.445.299.456.2]Tabel 12 sedangkan data selengkapnya dapat dilihat pada Lampiran 2a.
Tabel 12. Perolehan selulosa triasetat pada berbagai kondisi aktivasi
Suhu aktivasi Waktu (jam) Perolehan (g/g)
0 1.20
2 1.48
4 1.60
6 1.63
50 oC
8 1.63
4 1.30
8 1.45
12 1.54
Suhu kamar
16 1.63
Hasil pengukuran perolehan selulosa triasetat (Tabel 12) menunjukkan
perolehan selulosa triasetat cenderung meningkat dengan semakin lama waktu
aktivasi baik pada suhu 50 oC maupun pada suhu kamar. Diduga hal ini disebabkan oleh perendaman serbuk selulosa mikrobial dalam waktu yang lebih
lama dapat menjadikan serat selulosa lebih menggembung (swelling) sehingga
memudahkan masuknya pereaksi.
Kondisi aktivasi selulosa mikrobial yang menghasilkan perolehan selulosa
mikrobial pada penelitian ini relatif lebih lama dibandingkan waktu aktivasi pulp
kayu yang dilakukan oleh Saka dan Takanashi (1998) pada pembuatan selulosa
triasetat dari pulp kayu yaitu selama satu jam. Nevel dan Zeronian (1985)
menyatakan aktivasi selulosa pulp kayu umumnya dilakukan kira-kira selama 1-2
jam. Lama waktu aktivasi yang dicobakan pada penelitian ini jauh lebih rendah
dibandingkan dengan lama waktu aktivasi selulosa mikrobial yang dilakukan oleh
Tabuchi et al. (1998) yaitu 72 jam pada suhu kamar.
Kuo et al. (1997) menyatakan waktu aktivasi selulosa bergantung pada
jenis selulosa yang digunakan. Waktu aktivasi selulosa mikrobial yang lebih lama
pada penelitian ini diduga terjadi karena perbedaan sifat kristalinitas selulosa
mikrobial dengan selulosa dari kayu. Selulosa mikrobial mempunyai daerah
kristalin yang lebih besar dibandingkan daerah amorf. White dan Brown (1988)
menyatakan bahwa selulosa mikrobial bersifat kristalin, dengan derajat
kristalinitas lebih besar dari 60 %, yang berarti lebih banyak terdapat daerah
kristalin dibandingkan daerah amorf.
Daerah kristalin merupakan bagian yang mempunyai ikatan antar rantai
lebih erat dan lebih rapat (Achmadi, 1990). Daerah kristalin mempunyai sifat
reaktifitas yang rendah, sehingga sukar terjadi reaksi asetilasi, sedangkan bagian
amorf merupakan bagian yang lebih mudah dicapai oleh pereaksi sehingga lebih
reaktif. Agar daerah kristalin dapat dicapai oleh pereaksi perlu dilakukan
penggembungan (swelling) selulosa dengan menggunakan pelarut. Semakin besar
daerah kristalin suatu selulosa maka semakin lama waktu yang dibutuhkan untuk
menggembungkannya. Penggembungan selulosa akan menyebabkan
pereaksi. Semakin lama waktu aktivasi maka semakin banyak asam asetat yang
masuk diantara serat selulosa. Keadaan ini menyebabkan reaksi asetilasi lebih
mudah terjadi.
Penentuan Faktor-faktor yang Berpengaruh Terhadap Perolehan STA
Proses asetilasi selulosa bertujuan untuk menggantikan sebagian atau
semua gugus hidroksil (OH) pada molekul selulosa dengan gugus asetil (CH3CO)
dari anhidrida asetat sehingga membentuk selulosa asetat. Selulosa memiliki 3
gugus hidroksil per residu anhidroglukosa sehingga memungkinkan untuk
menghasilkan selulosa asetat dalam bentuk monoasetat, diasetat dan triasetat.
Selama proses asetilasi diharapkan semua selulosa mikrobial dapat dikonversi
menjadi selulosa triasetat. Perolehan selulosa triasetat pada penelitian ini
dihitung dengan cara membandingkan bobot kering selulosa triasetat yang
diperoleh dengan bobot kering selulosa mikrobial yang digunakan (bk/bk).
Perolehan selulosa triasetat pada tahap ini dapat dilihat pada Tabel 13.
Hasil penelitian pada rancangan faktorial dan titik pusat menunjukkan
respon perolehan selulosa triasetat yang dihasilkan berkisar antara 0,80 – 1.70 (g/g), seperti terlihat pada Tabel 13. Secara umum bobot kering selulosa triasetat yang dihasilkan pada penelitian ini cenderung lebih besar dari bobot selulosa mikrobial yang digunakan. Hal ini terjadi karena bobot molekul selulosa triasetat yang dihasilkan lebih besar daripada bobot molekul selulosa mikrobial yang digunakan.
Tabel 13. Perolehan selulosa triasetat pada tahap penentuan faktor -faktor yang berpengaruh pada proses asetilasi
No Konsentrasi Rasio Waktu Suhu Perolehan
katalis pereaksi (menit) Reaksi X1 X2 X3 X4 Selulosa
(%) (X1) (X2) (X3) (oC)(X4) triasetat (g/g)
1 0.5 2 240 40 -1 -1 -1 -1 0.85
2 0.5 4 240 40 1 -1 -1 -1 0.80
3 0.5 2 360 40 -1 1 -1 -1 1.36
4 0.5 4 360 40 1 1 -1 -1 1.66
5 1.5 2 240 40 -1 -1 1 -1 1.38
6 1.5 4 240 40 1 -1 1 -1 1.38
7 1.5 2 360 40 -1 1 1 -1 1.69
8 1.5 4 360 40 1 1 1 -1 1.70
9 0.5 2 240 60 -1 -1 -1 1 0.81
10 0.5 4 240 60 1 -1 -1 1 1.52
11 0.5 2 360 60 -1 1 -1 1 1.67
12 0.5 4 360 60 1 1 -1 1 1.70
13 1.5 2 240 60 -1 -1 1 1 1.57
14 1.5 4 240 60 1 -1 1 1 1.53
15 1.5 2 360 60 -1 1 1 1 1.63
16 1.5 4 360 60 1 1 1 1 1.67
17 1 3 300 50 0 0 0 0 1.67
18 1 3 300 50 0 0 0 0 1.68
19 1 3 300 50 0 0 0 0 1.68
20 1 3 300 50 0 0 0 0 1.69
Selulosa merupakan polimer linier glukosa yang unit-unitnya terikat
dengan ikatan 1,4-β-D glukopiranosa. Bila diasumsikan satu molekul selulosa
terdiri atas n unit glukosa maka secara teoritis pada reaksi asetilasi sempurna , setiap 1 mol selulosa membutuhkan 3n mol anhidrida asetat dan akan menghasilkan 1 mol selulosa triasetat dan 3n mol asam asetat.
memiliki rumus empirik [C6H7O2(CH3CO)3]n. Bila diasumsikan bobot molekul
selulosa mikrobial (C6H7O2( OH)3 )n adalah 162n gram/mol dan bobot molekul
selulosa triasetat adalah 288n gram/mol maka setiap 1 gram selulosa mikrobial (setara dengan 0,0062/n mol selulosa mikrobial) akan menghasilkan 0,0062/n mol selulosa triasetat atau setara dengan 1,79 gram selulosa triasetat. Bila reaksi asetilasi selulosa berlangsung sempurna dan tidak terjadi degradasi selulosa maka dari setiap satu gram selulosa yang digunakan akan diperoleh selulosa triasetat sebanyak 1,79 gram.
Hasil analisis keragaman terhadap perolehan selulosa triasetat (Lampiran 2b) menunjukkan faktor rasio anhidrida asetat dengan selulosa mikrobial berpengaruh secara sangat nyata (a = 0,0044) terhadap perolehan selulosa triasetat sedangkan faktor waktu asetilasi berpengaruh nyata (a = 0,0128) terhadap
perolehan selulosa triasetat. Konsentrasi asam sulfat dan suhu asetilasi tidak
berpengaruh nyata (a > 0,05) terhadap perolehan selulosa triasetat.
Penambahan katalis asam sulfat pada proses asetilasi bertujuan untuk
mempercepat terjadinya reaksi antara gugus hidroksil pada selulosa dengan
anhidrida asetat. Penambahan katalis pada reaksi asetilasi akan menurunkan
energi aktivasi reaksi sehingga pada waktu yang sama lebih banyak produk yang
diperoleh. Energi aktivasi adalah jumlah energi yang dibutuhkan agar molekul
yang bertabrakan mencapai keadaan transisi (Fesseden dan Fesseden , 1983: Pine
et al., 1988). Pada penelitian ini faktor konsentrasi asam sulfat yang dicobakan
pada proses asetilasi tidak berpengaruh nyata terhadap perolehan selulosa
triasetat. Keadaan ini berbeda dengan yang dinyatakan oleh Ott et al. (1954)
reaksi asetilasi. Diduga hal ini terjadi karena konsentrasi katalis yang diujikan
relatif kecil (kurang dari 2%). Menurut Nevel dan Zeronian (1985) pada produksi
selulosa triasetat dari pulp kayu secara komersial umumnya digunakan katalis
dalam konsentrasi tinggi yaitu 7 – 10%. Pemilihan konsentrasi katalis lebih kecil
dari 2 % dengan beda antara taraf rendah, tengah dan tinggi sebesar 0,5%
dilakukan karena selulosa triasetat yang ingin diperoleh pada penelitian ini
diharapkan mempunyai bobot molekul yang relatif tinggi. Menurut Ott et al.
(1954) dan Kuo et al. (1997) penambahan asam sulfat dalam jumlah banyak
dapat menyebabkan terjadinya kerusakan pada molekul selulosa. Penambahan
asam sulfat dalam jumlah banyak pada selulosa dapat menyebabkan terjadi reaksi
hidrolisis yang mengakibatkan terjadi pemutusan rantai selulosa. Hal ini akan
menyebabkan selulosa triasetat yang dihasilkan mempunyai kekuatan mekanik
rendah (rapuh). Selulosa triasetat yang ingin diperoleh pada penelitian ini adalah
selulosa triasetat yang mempunyai derajat polimerisasi tinggi.
Perlakuan suhu asetilasi yang dicobakan pada penelitian ini juga tidak
berpengaruh nyata terhadap perolehan selulosa triasetat. Hal ini diduga terjadi
suhu yang dicobakan relatif rendah dan beda antara suhu taraf rendah, tengah dan
tinggi relatif kecil (40, 50, 60 oC). Pemilihan suhu asetilasi pada penelitian ini dibatasi tidak lebih besar dari 60 oC. Hal ini dilakukan untuk mengurangi kemungkinan terjadi degradasi molekul selulosa selama proses asetilasi sehingga
selulosa triasetat yang dihasilkan diharapkan mempunyai sifat mekanik yang
relatif tinggi. Menurut Nevel dan Zeronian (1985) proses asetilasi pada suhu
kerusakan pada selulosa. Kuo et al. (1997) menyatakan proses asetilasi selulosa
sebaiknya dilakukan pada suhu berkisar 50 – 85 oC.
Reaksi asetilasi pada pembuatan selulosa triasetat mer upakan reaksi
subsitusi. Menurut Pine et al. (1988) peningkatan suhu pada suatu reaksi kimia
bertujuan meningkatkan energi kinetik molekul-molekul yang bereaksi sehingga
molekul–molekul tersebut bergerak lebih cepat akibatnya tumbukan antar molekul
lebih banyak terjadi. Keadaan ini menyebabkan molekul-molekul tersebut
mempunyai energi yang cukup untuk mencapai keadaan transisi.
Pembentukan Model Linier Perolehan Selulosa Triasetat
Hasil pembentukan model tahap pertama dengan menggunakan data
perolehan pada rancangan faktorial dan titik pusat menunjukkan model perolehan
selulosa triasetat tidak merupakan persamaan linier tetapi cenderung kuadratik.
Parameter dan koefisien parameter pembentuk model linier perolehan selulosa
triasetat dapat dilihat pada Lampiran 2c.
Hasil uji penyimpangan model linier bersifat sangat nyata dengan nilai
peluang 0,0014 (Lampiran 2d). Hal ini berarti model linier yang dibuat
menyimpang dari keadaan nyata. Meskipun model ini mempunyai koefisien
determinan relatif tinggi (R2 = 0,9264), namun model yang dihasilkan tidak dapat digunakan karena tidak memenuhi syarat model yang baik. Menurut Box et al.
(1978) dan Gaspersz (1995) syarat model yang baik mempunyai hasil uji
Pembentukan Model Kuadratik Perolehan Selulosa Triasetat
Pembuatan model kuadratik dilakukan hanya dengan menggunakan
peubah yang berpengaruh nyata atau sangat nyata terhadap respon perolehan
selulosa triasetat yaitu peubah rasio pereaksi anhidrida asetat terhadap selulosa
mikrobial yang digunakan dan waktu reaksi asetilasi. Respon perolehan se