PEMBUATAN BIOFILM SELULOSA ASETAT DARI
SELULOSA MIKROBIAL
NATA DE CASSAVA
TUTUS KURYANI
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Pembuatan Biofilm Selulosa Asetat dari Selulosa Mikrobial Nata de cassava adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
TUTUS KURYANI. Pembuatan Biofilm Selulosa Asetat dari Selulosa Mikrobial Nata de cassava. Dibimbing oleh KHASWAR SYAMSU.
Selulosa asetat merupakan senyawa turunan hasil asetilasi selulosa dengan pereaksi asetat anhidrida. Tujuan penelitian ini adalah menghasilkan biofilm selulosa asetat dari selulosa mikrobial nata de cassava. Nata de cassava yang diperoleh melalui fermentasi limbah cair tapioka dengan bantuan bakteri Acetobacter xylinum selama 8 hari dikeringkan dan dihancurkan hingga membentuk serbuk. Serbuk selulosa mikrobial yang diperoleh diaktivasi menggunakan asam asetat glasial, diasetilasi menggunakan pelarut asetat anhidrida dengan perbandingan selulosa:pelarut 1:3, 1:4, dan 1:5 selama 1, 2, dan 3 jam kemudian dihidrolisis menggunakan asam asetat encer. Larutan selulosa asetat diendapkan dengan aquades, dikeringkan lalu dihancurkan hingga terbentuk serbuk selulosa asetat. Serbuk selulosa asetat dilarutkan dalam aseton dan dilakukan penambahan pemlastis gliserin sebanyak 15% dan 25% dari bobot selulosa asetat lalu dicetak menggunakan plat kaca. Selulosa asetat yang terbentuk memiliki kadar asetil antara 30,60-44,51%. Biofilm yang terbentuk memiliki rata-rata kekuatan tarik 320,50 kgf/cm2, elongasi 3,06%, WVTR 461,97 g/m2/24 jam, dan daya serap air 10,52%.
Kata kunci: nata de cassava, selulosa mikrobial, selulosa asetat, biofilm
ABSTRACT
TUTUS KURYANI. Cellulose Acetat Biofilm Production from Microbial Cellulose Nata de Cassava. Supervised by KHASWAR SYAMSU.
Cellulose acetate is one of cellulose derivative produced by acetylation in acetate anhydride reactant. The objectives of this research are to produce cellulose acetate biofilm from microbial cellulose nata de cassava. Nata de cassava as fermentation product of tapioca liquid waste assisted by Acetobacter xylinum for 8 days dried and crushed into powder. Microbial cellulose powder was activated by glacial acetate acid, acetyled in acetate anhydride using ratio 1:3, 1:4, and 1:5 for 1, 2, and 3 hours then hydrolyzed by weak acetate acid. The suspension deposited in aquades, dried then crushed into powder form. Cellulose acetate powder diluted in acetone and added by glycerin then poured into glasses plate. Cellulose acetate has acetyl number between 30,60-44,51%. Biofilm has average tensile strength 320,50 kgf/cm2, elongation 3,06%, WVTR 461,97 g/m2/24 jam, and water absorbing power 10,52%.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Teknologi Industri Pertanian
PEMBUATAN BIOFILM SELULOSA ASETAT DARI
SELULOSA MIKROBIAL
NATA DE CASSAVA
TUTUS KURYANI
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Pembuatan Biofilm Selulosa Asetat dari Selulosa Mikrobial Nata de Cassava
Nama : Tutus Kuryani
NIM : F34090007
Disetujui oleh
Prof. Dr. Ir. Khaswar Syamsu, M.Sc. Pembimbing
Diketahui oleh
Prof. Dr. Ir. Nastiti Siswi Indrasti Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah swt. atas segala karunia-Nya sehingga skripsi yang berjudul Pembuatan Biofilm Selulosa Asetat dari Selulosa Mikrobial Nata de Cassava ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan bulan Maret-Juli 2013 ini ialah teknologi bioindustri.
Terima kasih penulis sampaikan kepada:
1. Prof. Dr. Ir. Khaswar Syamsu, M.Sc. selaku dosen pembimbing atas bimbingan dan motivasi yang diberikan.
2. Dr. Prayoga Suryadarma, S.TP. MT. dan Drs. Purwoko, M.Si. sebagai dosen penguji.
3. Segenap dosen dan staff Departemen Teknologi Industri Pertanian. 4. Segenap laboran Laboratorium TIN yang telah membantu selama proses
penelitian.
5. Pimpinan dan dewan CSR PT. Rabobank International Indonesia atas beasiswa Rabobank Undergraduate Scholarship yang telah diberikan. 6. Bapak Sarino, Ibu Wagiyem, kakak Nanik Sri Suryani, adik Randy
Ardhika Putra, Muhamad Haris, serta seluruh keluarga dan sahabat, atas segala doa dan kasih sayangnya.
7. Teman-teman Pondok Harmoni dan TIN 46 atas kebersamaan yang berkesan, doa, dan semangat yang diberikan.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Manfaat Penelitian 2
Ruang Lingkup Penelitian 3
TINJAUAN PUSTAKA 3
Limbah Cair Tapioka 3
Nata de cassava 4
Selulosa asetat 4
Biofilm dan Bioplastik 5
METODE 6
Alat & Bahan 6
Prosedur Penelitian 6
HASIL DAN PEMBAHASAN 8
Nata de cassava 8
Selulosa asetat 9
Biofilm dan Bioplastik 12
Karakteristik fisik biofilm 13
SIMPULAN DAN SARAN 16
Simpulan 16
Saran 16
DAFTAR PUSTAKA 17
LAMPIRAN 17
DAFTAR TABEL
1 Analisis Proksimat dan Mineral Limbah Cair Tapioka 3 2 Hubungan Kandungan Asetil, Derajat Substitusi, Jenis Pelarut, dan
Kegunaannya 5
3 Analisis Proksimat Serbuk Selulosa Mikrobial Nata de cassava 9 4 Perbandingan Nilai Karakteristik Fisik Selulosa Asetat dari Berbagai
Jenis Selulosa Mikrobial 15
DAFTAR GAMBAR
1 Hubungan Rasio Asetat Anhidrida terhadap Rendemen Selulosa Asetat 11 2 Hubungan Rasio Asetat Anhidrida terhadap Kadar Air Selulosa Asetat 11 3 Hubungan Rasio Asetat Anhidrida terhadap Kadar Asetil Selulosa
Asetat 12
4 Hubungan Kadar Asetil dan Jumlah Pemlastis terhadap Kuat Tarik
Biofilm 13
5 Hubungan Kadar Asetil dan Jumlah Pemlastis terhadap Elongasi
Biofilm 14
6 Hubungan Kadar Asetil dan Jumlah Pemlastis terhadap Laju Transmisi
Uap (WVTR) Biofilm 14
7 Hubungan Kadar Asetil dan Jumlah Pemlastis terhadap Daya Serap Air
Biofilm 15
DAFTAR LAMPIRAN
1 Prosedur Pengujian 19
2 Data Uji Rendemen Selulosa Asetat 21
3 Uji Keragaman Rendemen Selulosa Asetat 21
4 Data Uji Kadar Air Selulosa Asetat 22
5 Uji Keragaman Kadar Air Selulosa Asetat 22
6 Data Uji Kadar Asetil Selulosa Asetat 22
7 Uji Keragaman Kadar Asetil Selulosa Asetat 22
8 Data Uji Kuat Tarik Biofilm 23
9 Uji Keragaman Kuat Tarik Biofilm 23
10 Data Elongasi Tarik Biofilm 23
11 Uji Keragaman Elongasi Biofilm 23
12 Data Laju Transmisi Uap (WVTR) Biofilm 24
14 Data Daya Serap Air Biofilm 24
1
PENDAHULUAN
Latar Belakang
Selulosa asetat merupakan senyawa turunan selulosa yang diperoleh melalui esterifikasi menggunakan pereaksi asetat anhidrida. Selulosa asetat merupakan salah satu jenis polimer yang banyak digunakan untuk industri. Selulosa asetat secara umum dibedakan atas dua jenis yaitu selulosa triasetat (selulosa asetat primer) dan selulosa diasetat (selulosa asetat sekunder). Selulosa asetat primer dibuat melalui reaksi esterifikasi (asetilasi) selulosa dengan pereaksi anhidrida asetat, sedangkan selulosa asetat sekunder dibuat dengan cara menghidrolisis selulosa asetat primer (Desiyarni, 2006)
Secara komersial selulosa asetat dibuat dengan menggunakan bahan baku pulp kayu berkualitas tinggi. Salah satu masalah dalam produksi selulosa asetat dari pulp kayu adalah rendahnya kualitas dan kemurnian selulosa kayu karena pulp kayu masih mengandung hemiselulosa dan lignin. Selulosa mikrobial adalah jenis selulosa yang dihasilkan oleh mikroorganisme. Selulosa mikrobial bersifat renewable (dapat diperbarui), mempunyai karakteristik yang unik dan relatif lebih murni dibandingkan dengan selulosa kayu. Selulosa mikrobial merupakan salah satu alternatif sumber selulosa pada pembuatan selulosa asetat. Selulosa mikrobial mempunyai beberapa keunggulan antara lain relatif murni sehingga tidak membutuhkan proses delignifikasi, sifat hidrofilik yang sangat tinggi dan dapat diproduksi dari berbagai macam substrat yang relatif mudah dan murah. Berdasarkan keunggulan yang dimiliki tersebut maka selulosa jenis ini merupakan alternatif sumber selulosa yang relatif murni pada produksi selulosa asetat.
Penelitian pembuatan selulosa asetat dari selulosa mikrobial telah dilakukan antara lain oleh Safriani (2000), Darwis et al. (2003), dan Sani (2012). Safriani (2000) telah meneliti pembuatan selulosa asetat dari selulosa mikrobial berbahan baku kedelai (nata de soya) dan menggunakan selulosa asetat yang dihasilkan sebagai polimer pada pembuatan coating. Darwis et al. (2003) telah meneliti pembuatan selulosa triasetat dari selulosa mikrobial berbahan baku air kelapa (nata de coco) dan menggunakan selulosa triasetat yang dihasilkan sebagai polimer pada pembuatan membran mikrofiltrasi. Sani (2012) telah meneliti potensi nata de cassava dari limbah cair tapioka sebagai membran selulosa asetat. Safriani (2000) melakukan asetilasi dalam waktu 5, 7,5, dan 10 jam dengan rasio asetat anhidrida 1:2, 1:3, dan 1:4 menghasilkan kadar asetil 14,55-41,72%. Film selulosa asetat yang dihasilkan digunakan sebagai penyaring, kemasan, dan amplop.
2
Perumusan Masalah
Selulosa mikrobial merupakan alternatif sumber selulosa dalam pembuatan selulosa asetat. Selulosa asetat dapat digunakan sebagai bahan pembuatan biofilm yang dapat diaplikasikan sebagai susbstitusi plastik. Kadar asetil selulosa asetat dipengaruhi oleh rasio asetat anhidrida dan waktu asetilasi. Proses asetilasi pada penelitian Safriani (2000) dilakukan dalam waktu 5, 7,5, dan 10 jam dengan rasio asetat anhidrida 1:2, 1:3, dan 1:4 menghasilkan kadar asetil 14,55-41,72%. Sani (2012) melakukan asetilasi dalam waktu 2 jam dengan rasio asetat anhidrida 1:5 menghasilkan kadar asetil 40,38%. Waktu asetilasi dalam penelitian ini dilakukan dalam waktu lebih pendek daripada penelitian sebelumnya untuk mendapatkan kadar asetil yang lebih rendah. Kadar asetil selulosa asetat untuk tujuan biofilm harus mempunyai kadar asetil 36,5-42,2% agar dapat larut dalam pelarut aseton.
Karakteristik fisik biofilm selulosa asetat dipengaruhi oleh kadar asetil yang digunakan dan penambahan pemlastis. Penelitian Safriani (2000) dilakukan dengan menambahkan pemlastis jenis dietilena glikol, dimetil ftalat, dan tributil fosfat dengan konsentrasi 17 dan 25% pada selulosa asetat nata de soya. Pada penelitian ini dilakukan penambahan pemlastis gliserin terhadap selulosa asetat yang dihasilkan. Nilai karakteristik fisik biofilm selulosa asetat diharapkan mendekati nilai karakteristik plastik sintetis yang sudah ada sehingga dapat menjadi substitusi jenis plastik tersebut.
Tujuan Penelitian
Penelitian ini mempunyai tujuan umum untuk mendapatkan selulosa asetat dari selulosa mikrobial yang berasal dari nata de cassava yang diolah secara fermentasi dari limbah cair tapioka sebagai bahan biofilm. Tujuan khusus dari penelitian ini adalah sebagai berikut:
1. Mendapatkan selulosa mikrobial dari limbah cair tapioka dalam bentuk nata de cassava.
2. Mengetahui pengaruh variasi rasio asetat anhidrida dan waktu asetilasi terhadap penurunan kadar asetil.
3. Mendapatkan biofilm dari selulosa asetat dengan pelarut aseton dan penambahan pemlastis gliserin.
4. Mengetahui pengaruh jumlah pemlastis dan kadar asetil selulosa asetat terhadap nilai parameter/karakteristik biofilm yang dihasilkan.
Manfaat Penelitian
Penelitian ini memberikan manfaat antara lain: 1. Bagi peneliti
Menambah pengetahuan tentang pemanfaatan limbah cair tapioka, pembuatan selulosa asetat dari selulosa mikrobial serta karakteristik produk biofilm yang dihasilkan.
2. Bagi peneliti selanjutnya
3 3. Bagi perusahaan
Mengurangi cemaran limbah cair tapioka bagi industri tapioka serta menjadi pertimbangan pemilihan bahan baku bagi industri biofilm.
Ruang Lingkup Penelitian
Penelitian ini dibatasi pada proses pembuatan nata de cassava dari limbah cair tapioka, pembuatan selulosa asetat dari serbuk selulosa mikrobial nata de cassava, dilanjutkan dengan pembuatan biofilm dengan tambahan pemlastis gliserin, serta pengujian karakteristik fisik biofilm.
TINJAUAN PUSTAKA
Limbah Cair Tapioka
Limbah cair industri tapioka dihasilkan dari proses pembuatan, baik dari pencucian bahan baku sampai pada proses pemisahan pati dari airnya atau proses pengendapan yang mengandung bahan organik. Seringkali limbah cair ini dibuang langsung ke badan air tanpa pengolahan terlebih dahulu, sehingga berpotensi menyebabkan pencemaran lingkungan (Nurhasan dan Pramudyanto 1996).
Proses degradasi bahan organik tersebut berlangsung lambat dan tidak sempurna, sehingga dihasilkan senyawa organik berbau tajam. Limbah cair tapioka yang digunakan sebagai air irigasi langsung dapat mengakibatkan tanaman padi berumur muda mengalami cekaman dan mati. Tingginya nilai BOD dan COD dalam limbah tersebut dapat menyebabkan kegagalan panen tambak udang. Racun sianida dalam limbah berpotensi mencemari sungai penduduk setempat.
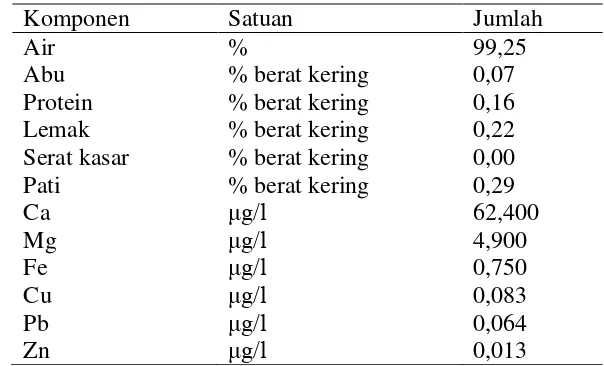
Fauzi dkk (2010) menyatakan bahwa dari 100 kg ubi kayu dibutuhkan air 1.255 liter untuk proses produksi tapioka menghasilkan rendemen tapioka kasar 22 kg dan limbah cair 1.242,5 liter. Tabel 4 berikut ini menampilkan hasil analisis proksimat dan mineral limbah cair tapioka:
Tabel 1 Analisis proksimat dan mineral limbah cair tapioka
4
Nata de cassava
Nata adalah hasil fermentasi oleh bakteri Acetobacter xylinum, berbentuk gel yang mengapung pada permukaan media atau tempat yang mengandung gula dan asam. Selama ini masyarakat mengetahui nata hanya bisa dibuat dari air kelapa. Oleh karena itu pada penelitian ini air sisa pengendapan pati dimanfaatkan sebagai bahan baku media pembuatan Nata de cassava yang merupakan salah satu usaha diversifikasi produk hasil pertanian.
Nata berasal dari Philipina untuk menyebut suatu pertumbuhan menyerupai gel (agar-agar) yang terapung di permukaan, dimana gel tersebut merupakan selulosa yang dihasilkan oleh bakteri Acetobacter xylinum. Bakteri Acetobacter
xylinum tergolong famili Pseudomonadaceae dan termasuk genus Acetobacter.
Berbentuk bulat, panjang 2 mikron, biasanya terdapat sel tunggal atau kadang-kadang mempunyai rantai dengan sel yang lain. Acetobacter xylinum digunakan dalam pembuatan nata karena bakteri ini mempunyai sifat yang spesifik. Bakteri ini mempunyai kemampuan untuk membentuk selaput tebal pada permukaan cairan fermentasi, yang ternyata adalah komponen menyerupai selulosa (selulosa material). Komponen inilah yang lebih lanjut disebut nata. (Stainer et al 1963)
Pertumbuhan Acetobacter xylinum dalam medium yang cocok menghasilkan massa berupa selaput tebal pada permukaan medium. Selaput tebal tersebut mengandung 35-62% (bk) selulosa. Lapisan tebal tersebut terbentuk pada permukaan medium, merupakan hasil akumulasi polisakarida ekstraseluler (nata) yang tersusun oleh jaringan mikrofibril / pelikel. Pelikel tersebut adalah tipe selulosa yang mempunyai struktur kimia seperti selulosa yang dibentuk oleh tumbuhan tingkat tinggi. (Collado 1987 dan Moat 1988)
Pembentukan nata (polisakarisa ekstraseluler) memerlukan senyawa antara lain yaitu heksosa fosfat. Heksosa fosfat mengalami oksidasi melalui lintasan pentosa fosfat menghasilkan senyawa NADPH (senyawa penyimpan tenaga pereduksi) dan melepas CO2. Gas CO2 yang dilepas akan terhambat dan menempel pada mikrofibril selulosa, sehingga selulosa naik ke permukaan cairan (Meyer, 1960).
Selulosa disintesis melalui reaksi bertahap UDPG (uridin difosfat glukosa) dan selodekstrin. Selodekstrin dihasilkan dari penggabungan UDP (uridin difosfat) glukosa dengan unit glukosa (Meyer, 1960). Reaksi pembentukan selodekstrin berlangsung terus sampai terbentuk senyawa, yang terdiri dari 30 unit
glukosa dengan ikatan β-1,4. Selodekstrin bergabung dengan lemak dan protein. Proses tersebut merupakan proses antara dari UDP glukosa yang melibatkan enzim selulosa sintetase (Moat 1988). Pembentukan polisakarida ekstrasellular (nata) dapat terjadi 24 jam setelah inkubasi dan meningkat dengan cepat 4 hari inkubasi, kemudian cenderung lambat pada hari berikutnya. Hal ini dikarenakan keasaman medium bertambah serta gula dalam substrat berkurang. ( Alaban 1962)
Selulosa asetat
5 agak liat, tidak memiliki barier yang baik untuk uap air dan gas; barier yang baik bagi minyak dan lemak, tidak edible, dan aplikasi secara umum untuk barang-barang moulding, sebagai lapisan untuk diwarnai. (Desiyarni 2006)
Reaksi yang berlangsung merupakan reaksi bolak-balik dan bersifat eksotermis, yaitu:
� �+ � + �
⇌ � � , � , �, ∆ℎ = − ,
(I. Harrison et al 2004)
Reaksi bolak-balik merupakan reaksi kesetimbangan, terjadi pada konversi yang maksimum. Selulosa triasetat maksimum didapat pada waktu 1 jam asetilasi dengan kadar asetil 44,175%. Untuk mendapatkan selulosa diasetat, maka proses dilanjutkan ke tahap hidrolisa. Kadar asetil yang diperoleh adalah 39% pada waktu asetilasi 15 jam, suhu 50oC dengan kadar air 0,537% bersifat serbuk putih, tidak berbau, tidak berasa, dan tidak beracun. (Rosnelly dkk 2009)
Sifat selulosa asetat ditentukan oleh derajat substitusinya karena berhubungan dengan kelarutannya dalam pelarut tertentu. Kadar asetil merupakan ukuran jumlah gugus asetil yang diesterifikasi pada rantai selulosa dan menentukan derajat substitusi (DS). Hubungan antara kadar asetil dengan derajat substitusi ditunjukkan pada Tabel 2 berikut ini:
Tabel 2 Hubungan kandungan asetil , derajat substitusi, jenis pelarut, dan kegunaannya
Kandungan asetil Derajat substitusi Pelarut Penggunaan
13.0-18.6 0.6-0.9 Air -
22.2-32.2 1.2-1.8 2-Metoksi-etanol plastik
36.5-42.2 2.2-2.7 Aseton benang, film
43.0-44.8 2.8-3.0 Kloform kain, pembungkus
Sumber: Fengel and Wegener (1984)
Biofilm dan Bioplastik
Biofilm diartikan sebagai film kemasan yang dapat didaur ulang dan dapat dihancurkan secara alami. Proses pembentukan biofilm diawali dengan melemahnya jarak antar partikel yang saling berkaitan dalam suatu cairan, sehingga setelah terjadi proses penguapan akan terbentuk lembaran (Buckmann et al 2002). Biofilm dapat dikembangkan menjadi bahan pengemas atau bioplastik (Apriyanto 2007).
6
Pembuatan biofilm dibantu oleh penambahan pemlastis (plasticizer). Plasticizer merupakan bahan dengan berat molekul kecil sehingga dapat bergabung ke dalam matriks protein dan polisakarida untuk meningkatkan sifat fleksibilitas dan kemampuan membentuk film. Plasticizer meningkatkan volume bebas atau mobilitas molekul primer dengan mengurangi ikatan hidrogen, termasuk juga kemampuannya untuk mengikat air ke dalam sistem protein yang mengandung plasticizer. Salah satu jenis plasticizer adalah gliserol. Gliserol adalah senyawa alkohol dengan tiga buah gugus hidroksil dalam satu molekul (alkohol trivilen). Gliserol ini berbentuk cair, kental, tidak berbau, transparan, higroskopis, serta dapat larut dalam air dan alkohol. Selain itu, molekul gliserol ini relatif kecil sehingga dapat dengan mudah disisipkan di antara rantai polimer (Gontrad et al. 1993).
METODE
Penelitian ini dilakukan dalam empat tahap yaitu pembuatan nata de cassava dari limbah cair tapioka, pembuatan selulosa asetat dari serbuk selulosa mikrobial nata de cassava, pembuatan biofilm, dan pengujian karakteristik fisik biofilm.
Alat & Bahan
Peralatan yang digunakan dalam penelitian ini antara lain pengempa hidrolik, pH meter, hammer mill dan saringan 40 mesh, shaker inkubator, hot plate dan stirer, oven, vacuum filter, sentrifus dan tabung sentrifugasi.
Bahan yang digunakan dalam penelitian ini antara lain limbah cair tapioka, Acetobacter xylinum, asam asetat (CH3COOH), gula (C12H22O11), amonium sulfat ((NH4)2SO4), asetat anhidrida ((CH3CO)2O), asam sulfat (H2SO4), aseton (CH3COCH3), gliserin (C3H8O3), kertas saring, dan aquades.
Prosedur Penelitian
Pembuatan Nata de cassava
7 satu malam. Keesokan harinya, sebanyak 20% (v/v) inokulum dituang ke dalam media secara aseptis dan diinkubasi selama 8 hari hingga terbentuk nata.
Pembuatan serbuk selulosa mikrobial
Prosedur ini merupakan modifikasi penelitian Sani (2012). Lembaran nata de cassava dicuci berulang dengan air dan dikelupas lapisan terluarnya kemudian direbus hingga mendidih untuk mematikan bakteri yang tersisa. Nata kemudian dimurnikan dengan perendaman dalam larutan NaOH 1% (b/v) selama 24 jam lalu dinetralkan dengan perendaman dalam larutan asam asetat teknis 1% (v/v) selama 24 jam. Nata selanjutnya dipress dengan pengempa hidrolik untuk mengurangi kandungan air dan mempercepat proses pengeringan. Pengeringan nata dilakukan dengan penjemuran dalam greenhouse selama 2 hari. Nata yang telah kering kemudian dipotong kecil lalu digiling menggunakan hammer mill 40 mesh.
Pembuatan selulosa asetat
Pembuatan selulosa asetat menggunakan modifikasi prosedur Safriani (2000) dan Sani (2012). Sebanyak 10 gram serbuk selulosa mikrobial dicuci untuk menyerap kandungan air dengan asam asetat glasial 50 mL lalu disaring dengan vacuum filter. Serbuk nata yang telah bebas air kemudian diaktivasi dengan asam asetat glasial 50mL dan H2SO4 0,2mL sebagai katalis dalam shaker inkubator pada suhu 38oC selama 30 menit. Asetat anhidrid ditambahkan sebagai pelarut dalam proses asetilasi dengan rasio serbuk nata:asetat anhidrida 1:3, 1:4, 1:5 (b:v). Proses asetilasi dilakukan pada shaker inkubator selama 1, 2 dan 3 jam dengan suhu 38oC hingga terbentuk larutan yang lebih kental berwarna cokelat. Setelah proses asetilasi selesai, suspensi dihidrolisis dengan larutan asam asetat encer dengan perbandingan 1:2 (asam asetat:aquades) sebanyak 12mL dalam shaker inkubator pada suhu 50oC selama 30 menit. Larutan kemudian disentrifugasi. Supernatan yang diperoleh dimasukkan ke dalam 500mL aquades sehingga terbentuk serpihan selulosa asetat berwarna putih. Serpihan selulosa asetat kemudian disaring menggunakan vacuum filter dan dicuci dengan aquades sampai bau asam hilang. Serpihan kemudian dikeringkan dalam oven 50oC selama 6 jam atau hingga kering.
Pembuatan biofilm
8
Pengujian karakteristik fisik biofilm
Pengujian biofilm dilakukan untuk mengetahui nilai beberapa karakter fisiknya meliputi ketebalan, kuat tarik dan elongasi, laju transmisi uap (WVTR) dan daya serap air. Uji kuat tarik dan elongasi dilakukan menggunakan metode ASTM D638, WVTR menggunakan metode ISO 2528-1974(E) dan daya serap air menggunakan metode ASTM D570. Prosedur pengujian karakteristik fisik biofilm tercantum dalam Lampiran 1 poin 5-7.
HASIL DAN PEMBAHASAN
Nata de cassava
Limbah cair tapioka merupakan hasil samping produksi tapioka yang masih banyak mengandung bahan organik. Kandungan pati 0,29% dapat digunakan sebagai sumber karbon sehingga merupakan media yang baik bagi Acetobacter
xylinum untuk membentuk nata de cassava. Bakteri ini mempunyai kemampuan
untuk mengkonversi glukosa menjadi selulosa membentuk matriks yang disebut nata (Yoshino et al 1995).
Aktivitas pembentukan nata optimum pada pH 3,5-4,5 pada suhu ruang sehingga perlu dilakukan pengaturan pH menggunakan asam asetat glasial. Penambahan gula berfungsi sebagai sumber C sedangkan amonium sulfat sebagai sumber N. Kondisi aseptis sangat dibutuhkan saat proses inokulasi untuk mencegah kontaminasi kapang yang dapat mengganggu proses pembentukan nata.
Nata de cassava yang diperoleh pada penelitian ini mempunyai ukuran
30x22,5 cm dan ketebalan rata-rata 1,5cm dan rendemen basah 986,25 gram per 1000 mL media. Peningkatan rendemen dapat dilakukan dengan memperpanjang waktu fermentasi, semakin lama waktu fermentasi nata yang dihailkan semakin tebal selain itu juga dapat meningkatkan kerapatan selulosa yang dihasilkan. Nata perlu direbus untuk mematikan bakteri yang tersisa dan dilanjutkan dengan perendaman dalam larutan NaOH 1%. Perendaman ini bertujuan mengurangi pengotor seperti kandungan gula dan protein dalam nata sehingga tidak terjadi browning pada saat pengeringan. NaOH sebagai cleaning agent bereaksi menyabunkan lemak dan melarutkan protein. Selain itu, struktur selulosa akan membengkak dan memudahkan saat proses asetilasi. Namun proses pembengkakan akan berdampak pada peningkatan kristalinitas sehingga diperlukan perendaman dalam asam asetat 1% untuk menetralkan nata dan mengurangi kristalinitas struktur selulosa.
9 menggunakan pelarut. Semakin besar daerah kristalin suatu selulosa maka semakin lama waktu yang dibutuhkan untuk menggembungkannya. Penggembungan selulosa akan menyebabkan berkurangnya ikatan antar serat selulosa, sehingga memudahkan masuknya pereaksi. Daerah kristalin sulit dipenetrasi oleh pereaksi karena adanya ikatan intra dan antar rantai selulosa yang sangat kuat melalui ikatan hidrogen dan gaya van der Waals (Dadi et al. 2006)
Pembuatan serbuk selulosa mikrobial dilakukan dengan mengeringkan lembaran nata. Proses pengempaan perlu dilakukan untuk mempercepat pengeringan. Proses pengeringan dilakukan dengan penjemuran di dalam greenhouse untuk mengurangi resiko yang diakibatkan cuaca. Pengeringan menggunakan dryer dapat menyebabkan browning sehingga sangat tidak disarankan. Lembaran nata kering kemudian dipotong kecil untuk memudahkan saat penggilingan. Penggilingan dilakukan dengan hammer mill 40 mesh. Tujuan dilakukan pengecilan ukuran adalah untuk mempercepat proses asetilasi.
Serbuk selulosa yang dihasilkan pada penelitian ini mempunyai rendemen 0,59% terhadap berat nata basah. Hasil analisis proksimat serbuk selulosa mikrobial disajikan dalam Tabel 3 berikut ini:
Kandungan selulosa sebesar 82,37% membuktikan bahwa kemurnian selulosa mikrobial yang dihasilkan cukup tinggi meskipun masih terdapat kandungan non selulosa. Kandungan non selulosa akan dihilangkan sebelum proses aktivasi pada tahap pembuatan selulosa asetat.
Selulosa asetat
Selulosa asetat merupakan produk turunan selulosa melalui proses asetilasi menggunakan pelarut asetat anhidrida. Asetilasi mensyaratkan kondisi bebas air (Arifin 2004). Oleh karena itu perlu dilakukan perlakuan awal yaitu perendaman serbuk selulosa mikrobial dalam asam asetat glasial. Perendaman ini selain bertujuan menarik air juga melarutkan impurities dalam serbuk selulosa mikrobial yang ditunjukkan dengan perubahan warna asam asetat menjadi kecoklatan. Berdasarkan hasil analisis proksimat yang ditampilkan pada Tabel 3, dapat diduga bahwa impurities berasal dari kandungan protein dan lemak dalam serbuk selulosa mikrobial.
Proses aktivasi diperlukan untuk tujuan menggembungkan struktur selulosa sehingga proses asetilasi dapat berlangsung dengan lebih baik dan cepat. Aktivasi dilakukan dengan menambahkan asam asetat glasial. Pada proses ini pula dilakukan penambahan katalis H2SO4 pekat. Penambahan katalis berfungsi mempercepat proses asetilasi.
Tabel 3 Analisis kandungan serbuk selulosa mikrobial nata de cassava
Parameter Nilai (% wb)
Kadar air 4,24 ± 0,01
Kadar abu 0,43 ± 0,06
Kadar protein 3,13 ± 0,04
Kadar lemak 1,09 ± 0,01
10
Asetilasi merupakan proses utama dalam pembuatan selulosa asetat. Pada penelitian ini digunakan variasi rasio asetat anhidrida 1:3, 1:4, dan 1:5. Landasan menggunakan variasi ini berdasarkan persamaan reaksi asetilasi. Selulosa merupakan polimer linier glukosa yang unit-unitnya terikat dengan ikatan 1,4-β-D glukopiranosa. Bila diasumsikan satu molekul selulosa terdiri atas n unit glukosa maka secara teoritis pada reaksi asetilasi sempurna, setiap 1 mol selulosa membutuhkan 3n mol asetat anhidrida dan akan menghasilkan 1 mol selulosa triasetat dan 3n mol asam asetat.
Selulosa triasetat hasil asetilasi sempurna memiliki rumus empirik [C6H7O2(CH3CO)3]n. Bila diasumsikan bobot molekul selulosa mikrobial (C6H7O2(OH)3)n adalah 162n gram/mol dan bobot molekul selulosa triasetat adalah 240n gram/mol maka setiap 1 gram selulosa mikrobial (setara dengan 0,0062/n mol selulosa mikrobial) akan menghasilkan 0,0062/n mol selulosa triasetat atau setara dengan 1,79 gram selulosa triasetat. Bila reaksi asetilasi selulosa berlangsung sempurna dan tidak terjadi degradasi selulosa maka dari setiap satu gram selulosa yang digunakan akan diperoleh selulosa triasetat sebanyak 1,79 gram (Desiyarni, 2006).
Persamaan reaksi pembentukan selulosa triasetat tersebut adalah sebagai berikut:
RSel-(OH)3 + 3(CH3CO)2O ↔ RSel-(OCOCH3)3 + 3CH3COOH
0,0062/n mol 0,0186/n mol 0,0062/n mol 0,0186/n mol
162n g/mol 102n g/mol 240n g/mol 60n g/mol
1,0044 gram 1,8972 gram 1,488 gram 1,116 gram
Berdasarkan perhitungan tersebut, dapat disimpulkan bahwa untuk dapat bereaksi dibutuhkan rasio selulosa:asetat anhidrida sebesar 1:2. Hasil penelitian Safriani (2000) menunjukkan bahwa pada rasio tersebut rendemen selulosa asetat rendah yaitu kurang dari 50% dengan kadar asetil di bawah 25% sedangkan pada penelitian ini selulosa asetat yang dihasilkan diharapkan mempunyai kadar asetil 36,5-42,2% sehingga dapat dilarutkan dalam aseton pada pembuatan biofilm. Oleh karena itu rasio dimulai dari 1:3.
Pertimbangan pemilihan variasi waktu asetilasi didasarkan pada penelitian Sani (2012) dimana asetilasi dalam waktu 2 jam mampu menghasilkan kadar asetil yang cukup tinggi yaitu 40,38%. Oleh karena itu perlu dilakukan penurunan waktu asetilasi untuk memperoleh kadar asetil di bawah angka tersebut sehingga variasi waktu asetilasi adalah 1, 2 dan 3 jam.
Reaksi asetilasi dihentikan dengan penambahan asam asetat encer kemudian mulai dihidrolisis pada suhu 50oC menggunakan perbandingan asam asetat:aquades 2:1. Pada proses ini terjadi pemotongan rantai selulosa triasetat menjadi selulosa diasetat. Persamaan reaksi hidrolisis adalah sebagai berikut:
RSel-(OCOCH3)3 + H2O → RSel-(OCOCH3)2OH + CH3COOH
1 mol 1 mol 1 mol 1 mol
240 g/mol 18 g/mol 181 g/mol 60 g/mol
240 gram 18 gram 181 gram 60 gram
11 mikrobial belum larut seluruhnya. Pada rasio 1:4 dan 1:5 selulosa dapat larut seluruhnya. Supernatan yang diperoleh kemudian dituang ke 500mL aquades sehingga terbentuk serpihan selulosa asetat berwarna putih.
Selulosa asetat yang diperoleh dalam penelitian ini mempunyai rendemen 20,56-28,15%. Rendemen perolehan selulosa asetat disajikan pada Gambar 1 sebagai berikut:
Berdasarkan grafik tersebut dapat ketahui bahwa rendemen turun seiring bertambahnya rasio asetat anhidrida namun meningkat seiring bertambahnya waktu asetilasi. Hasil analisis keragaman rendemen selulosa asetat (Lampiran 3) menunjukkan bahwa baik rasio selulosa asetat maupun waktu asetilasi berpengaruh terhadap rendemen. Asetat anhidrida yang ditambahkan tidak semua dapat bereaksi dengan selulosa sehingga rasio produk dan bahan yang digunakan semakin kecil. Peningkatan waktu asetilasi memberikan kesempatan selulosa untuk bereaksi dengan asetat anhidrida sehingga rendemen meningkat.
Selulosa asetat yang dihasilkan dalam penelitian ini kemudian diuji kadar air. Hasilnya adalah selulosa asetat memiliki kadar air antara 3,81-4,38%. Kadar air selulosa asetat secara lengkap disajikan pada Gambar 2 berikut ini:
Gambar 2 Hubungan rasio asetat anhidrida dan waktu asetilasi terhadap kadar air selulosa asetat
12
Berdasarkan grafik tersebut dapat diketahui bahwa kadar air cenderung turun seiring bertambahnya rasio asetat anhidrida namun naik seiring bertambahnya waktu asetilasi. Hasil uji keragaman terhadap kadar air selulosa asetat (Lampiran 5) menunjukkan bahwa baik rasio asetat anhidrida maupun waktu asetilasi tidak berpengaruh terhadap kadar air selulosa asetat. Hal ini disebabkan kadar air selulosa asetat lebih dipengaruhi oleh waktu dan suhu pengeringan.
Terhadap selulosa asetat yang dihasilkan juga diuji kadar asetilnya. Hasilnya adalah selulosa asetat memiliki kadar asetil 30,60-44,51%. Kadar asetil selulosa asetat ditampilkan pada Gambar 3 berikut ini:
Gambar 3 Hubungan rasio asetat anhidrida dan waktu asetilasi terhadap kadar asetil selulosa asetat
Berdasarkan grafik diatas dapat diketahui bahwa kadar asetil selulosa asetat meningkat seiring bertambahnya rasio asetat anhidrida maupun waktu asetilasi. Hasil uji keragaman kadar asetil (Lampiran 7) menunjukkan bahwa rasio asetat anhidrida dan waktu asetilasi berpengaruh terhadap kadar asetil selulosa asetat. Peningkatan jumlah asetat anhidrida maupun waktu asetilasi memberikan kesempatan bagi selulosa untuk bereaksi membentuk selulosa asetat. Semakin banyak selulosa yang terkonversi menjadi selulosa asetat semakin tinggi pula kadar asetilnya.
Selulosa asetat yang ditargetkan dalam penelitian ini sesuai Tabel 2 yaitu dengan kadar asetil 36,5-42,2%. Oleh karena itu perlakuan yang memenuhi syarat yaitu pada rasio asetat anhidrida 1:4 dengan waktu asetilasi 1, 2, dan 3 jam serta rasio asetat anhidrida 1:5 dengan waktu asetilasi 1 jam.
Biofilm dan Bioplastik
Selulosa asetat yang telah dihasilkan kemudian digunakan sebagai bahan pembuat biofilm. Penelitian ini menggunakan metode cetak larut (solution casting), maka selulosa asetat harus dilarutkan dengan pelarut yang sesuai. Jenis pelarut untuk tujuan film yaitu aseton sehingga diperlukan selulosa asetat dengan
13 kadar 36,5-42,2%. Selulosa asetat yang digunakan berasal dari 4 perlakuan yaitu dengan kadar asetil 36,7%, 37,72%, 38,7%, dan 40,19%.
Penambahan pemlastis perlu dilakukan karena film selulosa asetat yang dihasilkan tanpa pemlastis sangat rapuh sehingga tidak dapat dikelupas dari cetakan. Jenis pemlastis yang dipilih yaitu pemlastis dasar berupa gliserin. Jumlah gliserin yang digunakan yaitu 15 dan 25 % dari bobot selulosa asetat yang digunakan. Menurut Taskier dan Englewood (1970), jumlah pemlastis dalam larutan sekitar 5-40% dan lebih disukai 9-25% berdasarkan bobot serpihan (flake) diasetat yang digunakan dalam larutan. Namun penelitian Safriani (2000) yang menggunakan jumlah pemlastis 9, 17, dan 25% menunjukkan bahwa pada konsentrasi 9% tidak terbentuk film yang baik.
Film selulosa asetat yang dihasilkan pada penelitian ini berwarna kekuningan, transparan, dan memiliki ketebalan rata-rata 43µm. Ketebalan film dapat diatur dengan mengubah kedalaman pencetak yang digunakan. Terhadap biofilm yang dihasilkan kemudian dilakukan pengujian kuat tarik, elongasi, laju transmisi uap (WVTR), dan daya serap air.
Karakteristik fisik biofilm
Rata-rata kuat tarik biofilm yang dihasilkan adalah 320,50 kgf/cm2. Kuat tarik biofilm secara lengkap disajikan pada Gambar 4 berikut ini:
Gambar 4 Hubungan kadar asetil dan jumlah pemlastis terhadap kuat tarik biofilm Berdasarkan grafik di atas kuat tarik biofilm meningkat seiring peningkatan kadar asetil dan jumlah pemlastis. Hasil uji keragaman kuat tarik biofilm (Lampiran 9) menunjukkan bahwa kadar asetil dan jumlah pemlastis berpengaruh terhadap kuat tarik biofilm. Kadar asetil yang semakin tinggi mengakibatkan jumlah polimer semakin banyak sehingga kerapatannya semakin tinggi dan mengakibatkan kenaikan kekuatan tarik. Pemlastis berfungsi mengikat polimer tersebut sehingga dihasilkan biofilm yang lebih elastis.
Elongasi biofilm yang dihasilkan mempunyai rata-rata 3,06%. Elongasi biofilm secara lengkap disajikan pada Gambar 5 berikut ini:
14
Gambar 5 Hubungan kadar asetil dan jumlah pemlastis terhadap elongasi biofilm Berdasarkan grafik di atas elongasi biofilm meningkat seiring peningkatan kadar asetil dan jumlah pemlastis. Hasil uji keragaman elongasi biofilm (Lampiran 11) menunjukkan bahwa kadar asetil dan jumlah pemlastis berpengaruh terhadap elongasi biofilm.
Laju transmisi uap (WVTR) biofilm yang dihasilkan rata-rata 461,97 g/m2/24 jam. Laju transmisi uap (WVTR) biofilm secara lengkap disajikan pada Gambar 6 berikut ini:
Gambar 6 Hubungan kadar asetil dan jumlah pemlastis terhadap laju transmisi uap (WVTR) biofilm
Berdasarkan grafik di atas laju transmisi uap (WVTR) biofilm meningkat seiring peningkatan kadar asetil dan jumlah pemlastis. Hasil uji keragaman laju transmisi uap (WVTR) biofilm (Lampiran 13) menunjukkan bahwa kadar asetil dan jumlah pemlastis berpengaruh terhadap laju transmisi uap (WVTR). Polimer
15 selulosa asetat bersifat hidrofilik. Selain itu penambahan jumlah pemlastis dapat meningkatkan permeabilitas.
Daya serap air biofilm yang dihasilkan rata-rata 10,52%. Daya serap air biofilm secara lengkap disajikan pada Gambar 7 berikut ini:
Gambar 7 Hubungan kadar asetil dan jumlah pemlastis terhadap daya serap air biofilm
Berdasarkan grafik di atas daya serap air biofilm meningkat seiring peningkatan kadar asetil namun menurun seiring bertambahnya jumlah pemlastis. Hasil uji keragaman daya serap air biofilm (Lampiran 15) menunjukkan bahwa hanya jumlah pemlastis yang berpengaruh terhadap daya serap air. Peningkatan jumlah pemlastis yang akan mengisi ruang diantara polimer menyebabkan berkurangnya jumlah air yang dapat diserap.
Perbandingan penelitian ini dengan hasil penelitian sebelumnya dirangkum pada Tabel 4 berikut.
Berdasarkan Tabel 4 di atas sebagian besar nilai karakteristik fisik biofilm selulosa asetat hasil penelitian ini mendekati nilai karakteristik fisik selulosa asetat dari jenis selulosa mikrobial lainnya. Kuat tarik dan daya serap air biofilm selulosa asetat nata de cassava lebih rendah dibanding selulosa asetat nata de
16
coco. Hal tersebut disebabkan aplikasi selulosa asetat nata de coco adalah sebagai membran sehingga harus dapat meneruskan larutan yang melaluinya.
Kuat tarik biofilm pada penelitian ini lebih besar dibandingkan dengan kuat tarik selulosa asetat menurut I. Harrison dkk (2004) yaitu 30 MPa atau setara dengan 305,91 kgf/cm2, namun elongasi biofilm penelitian ini lebih rendah dibandingkan dengan elongasi selulosa asetat menurut I. Harrison dkk (2004) yaitu 3,9%.
Sasaran aplikasi biofilm ini jika digunakan sebagai safety film tidak memenuhi kriteria. Jika dibandingkan dengan karakteristik fisik Llumar Safety
and Security Film (CPFilms 2009) yaitu pada ketebalan 50 mikron, film
mempunyai kuat tarik 193 MPa setara dengan 19680,21 kgf/cm2 dan elongasi >100%. Jika dibandingkan dengan nilai kuat tarik polyetilene film for packaging JIS Z 1702-1986 (JIS 1986) yaitu 120 kg/cm2 maka film ini memenuhi syarat, namun dilihat dari elongasi yaitu 150% maka biofilm ini tidak memenuhi syarat. Oleh karena itu aplikasi biofilm ini masih harus dikombinasikan dengan bahan pemlastis yang dapat meningkatkan kuat tarik dan elongasinya.
Biofilm ini dapat diaplikasikan sebagai pengganti HDPE. Nilai karakteristik fisik biofilm ini memenuhi syarat berdasarkan Suyadi (2010) bahwa kuat tarik HDPE adalah 21,73 N/mm2 atau setara dengan 221,58 kgf/cm2 dan elongasi 4,5%. Aplikasi HDPE antara lain untuk jerigen minyak pelumas, botol susu dan kursi lipat.
SIMPULAN DAN SARAN
Simpulan
Limbah cair tapioka dapat dimanfaatkan untuk pembuatan selulosa mikrobial nata de cassava dengan karakteristik liat, tebal, dan kuat. Selulosa mikrobial yang dihasilkan dapat digunakan sebagai bahan pembuatan selulosa asetat dengan pelarut asetat anhidrida. Selulosa asetat yang dihasilkan dalam penelitian ini mempunyai kadar asetil antara 30,60-44,51%. Selulosa asetat yang mempunyai kadar asetil 36,5-42,2% dapat digunakan untuk membuat biofilm dengan pelarut aseton dan pemlastis gliserin. Biofilm yang terbentuk memiliki rata-rata kekuatan tarik 320,50 kgf/cm2, elongasi 3,06%, WVTR 461,97 g/m2/24 jam, dan daya serap air 10,52%.
Saran
17
DAFTAR PUSTAKA
Alaban CA. 1962. Studies on The Optimum Condition for Nata de Coco
Bacterium or Nata for Formation in Coconut Water. The Philipine
Agriculturist volume 45.
[AOAC] Association of Official Analytical Chemists. 1980. Official Method of Analysis. Washington DC: Association of Official Analytical Chemists Inc. [AOAC] Association of Official Analytical Chemists. 1995. Official Method of
Analysis. Washington DC: Association of Official Analytical Chemists Inc. Apriyanto J. 2007. Karakteristik Biofilm dari Bahan Dasar Polivinil Alkohol
(PVOH) dan Kitosan [Skripsi]. Bogor: Institut Pertanian Bogor.
Arifin B. 2004. Optimasi Kondisi Asetilasi Selulosa Bakteri dari Nata de Coco [Skripsi]. Bogor: Institut Pertanian Bogor.
[ASTM] American Society for Testing and Material. 1989. ASTM Book of Standard D638: Standard Test Method for Tensile Properties of Plastic. Philadelphia.
[ASTM] American Society for Testing and Material. 1991. ASTM Book of Standard D871-91: Standard Methods of Testing Cellulose Acetate. Philadelphia.
[ASTM] American Society for Testing and Material. 2010. ASTM Book of Standard D570: Standard Test Method for Water Absorption of Plastics. Philadelphia.
Buckmann AJP, T Nabuurs, GC Overbeek. 2002. Self Crosslinking Polymeric Dispersants Used in Emulsion Polymerization. Netherland.
Collado LS. 1987. Nata; Processing and Problems of the Industry in the
Philipines traditional Food and their Processing in Asia. Japan: Nodai
Research Institute Tokyo University of Agriculture.
CPFilms. 2009. Llumar Safety and Security Film Physycal Properties. St Louis, Missouri, USA: Solutia Inc.
Dadi AP, Varanasi S, Schall CA. 2006. Enhancement of Cellulose Saccharification Kinetics Using an Ionic Liquid Pretreatment Step. Wiley Periodicals. Inc. Wiley Interscience. 95(5):904-910.
Darwis A, Syamsu K, Suryani A, Yarni D. 2003. Proses Pembuatan Selulosa Triasetat dari Selulosa Mikrobial untuk Pembuatan Membran Mikrofiltrasi. Paten Indonesia No: ID 0 000 619 S.
Desiyarni. 2006. Perancangan Proses Pembuatan Selulosa Asetat dari Selulosa Mikrobial untuk Membran Ultrafiltrasi [Disertasi]. Bogor: Institut Pertanian Bogor.
Fauzi AM, Rahmawakhida A, Hidetoshi Y. 2010. Kajian Strategi Produksi Bersih di Industri Kecil Tapioka: Kasus Kelurahan Ciluar, Kecamatan Bogor Utara. Jurnal Teknologi Industri Pertanian. 18(2):60-65.
Fengel D, Wegener G. 1984. Wood: Chemistry, Ultrastructure, Reactions. Berlin: Walter de Gruyter.
18
Gontrad N, S Gulibert, dan JL Cuq. 1993. Water and glycerol as plasticizers affect mechanical and water vapor barrier properties of an ediblewheat film. J. Food Science. 58: 206-211.
I. Harrison, Huttenhuis PJG, Heesink ABM. 2004. BIOCA-Biomass Streams to Produce Cellulose Acetate. Department of Chemical Engineering, Twente University, Enschede. The Netherlands.
[ISO] International Organization for Standardization. ISO 2528-1974(E): Water Vapour Transmision Rate (WVTR) Plate Method. Geneva, Switzerland.
Jenie B, Ridawati, Rahayu WP. 1994. Produksi Angkak oleh Monascus purpureus dalam Medium Limbah Cair Tapioka, Ampas Tapioka dan Ampas Tahu. Buletin Teknologi dan Industri Pangan. 5(3):60-64.
[JIS] Japanese Industrial Standard. 1986. JIS Z 1702-1986: Polyetylene Film for Packaging. Tokyo.
Meyer LH. 1960 Food Chemistry. NewYork: Reinhold Publishing Co.
Moat AG. 1988. Microbial Physiology. New York: John Wiley and Sons Inc. NewYork.
Nurhasan dan Bb. Pramudyanto. 1996. Buku Panduan Penanganan Limbah Cair Industri Kecil Tapioka. Gramedia Pustaka, Jakarta.
Rosnelly CM, Darwis A, Noor E, Kaseno. 2009. Pembuatan Selulosa Diasetat dari Pulp Sengon (Paraserianthes falcataria) sebagai Bahan Baku Pembuatan Membran. Jurnal Agritek. 10(1):61-70
Safriani. 2000. Produksi Biopolimer dari Selulosa Asetat Nata de Soya [tesis]. Bogor: Institut Pertanian Bogor.
Sani CDS. 2012. Potensi Nata de cassava dari Limbah Cair Tapioka sebagai Membran Selulosa Asetat [skripsi]. Bogor: Institut Pertanian Bogor.
Stainer, Doudoroff, Adelberg. 1963. The Microbial World. Prentice Hall, Inc. Suyadi. 2010. Kaji Esksperimen Kekuatan Tarik Produk-Produk Berbahan Plastik
Daur Ulang. Di dalam: Peran Teknologi Tepat Guna dalam Menanggulangi Krisis Energi dan Menjaga Ketahanan Pangan. Semarang: Wahid Hasyim University Press.
Taskier HT dan NJ Englewood. 1970. United States Paten Office No. 3.567.809. White DG dan Brown RM. 1983. Prospects for The Commercialization of The
Biosynthesis of Microbial Cellulose. Munich.
19 Lampiran 1 Prosedur pengujian
1. Analisis kadar air (AOAC, 1995)
Pinggan aluminium dipanaskan pada suhu 105oC dan didinginkan dalam desikator sebelum ditimbang. Kemudian 2g contoh dimasukkan ke dalam pinggan aluminium yang telah diketahui bobot tetapnya dan dipanaskan dalam oven 105oC selama 1 jam. Pinggan dimasukkan dengan cepat ke dalam desikator, setelah dingin kemudin ditimbang dan pemanasan diulangi sampai bobot yang tetap. Sisa contoh dihitung sebagai total padatan dan air yang hilang sebagai kadar air.
� � = − %
Keterangan:
W1 = bobot contoh (g)
W2 = bobot contoh setelah dikeringkan (g) 2. Analisis kadar abu (AOAC, 1980)
Cawan perabuan dibakar dalam tanur, didinginkan dalam desikator dan ditimbang. Contoh kemudian dimasukkan ke dalam cawan, diarangkan terlebih dahulu dengan bunsen, lalu dibakar dalam tanur perabuan sampai didapat abu. Kadar abu dihitung dengan rumus:
� = %
Keterangan: A = bobot abu (g) B = bobot contoh (g)
3. Analisis kadar selulosa (Goering dan Van Soest, 1970)
Sebanyak 1 g contoh kering ditempatkan di dalam labu refluks. Kemudian ke dalamnya ditambahkan 100 ml pereaksi ADF. Reaksi ADF ini dibuat dengan melarutkan 80 g CTAB (C19H442BrN) dan x ml H2SO4 ke dalam 4 l aqua destilata. Campuran selanjutnya dididihkan selama 10 menit, kemudian di refluks selama 1 jam. Campuran yang telah di refluks kemudian di saring dengan kaca masir yang telah diketahui bobotnya (W1). Sisa saringan dibilas dengan air panas, aseton, dan hexana. Kaca masir beserta residu hasil bilasan tersebut dikeringkan dengan oven pada suhu 105oC selama 12 jam. Setelah pengeringan, hasil yang diperoleh didinginkan dan ditimbang (W2). Kaca masir selanjutnya direndam dengan 25 ml H2SO4 72%. Perendaman dilakukan selama 3 jam dengan pengadukan setiap 1 jam. Setelah 3 jam, kaca masir dan contoh dicuci dengan air panas sehingga bebas asam. Hasil pencuncian dikeringkan dengan oven selama 12 jam dan setelah dingin kaca masir dan contoh ditimbang (W3). Kadar selulosa dinyatakan dengan rumus:
� % = − ℎ % 4. Analisi kandungan asetil (ASTM D-871-91)
20
melewati saringan 20 mesh. Contoh dikeringkan selama 2 jam pada suhu 105±3oC. Contoh kering tersebut dengan bobot 1g dimasukkan ke dalam erlenmeyer, kemudian ditambahkan 40 ml etanol (75%) dan dipanaskan selama 30 menit pada suhu 50-60oC. Setelah itu ke dalam contoh ditambahkan 40ml larutan NaOH (0,5N) dan pemanasan dilanjutkan selama 15 menit dengan suhu yang sama. Contoh kemudian didiamkan selama 48-72 jam, dan kelebihan NaOH dititrasi dengan HCl (0,5N) dengan indikator fnolftalein. Contoh didiamkan selama satu hari untuk memberi kesempatan bagi NaOH berdifusi. Selanjutnya contoh dititrasi dengan NaOH (0,5N) dengan indikator merah metil sampai terbentuk warna merah. Blanko dilakukan dengan cara yang sama dengan contoh. Kadar asetil dan kandungan asam asetat dihitung dengan rumus
� � % = [ − + − ] �
Keterangan:
A = ml NaOH yang dibutuhkan untuk titrasi contoh B = ml NaOH yang dibutuhkan untuk titrasi blanko C = ml HCl yang dibutuhkan untuk titrasi contoh D = ml HCl yang dibutuhkan untuk titrasi blanko Na = normalitas HCl
Nb = normalitas NaOH
F = 4,305 untuk kadar asetil dan 6,005 untuk kadar asam asetat W = bobot contoh (g)
5. Uji kuat tarik dan elongasi (ASTM D638)
Sampel dibentuk sesuai dengan standar seperti gambar berikut:
Kedua ujung sampel dijepitkan dengan kuat pada penjepit mesin pengujian kuat tarik. Jepitan digerakkan dengan laju 0,05; 0,2; 0,5; dan 2,20 inci per menit yang menarik sampel dari kedua ujungnya. Tegangan dan regangan (elongasi) diplotkan secara otomatis pada kertas grafik. Gaya yang diperlukan untuk menarik sampel dapat diperoleh bersama-sama seberapa panjang bahan tertarik sebelum putus. Modulus elastis (modulus elastisitas atau modul tarik) adalah nisbah tegangan dengan regangan yang digunakan. Total daerah di bawah kurva tegangan-regangan menunjukkan keliatan keseluruhan.
Cawan-21 cawan tersebut dibiarkan selama 24 jam dan kemudian ditimbang dengan ketelitian 0,0001g. Selanjutnya cawan-cawan tersebut diletakkan kembali ke dalam chamber dan prosesnya diulang kembali. WVTR dihitung dengan menggunakan rumus
=
Keterangan:
WVTR = transmisi uap air (g/m2 24 jam) m = pertambahan bobot (g)
T = waktu antara 2 penimbangan terakhir (jam) S = luas permukaan contoh
7. Penyerapan air (ASTM D570)
Sampel yang digunakan berupa lembaran berukuran 3 inci x 1 inci x ketebalan bahan. Sampel sebelumnya dikeringkan selama 24 jam di dalam oven pada suhu 50oC, didinginkan di desikator dan segera ditimbang. Data penyerapan air diperoleh dengan merendam sampel dalam air selama 24 jam atau lebih pada suhu 73,4oF. Kemudian sampel dikeringkan dengan cara menyekanya dengan kain dan segera ditimbang. Penambahan bobot dihitung sebagai persen, untuk bahan-bahan yang kehilangan bahan-bahan terlarut selama perendaman (seperti bahan-bahan-bahan-bahan yang mengandung selulosa) sampel harus dikeringkan kembali, ditimbang kembali dan dilaporkan sebagai persen bahan terlarut yang hilang.
� %
= ℎ %
+ ℎ � ℎ� � %
Lampiran 2 Data Uji Rendemen Selulosa Asetat Rasio Asetat
Anhidrida Ulangan
Waktu
1 2 3
1:3 1 24,578 26,724 28,257
2 24,788 26,882 28,047
1:4 1 22,602 23,451 24,348
2 22,784 23,750 24,261
1:5 1 20,478 20,783 20,867
2 20,642 20,822 20,905 Lampiran 3 Uji Keragaman Rendemen Selulosa Asetat
Sumber Ragam DB JK KT F-hit F-0,05 F-0,01
Rasio Asetat Anhidrida (A) 2 100,851 50,426 3323,317 4,26 8,02
Waktu (B) 2 9,886 4,943 325,776 4,26 8,02
(AxB) 4 5,071 1,268 83,558 3,63 6,42
Galat 9 0,137 0,015
Total 17 115,945
22
Lampiran 4 Data Uji Kadar Air Selulosa Asetat Rasio Asetat
Anhidrida Ulangan
Waktu
1 2 3
1:3 1 3,5945 3,5436 4,1632
2 4,6729 4,8193 4,5795
1:4 1 3,4941 4,2017 4,1322
2 4,3326 4,2857 4,6281
1:5 1 3,2895 4,2373 3,2916
2 4,6053 3,3898 4,5425 Lampiran 5 Uji Keragaman Kadar Air Selulosa Asetat
Sumber Ragam DB JK KT F-hit F-0,05 F-0,01
Rasio Asetat Anhidrida (A) 2 0,3950 0,1975 0,4481 4,26 8,02
Waktu (B) 2 0,1553 0,0776 0,1762 4,26 8,02
(AxB) 4 0,1580 0,0395 0,0896 3,63 6,42
Galat 9 3,9670 0,4408
Total 17 4,6754
Lampiran 6 Data Uji Kadar Asetil Selulosa Asetat
Rasio Asetat
Anhidrida Ulangan
Waktu
1 2 3
1:3 1 30,4128 33,2632 35,2622
2 30,7777 34,2857 34,7386
1:4 1 37,2308 37,7688 38,5333
2 36,1657 37,6671 38,4029
1:5 1 39,9128 42,9038 44,8305
2 40,4645 43,3677 44,1828 Lampiran 7 Uji Keragaman Kadar Asetil Selulosa Asetat
Sumber Ragam DB JK KT F-hit F-0,05 F-0,01
Rasio Asetat
Anhidrida (A) 2 270,2366 135,1183 684,3951 4,26 8,02
Waktu (B) 2 38,3046 19,1523 97,0094 4,26 8,02
(AxB) 4 5,0023 1,2506 6,3344 3,63 6,42
Galat 9 1,7768 0,1974
Total 17 315,3203
23 Lampiran 8 Data Uji Kuat Tarik Biofilm
Kadar Asetil
Lampiran 9 Uji Keragaman Kuat Tarik Biofilm
Sumber Ragam DB JK KT F-hit F-0,05 F-0,01 Lampiran 10 Data Elongasi Tarik Biofilm
Kadar Asetil
Lampiran 11 Uji Keragaman Elongasi Biofilm
24
Lampiran 12 Data Laju Transmisi Uap (WVTR) Biofilm Kadar Asetil
Lampiran 13 Uji Keragaman Laju Transmisi Uap (WVTR) Biofilm
Sumber Ragam DB JK KT F-hit F-0,05 F-0,01 Lampiran 14 Data Daya Serap Air Biofilm
Kadar Asetil
Lampiran 15 Uji Keragaman Daya Serap Air Biofilm
25
RIWAYAT HIDUP
Penulis dilahirkan di Sukoharjo pada tanggal 1 Oktober 1990 sebagai putri kedua dari bapak Sarino dan ibu Wagiyem. Tahun 2009 penulis lulus dari SMA Negeri 1 Glagah Banyuwangi dan pada tahun yang sama diterima di Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB di Departemen Teknologi Industri Pertanian, Fakultas Pertanian.