KAJIAN SPEKTROSKOPI INFRAMERAH TRANSFORMASI
FOURIER DAN MIKROSKOP SUSURAN ELEKTRON
MEMBRAN SELULOSA ASETAT DARI LIMBAH NANAS
ASTIKA TRESNAWATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ASTIKA TRESNAWATI. Kajian Spektroskopi Inframerah Transformasi Fourier dan Mikroskop Susuran Elektron Membran Selulosa Asetat dari Limbah Nanas. Dibimbing oleh BETTY MARITA SOEBRATAdan SRI MULIJANI.
Produksi nanas di Indonesia meningkat setiap tahunnya. Satu buah nanas yang dapat dikonsumsi hanya 53%-nya, sedangkan sisanya menumpuk tanpa mengalami pengolahan. Salah satu cara pemanfaatan limbah nanas adalah dengan mengolah kulit nanas menjadi nata de pina yang lebih lanjut dapat diolah menjadi membran.
Penelitian ini diawali dengan pembuatan nata de pina, kemudian dimurnikan dan diperoleh serbuk nata de pina. Serbuk ini diasetilasi dengan anhidrida asetat (1:5) selama 2 jam untuk memperoleh serpihan selulosa asetat. Membran dibuat dengan melarutkan selulosa asetat dalam larutan diklorometana, lalu dianalisis dengan spektroskopi inframerah transformasi Fourier (FTIR) dan mikroskop elektron susuran(SEM).
ABSTRACT
ASTIKA TRESNAWATI. Study of Fourier Transform Infrared Spectroscopy and
Scanning Electron Microscope of The Cellulose Acetate Membrane from Pineapple Waste. Under the direction of BETTY MARITA SOEBRATAand SRI MULIJANI.
Pineapple production in Indonesia increases annually. Only 53% of pineapple can be consumed and the rest is thrown away. Pineapple peel can be converted into nata de pina
to get a more valuable product. Next, nata de pina can be used as a raw material to produce membrane.
This research begun with preparing nata de pina, purifying it to obtainthe nata de pina powder. The powder were acetylated with acetic anhydride (1:5) for 2 h, to get cellulose acetate flakes. The membran was formed by dilluting cellulose acetate in dichloromethane solution and analyzed with Fourier transform infrared spectroscopy (FTIR) and scanning electron microscope (SEM).
KAJIAN SPEKTROSKOPI INFRAMERAH TRANSFORMASI
FOURIER DAN MIKROSKOP SUSURAN ELEKTRON
MEMBRAN SELULOSA ASETAT DARI LIMBAH NANAS
ASTIKA TRESNAWATI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Kajian Spektroskopi Inframerah Transformasi Fourier dan Mikroskop Susuran Elektron Membran Selulosa Asetat dari Limbah Nanas
Nama : Astika Tresnawati NIM : G44201077
Menyetujui:
Pembimbing I, Pembimbing II,
Betty Marita Soebrata, S.Si, M.Si. Dra. Sri Mulijani, M.S. NIP 131694523 NIP 131950978
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Dr. Ir. Yonny Koesmaryono, M.S. NIP 131473999
Penelitian ini didanai oleh Program Hibah Kompetisi A
2, Departemen Kimia,
PRAKATA
Alhamdulillah, segala puji bagi Allah SWT, karena atas rahmat dan karunia-Nya Penulis dapat menyelesaikan karya ilmiah ini. Karya ilmiah ini berjudul Kajian FTIR dan SEM Membran Selulosa Asetat Berbahan Dasar Hasil Fermentasi Limbah Ananas comosus, yang dilaksanakan pada bulan Juni sampai dengan November 2005 bertempat di laboratorium Kimia Anorganik dan Kimia Organik, IPB.
Penulis mengucapkan terima kasih kepada berbagai pihak yang telah membantu terselesaikannya karya ilmiah ini, di antaranya Ibu Betty Marita Soebrata, S.Si, M.Si dan Dra. Sri Mulijani, MS selaku pembimbing yang telah banyak memberikan masukan dan pengarahan kepada penulis, juga kepada Kak Budi Arifin, S.Si, Bapak Drs. Ahmad Sjahriza, Bapak Muhammad Farid, S.Si, dan Bapak Rudi Heryanto, M.Si atas diskusi-diskusi berharga yang berkaitan dengan penelitian ini; laboran: Pak Sawal, Om Em, Pak Sabur, Pak Caca, dan Mba Nur; dan teman-teman seperjuangan: Andri, Ebink, Rene, Riya, BT, Akbar, dan Atik I serta rekan-rekan satu Lab. : Daeng, Aldi, Dyah, dan Eka.
Ungkapan terima kasih juga penulis haturkan kepada keluarga: papa, mama, ceu Ella, ceu Ira, kak Heri, ceu Wiwit, dan kang Tami atas doa dan semangat yang diberikan kepada penulis. Ungkapan terima kasih yang terdalam juga kepada Jaka atas segala doa, nasihat, dorongan, semangat, senyum, cinta, dan kasih sayangnya kepada penulis. Ucapan terima kasih juga disampaikan kepada Ika, Maya, Woro, Anie, dan keluarga Cinta atas keceriaan dan persahabatan yang telah terjalin. Terima kasih kepada Steven, Yanshen dan rekan-rekan Kimia 37, 38, dan 39 serta Keluarga Besar M20 (Mba Atin, Teh Imas, Mba Yayu, Kak Ullie, Mba Eva, Eris, Irma, Aan, Yance, Ika, dan Geril) atas canda tawa dan semangat yang diberikan kepada penulis.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, Februari 2006
RIWAYAT HIDUP
Penulis dilahirkan di Bengkulu pada tanggal 10 Agustus 1983 sebagai anak keempat dari pasangan Asri Usman Tanjung dan Wahyuwati. Tahun 2001, Penulis lulus dari SMU Negeri 5 Bengkulu, dan pada tahun yang sama masuk Institut Pertanian Bogor (IPB) melalui Ujian Masuk Perguruan Tinggi Negeri (UMPTN) pada Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, IPB. Tahun 2004, Penulis mengikuti kegiatan Praktik Lapangan di Pusat Penelitian dan Pengembangan Teknologi Isotop dan Radiasi–Badan Tenaga Atom Nasional (P3TIR-Batan), Pasar Jumat, dengan judul Pemantauan Pencemaran Surfaktan di Teluk Jakarta.
DAFTAR ISI
Halaman
DAFTAR TABEL ... x
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Ananas comosus ... 1
Selulosa Bakteri... 1
Selulosa Asetat ... 2
Membran... 3
Karakterisasi Membran... 4
Membran Selulosa Asetat ... 5
BAHAN DAN METODE Bahan dan Alat ... 5
Metode ... 5
HASIL DAN PEMBAHASAN Pemurnian selulosa. ... 7
Asetilasi ... 8
Membran Selulosa Asetat ... 9
Analisis FTIR ...10
Analisis SEM ...11
SIMPULAN DAN SARAN Simpulan ...13
Saran ...13
DAFTAR PUSTAKA...13
DAFTAR TABEL
Halaman
1 Syarat mutu selulosa asetat ... 2
2 Hubungan derajat substitusi selulosa asetat, kadar asetil, dan aplikasinya. ... 3
DAFTAR GAMBAR
Halaman 1 Struktur selulosa. ... 22 Reaksi asetilasi selulosa asetat ... 2
3 Ilustrasi penggembungan struktur selulosa ... 7
4 SEM membran selulosa contoh ... 8
5 SEM membran selulosa komersial (referensi)... 8
6 Membran selulosa asetat contoh... 9
7 FTIR membran selulosa murni ...10
8 FTIR membran selulosa asetat contoh ...11
9 FTIR membran selulosa asetat komersial (referensi)...11
10 SEM membran selulosa asetat contoh ...11
11 SEM membran selulosa asetat komersial...12
12 SEM membran selulosa asetat komersial (referensi) ...12
DAFTAR LAMPIRAN
Halaman 1 Diagram alir penelitian. ...162 (a) Penetapan kadar air selulosa; (b) Penetapan kadar á-selulosa ...17
3 Penetapan kadar air dan kadar asetil selulosa asetat ...18
4 Data kadar air dan kadar á-selulosa ...19
5 (a) Data kadar air selulosa asetat contoh dan komersial; (b) Data kadar asetil selulosa asetat contoh dan komersial ...20
PENDAHULUAN
Usaha peningkatan hasil pertanian di Indonesia untuk mendapatkan produk yang bernilai ekonomis tinggi telah banyak dilakukan. Salah satunya adalah pengolahan limbah pertanian. Limbah pertanian meru-pakan bagian dari produk pertanian yang belum banyak dimanfaatkan. Limbah pertanian dapat dimanfaatkan sebagai bahan baku untuk menghasilkan produk yang bernilai ekonomis tinggi.
Menurut BPS (2005), produksi nanas di Indonesia tahun 2001, 2002, dan 2003 masing-masing mencapai 494.968 ton, 555.588 ton, dan 677.089 ton. Satu buah nanas yang dapat dikonsumsi hanya 53%-nya saja, sedangkan sisanya dibiarkan menumpuk begitu saja tanpa mengalami pengolahan lebih lanjut. Hal ini menimbulkan permasalahan lingkungan, sehingga diperlukan upaya pemanfaatan limbah kulit nanas. Salah satu cara adalah dengan mengolah kulit nenas menjadi produk nata de pina yang kemudian dapat diolah lebih lanjut menjadi suatu membran.
Nata adalah biomassa yang sebagian besar terdiri dari selulosa, berbentuk agar, dan berwarna putih. Massa ini berasal dari pertumbuhan Acetobacter xylinum pada permukaan media cair yang asam dan mengandung gula. Nata dapat dibuat dari bahan baku air kelapa, sari buah nanas, dan limbah cair pengolahan tahu (whey tahu).
Nata yang dibuat dari air kelapa disebut dengan nata de coco, dari sari buah nanas disebut dengan nata de pina, dan yang dari whey tahu disebut dengan nata de soya. Bentuk, warna, tekstur dan rasa semua jenis nata tersebut tidak berbeda (Warintek 2005).
Penelitian nata de pina pernah dilakukan sebelumnya oleh Susanto et al. (2000) dan Rulianah (2002) yang membuat nata de pina
dari kulit nanas. Akan tetapi, belum ditemukan penelitian tentang nata de pina
yang diolah lebih lanjut menjadi selulosa asetat, seperti beberapa penelitian sebelumnya yang pernah dilakukan tentang aplikasi dari
nata de coco dan nata de soya. Penelitian
yang dilakukan Yulianawati (2002) dan Arifin (2004) adalah mengolah nata de coco menjadi selulosa asetat. Safriani (2000) juga melakukan penelitian mengubah nata de soya
menjadi produk biopolimer yang berupa film tipis. Penelitian-penelitian yang pernah dilakukan tersebut dapat dijadikan acuan untuk mengolah nata de pina menjadi selulosa
asetat dan lebih lanjut dapat diaplikasikan menjadi membran.
Membran dapat ditemui pada hampir semua industri, seperti industri tekstil, makanan, minuman, dan lain sebagainya. Membran mengalami proses lebih lanjut berdasarkan pertimbangan keselarasan teknik dan nilai ekonomisnya. Perkembangan teknologi membran dari waktu ke waktu semakin meningkat sesuai dengan berkembangnya berbagai metode yang digunakan untuk mengkarakterisasinya, se-perti FTIR dan SEM. SEM dapat memperlihatkan topografi dan morfologi membran dengan batas resolusi sampai dengan ukuran mikrometer, sedangkan FTIR dapat mengidentifikasi senyawa berdasarkan informasi dalam memprediksi gugus fungsi berupa spektrum.
Penelitian ini bertujuan mengidentifikasi sifat membran selulosa asetat melalui analisis FTIR dan SEM. Analisis ini bermanfaat untuk menentukan jenis membran yang dibentuk. Hipotesis penelitian ini adalah nata de pina
merupakan selulosa bakteri yang dapat dijadikan bahan baku dalam pembuatan membran selulosa asetat
.
TINJAUAN PUSTAKA
Ananas comosus
Ananas comosus yang dikenal sebagai
nanas di Indonesia termasuk dalam divisi
Plantae, subdivisi spermatophyta, klas
Monocotyledonae, ordo Farinosae, famili
bromoliaceae, genus Ananas, dan spesies
comosus (Collins 1968).
Bagian dari buah nanas adalah kulit, daging, dan hati. Kulit nanas di berbagai industri merupakan bagian yang paling melimpah dan tidak mengalami pengolahan lebih lanjut. Bagian kulit inilah yang akan digunakan pada penelitian ini.
Nanas mengandung nutrisi yang lengkap untuk pertumbuhan bakteri A. xylinum. Pertumbuhan A. xylinum dipengaruhi oleh beberapa faktor antara lain pH, suhu, sumber nitrogen, dan sumber karbon.
Selulosa Bakteri
Tahun 1886, untuk pertama kalinya dilaporkan oleh Brown bahwa galur
Acetobacter tertentu dapat menghasilkan
2
(BC), pada permukaan media air dalam sistem kultur diam (Toyosaki et al. 1995). A.
xylinum, yang baru-baru ini diklasifikasi ulang
sebagai Gluconobacter xylinus, ialah jenis
Acetobacter penghasil-selulosa yang telah
banyak dipelajari (Krystynowicz dan Bielecki 2001). Unit ulang dari rantai struktur selulosa adalah unit selobiosa. Struktur selulosa terlihat pada Gambar 1.
Gambar 1 Struktur selulosa (Fengel dan Wegener 1989).
Kekhasan BC
Produk BC dari suatu galur Acetobacter
adalah murni secara kimiawi, yaitu bebas dari lignin dan hemiselulosa serta produk-produk biogenik lainnya (Masaoka et al. 1993 & Geyer et al. 1994). Pemurnian BC dari sel-sel bakteri di dalamnya dapat dilakukan dengan perlakuan menggunakan NaOH 0.1 N, selama 20 menit, pada suhu 80oC (Toyosaki et al. 1995).
Selulosa Asetat
Selulosa memiliki tiga gugus hidroksil per residu anhidroglukosa. Indikator kemurnian suatu selulosa dapat dinyatakan sebagai kadar á-selulosa (Tanaka et al. 2000). á-Selulosa adalah komponen polisakarida yang setelah dilarutkan dengan NaOH 17,5% (b/v), tetap tidak larut ketika basa diencerkan ke sekitar 8% (b/v) (Fengel dan Wegener 1989). â -Selulosa adalah komponen selulosa yang larut dalam larutan alkali, namun dapat terendap kembali jika larutan tersebut dinetralkan, sedangkan ã-selulosa adalah komponen selulosa yang larut dalam larutan alkali dan tetap larut jika larutan tersebut dinetralkan (Etherington dan Roberts 2005). K adar á-, â-, dan ã-selulosa dibedakan hanya dari kelarutannya dalam NaOH.
Selulosa dapat direaksikan melalui reaksi-reaksi seperti esterifikasi, eterifikasi dan lain-lain. Selulosa asetat yang dihasilkan harus memenuhi syarat SNI (Tabel 1).
Tabel 1 Syarat mutu selulosa asetat (SNI 1991)
Parameter Persyaratan Kadar asetil
Kekentalan intrinsik (pelarut aseton) Kestabilan terhadap kalor
39.0-40.0% 1.5-1.8 dl/g
Tidak terjadi pengarangan saat dipanaskan (180ºC, 8 jam); perubahan kekentalan
intrinsik akibat pemanasan dicantumkan
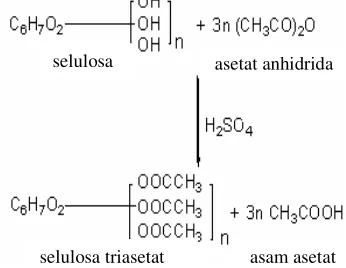
Salah satu bentuk esterifikasi adalah asetilasi selulosa dengan menggunakan asam asetat yang menghasilkan selulosa asetat (dapat dilihat pada Gambar 2.
Gambar 2 Reaksi asetilasi selulosa asetat (Anonim 2005).
Selulosa asetat merupakan ester organik selulosa yang berupa padatan tidak berbau, tidak beracun, tidak berasa, dan berwarna putih yang dibuat dengan mereaksikan selulosa dengan bantuan asam sulfat sebagai katalis (Kroschwitch 1990). Menurut Mark et al. (1965), produk-produk yang terbuat dari plastik selulosa asetat di antaranya adalah gagang obeng, gagang pisau, rambu-rambu untuk di dalam dan luar ruangan, pipa gas alam, tombol-tombol radio dan televisi, kemasan, jendela pada amplop, pena, pensil, boneka, dan mainan lainnya. Aplikasi ini bergantung pada jenis selulosa asetat yang diperoleh yang dapat dilihat dari derajat substitusinya. Hubungan antara aplikasi selulosa asetat terhadap pelarut dan derajat substitusi disenaraikan pada Tabel 2.
n
selulosa asetat anhidrida
3
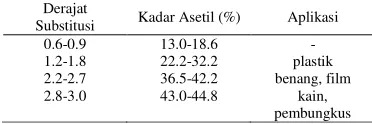
Tabel 2 Hubungan derajat substitusi selulosa asetat, kadar asetil, dan aplikasinya (Fengel dan Wegener 1989)
Derajat
Substitusi Kadar Asetil (%) Aplikasi 0.6-0.9 1.2-1.8 2.2-2.7 2.8-3.0 13.0-18.6 22.2-32.2 36.5-42.2 43.0-44.8 - plastik benang, film kain, pembungkus Praperlakuan
Sebelum proses asetilasi, perlu dilakukan tahap praperlakuan dengan memberikan aktivasi menggunakan asam asetat glasial. Nisbah asam asetat dan selulosa bergantung pada selulosa dan jumlah katalis (H2SO4)yang
digunakan. Tujuan aktivasi ialah untuk meningkatkan reaktivitasnya, sehingga me-mudahkan difusi asam sulfat sebagai reagen asetilasi ke dalam serat selulosa.
Asetilasi
Proses asetilasi bertujuan mensubstitusi gugus hidroksil selulosa dengan gugus asetil, sehingga terbentuk selulosa asetat. Asetilasi dilakukan dalam kondisi asam dengan pereaksi anhidrida asetat dan katalis H2SO4.
Reaksi asetilasi adalah reaksi eksoterm, sehingga suhu harus dijaga kurang dari 50oC, supaya tidak terjadi degradasi rantai selulosa dan menghindari penguapan (Kirk dan Othmer 1993).
Proses asetilasi berlangsung selama 5-10 jam atau sampai materi larut sempurna dalam campuran asetilasi. Selanjutnya, selulosa asetat yang diperoleh ditentukan kadar asetilnya, yang kemudian dapat diketahui seberapa besar derajat substitusi gugus hidroksil dengan asetil (Tabel 2). Arifin (2004) melakukan asetilasi dengan modifikasi prosedur Geyer et al. (2004), menghasilkan selulosa asetat pada lama asetilasi 1 jam dan kadar asetil 36.27%. Yulianawati (2002) melakukan proses asetilasi lebih lama dari Arifin dengan variasi waktu asetilasi 2, 4, dan 6 jam dan menghasilkan selulosa asetat dengan perlakuan terbaik dengan lama asetilasi 2 jam; rendemen 14.95%; dan kadar asetil 43.90%.
Hidrolisis
Tujuan utama hidrolisis ialah untuk menghilangkan sebagian gugus asetil dari selulosa triester. Laju hidrolisis dikendalikan oleh suhu dan konsentrasi katalis. Konsentrasi katalis yang lebih tinggi akan meningkatkan laju hidrolisis. Suhu yang biasa digunakan pada proses ini antara 40−80oC. Kandungan
air dan asam asetat yang ditambahkan pada saat hidrolisis bervariasi antara 20−25% dari
bobot total cairan dan bergantung pada suhu serta produk akhir yang diinginkan (Fengel dan Wegener 1989).
Pengendapan
Sebelum proses pengendapan, larutan produk biasanya dicampurkan dengan asam asetat encer bertujuan menurunkan viskositas. Jika diinginkan endapan dalam bentuk serpihan (flake), larutan produk dituangkan ke dalam asam asetat encer (10−15%) yang diaduk dengan kuat (Kirk dan Othmer 1993).
Membran
Membran adalah lapisan semipermeabel berupa padatan polimer tipis yang menahan pergerakan bahan tertentu (Scott dan Hughes, 1996). Menurut Osada dan Nakagawa (1992), membran merupakan lapisan semipermeabel yang tipis dan dapat digunakan untuk memisahkan dua komponen dengan cara menahan dan melewatkan komponen tertentu melalui pori-pori. Menurut Eryan (2004), membran adalah film tipis dari suatu material berpori yang dapat digunakan untuk beberapa proses pemisahan.
Klasifikasi Membran
Menurut Mulder (1996) dan Wenten (1999), klasifikasi membran ada beberapa macam, yaitu berdasarkan material asal, morfologi, bentuk, dan fungsi.
Material Asal
Membran bedasarkan material dibagi menjadi dua golongan, yaitu membran alamiah dan membran sintetis.
Membran alamiah terdapat pada sel tumbuhan, hewan, dan manusia, sedangkan membran sintetis dibuat sesuai dengan kebutuhan dan sifatnya disesuaikan dengan membran alamiah. Membran sintetis dibagi lagi menjadi membran organik dan anorganik.
Morfologi
4
bawah makin besar dan lapisan aktif (ketebalan 0,2-1,0 ìm) memiliki pori yang rapat. Menurut Scott dan Hughes (1996), membran asimetrik menggunakan bahan pendukung bagi lapisan aktif yang berada di atasnya dan berfungsi untuk kebutuhan mekanik.
Bentuk
Bentuk membran dapat dibagi menjadi dua kelompok, yaitu membran datar dan tubular. Membran datar memiliki bentuk melebar dan penampang lintang yang besar. Ada beberapa macam membran datar, antara lain membran datar yang terdiri atas satu lembar; membran datar bersusun, terdiri atas beberapa lembar yang disusun bertingkat dengan menempatkan pemisah di antara dua membran yang berdekatan; dan membran spiral bergulung merupakan membran yang disusun bertingkat dan digulung dengan pipa sentral membentuk spiral. Membran tubular terbagi menjadi tiga, yaitu membran serat berongga (diameter <0.5 mm), membran kapiler (diameter 0.5-5.0 mm), dan membran tubular (diameter >5.0 mm).
Fungsi
Ada beberapa macam membran berdasarkan fungsinya, yaitu membran mikrofiltrasi, ultrafiltrasi, osmosis balik, dialisis, dan elektrodialisis.
Mikrofiltrasi merupakan proses pemisahan antar partikel (bakteri, ragi) dan berfungsi untuk menyaring makromolekul > 500.000 g/mol atau partikel berukuran 0.1-10 ìm. Tekanan yang digunakan 0.5-2.0 atm. Membran ini memiliki struktur asimetrik dan simetrik.
Ultrafiltrasi merupakan proses pemisahan antar molekul dan berfungsi menyaring makromolekul >5000 g/mol atau partikel berukuran 0.001-0.1 ìm. Tekanan yang digunakan 1.0-3.0 atm. Membran ini memiliki struktur asimetrik.
Fungsi membran osmosis balik adalah menyaring garam-garam organik >50 g/mol atau partikel berukuran 0.0001-0.001 ìm. Tekanan yang digunakan, yaitu 8.0-12.0 atm. Fungsi dari membran dialisis adalah memisahkan larutan koloid yang mengandung elektrolit dengan berat molekul kecil. Berbeda dengan membran elektrodialisis yang berfungsi memisahkan larutan dengan membran melalui pemberian muatan listrik. Gaya pendorongnya adalah gaya gerak listrik.
Karakterisasi Membran
SEM
Analisis SEM merupakan metode yang tepat untuk mengkarakterisasi membran mikrofiltrasi. Batas resolusi mikroskop elektron 0.01 ìm (10 nm) dan sekitar 0.005 ìm (5 nm). Prinsip SEM adalah elektron dengan energi kinetik tinggi dipancarkan dari sumbernya mengenai sampel membran. Pantulan elektron ini (elektron kedua) akan ditangkap oleh detektor, sehingga membentuk bayangan tertentu. Tampilan permukaan sampel bergantung pada intensitas pengukuran elektron kedua (Darwo 2003).
Teknik SEM pada hakikatnya merupakan pemeriksaan dan analisis permukaan. Tampilan merupakan data yang berasal dari permukaan atau lapisan yang tebalnya sekitar 20 ìm dari permukaan. Hasil foto SEM merupakan gambar topografi dengan segala tonjolan, lekukan, atau lubang permukaan. Gambar tersebut diperoleh dari penangkapan elektron sekunder yang dipancarkan oleh spesimen melalui celah logam lensa magnetik, membentuk cahaya monokromatik. Sinar yang mengenai sampel menyebabkan terjadinya interaksi yang menimbulkan pancaran elektron baru. Sinyal elektron yang dihasilkan ditangkap oleh detektor, kemudian diteruskan ke monitor. Pada monitor akan diperoleh gambar yang khas yang memperlihatkan struktur permukaan spesimen. Selanjutnya, gambar di monitor dapat dipotret dengan menggunakan film hitam putih atau dapat pula direkam ke dalam suatu disket. (Sutiani 1997). Sebelum dianalisis dengan SEM, sampel harus dipreparasi terlebih dahulu. Hal-hal yang harus dipenuhi untuk menyiapkan sampel, yaitu menghilangkan seluruh pelarut, air, atau bahan lain yang dapat menguap ketika di dalam vakum dan menipiskan sampel yang akan dianalisis. Jika spesimen merupakan suatu isolator, seperti tanaman, kuku jari, dan keramik, maka perlu dilapisi dengan bahan konduktor. Bahan konduktor yang biasa digunakan adalah emas, perak, dan aliansi emas dan paladium. Pelapisan dilakukan dalam ruang penguapan vakum (Sutiani 1997).
FTIR
5
0.78 sampai 1000 nm atau bilangan gelombang dari 12800 sampai 10 cm-1 (Nur dan Adijuwana 1989). Gugus fungsi yang ada pada rantai selulosa adalah hidroksil. Gugus tersebut terikat pada setiap unit glukosa. Gugus hidroksil pada selulosa tidak hanya menentukan struktur supramolekul, tetapi juga menentukan sifat fisika dan kimia selulosa (Fengel dan Wegener 1989).
FTIR merupakan instrumen standar untuk analisis secara kimia. FTIR dapat memperlihatkan informasi dalam mempre-diksi dan mengidentifikasi gugus fungsi yang ada dalam suatu senyawa. FTIR merupakan cara yang paling mudah dan cepat untuk melihat senyawa-senyawa kimia pada permukaan membran. Hal tersebut dapat dilakukan dengan menganalisis spektrum-spektum yang dihasilkan sesuai dengan puncak-puncak yang dibentuk dari suatu gugus fungsi. (Anonim tt).
Membran Selulosa Asetat
Selulosa asetat merupakan salah satu bahan dasar membran asimetrik, baik untuk osmosis balik, ultrafiltrasi dan mikrofiltrasi. Pembuatan selulosa asetat biasanya dilakukan dengan cara pembalikan fasa melalui proses pencelupan (Mulder 1996).
Perkembangan pembuatan membran dengan cara pembalikan fasa dilakukan oleh Loeb dan Sourajan. Membran yang dihasilkan sering disebut sebagai membran tipe Loeb-Sourajan. Membran yang dihasilkan berstruktur asimetrik, terdiri atas lapisan tipis setebal 0.02−0.05 µm didukung substrat pori dengan ketebalan 50−100 µm.
Tahapan pembuatan membran menggu-nakan metode pembalikan fasa diawali dengan pembuatan larutan homogen dengan kekentalan yang diinginkan, lalu pencetakan larutan polimer sebagai lapisan tipis. Selanjutnya, penguapan sebagian pelarut dari polimer. Setelah itu, pengendapan polimer dengan cara pencelupan. Tahap akhir adalah perlakuan suhu untuk menyusutkan ukuran pori. Tahapan di atas berpengaruh terhadap penampilan akhir membran yang dihasilkan.
BAHAN DAN METODE
Bahan dan Alat
Bahan–bahan yang diperlukan dalam penelitian ini ialah starter (bakteri
Acetobacter xylinum) yang diperoleh dari
pengusaha nata de coco di daerah Cipaku Bogor, kulit buah nenas yang diperoleh dari limbah penjual rujak depan kampus IPB Baranangsiang, selulosa asetat komersial teknis, kertas pH, kertas koran, kertas saring, karet pengikat, cuka pekat teknis 98% (v/v), asam asetat glasial 100% (v/v), anhidrida asetat 98% (v/v), gula pasir, pelarut diklorometana, NaOH pelet, HCl 25% (b/b), etanol teknis 95% (v/v), H2SO4 95-97% (v/v),
air suling, (NH4)2SO4, K2Cr2O7, Na2CO3, dan
(COOH)2.2H2O.
Alat-alat yang digunakan dalam penelitian ini ialah alat-alat gelas laboratorium, kaca masir, pompa vakum, hot plate, oven, penangas, pengaduk magnetik, blender
Philips, panci, pisau pemotong, wadah fermentasi berukuran 30x20x4,5 cm3 merk Komet Star Plastics jenis Tripoly nomor 3, neraca analitik, sentrifus Hermle Z300 (Labnet), pengaduk magnetik, plat kaca, pelapis ion Polaron SC 7610 Sputter Coater, SEM LEO 4201 Oxford Link Penafet model 6599, dan FTIR-8201PC Shimadzu FTCOM-1. Analisis FTIR dilakukan di laboratorium
Quality Assurance, PT Abbot, Cibinong dan
SEM dilakukan di Laboratorium SEM, Departemen Metalurgi dan Material, Fakultas Teknik, Universitas Indonesia, Jakarta.
Metode
Diagram alir penelitian ini dapat dilihat secara garis besar pada Lampiran 1.
Pembuatan Selulosa Bakteri (Nata de pina) (Susanto et al. 2000)
6
dingin dan diinkubasikan pada suhu kamar selama 4-5 hari.
Pemurnian Selulosa (Safriani 2000)
Nata de pina lembaran dipotong –potong
dengan ukuran sekitar 4x5 cm. Potongan nata
ini selanjutnya direbus dalam air mendidih selama ±20 menit. Setelah itu, nata direndam dalam larutan NaOH 1% (v/v) pada suhu kamar selama 24 jam, kemudian dinetralkan dengan perendaman dalam asam asetat 1% (v/v) selama 24 jam. Produk selanjutnya dicuci beberapa kali dengan air, kemudian disaring-vakum untuk menarik air sampai diperoleh lembaran nata yang tipis. Lembaran ini dikeringkan pada suhu kamar selama 1-2 hari. Nata de pina kering selanjutnya dihancurkan dengan menggunakan blender, sehingga berbentuk serbuk yang berukuran 40 mesh. Serbuk nata de pina kering ini selanjutnya diuji kadar air dan kadar á -selulosa (Lampiran 2).
Pembuatan Selulosa Asetat
Pembuatan selulosa asetat pada penelitian ini merupakan modifikasi prosedur pembuatan selulosa asetat yang dilakukan oleh Arifin (2004). Prosedur pembuatan selulosa asetat sebagai berikut:
Praperlakuan
Selulosa yang dihasilkan dari tahap pemurnian sebanyak 0,9 gram dicampurkan dengan 100 ml asam asetat glasial di dalam botol bertutup ganda, lalu dikocok dengan
shaker (200 rpm, 20 menit) dengan
pengadukan kuat beberapa menit pertama. Selanjutnya, selulosa disaring-vakum dan diperas sekuat mungkin. Perlakuan ini dilakukan duplo. Hasil perasan yang kedua dikembalikan ke dalam botol bertutup ganda dan direndam dalam 50 ml asam asetat glasial murni selama 3 jam pada suhu kamar. Botol dikocok dengan shaker (200 rpm). Setelah 3 jam, selulosa disaring-vakum dan diperas sekuat mungkin.
Asetilasi
Asam asetat glasial 95% dan H2SO4
95-97% ditambahkan pada selulosa hasil aktivasi dengan perbandingan 100:1 (10.1 ml). Campuran diaduk kuat selama 1 menit. Anhidrida asetat 98% ditambahkan dengan nisbah 1:5 tetes demi tetes, kemudian diaduk
dalam penangas bersuhu 40oC. Larutan dibiarkan selama 2 jam dalam penangas bersuhu 40 oC. Waktu 2 jam dihitung sejak ditambahkannya anhidrida asetat 98%.
Hidrolisis
Setelah proses asetilasi, campuran air dan asam asetat glasial (2:1) sebanyak 2,4 ml ditambahkan ke dalam larutan hasil asetilasi dan dilakukan pengadukan pada beberapa menit pertama. Larutan dibiarkan pada suhu 40 oC selama 30 menit dihitung sejak ditambahkannya asam asetat encer.
Pemurnian
Larutan hasil hidrolisis dipisahkan menggunakan sentrifus selama 15 menit dengan kecepatan 4000 rpm untuk memisahkan kotoran sisa asetilasi. Selanjutnya, supernatan dituang ke dalam 500 ml air destilasi yang diaduk kuat dengan pengaduk magnetik. Endapan yang terbentuk disaring vakum. Serbuk selulosa asetat ini dinetralkan pH-nya dengan NaHCO3 1 N, lalu
dicuci dengan air destilata. Hasil produk selulosa asetat ini selanjutnya dimasukkan ke dalam gelas piala yang telah diketahui bobot kosongnya, lalu dimasukkan ke dalam oven
dengan suhu ±50 °C selama 24 jam. Produk selulosa asetat yang dihasilkan selanjutnya dianalisis kadar air dan kadar asetilnya (Lampiran 3), lalu dihitung rendemennya dengan menggunakan persamaan sebagai berikut:
(1-M2) (W3 – W2)
Rendemen (%) = --- x 100% C(1-M1)W1
dengan: W1 = bobot contoh uji (gram)
M1 = kadar air contoh uji (%)
C = kadar á-selulosa (%)
W2 = bobot gelas piala (gram)
W3 = bobot gelas piala+selulosa
asetat kering (gram), dan
M2 = kadar air selulosa asetat (%).
Pembuatan Membran Selulosa Asetat
7
membuat membran dengan ketebalan yang sama, selanjutnya sebagian pelarut dari polimer diuapkan. Polimer kemudian diendapkan dengan cara pencelupan dalam air. Membran dianalisis dengan FTIR dan SEM.
Karakterisasi Membran
SEM
Suatu silinder logam steril yang diameternya lebih besar daripada ukuran contoh, direkatkan menggunakan double-tip. Penutup sisi lain double-tip diungkit, lalu contoh dengan ukuran 1x1 cm direkatkan. Silinder diletakkan ke dalam pelapis ion untuk divakum selama 3 jam dengan tekanan 0.1 mbar. Setelah 3 jam, contoh dilapisi dengan logam Pt-Au menggunakaan pelapis ion, lalu difoto dengan instrumen.
FTIR
Contoh membran yang berbentuk lembaran dipotong dengan ukuran 3x1,5 cm. Contoh dijepit dengan pinset, lalu diletakkan ke dalam tempat contoh. Tempat contoh itu dimasukkan ke dalam instrumen yang telah dipanaskan terlebih dahulu selama 15 menit, lalu lampu dinyalakan tepat mengenai sampel, dengan bilangan gelombang diatur pada 400-4000 cm-1.
HASIL DAN PEMBAHASAN
Pemurnian Selulosa
Nilai kadar á-selulosa yang diperoleh dalam percobaan ini adalah sebesar 88.72% dan kadar airnya sebesar 7.56% (Lampiran 2). Persentase yang lainnya diperkirakan abu dan â- serta ã-selulosa. á-Selulosa dapat terdegradasi menjadi â-selulosa. Bila kadar á -selulosa menurun, maka beberapa á-selulosa telah terdegradasi menjadi â-selulosa. Akan tetapi, â-selulosa dapat larut kembali dengan peningkatan konsentrasi alkali yang digunakan (Arifin 2004). Nilai ini lebih tinggi jika dibandingkan dengan kadar á-selulosa yang dihasilkan Yulianawati (2002) dan Arifin (2004). Faktor utamanya kemungkinan besar adalah kondisi pengeringan yang berbeda. Nata de pina pada penelitian ini disaring-vakum terlebih dahulu, kemudian dikeringkan pada suhu kamar, sehingga tidak terjadi degradasi rantai selulosa akibat pemanasan pada suhu tinggi.
Kadar air selulosa yang diperoleh sebesar 7.56%. Nilai kadar air ini jauh lebih tinggi
dibandingkan dengan hasil kadar air Yulianawati (2002) dan Arifin (2004). Faktor penyebab perbedaan nilai kadar air ini adalah kondisi suhu pengeringan yang berbeda. Nilai ini juga dianggap cukup tinggi. Kadar air yang rendah dapat meningkatkan reaktivitas selulosa karena gugus hidroksil dalam air lebih reaktif daripada gugus dalam selulosa. Jadi, untuk mendapatkan tingkat reaktivitas yang tinggi dibutuhkan kadar air yang rendah, sehingga proses substitusi dapat berlangsung dengan baik.
K adar á-selulosa dapat ditingkatkan dengan ekstraksi menggunakan alkali Semakin tinggi kadar á-selulosa, maka semakin efektif alkali yang digunakan. Konsentrasi alkali yang digunakan dalam pemurnian ini adalah NaOH 1%. Terjadinya penggembungan struktur selulosa (swelling
process) dikarenakan perendaman dalam
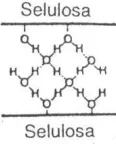
NaOH 1% (b/v). Lalu, penetralan dengan asam asetat 1% akan membuat serat-serat selulosa menjadi lebih terbuka. Proses ini dinamakan merserisasi (Munk 1989). Struktur selulosa yang menggembung merupakan proses perubahan ikatan hidrogen dalam struktur selulosa. Awalnya, ikatan yang terjadi adalah ikatan hidrogen antara selulosa dan selulosa, kemudian berubah menjadi ikatan hidrogen antara selulosa dan air. Ilustrasi penggembungan struktur selulosa dapat dilihat pada Gambar 3.
Gambar 3 Ilustrasi penggembungan struktur selulosa (Fengel dan Wegener 1989)
Struktur selulosa yang menggembung dapat meningkatkan aksesibilitas gugus hidroksil pada selulosa, sehingga proses penetrasi pereaksi ke bagian dalam selulosa menjadi lebih mudah. Hal ini dapat ditegaskan melalui pengamatan dengan mikroskop elektron transmisi (TEM) karena dengan SEM dapat melihat struktur permukaannya saja, sedangkan TEM dapat menunjukkan struktur membran tersebut hingga ke bagian dalam.
8
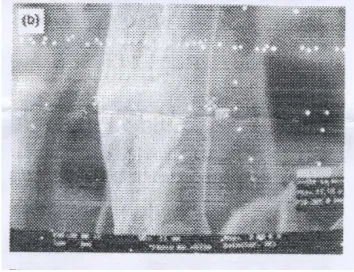
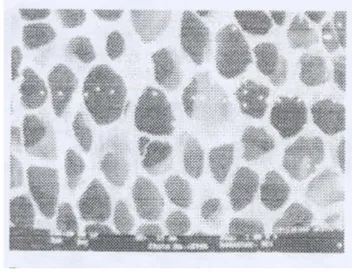
referensi (Meenakshi et al. 2002). Gambar 4 dan 5 menunjukkan keberadaan struktur serat yang dihasilkan dari rantai selulosa. Jika kedua gambar ini dibandingkan (dengan pembesaran yang sama) akan memperlihatkan struktur permukaan membran dengan serat-serat yang berbeda. Struktur permukaan pada membran selulosa contoh tidak begitu jelas karena kemungkinan besar struktur selulosa yang dianalisis terlalu rapat. Hasil analisis SEM hanya memperlihatkan bagian permukaan membran, sehingga tidak dapat dilihat struktur bagian dalam membran yang diduga tidak sama kerapatannya dengan bagian permukaan.
Gambar 4 SEM membran selulosa contoh.
Gambar 5 SEM membran selulosa referensi (Meenakshi P et al. 2002).
Selulosa yang telah direndam dalam NaOH selama 24 jam yang dilanjutkan penetralan dengan asam asetat selama 24 jam akan membuat permukaan selulosa menggembung. Terlalu rapatnya struktur permukaan ini mungkin disebabkan oleh konsentrasi NaOH yang terlalu kecil.
Struktur permukaan SEM membran selulosa contoh berbeda dengan struktur permukaan membran selulosa referensi
disebabkan sumber selulosanya berbeda. Hal ini sesuai dengan yang diungkapkan Safriani (2000) bahwa perbedaan selulosa dapat dilihat dari sumber selulosa yang digunakan. Membran selulosa contoh berasal dari selulosa bakteri, sedangkan membran selulosa referensi berasal dari selulosa tanaman. Serat-serat dari membran selulosa referensi terlihat jauh lebih halus dibandingkan dengan serat-serat pada membran selulosa contoh. Menurut Geyer et al. (1994), selulosa yang bersumber dari bakteri akan menghasilkan pita-pita fibril yang jauh lebih halus daripada selulosa yang bersumber dari tanaman.
Asetilasi
Reaksi asetilasi diawali dengan aktivasi selulosa menggunakan asam asetat glasial sebanyak 50 ml selama 3 jam pada suhu ruang. Asam asetat ini akan menggem-bungkan serat selulosa. Penggembungan serat selulosa akan mengurangi ikatan hidrogen intramolekul antara selulosa dan selulosa yang dapat mempercepat difusi pereaksi asetilasi, yaitu anhidrida asetat. Reaksi esterifikasi yang terjadi berupa penggantian satu, dua, atau tiga gugus hidroksil dari unit glukosa dengan gugus asetil dari asam anhidrida. Selama berlangsungnya reaksi, dibentuk ikatan-ikatan hidrogen baru antara gugus hidroksil asam asetat dan gugus hidroksil selulosa.
Selulosa yang telah diaktivasi diperas sekuatnya dan divakum, sehingga benar-benar bebas air. Kadar air selulosa memengaruhi terhadap jalannya reaksi esterifikasi. Reaksi asetilasi bersifat reversibel, sehingga kadar air selulosa yang terlalu tinggi akan menyebabkan hasil reaksi yang diinginkan tidak tercapai. Kadar air juga akan berpengaruh terhadap anhidrida asetat. Kadar air yang terlalu banyak akan mengakibatkan laju hidrolisis selulosa asetat lebih cepat daripada substitusi.
Suhu asetilasi yang digunakan pada penelitian ini adalah 40°C. Suhu asetilasi harus dijaga di bawah 50°C, sehingga penambahan anhidrida asetat dilakukan tetes demi tetes. Volume peraksi asetilasi yang digunakan adalah 4.5 ml dengan nisbah bobot á-selulosa dan volume anhidrida asetat adalah 1:5. Volume pereaksi sebaiknya tidak digunakan terlalu banyak karena proses akan menjadi tidak ekonomis.
9
kadar asetil yang tinggi. Derajat substitusi adalah jumlah rerata atom H pada gugus hidroksil, yang diubah menjadi gugus asetil, dalam setiap residu anhidro-glukosa (Arifin 2004). Kadar asetil yang diperoleh pada penelitian ini sebesar 43.0% (Lampiran 5b) yang setara dengan kisaran derajat substitusi 2.8-3.0 (Tabel 2). Jenis selulosa asetat yang diperoleh adalah selulosa triasetat. Reaksi yang terjadi pada selulosa triasetat ini diduga mendekati dengan reaksi yang disenaraikan pada Gambar 2 yang juga menghasilkan selulosa triasetat.
Kadar asetil selulosa asetat contoh tidak memenuhi syarat selulosa asetat yang ditetapkan oleh SNI (Tabel 1). Hal ini berarti proses hidrolisis yang dilakukan saat pembuatan selulosa asetat kurang lama. Hidrolisis berfungsi mengurangi sebagian gugus asetil, sehingga diharapkan selulosa asetat yang diperoleh mempunyai nilai kadar asetil seperti yang ditetapkan oleh SNI. Kadar asetil yang tinggi menunjukkan aksesibilitas gugus hidroksil yang tinggi. Walaupun struktur permukaan membran selulosa cukup rapat, namun diperkirakan proses merserisasi yang terjadi pada bagian dalam membran cukup besar. Proses merserisasi menghasilkan penggembungan serat-serat selulosa sampai ke daerah kristalin, sehingga pereaksi dapat berpenetrasi dengan mudah ke bagian dalam selulosa. Hal ini berarti nilai kadar asetil yang tinggi dihasilkan oleh gugus hidroksil di bagian dalam membran.
Kadar air selulosa asetat yang diperoleh sebesar 34.06% (Lampiran 5a) dan rendemen yang diperoleh sebesar 148.33% (Lampiran 6). Sebagai perbandingan ditetapkan juga kadar asetil dan kadar air selulosa asetat komersial masing-masing sebesar 11.51% dan 39.87% (Lampiran 5). Kadar asetil selulosa asetat komersil ini sesuai dengan yang ditetapkan oleh SNI (Tabel 2). Penentuan kadar air selulosa asetat dapat digunakan untuk perhitungan rendemen dan kadar asetil. Nilai kadar air selulosa asetat ini berbeda jauh dari kadar air selulosa asetat yang diperoleh Arifin (2004). Kondisi asetilasi yang tidak sama pada setiap tahapnya dapat menjadi faktor perbedaan kadar air. Selain itu, faktor waktu dan suhu proses pengeringan selulosa asetat juga diduga menjadi sebab utama dari nilai kadar air selulosa asetat yang tinggi.
Membran Selulosa Asetat Pembuatan membran selulosa asetat dilakukan dengan pembalikan fasa. Tahap pencetakan dilakukan di atas pelat kaca dengan gelas pengaduk, sehingga dimungkinkan membran yang dihasilkan mempunyai ketebalan yang tidak sama di setiap sisinya. Selulosa asetat yang diperoleh membentuk lembaran plastik berwarna putih seperti terlihat pada Gambar 6. Selulosa asetat yang dihasilkan larut baik dalam pelarut diklorometana dan dimetilsulfoksida (DMSO), tetapi tidak larut dalam aseton.
Gambar 6 Membran selulosa asetat contoh.
Konsentrasi selulosa asetat yang digunakan pada saat pelarutan membran adalah 14% (b/v), yang telah dioptimasi oleh Yulianawati (2002). Selulosa asetat dengan kisaran derajat substitusi 2.8-3.0 berarti mempunyai lebih banyak gugus asetil dibandingkan dengan gugus hidroksilnya. Banyaknya gugus asetil ini akan membuat sifat nonpolar dari selulosa asetat lebih dominan dibandingkan dengan sifat polarnya, sehingga selulosa asetat ini larut baik dalam diklorometana dibandingkan dengan aseton. Membran selulosa asetat yang larut dalam diklorometana dapat diaplikasikan sebagai kain dan pembungkus (Tabel 2).
10
Analisis FTIR
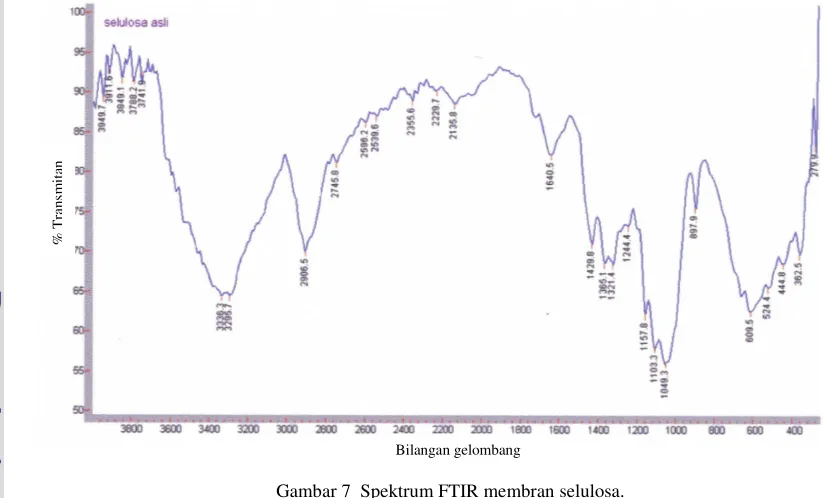
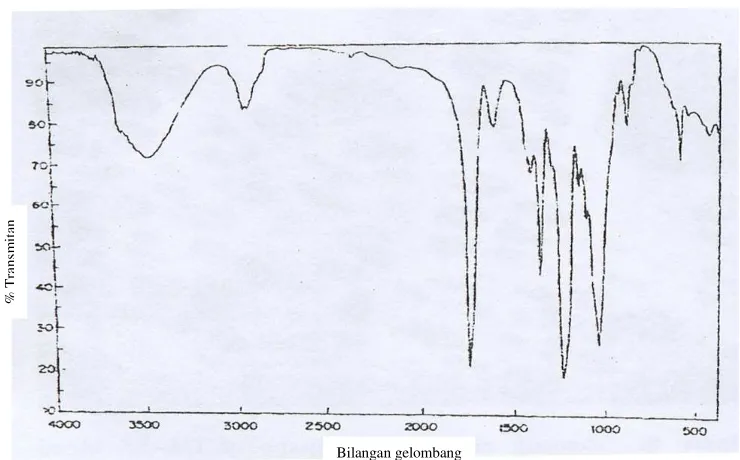
Pembuktian membran selulosa asetat ini menggunakan analisis FTIR. Analisis FTIR ini juga dapat membuktikan bahwa gugus hidroksil telah tersubstitusi oleh gugus asetil melalui reaksi asetilasi. Spektrum FTIR dari membran selulosa murni dan membran selulosa asetat contoh dapat dilihat pada Gambar 7 dan 8. Perbedaan kedua spektrum FTIR ini terletak pada daerah bilangan gelombang 1733.9 cm-1 yang diidentifikasi sebagai gugus C=O ester. Hal tersebut menunjukkan bahwa membran selulosa telah diasetilasi. Spektrum FTIR selulosa asetat referensi (Meenakshi et al. 2002) dapat dilihat pada Gambar 9 yang dapat digunakan sebagai perbandingan.
Spektrum FTIR membran selulosa asetat contoh (Gambar 8) memperlihatkan pita serapan pada beberapa bilangan gelombang. Menurut Shriner et al. (2004), karakteristik vibrasi ulur gugus hidroksil terlihat pada daerah bilangan gelombang 3700-3100 cm-1. Gugus -OH yang dihasilkan ini diduga adalah gugus hidroksil dari selulosa yang tidak tersubstitusi oleh gugus asetil. Pernyataan ini didukung oleh hasil penetapan kadar asetil,
yaitu sebesar 43.0%, setara dengan kisaran derajat substitusi 2.8-3.0, yang berarti belum semua gugus hidroksil dari selulosa tersubstitusi oleh gugus asetil dari anhidrida asetat. Hasil spektrum FTIR membran selulosa asetat (referensi) (Gambar 9) mempunyai derajat substitusi 2.5 (Meenakshi
et al. 2002), yang juga berarti masih ada
gugus hidroksil yang belum disubstitusi, sehingga menghasilkan karakteristik pita serapan gugus hidroksil pada daerah bilangan gelombang sekitar 3500 cm-1. Serapan pada daerah bilangan gelombang 1750-1730 cm-1 adalah untuk vibrasi ulur C=O terlihat dengan puncaknya yang tajam dan pada daerah 1300-1000 cm-1 untuk vibrasi ulur C-O pada puncak 1218 cm-1. Gugus fungsi yang dimiliki oleh spektrum FTIR membran selulosa asetat contoh menyerupai gugus fungsi yang dimiliki spektrum FTIR membran selulosa asetat referensi. Hal ini berarti bahwa proses asetilasi membran selulosa menjadi selulosa asetat dapat dikatakan berhasil. Serapan lainnya ada pada daerah panjang gelombang 1370-1450 cm-1 untuk vibrasi ulur -CH dan pada daerah 2944 cm-1 untuk vibrasi ulur –CH3.
Gambar 7 Spektrum FTIR membran selulosa.
Bilangan gelombang
%
T
ra
n
sm
it
11
Gambar 8 Spektrum FTIR membran selulosa asetat contoh.
Analisis SEM
Hasil gambar SEM membran selulosa asetat contoh (Gambar 10) memperlihatkan struktur permukaan pori yang tidak seragam. Struktur permukaan yang terlihat pada Gam-
bar 10 jauh berbeda dengan Gambar 11 (SEM selulosa asetat komersial). Struktur permukaan membran selulosa asetat contoh menghasilkan bagian gambar yang lebih gelap dari lainnya. Hal ini diperkirakan sebagai bagian sisi membran yang lapisannya lebih tebal dari yang lainnya. Gambar 9 Spektrum FTIR membran selulosa asetat (referensi) (Meenakshi P
et al. 2002).
Bilangan gelombang
%
T
ra
n
sm
it
an
Bilangan gelombang
%
T
ra
n
sm
it
12
Pori membran pada bagian ini tidak begitu jelas disebabkan lapisan yang terlalu tebal.
Gambar 10 SEM membran selulosa asetat contoh.
Lapisan membran yang mempunyai ketebalan yang tidak sama pada setiap sisinya disebabkan proses pembuatan membran ini secara manual menggunakan gelas pengaduk untuk membuat permukaan membran rata. Penetapan kisaran ukuran pori membran selulosa asetat contoh diukur dari pori yang paling besar dan pori yang paling kecil, yaitu pori dengan kisaran ukuran 0.7-6.0 µm, karena diameter pori yang terlihat pada permukaan membran beragam.
Berdasarkan kisaran ukuran porinya, membran selulosa asetat ini dapat digolongkan sebagai membran mikrofiltrasi. Membran mikrofiltrasi dapat digunakan pada proses pemisahan larutan garam, penjernihan sari buah, dan juga mempunyai permeabilitas yang tinggi terhadap air (Anonim tt). Kisaran ukuran diameter pori membran selulosa asetat contoh ini cukup besar karena pori yang terdapat pada membran besarnya tidak seragam. Kemungkinan membran ini untuk diaplikasikan sesuai dengan kegunaannya yang disenaraikan pada Tabel 2, yaitu sebagai kain dan pembungkus, adalah kecil. Hal ini mengakibatkan kegagalan yang akan terjadi cukup besar karena ukuran diameter porinya akan menyebabkan beberapa materi yang diharapkan dapat ditahan, tetapi dapat dilewatkan.
Membran selulosa asetat ini diduga dapat digolongkan sebagai membran asimetrik karena proses pembuatannya dengan metode pembalikan fasa. Membran asimetrik ini mempunyai dua lapisan, yaitu lapisan atas yang kaya polimer dan lapisan penyokong
(lapisan bawah) yang kaya pelarut. Kedua lapisan ini mempunyai ukuran pori yang tidak sama karena pada saat penguapan pelarut pengendapan terjadi lebih dulu dan lebih cepat pada permukaan membran bagian atas, sehingga lapisan ini mempunyai pori-pori yang jauh lebih kecil dibandingkan dengan lapisan bawah membran. Pada tahap pengendapan terjadi difusi pelarut ke dalam air dan meninggalkan ruang-ruang yang membentuk pori-pori membran. Lapisan atas membran memiliki volume pelarut yang lebih sedikit daripada lapisan bawahnya, sehingga menghasilkan porositas yang lebih rendah dan pori-pori yang lebih kecil. Informasi dari hasil analisis SEM tidak dapat menunjukkan struktur permukaan dan ukuran pori lapisan bawah membran.
Gambar SEM selulosa asetat komersial, dan SEM membran asetat dari referensi (Meenakshi et al. 2002) dapat dilihat pada Gambar 11 (perbesaran x3000) dan 12 (perbesaran x1000). Struktur permukaan Gambar 11 terlihat halus dan merata serta ukuran pori yang seragam, begitu pula dengan Gambar 12, yaitu dengan kisaran ukuran 0.3-0.8 µm. Membran ini diduga juga tergolong membran mikrofiltrasi yang mempunyai struktur pori yang asimetrik karena pembuatannya dengan cara pembalikan fasa. Kedua gambar ini merupakan gambar SEM selulosa asetat yang berasal dari sumber yang berbeda. Perbedaan sumber selulosa ini diduga sebagai penyebab perbedaan hasil struktur permukaan dan keseragaman pori membran.
13
Gambar 12 SEM membran selulosa asetat (referensi) (Meenakshi P et al. 2002).
Perbedaan kedua gambar 10 dan 11 ini terletak pada proses pengocokan dan penguapan pelarut pada saat pencetakan. Proses pengocokan yang homogen akan menghasilkan struktur permukaan membran yang lebih terang seperti yang dapat dilihat pada Gambar 11 dan 12. Penguapan pelarut yang cepat akan membentuk pori yang besar, sehingga kerapatannya rendah. Selain itu, suhu ruang juga berpengaruh terhadap proses penguapan pelarut. Suhu ruang yang tidak stabil dan tidak konstan akan membentuk pori yang tidak merata.
SIMPULAN DAN SARAN
Simpulan
Selulosa asetat mempunyai kadar air sebesar 34.06% dan kadar asetil sebesar 43.0% (yang setara dengan kisaran derajat substitusi 2.8-3.0) serta rendemen sebesar 148.33%. Hasil analisis FTIR .yang diperoleh menghasilkan gugus C=O ester pada daerah bilangan gelombang 1733.9 cm-1. Membran selulosa asetat yang terbentuk termasuk membran mikrofiltrasi dengan kisaran ukuran pori sebesar 0.7-6.0
µm. Proses pencetakan membran dengan menggunakan metode pembalikan fasa diduga menghasilkan membran dengan struktur asimetrik.
Saran
Metode pengeringan selulosa yang lebih baik perlu dilakukan untuk memperoleh kadar air selulosa yang rendah. Hal ini juga berlaku pada selulosa asetat, sehingga diperoleh selulosa asetat dengan kadar air
yang rendah. Selain itu, proses pencetakan membran penting dilakukan di ruang atau tempat yang suhunya stabil, sehingga dapat dilihat pengaruh suhu terhadap proses penguapan pelarut dan juga perlu dilakukan pengukuran terhadap ketebalan membran. Metode untuk penyeragaman ukuran pori membran perlu dilakukan, sehingga pori membran yang dihasilkan ukurannya seragam dan merata. Analisis TEM terhadap penampang melintang membran perlu dilakukan untuk melihat bentuk asimetrik membran dan struktur membran bagian dalam.
DAFTAR PUSTAKA
[Anonim]. tt. Commercial RO technology. http://www.osmolabstore.com/OsmoLa bPage.dll?BuildPage&1&1&897 [17 Juni 2005].
[Anonim].2005. Processing routes to acetic anhydride. http://www.chemsystems.co m/newsletters/perp/Jun04_N03S1.cfm [9 Desember 2005].
Arifin B. 2004. Optimasi kondisi asetilasi
selulosa bakteri dari nata de coco
[skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
ASTM.1991. ASTM D871: Standard
Methods of Testing Cellulose Acetate.
Philadelphia: American Society for Testing and Materials.
Awaludin A, Achmadi SS, Nurhidayati N. 2004. Karboksimetilasi Selulosa
Bakteri. Di dalam: Prosiding
Pertemuan Ilmiah Ilmu Pengetahuan
dan Teknologi Bahan; Serpong, 7
September 2004. Jakarta: LIPI BATAN Serpong; 2004. hlm 305-312.
Biro Pusat Statistika. 2005. Produksi buah-buahan Indonesia. http://www.BPS.Go. Id [1 Desember 2005].
Brocks TD. 1983. Membrane Filtration: A
User’s Guide and Reference Manual.
Madison: Science Tech. Inc.
Collins JL. 1968. Pineapple Botany,
Cultivation and Utilization. London:
14
.
Darwati, Natanael CL, Rahayu I. 2002. Pembuatan dan karakterisasi membran ultrafiltrasi dan bahan selulosa asetat dengan variasi konsentrasi aditif (formamida) dan aplikasinya untuk penanganan limbah tapioka [laporan penelitian]. Bandung: Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Padjadjaran.
Darwo AA. 2003. Proyek Pengkajian dan Penelitian Ilmu Pengetahuan Terapan Direktorat Jenderal Departemen
Pendidikan Nasional. Produksi
membran filtrasi dari selulosa mikrobial dan penerapannya dalam industri hasil pertanian [laporan penelitian]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Eryan. 2004. Pemisahan Gas Dengan Membran Berpori. http://www.eryan@ tf.itb.ac.id. 5 Juni 2005.
Etherington, Roberts. 2005. A Dictionary of Descriptive Terminology. http://palim psest.stanford.edu/don/dt/dt0277.html [9 Desember 2005].
Fengel D, Wegener G. 1989. Wood: Chemistry, Ultrastructure, and
Reactions. Berlin: Walter de Gruyter.
Geyer U et al. 1994. Formation, derivatization, and applications of bacterial cellulose. Int J Biol Macromol. 16:343-347.
Kirk RE, Othmer DF. 1993. Encyclopedia of
Polymer Science and Technology. New
York: Interscience.
Kroscwitch JI. 1990. Concise of Polymer
Science and Engineering. New York:
John Wiley and Sons.
Krystynowicz A, Bielecki S. 2001. Biosynthesis of bacterial cellulose and its potential application in the different industries. http://216.239.53.104/search ?q=cache:i9mZFFPoDfYJ:www.biotech nology-pl.com/science/krystnowicz.htm +krystynowicz&hl=id&ie=UTF-8 [25 April 2005].
Mark HF, Gaylord NG, Bikales NM. 1965.
Encyclopedia of Polymer Science and
Technology. New York: Interscience
Publisher.
Masaoka S, Ohe T, Sakota N. 1993. Production of cellulose from glucose by
Acetobacter xylinum. J Ferment
Bioeng. 75:18-22.
Meenakshi P et al. 2002. Mechanical and microstructure studies on the modification of CA film blending with
PS. Bull Mater Sci 25:25-29.
Mulder M. 1996. Basic Principles of
Membrane Technology. Netherland:
Kluwer Academic.
Munk P. 1989. Introduction to
Macromo-lecular Science. New York: John Wiley
and Sons.
Nur MA, Adijuwana H. 1989. Spektroskopi. Bogor: Pusat Antar Universitas, Institut Pertanian Bogor.
Osada Y, Nakagawa T. 1992. Membrane
Science and Technology. New York:
Marcel Dekker.
Pavia, Lampman, Kriz. 2000. Introduction
to Spectroscopy. New York: John Wiley
and Sons.
Rulianah S. 2002. Studi pemanfaatan kulit buah nanas sebagai nata de pina. Jurnal
Bisnis dan Teknologi. 10:8-12.
Safriani. 2000. Produksi biopolymer selulosa asetat dari nata de soya [Tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Scott K, Hughes R. 1996. Industrial Membrane Separation Technology.
London: Blackie Academic and Profesionals.
Shriner R, Hermann C, Morril T, Curtin D, Fuson R. 2004. The Systematic
Identification of Organic Compound.
New York: John Wiley and Sons.
SNI. 1991. SNI 06-2115-1991: Selulosa
Asetat. Jakarta: Dewan Standardisasi
Nasional.
15
nanas: kajian dari sumber karbon dan pengenceran medium fermentasi. Jurnal
Teknologi Pertanian. 1:58-66.
Sutiani A. 1997. Biodegradasi poliblend polistiren-pati [Tesis]. Bandung: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Teknologi Bandung.
Tanaka R, Daud WRW. 2002. Preparation of cellulose pulp from empty fruit bunches of oil palm. http://ss.jircas.af frc.go.jp/kanko/newsletter/nl2003/No.3 4/34p04.pdf [1 Desember 2005].
Toyosaki H et al.. 1995. Screening of bacterial cellulose producing
Acetobacter strain suitable for agitated
culture. Biosci Biotechnol Biochem
59:1498-1502.
Warintek. 2005. Nata de soya. http://warintek/natadesoya/pagan/merint isbisnis/progressio/html [8 Mei 2005].
Wenten IG. 1996. Teknologi Industrial
Membran. Bandung: Penerbit Institut
Teknologi Bandung.
17
Lampiran 1 Diagram alir penelitian
Pembuatan nata de pina
Pemurnian selulosa
Penetapan kadar á-selulosa dan kadar air
Asetilasi
Penetapan rendemen, kadar air, dan kadar asetil
Pembuatan membran selulosa asetat
18
Lampiran 2 (a) Penetapan kadar air selulosa; (b) Penetapan kadar á-selulosa
(a) Penetapan kadar air selulosa
Petri kosong dikeringkan selama 1 jam pada suhu (105±3)°C dalam oven bersirkulasi-udara, lalu ditimbang bobotnya dengan teliti (W1), setelah didinginkan di
dalam desikator. Sebanyak 0,2-1 gram contoh uji ditimbang teliti (W2) di dalam petri itu,
lalu dikeringkan kembali pada suhu yang sama. Bobot (contoh uji+petri) ditetapkan setiap interval 1-3 hari, setelah didinginkan di dalam desikator. Setelah tercapai bobot konstan (W3), kadar air dapat dihtung dengan persamaan berikut:
W3 – W1
Kadar air (%) = ( 1 - ---) x 100% W2
(b) Penetapan kadar á-selulosa (modifikasi Yosep 1999)
Kaca masir kosong dengan 20 ml larutan pencuci sulfat-kromat dan dibiarkan 1-2 hari. Larutan pencuci ini dibuat denganmelarutkan 5 gram K2CrO7 teknis ke dalam 100
ml H2SO4 teknis (aq) 1:1. Setelah pencucian ini, kaca masir menjadi berwarna merah
kecoklatan, lalu dibilas dengan etanol teknis, sehingga sisa kromat tereduksi menjadi berwarna hijau, yang lolos dari kaca masir. Jika kaca masir masih agak kehijauan, dibilas lagi dengan air suling seperlunya. Setelah putih bersih, kaca masir dikeringkan selama 1 jam pada suhu (105±3)°C dalam oven bersirkulasi-udara, lalu ditimbang bobotnya dengan teliti (W1), setelah didinginkan di dalam desikator.
Sebanyak 1 gram contoh uji ditimbang teliti (W2) dalam gelas piala 250 ml. Ke
dalam gelas piala itu, ditambahkan NaOH teknis 17,5% (b/v), lalu diaduk selama 5 menit. Setelah 15 menit, ditambahkan 25 ml air suling, dan diaduk kembali selama 1 menit. Setelah 5 menit, contoh uji disaring-vakum dengan kaca masir tadi, lalu dicuci 12 kali, dengan 25 ml air suling tiap pencucian. Residu dalam kaca masir lalu diberi 40 ml CH3COOH 10%, dan dibiarkan selama 5 menit, sebelum disaring-vakum kembali. Residu
dalam kaca masir dikeringkan pada suhu (105±3)°C dalam oven bersirkulasi-udara, sampai tercapai bobot konstannya (W3). Bobot (residu+kaca masir) itu ditetapkan setiap
interval 1-3 hari, setelah didinginkan di dalam desikator.
Karena sifat sangat-higroskopis dari selulosa penetapan kadar á-selulosa harus disertai penetapan kadar air. Penimbangan contoh uji untuk kedua penetapan ini harus dilakukan bersamaan. Jika kadar air contoh uji dilambangkan M, kadar á-selulosa dapat dihitung dari persamaan berikut ini:
W3 – W1
19
Lampiran 3 Penetapan kadar air dan kadar asetil selulosa asetat
Labu Erlenmeyer 250 ml kosong dikeringkan selama 1 jam pada suhu (105±3)°C dalam oven bersirkulasi-udara, lalu ditimbang bobotnya dengan teliti (W1), setelah
didinginkan di dalam desikator. Sebanyak 0,01-1 gram selulosa asetat ditimbang teliti (W2) di dalam labu itu, lalu dikeringkan kembali pada suhu yang sama selama 24 jam.
Bobot (selulosa asetat+labu) ditetapkan setiap interval 1-3 hari, setelah didinginkan di dalam desikator. Setelah tercapai bobot konstan (W3), kadar air dapat dihtung dengan
persamaan berikut:
W3 – W1
Kadar air (%) = ( 1 - ---) x 100% W2
Penetapan kadar asetil dilakukan dengan modifokasi prosedur ASTM (1991), dan volume larutan-larutan yang dituliskan berikut adalah untuk ±1 gram selulosa asetat. Jika digunakan kurang dari 0,5 gram, digunakan volume sebanyak yang untuk 0,5 gram.
Ke dalam labu, ditambahkan 40 ml etanol 75% (v/v) dengan pipet, lalu labu dipanaskan di penangas air bersuhu 55°C selama 30 menit. Labu dikeluarkan dari penangas, keudian dimasukkan 40 ml NaOH 0,5 N ke dalamnya, dengan buret. Labu dipanaskan kembali selama 15 menit pada suhu yang sama. Selanjutnya, labu ditutup rapat dengan lembaran aluminium dan dibiarkan selama 72 jam pada suhu ruang.
Setelah itu, sisa NaOH dititrasi dengan HCl 0,5 N standar menggunakan indikator fenolftalein (pp) sampai lenyapnya warna merah muda. Sebanyak 1 ml titran dilebihkan dari titik akhir itu, lalu labu ditutup rapat kembali, dan dibiarkan selama 24 jam pada suhu kamar untuk menarik NaOH yang berdifusi ke dalam selulosa teregenerasi. Kemudian sisa HCl dititrasi dengan NaOH 0,5 N standar sampai muncul warna merah muda permanen pertama kali. Titrasi dilakukan dengan hati-hati karena titrat tidak tanwarna, tetapi berwarna kuning muda sampai coklat, bergantung pada warna selulosa asetat setelah penetapan kadar air. Blangko, yaitu perlakuan serupa dengan penetapan kadar asetil contoh, tetapi tanpa menggunakan contoh, dibuat bersamaan dengan contoh. Kadar asetil selulosa asetat dapat dihitung dari persamaan sebagai berikut:
4,305[(D-C)Na + (A-B)Nb]
Kadar asetil (%) = --- (1-M)W
dengan: A = ml NaOH untuk titrasi contoh, B = ml NaOH untuk titrasi blangko, Nb =
20
Lampiran 4 Data kadar air dan kadar á-selulosa contoh
(a) Kadar air
Ulangan W1 (g) W2 (g) W3 (g) Kadar air (%) 1 28,3449 0,3001 28,6241 6,96 2 26,9846 0,3001 27,2602 8,16
Rerata kadar air selulosa contoh adalah sebesar 7,56%.
(b) K adar á-selulosa
Ulangan W1 (g) W2 (g) W3 (g) Kadar á-selulosa (%) 1 29,7774 0,5000 30,2159 94,87 2 29,9398 0,5000 30,3214 82,56
Rerata kadar á-selulosa contoh adalah sebesar 88,72%.
Contoh perhitungan ulangan 1:
28,6241 - 28,3449
Kadar air = (1 - ---) x 100% 0,3001
= 6,96%
6,96% + 8,16% Rerata kadar air = --- 2
= 7,56%
30,2159 - 29,7774
K adar á-selulosa (%) = (---) x 100% (1-0,0756) 0,5000
= 94,87%
94,87% + 82,56% Rerata kadar á-selulosa = --- 2
21
Lampiran 5 (a) Data kadar air selulosa asetat contoh dan komersial; (b) Data kadar asetil selulosa asetat contoh dan komersial
(a) Data kadar air
1. Kadar air selulosa asetat contoh
Ulangan W1 (g) W2 (g) W3 (g) Kadar air (%) 1 108,4644 0,2128 108,6055 33,69 2 98,5472 0,2179 98,6901 34,42
Rerata kadar air selulosa asetat contoh adalah sebesar 34,06%.
2. Kadar air selulosa asetat komersial
Ulangan W1 (g) W2 (g) W3 (g) Kadar air (%) 1 111,0502 0,2141 111,2414 10,70 2 103,1028 0,2145 103,2909 12,31
Rerata kadar air selulosa asetat komersial adalah sebesar 11,51%.
(b) Data kadar asetil
Selulosa asetat
Ulangan W (g) M (%) C (ml) Na (N) A (ml) Nb (N) Kadar asetil (%) Rerata (%) Contoh Komersial 1 2 1 2 0,2128 0,2179 0,2141 0,2145 33,69 34,42 10,70 12,31 17,10 16,85 15,90 15,80 0,4719 0,4719 0,4719 0,4719 0,60 0,60 0,15 0,20 0,4545 0,4545 0,4545 0,4545 40,90 44,52 38,76 39,88 42,71 39,88
Keterangan: ml HCl untuk titrasi blangko: 19,50 ml dan ml NaOH untuk titrasi blangko: 0,10 ml.
Contoh perhitungan untuk selulosa asetat ulangan 1: 108,6055-108,4644
Kadar air = (1 - ---) x 100% 0,2128
= 33,69%
33,69% + 34,42% Rerata kadar air = --- 2
= 34,06%
4,305x[(19,5-17,1)0,4719 + (0,6-0,1)0,4545)]
Kadar asetil (%) = --- (1- 0,3369) x 0,2128
= 40,90%
40,90% + 44,52% Rerata kadar asetil = --- 2
22
Lampiran 6 Perhitungan rendemen selulosa asetat contoh
(1-M2) (W3 – W2)
Rendemen (%) = --- x 100% C(1-M1)W1
(1- 0,3406) x (71,0520 – 67,7288)
Rendemen (%) = --- x 100% 0,8872 x (1- 0,0756) x 1,8013
= 148,33%
dengan: W1 = bobot contoh uji (gram) M1 = kadar air contoh uji (%)
C = kadar á-selulosa (%)
W2 = bobot gelas piala (gram) W3 = bobot gelas piala+selulosa
asetat kering (gram), dan