ABSTRAK
ISMIAINI NURPATRIA PUTRI. Kajian Spektroskopi Inframerah Transformasi Fourier dan Mikroskop Elektron Payaran Membran Selulosa Asetat dari Limbah Cair Tapioka. Dibimbing oleh BETTY MARITA SOEBRATA dan SRI MULIJANI.
Limbah cair tapioka merupakan limbah yang dihasilkan dari proses pengendapan pati atau pemisahan pati dari airnya pada industri tapioka. Limbah ini masih mengandung karbohidrat seperti glukosa sehingga dapat dimanfaatkan sebagai bahan baku untuk membuat selulosa dan membran selulosa asetat (CA). Nata de cassava dibuat melalui proses fermentasi dengan Acetobacter xylinum di dalam media limbah cair tapioka. Nata kemudian dikeringkan dan dihancurkan sehingga diperoleh serbuk selulosa bakteri (BC). Serbuk BC diasetilasi dengan pereaksi anhidrida asetat untuk membentuk serbuk CA. Serbuk CA dilarutkan ke dalam pelarut aseton (sesuai kadar asetil CA yang diperoleh) dengan nisbah 16% b/v kemudian dicetak menjadi membran. Membran CA ini dicirikan menggunakan spektroskopi Inframerah Tranformasi Fourier (FTIR) dan Mikroskop Elektron Payaran (SEM). Hasil analisis spektrum FTIR pada membran CA membuktikan bahwa CA telah terbentuk sesuai dengan adanya pita serapan C karbonil pada daerah 1754.81 cm-1serta C-O asetil pada 1042.34 cm-1. Hasil analisis SEM pada membran CA menunjukkan bahwa membran yang dihasilkan merupakan jenis membran mikrofiltrasi dan asimetrik dengan diameter pori membran sekitar 0.37-0.95 μm. Serbuk CA yang dihasilkan mempunyai kadar air 21.49% dan kadar asetil 40.38% (setara dengan derajat substitusi 2.51).
ABSTRACT
ISMIAINI NURPATRIA PUTRI. Study of Fourier Transform Infrared Spectroscopy and Scanning Electron Microscope of Cellulose Acetate Membrane From Wastewater of Tapioca. Supervised by BETTY MARITA SOEBRATA and SRI MULIJANI.
PENDAHULUAN
Ketela pohon (Manihot esculenta) merupakan tanaman pangan berupa perdu yang berasal dari Benua Amerika serta memiliki nama lain ubi kayu atau singkong. Di Indonesia, singkong merupakan sumber karbohidrat yang penting setelah beras dengan kandungan karbohidrat sebesar 34.7% (Soetanto 2001). Singkong dapat tumbuh sekalipun di tanah yang kurang subur, asalkan beriklim tropis. Indonesia saat ini merupakan negara penghasil singkong terbesar ketiga di dunia setelah Brazil dan Thailand sehingga banyak masyarakat Indonesia beralih dari bertanam padi menjadi bertanam singkong (Sumiyati 2009). Menurut data Badan Pusat Statistik (BPS 2011), jumlah produksi singkong di Indonesia pada tahun 2009 adalah 22,039,145 ton dan pada tahun 2010 meningkat menjadi sebesar 23,908,459 ton (angka sementara).
Singkong dapat dikonsumsi langsung sebagai bahan makanan atau digunakan sebagai bahan baku industri pangan, salah satunya adalah industri tapioka. Proses pembuatan tapioka pada industri akan menghasilkan limbah padat (onggok) dan limbah cair. Limbah cair tapioka dapat dihasilkan dari tahap pencucian bahan baku (singkong) serta proses pengendapan untuk memisahkan pati dari airnya. Teknologi yang ada saat ini belum mampu memisahkan seluruh pati yang terlarut dalam air sehingga limbah cair yang dilepaskan ke lingkungan masih mengandung pati. Limbah cair akan mengalami dekomposisi secara alami di badan-badan perairan dan menimbulkan bau yang tidak sedap. Bau tersebut dihasilkan pada proses penguraian senyawa yang mengandung nitrogen, sulfur, dan fosforus dari bahan berprotein (Zaitun 1999 dan Hanifah et al. 1999). Alternatif lain yang dapat dilakukan untuk mengolah limbah cair ini menjadi produk yang dapat dimanfaatkan lebih lanjut adalah mengolahnya menjadi nata yang disebut nata de cassava.
Pembentukan nata membutuhkan unsur C yang berasal dari glukosa serta unsur N dan O yang berasal dari penambahan amonium sulfat. Unsur-unsur ini digunakan sebagai nutrisi dan sumber karbon bagi bakteri
Acetobacter xylinum agar dapat membentuk nata. Limbah cair tapioka mengandung glukosa sebagai unsur karbon sehingga dapat digunakan sebagai medium yang baik untuk merangsang pertumbuhan bakteri tersebut saat membentuk nata. Oleh karena itu, limbah cair
tapioka berpotensi menghasilkan nata. Nata tersebut berupa selulosa yang dihasilkan oleh bakteri sehingga dapat disebut sebagai selulosa bakteri (BC). Selain itu, nata dapat dicirikan sebagai gabungan dari serat-serat karbon yang menjadi suatu bentuk yang kokoh dan berpori sehingga nata berpotensi untuk dimanfaatkan sebagai membran selulosa. Akan tetapi, membran selulosa tersebut tidak memiliki nilai komersial yang tinggi. Oleh karena itu, pengolahan lebih lanjut diperlukan untuk mengubahnya menjadi membran selulosa asetat (CA) yang memiliki nilai jual lebih tinggi.
Membran merupakan lapisan semipermeabel yang tipis dan dapat digunakan untuk memisahkan 2 komponen dengan cara menahan dan melewatkan komponen tertentu melalui pori-pori (Osada dan Nakagawa 1992). Beberapa keuntungan dalam penggunaan teknologi membran pada proses pemisahan antara lain prosesnya sangat sederhana, konsumsi energi rendah, tidak merusak material, tidak menggunakan zat kimia tambahan, dan tidak menghasilkan limbah baru sehingga tergolong sebagai teknologi bersih (Lindu et al. 2008).
Penelitian ini bertujuan membuat membran CA berbahan dasar limbah cair tapioka, serta mengidentifikasinya dengan spektroskopi inframerah transformasi fourier (FTIR) dan Mikroskop Elektron Payaran (SEM). Analisis ini dilakukan untuk mencirikan gugus fungsi dan jenis membran CA yang dihasilkan.
TINJAUAN PUSTAKA
Limbah Cair Tapioka
Salah satu pemanfaatan singkong selain sebagai bahan pangan kaya karbohidrat adalah sebagai bahan baku industri tapioka. Proses pembuatan tapioka di industri besar maupun industri kecil secara umum meliputi tahap pengupasan kulit, pencucian, pemarutan, pengekstrakan, pengendapan pati, dan pengeringan.
PENDAHULUAN
Ketela pohon (Manihot esculenta) merupakan tanaman pangan berupa perdu yang berasal dari Benua Amerika serta memiliki nama lain ubi kayu atau singkong. Di Indonesia, singkong merupakan sumber karbohidrat yang penting setelah beras dengan kandungan karbohidrat sebesar 34.7% (Soetanto 2001). Singkong dapat tumbuh sekalipun di tanah yang kurang subur, asalkan beriklim tropis. Indonesia saat ini merupakan negara penghasil singkong terbesar ketiga di dunia setelah Brazil dan Thailand sehingga banyak masyarakat Indonesia beralih dari bertanam padi menjadi bertanam singkong (Sumiyati 2009). Menurut data Badan Pusat Statistik (BPS 2011), jumlah produksi singkong di Indonesia pada tahun 2009 adalah 22,039,145 ton dan pada tahun 2010 meningkat menjadi sebesar 23,908,459 ton (angka sementara).
Singkong dapat dikonsumsi langsung sebagai bahan makanan atau digunakan sebagai bahan baku industri pangan, salah satunya adalah industri tapioka. Proses pembuatan tapioka pada industri akan menghasilkan limbah padat (onggok) dan limbah cair. Limbah cair tapioka dapat dihasilkan dari tahap pencucian bahan baku (singkong) serta proses pengendapan untuk memisahkan pati dari airnya. Teknologi yang ada saat ini belum mampu memisahkan seluruh pati yang terlarut dalam air sehingga limbah cair yang dilepaskan ke lingkungan masih mengandung pati. Limbah cair akan mengalami dekomposisi secara alami di badan-badan perairan dan menimbulkan bau yang tidak sedap. Bau tersebut dihasilkan pada proses penguraian senyawa yang mengandung nitrogen, sulfur, dan fosforus dari bahan berprotein (Zaitun 1999 dan Hanifah et al. 1999). Alternatif lain yang dapat dilakukan untuk mengolah limbah cair ini menjadi produk yang dapat dimanfaatkan lebih lanjut adalah mengolahnya menjadi nata yang disebut nata de cassava.
Pembentukan nata membutuhkan unsur C yang berasal dari glukosa serta unsur N dan O yang berasal dari penambahan amonium sulfat. Unsur-unsur ini digunakan sebagai nutrisi dan sumber karbon bagi bakteri
Acetobacter xylinum agar dapat membentuk nata. Limbah cair tapioka mengandung glukosa sebagai unsur karbon sehingga dapat digunakan sebagai medium yang baik untuk merangsang pertumbuhan bakteri tersebut saat membentuk nata. Oleh karena itu, limbah cair
tapioka berpotensi menghasilkan nata. Nata tersebut berupa selulosa yang dihasilkan oleh bakteri sehingga dapat disebut sebagai selulosa bakteri (BC). Selain itu, nata dapat dicirikan sebagai gabungan dari serat-serat karbon yang menjadi suatu bentuk yang kokoh dan berpori sehingga nata berpotensi untuk dimanfaatkan sebagai membran selulosa. Akan tetapi, membran selulosa tersebut tidak memiliki nilai komersial yang tinggi. Oleh karena itu, pengolahan lebih lanjut diperlukan untuk mengubahnya menjadi membran selulosa asetat (CA) yang memiliki nilai jual lebih tinggi.
Membran merupakan lapisan semipermeabel yang tipis dan dapat digunakan untuk memisahkan 2 komponen dengan cara menahan dan melewatkan komponen tertentu melalui pori-pori (Osada dan Nakagawa 1992). Beberapa keuntungan dalam penggunaan teknologi membran pada proses pemisahan antara lain prosesnya sangat sederhana, konsumsi energi rendah, tidak merusak material, tidak menggunakan zat kimia tambahan, dan tidak menghasilkan limbah baru sehingga tergolong sebagai teknologi bersih (Lindu et al. 2008).
Penelitian ini bertujuan membuat membran CA berbahan dasar limbah cair tapioka, serta mengidentifikasinya dengan spektroskopi inframerah transformasi fourier (FTIR) dan Mikroskop Elektron Payaran (SEM). Analisis ini dilakukan untuk mencirikan gugus fungsi dan jenis membran CA yang dihasilkan.
TINJAUAN PUSTAKA
Limbah Cair Tapioka
Salah satu pemanfaatan singkong selain sebagai bahan pangan kaya karbohidrat adalah sebagai bahan baku industri tapioka. Proses pembuatan tapioka di industri besar maupun industri kecil secara umum meliputi tahap pengupasan kulit, pencucian, pemarutan, pengekstrakan, pengendapan pati, dan pengeringan.
H2SO4
2313.54 mg L-1, COD sebesar 3200 mg L-1, padatan terlarut 638–2836 mg L-1, serta kandungan sianida (CN) sebesar 19.58–33.75 mg L-1 (Vegantara 2009). Oleh karena itu, apabila limbah ini dibuang ke lingkungan akan menyebabkan pencemaran lingkungan, seperti bau yang tidak sedap dan beberapa sumur warga yang tidak layak untuk dikonsumsi.
Selulosa Bakteri (BC)
Selulosa (Gambar 1) ialah polimer tak bercabang dari sejumlah glukosa yang tergabung melalui ikatan 1,4-β-glikosida. Pemeriksaan selulosa dengan sinar-X menunjukkan bahwa selulosa merupakan rantai linear dari selobiosa, yang oksigen cincinnya berselang-seling dengan posisi “ke
depan” dan “ke belakang” (Hart et al. 2003).
Gambar 1 Struktur selulosa.
A. xylinum (Gambar 2) merupakan bakteri Gram negatif, aerob, berbentuk batang dengan panjang 2 mikron, tidak membentuk spora dan nonmotil, serta umumnya berupa sel tunggal atau membentuk rantai dengan sel yang lain. Bakteri A. xylinum tergolong famili Pseudomonadaceae dan termasuk genus
Acetobacter. Sifat khas bakteri ini adalah kemampuannya untuk membentuk selaput tebal nata pada permukaan cairan fermentasi yang mengandung selulosa (Nurfiningsih 2009). Selain media yang mengandung gula, bakteri ini juga menyukai lingkungan yang asam dan membutuhkan sumber nitrogen untuk aktivitasnya. A. xylinum bersifat peka terhadap perubahan fisik dan kimia lingkungannya yang akan berpengaruh terhadap nata yang dihasilkan.
Gambar 2 Acetobacter xylinum.
Pembentukan BC terjadi karena proses pengambilan glukosa dari media yang mengandung gula oleh sel-sel A. xylinum. Glukosa tersebut kemudian digabungkan dengan asam lemak membentuk bahan pendahulu nata (prekursor) pada membran sel. Prekursor ini selanjutnya disekresi dan bersama enzim mempolimerisasikan glukosa menjadi selulosa di luar sel (Susanto et al. 2000). Menurut Nurfiningsih (2009), selulosa ini akan membentuk jaringan mikrofibril yang panjang dalam cairan fermentasi. Gelembung CO2 yang dihasilkan selama fermentasi
cenderung melekat pada jaringan ini sehingga menyebabkan jaringan ini terangkat ke permukaan cairan.
Pertumbuhan A. xylinum dipengaruhi oleh beberapa faktor, antara lain pH, suhu, sumber nitrogen, dan sumber karbon (Lapuz et al. 1967). Faktor lain yang berpengaruh terhadap hasil nata adalah wadah fermentasi atau jumlah larutan induk. Jumlah larutan induk yang relatif besar dapat meningkatkan rendemen nata karena akan semakin banyak pula jumlah bakteri A. xylinum yang ada (Nurfiningsih 2009).
Selulosa Asetat (CA)
Selulosa asetat (CA) secara umum terdiri atas 2 jenis, yaitu selulosa triasetat (CA primer) dan selulosa diasetat (CA sekunder). CA primer dibuat melalui reaksi esterifikasi (asetilasi) selulosa sedangkan CA sekunder dibuat dengan cara menghidrolisis CA primer (Desiyarni 2006).
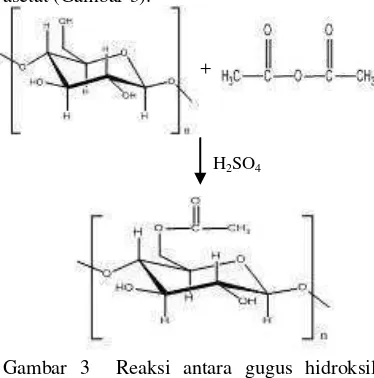
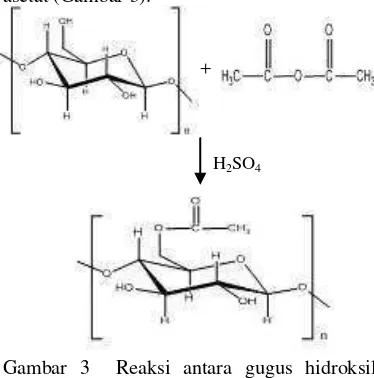
Selulosa triasetat diperoleh dari reaksi selulosa dengan anhidrida asetat dan katalis H2SO4. Gugus hidroksil (-OH) pada selulosa
digantikan dengan gugus asetil pada anhidrida asetat (Gambar 3).
+
3
Asetilasi merupakan tahap terpenting dalam pembuatan CA karena berhubungan dengan kemampuannya larut dalam pelarut organik tertentu pada proses pembuatan membran. Kelarutan CA dalam pelarut organik dipengaruhi oleh kadar asetil yang dihasilkan (Desiyarni 2006). Pengaturan kadar asetil tersebut dilakukan melalui reaksi hidrolisis menggunakan asam asetat encer hingga diperoleh derajat substitusi yang sesuai. Hubungan antara kadar asetil dan derajat substitusi ditunjukkan pada Tabel 1, sedangkan hubungan antara kadar asetil dan pelarut yang sesuai ditunjukkan pada Tabel 2.
Tabel 1 Hubungan derajat substitusi dengan kadar asetil
Derajat substitusi Kadar asetil (%bobot)
0.6–0.9 1.2–1.8 2.2–2.7 2.8–3.0
13.0–18.6 22.2–32.2 36.5–42.2 43.0–44.8
Sumber: Fengel dan Wegener (1985).
Tabel 2 Kelarutan selulosa asetat Kadar asetil
(%) Pelarut
43.0–44.8 Diklorometana 37.0–42.0 Aseton 24.0–32.0 2-Metoksietanol 15.0–20.0 Air
<13.0 Tidak ada
Sumber: Kirk dan Othmer (1993).
Membran
Membran merupakan lapisan semipermeabel berupa padatan polimer tipis yang menahan pergerakan bahan tertentu (Scott dan Hughes 1996). Menurut Gosh (2003), membran adalah pembatas tipis atau film sebagai tempat pengangkutan pelarut dan zat terlarut secara selektif. Menurut Osada dan Nakagawa (1992), membran merupakan lapisan semipermeabel tipis yang dapat digunakan untuk memisahkan 2 komponen dengan cara menahan dan melewatkan komponen tertentu melalui pori-pori. Pemisahan menghasilkan produk yang telah hilang komponen tertentunya kemudian komponen yang hilang tersebut bergabung menjadi semakin pekat membentuk produk tersendiri (Scott dan Hughes 1996).
Kegunaan Membran
Membran dalam industri memiliki fungsi utama untuk filtrasi padatan taklarut dari cairan dan gas yang mengandung padatan terlarut. Selain itu, fungsi lain membran adalah untuk pemindahan makromolekul dan koloid dari cairan yang mengandung ion, pemisahan campuran terlarut, pemisahan selektif gas dan uap dari aliran gas dan uap, serta transpor selektif spesies ion. (Scott dan Hughes 1996).
Klasifikasi Membran
Membran dapat diklasifikasikan menjadi 4 macam, yaitu berdasarkan material asal, morfologi, bentuk, dan fungsi. Menurut Mulder (1996), klasifikasi membran berdasarkan material asalnya dibagi menjadi dua golongan, yaitu membran alami dan membran sintetis. Membran alami berasal dari sel tumbuhan, hewan, dan manusia sedangkan membran sintetis dibuat sesuai dengan kebutuhan dan sifatnya disesuaikan dengan membran alami. Membran sintetis dibagi lagi menjadi membran organik dan anorganik. Membran organik merupakan membran yang dibuat dari polimer organik seperti polisulfon, selulosa asetat, polietersulfon, dan poliakrilamida sedangkan membran anorganik dibuat dari material anorganik seperti kaca, logam, dan keramik (Gosh 2003).
Mallevialle et al. (1996) menyatakan bahwa membran berdasarkan morfologinya dibedakan menjadi 3, yaitu (1) membran simetrik, yang memiliki morfologi homogen pada semua posisi di dalamnya, (2) membran asimetrik, yang memiliki morfologi pada bagian atas berbeda dengan bagian bawah, dan (3) membran komposit, yang terbuat dari dua jenis bahan yang berbeda.
Berdasarkan bentuknya, membran dibagi menjadi dua, yaitu membran datar dan tubular. Membran datar memiliki bentuk melebar dan penampang lintang yang besar. Membran ini memiliki 3 macam bentuk antara lain: (a) satu lembaran, (b) beberapa lembaran yang disusun bertingkat dengan menempatkan pemisah antara 2 membran yang berdekatan, dan (c) membran spiral bergulung yang disusun bertingkat dan digulung dengan pipa sentral membentuk spiral. Membran tubular terdiri atas 3 jenis, yaitu membran serat berongga (diameter <0.5 mm), membran kapiler (diameter 0.5–5.0 mm), dan membran tubular (diameter >5 mm) (Mulder 1996).
dialisis, dan elektrodialisis. Membran mikrofiltrasi digunakan untuk pemisahan antarpartikel (bakteri, ragi, dan sejenisnya), berfungsi menyaring makromolekul dengan bobot molekul >500000 g/mol atau partikel berukuran 0.1–10 µm, menggunakan tekanan 0.5–2 atm, serta memiliki struktur simetrik dan asimetrik. Membran ultrafiltrasi digunakan pada proses pemisahan antarmolekul, berfungsi menyaring makromolekul dengan bobot molekul >5000 g/mol atau partikel berukuran 0.001–0.1 µm, menggunakan tekanan 1.0–3.0 atm, dan memiliki struktur asimetrik. Membran osmosis balik berfungsi menyaring molekul berbobot molekul rendah, yaitu >50 g/mol seperti garam, atau partikel berukuran 0.0001– 0.001 µm, serta menggunakan tekanan 8.0– 12.0 atm. Membran dialisis berfungsi memisahkan larutan koloid yang mengandung elektrolit dengan bobot molekul rendah. Membran elektrodialisis berperan pada proses elektrodialisis, yaitu proses separasi membran yang didorong oleh medan listrik (McGregor 1986).
Pencirian Membran
Membran yang telah dibentuk perlu dicirikan antara lain sifat morfologinya dengan menggunakan SEM dan gugus fungsinya dengan menggunakan FTIR. SEM merupakan sejenis mikroskop yang menggunakan sinar elektron berenergi tinggi dengan faktor pembesaran hingga 10000 kali sehingga dapat melihat objek pada skala yang sangat kecil. Batas resolusi mikroskop elektron adalah 0.01 µm (10 nm) dan 0.005 µm (5nm) (Andriansyah 2006). Sementara itu, pencirian membran dengan FTIR, gugus fungsi yang ada diidentifikasi berdasarkan puncak serapan inframerahnya. Masing-masing gugus fungsi memiliki puncak serapan yang khas.
BAHAN DAN METODE
Bahan dan Alat
Bahan–bahan yang digunakan dalam penelitian ini adalah starter (bakteri A. xylinum) dari Balai Besar Industri Agro, limbah cair tapioka dari industri tapioka di Kedung Halang Bogor, asam asetat glasial, amonium sulfat, anhidrida asetat, gula pasir, aseton, H2SO4, NaHCO3, dan air suling.
Alat-alat yang digunakan dalam penelitian ini antara lain panci, loyang plastik sebagai
wadah fermentasi, blender, neraca analitik, sentrifus, botol bertutup ganda, mortar, corong Büchner dan pompa vakum, pelat kaca, pengaduk magnet, hot plate, pH meter, FTIR Perkin Elmer Spectrumone, SEM JEOL JSM-8360LA, serta alat-alat kaca.
Pembuatan BC (Nata de Cassava)
Limbah cair tapioka yang telah disaring diambil sebanyak 1 L kemudian ditambahkan gula pasir sebanyak 10% (b/v) dan amonium sulfat sebanyak 0.5% (b/v), campuran dipanaskan hingga mendidih sambil diaduk, lalu yang telah mendidih dituang ke wadah fermentasi yang telah disiapkan dan diatur pHnya menjadi 4–4.5 dengan penambahan asam asetat glasial. Wadah lalu ditutup dengan kertas steril dan diikat dengan karet. Keesokan harinya, sebanyak 20% (v/v) inokulum dimasukkan ke dalam media dan diinkubasi selama 6 hari pada suhu kamar hingga terbentuk nata (Arviyanti dan Yulimartani 2009).
Penyiapan Serbuk Kering BC
Lembaran nata de cassava dicuci dengan air kemudian direbus hingga mendidih untuk menghilangkan bakteri yang tersisa. Selanjutnya, lembaran nata direndam dalam larutan NaOH 1% (b/v) pada suhu kamar selama 24 jam, dilanjutkan dalam asam asetat 1% selama 24 jam untuk menetralkan pH-nya. Lembaran nata yang telah dinetralkan kemudian dicuci dengan air dan diperas menggunakan corong Büchner dan pompa vakum hingga terbentuk lembaran tipis yang masih basah. Lembaran tipis tersebut dikeringkan di bawah sinar matahari lalu dihancurkan dengan blender hingga berupa serbuk.
Sintesis Selulosa Asetat
Asetilasi serbuk BC dilakukan dengan modifikasi prosedur Arifin (2004) dan Pasla (2006). Sebanyak 1.8 g serbuk BC ditimbang di dalam botol plastik bertutup ganda kemudian ditambahkan 100 mL asam asetat. Botol dikocok kuat dengan tangan selama 1 menit, kemudian dikocok kembali dengan
4
dialisis, dan elektrodialisis. Membran mikrofiltrasi digunakan untuk pemisahan antarpartikel (bakteri, ragi, dan sejenisnya), berfungsi menyaring makromolekul dengan bobot molekul >500000 g/mol atau partikel berukuran 0.1–10 µm, menggunakan tekanan 0.5–2 atm, serta memiliki struktur simetrik dan asimetrik. Membran ultrafiltrasi digunakan pada proses pemisahan antarmolekul, berfungsi menyaring makromolekul dengan bobot molekul >5000 g/mol atau partikel berukuran 0.001–0.1 µm, menggunakan tekanan 1.0–3.0 atm, dan memiliki struktur asimetrik. Membran osmosis balik berfungsi menyaring molekul berbobot molekul rendah, yaitu >50 g/mol seperti garam, atau partikel berukuran 0.0001– 0.001 µm, serta menggunakan tekanan 8.0– 12.0 atm. Membran dialisis berfungsi memisahkan larutan koloid yang mengandung elektrolit dengan bobot molekul rendah. Membran elektrodialisis berperan pada proses elektrodialisis, yaitu proses separasi membran yang didorong oleh medan listrik (McGregor 1986).
Pencirian Membran
Membran yang telah dibentuk perlu dicirikan antara lain sifat morfologinya dengan menggunakan SEM dan gugus fungsinya dengan menggunakan FTIR. SEM merupakan sejenis mikroskop yang menggunakan sinar elektron berenergi tinggi dengan faktor pembesaran hingga 10000 kali sehingga dapat melihat objek pada skala yang sangat kecil. Batas resolusi mikroskop elektron adalah 0.01 µm (10 nm) dan 0.005 µm (5nm) (Andriansyah 2006). Sementara itu, pencirian membran dengan FTIR, gugus fungsi yang ada diidentifikasi berdasarkan puncak serapan inframerahnya. Masing-masing gugus fungsi memiliki puncak serapan yang khas.
BAHAN DAN METODE
Bahan dan Alat
Bahan–bahan yang digunakan dalam penelitian ini adalah starter (bakteri A. xylinum) dari Balai Besar Industri Agro, limbah cair tapioka dari industri tapioka di Kedung Halang Bogor, asam asetat glasial, amonium sulfat, anhidrida asetat, gula pasir, aseton, H2SO4, NaHCO3, dan air suling.
Alat-alat yang digunakan dalam penelitian ini antara lain panci, loyang plastik sebagai
wadah fermentasi, blender, neraca analitik, sentrifus, botol bertutup ganda, mortar, corong Büchner dan pompa vakum, pelat kaca, pengaduk magnet, hot plate, pH meter, FTIR Perkin Elmer Spectrumone, SEM JEOL JSM-8360LA, serta alat-alat kaca.
Pembuatan BC (Nata de Cassava)
Limbah cair tapioka yang telah disaring diambil sebanyak 1 L kemudian ditambahkan gula pasir sebanyak 10% (b/v) dan amonium sulfat sebanyak 0.5% (b/v), campuran dipanaskan hingga mendidih sambil diaduk, lalu yang telah mendidih dituang ke wadah fermentasi yang telah disiapkan dan diatur pHnya menjadi 4–4.5 dengan penambahan asam asetat glasial. Wadah lalu ditutup dengan kertas steril dan diikat dengan karet. Keesokan harinya, sebanyak 20% (v/v) inokulum dimasukkan ke dalam media dan diinkubasi selama 6 hari pada suhu kamar hingga terbentuk nata (Arviyanti dan Yulimartani 2009).
Penyiapan Serbuk Kering BC
Lembaran nata de cassava dicuci dengan air kemudian direbus hingga mendidih untuk menghilangkan bakteri yang tersisa. Selanjutnya, lembaran nata direndam dalam larutan NaOH 1% (b/v) pada suhu kamar selama 24 jam, dilanjutkan dalam asam asetat 1% selama 24 jam untuk menetralkan pH-nya. Lembaran nata yang telah dinetralkan kemudian dicuci dengan air dan diperas menggunakan corong Büchner dan pompa vakum hingga terbentuk lembaran tipis yang masih basah. Lembaran tipis tersebut dikeringkan di bawah sinar matahari lalu dihancurkan dengan blender hingga berupa serbuk.
Sintesis Selulosa Asetat
Asetilasi serbuk BC dilakukan dengan modifikasi prosedur Arifin (2004) dan Pasla (2006). Sebanyak 1.8 g serbuk BC ditimbang di dalam botol plastik bertutup ganda kemudian ditambahkan 100 mL asam asetat. Botol dikocok kuat dengan tangan selama 1 menit, kemudian dikocok kembali dengan
disaring-vakum dan diperas sekuat-kuatnya kemudian dimasukkan ke dalam wadah yang baru.
Serbuk BC kemudian ditambahkan dengan larutan asam asetat glasial-H2SO4 dengan
nisbah 100:1 (10:0.1 mL) dan diaduk kuat. Setelah itu, anhidrida asetat dengan nisbah 1:5 ditambahkan dengan pipet tetes sedikit demi sedikit sambil diaduk dengan batang pengaduk hingga mengental dan didiamkan selama 2 jam terhitung sejak penambahan anhidrida asetat tetesan pertama. Setelah proses asetilasi selesai, suspensi dihidrolisis dengan 2.4 mL larutan asam asetat glasial-air suling (2:1) dan diaduk pada beberapa menit pertama. Larutan kemudian didiamkan selama 30 menit terhitung sejak penambahan asam asetat encer. Selanjutnya, larutan hasil hidrolisis disentrifugasi selama 15 menit pada kecepatan 4000 rpm. Supernatan yang dihasilkan kemudian dimasukkan ke dalam gelas piala yang berisi 500 mL air suling dan diaduk sekuat mungkin dengan pengaduk magnet hingga terbentuk serpihan (CA) berwarna putih.
Serpihan CA yang diperoleh disaring-vakum dengan corong Büchner dan dicuci dengan NaHCO3 1N hingga gelembung gas
CO2 menghilang, lalu dicuci kembali dengan
air suling. Serpihan netral ini diperas lalu dikeringkan dalam oven dengan suhu 50 ºC selama 24 jam hingga CA yang diperoleh benar-benar kering. Produk CA yang dihasilkan selanjutnya dianalisis kadar air dan kadar asetilnya (Lampiran 2).
Diagram alir penelitian dapat dilihat pada Lampiran 1.
Pembuatan Membran
Pembuatan membran dilakukan dengan modifikasi prosedur Pasla (2006). Tahap pertama, CA kering dilarutkan ke dalam pelarut aseton (sesuai dengan derajat asetilasi yang dihasilkan) menggunakan pengaduk magnet. Nisbah polimer dan pelarut yang digunakan sebanyak 16% (b/v). Larutan tersebut kemudian dituang ke atas pelat kaca. Selanjutnya, larutan dicetak dengan cara menekan lalu menarik larutan menggunakan batang pengaduk hingga diperoleh lapisan tipis yang menempel pada kaca dan dibiarkan selama 15 menit untuk menguapkan pelarut. Penampang kaca tersebut kemudian direndam di dalam air hingga lapisan tipis membran yang menempel pada kaca terlepas.
Pencirian Membran
Analisis FTIR
Analisis FTIR dilakukan terhadap serbuk selulosa dan membran selulosa asetat. Masing-masing sampel dipreparasi hingga berbentuk pelet lalu ditempatkan di dalam tempat sampel. Sampel kemudian dianalisis gugus fungsinya dengan alat FTIR di Laboratorium Terpadu, Universitas Islam Negeri Syarif Hidayatullah, Jakarta.
Analisis SEM
Analisis dilakukan di laboratorium Penelitian dan Pengembangan Geologi dan Kelautan. Membran CA dipotong kecil lalu ditempelkan pada tempat sampel. Kemudian, sampel ditempatkan dalam sebuah tabung untuk dilapisi permukaannya oleh emas selama 20 menit. Selanjutnya, sampel yang telah dilapisi ditempatkan dalam alat SEM dan dicari perbesaran terbaik agar morfologi permukaannya dapat diamati. Gambar yang diperoleh kemudian difoto dan disimpan.
HASIL DAN PEMBAHASAN
Nata de cassava
Penambahan gula pasir sebagai sumber karbon sebanyak 10%, amonium sulfat sebagai sumber nitrogen 0.5%, A. xylinum
sebagai starter sebanyak 20%, serta pengaturan pH menjadi 4 dengan penambahan asam asetat glasial merupakan kondisi optimum yang dibutuhkan untuk membuat
nata de cassava dari 1 L limbah cair tapioka (Avriyani dan Yulimartani 2009). Penambahan gula kurang dari 10% tidak menyediakan sumber karbon yang cukup sehingga mengganggu metabolisme bakteri dan pertumbuhan bakteri pun akan terhambat, sedangkan penambahan gula lebih dari 10% akan menyebabkan media terlalu pekat sehingga kerja bakteri menjadi tidak optimum. Pengaturan pH menjadi 4 bertujuan membuat
A. xylinum lebih unggul dibandingkan dengan bakteri lain dalam hal mendapatkan nutrien dari media untuk pertumbuhannya sehingga mencegah tumbuhnya bakteri lain yang dapat menganggu pertumbuhan nata.
5
disaring-vakum dan diperas sekuat-kuatnya kemudian dimasukkan ke dalam wadah yang baru.
Serbuk BC kemudian ditambahkan dengan larutan asam asetat glasial-H2SO4 dengan
nisbah 100:1 (10:0.1 mL) dan diaduk kuat. Setelah itu, anhidrida asetat dengan nisbah 1:5 ditambahkan dengan pipet tetes sedikit demi sedikit sambil diaduk dengan batang pengaduk hingga mengental dan didiamkan selama 2 jam terhitung sejak penambahan anhidrida asetat tetesan pertama. Setelah proses asetilasi selesai, suspensi dihidrolisis dengan 2.4 mL larutan asam asetat glasial-air suling (2:1) dan diaduk pada beberapa menit pertama. Larutan kemudian didiamkan selama 30 menit terhitung sejak penambahan asam asetat encer. Selanjutnya, larutan hasil hidrolisis disentrifugasi selama 15 menit pada kecepatan 4000 rpm. Supernatan yang dihasilkan kemudian dimasukkan ke dalam gelas piala yang berisi 500 mL air suling dan diaduk sekuat mungkin dengan pengaduk magnet hingga terbentuk serpihan (CA) berwarna putih.
Serpihan CA yang diperoleh disaring-vakum dengan corong Büchner dan dicuci dengan NaHCO3 1N hingga gelembung gas
CO2 menghilang, lalu dicuci kembali dengan
air suling. Serpihan netral ini diperas lalu dikeringkan dalam oven dengan suhu 50 ºC selama 24 jam hingga CA yang diperoleh benar-benar kering. Produk CA yang dihasilkan selanjutnya dianalisis kadar air dan kadar asetilnya (Lampiran 2).
Diagram alir penelitian dapat dilihat pada Lampiran 1.
Pembuatan Membran
Pembuatan membran dilakukan dengan modifikasi prosedur Pasla (2006). Tahap pertama, CA kering dilarutkan ke dalam pelarut aseton (sesuai dengan derajat asetilasi yang dihasilkan) menggunakan pengaduk magnet. Nisbah polimer dan pelarut yang digunakan sebanyak 16% (b/v). Larutan tersebut kemudian dituang ke atas pelat kaca. Selanjutnya, larutan dicetak dengan cara menekan lalu menarik larutan menggunakan batang pengaduk hingga diperoleh lapisan tipis yang menempel pada kaca dan dibiarkan selama 15 menit untuk menguapkan pelarut. Penampang kaca tersebut kemudian direndam di dalam air hingga lapisan tipis membran yang menempel pada kaca terlepas.
Pencirian Membran
Analisis FTIR
Analisis FTIR dilakukan terhadap serbuk selulosa dan membran selulosa asetat. Masing-masing sampel dipreparasi hingga berbentuk pelet lalu ditempatkan di dalam tempat sampel. Sampel kemudian dianalisis gugus fungsinya dengan alat FTIR di Laboratorium Terpadu, Universitas Islam Negeri Syarif Hidayatullah, Jakarta.
Analisis SEM
Analisis dilakukan di laboratorium Penelitian dan Pengembangan Geologi dan Kelautan. Membran CA dipotong kecil lalu ditempelkan pada tempat sampel. Kemudian, sampel ditempatkan dalam sebuah tabung untuk dilapisi permukaannya oleh emas selama 20 menit. Selanjutnya, sampel yang telah dilapisi ditempatkan dalam alat SEM dan dicari perbesaran terbaik agar morfologi permukaannya dapat diamati. Gambar yang diperoleh kemudian difoto dan disimpan.
HASIL DAN PEMBAHASAN
Nata de cassava
Penambahan gula pasir sebagai sumber karbon sebanyak 10%, amonium sulfat sebagai sumber nitrogen 0.5%, A. xylinum
sebagai starter sebanyak 20%, serta pengaturan pH menjadi 4 dengan penambahan asam asetat glasial merupakan kondisi optimum yang dibutuhkan untuk membuat
nata de cassava dari 1 L limbah cair tapioka (Avriyani dan Yulimartani 2009). Penambahan gula kurang dari 10% tidak menyediakan sumber karbon yang cukup sehingga mengganggu metabolisme bakteri dan pertumbuhan bakteri pun akan terhambat, sedangkan penambahan gula lebih dari 10% akan menyebabkan media terlalu pekat sehingga kerja bakteri menjadi tidak optimum. Pengaturan pH menjadi 4 bertujuan membuat
A. xylinum lebih unggul dibandingkan dengan bakteri lain dalam hal mendapatkan nutrien dari media untuk pertumbuhannya sehingga mencegah tumbuhnya bakteri lain yang dapat menganggu pertumbuhan nata.
dalam CH3COOH 1% dimaksudkan untuk
menetralkan sifat basa dari struktur BC yang telah dimurnikan. Struktur selulosa yang membengkak dapat meningkatkan aksesibilitas gugus –OH pada selulosa terhadap pereaksi asetilasi.
BC kemudian dikeringkan, lalu dihaluskan sehingga diperoleh serbuk berwarna kecokelatan. Serbuk BC yang dihasilkan memiliki struktur yang rapat karena adanya ikatan hidrogen antarmolekul selulosa (Arifin 2004).
Gambar 4 Nata de cassava.
Selulosa Asetat (CA)
Pembuatan selulosa asetat meliputi 4 tahap, yaitu aktivasi, asetilasi, hidrolisis, dan purifikasi. Tahap aktivasi menggunakan asam asetat pekat untuk menarik air yang masih tersisa di dalam serbuk BC karena serbuk BC bersifat higroskopis. Proses perendaman dalam asam asetat juga meningkatkan reaktivitas gugus selulosa karena matriks BC yang sulit dimasuki pereaksi kimia akan dibengkakkan sehingga dapat mempercepat penetrasi anhidrida asetat ke dalam matriks pada saat asetilasi.
Proses asetilasi dimaksudkan untuk menyubstitusi gugus hidroksil BC dengan gugus asetil sehingga terbentuk CA. Asetilasi adalah reaksi yang eksoterm, maka suhu harus dijaga tetap rendah agar tidak terjadi degradasi rantai selulosa dan untuk menghindari penguapan (Winding dan Hasche 1947). Hal ini dapat menurunkan rendemen yang dihasilkan, atau produk CA dapat tidak terbentuk sama sekali. Penambahan anhidrida asetat tetes demi tetes yang diikuti pengadukan selama proses asetilasi dapat menjaga suhu larutan tetap rendah dan menghindari hal tersebut karena penambahan anhidrida asetat dalam jumlah yang signifikan dapat menyebabkan suhu sistem meningkat dengan cepat.
Tahap yang ketiga adalah hidrolisis, yaitu proses penghentian asetilasi dengan penambahan asam asetat encer. Hidrolisis dengan asam asetat encer ini dapat mengurangi kadar asetil serta mengurangi derajat substitusi CA ke nilai yang diinginkan. Hasil reaksi kemudian dimurnikan dengan cara sentrifugasi untuk memisahkan BC yang terasetilasi dan yang tidak. Bagian yang terasetilasi berupa supernatan yang selanjutnya didispersikan ke dalam air suling sehingga diperoleh serpihan berwarna putih kecokelatan yang merupakan selulosa asetat (Gambar 5).
Gambar 5 Serbuk selulosa asetat.
Membran Selulosa Asetat (CA)
Serbuk CA yang dihasilkan mempunyai kadar asetil sebesar 40.38%. CA dengan kadar asetil 37 hingga 42% dapat larut di dalam pelarut aseton (Tabel 2). Oleh karena itu, serbuk CA yang dihasilkan pada penelitian ini dilarutkan dalam aseton untuk membuat membran CA. Pembuatan membran CA dilakukan dengan metode inversi fase. Larutan polimer dicetak di atas pelat kaca yang sisi-sisinya sudah dilapisi dengan selotip. Larutan CA yang telah dicetak dibiarkan 15 menit untuk menguapkan aseton hingga larutan menjadi kering dan membentuk lembaran membran. Lembaran membran ini kemudian direndam dalam air hingga terlepas dari kaca. Membran yang dihasilkan berwarna putih kecokelatan (Gambar 6).
7
Kadar Air dan Kadar Asetil CA
Kadar asetil menunjukkan banyaknya gugus –OH pada BC yang sudah terasetilasi atau banyaknya gugus asetil yang terdapat pada CA. Faktor-faktor yang dapat mempengaruhi besarnya kadar asetil adalah metode pengeringan selulosa, konsentrasi NaOH pada tahap merserisasi atau pemurnian selulosa, dan nisbah antara bobot selulosa dan volume anhidrida asetat (Pasla 2006). Faktor-faktor di atas telah dioptimisasi oleh Arifin (2004) dan Yulianawati (2002).
Selulosa bakteri yang diperoleh diusahakan mengandung kadar air yang rendah karena kadar air dapat memengaruhi jalannya reaksi asetilasi. Gugus –OH pada air lebih mudah bereaksi dengan anhidrida asam asetat dibandingkan dengan gugus –OH pada selulosa. Oleh karena itu, aksesibilitas yang tinggi pada gugus –OH selulosa diperlukan untuk mempermudah terjadinya reaksi asetilasi oleh pereaksi anhidrida asam asetat. Semakin tinggi aksesibilitas –OH pada selulosa, kadar asetil pun akan semakin tinggi. Kadar asetil CA yang diperoleh pada penelitian ini sebesar 40.38%. Nilai kadar asetil ini setara dengan derajat substitusi 2.51. Derajat substitusi (DS) adalah jumlah rerata atom H pada gugus hidroksil (-OH) yang diubah menjadi gugus asetil dalam setiap residu anhidroglukosa. DS ini berhubungan dengan aplikasi CA dalam industri. Menurut Fengel dan Wegener (1984), CA dengan DS 2.2 sampai 2.7 dapat diaplikasikan sebagai benang dan film. Perhitungan penentuan kadar asetil dapat dilihat di Lampiran 3.
CA dengan kadar asetil sebesar 40.38% dapat larut dalam aseton (Kirk dan Othmer 1993). Oleh karena itu, pelarut yang digunakan untuk membuat membran CA pada penelitian ini adalah aseton. Menurut Wenten (1999), semakin tinggi kadar asetil, ukuran pori-pori membran akan semakin kecil dan permeabilitas air akan semakin berkurang. Berdasarkan pernyataan tersebut, CA yang diperoleh pada penelitian ini memiliki pori-pori yang cukup kecil dan permeabilitas air yang cukup rendah dilihat dari nilai kadar asetilnya yang cukup tinggi. Hal ini dapat dibuktikan dengan hasil analisis SEM pada permukaan membran CA yang menunjukan kisaran ukuran pori membran (Gambar 8).
Kadar air CA yang diperoleh adalah 21.49% (Lampiran 3). Besarnya kadar air tersebut dapat disebabkan oleh waktu proses pengeringan CA yang kurang lama saat di oven sehingga belum diperoleh bobot yang
benar-benar konstan. Selain itu, kebersihan wadah dan tempat pengukuran pun dapat berpengaruh karena dapat menambah bobot yang ditimbang. Nilai kadar air ini diperlukan untuk menghitung kadar asetil CA.
Analisis Spektrum FTIR
Analisis spektrum FTIR dilakukan pada selulosa nata de coco, serbuk nata de cassava, dan CA. Selulosa nata de coco ini merupakan hasil pembiakan bakteri A. xylinum pada media air kelapa tanpa penambahan apapun.
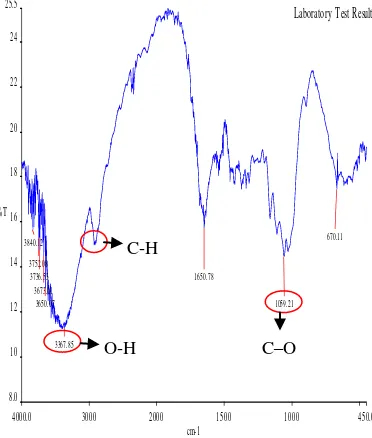
Pada spektrum FTIR serbuk nata de cassava (Gambar 8) terdapat pita serapan pada daerah bilangan gelombang 3394.46 cm
-1
yang merupakan pita serapan ulur dari gugus
–OH serta pada daerah bilangan gelombang 1059.15 cm-1 yang merupakan pita serapan ulur dari gugus C-O. Selain itu, terdapat pula pita serapan untuk gugus C-H ulur pada daerah bilangan gelombang sekitar 2900– 3000 cm-1. Nilai serapan yang tidak jauh berbeda juga terdapat pada spektrum FTIR selulosa nata de coco (Gambar 7), yaitu 3367.85 cm-1 untuk gugus –OH, 1059.21 cm-1 untuk gugus C-O, serta sekitar 2900–3000 cm
-1
untuk gugus C-H ulur. Hal ini menunjukkan bahwa struktur penyusun yang terdapat pada serbuk nata de cassava sama dengan struktur penyusun pada selulosa nata de coco. Oleh karena itu, berdasarkan spektrumnya, serbuk
nata de cassava dapat dikatakan sebagai selulosa walaupun masih terdapat adanya zat lain yang kemungkinan adalah pengotor.
Gambar 7 Spektrum FTIR selulosa nata de coco.
4000.0 3000 2000 1500 1000 450.0
8.0 10 12 14 16 18 20 22 24 25.5 cm-1 %T
Laboratory Test Result
3840.12 3752.08 3736.53 3673.01 3650.07 3367.85 1650.78 1059.21 670.11 O-H C-H
Gambar 8 Spektrum FTIR serbuk nata de cassava.
Serbuk nata de cassava dibandingkan spektrum FTIRnya dengan membran CA untuk melihat keberhasilan proses asetilasi yang telah dilakukan. Pada spektrum FTIR membran CA (Gambar 9) terdapat pita serapan yang khas untuk gugus karbonil atau C=O, yaitu pada daerah bilangan gelombang 1754.81 cm-1. Selain itu, terdapat pita serapan untuk gugus C-O asetil pada daerah bilangan gelombang 1042.34 cm-1. Hal ini menandakan sudah terbentuknya gugus asetil pada selulosa
nata de cassava setelah diasetilasi sehingga menjadi CA. Adanya pita serapan untuk gugus
–OH pada daerah 3445.12 cm-1 menunjukkan bahwa ada sebagian gugus hidroksil pada setiap residu anhidroglukosa yang belum terasetilasi. Hal ini dapat dibuktikan dari nilai DS pada CA yang tidak mencapai nilai maksimumnya, yaitu 3.
Gambar 9 Spektrum FTIR membran CA.
Analisis Membran CA dengan SEM
Pencirian dengan SEM bertujuan mengamati morfologi permukaan membran, yaitu dengan melihat keberadaan dan ukuran pori-pori membran serta penampang lintangnya. Dari hasil pengamatan tersebut, jenis membran yang sedang dianalisis dapat diketahui.
Pengamatan dilakukan pada 2 bagian membran, yaitu bagian permukaan dan penampang lintangnya. Hasil SEM dengan perbesaran 5000x pada permukaan membran memperlihatkan adanya pori-pori yang menyebar pada membran (Gambar 10). Diameter pori-pori tersebut sekitar 0.37-0.95 µm. Hal ini menunjukkan bahwa membran tersebut dapat menahan partikel yang berukuran lebih besar dari 0.95 µm. Dengan kata lain, permeat yang terbentuk terdiri atas
partikel yang berukuran ≤0.95 µm sedangkan
rentetatnya berupa partikel berukuran ≥0.95 µm. Menurut Mulder (1996), membran yang memiliki ukuran pori 0.1-10.0 µm tergolong sebagai membran mikrofiltrasi. Oleh karena itu, membran CA yang dihasilkan merupakan membran mikrofiltrasi.
Gambar 10 Permukaan membran CA dengan perbesaran 5000 kali.
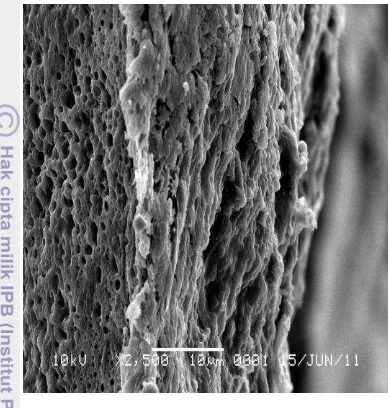
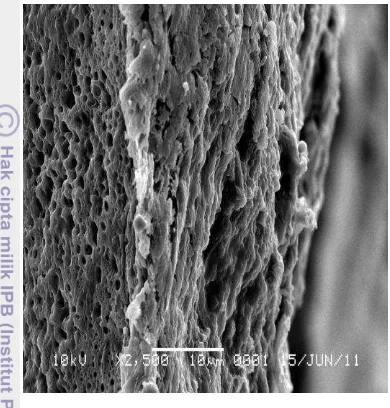
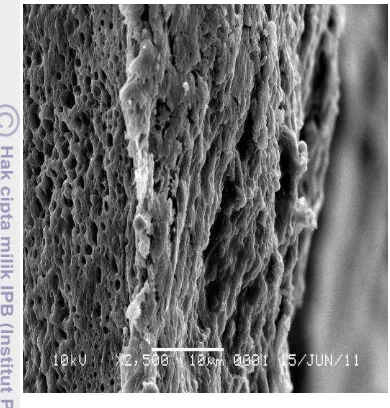
Berdasarkan morfologinya, pengamatan penampang lintang membran dengan perbesaran 2500 kali (Gambar 11) menunjukkan bahwa membran yang dihasilkan termasuk membran asimetrik karena tersusun oleh beberapa lapisan. Struktur membran asimetrik terdiri atas lapisan yang sangat padat dan lapisan berpori sebagai penyangga. Pada membran asimetrik,
4000.0 3000 2000 1500 1000 450.0
5.0 6 7 8 9 10 11 12 13 14 15 16.0
cm-1 %T
selulosa Laboratory Test Result
3394.46
9
permeasi terjadi pada lapisan padat yang mempunyai tahanan perpindahan massa yang besar (Lindu et a.l 2008).
Gambar 11 Penampang lintang membran CA dengan perbesaran 2500 kali.
SIMPULAN DAN SARAN
SimpulanLimbah cair tapioka dapat dibuat menjadi
nata de cassava. Hal ini dibuktikan dari kesamaan spektrum selulosa dari nata de cassava dengan nata de coco. Selulosa nata de cassava dapat diasetilasi, kemudian CA yang dihasilkan dibuat menjadi membran dengan teknik inversi fase menggunakan pelarut aseton. Terbentuknya CA ditunjukkan dengan hasil analisis FTIR pada membran CA yang menunjukkan adanya pita serapan C=O pada daerah bilangan gelombang 1754.81 cm
-1
serta C-O asetil pada daerah 1042.34 cm-1. CA yang diperoleh mempunyai kadar air sebesar 21.49% dan kadar asetil sebesar 40.38% (setara dengan kisaran derajat substitusi 2.51). Pengamatan SEM pada membran CA memperlihatkan bahwa membran yang dihasilkan merupakan jenis membran mikrofiltrasi (berdasarkan fungsi) dan asimetrik (berdasarkan morfologi).
Saran
Kadar air dan α-selulosa BC harus
ditentukan untuk mengetahui tingkat kemurnian selulosa yang terbentuk. Pengujian lain juga perlu dilakukan untuk mengetahui kinerja membran lebih lanjut, seperti nilai fluks air dan indeks rejeksi. Berkaitan dengan hasil SEM yang menunjukkan ukuran pori
yang tidak seragam pada membran CA, penambahan suatu zat aditif dalam pembuatan membran perlu dilakukan untuk mengatur ukuran pori agar lebih seragam.
DAFTAR PUSTAKA
Andriansyah M. 2006. Sifat-sifat membran yang terbuat dari sari kulit buah nanas [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Arifin B. 2004. Optimasi kondisi asetilasi selulosa bakteri dari nata de coco
[skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Arviyanti E, Yulimartani N. 2009. Pengaruh penambahan air limbah tapioka pada proses pembuatan nata [skripsi]. Semarang: Fakultas Teknik, Universitas Dipenogoro.
[BPS] Badan Pusat Statistik. 2011. Tabel Luas Panen-Produktivitas-Produksi Tanaman Ubi Kayu Seluruh Propinsi [terhubung berkala]. http://www.bps.go.id [24 Juli 2011].
Desiyarni. 2006. Perancangan proses pembuatan selulosa asetat dari selulosa mikrobial untuk membran ultrafiltrasi. [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Fengel D, Wegener G. 1984. Wood: Chemistry, Ultrastructure, Reaction. Berlin: Walter de Gruyter.
Gosh R. 2003. Protein Bioseparation Using Ultrafiltration Theory, Application, and New Development. Oxford: Imperial College Press.
Hanifah TA, Saeni MS, Adijuwana H, Bintoro HMH. 1999. Evaluasi kandungan logam berat timbal dan kadmium dalam ubi kayu (Manihot esculenta Crantz) yang dipupuk sampah kota. Buletin Ilmiah Gaku-ryoku 1:38-45.
permeasi terjadi pada lapisan padat yang mempunyai tahanan perpindahan massa yang besar (Lindu et a.l 2008).
Gambar 11 Penampang lintang membran CA dengan perbesaran 2500 kali.
SIMPULAN DAN SARAN
SimpulanLimbah cair tapioka dapat dibuat menjadi
nata de cassava. Hal ini dibuktikan dari kesamaan spektrum selulosa dari nata de cassava dengan nata de coco. Selulosa nata de cassava dapat diasetilasi, kemudian CA yang dihasilkan dibuat menjadi membran dengan teknik inversi fase menggunakan pelarut aseton. Terbentuknya CA ditunjukkan dengan hasil analisis FTIR pada membran CA yang menunjukkan adanya pita serapan C=O pada daerah bilangan gelombang 1754.81 cm
-1
serta C-O asetil pada daerah 1042.34 cm-1. CA yang diperoleh mempunyai kadar air sebesar 21.49% dan kadar asetil sebesar 40.38% (setara dengan kisaran derajat substitusi 2.51). Pengamatan SEM pada membran CA memperlihatkan bahwa membran yang dihasilkan merupakan jenis membran mikrofiltrasi (berdasarkan fungsi) dan asimetrik (berdasarkan morfologi).
Saran
Kadar air dan α-selulosa BC harus
ditentukan untuk mengetahui tingkat kemurnian selulosa yang terbentuk. Pengujian lain juga perlu dilakukan untuk mengetahui kinerja membran lebih lanjut, seperti nilai fluks air dan indeks rejeksi. Berkaitan dengan hasil SEM yang menunjukkan ukuran pori
yang tidak seragam pada membran CA, penambahan suatu zat aditif dalam pembuatan membran perlu dilakukan untuk mengatur ukuran pori agar lebih seragam.
DAFTAR PUSTAKA
Andriansyah M. 2006. Sifat-sifat membran yang terbuat dari sari kulit buah nanas [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Arifin B. 2004. Optimasi kondisi asetilasi selulosa bakteri dari nata de coco
[skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Arviyanti E, Yulimartani N. 2009. Pengaruh penambahan air limbah tapioka pada proses pembuatan nata [skripsi]. Semarang: Fakultas Teknik, Universitas Dipenogoro.
[BPS] Badan Pusat Statistik. 2011. Tabel Luas Panen-Produktivitas-Produksi Tanaman Ubi Kayu Seluruh Propinsi [terhubung berkala]. http://www.bps.go.id [24 Juli 2011].
Desiyarni. 2006. Perancangan proses pembuatan selulosa asetat dari selulosa mikrobial untuk membran ultrafiltrasi. [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Fengel D, Wegener G. 1984. Wood: Chemistry, Ultrastructure, Reaction. Berlin: Walter de Gruyter.
Gosh R. 2003. Protein Bioseparation Using Ultrafiltration Theory, Application, and New Development. Oxford: Imperial College Press.
Hanifah TA, Saeni MS, Adijuwana H, Bintoro HMH. 1999. Evaluasi kandungan logam berat timbal dan kadmium dalam ubi kayu (Manihot esculenta Crantz) yang dipupuk sampah kota. Buletin Ilmiah Gaku-ryoku 1:38-45.
KAJIAN SPEKTROSKOPI INFRAMERAH TRANSFORMASI
FOURIER DAN MIKROSKOP ELEKTRON PAYARAN
MEMBRAN SELULOSA ASETAT DARI LIMBAH CAIR
TAPIOKA
ISMIAINI NURPATRIA PUTRI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
permeasi terjadi pada lapisan padat yang mempunyai tahanan perpindahan massa yang besar (Lindu et a.l 2008).
Gambar 11 Penampang lintang membran CA dengan perbesaran 2500 kali.
SIMPULAN DAN SARAN
SimpulanLimbah cair tapioka dapat dibuat menjadi
nata de cassava. Hal ini dibuktikan dari kesamaan spektrum selulosa dari nata de cassava dengan nata de coco. Selulosa nata de cassava dapat diasetilasi, kemudian CA yang dihasilkan dibuat menjadi membran dengan teknik inversi fase menggunakan pelarut aseton. Terbentuknya CA ditunjukkan dengan hasil analisis FTIR pada membran CA yang menunjukkan adanya pita serapan C=O pada daerah bilangan gelombang 1754.81 cm
-1
serta C-O asetil pada daerah 1042.34 cm-1. CA yang diperoleh mempunyai kadar air sebesar 21.49% dan kadar asetil sebesar 40.38% (setara dengan kisaran derajat substitusi 2.51). Pengamatan SEM pada membran CA memperlihatkan bahwa membran yang dihasilkan merupakan jenis membran mikrofiltrasi (berdasarkan fungsi) dan asimetrik (berdasarkan morfologi).
Saran
Kadar air dan α-selulosa BC harus
ditentukan untuk mengetahui tingkat kemurnian selulosa yang terbentuk. Pengujian lain juga perlu dilakukan untuk mengetahui kinerja membran lebih lanjut, seperti nilai fluks air dan indeks rejeksi. Berkaitan dengan hasil SEM yang menunjukkan ukuran pori
yang tidak seragam pada membran CA, penambahan suatu zat aditif dalam pembuatan membran perlu dilakukan untuk mengatur ukuran pori agar lebih seragam.
DAFTAR PUSTAKA
Andriansyah M. 2006. Sifat-sifat membran yang terbuat dari sari kulit buah nanas [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Arifin B. 2004. Optimasi kondisi asetilasi selulosa bakteri dari nata de coco
[skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Arviyanti E, Yulimartani N. 2009. Pengaruh penambahan air limbah tapioka pada proses pembuatan nata [skripsi]. Semarang: Fakultas Teknik, Universitas Dipenogoro.
[BPS] Badan Pusat Statistik. 2011. Tabel Luas Panen-Produktivitas-Produksi Tanaman Ubi Kayu Seluruh Propinsi [terhubung berkala]. http://www.bps.go.id [24 Juli 2011].
Desiyarni. 2006. Perancangan proses pembuatan selulosa asetat dari selulosa mikrobial untuk membran ultrafiltrasi. [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Fengel D, Wegener G. 1984. Wood: Chemistry, Ultrastructure, Reaction. Berlin: Walter de Gruyter.
Gosh R. 2003. Protein Bioseparation Using Ultrafiltration Theory, Application, and New Development. Oxford: Imperial College Press.
Hanifah TA, Saeni MS, Adijuwana H, Bintoro HMH. 1999. Evaluasi kandungan logam berat timbal dan kadmium dalam ubi kayu (Manihot esculenta Crantz) yang dipupuk sampah kota. Buletin Ilmiah Gaku-ryoku 1:38-45.
10
Kirk RE, Othmer DF. 1993. Encyclopedia of Polymer Science and Technology. New York: Interscience.
Lapuz MM, Gallerdo EG, Palo MA. 1967. The nata organism-cultural requirements characteristic and identify. Philippines J Sci 96:91-107.
Lindu M, Puspitasari T, Ismi E. 2008. Sintesis dan uji kemampuan membran selulosa asetat dari nata de coco sebagai membran ultrafiltrasi untuk menyisihkan zat warna pada air limbah artifisial. Badan Tenaga Nuklir 4:107-112.
Mallevialle J, Odendaals PE, Wischer MR. 1996. Water Treatment Membrane Processes. New York: McGraw-Hill.
McGregor WC. 1986. Membrane Separation in Biotechnology. New York: Marcel Dekker.
Mulder M. 1996. Basic Principles of Membrane Technology. Netherland: Kluwer.
Nurfiningsih. 2009. Pembuatan nata de corn
dengan Acetobacter xylinum [skripsi]. Semarang: Fakultas Teknik, Universitas Dipenogoro.
Osada Y, Nakagawa T. 1992. Membrane Science and Technology. New York: Marcel Dekker.
Pasla FR. 2006. Pencirian membran selulosa asetat berbahan dasar selulosa bakteri dari limbah nanas [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Scott K, Hughes R. 1996. Industrial Membrane Separation Technology.
London: Blackie Academic and Professionals.
Soetanto E. 2001. Membuat Patilo dan Kerupuk Ketela. Yogyakarta: Kanisius.
Sumiyati. 2009. Kualitas nata de cassava
limbah cair tapioka dengan penambahan gula pasir dan lama fermentasi yang berbeda [skripsi]. Surakarta: Fakultas
Pendidikan dan Ilmu Keguruan, Universitas Muhammadiyah Surakarta.
Susanto T, Adhitia R, Yunianta. 2000. Pembuatan nata de pina dari kulit buah nanas, kajian dari sumber karbon dan pengenceran medium fermentasi. J Teknologi Pertanian 1:58-66.
Vegantara DA. 2009. Pengolahan limbah cair tapioka menggunakan kotoran sapi perah dengan sistem anaerobik [skripsi]. Bogor: Fakultas Peternakan, Institut Pertanian Bogor.
Wenten IG. 1999. Keberadaan teknologi membran dalam industri pangan dan minuman. Di dalam Prosiding Seminar Nasional Rekayasa Kimia dan Proses, Semarang. F15(1-10).
Winding CC, Hasche RL. 1947. Chemical Engineering Series: The Technology of High Polymer. London: McGraw-Hill.
Yulianawati N. 2002. Kajian pengaruh nisbah selulosa dengan pereaksi asetilasi dan lama asetilasi terhadap produksi selulosa dari nata de coco [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
KAJIAN SPEKTROSKOPI INFRAMERAH TRANSFORMASI
FOURIER DAN MIKROSKOP ELEKTRON PAYARAN
MEMBRAN SELULOSA ASETAT DARI LIMBAH CAIR
TAPIOKA
ISMIAINI NURPATRIA PUTRI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ISMIAINI NURPATRIA PUTRI. Kajian Spektroskopi Inframerah Transformasi Fourier dan Mikroskop Elektron Payaran Membran Selulosa Asetat dari Limbah Cair Tapioka. Dibimbing oleh BETTY MARITA SOEBRATA dan SRI MULIJANI.
Limbah cair tapioka merupakan limbah yang dihasilkan dari proses pengendapan pati atau pemisahan pati dari airnya pada industri tapioka. Limbah ini masih mengandung karbohidrat seperti glukosa sehingga dapat dimanfaatkan sebagai bahan baku untuk membuat selulosa dan membran selulosa asetat (CA). Nata de cassava dibuat melalui proses fermentasi dengan Acetobacter xylinum di dalam media limbah cair tapioka. Nata kemudian dikeringkan dan dihancurkan sehingga diperoleh serbuk selulosa bakteri (BC). Serbuk BC diasetilasi dengan pereaksi anhidrida asetat untuk membentuk serbuk CA. Serbuk CA dilarutkan ke dalam pelarut aseton (sesuai kadar asetil CA yang diperoleh) dengan nisbah 16% b/v kemudian dicetak menjadi membran. Membran CA ini dicirikan menggunakan spektroskopi Inframerah Tranformasi Fourier (FTIR) dan Mikroskop Elektron Payaran (SEM). Hasil analisis spektrum FTIR pada membran CA membuktikan bahwa CA telah terbentuk sesuai dengan adanya pita serapan C karbonil pada daerah 1754.81 cm-1serta C-O asetil pada 1042.34 cm-1. Hasil analisis SEM pada membran CA menunjukkan bahwa membran yang dihasilkan merupakan jenis membran mikrofiltrasi dan asimetrik dengan diameter pori membran sekitar 0.37-0.95 μm. Serbuk CA yang dihasilkan mempunyai kadar air 21.49% dan kadar asetil 40.38% (setara dengan derajat substitusi 2.51).
ABSTRACT
ISMIAINI NURPATRIA PUTRI. Study of Fourier Transform Infrared Spectroscopy and Scanning Electron Microscope of Cellulose Acetate Membrane From Wastewater of Tapioca. Supervised by BETTY MARITA SOEBRATA and SRI MULIJANI.
KAJIAN SPEKTROSKOPI INFRAMERAH TRANSFORMASI
FOURIER DAN MIKROSKOP ELEKTRON PAYARAN
MEMBRAN SELULOSA ASETAT DARI LIMBAH CAIR
TAPIOKA
ISMIAINI NURPATRIA PUTRI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Kajian Spektroskopi Inframerah Transformasi Fourier dan Mikroskop
Elektron Payaran Membran Selulosa Asetat Dari Limbah Cair Tapioka
Nama : Ismiaini Nurpatria Putri
NIM : G44062097
Disetujui:
Betty Marita Soebrata S.Si, M.Si
NIP 19630621 198703 2 013
Dr. Sri Mulijani, MS
NIP
19630401 199103 2 001
Diketahui:
Ketua Departemen Kimia
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP
19501227 197603 2 002
atas berkat rahmat dan hidayah-Nya penulis dapat menyelesaikan karya ilmiah ini. Karya ilmiah ini berjudul Kajian
Spektroskopi Inframerah Transformasi Fourier dan
Mikroskop Elektron Payaran Membran Selulosa Asetat Dari Limbah Cair
Tapioka
, yang dilaksanakan pada bulan Januari sampai dengan Juli 2011 bertempat di Laboratorium Kimia Fisik dan Lingkungan, Departemen Kimia, Institut Pertanian Bogor.Penulis mengucapkan terima kasih kepada berbagai pihak yang telah membantu terselesaikannya karya ilmiah ini, di antaranya Ibu Betty Marita Soebrata S.Si, M.Si dan Ibu Dr. Sri Mulijani, MS. selaku pembimbing yang telah banyak memberikan pengarahan dan saran selama penelitian serta penyusunan karya ilmiah ini kepada Penulis. Ucapan terima kasih juga Penulis sampaikan kepada staf Laboratorium Kimia Fisik dan Lingkungan atas segala bantuan, fasilitas, dan saran yang diberikan.
Terima kasih yang tak terhingga penulis ucapkan kepada Ayah, Umi,dan adik-adik atas segala doa, nasihat, dan semangat yang diberikan kepada penulis. Selain itu, penulis juga mengucapkan terima kasih kepada Irvan, Charisna, Anis, Yuyun, Ina, dan teman-teman di Laboratorium Kimia Fisik dan Lingkungan, serta teman-teman-teman-teman Kimia 43 atas segala bantuan dan dukungannya selama penelitian.
Semoga karya ilmiah ini dapat bermanfaat dan menambah wawasan.
Bogor, Juni 2011
RIWAYAT HIDUP
Penulis dilahirkan di Bekasi pada tanggal 23 Desember 1988 dari ayah H. Buyung Iksal dan ibu Hj. Nuraini. Penulis merupakan anak pertama dari tiga bersaudara.
Tahun 2006 penulis lulus dari SMA Negeri I Tambun Selatan dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur SPMB. Setelah masa satu tahun perkuliahan bersama, penulis mendapat mayor Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii DAFTAR GAMBAR ... vii DAFTAR LAMPIRAN ... vii PENDAHULUAN ... 1 TINJAUAN PUSTAKA
Limbah Cair Tapioka ... 1 Selulosa Bakteri (BC) ... 2 Selulosa Asetat (CA) ... 2 Membran... 3 Pencirian Membran ... 4 BAHAN DAN METODE
Bahan dan Alat ... 4 Pembuatan Selulosa Bakteri (Nata de Cassava) ... 4 Penyiapan Serbuk Kering BC ... 4 Sintesis Selulosa Asetat ... 4 Pembuatan Membran ... 5 Pencirian Membran ... 5 HASIL DAN PEMBAHASAN
Nata de Cassava ... 5 Selulosa Asetat (CA) ... 6 Membran Selulosa Asetat (CA) ... 6 Kadar Air dan Kadar Asetil CA ... 7 Analisis Spektrum FTIR ... 7 Analisis SEM ... 8 SIMPULAN DAN SARAN
DAFTAR TABEL
Halaman
1 Hubungan derajat substitusi dengan kadar asetil ... 3 2 Kelarutan selulosa asetat ... 3
DAFTAR GAMBAR
Halaman
1 Struktur selulosa ... 2 2 Acetobacter xylinum ... 2 3 Reaksi asetilasi selulosa ... 2 4 Nata de cassava... 6 5 Serbuk CA ... 6 6 Membran CA ... 6 7 Spektrum FTIR selulosa nata de coco ... 7 8 Spektrum FTIR serbuk nata de cassava ... 8 9 Spektrum FTIR membran CA ... 8 10Permukaan membran CA dengan perbesaran 5000x... ... 8 11Penampang lintang membran CA dengan perbesaran 2500x... ... 9
DAFTAR LAMPIRAN
Halaman
PENDAHULUAN
Ketela pohon (Manihot esculenta) merupakan tanaman pangan berupa perdu yang berasal dari Benua Amerika serta memiliki nama lain ubi kayu atau singkong. Di Indonesia, singkong merupakan sumber karbohidrat yang penting setelah beras dengan kandungan karbohidrat sebesar 34.7% (Soetanto 2001). Singkong dapat tumbuh sekalipun di tanah yang kurang subur, asalkan beriklim tropis. Indonesia saat ini merupakan negara penghasil singkong terbesar ketiga di dunia setelah Brazil dan Thailand sehingga banyak masyarakat Indonesia beralih dari bertanam padi menjadi bertanam singkong (Sumiyati 2009). Menurut data Badan Pusat Statistik (BPS 2011), jumlah produksi singkong di Indonesia pada tahun 2009 adalah 22,039,145 ton dan pada tahun 2010 meningkat menjadi sebesar 23,908,459 ton (angka sementara).
Singkong dapat dikonsumsi langsung sebagai bahan makanan atau digunakan sebagai bahan baku industri pangan, salah satunya adalah industri tapioka. Proses pembuatan tapioka pada industri akan menghasilkan limbah padat (onggok) dan limbah cair. Limbah cair tapioka dapat dihasilkan dari tahap pencucian bahan baku (singkong) serta proses pengendapan untuk memisahkan pati dari airnya. Teknologi yang ada saat ini belum mampu memisahkan seluruh pati yang terlarut dalam air sehingga limbah cair yang dilepaskan ke lingkungan masih mengandung pati. Limbah cair akan mengalami dekomposisi secara alami di badan-badan perairan dan menimbulkan bau yang tidak sedap. Bau tersebut dihasilkan pada proses penguraian senyawa yang mengandung nitrogen, sulfur, dan fosforus dari bahan berprotein (Zaitun 1999 dan Hanifah et al. 1999). Alternatif lain yang dapat dilakukan untuk mengolah limbah cair ini menjadi produk yang dapat dimanfaatkan lebih lanjut adalah mengolahnya menjadi nata yang disebut nata de cassava.
Pembentukan nata membutuhkan unsur C yang berasal dari glukosa serta unsur N dan O yang berasal dari penambahan amonium sulfat. Unsur-unsur ini digunakan sebagai nutrisi dan sumber karbon bagi bakteri
Acetobacter xylinum agar dapat membentuk nata. Limbah cair tapioka mengandung glukosa sebagai unsur karbon sehingga dapat digunakan sebagai medium yang baik untuk merangsang pertumbuhan bakteri tersebut saat membentuk nata. Oleh karena itu, limbah cair
tapioka berpotensi menghasilkan nata. Nata tersebut berupa selulosa yang dihasilkan oleh bakteri sehingga dapat disebut sebagai selulosa bakteri (BC). Selain itu, nata dapat dicirikan sebagai gabungan dari serat-serat karbon yang menjadi suatu bentuk yang kokoh dan berpori sehingga nata berpotensi untuk dimanfaatkan sebagai membran selulosa. Akan tetapi, membran selulosa tersebut tidak memiliki nilai komersial yang tinggi. Oleh karena itu, pengolahan lebih lanjut diperlukan untuk mengubahnya menjadi membran selulosa asetat (CA) yang memiliki nilai jual lebih tinggi.
Membran merupakan lapisan semipermeabel yang tipis dan dapat digunakan untuk memisahkan 2 komponen dengan cara menahan dan melewatkan komponen tertentu melalui pori-pori (Osada dan Nakagawa 1992). Beberapa keuntungan dalam penggunaan teknologi membran pada proses pemisahan antara lain prosesnya sangat sederhana, konsumsi energi rendah, tidak merusak material, tidak menggunakan zat kimia tambahan, dan tidak menghasilkan limbah baru sehingga tergolong sebagai teknologi bersih (Lindu et al. 2008).
Penelitian ini bertujuan membuat membran CA berbahan dasar limbah cair tapioka, serta mengidentifikasinya dengan spektroskopi inframerah transformasi fourier (FTIR) dan Mikroskop Elektron Payaran (SEM). Analisis ini dilakukan untuk mencirikan gugus fungsi dan jenis membran CA yang dihasilkan.
TINJAUAN PUSTAKA
Limbah Cair Tapioka
Salah satu pemanfaatan singkong selain sebagai bahan pangan kaya karbohidrat adalah sebagai bahan baku industri tapioka. Proses pembuatan tapioka di industri besar maupun industri kecil secara umum meliputi tahap pengupasan kulit, pencucian, pemarutan, pengekstrakan, pengendapan pati, dan pengeringan.
2
H2SO4
2313.54 mg L-1, COD sebesar 3200 mg L-1, padatan terlarut 638–2836 mg L-1, serta kandungan sianida (CN) sebesar 19.58–33.75 mg L-1 (Vegantara 2009). Oleh karena itu, apabila limbah ini dibuang ke lingkungan akan menyebabkan pencemaran lingkungan, seperti bau yang tidak sedap dan beberapa sumur warga yang tidak layak untuk dikonsumsi.
Selulosa Bakteri (BC)
Selulosa (Gambar 1) ialah polimer tak bercabang dari sejumlah glukosa yang tergabung melalui ikatan 1,4-β-glikosida. Pemeriksaan selulosa dengan sinar-X menunjukkan bahwa selulosa merupakan rantai linear dari selobiosa, yang oksigen cincinnya berselang-seling dengan posisi “ke
depan” dan “ke belakang” (Hart et al. 2003).
Gambar 1 Struktur selulosa.
A. xylinum (Gambar 2) merupakan bakteri Gram negatif, aerob, berbentuk batang dengan panjang 2 mikron, tidak membentuk spora dan nonmotil, serta umumnya berupa sel tunggal atau membentuk rantai dengan sel yang lain. Bakteri A. xylinum tergolong famili Pseudomonadaceae dan termasuk genus
Acetobacter. Sifat khas bakteri ini adalah kemampuannya untuk membentuk selaput tebal nata pada permukaan cairan fermentasi yang mengandung selulosa (Nurfiningsih 2009). Selain media yang mengandung gula, bakteri ini juga menyukai lingkungan yang asam dan membutuhkan sumber nitrogen untuk aktivitasnya. A. xylinum bersifat peka terhadap perubahan fisik dan kimia lingkungannya yang akan berpengaruh terhadap nata yang dihasilkan.
Gambar 2 Acetobacter xylinum.
Pembentukan BC terjadi karena proses pengambilan glukosa dari media yang mengandung gula oleh sel-sel A. xylinum. Glukosa tersebut kemudian digabungkan dengan asam lemak membentuk bahan pendahulu nata (prekursor) pada membran sel. Prekursor ini selanjutnya disekresi dan bersama enzim mempolimerisasikan glukosa menjadi selulosa di luar sel (Susanto et al. 2000). Menurut Nurfiningsih (2009), selulosa ini akan membentuk jaringan mikrofibril yang panjang dalam cairan fermentasi. Gelembung CO2 yang dihasilkan selama fermentasi
cenderung melekat pada jaringan ini sehingga menyebabkan jaringan ini terangkat ke permukaan cairan.
Pertumbuhan A. xylinum dipengaruhi oleh beberapa faktor, antara lain pH, suhu, sumber nitrogen, dan sumber karbon (Lapuz et al. 1967). Faktor lain yang berpengaruh terhadap hasil nata adalah wadah fermentasi atau jumlah larutan induk. Jumlah larutan induk yang relatif besar dapat meningkatkan rendemen nata karena akan semakin banyak pula jumlah bakteri A. xylinum yang ada (Nurfiningsih 2009).
Selulosa Asetat (CA)
Selulosa asetat (CA) secara umum terdiri atas 2 jenis, yaitu selulosa triasetat (CA primer) dan selulosa diasetat (CA sekunder). CA primer dibuat melalui reaksi esterifikasi (asetilasi) selulosa sedangkan CA sekunder dibuat dengan cara menghidrolisis CA primer (Desiyarni 2006).
Selulosa triasetat diperoleh dari reaksi selulosa dengan anhidrida asetat dan katalis H2SO4. Gugus hidroksil (-OH) pada selulosa
digantikan dengan gugus asetil pada anhidrida asetat (Gambar 3).
+
Asetilasi merupakan tahap terpenting dalam pembuatan CA karena berhubungan dengan kemampuannya larut dalam pelarut organik tertentu pada proses pembuatan membran. Kelarutan CA dalam pelarut organik dipengaruhi oleh kadar asetil yang dihasilkan (Desiyarni 2006). Pengaturan kadar asetil tersebut dilakukan melalui reaksi hidrolisis menggunakan asam asetat encer hingga diperoleh derajat substitusi yang sesuai. Hubungan antara kadar asetil dan derajat substitusi ditunjukkan pada Tabel 1, sedangkan hubungan antara kadar asetil dan pelarut yang sesuai ditunjukkan pada Tabel 2.
Tabel 1 Hubungan derajat substitusi dengan kadar asetil
Derajat substitusi Kadar asetil (%bobot)
0.6–0.9 1.2–1.8 2.2–2.7 2.8–3.0
13.0–18.6 22.2–32.2 36.5–42.2 43.0–44.8
Sumber: Fengel dan Wegener (1985).
Tabel 2 Kelarutan selulosa asetat Kadar asetil