KAJIAN SPEKTROSKOPI INFRAMERAH TRANSFORMASI
FOURIER DAN MIKROSKOPI SUSURAN ELEKTRON
MEMBRAN SELULOSA ASETAT DENGAN PENAMBAHAN
POLI(ETILENA GLIKOL)
NAZER VENTURA RENAISSANCE
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
KAJIAN SPEKTROSKOPI INFRAMERAH TRANSFORMASI
FOURIER DAN MIKROSKOPI SUSURAN ELEKTRON
MEMBRAN SELULOSA ASETAT DENGAN PENAMBAHAN
POLI(ETILENA GLIKOL)
NAZER VENTURA RENAISSANCE
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Kajian Spektroskopi Inframerah Transformasi Fourier dan Mikroskopi
Susuran Elektron Membran Selulosa Asetat dengan Penambahan Poli(etilena
glikol)
Nama : Nazer Ventura Renaissance
NIM
: G44201059
Menyetujui:
Pembimbing I,
Pembimbing II,
Betty Marita Soebrata, S.Si, M.Si.
Dra. Sri Mulijani, MS
NIP 131 694 523
NIP 131 950 978
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. Ir. Yonny Koesmaryono, MS
NIP 131473999
PRAKATA
Alhamdulillahirobbilalamin
, segala puji bagi Allah SWT Tuhan Yang Maha
Kuasa, berkat limpahan rahmat dan karunia -Nya Penulis dapat menyelesaikan karya
ilmiah ini. Shalawat dan salam semoga selalu tercurah kepada Nabi Allah Muhammad
SAW beserta keluarga. Karya ilmiah ini berjudul
Kajian Spektroskopi Inframerah
Transformasi Fourier dan Mikroskopi Susuran Elektron Membran Selulosa Asetat
dengan Penambahan Poli(etilena glikol).
Penelitian ini didanai oleh Program Hibah
Kompetisi A2, Departemen Kimia, Institut Pertanian Bogor, tahun 2005,
yang
dilaksanakan pada bulan November sampai dengan Juni 2006 bertempat di laboratorium
Kimia Anorganik dan Kimia Organik, IPB.
Penulis mengucapkan terima kasih bagi semua pihak yang telah membantu
penyelesaian karya ilmiah ini, terutama kepada Ibu Betty Marita Soebrata, S.Si, M.Si dan
Dra. Sri Mulijani, MS selaku pembimbing yang baik dan senantiasa menyempatkan
waktu untuk berkonsultasi terutama dimasa-masa sulit Penulis selama penelitian, serta
kepada Mama, Papa,
Kak
Petit,
Teh
Iis,
Om
Monang yang telah banyak berkorban materi,
waktu, tenaga, dan juga senantiasa membantu dengan doa untuk suksesnya penelitian ini.
Penulis juga mengucapkan terima kasih kepada Budi Arifin, S.Si, Bapak Drs. Ahmad
Sjahriza, Bapak Muhammad Farid, S.Si, atas diskusi-diskusi yang begitu berharga
berkaitan dengan penelitian ini dan teman seperjuangan yang tak pernah menyerah dalam
suka dan duka, Riya. Penulis juga mengucapkan ucapan terima kasih yang tulus kepada
Fithrie atas semangat dan motivasinya kepada Penulis. Terima kasih juga kepada
Red
House Family
atas keceriaan yang terjalin.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, April 2006
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 16 September 1982 dari ayah Zulnazri
Jaya dan Ibu Sofnawati Penulis merupakan anak ke dua dari dua bersaudara. Tahun 2001
penulis lulus dari SMU Negeri 38 Jakarta dan pada tahun yang sama diterima Institut
Pertanian Bogor (IPB) melalui jalur Ujian Masuk Perguruan Tinggi Negeri di Program
Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... x
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Ananas comosus L
... 1
Selulosa Asetat ... 1
Poli(etilena glikol) (PEG) ... 2
Membran... 2
Pencirian Membran ... 3
Membran Selulosa Asetat ... 3
BAHAN DAN METODE
Bahan dan Alat ... 3
Metode ... 3
HASIL DAN PEMBAHASAN
Pembuatan
Nata de Pina
... 5
Asetilasi ... 5
Membran Selulosa Asetat ... 5
Analisis FTIR ... 6
Analisis SEM ... 7
SIMPULAN DAN SARAN
Simpulan ... 8
Saran ... 8
DAFTAR PUSTAKA ... 8
DAFTAR TABEL
Halaman
1 Syarat mutu selulosa asetat ... 1
2 Hubungan derajat substitusi selulosa asetat, kadar asetil,
dan aplikasinya ... 2
3 Kisaran tekanan, pori, dan bobot molekul berbagai jenis membran ... 2
DAFTAR GAMBAR
Halaman
1
Reaksi asetilasi selulosa asetat ... 2
2
Struktur Poli( etilena glikol) (PEG) ... 2
3
Membran selulosa asetat dengan penambahan PEG ... 6
4
FTIR selulosa ... 6
5
FTIR membran selulosa asetat dengan penambahan PEG ... 7
6
FTIR membran selulosa asetat tanpa penambahan PEG ... 7
7
SEM membran selulosa asetat dengan penambahan PEG... 7
8
SEM membran selulosa asetat tanpa penambahan PEG ... 8
DAFTAR LAMPIRAN
Halaman
1
Diagram alir penelitian ... 11
PENDAHULUAN
Teknologi pemisahan menggunakan membran semakin berkembang pesat dari waktu ke waktu. Penggunaan membran dapat ditemui pada hampir semua industri, seperti industri tekstil, m akanan, dan minuman. Teknologi pemisahan menggunakan membran memiliki beberapa kelebihan, antara lain energi yang dibutuhkan untuk pemisahan bahan terlarut rendah serta proses pemisahan tidak dilakukan dalam fase uap tetapi dalam fase cair. Selain itu, pemisahan menggunakan membran juga lebih sederhana, tidak memerlukan bahan kimia tambahan, dan ramah lingkungan (Fadillah 2003).
Nanas merupakan salah satu komoditas pertanian Indonesia. Produksi nanas Indonesia dari tahun ke tahun kian meningkat. Menurut BPS (2005), produksi nanas di Indonesia pada tahun 2001, 2002, dan 2003 mencapai berturut -turut 494.968 ton, 555.588 ton, dan 677.089 ton. Satu buah nanas hanya dapat dikonsumsi sebanyak 53% -nya saja sehingga apabila limbah kulit nanas tidak dimanfaatkan, maka akan membusuk dan mencemari lingkungan. Untuk itu, diperlukan upaya pemanfaatan limbah kulit nanas dengan cara mengubah kulit nanas menjadi nata de pina dengan bantuan Acetobacter xylinum, selanjutnya diolah menjadi membran.
Nata atau selulosa bakteri merupakan hasil fermentasi substrat yang mengandung gula dari aktivitas bakteri A. xylinum. Salah satu produk selulosa bakteri yang telah dikenal oleh sebagian besar masyarakat sebagai bahan pangan adalah nata de coco yang dibentuk dari media air kelapa. Selain itu, dikenal pula nata yang dibentuk dari media ampas tahu (nata de soya), ekstrak nanas (nata de pina) atau ekstrak mangga (nata de mango).
Penelitian tentang membran yang dibuat dari nata de pina telah dilakukan oleh Andriansyah (2005) dan Prawesti (2006). Tresnawati (2006) dan Pasla (2006) melakukan proses asetilasi terlebih dahulu terhadap nata de pina menghasilkan membran selulosa asetat. Arifin (2004) juga melakukan penelitian terhadap nata de coco menjadi selulosa asetat. Penelitian tentang pembuatan membran selulosa asetat dengan menambahkan poli(etilena glikol) (PEG) dilakukan oleh Fadhillah (2003). Ia membuat membran dari selulosa asetat komersial dengan penambahan PEG sebagai
pembentuk pori. Penelitian-penelitian yang pernah dilakukan tersebut dijadikan acuan untuk mengolah nata de pina menjadi selulosa asetat yang lebih lanjut dapat diaplikasikan sebagai membran. Membran yang diperoleh kemudian dicirikan dengan Spektroskopi Inframerah Transformasi Fourier (FTIR) dan Mikroskopi Susu ran Elektron (SEM). SEM dapat memperlihatkan topografi dan morfologi membran dengan batas resolusi sampai ukuran mikrometer sedangkan FTIR dapat mengidentifikasi senyawa-senyawa organik berdasarkan informasi dari gugus fungsi yang ditunjukkan dalam spektrum.
Penelitian ini bertujuan untuk mempelajari pengaruh penambahan PEG pada membran selulosa asetat dari kulit nanas melalui analisis FTIR dan SEM.
TINJAUAN PUSTAKA
Ananas comosus L.
Ananas comosus yang dikenal sebagai nanas di Indonesia termasuk dalam divisi Plantae, subdivisi Spermatophyta, kelas Monocotyledonae, ordo Farinosae, famili Bromoliaceae, genus Ananas, dan spesies Ananascomosus (Collins 1968).
Bagian dari buah nanas yang digunakan pada penelitian ini adalah kulitnya, karena pada industri pengolahan buah nanas, kulit nanas merupakan limbah yang melimpah. Pengolahan kulit nanas salah satunya ialah dengan menjadikannya produk nata de pina yang kemudian dapat diolah lebih lanjut menjadi membran.
Selulosa Asetat
9
C C O
H
H H
H n
Tabel 1 Syarat mutu selulosa asetat (SNI 1991)
Parameter Persyaratan
Kadar asetil Kekentalan intrinsik (pelarut aseton) Kestabilan terhadap kalor 39.0–40.0% 1.5–1.8 dl/g
Tidak terjadi pengarangan saat dipanaskan (180ºC, 8
jam); perubahan kekentalan intrinsik akibat
pemanasan dicantumkan
Salah satu bentuk esterifikasi adalah asetilasi selulosa dengan menggunakan anhidrida asetat yang menghasilkan selulosa asetat. Reaksi asetilasi selulosa asetat dapat dilihat pada Gambar 1.
Gambar 1 Reaksi asetilasi selulosa asetat (Anonim 2005).
Menurut Mark et al. (1965), produk-produk yang terbuat dari plastik selulosa asetat di antaranya adalah gagang obeng, gagang pisau, rambu-rambu, pipa gas alam, tombol-tombol radio dan televisi, pena, pensil, boneka, dan mainan lainnya. Aplikasi ini bergantung pada jenis selulosa asetat yang diperoleh yang dapat dilihat dari derajat substitusinya. Hubungan antara aplikasi selulosa asetat terhadap pelarut dan derajat substitusi disenaraikan pada Tabel 2.
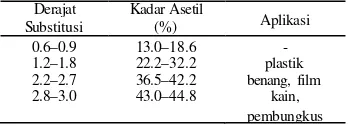
Tabel 2 Hubungan antara derajat substitusi selulosa asetat, kadar asetil, dan aplikasinya (Fengel & Wegener 1989)
Derajat Substitusi
Kadar Asetil
(%) Aplikasi
0.6–0.9 1.2–1.8 2.2–2.7 2.8–3.0 13.0–18.6 22.2–32.2 36.5–42.2 43.0–44.8 - plastik benang, film kain, pembungkus
Poli(etilena glikol) (PEG)
Poli(etilena glikol) (PEG) adalah molekul sederhana dengan struktur moleku l linear atau bercabang. Pada suhu ruang, PEG dengan bobot molekul di bawah 700 berbentuk cair, sedangkan yang memiliki
bobot molekul 700–900 berbentuk semi padat, dan PEG dengan bobot molekul 900–1000 atau lebih berbentuk padatan. PEG larut dalam air dan beberapa pelarut organik seperti toluena, aseton, metanol, dan metilklorida tetapi tidak larut dalam heksana dan hidrokarbon alifatik yang sejenis (Fadillah 2003).
PEG secara komersial dibuat dari reaksi antara etilena glikol (HOCH2CH2OH) dengan sejumlah kecil katalis natrium klorida. Jumlah etilena glikol menentukan bobot molekul dari PEG. Struktur PEG ditunjukkan oleh Gambar 2.
Gambar 2 Struktur PEG.
Menurut Fadillah (2003), interaksi konsentrasi PEG dengan selulosa asetat menunjukkan pengaruh yang sangat nyata terhadap ukuran pori-pori membran. Fluks membran didapati bertambah dengan bertambahnya konsentrasi PEG dan dengan berkurangnya konsentrasi selulosa asetat. Dalam penelitian yang lain (Yang et al. 2001), nilai fluks membran komposit selulosa-kitosan semakin meningkat dengan meningkatkan konsentrasi PEG.
Membran
Membran adalah lapisan semipermeabel berupa padatan polimer tipis yang dapat menahan pergerakan bahan tertentu (Scott & Hughes 1996). Menurut Osada & Nakagawa (1992), membran merupakan lapisan semipermeabel tipis yang dapat digunakan untuk memisahkan dua komponen dengan cara menahan dan melewatkan komponen tertentu melalui pori-porinya.
Klasifikasi Membran
10
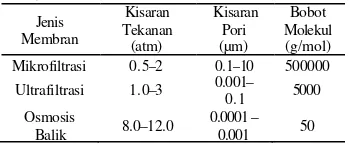
Tabel 3 Kisaran tekanan, pori, dan bobot molekul berbagai jenis membran (Mulder 1996) Jenis Membran Kisaran Tekanan (atm) Kisaran Pori (µm) Bobot Molekul (g/mol)
Mikrofiltrasi 0.5–2 0.1–10 500000
Ultrafiltrasi 1.0–3 0.001–
0.1 5000
Osmosis
Balik 8.0–12.0
0.0001 –
0.001 50
Pencirian Membran
Ciri, desain, dan aspek segi teknik kimia merupakan beberapa faktor yang harus diperhatikan dalam pengendalian kinerja membran. Menurut Brocks (1983), Osada & Nakagawa (1992), dan Wenten (1999), ciri-ciri membran terdiri dari struktur, ukuran pori, dan sifat fisik mekanik, dan kimia dari membran.
FTIR
Analisis FTIR digunakan untuk mengidentifikasi senyawa organik dari gugus fungsional yang dimilikinya yang diperoleh dengan mengkaji spektrum yang terbaca. Hal ini terjadi karena gugus-gugus fungsi dalam senyawa organik dapat menyerap radiasi elektromagnetik pada daerah inframerah dengan panjang gelombang 2.5–25 µm atau dari bilangan gelombang 400–4000 cm-1 (Pavia et al 2000).
S EM
Analisis SEM merupakan salah satu metode yang digunakan untuk mencirikan membran mikrofiltrasi. Batas resolusi mikroskop elektron 0,01 µm (10 nm) sampai sekitar 0,005 µm (5 nm). Prinsip SEM dapat dijelaskan sebagai berikut. Elektron dengan energi kinetik tinggi dipancarkan oleh sumber mengenai sampel membran. Pantulan elektron ini (elektron kedua) akan ditangkap oleh detektor sehingga membentuk bayangan tertentu. Tampilan permukaan sampel bergantung pada intensitas pengukuran elektron kedua (Darwo 2003). Hasil foto SEM merupakan gambar topografi yang memperlihatkan segala tonjolan, lekukan, maupun lubang permukaan.
Membran Selulosa Asetat
Selulosa asetat merupakan salah satu bahan dasar membran asimetrik, baik untuk
osmosis balik, ultrafiltrasi, atau mikrofiltrasi. Pembuatan selulosa asetat biasanya dilakukan dengan cara pembalikan fase melalui proses pencelupan (Mulder 1996).
Membran yang dihasilkan dengan cara ini sering disebut sebagai membran tipe Loeb-Sourajan, merujuk pada nama penemunya. (Baker 2004). Membran yang dihasilkan berstruktur asimetrik, dengan lapisan tipis berketebalan 0.02−0.05 µm.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang diperlukan dalam penelitian ini ialah starter (bakteri A. xylinum) yang diperoleh dari pengusaha nata de coco di daerah Cipaku Bogor, kulit buah nanas yang diperoleh dari limbah penjual rujak depan kampus IPB Baranangsiang, cuka pekat teknis 98% (v/v), asam asetat glasial 100%, anhidrida asetat, gula pasir, diklorometana, NaOH kristal, H2SO4 95–97%(b/b), PEG(BM=6000), (NH4)2SO4 kristal, dan air suling.
Alat-alat yang digunakan dalam penelitian ini ialah alat -alat kaca, pompa vakum, hot plate, oven, penangas, pengaduk magnetik, blender Philips, wadah fermentasi berukuran 30×20×4,5 cm3 merk Komet Star Plastics jenis Tripoly nomor 3 yang dibeli di toko Sejahtera Surya Kencana, neraca analitik, sentrifus Hermle Z300 (Labnet), pengaduk magnetik, lempeng kaca, pelapis ion Polaron SC 7610 Sputter Coater, Scanning Electron Microscopy (SEM) LEO Oxford Link Penafet model 6599, dan Fourier Transform Infrared Spectroscopy (FTIR)-8201PC Shimadzu FTCOM-1. Analisis FTIR dilakukan di laboratorium jaminan mutu, PT Abbot, Cibinong dan SEM dilakukan di Laboratorium SEM, Departemen Metalurgi dan Material, Fakultas Teknik, Universitas Indonesia, Jakarta.
Metode
Diagram alir penelitian ini dapat dilihat secara garis besar pada Lampiran 1.
Pembuatan Selulosa Bakteri (Nata de pina)
(Susanto et al. 2000)
11
ini dilakukan dengan volume larutan 600 mL nisbah ekstrak nanas -air 1:4. Larutan ini direbus sampai mendidih pada suhu 100 °C. Setelah itu, ditambahkan gula pasir 7.5%(b/v) dan (NH4)2SO4 0.5%(b/v). Media yang diperoleh segera dipindahkan dalam keadaan panas ke dalam nampan plastik dan diatur pH-nya menjadi 4.5 dengan penambahan asam asetat glasial. Nampan segera ditutup dengan kertas koran yang sebelumnya telah dipanaskan dan diikat dengan karet pengikat, kemudian dibiarkan selama semalam pada suhu kamar. Selanjutnya, inokulum sebanyak 10%(v/v) ditambahkan ke dalam larutan dan diinkubasikan pada suhu kamar selama 7 hari.
Pemurnian selulosa (Safriani 2000)
Lembaran nata de pina dicuci menggunakan air keran, lalu dipotong-potong dengan ukuran sekitar 4×5 cm. Potongan nata ini selanjutnya direbus dalam air mendidih selama kira-kira 20 menit. Setelah itu, nata direndam dalam larutan NaOH 1%(v/v) pada suhu kamar selama 24 jam, kemudian dinetralkan dengan perendaman dalam asam asetat 1%(v/v) selama 24 jam. Produk yang diperoleh dicuci beberapa kali dengan air, lalu disaring-vakum untuk menarik air sehingga diperoleh lembaran nata yang tipis. Lembaran ini dikeringkan pada suhu kamar selama 2-3 hari. Nata de pina kering selanjutnya dihancurkan dengan blender, sehingga berbentuk serbuk yang berukuran 40 mesh.
Pembuatan Selulosa Asetat
Selulosa asetat pada penelitian ini dibuat dengan modifikasi prosedur pembuatan selulosa asetat yang dilakukan oleh Arifin (2004). Prosedurnya ialah sebagai berikut:
Aktivasi
Sebanyak 0.9 gram selulosa yang diperoleh dari tahap pemurnian dicampurkan dengan 100 mL asam asetat glasial di dalam botol bertutup ganda, lalu dikocok dengan kecepatan 200 rpm selama 20 menit dengan pengadukan kuat pada beberapa menit pertama. Selanjutnya, selulosa disaring-vakum dan diperas sekuat mungkin. Perlakuan yang sama diulangi sekali lagi. Selulosa yang telah diperas dikembalikan ke
dalam botol yang sama dan direndam dalam 50 mL asam asetat glasial murni selama 3 jam pada suhu kamar. Botol kemudian dikocok dengan shaker (200 rpm). Setelah 3 jam, selulosa di saring-vakum dan diperas sekuat mungkin.
Asetilasi
Ke dalam botol bertutup ganda yang berisi selulosa yang diaktivasi, ditambahkan asam asetat glasial dan asam sulfat 95–97% dengan perbandingan 100:1 (10.1 mL). Campuran dikocok kuat selama 1 menit lalu anhidrida asetat ditambahkan tetes demi tetes sambil diaduk dengan nisbah bobot contoh terhadap volume anhidrida sebesar 1:5, dalam penangas bersuhu 40 °C. Larutan dibiarkan selama 2 jam dalam penangas bersuhu 40 °C. Waktu 2 jam dihitung sejak ditambahkannya anhidrida asetat.
Hidrolisis
Campuran air dan asam asetat glasial (2:1) sebanyak 2.4 mL ditambahkan ke dalam larutan hasil asetilasi dengan diaduk pada beberapa menit pertama. Larutan dibiarkan pada suhu 40 °C selama 30 menit terhitung sejak
ditambahkannya asam asetat encer.
Pemurnian
Larutan hasil hidrolisis dipisahkan dari contoh yang tidak terasetialsi dengan disentrifugasi dengan kecepatan 4000 rpm selama 15 menit. Selanjutnya, supernatan dituang ke dalam 500 mL air distilasi yang diaduk kuat dengan pengaduk magnetik. Endapan yang terbentuk disaring-vakum. Serbuk selulosa asetat ini dinetralkan pH-nya dengan NaHCO3 1 N, lalu dicuci dengan air distilata.
Pembuatan membran selulosa asetat
(Fadhillah 2003)
12
Pencirian Membran
S EM
Salah satu sisi double-tip direkatkan pada suatu silinder logam steril yang diameternya lebih besar daripada ukuran contoh. Penutup sisi lainnya diungkit, lalu contoh dengan ukuran 1×1 cm direkatkan. Silinder diletakkan di dalam pelapis ion untuk divakum selama 3 jam dengan tekanan 0.1 mbar. Setelah 3 jam, contoh dilapisi dengan logam Pt-Au menggunakan pelapis ion Polaron SC 7610 Sputter Coater, lalu difoto dengan instrumen LEO Oxford Link Penafet model 6599.
FTIR
Lembaran membran dipotong dengan ukuran 3×1,5 cm. Contoh dijepit dengan pinset, lalu diletakkan di dalam tempat contoh. Tempat contoh itu dimasukkan ke dalam instrumen FTIR 8201PC Shimadzu FTCOM -1 yang telah dipanaskan selam a 15 menit, lalu lampu dinyalakan tepat mengenainya, dengan bilangan gelombang 400–4000 cm-1.
HASIL DAN PEMBAHASAN
Pembuatan nata de pina
Pembuatan nata terdiri atas tiga tahapan, yaitu penyiapan media, inokulasi bakteri, dan pemurnian nata. Pada tahap penyiapan media sari kulit nanas terlebih dahulu dididihkan untuk mencegah kontaminasi oleh bakteri. Setelah itu, ditambahkan amonium sulfat yang menjadi sumber nitrogen dan gula pasir sebagai sumber karbon. Menurut Susanto et al. (2000) penambahan amonium sulfat dan gula pasir merupakan faktor yang penting dalam tumbuh kembang A. xylinum. Selain hal tersebut, ketersediaan udara yang cukup pada media fermentasi akan mempercepat pembentukan nata. Oleh karena itu, pada penelitian ini digunakan wadah berbentuk segi empat dengan luas permukaan yang lebar. Hal ini dimaksudkan agar pertukaran oksigen dapat berlangsung dengan baik. Sebelum inokulasi bakteri, media diatur pH nya menjadi 4.5 yang merupakan kondisi optimum pembentukan nata oleh A. xylinum. Bakteri yang diinokulasi konsentrasinya 10%(v/v), karena dengan konsentrasi tersebut diharapkan rendemen yang dihasilkan cukup tinggi dan pembentukan nata lebih cepat. Setelah 24
jam, di dalam media terlihat serat -serat halus berlendir membentuk suatu lapisan teba l atau pelikel. Pembentukan nata ini mencapai optimum terjadi pada hari ke-7, yaitu saat terbentuknya nata secara sempurna yang ditandai dengan tidak bersisanya larutan pada media.
Asetilasi
Proses asetilasi mensyaratkan kondisi bebas-air karena reaksi esterifikasi bersifat reversibel sehingga kadar air yang terlalu tinggi pada selulosa akan meningkatkan laju hidrolisis dan tidak terbentuknya produk selulosa asetat. Berdasarkan persyaratan tersebut, selulosa yang akan diasetilasi harus diaktivasi terlebih dahulu. Digunakan 50 ml asam asetat glasial dengan cara direndam selama 3 jam untuk menarik air yang ada pada selulosa. Proses dilanjutkan dengan penyaringan vakum, lalu selulosa diperas sekuat mungkin untuk menarik air yang telah berikatan hidrogen dengan asam asetat.
Reaksi esterifikasi yang terjadi berupa substitus satu, dua, atau tiga gugus hidroksil dari unit anhidro glukosa dengan gugus asetil dari anhidrida asetat. Nisbah bobot selulosa dan volume anhidrida asetat yang digunakan adalah 1:5. Penambahan anhidrida asetat dilakukan tetes demi tetes pada suhu 40 °C. Suhu asetilasi harus dijaga agar tidak melebihi 50 °C, karena reaksi asetilasi adalah reaksi eksoterm sehingga apabila suhu melebihi 50 0C akan mengakibatkan pemutusan rantai selulosa (Kirk dan Othmer 1993).
Tetesan awal anhidrida asetat mengakibatkan selulosa di dalam botol menggumpal. Kemudian secara bertahap selulosa akan larut sempurna yang ditandai dengan tidak ada lagi sisa cairan pereaksi di dalam
Membran Selulosa Asetat
13
mengalami kegagalan dalam proses pencetakan sebagai lapisan tipis. Hal ini terjadi karena komposisi PEG yang meningkat menyebabkan viskositas menjadi lebih tinggi, sehingga menimbulkan kesulitan dalam proses pencetakan membran. Larutan polimer selulosa asetat dalam pelarut diklorometana harus dikocok agar homogen sehingga mempermudah proses pencetakan membran. Menurut Darwati etal. (2002), larutan polimer yang tidak homogen akan memerangkap gelembung-gelembung udara sehingga permukaan membran menjadi tidak rata.
Membran selulosa asetat yang diperoleh membentuk lembaran plastik transparan seperti terlihat pada Gambar 3.
Gambar 3 Membran selulosa asetat dengan penambahan PEG.
Analisis FTIR
Analisis FTIR digunakan untuk membuktikan bahwa gugus hidroksil telah tersubstitusi oleh gugus asetil dari anhidrida asetat melalui reaksi asetilasi. Selain itu, analisis FTIR digunakan untuk melihat interaksi PEG yang ditambahkan pada membran. Spektrum FTIR selulosa murni dapat dilihat pada Gambar 4. Spektrum membran selulosa asetat dengan penambahan PEG dan tanpa PEG dapat dilihat pada Gambar 5 dan 6. Spektrum FTIR pada Gambar 4 dan 5 memperlihatkan
perbedaan pada bilangan gelombang 1725 cm-1 yang diidentifikasi sebagai gugus C=O ester, karena terdapat pula vibrasi ulur C-O pada puncak 1030.9 cm-1. Hal ini berarti membran telah terasetilasi.
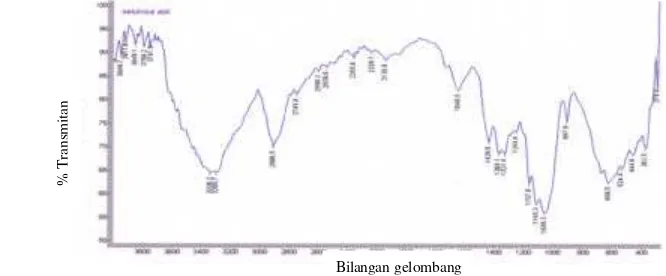
Gambar 5 memperlihatkan beberapa pita serapan. Pita serapan gugus -OH terdapat pada bilangan gelombang 3468,7 cm-1. Gugus -OH ini diduga adalah gugus -OH dari selulosa yang tidak terasetilasi oleh anhidrida asetat. Hal ini sesuai dengan penetapan kadar asetil yang diperoleh Tresnawati (2006), yaitu sebesar 43.0% (Lampiran 2). Setara dengan kisaran derajat substitusi 2.8–3.0 (Tabel 2). Hal ini berarti tidak semua gugus -OH dari selulosa diasetilasi oleh anhidrida asetat sehingga masih terdapatnya pita serapan gugus hidroksil pada bilangan gelombang 3468,7 cm-1. Serap an lainnya ada pada daerah panjang gelombang 1370–1450 cm-1 untuk vibrasi ulur -CH dan pada daerah 2946.1 cm-1 untuk vibrasi ulur-CH3.
Spektrum FTIR pada Gambar 5 masih memperlihatkan perbedaaan spektrum dengan Gambar 6 yaitu munculnya serapan baru pada bilangan gelombang 2339.5 dan 2120.6 cm-1 serta hilangnya puncak pada bilangan gelombang 1562.2 cm-1. Hal ini berarti terjadi interaksi kimiawi antara PEG yang ditambahkan dengan membran selulosa asetat.
Gambar 4 Spektrum FTIR selulosa murni.
Bilangan gelombang
14
Gambar 5 Spektrum FTIR membran selulosa asetat dengan penambahan PEG.
Gambar 6 Spektrum FTIR membran selulosa asetat tanpa penambahan PEG.
Analisis SEM
Hasil SEM membran selulosa asetat dengan penambahan PEG dapat dilihat pada Gambar 7. Foto SEM tersebut memperlihatkan permukaan yang rata dan ukuran pori yang seragam. Hal ini diperkirakan karena membran tersebut memiliki ketebalan yang hampir sama pada permukaannya. Ketebalan yang merata disebabkan oleh homogennya larutan yang terjadi antara polimer selulosa asetat dan PEG dalam pelarut diklorometana. Pembuatan larutan polimer yang tidak homogen menyebabkan terperangkapnya gelembung-gelembung udara sehingga pada saat pencetakan pada lempeng kaca dengan batang pengaduk, membran yang dihasilkan memiliki ketebalan yang tidak sama, bahkan berlubang.
Ukuran pori pada Gambar 7 berkisar 0.1– 0.2 µm. Menurut Mulder (1996) (Tabel 3) berdasarkan kisaran ukuran porinya membran ini tergolongkan membran mikrofiltrasi.
Gambar 7 SEM permukaan atas membran selulosa asetat dengan penambahan PEG.
Membran mikrofiltrasi digunakan pada proses penjernihan sari buah, pemisahan bakteri, dan juga mempunyai permeabilitas yang lebih tinggi terhadap air (Anonim tt).
Membran selulosa asetat dengan penambahan PEG diperkirakan menghasilkan membran simetrik. Tampaknya penambahan PEG memperbaiki ciri-ciri membran, yaitu
% Transmitan
Bilangan gelombang
% Transmitan
15
membentuk pori dengan ukuran yang lebih seragam dibandingkan dengan tanpa penambahan PEG. Hal ini dikarenakan PEG yang berada pada matriks polimer akan larut dalam pelarut nonpolar yaitu diklorometana, dan pada saat pencelupan dalam air PEG tersebut larut dengan meninggalkan rongga pada membran yang disebut pori.
Foto SEM membran selulosa asetat tanpa penambahan PEG diberikan pada Gambar 8. Struktur pori pada permukaannya tidak begitu jelas karena ketebalan yang tidak merata pada setiap sisinya. Perbedaan ketebalan ini dikarenakan membran masih dibuat secara manual menggunakan batang pengaduk pada lempeng kaca untuk meratakan permukaan membran. Gaya tekan yang berbeda-beda antara batang pengaduk dan lempeng kaca akan menghasilkan permukaan yang tidak merata pada setiap sisi membran. Penetapan kisaran ukuran pori pada membran selulosa asetat tanpa penambahan PEG (Gambar 8) dilakukan dengan mengukur dari pori yang kecil sampai yang besar, karena beragamnya ukuran pori yang diperoleh. Ukuran pori yang diperoleh pada Gambar 8, berkisar 0.7 –6.0 µm.
Gambar 8 SEM permukaan atas membran selulosa asetat tanpa penambahan PEG.
Membran selulosa asetat tanpa penambahan PEG (Gambar 8) menghasilkan struktur pori yang asimetrik berdasarkan pembuatannya secara pembalikan fase. Membran asimetrik ini memiliki dua lapisan, yaitu lapisan bawah yang kaya pelarut dan lapisan atas yang kaya polimer. Lapisan atas memiliki ukuran pori yang lebih kecil daripada lapisan bawah karena pada saat penguapan pelarut, pengendapan akan terjadi lebih dahulu pada bagian atas. Saat
pengendapan akan terjadi difusi pelarut ke dalam air, meninggalkan rongga pada membran yang disebut pori. Karena volume pelarut pada lapisan atas lebih sedikit daripada lapisan bawah, pori-pori pada lapisan atas lebih kecil dibandingkan dengan yang di bawah.
SIMPULAN DAN SARAN
Simpulan
Hasil FTIR menunjukkan bahwa penambahan PEG memperlihatkan adanya interaksi kimiawi dengan membran selulosa asetat.
Membran selulosa asetat yang diperoleh memiliki kisaran ukuran pori 0.1–0.2 µm dan digolongkan sebagai membran mikrofiltrasi.
Saran
Foto SEM permukaan bawah, atas dan analisis TEM bagian dalam dari membran perlu dilakukan untuk membuktikan kesimetrisan membran yang dihasilkan dari metode pembalikan fase.
DAFTAR PUSTAKA
Andriansyah M. 2006. Sifat-sifat membran yang terbuat dari sari kulit buah nanas [Skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
[Anonim]. 2005. Processing routes to acetic anhydride. http://www.chemsystems.com/
newsletters/perp/Jun04_N03S1.cfm [9
Desember 2005].
Arifin B. 2004. Optimasi kondisi asetilasi selulosa bakteri dari nata de coco [Skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
16
Collins JL. 1968. Pineapple Botany, Cultivation and Utilization. London: Leonard Hill.
Darwati, Natanael CL, Rahayu I. 2002. Pembuatan dan karakterisasi membran ultrafiltrasi dan bahan selulosa asetat dengan variasi konsentrasi aditif (formamida) dan aplikasinya untuk penanganan limbah tapioka [Laporan Penelitian]. Bandung: Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Padjadjaran.
Darwo AA. 2003. Proyek Pengkajian dan Penelitian Ilmu Pengetahuan Terapan Direktorat Jenderal Departemen Pendidikan Nasional. Produksi membran filtrasi dari selulosa mikrobial dan penerapannya dalam industri hasil pertanian [laporan penelitian]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Fadillah F. 2003. Pengaruh penambahan PEG terhadap karakterisasi membran selulosa asetat [Skripsi]. Bogor: Fakultas Teknologi Industri Pertanian, Institut Pertanian Bogor.
Fengel D dan G. Wegener. 1989. Wood Chemistry, Ultrastructure, and Reactions. Berlin: Walter de Gruyter.
Kirk RE, Othmer DF. 1993. Encyclopedia of Polymer Science and Technology. New York: Interscience.
Mulder M. 1996. Basic Principles of Membrane Technology. Netherland: Kluwer Academic.
Osada Y, Nakagawa T. 1992. Membrane Science and Technology. New York: Marcel Dekker.
Pasla FR. 2006. Pencirian membran selulosa asetat berbahan dasar selulosa bakteri dari limbah nanas [Skripsi]. Bogor : Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Pavia, Lampman, Kriz. 2000. Introduction to Spectroscopy. New York: John Wiley and Sons.
Safriani. 2000. Produksi biopolimer selulosa asetat dari nata de soya [Tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
SNI. 1991. SNI 06-2115-1991: Selulosa Asetat. Jakarta: Dewan Standardisasi Nasional.
Susanto T, R Adhitia, dan Yunianta. 2000. Pembuatan nata de pina dari kulit nanas: kajian dari sumber karbon dan pengenceran medium fermentasi. Jurnal Teknologi Pertanian. 1:58–66.
Tresnawati A. 2006. K ajian spektroskopi inframerah transformasi Fourrier dan mikroskop susuran elektron membran selulosa asetat dari limbah nanas [Skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Tya P. 2006. Ciri membran selulosa berpori dari sari kulit nanas. [Skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Wenten. 1996. Teknologi Industrial Membran. Teknik Kimia, Institut Teknologi Bandung.
Yang L, Hsiao WW, Chen P. 2001. Chitosan cellulose composite membrane for affinity purifications of biopolymers and immunoadsorption. J. Membr Sci. 5084: 1–13.