Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN DARI EKSTRAK ETANOL BUAH TERONG BELANDA (Solanum betaceum
Cav.)
SKRIPSI
OLEH:
IRMA L. H. SINAGA 040804062
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN DARI EKSTRAK ETANOL BUAH TERONG BELANDA (Solanum betaceum
Cav.)
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
IRMA L. H. SINAGA
NIM 040804062
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
KATA PENGANTAR
Segala puji, hormat serta syukur penulis persembahkan kepada Allah yang hidup di dalam nama Yesus Kristus, Tuhan dan Juru Selamat Yang Mulia atas segala kemurahan-Nya penulis dapat menyelesaikan penelitian dan penulisan skripsi ini yang dibuat untuk memenuhi salah satu syarat mencapai gelar Sarjana Farmasi di Fakultas Farmasi USU Medan.
Ucapan terima kasih tak terhingga buat seorang wanita yang luar biasa tangguh yang terus berjuang memberi yang terbaik kepada penulis, my lovely mom Jenny Dermi Gultom. Pernyataan maaf penuh penyesalan juga penulis sampaikan untuk ayahanda tercinta Alm. Kaman Sinaga, karena tak mampu penuhi segala mimpi dan harapan yang telah dipercayakan kepada penulis. Juga ucapan terima kasih buat abang Renhard ( my king dragon), adik Ani (my sweet honey), adik Beatrich (my sweet princess) dan adik Fransiskus (my youngest dragon) atas segala doa, dukungan dan kasih sayang kepada penulis sehingga penulis tetap semangat dan termotivasi dalam menyelesaikan penelitian hingga penyelesaian skripsi ini.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada: 1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt. sebagai Dekan Fakultas
Farmasi, Ibu Dra. Siti Aman, M.Si., Apt. sebagai Dosen Wali beserta seluruh staf pengajar Fakultas Farmasi USU Medan yang telah mendidik penulis.
2. Bapak dan Ibu Dosen Penguji atas kritik dan saran kepada penulis.
3. Teman-teman Farmasi 2004 khususnya anak-anak ”CaBe LoTiSS”, kalian adalah hadiah terindah dari Tuhan bagiku selama di Farmasi yang terus mendukung aku di dalam tangis dan juga tawaku, Jose & Dika, Eka Yana dan seluruh anak-anak KMKS serta semua pihak yang selalu setia memberikan dukungan kepada penulis.
Akhir kata penulis memohon maaf atas segala keterbatasan dan kekurangan penulis dalam penulisan skripsi ini. Semoga skripsi ini dapat menjadi sumbangan yang berarti bagi ilmu pengetahuan.
Medan, Maret 2009 Penulis,
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
ABSTRAK
Dalam rangka meningkatkan pemanfaatan antioksidan alami dari makanan, telah dilakukan penelitian uji aktivitas antioksidan dari ekstrak etanol buah segar terong belanda (Solanum betaceum Cav.) yang diekstraksi secara maserasi. Selanjutnya ekstrak dipekatkan dengan alat rotary evaporator dan dikeringkan dengan freeze dryer.
Ekstrak diuji terhadap DPPH (2,2-Diphenyl-1-picrilhydrazil) sebagai radikal bebas dengan mengukur absorbansi DPPH pada panjang gelombang 494 nm, 514 nm dan 534 nm pada menit ke-18 dan menit ke-36 sesuai hasil pengukuran operating time, menggunakan spektrofotometer uv-visibel. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
ABSTRACT
In order to increase the usage of natural antioxidant from food, it had been tested the antioxidant activity from ethanol extracts of the fresh fruit of tree tomato (Solanum betaceum Cav.) which extracted by maceration. The extract was concentrated using rotary evaporator and then dried by freeze dryer.
Extracs were tested by DPPH (2,2-Diphenyl-1-picrilhydrazil) as free radical where the. absorbance of DPPH was measured at 494 nm, 514 nm and 534 nm in 18th and 36th minutes by used uv-visible spectrophotometer. Antioxidant ability was measured as the decrease in absorbance of DPPH solutions after the additions of the extract.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
DAFTAR ISI
Halaman
JUDUL ... ...i
LEMBAR PENGESAHAN ...ii
KATA PENGANTAR ...iii
ABSTRAK . ...v
ABSTRACT ...vi
DAFTAR ISI ...vii
DAFTAR TABEL ... ...xi
DAFTAR GAMBAR ...xii
DAFTAR LAMPIRAN ...xiii
BAB I. PENDAHULUAN ...1
1.1 Latar Belakang ...1
1.2 Perumusan Masalah ...3
1.3 Hipotesis ...4
1.4 Tujuan ...4
1.5 Manfaat ...4
BAB II. TINJAUAN PUSTAKA ...5
2.1 Uraian Tumbuhan ...5
2.1.1 Daerah Tumbuh . ...5
2.1.2 Nama Daerah ...6
2.1.3 Nama Asing ...6
2.1.4 Sistematika Tumbuhan. ...6
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
2.1.6 Morfologi Tumbuhan ...7
2.1.7 Kandungan Kimia ... ...8
2.1.8 Kegunaan ... ...9
2.2 Ekstraksi ... ...10
2.3 Radikal Bebas ... ...12
2.4 Antioksidan ... ...13
2.4.1 Antioksidan Alami ... ...14
2.4.2 Vitamin C ... ...14
2.5 Penentuan Aktivitas Antioksidan ... ...15
2.6 Spektrofotometri UV-Visibel ... ...17
BAB III. METODOLOGI PENELITIAN ... ...18
3.1 Alat-Alat ... ...18
3.2 Bahan-Bahan ... ...18
3.3 Pembuatan Larutan Pereaksi ... ...19
3.3.1 Larutan Pereaksi Bouchardat ... ...19
3.3.2 Larutan Pereaksi Mayer ... ...19
3.3.3 Larutan Pereaksi Dragendorff ... ...19
3.3.4 Larutan Pereaksi Molish ... ...19
3.3.5 Larutan Pereaksi Asam Klorida 2 N ...20
3.3.6 Larutan Pereaksi Asam Sulfat 2 N ...20
3.3.7 Larutan Pereaksi Asam Nitrat 0,5 N ... ...20
3.3.8 Larutan Pereaksi Timbal(II) Asetat 0,4 M ...20
3.3.9 Larutan Pereaksi Besi (III) Klorida 1 % ...20
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
3.4 Pengambilan dan Pengolahan Sampel ...20
3.4.1 Pengambilan Sampel. ...20
3.4.2 Identifikasi Tumbuhan . ...21
3.4.3 Pengolahan Sampel . ...21
3.5 Skrining Fitokimia ...21
3.5.1 Pemeriksaan Alkaloida ...22
3.5.2 Pemeriksaan Glikosida . ...22
3.5.3 Pemeriksaan Steroida/Triterpenoida ...23
3.5.4 Pemeriksaan Flavonoida ...23
3.5.5 Pemeriksaan Tanin ...23
3.5.6 Pemeriksaan Saponin ...24
3.5.7 Pemeriksaan Antrakinon ...24
3.6 Pembuatan Ekstrak Etanol Buah Terong Belanda ...24
3.7 Pengujian Kemampuan Antioksidan Sampel Uji Dengan Spektrofotometrei Visibe ... ...25
3.7.1 Prinsip Metode DPPH ... ...25
3.7.2 Pembuatan Larutan Blanko ... ...25
3.7.3 Penentuan Panjang Gelombang Serapan Maksimum dan Operating time Larutan DPPH dalam Metanol ... ...25
3.7.4 Pembuatan Larutan Induk ... ...26
3.7.5 Pembuatan Larutan Uji ... ...26
3.7.6 Penentuan Persen Peredaman ... ...26
3.7.7 Penentuan Nilai IC50 ... ...27
BAB IV. HASIL DAN PEMBAHASAN ...28
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
4.2 Hasil Skrining Fitokimia ...28
4.3 Hasil Penentuan Serapan Maksimum ...29
4.4 Hasil Penentuan Operating Time Larutan DPPH Dalam Metanol ...30
4.5 Hasil Analisis Aktivitas Antioksidan Sampel Uji ...30
4.6 Hasil Analisis Peredaman Radikal Bebas DPPH Oleh Sampel Uji ....33
4.7 Analisis Nilai IC50 (Inhibitory Concentration) Sampel Uji ...36
BAB V. KESIMPULAN DAN SARAN ...38
5.1 Kesimpulan ...38
5.2 Saran ...38
DAFTAR PUSTAKA ...39
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
DAFTAR TABEL
Halaman Tabel 1. Kandungan Nutrisi Dalam 100 g Terong Belanda ... 9 Tabel 2. Hasil Skrining Fitokimia Buah Terong Belanda
(Solanum betaceumCav.) ... 28 Tabel 3. Hasil Analisis Peredaman Radikal Bebas Oleh Ekstrak Etanol
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
DAFTAR GAMBAR
Halaman
Gambar 1. Kurva Serapan Maksimum Larutan DPPH 40 ppm Dalam
Metanol Secara Spektrofotometri Visibel ...29
Gambar 2. Kurva Absorbansi Operating Time Larutan DPPH Dalam Metanol ... ...30
Gambar 3. Hasil Analisis Aktivitas Antioksidan Sampel Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.) Pada Menit ke-18 ...31
Gambar 4. Hasil Analisis Aktivitas Antioksidan Sampel Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.) pada menit ke-36 . ...31
Gambar 5. Hasil Analisis Aktivitas Antioksidan Vitamin C Pada Menit ke-18 ...32
Gambar 6. Hasil Analisis Aktivitas Antioksidan Vitamin C Pada Menit ke-36 ...32
Gambar 7. Hubungan Konsentrasi Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.) dengan persen peredaman pada menit ke-18 dan menit ke-36 ...35
Gambar 8. Hubungan konsentrasi vitamin C (ppm) dengan persen Peredaman Pada Menit ke-18 dan menit ke-36 . ...35
Gambar 9. Tumbuhan Terong Belanda (Solanum betaceum Cav.) ...42
Gambar 10. Bunga Terong Belanda (Betacei flos.) ...42
Gambar 11. Buah Terong Belanda (Betacei fructus) ...43
Gambar 12. Buah Terong Belanda yang dibelah dua ...43
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Surat Hasil Identifikasi Tumbuhan ... 41
Lampiran 2. Tumbuhan Terong Belanda (Solanum betaceum Cav.) ... 42
Lampiran 3. Gambar Alat... 44
Lampiran 4. Bagan Ekstraksi Bahan Segar Secara Maserasi ... 45
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
BAB I
PENDAHULUAN
1.1Latar Belakang
Kondisi lingkungan yang semakin memburuk dan berlubangnya lapisan ozon menyebabkan makin mudahnya terbentuk zat-zat radikal baik dalam bentuk logam dan nonlogam, yang mau tidak mau akan mencemari pangan yang kita konsumsi (Kumalaningsih, 2001).
Radikal bebas adalah molekul yang kehilangan elektron, sehingga molekul tersebut menjadi tidak stabil dan selalu berusaha mengambil elektron dari molekul atau sel lain. Radikal bebas diproduksi secara alami oleh tubuh dalam jumlah kecil, tetapi akan timbul masalah bila diproduksi terlalu banyak (Kramer P., 2004).
Buah-buahan memegang peranan penting dalam menunjang kesehatan dan kebugaran tubuh. Sebab dalam buah-buahan terkandung berbagai macam vitamin, mineral, serat pangan dan komponen antioksidan (Anonim, 2008).
Antioksidan adalah zat yang dapat menetralisir radikal bebas sehingga atom dengan elektron yang tidak berpasangan mendapat pasangan elektron sehingga tidak liar lagi (Kosasih, 2004).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Banyak sekali ragam antioksidan alami, tetapi jarang yang memiliki komponen kimia yang lengkap. Terong belanda termasuk keluarga Solanaceae yang berasal dari Peru dan masuk ke Indonesia dikembangkan antara lain di Bali, Jawa Barat dan Tanah Karo Sumatera Utara. Terong belanda mempunyai macam-macam antioksidan yang lengkap baik dalam bentuk vitamin dan yang bukan, seperti vitamin A, vitamin C, vitamin B6, senyawa karotenoid, anthosianin dan serat. Lengkapnya antioksidan alami dalam buah terong belanda memungkinkan pemanfaatannya sebagai bahan baku pembuatan antioksidan (Kumalaningsih, 2001).
Terong belanda selain kaya akan air juga mengandung provitamin A yang bagus untuk kesehatan mata dan vitamin C untuk mengobati sariawan dan meningkatkan daya tahan tubuh. Serat yang tinggi di dalam terong belanda bermanfaat untuk mencegah kanker dan sembelit/konstipasi. Mineral penting seperti potasium, fosfor dan magnesium mampu menjaga dan memelihara kesehatan tubuh (Anonim, 2008).
Vitamin C (L-Asam askorbat) merupakan suatu antioksidan penting yang larut dalam air. Vitamin C menangkap secara efektif radikal-radikal O2-, OH-, peroksil dan oksigen singlet (Duthie dan Brown, 1994).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Vitamin C termasuk golongan antioksidan karena sangat mudah teroksidasi oleh panas, cahaya dan logam. Oleh karena itu penggunaan vitamin C sebagai antioksidan semakin sering dijumpai (Anonim, 2008).
Menurut Santosa et al. (1998) dan Okawa et al. (2001), metode aktivitas antiradikal bebas DPPH (1,1-diphenyl-2-picrylhydrazyl) merupakan metode terpilih untuk menapis aktivitas antioksidan bahan alam (Amrun dan Ummayah, 2007).
Metode analisa ini telah digunakan luas untuk menguji kemampuan dari suatu senyawa atau komponen untuk bereaksi sebagai penangkap radikal bebas atau donor hidrogen. Metode ini mengukur aktivitas dari antioksidan dalam melawan radikal bebas 1,1-diphenyl-2-picrylhydrazyl (DPPH) dan untuk mengevaluasi aktivitas antioksidan dari makanan (Anonim, 2001).
Pengungkapan potensi terong belanda (Solanum betaceum Cav.) sebagai sumber antioksidan berkaitan dengan senyawa kimia yang terdapat di dalamnya. Oleh sebab itu dalam penelitian ini dilakukan skrining fitokimia terlebih dahulu, dan uji aktivitas antioksidannya menggunakan metode DPPH dengan vitamin C sebagai kontrol positif.
1.2 Perumusan Masalah
a. Senyawa kimia golongan apa saja yang terkandung dalam buah terong belanda (Solanum betaceum Cav.)
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
c. Berapakah kekuatan antioksidan dari ekstrak etanol buah segar terong belanda (Solanum betaceum Cav.) dibandingkan dengan vitamin C sebagai kontrol positif.
1.3 Hipotesis
a. Buah terong belanda (Solanum betaceum Cav.) mengandung golongan senyawa kimia flavonoid yang memiliki aktivitas sebagai antioksidan. b. Ekstrak etanol buah segar terong belanda (Solanum betaceum Cav.)
mempunyai aktivitas antioksidan.
c. Ekstrak etanol buah segar terong belanda (Solanum betaceum Cav.) memiliki aktivitas antioksidan yang kuat.
1.4 Tujuan
a. Untuk mengetahui golongan senyawa kimia yang terdapat dalam buah terong belanda (Solanum betaceum Cav.).
b. Untuk mengetahui aktivitas antioksidan dari ekstrak etanol buah segar terong belanda (Solanum betaceum Cav.).
c. Untuk mengetahui besar kekuatan antioksidan ekstrak etanol buah segar terong belanda (Solanum betaceum Cav.) dibandingkan dengan vitamin C sebagai kontrol positif.
1.5 Manfaat
a. Sebagai informasi golongan senyawa-senyawa kimia yang terkandung dalam buah terong belanda (Solanum betaceum Cav.).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh (habitat), nama daerah, nama asing, morfologi tumbuhan, sistematika tumbuhan, kandungan kimia dan kegunaan dari tumbuhan.
2.1.1 Daerah Tumbuh
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
2.1.2 Nama Daerah
Batak : tiung (Toba), trung jepan (Karo) Jawa Tengah : terong mandras
Melayu : terong belanda Sunda : terong menen
(Departemen Kesehatan dan Kesehatan Sosial, 2001). 2.1.3 Nama Asing
Inggris : tree tomato Brazil : tomate de arvore Ekuador : tomate dulce
Guatemala : tomate, tomate extranjero, tomate de arbol, tomate granadilla, granadilla, pix, caxlan pix
Kolombia : pepino de arbol Kostarika : tomate cimarron New Zealand : tamarillo
Venezuella : tomate frances (Anonim, 2005). 2.1.4 Sistematika Tumbuhan
Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Klass : Dicotyledoneae
Ordo : Solanales
Famili : Solanaceae
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Spesies : Solanum betaceum Cav. (Departemen Kesehatan dan Kesehatan Sosial, 2001). 2.1.5 Sinonim Tunbuhan
Sinonim : Cyphomandra botacea Sendt.
Cyphomandra crassicaulis – (Ortega.)Kuntze Cyphomandra hartwegi Sendt. (Anonim, 2001). 2.1.6 Morfologi Tumbuhan
Tanaman ini memiliki daun yang berbulu berbentuk hati besar dan berwarna hijau. Daun yang hijau ini akan mudah sekali dirusak oleh terpaan angin yang kencang (Kumalaningsih, 2006).
Bunga tamarillo akan muncul pada akhir musim gugur sampai pada awal musim semi. Warnanya pink dan terletak pada ujung cabang batang serta biasanya berkelompok. Tanaman ini memiliki benang sari dan putik serta kelopak bunga yang berwarna ungu hijau. Tanaman ini melakukan penyerbukan sendiri tetapi terkadang juga dibantu lebah dan angin meskipun sangat kecil kemungkinannya (Kumalaningsih, 2006).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
dikelupas. Rasa buah ini seperti tomat dan teksturnya seperti buah plum dengan kandungan gizi yang relatif tinggi karena banyak mengandung vitamin A, C dan serat. Lapisan luar dari daging buah banyak mengandung air, sedikit kasar dan sedikit mengandung rasa manis (Kumalaningsih, 2006).
Biji buah ini keras, berwarna coklat muda sampai hitam. Bentuk biji agak tumpul, bulat dan kecil, tetapi lebih besar daripada biji tomat yang sebenarnya (Kumalaningsih, 2006).
2.1.7 Kandungan Kimia
Terong belanda adalah buah yang mempunyai kandungan nutrisi yang sangat baik, berisi beberapa kandungan vitamin yang sangat penting serta kaya akan besi dan potasium, kandungan sodium yang rendah dan berisi kurang dari 40 kalori (kurang lebih 160 kJ). Oleh karena kelengkapan dari kandungan gizi pada tamarillo, maka di Amerika Serikat buah terong belanda terkenal sebagai buah yang mengandung rendah kalori, sumber serat, bebas lemak (jenis reds) atau rendah lemak (jenis golden), bebas kolesterol dan sodium dan sumber vitamin C dan E yang sempurna (Kumalaningsih, 2006).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Menurut Kumalaningsih (2006), hasil analisis lengkap kandungan gizi buah terong belanda dapat dilihat pada tabel 1 berikut ini:
Tabel 1. Kandungan Nutrisi Dalam 100 g Terong Belanda Kandungan
Nutrisi
Terong Belanda (tiap 100g)
Vitamin A 540-5600 µg
Vitamin B1 0.03-0.14 mg
Vitamin B2 0.01-0.05 mg
Vitamin B6 0.01-0.05 mg
Vitamin C 15-42 mg
Vitamin E 2 mg
Niasin 0.3-1.4 mg
Potasium
(Kalium)
0.28-0.38 g
Kalsium 6-18 mg
Fosfor 22-65 mg
Magnesium 16-25 mg
Besi 0.3-0.9 mg
Seng 0.1-0.2 mg
Protein 1.4-2 g
Lemak 0.1-0.6 g
Serat 1.4-4.7 g
Kadar air 80-90 g
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Buah terong belanda berkhasiat sebagai obat tekanan darah tinggi dan penyegar badan. Untuk obat tekanan darah tinggi dipakai ± 3 buah terong belanda yang sudah masak, dikupas untuk sekali makan (Departemen Kesehatan dan Kesehatan Sosial, 2001).
Kandungan antosianin, vitamin-vitamin serta zat-zat gizi lainnya di dalam buah terong belanda bekerja sinergis untuk:
1. Mencegah kerusakan sel-sel jaringan tubuh penyebab berbagai penyakit (kanker, tumor dan lain-lain).
2. Melancarkan penyumbatan pembuluh darah (arterisklorosis) sehingga mencegah penyakit jantung & stroke serta menormalkan tekanan darah.. 3. Menurunkan kadar kolesterol dan mengikat zat-zat racun dalam tubuh. 4. Meningkatkan stamina, daya tahan tubuh dan vitalitas.
5. Membantu mempercepat proses penyembuhan (Anonim, 2009). 2.2 Ekstraksi
Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari jaringan tumbuhan maupun hewan. Sebelum ekstraksi dilakukan biasanya bahan – bahan dikeringkan terlebih dahulu kemudian dihaluskan pada derajat kehalusan tertentu (Harborne, 1987).
Menurut Departemen Kesehatan RI (2000), beberapa metode ekstraksi dengan menggunakan pelarut yaitu:
A.Cara dingin 1. Maserasi
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Maserasi yang dilakukan pengadukan secara terus menerus disebut maserasi kinetik sedangkan yang dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
2. Perkolasi
Perkolasi adalah proses penyarian simpilisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pelembaban bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan.
B. Cara panas 1. Refluks
Refluks adalah proses penyarian simpilisia dengan menggunakan alat pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperatur lebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40 – 500 C.
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan menggunakan alat soklet sehingga terjadi ekstraksi kontinu dengan pelarut relatife konstan dengan adanya pendingin balik.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada temperature 900 C selama 15 menit.
5. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperature 900 C selama 30 menit.
2.3 Radikal Bebas
Radikal bebas adalah molekul yang kehilangan elektron, sehingga molekul tersebut menjadi tidak stabil dan selalu berusaha mengambil elektron dari molekul atau sel lain. Zat ini dapat dihasilkan dari hasil metabolisme tubuh dan faktor eksternal seperti asap rokok, hasil penyinaran ultra violet, zat kimiawi dalam makanan dan polutan lain (Anomin, 2007).
Radikal bebas sangat reaktif dan dengan mudah menjurus ke reaksi yang tidak terkontrol, menghasilkan ikatan silang (cross-link) pada DNA, protein, lipida, atau kerusakan oksidatif pada gugus fungsional yang penting pada biomolekul ini. Perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga terlibat dan berperan dalam patologi dari berbagai penyakit degeneratif, yakni kanker, aterosklerosis, rematik, jantung koroner, katarak (Silalahi, 2006).
Radikal bebas yang sangat berbahaya dalam makhluk hidup antara lain adalah golongan hidroksil (OH-), seperoksida (O-2), nitrogen monooksida (NO), dan peroksidal (RO-2), peroksinitrit (ONOO-), asam hipoklorit (HOCL), hydrogen peroksida (H2O2) (Silalahi, 2006).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Namun bila dihasilkan melebihi batas kemampuan proteksi antioksidan selular, maka dia akan menyerang sel itu sendiri. Struktur sel yang berubah turut merubah fungsinya, yang akan mengarah pada proses munculnya penyakit (Suariasari, 2006).
2.4 Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektron dengan cuma – cuma kepada molekul radikal bebas tanpa terganggu sama sekali dan dapat memutuskan reaksi berantai dari radikal bebas (Kumalaningsih, 2006).
Antioksidan yang ada di alam ini dibagi atas tiga macam yaitu : (1) Antioksidan yang dibuat oleh tubuh kita sendiri yang berupa enzim antara lain superoksidadismutase, glutathinoneperoxidase, peroxidase dan katalase (2) Antioksidan alami yang dapat diperoleh dari tanaman atau hewan, yaitu tokoferol, vitamin C, betakaroten, flavonoid dan senyawa fenolik (3) Antioksidan sintetik dibuat dari bahan-bahan kimia yaitu Butylated hidroxy-anisole (BHA), Butylated Hydroxy-toluene (BHT), Propylgallate (PG), yang ditambah dalam makanan untuk mencegah kerusakan lemak (Kumalaningsih, 2006).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
yang bermanfaat untuk memperbaiki kerusakan biomolekular yang disebabkan oleh radikal bebas, misalnya DNA repair enzyme ( Silalahi, 2006).
2.4.1 Antioksidan Alami
Hasil penelitian menunjukkan bahwa buah-buahan, sayuran dan biji-bijian adalah sumber antioksidan yang baik dan bisa meredam reaksi berantai radikal bebas dalam tubuh, yang pada akhirnya dapat menekan proses penuaan dini (Kosasih, 2004).
Khasiat antioksidan untuk mencegah berbagai penyakit dan akan lebih efektif jika kita mengkonsumsi sayur-sayuran dan buah-buahan yang kaya akan antioksidan dari berbagai jenis daripada menggunakan antioksidan tunggal. Efek antioksidan dari sayur-sayuran dan buah-buahan lebih efektif daripada suplemen antioksidan yang diisolasi (Silalahi, 2006).
2.4.2 Vitamin C
Vitamin adalah senyawa organik kompleks yang essensial untuk pertumbuhan dan fungsi biologis yang lain bagi mahluk hidup. Berhubung vitamin tidak disintesa dalam tubuh kecuali vitamin K, maka vitamin harus ada dalam makanan yang dikonsumsi. Vitamin tidak dapat disimpan dalam tubuh, oleh karenanya harus selalu ada dalam bahan makanan yang dikonsumsi. Bahan makanan yang kaya akan vitamin adalah sayur-sayuran dan buah-buahan (Sudarmadji, 1989).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
besar hewan yang dapat mensintesis vitamin C. Di alam vitamin C terdapat dalam dua bentuk, yaitu L- asam askorbat ( bentuk tereduksi) dan L- dehidroasam askorbat ( bentuk teroksidasi).
2.5 Penentuan Aktivitas Antioksidan
Bermacam-macam metode pengukuran aktivitas antioksidan telah digunakan untuk memantau dan membandingkan aktivitas antioksidan pada makanan memberikan hasil yang beragam tergantung pada spesifitas dari radikal bebas yang digunakan sebagai reaktan (Anonim, 2001).
Sebuah metode yang cepat, sederhana dan murah untuk mengukur aktivitas antioksidan dari makanan yaitu dengan melibatkan penggunaan radikal bebas 1,1-diphenyl-2-picrylhydrazyl (DPPH). DPPH digunakan luas untuk menguji kemampuan dari suatu senyawa atau komponen untuk bereaksi sebagai penangkap radikal bebas atau donor hidrogen dan untuk mengevaluasi aktivitas antioksidan dari makanan. DPPH juga digunakan untuk menentukan antioksidan dalam kompleks biologi dalam beberapa tahun terakhir. Metode DPPH dapat digunakan untuk sampel padat ataupun cair dan telah digunakan untuk mengukur kadar antioksidan pada sampel (Anonim, 2001).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
N N N N N o o -o o -o o -N N N N N o o -o o -o o -N N N N N o o -o o -o o -N NH N N N o o -o o -o o
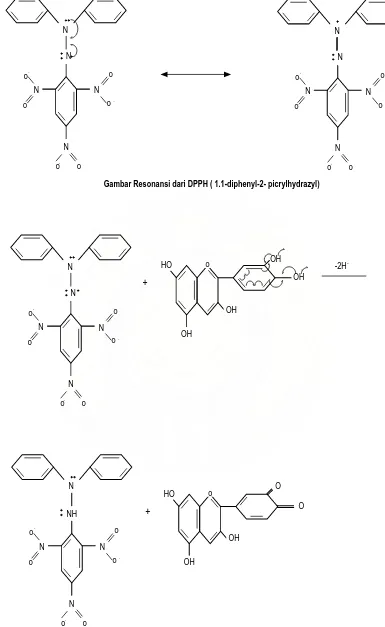
-Gambar Resonansi dari DPPH ( 1.1-diphenyl-2- picrylhydrazyl)
Gambar reaksi antara DPPH dengan atom H netral yang berasal dari antioksidan o HO OH OH OH OH
-2H .
[image:30.595.109.494.89.716.2]Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
2.6 Spektrofotometri UV-Visibel
Ahli kimia telah lama menggunakan warna sebagai bantuan dalam mengenali zat-zat kimia. Spektrofotometri dapat dianggap sebagai perluasan suatu pemeriksaan visual, yaitu dengan menggunakan alat untuk mengukur absorpsi energi radiasi macam-macam zat kimia dan memungkinkan dilakukannya pengukuran kualitatif dan kuantitatif dari suatu zat dengan ketelitian yang lebih besar (Day, 1994).
Spektrofotometri serapan adalah pengukuran serapan radiasi elektromagnit panjang gelombang tertentu yang sempit, mendekati monokromatik, yang diserap zat. Pengukuran serapan dapat dilakukan pada daerah ultraviolet (panjang gelombang 190–380 nm) atau pada daerah cahaya tampak (panjang gelombang 380–780 nm) (Depkes, 1979).
Spektrofotometer pada dasarnya terdiri atas sumber sinar monokromotor, tempat sel untuk zat yang diperiksa, detektor, penguat arus dan alat ukur atau pencatat (Departemen Kesehatan RI, 1979).
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
BAB III
METODOLOGI PENELITIAN
Penelitian ini dilakukan di Laboratorium Farmakognosi dan Laboratorium Kimia Farmasi Kwantitatif, Fakulatas Farmasi, Universitas Sumatera Utara. Metodologi penelitian meliputi pengumpulan dan pengolahan sampel, skrining fitokimia, pembuatan ekstrak dan pengujian kemampuan antioksidan secara spektrofotometri visibel.
3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah uv mini 1240-spektrofotometer uv-visibel (Shimadzu), penguap vakum putar (Heidolph VV 2000), frezee dryer (Modulyo/Edwards), neraca kasar (Ohaus), neraca analitik (Vibra), pisau dan sendok stainless steel, water bath, eksikator, krus porselin dan alat-alat gelas laboratorium.
3.2 Bahan-bahan
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
toluena, kloralhidrat, iodium, raksa (II) klorida, timbal (II) asetat, kalium iodida, bismut (III) nitrat, besi (III) klorida dan amil alkohol.
3.3 Pembuatan Larutan Pereaksi
Pembuatan larutan pereaksi dilakukan menurut Departemen Kesehatan RI tahun 1978 dan tahun 1979.
3.3.1 Larutan Pereaksi Bouchardat
Sebanyak 4 g kalium iodida ditimbang, kemudian dilarutkan dalam air suling, ditambahkan iodium sebanyak 2 g dan dicukupkan dengan air suling hingga 100 ml (Departemen Kesehatan RI, 1978).
3.3.2 Larutan Pereaksi Mayer
Sebanyak 1,4 g raksa (II) klorida, kemudian dilarutkan dalam air suling hingga 60 ml. Pada wadah lain ditimbang sebanyak 5 g kalium iodida lalu dilarutkan dalam 10 ml air suling. Kedua larutan dicampurkan dan ditambahkan air suling hingga diperoleh larutan 100 ml (Departemen Kesehatan RI, 1978). 3.3.3 Larutan Pereaksi Dragendorff
Sebanyak 8 g bismut (III) nitrat ditimbang, kemudian dilarutkan dalam 20 ml asam nitrat pekat. Pada wadah lain ditimbang sebanyak 27,2 g kalium iodida lalu dilarutkan dalam 50 ml air suling. Kemudian kedua larutan dicampurkan dan didiamkan sampai memisah sempurna. Larutan yang jernih diambil dan diencerkan dengan air suling hingga 100 ml (Departemen Kesehatan RI, 1978). 3.3.4 Larutan Pereaksi Molish
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
3.3.5 Larutan Pereaksi Asam Klorida 2 N
Sebanyak 17 ml asam klorida pekat dilarutkan dalam air suling hingga volume 100 ml (Departemen Kesehatan RI, 1979).
3.3.6 Larutan Pereaksi Asam Sulfat 2 N
Sebanyak 5,5 ml asam sulfat pekat diencerkan dengan air suling hingga volume 100 ml (Departemen Kesehatan RI, 1979).
3.3.7 Larutan Pereaksi Asam Nitrat 0,5 N
Sebanyak 3,4 ml asam nitrat pekat diencerkan dengan air suling hingga volume 100 ml (Departemen Kesehatan RI, 1979).
3.3.8 Larutan Pereaksi Timbal (II) Asetat 0,4 M
Sebanyak 15,17 g timbal asetat ditimbang, kemudian dilarutkan dalam air suling bebas karbondioksida hingga volume 100 ml (Departemen Kesehatan RI, 1979).
3.3.9 Larutan Pereaksi Besi (III) Klorida 1% b/v
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air suling hingga volume 100 ml (Departemen Kesehatan RI, 1979).
3.3.10 Larutan Pereaksi DPPH 0,5 mM
Sebanyak 19,7 mg DPPH ditimbang, kemudian dilarutkan dalam metanol hingga volume 100 ml (Departemen Kesehatan RI, 1979).
3.4 Pengambilan Dan Pengolahan Sampel 3.4.1 Pengambilan Sampel
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
pengambilan sampel dilakukan dengan memberi kesempatan yang sama pada setiap anggota populasi untuk menjadi anggota sampel (Anonim, 2003).
3.4.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Laboratorium Taksonomi Tumbuhan, Departemen Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara.
3.4.3 Pengolahan Sampel
Pengolahan buah terong belanda (Solanum betaceum Cav.) dilakukan terhadap sampel segar, berwarna merah tua sampai merah keunguan sebanyak 500 g. Proses pencucian dilakukan untuk menghilangkan kotoran yang menempel pada saat pemanenan atau pada saat penyimpanan. Pada tahap ini dilakukan juga pemisahan tangkai buah dari buahnya.
Buah yang sudah dicuci bersih kemudian dilap menggunakan tisu bersih, lalu dilakukan pembelahan secara melintang menggunakan pisau stainless steel, dengan tujuan agar memudahkan dalam proses pemisahan antara kulit buah dengan bagian dalam buah (daging dan biji). Proses selanjutnya adalah pemisahan daging buah serta bijinya dengan kulit buahnya menggunakan bantuan sendok. Kemudian daging buah dan biji dihaluskan dengan cara menekan (kneading), diperoleh bubur buah sebanyak 350 g, dimasukkan ke dalam wadah lalu ditutup. 3.5 Skrining Fitokimia
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
kimia golongan alkaloida, glikosida, steroida/triterpenoida, flavonoida, saponin, tanin dan antrakinon.
3.5.1 Pemeriksaan Alkaloida
Sebanyak 0,5 g buah segar yang telah dihaluskan, ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan dan disaring. Filtrat dipakai untuk uji alkaloida sebagai berikut :
a. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Mayer, akan terbentuk endapan menggumpal berwarna putih atau kuning
b. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Bouchardat, akan terbentuk endapan berwarna coklat sampai kehitaman c. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi
Dragendorff, akan terbentuk endapan merah atau jingga
Alkaloida positif jika terjadi endapan atau kekeruhan paling sedikit dua dari tiga percobaan diatas (Departemen Kesehatan RI, 1978).
3.5.2 Pemeriksaan Glikosida
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
dan 5 tetes larutan pereaksi Molish. Tambahkan hati-hati 2 ml asam sulfat pekat melalui dinding tabung, terbentuknya cincin ungu pada batas kedua cairan menunjukkan adanya glikosida (Departemen Kesehatan RI, 1978).
3.5.3 Pemeriksaan Steroida/Triterpenoida
Sebanyak 1 g buah segar yang telah dihaluskan, dimaserasi dengan 20 ml eter selama 2 jam, disaring, filtrat diuapkan dalam cawan penguap dan pada sisanya ditambahkan 20 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat (pereaksi Liebermann-Burchard). Apabila terbentuk warna ungu atau merah yang berubah menjadi biru hijau menunjukkan adanya steroida/triterpenoida (Harborne, 1987).
3.5.4 Pemeriksaan Flavonoida
Sebanyak 10 g buah segar yang telah dihaluskan, ditambahkan 10 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah atau kuning atau jingga pada lapisan amil alkohol (Fransworth, 1996).
3.5.5 Pemeriksaan Tanin
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
3.5.6 Pemeriksaan Saponin
Sebanyak 0,5 g buah segar yang telah dihaluskan, dimasukkan dalam tabung reaksi, ditambahkan 10 ml air panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik, jika terbentuk buih yang mantap setinggi 1 sampai 10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Departemen Kesehatan RI, 1978).
3.5.7 Pemeriksaan Antrakinon
Sebanyak 0,2 g buah segar yang telah dihaluskan, ditambah 5 ml asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzena, dikocok dan didiamkan. Lapisan benzena dipisahkan dan disaring. Lapisan benzena dikocok dengan 2 ml natrium hidroksida 2 N, didiamkan. Lapisan air berwarna merah dan lapisan benzena tidak berwarna menunjukkan adanya antrakinon (Departemen Kesehatan RI, 1978).
3.6 Pembuatan Ekstrak Etanol Buah Terong Belanda
Pembuatan ekstrak dilakukan secara maserasi menggunakan pelarut etanol (Departemen Kesehatan RI, 1979).
Caranya :
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
atau disaring. Filtrat yang diperoleh digabung dengan filtrat yang telah diperoleh sebelumnya. Pemekatan ekstrak dilakukan dengan alat rotary evaporator kemudian ekstrak dikeringkan dengan teknik freeze dryer.
3.7 Pengujian Kemampuan Antioksidan Sampel Uji Dengan Spektrofotometri Visibel
3.7.1 Prinsip Metode DPPH
DPPH (1,1-diphenyl-2-picryl-hydrazyl) sebagai radikal bebas dalam larutan etanol/metanol digunakan untuk menentukan aktivitas antioksidan sampel uji, yaitu kemampuan sampel uji dalam meredam proses oksidasi DPPH (peredaman warna ungu DPPH) dengan IC50 (konsentrasi sampel uji yang mampu meredam radikal bebas sebesar 50%) sebagai parameternya.
3.7.2 Pembuatan Larutan Blanko
Larutan DPPH 0,5 mM dipipet sebanyak 5 ml, kemudian dimasukkan ke dalam labu tentukur 25 ml, dicukupkan volumenya dengan metanol sampai garis tanda (konsentrasi 40 ppm).
3.7.3 Penentuan Panjang Gelombang Serapan Maksimum dan Operating
Time Larutan DPPH dalam Metanol
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
3.7.4 Pembuatan Larutan Induk
Sebanyak 25 mg sampel uji ditimbang kemudian dilarutkan dalam labu tentukur 25 ml dengan metanol lalu volumenya dicukupkan dengan metanol sampai garis tanda (konsentrasi 1000 ppm).
3.7.5 Pembuatan Larutan Uji
Larutan induk dipipet sebanyak 1 ml; 2 ml; 3 ml dan 4 ml kemudian dimasukkan ke dalam labu tentukur 25 ml (untuk mendapatkan konsentrasi 40 ppm, 80 ppm, 120 ppm dan 160 ppm), kemudian ke dalam masing-masing labu tentukur ditambahkan 5 ml larutan DPPH 0,5 mM (C = 40 ppm) lalu volume dicukupkan dengan metanol sampai garis tanda.
3.7.6 Penentuan Persen Peredaman
Menurut Santosa et al (1998) dalam Amrun dan Umayah (2007), absorbansi DPPH diukur pada panjang gelombang 494 nm, 514 nm dan 534 nm pada menit ke-18 dan sekali lagi pada menit ke-36. Kemampuan antioksidan diukur sebagai penurunan serapan larutan DPPH (peredaman warna ungu DPPH) akibat adanya penambahan sampel uji. Nilai serapan larutan DPPH sebelum dan sesudah penambahan sampel uji tersebut dihitung sebagai persen peredaman.
Perhitungan kapasitas antiradikal bebas DPPH sebagai persen peredaman absorban pada puncak 514 nm menggunakan perhitungan sebagai berikut:
(
)
100 %1
% x
A A peredaman
DPPH Hitung
uji bahan Hitung
− =
Dimana, absorban hitung 514 nm:
(
)
100%2 534 494
514 x
A A A
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
3.7.7 Penentuan Nilai IC50
Nilai IC50 merupakan bilangan yang menunjukkan konsentrasi sampel uji (µg/ml) yang memberikan peredaman DPPH sebesar 50% (mampu menghambat/meredam proses oksidasi sebesar 50 %). Nilai 0% berarti tidak mempunyai aktivitas antiradikal bebas atau antioksidan, sedangkan nilai 100% berarti peredaman total dan pengujian perlu dilanjutkan dengan pengenceran larutan uji untuk melihat batas konsentrasi aktivitasnya. Selanjutnya dibuat kurva linear antara konsentrasi larutan uji dengan % peredaman dan ditentukan harga IC50 , yaitu dengan memasukkan nilai dari konsentrasi larutan uji (µg/ml) sebagai absis (sumbu X) dan nilai persen peredaman (%) sebagai ordinat (sumbu Y) ke dalam persamaan garis linier.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Laboratorium Taksonomi Tumbuhan, Departemen Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara menunjukkan bahwa sampel termasuk suku Solanaceae, jenis Solanum betaceum Cav.
4.2 Hasil Skrining Fitokimia
Dari 200 g sampel segar buah terong belanda (Solanum betaceum Cav.) yang diekstraksi secara maserasi menggunakan pelarut etanol diperoleh ekstrak kental sebanyak 19,047 g (9,52 % b/b) yang berwarna ungu tua.
Hasil skrining fitokimia yang dilakukan selama 2 hari terhadap buah segar terong belanda (Solanum betaceum Cav.) mengandung senyawa-senyawa kimia seperti yang terlihat pada tabel 1 berikut ini:
Tabel 2. Hasil Skrining Fitokimia Buah Terong Belanda (Solanum betaceum Cav.)
No. PEMERIKSAAN Hasil
1 Alkaloida +
2 Flavonoida +
3 Tanin +
4 Saponin +
5 Glikosida +
6 Antrakuinon __
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Hasil di atas menunjukkan bahwa buah terong belanda (Solanum betaceum Cav.) memiliki aktivitas sebagai antioksidan, yaitu dengan adanya senyawa kimia golongan flavonoida. Senyawa flavonoida secara umum bertindak sebagai antioksidan yaitu sebagai penangkap radikal bebas karena mengandung gugus hidroksil. Flavonoida bersifat sebagai reduktor sehingga dapat bertindak sebagai donor hidrogen terhadap radikal bebas (Silalahi, J. 2006).
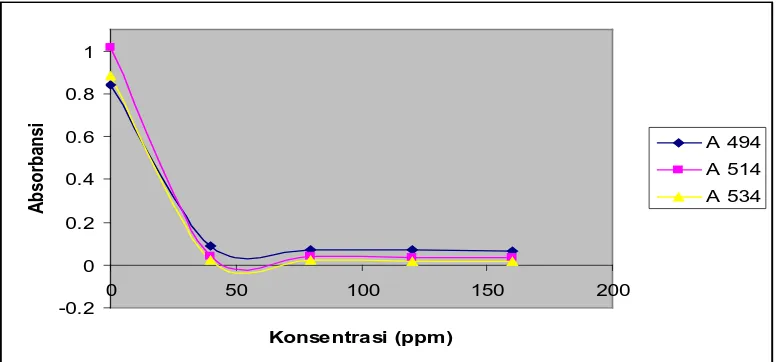
4.3 Hasil Penentuan Serapan Maksimum
Dari hasil pengukuran serapan maksimum larutan DPPH 40 ppm dalam metanol dengan menggunakan spektrofotometer UV-Vis diperoleh serapan maksimum pada panjang gelombang 514 nm. Hasil pengukuran serapan maksimum ini tidak jauh berbeda dari hasil pengukuran yang diperoleh oleh peneliti-peneliti sebelumnya. Data hasil pengukuran dapat dilihat pada gambar 1
berikut ini:
[image:43.595.114.506.406.652.2]
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
4.4 Hasil Penentuan Operating Time Larutan DPPH dalam Metanol
Penentuan operating time larutan DPPH 40 ppm dalam metanol dilakukan dengan waktu preparasi selama 6 menit dan dari hasil pengukuran diperoleh waktu kerja yang terbaik (stabil) selama 18 menit yaitu pada menit ke-18 sampai menit ke-36 setelah penambahan pelarut metanol. Kurva serapan untuk operating time larutan DPPH dalam metanol dapat dilihat pada gambar 2 berikut ini (data terlampir):
0.315 0.32 0.325 0.33 0.335 0.34 0.345 0.35 0.355
0 10 20 30 40 50 60 70
t (menit)
A
b
s
o
rb
a
n
s
[image:44.595.118.505.282.533.2]i
Gambar 2. Kurva Absorbansi Operating Time Larutan DPPH dalam Metanol
4.5 Hasil Analisis Aktivitas Antioksidan Sampel Uji
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
konsentrasi sampel uji dalam menganalisis aktivitas antioksidannya dapat dilihat dari kurva pada gambar 3 dan 4 untuk ekstrak etanol buah terong belanda (Solanum betaceum Cav.) dan gambar 5 dan 6 untuk vitamin C berikut ini:
0.8
0.9
1
1.1
1.2
1.3
0
50
100
150
200
Konsentrasi (ppm )
A b s o rb a n s i
A 514
A 534
A 494
Gambar 3. Hasil analisis aktivitas antioksidan sampel ekstrak etanol buah terong belanda (Solanum betaceum Cav.) pada menit ke-18
0.8 0.9 1 1.1 1.2 1.3
0 50 100 150 200
Konsentrasi (ppm )
A b s o rb a n s i A 514 A 534 A 494
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
-0.2 0 0.2 0.4 0.6 0.8 1
0 50 100 150 200
Konsentrasi (ppm) A b so rb an si A 494 A 514 A 534 Gambar 5. Hasil analisis aktivitas antioksidan vitamin C pada menit ke-18
-0.2 0 0.2 0.4 0.6 0.8 1 1.2
0 50 100 150 200
Konsentrasi (ppm) A b so rb an si A 494 A 514 A 534
Gambar 6. Hasil analisis aktivitas antioksidan vitamin C pada menit ke-36
[image:46.595.117.507.87.268.2]Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
4.6 Hasil Analisis Peredaman Radikal Bebas DPPH Oleh Sampel Uji
Analisis peredaman radikal bebas DPPH oleh sampel uji dapat diperoleh dengan terlebih dahulu menghitung nilai AHitung (absorbansi hitung) dari data hasil pengukuran absorbansi pada panjang gelombang 494 nm, 514 nm dan 534 nm pada menit ke-18 dan menit ke-36. Dari analisis yang telah dilakukan, diperoleh nilai persen peredaman pada setiap kenaikan konsentrasi sampel uji seperti yang terlihat pada tabel berikut ini (perhitungan terlampir):
Tabel 3. Hasil Analisis Peredaman Radikal Bebas Oleh Ekstrak Etanol Terong Belanda (Solanum betaceum Cav.)
Menit ke- Sampel A494 A514 A534 AHitung %peredaman
18
DPPH 1.0644 1.2604 1.1223 0.1671 __ 40 0.9859 1.1769 1.0394 0.1643 1.68 80 0.9636 1.1464 1.0153 0.1570 6.04 120 0.9066 1.0785 0.9498 0.1503 10.05 160 0.8693 1.0365 0.9113 0.1462 12.51
36
DPPH 1.0668 1.2601 1.1212 0.1661 __ 40 0.9734 1.1572 1.0236 0.1587 4.45 80 0.9509 1.1306 0.9988 0.1558 6.26 120 0.8986 1.0728 0.9473 0.1499 9.75 160 0.8536 1.0122 0.8920 0.1394 16.07
[image:47.595.113.513.343.645.2]Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
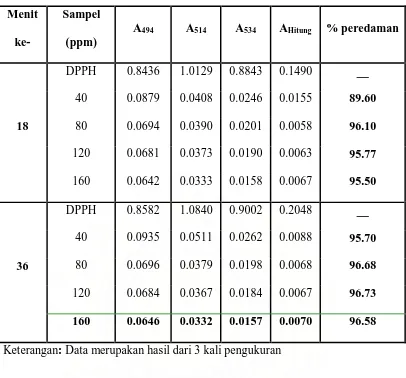
Tabel 4. Hasil Analisis Peredaman Radikal Bebas Oleh Vitamin C
Menit ke-
Sampel (ppm)
A494 A514 A534 AHitung % peredaman
18
DPPH 0.8436 1.0129 0.8843 0.1490 __ 40 0.0879 0.0408 0.0246 0.0155 89.60 80 0.0694 0.0390 0.0201 0.0058 96.10 120 0.0681 0.0373 0.0190 0.0063 95.77 160 0.0642 0.0333 0.0158 0.0067 95.50
36
DPPH 0.8582 1.0840 0.9002 0.2048 __ 40 0.0935 0.0511 0.0262 0.0088 95.70 80 0.0696 0.0379 0.0198 0.0068 96.68 120 0.0684 0.0367 0.0184 0.0067 96.73 160 0.0646 0.0332 0.0157 0.0070 96.58
Keterangan: Data merupakan hasil dari 3 kali pengukuran
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
0 2 4 6 8 10 12 14 16 18
0 20 40 60 80 100 120 140 160 180
konsentrasi (ppm)
%
p
er
ed
am
an
t = 36' t = 18'
Gambar 7. Hubungan konsentrasi ekstrak etanol buah terong belanda (Solanum betaceum Cav.) dengan persen peredaman pada menit ke-18 dan menit ke-36
0 20 40 60 80 100 120
0 20 40 60 80 100 120 140 160 180
konsentrasi (ppm)
%
p
er
ed
am
an
t = 36' t = 18'
[image:49.595.114.510.84.700.2]Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
4.7 Analisis Nilai IC50 (inhibitory concentration) Sampel uji
Analisis nilai IC50 dihitung berdasarkan persamaan regresi linier yang didapatkan dengan cara memplot konsentrasi larutan uji dan persen peredaman DPPH sebagai parameter aktivitas antioksidan, dimana konsentrasi larutan uji (ppm) sebagai absis dan nilai persen peredaman sebagai ordinat. Hasil persamaan regresi linier yang diperoleh untuk ekstrak etanol terong belanda (Solanum betaceum Cav.) adalah y = 0,0835X – 0,62 pada menit ke-18 dan y = 0,0936X – 0,182 pada menit ke-36 dan untuk vitamin C adalah y = 0,4929X + 35,958 pada menit ke-18 dan y = 0,4855X + 38,298 pada menit ke-36. Hasil analisis nilai IC50 yang diperoleh berdasarkan perhitungan persamaan regresi yang telah dilakukan dapat dilihat pada tabel berikut ini:
Tabel 5. Nilai IC50 ekstrak etanol terong belanda dan vitamin C Menit
ke-
SAMPEL
IC 50
(ppm)
18
Ekstrak etanol terong belanda Vitamin C
606.228 28.489
36
Ekstrak etanol terong belanda Vitamin C
536.132 24.103
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
BAB V
KESIMPULAN DAN SARAN 5.1 KESIMPULAN
• Buah terong belanda (Solanum betaceum Cav.) mengandung senyawa kimia golongan alkaloida, tanin, saponin, glikosida, steroida/triterpenoida dan flavonoida yang memiliki aktivitas sebagai antioksidan.
• Hasil pemeriksaan aktivitas antioksidan yang dilakukan terhadap ekstrak etanol buah segar terong belanda (Solanum betaceum Cav.) menggunakan spektrofotometer UV-visibel pada panjang gelombang 494 nm, 514 nm dan 534 nm pada menit ke-18 dan menit ke-36 menunjukkan adanya aktivitas antioksidan dengan nilai IC 50 sebesar 609,073 ppm pada menit ke-18 dan 534,989 ppm pada menit ke-36. Perlakuan yang sama juga dilakukan terhadap vitamin C sebagai kontrol positif dan diperoleh nilai IC50 sebesar 28,991 ppm pada menit 18 dan 24,077 ppm pada menit ke-36. Dengan demikian hal ini menunjukkan bahwa ekstrak etanol dari buah segar terong belanda (Solanum betaceum Cav.) memiliki aktivitas antioksidan yang sangat lemah dibandingkan dengan vitamin C sebagai kontrol positif.
5.2 SARAN
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
DAFTAR PUSTAKA
Amrun dan Umiyah. (2007). Uji Aktivitas Ekstrak Air dan Ekstrak Metanol Beberapa Varian Buah Kenitu (Chrysphyllum cainito L.) Dari Daerah Jember. Bagian Biologi Farmasi, Program Studi Farmasi Universitas Jember. Hal. 45-50
Anonim. Online 2001. Uji Aktivitas Antioksidan.
/
Anonim. Online 2003.Metode Sampling.USU digital Library.
Anonim. Online 2004. Antioksidan, Resep Sehat dan Umur Panjang http://www.Gizi.Net/pengumuman/index,shtml/
Anonim. Online 2005,Tanaman Obat Indonesia. http://www.iptek.go.id
Anonim.Online 2008.Panjang Umur dengan Antioksidan.
http://www . hersmagz.com/hers_magazine/view_catagory. Anonim. Online 2008.Rujak Makanan Masa Depan.
http://www.keluarga sehat.com Anonim. Online 2009. Sari Buah Tamarillo.
http://www.kotadaengnet.infokotamakassar_herbalif_saribuahtamarillo .com
Cahyana, A.H. dan Taufik, M. (2005). Isolasi Senyawa Antioksidan Kulit Batang Kayu Manis (Cinnamomum burmanii Nees ex Blume). Prosiding Simposium Nasional Kimia Bahan Alam XV. Departemen Kimia FMIPA. IPB. Bogor. Hal. 95-100
Coronel.R.E. and Verheij.E.W.M. (1992). Prosea Foundation Plant Resources of South-East Asia no 12.Vegetable.Bogor-Indonesia. Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi.
Padang: Andalas University Press. Hal. 1-7.
Day, R.A. dan Underwood, A.L. (1986). Analisis Kimia Kuatitatif. Edisi Ke-6. Terjemahan Iis Sopyan. Jakarta: Erlangga. Hal. 382.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Departemen Kesehatan RI. (1979). Farmakope Indonesia. Edisi III. Jakarta: Depkes RI. Hal. 29-31 33, 649, 748.
Departemen Kesehatan dan Kesehatan Sosial RI. (2001). Inventaris Tanaman Obat Indonesia. Cetakan pertama. Jilid kedua, Jakarta: Badan Penelitian dan Pengembangan Kesehatan. Hal. 17-18
Fransworth, N.R. (1996). Biological And Phytochemical Screening of Plants. Journal of Pharmaceutical Science. Volume 55 No. 3. Chicago: Reheis Chemical Company. Pages: 257-259, 263.
Harborne, J.B. (1987). Metode Fitokimia, Penuntun Cara Modern Menganalisa Tumbuhan. terjemahan K. Padmawinata. Edisi II. Bandung: ITB Press. Hal. 6, 71, 76, 84-85, 94-97.
Kosasih, dkk. (2004). Peranan Antioksidan Pada Lanjut Usia. Jakarta: Pusat Kajian Nasional Masalah Lanjut Usia. Hal. 48-49, 56-69.
Kumalaningsih. (2006). Antioksidan Alami. Surabaya: Trubus Agrisarana. Hal.16.
Kumalaningsih. (2006). Antioksidan Alami Terong Belanda (Tamarillo). Surabaya: Trubus Agrisarana. Hal.16.
Molyneux, P. (2004). The Use Of The Stable Free Radical diphenylpicrylhydrazyl (DPPH) For Estimating Antioxidant Activity. Songklanakarin J. Sci. Technol. 26(2): 211-9.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
[image:56.595.114.509.138.473.2]Lampiran 2. Tumbuhan Terong Belanda (Solanum betaceum Cav.)
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Gambar 10. Bunga Terong Belanda (Betacei flos)
Lampiran 2 (Lanjutan)
Gambar 11. Buah Terong Belanda (Betacei fructus)
[image:57.595.159.441.137.624.2]Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
[image:58.595.126.498.138.429.2]Lampiran 3. Gambar Alat Spektrofotometer
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Lampiran 4. Bagan Ekstraksi Bahan Segar Secara Maserasi
dimasukkan ke dalam sebuah bejana dituangi dengan 1500 ml etanol ditutup
dibiarkan selama 5 hari terlindung dari
cahaya sambil sesekali diaduk diserkai, diperas
dicuci dengan etanol 96%
secukupnya hingga diperoleh 2000 ml dipindahkan ke dalam bejana tertutup dibiarkan di tempat sejuk, terlindung
dari cahaya, selama 2 hari dienap-tuangkan dan disaring
digabung
dipekatkan dengan alat rotary evaporator
dikeringkan dengan alat Freeze dryer
200 g bahan segar yang telah
dihaluskan
Maserat Ampas
Ekstrak cair
Ampas Maserat
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Tabel 3. Analisis Peredaman Radikal Bebas Oleh Ekstrak Etanol Terong Belanda (Solanum betaceum Cav.)
Menit ke- Sampel A494 A514 A534 AHitung %peredaman
18
DPPH 1.0644 1.2604 1.1223 0.1671 __ 40 0.9859 1.1769 1.0394 0.1643 1.68 80 0.9636 1.1464 1.0153 0.1570 6.04 120 0.9066 1.0785 0.9498 0.1503 10.05 160 0.8693 1.0365 0.9113 0.1462 12.51
36
DPPH 1.0668 1.2601 1.1212 0.1661 __ 40 0.9734 1.1572 1.0236 0.1587 4.45 80 0.9509 1.1306 0.9988 0.1558 6.26 120 0.8986 1.0728 0.9473 0.1499 9.75 160 0.8536 1.0122 0.8920 0.1394 16.07
Keterangan: Data merupakan hasil dari 3 kali pengukuran AHitung : Absorbansi hitung (nm)
A494 : Absorbansi pada panjang gelombang 494 nm A514 : Absorbansi pada panjang gelombang 514 nm A534 : Absorbansi pada panjang gelombang 534 nm
(
)
100%2 534 494
514 x
A A A
AHitung = − +
(
)
100%1
% x
A A peredaman
DPPH Hitung
uji bahan Hitung
− =
Perhitungan AHitung ekstrak etanol terong belanda (Solanum betaceum
[image:62.595.111.514.118.581.2]Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
(
)
100%2 534 494 514 x A A A
AHitung = − +
Pada menit ke-18 :
(
)
100%2 1223 . 1 0644 . 1 2604 . 1 x A DPPH Hitung + − =
= 0.1671
- Pada menit ke-18 konsentrasi 40 ppm :
(
)
100%2 0394 . 1 9859 . 0 1769 . 1 x AHitung + − =
= 0.1643
- Pada menit ke-18 konsentrasi 80 ppm :
(
)
100%2 0153 . 1 9636 . 0 1464 . 1 x
AHitung = − +
= 0.1570
- Pada menit ke-18 konsentrasi 120 ppm :
(
)
100%2 9498 . 0 9066 . 0 0785 . 1 x
AHitung = − +
= 0.1503
- Pada menit ke-18 konsentrasi 160 ppm :
(
)
100%2 9113 . 0 8693 . 0 0365 . 1 x
AHitung = − +
= 0.1462
Pada menit ke-36 :
(
)
100%Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
= 0.1661
- Pada menit ke-36 konsentrasi 40 ppm :
(
)
100%2 0236 . 1 9734 . 0 1572 . 1 x
AHitung = − +
= 0.1587
- Pada menit ke-36 konsentrasi 80 ppm :
(
)
100%2 9988 . 0 9509 . 0 1306 . 1 x
AHitung = − +
= 0.1558
- Pada menit ke-36 konsentrasi 120 ppm :
(
)
100%2 9473 . 0 8986 . 0 0728 . 1 x
AHitung = − +
= 0.1499
- Pada menit ke-36 konsentrasi 160 ppm :
(
)
100%2 8920 . 0 8536 . 0 0122 . 1 x
AHitung = − +
= 0.1394
Perhitungan persen peredaman ekstrak etanol terong belanda
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
(
)
100%1 % x A A peredaman DPPH Hitung uji bahan Hitung − =
Pada menit ke-18 :
- Persen peredaman pada menit ke-18 konsentrasi 40 ppm:
(
)
100%1671 . 0 1643 . 0 1
% peredaman = − x
= 1.68 %
- Persen peredaman pada menit ke-18 konsentrasi 80 ppm:
(
)
100%1671 . 0 1570 . 0 1
% peredaman = − x
= 6.04 %
- Persen peredaman pada menit ke-18 konsentrasi 120 ppm:
(
)
100%1671 . 0 1503 . 0 1
% peredaman = − x
= 10.05 %
- Persen peredaman pada menit ke-18 konsentrasi 160 ppm:
(
)
100%1671 . 0 1462 . 0 1
% peredaman = − x
= 12.51 %
Pada menit ke-36 :
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
(
)
100%1661 . 0 1587 . 0 1
% peredaman = − x
= 4.45 %
- Persen peredaman pada menit ke-36 konsentrasi 80 ppm:
(
)
100%1661 . 0 1558 . 0 1
% peredaman = − x
= 6.26 %
- Persen peredaman pada menit ke-36 konsentrasi 120 ppm:
(
)
100%1661 . 0 1499 . 0 1
% peredaman = − x
= 9.75 %
- Persen peredaman pada menit ke-36 konsentrasi 160 ppm:
(
)
100%1661 . 0 1394 . 0 1
% peredaman = − x
= 16.07 %
[image:66.595.112.442.305.565.2]
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
Menit
ke-
Sampel
(ppm)
A494 A514 A534 AHitung % peredaman
18
DPPH 0.8436 1.0129 0.8843 0.1490 __ 40 0.0879 0.0408 0.0246 0.0155 89.60 80 0.0694 0.0390 0.0201 0.0058 96.10 120 0.0681 0.0373 0.0190 0.0063 95.77 160 0.0642 0.0333 0.0158 0.0067 95.50
36
DPPH 0.8582 1.0840 0.9002 0.2048 __ 40 0.0935 0.0511 0.0262 0.0088 95.70 80 0.0696 0.0379 0.0198 0.0068 96.68 120 0.0684 0.0367 0.0184 0.0067 96.73 160 0.0646 0.0332 0.0157 0.0070 96.58
Keterangan: Data merupakan hasil dari 3 kali pengukuran AHitung : Absorbansi hitung (nm)
A494 : Absorbansi pada panjang gelombang 494 nm A514 : Absorbansi pada panjang gelombang 514 nm A534 : Absorbansi pada panjang gelombang 534 nm
(
)
100%2 534 494 514 x A A A
AHitung = − +
(
)
100%1 % x A A peredaman DPPH Hitung uji bahan Hitung − =
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
(
)
100%2 534 494 514 x A A A
AHitung = − +
Pada menit ke-18 :
(
)
100%2 8843 . 0 8436 . 0 0129 . 1 x A DPPH Hitung + − =
= 0.1490
- Pada menit ke-18 konsentrasi 40 ppm :
(
)
100%2 0246 . 0 0879 . 0 0408 . 0 x AHitung + − =
= 0.0155
- Pada menit ke-18 konsentrasi 80 ppm :
(
)
100%2 0201 . 0 0694 . 0 0390 . 0 x
AHitung = − +
= 0.0058
- Pada menit ke-18 konsentrasi 120 ppm :
(
)
100%2 9498 . 0 9066 . 0 0785 . 1 x
AHitung = − +
= 0.1503
- Pada menit ke-18 konsentrasi 160 ppm :
(
)
100%2 0190 . 0 0681 . 0 0373 . 0 x
AHitung = − +
= 0.0063
Irma l. H. Sinaga : Skrining Fitokimia Dan Uji Aktivitas Antioksidan Dari Ekstrak Etanol Buah Terong Belanda (Solanum betaceum Cav.), 2009.
(
)
100%2 9002 . 0 8582 . 0 0840 . 1 x A DPPH Hitung + − =
= 0.2048
- Pada menit ke-36 konsentrasi 40 ppm :
(
)
100%2 0262 . 0 0935 . 0 0511 . 0 x AHitung + − =
= 0.0088
- Pada menit ke-36 konsentrasi 80 ppm :
(
)
100%2 0198 . 0 0696 . 0 0379 . 0 x
AHitung = − +
= 0.0068
- Pada menit ke-36 konsentrasi 120 ppm :
(
)<