PENGARUH KONSENTRASI H2SO4 DAN BERAT DARI
BENTONIT ALAM TERAKTIVASI DAN KOMERSIL
TERHADAP ADSORPSI LOGAM KADMIUM (Cd)
DAN TEMBAGA (Cu) DALAM LARUTAN
STANDAR DENGAN METODE
SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
EKO RAMADANI
070802017
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGARUH KONSENTRASI H2SO4 DAN BERAT DARI
BENTONIT ALAM TERAKTIVASI DAN KOMERSIL
TERHADAP ADSORPSI LOGAM KADMIUM (Cd)
DAN TEMBAGA (Cu) DALAM LARUTAN
STANDAR DENGAN METODE
SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
EKO RAMADANI
070802017
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH KONSENTRASI H2SO4 DAN BERAT
DARI BENTONIT ALAM TERAKTIVASI DAN KOMERSIL TERHADAP ADSORPSI LOGAM KADMIUM (Cd) DAN TEMBAGA (Cu) DALAM LARUTAN STANDAR DALAM METODE SPEKTROFOTOMETRI SERAPAN ATOM
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA)UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Agustus 2011
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Prof.Dr.Harry Agusnar.M.Sc.,M.Phill Prof.Dr.Zul Alfian.M.Sc NIP. 195308171983031002 NIP.195504051983031002
Diketahui/Disetujui oleh :
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENGARUH KONSENTRASI H2SO4 DAN BERAT DARI BENTONIT ALAM
TERAKTIVASI DAN KOMERSIL TERHADAP ADSORPSI LOGAM KADMIUM (Cd) DAN TEMBAGA (Cu) DALAM LARUTAN
STANDAR DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Agustus 2011
PENGHARGAAN
Bissmillahirrahmanirrahim,
Alhamdulillah, segala puji bagi Allah SWT semesta alam yang dengan curahan
cinta-Nya saya dapat menyelesaikan skripsi ini sebagai salah satu persyaratan untuk meraih
gelar Sarjana Kimia pada Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara. Serta shalawat dan salam saya sampaikan pada
Rasulullah, Muhammad SAW, sosok yang sangat saya idolakan semoga kelak
mendapat syafaat Beliau. Amin.
Selanjutnya saya menyampaikan penghargaan dan cinta kasih tulus kepada
Ayahanda tersayang Rasidin, yang dengan doa dan tetes peluhnya, mengorbankan
banyak hal untuk membesarkan dan mendidik saya dengan penuh cinta, Engkau selalu
dihati Ayah, juga kepada Ibunda tersayang Surip, yang dengan doa tiada henti dan
cintanya telah mengajarkan banyak hal untuk kehidupan saya sampai detik ini, serta
tak lupa saudara-saudara tercinta Jaya setiawan, Riki Wijaya, dan widia Puspita sari.
Semoga cinta itu selalu mengikat kita. Amin. Serta seluruh keluarga yang telah
memberikan banyak dukungannya.
Dengan segala kerendahan hati, saya mengucapkan terima kasih yang
sebesar-besarnya kepada:
1. Prof. Dr. Zul Alfian, M.Sc selaku pembimbing 1 dan Prof. Dr. Harry Agusnar,
M.Sc, M.Phill selaku dosen pembimbing 2 yang telah banyak memberikan
pengarahan dan bimbingan hingga terselesaikannya skripsi ini.
2. DR. Rumondang Bulan Nst. Ms dan Drs. Albert Pasaribu, M.Sc selaku Ketua
dan Sekretaris Departemen Kimia FMIPA USU.
3. Drs. Ahmad Darwin Bangun, M.Sc, selaku dosen wali saya yang telah banyak
memberi masukan selama saya mencari ilmu di FMIPA USU.
4. Prof. Dr. Harlem Marpaung selaku dosen penguji dalam yang telah banyak
memberikan saran dan masukan hingga terselesaikannya skripsi ini.
5. Dr. Darwin Yunus Nasution, MS selaku kepala laboratorium kimia dasar
6. Bapak dan Ibu Dosen yang telah memberikan ilmunya selama masa studi saya
di FMIPA USU.
7. Staf dan seluruh teman-teman asisten Laboratorium Kimia Dasar LIDA USU
Medan, abangda Rivan dan Hendi, Yuki, Deasy, Ani, Andreas, Arifin, Novi,
Nurul, Desi, Salmi, Ilman, Irwanto, Ayu, Dwi, Indah, Rina dan kak Ayu selaku
Analis Laboratorium yang telah memberikan segala fasilitas terbaik selama
saya melakukan penelitian, terutama untuk Bang Boby, terima kasih atas
masukan dan kerjasamanya.
8. Teman-teman seperjuangan saya: Yuki, Deasy, Ani, Fakhreni, Ulan, Kiki,
Husni, Tisna, Lifa dan seluruh personil Kimia stambuk 2007 yang tidaklah
dapat saya sebutkan satu per satu namanya, namun sungguh sangat berkesan di
hati saya. Terima kasih karena kalian telah menambah warna dalam hidup
saya. Persahabatan itu sungguh indah dan tak tergantikan.
9. Abangda Beni Hudaya dan Sony yang telah membantu dalam secara materi
dan moril, serta memberikan masukan kepadda saya. Terima kasih karena
telah membantu saya hingga terselesaikannya skripsi ini.
10.Teristimewa, Adinda Raissa Adelia Harahap yang dengan sabarnya
memberikan dorongan kepada saya. Terima kasih atas inspirasi, motivasi dan
kerjasamanya selama ini.
11.Serta segala pihak yang telah membantu saya menyelesaikan skripsi ini. Untuk
itu semua, semoga Allah membalasnya dengan segala yang terbaik. Amin.
Saya menyadari bahwa skripsi ini masih banyak kekurangan, karena keterbatasan
saya baik dalam literatur maupun pengetahuan. Oleh karena itu, saya
mengharapkan saran dan masukan yang membangun demi kesempurnaan skripsi
ini, dan semoga skripsi ini bermanfaat bagi kita semua.
Medan, Agustus 2011
ABSTRAK
Telah dilakukan penelitian tentang pengaruh variasi konsentrasi H2SO4 dan berat dari
bentonit alam teraktivasi dan komersil terhadap adsorpsi logam kadmium (Cd) dan tembaga (Cu) dalam larutan standar menggunakan metode Spektrofotometri Serapan Atom. Pada proses aktivasi bentonit dikaji variasi konsentrasi H2SO4 yaitu 0,4; 0,8;
1,2; 1,6; dan 2,0 M. Ke dalam larutan standar kadmium (Cd) dan tembaga (Cu) ditambahkan 1, 2, 3, 4, dan 5 g bentonit alam yang telah diaktivasi dengan H2SO4 1,2
M dan bentonit komersil, diaduk selama 6 jam, disaring dan diukur konsentrasi logam kadmium (Cd) dan tembaga (Cu) dengan Spektrofotometer Serapan Atom melalui kurva kalibrasi. Hasil penelitian menunjukkan bahwa bentonit H2SO4 1,2 M yang
THE CONCENTRATION EFFECT’S OF H2SO4 AND WEIGHT OF ACTIVATED BLEACHING EARTH AND COMMERCIAL TO
ADSORPTION CADMIUM METAL (Cd) AND COPPER (Cu) IN STANDARDSOLUTION USING ATOMIC
ABSORPTION SPECTROPHOTOMETRIC METHOD
ABSTRACT
The various concentration effect’s of H2SO4 and weight of activated bleaching earth
and commercial to adsoption of cadmium metal (Cd) and copper (Cu) in standard solution using Atomic Absorption Spectrophotometric method has been studied. Bleaching earth activation process assessed various concentration of H2SO4 which is
0,4; 0,8; 1,2; 1,6; and 2,0 M. 1, 2, 3, 4, and 5 g activated bleaching earth and commercial added into cadmium standard solution (Cd) and copper (Cu) , stirred up to 6 hours, filtered and measured by cadmium metal concentration (Cd) and copper (Cu) using Atomic Absorption Spectrophotometer instrument with calibration curve. The result of research show that H2SO4 1,2 M the best can adsorp cadmium metal (Cd) is
DAFTAR ISI
1.2Permasalahan 2
1.3Pembatasan Masalah 2
1.4Tujuan Penelitian 3
1.5Manfaat Penelitian 3
1.6Lokasi Penelitian 3
1.7Metodologi Penelitian 3
Bab 2 Tinjauan Pustaka 5
2.1 Bentonit 5
2.1.1 Proses Terjadinya di Alam 6
2.1.2 Struktur Bentonit 8
2.1.3 Sifat Fisik dan Kimia Bentonit 9
2.1.4 Komposisi Bentonit 9
2.1.5 Aktivasi Bentonit 10
2.1.5 Aplikasi Bentonit 10
2.2 Adsorpsi 12
2.6 Toksisitas Logam Berat 16
2.7 Spektrofotometri Serapan Atom 16 2.7.1 Prinsip dan Dasar Teori 17
2.7.2 Instrumntasi 17
2.7.3 Nyala Pembakar 19
2.7.4 Gangguan Pada SSA dan Cara Mengatasinya 20
Bab 3 Metodologi Penelitian 21
3.1.1 Alat-alat 21 3.1.2 Bahan-bahan 22
3.2 Prosedur Penelitian 22
3.2.1 Pembuatan Larutan Standar Tembaga (Cu) 100 mg/L 22 3.2.2 Pembuatan Larutan Standar Tembaga (Cu) 10 mg/L 22 3.2.3 Pembuatan Larutan Seri Standar Tembaga (Cu) 0,0; 0,1;
0,5; 1 ; 2 dan 3 mg/L 22
3.2.4 Pembuatan Larutan Standar Kadmium (Cd) 100 mg/L 22 3.2.5 Pembuatan Larutan Standar Kadmium (Cd) 10 mg/L 23 3.2.6 Pembuatan Larutan Seri Standar Kadmium (Cd) 0,0; 0,1;
0,5; 1; 2 dan 3 mg/L 23
3.2.7 Pembuatan Kurva Standar Logam Tembaga (Cu) 23 3.2.8 Pembuatan Kurva Standar Logam Kadmium (Cd) 23
3.2.9 Aktivasi Bentonit 23
3.2.10 Pengaruh H2SO4 Yang Digunakan 24
3.2.11 Pengaruh Berat Bentonit Alam Teraktivasi 24 3.2.12 Pengaruh Berat bentonit Komersil 24 3.2.13 Pembuatan H2SO4 0,4 M 24
3.2.14 Pembuatan H2SO4 0,8 M 25
3.2.15 Pembuatan H2SO4 1,2 M 25
3.2.16 Pembuatan H2SO4 1,6 M 25
3.2.17 Pembuatan H2SO4 2,0 M 25
3.3 Bagan Penelitian 26
3.3.1 Aktivasi Bentonitt 26
3.3.2 Pembuatan Larutan Seri Standar dan Kurva Kalibrasi
Logam Tembaga (Cu) 27
3.3.3 Pembuatan Larutan Seri Standar dan Kurva Kalibrasi
Logam Kadmium (Cd) 28
3.3.4 Pengaruh H2SO4 Yang Digunakan 29
3.3.5 Pengaruh Berat Bentonit Alam Teraktivasi 30 3.4.6 Pengaruh Berat Bentonit Komersil 31
Bab 4 Hasil dan Pembahasan 32
4.1 Hasil Penelitian 32
4.1.1 Logam Kadmium (Cd) 32
4.1.2 Pengolahan Data Logam Kadmium (Cd) 33 4.1.2.1 Penurunan Persamaan Garis Regresi dengan
Metode Least Square 33
4.1.2.2 Koefisien Korelasi 34 4.1.2.3 Persentasi (%) Penurunan Konsentrasi Logam
Kadmium (Cd) 35
4.1.3 Logam Tembaga (Cu) 37
4.1.4 Pengolahan Data Logam Tembaga (Cu) 38 4.1.4.1 Penurunan Persamaan Garis Regresi dengan
Metode Least Square 38
4.1.4.2 Koefisien Korelasi 40 4.1.4.3 Persentasi (%) Penurunan Konsentrasi Logam
Tembaga 41
Bab 5 Kesimpulan dan Saran 45
5.1 Kesimpulan 45
5.2 Saran 45
DAFTAR TABEL
Halaman Tabel 2.1 Komposisi Bentonit 9 Tabel 2.2 Temperatur nyala dengan berbagai bahan bakar 19 Tabel 4.1 Kondisi alat SSA merek Shimadzu tipe AA-6300 pada
pengukuran konsentrasi logam Kadmium (Cd) 32 Tabel 4.2 Data absorbansi larutan standar Kadmium (Cd) 32 Tabel 4.3 Penentuan persamaan garis regresi logam Kadmium (Cd)
berdasarkan pengukuran absorbansi larutan standar Kadmium
(Cd) 33
Tabel 4.4 Data persentase (%) penurunan konsentrasi logam kadmium (Cd) 3 mg/L dalam larutan standar setelah penambahan bentonit
alam teaktivasi dengan konsentrasi H2SO4 yang berbeda 36
Tabel 4.5 Data persentase (%) penurunan konsentrasi logam Kadmium (Cd) 3 mg/L dalam larutan standar setelah penambahan bentonit
alam teraktivasi dengan konsentrasi H2SO4 1,2 M 36
Tabel 4.6 Data persentase (%) penurunan konsentrasi logam Kadmium (Cd) 3 mg/L dalam larutan standar setelah penambahan bentonit
komersil 37
Tabel 4.7 Kondisi alat SSA merek Shimadzu tipe AA-6300 pada
pengukuran konsentrasi logam Tembaga (Cu) 37 Tabel 4.8 Data Absorbansi larutan standar Tembaga (Cu) 38 Tabel 4.9 Penentuan persamaan garis regresi logam Tembaga (Cu)
berdasarkan pengukuran absorbansi larutan standar Tembaga
(Cu) 39
Tabel 4.10 Data persentase (%) penurunan konsentrasi logam Tembaga (Cu) 3 mg/L dalam larutan standar setelah penambahan bentonit
alam teraktivasi dengan konsentrasi H2SO4 yang berbeda 41
Tabel 4.11 Data persentase (%) penurunan konsentrasi logam Tembaga (Cu) 3 mg/L dalam larutan standar setelah penambahan bentonit
alam teraktivasi dengan konsentrasi H2SO4 1,2 M 41
Tabel 4.12 Data persentase (%) penurunan konsentrasi logam Tembaga (Cu) 3 mg/L dalam larutan standar setelah penambahan bentonit
DAFTAR GAMBAR
Halaman
Gambar 2.1 Struktur bentonit 8
ABSTRAK
Telah dilakukan penelitian tentang pengaruh variasi konsentrasi H2SO4 dan berat dari
bentonit alam teraktivasi dan komersil terhadap adsorpsi logam kadmium (Cd) dan tembaga (Cu) dalam larutan standar menggunakan metode Spektrofotometri Serapan Atom. Pada proses aktivasi bentonit dikaji variasi konsentrasi H2SO4 yaitu 0,4; 0,8;
1,2; 1,6; dan 2,0 M. Ke dalam larutan standar kadmium (Cd) dan tembaga (Cu) ditambahkan 1, 2, 3, 4, dan 5 g bentonit alam yang telah diaktivasi dengan H2SO4 1,2
M dan bentonit komersil, diaduk selama 6 jam, disaring dan diukur konsentrasi logam kadmium (Cd) dan tembaga (Cu) dengan Spektrofotometer Serapan Atom melalui kurva kalibrasi. Hasil penelitian menunjukkan bahwa bentonit H2SO4 1,2 M yang
THE CONCENTRATION EFFECT’S OF H2SO4 AND WEIGHT OF ACTIVATED BLEACHING EARTH AND COMMERCIAL TO
ADSORPTION CADMIUM METAL (Cd) AND COPPER (Cu) IN STANDARDSOLUTION USING ATOMIC
ABSORPTION SPECTROPHOTOMETRIC METHOD
ABSTRACT
The various concentration effect’s of H2SO4 and weight of activated bleaching earth
and commercial to adsoption of cadmium metal (Cd) and copper (Cu) in standard solution using Atomic Absorption Spectrophotometric method has been studied. Bleaching earth activation process assessed various concentration of H2SO4 which is
0,4; 0,8; 1,2; 1,6; and 2,0 M. 1, 2, 3, 4, and 5 g activated bleaching earth and commercial added into cadmium standard solution (Cd) and copper (Cu) , stirred up to 6 hours, filtered and measured by cadmium metal concentration (Cd) and copper (Cu) using Atomic Absorption Spectrophotometer instrument with calibration curve. The result of research show that H2SO4 1,2 M the best can adsorp cadmium metal (Cd) is
BAB 1
PENDAHULUAN
1.1Latar Belakang
Mineral lempung merupakan salah satu kekayaan Indonesia yang berlimpah dan
belum dimanfaatkan secara optimal. Tanah lempung secara geolois adalah mineral
alam dari keluarga silikat yang berbentuk kristal dengan struktur berlapis (Karna,
2002). Bentonit merupakan salah satu jenis lempung yang banyak terdapat di beberapa
wilayah Indonesia diantaranya terdapat di sebagian besar daerah Nusa Tenggara,
Sulawesi, Jawa Barat, Jawa Tengah, Yogyakarta, Jawa Timur, Sumatera Selatan,
Jambi, dan Sumatera Utara (Soedjoko, 1987).
Bentonit mempunyai kemampuan daya koloid yang kuat, bila bercampur
dengan air maka dapat mengembang. Prinsip mengubah permukaan dan pori – pori
bentonit adalah dengan melarutkan logam – logam yang terdapat pada pori – pori
menjadi lebih luas (Supeno, M dan Sembiring, S. B, 2007).
Lempung bentonit sangat menarik untuk diteliti karena lempung ini
mempunyai struktur berlapis dengan kemampuan mengembang (swelling) dan
memiliki kation-kation yang dapat ditukarkan. Meskipun lempung bentonit sangat
berguna untuk adsorpsi, namun kemampuan adsorpsinya terbatas. Kelemahan tersebut
dapat diatasi melalui proses aktivasi menggunakan asam (HCl, H2SO4 dan HNO3)
sehingga dihasilkan lempung dengan kemampuan adsorpsi yang lebih tinggi. Asam
sulfat merupakan asam yang memiliki bilangan ekivalen H+ lebih tinggi dibanding
dengan asam klorida ataupun asam nitrat. Aktivasi lempung menggunakan asam akan
menghasilkan lempung dengan situs aktif lebih besar dan keasamaan permukan yang
lebih besar, sehingga akan dihasilkan lempung dengan kemampuan adsorpsi yang
Ada beberapa faktor yang menentukan keberhasilan aktivasi lempung
menggunakan H2SO4, salah satunya adalah konsentrasi asamnya. Konsentrasi yang
terlalu rendah menyebabkan tidak sempurnanya pembentukan situs aktif, sebaliknya
rasio yang terlalu besar akan menyebabkan rusaknya struktur lempung (Johnson and
Maxwell, 1981).
Dalam penelitian ini penulis menggunakan logam kadmium (Cd) dan tembaga
(Cu) yang diperoleh dari larutan standar. Logam kadmium (Cd) dan tembaga (Cu)
digunakan sebagai parameter pembanding untuk melihat aktivitas adsorpsi dari
bentonit alam teraktivasi dan komersil. Bentonit komersil yang digunakan peneliti
adalah bentonit alam yang telah diaktivasi dengan H2SO4 pada konsentrasi tertentu
yang dipeoleh dari pabrik bentonit di Kecamatan Hamparan Perak.
Metode pengujian pengaruh variasi konsentrasi H2SO4 yang digunakan
penulis adalah dengan membandingkan hasil penurunan persentase (%) kadar logam
kadmium (Cd) dan tembaga (Cu). Dan untuk pengujian berat bentonit alam teraktivasi
dan komersil dilakukan dengan membandingkan hasil penurunan persentase (%) kadar
logam kadmium (Cd) dan tembaga (Cu) sebelum dan setelah ditambahkan bentonit
alam teraktivasi dan komersil.
1.2 Permasalahan
1. Pada konsentrasi H2SO4 berapakah bentonit alam teraktivasi dapat
mengadsorpsi logam Kadmium (Cd) dan Tembaga (Cu) dalam larutan standar
secara optimal.
2. Apakah kemampuan adsorpsi dari bentonit alam teraktivasi lebih baik dari
pada bentonit komersil dalam mengadsorpsi logam kadmium (Cd) dan
tembaga (Cu) dalam larutan standar.
1.3 Pembatasan Masalah
1. Penentuan kadar logam Kadmium (Cd) dan Tembaga (Cu) pada larutan
standar.
2. Bentonit alam dan komersil diperoleh dari pabrik bentonit di Kecamatan
Hamparan Perak.
3. Bentonit alam dan komersil diaktivasi dengan H2SO4 dengan konsentrasi yang
berbeda.
1.4 Tujuan Penelitian
Penelitian ini bertujuan untuk menentukan konsentrasi H2SO4 yang optimum dan
persentase (%) penurunan kadar logam Kadium (Cd) dan Tembaga (Cu) pada larutan
standar setelah penambahan bentonit alam teraktivasi dan komersil.
1.5 Manfaat Penelitian
Hasil penelitian ini dapat digunakan sebagai sumber informasi yang berguna tentang
aktivasi bentonit menggunakan H2SO4 dan perbandingan kemampuan adsorpsi dari
bentonit alam teraktivasi dengan komersil terhadap logam Kadmium (Cd) dan
Tembaga (Cu) dalam larutan standar.
1.6 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Dasar LIDA Universitas Sumatera
Utara dan analisis Spektrofotometri Serapan Atom dilakukan di Laboratorium Kimia
Analitik Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas
Sumatera Utara.
1.7 Metodologi Penelitian
Penelitian ini adalah analisis laboratorium, dimana bentonit alam dan komersil yang
digunakan adalah bentonit yang diperoleh dari pabrik bentonit di Kecamatan
Hamparan perak. Bentonit alam direndam dengan H2SO4 0,4; 0,8; 1,2; 1,6; dan 2,0 M
menambahkan 5 gram bentonit alam teraktivasi ke dalam 30 mL larutan standar
kadmium (Cd) dan tembaga (Cu) dan diaduk dengan magnetik bar selama 6 jam.
Pengujian berat bentonit alam teraktivasi dan komersil dilakukan dengan
menambahkan 1, 2, 3, 4, dan 5 gram bentonit alam teraktivasi dan komersial ke dalam
30 mL larutan standar kadmium (Cd) dan tembaga (Cu) dan diaduk dengan magnetik
BAB 2
TINJAUAN PUSTAKA
2.1 Bentonit
Bentonit adalah clay yang sebagian besar terdiri dari montmorillonit dengan
mineral-mineral seperti kwarsa, kalsit, dolomit, feldspars, dan mineral-mineral lainnya. Montmorillonit
merupakan bagian dari kelompok smectit dengan komposisi kimia secara umum
(Mg,Ca)O.Al2O3.5SiO2.nH2O. Nama monmorilonit itu sendiri berasal dari Perancis
pada tahun 1847 untuk penamaan sejenis lempung yang terdapat di Monmorilon
Prancis yang dipublikasikan pada tahun 1853 – 1856 (www.dim.esdm.go.id).
Bentonit berbeda dari clay lainnya karena hampir seluruhnya (75%)
merupakan mineral monmorillonit. Mineral monmorillonit terdiri dari partikel yang
sangat kecil sehingga hanya dapat diketahui melalui studi mengunakan XRD (X-Ray
Difraction). Berdasarkan kandungan alumino silikat hidrat yang terdapat dalam
bentonit, maka bentonit tersebut dapat dibagi menjadi dua golongan :
a. Activated clay, merupakan lempung yang mempunyai daya pemucatan yang
rendah.
b. Fuller’s earth, merupakan lempung yang secara alami mempunyai sifat daya
serap terhadap zat warna pada minyak, lemak, dan pelumas.
Berdasarkan tipenya, bentonit dibagi menjadi dua, yaitu :
1. Na-bentonit
Na bentonit memiliki daya mengembang hingga delapan kali apabila
dicelupkan ke dalam air, dan tetap terdispersi beberapa waktu di dalam air.
terkena sinar matahari akan berwarna mengkilap. Suspensi koloidal
mempunyai pH: 8,5-9,8.
2. Ca-bentonit
Tipe bentonit ini kurang mengembang apabila dicelupkan ke dalam air, tetapi
secara alami setelah diaktifkan mempunyai sifat menghisap yang baik.
Suspensi koloidal mempunyai pH: 4-7. Dalam keadaan kering berwarna
abu-abu, biru, kuning, merah, coklat.
Na-bentonit dimanfaatkan sebagai bahan perekat, pengisi, lampur bor,
sesuai sifatnya mampu membentuk suspensi koloidal setelah bercampur
dengan air. Sedangkan Ca-bentonit banyak dipakai sebagai bahan penyerap.
Dengan penambahan zat kimia pada kondisi tertentu, Ca-bentonit dapat
dimanfaatkan sebagai bahan lumpur bor setelah melalui pertukaran ion,
sehingga terjadi perubahan menjadi Na-bentonit dan diharapkan menadi
peningkatan sifat reologi dari suspensi mineral tersebut
(http://www.tekmira.esdm.go.id/data/bentonit).
2.1.1 Proses Terjadinya Bentonit di Alam
Secara umum, asal mula terjadinya endapan bentonit ada 4, yaitu ;
1. Terjadi karena Proses Pelapukan Batuan
Faktor utama yang menyebabkan pelapukan batuan adalah komposisi kimiawi
mineral batuan induk, dan kelarutannya dalam air. Mineral-mineral utama
dalam pembentukan bentonit adalah plagioklas, kalium-feldspar, biotit,
muskovit, serta sedikit kandungan senyawa alumina dan ferromagnesia. Secara
umum, faktor yang mempengaruhi pelapukan batuan ini adalah iklim, jenis
batuan, relief, dan tumbuh-tumbuhan yang berada di atas bantuan tersebut.
Pembentukan bentonit sebagai hasil pelapukan batuan dapat juga
air, dan di dalam tanah dengan persenyawaan silikat yang terdapat di dalam air
dan batuan.
2. Terjadi karena Proses Hidrotermal di Alam
Proses batuan mempengaruhi alternasi yang sangat lemah, sehingga
mineral-mineral yang kaya akan magnesium, seperti biotit cenderung membentuk
mineral klorit. Kehadiran unsur-unsur logam alkali dan alkali tanah (kecuali
kalium), mineral mika, ferromagnesia, feldspar, dan plagioklas pada umumnya
akan membentuk monmorilonit, terutama disebabkan karena adanya unsur
magnesium.
Larutan hidrotermal merupakan larutan yang bersifat asam dengan
kandungan klorida, sulfur, karbon dioksida, dan silika. Larutan alkali ini
selanjutnya akan terbawa keluar dan bersifat basa, dan akan tetap bertahan
selama unsur alkali tanah tetap terbentuk sebagai akibat penguraian batuan asal
dan adanya unsur alakali tanah akan membentuk bentonit.
3. Terjadi karena Proses Transformasi
Proses transformasi (pengabuan) abu vulkanis yang mempunyai komposisi
gelas akan menjadi mineral lempung yang lebih sempurna, terutama pada
daerah danau, lautan, dan cekungan sedimentasi. Transformasi dari gunung
berapi yang sempurna akan terjadi apabila debu gunung berapi diendapkan
dalam cekungan seperti danau dan air. Bentonit yang terjadi akibat proses
transformasi pada umumnya bercampur dengan sedimen laut lainnya yang
berasal dari daratan, seperti batu pasir dan danau.
4. Terjadi karena Proses Pengendapan Batuan
Proses pengendapan bentonit secara kimiawi dapat terjadi sebagai endapan
sedimen dalam suasana basa (alkali), dan terbentuk pada cekungan sedimen
yang bersifat basa, dimana unsur pembentuknya antara lain: kabonat, silika,
fosfat, dan unsur lainnya yang bersenyawa dengan unsur alumunium dan
2.1.2 Struktur Bentonit
Struktur monmorillonit memiliki konfigurasi 2:1 yang terdiri dari dua silikon oksida
tetrahedral dan satu alumunium oksida oktahedral. Pada tetrahedral, 4 atom oksigen
berikatan dengan atom silikon di ujung struktur. Empat ikatan silikon terkadang
disubtitusi oleh tiga ikatan alumunium. Pada oktahedral atom alumunium
berkoordinasi dengan enam atom oksigen atau gugus-gugus hidroksil yang berlokasi
pada ujung oktahedron. Al3+ dapat digantikan oleh Mg2+, Fe2+, Zn2+, Ni2+, Li+ dan
kation lainnya. Subtitusi isomorphous dari Al3+ untuk Si4+ pada tetrahedral dan Mg2+
atau Zn2+ untuk Al3+ pada oktahedral menghasilkan muatan negatif pada permukaan
clay, hal ini diimbangi dengan adsorpsi kation di lapisan interlayer.
Gambar 2.1 Struktur Bentonit (http//:www.tekmira.esdm.go.id/data/bentonit)
Adanya atom-atom yang terikat pada masing-masing lapisan struktur
montmorillonit memungkinkan air atau molekul lain masuk di antara unit lapisan.
Akibatnya kisi akan membesar pada arah vertikal. Selain itu karena adanya pergantian
atom Si oleh Al menyebabkan terjadinya penyebaran muatan negatif pada permukaan
bentonit. Bagian inilah yang disebut sisi aktif (active site) dari bentonit dimana bagian
ini dapat menyerap kation dari senyawa-senyawa organik atau dari ion-ion senyawa
2.1.3 Sifat Fisik dan Kimia Bentonit
Dalam keadaan kering bentonit mempunyai sifat fisik berupa partikel butiran yang
halus berbentuk rekahan-rekahan atau serpihan yang khas seperti tekstur pecah kaca
(concoidal fracture), kilap lilin, lunak, plastis, berwarna kuning muda hingga abu-abu,
bila lapuk berwarna coklat kekuningan, kuning merah atau coklat, bila diraba terasa
licin, dan bila dimasukan ke dalam air akan menghisap air. Bentuk fisik dari bentonit
diperlihatkan pada gambar berikut :
Gambar 2.2 Bentuk fisik bentonit
Sifat fisik lainnya berupa massa jenis 2,2-2,8 g/L; indeks bias 1,547-1,557; dan titik
lebur 1330-1430oC. Bentonit termasuk mineral yang memiliki gugus aluminosilikat.
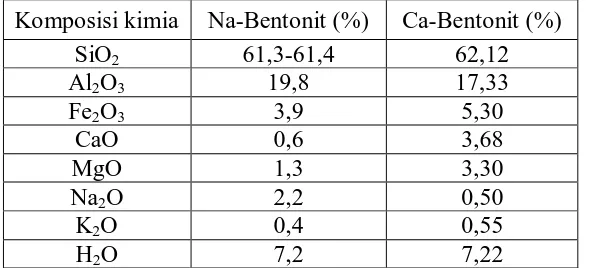
2.1.4 Komposisi Bentonit
Unsur-unsur kimia yang terkandung dalam bentonit diperlihatkan pada tabel berikut :
Tabel 2.1 Komposisi Bentonit
Komposisi kimia Na-Bentonit (%) Ca-Bentonit (%) SiO2 61,3-61,4 62,12
Al2O3 19,8 17,33
Fe2O3 3,9 5,30
CaO 0,6 3,68
MgO 1,3 3,30
Na2O 2,2 0,50
K2O 0,4 0,55
H2O 7,2 7,22
2.1.5 Aktivasi Bentonit
Sebelum digunakan dalam berbagai aplikasi, bentonit harus diaktifkan dan diolah
terlebih dahulu. Ada dua cara yang dapat dilakukan untuk aktivasi bentonit, yaitu :
1. Secara Pemanasan
Pada proses ini, bentonit dipanaskan pada temperatur 300-350oC untuk
memperluas permukaan butiran bentonit.
2. Secara Kontak Asam
Tujuan dari aktivasi kontak asam adalah untuk menukar kation Ca+ yang ada
dalam Ca-bentonit menjadi ion H+ dan melepaskan ion Al, Fe, dan Mg dan
pengotor-pengotor lainnya pada kisi-kisi struktur, sehingga secara fisik
bentonit tersebut menjadi aktif. Untuk keperluan tersebut asam sulfat dan asam
klorida adalah zat kimia yang umum digunakan. Selama proses bleaching
tersebut, Al, Fe, dan Mg larut dalam larutan, kemudian terjadi penyerapan
asam ke dalam struktur bentonit, sehingga rangkaian struktur mempunyai area
yang lebih luas.
Menurut Thomas, Hickey, dan Stecker, atom-atom al yang tersisa
masih terkoordinasi dalam rangkaian tetrahedral dengan empatt atom oksigen
tersisa. Perubahan dari gugus oktahedral menjadi tetrahedralmembuat kisi
kristal bermuatan negatif pada permukaan kristal, sehingga dapat dinetralisir
oleh ion hidrogen (Supeno, M dan Sembiring, S. B. 2007).
2.1.6 Aplikasi Bentonit
1. Bentonit sebagai Bahan penyerap (adsorben) atau Bahan Pemucat pada
Proses penyerapan zat warna (pigmen) merupakan proses yang sering
digunakan, seperti penyerapan zat warna pada minyak hewani, minyak nabati,
minyak bumi, dan lain-lain.
2. Bentonit sebagai Katalis
Penggunaan lempung sebagai katalis telah lama diperkenalkan, yaitu pada
proses perengkahan minyak bumi dengan menggunakan mineral
monmorillonit yang telah diasamkan. Namun, penggunaan lempung sebagai
katalis memiliki kelemahan, yaitu tidak tahan terhadap suhu tinggi.
3. Bentonit sebagai Bahan Penukar Ion
Pemanfaatan bentonit sebagai penukar ion didasarkan pada sifat permukaan
bentonit yang bermuatan negatif, sehingga ion-ion dapat terikat secara
elektrostatik pada permukaan bentonit.
4. Bentonit sebagai lumpur Bor
Penggunaan uatama bentonit adalah pada industri lumpur bor, yaitu sebagai
lumpur terpilar dalam pengeboran minyak bumi, gas bumi serta panas bumi.
Aktivasi bentonit untuk lumpur bor adalah merupakan suatu perlakuan
untuk mengubah Ca-bentonit menjadi Na-bentonit dengan penambahan bahan
alkali. Bahan alkali yang umum digunakan adalah Natrium karbonat dan
natrium hidroksida.
5. Bentonit untuk pembuatan Tambahan Makanan Ternak
Untuk dapat digunakan dalam pembuatan tambahan makanan ternak, bentonit
harus memenuhi persyaratan sebagai berikut : • Kandungan bentonit < 30 %
• Ukuran butiran bentonit adalah 200 mesh • Memiliki daya serap > 60 %
6. Bentonit untuk Industri kosmetik
Untuk dapat digunakan dalam industri kosmetik, bentonit harus memenuhi
persyaratan sebagai berikut :
• Mengandung mineral magnesium silikat (Ca-bentonit) • Mempunyai pH netral
• Kandungan air dalam bentonit adalah < 5 % • Ukuran buturin adalah 325 mesh
(Supeno, M dan Sembiring, S. B. 2007)
2.2. Adsorpsi
Adsorpsi adalah suatu proses pemisahan bahan dari campuran gas atau cair, bahan
yang harus dipisahkan ditarik oleh permukaan sorben padat dan diikat oleh gaya-gaya
yang bekerja pada permukaan tersebut.
Berkat selektivitasnya yang tinggi, proses adsorpsi sangat sesuai untuk
memisahkan bahan dengan konsentrasi yang kecil dari campuran yang mengandung
bahan lain yang berkonsentrasi tinggi. Bahan yang akan dipisahkan tentu saja harus
dapat diadsorpsi. Sebaliknya, untuk memisahkan bahan dengan konsentrasi yang lebih
besar lebih disukai proses pemisahan yang lain, karena mahalnya regenerasi adsorben.
2.2.1 Jenis Adsorpsi
Jenis Adsorpsi ada dua macam :
1. Adsorpsi fisik
- Panas adsorpsi kurang dari 40 KJ/mol
- Adsorpsi berlangsung pada suhu rendah
- Kesetimbangan adsorsi reversible dan cepat
- Tidak ada energi aktivasi yang terlibat dalam proses ini
2. Adsorpsi kimia
- Panas adsorpsi lebih besar dari ± 80 KJ/mol
- Adsorpsi berlangsung pada temperatur tinggi
- Kesetimbangan adsorpsi irreversible
- Energi aktivasi mungkin terlibat di dalam proses ini
- Terjadi adsorpsi monolapisan
(Gordon, M. Barrow, 1979)
2.2.2 Adsorben
Adsorben adalah bahan padat dengan luas permukaan dalam yang sangat besar.
Permukaan yang sangat luas ini terbenuk karena banyaknya pori yang halus pada
padatan tersebut. Biasanya luasnya berada dalam orde 200 – 1000 m2/g adsorben.
Diameter pori sebesar 0,0003 – 0,02 µm.
Di samping luas spesifik dan diameter pori, kerapatan, distribusi ukuran
partikel maupun kekerasannya merupakan data karakteristik yang penting dari suatu
adsorben. Tergantung pada tujuan penggunaannya, adsorben dapat berupa granulat
(dengan ukuran butir sebesar beberapa mm) atau serbuk (khusus untuk adsorpsi
campuran cair) (G. Bernasconi, 1995).
2.3 Logam
Logam menurut pengertian awam adalah barang yang padat dan berat yang biasanya
selalu digunakan oleh orang untuk alat-alat dapur atau untuk perhiasan, yaitu besi,
baja, emas, dan perak. Padahal masih banyak logam lain yang penting dan sangat kecil
serta berperan dalam proses biologis makhluk hidup misalnya selenium, kobalt,
mangan dan lain-lainya.
Logam juga dapat menyebabkan timbulnya suatu bahaya pada makhluk hidup.
Hal ini terjadi jika sejumlah logam mencemari lingkungan. Logam-logam tertentu
logam tersebut mempunyai sifat merusak tubuh makhluk hidup. Di samping hal
tersebut, beberapa logam sangat diperlukan dalam proses kehidupan makhluk hidup.
Dalam hal ini logam dapat dibagi menjadi dua bagian, yaitu logam esensial dan
nonesensial. Logam esensial adalah logam yang sangat membantu di dalam proses
fisiologis makhluk hidup dengan jalan membantu kerja enzim atau pembentukan
organ dari makhluk yang bersangkutan. Sedangakan logam non esensial adalah logam
yang perananya dalam tubuh makhluk hidup belum diketahui, kandungannya dalam
jaringan hewan sangat kecil dan apabila kandungannya tinggi akan merusak
organ-organ tubuh makhluk yang bersangkutan (Vogel, A.I, 1994).
Logam berat biasanya ditemukan sangat sedikit sekali dalam air secara
alamiah, yaitu kurang dari 1 µg/L. Bila terjadi erosi alamiah, konsentrasi logam
tersebut dapat meningkat. Dalam mempelajari konsentrasi dalam lingkungan perairan,
terlebih dahulu perlu diketahui tujuan dan pengetahuan mengenai spesiasi logam.
Idealnya penelitian tersebut harus terlebih dahulu mengetahui alur pergerakan logam
yang diteliti, hubungan interaksi masing-masing logam terhadap logam lain, model
distribusi logam dalam jaringan biota air, dan akumulasinya dalam setiap jaringan
(Darmono, 2001).
2.4 Kadmium (Cd)
Kadmium adalah metal berbentuk kristal putih keperakan. Kadium terutama terdapat
dalam kerak bumi bersama dengan seng. Kadmium yang terdapat di dalam lingkungan
pada kadar yang rendah berasal dari kegiatan penambangan seng, timah, dan kobalt
serta kuprum. Sementara dalam kadar tinggi, kadmium berasal dari emisi industri,
antara lain dari hasil sampingan penambangan, peleburan seng dan timbal
(Widowati,W.2008).
2.4.1 Efek Toksik Kadmium
Kadmium belum diketahui fungsinya secara biologis. Bagi manusia kadmium
sebenarnya merupakan logam asing. Tubuh sama sekali tidak membutuhkannya dalam
yang tidak terbatas, karena tidak adanya mekanisme tubuh yang dapat membatasinya.
Apabila kadmium masuk kedalam tubuh, maka sebagian besar akan terkumpul
didalam ginjal, hati dan ada sebagian yang keluar lewat saluran pencernaan.
Keracunan akut akan menyebabkan penyakit ginjal, penderita mengalami
pelunakan seluruh kerangka, dan kematian biasanya disebabkan gagal ginjal. Selain
itu didapat, bahwa masyarakat yang kekurangan gizi lebih peka terhadap Cd daripada
yang normal (Slamet, 1994).
2.5 Tembaga (Cu)
Tembaga adalah logam merah-muda, yang lunak, dapat ditempa, dan liat. Ia melebur
pada suhu 1038oC. Karena potensial elektroda standarnya positif, (+0,34 V untuk
pasangan Cu/Cu2+), ia tak larut dalam asam klorida dan asam sulfat encer, meskipun
dengan adanya oksigen ia dapat larut sedikit. Asam nitrat yang sedang pekatnya (8M)
dengan mudah melarutkan tembaga.
2.5.1 Efek Toksik Tembaga
Unsur Cu bisa ditemukan pada berbagai jenis makanan, air dan udara sehingga
manusia bisa terpapar Cu melalui jalur makanan, minuman, dan saat bernafas. Cu
merupakan unsur yang dibutuhkan dalam jumlah kecil. Apabila jumlah Cu telah
melampaui batas aman, akan muncul toksisitas. Manusia biasanya terpapar Cu dari
tanah, debu, makanan, serta minuman yang tercemar Cu yang berasal dari pipa bocor
pada penambangan Cu atau industri yang menghasikan limbah Cu. Kira-kira 75-99%
total in take Cu berasal dari makanan dan minuman. Setiap hari, manusia bisa terpapar
Cu yang antara lain berasal dari peralatan dapur ataupun koin.
Keracunan logam berat bersifat kronis dan dampaknya baru terlihat setalah
beberapa tahun. Logam berat bersifat akumulatif di dalam tubuh organisme dan
konsentrasi mengalami peningkatan (biomagnifikasi) dalam rantai makanan.
Biomagnifikasi berhubungan langsung dengan manusia yang menempati posisi top
makanan manusia telah mengalami peningkatan mulai dari komponen tingkat dasar
(produsen). Keracunan kronis Cu dapat mengurangi umur, menimbulkan berbagai
masalah reproduksi dan menurunkan fertilitas (Widowati, 2008).
2.6 Toksisitas Logam Berat
Toksisitas logam pada manusia menyebabkan beberapa akibat negatif, tetapi yang
terutama adalah timbulnya kerusakan jaringan, terutama jaringan detoksikasi dan
ekskresi (hati dan ginjal). Beberapa logam memiliki sifat karsinogenik (pembentuk
kanker), ataupun teratogenik (salah bentuk organ). Daya toksisitas ini dipengaruhi
oleh beberapa faktor yaitu kadar logam yang termakan, lamanya mengkonsumsi,
umur, spesies, jenis kelamin, kebiasaan makan makanan tertentu, kondisi fisik, dan
kemampuan jaringan tubuh untuk mengakumulasi logam. Beberapa logam toksik
dapat menyerang saraf sehingga dapat menyebabkan kelainan tingkah laku.
Toksisitas logam pada manusia kebanyakan terjadi karena logam berat
nonesensial saja, walaupun tidak menutup kemungkinan adanya keracunan logam
esensial yang melebihi dosis. Toksisitas logam esensial kadang-kadang dijumpai pada
orang, tetapi hanya terbatas pada logam tertentu saja, misalnya, Cu, Zn, dan Se
(Darmono, 1994)
2.7 Spektrofotometri Serapan Atom
Spektrofotometer serapan atom adalah suatu metode pengukuran kuantitatif suatu
unsur yang terdapat dalam suatu cuplikan berdasarkan penerapan cahaya pada panjang
gelombang tertentu oleh atom – atom bentuk gas dalam keadaan dasar. perpanjangan
SSA ke unsur lain semula merupakan akibat perkembangan spektroskopi pancaran
cahaya. Telah lama ahli kimia mengunakan pancaran radiasi oleh atom yang
dieksitasikan dalam suatu nyala sebagai alat analisis. Suatu nyala yang lain,
kebanyakan atom berada dalam keadaan tereksitasi. Fraksi atom – atom yang
tereksitasi berubah secara eksponensial dengan temperatur. Teknik ini digunakan
untuk penetapan sejumlah unsur, kebanyakan logam, dan sampel yang sangat
2.7.1 Prinsip Dan Dasar Teori
Spektrofotometri serapan atom didasarkan pada bahwa atom-atom pada suatu unsur
dapat mengabsorpsi energi sinar pada panjang gelombang tertentu. Banyak energi
sinar yang diabsorpsi berbanding lurus dengan jumlah atom-atom unsur yang
mengabsorpsi. Atom terdiri atas inti atom yang mengandung proton bermuatan positif
dan neutron berupa partikel netral, di mana inti atom dikelilingi oleh elektron-elektron
bermuatan negatif pada tingkat energi yang berbeda-beda. Jika energi diabsorpsi oleh
atom, maka elektron yang berada di kulit terluar (elektron valensi) akan tereksitasi dan
bergerak dari keadaan dasar atau tingkat energi yang terendah (ground state) ke
keadaan tereksitasi dengan tingkat energi yang lebih tinggi (excited state). Jumlah
energi yang dibutuhkan untuk memindahkan elektron ke tingkat energi tertentu
dikenal sebagai potensial eksitasi untuk tingkat energi tersebut. Pada waktu kembali
ke keadaan dasar, elektron melepaskan energi sebagai energi panas ataupun energi
sinar (Clark, D.V, 1979).
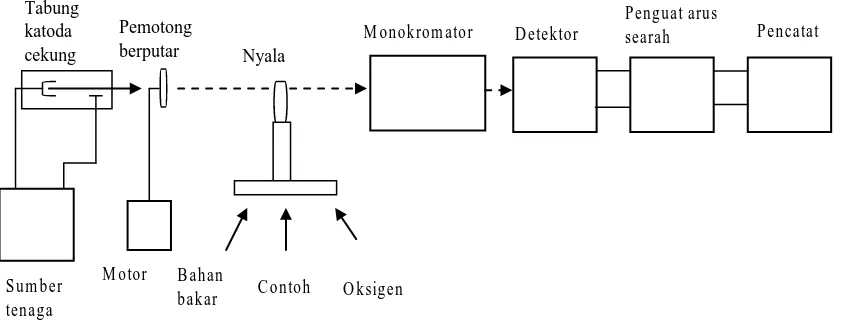
2.7.2 Instrumentasi
Komponen penting yang membentuk spektrofotometer serapan atom diperlihatkan
pada gambar di bawah ini.
Gambar 2.3 Instrumentasi SSA
(Day, R. A. Jr. dan Underwood A.L. 1988)
M onokrom ator D etektor
Penguat arus
searah Pencatat
Sum ber tenaga
B ahan
bakar C ontoh O ksigen
1. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga. Lampu ini
terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda.
Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau
dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon
atau argon) dengan tekanan rendah. Neon biasanya lebih disukai karena
memberikan intensitas pancaran lampu yang lebih rendah.
2. Tempat Sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam
keadaan asas. Ada berbagai macam alat yang dapat digunakan untuk
mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala dan tanpa
nyala.
a. Nyala (flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan
menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi.
b. Tanpa nyala (flameless)
Teknik atomisasi dengan nyala dinilai kurang peka karena atom gagal
mencapai nyala, tetesan sampel yang masuk kedalam nyala terlalu besar,
dan proses atomisasi kurang sempurna. Oleh karena itu muncullah suatu
teknik atomisasi yang baru yakni atomisasi tanpa nyala. Pengatoman dapat
dilakukan dalam tungku dari grafit. Sampel diletakkan dalam tabung grafit,
kemudian tabung tersebut dipanaskan dengan sistem elektris dengan cara
melewatkan arus listrik grafit. Akibat pemanasan ini, maka zat yang akan
dianalisis berubah menjadi atom-atom netral (Rohman, A. 2007).
Monokromator memisahkan, mengisolasi dan mengontrol intensitas dari
radiasi energi yang mencapai detektor. Pada hakekatnya mungkin saja dapat
dianggap sebagai suatu saringan yang dapat disesuaikan dengan suatu daerah
yang spesifik, yang mana spectrum transmisi yang tidak sesuai akan ditolak.
Idealnya monokromator harus mampu memisahkan garis resonansi. Karena
ada beberapa unsur yang mudah dan ada beberapa unsur yang sulit
(Haswell,S.J. 1991).
4. Detektor
Detektor dapat diatur sedemikian rupa pada nilai frekuensi tertentu, sehingga
tidak memberikan respon terhadap nilai emisi yang berasal dari eksitasi termal
(Khopkar,S.M. 2003).
5. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
sistem pencatat hasil.
2.7.3 Nyala Pembakar
Untuk spektroskopi nyala suatu persyaratan penting adalah bahwa nyalayang dipakai
hendaknya menghasilkan temperatur lebih dari 2000 K.
Tabel 2.2 Temperatur nyala dengan berbagai bahan bakar
Gas pembakar Temperatur (T/K)
Udara Dinitrogen oksida
Asetilena 2400 3200
Hidrogen 2300 2900
Propana 2200 3000
Gas kota 2100 -
Sejauh susunan nyala itu dipentingkan, dapatlah dicatat bahwa suatu campuran
asetilena-udara sesuai untuk penetapan sekitar tiga puluh logam, tetapi suatu nyala
uap atom. Untuk logam seperti alumunium dan titanium yang membentuk oksida
tahan api, temperatur nyala asetilena-nitrogen oksida yang lebih tinggi itu mutlak
perlu dan nyata kepekaan bertambah bila nyala kaya akan asetilena (Vogel, A.I,
1994).
2.7.4 Gangguan pada SSA dan Cara Mengatasinya
Gangguan nyata pada SSA adalah seringkali didapatkan suatu harga yang tidak sesuai
dengan konsentrasi sampel yang ditentukan. Penyebab dari gangguan ini adalah faktor
matriks sampel, faktor kimia adanya gangguan molekuler yang bersifat radiasi.
Sampel dalam bentuk molekul karena disosiasi yang tidak sempurna akan
cenderung mengabsorpsi radiasi dari sumber radiasi. Demikian juga terjadinya
ionisasi atom akan menjadi sumber kesalahan pada SSA oleh karena spektrum radiasi
oleh ion jauh berbeda dengan spektrum absorpsi atom netral yang memang akan
ditentukan. Ada beberapa usaha untuk mengurangi gangguan kimia pada SSA yaitu
dengan jalan:
1. Menaikkan temperatur nyala agar mempermudah penguraian untuk itu dipakai
gas pembakar campuran C2H2 + N2O yang memberikan nyala dengan
temperatur yang tinggi.
2. Menambahkan elemen pengikat gugus atom penyangga, sehingga terikat kuat
akan tetapi atom yang ditentukan bebas sebagai atom netral. Misalnya,
penentuan logam yang terikat sebagai garam, dengan penambahan logam,
yang lainnya akan terjadi ikatan lebih kuat dengan anion pengganggu.
3. Pengeluaran unsur pengganggu dari matriks sampel dengan cara eksitasi.
BAB 3
METODOLOGI PENELITIAN
3.1 Alat dan Bahan
3.1.1 Alat-alat
- Alu dan Lumpang
- Ayakan Mesh
- Corong
- Gelas Beaker Pyrex 500 mL
- Gelas Beaker Pyrex 250 mL
- Gelas Ukur Pyrex 50 mL
- Hotplate Cimarec
- Kertas Saring Whatman No 4
- Labu Takar Pyrex 100 mL
- Labu Takar Pyrex 50 mL
- Magnetik Bar
- Neraca Analitis AND
- Oven
- Pipet Skala Pyrex 5 mL
- Pipet Tetes
- Pipet Volum Pyrex 10 mL
- Pipet Volum Pyrex 5 mL
- Spatula
- Statif dan Klem
3.1.2 Bahan-bahan
- Bentonit alam Kec. Hamparan Perak
- Bentonit komersil Kec. Hamparan Perak
- H2SO4(p) p.a. (E. Merck)
- Akuades
- Larutan standar Cu 1000 mg/L p.a. (E. Merck)
- Larutan standar Cd 1000 mg/L p.a. (E. Merck)
3.2 Prosedur Penelitian
3.2.1 Pembuatan Larutan Standar Tembaga (Cu) 100 mg/L (SNI 06-6989.6-2004)
Sebanyak 5 mL larutan induk Tembaga 1000 mg/L dimasukkan ke dalam labu takar
50 mL lalu diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.2.2 Pembuatan Larutan Standar Tembaga (Cu) 10 mg/L
Sebanyak 10 mL larutan standar Tembaga 100 mg/L dimasukkan ke dalam labu takar
100 mL lalu diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.2.3 Pembuatan Larutan Seri Standar Tembaga (Cu) 0,0; 0,1; 0,5; 1,0; 2,0; dan
3,0 mg/L
Sebanyak 0,0; 0,5; 2,5; 5; 10; dan 15 mL larutan standar Tembaga 10 mg/L
dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuades sampai garis
tanda dan dihomogenkan.
3.2.4 Pembuatan Larutan Standar Kadmium (Cu) 100 mg/L (SNI
06-6989.16-2004)
Sebanyak 5 mL larutan induk Kadmium 1000 mg/L dimasukkan kedalam labu takar
3.2.5 Pembuatan Larutan Standar Kadmium (Cd) 10 mg/L
Sebanyak 10 mL larutan standar Kadmium 100 mg/L dimasukkan ke dalam labu takar
100 mL lalu diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.2.6 Pembuatan Larutan Seri Standar Kadmium (Cd) 0,0; 0,1; 0,5; 1,0; 2,0; dan
3,0 mg/L
Sebanyak 0,0; 0,5; 2,5; 5; 10; dan 15 mL larutan standar Kadmium 10 mg/L
dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuades sampai garis
tanda dan dihomogenkan.
3.2.7 Pembuatan Kurva Standar Tembaga (Cu)
Larutan blanko diukur absorbansinya dengan menggunakan Spektrofotometer Serapan
Atom pada λspesifik 324,8 nm. Perlakuan dilakukan sebanyak 3 kali. Dilakukan hal yang
sama untuk larutan seri standar Tembaga 0,0; 0,1; 0,5; 1,0; 2,0; dan 3,0 mg/L
3.2.8 Pembuatan Kurva Standar Kadmium (Cd)
Larutan blanko diukur absorbansinya dengan menggunakan Spektrofotometer Serapan Atom pada λspesifik 228,8 nm. Perlakuan dilakukan sebanyak 3 kali. Dilakukan hal yang
sama untuk larutan seri standar Kadmium 0,0; 0,1; 0,5; 1,0; 2,0; dan 3,0 mg/L.
3.2.9 Aktivasi Bentonit
Sampel bentonit alam dihaluskan hingga 200 mesh. Selanjutnya ditimbang sebanyak
25 g. Dimasukkan ke dalam gelas beaker 500 mL. Ditambahkan 100 mL H2SO4 0,4
M. Diaduk dengan magnetik bar selama 24 jam dan disaring. Dicuci endapan dengan
akuades hingga pH 7, kemudian disaring. Dipanaskan endapan di dalam oven pada
suhu 100-110oC. Dihaluskan, dan disimpan hasilnya di dalam desikator. Dilakukan
3.2.10 Variasi Konsentrasi H2SO4
Sebanyak 30 mL larutan seri standar Kadmium 3 mg/L dimasukkan ke dalam gelas
beaker 250 mL. Ditambahkan 5 g bentonit alam yang telah diaktivasi dengan H2SO4
0,4 M. Diaduk dengan menggunakan magnetik bar selama 6 jam. Disaring, dan filtrat
diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 228,8 nm.
Diulangi perlakuan yang sama untuk konsentrasi H2SO4 0,8; 1,2; 1,6; dan 2,0 M.
Diulangi perlakuan yang sama untuk larutan seri standar Tembaga 3 mg/L λspesifik
324,8 nm.
3.2.11 Variasi Berat Bentonit Alam Teraktivasi
Sebanyak 30 mL larutan seri standar Kadmium 3 mg/L dimasukkan ke dalam gelas
beaker 250 mL. Ditambahkan 1 g bentonit alam yang telah diaktivasi dengan H2SO4
1,2 M. Diaduk dengan menggunakan magnetik bar selama 6 jam. Disaring, dan filtrat
diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 228,8 nm.
Diulangi perlakuan yang sama untuk berat bentonit alam tearaktivasi 2, 3, 4, dan 5 g.
Diulangi perlakuan yang sama untuk larutan seri standar Tembaga 3 mg/L dengan λspesifik 324,8 nm.
3.2.12 Variasi Berat Bentonit Komersil
Sebanyak 30 mL larutan seri standar Kadmium 3 mg/L dimasukkan ke dalam gelas
beaker 250 mL. Ditambahkan 1 g bentonit komersil. Diaduk dengan menggunakan
magnetik bar selama 6 jam. Disaring, dan filtrat diukur absorbansinya dengan
Spektrofotometer SerapanAtom pada λspesifik 228,8 nm. Diulangi perlakuan yang sama
untuk berat bentonit komersil 2, 3, 4, dan 5 g. Diulangi perlakuan yang sama untuk larutan seri standar Tembaga 3 mg/L pada λspesifik 324,8 nm.
Sebanyak 2,1739 mL H2SO4(p) dimasukkan ke dalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan akuades secara perlahan-lahan sampai garis tanda. Di
tunggu sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3.2.14 Pembuatan H2SO4 0,8 M
Sebanyak 4,3478 mL H2SO4(p) dimasukkan ke dalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan akuades secara perlahan-lahan sampai garis tanda. Di
tunggu sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3.2.15 Pembuatan H2SO4 1,2 M
Sebanyak 6,5217 mL H2SO4(p) dimasukkan ke dalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan akuades secara perlahan-lahan sampai garis tanda. Di
tunggu sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3.2.16 Pembuatan H2SO4 1,6 M
Sebanyak 8,6956 mL H2SO4(p) dimasukkan ke dalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan akuades secara perlahan-lahan sampai garis tanda. Di
tunggu sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3.2.17 Pembuatan H2SO4 2,0 M
Sebanyak 10,8696 mL H2SO4(p) dimasukkan ke dalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan akuades secara perlahan-lahan sampai garis tanda. Di
3.3 Bagan Penelitian
3.3.1 Aktivasi Bentonit
Dihaluskan
Diayak hingga 200 mesh
Ditimbang 25 g
Dimasukkan ke dalam gelas beaker 500 mL
Ditambahkan 100 mL H2SO4 0,4 M
Diaduk dengan magnetik bar selama 24 jam
Disaring
Dicuci dengan akuades hingga pH 7
Disaring
Dikeringkan dalam oven pada suhu 100-110oC
Dihaluskan
Disimpan dalam desikator
Catatan : Diulangi perlakuan yang sama untuk konsentrasi H2SO4 0,8; 1,2; 1,6;
dan 2,0 M
Bentonit alam 200 mesh
Endapan Filtrat
Endapan Filtrat
Hasil
3.3.2 Pembuatan Larutan Seri Standar dan Kurva Kalibrasi Tembaga (Cu)
(SNI 06-6989.6-2004)
Dipipet sebanyak 5 mL dan dimasukkan ke dalam labu
takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 10 mL dan dimasukkan ke dalam labu
takar 100 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 0,0; 0,5; 2,5; 5; 10; dan 15 mL dan
dimasukkan ke dalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Diukur absorbansinya dengan Spektrofotometer Serapan
Atom pada λspesifik 324,8 nm
Larutan standar Tembaga 1000 mg/L
Larutan standar Tembaga 100 mg/L
Larutan standar Tembaga 10 mg/L
Larutan seri standar tembaga 0,0; 0,1; 0,5; 1,0; 2,0; dan 3,0 mg/L
3.3.3 Pembuatan Larutan Seri Standar dan Kurva Kalibrasi Kadmium(Cd)
(SNI 06-6989.16-2004)
Dipipet sebanyak 5 mL larutan dan dimasukkan ke dalam
labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 10 mL dan dimasukkan ke dalam labu
takar 100 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 0,0; 0,5; 2,5; 5; 10; dan 15 mL dan
dimasukkan ke dalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Diukur absorbansinya dengan Spektrofotometer Serapan Atom pada λspesifik 228,8 nm
Larutan standar Kadmium 1000 mg/L
Larutan standar Kadmium 100 mg/L
Larutan standar Kadmium 10 mg/L
Larutan seri standar Kadmium 0,0; 0,1; 0,5; 1,0; 2,0; dan 3,0 mg/L
3.3.4 Variasi Konsentrasi H2SO4
Diukur sebanyak 30 mL dan dimasukkan ke dalam gelas
beaker 250 mL
Ditambahkan 5 g bentonit alam yang telah diaktivasi
menggunakan H2SO4 0,4 M
Diaduk dengan menggunakan magnetik bar selama 6 jam
Disaring
Diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 228,8 nm
Diulangi perlakuan yang sama untuk konsentrasi H2SO4
0,8; 1,2; 1,6; dan 2,0 M.
Catatan : Diulangi perlakuan yang sama untuk larutan seri standar Tembaga 3
mg/L dengan λspesifik 324,8 nm
Larutan seri standar Kadmium 3 mg/L
filtrat Residu
3.3.5 Variasi Berat Bentonit Alam Teraktivasi
Diukur sebanyak 30 mL dan dimasukkan ke dalam gelas
beaker 250 mL
Ditambahkan 1 g bentonit alam yang telah diaktivasi
menggunakan H2SO4 1,2 M
Diaduk dengan menggunakan magnetik bar selama 6 jam
Disaring
Diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 228,8 nm
Diulangi perlakuan yang sama untuk konsentrasi bentonit
alam teraktivasi 2, 3, 4, dan 5 g
Catatan : Diulangi perlakuan yang sama untuk larutan seri standar Tembaga 3
mg/L dengan λspesifik 324,8 nm
Larutan seri standar Kadmium 3 mg/L
filtrat Residu
3.3.6 Variasi Berat Bentonit Komersil
Diukur sebanyak 30 mL dan dimasukkan ke dalam gelas
beaker 250 mL
Ditambahkan 1 g bentonit komersil
Diaduk dengan menggunakan magnetik bar selama 6 jam
Disaring
Diukur absorbansinya dengan Spektrofotometer Serapan Atom pada λspesifik 228,8 nm
Diulangi perlakuan yang sama untuk berat bentonit
komersil 2, 3, 4, dan 5 g
Catatan : Diulangi perlakuan yang sama untuk larutan seri standar Tembaga 3
mg/L dengan λspesifik 324,8 nm
Larutan seri standar Kadmium 3 mg/L
filtrat Residu
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
4.1.1 Logam Kadmium (Cd)
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran konsentrasi
logam Kadmium (Cd) dapat dilihat pada tabel 4.1.
Tabel 4.1 Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada pengukuran konsentrasi logam Kadmium (Cd)
No Parameter Logam Kadmium (Cd)
1
Kecepatan aliran gas pembakar (L/min)
Kecepatan aliran Udara (L/min)
Lebar Celah (nm)
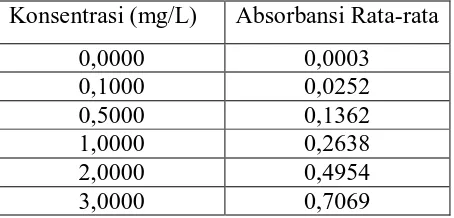
Tabel 4.2 Data absorbansi larutan standar Kadmium (Cd)
Konsentrasi (mg/L) Absorbansi Rata-rata
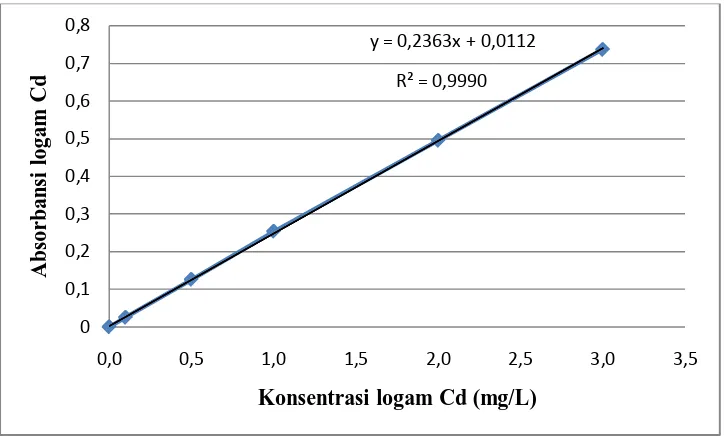
Gambar 4.1 Kurva kalibrasi larutan standar Kadmium (Cd).
4.1.2 Pengolahan Data Logam Kadmium (Cd)
4.1.2.1 Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar logam Kadmium (Cd) pada tabel 4.2.
diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa garis linier.
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode
least square dengan data pada tabel 4.3.
Tabel 4.3 Penurunan persamaan garis regresi logam Kadmium (Cd berdasarkan pengukuran absorbansi larutan standar Kadmium (Cd)
Y = = 0,2713
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
dimana :
Selanjutnya harga slope dapat ditentukan dengan mengunakan metode least square
sebagai berikut :
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.3. pada persamaan
ini maka diperoleh :
a =
a = 0,2365
b = 0,2713 – (0,2365)(1,1)
b = 0,2713 – 0,2601
b = 0,0112
Maka pesamaan garis yang diperoleh adalah :
4.1.2.2 Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
Koefisien korelasi untuk logam Kadmium (Cd) adalah:
r =
r =
r = 0,9990
4.1.2.3 Persentasi (%) penurunan konsentrasi logam Kadmium (Cd)
Persentase (%) penurunan konsentrasi logam Kadmium (Cd) dapat ditentukan dengan
menggunakan rumus :
x 100%
Maka persentasi (%) penurunan konsentrasi logam Kadmium (Cd) dalam larutan
standar setelah penambahan bentonit alam teraktivasi adalah :
x 100% = 83,85%
Dengan cara yang sama dapat dihitung persentasi (%) penurunan konsentrasi logam
Kadmium (Cd) dalam larutan standar setelah penambahan bentonit alam teraktivasi.
Tabel 4.4 Data persentase (%) penurunan konsentrasi logam kadmium (Cd) 3 mg/L dalam larutan standar setelah penambahan bentonit alam teaktivasi dengan variasi konsentrasi H2SO4
Konsentrasi H2SO4
(M)
Konsentrasi (mg/L) Persentase (%)
penurunan
Tabel 4.5 Data persentase (%) penurunan konsentrasi logam Kadmium (Cd) 3 mg/L dalam larutan standar setelah penambahan bentonit alam teraktivasi dengan konsentrasi H2SO4 1,2 M
Berat bentonit
alam teraktivasi
(g)
Konsentrasi (mg/L) Persentase (%)
Tabel 4.6 Data persentase (%) penurunan konsentrasi logam Kadmium (Cd) 3 mg/L dalam larutan standar setelah penambahan bentonit komersil
Berat bentonit
komersil(g)
Konsentrasi (mg/L) Persentase (%)
penurunan
4.1.3 Logam Tembaga (Cu)
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran konsentrasi
logam Tembaga (Cu) dapat dilihat pada tabel 4.7.
Tabel 4.7 Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada pengukuran konsentrasi logam Tembaga (Cu)
No Parameter Logam Tembaga (Cu)
1
Kecepatan aliran gas pembakar (L/min)
Kecepatan aliran Udara (L/min)
Tabel 4.8 Data absorbansi larutan standar Tembaga (Cu)
Konsentrasi (mg/L) Absorbansi Rata-rata
0,0000 0,0002
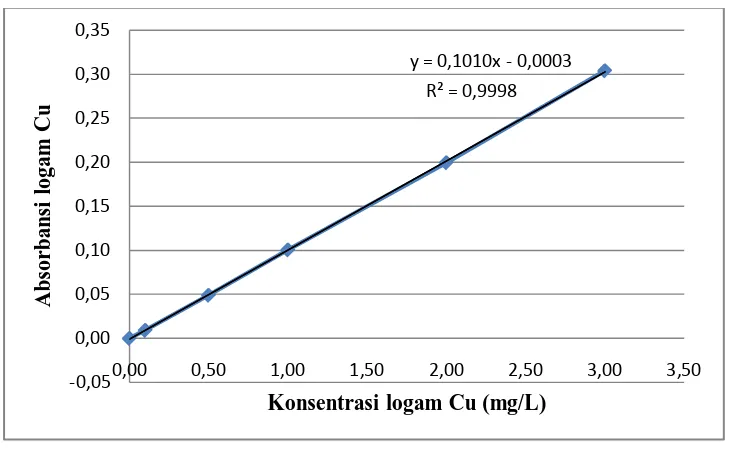
Gambar 4.2 Kurva kalibrasi larutan standar Tembaga (Cu)
4.1.4 Pengolahan Data Logam Tembaga (Cu)
4.1.4.1 Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar logam Tembaga (Cu) pada Tabel 4.7.
diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa garis linier.
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode
least square dengan data pada Tabel 4.9.
R² = 0,9998
0,00 0,50 1,00 1,50 2,00 2,50 3,00 3,50
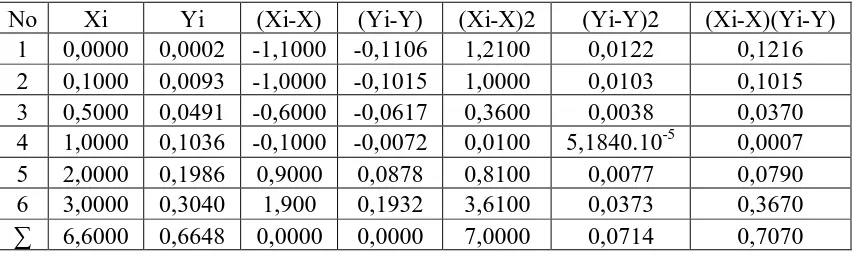
Tabel 4.9 Penurunan persamaan garis regresi logam Tembaga (Cu) berdasarkan pengukuran absorbansi larutan standar Tembaga (Cu)
No Xi Yi (Xi-X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y) 1 0,0000 0,0002 -1,1000 -0,1106 1,2100 0,0122 0,1216 2 0,1000 0,0093 -1,0000 -0,1015 1,0000 0,0103 0,1015 3 0,5000 0,0491 -0,6000 -0,0617 0,3600 0,0038 0,0370 4 1,0000 0,1036 -0,1000 -0,0072 0,0100 5,1840.10-5 0,0007 5 2,0000 0,1986 0,9000 0,0878 0,8100 0,0077 0,0790 6 3,0000 0,3040 1,900 0,1932 3,6100 0,0373 0,3670 ∑ 6,6000 0,6648 0,0000 0,0000 7,0000 0,0714 0,7070
X = = 1,1
Y = = 0,1108
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
dimana :
Selanjutnya harga slope dapat ditentukan dengan mengunakan metode least square
sebagai berikut :
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.11. pada
a =
a = 0,1010
b = 0,1108 – (0,1010)(1,1)
b = 0,1108 – 0,1111
b = - 0,0003
Maka pesamaan garis yang diperoleh adalah :
4.1.4.2 Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
r =
Koefisien korelasi untuk logam Tembaga (Cu) adalah:
r =
r =
r = 0,9998
4.1.4.3 Persentasi (%) penurunan konsentrasi logam Tembaga (Cu)
Persentase (%) penurunan konsentrasi logam Tembaga (Cu) dapat ditentukan dengan
menggunakan rumus :
Maka persentasi (%) penurunan konsentrasi logam Tembaga (Cu) dalam larutan
standar setelah penambahan bentonit alam teraktivasi.
x 100% = 83,16 %
Dengan cara yang sama dapat dihitung persentasi (%) penurunan konsentrasi logam
Tembaga (Cu) dalam larutan standar setelah penambahan bentonit teraktivasi dan
komersial. Data selengkapnya pada tabel 4.10., tabel 4.11., dan 4.12.
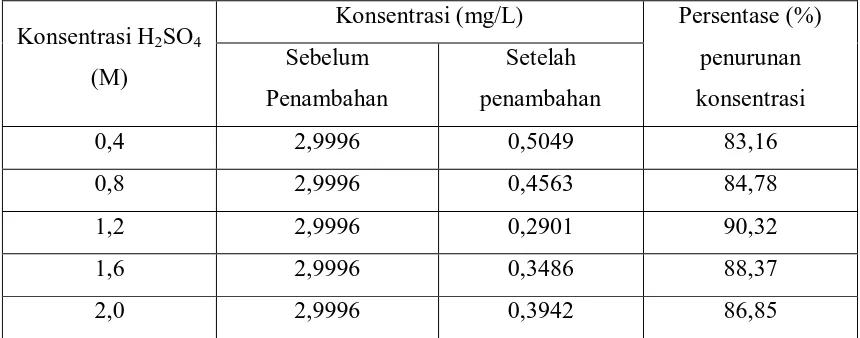
Tabel 4.10 Data persentase (%) penurunan konsentrasi logam Tembaga (Cu) 3 mg/L dalam larutan standar setelah penambahan bentonit alam teraktivasi dengan variasi konsentrasi H2SO4
Konsentrasi H2SO4
(M)
Konsentrasi (mg/L) Persentase (%)
penurunan
konsentrasi Sebelum
Penambahan
Setelah
penambahan
0,4 2,9996 0,5049 83,16
0,8 2,9996 0,4563 84,78
1,2 2,9996 0,2901 90,32
1,6 2,9996 0,3486 88,37
Tabel 4.11 Data persentase (%) penurunan konsentrasi logam Tembaga (Cu) 3 mg/L dalam larutan standar setelah penambahan bentonit alam teraktivasi dengan konsentrasi H2SO4 1,2 M
Berat bentonit alam
teraktivasi(g)
Konsentrasi (mg/L) Persentase (%)
penurunan
Tabel 4.12 Data persentase (%) penurunan konsentrasi logam Tembaga (Cu) 3 mg/L dalam larutan standar setelah penambahan bentonit komersil
Berat bentonit
komersil(g)
Konsentrasi (mg/L) Persentase (%)
penurunan
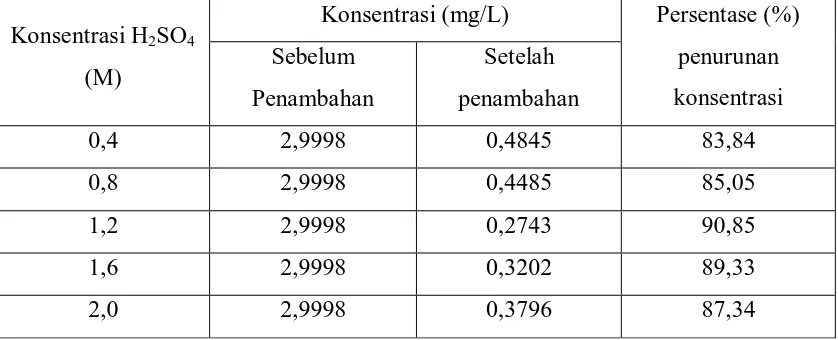
Dari hasil penelitian diperoleh bahwa persentase (%) konsentrasi logam
Kadmium (Cd) dan Tembaga (Cu) setelah penambahan bentonit alam teraktivasi
dengan variasi konsentrasi H2SO4 0,4; 0,8; 1,2; 1,6; dan 2,0 M mengalami penurunan.
Untuk logam Kadmium (Cd) larutan standar sebelum penambahan bentonit alam
bentonit teraktivasi dengan variasi konsentrasi H2SO4 0,4; 0,8; 1,2; 1,6; dan 2,0 M
masing-masing berkurang menjadi 0,4845; 0,4485; 0,2743; 0,3202; 0,3796 mg/L.
Dengan kata lain, konsentrasi logam Kadmium (Cd) berkurang setelah penambahan
bentonit alam teraktivasi dengan variasi konsentrasi H2SO4 0,4; 0,8; 1,2; 1,6; dan 2,0
M masing – masing sebesar 83,85%, 85,05%, 90,85%, 89,33% dan 87,34% (Tabel
4.4.).
Hal yang serupa juga terjadi pada logam Tembaga (Cu). Sebelum penambahan
bentonit alam teraktivasi memiliki konsentrasi sebesar 2,9998 mg/L dan setelah
penambahan bentonit teraktivasi konsentrasi H2SO4 0,4; 0,8; 1,2; 1,6; dan 2,0 M
masing-masing berkurang menjadi 0,5049; 0,4563; 0,2901; 0,3486; 0,3942 mg/L.
Dengan kata lain, konsentrasi logam Tembaga (Cu) berkurang setelah penambahan
bentonit alam teraktivasi dengan variasi konsentrasi H2SO4 0,4; 0,8; 1,2; 1,6; dan 2,0
M masing – masing sebesar 83,16%, 84,78%, 90,32%, 88,37% dan 86,85% (Tabel
4.10).
Dari hasil penelitian juga diperoleh bahwa persentase (%) penurunan
konsentrasi logam Kadmium (Cd) dan Tembaga (Cu) dengan menggunakan bentonit
alam teraktivasi lebih besar daripada bentonit komersil. Untuk logam Kadmium (Cd)
dalam dalam larutan standar, sebelum penambahan bentonit alam teraktivasi dan
komersil memiliki konsentrasi sebesar 2,9996 mg/L dan setelah penambahan bentonit
alam teraktivasi dan bentonit komersial 1, 2, 3, 4, dan 5 g berkurang masing – masing
menjadi 0,4357; 0,3964; 0,3521; 0,3241; dan 0,2743 mg/L untuk benonit alam
teraktivasi dan 0,4765; 0,4145; 0,3743; 0,3225 dan 0,2901 mg/L untuk bentonit
komersil. Dengan kata lain, konsentrasi Kadmium (Cd) berkurang setelah
penambahan bentonit alam teraktivasi dan bentonit komersil masing – masing sebesar
85,47; 86,78; 88,20; 89,52 dan 90,85% untuk bentonit alam teraktivasi dan 84,11;
86,18; 87,52; 88,91; dan 90,32% untuk bentonit komersil (Tabel 4.5. dan tabel 4.6.).
Hal yang serupa juga terjadi pada logam Tembaga (Cu). Sebelum penambahan
bentonit alam teraktivasi dan komersil memiliki konsentrasi sebesar 2,9996 mg/L dan
setelah penambahan bentonit alam teraktivasi dan komersil 1, 2, 3, 4, dan 5 g
berkurang masing – masing menjadi 0,4452; 0,4087; 0,3614; 0,3241; dan 0,2837
mg/L untuk bentonit komersil. Dengan kata lain, konsentrasi Kadmium (Cd)
berkurang setelah penambahan bentonit alam teraktivasi dan bentonit komersil
masing-masing sebesar 85,15; 86,37; 87,95; 89,19 dan 90,54% untuk bentonit alam
teraktivasi dan 83,47; 85,63; 87,21; 88,43; dan 90,04% untuk bentonit komersil (Tabel
4.11. dan 4.12.).
Ada beberapa faktor yang menentukan keberhasilan aktivasi bentonit
menggunakan H2SO4, salah satunya adalah konsentrasi asamnya. . Dari penelitian ini
diperoleh konsentrasi H2SO4 yang optimum adalah 1,2 M, sehingga konsentrasi yang
terlalu rendah, yaitu dibawah 1,2 M menyebabkan tidak sempurnanya pembentukan
situs aktif, sehingga kemampuan adsorpsi dari bentonit tidak optimum, sebaliknya
konsentrasi yang terlalu besar, yaitu diatas 1,2 M asam akan menghidrolisa
alumunium dari kerangka bentonit yang menyebabkan struktur menjadi rusak.
Tujuan dari aktivasi dengan penambahan asam adalah untuk menukar kation
Ca+ yang ada dalam Ca-bentonit menjadi ion H+ dan melepaskan ion Al, Fe, dan Mg
dan pengotor-pengotor lainnya pada kisi-kisi struktur, sehingga secara fisik bentonit
tersebut menjadi aktif. Untuk keperluan tersebut asam sulfat dan asam klorida adalah
zat kimia yang umum digunakan. Selama proses bleaching tersebut, Al, Fe, dan Mg
larut dalam larutan, kemudian terjadi penyerapan asam ke dalam struktur bentonit,
sehingga rangkaian struktur mempunyai area yang lebih luas.
Atom-atom Al yang tersisa masih terkoordinasi dalam rangkaian tetrahedral
dengan empat atom oksigen tersisa. Perubahan dari gugus oktahedral menjadi
tetrahedral membuat kisi kristal bermuatan negatif pada permukaan kristal, sehingga
dapat dinetralisir oleh ion hidrogen. Bagian inilah yang disebut sisi aktif (active site)
dari bentonit dimana bagian ini dapat mengadsorpsi kation dari senyawa-senyawa
organik atau dari ion-ion senyawa logam.
Proses adsorpsi dapat berlangsung ketika permukaan padatan pada molekul
adsorbat (zat yang akan diserap) membentur permukaan padatan, sehingga sebagian
akan menempel di permukaan padatan dan terserap. Pada awalnya, laju adsorpsi
cukup besar karena seluruh permukaan masih kosong. Namun setelah waktu kontak
semakin lama, permukaan yang terisi oleh molekul semakin banyak dan luas daerah
dalam proses adsorpsi logam kadmium (Cd) dan tembaga (Cu) hanya melibatkan gaya