EFEKTIVITAS PEMBERIAN BAKTERI METANOTROF DAN
OCHROBACTRUM ANTHROPI
TERHADAP PENURUNAN EMISI
GAS CH4 DAN N2O DAN PEMACUAN PERTUMBUHAN
PADI DI DATARAN RENDAH
SUKMAWATI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Efektivitas Pemberian Bakteri Metanotrof dan Ochrobactrum anthropi terhadap Penurunan Emisi Gas CH4 dan N2O dan Pemacuan Pertumbuhan Padi di Dataran Rendah adalah benar
karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, 26 Agustus 2015 Sukmawati G351130061
RINGKASAN
SUKMAWATI. Efektivitas Pemberian Bakteri Metanotrof dan Ochrobactrum
anthropi terhadap Penurunan Emisi Gas CH4 dan N2O dan Pemacuan
Pertumbuhan Padi di Dataran Rendah. Dibimbing oleh Iman Rusmana dan Nisa Rachmania Mubarik.
Beras adalah kebutuhan pokok masyarakat khususnya masyarakat Indonesia, dan salah-satu sumber penghasil gas rumah kaca ialah lahan sawah, pelepasan gas yang diemisikan dari lahan sawah seperti gas metan (CH4) dan dinitrogen oksida
(N2O). Beberapa metode sistem intensif untuk meningkatkan produktivitas padi
seperti pemupukan dengan senyawa kimia, perbaikan sistem irigasi, pengendalian hama dengan menggunakan pestisida kimia memberi dampak negatif terhadap lingkungan. Pemupukan dengan senyawa kimia dapat meningkatkan emisi gas metan (CH4) dan dinitrogen oksida (N2O) yang menyebabkan pemananasan global.
CH4 berpotensi menyebabkan pemanasan global 23 kali lebih besar dibandingkan
CO2. Gas N2O memiliki potensi sebagai penyebab pemanasan global 298 kali
lebih besar dibandingkan dengan CO2. CH4 dan N2O dapat direduksi melalui
proses oksidasi CH4 dan reduksi N2O oleh bakteri metanotrof dan bakteri
dinitrogen oksida serta dapat meningkatkan produktivitas padi.
Penelitian ini dilakukan dengan 2 perlakuan. Kontrol (P1) menggunakan pupuk senyawa kimia NPK (15:15:15) 250 kg/ha (takaran 100% pupuk dosis anjuran). Pada perlakuan (P2) digunakan pupuk senyawa kimia NPK 50 kg/ha (takaran 20% pupuk dosis anjuran) serta menambahkan bakteri metanotrof M. rosea BGM 1, M. parvus BGM 3, M. capculatus BGM 9, Methylobacter sp. SKM 14 dan bakteri pereduksi N2O O. anthropi BL2.
Tinggi tanaman, jumlah anakan, jumlah malai per rumpun dan skor warna hijau daun pada perlakuan (P2) masing-masing meningkat sebesar 12.50%, 23.76%, 16.49%, dan 35.92% dibandingkan dengan tanaman kontrol (P1). Rata-rata bobot kering tajuk, bobot kering akar, panjang akar, malai produktif, butir per malai dan bobot 1000 butir pada tanamn perlakuan (P2) meningkat sebesar 67.60%, 143.32%, 37.05%, 24.46%, 48.28%, dan 42.07% dari tanaman kontrol (P1).
Emisi metan pada pengamatan 21, 42, 63, dan 84 hari setelah tanam pada kontrol (P1) melepaskan emisi metan dengan nilai tertinggi 7.43 mol CH4/hari/m2
sedangkan pada perlakuan (P2) menunjukkan penurunan (sink) metan paling rendah sebesar 0.13 mol CH4/hari/m2. Emisi N2O pada perlakuan (P2) pada umur
21, 42, 63, dan 84 hari setelah tanam menunjukkan penurunan (sink) N2O paling
rendah sebesar 0.0023 mol N2O/hari/m2 sedangkan pada kontrol (P1)
menunjukkan pelepasan emisi dinitrogen oksida dengan nilai tertinggi 0.0026 mol N2O/hari/m2. Efektivitas bakteri metanotrof M. rosea BGM 1, M. parvus BGM 3,
M. capculatus BGM 9, Methylobacter sp. SKM 14, dan O. anthropi BL2 dapat
mengurangi emisi metan (CH4) dan dinitrogen oksida (N2O) serta memacu
pertumbuhan tanaman padi.
Kata kunci: Emisi CH4, Emisi N2O, Metanotrof, Lahan sawah, Ochrobactrum
SUMMARY
SUKMAWATI. Effectiveness of Methanotrophic Bacteria and Ochrobactrum
anthropi to Reduce CH4 and N2O Emissions and to Promote Paddy Growth in
Lowland Paddy Fields. Suvervised by Iman Rusmana and Nisa Rachmania Mubarik.
Rice is the most important basic needs in Indonesia, however paddy field is one of the sources of greenhouse gasses such as methane (CH4) and nitrous oxide
(N2O). Various methods such as application of inorganic fertilizer, irrigation
system, and pest control using pesticides were intensively applied to increase paddy productivity. Application of the methods could give an effect to environment. The use of inorganic fertilizers will increase CH4 and N2O
emissions causing global warming. Methane has a potency to cause global warming 23 times greater than that of CO2, meanwhile N2O gas has a potency to
cause global warming 298 times greater than that of CO2. Oxidation and reduction
process of CH4 and N2O by methanotrophic bacteria and dinitrogen oxide bacteria
BL2 can reduce CH4 and N2O emissions as well as increase paddy productivity.
This research was conducted with two treatments. The control (P1) using inorganic fertilizer NPK (15:15:15) 250 kg/ha (100% recommended normal dose) without application of bacteria. Meanwhile the treatment (P2) used inorganic fertilizers NPK 50 kg/ha (20% of recommended normal dose) with addition of methanotrophic bacteria (M. rosea BGM 1, M. parvus BGM 3, M. capculatus BGM 9, Methylobacter sp. SKM 14) and N2O reducing bacteria (O. anthropi
BL2).
Paddy growth parameters such as plant’s height, number of tiller, number of
panicles per cluster and green color score on the treatment (P2) were increased up to 12.50%, 23.76%, 16.49%, and 35.92% compared to control (P1) respectively.
Average of shoot’s dry weight, root’s dry weight, root’s length, grains per
panicles and weight of 1000 grains in the treatment (P2) plants were increased up to 67.60%, 143.32%, 37.05%, 48.28%, and 42.07% compared to control (P1)
control (P1) fields had high emission up to 0.0026 mole N2O/day/m2. In summary,
applcation of methanotrophic bacteria M. rosea BGM 1, M. parvus BGM 3, M. capculatus BGM 9, Methylobacter sp. SKM 14, and dinitrogen oxide bacteria can reduce CH4, N2O emission, and increase paddy’s growth in paddy fields.
Keywords: CH4 emission, N2O emission, Methanotrophs, paddy field,
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Mikrobiologi
EFEKTIVITAS PEMBERIAN BAKTERI METANOTROF DAN
OCHROBACTRUM ANTHROPI
TERHADAP PENURUNAN
EMISI GAS CH4 DAN N2O DAN PEMACUAN PERTUMBUHAN
PADI DI DATARAN RENDAH
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2015
Judul Tesis : Efektivitas Pemberian Bakteri Metanotrof dan Ochrobactrum
anthropi terhadap Penurunan Emisi Gas CH4 dan N2O dan
Pemacuan Pertumbuhan Padi di Dataran Rendah Nama : Sukmawati
NIM : G351130061
Disetujui oleh Komisi Pembimbing
Dr Iman Rusmana, MSi Ketua
Dr Nisa Rachmania Mubarik, MSi Anggota
Diketahui oleh
Ketua Program Studi Mikrobiologi
Departemen Biologi
Prof Dr Anja Meryandini, MS
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MSc Agr
Tanggal Ujian: 14 Agustus 2015
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah Subehanawata’ala atas segala karunia-Nya sehingga tesis ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Juni 2014 sampai Maret 2015 dengan judul Efektivitas Pemberian Bakteri Metanotrof dan Ochrobactrum
anthropi terhadap Penurunan Emisi Gas CH4 dan N2O dan Pemacuan
Pertumbuhan Padi di Dataran Rendah.
Terima kasih penulis ucapkan kepada Bapak Dr Iman Rusmana, MSi dan Ibu Dr Nisa Rachmania Mubarik, MSi selaku pembimbing, serta ucapan terima kasih kepada Bapak Dr Hamim, MSi sebagai penguji pada ujian tesis. Di samping itu, penghargaan penulis sampaikan kepada Bapak Jaka Permana dari staf Laboratorium Mikrobiologi, para warga Desa Citarik Kecamatan Pelabuhan Ratu Kabupaten Sukabumi, dan teman-teman mikrotropisian 2012/2013 yang telah membantu selama pengumpulan data. Ungkapan terima kasih juga disampaikan kepada ayah, ibu, Ibrahim, serta seluruh keluarga, atas doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL ix
DAFTAR GAMBAR x
DAFTAR LAMPIRAN xi
PENDAHULUAN 1
Latar Belakang 1
Tujuan Penelitian 2
TINJAUAN PUSTAKA 2
Emisi Metan (CH4) dan Dinitrogen Oksida (N2O) 2
Bakteri Metanotrof 4
Bakteri Pereduksi Gas Dinitrogen Oksida (N2O) 5
METODE 6
Waktu dan Tempat 6
Bahan 6
Prosedur Penelitian 6
Tahap Peremajaan Isolat 7
Tahap Pengolahan Sawah dan Penyiapan Bibit 7
Tahap Penanaman dan Inokulasi Bakteri Metanotrof 7
Tahap Pemasangan Sungkup 7
Tahap Pemeliharaan dan Parameter yang Diamati 7
Analisis Sifat Fisik dan Kimia Tanah 8
HASIL 8
Analisis Sifat Fisik dan Kimia Tanah 8
Emisi Metan (CH4) dan Dinitrogen Oksida (N2O) 9
Pertumbuhan Tanaman dan Hasil Panen 10
PEMBAHASAN 13
SIMPULAN DAN SARAN 17
Simpulan 17
Saran 18
DAFTAR PUSTAKA 18
LAMPIRAN 22
DAFTAR TABEL
1 Analisis sifat fisik kimia tanah pada petak perlakuan (P2) dan petak
kontrol (P1) sebelum penanaman tanaman padi 8
2 Komponen hasil panen pada perlakuan (P2) dengan pemberian pupuk NPK 20%, pemberian bakteri metanotrof serta O. anthropi dan pada kontrol (P1) yang diberikan pupuk NPK 100% dosis anjuran dengan
tanpa pemberian bakteri 13
DAFTAR GAMBAR
1 Skema siklus produksi metan pada lahan sawah 3
2 Siklus oksidasi metan dan asimilasi formaldehid 4 3 Siklus sumber N2O dan reduksi N2O pada lahan sawah 5
4 Laju akumulasi/penyerapan metan (CH4) 9
5 Laju akumulasi/penyerapan dinitrogen oksida (N2O) 10
6 Tinggi tanaman 10
7 Jumlah anakan per rumpun 11
8 Jumlah malai per rumpun 11
9 Warna daun 12
DAFTAR LAMPIRAN
1 Hasil analisis sifat fisik kimia tanah lahan sawah dataran rendah di Desa Citarik, Kec. Pelabuhan Ratu, Kab. Sukabumi, Jawa Barat 22
2 Kriteria penilaian sifat fisik kimia tanah 23
3 Analisis residu pestisida sebelum tanam dan sesudah panen lahan sawah dataran rendah di Desa Citarik, Kec. Pelabuhan Ratu, Kab.
PENDAHULUAN
Latar Belakang
Beras adalah kebutuhan pokok pangan utama untuk masyarakat di berbagai negara khususnya Indonesia, untuk memenuhi kebutuhan pokok tersebut perlu peningkatan produktivitas padi. Berbagai cara dilakukan secara intensif untuk meningkatkan produktivitas padi seperti pemupukan, perbaikan sistem irigasi, pengendalian hama dengan menggunakan pestisida kimia. Akan tetapi beberapa aplikasi tersebut dapat berdampak terhadap lingkungan, seperti penggunaan pupuk senyawa kimia berkontribusi terhadap penyebab pemanasan global.
Konsentrasi gas rumah kaca seperti karbondioksida (CO2), metan (CH4),
dan dinitrogen oksida (N2O) di atmosfir terus meningkat akibat dari aktivitas
manusia. Persentase peningkatan emisi gas rumah kaca mencapai 70% antara tahun 1970 hingga 2004 (IPCC 2007). Gas metan (CH4) mempunyai potensi
penyebab pemanasan global 23 kali lebih besar dibandingkan CO2. Gas N2O
memiliki potensi penyebab pemanasan global 298 kali lebih besar dibandingkan dengan CO2 (Millar et al. 2010).
Salah-satu solusi untuk mengatasi peningkatan emisi CH4 dan N2O yang
dihasilkan dari lahan persawahan dapat direduksi melalui proses oksidasi CH4 dan
reduksi N2O oleh bakteri metanotrof dan Ochrobactrum anthropi BL2. Hasil
penelitian terdahulu telah didapat empat isolat bakteri metanotrof terbaik dalam mengoksidasi CH4, yaitu isolat bakteri metanotrof BGM 1, BGM 3, BGM 9, dan
SKM 14 yang telah diisolasi oleh Hapsari (2008) di lahan persawahan Bogor dan Sukabumi. Keempat isolat tersebut telah diidentifikasi oleh Astuti (2009) sebagai Methylocystis rosea, M. parvus, Methylococcus capsulatus dan Methylobacter sp. demikian halnya dengan bakteri denitrifikasi telah diisolasi oleh Setyaningsih et al. (2010) dari lahan sawah di Belendung, Tangerang, Banten yang berpotensi dalam mereduksi emisi N2O. Bakteri isolat BL2 mampu mereduksi N2O sebanyak 5.41
μmol mL-1
. Berdasarkan analisis gen 16S rRNA, isolat tersebut teridentifikasi sebagai Ochrobactrum anthropi BL2.
Bakteri metanotrof dan O. anthropi BL2 telah diujicobakan sebagai agen pengoksidasi metan dan pereduksi N2O pada tanaman padi di rumah kaca Pusat
Penelitian Sumberdaya Hayati dan Bioteknologi (PPSHB) IPB dan rumah kaca Departemen Biologi, FMIPA, IPB (Muttaqin 2012). Selain itu isolat-isolat tersebut telah diujicobakan di lahan sawah dataran tinggi Desa Cicurug, Sukabumi Jawa-Barat. Pada percobaan tersebut, isolat-isolat tersebut mampu mereduksi CH4
dari lahan sawah hingga 20.47% jika dibandingkan dengan kontrol (Pingak et al. 2013; Sutanto et al. 2014). M. capsulatus BGM 9 dan Methylobacter sp. SKM 14 tidak hanya mampu mengoksidasi metan tetapi juga memiliki aktivitas nitrogenase, sehingga isolat tersebut memiliki kemampuan melakukan fiksasi N2
(Maisaroh 2009). Hadianta et al. (2014) melaporkan bahwa pertumbuhan tanaman padi dengan pemberian bakteri metanotrof lebih baik dibandingkan dengan kontrol yang diberi pupuk 100% sesuai rekomendasi. Kemampuan isolat M.
capsulatus BGM 9 dan Methylobacter sp. SKM 14 selain mampu mengoksidasi
2
tersebut berpotensi besar untuk dikembangkan sebagai agen hayati dalam pengendali gas rumah kaca di areal pertanian.
Tujuan Penelitian
Penelitian ini bertujuan untuk melihat efektivitas bakteri metanotrof dan
O. anthropi BL2 sebagai agen pengoksidasi metan dan pereduksi N2O serta
pemacu terhadap pertumbuhan padi pada lahan sawah di dataran rendah.
TINJAUAN PUSTAKA
Emisi Metan (CH4) dan Dinitrogen Oksida (N2O)
Gas rumah kaca adalah gas-gas di atmosfer yang memiliki kemampuan untuk menyerap radiasi matahari yang dipantulkan oleh bumi sehingga suhu bumi semakin meningkat yang menyebabkan suasana panas. Penyebab terjadinya efek rumah kaca adalah naiknya konsentrasi gas-gas rumah kaca, seperti karbondioksida (CO2), sulfur dioksida (SO2), nitrogen oksida (NO), dinitrogen
oksida (N2O), metan (CH4), dan klorofluorokarbon di atmosfer. Kenaikan
konsentrasi gas-gas tersebut disebabkan oleh kenaikan berbagai jenis pembakaran di permukaan bumi seperti pembakaran bahan bakar minyak (BBM), batu bara, dan bahan-bahan organik lainnya. Di Indonesia kontribusi terbesar GRK berasal dari karbondioksida, metan, dan dinitrogen oksida. Gas terbesar kedua dalam mempengaruhi pemanasan global adalah gas metan yang mayoritas berasal dari sektor pertanian (Rachman 2007).
Metan (CH4) merupakan salah satu gas rumah kaca utama yang dapat menyerap radiasi infra-merah sehingga berkontribusi terhadap pemanasan global. Gas metan mempunyai potensi pemanasan global 23 kali lebih besar dibanding karbondioksida. Sumber metan terutama dari lahan sawah, dengan sistem irigasi pada kegiatan pertanian menyediakan lingkungan ideal untuk proses metanogenesis. Hal tersebut terjadi akibat dari tingginya input karbon mudah terlapuk, kondisi anaerobik akibat tergenang, dan suhu optimum untuk bakteri penghasil metan (Venterea et al. 2005). Emisi metan pada lahan sawah tiap tahunnya mampu melepaskan emisi metan sebanyak 5-150 Tg/tahun (Jean 2001). Gas metan dihasilkan oleh bakteri matanogen dan arkhea. Bakteri metanogen menggunakan H2 ataupun asetat sebagai sumber energi, CO2 sebegai sumber
karbon untuk mengahasilkan gas metan. H2 dan asetat adalah hasil fermentasi
3
Gambar 1 Skema siklus produksi metan pada lahan sawah (Juottonen 2008)
Tipe siklus metanogen terdiri atas tiga: (1) Hidrogenetrophic methanogens: pada siklus tersebut H2 sebagai donor elektron sedangkan karbondioksida (CO2)
sebagai akseptor elektron, namun ada beberapa menggunakan format sebagai donor elektron. (2) Acetolastic methanogens: pada siklus tersebut senyawa asetat diubah menjadi metil dan grup karbonil, kemudian grup karbonil dioksidasi menjadi CO2, kemudian CO2 direduksi menjadi grup metil. Selanjutnya grup metil
diubah menjadi metan (CH4). (3) Methylotrophic methanogens: mikrob penghasil
metan mampu tumbuh pada senyawa metil seperti metanol, metilamin, dan metil sulpida. Ketiga senyawa tersebut mampu digunakan oleh mikrob penghasil metan sebagai donor elektron maupun akseptor elektron (Deppenmeier 2002). Gas selain metan dalam mempengaruhi pemanasan global adalah gas N2O yang juga berasal
dari sektor pertanian, salah-satunya adalah lahan sawah.
Gas N2O dapat meningkatkan suhu bumi 296 kali dibanding karbondioksida
(CO2) (IPCC 2007). Peningkatan gas N2O akibat dari pemberian pupuk senyawa
kimia yang memiliki kandungan karbon tinggi serta mudah termineralisasi sehingga meningkatkan biomassa mikrob yang meningkatkan emisi N2O.
Intensitas dan besarnya emisi N2O dari tanah ditentukan oleh beberapa faktor
yaitu suhu, curah hujan, kelembaban tanah, kandungan karbon mudah termineralisasi yang berjumlah atom karbon rendah sebagai donor elektron pada proses reduksi (Arth dan Frenzel 2000) (Gambar 3).
Emisi N2O sebagai salah-satu dampak dari pemberian pupuk senyawa kimia
pada lahan pertanian. Emisi tersebut dapat terjadi melalui dua cara, emisi langsung dan tak langsung. Emisi langsung N2O didefinisikan sebagai emisi N2O
dari tanah di lahan pertanian yang telah diberikan pupuk senyawa kimia, sedangkan hanyutan pupuk senyawa kimia pada badan air atau tanah di sekitar lahan pertanian yang menyebabkan terbentuknya emisi N2O disebut sebagai emisi
N2O tak langsung (Millar et al. 2010).
Tanaman padi salah-satu media untuk melepaskan gas metan (CH4) dan
4
tersebut dilepaskan melalui pembuluh aerenkima daun, batang dan akar padi. Metan akan dilepaskan melalui pori-pori mikro pada pelepah daun bagian bawah. Jumlah akar dan jumlah anakan juga mempengaruhi emisi CH4, makin banyak
jumlah akar yang terbentuk maka emisi CH4 makin tinggi pula. Jumlah anakan
juga merupakan faktor penentu besarnya pelepasan CH4. Semakin banyak anakan
maka kerapatan dan jumlah pembuluh aerinkima meningkat sehingga pelepasan metan juga meningkat (Wihardjaka 2001).
Bakteri Metanotrof
Bakteri metanotrof termasuk bakteri aerob obligat yang dapat menggunakan metan sebagai sumber karbon dan energi untuk pertumbuhannya (Roslev dan King 1994). Bakteri metanotrof dapat ditemukan pada bagian permukaan sawah yang bersifat aerob. Metan (CH4) pada lahan sawah dapat dioksidasi oleh bakteri
metanotrof sebab bakteri tersebut merupakan satu-satunya sistem biologi yang berperan sebagai penampung metan (Dubey 2005) dan telah disebutkan oleh Dedysh et al.(2005) bahwa bakteri metanotrof memiliki peran kunci dalam siklus metan di dunia. Bakteri metanotrof menggunakan metan dan methanol. Bakteri metanotrof merupakan subset dari metilotrof. Metilotrof didefinisikan sebagai kelompok bakteri dan arkaea yang mampu menggunakan substrat komponen C1
seperti CO2 dan CH4. Bakteri metanotrof mampu mengubah metan menjadi CO2
melalui proses oksidasi dengan menggunakan metan monooksigenase (MMO), oksidasi metan dapat terjadi pada lingkungan mikro yang bersifat aerob pada zona perakaran dan pada bagian yang bersifat toksik pada lapisan permukaan tanah (Semrau et al. 2010). Siklus oksidasi metan dan asimilasi formaldehid oleh bakteri metanotrof tergantung dari tipe bakteri tersebut (Gambar 2).
Gambar 2 Siklus oksidasi metan dan asimilasi formaldehid (Hanson dan Hanson 1996)
5 contoh tipe II ialah Methylocinus dan Methylocystis, dan contoh tipe X ialah Methylococcus capsulatus. Bakteri metanotrof tipe II dan tipe X memiliki kemampuan untuk memfiksasi N2. Fiksasi nitrogen ialah proses penambatan
nitrogen bebas yang diubah menjadi amonium sehingga dapat dimanfaatkan sebagai sumber nitrogen oleh tanaman, karena kemampuan fiksasinya maka dapat diaplikasikan pada lingkungan yang jumlah nitrogennya terbatas (Hanson dan Hanson 1996; Macalady et al. 2002).
Oksidasi metan merupakan tahap awal penggunaan metan sebagai sumber karbon dan energi untuk pertumbuhan bakteri metanotrof. Semakin tinggi aktivitas oksidasi metan maka semakin rendah kadar gas metan tersisa pada bagian headspace kultur. Isolat-isolat bakteri metanotrof yang memiliki aktivitas oksidasi metan yang tinggi, berpotensi untuk dikembangkan sebagai agen pengoksidasi metan di lahan sawah. Isolat-isolat bakteri metanotrof yang memiliki kemampuan fiksasi nitrogen yang tinggi berpotensi untuk dikembangkan sebagai agen pupuk hayati pada lahan sawah. Kombinasi kedua jenis bakteri metanotrof tersebut dapat dikembangkan sebagai agen pengoksidasi metan sekaligus pupuk hayati pada lahan sawah karena kemampuannya yang dapat menfiksasi nitrogen (Margareth 2011).
Bakteri Pereduksi Gas Dinitrogen Oksida (N2O)
Bakteri pereduksi gas N2O dapat tumbuh dengan menggunakan N2O karena
N2O sebagai akseptor elektron. Salah-satu bakteri pereduksi gas N2O ialah
Ochrobactrum anthropi. Ochrobactrum anthropi termasuk ke dalam subdivisi
beta bakteri ungu, bersifat motil, tidak berpigmen dan peritrik. Bakteri ini merupakan jenis bakteri Gram negatif, bersifat aerob, dan kemoorganotrof (Shapleigh 2006). Pemberian pupuk nitrogen pada lahan persawahan dan kelebihan atau hanyutannya menuju lingkungan perairan lain berpotensi sebagai sumber N2O melalui proses denitrifikasi oleh mikroorganisme (Dong et al. 2009).
Hasil penelitian Mulvaney et al. (1997) juga menyatakan bahwa proses denitrifikasi dan emisi N2O dipengaruhi oleh sumber N. Seperti pupuk Urea
menyebabkan proses denitrifikasi yang lebih tinggi dibanding dengan amonium sulfat seperti yang telah dilakukan pada studi rumah kaca dengan tanah tergenang. Kelimpahan gas rumah kaca N2O dapat dikendalikan oleh O. athropi melalui
proses reduksi N2O (Gambar 3).
6
Produksi N2O dapat terjadi melalui proses nitrifikasi (oksidasi amonia),
disimilasi nitrat (denitrifikasi dan nitrat amonifikasi). Nitrifikasi adalah proses pembentukan senyawa nitrat dari senyawa amonium. Proses ini terjadi dari ion amonium dioksidasi menjadi ion nitrit, lalu ion nitrit menjadi ion nitrat. Bakteri yang berperan dalam proses nitrifikasi adalah kelompok bakteri yang mampu menkonversi nitrat dari senyawa amonia yang umumnya bersifat aerob, bakteri tersebut bersifat kemolitotrof (menggunakan senyawa anorganik), bersifat non motil. Proses nitrifikasi berlangsung dalam dua tahapan: (1) Nitritasi, oksidasi amonia menjadi nitrit (2NH3+3O2 2HNO2 + 2H2O) oleh bakteri nitrit, contoh
Nitrosomonas. (2) Nitratasi, oksidasi senyawa nitrit menjadi nitrat (2HNO2 +
O2 2HNO3) oleh bakteri nitrat, contoh Nitrobacter yang bersifat autotrof
(Elizabeth dan Baggs 2011).
Proses denitrifikasi merupakan proses pengubahan nitrat (NO3-) menjadi
bentuk nitrogen yang lebih tereduksi, yaitu NO2-, NO, N2O, dan N2. Di antara
bentuk nitrogen tereduksi tersebut, N2O dan N2 kemudian diemisikan menuju
atmosfer. Rasio emisi N2O menuju atmosfer dipengaruhi oleh pH di mana terjadi
peningkatan emisi N2O ketika terjadi penurunan pH, contoh bakteri yang berperan
pada proses denitrifikasi alah Pseudomonas, Bacillus dan Paracoccus (Cuhel et al. 2010).
Proses nitrat amonifikasi merupakan konversi asam amino (hasil deaminasi) menjadi amonia (NH3), selanjutnya amonia pada tanah yang lembab terlarut
dalam air dan membentuk ion ammonium (NH4) (Elizabeth dan Baggs 2011).
METODE
Waktu dan Tempat
Penelitian dilaksanakan mulai bulan Juni 2014 – Maret 2015. Tahap peremajaan bakteri metanotrof dan O. anthropi BL2 bertempat di Laboratorium Mikrobiologi, Departemen Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Penanaman padi dilakukan di lahan persawahan dataran rendah di Desa Citarik, Kecamatan Pelabuhan Ratu, Kabupaten Sukabumi, Jawa-Barat.
Bahan
Mikroorganisme yang digunakan ialah bakteri metanotrof meliputi M. rosea BGM 1, M. parvus BGM 3, M. capculatus BGM 9, Methylobacter sp. SKM 14, bakteri pereduksi N2O O. anthropi BL2, dan bibit padi varietas IR64.
Prosedur Penelitian
7 (takaran 20% dari dosis anjuran) serta penambahan bakteri metanotrof dan bakteri pereduksi N2O.
Tahap Peremajaan Isolat
Isolat bakteri metanotrof M. rosea BGM 1, M. parvus BGM 3, M. capculatus BGM 9, dan Methylobacter sp. SKM 14 diremajakan pada media agar Nitrate Mineral Salt (NMS) + 1% metanol, kemudian diinkubasi pada suhu ruang selama 3-7 hari. Isolat bakteri pereduksi N2O O. anthropi BL2 diremajakan pada
media denitrifikasi, kemudian diinkubasi pada suhu ruang selama 3-7 hari. Isolat bakteri metanotrof hasil peremajaan masing-masing dikultur dalam media cair NMS + 1% metanol dan bakteri pereduksi N2O pada media cair denitrifikasi,
kemudian diinkubasi pada inkubator bergoyang dengan kecepatan 100 rpm pada suhu ruang sehingga diperoleh kultur dengan konsentrasi sel minimal 1x106 sel/ml.
Tahap Pengolahan Lahan Sawah dan Penyiapan Bibit
Lahan sawah digarap sekitar 3-5 hari. Padi varietas IR64 dikecambahkan dengan kondisi lembab dan gelap selama 24 jam. Setelah berkecambah padi disemai di sawah selama 20 hari hingga bibit padi tumbuh. Setelah bibit padi tumbuh, bibit padi siap untuk ditanam.
Tahap Penanaman dan Inokulasi Bakteri Metanotrof
Petak sawah berukuran 1000 m2 dengan jarak tanam 25 25 cm. Untuk
perlakuan (P2), bibit padi direndam pada kultur bakteri metanotrof dan
O. anthropi BL2 dengan konsentrasi sel bakteri minimal 1x106 sel/ml selama
15-30 menit sebelum ditanam. Kontrol (P1) tidak direndam pada kultur bakteri metanotrof dan O. anthropi BL2 sebelum penanaman. Pemberian pupuk NPK (nitrogen, fosfat, kalium) masing-masing diberikan pada waktu 21 hari setelah tanam. Pemberian pupuk NPK tersebut diberikan pada tanaman perlakuan (P2) dan kontrol (P1) untuk melihat pengaruhnya terhadap peningkatan pertumbuhan dan produktivitas antara dosis 20% dan dosis 100%.
Tahap Pemasangan Sungkup
Sungkup berukuran 55.5x89x89 cm3 masing-masing dipasang pada petak perlakuan (P2) dan petak kontrol (P1). Pemasangan sungkup dilakukan pada waktu 20 hari setelah tanam. Sungkup tersebut dilengkapi dengan kipas agar sampel gas yang diambil dalam kondisi homogen. Sungkup tersebut berfungsi sebagai penampung gas.
Tahap Pemeliharaan dan Parameter yang Diamati
Pengamatan pertumbuhan padi dan pengambilan gas CH4 dan N2O diamati
8
Pengambilan gas metan CH4 dan N2O dilakukan dengan menggunakan
sungkup tertutup. Sampel gas sebanyak 100 ml diambil dengan menggunakan
syringe dan dimasukkan ke dalam tabung vakum. Sampel gas diambil pada saat
Pengambilan sampel lumpur sawah diambil dan dimasukkan ke dalam wadah plastik sebanyak 2 wadah yang berasal dari petak Kontrol (P1) dan perlakuan (P2). Kedua sampel tersebut dianalisis di Laboratorium Tanah, Balai Penelitian Tanah BB SDLP, Badan Litbang Pertanian, Jl. Ir. H. Juanda No. 98 Bogor.
HASIL
Analisis Sifat Fisik dan Kimia Tanah
Kondisi sifat fisik dan kimia tanah pada lahan sawah di Desa Citarik, Kecamatan Pelabuhan Ratu, Kabupaten Sukabumi, Jawa-Barat memiliki tekstur tanah lempung liat berpasir baik pada petak perlakuan maupun pada petak kontrol. Analisis sifat fisik dan kimia tanah dilakukan sebelum penanaman padi, yang berarti sebelum pemberian bakteri maupun pemberian pupuk NPK (Tabel 1 Lampiran 1)
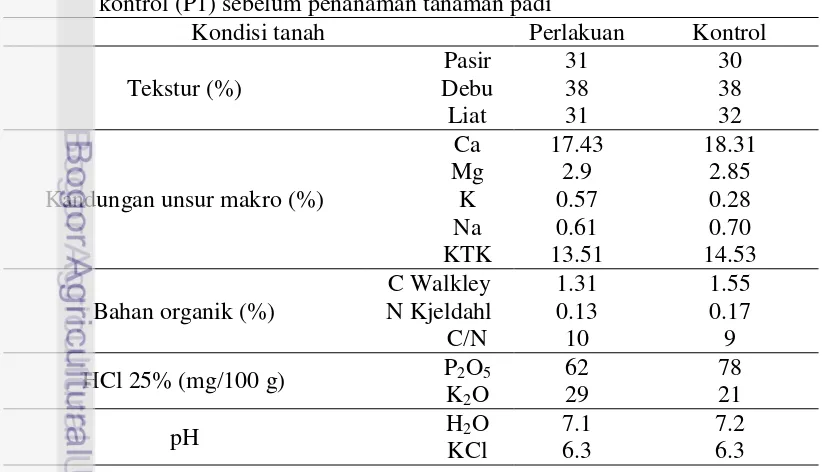
Tabel 1 Analisis sifat fisik kimia tanah pada petak perlakuan (P2) dan petak kontrol (P1) sebelum penanaman tanaman padi
Kondisi tanah Perlakuan Kontrol
9
Emisi Metan (CH4) dan Dinitrogen Oksida (N2O)
Pelepasan emisi metan pada pengamatan 21, 42, 63, dan 84 hari setelah tanam pada kontrol yang tanpa pemberian bakteri metanotrof menunjukkan nilai akumulasi tertinggi 7.43 mol CH4/hari/m2, sedangkan pada perlakuan dengan
pemberian bakteri metanotrof M. rosea BGM 1, M. parvus BGM 3, M. capculatus BGM 9, dan Methylobacter sp. SKM 14 menunjukkan penggunaan metan (sink) paling rendah sebesar 0.13 mol CH4/hari/m2 (Gambar 4)
Gambar 4 Emisi metan (CH4) pada perlakuan (P2) dengan pemberian pupuk
NPK 20%, pemberian bakteri metanotrof serta O. anthropi BL2 dan pada kontrol (P1) yang diberikan pupuk NPK 100% dosis anjuran dengan tanpa pemberian bakteri di lahan sawah dataran rendah
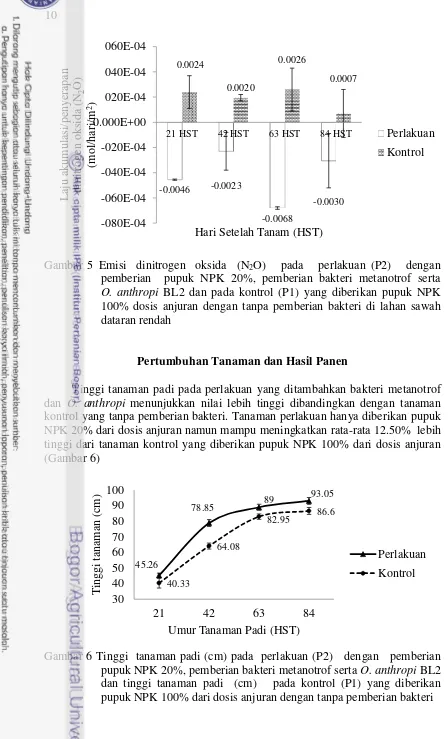
Emisi pada perlakuan dengan pemberian bakteri metanotrof dan O. anthropi BL2 pada umur 21, 42, 63, dan 84 hari setelah tanam menunjukkan nilai negatif yang berarti digunakan (sink) paling rendah sebesar 0.0023 mol N2O/hari/m2
sedangkan pada kontrol menunjukkan pelepasan emisi N2O dengan nilai tertinggi
10
Tinggi tanaman padi pada perlakuan yang ditambahkan bakteri metanotrof
dan O. anthropi menunjukkan nilai lebih tinggi dibandingkan dengan tanaman
kontrol yang tanpa pemberian bakteri. Tanaman perlakuan hanya diberikan pupuk NPK 20% dari dosis anjuran namun mampu meningkatkan rata-rata 12.50% lebih tinggi dari tanaman kontrol yang diberikan pupuk NPK 100% dari dosis anjuran (Gambar 6)
Gambar 6 Tinggi tanaman padi (cm) pada perlakuan (P2) dengan pemberian pupuk NPK 20%, pemberian bakteri metanotrof serta O. anthropi BL2 dan tinggi tanaman padi (cm) pada kontrol (P1) yang diberikan pupuk NPK 100% dari dosis anjuran dengan tanpa pemberian bakteri
11 Jumlah anakan per rumpun pada tanaman perlakuan yang diberikan bakteri metanotrof dan O. anthropi menunjukkan peningkatan rata-rata sebesar 23.76% jika dibandingkan dengan jumlah anakan per rumpun pada tanaman kontrol yang tanpa pemberian bakteri. Peningkatan jumlah anakan per rumpun pada tanaman perlakuan dan tanaman kontrol meningkat hingga hari 42 HST. Pada hari ke-63 HST dan 84 HST tidak terjadi peningkatan jumlah anakan per rumpun sebab pada waktu tersebut telah memasuki fase generatif (Gambar 7)
Gambar 7 Jumlah anakan tanaman padi per rumpun pada perlakuan (P2) dengan pemberian pupuk NPK 20%, pemberian bakteri metanotrof serta
O. anthropi BL2 dan jumlah anakan per rumpun pada kontrol (P1)
yang diberikan pupuk NPK 100% dosis anjuran dengan tanpa pemberian bakteri
Jumlah malai per rumpun mulai muncul pada umur 63 hari setelah tanam dan terus meningkat hingga umur 84 hari setelah tanam. Jumlah malai per rumpun pada tanaman perlakuan dengan pemberian bakteri metanotrof dan O. anthropi menunjukkan 16.49% lebih tinggi dibandingkan dengan tanaman kontrol. (Gambar 8)
12
Warna hijau daun merupakan salah-satu indikasi tingkat kesuburan tanaman, pada tanaman kontrol rata-rata skor warna hijau daun terlihat lebih rendah dibandingkan dengan skor warna hijau daun pada tanaman perlakuan. Peningkatan skor warna hijau daun pada tanaman perlakuan rata-rata meningkat sebesar 35.92% dari tanaman kontrol pada setiap pengamatan, meskipun pada tanaman perlakuan hanya diberikan pupuk NPK 20% dari dosis anjuran
Komponen hasil panen pada perlakuan dengan pemberian bakteri dan pupuk NPK 20% dari dosis anjuran menunjukkan peningkatan dibandingkan dengan komponen hasil panen pada kontrol dengan pemberian pupuk NPK 100% dari dosis anjuran dan tanpa pemberian bakteri. Rata-rata bobot kering tajuk (g) pada perlakuan meningkat sebesar 67.60% dibandingkan dengan kontrol. Bobot kering akar (g) juga mengalami peningkatan sebesar 143.32% dibandingkan dengan kontrol. Panjang akar (cm) pada perlakuan meningkat 37.05%, dibandingkan dengan kontrol. Malai produktif meningkat 24.46% pada perlakuan dibandingkan dengan kontrol. Selain itu butir per malai (butir) dan bobot 1000 butir (g) menunjukkan peningkatan sebesar 48.28% dan 42.07% dibandingkan dengan kontrol, sedangkan butir hampa pada tanaman perlakuan mangalami penurunan dibandingkan dengan butir hampa tanaman kontrol (Tabel 2)
13 Tabel 2 Komponen hasil panen pada perlakuan (P2) dengan pemberian pupuk NPK 20%, pemberian bakteri metanotrof serta O. anthropi BL2 dan pada kontrol (P1) yang diberikan pupuk NPK 100% dosis anjuran dengan tanpa pemberian bakteri. Waktu panen 98 hari setelah tanam
Bobot
Perlakuan 45.32±4.5 17.86±1.8 23.3±0.7 17.3±1.2 72.91±5.6 30.19±1.8 2.65±1.2
Kontrol 27.04±2.91 7.34±1.07 17±1.15 13.9±1.4 49.17±3.8 21.25±0.9 9.49±3.5
Keterangan: ±Standar Error
PEMBAHASAN
Sifat fisik kimia tanah pada petak perlakuan dan petak kontrol memiliki kisaran nilai yang hampir sama. Berdasarkan kriteria penilaian sifat fisik kimia tanah (Lampiran 2) menurut BPT (2009) petak sawah kontrol dan perlakuan memiliki sifat fisik kimia tanah yang sama kecuali kalium (K). Kalium (K) pada petak perlakuan tergolong sedang dan pada petak kontrol tergolong rendah. Sifat fisik kimia tanah yang lainnya memiliki kriteria yang sama yaitu tekstur tanah tergolong tanah lempung liat berpasir. Unsur makro; kandungan kalsium (Ca) tinggi, magnesium (Mg) tinggi, natrium (Na) sedang, kapasitas tukar kation (KTK) rendah. Bahan organik; karbon (C) walkley rendah, nitrogen (N) kjeldahl rendah, rasio C/N rendah. Asam klorida (HCl) 25%; fosfat pentoksida (P2O5)
sangat tinggi, potasium oksida (K2O) sedang dan pH; air (H2O) bersifat netral,
kalium klorida (KCl) agak masam. Keseragaman sifat fisik dan kimia tanah pada petak perlakuan (P2) dan petak kontrol (P1) mengindikasikan bahwa hasil pengamatan baik laju emisi gas CH4, N2O, pertumbuhan tanaman, dan hasil
produktivitas telah memenuhi standar, untuk dapat dibandingkan antara satu parameter dengan parameter lainnya.
Emisi pada pengamatan umur 21, 42, 63, dan 84 hari setelah tanam, pada petak kontrol (P1) yang tanpa pemberian bakteri melepaskan emisi metan dengan nilai tertinggi 7.43 CH4 mol/hari/m2. Pada perlakuan (P2) yang diberi bakteri
metanotrof dan O. anthropi BL2 menurunkan emisi metan tertinggi sebanyak 2.40 CH4 mol/hari/m2 pada 21 HST (Gambar 4). Nilai negatif pada perlakuan
menunjukkan bahwa bakteri metanotrof M. rosea BGM 1, M. parvus BGM 3, M. capculatus BGM 9, dan Methylobacter sp. SKM 14 menggunakan metan sebagai sumber karbon dan energi dalam pertumbuhannya sehingga terjadi penurunan pelepasan CH4. Penggunaan CH4 oleh bakteri metanotrof direduksi dengan cara
mengoksidasi CH4.
Oksidasi metan oleh bakteri metanotrof pada hasil penelitian yang lain sebanyak 0.469 mol/hari/m2 (Pingak et al. 2014) dan 1.672 g/mol/hari/m2
14
M. rosea BGM 1, M. parvus BGM 3, M. capculatus BGM 9 and, Methylobacter
sp. SKM 14 mampu mengoksidasi metan dengan nilai berturut-turut 969.62 mol/hari, 4186.25 mol/hari, 66556.82 mol/hari dan, 25654 mol/hari (Hapsari 2008).
Gas metan dapat dihasilkan melalui proses metanogenesis oleh bakteri metanogen atau penghasil metan. Proses metanogenesis terjadi dalam kondisi anaerob akibat tergenangnya air dan suhu optimum (Venterea et al. 2005). Bakteri metanogen mendapatkan sumber energi berupa H2 ataupun asetat, dan CO2
sebagai sumber karbon. H2, asetat dan CO2 dihasilkan oleh bakteri anaerob yang
mampu menfermentasikan senyawa organik yang berasal dari eksudat akar tanaman padi. Asetat, H2, dan CO2 merupakan senyawa yang dapat dimanfaatkan
oleh bakteri metanogen sebagai sumber karbon dan energi (Jean dan Roger 2001). Metan (CH4) pada lahan sawah dapat dioksidasi oleh bakteri metanotrof
sebab bakteri tersebut merupakan bakteri yang menggunakan senyawa C1 sebagai
sumber energi, sehingga disebutkan bahwa bakteri metanotrof merupakan penampung (sink) metan (Dubey 2005). Dedysh et al. (2005) menyatakan dalam artikelnya bahwa bakteri metanotrof memiliki peranan penting dalam siklus metan di dunia. Bakteri metanotrof mampu mengubah metan menjadi sumber karbon dan energi untuk pertumbuhannya melalui proses oksidasi dengan menggunakan enzim metan monooksigenase (MMO) (Semrau et al. 2010). Oksidasi metan oleh bakteri metanotrof terdiri dari dua jalur biosintesis yakni jalur serin dan jalur formal dehid atau jalur RuMP. Kedua jalur biosintesis tersebut tergantung dari tipe bakteri metanotrof. Methylococcus termasuk tipe X,
Methylobacter termasuk bakteri metanotrof tipe I, dan Methylocystis termasuk
bakteri metanotrof tipe II (Hanson dan Hanson 1996).
Bakteri yang digunakan adalah Methylocystis rosea BGM 1, M. parvus BGM 3 termasuk bakteri metanotrof tipe II, sehingga proses biosintesis bakteri tersebut menggunakan jalur serin. Enzim yang berperan dalam jalur serin ialah
hydroxymethyl transferase (STHM), hydroxypyruvate reductase (HPR), malate
thiokinase (MTK), dan malyl coenzyme A lyase (MCL). Reaksi keseluruhan dan hasil akhir dari jalur tersebut ialah:
Methylococcus capculatus BGM 9 termasuk tipe X dan Methylobacter sp.
SKM 14 termasuk bakteri metanotrof tipe I, proses biosintesis bakteri metanotrof tipe X dan tipe I memiliki jalur biosintesis yang sama yakni jalur RuMP. Enzim yang berperan dalam jalur RuMP ialah hexulose-6-phosphate synthase dan hexulose phosphate isomerase. Reaksi keseluruhan dan hasil akhir dari jalur tersebut ialah:
Demikian halnya dengan dinitrogen oksida (N2O) yang menunjukkan
pelepasan emisi dinitrogen oksida (N2O) pada kontrol (P1) di setiap waktu
N2O reduktase yang mampu mereduksi N2O menjadi N2. Dinitrogen oksida (N2O)
15 N2O yang mampu direduksi oleh O. anthropi BL 2 pada penelitian lainnya
sebanyak 127.19 µmol/hari/m2 (Pingak et al. 2014), sedangkan dalam kondisi in
vitro O. anthropi BL 2 mampu mereduksi N2O dengan mencapai 5.41 μmol/ mL
(Setyaningsih et al. 2010). Setyaningsih et al. (2010) telah mengidentifikasi bakteri pereduksi dinitrogen oksida yang berpotensi sebanyak tiga galur antara-lain O. anthropi BL 1, O. anthropi BL 2, dan O. anthropi BLN 1. Pada kondisi lapang O. anthropi BL 1 mampu mereduksi N2O sebanyak 0.26 µmol/mL/jam
sedangkan O. anthropi BLN 1 mampu mereduksi N2O sebanyak 0.43
µmol/mL/jam pada lahan sawah (Setyaningsih et al. 2013).
N2O dihasilkan melalui beberapa jalur biosintesis diantaranya ialah proses
nitrat amonifikasi, nitrifikasi, dan nitrifier denitrifikasi (Gambar 3). Salah-satu pemicu meningkatnya emisi N2O karena pemberian pupuk senyawa kimia pada
lahan persawahan atau ada hanyutannya menuju lingkungan, sehingga berpotensi sebagai sumber N2O (Dong et al. 2009). Bakteri penghasil N2O menggunakan
senyawa N dari pupuk senyawa kimia tersebut sebagai sumber energinya dan menghasilkan hasil samping berupa N2O.
Nilai negatif pada perlakuan (P2) mengindikasikan terjadinya penurunan emisi N2O. Hal tersebut membuktikan bahwa O. anthropi BL2 mampu mereduksi
N2O menjadi N2 oleh enzim N2O reduktase sehingga dapat memenuhi kebutuhan
sel O. anthropi BL2 dalam pertumbuhannya. Shapleigh (2006) mangatakan dalam hasil penelitiannya bahwa O. anthropi merupakan jenis bakteri Gram negatif yang mampu mereduksi N2O melalui proses denitrifikasi (Gambar 3).
Kemampuan O. anthropi BL 2 dan bakteri metanotrof dalam mereduksi N2O dan mengoksidasi CH4 memiliki peran yang sangat penting terhadap
penurunan gas rumah kaca penyebab pemanasan global. Bakteri metanotrof tidak hanya berperan dalam penurunan gas rumah kaca namun juga mampu mereduksi residu pestisida melalui proses oksidasi. Bakteri metanotrof mampu mereduksi senyawa residu pestisida melalui proses oksidasi karena bakteri tersebut mampu menggunakan senyawa C1 sebagai sumber energi, contoh senyawa pestisida yang
struktur kimianya C1 ialah karbofuran. Proses penelitian ini juga dilakukan
pengamatan tambahan mengenai analisis residu pestisida sebelum tanam dan sesudah panen baik pada petak kontrol (P1) maupun pada petak perlakuan (P2). Pada perlakuan yang menggunakan bakteri metanotrof dan O. anthropi BL 2 mengalami penurunan senyawa klorpirifos setelah panen, sedangkan senyawa profenofos dan karbofuran tidak terjadi penurunan (Lampiran 3). Terjadinya peningkatan nilai profenofos dan karbofuran karena dalam penelitian tersebut tidak dilakukan pemberian pestisida selama pemeliharaan tanaman padi.
Penurunan konsentrasi residu pestisida klorpirifos kemungkinan disebabkan oleh penambahan bakteri metanotrof dan Ochrobactrum anthropi BL 2 pada lahan sawah. Wang et al. (2007) melaporkan bahwa penurunan konsentrasi klorpirifos pada tanah terjadi akibat adanya adsorpsi dan degradasi oleh bakteri. Proses degradasi profenofos terjadi karena reaksi-reaksi hidrolisis, fotolisis, dan aktivitas mikrob (Chaurasia 2014). Sedangkan karbofuran dapat terdegradasi melalui proses hidrolisis, proses kimia dan mikrob (Seo et al. 2007). Karbofuran merupakan senyawa C1 yang mampu digunakan oleh bakteri metanotrof sebagai
16
Keefektivitasan bakteri metanotrof dalam memacu pertumbuhan tanaman padi dapat dilihat pada peningkatan tinggi tanaman (cm) (Gambar 6), jumlah anakan per rumpun (Gambar 7), jumlah malai per rumpun (Gambar 8) dan skor warna hijau daun (Gambar 9). Pada perlakuan (P2) masing-masing meningkat sebesar 12.50%, 23.76%, 16.49%, dan 35.92% dibandingkan tanaman kontrol (P1). Kecukupan pupuk NPK pada warna hijau daun dilihat hingga batas umur 42 HST, karena pada umur 63 dan 84 HST warna daun mulai menguning sebab nutrisinya digunakan untuk pengisian malai, serta aktivitas laju fotosintesis menurun. Demikian pula hasil panen pada perlakuan (P2) mengalami peningkatan hasil dibandingkan dengan kontrol (P1) (Tabel 2).
Bobot 1000 butir (g) pada perlakuan meningkat sebesar 42.07% dibandingkan tanaman kontrol. Hasil penelitian yang lain melaporkan bobot 1000 butir (g) pada metode konvensional meningkat sebesar 2.51% (Cepy dan Wangiyana 2011). Produktivitas hasil panen pada tanaman perlakuan (P2) dan tanaman kontrol (P1), jika diestimasikan dalam ton/hektar sebanyak 9.45 ton/ha pada tanaman perlakuan, sedangkan produktivitas pada tanaman kontrol sebanyak 3.84 ton/ha.
Peningkatan persentase pertumbuhan tanaman padi dan persentase komponen hasil panen pada perlakuan (P2), lebih baik dibandingkan kontrol (P1) meskipun pemberian pupuk NPK (15:15:15) pada perlakuan hanya 20% dari dosis anjuran, dibandingkan kontrol yang diberikan pupuk NPK (15:15:15) 250 kg/ha (takaran 100% pupuk dosis anjuran) (Permentan 2007). Pupuk NPK pada kontrol tidak dimanfaatkan seluruhnya tetapi mengalami proses pencucian (bleaching), oleh sebab itu pertumbuhan dan hasil panen pada kontrol lebih kerdil. Duan et al. (2007) menyatakan dalam penelitiannya bahwa tanaman mengambil 30-70% selebihnya terbuang karena mengalami proses pencucian.
Peningkatan hasil pertumbuhan dan komponen hasil panen pada perlakuan (P2) dibandingkan dengan kontrol (P1), karena pada perlakuan diberikan bakteri metanotrof dan Ochrobactrum anthropi BL2. Bakteri metanotrof M. rosea BGM 1, M. capculatus BGM 9 dan Methylobacter sp. SKM 14 selain kemampuannya dapat mengoksidasi metan juga memiliki kemampuan untuk memfiksasi nitrogen (N2). Kemampuan menfiksasi nitrogen (N2) karena M. rosea BGM 1, M.
capculatus dan Methylobacter sp. memiliki gen nif HDK yang mengkodekan
enzim-enzim nitrogenase (Hanson dan Hanson 1996). M. capculatus BGM 9 dan Methylobactersp. SKM 14 memiliki kemampuan dalam mengakumulasi amonia sebanyak sebanyak 47 µM dan 15 µM dalam kondisi in vitro (Sagala 2009), namun jika kultur bakteri M. rosea BGM 1 dicampur dengan kultur bakteri
Methylobacter sp. SKM 14 kemampuan aktivitas nitrogenasenya 11.27
μmol/jam/mL dalam kondisi in vitro (Chatrina 2010).
17 bertambahnya jumlah anakan. Semakin banyak jumlah anakan maka semakin banyak jumlah malai dan jumlah bulir juga semakin meningkat.
Macalady et al. (2002) menyatakan dalam laporan hasil penelitiannya bahwa fiksasi nitrogen ialah proses penambatan nitrogen bebas yang diubah menjadi amonium yang akan dikonversi menjadi asam amino, asam nukleat, dan protein. Hasil konversi dapat dimanfaatkan untuk pertumbuhan tanaman. Nitrogen berperan sebagai penyusun klorofil yang terlibat dalam proses fotosintesis sehingga meningkatkan jumlah butir padi yang produktif, meningkatkan persentase protein, dan berperan dalam penyusunan komponen penting organ tanaman (Chaturvedi 2005; Netto et al. 2005; Watanabe dan Kitagawa 2000).
Fiksasi nitrogen terjadi melalui proses nitrogenase dengan penguraian 1 mol N2 menjadi 2NH3 yang melibatkan 16 ATP jika Fe dalam kondisi teroksidasi
sebab butuh 4 ATP untuk mengaktifkan 2H dalam mereduksi Fe, jika dalam
kondisi tereduksi butuh 12 ATP. Nitrogenase kompleks terjadi karena adanya enzim yang terdiri dari 2 protein yaitu Fe protein dan MoFe protein. Enzim nitrogenase sensitif terhadap oksigen, meskipun bakteri M.capsulatus BGM 9 dan
Methylobacter sp SKM 14 bersifat aerob, bakteri ini tetap mampu menfiksasi
nitrogen dengan cara mempercepat laju respirasinya, sehingga kadar oksigen dalam sitoplasma sedikit. Reaksi terjadi ketika nitrogen (N2) mengikat kompleks
enzim MoFe protein. Pertama-tama Fe protein tereduksi oleh elektron feredoxin kemudian Fe protein tereduksi mengikat ATP lalu mereduksi MoFe protein, yang selanjutnya menjadi donor e- bagi N2 untuk memproduksi HN=NH, dua siklus
selanjutnya masing-masing membutuhkan e- dari feredoxin untuk memproduksi HN=NH H2N-NH2,H2N-NH2 2NH3. Reaksinya dapat dituliskan N2 + 6e- +
6H + 12 ATP 2NH3 + 12 ADP + 12 pi (Moat et al 2002). Berdasarkan hasil
penelitian ini, maka bakteri metanotrof Methylocystis rosea BGM 1, M. parvus BGM 3, Methylococcus capculatus BGM 9, Methylobacter sp. SKM 14 dan
Ochrobactrum anthropi BL2 dapat diaplikasikan sebagai agen dalam pengendali
gas rumah kaca dan dapat dikembangkan sebagai pupuk hayati yang bersifat ramah lingkungan di lahan sawah dataran rendah.
SIMPULAN DAN SARAN
Simpulan
Efektivitas bakteri metanotrof Methylocystis rosea BGM 1, M. parvus BGM 3, Methylococcus capculatus BGM 9, Methylobacter sp. SKM 14, dan
Ochrobactrum anthropi BL2 dapat mengurangi emisi metan (CH4) dan dinitrogen
oksida (N2O) serta dapat memacu pertumbuhan tanaman padi. Penambahan
formula bakteri pada lahan sawah menurunkan (sink) untuk CH4 dan N2O sebesar
0.13 mol CH4/hari/m2 dan 0.0023 mol N2O/hari/m2. Formulasi bakteri tersebut
18
Saran
Perlunya dilakukan penelitian lanjutan mengenai pembuatan formulasi bakteri metanotrof dan Ochrobactrum anthropi BL2 dalam bentuk padat untuk melihat keefektivitasannya terhadap penurunan emisi metan (CH4) dan dinitrogen
oksida (N2O) serta kemampuannya dalam memacu produktivitas tanaman padi.
Selain itu, karena bakteri metanotrof menggunakan senyawa C1 maka perlu
dilakukan penelitian analisis residu pestisida dalam kondisi in vitro.
DAFTAR PUSTAKA
Arth I, Frenzel P. 2000. Nitrification and denitrification in the rhizosphere of rice: the detection of processes by a new multi-channel electrode. Biol Fertil Soils. 31(5): 427-435.
Astuti DD. 2009. Karakterisasi fisiologi dan identifikasi molekuler isolat-isolat bakteri metanotrof asal sawah wilayah Bogor dan Sukabumi [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Baggs EM. 2008. Stable isotope techniques for N2O source partitioning in soils: a
review. R Com in Mass Spectro.22 (1): 1664-1672.
[BPT] Balai Penelitian Tanah. 2009. Balai Besar Litbang Sumber Daya Lahan
Pertanian Badan Penelitian dan Pengembangan Pertanian. Departemen
pertanian Bogor (ID): Departemen pertanian.
Cepy, Wangiana W. 2011. Growth and yield rice on vertisol and entisol media under various irrigation techniques an types of fertilizers. Crop Agro. 4(2): 2011.
Chaturvedi I. 2005. Effect of nitrogen fertilizer on growth yield and quality of hybrid rice (Oryza sativa L.). J Eur Agric. 6(4): 611-618.
Chaurasia N. 2014. Used fungicide mancozeb and insecticide profenofos in rice fields of meghalaya on the soil microflora. Int J Pharm Bio Sci. 5(3): 1049 – 1060.
Chatrina V. 2010. Efektivitas fiksasi N2 dan oksidasi metan kultur campuran
bakteri metanotrof asal sawah [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Cuhel J. 2010. Insights into the effect of soil pH on N2O and N2 emissions and
denitrifier community size and activity. Appl Environ Microbiol. 76(6): 1870–1878.
Dedysh SN, Knief C, Dunfield PF. 2005. Methylocella species are facultatively methanotrophic. J Bacteriol. 187(13): 4665–4670.
Departemen Pertanian. 2003. Panduan Sistem Karakterisasi dan Evaluasi Tanaman Padi. Bogor (ID): Departemen Pertanian Badan Penelitian dan Pengembangan Pertanian Komisi Nasional Plasma Nutfah.
Deppenmeier U. 2002. The unique biochemistry of methanogenesis. Prog Nucleic Acid Res Mol Biol. 71(10): 223-283.
19 process rates and nitrate and nitrite reductase gene abundances along and estuarine nutrient gradient. Appl Environ Microbiol. 75(10): 3171-3179. Duan YH, Zhang YL, Ye LY, Fan XR, Xu GH, Shen QR. 2007. Responses of rice
cultivars with different nitrogen use efficiency to partial nitrate nutrition.
Ann Bot. 2(99): 1153–1160.
Dubey SK. 2005. Microbial ecology of methane emission in rice agroecosystem: a review. Appl Ecol Environ Res. 3(2): 1-27.
Elizabeth M, Baggs EM. 2011. Soil microbial sources of nitrous oxide: recent advances inknowledge, emerging challenges and future direction. Curr Op
in Environ Sustain. 3(10): 321–327.
Hanson RS, Hanson TE. 1996. Methanotrophic bacteria: a review. Microbiol. 60(2): 439–471.
Hapsari W. 2008. Isolasi dan karakterisasi bakteri metanotrof dari lahan persawahan di daerah Bogor dan Sukabumi [skripsi]. Bogor (ID):Institut Pertanian Bogor.
Hadianta R, Rusmana I, Mubarik NR. 2014. Diversity of nitrogen fixing bacteria based on nifH gene in rice field. Adv Environ Biol. 8(14): 63-69.
[IPCC] Intergovernmental Panel on Climate Change. 2007. Mitigation of Climate Change. Cambridge (GB): Cambridge University Pr.
Jean L M, Roger P. 2001. Production, oxidation, emission and consumption of methane by soils: a review. Eur J Soil Biol. 37 (1): 25−50.
Juottonen H. 2008. Archaea, bacteria, and methane production along environmental gradients in fens and bogs [disertasi]. Helsinki (FI): University of Helsinki.
Macalady JL, Andrew MS, Millan MC, Angela F, Dickens, Stanley C, Kate MS. 2002. Population dynamics of type I and II methanotrophic bacteria in rice soils. Environ Microbiol. 4(3): 48–157.
Margareth M. 2011. Isolasi dan seleksi bakteri metanotrof pemfiksasi nitrogen dari sawah di Sragen Jawa Tengah [tesis]. Bogor (ID): Institut Pertanian Bogor.
Maisaroh. 2009. Aktivitas enzim nitrogenase dan oksidasi metan bakteri metanotrof asal sawah [tesis]. Bogor (ID): Institut Pertanian Bogor.
Millar N, Robertson GP, Grace PR, Gehl RJ, Hoben JP. 2010. Nitrogen fertilizer management for nitrous oxide (N2O) mitigation in intensive corn (Maize)
production: an emissions reduction protocol for US Midwest agriculture. Mitig Adapt Strateg Glob Change. 10(7): 1007-1027.
Moat AG, Foster JW, Spector MP. 2002. Microbial Physiology. Edisi ke-4. New York (US): Wiley-Liss. hlm 479.
Muttaqin M. 2012. Kombinasi bakteri metanotrof, pereduksi dinitrogen oksida, dan penambat nitrogen sebagai agen pereduksi gas rumah kaca dan pupuk hayati pada tanaman padi [tesis]. Bogor (ID): Institut Pertanian Bogor. Mulvaney RL, Khan SA, Mulvaney CS. 1997. Nitrogen fertilizers promote
denitrification. Biol Fertil Soils. 24(5): 211-220.
20
Nurhasanah. 2009. Eksplorasi dan karakterisasi bakteri metanotrof toleran senyawa organoklorin dari lahan sawah di Bogor [tesis]. Bogor (ID): Institut Pertanian Bogor.
[Permentan] Peraturan Menteri Pertanian. 2007. Acuan penetapan rekomendasi pupuk NPK pada lahan sawah. Jakarta (ID): Permentan. 140 (04): 2007. Pingak GMF, Sutanto H, Akhdiya A, Rusmana I. 2013. Effectivity of
methanotrophic bacteria and Ochrobactrum anthropi as biofertilizer and emission reducer of CH4 and N2O in inorganic paddy fields. J Med Bioeng.
3(3): 217-221.
Sagala BT.2009. Seleksi dan uji aktivitas fiksasi nitrogen (N2)Bakteri metanotrof
asal sawah Pada konsentrasi oksigen (O2) berbeda [skripsi]. Bogor (ID):
Institut Pertanian Bogor.
Semrau JD, Dispirito AA, Yoon S. 2010. Methanotrophs and copper: a review. FEMS Microbiol. 34(10): 496-531.
Seo J, Jeon J, Kim S, Kang, S, Han J, Hur, H. 2007. Fungal biodegradation of carbofuran and carbofuran phenol by the fungus Mucor ramannianus. W Sci Technol. 55 (1-2): 163-167).
Setyaningsih R, Rusmana I, Setyanto P, Suwanto A. 2010. Physiological characterization and molecular identification of denitrifying bacteria possesing nitrous oxide high reduction activity isolated from rice soils. J Microbiol Indones. 4(1): 75-78.
Setyaningsih R, Rusmana I, Setyanto P, Suwanto A. 2013. Nitrous oxide reduction activity of denitrifying Ochrobactrum anthropi isolated from rice field. J Microbiol Indones. 7(2): 45-50.
Shapleigh P. 2006. The denitrifiying prokaryotes. Di dalam: Dworkin M, Falkow S, Rosenberg E, Schleifer KH, Stackebrandt E, editor. The Prokaryotes Ecophysiology and Biochemistry. 3th ed. Minneapolis (US): Springer. hlm 769–792.
Sutanto H, Rusmana I, Mubarik NR. 2014. Community succession of methanotrophic bacteria based on PMOA gene in rice fields. Adv Environ Biol. 8(14): 50-56.
Venterea RT, Burge M, dan Spokas KA. 2005. Nitrogen oxide and methane emissions under varying tillage and fertilizer management. J Environ Qual. 34(10): 1467-1477.
Wang L, Jiang X, Yan D, Wu J, Bian Y, Wang F. 2007 Behaviour and fate of chlorpyrifos introduced intosoil crop systems by irrigation. Chemosphere. 66(9): 391–396.
Wangiyana W, Laiwan Z, Sanisah. 2009. Growth and yield of rice under “sri
(system of rice intensification)” Technique at various ages and numbers of
seedlings per hill. Crop Agro. 2(1): 70-78.
21 Wihardjaka A. 2001. Emisi gas metan di tanah sawah irigasi dengan pemberian
22
Lampiran 1 Hasil analisis sifat fisik kimia tanah lahan sawah dataran rendah di Desa Citarik, Kec. Pelabuhan Ratu, Kab. Sukabumi, Jawa Barat
Kontrol Perlakuan Tekstur
Pasir
%
30 31
Debu 38 38
Liat 32 31
Ekstrak 1.5 pH H2O 7.2 7.1
KCl 6.3 6.3
Bahan Organik
Walkley & Black (C)
% 1.55 1.31
Kjeldahl (N) 0.17 0.13
C/N 9 10
HCl 25% P2O5 Mg/100 g 78 62
K2O 21 29
Olsen P2O5 7 46
Bray 1 P2O5 - -
Morgan K2O 143 289
Nilai Tukar Kation
Ca 18.31 17.43
Mg 2.85 2.90
K 0.28 0.57
Na 0.70 0.61
Jumlah 22.14 21.51
KTK 14.53 13.51
KB* >100 >100
Al 0.0 0.0
23
24
Lampiran 3 Analisis residu pestisida sebelum tanam dan sesudah panen lahan sawah dataran rendah di Desa Citarik, Kec. Pelabuhan Ratu, Kab. Sukabumi,
Jawa Barat
Klorpirifos Profenofos Karbofuran Klorpirifos Profenofos Karbofuran
Perlakuan 0.0133 0.0112 0.0116 0.0101 ttd 0.0152 Kontrol 0.0244 0.0181 0.0154 ttd 0.0114 0.0211
Keterangan: ttd= tidak terdeteksi
Analisis residu pestisida sebelum tanam dan sesudah panen pada lahan sawah dataran rendah di Desa Citarik, Kec. Pelabuhan Ratu, Kab. Sukabumi, Jawa Barat. Residu pestisida dianalisis dengan menggunakan metode GC-ECD di Laboratorim Pasca Panen, Jl. Tentara Pelajar, Bogor, Jawa Barat.
Perlakuan Kontrol
Karbofuran 0.0116 0.0152 0.0154 0.0211
BPMC ttd - ttd -
25
RIWAYAT HIDUP
Penulis dilahirkan di Kassilohe, Kec. Kajang, Kab. Bulukumba, Sulawesi-Selatan 11 November 1989 sebagai anak kelima dari lima bersaudara dari pasangan Nurdin dan Haisa. Pendidikan sarjana ditempuh di Program Studi Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Makassar, lulus pada tahun 2012. Pada tahun 2013 penulis diterima di Program Studi/Mayor Mikrobiologi pada Sekolah Pascasarjana IPB dan menamatkannya pada tahun 2015. Beasiswa pendidikan Pascasarjana diperoleh dari program BPP-DN Dikti Kementrian Pendidikan dan Kebudayaan Republik Indonesia. Artikel ilmiah berjudul The effectiveness of methanotrophic bacteria and
Ochrobactrum anthropi to reduce CH4 and N2O emissions and to promote paddy
growth in lowland paddy fields diterbitkan pada jurnal Malaysian Journal of