KEPARAHAN PENYAKIT JANTUNG KORONER
BERDASARKAN SULLIVAN VESSEL SCORE
Laporan Penelitian ini ditulis sebagai salah satu syarat untuk memperoleh gelar SARJANA KEDOKTERAN
OLEH:
Amaryllis Anandini
NIM: 1113103000030
PROGRAM STUDI KEDOKTERAN DAN PROFESI DOKTER
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI
SYARIF HIDAYATULLAH
JAKARTA
v
Segala puji dan syukur penulis panjatkan kehadirat Allah SWT atas segala rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan laporan penelitian yang
berjudul ―NILAI KREATININ SEBAGAI FAKTOR PREDIKTOR
KEPARAHAN PENYAKIT JANTUNG KORONER BERDASARKAN SULLIVAN VESSEL SCORE‖ sebagai salah satu syarat dalam menyelesaikan jenjang program sarjana kedokteran di Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
Penulis menyadari bahwa karya ilmiah ini terwujud karena adanya bantuan dan dukungan dari berbagai pihak. Oleh karena itu, penulis menyampaikan penghargaan, rasa hormat dan terima kasih kepada:
1. Prof. Dr. Arief Sumantri, M.Kes selaku Dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
2. dr. Achmad Zaki, Sp.OT, M.Epid selaku Ketua Program Studi Kedokteran dan Profesi Dokter Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
3. dr. Sayid Ridho, Sp.PD, FINASIM dan dr. Dede Moeswir, Sp.PD-KKV selaku dosen pembimbing riset
4. Kedua orang tua penulis, Subbur Widodo dan Wiwik Utari, yang selalu mendoakan dan memberi semangat setiap saat.
5. Adik-adik penulis, Hafizh R. Amrullah dan Amyra L. Mumpuni, yang menjadi motivasi untuk menyelesaikan pendidikan kedokteran dengan baik.
vi
Angkatan 2013 Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta, khususnya Ulfah, Zahrotu, Kirana, dan Herlin.
9. Semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah memberikan bantuan, serta dukungan sehingga penulis bisa menyelesaikan penelitian ini.
Demikian yang dapat penulis sampaikan, semoga laporan ini dapat bermanfaat bagi penelitian berikutnya dan menambah pengetahuan bagi yang membacanya.
Jakarta, 9 November 2016
vii
Amaryllis Anandini. Program Studi Kedokteran dan Profesi Dokter. Kreatinin sebagai Faktor Prediktor Keparahan Penyakit Jantung Koroner Berdasarkan Sullivan Vessel Score. 2016.
Latar Belakang: Penyakit kardiovaskular merupakan penyakit penyebab kematian utama di dunia. Tingkat keparahan penyakit jantung koroner (PJK) dapat dikuantifikasikan dengan sistem skoring angiografik di antaranya Sullivan
Vessel Score (SVS). Telah banyak penelitian yang menemukan bahwa kreatinin
berhubungan dengan penyakit jantung koroner, namun belum ada yang menemukan hubungan kreatinin dengan tingkat keparahan PJK berdasarkan SVS. Tujuan: Mengetahui kreatinin sebagai faktor prediktor keparahan PJK berdasarkan SVS. Metode: Penelitian menggunakan desain kohort retrospektif pada 86 pasien PJK yang dirawat di RS Hermina Bekasi pada Januari-Oktober 2016. Hasil: Dengan uji Chi Square didapatkan nilai kreatinin < 1,2 mg/dl memiliki RR:3.47, 95%CI: 1,01-11,82, p<0.05 (SVS 1 vs 3), RR: 4,1, 95%CI: 1,34-12,02, p<0.05 (SVS 1 vs 2), dan RR: 0,85, 95%CI: 0,27-2,62, p>0.05 (SVS 2 vs 3). Kesimpulan: Nilai kreatinin berhubungan dengan tingkat keparahan PJK berdasarkan SVS. Namun belum bisa dijadikan faktor prediktor.
Kata Kunci: Penyakit Jantung Koroner, Skor Angiografik, Sullivan Vessel Score, Kreatinin
ABSTRACT
Amaryllis Anandini. Program Studi Kedokteran dan Profesi Dokter. Creatinine as a Predictor of Coronary Artery Disease Burden Based on Sullivan Vessel Score. 2016.
Background: Cardiovascular disease is the leading cause for mortality in the world. Coronary artery disease (CAD) burden can be quantified by angiographic scoring system such as Sullivan Vessel Score (SVS). Many studies have found that creatinine correlates with CAD, however there has not been a study found that
creatinine correlates with CAD burden based on SVS. Aim: To determine
creatinine as a predictor of CAD burden based on SVS. Methods: The study used
retrospective cohort design in 86 CAD patients admitted in Hermina Bekasi
Hospital on January-October 2016. Results: With Chi Square test, obtained
creatinine <1,2 mg/dl had RR:3.47, 95%CI: 1,01-11,82, p<0.05 (SVS 1 vs 3), RR: 4,1, 95%CI: 1,34-12,02, p<0.05 (SVS 1 vs 2), dan RR: 0,85, 95%CI: 0,27-2,62,
p>0.05 (SVS 2 vs 3). Conclusion: Creatinine correlates with CAD burden based
on SVS. However it can not be used as a predictor for it.
viii
Lembar Pernyataan Keaslian Karya ... ii
Lembar Persetujuan Pembimbing... iii
Lembar Pengesahan Panitia Ujian ... iv
Kata Pengantar ... v 1.1 Latar Belakang Masalah ...1
1.2 Rumusan Masalah ... 3
1.5.2 Manfaat di bidang pelayanan kesehatan ...4
1.5.3 Manfaat di bidang pengembangan penelitian...5
1.5.4 Manfaat bagi institusi...5
ix
2.1.1.5 Epidemiologi Penyakit Jantung Koroner...13
2.1.1.6 Tata Laksana Penyakit Jantung Koroner...14
3.2 Lokasi Dan Waktu Penelitian ...29
3.3 Populasi dan Sampel Penelitian...29
3.3.1 Populasi...29
3.3.2 Sampel dan Cara Pemilihan Sampel...29
3.3.3 Perkiraan Besar Sampel ...29
3.4 Kriteria Inklusi dan Eksklusi ...30
3.4.1 Kriteria Inklusi ...30
3.4.2 Kriteria Eksklusi...30
3.5 Cara Kerja Penelitian ...31
3.6 Alur Penelitian...31
x
4.1.1 Karakteristik Dasar Subjek Penelitian...33
4.1.2 Analisis Univariat...34
4.1.3 Analisis Bivariat ...36
4.1.4 Analisis Multivariat ...38
4.2 Pembahasan ...38
4.2.1 Karakteristik Subjek Penelitian ...38
4.2.2 Hubungan Nilai Kreatinin dengan Tingkat Keparahan Penyakit Jantung Koroner berdasarkan Sullivan Vessel Score... 39
4.3 Keterbatasan Penelitian ...40
BAB V Simpulan dan Saran 5.1 Simpulan...41
5.2 Saran...42
xi
Gambar 2.1 Skema evolusi plak aterosklerosis...9
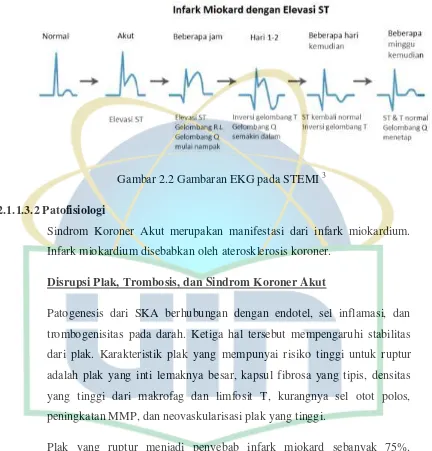
Gambar 2.2 Gambaran EKG pada STEMI...11
Gambar 2.3 Konsekuensi thrombosis koroner...12
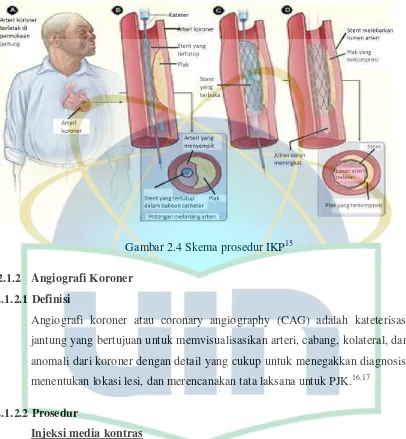
Gambar 2.4 Skema prosedur IKP...16
Gambar 2.5 Nomenklatur untuk proyeksi angiografi...17
Gambar 2.6 Gambaran angiografik...18
xii
Tabel 4.1 Karakteristik Dasar Subjek Penelitian...33 Tabel 4.2 Karakteristik Hasil Laboratorium Subjek Penelitian...34 Tabel 4.3 Distribusi Frekuensi Kreatinin dan Sullivan Vessel Score...35 Tabel 4.4 Hubungan Nilai Kreatinin dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score...36
Tabel 4.5 Hubungan Nilai Kreatinin dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score 1 vs 3...37
Tabel 4.6 Hubungan Nilai Kreatinin dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score 1 vs 2...37
Tabel 4.7 Hubungan Nilai Kreatinin dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score 2 vs 3...38
xiii PJK : Penyakit Jantung Koroner SKA : Sindrom Koroner Akut
STEMI : ST Elevation Myocardial Infarct CAG : Coronary Angiography
IVUS : Intravascular Ultrasound SVS : Sullivan Vessel Score
NADH : Nicotinamide adenine dinucleotide
NADPH : Nicotinamide adenine dinucleotide phosphate VCAM-1 : Vascular cell adhesion molecule 1
ICAM-1 : Intercellular adhesion molecule 1 MCP-1 : Monocyte chemoattractant protein 1 M-CSF : Macrophage colony-stimulating factor CD40 : cluster of differentiation 40
TNF-α : Tumor necrosis factor-α PDGF : Platelet-derived growth factor MMP : Matrix metalloproteinase
VEGF : Vascular endothelial growth factor RANKL : Receptor activator of NF-κB ligand BNP4 : Bone morphogenetic protein 4 EKG : Elektrokardiogram
CK-MB : Creatinine kinase muscle and brain IKP : Intervensi koroner perkutan
xiv RR : Risiko relatif
BAB I PENDAHULUAN
1.1Latar Belakang Masalah
Penyakit kardiovaskular merupakan penyakit penyebab kematian utama di dunia. Pada tahun 2012, sebanyak 17,5 juta orang meninggal akibat penyakit kardiovaskular atau sebanyak 31% dari kematian di dunia. Dari jumlah tersebut, sebanyak 7,4 juta orang meninggal akibat Penyakit Jantung Koroner (PJK).1 Hasil Riset Kesehatan Dasar 2013 menunjukan bahwa prevalensi PJK berdasarkan diagnosis dokter di Indonesia sebesar 0,5%, dan berdasarkan diagnosis dokter atau gejala sebesar 1,5% dari 1.027.763 orang.2
Penyakit Jantung Koroner digambarkan dengan adanya aterosklerosis di arteri koroner epikardium. Plak aterosklerotik akan mempersempit lumen arteri koroner dan mengganggu aliran darah miokardium sehingga menyebabkan nyeri dada. PJK dibagi menjadi beberapa subkategori, di antaranya yaitu Stable Ischemic Heart Disease atau penyakit jantung iskemik stabil, serta Acute Coronary Syndrome atau Sindrom Koroner Akut.3 Sindrom Koroner Akut (SKA) merujuk kepada gejala-gejala klinis yang berhubungan dengan iskemi miokard akut. SKA terdiri dari Unstable Angina
Pectoris, ST Elevation Myocardial Infarct (STEMI), dan Non STEMI.4
Aterosklerosis pada PJK dapat menyebabkan penyempitan abnormal pada pembuluh darah yang disebut stenosis.5 Angiografi koroner atau Coronary Angiography (CAG) adalah alat radiologi yang paling sederhana dan dapat dipercaya
Terdapat beberapa sistem skoring angiografik untuk menilai beban atau keparahan PJK, yaitu Gensini, CASS, Duke CAD Severity, Syntax, Duke Jeopardy, Jenkins, Friesinger, Sullivan, Approach, dan BARI-jeopardy index.7 Pada penelitian ini digunakan Sullivan Vessel Score (SVS). Pada penelitian yang dilakukan oleh Ian Neeland dkk, didapatkan skor Sullivan mempunyai korelasi terhadap keparahan dan luas plak aterosklerosis yang dinilai menggunakan IVUS (Spearman's multiple rho
rank correlation: 0.76, p<0.0001).7
Penilaian tingkat keparahan PJK berperan dalam penentuan tata laksana selanjutnya untuk pasien PJK, yaitu dengan pengobatan atau dengan tindakan invasif revaskularisasi. Kedua tata laksana tersebut sangatlah berbeda walaupun tujuannya sama. Dilihat dari segi biaya dan tenaga medis, tindakan invasif revaskularisasi tentu memerlukan biaya yang lebih mahal dan tenaga medis yang ahli. Oleh karena itu, penilaian tingkat keparahan stenosis dari CAG sangatlah penting bagi pasien PJK.
Hampir semua pasien PJK yang akan menjalani CAG diperiksa kadar kreatinin dalam darahnya terlebih dahulu. Salah satu langkah dalam tindakan CAG adalah memasukkan kontras ke pembuluh darah pasien.3 Kontras tersebut akan diekskresi melalui ginjal sehingga perlu dilakukan penilaian fungsi ginjal pasien PJK yang akan menjalani CAG.
Masih sedikit penelitian yang mencari hubungan kreatinin dengan tingkat keparahan PJK. Selain itu, karena pemeriksaan kadar kreatinin hampir selalu diperiksa sebelum CAG maka kemungkinan besar data dapat diperoleh secara lengkap. Oleh karena itu, peneliti ingin mengetahui apakah nilai kreatinin dapat dijadikan faktor prediktor keparahan PJK berdasarkan skor angiografik yaitu Sullivan Vessel Score pada pasien PJK.
1.2 Rumusan Masalah
Berdasarkan latar belakang masalah di atas, maka rumusan masalah penelitian ini adalah:
1. Bagaimana proporsi tingkat keparahan PJK berdasarkan Sullivan Vessel Score?
2. Apakah nilai kreatinin pasien dapat dijadikan faktor prediktor tingkat keparahan PJK berdasarkan Sullivan Vessel Score?
1.3 Hipotesis
Pada penelitian ini didapati hipotesis yang akan diuji, yaitu:
Nilai reatinin dapat digunakan sebagai faktor prediktor untuk menilai tingkat keparahan PJK berdasarkan Sullivan Vessel Score.
1.4 Tujuan Penelitian 1.4.1 Tujuan Umum
1.4.2 Tujuan Khusus
1. Mengetahui angka kejadian penyakit jantung koroner yang meliputi penyakit jantung iskemik stabil, Unstable Angina Pectoris, ST Elevation Myocardial Infarct (STEMI), dan Non STEMI di RS Hermina Bekasi
2. Mengetahui proporsi tingkat keparahan PJK secara angiografik berdasarkan Sullivan Vessel Score 0, 1, 2, dan 3 pada pasien PJK di RS Hermina Bekasi
3. Mengetahui data nilai kreatinin pasien PJK di RS Hermina Bekasi
4. Mengetahui hubungan nilai kreatinin pasien dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score pada pasien PJK di RS Hermina Bekasi
5. Mengetahui kreatinin dapat digunakan sebagai faktor prediktor tingkat keparahan PJK berdasarkan Sullivan Vessel Score pada pasien PJK di RS Hermina Bekasi
1.5 Manfaat Penelitian
1.5.1 Manfaat di bidang ilmiah
Penelitian ini diharapkan dapat memberikan data ilmiah mengenai tingkat keparahan PJK menggunakan Sullivan Vessel Score pada pasien PJK dengan nilai kreatinin pasien sebagai faktor prediktornya.
1.5.2 Manfaat di bidang pelayanan kesehatan
Hasil penelitian dapat dijadikan untuk pertimbangan tenaga kerja kesehatan untuk menilai tingkat keparahan PJK menggunakan Sullivan Vessel Score. Selain itu, penilaian risiko pada pasien dapat dilakukan
1.5.3 Manfaat di bidang pengembangan penelitian
Penelitian ini diharapkan dapat menjadi bahan penelitian selanjutnya mengenai tingkat keparahan PJK menggunakan Sullivan Vessel Score. 1.5.4 Manfaat bagi institusi
Bab II
TINJAUAN PUSTAKA
2.1.Landasan Teori
2.1.1 Penyakit Jantung Koroner 2.1.1.1 Definisi
Penyakit Jantung Koroner digambarkan dengan adanya aterosklerosis di arteri koroner epikardium. PJK dibagi menjadi beberapa subkategori, di antaranya yaitu Stable Ischemic Heart Disease, serta Acute Coronary Syndrome atau Sindrom Koroner Akut.3,4 Sindrom Koroner Akut (SKA) merujuk kepada gejala-gejala klinis yang berhubungan dengan iskemi miokard akut. SKA terdiri dari Unstable Angina Pectoris, ST Elevation Myocardial Infarct (STEMI), dan Non STEMI.3
2.1.1.2 Patofisiologi
Inisiasi Aterosklerosis
Akumulasi lipid ekstraseluler
Diet tinggi kolesterol dan lemak jenuh akan menyebabkan lipoprotein, terutama LDL, menumpuk di lapisan intima pembuluh darah. Lipoprotein ini berikatan dengan proteoglikan di lapisan intima dan beragregasi. Ikatan ini menyebabkan peningkatan kerentanan terhadap zat oksidatif. Stres oksidatif dapat disebabkan oleh nicotinamide adenine dinucleotide / nicotinamide
adenine dinucleotide phosphate (NADH/NADPH) oksidase yang
Pengerahan leukosit
Leukosit, terutama monosit dan limfosit T, akan adhesi ke lapisan endotel pembuluh darah. Molekul yang mengatur adhesi leukosit ini adalah vascular
cell adhesion molecule 1 (VCAM-1), intercellular adhesion molecule 1
(ICAM-1) ,dan E-selectin.
Ketika monosit sudah adhesi ke lapisan endotel, monosit akan penetrasi ke lapisan intima. Hal tersebut diatur oleh chemoattractant cytokines atau kemokin, diantaranya monocyte chemoattractant protein 1 (MCP-1). MCP-1 diproduksi oleh endotel yang terstimulasi oleh adanya lipoprotein yang teroksidasi.
Akumulasi lipid intraselular: pembentukan sel busa
Jika monosit sudah mencapai lapisan intima, monosit akan menyerap lipid dan menjadi sel busa atau makrofag sarat-lemak. Sel busa ini dapat bereplikasi yang dipicu oleh macrophage colony-stimulating factor (M-CSF).
Evolusi Ateroma
Inflamasi pada Aterogenesis
Sel busa bertindak sebagai sumber mediator proinflamasi seperti sitokin, kemokin, dan aktivator platelet. Selain itu, sel busa juga dapat mengembangkan sejumlah besar spesies oksidan seperti anion superoksida. Kedua fungsi sel busa tersebut dapat mendorong inflamasi dan berkontribusi terhadap perkembangan lesi.
T-helper 1 dapat mengeluarkan beberapa sitokin yaitu interferon-γ, limfotoksin, cluster of differentiation 40 (CD40), and tumor necrosis factor-α (TNF-α). Sitokin-sitokin tersebut akan mengaktivasi sel dinding vaskular yang mengakibatkan plak menjadi tidak stabil dan meningkatnya trombogenitas. Di sisi lain, T-helper 2 dapat mengeluarkan interleukin 10 (IL-10) yang bisa menginhibisi inflamasi pada proses aterogenesis. Sel T sitolitik dapat mengekspresikan ligan Fas dan faktor sitotoksik lainnya yang akan menyebabkan apoptosis sel target seperti sel otot polos, sel endotel, dan makrofag. Apoptosis dari ketiga sel ini berkontribusi terhadap progresi dan komplikasi plak.
Migrasi dan proliferasi sel otot polos
Makrofag yang teraktivasi akan melepaskan platelet-derived growth factor (PDGF). PDGF akan menstimulasi proliferasi dari sel otot polos yang ada di tunika media pembuluh darah ke tunika intima. Namun sel otot polos yang dihasilkan kurang matur. Sel tersebut mempunyai lebih banyak retikulum endoplasma kasar, dan lebih sedikit serat kontraktil dibandingkan sel otot polos normal.
Matriks ekstraseluler arteri
Plak aterosklerosis, selain terdiri dari sel-sel, juga terbentuk dari matriks ekstraseluler. Di antaranya adalah kolagen tipe I dan III, proteoglikan (versican, biglycan, aggrecan, dan decorin), serta serat elastin. Matriks tersebut diproduksi oleh sel otot polos yang distimulasi oleh PDGF dan TGFβ.
Angiogenesis plak
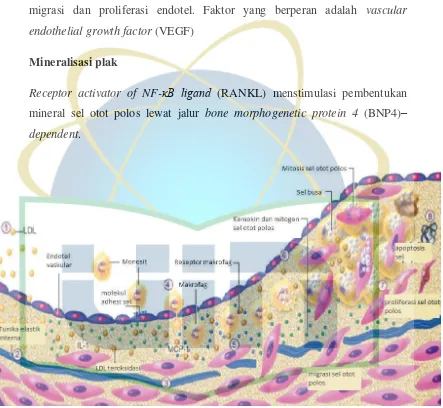
Plak aterosklerosis dapat mengembangkan mikrosirkulasinya sendiri karena migrasi dan proliferasi endotel. Faktor yang berperan adalah vascular endothelial growth factor (VEGF)
Mineralisasi plak
Receptor activator of NF-κB ligand (RANKL) menstimulasi pembentukan
mineral sel otot polos lewat jalur bone morphogenetic protein 4 (BNP4)– dependent.
2.1.1.3 Sindrom Koroner Akut 2.1.1.3.1 Definisi
Istilah Sindrom Koroner Akut (SKA) mengarah kepada gejala-gejala klinis dari iskemi miokardium akut. Berdasarkan gambaran dari elektrokardiogram (EKG) dan biomarker jantung, SKA dibagi menjadi
Unstable Angina Pectoris, Non ST Elevation Myocardial Infarction
(NSTEMI), dan ST Elevation Myocardial Infarction (STEMI).
Unstable Angina Pectoris digambarkan dengan satu dari gejala-gejala
berikut seperti nyeri dada yang terjadi saat beristirahat (biasanya berlangsung lebih dari 20 menit), onset baru (< 2 bulan sebelumnya) angina yang parah, nyeri dada dengan pola crescendo (intensitas, durasi, dan frekuensi meningkat).
Diagnosis NSTEMI ditegakkan bila terjadi iskemi sampai kerusakan miokardium sehingga menyebabkan biomarker dari nekrosis miokardium terlepas ke sirkulasi. Salah satu biomarkernya adalah Troponin T atau I, dan creatinine kinase muscle and brain (CK-MB).
Gambar 2.2 Gambaran EKG pada STEMI 3 2.1.1.3.2 Patofisiologi
Sindrom Koroner Akut merupakan manifestasi dari infark miokardium. Infark miokardium disebabkan oleh aterosklerosis koroner.
Disrupsi Plak, Trombosis, dan Sindrom Koroner Akut
Patogenesis dari SKA berhubungan dengan endotel, sel inflamasi, dan trombogenisitas pada darah. Ketiga hal tersebut mempengaruhi stabilitas dari plak. Karakteristik plak yang mempunyai risiko tinggi untuk ruptur adalah plak yang inti lemaknya besar, kapsul fibrosa yang tipis, densitas yang tinggi dari makrofag dan limfosit T, kurangnya sel otot polos, peningkatan MMP, dan neovaskularisasi plak yang tinggi.
Plak yang ruptur menjadi penyebab infark miokard sebanyak 75%. Sedangkan sisanya diakibatkan oleh erosi endotel superfisial. Setelah plak ruptur ataupun erosi endotel superfisial terjadi, matriks subendotel (yang banyak mengandung prokoagulan) akan terpapar oleh darah sirkulasi. Paparan ini akan menyebabkan adhesi platelet dan diikuti pembentukan trombus. 4
aliran darah di arteri. (2) Trombus putih terdiri dari banyak platelet. Trombus putih terbentuk pada area dengan aliran bertekanan tinggi. Trombus merah biasanya melapisi trombus putih dan menyebabkan oklusi total.
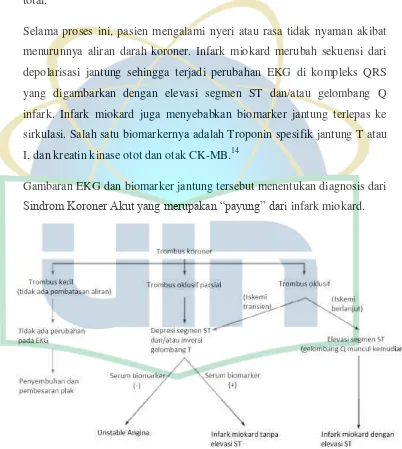
Selama proses ini, pasien mengalami nyeri atau rasa tidak nyaman akibat menurunnya aliran darah koroner. Infark miokard merubah sekuensi dari depolarisasi jantung sehingga terjadi perubahan EKG di kompleks QRS yang digambarkan dengan elevasi segmen ST dan/atau gelombang Q infark. Infark miokard juga menyebabkan biomarker jantung terlepas ke sirkulasi. Salah satu biomarkernya adalah Troponin spesifik jantung T atau I, dan kreatin kinase otot dan otak CK-MB.14
Gambaran EKG dan biomarker jantung tersebut menentukan diagnosis dari
Sindrom Koroner Akut yang merupakan ―payung‖ dari infark miokard.
2.1.1.4 Penyakit Jantung Iskemik Stabil
Penyakit jantung iskemik stabil bersifat kronis dengan manifestasi berupa nyeri dada transien yang dapat diprediksi. Nyeri dada muncul saat pasien mengalami stres emosional dan aktivitas fisik yang berlebih.3
2.1.1.4.1Patofisiologi
Penyakit jantung iskemik stabil umumnya disebabkan oleh plak aterom yang terfiksasi. Saat keadaan istirahat, kebutuhan oksigen jantung masih dapat terpenuhi walaupun lumen arteri koroner menyempit. Namun pada saat pasien mengalami stres emosional dan aktivitas fisik yang berlebih, sistem saraf simpatis akan teraktivasi. Hal tersebut akan menyebabkan denyut jantung dan tekanan darah meningkat sehingga kebutuhan oksigen meningkat. Arteri koroner yang menyempit karena plak aterom tidak bisa memenuhi kebutuhan oksigen jantung sehingga terjadi iskemi. Nyeri dada akibat iskemi tersebut akan mereda jika pasien mengambil waktu untuk beristirahat.
2.1.1.5 Epidemiologi Penyakit Jantung Koroner
2.1.1.6 Tata Laksana Penyakit Jantung Koroner
Salah satu tata laksana penyakit jantung koroner untuk revaskularisasi yang minimal invasif adalah intervensi koroner perkutan (IKP) atau percutaneous coronary intervention. IKP adalah prosedur non bedah yang menggunakan
kateterisasi jantung untuk menempatkan stent untuk mengatasi stenosis arteri koroner 4
Indikasi
IKP merupakan tata laksana utama bagi STEMI. Jika tidak dapat dilakukan, STEMI ditangani dengan pemberian terapi fibrinolitik. Sedangkan untuk UA/NSTEMI, IKP hanya diindikasikan bagi pasien yang mempunyai risiko tinggi. Pengukuran risiko pada pasien UA/NSTEMI dapat menggunakan sistem scoring Thrombolysis in Myocardial Infarction (TIMI).13 TIMI mempunyai tujuh variabel, yaitu:
Umur > 65 tahun
Mempunyai ≥ 3 faktor risiko untuk penyakit jantung koroner, yaitu:
Faktor risiko yang dapat diubah: − Dislipidemia
− Merokok
− Hipertensi
− Diabetes, sindrom metabolik − Kurangnya aktivitas fisik Faktor risiko yang tidak dapat diubah:
− Usia lanjut
− Jenis kelamin pria − Genetik
Deviasi segmen ST pada gambaran EKG
Mengalami dua episode angina 24 jam sebelumnya
Penggunaan aspirin selama tujuh hari sebelumnya (menunjukan resistensi terhadap aspirin)
Peningkatan serum troponin dan CK-MB
Risiko kematian atau kejadian iskemi dalam waktu 14 hari:
Rendah: 0-2 (<8.3%)
Sedang: 3-4 (<19.3%)
Tinggi: 5-7 (41%)
Pasien UA/NSTEMI dengan skor 3-4 merupakan indikasi dilakukannya IKP.13
Sedangkan untuk kasus penyakit jantung iskemik stabil, IKP diindikasikan pasien yang mempunyai gejala. Selain itu, terdapat beberapa indikasi sesuai penemuan pada angiografi, yaitu:
Stenosis 50% pada arteri koroner kiri atau left main
Stenosis 70% pada non left main
Gambar 2.4 Skema prosedur IKP15 2.1.2 Angiografi Koroner
2.1.2.1 Definisi
Angiografi koroner atau coronary angiography (CAG) adalah kateterisasi jantung yang bertujuan untuk memvisualisasikan arteri, cabang, kolateral, dan anomali dari koroner dengan detail yang cukup untuk menegakkan diagnosis, menentukan lokasi lesi, dan merencanakan tata laksana untuk PJK.16,17
2.1.2.2 Prosedur
Injeksi media kontras
Kecepatan Filming Frame
Kecepatan filming frame biasanya 15-30 frame/detik. Jika denyut nadi >95 kali/menit, maka kecepatan filming frame menjadi 60 frame/detik.
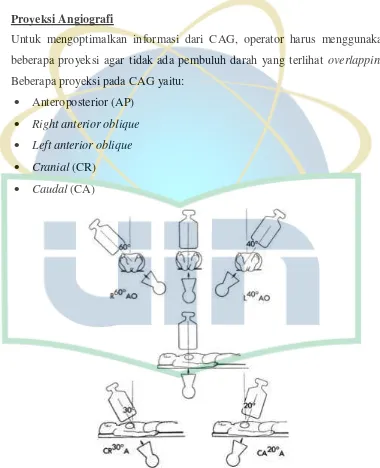
Proyeksi Angiografi
Untuk mengoptimalkan informasi dari CAG, operator harus menggunakan beberapa proyeksi agar tidak ada pembuluh darah yang terlihat overlapping. Beberapa proyeksi pada CAG yaitu:
Anteroposterior (AP)
Right anterior oblique
Left anterior oblique
Cranial (CR)
Caudal (CA)
2.1.2.3 Penilaian Stenosis Koroner
Evaluasi derajat stenosis dilihat dari persentase reduksi diameter pembuluh darah. Persentase ini dihitung dari penyempitan pembuluh darah paling besar yang bisa dilihat. Segmen stenosis dibandingkan dengan lumen terdekat yang tampak tidak ada obstruksi.
Gambar 2.6 Gambaran angiografik17 2.1.3 Skor Angiografik
Terdapat beberapa sistem skoring angiografik untuk mengkuantifikasi tingkat keparahan penyakit jantung koroner. Di antaranya yaitu Gensini, CASS, Duke CAD Severity, Syntax, Duke Jeopardy, Jenkins, Friesinger, Sullivan, Approach, dan BARI-jeopardy index.7 Pada penelitian yang dilakukan oleh Ian Neeland dkk, didapatkan bahwa semua skor angiografik tersebut saling berkorelasi satu sama lain (range untuk koefisien Spearman: 0,79-0,98,
p<0,01)7. Skor angiografik tersebut juga berkorelasi dengan pemeriksaan
beban dan luas plak aterosklerosis yang diperiksa menggunakan intravascular ultrasound (IVUS) (range untuk koefisien Spearman: 0,56-0,78 p<0,0001 dan
komposisinya, sedangkan CAG hanya dapat menilai derajat penyempitan lumen arteri atau stenosis.7
2.1.3.1 Sullivan Vessel Score
Sullivan Vessel Score adalah skor angiografik untuk mengkuantifikasi
tingkat keparahan PJK. Sullivan Vessel Score dihitung dengan menjumlahkan jumlah pembuluh darah dengan stenosis >70% reduksi diameter lumen arteri Left Artery Descending (LAD), Left Circumflex (LCx),
Right Coronary Artery (RCA) dan stenosis >50% pada arteri Left Main
(LM). Hasil skor tergantung jumlah pembuluh darah yang terdapat stenosis, yaitu 0, 1, 2, dan 3.18 Skor 0 menunjukkan tidak adanya pembuluh darah dengan stenosis bermakna. Skor 1 menunjukkan adanya satu pembuluh darah dengan stenosis bermakna. Skor 2 menunjukkan adanya dua pembuluh darah dengan stenosis bermakna. Skor 3 menunjukkan adanya tiga pembuluh darah dengan stenosis bermakna. Pada penelitian yang dilakukan oleh Ian Neeland dkk, didapatkan skor Sullivan mempunyai korelasi terhadap keparahan dan luas plak aterosklerosis yang dinilai menggunakan IVUS (Spearman's multiple rho rank correlation: 0.76, p<0.0001).7
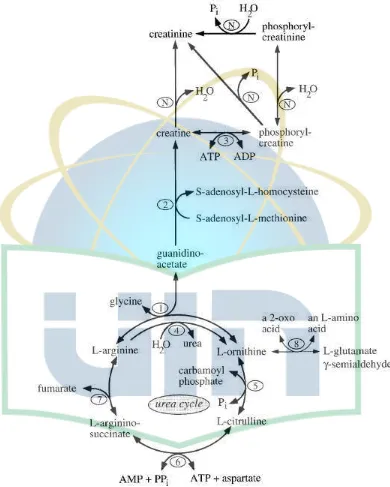
2.1.4 Kreatinin
Gambar 2.7 Metabolisme kreatin dan kreatinin20
dapat digunakan untuk menentukan laju filtrasi glomerulus (LFG) dengan rumus dari Modification of Diet in Renal Disease (MDRD)22, yaitu:
LFG (mL/menit/1.73 m2 ) = 186 x (PCr [mg/dL])-1.154x (umur)-0.203 x (0.742 jika perempuan)
Nilai kreatinin dalam serum ataupun plasma yang meningkat dapat menunjukan adanya penurunan fungsi ginjal. Nilai normal kreatinin adalah <1,2 mg/dl. Pasien dikatakan mempunyai nilai kreatinin yang tinggi jika nilai kreatinin 1,2 mg/dl.8
2.1.5 Hubungan Kreatinin dengan Tingkat Keparahan Penyakit Jantung Koroner
Banyak penelitian yang menunjukkan bahwa nilai kreatinin dapat dijadikan faktor prediktor independen terhadap penyakit kardiovaskuler. Pada penelitian yang dilakukan oleh Akanda, et al, ditemukan bahwa peningkatan kreatinin serum adalah faktor risiko independen untuk penyakit jantung koroner dengan hazard ratio (HR): 3.9, p<0.001.8 Penelitian yang dilakukan oleh Sule Korkmaz, et al, ditemukan bahwa kreatinin dapat dijadikan sebagai faktor prediktor tingkat keparahan PJK menggunakan Sullivan Extent Score (RR: 3.814, 95% CI: 2.149-6.768, p<0.0001) dan Sullivan Stenosis Score (RR: 4.037, 95% CI: 2.530-6.443, p<0.0001)10
Walaupun banyak penelitian yang menunjukkan bahwa kreatinin dapat dijadikan faktor prediktor penyakit jantung koroner, penelitian-penelitian tersebut masih belum bisa menjelaskan hubungan secara langsung antara kreatinin dengan penyakit jantung koroner.
dapat menyebabkan efek yang berbahaya bagi pasien penyakit jantung koroner.12 Terdapat beberapa mekanisme yang mendasari hal tersebut, yakni:
Insufisiensi ginjal akan menyebabkan metabolisme abnormal dari protein dan asam amino sehingga menyebabkan kadar homosistein meningkat. Hiperhomosisteinemia (kadar homosistein: 12 µmol/l. Kadar normal: 6 µmol/hari) sudah dapat terjadi pada pasien dengan LFG <60 ml/menit. Kadar homosistein yang meningkat akan menginduksi disfungsi endotel dan abnormalitas faktor koagulan dan platelet. 23,24,25,26
Insufisiensi ginjal akan menyebabkan berkurangnya Apo-I dan Apo-II, maturasi high density protein (HDL) terganggu, fungsi antioksidan dari HDL terganggu, serta pembersihan lipoprotein tinggi trigliserida seperti
low density protein (LDL) dan very low density protein (VLDL)
terganggu sehingga kadarnya meningkat. Hal tersebut akan menyebabkan inti lemak dari plak aterosklerosis semakin besar sehingga plak mudah ruptur.27,28
Sel tubular proksimal ginjal merupakan sumber utama glutathione
peroxidase yang merupakan antioksidan.29 Glutathione peroxidase akan
Ketiga mekanisme tersebut dapat mendorong terjadinya pembentukan plak aterosklerosis pembuluh darah koroner dan menimbulkan stenosis sehingga pasien mengalami penyakit jantung koroner.
2.3 Kerangka Konsep
Jumlah pembuluh darah dengan stenosis >70% reduksi pada arteri Left Artery Descending (LAD), Left Circumflex (LCx), Right Coronary Artery (RCA) dan stenosis >50% pada arteri Left Main (LM).
2.4 Definisi Operasional
No. Variabel Definisi Alat Ukur Cara Pengukuran Skala
Pengukuran
Diagnosis berdasarkan anamnesis, gambaran EKG, dan biomarker jantung
Diagnosis penyakit jantung iskemik stabil didapat dari anamnesis berupa adanya nyeri dada transien yang dapat diprediksi. Nyeri dada muncul saat pasien
mengalami stres
emosional dan aktivitas fisik yang berlebih. Selain
Nominal Ya
terdiri dari
itu, diagnosis penyakit jantung iskemik stabil didapat dari hasil angiografi
stenosis >50% pada arteri Left Main (LM). Hasil
skor tergantung jumlah pembuluh
darah yang
terdapat stenosis, yaitu 0, 1, 2, dan 3.18
3 Kreatinin Produk akhir
metabolisme otot yang dilepaskan ke sirkulasi secara konstan.19
Rekam medis
Sesuai yang tertera dalam rekam medis.
Kategorik Nilai kreatinin normal (<1,2 mg/dl)
BAB III
METODE PENELITIAN
3.1 Desain Penelitian
Desain penelitian ini menggunakan desain kohort retrospektif berbasis penelitian prognostik.
3.2 Lokasi Dan Waktu Penelitian
Penelitian ini dilakukan di RS Hermina Bekasi pada September-Oktober 2016
3.3 Populasi dan Sampel Penelitian 3.3.1 Populasi
Populasi target adalah pasien penyakit jantung koroner yang menjalani angiografi koroner.
Populasi terjangkau adalah pasien penyakit jantung koroner yang menjalani angiografi koroner yang dirawat di RS Hermina Bekasi pada Januari-Oktober 2016.
3.3.2 Sampel dan Cara Pemilihan Sampel
Sampel penelitian adalah populasi terjangkau yang memenuhi kriteria inklusi penelitian. Pemilihan sampel dengan metode konsekutif
3.3.3 Perkiraan Besar Sampel
Besar sampel minimal untuk penelitian prognostik dihitung dengan rumus Rule of Thumbs
Keterangan: n = besar sampel
Vb = Jumlah variable bebas yang diteliti
p = Prevalensi pasien yang terbukti mengalami PJK yang signifikan setelah pemeriksaan angiografi koroner
Pada studi sebelumnya diketahui prevalensi pasien yang terbukti mengalami PJK yang signifikan setelah pemeriksaan angiografi koroner adalah 78,82%8 sehingga besar sampel yang diperlukan untuk penelitian adalah 76 sampel.
3.4 Kriteria Inklusi dan Eksklusi 3.4.1 Kriteria Inklusi
Pasien PJK yang mempunyai data rekam medis mengenai identitasnya, diagnosis penyakitnya, tindakan angiografi koroner yang diterimanya, hasil pemeriksaan laboratorium, nilai serum kreatinin sebelum pemeriksaan angiofrafi koroner, dan dirawat di RS Hermina Bekasi.
3.4.2 Kriteria Eksklusi
3.5 Cara Kerja Penelitian
Mengambil data sampel penelitian dari rekam medis, meliputi:
Identitas pasien
Data anamnesis
Hasil laboratorium: hemoglobin, hematokrit, leukosit, trombosit, ureum, gula darah sewaktu
Kreatinin pasien
Diagnosis penyakit jantung koroner pasien (Sindrom Koroner Akut: UAP, NSTEMI, dan STEMI)
Laporan angiografi koroner
3.6 Alur Penelitian
Populasi Target: Pasien PJK yang menjalani angiografi koroner
Populasi Terjangkau: Pasien PJK yang menjalani angiografi koroner dan dirawat di RS Hermina Bekasi
Sampel memenuhi kriteria inklusi dan tanpa kriteria eksklusi
Ya Tidak
Diikutsertakan dalam penelitian
Pengumpulan data rekam medis
Analisis dan pengolahan data
3.7 Analisis dan Pengolahan Data
Pada penelitian ini, variabel independen dipresentasikan dalam bentuk frekuensi dan persentase atau rata-rata dan standar deviasinya. Pengolahan data menggunakan program SPSS versi 22.0. Dilakukan analisis bivariat antara faktor prediktor, yakni nilai kreatinin dengan tingkat keparahan PJK berdasarkan
Sullivan vessel score menggunakan uji Chi Square untuk mendapatkan risiko
relatif dan interval kepercayaan. Kemudian dilakukan analisis multivariat menggunakan regresi logistik untuk mendapatkan odds ratio dan interval kepercayaan.
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
4.1.1 Karakteristik Dasar Subjek Penelitian
Data penelitian diambil dari RS Hermina Bekasi berdasarkan data pasien penyakit jantung koroner yang menjalani pemeriksaan angiografi koroner sejak Januari 2016 sampai Oktober 2016 dan memenuhi kriteria inklusi penelitian. Hasil penelitian secara terperici sebagai berikut:
Tabel 4.1 Karakteristik Dasar Subjek Penelitian
Karakteristik Frekuensi
Penyakit Ginjal Kronik 5 (5,7%)
Penyakit iskemik jantung stabil 36 (40,9%)
Tabel 4.2 Karakteristik Hasil Laboratorium Subjek Penelitian
hemoglobin hematokrit leukosit trombosit ureum Gula Darah Sewaktu
Rata-rata 14,08 40,60 9.212,05 262.931,82 32,9 137,91
Median 14.10 40,55 8.780,00 246.000 30 115,50
Std. Deviasi 1,84 4,72 2.910,27 80.512,69 10,54 63,25
Range 10,30 29 15.240 455.000 55,6 366
Minimum 9,50 29,10 3.990 27.000 13,3 72
Maksimum 19,80 58,10 19.230 482.000 68,9 438
Dalam kurun waktu dari Januari-Oktober 2016, terdapat 90 pasien PJK yang menjalani pemeriksaan angiografi koroner. Di antara 90 pasien tersebut, terdapat 2 pasien dieksklusi karena data pada rekam medis tidak lengkap. Sehingga jumlah sampel pada karakteristik dasar penelitian ini adalah 88 pasien.
4.1.2 Analisis Univariat
Tabel 4.3 Distribusi Frekuensi Kreatinin, Penyakit Jantung Koroner, dan Sullivan Vessel Score
Karakteristik Frekuensi
Kreatinin
< 1,2 mg/dl
1,2 mg/dl Rata-rata ± SD
55 (61,6%) 33 (38,4%) 1,10 ± 0,34 Penyakit Jantung Koroner
Penyakit jantung iskemik stabil
Sindrom koroner akut
36 (41,9%)
50 (58,1%) Sullivan Vessel Score
1
2
3
4.1.3 Analisis Bivariat
Hasil analisis bivariat antara nilai kreatinin dan tingkat keparahan PJK berdasarkan Sullivan Vessel Score adalah sebagai berikut:
Tabel 4.4 Hubungan Nilai Kreatinin dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score
Sullivan Vessel Score
Total
1 2 3
Kreatinin <1,2 Frekuensi 27 16 10 53
Persentase 79,4% 48,5% 52,6% 61,6%
>=1,2 Frekuensi 7 17 9 33
Persentase 20,6% 51,5% 47,4% 38,4%
Total Frekuensi 34 33 19 86
Persentase 100,0% 100,0% 100,0% 100,0%
Tabel 4.5 Hubungan Nilai Kreatinin dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score 1 vs 3
Dari uji Chi Square didapatkan RR: 3.47, 95% CI: 1,01-11,82, p<0.05
Tabel 4.6 Hubungan Nilai Kreatinin dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score 1 vs 2
Sullivan Vessel Score
Total
1 2
Kreatinin <1,2 Frekuensi 27 16 43
Persentase 79,4% 48,5% 64,2%
>=1,2 Frekuensi 7 17 24
Persentase 20,6% 51,5% 35,8%
Total Frekuensi 34 33 67
Persentase 100,0% 100,0% 100,0%
Dengan uji Chi Square didapatkan RR: 4,1, 95% CI: 1,34-12,02, p <0.05 Sullivan Vessel Score
Total
1 3
Kreatinin <1,2 Frekuensi 27 10 37
Persentase 73,0% 27,0% 100,0%
>=1,2 Frekuensi 7 9 16
Persentase 43,8% 56,3% 100,0%
Total Frekuensi 34 19 53
Tabel 4.7 Hubungan Nilai Kreatinin dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score 2 vs 3
Sullivan Vessel Score
Dengan uji Chi Square didapatkan RR: 0,85, 95% CI: 0,27-2,62, p >0.05
4.1.4 Analisis Multivariat
Karena pada penelitian ini hanya didapatkan satu faktor risiko atau faktor independen yang berhubungan, yakni kreatinin, maka penelitian hanya dapat dilakukan sampai analisis bivariat.
4.2 Pembahasan
4.2.1 Karakteristik Subjek Penelitian
dengan diabetes (23,9%), 60 orang dengan gagal jantung (68,2%), 5 orang gagal ginjal (5,7%), 36 orang menderita penyakit iskemik jantung stabil (40,9%), dan 52 orang menderita sindrom koroner akut (59,1%).
Karakteristik hasil pemeriksaan laboratorium subjek penelitian adalah sebagai berikut: rata-rata kadar hemoglobin adalah 14,08 ± 1,84 g/dl, rata-rata hematokrit adalah 40,6 ± 1,84 %, rata-rata jumlah leukosit adalah 9.212,05 ± 2.910,21 /µl, rata-rata jumlah trombosit adalah 262.931,82 ± 80.512,69 /µl, rata-rata kadar ureum adalah 32,9 ± 10,54 mg/dl, dan rata-rata kadar gula darah sewaktu adalah 137,91 ± 63,25 g/dl.
4.2.2 Hubungan Nilai Kreatinin dengan Tingkat Keparahan Penyakit Jantung Koroner berdasarkan Sullivan Vessel Score
Penelitian ini menunjukkan bahwa terdapat hubungan antara nilai kreatinin dengan tingkat keparahan penyakit jantung koroner berdasarkan
Sullivan Vessel Score (p < 0,05). Dengan analisis bivariat menggunakan Chi
Square, didapatkan bahwa pasien yang mempunyai nilai kreatinin < 1,2 mg/dl
mempunyai kemungkinan 3,47 kali untuk mengalami tingkat keparahan PJK dengan SVS lebih kecil yaitu 1 (bila dibandingkan dengan SVS 3, dengan RR:3.47, 95% CI: 1,01-11,82, p<0.05). Pasien yang mempunyai nilai kreatinin <1,2 mg/dl mempunyai kemungkinan 4,1 kali untuk mengalami tingkat keparahan PJK dengan SVS lebih kecil yaitu 1 (bila dibandingkan dengan SVS 3, dengan RR: 4,1, 95% CI: 1,34-12,02, p<0.05). Sedangkan jika variabel dependen dibandingkan antara SVS 2 dengan SVS, maka didapatkan hasil yang tidak bermakna (RR: 0,85, 95% CI: 0,27-2,62 p > 0,05).
hazard ratio (HR): 3.9, p<0.001.8 Hasil penelitian ini juga sesuai dengan penelitian yang dilakukan oleh Sule Korkmaz, et al, yang menemukan bahwa kreatinin dapat dijadikan sebagai faktor prediktor tingkat keparahan PJK menggunakan Sullivan Extent Score (RR: 3.814, 95% CI: 2.149-6.768, p<0.0001) dan Sullivan Stenosis Score (RR: 4.037, 95% CI: 2.530-6.443, p<0.0001)10
Walaupun tidak berhubungan secara langsung, kreatinin dapat dihubungkan dengan fungsi ginjal dan masih digunakan untuk menghitung laju filtrasi glomerulus. Nilai kreatinin yang meningkat menunjukan penurunan fungsi ginjal. Penurunan fungsi ginjal akan meningkatkan faktor risiko penyakit kardiovaskular seperti peningkatan kadar homosistein, stres oksidatif, partikel kolesterol, serta remodeling ventrikel.12
4.3 Keterbatasan Penelitian
Penelitian ini memiliki beberapa keterbatasan, antara lain:
Desain Penelitian
Penelitian ini menggunakan desain kohort retrospektif dengan menggunakan data sekunder yaitu rekam medis. Jika ada data inklusi penelitian yang tidak tercantum dalam rekam medis, maka pasien tidak bisa menjadi subjek dalam penelitian
Jumlah Sampel
Pada penelitian ini hanya meneliti 86 subjek
Tidak dapat meneliti faktor prediktor lain
BAB V
SIMPULAN DAN SARAN
5.1 Simpulan
Penyakit jantung koroner di RS Hermina Bekasi meliputi 36 (41,9%) kasus penyakit jantung iskemik stabil dan 50 (58,1%) kasus sindrom koroner akut
Prevalensi pasien PJK yang mempunyai SVS sebesar 1 adalah sebanyak 34 orang (39,5%). Sedangkan 33 orang (38,4%) mempunyai skor 2, dan 19 orang (22,1%) mempunyai skor 3.
Rata- rata nilai kreatinin pasien PJK di RS Hermina Bekasi adalah 1,38 ± 0,48 mg/dl. Pasien dengan nilai kreatinin <1,2 mg/dl adalah sebanyak 53(61,6%) dan pasien dengan nilai kreatinin ≥1,2 mg/dl adalah sebanyak 33(38,4%).
Nilai kreatinin pasien mempunyai hubungan yang bermakna dengan tingkat keparahan PJK berdasarkan Sullivan Vessel Score pada pasien PJK di RS Hermina Bekasi (p <0,05). Pasien yang mempunyai nilai kreatinin <1,2 mg/dl mempunyai kemungkinan 3,47 kali untuk mengalami tingkat keparahan PJK dengan SVS lebih kecil yaitu 1 (bila dibandingkan dengan SVS 3, dengan RR: 3.47, 95% CI: 1,01-11,82, p<0.05). Pasien yang mempunyai nilai kreatinin <1,2 mg/dl mempunyai kemungkinan 4,1 kali untuk mengalami tingkat keparahan PJK dengan SVS lebih kecil yaitu 1 (bila dibandingkan dengan SVS 3, dengan RR: 4,1, 95% CI: 1,34-12,02, p<0.05). Sedangkan jika variabel dependen dibandingkan antara SVS 2 dengan SVS 3, maka didapatkan hasil yang tidak bermakna (RR: 0,85, 95%CI: 0,27-2,62 p >0,05).
5.2 Saran
DAFTAR PUSTAKA
1
American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Heart disease and stroke statistics— 2015 update: a report from the
American Heart Association. Diunduh dari:
https://www.heart.org/idc/groups/ahamahpublic/@wcm/@sop/@smd/documents/dow
nloadable/ucm_470704.pdfpada tanggal 2 Febuari 2016
2
Badan Penelitian dan Pengembangan Kesehatan. Laporan Hasil Riset Kesehatan Dasar 2013. Diunduh dari:
http://terbitan.litbang.depkes.go.id/penerbitan/index.php/blp/catalog/book/64pada
tanggal 2 Febuari 2016
3
Lilly, Leonard S. 2011. Pathophysiology of Heart Disease 5th Ed. Philadelphia: Lippincott Williams & Wilkins
4
Bonow RO, Mann DL, Zipes DP, Libby P, Braunwald E. 2012. Braunwald’s Heart
Disease: A Textbook Of Cardiovascular Medicine 9th Ed. Philadelpia: Elsevier
Saunders
\5
Anderson, MD, Novak, PD, Van Pelt, L, et al. 2012. Dorland’s Illustrated Medical
Dictionary 32nd Edition. Philadelpia: Elsevier Saunders
6
Annapoorna SK. Coronary angiography, lesion classificationand severity assessment. Cardiol Clin. 2006; 24:153–162
7
8
MAK Akanda, KN Choudhury, MZ Ali, et al. Serum creatinine and blood urea nitrogen levels in patients with coronary artery disease. Cardiovasc J. 2013; 5(2): 141-145
9
Powell J, Hicham S, Nagesh A. Increase in creatinine and cardiovascular risk in patients with systolik disfunction after myocardial infarction. J Am Soc Nephrol. 2006; 17: 2886 –2891
10
Sule K, Burcu D, Hakan A, et al. Serum creatinine is independently associated with angiographic extent of coronary artery disease in patients with stable angina pectoris. Anadolu Kardiyol Derg. 2011; 11: 407-413
11
F Irie, H Iso, TT Sairenchi, et al. The relationships of proteinuria, serum creatinine, glomerular filtration rate with cardiovascular disease mortality in Japanese general population. Kidney International.2006; 69: 1264–1271.
12
Guruprasad M, Hocine T, Hassan I. Level of kidney function as a risk factor for atherosclerotic cardiovascular outcomes in the community. J o Am Coll o Cardiology. 2003; 41(1):47-55
13
Glenn NL, Eric RB, James CB, et al. 2011 ACCF/AHA/SCAI Guideline for Percutaneous Coronary Intervention. Diunduh pada tanggal 3 April 2016 dari
http://circ.ahajournals.org
14
Manesh RP, Gregory JD, John WH, et al. ACCF/SCAI/STS/AATS/AHA/ASNC /HFSA/SCCT 2012 Appropriate Use Criteria for Coronary Revascularization
Focused Update. Diunduh dari
http://content.onlinejacc.org/cgi/content/full/j.jacc.2011.12.001v1 pada 3 September
15
www.nhlbi.nih.gov/files/images/Percutaneous-Coronary-Intervention-With-Stent-Placement.jpg
16
Baim, Donald S. 2006. Grossman's Cardiac Catheterization, Angiography, and Intervention 7th Edition. Philadelpia: Lippincott Williams and Wilkins
17
Bitar, S, Bleyer, F, Bradley, A, et al. 2003. The Cardiac Catheterization Handbook
4th Edition. Philadelpia: Mosby
18
Farhanah M, Nugroho EP. Correlation between plasma nitric oxide level and coronary artery stenosis severity based on sullivan scoring system in stable angina patients. Folia Medica Indonesiana. January – March 2015; 51(1): 22-30
19
Lieberman, M, Marks, AD. 2013. Marks’ Basic Medical Biochemistry: A Clinical Approach Fourth Edition. Baltimore: Lippincott Williams and Wilkins
20
Markus W, Rima K. Creatine and creatinine metabolism. Physiological Review. 2000; 80(3): 1108-1182
21
Sherwood, Lauralee. 2009. Fisiologi Manusia dari Sel ke Sistem Edisi 6. Jakarta: Penerbit Buku Kedokteran EGC
22
Kavoussi, LR, Novick, AC, Partin, AW, et al. 2012. Campbell-Walsh Urology, Tenth Edition. Philadelphia: Elsevier
23
Killian Robinson. Renal disease, homocysteine, and cardiovascular complications. Circulation. 2004;109:294-295
24
Coen VG. Why is homocysteine elevated in renal failure and what can be expected from homocysteine-lowering?. Nephrol Dial Transplant.May 2006; 21(5): 1161-1166.
25
Suliman ME, Lindholm B, Barany P, et al. Hyperhomocysteinemia in chronic renal failure patients: relation to nutritional status and cardiovascular disease. Clin Chem
26
Paul G, Sreyoshi FA. Role of homocysteine in the development of cardiovascular disease. Nutr J. 2015; 14: 6
27
Vaziri ND. Causes of dysregulation of lipid metabolism in chronic renal failure. Semin Dial. 2009 Nov-Dec;22(6):644-51
28
Eberhard R, Christoph W. Lipid abnormalities and cardiovascular risk in renal disease. J o Am Soc o Nephrol. June 2008; 19 (6): 1065-1070
29
El-Far MA, Bakr MA, Farahat SE, et al. Glutathione peroxidase activity in patients with renal disorders. Clin Exp Nephrol. 2005 Jun;9(2):127-31
30
Stefan B, Hans JR, Christoph B, et al. Glutathione peroxidase 1 activity and cardiovascular events in patients with coronary artery disease. N Engl J Med. 2003; 349:1605-1613
31
Fellah H, Feki M, Souissi M, et al. Oxidative stress in end stage renal disease: evidence and association with cardiovascular events in Tunisian patients. Tunis Med.