PENGARUH PEMBERIAN PUPUK KASCING (Bekas Cacing)
TERHADAP KELIMPAHAN Nannochloropsis sp. SEBAGAI
PAKAN ALAMI
RINA MARITO DAULAY 090302067
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
PENGARUH PEMBERIAN PUPUK KASCING (Bekas Cacing)
TERHADAP KELIMPAHAN Nannochloropsis sp. SEBAGAI
PAKAN ALAMI
SKRIPSI
Oleh :
RINA MARITO DAULAY 090302067
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
PENGARUH PEMBERIAN PUPUK KASCING (Bekas Cacing)
TERHADAP KELIMPAHAN Nannochloropsis sp. SEBAGAI
PAKAN ALAMI
SKRIPSI
Oleh :
RINA MARITO DAULAY 090302067
Skripsi sebagai Satu diantara beberapa Syarat untuk memperoleh Gelar Sarjana Perikanan di Program Studi Manajemen Sumberdaya Perairan,
Fakultas Pertanian,Universitas Sumatera Utara
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
LEMBAR PENGESAHAN
Judul Penelitian : Pengaruh Pemberian Pupuk Kascing (Bekas Cacing) terhadap Kelimpahan Nannochloropsis sp. sebagai
Pakan Alami
Nama : Rina Marito Daulay
NIM : 090302067
Program Studi : Manajemen Sumberdaya Perairan
Menyetujui: Komisi Pembimbing
Pindi Patana, S. Hut. M. Sc Indra Lesmana, S. Pi. M. Si
Ketua Anggota
Mengetahui
Dr. Ir. Yunasfi, M. Si
ABSTRAK
RINA MARITO DAULAY. Pengaruh Pemberian Pupuk Kascing (Bekas Cacing)
terhadap Kelimpahan Nannochloropsis sp. sebagai Pakan Alami. Dibimbing oleh
PINDI PATANA dan INDRA LESMANA.
Perkembangan budidaya perikanan saat ini belum diiringi dengan
penyediaan benih yang memadai karena adanya hambatan dalam penyediaan
benih yang disebabkan kesulitan dalam penyediaan pakan alami dengan kualitas
yang baik. Kultur pakan alami Nannochloropsis sp. dengan menggunakan pupuk
kascing belum pernah dilakukan sebelumnya, sementara kandungan hara kascing
memiliki hara yang dibutuhkan oleh Nannochloropsis sp. untuk menunjang
pertumbuhan dan reproduksi. Penelitian bertujuan untuk mengetahui pengaruh
yang ditimbulkan oleh perlakuan pupuk kascing terhadap kelimpahan sel dan
untuk mengetahui konsentrasi optimum bagi pertumbuhan Nannochloropsis sp.
Penelitian ini dilakukan di Balai Budidaya Air Payau (BBAP) Ujung Batee,
Banda Aceh. Kultur pakan alami dilakukan dengan volume 10 liter selama 10
hari. Parameter yang diamati meliput pertumbuhan, dan kualitas air.
Rancangan percobaan menggunakan Rancangan Acak Lengkap (RAL)
dengan 5 perlakuan dan 3 ulangan. Sebagai perlakuan adalah kontrol dengan
menggunakan pupuk teknis (yang biasa digunakan), 0 ppm (tanpa perlakuan
pupuk kascing), 50 ppm, 100 ppm, dan 150 ppm. Hasil penelitian menunjukkan
bahwa pemberian pupuk kascing berpengaruh nyata terhadap pertumbuhan
kelimpahan Nannochloropsis sp. konsentrasi kascing yang optimum adalah 100
ppm dan puncak kepadatan tertinggi terjadi pada hari ke-5 dengan kepadatan
mencapai 6.895.000 sel/ml.
ABSTRACT
RINA MARITO DAULAY. The influenceof vermicompost fertilizer treatments on the growth abundance Nannochloropsis sp. as a food life this research was suvervised by PINDI PATANA and INDRA LESMANA.
The current of aquaculture depelopment does not accompanied with the fry supply sufficient because there are constraints in the supply of fry caused by difficulties in the supply of life food with good quality. The life food culture
Nannochloropsis sp. by using vermicompost fertilizer has never been used before, while the vermicompost contains nutrient required by cells of Nannochloropsis
sp. to support the growth and reproductions. The purpose of this research is to know the influence of the vermicompost fertilizer treatments on the growth abundance of the cells Nannochloropsis sp. and how much the optimum concentration. This research has been done in Balai Budidaya Air Payau (BBAP) Ujung Batee, Banda Aceh. The life food culture done with 10 liters volume of water abaut 10 days. Parameter were observe are the growth of abundance
Nannochloropsis sp. cells and quality of water.
The effort scheme used by completely randomized design with 5 treatments and 3 times repetitions. Those 5 treatments are as follows the control treatment with technical fertilizer, 0 ppm (without treatment vermicompost), 50 ppm, 100 ppm, and 150 ppm. The result of research shows that the used vermicompost fertilizer is effect on the growth Nannochloropsis sp., that is significant difference and the optimum concentration is 100 ppm and the medium aboundance is days 5 with density 6.895.000 cells/ml.
RIWAYAT HIDUP
Penulis dilahirkan di Panyabungan Kabupaten
Mandailing Natal, Provinsi Sumatera Utara pada
tanggal 11 April 1991 sebagai anak keempat dari
enam bersaudara pasangan Sahala Tua Daulay, S.Pd
dan Azizah Batubara. Penulis memulai jenjang
pendidikan formal di SDN 200112 Panyanggar,
Kota Padangsidimpuan sampai tahun 2003.
Penulis kemudian melanjutkan pendidikan di MTSN Model
Padangsidimpuan (tahun 2003 – 2006). Tahun 2009 penulis menyelesaikan
pendidikan menengah atas di SMA Neg. 6 Padangsidimpuan. Pada tahun yang
sama penulis diterima sebagai mahasiswa di Universitas Sumatera Utara melalui
jalur ujian tertulis Seleksi Penerimaan Mahasiswa Baru Program Studi
Manajemen Sumberdaya Perairan.
Selama masa perkuliahan penulis juga aktif sebagai anggota Ikatan
Mahasiswa Manajemen Sumberdaya Perairan (IMMASPERA). Penulis juga aktif
sebagai asisten praktikum mata kuliah Dasar Ilmu Perairan dan Ekotoksikologi
Perairan. Penulis melakukan Praktik Kerja Lapangan (PKL) di Balai Budidaya Air
Payau (BBAP) Ujung Batee, Banda Aceh mulai bulan Agustus sampai dengan
KATA PENGANTAR
Puji dan syukur penulis panjatkan atas kehadirat Allah SWT yang telah
memberikan nikmat kesehatan dan kesempatan sehingga penulis dapat
menyelesaikan skripsi yang berjudul “Pengaruh Pemberian Pupuk Kascing (Bekas
Cacing) terhadap Kelimpahan Nannochloropsis sp. sebagai Pakan Alami”.
Penulis mengucapkan terima ksih kepada kedua orang tua penulis
ayahanda Sahala Tua Daulay, S.Pd dan Ibu Azizah Batubara yang telah
melahirkan, merawat, dan mendidik serta memberikan dukungan yang sangat kuat
bagi penulis sehingga penulis sampai pada tahap ini. Penulis mengucapkan terima
kasih kepada Bapak Pindi Patana, S.Hut. M.Sc dan Bapak Indra Lesmana, S.Pi,
M.Si selaku pembimbing yang telah membantu penulis dalam menyelesaikan
skripsi ini, serta terima kasih penulis ucapkan kepada Bapak Dr. Ir. Yunasfi, M.Si
yang telah meluangkan waktunya dalam mengoreksi dan memberikan masukan
untuk menuju kesempurnaan penulisan skripsi ini.
Penulis berharap semoga skripsi ini dapat bermanfaat dalam
pengembangan ilmu dan pengetahuan khususnya bidang manajemen sumber daya
Hasil
Tingkat Kelimpahan Nannochloropsis sp. ... 24 Laju Kelimpahan Harian Nannochloropsis sp. ... 25 Kualitas Air ... 25
Pembahasan
Tingkat Kelimpahan Nannochloropsis sp. ... 26 Laju Kelimpahan Nannochloropsis sp. ... 27 Kualitas Air ... 30
KESIMPULAN DAN SARAN
Kesimpulan ... 34 Saran ... 34
DAFTAR TABEL
No. Teks Halaman
1.Data Kisaran Kualitas Air ... 26
DAFTAR GAMBAR
No. Teks Halaman
1. Kerangka Pemikiran Penelitian ... 4
2. Nannochloropsis sp. ... 7
3. Sel Nannochloropsis sp. ... 8
4. Pupuk Organik Kascing ... 16
5. Susunan Media Uji Acak ... 20
6. Perbandingan Rata-rata Kelimpahan Nannochloropsis sp. setiap Perlakuan ... 24
7. Peningkatan Kelimpahan Nannochloropsis sp. pada setiap Perlakuan . 25
DAFTAR LAMPIRAN
No. Teks Halaman
1.Analisis rata-rata Kelimpahan sel Nannochloropsis sp. ... 37
2.Alat dan Bahan ... 40
3.Data Kelimpahan Nannochloropsis sp. ... 43
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Yang bertanda tangan dibawah ini:
Nama : Rina Marito Daulay
NIM : 090302067
Menyatakan bahwa skripsi yang berjudul “Pengaruh Pemberian Pupuk
Kascing (Bekas Cacing) terhadap Kelimpahan Nannochloropsis sp. sebagai Pakan
Alami.” adalah hasil karya saya dan bukan merupakan duplikasi sebagian atau
seluruhnya dari karya orang lain, kecuali bagian yang sumber informasi
dicantumkan.
Pernyataan ini dibuat dengan sebenar-benarnya secara sadar dan
bertanggung jawab dan saya bersedia menerima sanksi pembatalan skripsi apabila
terbukti melakukan duplikasi terhadap skripsi atau karya ilmiah orang lain yang
sudah ada.
Medan, Mei 2014
ABSTRAK
RINA MARITO DAULAY. Pengaruh Pemberian Pupuk Kascing (Bekas Cacing)
terhadap Kelimpahan Nannochloropsis sp. sebagai Pakan Alami. Dibimbing oleh
PINDI PATANA dan INDRA LESMANA.
Perkembangan budidaya perikanan saat ini belum diiringi dengan
penyediaan benih yang memadai karena adanya hambatan dalam penyediaan
benih yang disebabkan kesulitan dalam penyediaan pakan alami dengan kualitas
yang baik. Kultur pakan alami Nannochloropsis sp. dengan menggunakan pupuk
kascing belum pernah dilakukan sebelumnya, sementara kandungan hara kascing
memiliki hara yang dibutuhkan oleh Nannochloropsis sp. untuk menunjang
pertumbuhan dan reproduksi. Penelitian bertujuan untuk mengetahui pengaruh
yang ditimbulkan oleh perlakuan pupuk kascing terhadap kelimpahan sel dan
untuk mengetahui konsentrasi optimum bagi pertumbuhan Nannochloropsis sp.
Penelitian ini dilakukan di Balai Budidaya Air Payau (BBAP) Ujung Batee,
Banda Aceh. Kultur pakan alami dilakukan dengan volume 10 liter selama 10
hari. Parameter yang diamati meliput pertumbuhan, dan kualitas air.
Rancangan percobaan menggunakan Rancangan Acak Lengkap (RAL)
dengan 5 perlakuan dan 3 ulangan. Sebagai perlakuan adalah kontrol dengan
menggunakan pupuk teknis (yang biasa digunakan), 0 ppm (tanpa perlakuan
pupuk kascing), 50 ppm, 100 ppm, dan 150 ppm. Hasil penelitian menunjukkan
bahwa pemberian pupuk kascing berpengaruh nyata terhadap pertumbuhan
kelimpahan Nannochloropsis sp. konsentrasi kascing yang optimum adalah 100
ppm dan puncak kepadatan tertinggi terjadi pada hari ke-5 dengan kepadatan
mencapai 6.895.000 sel/ml.
ABSTRACT
RINA MARITO DAULAY. The influenceof vermicompost fertilizer treatments on the growth abundance Nannochloropsis sp. as a food life this research was suvervised by PINDI PATANA and INDRA LESMANA.
The current of aquaculture depelopment does not accompanied with the fry supply sufficient because there are constraints in the supply of fry caused by difficulties in the supply of life food with good quality. The life food culture
Nannochloropsis sp. by using vermicompost fertilizer has never been used before, while the vermicompost contains nutrient required by cells of Nannochloropsis
sp. to support the growth and reproductions. The purpose of this research is to know the influence of the vermicompost fertilizer treatments on the growth abundance of the cells Nannochloropsis sp. and how much the optimum concentration. This research has been done in Balai Budidaya Air Payau (BBAP) Ujung Batee, Banda Aceh. The life food culture done with 10 liters volume of water abaut 10 days. Parameter were observe are the growth of abundance
Nannochloropsis sp. cells and quality of water.
The effort scheme used by completely randomized design with 5 treatments and 3 times repetitions. Those 5 treatments are as follows the control treatment with technical fertilizer, 0 ppm (without treatment vermicompost), 50 ppm, 100 ppm, and 150 ppm. The result of research shows that the used vermicompost fertilizer is effect on the growth Nannochloropsis sp., that is significant difference and the optimum concentration is 100 ppm and the medium aboundance is days 5 with density 6.895.000 cells/ml.
PENDAHULUAN
Latar Belakang
Perkembangan budidaya perikanan yang berkembang pesat pada saat ini
belum diiringi dengan upaya penyediaan benih yang memadai. Hambatan dalam
penyediaan benih ini salah satunya disebabkan oleh karena adanya kesulitan
dalam penyediaan pakan alami dengan kualitas yang baik. Selain itu, kendala lain
adalah tingkat mortalitas yang tinggi pada stadia awal larva. Salah satu penyebab
tingginya tingkat kematian pada stadia larva adalah kegagalan larva pada awal
pemangsaan. Keberhasilan larva pada awal pemangsaan dipengaruhi oleh
kepadatan pakan alami, ukuran pakan alami dan kandungan gizinya (Fajar, 2005).
Pakan terdiri atas pakan alami dan pakan buatan. Pakan alami adalah
pakan yang telah tersedia langsung di alam, contohnya mikro/makro alga dan
mikro/makro bentos. Zooplankton adalah salah satu pakan alami yang
digunakan dalam usaha pembenihan. Jenis zooplankton yang digunakan sebagai
pakan alami adalah rotifer (Brachionus plicatilis). Sebagai zooplankton rotifer
memakan fitoplankton, dan salah satu jenis fitoplankton yang digunakan sebagai
pakan alami adalah Nannochloropsis sp. (Irwanto, dkk, 2012).
Nannochloropsis sp. sebagai mikro alga yang dibudidayakan di dalam
air juga membutuhkan pupuk untuk mencukupi kebutuhan unsur hara.
Berbagai unsur hara, baik mikronutrien maupun makronutrien sangat
dibutuhkan untuk menunjang kehidupan dan pertumbuhan mikro alga tersebut.
Penambahan unsur hara pada Nannochloropsis sp. akan mempengaruhi
banyak digunakan berbagai macam pupuk seperti pupuk kompos, walne, urea,
ZA, EDTA, SP36, dengan penambahan vitamin B12, dan lain-lain.
Pupuk organik kascing (bekas cacing) merupakan pupuk yang berasal dari
hasil metabolisme cacing yang diketahui mengandung banyak unsur hara mikro
dan makro yang dibutuhkan oleh tumbuhan pada umumnya. Kascing mengandung
nitrogen, fosfor, kalium, belerang, magnesium, dan besi yang mampu menunjang
kehidupan, pertumbuhan dan reproduksi fitoplankton.
Sejauh ini belum ada penelitian yang meneliti apakah pupuk kascing dapat
digunakan dalam kultur pakan alami yakni fitoplakton seperti Nannochloropsis
sp. karena ditinjau dari koposisi kandungan kascing yang memiliki hara makro
dan mikro yang mampu menunjang pertumbuhan dan reproduksi Nannochloropsis
sp. oleh karena itu penulis melakukan penelitian “Pengaruh Pemberian Pupuk
Kascing (bekas cacing) terhadap Kelimpahan Nannochloropsis sp. sebagai Pakan
Alami” sehingga diharapkan pemberian pupuk kascing dapat meningkatkan
kepadatan sel serta mendapatkan konsentrasi yang optimum bagi pertumbuhan
Nannochloropsis sp.
Perumusan Masalah
Penelitian tentang kultur pakan alami Nannochloropsis sp. mengunakan
berbagai jenis pupuk yang berbeda-beda untuk mengetahui tingkat kelimpahan
Nannochloropsis sp. sudah banyak dilakukan. contohnya dengan menggunakan
pupuk NPK, kompos, walne, ZA, EDTA, urea, SP36 dan lain-lain, namun sejauh
ini belum ada penelitian yang menggunakan pupuk kascing (bekas cacing) dalam
kandungan hara yang dibutuhkan oleh fitoplankton dalam siklus hidupnya untuk
pertumbuhan, kelangsungan hidup dan reproduksinya.
Berdasarkan uraian diatas dapat dirumuskan beberapa permasalahan
sebagai berikut:
1. Bagaimana pengaruh pupuk kascing terhadap kelimpahan
Nannochloropsis sp. yang dikultur dalam ruangan semi outdoor ?
2. Seberapa besar tingkat kelimpahan Nannochloropsis sp. yang dikultur
dengan pupuk kascing dibandingkan dengan perlakuan kontrol ?
3. Berapa konsentrasi optimum yang digunakan untuk pertumbuhan
Nannochloropsis sp. ?
Tujuan
Tujuan dari penelitian ini adalah sebagai berikut :
1. Untuk mengetahui pengaruh pupuk kascing (bekas cacing) terhadap
kelimpahan Nannochloropsis sp. yang dikultur dalam ruangan semi
outdoor.
2. Mengetahui berapa konsentrasi yang optimum bagi pertumbuhan
Nannochloropsis sp.
Manfaat
Manfaat penelitian ini adalah sebagai terobosan baru dalam kultur pakan
alami khususnya Nannochloropsis sp. dengan menggunakan pupuk kascing
(bekas cacing) yang dapat diaplikasikan oleh pembudidaya ikan dengan mudah
dan murah dalam waktu yang relatif singkat sehingga kebutuhan nutrisi ikan
Hipotesis
Pemberian pupuk kascing (bekas cacing) dalam kultur pakan alami dapat
meningkatkan kelimpahan Nannochloropsis sp.
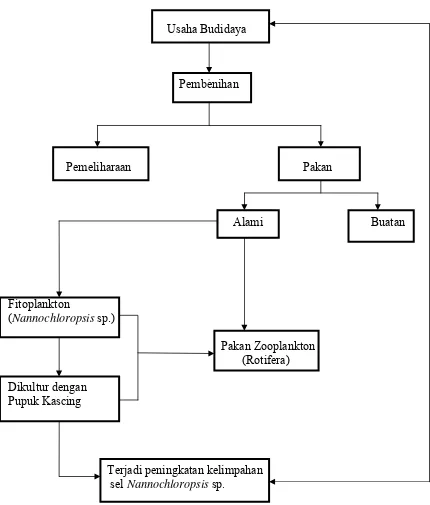
Kerangka Pemikiran
Usaha Budidaya
Pembenihan
Pemeliharaan Pakan
Alami Buatan
Fitoplankton
(Nannochloropsis sp.)
Pakan Zooplankton
(Rotifera)
Dikultur dengan Pupuk Kascing
Terjadi peningkatan kelimpahan sel Nannochloropsis sp.
TINJAUAN PUSTAKA
Fitoplankton
Fitoplankton merupakan mikro alga sehingga dalam dunia pembenihan
sering hanya disebut alga. Alga merupakan organisme yang tersedia melimpah
di alam dan dibedakan menjadi 1.800 genus dan 21.000 spesies. Alga mikro
mempunyai tingkat pertumbuhan lebih cepat dibandingkan dengan tanaman
terestrial. Menurut Inansetyo dan Kurniastuty (1995), terdapat beberapa alga
mikro yang berpotensi untuk dibudidayakan baik sebagai pakan alami di bidang
perikanan maupun sebagai sumber energi alternatif baru, diantaranya yaitu
Chlorella, Nannochloropsis, Skeletonema, Tetraselmis, Dunaliella, Scenedesmus,
dan Spirulina.
Fitoplankton merupakan kelompok yang memegang peranan sangat
penting dalam ekosistem air, karena kelompok ini dengan adanya kandungan
klorofil mampu melakukan fotositesis. Proses fotosintesis pada ekosistem air yang
dilakukan oleh fitoplankton (produsen), merupakan sumber nutrisi utama bagi
kelompok organisma air lainnya yang membentuk rantai makanan. Dalam
ekosistem air hasil dari fotosintesis yang dilakukan oleh fitoplankton bersama
dengan tumbuhan air lainnya disebut sebagai produktivitas primer (Barus, 2004).
Pertumbuhan suatu jenis fitoplankton sangat erat kaitannya dengan
ketersediaan hara makro dan mikro serta dipengaruhi oleh kondisi lingkungan.
Pada kultur fitoplankton sangat dibutuhkan berbagai macam senyawa organik baik
sebagai hara makro (N, P, K, S, Na, Si, dan Ca) maupun hara mikro (Fe, Zn, Mn,
Cu, Mg, Mo, Co, B dan lain-lain). Setiap unsur hara mempunyai fungsi- fungsi
mengesampingkan pengaruh kondisi lingkungan. Unsur N, P, dan S penting untuk
pembentukan protein, dan K berfungsi dalam pembentukan metabolisme
karbohidrat. Fe dan Na berperan untuk pembentukan klorofil. Sedangkan Si dan
Ca merupakan bahan untuk pembentukan dinding sel atau cangkang. B12 banyak
digunakan untuk memacu pertumbuhan melalui rangsangan fotosintetik
(Isnansetyo dan Kurniastuty, 1995).
Fitoplankton dalam pembenihan dapat berperan ganda, selain dapat
digunakan sebagai pakan dalam kultur zooplankton juga dapat ditambahkan
secara langsung dalam bak pemeliharaan larva. Penambahan fitoplankton dalam
media pemeliharaan larva tidak hanya berfungsi sebagai pakan larva secara
langsung, tetapi berfungsi sebagai penyagga kualitas air dan pakan zooplankton
yang diberikan pada bak pemeliharaan larva. Dengan adanya fitoplankton tersebut
maka kualitas nutrisi zooplankton dapat dipertahankan (Isnansetyo dan
Kurniastuty, 1995).
Biologi, Morfologi, dan Habitat Nannochloropsis sp.
Nannochloropsis sp. lebih dikenal dengan nama Chlorella laut. dalam
pembenihan mempunyai tiga peranan yaitu digunakan sebagai pakan pada klutur
rotifera, untuk pengkayaan rotifera, dan untuk menghasilkan efek “green water”
pada pemeliharaan larva. Nannochloropsis sp. dapat digunakan sebagai pakan
rotifera, karena ukuran tubuhnya sesuai dengan bukaan mulut rotifera, mempunyai
kandungan vitamin B12 yang sangat penting untuk populasi rotifera dan penting
untuk nilai nutrisi rotifera untuk pakan larva dan juvenil ikan laut (Meritasari.
Gambar 2. Nannochloropsis sp (Rezza, 2011).
Klasifikasi Nannochloropsis sp. menurut Adehoog dan Simon (2001)
diacu oleh Anon. dkk, (2009) adalah sebagai berikut:
Filum : Chromophyta
Kelas : Eustigmatophyceae
Ordo : Eustigmatales
Famili : Eustigmataceae
Genus : Nannochloropsis
Spesies : Nannochloropsis sp.
Kepadatan optimum yang dapat dicapai untuk skala laboratrium 50-60 juta
sel/mL, skala semi massal 20-25 juta sel/mL dan massal 15-20 juta sel/mL dengan
masa kultur 4-7 hari (Anon, 2009). Nannochloropsis sp. memiliki kandungan
lipid yang cukup tinggi yaitu antara 31-68% berat kering (Rezza, 2011).
Nannochloropsis sp. memiliki sejumlah kandungan pigmen dan nutrisi
seperti protein (52,11%), karbohidrat (16%), lemak (27,64%), vitamin C (0,85%),
dan klorofil A (0,89%). Selnya berbentuk bola dan berukuran kecil.
pada umumnya merupakan organisme filter feeder (penyaring) (Anon, dkk.,
2009).
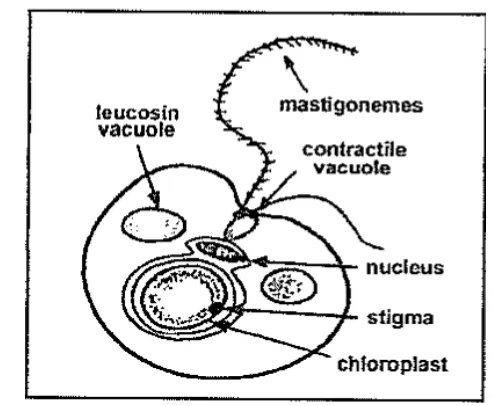
Gambar 3. Sel Nannochloropsis sp. (Aliabbas, 2002).
Nannochloropsis sp. memiliki ukuran sel 2 - 4 mikrometer, berwarna hijau
dan memilki dua flagella (Heterokontous) yang salah satu flagella berambut tipis.
Nannochloropsis sp. memiliki kloroplas dan nukleus yang dilapisi membran.
Kloroplas memiliki stigma (bintik mata) yang bersifat sensitif terhadap cahaya.
Nannochloropsis sp. dapat berfotosintesis karena memiliki klorofil. Ciri khas dari
Nannochloropsis sp. adalah memiliki dinding sel yang terbuat dari komponen
selulosa (Rezza, 2011).
Nannochloropsis sp. bersifat kosmopolit dapat tumbuh pada salinitas
0-35‰. Salinitas optimum untuk pertumbuhannya adalah 25-35 ‰, dan suhu 25-
30 0C merupakan kisaran suhu yang optimal. Mikroalga ini dapat tumbuh baik
pada kisaran pH 8-9,5 dan intensitas cahaya 100-10000 lux (Rezza, 2011).
Selama masa inkubasi Nannochloropsis oculata mengalami proses
pertumbuhan yang terbagi menjadi empat fase. 4 fase dalam pertumbuhan
1. Fase Istirahat (lag)
Fase dimana populasi tidak mengalami perubahan, tetapi ukuran sel
meningkat. Fotosintesis masih aktif berlangsung dan organisme mengalami
metabolisme tetapi belum terjadi pembelahan sel sehingga kepadatannya
belum meningkat.
2. Fase Pertumbuhan Eksponensial (Logaritmik)
Fase yang diawali dengan pembelahan sel dengan laju pertumbuhan yang
terus menerus, pertumbuhan pada fase ini mencapai maksimal.
3. Fase Pertumbuhan Stabil (Stasioner)
Fase dengan pertumbuhan yang dimulai mengalami penurunan dibandingkan
fase logaritmik. Laju reproduksi sama dengan laju kematian dalam arti
penambahan dan pengaurangan plankton relative sama sehingga kepadatan
plankton cenderung tetap.
4. Fase Kematian (mort)
Fase dimana terjadi penurunan jumlah atau kepadatan plankton, pada fase ini
laju kemtian lebih cepat dibandingkan laju reproduksi. Laju kematian plankton
dipengaruhi oleh ketersedian nutrien, cahaya, suhu, dan umur plankton itu
sendiri.
Budidaya Nannochloropsis sp.
Usaha untuk memenuhi ketersediaan pakan adalah memproduksi pakan
alami karena pakan alami mudah didapatkan dan tersedia dalam jumlah yang
banyak serta untuk memproduksi pakan alami tidak membutuhkan biaya yang
mahal. Pakan alami juga memiliki nilai nutrisi yang tinggi, mudah dibudidayakan,
yang mampu memberikan rangsangan bagi larva untuk memangsanya serta
memiliki kemampuan berkembang biak dengan cepat dalam waktu yang
relatif singkat (Rostini, 2007).
Budidaya Nannochloropsis dapat dilakukan dengan menggunakan
berbagai jenis pupuk anorganik. Budidaya Nannochloropsis pada skala semi
massal di BBAP Situbondo menggunakan pupuk teknis (TG), pupuk Walne dapat
digunakan sebagai medium berbasis pupuk komersial untuk kultur
Nannochloropsis sp. yang mampu menghasilkan berat biomassa kering tertinggi
yaitu sebesar 6,78 gram dari kepadatan awal inokulum sebanyak 10 sel/ml
(Amalia, 2012).
Kultur Nannochloropsis dimulai dari kegiatan isolasi kemudian
dikembangkan sedikit demi sedikit secara bertingkat. Media kultur yang
dikembangkan mula-mula hanya beberapa mililiter, kemudian secara bertahap
meningkat ke volume yang lebih besar hingga mencapai skala massal. Kultur
fitoplankton hingga volume 3 liter masih dilakukan di dalam laboratorium
sehingga sering disebut dengan kultur skala laboratorium. Selanjutnya dilakukan
kultur semi outdoor yang dapat mencapai volume 60-100 liter. Kultur outdoor
merupakan tahapan kultur selanjutnya yang dimulai dari volume 1 ton hingga
lebih dari 20 ton, tergantung besar kecilnya skala pembenihan. Prinsip kultur
fitoplankton yang menggunakan proses bertingkat dari volume kecil ke volume
yang lebih besar disebut dengan kultur bertingkat (Isnansetyo dan Kurniastuty,
1995).
Achmad, (1993) mengatakan, keberhasilan budidaya Nannochloropsis
oculata sangat ditentukan oleh kemurnian, kepadatan awal, pupuk, kualitas air,
Nannochloropsis oculata. Ditentukan oleh penanganan yang bersih, penggunaan
peralatan yang steril serta kultur dengan dosis pupuk yang tepat sehingga dapat
digunakan sebagai bibit dalam kultur skala besar yang merupakan makanan bagi
rotifer dan ikan budidaya.
Faktor-faktor yang Mempengaruhi Pertumbuhan Nannochloropsis sp.
Faktor eksternal berkaitan dengan kertersedian unsur hara amkro dan
mikro serta kondisi lingkungan. Faktor-faktor lingkungan yang berpengaruh
terhadap pertumbuhan fitoplankton antara lain cahaya, salinitas, suhu, kandungan
O2, kandungan, dan pH air (Meritasari. dkk, 2010).
Suhu
Pola suhu ekosistem air dipengaruhi oleh berbagai faktor seperti intensitas
cahaya matahari, pertukaran panas antara cahaya matahari dengan udara
sekelilingnya. Suhu air sangat mempengaruhi aktivitas fisiologis dari organisme
air seperti dijelaskan dalam hukum Van’t Hoffs, kenaikan suhu sebesar 10OC
(hanya pada kisaran yang ditolerir) akan meningkatkan laju metabolisme dari
organisme sebesar 2 – 3 kali lipat. Akibat meningkatnya laju metabolisme akan
menyebabkan konsumsi oksigen meningkat, sementara dilain pihak dengan
naiknya suhu akan menyebabkan kelarutan oksigen dalam air menjadi berkurang
(Barus, 2004).
Suhu media pemeliharaan di ukur dengan menggunakan
thermometer. Thermometer di masukkan ke dalam air selama kurang lebih
dua menit kemudian pembacaan nilai suhu dilakukan pada saat thermometer
suhu udara. Pembacaan nilai suhu sampai menunjukkan nilai yang konstan (Anita.
dkk, 2010).
pH
Nilai pH menyatakan nilai konsentrasi ion hydrogen dalam suatu larutan,
didefenisikan sebagai logaritma dari resiprokal aktivitas ion hidrogen dan secara
matematis dinyatkan sebagai pH= log 1/H+ , dimana H+ adalah banyaknya ion
hidrogen dalam mol per liter larutan. Kemampuan air untuk mengikat atau
melepaskan sejumlah ion hidrogen akan menunjukkan apakah larutan tersebut
bersifat asam atau basa. Organisme air dapat hidup dalam suatu perairan yang
mempunyai nilai pH netral dengan kisaran toleransi antara asam lemah sampai
basa lemah.
Pengukuran pH dilakukan dengan menggunakan alat pH meter. Mula-
mula ujung elektroda dibilas dengan akuades, kemudian dimasukkan dalam
larutan penyangga untuk kalibrasi. Kontrol pada pH meter diatur sampai terbaca
pH larutan penyangga. Ujung elektroda dibilas kembali dengan akuades, lalu
dimasukkan ke dalam air sample sampai beberapa saat sampai skala menunjukkan
angka yangkonstan. Nilai yang terbaca menunjukkan nilai pH (Anita. dkk, 2010).
Salinitas
Salinitas merupakan nilai yang menunjukkan jumlah garam-garam terlarut
dalam suatu volum air yang biasanya dinyatakan dengan satuan promil (‰).
Kandungan utama dari air laut dibentuk oleh ion Na+ dan Cl-, ditambah berbagai
jenis unsur lain yang jumlahnya relatif sedikit.
Pengukuran salinitas dilakukan dengan menggunakan alat Hand
Refractometer. Refraktometer dikalibrasi dengan akuades sampai skala 0 ppt.
media pemeliharaan pada prisma refraktometer dengan menggunakan pipet tetes.
Nilai yang tertera pada skala refraktometer menyatakan salinitas air laut (Anita.
dkk, 2010).
Oksigen Terlarut (DO)
Oksigen terlarut merupakan suatu faktor yang sangat penting di dalam
ekosistem air, terutama sekali dibutuhkan untuk proses repirasi bagi sebagian
besar organisme air. Umumnya, kelarutan oksigen dalam air sangat terbatas.
Dibandingkan dengan kadar oksigen di udara yang mempunyai konsentrasi
sebanyak 21%. Air hanya mampu menyerap oksigen sebanyak 1% saja.
Nilai oksigen terlarut disuatu perairan mengalami fluktuasi harian.
Fluktuasi ini selain dipengaruhi oleh perubahan suhu juga dipengaruhi oleh
aktivitas fotosintesis dari tumbuhan yang menghasilkan oksigen. Nilai oksigen
terlarut di perairan sebaiknya berkisar antara 6- 8mg/l (Barus, 2004).
Pengukuran oksigen terlarut dilakukan dengan menggunakan DO meter,
yaitu dengan cara memasukkan salah satu elemen DO meter ke dalam air sampel,
kemudian ditunggu beberapa saat untuk memperoleh kisaran kandungan oksigen
terlarut dalam air sampel (Anita. dkk, 2010).
Intensitas Cahaya Matahari
Faktor cahaya matahari yang masuk kedalam air akan mempengaruhi sifat
optis air. Sebagian cahaya matahari tersebut akan diabsorbsi dan sebagian lagi
akan dipantulkan keluar dari permukaan air. Kondisi optik dalam air selain
dipengaruhi oleh intensitas cahaya matahari, juga dipengaruhi oleh berbagai
substrat dan benda lain yang terdapat dalam air, misalnya oleh plankton yang ada
dalam air. Bagi organisme air, intensitas cahaya berfungsi sebagai alat orientasi
Pupuk
Menurut Noviani (2010), pupuk adalah bahan untuk diberikan kepada
tanaman baik langsung maupun tidak langsung, guna mendorong
pertumbuhan tanaman, meningkatkan produksi atau memperbaiki kualitasnya,
sebagai akibat perbaikan nutrisi tanaman. Pupuk akan sampai pada sasarannya
jika diaplikasikan secara benar. Dalam aplikasi pupuk, hal penting yang perlu
diperhatikan adalah jenis tanaman yang akan dipupuk dan jenis pupuk yang
digunakan. Dengan aplikasi yang tepat dan benar maka akan diperoleh efisiensi
dan efektivitas pemupukan (Irwanto. dkk, 2012).
Pupuk adalah unsur yang ditambahkan ke dalam tanah untuk memenuhi
unsur mikro dan makro yang dibutuhkan tanaman. Makronutrien adalah unsur
hara yang dibutuhkan tanaman dalam jumlah besar, misalnya karbon (C),
hidrogen (H), oksigen (O), nitrogen (N), fosfor (P), kalium (K), belerang (S),
kalsium (Ca), dan magnesium (Mg). Mikronutrien adalah unsur hara yang
dibutuhkan tanaman dalam jumlah kecil, misalnya boron (Bo), besi (Fe),
mangan (Mn), tembaga (Cu), seng (Zn), molibdenum (Mo), dan klorin (Cl)
(Irwanto. dkk, 2012).
Secara garis besar, aplikasi pemupukan dapat dibedakan berdasarkan
aplikasi pupuk padat dan aplikasi pupuk cair. Pemupukan dilakukan karena
tanah tidak mampu menyediakan satu atau beberapa unsur hara untuk
menjamin suatu tingkat produksi tertentu. Tujuan dilakukan pemupukan yaitu
untuk memperoleh produksi yang tinggi dan bernilai dengan memperbaiki
penyediaan hara sambil memperhatikan atau memperbaiki kesuburan tanah tanpa
Pengertian klasifikasi pupuk dapat dilihat dari beberapa segi yaitu
atas dasar pembentukannya yang terdiri dari pupuk alam dan pupuk buatan,
atas dasar kandungan unsur hara yang dikandungnya yang terdiri dari pupuk
tunggal dan pupuk majemuk dan atas susunan kimiawi yang mempunyai
hubungan penting dengan perubahan-perubahan di dalam tanah. Pupuk alam
diantaranya terdiri dari pupuk kandang pupuk hijau, kompos dan guano (Irwanto.
dkk, 2012).
Menurut Noviani (2010), yang dimaksud dengan pupuk buatan adalah
pupuk yang dibuat di pabrik-pabrik yang mengandung unsur hara tertentu,
yang pada umumnya mempunyai kadar unsur hara tinggi. Manfaat pupuk adalah
meyediakan unsur hara yang kurang atau bahkan tidak tersedia di tanah untuk
mendukung pertumbuhan tanaman Peningkatan pertumbuhan pada fase anakan
dapat dilakukan dengan pemberian pupuk dan zat pengatur tumbuh. Pemberian
pupuk bertujuan untuk meningkatkan ketersediaan unsur hara yang dapat diserap
tanaman untuk pertumbuhan optimum (Irwanto, dkk. 2012).
Pupuk kascing
Pupuk Kascing sudah dikenal dan digunakan di seluruh dunia dengan hasil
yang luar biasa untuk meningkatkan pertumbuhan tanaman. Bahkan beberapa
orang menyebutnya sebagai pupuk organik terbaik. Banyak aplikasi baru yang
sudah diriset oleh universitas di Amerika dan sudah melalui pengujian di
lapangan. Apapun jenis tanah atau tanaman akan diuntungkan oleh penggunaan
Gambar 4. Pupuk Organik Kascing
Hasil dari penguraian bahan organik yang dikeluarkan dalam bentuk
kotoran cacing tanah yang merupakan pupuk organik yang dikenal dengan istilah
kascing (bekas cacing). Kascing ini berupa partikel-partikel tanah berwarna
kehitaman yang ukurannya lebih kecil dari partikel tanah biasa sehingga lebih
cocok untuk pertumbuhan tanaman (Nugraha, 2009).
Pupuk organik yang diproduksi melalui proses pengomposan dengan
bantuan cacing tanah yang dibantu oleh mikroorganisme lain seperti bakteri, dan
fungi, dinamakan kascing (bekas cacing). Mikroorganisme tersebut membantu
dalam proses daur ulang limbah organik. Cacing tanah mencerna makanannya
secara tidak langsung karena perombakan bahan organik tersebut dibantu oleh
mikroflora seperti bakteri atau fungi. Sementara mencerna secara intermedient
dengan menggunakan senyawa organik yang disediakan mikroflora untuk
menguraikan serasah daun (Aisyah, dkk, 2000).
Kascing merupakan metabolisme cacing tanah yang bercampur dengan
kandungan hara yang tinggi sehingga baik untuk dijadikan pupuk. Bahan- bahan
makanan utama cacing tanah yang umumnya sudah terfermentasi melalui
pengomposan (Minnich, 1997).
Menurut Gaur (1980) bagan organik sebagai makanan cacing tanah juga
diperhatikan mengenai nisbah C/N, ukuran bahan yang difermentasi, kelembaban
bahan dan aerasi, suhu, reaksi kompos, penambahan CaCO3, penghancur patogen
dan parasit. Dengan demikian cacing tanah mudah mencerna makanannya dari
berbagai macam bahan organik tersebut. Zat makanan dari bahan organik tersebut
masih mempunyai kandungan karbohidrat, protein, lemak, vitamin dan mineral
yang cukup tinggi, sehingga mencukupi kebutuhan nutrisi cacing tanah. Selain
kandungan gizinya, perlu diperhatikan pula mengenai kandungan unsur hara yang
tersusun dalam bahan organik.
Aktifitas cacing tanah dalam melakukan dekomposisi bahan organik selain
mempengaruhi sifat- sifat fisiknya juga mempengaruhi sifat kimia karena adanya
proses mineralisasi dari bahan-bahan organik yang dilakukan oleh
mikroorganisme yang dibantu oleh cacing tanah. Peran cacing tanah dalam proses
mineralisasi adalah mempercepat proses tersebut bersama mikroorganisme,
sehingga menghasilkan unsur hara yang lebih tersedia bagi tanaman. Hara yang
terakumulasi dalam kascing baik itu hara mikro merupakan cerminan dari
kandungan hara bahan organik sebagai sumber makanan utama cacing tanah
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada tanggal 18 November – 25 Desember 2013
di Balai Budidaya Air Payau (BBAP) Ujung Batee Kabupaten Aceh Besar,
Provinsi Aceh.
Alat dan Bahan
Alat yang digunakan dalam penelitian ini antara lain toples bening ukuran
16 liter mineral, filter bag, selang air, gayung literan, perlengkapan aerasi, neraca/
timbangan, sponge, sikat/brus, pH meter, refraktometer, DO meter, lux meter,
mikroskop, beaker glass, pipet tetes, handcounter, Haemacytometer.
Sedangkan bahan yang digunakan adalah bibit Nannochloropsis sp., pupuk
kascing, dan pupuk ZA, Urea, SP36, dan vitamin B12 yang biasa dipakai di
BBAP Ujung Batee dalam pengkulturan Nannochloropsis sp. dan digunakan
sebagai perlakuan kontrol, air tawar, air laut, dan sabun cuci piring.
Metode Penelitian
Metode yang digunakan dalam penelitian ini adalah metode eksperimen
dengan melakukan pengamatan langsung di laboratorium terhadap perkembangan
Nannochloropsis sp. yang dikultur dengan pupuk kascing dengan menggunakan
mikroskop. Dalam penelitian ini, untuk menentukan konsentrasi yang digunakan
terlebih dahulu dilakukan uji pendahuluan untuk mendapatkan rentang konsentrasi
Pengamatan dilakukan untuk mendapatkan data kelimpahan
Nannochloropsis sp. dan peningkatan kelimpahan setiap hari dengan berbagai
perlakuan konsentrasi yaitu 0 ppm (sebagai kontrol negatif), 50 ppm, 100 ppm,
dan 150 ppm dan menggunakan pupuk ZA, Urea, SP36, dan vitamin B12 (sebagai
kontrol positif). Selain itu dilakukan juga pengukuran kualitas air yakni suhu, pH,
salinitas, DO, dan intensitas cahaya setiap hari selama penelitian.
Rancangan Penelitian
Rancangan penelitian yang dugunakan adalah Rancangan Acak Lengkap
(RAL) dengan 3 perlakuan konsentrasi 50 ppm, 100 ppm, dan 150 ppm.
Digunakan pupuk ZA, Urea, SP36, dan penambahan vitamin B12 (sebagai kontrol
positif) dan pupuk kascing 0 ppm atau (tanpa perlakuan) sebagai kontrol negatif.
Untuk mengurangi tingkat error pada penelitian maka dibuat ulangan sebanyak 3
kali serta penempatan media perlakuan ditempatan secara acak di ruangan kultur.
Adapun perlakuan yang diberikan adalah :
Perlakuan 1 = Nannochloropsis sp. + Pupuk ZA, Urea, SP36, dan vitamin B12
Perlakuan 2 = Nannochloropsis sp. + 0 ppm pupuk kascing
Perlakuan 3 = Nannochloropsis sp. + 50 ppm pupuk kascing
Perlakuan 4 = Nannochloropsis sp. + 100 ppm pupuk kascing
Perlakuan 5 = Nannochloropsis sp. + 150 ppm pupuk kascing
Penempatan media pada perlakuan dan ulangan disusun secara acak di
ruangan yang sudah disiapkan. Susunan media uji acak dapat dilihat pada Gambar
C3 C1 B3 B4 A4
C2 C5 A1 C4 B1
A5 A3 B5 A2 B2
Gambar 5. Susunan Media Uji Acak
Persiapan
Langkah pertama adalah mempersiapkan wadah dan melengkapi alat dan
bahan yang akan digunakan pada saat penelitian. Persiapan wadah dimulai dari
sterilisasi alat yaitu wadah, ruangan, dan alat-alat yang akan digunakan. Persiapan
wadah dilakukan dengan mencuci dan menyikat wadah toples bening bervolume
16 liter dengan menggunakan sabun dan brush dan membilasnya dengan air tawar
hingga bersih. Untuk menghindari serangan jamur dan bakteri yang mungkin
melekat pada wadah dilakukan pencampuran kaporit kedalam sabun pencuci
piring. Wadah yang sudah dibilas bersih dikeringkan terlebih dahulu dan
kemudian diberi air laut sebanyak 10 liter dan kemudian diaerasi selama 24 jam.
Pelaksanaan
Pelaksanaan kultur pakan alami Nannochloropsis sp. dilakukan sesuai
dengan metode kultur yang ditetapkan oleh laboratorium Pakan Alami Balai
Budidaya Air Payau (BBAP) Ujung Batee. Pada penelitian ini dilakukan uji
pendahuluan selama 7 hari dengan menggunakan dosis yang telah ditetapkan, hal
konsentrasi pupuk kascing yang digunakan, oleh karena itu dibutuhkan uji
pendahuluan untuk menentukan rentang konsentrasi yang akan digunakan pada
saat penelitian.
Media yang sudah diaerasi selama 24 jam pada saat persiapan kemudian
dimasukkan bibit Nannochloropsis sp. yang diambil dari balai budidaya sebanyak
20 % dari volume air media (2 liter) dengan kepadatan 5.630.000 cells/ml. Jumlah
Nannochloropsis sp. dihitung dengan cara sampling dari volume yang dihitung.
Nannochloropsis sp. yang telah dimasukkan kedalam media diberi pakan pupuk
kascing masing- masing sebanyak perlakuan konsentrasi.
Pakan pupuk kascing yang digunakan dan diberikan selama penelitian
yakni 50 ppm, 100 ppm, dan 150 ppm. Pengamatan kepadatan dilakukan
keesokan harinya dengan mengambil sampel dari setiap media uji dan kemudian
diamati dibawah mikroskop dan dihitung kepadatan selnya. Selain itu pegukuran
kualitas air pada media juga dilakukan setiap hari pada waktu pagi hari berkisar
pukul 09.00 WIB – 10.30 WIB.
Dalam uji pendahuluan dilakukan pengamatan kelimpahan
Nannochloropsis sp. setiap hari untuk melihat laju kelimpahan selama 7 hari.
Pada penelitian ini dilakukan 4 kali percobaan dengan menggunakan konsentrasi
yang berbeda untuk memperoleh konsentrasi yang diinginkan. Percobaan pertama
adalah dengan menggunakan konsentrasi 5 ppm, 10 ppm, 15 ppm. Ke-2 dengan
konsentrasi 25 ppm, 50 ppm, dan 75 ppm. Percobaan ke-3 dengan konsentrasi 100
ppm, 125 ppm, dan 150 ppm. Kemudian didadapatkan rentang konsentrasi yang
akan dipakai untuk uji berikutnya yaitu dengan konsentrasi 50 ppm, 100 ppm dan
150 ppm. Uji lanjutan dilakukan untuk mengamati kelimpahan sel
Pengamatan
Pengamatan yang dilakukan hanya melihat pertambahan dari jumlah
kelimpahan sel Nannochloropsis sp. yang diuji dengan pupuk kascing dari
berbagai perlakuan konsentrasi. Perhitungan kelimpahan bertujuan untuk
menentukan kondisi laju peningkatan kelimpahan setiap harinya (sel yang
bertambah banyak). Perhitungan sel Nannochloropsis sp. menggunakan
haemacytometer dan alat bantu handcounter untuk mencatat jumlah perhitungan.
Haemacytometer terbuat dari gelas yang dibagi menjadi kotak-kotak pada
dua tempat bidang pandang untuk menghitung jumlah kepadatan sel. Kotak
tersebut berbentuk bujur sangkar dengan sisi 1 mm dan tinggi 0,1 mm, sehingga
bila ditutup dengan cover glass, akan menghasilkan volume ruangan 0,1 mm3 atau
10-4 ml. Kotak tersebut dibagi lagi menjadi dua puluh lima kotak bujur sangkar,
yang masing-masing dibagi lagi menjadi enam belas kotak bujur sangkar yang
lebih kecil (Isnansetyo, 1995).
Pengamatan yang dilakukan hanya melihat perkembangan kelimpahan sel
Nannochloropsis sp. selama penelitian dengan berbagai perlakuan konsentrasi
yang berbeda- beda. Cara menghitung kelimpahan Nannochloropsis sp. adalah
sebagai berikut :
1. Diambil sampel air pada setiap media lalu memasukkannya ke dalam botol
film yang sudah diberi label.
2. Amati di laboratorium dengan menggunakan haemocytometer lengkap
dengan cover glass.
3. Tetesi haemocytometer dengan pipet tetes lalu tutup dengan cover glass,
4. Amati kelimpahan Nannochloropsis sp. dalam 1 kotak besar yang terdiri
dari 16 kotak kecil. Hitung dengan bantuan handcounter.
5. Dihitung kelimpahan Nannochloropsis sp. dengan menggunakan rumus
menurut Isnansetyo dan Kurniastuty, 1995 sebagai berikut:
N = n x 104
Keterangan :
N = Jumlah Nannochloropsis sp. dalam 1 ml.
n = Jumlah Nannochloropsis sp. yang terdapat dalam 1 kotak kecil.
Selain kelimpahan sel dilakukan juga pengukuran kualitas air pada setiap
media yakni suhu, salinitas, intensitas cahaya, pH, dan DO. Pengukuran kualitas
air dilakukan pada pagi hari berkisar pukul 09.00 WIB – 10.30 WIB.
Analisis Data
Data yang diperoleh dalam penelitian ini disajikan dalam bentuk
tabel dan grafik. Untuk mengetahui pengaruh pemberian pupuk kascing
dengan dosis yang berbeda pada media terhadap laju kelimpahan maksimum
Nannochloropsis sp. sehingga dapat mengetahui puncak dari kepadatan
Nannochloropsis sp. dari masing- masing perlakuan.
Data dianalisis menggunakan One Way Analysis of Varian (ANOVA)
sebagai uji statistik yang digunakan untuk mengetahui pengaruh dari setiap
perlakuan dan hubungannya dengan beberapa indikator yang diamati dengan
HASIL DAN PEMBAHASAN
Hasil
1. Tingkat Kelimpahan Nannochloropsis sp.
Tingkat kelimpahan sel Nannochloropsis sp. pada setiap ulangan terhadap
perlakuan terlihat sama. Setiap ulangan kelimpahan tertinggi terdapat pada
konsentrasi 100 ppm dengan rata-rata kelimpahan mencapai 2.871.000 sel/ml dan
kelimpahan terendah terdapat pada perlakuan 0 ppm tanpa pemberian pupuk atau
sebagai kontrol negatif dengan rata-rata 706.309 sel/ml. Perbedaan kelimpahan sel
Nannochloropsis sp. ulangan pada tiap perlakuan dapat dilihat pada Gambar 6.
Gambar 6. Perbandingan rata-rata kelimpahan sel Nannochloropsis sp. setiap perlakuan.
Hasil uji statistik Anova menunjukkan bahwa kelimpahan sel pada
konsentrasi 100 ppm berbeda nyata dengan kelimpahan sel pada konsentrasi 0
kontrol, dengan demikian konsentrasi yang optimum untuk pertumbuhan sel
Nannochloropsis sp. adalah 100 ppm atau dapat dilihat pada Lampiran 1.
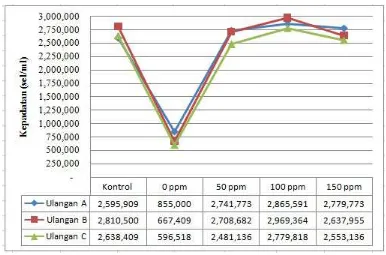
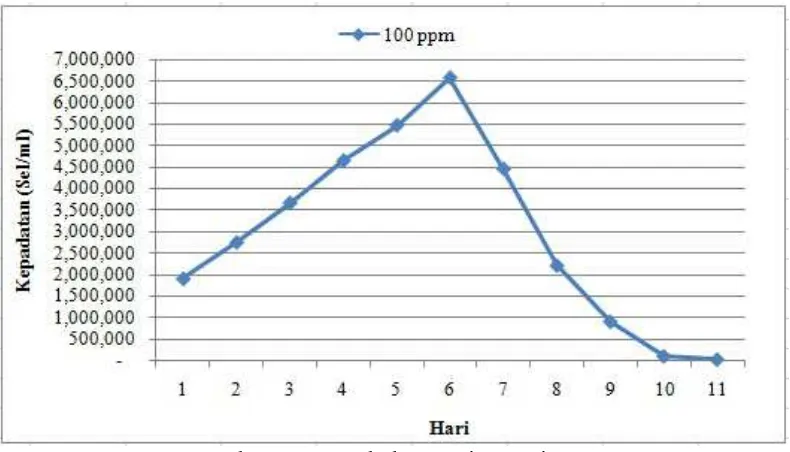
2. Laju Kelimpahan Harian Nannochloropsis sp.
Peningkatan kelimpahan pada tiap perlakuan terjadi setiap hari kecuali
pada perlakuan 0 ppm. Puncak kelimpahan sel Nannochloropsis sp. terjadi pada
hari ke lima disetiap perlakuan dan untuk perlakuan yang paling tinggi
kelimpahannya adalah perlakuan dengan konsentrasi kascing 100 ppm mencapai
6.895.000 sel/ml. Sedangakan pada perlakuan 0 ppm atau sebagai kontrol negatif
tanpa perlakuan pupuk menunjukkan penurunan kelimpahan dari hari pertama
sampai terakhir (2.000.000 – 2500 sel/ml). Puncak kelimpahan dapat dilihat pada
Gambar 7.
Gambar 7. Laju Peningkatan Kelimpahan Nannochloropsis sp. setiap Perlakuan selama 10 Hari.
3. Kualitas Air
Pertumbuhan organisme air sangat tergantung pada kualitas air, sehingga
kualitas air dilakukan agar mengetahui kelayakan nilai kualitas air selama
penelitian terhadap kelimpahan Nannochloropsis sp. Data kisaran kualitas air
selama penelitian dapat dilihat pada Tabel 1.
Tabel 1. Data Kisaran Kualitas Air
Data Kualitas Air
1. Tingkat Kelimpahan Nannochloropsis sp.
Penggunaan pupuk kascing dalam kultur pakan alami berhasil dilakukan,
bahwa ada pengaruh pupuk kascing terhadap kelimpahan sel Nannochloropsis sp.
pengaruh yang ditunjukkan berupa terjadinya peningkatan sel. Hasil penelitian
menunjukkan perbedaan laju kelimpahan antar perlakuan. Kelimpahan tertinggi
terdapat pada perlakuan konsentrasi pupuk kascing 100 ppm, hal ini disebabkan
kandungan unsur hara yang terkandung dalam pupuk kascing. Menurut Nugraha,
2009 komponen bologis yang terkandung dalam pupuk kascing diantaranya
hormon pengatur tumbuh seperti giberilin, sitokinin, dan auxin dan juga
mengandungan unsur hara makro dan mikro seperti nitrogen, fosfor, kalium,
belerang, magnesium dan besi yang dibutuhkan oleh fitoplankton untuk
Sedangkan kelimpahan yang paling rendah adalah perlakuan 0 ppm atau
tanpa pemberian pupuk hal ini dikarenakan pada perlakuan ini tidak menggunakan
pupuk sama sekali atau sebagai kontrol negatif artinya tidak terdapat unsur hara
dalam air sebagai nutrisi yang diperlukan untuk pertumbuhan sel Nannochloropsis
sp. sehingga tidak terjadi peningkatan kelimpahan melainkan terjadi kematian
sel-sel sehingga menurunkan kelimpahan setiap hari.
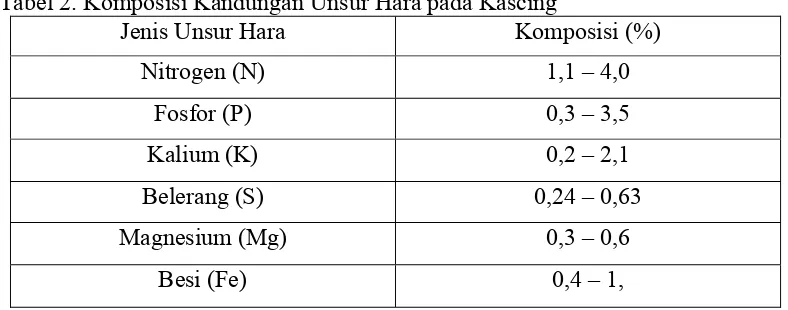
Persentasi kandungan hara kascing dapat dilihat pada Tabel 2.
Tabel 2. Komposisi Kandungan Unsur Hara pada Kascing
Jenis Unsur Hara Komposisi (%)
Nitrogen (N) 1,1 – 4,0
Fosfor (P) 0,3 – 3,5
Kalium (K) 0,2 – 2,1
Belerang (S) 0,24 – 0,63
Magnesium (Mg) 0,3 – 0,6
Besi (Fe) 0,4 – 1,
Sumber : Nugraha, 2009
2. Laju Kelimpahan Harian Nannochloropsis sp.
Pengamatan laju kelimpahan harian dilakukan untuk mengetahui
peningkatan kelimpahan Nannochloropsis sp. setiap hari. Pengambilan sampel
dilakukan setelah pengukuran kualitas air, kemudian sampel dibawa ke
laboratorium pakan alami untuk pengamatan kelimpahan. Pengamatan dilakukan
menggunakan mikroskop, haemocytometer dan penghitungan sel dibantu dengan
alat handcounter. Kultur Nannochloropsis sp. dilakukan selama 10 hari dan
dilakukan pengamatan kelimpahan dan pengukuran kualitas air setiap harinya.
Data yang diperoleh selama 10 hari ditabulasi dan dimasukkan ke Microsoft excel
perubahan kelimpahan sel selama penelitian. Laju kelimpahan harian
Nannochloropsis sp. terlihat seperti Gambar 8.
Gambar 8. Pertumbuhan Harian Optimum
Siklus hidup dari golongan fitoplankton terbilang singkat yaitu
berlangsung hanya beberapa hari saja. Hal ini didukung oleh pernyataan
Isnansetyo dan Kurniastuty (1995) yaitu fitoplankton mempunyai daur hidup yang
pendek sehingga mampu berkembang biak dalam waktu yang singkat dan
fitoplankton dapat dipanen sekitar 3 – 7 hari. Dari hasil penelitian yang dilakukan
peningkatan kelimpahan setiap harinya meningkat sampai hari ke-5 dan
kelimpahan optimum Nannochloropsis sp. terjadi pada hari ke-5 dan setelah itu
terjadi penurunan kepadatan mulai dari hari ke-6 sampai ke-10 atau dapat dilihat
pada Gambar 8.
Kelimpahan Nannochloropsis sp. mengalami beberapa fase pertumbuhan
yaitu fase adaptasi, eksponensial, stasioner, dan fase kematian. Sesaat setelah
pemasukan bibit Nannochloropsis sp. merupakan fase adaptasi yang ditandai
dengan tidak bertambahnya jumlah sel. Pada fase adaptasi, Nannochloropsis sp.
sel belum meningkat. Fase adaptasi pada masing-masing perlakuan tidak terlihat
jelas pada grafik pertumbuhan Nannochloropsis sp. Hal ini dikarenakan fase
adaptasi Nannochloropsis sp. terjadi sangat singkat yaitu sebelum 24 jam
(Wijaya, 2006).
Peningkatan kelimpahan sel Nannochloropsis sp. pada masing-masing
perlakuan mulai nampak pada pengamatan sehari setelah penebaran bibit. Adanya
peningkatan kelimpahan sel yang menunjukkan bahwa Nannochloropsis sp. mulai
memasuki fase eksponensial. Fase ini ditandai dengan meningkatnya pembelahan
sel (Wijaya, 2006), sesuai dengan hasil penelitian yakni pertumbuhan kepadatan
Nannochloropsis sp. terjadi peningkatan di hari pertama dari kepadatan 1.895.000
sel/ml menjadi 2.742.000 sel/ml.
Menurut Kanibawa (2006) sel inokulum pada fase eksponensial sudah
memanfaatkan nutrien dalam media tumbuh dan telah terjadi proses biosintesis sel
sehingga sel mampu tumbuh dan bereproduksi lebih banyak dan pada fase
eksponensial sel inokulum mengalami pembelahan maksimal yaitu menjadi dua
kali lipat dari sebelumnya. Faktor yang mempengaruhi hal tersebut adalah kondisi
lingkungan dan komposisi medium, didukung oleh pernyataan Suantika (2009)
bahwa fase eksponensial terjadi ketika nutrien, pH dan intensitas cahaya pada
medium masih dapat memenuhi kebutuhan fisiologis Nannochloropsis sp.
sehingga dalam fase ini sel masih memiliki kemampuan bereproduksi hingga
kepadatannya masih bertambah, hal ini juga dapat dibuktikan dari hasil penelitian
bahwa kelimpahan sel Nannochloropsis sp. terus meningkat sampai hari ke 5 yang
merupakan puncak kelimpahan optimum yakni mencapai 6.895.000 sel/ml.
Menurut Isnansetyo dan kurniastuty (1995) fase stasioner merupakan fase
eksponensial. Pada fase ini laju reproduksi sama dengan laju kematian dengan
demikian fase kematian sama dengan laju reproduksi sehingga popoulasi menjadi
tetap untuk sementara waktu. Fase stasioner pada penelitian ini dapat terlihat
karena terjadi penurunan yang cukup drastis namun relatif tidak tetap yakni dari
hari ke 5 kelimpahan mencapai 6.895.000 sel/ml turun pada hari ke 6 menjadi
4.456.000 sel/ml. Sementara fase kematian terjadi penurunan kelimpahan
Nannochloropsis sp. pada penelitian ini juga dapat dilihat pada hari ke 7 sampai
ke 10 yakni kelimpahan turun hingga menjadi 20.000 sel/ml.
Menurut penelitian yang dilakukan oleh Indah dan Abdul, 2012 bahwa
kelimpahan optimum sel Nannochloropsis sp. yang dikultur dengan menggunakan
pupuk walne dapat mencapai 12.000.000 sel/ml. dengan pernyataan berikut
terdapat perbedaan kelimpahan yang berbeda jauh dibandingkan dengan
menggunakan pupuk kascing yang kelimpahan optimumnya mencapai 6.895.00
sel/ml. Hal ini dikarenakan beberapa hal salah satunya musim, bahwa pada saat
penelitian ini berlangsung pada bulan November – Desember dimana pada bulan
ini merupakan musim penghujan. Pada saat penelitiaan berlangsung hampir setiap
hari turun hujan dan mendung sehingga menyebabkan intensitas cahaya matahari
kurang untuk memicu terjadinya fotosintesis.
3. Kualitas Air
Menurut Barus, 2004 Dalam setiap penelitian pada ekosistem air,
pengukuran suhu air merupakan hal yang mutlak dilakukan. Hal ini disebabkan
karena kelarutan berbagai jenis gas didalam air serta semua ktivitas
biologis-fisiologis di dalam ekosistem air sangat dipengaruhi oleh suhu. Suhu merupakan
hukum Han’t Hoff peningkatan suhu hingga 100C akan menaikkan laju
metabolisme organisme air hingga 2 kali lipat. Hasil pengamatan untuk suhu air
berkisar 26,3 oC – 31oC, kisaran tersebut masih sesuai dengan kisaran suhu yang
baik untuk pertumbuhan Nannochloropsis sp. hal ini sesuai dengan pernyataan
Zumaritha, 2011 yang menyatakan bahwa suhu optimum pertumbuhan
Nannochloropsis sp. antara 25–35 °C.
Kisaran pH yang diperoleh adalah antara 7,1 – 8,5 kisaran ini masih sesui
dengan pertumbuhan Nannochloropsis sp. hal ini didukung oleh pernyataan
Barus, 2004 bahwa Nilai pH yang ideal bagi kehidupan organisme air umumnya
terdapat antara 7 sampai 8,5. Selain itu pernyataan Djarijah, 1995 yang
menyatakan bahwa pH optimum untuk pertumbuhan Nannochloropsis sp. antara
7–9. Berdasarkan pengukuran, rata-rata kisaran suhu, pH dan salinitas dari ketiga
media kultur masih layak dan baik untuk mendukung proses metabolisme sel
Nannochloropsis sp. selama penelitian.
Faktor pendukung dalam pertumbuhan Nannochloropsis sp. yang baik
selain dipengaruhi oleh kandungan nutrien juga dipengaruhi oleh kondisi
lingkungan di dalam media pemeliharaan, seperti salinitas, suhu dan pH (Djarijah,
1995). Salinitas media kultur Nannochloropsis sp. dalam penelitian ini adalah
berkisar 29 ppt - 33 ppt. Setelah dilakukan pengukuran setiap harinya hingga hari
terakhir pengamatan, salinitas medium berkisar antara 29–32 ppt. Hal ini
menunjukkan bahwa salinitas media kultur mengalami penurunan, namun
salinitas media kultur masih berada dalam kondisi optimal, sesuai dengan
pendapat Zumaritha (2011) bahwa Nannochloropsis sp. dapat berkembang dengan
baik pada salinitas 31 ppt dan dapat terus menerus berkembang pada kisaran
yaitu kontrol dengan menggunkan pupuk teknis yang biasa digunakan yaitu ZA,
urea, SP36 dan vitamin B12 sehingga dengan pencampuran beberapa jenis pupuk
ini kedalam media uji dapat menurunkan salinitas air.
Kelarutan oksigen (Do) diukur untuk mengetahui berapa banyak suplay
oksigen yang terdapat dalam media air. Oksigen yang terkandung dalam air sangat
berkaitan dengan suhu. Sehubungan dengan hukum Van’t Hoff yang dibahas
sebelumnya bahwa jika terjadi kenaikan suhu hingga 100C akan meningkatkan
metabolisme organisme air hingga 2 kali lipat dengan demikian kebutuhan
oksigen dalam air akan meningkat. Jika ketersediaan oksigen dalam air kurang
akan terjadi penurunan kepadatan Nannochloropsis sp. diakibatkan karena sel
banyak yang mati atau tidak mampu berkembang karena kekurangan oksigen
untuk melakukan fotosintesis. Dengan demikian, agar oksigen selalu tersedia
dalam media dilakukan pemberian aerasi dengan kekuatan sedang. Kelarutan
oksigen (Do) diukur dengan menggunakan Do meter dan diperoleh hasil berkisar
5 – 6,09 mg/l, kisaran dikatakan masih baik untuk pertumbuhan Nannochloropsis
sp. karena menurut Sastrawijaya (1991) kehidupan organisme akuatik berjalan
dengan baik apabila kandungan oksigennya minimal 5 mg/l.
Pada mikroalga, semua sel yang memiliki kloroplas berpotensi untuk
melangsungkan reaksi fotosintesis. Pada dasarnya, rangkaian reaksi fotosintesis
dapat dibagi menjadi dua bagian utama: reaksi terang (karena memerlukan
cahaya) dan reaksi gelap (tidak memerlukan cahaya tetapi memerlukan karbon
dioksida). Dalam penelitian ini satu satunya sumber cahaya yang digunakan untuk
proses fotosintesis untuk perkembangbiakan Nannochloropsis sp. diperoleh dari
sinar matahari. Selain cahaya matahari, dalam proses fotosintesis membutuhkan
cahaya matahari dengan suplay oksigen. Reaksi foto sintesis dapat dilihat sebagai
berikut :
6CO2 + 6H2O Cahaya Matahari C6H12O6 (glukosa) + 6O2
Kisaran intensitas cahaya yang diperoleh selama penelitian adalah 600 lux
– 1050 lux kisaran ini masih sesuai dengan pendapat Kurniastuti dan Isnansetyo
(1995) yang mengatakan bahwasanya besar intensitas cahaya adalah berkisar
KESIMPULAN DAN SARAN
Kesimpulan
1. Dari hasil penelitian dapat disimpulkan bahwa pupuk kascing (bekas cacing)
dapat digunakan dalam kultur Nannochloropsis sp. dan mampu memberikan
pengaruh peningkatan kepadatan Nannochloropsis sp. yang dikultur selama 10
hari dan pertumbuhan optimum terjadi pada hari ke-5 dengan kepadatan
6.895.000 sel/ml.
2. Konsentrasi pupuk kascing yang optimum untuk pertumbuhan
Nannochloropsis sp. adalah 100 ppm.
Saran
Nannochloropsis sp. dapat dikultur dengan menggunakan pupuk kascing
(bekas cacing) dengan hasil yang hampir sama dengan menggunakan pupuk yang
biasa dilakukan, namun dengan pupuk kascing biaya kultur lebih murah sehingga
para pembudidaya ikan terutama dibidang pembenihan dapat menggunakan
DAFTAR PUSTAKA
Achmad, T. 1993. Pedoman Teknis Pembenihan Ikan Bandeng. Pusat Penelitian dan Pengembangan Perikanan Badan Penelitian dan Pengembangan Pertanian. Jakarta.
Aisyah, D, Suyono, Dadang A, Mustofa, dan Jumsih. 2000. Jurnal Kandungan Hara N, P, K, Kascing Lumbricus Rubellus yang Dibudidayakan dengan Pakan Limbah Organik.
Aliabbas, A. 2002. Kualitas Nannochloropsis sp. Akibat Lama Penyimpaan Nata de Nanno. Skripsi. IPB. Bogor.
Amalia, S, Wisanti, dan Evie Ratnasari. 2012. Pengaruh Pemberian Jenis Pupuk yang Berbeda terhadap Laju Pertumbuhan Populasi dan Kadar Lemak
Nannochloropsis oculata. LenteraBio Vol. 1 No. 1: 55-61.
Anita, Natrici, M. Yusuf, dan Ferbriana. 2010. Pemanfaatan Molase sebagai Nutrient Pengkayaan pada Kultur Nannochloropsis sp.
Anon, Sen M.A.T., Kocer M.T. Alp, dan H. Erbas. 2009. Studies on Growth Marine Microalgae in Batch Cultures: III. Nannochloropsis oculata (Eustigmatophyta). Departement of Basic Aquatic Sciences, Faculty of Aquaculture, Firat University, Elazig, Turkey. Asian Journal of Plant Sciences 4(6) : 642-644.
Barus. T. 2004. Pengantar Limnologi Studi tentang Ekosistem Air Daratan. USU Press. Medan.
Djarijah. A. S. 1995. Pakan Ikan Alami. Kanisius. Yogyakarta.
Effendi, H. 2003. Telaah Kualitas Air bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Kanisius, Yogyakarta.
Fajar, T. 2005. Pengaruh Pemberian Nannochloropsis sp., Natan dan Coccolith sp. pada Rotifera terhadap Kelangsungan Hidup dan Pertumbuhan Larva Ikan Kerapu Macan (Epinephelus fuscoguttatus). Skripsi. IPB. Bogor.
Gaur, J. A. 1980. A Manual orf Rural Composting. Project Field Document No. 15. Division of Microbiology, Indian Agricultural Research Institut. New Delhi Food Organization of The United Nation.
Irwanto, Sartika, T, Dewi, S, Kadek, A, dan Teguh, P. 2012. Jurnal. Aplikasi Pupuk NPK terhadap Pertumbuhan Nannochloropsis sp.
Kabinawa, I. N. K. 2006. Spirulina: Ganggang Penggempur Aneka Penyakit. Agro Media. Jakarta.
Lavelle, P. 1988. Earthworm Activities and The Soil System. Biol. Fertil. Soil 6 : 237-251.
Meritasari. D, Riyadhul, Dina, dan Sathiul. 2010. PKM Penelitian Universitas Airlangga. Surabaya. Eksplorasi bahan aktif mikroalga Nannochloropsis oculata sebagai antibakteri (penghambat) Vibrio alginolyticus.
Minnich, J. 1997. The Earthworm Book. How to Rise and Use Earthworm for your Farm and Garden. Rodale Press. New York.
Noviani, D. 2010. Pengaruh Pemberian Pupuk NPK dan Kompos terhadap Pertumbuhan Semai Jabon (Anthocephalus cadamba Roxb Miq.) pada Media Tanah Bekas Tambang Emas (Tailing). Skripsi. Bogor: IPB. 69 hlm.
Nugraha, E. 2009. Potensi dan Manfaat Budidaya Cacing Tanah. Titian Ilmu,
Bandung.
Restiade, I Nyoman, Muhdiat, Kenak, dan Ni Putu Ayu.2010. Populasi Kultur Massal Nannochloropsis oculata pada Salinitas Berbeda.
Rezza. M. 2011. Laju Pertumbuhan Mikroalga Penghasil Biofuel Jenis Chlorella
sp. dan Nannochloropsis sp. yang Dikultivasi Menggunakan Air Limbah Hasil Penambangan Timah di Pulau Bangka. Skripsi. Bogor: IPB. 102 hlm.
Rostini, I. 2007. Kultur fitoplankton (Chlorella sp. dan Tetraselmis chuii) pada skala laboratorium. Skripsi. Jatinagor: Universitas Padjajaran. 33 hlm.
Sastrawijaya, A, T. 1991. Pencemaran Lingkungan. Rineka Cipta, Jakarta.
Suantika, G. dan D. Hendrawandi. 2009. Efektivitas Teknik Kultur Menggunakan Sistem Kultur Statis, Semi-kontinyu dan Kontinyu Terhadap Produktivitas dan Kualitas Kultur Spirulina sp. Institut Teknologi Bandung. Bandung.
Wijaya, S. A. 2006. Pengaruh Pemberian Konsentrasi Urea yang Berbeda Terhadap Pertumbuhan Nannochloropsis oculata. Universitas Airlangga. Surabaya.
FK = 80.184.652.972.540
KK = 3,969475199
SED =
=
= √336.919.517.6
= 18.355, 36754
Uji BNT Kelimpahan sel
BNT = t 0,05 x SED
BNT 0,05 = T0,05 (8) x
=2,306 x
= 2,306 x √336.919.517.6
= 2,306 x 18.355, 36754
= 42.327,47755
BNT 0,01 = T0,01(8) x
= 3,355 x
= 3, 335 x √336.919.517.6
= 3,355 x 18.355, 36754
= 61.582,2581
Maka diperoleh Uji BNT:
BNT 0,05 = 42.327,47755
Perlakuan Rata-rata Pertumbuhan
Nilai BNT
0,05 Hitung Notasi
0 ppm 706.309
42.327.47755
748.636.477 A
50 ppm 2.643.864 2.648.096.478 B
150 pm 2.656.954 2.699.281.478 C
Kontrol 2.681.606 2.723.933.478 CD
100 ppm 2.871.591 2.913.918.478 D
Pada taraf uji 5% pengaruh pupuk kascing terhadap kelimpahan
Nannochloropsis sp. pada konsentrasi 100 ppm hanya berbeda tidak nyata
terhadap perlakuan kontrol dan berbeda nyata dengan pengaruh konsentrasi
lainnya.
Perlakuan Rata-rata Pertumbuhan
Nilai BNT
0,01 Hitung Notasi
0 ppm 706309 61.582,26 767.891 A
50 ppm 2.643.864 61.582,26 2.705.446 B
150 pm 2.656.954 61.582,26 2.718.536,26 BC
Kontrol 2.681.606 61.582,26 2.743.188,26 CD
100 ppm 2.871.591 61.582,26 2.933.173,26 D
Pada taraf uji 1% pengaruh pupuk kascing terhadap kelimpahan sel
Nannochloropsis sp. pada konsentrasi 100 ppm juga hanya berbeda tidak nyata
Lampiran 2. Alat dan Bahan
Alat
Haemocytometer Lux Meter
Toples Bening Bak media
Handcounter Timbangan Digital Mikroskop
Bahan
ZA SP36 Urea
Pupuk Kacing Vitamin B12
Pelaksanaan
Sterilisasi Pengisisan air ke dalam
media
Pemberian Perlakuan Kultur selama 10 hari