ISOLASI DAN KARAKTERISASI BAKTERI ENDOFIT POTENSIAL LENGKUAS MERAH (Alpinia purpuruta) DAN ANALISIS
SENYAWA ANTIBAKTERINYA
ELFIRA JUMRAH
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Isolasi dan Karakterisasi Bakteri Endofit Potensial Lengkuas Merah (Alpinia purpuruta) dan Analisis Senyawa Antibakterinya adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor (IPB).
Bogor, April 2016
Elfira Jumrah
RINGKASAN
ELFIRA JUMRAH. Isolasi dan Karakterisasi Bakteri Endofit Potensial Lengkuas Merah (Alpinia purpuruta) dan Analisis Senyawa Antibakterinya. Dibimbing oleh MARIA BINTANG dan FACHRIYAN HASMI PASARIBU.
Lengkuas merah (Alpinia purpuruta) merupakan tanaman yang banyak digunakan sebagai obat tradisional dan mengandung senyawa antibakteri. Bakteri endofit adalah mikroorganisme yang bersimbiosis mutualisme dengan tanaman inangnya dan dapat menghasilkan senyawa aktif, salah satunya yaitu senyawa antibakteri.
Penelitian ini bertujuan untuk mengisolasi bakteri endofit lengkuas merah, menguji aktivitas antibakteri terhadap bakteri patogen, mengkarakterisasi isolat bakteri endofit potensial secara konvensional dan molekuler, mengekstrak senyawa antibakteri yang dihasilkan serta menganalisis senyawa antibakterinya menggunakan GC-MS. Tahap awal penelitian yaitu isolasi bakteri endofit dari lengkuas merah, menguji setiap isolat bakteri endofit terhadap bakteri patogen menggunakan inokulasi titik, isolat potensial dikarakterisasi dan diekstraksi senyawa aktif dengan cara fermentasi 36 jam dalam nutrient broth. Hasil ekstrak diuji aktivitasnya dengan metode difusi sumur dan diperoleh ekstrak etil asetat sebagai fraksi potensial yang selanjutnya dianalisis menggunakan GC-MS yang bertujuan untuk mengetahui komponen senyawa aktif yang memiliki aktivitas antibakteri.
Hasil penelitian diperoleh sebanyak 16 isolat bakteri endofit, isolat potensial yang dapat menghambat bakteri patogen Gram positif (Staphylococcus
aureus dan Streptococcus mutans) dan Gram negatif (Salmonella sp. dan
Escherichia coli) yaitu isolat RL4, BL3 dan DL4. Berdasarkan karakterisasi
morfologi, biokimia dan molekuler menggunakan analisis sekuen 16S rRNA diperoleh bahwa isolat RL4 memiliki kemiripan 99% dengan Burkholderia
cenocepacia J231, isolat BL3 memiliki kemiripan 99% dengan Burkholderia
gladioli BSR3 strain BSR3 sedangkan isolat DL4 memiliki kemiripan 99% dengan
Bacillus amyloliquefaciens DSM7. Fraksi aktif hasil ekstraksi yaitu isolat RL4
ekstrak etil asetat. Hasil GC-MS menunjukkan senyawa dalam ekstrak etil asetat yaitu dokosan, eikosan, tetrakosan, heneikosan, heksadekanamida, pentakosan, oktadekan, asam heksanedioat dan pentadekan.
SUMMARY
ELFIRA JUMRAH. Isolation and Characterization of Bacteria Endophytic Potential Red galangal (Alpinia purpurata) and Analysis of Antibacterial Compounds. Supervised by MARIA BINTANG and FACHRIYAN HASMI PASARIBU.
Red galangal (Alpinia purpurata) is a plant widely used as traditional medicine and contains antibacterial compounds. Endophytic bacteria are microorganisms that are symbiotic mutualism with the host plant and can produce active compounds, one of them is antibacterial compound.
This study aims to isolate the endophytic bacteria red galangal, test antibacterial activity against pathogenic bacteria, characterize endophytic bacterial potential of conventional and molecular, extracted antibacterial compounds which produced and analysis antibacterial compounds using GC-MS. This research started of with isolation of endophytic from red galangal, tested each isolate endophytic bacteria against pathogens using inoculation point, potential isolates were characterized and extracted active compound by fermentation of 36 hours in a nutrient broth. The extract tested their activity with the well diffusion method and ethyl acetate extract obtained as a fraction potential to be further analyzed using GC-MS which aims to identified components of the active compound had antibacterial activity.
The results obtained showed that they were 16 isolates of endophytic bacteria, isolate potential to inhibit pathogenic Gram-positive bacteria
(Staphylococcus aureus and Streptococcus mutans) and Gram negative
(Salmonella sp. and Escherichia coli) that isolates RL4, BL3 and DL4. Based on
morphological, biochemical characterization and molecular sequences of 16S rRNA analysis showed that isolates RL4 has a 99% similarity with Burkholderia
cenocepacia J231, isolates BL3 has 99% similarity with Burkholderia gladioli
BSR3 strain BSR3, while isolates DL4 has 99% similarity with Bacillus
amyloliquefaciens DSM7. The active fraction extraction results that isolates RL4
ethyl acetate extract. The results of GC-MS showed the compounds in the ethyl acetate extract are docosane, eicosane, tetracosane, heneicosane, hexadecanamide, pentacosane, octadecane, hexanedioic acid and pentadecane
Keywords : endophytic bacteria, GC-MS, red galangal, 16S rRNA
© Hak Cipta Milik IPB, Tahun 2016
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB.
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Biokimia
ISOLASI DAN KARAKTERISASI BAKTERI ENDOFIT POTENSIAL LENGKUAS MERAH (Alpinia purpuruta) DAN ANALISIS
SENYAWA ANTIBAKTERINYA
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2016
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala rahmat dan hidayah sehingga penulis dapat menyelesaikan tesis yang berjudul “Isolasi dan Karakterisasi Bakteri Endofit Potensial Lengkuas Merah
(Alpinia purpuruta) dan Analisis Senyawa Antibakterinya” dapat diselesaikan
dengan baik. Penelitian ini berlangsung selama 5 bulan dari Oktober 2015 sampai Maret 2016 di Laboratorium Bakteriologi Divisi Mikrobiologi Medik Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner Fakultas Kedokteran Hewan dan Laboratorium Penelitian Departemen Biokimia Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor (IPB).
Penulis mengucapkan terima kasih kepada semua pihak yang telah membantu dalam menyelesaikan tesis ini, terutama kepada:
1. Prof Dr Drh Maria Bintang MS dan Prof Dr Drh Fachriyan Hasmi Pasaribu selaku pembimbing yang telah banyak memberikan arahan dan bimbingan, nasehat, waktu konsultasi serta solusi dari setiap permasalahan yang dihadapi penulis selama menyelesaikan tesis ini.
2. Bapak Agus Somantri dan staf Laboratorium Bakteriologi Divisi Mikrobiologi Medik yang banyak membantu selama penelitian penulis.
3. Kedua orang tua, bapak Jumasing dan ibu Rahmatiyah yang selalu mendoakan, mendukung dan memotivasi penulis untuk menyelesaikan tesis ini.
4. Keluarga besar Puang H. Colleng dan Puang H. Baido
5. Keluarga besar mahasiswa pascasarjana program studi Biokimia, sahabat dan semua pihak yang tidak bisa disebutkan satu persatu.
Akhir kata, Semoga karya ilmiah ini bermanfaat bagi semua pihak untuk kemajuan ilmu pengetahuan dibidang ilmu biokimia dan biomedis.
Bogor, April 2016
DAFTAR ISI
Waktu dan Tempat Penelitian 4 Alat dan Bahan 4
DAFTAR TABEL
1 Morfologi koloni isolat bakteri endofit lengkuas merah 9 2 Hasil pengujian isolat bakteri endofit terhadap bakteri patogen 10
3 Karakterisasi morfologi sel dan biokimia 11
4 Aktivitas antibakteri fraksi isolat bakteri endofit potensial 12 5 Aktivitas antibakteri fraksi etil asetat isolat bakteri endofit RL4 13
DAFTAR GAMBAR
1 Tanaman lengkuas merah 8
2 Koloni bakteri endofit lengkuas merah 8
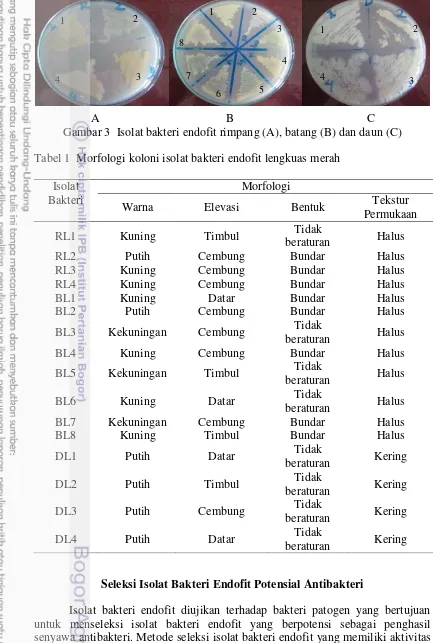
3 Isolat bakteri endofit rimpang (A), batang (B) dan daun (C) 9 4 Pewarnaan Gram sel bakteri isolat BL3 (A), RL4 (B) dan DL4 (C) 11 5 Kromatogram hasil analisis GC-MS fraksi etil asetat isolat RL4 13
DAFTAR LAMPIRAN
1 Bagan alir penelitian 32
2 Hasil BLAST isolat RL4, BL3 dan DL4 33
3 Rekonstruksi pohon filogenik isolat RL4, BL3 dan DL4 34
4 Kurva pertumbuhan isolat RL4 35
1 PENDAHULUAN
Latar Belakang
Resistensi bakteri patogen terhadap antibiotik merupakan tantangan terbesar pada pengobatan penyakit infeksi (Wright 2010), beberapa bakteri patogen seperti Salmonella resisten terhadap antibiotik komersial streptomycin,
Escherichia coli resisten terhadap streptomycin, rifampicin, norfloxacin,
fosfomycin dan bakteri Staphylococcus aureus, resisten terhadap antibiotik
vancomycin, methicilin, mupiricin, rifampicin dan fusidic acid (Andersson &
Hughes 2010). Pemanfaatan mikroorganisme untuk menghasilkan antibiotik telah lama dikembangkan seperti pada penelitian Yulinah (1987) yang berhasil mengisolasi Streptomyces indonesiensis ATCC 45859 yang memiliki aktivitas kuat sebagai antijamur, hasil ini telah dipatenkan di Amerika Serikat. Pemanfaatan mikroorganisme yang bersimbiosis dengan tanaman inangnya yang dikenal dengan sebutan mikroba endofit dapat juga dijadikan sebagai salah satu sumber senyawa antibiotik. Penelitian mikroba endofit yang menghasilkan senyawa antibiotik berspektrum luas munumbicin yaitu dari endofit Streptomyces
spp. strain NRRL 30562 yang merupakan endofit yang diisolasi dari tanaman
Kennedia nigriscans (Castillo et al. 2002) dan antibiotik kakadumycin yang telah
diisolasi dari endofit tanaman Grevillea pteridifolia (Castillo et al. 2003). Salah satu, tanaman inang yang berpotensi sebagai sumber bakteri endofit yaitu lengkuas merah, masyarakat umum banyak memanfaatkan lengkuas merah sebagai obat tradisional.
Tanaman lengkuas termasuk dalam genus Alpinia. Alpinia adalah genus terbesar, paling luas dan taksonomi paling kompleks pada famili Zingiberaceae
dengan 230 spesies yang terdapat di seluruh daerah tropis dan subtropis Asia (Kress et al. 2005). Berdasarkan penelitian etnobotani, spesies Alpinia telah banyak dimanfaatkan sebagai bahan obat-obatan di negara Asia (Phang et al. 2013) dan menurut Ghosh dan Rangan (2012), genus Alpinia memiliki potensi biomedis yang dapat digunakan dimasa yang akan datang. Di Indonesia lengkuas banyak dimanfaatkan sebagai bumbu dapur, pengawet makanan dan digunakan sebagai obat gosok untuk mengobati penyakit kulit seperti panu (Handajani & Purwoko 2008). Tanaman lengkuas ada beberapa jenis antara lain lengkuas putih
(Alpinia galangal) yang banyak digunakan sebagai bumbu dapur dan lengkuas
merah (Alpinia purpuruta) digunakan sebagai obat oleh masyarakat umum (Bermawie et al. 2012). Berbagai manfaat lengkuas yang dipercaya masyarakat yaitu menghilangkan panu, menghilangkan bau mulut, mengobati sakit gigi, melancarkan peredaran darah dan mengobati asam urat. Itokawa dan Takeya (1993) menjelaskan bahwa tanaman lengkuas mengandung golongan senyawa flavonoid, fenol dan terpenoid yang dapat digunakan sebagai bahan dasar obat-obatan modern.
Secara farmakologis, ekstrak lengkuas mempunyai aktivitas sebagai antijamur (Khattak et al. 2005), antikanker (Rusmarilin 2003), antioksidan yang cukup tinggi (Juntachote & Berghofer 2005), sebagai immunomodulator (Weidner
et al. 2007), penurun tekanan darah tinggi, obat gatal (Morikawa et al. 2005) serta
2
dalam lengkuas dapat menghambat perkembangan virus HIV (Ying & Baoan 2006), sebagai antitumor dan antimikroba (Vankar et al. 2006; Voravuthikunchai
et al. 2006). Menurut Oonmetta-aree (2006), ekstrak lengkuas memiliki aktivitas
daya hambat yang tinggi terhadap Staphylococcus aureus dibandingkan kunyit, jahe dan krachai. Penelitian bunga lengkuas merah (Santos et al. 2012) menghasilkan 42 minyak esensial, komponen utama minyak esensial yang
dihasilkan yaitu α-pinene, β-pinene dan β-caryophyllene yang dianalisis menggunakan GC-MS. Minyak esensial yang diperoleh diujikan pada larva nyamuk Aedes aegypti dan larva nyamuk demam berdarah yang memberikan hasil positif, serta pengujiannya pada bakteri Gram negatif dan bakteri Gram positif yang hasilnya dapat dihambat secara signifikan. Dan menurut Victorio et al. (2009), Rimpang lengkuas merah mengandung senyawa flavonoid, kaempferol-3-rutinoside dan kaempferol-3-oliucronide.
Berbagai manfaat tanaman lengkuas merah ini dapat menjadi acuan untuk memperoleh senyawa aktif yang terdapat dalam tanaman lengkuas yang nantinya dapat dikembangkan sebagai senyawa antibakteri. Namun, pengambilan senyawa bioaktif dari tanaman membutuhkan banyak biomassa. Cara efisien untuk memperoleh senyawa bioaktif tersebut adalah menggunakan mikroba endofit. Endofit diketahui mampu menghasilkan sejumlah senyawa bioaktif, sehingga tidak harus mengekstrak senyawa bioaktif tersebut dari tanaman inangnya. Beragam metabolit telah diisolasi dari endofit seperti alkaloid, peptida, steroid, terpenoid, fenol, kuinon dan flavonoid (Sun et al. 2010). Bakteri endofit memiliki potensi yang besar untuk dimanfaatkan sebagai penghasil senyawa aktif seperti yang terkandung dalam tanaman inangnya.
Pemanfaatan mikroorganisme jenis bakteri endofit telah banyak menarik perhatian karena kemampuannya menghasilkan senyawa aktif, senyawa aktif ini digunakannya untuk mempertahankan diri dari serangan hama maupun lingkungan. Bakteri endofit dan inangnya memiliki jalur sintesis senyawa aktif yang sama karena transfer gen, sehingga senyawa aktif yang dihasilkan oleh inangnya juga dapat diproduksi oleh bakteri endofit, bahkan dipercaya bahwa bakteri endofit dapat menghasilkan senyawa aktif jauh melampaui inangnya (Wang & Dai 2011).
Berdasarkan hal diatas, tanaman lengkuas merah dapat dimanfaatkan sebagai sumber bakteri endofit yang dapat menghasilkan senyawa aktif yang aktivitas dan manfaat serupa dengan tanaman inangnya, seperti senyawa antibakteri. Senyawa antibakteri yang dihasilkan dapat berperan penting dalam dunia medis. Sampai saat ini, belum ada publikasi tentang isolasi dan pengujian terhadap senyawa aktif yang diproduksi oleh bakteri endofit tanaman lengkuas merah.
Perumusan Masalah
3
Tujuan Penelitian
Penelitian ini bertujuan mengisolasi dan mengkaraterisasi bakteri endofit yang menghasilkan senyawa antibakteri yang diperoleh dari tanaman lengkuas merah (Alpinia purpuruta) dan menganalisis senyawa aktif potensial antibakteri.
Manfaat Penelitian
Hasil penelitian ini diharapkan dapat menambah informasi tentang cara mengisolasi dan mengkaraterisasi bakteri endofit yang menghasilkan senyawa antibakteri yang diperoleh dari tanaman lengkuas merah (Alpinia purpuruta) dan menganalisis senyawa aktif potensial antibakteri.
Hipotesis
2 METODE
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Oktober 2015 hingga Maret 2016 di Laboratorium Bakteriologi, Divisi Mikrobiologi Medik Fakultas Kedokteran Hewan IPB dan Laboratorium Penelitian Departemen Biokimia FMIPA IPB.
Alat dan Bahan
Alat yang akan digunakan sebagai berikut : Pipet mikro, tabung reaksi, gelas kimia, jangka sorong, cawang Petri, Ose, bunsen, autoklaf, mesin sentrifugasi, corong pisah, vakum evaporator, inkubator (Orbital Shaking
Incubator), spektrofotometri UV-VIS, mikroskop, mesin Polymerase Chain
Reaction (PCR), Applied Biosystems model 3730XL automated DNA sequencing
system (Applied BioSystems, USA) dan alat GC-MS (Agilent Technologies,
USA). Bahan yang akan digunakan sebagai berikut : Rimpang (RL), batang (BL) dan daun (DL) tanaman lengkuas merah segar yang diperoleh dari Pusat Studi Biofarmaka IPB, kultur Staphylococcus aureus, Streptococcus mutans,
Salmonella sp. dan Escherichia coli (koleksi dari Laboratorium Bakteriologi
Fakultas Kedokteran Hewan, Institut Pertanian Bogor), Nutrient Agar (Oxoid)
dan Nutrient Broth (Difco), Na-hipoklorit 5%, alkohol 75%, etil asetat, n-heksan,
kloroform, larutan garam steril, kloramfenikol, aquades, nistanin, katalase, oksidase, urease, sitrat, TSA, MacConkey, manitol, maltosa, glukosa, laktosa, sukrosa, kristal violet, safranin, kertas tetrametil, primer (27F, 1492R, 785F dan 907R), InstaGene Matrix (Bio-Rad, USA), Montage PCR Clean up kit (Milipore)
dan Big Dye terminator cycle sequencing kit (Applied BioSystems, USA).
Prosedur Penelitian Isolasi Bakteri Endofit dari Lengkuas Merah
Seleksi Isolat Bakteri Endofit yang Potensial sebagai Antibakteri (Simarmata et al. 2007)
Kultur bakteri uji (Staphylococcus aureus, Streptococcus mutans,
Salmonella sp. dan Escherichia coli) ditumbuhkan di media cair (Nutrient Broth)
dan diinkubasi selama 24 jam pada suhu 37°C, dan diambil sebanyak 0.4 mL kemudian ditambahkan ke dalam 80 mL media NA yang bersuhu ±40°C dan dikocok. Media NA yang berisi bakteri uji dituang kedalam cawan Petri steril sebanyak 20 mL dan didiamkan hingga memadat. Isolat bakteri endofit yang telah diregenerasi, diinokulasi ke media yang berisi bakteri uji menggunakan Ose dan diinkubasi disuhu 37°C selama 24-48 jam secara aseptik. Zona hambat yang terbentuk diamati dan diukur menggunakan jangka sorong, dengan adanya zona hambat di sekeliling isolat bakteri endofit menunjukkan adanya aktivitas senyawa antibakteri yang dihasilkan oleh bakteri endofit. Isolat endofit potensial sebagai antibakteri dianalisis lebih lanjut.
Karakterisasi Morfologi Sel dan Biokimia Isolat Bakteri Endofit Potensial (Cowan 1974)
Isolat bakteri endofit potensial dikarakterisasi dengan metode konvensional yaitu uji morfologi dan biokimia, meliputi: pewarnaan Gram, uji katalase, uji oksidase, urease, pertumbuhan (MacConkey, TSA dan sitrat), fermentasi karbohidrat (manitol, maltosa, glukosa, sukrosa dan laktosa). Isolat bakteri endofit potensial diregenerasi pada media NA dan diinkubasi selama 24 jam. Isolat bakteri endofit potensial yang telah siap selanjutnya dilakukan pewarnaan Gram dengan cara, menggoreskan isolat bakteri endofit pada keseluruh plat kaca menggunakan kawat Ose dan ditambahkan sedikit larutan garam steril. Selanjutnya dikeringkan, setelah kering ditetesi larutan kristal violet hingga menutupi seluruh plat kaca dan didiamkan selama 1 menit. Ditetesi lagi larutan lugol iodin dan didiamkan 1 menit. Kemudian dibilas dengan aquades dan alkohol selama 15 detik setelah itu, dibilas lagi dengan aquades. Terakhir ditetesi safranin selama 1 menit dan dibilas dengan aquades. Plat kaca dikeringkan dan kemudian diamati dengan menggunakan mikroskop.
Isolat bakteri endofit yang telah diregenerasi di media NA ditumbuhkan lagi pada media pertumbuhan MacConkey, TSA dan sitrat dengan cara digoreskan menggunakan kawat Ose, dan diinkubasi selama 24 jam pada suhu 30°C. Pengujian selanjutnya yaitu untuk melihat kemampuan fermentasi karbohidrat isolat bakteri endofit, dengan menggunakan kawat Ose isolat bakteri endofit masing-masing dimasukkan dalam larutan manitol, maltosa, glukosa, sukrosa dan laktosa dan diinkubasi pada suhu 30°C dan diamati perubahannya setelah 24 jam. Karakterisasi Molekuler Isolat Bakteri Endofit Potensial dengan Analisis Sekuen 16S rRNA (Macrogen)
dan dipanaskan 10 menit pada suhu 100°C. Supernatan yang diperoleh setelah pemanasan selanjutnya dapat digunakan untuk proses PCR.
Amplifikasi DNA dan pengurutan basa (sequencing) gen 16S rRNA. Proses amplifikasi ini menggunakan PCR (Polymerase Chain Reaction).
Sebanyak 1 μL DNA dimasukkan kedalam 20 μL larutan reaksi PCR yang berisi
primer 27F dan 1492R. Pengulangan dilakukan sebanyak 35 siklus dengan beberapa tahapan: tahap denaturasi (suhu 94°C selama 45 detik), penempelan (55°C selama 60 detik) dan perpanjangan (72°C selama 60 detik). Hasil yang diperoleh dipurifikasi dengan menggunakan alat Montage PCR Clean up kit
(Millipore). Dengan menggunakan primer 785F dan 907R, hasil PCR di
sequencing dengan menggunakan Big Dye terminator cycle sequencing kit
(Applied BioSystems, USA), dan dianalisis menggunakan Applied Biosystems
model 3730XL automated DNA sequencing system (Applied BioSystems, USA).
Analisis hasil sequencing. Urutan basa DNA hasil sequencing selanjutnya disejajarkan dengan menggunakan program BioEdit Sequence Alignment Editor ver. 7.2.0. Hasil pensejajaran kemudian dianalisis menggunakan program BLAST pada situs www.ncbi.nlm.nih.gov yang bertujuan untuk mengetahui spesies isolat bakteri endofit yang potensial dan rekonstruksi pohon filogenik metode Neighbor Joining .
Fermentasi dan Ekstraksi Senyawa Antibakteri dari Isolat Bakteri Endofit Potensial (Melliawati et al. 2006 modifikasi)
Satu Ose isolat bakteri endofit BL3, RL4 dan DL4 dikultivasi dalam media
nutrient broth 50 mL dan diinkubasi dalam penggoyang berputar (Orbital Shaking
Incubator) pada suhu 30°C selama 36 jam dengan kecepatan 150 rpm. Kemudian
hasil fermentasi disetrifugasi yang bertujuan memisahkan pelet dan supernatan, selama 15 menit dengan kecepatan 3600 rpm. Supernatan ditambahkan pelarut n -heksan, etil asetat, klorofrom (1:1 v/v), kemudian diinkubasi dalam penggoyang berputar (Orbital Shaking Incubator) pada suhu 30°C selama 2 jam dengan kecepatan 150 rpm, selanjutnya supernatan dan ekstrak n-heksan, etil asetat dan kloroform dipisahkan menggunakan corong pisah, ekstrak yang diperoleh diuji masing-masing aktivitas antibakteri terhadap Staphylococcus aureus,
Streptococcus mutans, Salmonella sp. dan Escherichia coli dengan menggunakan
metode difusi sumur dan masing-masing pelarut sebagai kontrol negatif, selanjutnya ekstrak potensial sebagai antibakteri dievaporasi pada suhu 50°C. Ekstrak kental yang potensial dengan berbagai konsentrasi (100 ppm, 250 ppm, 500 ppm, 750 ppm, 1000 ppm) diujikan menggunakan metode difusi sumur terhadap bakteri Staphylococcus aureus, Streptococcus mutans, Salmonella sp.
dan Escherichia coli, pelarut sebagai kontrol negatif dan kloramfenikol 100
µg/mL kontrol positif.
Identifikasi Senyawa Antibakteri Ekstrak Etil Asetat dengan GC-MS
Ekstrak etil asetat isolat RL4 diinjeksikan 1 µL ke kolom GC-MS. Proses GC-MS menggunakan kolom kapiler tipe Agilent J & W GC diameter 0.25 mm, panjang 60 m, gas pembawa helium, temperatur max detektor 325°C, split ratio 1:1, dan suhu kolom 100°C. Suhu dinaikkan 15°C permenit hingga mencapai suhu 290°C yang stabil pada menit ke-30. Hasil GC-MS yang diperoleh
dibandingkan dengan database (Willey9N11.L). Hasil analisis ini berupa bobot molekul dan pola fragmentasi.
3 HASIL
Isolat Bakteri Endofit Lengkuas Merah (Alpinia purpuruta)
Bakteri endofit berhasil diisolasi dari lengkuas merah. Lengkuas merah merupakan tanaman yang tumbuh tegak, batangnya terdiri dari susunan pelepah daun. Daunnya bulat panjang yang bagian bawah terdiri atas pelepah-pelepah. Rimpang umbinya berwarna kemerahan, berserat kasar dan beraroma khas (Gambar 1). Lengkuas merah ini diperoleh dari kebun Biofarmaka IPB. Lengkuas merah yang digunakan adalah lengkuas merah segar. Sampel lengkuas merah disterilisasi permukaan menggunakan sodium hipoklorit dan alkohol tujuannya untuk menghilangkan mikroorganisme epifit, sebelum diinokulasi pada media
nutrien agar. Selanjutnya, diinkubasi di ruang gelap dan suhu 30°C selama 48
jam. Koloni yang tumbuh selanjutnya dipisahkan berdasarkan morfologi koloninya (Gambar 2). Bakteri endofit diisolasi sebanyak 16 isolat, masing-masing 4 isolat dari daun (RL) dan rimpang (DL), sedangkan pada batang (BL) sebanyak 8 isolat (Gambar 3). Karakterisasi morfologi bakteri endofit dapat dilakukan dengan melihat keragaman bakteri endofit dari lengkuas merah, meliputi warna, elevasi, bentuk dan tekstur permukaan (Tabel 1).
Gambar 1 Tanaman lengkuas merah (Dokumentasi pribadi 2015)
A B C
Gambar 2 Koloni bakteri endofit lengkuas merah rimpang (A), batang (B) dan daun (C)
A B C Gambar 3 Isolat bakteri endofit rimpang (A), batang (B) dan daun (C) Tabel 1 Morfologi koloni isolat bakteri endofit lengkuas merah
Seleksi Isolat Bakteri Endofit Potensial Antibakteri
Isolat bakteri endofit diujikan terhadap bakteri patogen yang bertujuan untuk menseleksi isolat bakteri endofit yang berpotensi sebagai penghasil senyawa antibakteri. Metode seleksi isolat bakteri endofit yang memiliki aktivitas
Isolat Bakteri
Morfologi
Warna Elevasi Bentuk Tekstur
Permukaan
BL3 Kekuningan Cembung Tidak
beraturan Halus
BL4 Kuning Cembung Bundar Halus
BL5 Kekuningan Timbul Tidak
beraturan Halus
BL6 Kuning Datar Tidak
beraturan Halus
BL7 Kekuningan Cembung Bundar Halus
antibakteri yaitu dengan inokulasi titik terhadap bakteri patogen. Bakteri patogen yang digunakan yaitu bakteri Gram positif (Staphylococcus aureus dan
Streptococcus mutans) dan bakteri Gram negatif (Salmonella sp. dan Escherichia
coli). Isolat bakteri endofit ini memiliki aktivitas yang berbeda-beda dalam menghambat bakteri patogen. Tabel 2 menunjukkan aktivitas antibakteri setiap isolat bakteri endofit. Isolat bakteri endofit yang memiliki aktivitas kuat dalam menghambat bakteri patogen merupakan bakteri potensial yang selanjutnya dikarakterisasi untuk mengetahui jenis spesies bakterinya.
Tabel 2 Hasil pengujian isolat bakteri endofit terhadap bakteri patogen Isolat
Keterangan : (v) terdapat zona hambat tetapi sangat kecil dan sulit terukur
Isolat bakteri endofit pada batang (BL3, BL5, dan BL7) memiliki daya hambat yang kuat dibanding isolat bakteri endofit batang lainnya yang ditandai dengan luasnya zona bening yang terbentuk. Sedangkan, isolat bakteri endofit rimpang kode (RL4) dan isolat bakteri endofit daun kode (DL4) mampu menghambat bakteri Gram positif dan Gram negatif namun, aktivitasnya jauh lebih kecil dibanding isolat pada batang. Isolat bakteri endofit RL4, BL3 dan DL4 adalah bakteri potensial karena mampu menghambat keempat bakteri patogen dan aktivitas hambatanya jauh lebih besar dibanding isolat bakteri endofit lainnya ditandai dengan luas zona bening yang terukur.
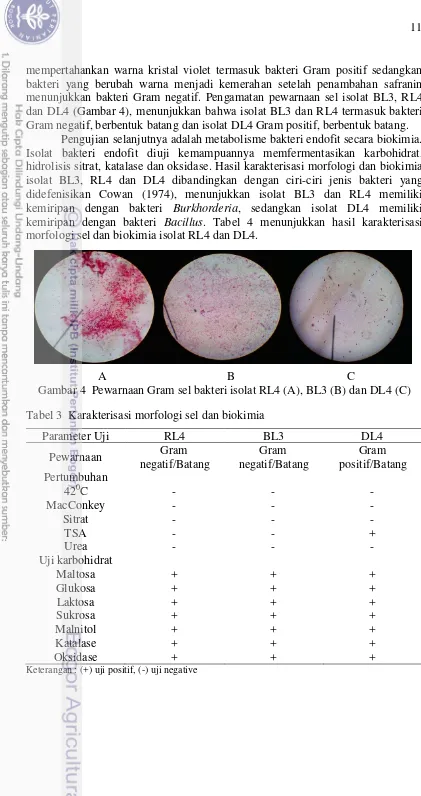
mempertahankan warna kristal violet termasuk bakteri Gram positif sedangkan bakteri yang berubah warna menjadi kemerahan setelah penambahan safranin menunjukkan bakteri Gram negatif. Pengamatan pewarnaan sel isolat BL3, RL4 dan DL4 (Gambar 4), menunjukkan bahwa isolat BL3 dan RL4 termasuk bakteri Gram negatif, berbentuk batang dan isolat DL4 Gram positif, berbentuk batang.
Pengujian selanjutnya adalah metabolisme bakteri endofit secara biokimia. Isolat bakteri endofit diuji kemampuannya memfermentasikan karbohidrat, hidrolisis sitrat, katalase dan oksidase. Hasil karakterisasi morfologi dan biokimia isolat BL3, RL4 dan DL4 dibandingkan dengan ciri-ciri jenis bakteri yang didefenisikan Cowan (1974), menunjukkan isolat BL3 dan RL4 memiliki kemiripan dengan bakteri Burkhorderia, sedangkan isolat DL4 memiliki kemiripan dengan bakteri Bacillus. Tabel 4 menunjukkan hasil karakterisasi morfologi sel dan biokimia isolat RL4 dan DL4.
A B C
Gambar 4 Pewarnaan Gram sel bakteri isolat RL4 (A), BL3 (B) dan DL4 (C) Tabel 3 Karakterisasi morfologi sel dan biokimia
Parameter Uji RL4 BL3 DL4
Keterangan : (+) uji positif, (-) uji negative
Karakterisasi Molekuler 16S rRNA Isolat Bakteri Endofit Potensial Isolat BL3, RL4 dan DL4 dikarakterisasi menggunakan analisis 16S rRNA, hasil sekuensing berdasarkan warna puncak kromatogram yang menggambarkan letak nukleotida amplifikasi hulu dan hilir. Urutan basa hasil analisis 16S rRNA ini, dibandingkan dengan urutan basa pada NCBI-GenBank
database. Hasil pensejajaran sekuen 16S rRNA, menunjukkan bahwa panjang
pasangan basa isolat BL3 1483 bp, RL4 1467 bp dan DL4 1494 bp.
Urutan basa hasil sekuensing dianalisis menggunakan program BLAST. Hasil BLAST menunjukkan persentase kemiripan isolat BL3 dengan
Burkholderia gladioli BSR3 strain BSR3 sebesar 99%, nilai bit score 2717 dan
E-value 0, isolat RL4 memiliki kemiripan 99%, nilai bit score 2699, E-value 0
dengan Burkholderia cenocepacia J2315, sedangkan isolat DL4 memiliki kemiripan 99% dengan Bacillus amyloliquefaciens DSM7, bit score 2736 dan
E-value 0. Perbandingan tingkat kemiripan sekuen isolat BL3, RL4 dan DL4 dengan
sekuen 16S rRNA yang terdapat pada GenBank NCBI dengan progam BLAST dapat dilihat pada (Lampiran 2). Hasil BLAST diperkuat dengan rekonstruksi pohon filogenik metode Neighbor Joining (Lampiran 3).
Aktivitas Antibakteri Senyawa Aktif Isolat Potensial
Senyawa aktif yang memiliki aktivitas antibakteri dari bakteri endofit isolat BL3, RL4 dan DL4 diisolasi dengan proses fermentasi dan ekstraksi. Isolat BL3, RL4 dan DL4 dikultivasi selama 36 jam berdasarkan kurva pertumbuhan yang telah dibuat (Lampiran 4). Ekstraksi senyawa antibakteri isolat BL3, RL4 dan DL4 menggunakan pelarut n-heksan, etil asetat dan kloroform. Ekstrak masing-masing pelarut diujikan terhadap bakteri patogen. Hasil uji aktivitas fraksi setiap pelarut isolat BL3, RL4 dan DL4 terhadap bakteri patogen ditunjukkan pada Tabel 4.
Tabel 4 Aktivitas antibakteri fraksi isolat bakteri endofit potensial Jenis
Keterangan : (v) terdapat zona hambat tetapi sangat kecil dan sulit terukur
Fraksi etil asetat RL4 memiliki aktivitas antibakteri yang lebih besar dibanding fraksi lainnya. Fraksi etil asetat RL4 ini diuapkan pelarutnya pada suhu 500C dengan menggunakan evaporator hingga diperoleh ekstrak kental. Ekstrak kental yang diperoleh sebanyak 14,80 mg. Ekstrak kental fraksi etil asetat RL4 dilarutkan kembali dengan pelarut etil asetat dengan konsentrasi bertingkat (100 ppm, 250 ppm, 500 ppm, 750 ppm dan 1000 ppm). Masing-masing konsentrasi fraksi etil asetat isolat RL4 diujikan kembali terhadap bakteri Staphylococcus
aureus, Salmonella sp. dan Escherichia coli. Kloramfenikol digunakan sebagai
1 0 . 0 0 1 5 . 0 0 2 0 . 0 0 2 5 . 0 0 3 0 . 0 0 3 5 . 0 0 4 0 . 0 0
Tabel 5 Aktivitas antibakteri fraksi etil asetat isolat bakteri endofit RL4 Bakteri
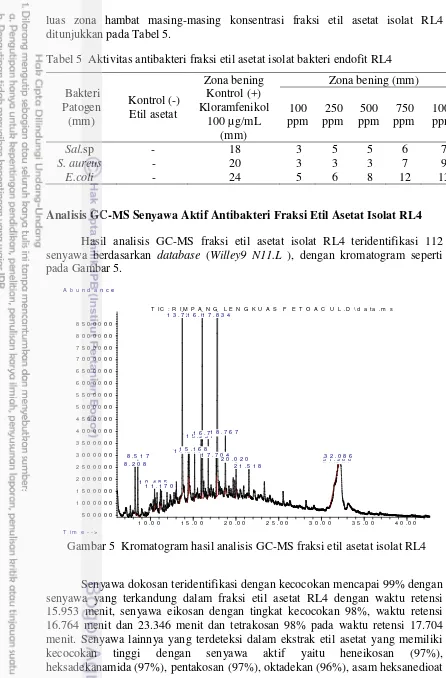
Analisis GC-MS Senyawa Aktif Antibakteri Fraksi Etil Asetat Isolat RL4 Hasil analisis GC-MS fraksi etil asetat isolat RL4 teridentifikasi 112 senyawa berdasarkan database (Willey9 N11.L ), dengan kromatogram seperti pada Gambar 5.
Gambar 5 Kromatogram hasil analisis GC-MS fraksi etil asetat isolat RL4
(95%) dan pentadekan (95%), setiap senyawa memiliki pola fragmentasi yang berbeda-beda (Lampiran 5).
4 PEMBAHASAN
Isolat Bakteri Endofit Lengkuas Merah (Alpinia purpuruta)
Bakteri endofit dapat diisolasi dari jaringan tanaman lengkuas merah baik dari daun, batang maupun rimpang. Menurut Yu et al. (2010), bakteri endofit dapat ditemukan di seluruh spesies tanaman di dunia dan memberikan keuntungan terhadap inangnya. Bakteri endofit adalah mikroorganisme yang seluruh atau sebagian hidupnya berada dalam jaringan tumbuhan (akar, batang, cabang atau ranting tumbuhan), yang mana diantara keduanya terjalin hubungan yang saling menguntungkan. Mikroba ini hidup diantara sel tumbuhan dan bersimbiosis mutualisme dengan tanaman inangnya (Kumala & Siswanto. 2007). Kebanyakan tanaman inang memiliki satu atau lebih jenis bakteri endofit yang dimilikinya (Castilo et al. 2003). Bakteri endofit memberikan keuntungan untuk tanaman inang dengan memproduksi senyawa pengatur pertumbuhan tanaman yang dapat memberikan ketahanan terhadap penyakit dan juga membantu dalam fitoremediasi (Lodewyckx et al. 2002). Selain itu, bakteri endofit juga mampu menghasilkan senyawa aktif, yang sama dengan inangnya. Bakteri endofit telah berhasil diisolasi dari tanaman padi (Sang et al. 2014), akar jagung (Szilagyi-Zecchin et al. 2014 ), bawang putih yang menghasilkan endofit jenis Trichoderma brevicompactum
yang memiliki aktivitas penghambat Rhizoctonia solani, Botrytis cinerea, dan
Colletotrichum lindemuthianum (Shentu et al. 2014) dan Bakteri endofit jenis
Lysinibacillus sp. telah berhasil diidentifikasi dari tanaman bakau (Avicennia
marina) yang memiliki kemampuan menghasilkan adenosine deaminase
(Kathiresan et al. 2014). Menurut (Retnowati et al. 2012), kemampuan bakteri endofit menghasilkan senyawa metabolit sekunder akan berbeda-beda bergantung pada asal isolat bakteri endofit, jenis bakterinya dan kondisi perakaran tanaman inangnya.
Bakteri endofit diisolasi dari jaringan lengkuas merah melalui proses sterilisasi permukaan, menggunakan sodium hipoklorit 5% yang berfungsi sebagai disinfektan mikroorganisme epifit dari permukaan sampel. Menurut Valera et al.
Hasil isolasi bakteri endofit pada lengkuas merah diperoleh 16 isolat (Gambar 3), isolat terbanyak terdapat di batang yaitu 8 isolat, sedangkan pada daun dan rimpang masing-masing 4 isolat. Menurut Lodewyckx et al. (2002), bakteri endofit dapat diisolasi dari akar, daun, batang, bunga, buah dan biji tanaman. Keragaman morfologi koloni bakteri endofit ditunjukkan pada Tabel 1. Keragaman bakteri endofit bergantung pada kondisi tanaman inang, misal umur tanaman, jenis tanaman, tempat tumbuh, waktu pengambilan sampel, dan sebaran geografis (Seo et al. 2010; Mano et al. 2007).
Seleksi Aktivitas Antibakteri Isolat Bakteri Endofit
Isolat bakteri endofit yang diperoleh diuji aktivitas antibakterinya terhadap bakteri patogen Gram positif (Staphylococcus aureus dan Streptococcus mutans) dan bakteri Gram negatif (Salmonella sp. dan Escherichia coli) melalui metode inokulasi titik. Uji positif isolat bakteri endofit menghambat bakteri patogen Gram positif dan Gram negatif ditandai dengan terbentuknya zona bening di sekitar titik isolat. Menurut Kusumawati (2014), zona bening yang terbentuk adalah bentuk hambatan dari senyawa metabolit yang dihasilkan bakteri endofit.
Hasil uji aktivitas antibakteri isolat bakteri endofit lengkuas merah menunjukkan spektrum yang luas karena dapat menghambat bakteri patogen Gram positif dan Gram negatif, isolat bakteri endofit yang mampu menghambat bakteri Gram positif dan Gram negatif adalah RL4, BL1, BL3, BL4, BL5, BL7, DL3 dan DL4 (Tabel 2). Isolat bakteri endofit potensial terpilih yaitu RL4, BL3 dan DL4, isolat ini memiliki aktivitas hambatan terhadap bakteri patogen Gram positif maupun Gram negatif lebih kuat dibandingkan isolat lainnya disetiap bagian jaringannya sehingga dilanjutkan untuk karakterisasi. Setiap isolat bakteri endofit memiliki aktivitas antibakteri berbeda-beda dan beberapa isolat tidak memiliki aktivitas antibakteri, namun bisa jadi menghasilkan senyawa lain seperti senyawa anti insektisida, antifungi atau hormon pertumbuhan Indole-3 Acetic Acid (IAA) seperti yang dihasilkan bakteri endofit dari Oryza sativa L. organik (Duangpaeng et al. 2012).
Isolat bakteri endofit yang memiliki aktivitas antibakteri menunjukkan jika terdapat senyawa antibakteri yang dihasilkannya. Penelitian Parwata dan Dewi (2008) menggunakan ekstrak rimpang lengkuas yang mengandung minyak atsiri mampu menghambat bakteri Staphylococcus aureus. Hal ini menandakan, bakteri endofit mampu mensintesis senyawa antibakteri yang sama dengan inangnya.
Berdasarkan penelitian, isolat potensial yang memiliki kemampuan menghambat keempat bakteri patogen, masing-masing disetiap jaringan lengkuas merah yaitu BL3 di jaringan batang, DL4 di jaringan daun dan RL4 di jaringan rimpang. Selanjutnya isolat potensial dikarakterisasi dengan metode konvensional dan analisis 16S rRNA.
pengamatan morfologi koloni tidak cukup untuk mengidentifikasi jenis bakteri endofit. Hasil pengujian ini dapat mendukung hasil karakterisasi molekuler dalam mengidentifikasi spesies bakteri setiap isolat.
Pewarnaan Gram merupakan pewarnaan diferensial yang paling sering digunakan dalam pengidentifikasian bakteri. Metode ini menggunakan beberapa larutan pewarna yaitu kristal violet, lugol iodin, alkohol dan safranin. Pada bakteri Gram negatif, pemberian larutan kristal violet akan mengubah warna dinding sel menjadi warna ungu. Penambahan lugol iodin akan menempelkan warna ungu hingga ke dalam sel dan membentuk kompleks ungu kristal yodium. Pembilasan dengan alkohol akan melunturkan warna ungu tadi karena bakteri Gram negatif mengandung lipid dalam persentase yang lebih tinggi daripada yang terkandung dalam bakteri Gram positif dan dinding sel bakteri Gram negatif juga lebih tipis daripada dinding sel bakteri Gram positif. Oleh karena itulah pembilasan dengan alkohol menyebabkan terekstraksinya lipid sehingga memperbesar daya rembes atau permeabilitas dinding sel. Jadi kompleks ungu kristal yodium yang telah memasuki dinding sel dapat diekstraksi dan menyebabkan kehilangan zat warna ungu. Penambahan larutan safranin adalah untuk memberikan warna merah pada sel bakteri. Sel bakteri Gram negatif akan menyerap zat pewarna ini. Perbedaan antara bakteri Gram positif dan Gram negatif disebabkan oleh perbedaan dinding sel. Dinding sel bakteri Gram positif sebagian besar terdiri atas beberapa lapisan peptidoglikan yang membentuk suatu struktur yang tebal dan kaku. Peptidoglikan pada dinding sel bakteri ini membuat bakteri Gram positif resisten terhadap lisis osmotik. Sehingga, bakteri Gram positif mempertahankan warna violet, sedangkan bakteri Gram negatif berwarna merah. Berdasarkan pewarnaan Gram, isolat BL3 dan RL4 termasuk Gram negatif berbentuk batang, sedangkan isolat DL4 Gram positif berbentuk batang (Gambar 4).
Uji karbohidrat dilakukan untuk mengetahui apakah bakteri dapat memfermentasi gula-gula seperti maltosa, laktosa, glukosa dan sukrosa. Uji positif bakteri memfermentasi karbohidrat yaitu dapat mengubah warna larutan merah menjadi kuning, Pada proses fermentasi, karbohidrat akan diubah oleh bakteri menjadi asam organik, seperti asam laktat, asam format, atau asam asetat. Suasana asam pada medium akan mengubah warna indikator fenol merah menjadi kuning tua. Pada beberapa bakteri, proses fermentasi ini juga menghasilkan asam dan gas (CO2). Gas yang dihasilkan akan terperangkap dalam tabung Durham, sehingga akan tampak gelembung dalam tabung tersebut (Sulistiyaningsih 2008). Isolat RL4, BL3 dan DL4 mampu memfermentasi karbohidrat.
karena mereka menghasilkan enzim katalase yang dapat mengubah hidrogen peroksida menjadi air dan oksigen. Uji oksidase menunjukkan hasil positif dengan memberikan perubahan warna pada kertas tetrametil dari putih menjadi ungu (Huda et al. 2012). Berdasarkan pengujian morfologi dan biokimia isolat RL4, BL3 dan DL4 mampu memfermentasi karbohidrat, dapat menghasilkan enzim oksidase dan positif pengujian katalase sehingga dapat dikatakan bahwa ketiga isolat bakteri endofit tersebut adalah bateri aerob.
Karakterisasi Molekuler 16S rRNA Isolat Bakteri Endofit Potensial Karakterisasi morfologi dan biokimia tidak cukup untuk mengidentifikasi spesies masing-masing isolat bakteri endofit sehingga diperlukan karakterisasi secara molekuler sehingga data morfologi dan biokimia ini dapat dijadikan data pendukung untuk menentukan spesies isolat bakteri endofit RL4, BL3 dan DL4.
Isolat Bakteri endofit dikarakterisasi menggunakan analisis 16S rRNA. 16S rRNA merupakan penyusun subunit 30S yang penting untuk translasi dan terdiri dari 1550 pasangan basa (Clarridge 2004). Gen 16S rRNA sebagai penanda molekuler yang banyak digunakan dalam studi filogenetik, evolusi dan taksonomi prokariota (Rajendhran & Gunasekaran 2011). Gen 16S rRNA telah terbukti sebagai penanda molekuler yang stabil dan spesifik untuk mengidentifikasi bakteri. Selain itu, jumlah salinan gen 16S rRNA dapat berfluktuasi dari 1 sampai 15 diantara genom bakteri yang berbeda (Singh et al. 2012). Pada prokariota terdapat tiga jenis RNA ribosomal yaitu 5S, 16S dan 23S rRNA. Diantara ketiganya, 16S rRNA yang paling sering digunakan. Molekul 5S rRNA memiliki urutan basa terlalu pendek, sehingga tidak ideal dari segi analisis statistika, sementara molekul 23S rRNA memiliki struktur sekunder dan tersier yang cukup panjang sehingga menyulitkan analisis (Clarridge 2004). Penelitian Aarti & Khusro (2015) berhasil mengidentifikasi Bacillus tequilensis yang menghasilkan enzim poligalakturonase menggunakan analisis 16S rRNA.
Berdasarkan hasil BLAST bakteri endofit isolat RL4 menunjukkan kemiripan 99% dengan Burkholderia cenocepacia J2315, sedangkan isolat BL3 yaitu Burkholderia gladioli BSR3 strain BSR3 dan isolat DL4 99% mirip dengan
Bacillus amyloliquefaciens DSM7.
Genus Burkholderia tersebar luas diberbagai ekologi, namun paling banyak ditemukan dalam tanah dan menunjukkan interaksi non-patogenic
terhadap tanaman. Burkholderia juga mampu melarutkan mineral dalam tanah dengan menghasilkan asam organik, serta meningkatkan ketersediaan nutrisi untuk tanaman sehingga sangat menjanjikan untuk dimanfaatkan dalam bidang bioteknologi (Rambola et al. 2014).
Bakteri Burkholderia cenocepacia J2315 adalah bagian dari bakteri
Burkholderia cepacia complex (Bcc) yang merupakan bakteri patogen Gram
negatif yang menyebabkan penyakit cystic fibrosis (CF) (Bazzini et al. 2011), namun berperan besar dalam bidang bioteknologi dan industri pertanian yaitu sebagai biokontrol, bioremediasi dan promotor tanaman. Schmerk et al. (2011) mengisolasi hopanoid dari Burkholderia cenocepacia yang merupakan senyawa triterpenoid yang berperan penting dalam fisiologi bakteri Burkholderia
cenocepacia. Wartono (2012) melaporkan Burkholderia cepacia isolat E76
konsentrasi formulasi 3%. Lipooligosakarida diisolasi dari Burkholderia
cenocepacia dan dikembangkan sebagai antimikroba dan terapi inflamasi (Silipo
et al. 2007).
Bakteri Burkholderia gladioli BSR3 strain BSR3 merupakan bakteri negatif yang ditemukan diberbagai habitat seperti di dalam tanah dan tanaman.
Jha et al. (2015) mengisolasi Burkholderia gladioli strain NGJ1 dari biji beras dan
menunjukkan spektrum luas sebagai antijamur pada Rhizoctonia solani,
Magnaporthe oryzae, Venturia inaqualis dan Fusarium oxysporum. Burkholderia
gladioli dapat menghasilkan antibiotik enacyloxin (Ross et al. 2014) dan enzim
esterase (Wagner et al. 2001). Burkholderiagladioli OR1 menghasilkan antibiotik phthalate yang efektif terhadap multi-resistant Staphylococcus aureus (Bharti & Tewari 2015). Penelitian Chen et al. (2015) mengungkapkan bahwa enzim dehidrogenase 3-Alkohol dari Burkholderia gladioli berpotensi besar sebagai dinamik transformasi kinetika asimetrik methyl
2-benzamido-methyl-3-oxobutanoate.
Bakteri Burkhorderia jenis lainnya seperti Burkholderia glumae memiliki aktivitas antifungi terhadap Rhizoctonia solani dan memproduksi taxoflavin (Karki et al. 2012). Burkholderia glumae dapat menghasilkan antimikroba
phenomycin dan antibakteri pyrazole (Han et al. 2014). Burkholderia multivorans
NKI379 adalah bakteri tanah yang menunjukkan efek antagonis terhadap pertumbuhan Burkholderia pseudomallei yang merupakan agen penyebab penyakit menular melioidosis (Hsueh et al. 2015). Chaiyaso et al. (2012) melaporkan bahwa enzim lipase dapat diisolasi dari bakteri Burkholderia
multivorans PSU-AH130 yang dapat diaplikasikan dalam produksi biodisel, selain
itu enzim lipase juga banyak dimanfaatkan dalam bidang industri kosmetik maupun farmasi. Burkholderia multivorans telah dikembangkan untuk agen insektisida dan suplemen pupuk yang berguna untuk meningkatkan pertumbuhan tanaman (Cordova-Kreylos et al. 2013). Burkholderia sp. 7016 dapat menghambat pertumbuhan fungi patogen seperti Sclerotinia sclerotiorum, Gibberella zeae dan
Verticillium dahliae, sebagai biofertiliser, menghasilkan
1-aminocyclopropane-1-carboxylic acid (ACC) deaminase dan indole acetic acid (IAA) (Miao et al.
2015). Burkholderia jenis contaminans strain MS14 juga mampu menghasilkan senyawa antifungi oligopeptida yang dapat menghambat patogen Geotrichum
candidum (Gu et al. 2009)
Bakteri endofit isolat DL4 memiliki kemiripan dengan bakteri Bacillus
amyloliquefaciens DSM7. Menurut Yoo et al. (1988) dan Abd-Elhalem et al.
(2015), Bacillus amyloliquefaciens DSM7 dapat menghasilkan enzim α-amilase. Bakteri genus Bacillus dapat menghasilkan senyawa peptida yang memiliki aktivitas antimikroba dengan struktur kimia yang berbeda-beda seperti bakteriozin dan lipopeptida (Stein 2005). Bakteri endofit dari Scutellaria baicalensis Georgi yang berdasarkan identifikasi filogenetik dan fisiologi adalah Bacillus
amyloliquefaciens ES-2, mampu menghasilkan senyawa metabolit sekunder
surfactins dan fengycins yang memiliki spektrum luas sebagai antibakteri dan
antifungi (Sun et al. 2006). Bakteri Bacillus amyloliquefaciens dapat juga mempromosikan pertumbuhan tanaman dengan meningkatkan komponen N, P, K dan klorofil daun tanaman, selain itu mampu dijadikan agen biokontrol Bacterial
fruit blotch (BFB) (Jiang et al. 2015). Bacillus amyloliquefaciens YB-1405
antibakteri terhadap Bacillus cereus, Escherichia coli, Staphylococcus aureus dan
Salmonella enteritidis (Saputri 2015). Selain itu, Bacillus amyloliquefaciens
CCMI 1051 juga memiliki aktivitas antifungi terhadap Rhizopus sp.,
Cladosporium resinae CCMI 667 dan Botrytis cinerea CCMI 899 (Caldeira et al.
2007). Menurut Chen et al. (2016) Bacillus amyloliquefaciens PG12 dapat diisolasi dari buah apel yang memiliki aktivitas antifungi yang berspektrum luas dan agen biokontrol. Biosurfaktan dapat diisolasi dari Bacillus amyloliquefaciens
AG1 yang memiliki aktivitas insektisida terhadap larva Tuta absoluta (Khedher et al. 2015), selain itu biosurfaktan juga bersifat antifungi terhadap Sclerotium rolfsii
dan Macrophomina phaseolina yang diisolasi dari bakteri B. amyloliquefaciens
RHNK22 (Kumar et al. 2015). Wang et al. (2014) membuat mikrokapsul yang berisi lipopeptida antimikroba yang berasal dari bakteri Bacillus
amyloliquefaciens ES-2. Chen et al. (2010) melaporkan bahwa B.
amyloliquefaciens SH-B10 yang diisolasi dari sedimen laut dalam mampu
menghasilkan dua lipopeptida yang bermanfaat sebagai antifungi yaitu C16
fengycin A dan aminobutyric acid. Senyawa kitin yang dihidrolisis oleh enzim
kasar dari Bacillus amyloliquefaciens V656 memiliki aktivitas antitumor (Liang et al. 2007). Hasil karakterisasi morfologi dan biokimia mendukung hasil karakterisasi molekuler. Bakteri Burkholderia cenocepacia J2315 dan
Burkholderia gladioli BSR3 strain BSR3 merupakan bakteri Gram negatif, mampu
memfermentasi karbohidrat dan bersifat aerob. Sedangkan Bacillus
amyloliquefaciens DSM7 adalah bakteri Gram positif, mampu memfermentasi
karbohidrat dan bersifat aerob.
Aktivitas Antibakteri Senyawa Aktif Isolat Bakteri Endofit Potensial Bakteri endofit isolat RL4, BL3 dan DL4 difermentasi dalam media
nutrient broth yang bertujuan untuk mengisolasi senyawa aktif yang memiliki
aktivitas antibakteri. Fermentasi masing-masing isolat selama 36 jam sesuai dengan kurva pertumbuhan (Lampiran 4). Menurut Seo et al. (2010) senyawa aktif yang dihasilkan bakteri endofit bersifat ekstraseluler sehingga diperlukan pemisahan antara sel bakteri dan supernatan. Pemisahan dapat dilakukan dengan sentrifugasi. Supernatan yang diperoleh dari hasil sentrifugasi ini selanjutnya ditambahkan beberapa pelarut seperti n-heksan, etil asetat dan kloroform yang bertujuan untuk mengekstraksi senyawa aktif yang dihasilkan masing-masing bakteri endofit potensial. Supernatan yang ditambahkan masing-masing pelarut berbeda diinkubasi shaker yang bertujuan mengoptimalkan ekstraksi senyawa aktif ke dalam pelarut. Supernatan dan pelarut selanjutnya dipisahkan menggunakan corong pisah dan diharapkan dalam pelarut telah terekstrak senyawa aktif yang sebelumnya terdapat dalam supernatan.
tidak memiliki aktivitas antibakteri baik terhadap bakteri Gram positif maupun Gram negatif (Tabel 4).
Ekstrak etil asetat diuapkan pelarutnya menggunakan evaporator, tujuannya untuk memekatkan ekstrak dan diperoleh 14,80 mg ekstrak kental etil asetat. Ekstrak kental tersebut selanjutnya dilarutkan kembali dengan berbagai konsentrasi menggunakan etil asetat tujuannya untuk melihat kemampuan konsetrasi daya hambat minimum ekstrak etil asetat isolat RL4 terhadap bakteri patogen. Berdasarkan pengujian tersebut menunjukkan konsetrasi terkecil 100 ppm mampu menghambat bakteri Staphylococcus aureus, Salmonella sp. dan
Escherichia coli (Tabel 5). Semakin tinggi konsetrasi maka semakin tinggi pula
aktivitas daya hambatnya terhadap bakteri patogen. Kloramfenikol 100 µg/mL digunakan sebagai kontrol positif. Kloramfenikol adalah jenis antibiotik yang menghambat sintesis protein pada ribosom 50S dan memiliki spektrum luas yang dapat menghambat bakteri Gram negatif dan Gram positif (Kohanski et al. 2010). Sedangkan, pelarut etil asetat digunakan sebagai kontrol negatif, hasil pengujian tidak menunjukkan aktivitas daya hambat terhadap bakteri patogen. Ini membuktikan bahwa zona hambat yang terbentuk adalah benar aktivitas senyawa aktif yang terdapat dalam ekstrak etil asetat bukan pelarutnya. Penelitian Leonita (2015) menunjukkan bahwa fraksi etil asetat isolat BH2 dari Ficus variegata B. memiliki daya hambat tinggi terhadap bakteri patogen Gram negatif maupun Gram positif.
Analisis GC-MS Senyawa Aktif Antibakteri Fraksi Etil Asetat Isolat RL4 Hasil analisis GC-MS ekstrak etil asetat isolat RL4 teridentifikasi 112 senyawa berdasarkan database (Willey9 N11.L). Dokosan, eikosan dan tetrakosan merupakan senyawa yang terdeteksi dalam ekstrak etil asetat isolat RL4 dengan tingkat kecocokan paling tinggi yaitu masing-masing 99% dan 98%. Senyawa dokosan (1.35%) pada waktu retensi 15.953 menit teridentifikasi dengan kecocokan mencapai 99% dan waktu retensi 17.439 menit, dokosan (0.61%) teridentifikasi dengan kecocokan 90% dengan ekstrak etil asetat isolat RL4. Dokosan, eikosan dan tetrakosan termasuk dalam senyawa diterpen. Berdasarkan analisis GC-MS, senyawa dokosan diidentifikasi dalam ekstrak petroleum eter
Trifolium angustifolium var. Angustifolium yang memiliki aktivitas antioksidan
(Ertas et al. 2015). Uma dan Parvathavarthini (2010) melaporkan bahwa senyawa dokosan merupakan salah satu komponen senyawa yang terdapat dalam ekstrak n -heksan Temnopleurus alexandri yang memiliki aktivitas antibakteri terhadap bakteri Gram positif (Staphylococcus aureus ATCC 25923, Bacillus subtilis
MTCC 441 dan Enterococcus faecalis ATCC 29212) dan bakteri Gram negatif
(Escherichia coli ATCC 25922, Pseudomonas aeruginosa ATCC 27853 dan
Proteus vulgaris MTCC 1771). Senyawa dokosan teridentifikasi pada daun
Lysimachia fortumei (11.02%) (Wei et al. 2014), Marrubium crassidens (7,2%)
(Hamedeyazdan et al. 2013) dan Agave attenuata (6.30%) yang memiliki aktivitas antimikroba serta berpotensi sebagai antioksidan (Rizwan et al. 2012).
senyawa eikosan dalam ekstrak etil asetat isolat RL4 yaitu 11.91%. Senyawa eikosan (6.22%) pada daun Perovskia abrotanoides memiliki aktivitas antimikroba terhadap B. cereus dan S. aureus (Ashraf et al. 2014). Omoruyi et al. (2014) melaporkan bahwa eikosan (1.43%) memiliki aktivitas antifungi terhadap
Candida albican, Candida krusei, Candida rugosa, Candida glabrata dan
Cryptococcus neoformans yang diisolasi dari daun Mesembryanthemum edule
(L.). Senyawa eikosan pada ekstrak Ceratonia siliqua menunjukkan aktivitas antifungi, antibakteri dan efek sitotoksik terhadap sel kanker Hela dan MCF-7 (Hsouna et al. 2011). Naemi et al (2014) melaporkan bahwa minyak essensial yang terdapat dalam ekstrak daun, batang dan bunga Rheum ribes L. menunjukkan aktivitas anti trikomonas dan salah satu komposisi minyak essensial
Rheum ribes L yaitu eikosan (9.9%).
Senyawa tetrakosan terdeteksi pada waktu retensi 17.704 menit dengan kecocokan 98% dengan senyawa aktif dalam ekstrak etil asetat (1.31%). Tetrakosan terdapat dalam Acrostichum aureum L. yang merupakan tanaman tradisional yang banyak digunakan sebagai obat kanker perut. Tetrakosan yang diperoleh dari Acrostichum aureum L. ini diujikan terhadap sel AGS MDA-MB-231, HT-29 dan NIH 3T3 menunjukkan aktivitas sitotoksik dengan nilai IC50 dari 128.7 hingga >250 μM (Uddin et al. 2012). Penelitian Saputri (2015), menemukan tetrakosan sebagai senyawa dominan yang terdapat dalam ekstrak klorofom isolat BT22 yang berpotensi sebagai antibakteri. Selain itu, dokosan dan asam heksanedioat teridentifikasi juga dalam ekstrak klorofom isolat BT22.
Senyawa lainnya yang terdeteksi dalam ekstrak etil asetat yang memiliki kecocokan tinggi dengan senyawa aktif yaitu heneikosan (2.24%), heksadekanamida (4.84%), pentakosan (1.91%), oktadekan (2.17%), asam heksanedioat (20.37%) dan pentadekan (0.52%). Senyawa heneikosan, pentakosan, oktadekan dan pentadekan merupakan senyawa golongan alkana (Jin
et al. 2016).
Pada waktu retensi 15.165 dan 20.021 terdeteksi senyawa heneikosan dengan tingkat kecocokan senyawa aktif dalam ekstrak etil asetat sebesar 95% dan 97%, dengan total konsentrasi area 2.24%. Heneikosan merupakan senyawa volatil yang ditemukan pada Anchomenus dorsalis (Bonacci et al. 2011). Evstatieva et al. (2010) mengidentifikasi heneikosan dan pentakosan dalam
Rhodiola rosea L. yang secara farmakologi menunjukkan aktivitas sebagai
antioksidan, antidepresi dan antikanker. Senyawa pentakosan (9.81%) diidentifikasi dalam daun L. fortumei sedangkan heneikosan (5.38%) terdapat dalam L. chikungensis (Wei et al. 2014). Selain itu, heneikosan dan pentakosan terdapat juga dalam tanaman Rosa damascena (Mahboubi 2015). Menurut penelitian Metboki (2015), heksadekanamida terdapat dalam kulit batang ampupu
(Eucalyptus alba R.) yang memiliki efek antifungi terhadap Fusarium
moniliforme penyebab penyakit busuk tongkol jagung.
Asam heksanedioat (95%) yang terdeteksi pada waktu retensi 17.824, dengan konsentrasi area terbesar 20.37% dalam ekstrak etil asetat isolat RL4 merupakan senyawa organik yang sejenis dengan asam dikarboksilat dan lebih dikenal sebagai asam adipat (Fun & Chantrapromma 2009). Menurut penelitian
Chu et al. (2014), asam heksanedoiat yang diperoleh dari larva Hermetia illucens
dapat menghambat pertumbuhan dan proliferasi Staphylococcus aureus, MRSA
dan Shigella dysenteriae (Choi & Jiang. 2014). Asam heksanedioat juga
ditemukan pada alga merah F. hillebrandii yang memiliki aktivitas antibakteri terhadap Salmonella typhi, Enterococcus faecalis dan Shigella sp. (Manilal et al. 2009).
5 KESIMPULAN DAN SARAN
Kesimpulan
Bakteri endofit diisolasi dari tanaman lengkuas merah (Alpinia purpuruta) sebanyak 16 isolat. Isolat DL4, BL3 dan RL4 adalah bakteri endofit potensial yang mampu menghambat bakteri patogen Gram positif dan Gram negatif. Berdasarkan karakterisasi morfologi dan biokimia serta molekuler menunjukkan isolat DL4 memiliki kemiripan dengan bakteri Bacillus amyloliquefaciens DSM7, isolat BL3 memiliki kemiripan dengan bakteri Burkholderia gladioli BSR3 strain BSR3 dan isolat RL4 memiliki kemiripan dengan bakteri Burkholderia
cenocepacia J2315. Isolat potensial yang mampu menghasilkan senyawa aktif
yaitu isolat RL4. Berdasarkan pengujian GC-MS diperoleh beberapa jenis senyawa aktif yang memiliki kecocokan tertinggi dengan senyawa aktif yang terdapat dalam ekstrak etil asetat isolat RL4 yaitu dokosan, eikosan, tetrakosan, heneikosan, heksadekanamida, pentakosan, oktadekan, asam heksanedioat dan pentadekan.
Saran
DAFTAR PUSTAKA
Aarti C, Khusro A. 2015. Discovery of polygalacturonase producing Bacillus
tequilensis strain ARMATI using 16s rRNA gene sequencing. Asian J
Pharm Clin Res. 8(5): 58-62
Abd-Elhalem BT, El-Sawy M, Gamal RF, Abou-Taleb KA. 2015. Production of amylases from Bacillus amyloliquefaciens under submerged fermentation using some agroindustrial by products. Annals of Agricultural Sci. 60 (2): 193-202
Andersson DI, Hughes D. 2010. Antibiotic resistance and its cost: is it possible to reverse resistance?. Nature Reviews Microbiology. 8: 260-271
Ashraf SN, Zubair M, Rizwan K, Tareen RB, Rasool N, Zia-Ul-Haq M, Ercisli S. 2014. Compositional studies and biological activities of Perovskia
abrotanoides Kar. Oils. Bio. Resch. 47: 12
Bazzini S, Udine C, Sass A, Pasca MR, Longo F, Emiliani G, Fondi M, Perrin E, Decorosi F, Viti C, et al. 2011. Deciphering the role of RNd effulx transporters in Burkholderia cenocepacia. PLoS ONE 6(4)e18902
Bermawie N, Purwiyanti S, Melati, Meilawati NLW. 2012. Karakter morfologi, hasil, dan mutu enam genotip lengkuas pada tiga agroekologi. BPTRO.
Bul. Littro. 23(2): 125-135
Bharti P, Tewari R. 2015. Purification and structural characterization of a phthalate antibiotic from Burkholderiaa gladioli OR1 effective against multi-drug resistant Staphylococcus aureus. J Microbiol Biotech Food Sci.5(3): 207-211
Bonacci T, Brandmayr. Zetto T, Perrotta ID, Salvatore G, Peri E, Colazza S. 2011. Volatile compounds released by disturbed and undisturbed adults
of Anchomenus dorsalis (Coleoptera, Carabidae, Platynini) and structure
of the pygidial gland. ZooKeys. 81: 13-25
Caldeira AT, Feio SS, Arteiro JMS, Roseira JC. 2007. Bacillus amyloliquefaciens
CCMI 1051 in vitro activity against wood contaminant fungi. Annals of
Microbiology. 57(1): 29-33
Castillo UF, Strobel GA, Ford EJ, Hess WM, Poter H, Jenson JB, Albert H, Robinson R, Condron MA, Teplow DB, Stevens D, Yaver D. 2002. Munumbicins, wide spectrum antibiotics produced by Streptomyces NRRL 30562, endophytic on Kennedia nigriscans. Microbiology. 148: 2675-2685 Castillo UJ, Harper K, Strobel GA, Sears J, Alesi K, Ford E, Lin J, Hunter M, Maranta M, Ge H, Yaver D, Jensen JB, Porter H, Robinsons R, Miller D, Hess WM, Condron M, Teplow D. 2003. Kakadumycins, novel antibiotics from Streptomyces sp. NRRL 30566, an endophyte of Grevillea pteridifolia. FEMS Microbiology Letter 224: 183-190
Chaiyaso T, Seesuriyachan P, Zimmermann W, Kittikum AH. 2012. Purification and characterization of lipase from newly isolated Burkholderia
multivorans PSU-AH130 and its application for biodiesel production.
Ann Microbiol. 62: 1615-1624
Chen L, Wang N, Wang X, Hu J, Wang S. 2010. Characterization of two anti fungal lipopeptides produced by Bacillus amyloliquefaciens SH-B10.
Chen X, Liu ZQ, Huang JF, Lin CP, Zheng YG. 2015. Asymmetric synthesis of optically active methyl-2-benzamido-methyl-3-hydroxy-butyrate by robust. short-chain alcohol dehydrogenases from Burkholderia gladioli.
Chem. Commun.51: 12328-12331
Chen X, Zhang Y, Fu X, Li Y, Wang Q. 2016. Isolation and characterization of
Bacillus amyloliquefaciens PG12 for the biological control of apple ring
rot. Postharvest Biology aand Technology. 115: 113-121
Choi WH, Jiang MH. 2014. Evaluation of antibacterial activity of hexanedioic acid isolated from Hermetia illucens larvae. J. Appl. Biomed
Chu KB, Jeon GC, Quan FS. 2014. Hexanedioic acid from Hermetia illucens
larvae (Diptera: Stratiomydae) protects mice against Klebsiella
pneumoniae infection. Entomological Research. 44: 1-8
Chudiwal AK, Jain DP,Somani RS. 2010. Alpinia galangal willd.-an overview of phyto-pharmacological propertis. IJNPR 1(2): 143-149
Clarridge JE. 2004. Impact of 16s rRNA gene sequence analysis for identification of bacteria on clinical microbiology and infectious diseases. Clinical
Microbiology Reviews. 17(4): 840-862
Cordova-Kreylos A, Fernandez LE, Koivunen M, Yang A, Flow-Weiler L, Marrone P. 2013. Isolation and characterization of Burkholderia
rinojensis sp. nov., a non-Burkholderia cepacia complex soil bacterium
with insecticidal and miticidal activities. American Society for
Microbiology. 79(24): 7669-7678
Cowan SJ. 1974. Mannual for the identification of medical bacteria. Cambridge (GB): Cambridge University Press
Duangpaeng A, Phetcharat P, Chanthapho, Boonkantong N, Okuda N. 2012. The study development of endophytic bacteria for enhancing organic rice growth. Procedia Engineering. 32: 172-176
Ertas A, Boga M, Hasimi N, Yilmaz MA. 2015. Fatty acid and essential oil compositions of Trifolium angustifolium var. angustifolium with antioxidant, anticholinesterase and antimicrobial activities. IJPR. 14(1): 233-241
Estrela C, Estrela CRA, Barbin EL, Spano JCE, Marchesan MA, Pecora JD. 2002. Mechanism of action of sodium hypochlorite. Braz. Dent. J. 13(2): 113-117.
Evstatieva L, Todorova M, Antonova D, Staneva J. 2010. Chemical composition of the essential oils of Rhodiola rosea L. of three different origins.
Gu G, Smith L, Wang H, Lu SE. 2009. Biosynthesis of an antifungal oligopeptide
in Burkholderia contaminans strain MS14. Biochem. Biophys. Research
Communications. 380: 328-332
Hamedeyazdan S, Asnaashari S, Fathiazad F. 2013. Characterization of non terpenoids in Marrubium crassidens Boiss. essential oil. Advan. Pharm. Bull. 3(2): 429-432
Han JW, Kim JD, Lee JM, Ham JH, Lee D, Kim BS. 2014. Structural elucidation and antimicrobial activity of new phencomycin derivatives isolated from
Burkholderia glumae strain 411gr-6. The Journal of Antibiotics. 1-3
Handajani NS, Purwoko T. 2008. Aktivitas ekstrak rimpang lengkuas (Alpinia
galanga) terhadap pertumbuhan jamur Aspergillus spp. penghasil
aflatoksin dan Fusarium moniliforme. Biodiversitasi. 9(3): 161-164 Hsouna AB, Trigui, Mansour RB, Jarraya RM. 2011. Chemical composition,
cytotoxicity effect and antimicrobial activity of Ceratonia siliqua
essential oil with preservative effects against Listeria inoculated in minced beef meat. Inter. J Food Microbiology. 148: 66-72
Hsueh PT, Liu JK, Chen YL, Ni WF, Chen YS, Wu KM, Lin HH. 2015. Genomic sequence of Burkholderia multivorans NKI379, soil bacterium that inhibits the growth of Burkholderia pseudomallei. G. Announcements. 3(6) e01294-15
Huda C, Salni, Melki. 2011. Penapisan aktivitas antibakteri dari bakteri yang berasosiasi dengan karang lunak Sarcophyton sp. Maspari Journal 4(1): 69-75
Itokawa H, Takeya K. 1993. Antitumor subtances from higher plants.
Heterocycles. 35: 1467-1501
Jha G, Tyagi I, Kumar R, Ghosh S. 2015. Draft genome sequence of broad-spectrum antifungal bacterium Burkholderia gladioli Strain NGJ1, Isolated from Healthy Rice Seeds. Genome Announc.3(4): 15
Jiang CH, Wu F, Yu ZY, Xie P, Ke HJ, Wei H, Yu YY, Guo JH. 2015. Study on screening and antagonistic mechanisms of Bacillus amyloliquefaciens 54 against bacterial fruit blotch (BFB) caused by Acidovorax avenae subsp. Citrulli. Microbiological Research. 170: 95-104
Jin Q, Jiao C, Sun S, Song C, Cai Y, Lin Y, Fan H, Zhu Y. 2016. Metabolic analysis of medicinal Dendrobium officinale and Dendrobium
huoshanense during different growth years. PLoS ONE. 11(1): 1-17
Juntachote T, Berghofer E. 2005. Antioxidative properties and stability of ethanolic extracts of holy basil and galangal. Food Chemistry. 92: 193-202
Karki HS, Shrestha BK, Han JW, Groth DE, Barphagha IK, Rush MC, Melanson RA, Kim BS, Ham JH. 2012. Diversities in virulence, antifungal activity, pigmentation and DNA fingerprint among strains of Burkholderia glumae.
PLoS ONE. 7(9) e45376
Kathiresan K, Saravanakumar K, Sahu SK, Sivasankaran M. 2014. Adenosine deaminase production by an endophytic bacterium (Lysinibacillus sp.) from avicennia marina. 3 Biotech. 4: 235-239
Khattack S, Saeed-Ur-Rehman HUS, Ahmad W, Ahmad M. 2005. Biological effects of indigenous medicinal plants Curcuma longa and Alpinia
galanga. Fitoterapia. 76: 254-257
Khedher SB, Boukedi H, Feki OK, Chaib I, Laarif A, Mesrati LA, Tounsi S. 2015. Bacillus amyloliquefaciens AG1 biosurfactant: putative receptor diversity and histopathological effects on Tuta absoluta midgut. J.
Invertebrate Pathology. 132: 42-47
Kohanski MA, Dwyer DJ, Collins JJ. 2010. How antibiotics kill bacteria: from targets to networks. Nature Reviews Microbiology. 8: 423-435