PENENTUAN FRAKSI AKTIF EKSTRAK DAUN JAMBU BIJI
(
Psidium guajava
) SEBAGAI ANTIOKSIDAN
TRI HIDAYATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi Penentuan Fraksi Aktif Ekstrak Daun Jambu Biji (Psidium guajava) sebagai antioksidanadalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, April 2015
Tri Hidayati
ABSTRAK
TRI HIDAYATI. Penentuan Fraksi Aktif Ekstrak Daun Jambu Biji (Psidium guajava) sebagai Antioksidan. Dibimbing oleh IRMA HERAWATI SUPARTO dan WULAN TRI WAHYUNI.
Ekstrak daun jambu biji mempunyai kandungan metabolit sekunder yang berperan aktif sebagai antioksidan untuk menangkal radikal bebas dalam tubuh. Penelitian ini bertujuan menetapkan fraksi aktif ekstrak daun jambu biji yang berperan mengurangi radikal bebas dari 1,1-difenil-2-pikrilhidrazil (DPPH). Aktivitas antioksidan ditentukan berdasarkan nilai IC50 yang diperoleh dari nilai
penangkapan radikal bebas DPPH. Sampel diekstraksi menggunakan pelarut etil asetat, metanol dan etanol 70% (v/v) untuk memperoleh ekstrak kasar. Hasil penelitian menunjukkan simplisia daun jambu biji mengandung flavonoid, tanin, alkaloid, saponin, dan steroid. Standar kontrol positif antioksidan yang digunakan adalah asam askorbat dan kuersetin. Ekstrak kasar yang mempunyai aktivitas antioksidan paling kuat adalah ekstrak etanol 70% (v/v). Fraksionasi ekstrak etanol 70% (v/v) dengan kolom kromatografi menghasilkan 7 fraksi. Fraksi dengan aktivitas antioksidan teraktif adalah fraksi ke 3. Nilai IC50 ekstrak dan fraksi teraktif
etanol 70% (v/v) masih lebih rendah dari pada standar yang digunakan, tapi termasuk mempunyai aktivitas sangat kuat karena nilainya kurang dari 50 mg/L.
Kata kunci: antioksidan, DPPH, fraksionasi, IC50, daun jambu biji
ABSTRACT
TRI HIDAYATI. Determination of Active Fraction of Psidium guajava Leaves Extract as Antioxidants. Supervised by IRMA HERAWATI SUPARTO and WULAN TRI WAHYUNI.
Guava leaves extract contains secondary metabolites with their active role as antioxidants and free radicals scavengers in the body. This study was to determine active fraction of guava leaves extract as antioxidant. The antioxidant activity was determined based on the IC50 values obtained from 1,1-diphenyl-2-picrylhydrazyl
(DPPH) free radical scavenging assay. Samples were extracted using ethyl acetate, methanol, and 70% ethanol. The results showed that guava leaves simplicia con-tained flavonoids, tannins, alkaloids, saponins, and steroids. Ascorbic acid and quercetin were used as positive control in the antioxidant assay. Extract of 70% ethanol showed the highest antioxidant activity. Fractionation by column chroma-tography resulted seven fractions, the fraction with highest antioxidant activity was the 3th fraction. The IC50 value of most active fractions of 70% ethanol was lower
than the standards, yet it is categorized as very strong activity for the value of being below 50 mg/L.
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan penulisan tersebut tidak merugikan kepentingan IPB
PENENTUAN FRAKSI AKTIF EKSTRAK DAUN JAMBU BIJI
(
Psidium guajava
) SEBAGAI ANTIOKSIDAN
TRI HIDAYATI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
iii
PRAKATA
Puji syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan penelitian dan penulisan karya ilmiah dengan judul Penentuan Fraksi Aktif Ekstrak Daun Jambu Biji (Psidium guajava) sebagai Antioksidan. Skripsi ini disusun berdasarkan penelitian yang dilaksanakan di Laboratorium Anorganik dan Laboratorium Analitik, Departemen Kimia IPB, serta Laboratorium Pusat Studi Biofarmaka (PSB) IPB, yang dilaksanakan mulai bulan April 2014 sampai bulan Januari 2015.
Penulis mengucapkan banyak terima kasih kepada pihak-pihak yang telah mendukung dan membantu dalam pelaksanaan penelitian dan penyusunan karya ilmiah ini, sehingga dapat terselesaikan dengan baik. Terima kasih kepada Ibu Dr dr Irma Herawati Suparto, MS selaku pembimbing I dan Ibu Wulan Tri Wahyuni, SSi, MSi selaku pembimbing II yang senantiasa memberikan arahan, masukan, dorongan semangat dan do’a kepada penulis selama pelaksanaan penelitian. Terima kasih kepada staf Laboratorium Anorganik dan staf Laboratorium Analitik, Departemen Kimia IPB, serta staf Laboratorium Pusat Studi Biofarmaka, IPB yang telah memberikan banyak bimbingan dan bantuan kepada penulis selama pelaksanaan penelitian.
Terima kasih juga penulis ucapkan kepada teman-teman satu bimbingan Fahmi Luthfie, Ignasius Setiadi, Fatia Izzaty, dan Nadia Ulfa atas bantuan dan dukungannya sehingga penelitian ini dapat terselesaikan dengan baik. Penulis juga mengucapkan terima kasih kepada Ayah, Ibu, Kakak, Adik dan seluruh teman-teman kimia angkatan 47 lainnya yang senantiasa memberikan dukungan, kasih sayang dan do’a kepada penulis. Penulis berharap laporan ini dapat bermanfaat bagi perkembangan ilmu pengetahuan dan kemajuan bangsa.
Bogor, April 2015
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
METODE 2
Waktu dan Tempat Penelitian 2
Alat dan Bahan 2
Metode Penelitian 2
HASIL DAN PEMBAHASAN 5
Karakteristik Simplisia Daun Jambu Biji 5
Ekstraksi Daun Jambu Biji 6
Uji Aktivitas Ekstrak Daun Jambu Biji 7 Fraksionasi Ekstrak Teraktif 9
SIMPULAN DAN SARAN 11
Simpulan 11
Saran 12
DAFTAR PUSTAKA 12
v
DAFTAR TABEL
1 Hasil uji fitokimia simplisia daun jambu biji 6 2 Data rendemen dan IC50 ekstrak daun jambu biji 8
3 Nilai rendemen dan aktivitas antioksidan fraksi ekstrak etanol 70% (v/v) 11
DAFTAR GAMBAR
1 Daun jambu biji 1
2 Ekstrak kasar metanol, etil asetat, dan etanol 70% (v/v) 7 3 Hubungan antara konsentrasi dengan nilai %inhibisi 7 4 Mekanisme pengkapan radikal bebas DPPH 8 5 Profil noda eluen tunggal untuk pencarian eluen terbaik 9 6 Profil spot pencarian eluen terbaik 10 7 Hubungan konsentrasi dengan nilai % inhibisi hasil fraksionasi etanol 70%
(v/v) 10
DAFTAR LAMPIRAN
1 Diagram alir penelitian 14 2 Data penentuan nilai IC50 ekstrak kasar daun jambu biji 15
3 Data nilai IC50 asam askorbat dan standar kuersetin 18
1
PENDAHULUAN
Jambu biji merupakan tanaman obat tradisional yang potensial dan tersedia melimpah di alam. Tanaman tropis ini banyak dibudidayakan dan dapat beradaptasi dengan berbagai kondisi lingkungan. Daun jambu biji (Gambar 1) sebagai biofarmaka mempunyai khasiat farmakologis antara lain antioksidan, antidiare, antiradang, antibakteri, antikanker, antihipertensi, antivirus dan penambah trombosit (Daud et al. 2011). Menurut Porwal et al. (2012), daun jambu biji mengandung flavonoid dan tanin yang memiliki aktivitas aktif sebagai anti-radang, antioksidan dan antimikrob. Menurut Joseph et al. (2011), Daud et al. (2011), dan Mesah (2013) khasiat daun jambu biji yang sangat potensial salah satunya adalah sebagai antioksidan.
Gambar 1 Daun jambu biji (Joseph et al. 2010)
Antioksidan diperlukan tubuh untuk menangkap radikal bebas. Reaksi antara radikal bebas dan molekul di sekitarnya dapat berlangsung terus menerus dalam tubuh dan bila tidak dihentikan, maka akan berpotensi menimbulkan berbagai penyakit seperti kanker, jantung, katarak, penuaan dini, dan penyakit degeneratif lainnya (Harnly et al. 2006).
Hasil uji aktivitas antioksidan pada daun jambu biji menggunakan 1,1-difenil-2-pikrilhidrazil (DPPH) menunjukkan hasil yang positif. Penelitian Daud et al.
(2011) menunjukkan nilai aktivitas penangkapan radikal bebas (IC50) fraksi
heksana, etil asetat, dan air ekstrak etanol 70% (v/v) daun jambu biji, berturut-turut 35, 29, dan 42 mg/L. Menurut Zuhra (2008), suatu senyawa dikatakan bersifat antioksidan sangat kuat apabila mempunyai nilai IC50 kurang dari 50 mg/L, kuat
apabila IC50 50−100 mg/L, sedang antara 100 dan 150 mg/L, serta lemah apabila
IC50 antara 150 dan 200 mg/L. Hasil penelitian Daud et al. (2011) menunjukkan
bahwa daun jambu biji mempunyai potensi yang sangat kuat sebagai antioksidan terutama pada fraksi etil asetatnya yang mempunyai nilai IC50 29 mg/L.
metanol dan etanol adalah pelarut yang cocok untuk mengekstraksi senyawa antioksidan dari daun jambu biji.
Khasiat daun jambu biji sebagai antioksidan dapat distandardisasi dengan mengidentifikasi kandungan senyawa aktif antioksidan. Fraksi teraktif terlebih dahulu perlu diketahui, dan ditentukan kandungan metabolit sekundernya baik secara kualitatif maupun kuantitatif. Menurut Kusumawati (2004), senyawa aktif yang menjadi penciri (marker) pada ekstrak daun jambu biji adalah kuersetin yang merupakan salah satu golongan flavonoid. Kuersetin diduga kuat sebagai antioksidan menurut Powal et al. (2012), sehingga pada penelitian ini digunakan standar kuersetin sebagai pembanding aktivitas antioksidan. Penelitian ini bertujuan menentukan aktivitas antioksidan daun jambu biji dengan mengetahui fraksi terbaik yang berpotensi sebagai antioksidan.
METODE
Waktu dan Tempat Penelitian
Penelitian dilakukan dari bulan April 2014 hingga bulan Januari 2015. Penelitian bertempat di Laboratorium Anorganik dan Laboratorium Analitik, Departemen Kimia IPB, serta Laboratorium Pusat Studi Biofarmaka (PSB), IPB.
Alat dan Bahan
Bahan-bahan yang digunakan terdiri atas simplisia daun jambu biji dari PSB, metanol p.a, etanol p.a, etil asetat p.a, n-heksana p.a, DPPH, asam askorbat (vitamin C), serbuk Mg, amil alkohol, NH4OH, H2SO4, pereaksi Mayer, pereaksi
Dragendorf, kloroform p.a, pereaksi Lieberman Burchard, FeCl3 1%, akuades,
serbuk silika gel 60 (0.040-0.063 mm), wol kaca. Alat yang digunakan pada penelitian ini terdiri atas tanur, cawan porselen, pembakar bunsen, alat-alat kaca, neraca analitik, oven, penguap putar, kromatografi lapis tipis (KLT) G60 F254, kolom
kromatografi, lempeng 96-sumur (96-well plate), dan perangkat enzyme-linked immunosorbent assay (ELISA).
Metode Penelitian
3
antioksidannya dengan metode DPPH untuk mendapatkan fraksi yang mempunyai aktivitas terbaik.
Preparasi Sampel
Daun jambu biji sebagai bahan baku sampel harus bebas dari penyakit, biasanya diambil yang tidak terlalu tua dan tidak terlalu muda, yaitu sekitar 4−5 lembar dari pucuk daun. Daun segar dikeringkan dalam oven selama 2 jam kemudian digiling agar menjadi simplisia dengan ukuran ≥ 40 mesh. Kadar air dan kadar abu ditentukan dengan menggunakan metode AOAC (2007).
Penentuan Kadar Air (AOAC 2007)
Cawan porselen dikeringkan di dalam oven pada suhu 105−110 oC selama 30 menit dan ditimbang hingga diperoleh bobot konstan. Sebanyak 2 g sampel ditimbang, lalu diletakkan ke dalam cawan tersebut. Cawan berisi sampel dipanaskan dalam oven pada suhu 105−110 oC selama 3−4 jam, kemudian
didinginkan di dalam desikator selama 30 menit. Setelah itu, cawan berisi sampel ditimbang bobotnya. Tahap ini diulang hingga diperoleh bobot konstan. Kadar air dapat dihitung menggunakan rumus sebagai berikut:
Kadar air (%) = Bobot air × 100% Bobot sampel awal
Penentuan Kadar Abu (AOAC 2007)
Cawan porselen dikeringkan dalam oven selama 30 menit pada suhu 100−105 ºC, kemudian dimasukkan ke dalam tanur pada suhu 600 oC selama 30 menit dan didinginkan di dalam desikator, cawan ditimbang hingga bobotnya konstan. Sebanyak 2 g sampel ditimbang di dalam cawan tersebut, lalu cawan berisi sampel dibakar menggunakan pembakar bunsen hingga tidak berasap selama kurang lebih 20 menit, dilanjutkan dengan pengabuan di dalam tanur pada suhu 600 ºC sampai terabukan sempurna. Abu sampel didinginkan di dalam desikator dan ditimbang sampai bobot konstan. Kadar abu dihitung menggunakan rumus sebagai berikut:
Kadar abu (%) = Bobot abu × 100% Bobot sampel kering
Ekstraksi Simplisia
Uji Fitokimia (Harborne 1987)
Uji fitokimia dilakukan untuk mengetahui kandungan golongan senyawa di dalam sampel daun jambu biji yang akan diuji aktivitasnya.
Uji Flavonoid
Sebanyak 0.5 g simplisia ditambahkan dengan 10 mL air panas kemudian dididihkan selama 5 menit dan disaring. Filtrat dimasukkan ke dalam tabung reaksi kemudian 0.5 g serbuk Mg, 1 mL HCl pekat, dan 1 mL amil alkohol ditambahkan. Campuran dikocok kuat-kuat. Uji positif ditandai dengan munculnya warna merah, kuning, jingga pada lapisan amil alkohol.
Uji Alkaloid
Sebanyak 0.5 g simplisia diekstraksi dengan 10 mL kloroform dan beberapa tetes NH4OH pekat. Ekstrak disaring ke dalam tabung reaksi tertutup, lalu dikocok
sambil menambakan 10 tetes H2SO4 2 M. Lapisan asam dipindahkan ke dalam
tabung reaksi lain, kemudian diteteskan pada lempeng tetes untuk ditambahkan pereaksi Mayer, Wagner, dan Dragendrorf. Uji positif ditandai dengan berturut-turut munculnya endapan berwarna putih, cokelat, dan merah jingga.
Uji Terpenoid dan Steroid
Sebanyak 0.5 g simplisia dilarutkan dengan 25 mL etanol panas (50 ºC) selama 1 jam, lalu filtrat disaring. Residunya ditambahkan eter, kemudian filtrat yang diperoleh ditambahkan dengan 3 tetes anhidrida asam asetat dan 1 tetes asam sulfat pekat secara berurutan (pereaksi Lieberman-Burchard). Larutan dikocok perlahan dan dibiarkan beberapa menit. Uji positif ditandai dengan terbentuknya warna merah atau ungu untuk triterpenoid serta biru atau hijau untuk steroid.
Uji Tanin
Sebanyak 0.5 g simplisia dilarutkan dengan 10 mL air panas, dididihkan selama 5 menit, lalu disaring. Ke dalam filtrat lalu ditambahkan 10 mL FeCl3 1%/
Uji positif ditandai dengan munculnya warna hitam atau biru tua.
Uji Saponin
Sebanyak 0.1 g simplisia ditambahkan 10 mL air panas, kemudian disaring. Filtrat dikocok selama 10 menit dengan keadaan tertutup. Terbentuknya buih yang stabil menunjukkan ekstrak mengandung saponin.
Uji Antioksidan dengan DPPH
5
ºC selama 30 menit pada ruangan yang gelap. Setelah itu, absorbans diukur pada panjang gelombang 517 nm. Perlakuan yang sama dilakukan juga untuk kontrol positif. Absorban masing-masing diukur 3 kali ulangan. Ekstrak yang mempunyai aktivitas antioksidan paling tinggi difraksionasi menggunakan kromatografi kolom. Aktivitas penangkapan radikal bebas ditentukan dengan rumus
Aktivitas penangkapan radikal bebas = ADPPH - Asampel × 100 %
ADPPH
Keterangan: A = Absorbans
Fraksionasi Menggunakan Kromatografi Kolom
Eluen terbaik untuk fraksionasi ditentukan terlebih dahulu (Houghton dan Raman 1998). Ekstrak teraktif daun jambu biji ditotolkan pada pelat KLT sebanyak 20 kali. Pelat KLT yang digunakan adalah plat jenis silika gel G60F254 berukuran
panjang 10 cm dan lebar 1 cm. Setelah kering, totolan dielusi dengan eluen tunggal kloroform, metanol, etanol, dan etil asetat. Noda hasil elusi diamati dengan bantuan sinar UV 254 dan 366 nm. Eluen yang menghasilkan noda terbanyak dan terpisah secara baik, dipilih sebagai eluen terbaik. Jika terdapat 2 eluen yang dapat memisahkan noda dengan baik, maka kedua eluen tersebut dicampurkan dengan nisbah tertentu untuk mendapatkan campuran eluen terbaik.
Sebanyak 2.5 g ekstrak simplisia difraksionasi menggunakan kromatografi kolom dengan eluen terbaik menggunakan sistem gradien berundak. Eluat yang dihasilkan ditampung dalam tabung-tabung vial yang telah diberi nomor dengan volume masing-masing 5 mL. Eluat yang diperoleh kemudian diuji spotnya menggunakan KLT dengan eluen terbaik setiap 5 tabung reaksi. Noda pemisahan dilihat dengan bantuan sinar UV 254 dan 366 nm. Eluat yang memiliki noda pemisahan dengan nilai Rf dan pola yang sama digabungkan menjadi 1 fraksi.
Fraksi-fraksi ini kemudian diuji lagi aktivitas antioksidannya.
HASIL DAN PEMBAHASAN
Karakteristik Simplisia Daun Jambu Biji
Uji fitokimia dilakukan untuk mengetahui secara kualitatif kandungan metabolit sekunder dalam daun jambu biji. Hasil uji menunjukkan bahwa simplisia mengandung metabolit sekunder berupa flavonoid, alkaloid, tanin, saponin, dan steroid, tetapi tidak mengandung triterpenoid. Hasil ini tidak jauh berbeda dengan hasil uji sebelumnya oleh Indriani (2006) dan Lutfhie (2014), sebagaimana ditunjukkan pada Tabel 1. Tumbuhan yang sama dapat mempunyai kandungan metabolit sekunder yang berbeda. Hal ini dapat dipengaruhi karena beberapa faktor, antara lain faktor lingkungan, umur tanaman saat dipanen, waktu panen, serta kegiatan pasca panen (Dewoto 2007).
Tabel 1 Kandungan fitokimia simplisia daun jambu biji Metabolit
sekunder
Hasil
penelitian ini Indriani (2006) Lutfhie (2014)
Flavonoid + + +
Simplisia daun jambu biji diekstraksi dengan 3 pelarut yang berbeda, yaitu metanol, etil asetat, dan etanol 70% (v/v) dengan metode maserasi. Metode maserasi untuk menghindari adanya kerusakan pada komponen senyawa yang tidak tahan terhadap panas. Ekstraksi dilakukan dengan mencampurkan 1 L pelarut dengan 100 g simplisia daun jambu biji, kemudian dimaserasi selama 3×24 jam. Pemilihan 3 pelarut dengan kepolaran berbeda bertujuan memisahkan senyawa metabolit sekunder berdasarkan kepolarannya dan memilih pelarut yang paling baik dalam mengekstraksi metabolit sekunder dalam daun jambu biji. Pemilihan didasarkan pada kriteria rendemen serta nilai aktivitas antioksidan yang tinggi pada konsentrasi yang kecil.
Rendemen ekstrak pekat metanol, etil asetat dan etanol 70% (v/v), berturut-turut adalah 13.25%, 6.69%, dan 18.25%. Rendemen ekstrak etanol 70% (v/v) paling tinggi, simplisia daun jambu biji lebih banyak mengandung senyawa yang mempunyai sifat kepolaran dekat dengan kepolaran etanol 70% (v/v). Etanol 70% (v/v) mempunyai kepolaran antara etanol dan air.
7
Gambar 2 Ekstrak kasar daun jambu biji yang telah dipekatkan, terdiri atas ekstrak metanol (a), ekstrak etil asetat (b), dan ekstrak etanol 70% (v/v) (c)
Uji Aktivitas Ekstrak Daun Jambu Biji
Penapisan konsentrasi setiap ekstrak daun jambu biji dilakukan pada 80, 40, 20, 10, 5, 2.5, 1.25, 0.625, dan 0.3125 mg/L. Nilai persen inhibisi radikal bebas DPPH, yang diperoleh menunjukkan bahwa semakin tinggi konsentrasi ekstrak nilai peredaman atau penangkapan radikal bebas DPPH semakin meningkat (Gambar 3). Nilai persen inhibisi ketiga ekstrak beragam untuk konsentrasi yang sama. Hal ini menunjukkan adanya perbedaan aktivitas penangkapan radikal bebas dari ketiga ekstrak. Nilai persen inbihisi ekstrak metanol dan etanol 70% (v/v) tidak jauh berbeda (kurva hampir berimpit), sebab kepolaran kedua pelarut tersebut tidak jauh berbeda. Ekstrak metanol dan etanol 70% (v/v) mampu mereduksi hampir 50% radikal bebas pada selang konsentrasi 10 sampai 20 mg/L. Ekstrak etil asetat menunjukkan nilai persen inhibisi yang paling rendah dan baru mereduksi 50% radikal bebas pada kisaran konsentrasi 40 mg/L (Gambar 3)
Gambar 3 Aktivitas penangkapan radikal bebas ekstrak kasar daun jambu biji dan kontrol positif.
menandakan kondisi jenuh, yang di dalamnya semua radikal DPPH telah tereduksi. Radikal bebas DPPH akan tereduksi menjadi senyawa difenil pikrilhidrazina, melalui pengikatan 1 elektron H oleh atom N yang elektronnya tidak berpasangan (Gambar 4). Hal ini ditandai dengan adanya perubahan warna ungu DPPH menjadi kuning (Molyneux 2004).
Gambar 4 Mekanisme pengkapan radikal bebas DPPH (Molyneux 2004)
Nilai IC50 merupakan parameter utama aktivitas antioksidan yang ditentukan
dengan mengevaluasi nilai persen inhibisi. Nilai IC50 yang diperoleh menunjukkan
bahwa ekstrak etanol 70% (v/v) mempunyai aktivitas antioksidan yang paling baik, karena mempunyai nilai IC50 yang paling kecil di antara ekstrak yang lain dan
mempunyai rendemen tertinggi (Tabel 2). Ekstrak metanol dan etanol 70% (v/v) mempunyai aktivitas antioksidan yang tidak jauh berbeda dan dapat dikatakan sangat kuat aktivitasnya karena memberikan nilai IC50 kurang dari 50 mg/L (Zuhra
2008). Namun, aktivitas antioksidan pada kontrol positif yaitu asam askorbat dan standar kuersetin masih lebih baik. Kuersetin digunakan sebagai standar pembanding karena menurut Porwal et al. (2012) dan Joseph et al. (2011), senyawa ini termasuk salah satu senyawa antioksidan golongan flavonoid dalam daun jambu biji. Menurut Farmakope Herbal Indonesia, kuersetin merupakan senyawa penciri yang dimiliki oleh daun jambu biji. Penentuan nilai IC50 ekstrak daun jambu biji
serta standar asam askorbat dan kuersetin terdapat pada Lampiran 2 dan 3.
Tabel 2 Rendemen dan IC50 ekstrak kasar daun jambu biji
Ekstrak Rendemen (%b/b) IC50 (mg/L)
Metanol 6.69 10.00
Etil asetat 13.25 27.29 Etanol 70% (v/v) 18.25 8.29
Asam askorbat - 1.25
Kuersetin - 2.95
Uji fitokimia dilakukan lagi pada ekstrak teraktif untuk mengetahui secara kualitatif golongan senyawa yang kemungkinan berperan sebagai antioksidan. Berdasarkan hasil uji fitokimia ekstrak etanol 70% (v/v) sebagai ekstrak teraktif terbukti mengandung golongan senyawa flavonoid dan tanin. Menurut Porwal et al.
9
bertindak sebagai donor hidrogen untuk radikal bebas. Senyawa golongan tanin, menurut Hagerman (2002) memiliki peranan biologis yang kompleks mulai dari pengendapan protein, hingga pengkelatan logam serta berfungsi sebagai antioksidan biologis.
Fraksionasi Ekstrak Teraktif
Ekstrak teraktif difraksionasi metode kromatografi kolom, dengan terlebih dahulu menentukan eluen terbaik. Eluen tunggal yang digunakan, yaitu metanol. etanol, etil asetat dan kloroform. Hasil elusi menunjukkan bahwa kloroform memisahkan noda terbanyak, sementara. metanol dan etil asetat dapat memisahkan noda dengan keterpisahan yang jelas (Gambar 5). Pemilihan eluen terbaik dilakukan dengan mengkombinasikan campuran kloroform:etil asetat dan kloroform:metanol dengan nisbah 1:9 sampai 9:1.
a b c d
Gambar 5 Noda KLT ekstrak teraktif degan fase gerak etanol (a), etil asetat (b), kloroform (c), dan metanol (d)
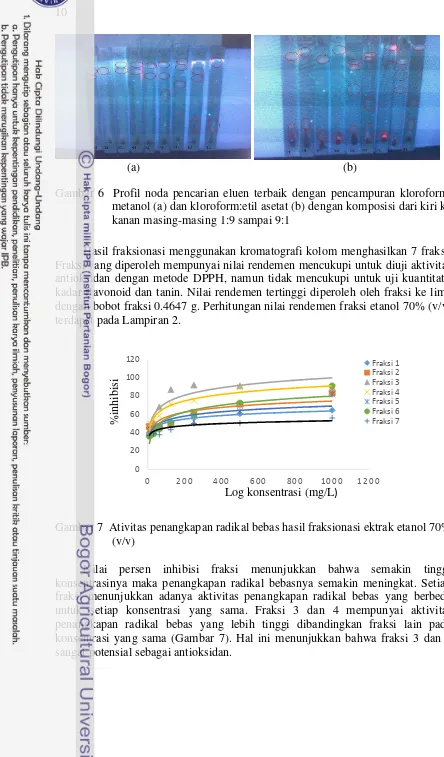
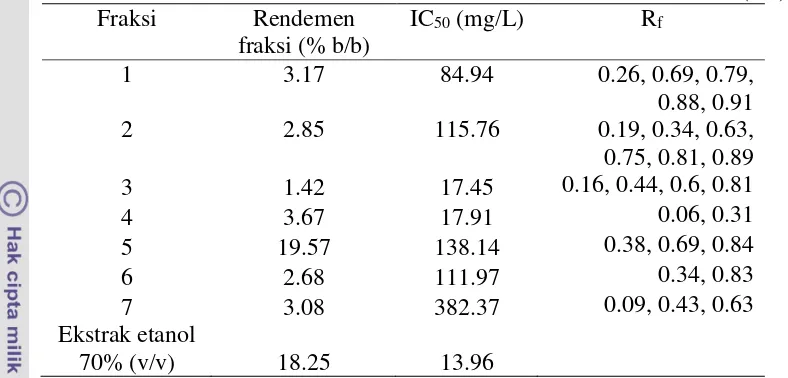
Hasil elusi campuran menunjukkan distribusi noda pada kombinasi kloroform:etil asetat umumnya lebih baik dari pada distribusi noda pada kombinasi kloroform:metanol (Gambar 6). Eluen terbaik pada pencampuran kloroform:etil asetat terlihat pada komposisi 8:2, sementara pada pencampuran kloroform:metanol terlihat pada komposisi 6:4.
(a) (b)
Gambar 6 Profil noda pencarian eluen terbaik dengan pencampuran kloroform: metanol (a) dan kloroform:etil asetat (b) dengan komposisi dari kiri ke kanan masing-masing 1:9 sampai 9:1
Hasil fraksionasi menggunakan kromatografi kolom menghasilkan 7 fraksi. Fraksi yang diperoleh mempunyai nilai rendemen mencukupi untuk diuji aktivitas antioksidan dengan metode DPPH, namun tidak mencukupi untuk uji kuantitatif kadar flavonoid dan tanin. Nilai rendemen tertinggi diperoleh oleh fraksi ke lima dengan bobot fraksi 0.4647 g. Perhitungan nilai rendemen fraksi etanol 70% (v/v) terdapat pada Lampiran 2.
Gambar 7 Ativitas penangkapan radikal bebas hasil fraksionasi ektrak etanol 70% (v/v)
Nilai persen inhibisi fraksi menunjukkan bahwa semakin tinggi konsentrasinya maka penangkapan radikal bebasnya semakin meningkat. Setiap fraksi menunjukkan adanya aktivitas penangkapan radikal bebas yang berbeda untuk setiap konsentrasi yang sama. Fraksi 3 dan 4 mempunyai aktivitas penangkapan radikal bebas yang lebih tinggi dibandingkan fraksi lain pada konsentrasi yang sama (Gambar 7). Hal ini menunjukkan bahwa fraksi 3 dan 4 sangat potensial sebagai antioksidan.
0 20 40 60 80 100 120
0 2 0 0 4 0 0 6 0 0 8 0 0 1 0 0 0 1 2 0 0
Fraksi 1 Fraksi 2 Fraksi 3 Fraksi 4 Fraksi 5 Fraksi 6 Fraksi 7
Log konsentrasi (mg/L)
%
inhi
11
Tabel 3 Nilai rendemen dan aktivitas antioksidan fraksi ekstrak etanol 70% (v/v) Fraksi Rendemen
perameter utama aktivitas antioksidan. Fraksi 3 dan 4 mempunyai aktivitas antioksidan sangat kuat karena mempunyai nilai IC50 kurang dari 50 mg/L (Tabel
3). Nilai IC50 antara fraksi 3 dan 4 tidak jauh berbeda, kemungkinan keduanya
mempunyai komponen senyawa yang sama atau hampir sama. Fraksi 1 mempunyai aktivitas antioksidan kuat karena nilai IC50 antara 50 dan 100 mg/L, dan fraksi 2, 5,
6 termasuk sedang dengan IC50 antara 100 dan 150 mg/L, sedangkan fraksi 7 tidak
mempunyai potensi sebagai antioksidan karena nilai IC50 lebih dari 200 mg/L
(Zuhra 2008). Penentuan nilai IC50 terdapat dalam Lampiran 4. Fraksi yang
mempunyai aktivitas teraktif adalah fraksi ke tiga dengan nilai IC50 sebesar 17.45
mg/L.
Nilai aktivitas antioksidan hasil fraksionasi etanol 70% (v/v) menunjukkan adanya penurunan dibandingkan dengan nilai aktivitas ekstrak kasar etanol 70% (v/v). Hal ini dapat disebabkan karena adanya interaksi antara senyawa tertentu dalam ekstrak kasar yang memberikan pengaruh sinergis sehingga dapat menyebabkan peningkatan pada nilai aktivitas antioksidannya. Faktor lain yang dapat menjadi penyebab menurunnya aktivitas antioksidan adalah terjadinya oksidasi pada sampel pada saat penyimpanan atau pada saat proses fraksionasi, adanya senyawa aktif yang tertahan dalam kolom, hal ini dapat dilihat dari nilai total rendemen fraksi yang hanya mencapai 36.44%.
SIMPULAN DAN SARAN
Simpulan
mempunyai aktivitas antioksidan teraktif adalah fraksi ketiga dengan nilai IC50
17.45 mg/L. Nilai IC50 ekstrak dan fraksi teraktif etanol 70% (v/v) menunjukkan
aktivitas antioksidannya lebih lemah dibandingkan standar asam askorbat dan kuersetin yang mempunyai nilai IC50 berturut-turut 1.25 dan 2.65 mg/L.
Saran
Perlu dilakukan analisis gugus fungsi antara fraksi ke tiga dan ke empat untuk mengetahui perbedaan keduanya Perlu dilakukan uji lebih lanjut terhadap fraksi aktif untuk mengisolasi senyawa yang berperan lebih spesifik sebagai antioksidan dan mengetahui mekanisme penghambatan radikal bebasnya secara spesifik. Perlu juga dilakukan uji lebih lanjut untuk mengetahui kadar kuantitatif metabolit sekunder fraksi yang mempunyai aktivitas antioksidan tertinggi terutama kadar flavoniod dan taninnya..
DAFTAR PUSTAKA
Amelia N, Prayitno SB. 2012. Pengaruh ekstrak daun jambu biji (Psidium guajava) untuk menginaktifkan viral nervous nekrosis (VNN) pada ikan kerapu bebek (Epinephelus fuscoguttatus). JAMT . 1(1):264-278.
Arini SRD, Susilowati E, Susanti E, Setiyani. 2008. Activity test of Guajava (Psidium guajava L) leaf methanol extract as contraception in (Rattus norvegicus). Indo J Chem. 8 (2): 264-270.
Coskun O, Kanter M, Armutcu F, Cetin K, Kaybolbaz B, Kaygan O. 2004. Protective effects of quercetine, a flavonoid, antioxidant, in absolut etanol-induced acu gastrict uclear. Eur J Gen Med. 1(3) 37-42.
Daud MF, Sadiyah ER, Rismawati E. 2011. Pengaruh perbedaan metode ekstraksi terhadap aktivitas antioksidan ekstrak etanol daun jambu biji (Psidium guajava L) berdaging buah putih. Seminar Nasional Peneliatian dan PKM Sains, Teknologi dan Kesehatan.Bandung, Indonesia. Bandung (ID): 2(1). Haliwell B, Gutteridge JMC. 1997. Free Radical in Biology and Madicine.
Oxford(ENG): Oxford UnivPr.
Harborne JB. 1987. Metode Fitokimia:Penentuan Cara Modern Menganalisis Tumbuhan. Padmawinata K, Sudiro I, penerjemah. Bandung (ID): Penerbit ITB. Terjemahan dari Phytohemical Methods.
Hagerman AE. 2002. Tannin Handbook. Department of Chemistry and Biochemistry. Florida (USA) : Miami Univ Pr.
Hayati EK, Fasyah AG, Sa’adah L. 2010. Fraksinasi dan identifikasi senyawa tanin pada daun bimbing wuluh (Averrhoa bilimbi L). Nilai persen inhibisi digunakan untuk menentukan nilai IC50 yang merupakan parameter utama aktivitas antioksidan. 193-200.
Harnly J, . 2006. Flavonoid content of U.S. fruit, vegetables, and nuts. J Agri Food Chem. 54: 9966-9977
13
Joseph B, Priya M. 2011. Review on Nutritional, Medicinal, and Parmalogical Properties of Guava (Psidium guajava Linn). Int J Pharm Biol Scie. 21: 53-69.
[Kemenkes] Kementrian Kesehatan 2009. Keputusan Mentri Kesehatan Republik Indonsesia Nomer 261 Tahun 2009 tentang Farmakope Herbal Indonesia Edisi I. Jakarta (ID): Kemenkes
Kusumawati I. 2004. Penetapan Senyawa Marker dan Profil Metabolit Ekstrak Daun Jambu Biji (Psidium guajava L.) sebagai Obat Fitofarmaka Demam Berdarah Dengue. [Tesis]. Surabaya (ID): Universitas Airlangga.
Luthfie F. 2014. Fraksi Polar Daun Jambu Biji (Psidium guajava) sebagai Antiretroviral terhadap Simian Retrovirus. [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Markham KR. 1988.Cara Mengidentifikasi Flavonoid. Padmawinata K, penerjemah. Bandung: penerbit ITB. Terjemahan dari: Techniques of Flavonoid Identi-fication.
Mesah A. 2013. Aktivitas antioksidan ekstrak metanol daun dan buah jambu biji (Psidium guajava L) asal pulau Timor. J Kimia Terapan. 1: 50-54.
Miller AL. 1996. Antioxidant flavonoid: struktur, function, and clinical usage. Alt Med Rev. 1(2): 103-111.
Molyneux P. 2004. The use of the stable free radical diphenylpicrilhydrazil (DPPH) for estimating antioxidant activity. J Sci Technol. 26(2) : 211-219
Prakash A. 2001. Antioxidant Activity. Medallion Laboratories: Analytical Progress 19(2): 1-4.
Porwal V, Singh P, Gurjar D. 2012. A Comprehensive Study On Different MethodsOf Extraction From Guajava Leaves For Curing Various Health Problem. Intrn J Engin. 2(6): 490-496.
Rahman F, Logawa ED, Hegartika H, Simanjuntak E. 2008. Aktivitas antioksidan ekstrak tunggal dan kombinasinya dari tanaman Curcuma spp. JIKI. 6(2): 69-74.
Rasidah, Afizia WM. 2012. Potensi ekstrak daun jambu biji sebagai antibakterial untuk menggulangi serangan bakteri Aeromonas hydrophila pada ikan gurame (Oshpronemus gouramylacepede). J Akuat.1(1): 19-27.
Refli R. 2012.Potensi ekstrak daun Tin (Ficuscarica L) sebagai antioksidan dan aktivitas hambatnya terhadap proliferasi sel keneker HeLa [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Sharon S, Anam S, Yuliet. 2013. Formulasi krim antioksidan ekstrak etanol bawang hutan (Eleutherine palmifolia L Merr). J Natur Scie. 2(3): 111-122.
LAMPIRAN
Lampiran 1 Diagram alir penelitian
Lampiran 2 Data penentuan nilai IC50 ekstrak kasar daun jambu biji
Nilai persen inhibisi ekstrak metanol Konsentrasi
(mg/L)
Absorbans
Rata-rata % Inhibisi Ulangan 1 Ulangan 2 Ulangan 3
80 0.136 0.146 0.138 0.140 81.26 40 0.262 0.271 0.248 0.260 65.15 20 0.342 0.331 0.338 0.337 54.89 10 0.390 0.388 0.390 0.389 47.88 5 0.405 0.406 0.414 0.408 45.34
Kurva hubungan konsentrasi dan % inhibisi ekstrak metanol
Contoh Perhitungan:
Absorbans kontrol (DPPH) = 0.747 +0.745+0.748 = 0.74666 = 0.747 3
y = 12,856ln(x) + 20,391 R² = 0,9229
0 10 20 30 40 50 60 70 80 90
0 20 40 60 80 100
Log konsentrasi (mg/L)
%in
h
ib
is
15
Nilai persen inhibisi ekstrak etil asetat Konsentrasi
Absorbans kontrol (DPPH) = 0.814 +0.819+0.813 = 0.81533 = 0.815 3
%inhibisi = A DPPH- A sampel × 100 %
A DPPH
= 0.815 – 0.336 × 100 % = 81.26% 0.815
Kurva hubungan konsentrasi dengan % inhibisi ekstrak etil asetat
Perhitungan nilai IC50 ekstrak etil asetat
lanjutan Lampiran 2
Nilai persen inhibisi ekstrak etanol 70% (v/v) Konsentrasi Absorbans kontrol (DPPH)= 0.814 +0.819+0.813 = 0.81533 = 0.815
3
%inhibisi = A DPPH- A sampel × 100 %
A DPPH
= 0.815 – 0.174 × 100 % = 78.69% 0.815
Kurva hubungan konsentrasi dengan %inhibisi ekstrak etanol 70% (v/v)
Perhitungan nilai IC50. Ekstrak etanol 70% (v/v)
Y = 9.7448ln(x) + 29.38 50 = 9.7448ln(x)+ 29.38
ln(x) = (50 – 29.38) / 9.7448 = 2.116 mg/L x = 8.29 mg/L
Lampiran 3 Data nilai IC50 asam askorbat dan standar kuersetin
17
Absorbans kontrol (DPPH) = 0.747 +0.745+0.748 = 0.74666 = 0.747 3
%inhibisi = A DPPH- A sampel × 100 %
A DPPH
= 0.747 – 0.060 × 100 % = 90.90% 0.747
Kurva hubungan %inhibisi dengan konsentrasi asam askorbat
Perhitungan nilai IC50 vitamin C
Contoh perhitungan:
Absorbans kontrol (DPPH)= 0.747 +0.745+0.748 = 0.74666 = 0.747 3
%inhibisi = A DPPH- A sampel × 100 %
A DPPH
= 0.747 – 0.058 × 100 % = 90.28% 0.747
Kurva hubungan %inhibisi dengan konsentrasi kuersetin
Perhitungan nilai IC50 kuersetin
Y = 13.736ln(x) + 35.1 50 = 13.736 (x)+ 35.1
ln(x) = (50 – 35.1) / 7313.6 = 1.085mg/L x = 2.95 mg/L
Lampiran 4 Data nilai IC50 fraksi ekstrak etanol 70% (v/v)
19
Lanjutan Lampiran 4
= 1.065 – 0.060 × 100 % = 64.29% 1.065
Kurva hubungan konsentrasi dengan %inhibisi fraksi 1
Perhitungan nilai IC50 fraksi 1
Y = 5.4992ln(x) + 25.573
Kurva hubungan nilai %inhibisi dan konsentrasi fraksi 2
Perhitungan nilai IC50 fraksi 2
Y = 13.844ln(x) – 14.238
0 200 400 600 800 1000 1200
Log konsentrasi (mg/L)
0 200 400 600 800 1000 1200
Log konsentrasi (mg/L)
%i
nh
ib
lanjutan Lampiran 4
Kurva hubungan %inhibisi dengan konsentrasi frasksi 3
Perhitungan nilai IC50 fraksi 3
21
lanjutan Lampiran 4
Kurva hubungan %inhibisi dengan konsentrasi fraksi 4
Perhitungan nilai IC50 fraksi 4
Y =10.16ln(x) + 20.679
Kurva hubungan %inhibisi dan konsentrasi fraksi 5
Perhitungan nilai IC50 fraksi 5
Y =12.964ln(x) -13.871
0 200 400 600 800 1000 1200
lanjutan Lampiran 4
Kurva hubungan %inhibisi dan konsentrasi frasksi 6
Perhitungan nilai IC50 fraksi 6
23
lanjutan Lampiran 4
Kurva hubungan %inhibisi dan konsentrasi frasksi 7
Perhitungan nilai IC50 fraksi 7
Y = 6.2675ln(x) + 12.731 50 = 6.2675ln (x)+ 12.731
ln(x) = (50 – 12.731) / 6.2675 = 5.9464 mg/L x = 382.37mg/L
y = 6,2675ln(x) + 12,731 R² = 0,9547
0 10 20 30 40 50 60
0 200 400 600 800 1000 1200
%
in
h
ib
isi
RIWAYAT HIDUP
Penulis dilahirkan di Kebumen pada tanggal 21 Oktober 1991 dari ayah Basirun dan ibu Siti Rochmah. Penulis adalah putri ketiga dari empat bersaudara. Tahun 2010 penulis lulus dari SMA N 2 Purworejo dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB dan diterima di Departemen Kimia. Fakultas Matematika dan Ilmu Pengetahuan Alam.