Lampiran 1. Hasil Identifikasi Tumbuhan
Lampiran 2. Gambar Sampel
Gambar 1. Sayur Selada yang Ditanam
Lampiran 3. Alat-alat yang Digunakan dalam Penelitian
Gambar 3. Spektrofotometer Sinar Tampak
Lampiran 4. Uji Kualitatif Nitrit dan Nitrat
Gambar 5. Uji kualitatif nitrit dengan penambahan pereaksi Asam Sulfanilat dan N-(1-naftil) etilendiamin dihidroklorida
Keterangan:
a. Selada yang ditanam dengan pupuk urea b. Selada yang ditanam dengan pupuk kompos c. Selada yang ditanam tanpa pupuk
d. Baku nitrit
Gambar 6. Uji kualitatif nitrat dengan penambahan Larutan Besi (II) Sulfat dan Asam Sulfat Pekat (Uji Cincin Coklat)
Keterangan:
a. Selada yang ditanam dengan pupuk urea b. Selada yang ditanam dengan pupuk kompos c. Selada yang ditanam tanpa pupuk
d. Baku nitrat
a b c d
Lampiran 5. Bagan Alir Pembuatan Larutan Induk Baku Nitrit, Penentuan Panjang Gelombang Maksimum, Waktu Operasional dan Kurva Kalibrasi Nitrit Baku
Natrium Nitrit
← ditimbang 100 mg
← dimasukkan ke dalam labu tentukur 100 mL
← dilarutkan dan dicukupkan dengan air suling sampai garis tanda
LIB I Nitrit (C= 1000 µg/mL)
← Dipipet 1 mL
← Dimasukkan ke dalam labu tentukur 100 Ml
← dilarutkan dan dicukupkan dengan air suling sampai garis tanda
← Dimasukkan ke dalam labu tentukur 50 mL
← Dimasukkan ke dalam labu tentukur 50 mL
← Ditambahkan 2,5
← Ditambahkan 2,5 mL asam sulfanilat, kocok selama 5 menit kemudian tambahkan 2,5 mL N-(1-naftil) etilendiamin
← Ditambahkan 2,5 mL asam sulfanilat, kocok selama 5
menit kemudian
← Diukur serapan pada panjang gelombang 540 nm setiap menit selama 60 menit
← Diukur masing-masing serapan pada panjang gelombang 540 nm pada menit ke-21
Waktu Operasional ← Dibuat kurva kalibrasi
Lampiran 6. Bagan Alir Penentuan Kadar Nitrit dan Nitrat dalam Sayur Selada Sampel
← ditimbang 10 g sampel yang telah dihaluskan
← dimasukkan ke dalam beaker glass 250 mL
← ditambahkan air suling (±80˚C) sampai 150 mL
← dihomogenkan kemudian dipanaskan di atas penangas air hingga 2 jam sambil diaduk
← didinginkan pada suhu kamar
← dipindahkan secara kuantitatif ke dalam labu tentukur 250 mL
← ditambahkan air suling sampai garis tanda
← dihomogenkan kemudian disaring
← dibuang 10 mL filtrat pertama
Filtrat
← dipipet 10 mL
← dimasukkan ke dalam labu tentukur 50 mL
← ditambahkan 2,5 mL asam sulfanilat, dikocok selama 5 menit kemudian ditambahkan 2,5 mL N-(1-naftil) etilendiamin dihidroklorida
← dicukupkan dengan air suling sampai garis tanda
← diukur serapan pada lamda 540 nm pada menit ke 21
Nilai Absorbansi
← dihitung
Lampiran 6. (Lanjutan) Sampel
← ditimbang 10 g sampel yang telah dihaluskan
← dimasukkan ke dalam beaker glass 250 mL
← ditambahkan air suling (±80˚C) sampai 150 mL
← dihomogenkan kemudian dipanaskan di atas penangas air hingga 2 jam sambil diaduk
← didinginkan pada suhu kamar
← dipindahkan secara kuantitatif ke dalam labu tentukur 250 mL
← ditambahkan air suling sampai garis tanda
← dihomogenkan kemudian disaring
← dibuang 10 mL filtrat pertama
Filtrat
← dipipet 10 mL
← dimasukkan ke dalam labu tentukur 50 mL
← ditambahkan sedikit logam Zn (0,1g) dalam larutan asam dan didiamkan selama 5 menit
← ditambahkan 2,5 mL asam sulfanilat, dikocok selama 5 menit kemudian ditambahkan 2,5 mL N-(1-naftil) etilendiamin dihidroklorida
← dicukupkan dengan air suling sampai garis tanda
← diukur serapan pada lamda 540 nm pada menit ke 21
Nilai Absorbansi
← dihitung
Lampiran 9. Data Kalibrasi Nitrit Baku, Persamaan Regresi dan Koefisien Korelasi
1. Data Kalibrasi Serapan Nitrit pada Panjang Gelombang 540 nm No. Konsentrasi (µg/mL) (X) Absorbansi (Y)
1 0,0000 -0,00052
2. Perhitungan Persamaan Regresi
a =
Sehingga diperoleh persamaan regresi Y = 0,54794 X + 0,00754
3. Perhitungan Koefisien Korelasi (r) r =
(∑XY )−(∑X)(∑Y)/n
Lampiran 10. Perhitungan Batas Deteksi (Limit of Detection, LOD) dan Batas Kuantitasi (Limit of Quantitation, LOQ) Nitrit
Persamaan garis regresi adalah Y = 0,54794 X + 0,00754
No. X Y Yi Y-Yi (Y-Yi)2
1 0,0000 -0,00052 0,00754 -0,00806 0,00006 2 0,1000 0,06137 0,062334 -0,00096 0,00000 3 0,2000 0,11859 0,117128 0,00146 0,00000 4 0,4000 0,23584 0,226716 0,00912 0,00008 5 0,6000 0,34180 0,336304 0,00550 0,00003 6 0,8000 0,44629 0,445892 0,00040 0,00000 7 1,0000 0,54802 0,555480 -0,00746 0,00006
TOTAL 0,00024
Simpangan Baku = �∑(�−��)2 �−2 = �
0,00024
7−2 = 0,006889 mg/Kg
Batas Deteksi = 3 ��� ����� =
3 � 0,006889
0,54794 = 0,037718 mg/Kg
Batas Kuantitasi = 10 ��� ����� =
10 � 0,006889
Lampiran 11. Contoh Perhitungan Kadar Nitrit dalam Sayur Selada
• Bobot sampel = 10,0359 g • Absorbansi analisis nitrit = 0,10632
• Persamaan Regresi (Y) = 0,54794 X + 0,00754 • Konsentrasi nitrit
Y = 0,54794 X + 0,00754 0,10632 = 0,54794 X + 0,00754
X = 0,10632−0,00754
0,54794
X = 0,18028 µg/mL • Kadar Nitrit dalam sampel = ������
����� ������
= 0,18028 µ�/��� 250 ��� 5
10,0359 �
= 22,4544 µg/g
Dengan cara yang sama dapat dihitung kadar nitrit pada semua sampel. Keterangan:
X : konsentrasi nitrit di dalam sampel (µg/mL) Y : volume larutan pengenceran (mL)
Lampiran 12. Contoh Perhitungan Kadar Nitrat dalam Sayur Selada
• Bobot sampel = 10,0359 g • Absorbansi analisis nitrit = 0,19646
• Persamaan Regresi (Y) = 0,54794 X + 0,00754
• Kadar nitrit = kadar nitrit setelah reduksi-kadar nitrit sebelum reduksi = 42,9433 µg/g - 22,4544 µg/g
= 20,4889 µg/g
Karena hasil pembacaan alat spektrofotometeruntuk nitrat adalah sebagai nitrit, oleh karena itu hasil pembacaan harus dikonversikan.
Kadar nitrat = kadar nitrit hasil reduksi nitrat x ����3 ����2
= 20,4889 µg/g x 62
46
= 27,6155 µg/g
Dengan cara yang sama dapat dihitung kadar nitrat pada semua sampel. Keterangan:
X : konsentrasi nitrit di dalam sampel (µg/mL) Y : volume larutan pengenceran (mL)
Lampiran 13. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada Tanpa Pemupukan Panen Hari ke-52
No
Kadar nitrit pada sayur selada tanpa pemupukan panen hari ke-52: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 14. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada dengan Pupuk Kompos Panen Hari ke-52
No.
Kadar nitrit pada sayur selada dengan pupuk kompos panen hari ke-52: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 15. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada dengan Pupuk Urea Panen Hari ke-52
No.
SB = �∑(�−�����)2 �−1 = �
0,2364
5−1 = 0,2431
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrit pada sayur selada dengan pupuk urea panen hari ke-52: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 16. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada Tanpa Pemupukan Panen Hari ke-54
No.
Kadar nitrit pada sayur selada tanpa pemupukan panen hari ke-54: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 17. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada dengan Pupuk Kompos Panen Hari ke-54
No.
SB = �∑(�−�����)2 �−1 = �
0,1077
5−1 = 0,16407
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrit pada sayur selada dengan pupuk kompos panen hari ke-52: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 18. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada dengan Pupuk Urea Panen Hari ke-54
No.
Kadar nitrit pada sayur selada dengan pupuk urea panen hari ke-54: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 19. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada Tanpa Pemupukan Panen Hari ke-60
No.
SB = �∑(�−�����)2 �−1 = �
0,2386
5−1 = 0,24424
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrit pada sayur selada tanpa pemupukan panen hari ke-60: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 20. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada dengan Pupuk Kompos Panen Hari ke-60
No.
Kadar nitrit pada sayur selada dengan pupuk kompos panen hari ke-52: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 21. Analisis Data Statistik untuk Menghitung Kadar Nitrit pada Sayur Selada dengan Pupuk Urea Panen Hari ke-60
No.
SB = �∑(�−�����)2 �−1 = �
2,0767
5−1 = 0,72054
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrit pada sayur selada dengan pupuk urea panen hari ke-60: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 22. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada Tanpa Pemupukan Panen Hari ke-52
No.
SB = �∑(�−�����)2 �−1 = �
3,6850
5−1 = 0,95981
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrat pada sayur selada tanpa pemupukan panen hari ke-52: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 23. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada dengan Pupuk Kompos Panen Hari ke-52
No.
Kadar nitrat pada sayur selada dengan pupuk kompos panen hari ke-52: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 24. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada dengan Pupuk Urea Panen Hari ke-52
No.
Kadar nitrat pada sayur selada dengan pupuk urea panen hari ke-52: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 25. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada Tanpa Pemupukan Panen Hari ke-54
No.
SB = �∑(�−�����)2 �−1 = �
2,0543
5−1 = 0,71664
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrat pada sayur selada tanpa pemupukan panen hari ke-60: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 26. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada dengan Pupuk Kompos Panen Hari ke-54
No.
SB = �∑(�−�����)2 �−1 = �
6,0883
5−1 = 1,23372
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrat pada sayur selada dengan pupuk kompos panen hari ke-60: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 27. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada dengan Pupuk Urea Panen Hari ke-54
No.
Kadar nitrat pada sayur selada dengan pupuk urea panen hari ke-60: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 28. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada Tanpa Pemupukan Panen Hari ke-60
No.
SB = �∑(�−�����)2 �−1 = �
0,3820
5−1 = 0,30903
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrat pada sayur selada tanpa pemupukan panen hari ke-60: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 29. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada dengan Pupuk Kompos Panen Hari ke-60
No.
0,19199 18,1745 -14,2440 202,8912 4,0321 4,7718 Ditolak 5
SB = �∑(�−�����)2 �−1 = �
23,8430
5−1 = 2,4415
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1 =5, maka t(α/2,dk) =
4,60409. t hitung = � �−��
SB / √��
Data diterima jika t hitung < t tabel
Kadar nitrat pada sayur selada dengan pupuk kompos panen hari ke-60: µ = �� ± (t(α/2,dk) x SB/ √�)
Lampiran 30. Analisis Data Statistik untuk Menghitung Kadar Nitrat pada Sayur Selada dengan Pupuk Urea Panen Hari ke-60
No.
Kadar nitrat pada sayur selada dengan pupuk urea panen hari ke-60: µ = �� ± (t(α/2,dk) x SB/ √�)
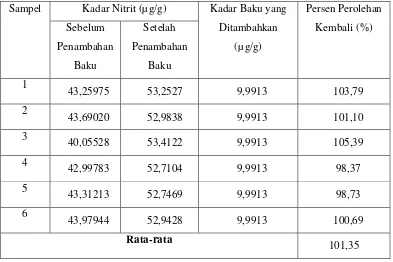
Lampiran 31. Hasil Uji Perolehan Kembali Nitrit dan Nitrat Setelah Penambahan Masing-Masing Larutan Standar pada Sampel Sayur Selada
1. Uji Perolehan Kembali Setelah Penambahan Larutan Standar Nitrit
Sam pel
Serapan Kadar Nitrit (µg/g) Kadar Baku
0,19748 0,24127 43,2597
5 53,2527 9,9913 103,79 2
0,19937 0,24009 43,6902
0 52,9838 9,9913 101,10 3
0,18341 0,24197 40,0552
8 53,4122 9,9913 105,39 4
0,19633 0,23889 42,9978
3 52,7104 9,9913 98,37 5
0,19771 0,23905 43,3121
3 52,7469 9,9913 98,73 6
0,20064 0,23991 43,9794
4 52,9428 9,9913 100,69 Rata-rata
Lampiran 31. (Lanjutan)
2. Uji Perolehan Kembali Setelah Penambahan Larutan Standar Nitrat
Sam pel
Lampiran 32. Contoh Perhitungan Uji Perolehan Kembali Nitrit dalam Sayur Selada
• Bobot
o sampel tambah baku = 10,0127 g • Absorbansi analisis nitrit
o sampel tambah baku = 0,24127
• Rata-rata kadar nitrit tanpa baku = 42,8824 µg/g (CA) • Kadar Baku yang ditambahkan = 9,9913 µg/g (C*A) • Persamaan Regresi (Y) = 0,54794 X + 0,00754 • Konsentrasi nitrit
o Sampel tambah baku
Y = 0,54794 X + 0,00754 0,24127 = 0,54794 X + 0,00754
X = 0,24127−0,00754 0,54794
X = 0,42656 µg/mL • Kadar Nitrit dalam sampel
o Tambah Baku = ������
����� ������
= 0,42656 µg/mL � 250 ��� 5
10,0127 �
= 53,2524 µg/g (CF)
Perhitungan Uji Perolehan Kembali Nitrit % Recovery Nitrit = ��−��
�∗� x 100% = (53,2524 −42,8824 ) µg/g
9,9913 µg/g x 100%
Lampiran 33. Contoh Perhitungan Uji Perolehan Kembali Nitrat dalam Sayur Selada
• Bobot
o sampel tambah baku = 10,0065 g • Absorbansi analisis nitrat
o sampel tambah baku = 0,36554
• Kadar nitrit sebelum reduksi = 30,46514 µg/g • Rata-rata kadar nitrat tanpa baku = 49,3758 µg/g (CA) • Kadar baku yang ditambahkan = 19,9950 µg/g (C*A) • Persamaan Regresi (Y) = 0,54794 X + 0,00754 • Konsentrasi nitrat
o Tambah baku
Y = 0,54794 X + 0,00754 0,36554 = 0,54794 X + 0,00754
X = 0,36554−0,00754
0,54794
X = 0,65335 µg/mL • Kadar Nitrat dalam sampel
o Sampel tambah baku = ������
����� ������
= 0,65335 µg/mL � 250 ��� 5
10,0065 �
= 81,6157 µg/g
Kadar nitrit = kadar nitrit setelah reduksi-kadar nitrit sebelum reduksi = 81,6157 µg/g – 30,46514 µg/g
Kadar nitrat = kadar nitrit hasil reduksi x ����3 ����2
= 51,1506 µg/g x 62
46
= 68,9421 µg/g (CF)
Perhitungan Uji Perolehan Kembali Nitrat % Recovery Nitrat = ��−��
�∗� x 100% = (68,9421 −49,3758 ) µg/g
19,9950 µg/g x 100%
Lampiran 34. Perhitungan Simpangan Baku Relatif (Relative Standard Deviation, RSD) Persen Perolehan Kembali Nitrit
Sampel Persen Perolehan Kembali (%) (Xi – ����) (Xi – ����)2
1
103,79 2,45 5,9906
2
101,10 -0,24 0,0592
3
105,39 4,04 16,3524
4
98,37 -2,98 8,8783
5
98,73 -2,61 6,8371
6
100,69 -0,65 0,4273
�� = 101,35 ∑ = 38,5449
SD = �∑( �−�⃛)2 �−1
= �38,5449
5
= 2,7765 RSD = ��
�⃛ x 100% = 2,7765
101,35 x 100%
Lampiran 35. Perhitungan Simpangan Baku Relatif (Relative Standard Deviation, RSD) Persen Perolehan Kembali Nitrat
Sampel Persen Perolehan Kembali (%) (Xi – ����) (Xi – ����)2
1
91,01 -2,28 5,2196
2
91,71 -1,58 2,4892
3
91,77 -1,52 2,2991
4
97,86 4,57 20,8783
5
95,48 2,19 4,7843
6
91,91 -1,38 1,8988
�� = 93,29 ∑ = 37,5693
SD = �∑( �−�⃛)2 �−1
= �37,5693
5
= 2,7411 RSD = ��
�⃛ x 100% = 2,7411
93,29 x 100%
Lampiran 36. Pengujian Beda Nilai Rata-Rata Kadar Nitrit Masa Panen H-52
Dari hasil pengujian statistik di atas, terdapat perbedaan yang signifikan dengan probabilitas lebih kecil dari 0,05 antara nilai rata-rata kadar nitrit dari ketiga sampel (F=2,742; P=0,000). Dengan kata lain H0 ditolak dan H1 diterima
Multiple Comparisons
Nitrit Tukey HSD
(I) Perlakuan (J) Perlakuan
Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Tanpa Pupuk Kompos -.3555833 .2026637 .221 -.886011 .174844
Urea -14.0107533* .2125555 .000 -14.567071 -13.454436
Kompos Tanpa Pupuk .3555833 .2026637 .221 -.174844 .886011
Urea -13.6551700* .2125555 .000 -14.211487 -13.098853
Urea Tanpa Pupuk 14.0107533* .2125555 .000 13.454436 14.567071
Kompos 13.6551700* .2125555 .000 13.098853 14.211487
*. The mean difference is significant at the 0.05 level.
Dari pengujian Post Hoc menggunakan uji Tukey dapat disimpulkan bahwa: 1. Nilai rata-rata kadar nitrit selada yang ditanam tanpa pemupukan tidak
2. Nilai rata-rata kadar nitrit pada selada yang ditanam tanpa pemupukan mempunyai perbedaan yang signifikan dengan selada yang ditanam dengan menggunakan pupuk urea dengan nilai signifikansi 0,000
Lampiran 37. Pengujian Beda Nilai Rata-Rata Kadar Nitrit Masa Panen H-54
Dari hasil pengujian statistik di atas, terdapat perbedaan yang signifikan dengan probabilitas lebih kecil dari 0,05 antara nilai rata-rata kadar nitrit dari ketiga sampel (F=3,307; P=0,000). Dengan kata lain H0 ditolak dan H1 diterima
Multiple Comparisons
Nitrit Tukey HSD
(I) Perlakuan (J) Perlakuan
Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Tanpa Pupuk Kompos -.9287933* .2658163 .009 -1.624509 -.233078
Urea -18.5237333* .2534459 .000 -19.187072 -17.860394
Kompos Tanpa Pupuk .9287933* .2658163 .009 .233078 1.624509
Urea -17.5949400* .2658163 .000 -18.290656 -16.899224
Urea Tanpa Pupuk 18.5237333* .2534459 .000 17.860394 19.187072
Kompos 17.5949400* .2658163 .000 16.899224 18.290656
*. The mean difference is significant at the 0.05 level.
Dari pengujian Post Hoc menggunakan uji Tukey dapat disimpulkan bahwa:
2. Nilai rata-rata kadar nitrit pada selada yang ditanam tanpa pemupukan mempunyai perbedaan yang signifikan dengan selada yang ditanam dengan menggunakan pupuk urea dengan nilai signifikansi 0,000
Lampiran 38. Pengujian Beda Nilai Rata-Rata Kadar Nitrit Masa Panen H-60
Dari hasil pengujian statistik di atas, terdapat perbedaan yang signifikan dengan probabilitas lebih kecil dari 0,05 antara nilai rata-rata kadar nitrit dari ketiga sampel (F=2,329; P=0,000). Dengan kata lain H0 ditolak dan H1 diterima.
Multiple Comparisons
Nitrit Tukey HSD
(I) Perlakuan (J) Perlakuan
Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Tanpa Pupuk Kompos -4.2128467* .2855972 .000 -4.966948 -3.458745
Urea -19.2484800* .2982965 .000 -20.036113 -18.460847
Kompos Tanpa Pupuk 4.2128467* .2855972 .000 3.458745 4.966948
Urea -15.0356333* .2855972 .000 -15.789735 -14.281532
Urea Tanpa Pupuk 19.2484800* .2982965 .000 18.460847 20.036113
Kompos 15.0356333* .2855972 .000 14.281532 15.789735
*. The mean difference is significant at the 0.05 level.
Dari pengujian Post Hoc menggunakan uji Tukey dapat disimpulkan bahwa: 1. Nilai rata-rata kadar nitrit selada yang ditanam tanpa pemupukan mempunyai
2. Nilai rata-rata kadar nitrit pada selada yang ditanam tanpa pemupukan mempunyai perbedaan yang signifikan dengan selada yang ditanam dengan menggunakan pupuk urea dengan nilai signifikansi 0,000
Lampiran 39. Pengujian Beda Nilai Rata-Rata Kadar Nitrat Masa Panen H-52
Dari hasil pengujian statistik di atas, terdapat perbedaan yang signifikan dengan probabilitas lebih kecil dari 0,05 antara nilai rata-rata kadar nitrit dari ketiga sampel (F=28,983; P=0,000). Dengan kata lain H0 ditolak dan H1 diterima.
Multiple Comparisons
Nitrat Tukey HSD
(I) Perlakuan (J) Perlakuan
Mean
Difference (I-J) Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Tanpa Pupuk Kompos -.9007667 1.6487346E0 .850 -5.215968 3.414434
Urea -10.9851833* 1.6487346E0 .000 -15.300384 -6.669982
Kompos Tanpa Pupuk .9007667 1.6487346E0 .850 -3.414434 5.215968
Urea -10.0844167* 1.5720068E0 .000 -14.198799 -5.970034
Urea Tanpa Pupuk 10.9851833* 1.6487346E0 .000 6.669982 15.300384
Kompos 10.0844167* 1.5720068E0 .000 5.970034 14.198799
*. The mean difference is significant at the 0.05 level.
Dari pengujian Post Hoc menggunakan uji Tukey dapat disimpulkan bahwa: 1. Nilai rata-rata kadar nitrat selada yang ditanam tanpa pemupukan tidak
2. Nilai rata-rata kadar nitrat pada selada yang ditanam tanpa pemupukan mempunyai perbedaan yang signifikan dengan selada yang ditanam dengan menggunakan pupuk urea dengan nilai signifikansi 0,000
Lampiran 40. Pengujian Beda Nilai Rata-Rata Kadar Nitrat Masa Panen H-54
Dari hasil pengujian statistik di atas, terdapat perbedaan yang signifikan dengan probabilitas lebih kecil dari 0,05 antara nilai rata-rata kadar nitrit dari ketiga sampel (F=402,483; P=0,000). Dengan kata lain H0 ditolak dan H1 diterima.
Multiple Comparisons
Nitrat Tukey HSD
(I) Perlakuan (J) Perlakuan
Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Tanpa Pupuk Kompos 1.2869200 .7525136 .239 -.700045 3.273885
Urea -16.7572567* .7204769 .000 -18.659631 -14.854883
Kompos Tanpa Pupuk -1.2869200 .7525136 .239 -3.273885 .700045
Urea -18.0441767* .7204769 .000 -19.946551 -16.141803
Urea Tanpa Pupuk 16.7572567* .7204769 .000 14.854883 18.659631
Kompos 18.0441767* .7204769 .000 16.141803 19.946551
*. The mean difference is significant at the 0.05 level.
Dari pengujian Post Hoc menggunakan uji Tukey dapat disimpulkan bahwa: 1. Nilai rata-rata kadar nitrat selada yang ditanam tanpa pemupukan tidak
2. Nilai rata-rata kadar nitrat pada selada yang ditanam tanpa pemupukan mempunyai perbedaan yang signifikan dengan selada yang ditanam dengan menggunakan pupuk urea dengan nilai signifikansi 0,000
Lampiran 41. Pengujian Beda Nilai Rata-Rata Kadar Nitrat Masa Panen H-60
Dari hasil pengujian statistik di atas, terdapat perbedaan yang signifikan dengan probabilitas lebih kecil dari 0,05 antara nilai rata-rata kadar nitrit dari ketiga sampel (F=129,730; P=0,000). Dengan kata lain H0 ditolak dan H1 diterima.
Multiple Comparisons
Nitrat Tukey HSD
(I) Perlakuan (J) Perlakuan
Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound Tanpa Pupuk Kompos -6.6673200* 1.2365019E0 .000 -9.932226 -3.402414
Urea -18.6578200* 1.1838605E0 .000 -21.783729 -15.531911
Kompos Tanpa Pupuk 6.6673200* 1.2365019E0 .000 3.402414 9.932226
Urea -11.9905000* 1.1838605E0 .000 -15.116409 -8.864591
Urea Tanpa Pupuk 18.6578200* 1.1838605E0 .000 15.531911 21.783729
Kompos 11.9905000* 1.1838605E0 .000 8.864591 15.116409
*. The mean difference is significant at the 0.05 level.
Dari pengujian Post Hoc menggunakan uji Tukey dapat disimpulkan bahwa: 1. Nilai rata-rata kadar nitrat selada yang ditanam tanpa pemupukan mempunyai
2. Nilai rata-rata kadar nitrat pada selada yang ditanam tanpa pemupukan mempunyai perbedaan yang signifikan dengan selada yang ditanam dengan menggunakan pupuk urea dengan nilai signifikansi 0,000
Lampiran 42. Daftar Nilai Distribusi t
Pr 0.25 0.10 0.05 0.025 0.01 0.005 0.001
df 0.50 0.20 0.10 0.050 0.02 0.010 0.002
DAFTAR PUSTAKA
Afzali, S. F., dan Elahi, R. (2014). Measuring Nitrate and Nitrite Concentrations in Vegetables. Journal Application of Scientific Environmental Management. Vol. 18 (3): 451-457.
Damanik, M. M. B., Hasibuan, B. E., Fauzi., Sarifuddin., dan Hanum, Hamidah. (2010). Kesuburan Tanah dan Pemupukan. Medan: USU Press. Hal. 63, 68.
Djamaan, D. (2006). Pemberian Nitrogen (Urea) Terhadap Pertumbuhan dan Hasil Selada (Lactuca sativa). Balai Pengkajian Teknologi Pertanian Sumatera Barat.
Ermer, J., dan McB. Miller, J. H. (2005). Method Validation in Pharmaceutical Analysis. A Guide to Best Practice. Weinheim: Willey – VCH Verlag GmbH & Co. KgaA. Hal. 253.
Gandjar, I. G., dan Rohman, A. (2012). Kimia Farmasi Analisis. Cetakan X. Yogyakarta: Pustaka Pelajar. Hal. 220, 222-223, 240-242, 252-254, 468. Harahap, F. (2012). Fisiologi Tumbuhan Suatu Pengantar. Medan: Unimed Press.
Hal. 148-149.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. Vol. 1 (3): 117-135.
Issac, R.A. (1990). Plants. Dalam: Helrich, K. (1990). Official Methods of Analysis of The Association of Official Analytical Chemists. Edisi XV. Virginia: Association of Official Analytical Chemist, Inc. Hal. 42.
Keeton, J. T. (2011). History of Nitrite and Nitrate in Food. Dalam: Bryan, N. S., and Loscalzo, J. Nitrite and Nitrate in Human Health and Disease.New York: Humana Press. Hal. 77, 79.
Keeton, J. T., Osburn, W. N., Hardin, M. D., dan Bryan, N. S. (2009). A National Survey of Nitrite/ Nitrate Concentration in Cured Meat Products and Non Meat Foods Avalable at Retail. Research Report Human Nutrition. Des Moines: American Meat Institute Foundation. Hal. 9, 22.
Keshavarz, M., Mazloomi, S. M., dan Siavash, B. (2015). The Effect of Home Cooking Method and Refrigeration Processes on The Level of Nitrat and Nitrite in Spinach. J Health Sci Surveillance Sys Vol. 3 (3): 88.
Manuhuttu, A. P., Rehatta, H., dan Kailola, J. J. G. (2014). Pengaruh Konsentrasi Pupuk Hayati Bioboost Terhadap Peningkatan Produksi Tanaman Selada (Lactuca sativa L). Jurnal Ilmu Budidaya Tanaman Agrologia Vol. 3 (1): 19.
Maynard, D. N., Barker,A. V., Minotti,P. L., dan Peck, N. H. (1976). Nitrat Accumulation in Vegetables. Advances in Agronomy. Vol. 28: 71-118.
Munawar, A. (2011). Kesuburan Tanah dan Nutrisi Tanaman. Bogor: IPB Press. Hal. 55, 63-66.
Musnamar, E. I. (2005). Pembuatan dan Aplikasi Pupuk Organik Padat. Jakarta: Penebar Swadaya. Hal. 25.
Narayana, B. and Sunil, K. (2009). A Spectrophotometric Method for The Determination of Nitrite and Nitrate. Euration Journal of Analytical Chemistry: Vol. 4 (2): 206-207.
Pracaya. (2006). Bertanam Sayuran Organik di Kebun, Pot dan Polibag. Jakarta: Penebar Swadaya. Hal. 52-63.
Prasetyo, B. (2013). Farm Bigbook Budidaya Sayuran Organik di Pot. Yogyakarta: Lily Publisher. Hal. 105-112.
Riwidikdo, H. (2008). Statistik Kesehatan. Yogyakarta: Mitra Cendekia Press Yogyakarta. Hal. 131.
Rosmarkam, A., dan Yuwono, N. W. (2006). Ilmu Kesuburan Tanah. Yogyakarta: Penerbit Kanisius. Hal. 168.
Samadi, B. (2014). Rahasia Budidaya Selada. Jakarta: Pustaka Mina. Hal. 17. Silalahi, J. (2005). Masalah Nitrit dan Nitrat dalam Makanan. Medika Jurnal
Kedokteran Indonesia. Vol. 31 (5): 460.
Sudjana. (2005). Metode Statistik. Edisi Keenam. Bandung: Penerbit Tarsito. Hal. 93 dan 201.
Sutedjo, M. M. (2002). Pupuk dan Cara Pemupukan. Jakarta: Rineka Cipta. Hal. 10, 92 dan 93.
Walters, C. L. (2000). Nitrate and Nitrite in Foods. Dalam: Hill, M. J. Nitrates and Nitrites in Food and Water in Relation to Human Desease. Cambridge England: Woodhead Publishing Limited. Hal. 94-97.
Watson, D. G. (2005). Pharmaceutical Analysis: A Textbook for Pharmacy Students and Pharmaceutical Chemists. 2 Edition. Penerjemah: Syarief, W. R. (2007). Analisis Farmasi: Buku Ajar Untuk Mahasiswa Farmasi dan Praktisi Kimia Farmasi. Edisi Kedua. Jakarta: EGC. Hal. 107.
BAB III
METODE PENELITIAN
3.1 Lokasi dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan Februari 2016 sampai Mei 2016
3.2 Jenis Penelitian
Jenis penelitian ini adalah penelitian eksperimental yang bertujuan untuk mengetahui pengaruh pemberian pupuk organik dan pupuk kimia terhadap kadar nitrat dan nitrit pada selada (Lactuca sativa L.).
3.3 Sampel
Sampel pada penelitian ini adalah sayur selada yang ditanam di Fakultas Pertanian Universitas Sumatera Utara yaitu tiga jenis sampel sayur selada yang ditanam di dalam polibag tanpa menggunakan pupuk, menggunakan pupuk organik dan selada yang ditanam dengan menggunakan pupuk kimia.
3.4 Alat dan Bahan 3.4.1 Alat
termometer, tabung reaksi, batang pengaduk, lumpang dan alu serta alat-alat gelas sesuai dengan kebutuhan.
3.4.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini bersifat pro analisis yaitu natrium nitrit, natrium nitrat, asam sulfanilat, N-(1-naftil) etilendiamin dihidroklorida, asam asetat glasial, asam klorida pekat, ferro sulfat, asam sulfat pekat dan yang tidak bersifat pro analisis yaitu air suling dan serbuk Zn.
3.5 Penanaman Selada dengan Variasi Pemupukan 1. Penyemaian benih
Benih direndam dalam air hangat (50oC) selama satu malam kemudian dikeringkan. Benih disebar merata pada tempat penyemaian dengan media tanah humus.
2. Penanaman
Setelah berumur 3-4 minggu, selada siap untuk dipindahkan ke polibag. Siapkan polibag dengan tiga jenis perlakuan:
− Tanpa pemupukan: tanah humus dan pasir (1:1)
− Pupuk organik: tanah humus dan pasir (1:1), 3 hari sebelum tanam ditambahkan pupuk kompos sebanyak 300 gram per polibag
− Pupuk urea: tanah humus dan pasir (1:1), 3 hari sebelum tanam ditambahkan pupuk urea sebanyak 0,3 gram per polibag (Djamaan) 3. Penyiraman dilakukan agar kondisi tanah tetap terjaga kelembabannya.
penyiraman dua kali sehari pada pagi dan sore hari. Siram menggunakan air bersih yang bebas dari zat-zat kimia berbahaya.
4. Pemupukan susulan dilakukan setiap dua minggu sekali
5. Pemanenan dapat dilakukan setelah selada berumur 2-2,5 bulan.
3.6 Pembuatan Larutan Pereaksi 1. Larutan asam asetat 15% (v/v)
Encerkan 75 mL asam asetat glasial dengan air suling dalam labu tentukur 500 mL
2. Larutan N-(1-naftil) etilendiamin dihidroklorida
Larutkan 0,350 g N-(1-naftil) etilendiamin dihidroklorida di dalam 250 mL asam asetat 15% (v/v), disaring dengan kertas saring kemudian disimpan di dalam botol berwarna coklat.
3. Larutan ferro sulfat
Larutkan 2,8 gram ferro sulfat dalam air yang baru dididihkan dan telah dingin. Larutan ferro sulfat harus dibuat baru.
4. Larutan induk baku nitrit
3.7 Identifikasi Nitrit
Identifikasi nitrit dilakukan dengan cara masukkan sebagian sampel yang telah dihaluskan ke dalam beaker glass, ditambahkan air suling secukupnya, dipanaskan di atas penangas air selama beberapa saat sambil diaduk kemudian didinginkan pada suhu kamar dan disaring. Lalu masukkan sejumlah filtrat ke dalam tabung reaksi, kemudian tambahkan beberapa tetes asam sulfanilat dan larutan NED. Dibiarkan selama beberapa menit, warna ungu merah menunjukkan adanya nitrit (Vogel, 1979).
3.8 Identifikasi Nitrat
Identifikasi nitrat dilakukan dengan cara masukkan sebagian sampel yang telah dihaluskan ke dalam beaker glass, ditambahkan air suling secukupnya, dipanaskan di atas penangas air selama beberapa saat sambil diaduk kemudian didinginkan pada suhu kamar dan disaring. Lalu masukkan sejumlah filtrat ke dalam tabung reaksi, tambahkan beberapa tetes larutan ferro sulfat yang baru dibuat kemudian tambahkan beberapa tetes asam sulfat pekat secara perlahan-lahan melalui dinding tabung sehingga asam ini membentuk suatu lapisan di sebelah bawah campuran tersebut. Sebuah cincin coklat akan terbentuk pada tempat di mana kedua cairan bertemu (Vogel, 1979).
3.9 Penetapan Kadar Nitrat dan Nitrit
3.9.1 Penentuan Panjang Gelombang Nitrit Baku
pereaksi N-(1-naftil) etilendiamin dihidroklorida dan dicukupkan dengan air suling sampai garis tanda kemudian dihomogenkan, diukur serapan pada panjang gelombang 400-800 nm dengan blanko air suling (C = 0,8 µg/mL).
3.9.2 Penentuan Waktu Operasional Nitrit Baku
Masukkan 4 mL LIB II ke dalam labu tentukur 50 mL, ditambahkan 2,5 mL pereaksi asam sulfanilat dan dikocok selama 5 menit, ditambahkan 2,5 mL pereaksi N-(1-naftil) etilendiamin dihidroklorida dan dicukupkan dengan air suling sampai garis tanda kemudian dihomogenkan, diukur serapan pada panjang gelombang 540 nm setiap menit selama 60 menit dengan blanko air suling (C = 0,8 µg/mL).
3.9.3 Pembuatan Kurva Kalibrasi Nitrit Baku
Dari LIB II (C = 10 µg/mL), dipipet masing-masing sebanyak 0,5 mL; 1 mL; 2 mL; 3 mL; 4 mL dan 5 mL (0,1 µg/mL; 0,2 µg/mL; 0,4 µg/mL; 0,6 µg/mL; 0,8 µg/mL; 1,0 µg/mL). Masing-masing dimasukkan ke dalam labu tentukur 50 mL, kemudian ditambahkan 2,5 mL pereaksi asam sulfanilat dan dikocok selama 5 menit. Tambahkan 2,5 mL pereaksi N-(1-naftil) etilendiamin dihidroklorida dan dicukupkan dengan air suling sampai garis tanda kemudian homogenkan. Diukur serapan pada menit ke-21 pada panjang gelombang 540 nm.
3.9.4 Penentuan Kadar Nitrit dalam Sayur Selada
tanda, dihomogenkan kemudian disaring, 10 mL filtrat pertama dibuang. Dipipet sebanyak 10 mL filtrat, dimasukkan ke dalam labu tentukur 50 mL, ditambahkan 2,5 mL pereaksi asam sulfanilat kemudian dikocok selama 5 menit. Tambahkan 2,5 mL pereaksi N-(1-naftil) etilendiamin dihidroklorida dan dicukupkan dengan air suling sampai garis tanda dan dihomogenkan (Isaac, 1990). Kemudian diukur serapan pada menit ke-21. Konsentrasi nitrit dalam sampel dapat dihitung dengan persamaan regresi Y = aX+b.
Menurut Issac (1990), kadar nitrit dapat dihitung dengan rumus: Kadar (µg/g) = ������
����� ������ (�)
Keterangan: Y = Absorban
X = konsentrasi nitrit dalam larutan sampel (µg/mL) V = volume larutan sampel sebelum pengenceran (mL) Fp = faktor pengenceran
3.9.5 Penentuan Kadar Nitrat dalam Sayur Selada
pereaksi N-(1-naftil) etilendiamin dihidroklorida dan dicukupkan dengan air suling sampai garis tanda dan dihomogenkan (Isaac, 1990). Kemudian diukur serapan pada menit ke-21.. Konsentrasi nitrit dalam sampel dapat dihitung dengan persamaan regresi Y = aX+b.
Menurut Issac (1990), kadar nitrit dapat dihitung dengan rumus: Kadar (µg/g) = ������
����� ������ (�)
Keterangan: Y = Absorban
X = konsentrasi nitrit dalam larutan sampel (µg/ mL) V = volume larutan sampel sebelum pengenceran (mL) Fp = faktor pengenceran
Kadar nitrit dari reduksi nitrat diperoleh melalui pengurangan kadar total nitrit setelah reduksi dengan kadar nitrit sebelum reduksi.
Karena hasil pembacaan alat spektrofotometer untuk nitrat adalah sebagai nitrit, maka hasil pembacaan harus dikonversikan. Sehingga diperoleh:
Kadar nitrat = kadar nitrit dari hasil reduksi x ��������
��������
3.10 Uji Validasi Metode Analisis 3.10.1 Uji Perolehan Kembali
Uji perolehan kembali nitrit dan nitrat dapat dilakukan dengan menambahkan larutan baku ke dalam sampel kemudian dianalisis dengan perlakuan yang sama pada sampel. Larutan baku nitrit yang ditambahkan sebanyak 10 mL dengan konsentrasi 10 µg/mL dan untuk nitrat sebanyak 2 mL dengan konsentrasi 100 µg/mL.
% perolehan kembali = ��−��
�∗� x 100 %
Keterangan:
CF = konsentrasi analit dalam sampel setelah penambahan baku
CA = konsentrasi analit dalam sampel sebelum penambahan baku
C*A = konsentrasi bahan baku yang ditambahkan ke dalam sampel 3.10.2 Uji Presisi
Berdasarkan hasil perolehan kembali nitrit dan nitrat ditentukan standar deviasi nitrit dan nitrat. Menurut Sudjana (2005), untuk menghitung standar deviasi (SD) digunakan rumus:
SD = �∑(�−����)2
Berdasarkan nilai standar deviasi yang didapat, dihitung simpangan baku relatif nitrit dan nitrat. Simpangan baku relatif dapat dihitung dengan rumus:
RSD = ��
�̅ x 100%
Keterangan:
�̅ = rata-rata kadar zat yang terkandung dalam sampel SD = standar deviasi
RSD = Relatif Standard Deviation, Simpangan Baku Relatif 3.10.3 Penentuan Batas Deteksi dan Batas Kuantitasi
ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan (Gandjar dan Rohman, 2012).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku (����) = �∑(�−��)2
(�−2)
Batas deteksi (LOD) = 3 ���/�
�����
Batas kuantitasi (LOQ) = 10 ���/�
�����
3.10.4 Analisis Data Secara Statistik
Kadar yang telah diperoleh dari hasil perhitungan selanjutnya dianalisis apakah data tersebut ditolak atau diterima dengan menggunakan metode t hitung.
Menurut Sudjana (2005), penyimpangan dari hasil yang diperoleh dapat diketahui dengan menggunakan uji distribusi t sebagai berikut:
t hitung =
�
�−�̅��/ √�
�
dengan dasar penolakan apabila t hitung ≥ t tabel. Untuk mencari kadar sebenarnya
dengan %, α ½, dk, dk = n-1, dapat digunakan rumus:
µ = �̅± (t (α ½, dk) x SD/ √�)
keterangan:
µ : kadar sebenarnya
�̅ : rata-rata kadar analit dalam sampel SD : standar deviasi
α : tingkat kepercayaan
n : jumlah pengulangan 3.11 Pengujian Beda Nilai Rata-Rata
Pengujian beda nilai rata-rata dilakukan dengan metode One Way ANOVA menggunakan perangkat lunak SPSS (Statistical Package for The Social Sciences) versi 16 dengan taraf kepercayaan 99% untuk mengetahui apakah variasi ketiga sampel sama atau berbeda.
H0 : tidak terdapat perbedaan yang signifikan antara nilai rata-rata kadar
nitrat dan nitrit pada ketiga sampel
H1 : tidak terdapat perbedaan yang signifikan antara nilai rata-rata kadar
nitrat dan nitrit pada ketiga sampel
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Medanesse, Medan, menunjukkan bahwa tumbuhan yang diteliti adalah Lactuca sativa L., famili asteraceae. Hasil Identifikasi dapat dilihat pada Lampiran 1 halaman 50.
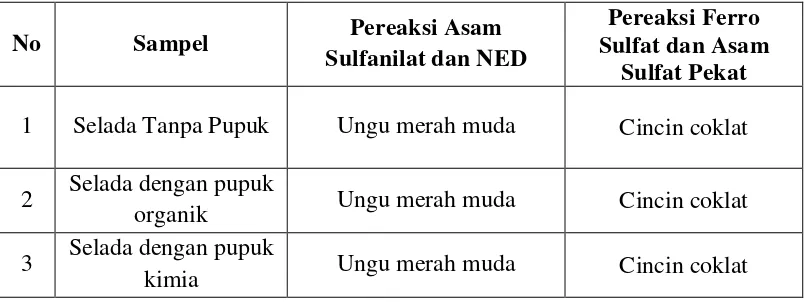
4.2 Identifikasi Nitrit dan Nitrat dalam Sayur Selada
Identifikasi nitrit yang telah dilakukan dengan menggunakan pereaksi asam sulfanilat dan NED menunjukkan bahwa semua sampel mengandung nitrit. Identifikasi nitrat yang dilakukan dengan pereaksi ferro sulfat dan asam sulfat pekat juga menunjukkan semua sampel mengandung nitrat dengan terbentuknya cincin coklat. Hasil uji kualitatif nitrit dan nitrat yang terkandung dalam selada dapat dilihat pada Tabel 4.1dan Gambar hasil identifikasi nitrat dapat dilihat pada Lampiran 4 halaman 53.
Tabel 4.1 Identifikasi Nitrit dan Nitrat dalam Sayur Selada
No Sampel Pereaksi Asam
Sulfanilat dan NED
Pereaksi Ferro Sulfat dan Asam
Sulfat Pekat 1 Selada Tanpa Pupuk Ungu merah muda Cincin coklat
2 Selada dengan pupuk
organik Ungu merah muda Cincin coklat 3 Selada dengan pupuk
4.3 Kurva Serapan Nitrit
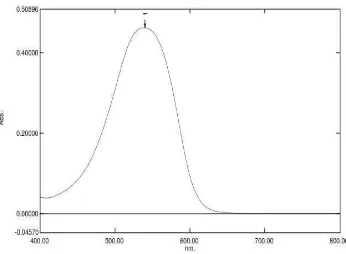
Pengukuran serapan maksimum nitrit dilakukan menggunakan konsentrasi 0,8 µg/mL pada panjang gelombang 400-800 nm dan diperoleh kurva serapan nitrit pada Gambar 4.1.
Gambar 4.1 Kurva Serapan Nitrit pada Konsentrasi 0,8 µg/mL
Berdasarkan penentuan kurva serapan maksimum, serapan nitrit berada pada panjang gelombang 540 nm. Kurva serapan selanjutnya digunakan untuk penentuan waktu kerja dan penentuan kadar nitrit dan nitrat dalam sampel.
4.4 Waktu Operasional
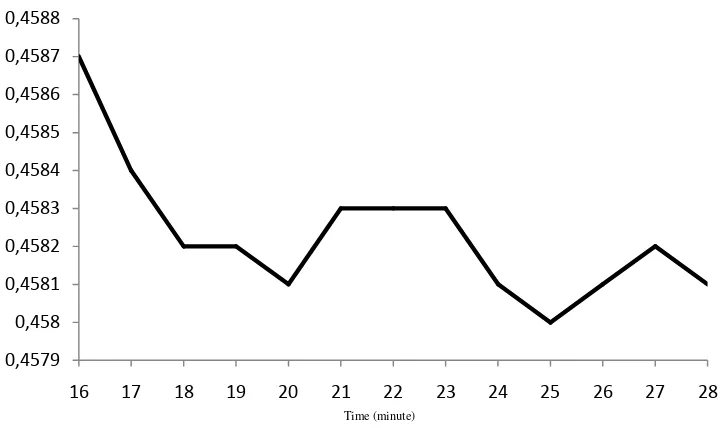
halaman 58 sedangkan kurva waktu operasional nitrit dapat dilihat pada Gambar 4.2.
Gambar 4.2 Waktu Operasional Nitrit Baku
Berdasarkan Gambar 4.2, diperoleh waktu operasional yang paling stabil adalah pada menit ke-21 sampai menit ke-23. Waktu operasional ini selanjutnya digunakan untuk penentuan kadar nitrit dan nitrat pada sampel.
4.5 Linieritas Kurva Kalibrasi
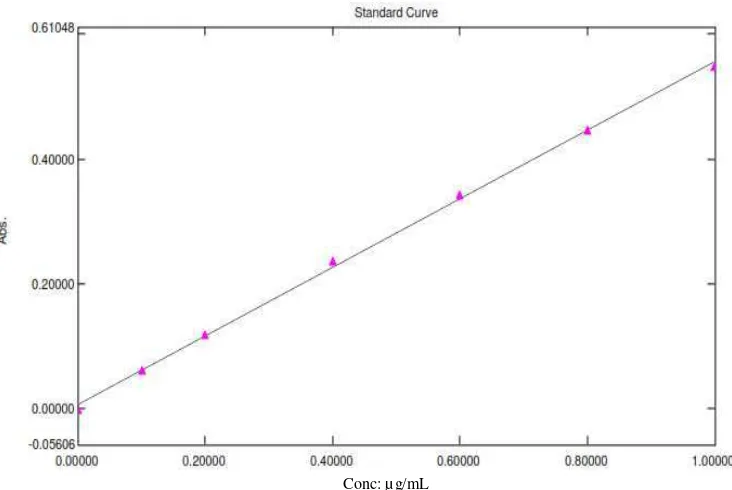
Kurva kalibrasi merupakan suatu hubungan antara konsentrasi dengan absorbansi yang berupa garis lurus apabila memenuhi hukum Lambert-Beer. Pembuatan kurva kalibrasi dilakukan dengan konsentrasi 0,1 µg/mL; 0,2 µg/mL; 0,4 µg/mL; 0,6 µg/mL; 0,8 µg/mL; 1,0 µg/mL dan diperoleh hasil sebagai berikut:
0,4579 0,458 0,4581 0,4582 0,4583 0,4584 0,4585 0,4586 0,4587 0,4588
Gambar 4.3 Kurva Kalibrasi Nitrit Baku
Dari Gambar 4.3 diperoleh hubungan yang linier antara konsentrasi dengan absorbansi. Persamaan garis regresi yang diperoleh yaitu Y = 0,54794X + 0,00754 dengan koefisien korelasi sebesar 0,99953 yang menunjukkan adanya hubungan yang linier antara absorbansi dan konsentrasi.
4.6 Batas Deteksi dan Batas Kuantitasi
Dari hasil perhitungan diperoleh batas deteksi nitrat dan nitrit adalah sebesar 0,037718 µg/g sedangkan batas kuantitasi sebesar 0,125725 µg/g. Perhitungan tersebut dapat dilihat pada Lampiran 10 halaman 62.
Batas deteksi didefinisikan sebagai jumlah terkecil analit di dalam sampel yang dapat dideteksi yang masih membetikan respon signifikan dibandingkan dengan blanko. Batas deteksi merupakan parameter uji batas. Batas kuantitasi merupakan parameter pada analisis renik dan diartikan sebagai kuantitas terkecil
analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
4.7 Pengaruh Pupuk Organik dan Pupuk Kimia Terhadap Kadar Nitrat dan Nitrit dalam Sayur Selada
Tanaman selada yang digunakan sebagai sampel pada penelitian ini ditanam dengan tiga perlakuan yang berbeda. Perlakuan pertama tanpa menggunakan pupuk, perlakuan kedua menggunakan pupuk organik berupa pupuk kompos dan perlakuan ketiga menggunakan pupuk kimia yaitu pupuk urea. Sampel kemudian diukur pada panjang gelombang 540 nm. Pengaruh pemberian pupuk organik dan pupuk kimia terhadap kadar nitrat dan nitrit pada tanaman selada dapat dilihat pada Tabel 4.2, Tabel 4.3, Gambar 4.4, Gambar 4.5 dan Gambar 4.6.
Tabel 4.2 Pengaruh Pupuk Organik dan Pupuk Kimia Terhadap Kadar Nitrit pada Selada
No. Sampel Kadar Nitrit (µg/g)
H-52 H-54 H-60
1 Tanpa Pupuk 22,6209 ± 0,2503 23,1304 ± 0,2809* 23,7401 ± 0,5029* 2 Pupuk Organik 22,9765 ± 0,8626 24,0591 ± 0,3378* 27,9530 ± 0,5590* 3 Pupuk Kimia 36,6316 ± 0,5006* 41,6541 ± 1,1510* 42,9886 ± 1,4836*
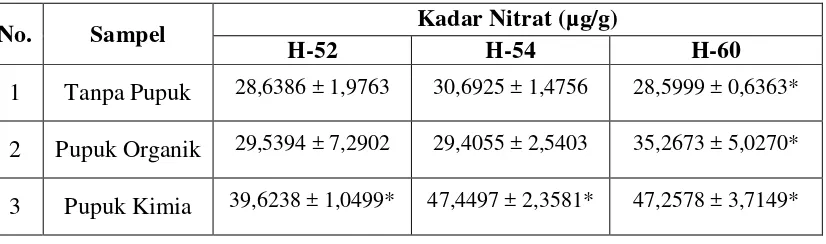
Tabel 4.3 Pengaruh Pupuk Organik dan Pupuk Kimia Terhadap Kadar Nitrat pada Selada
No. Sampel Kadar Nitrat (µg/g)
H-52 H-54 H-60
Keterangan:
H-52 : Panen hari ke-52 H-54 : Panen hari ke-54 H-60 : Panen hari ke-60
* : Berbeda signifikan (α = 0,05)
Hasil merupakan rata-rata ± standar deviasi dari 6 kali pengulangan
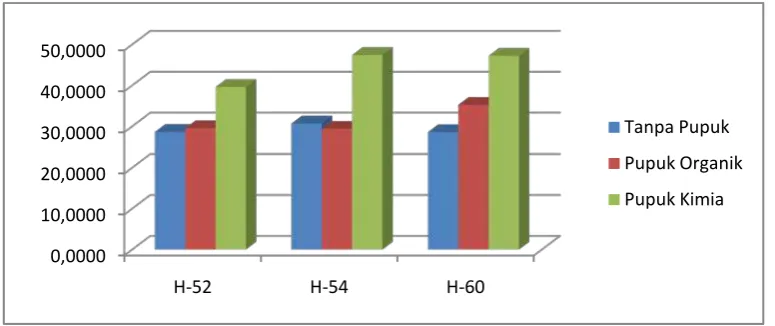
Gambar 4.4 Pengaruh Pemupukan Terhadap Kadar Nitrit pada Selada
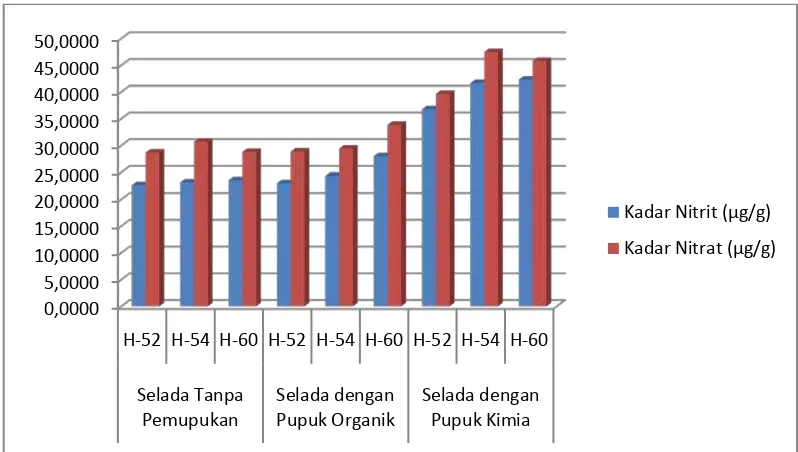
Gambar 4.6 Perbandingan Kadar Nitrit dan Nitrat pada Selada
Dari Gambar 4.4 dan Gambar 4.5 dapat dilihat adanya perbedaan kadar nitrit dan nitrat antara sampel sayur selada yang ditanam tanpa menggunakan pupuk, dengan pupuk organik dan sayur selada yang ditanam dengan menggunakan pupuk kimia. Kandungan nitrit paling tinggi terkandung dalam sayur selada yang ditanam dengan menggunakan pupuk kimia, sebesar 42,9886 µg/g pada masa panen hari ke-60. Sedangkan kandungan nitrit terendah terdapat pada sayur selada yang ditanam tanpa pemupukan, yaitu sebesar 22,6209 µg/g pada masa panen hari ke-52.
Demikian juga kadar nitrat tertinggi terkandung dalam sayur selada yang ditanam dengan menggunakan pupuk kimia yaitu sebesar 47,4497 µg/g untuk masa panen hari ke-54. Sedangkan kadar nitrat terendah terkandung dalam sayur selada yang ditanam tanpa pemupukan, yaitu sebesar 28,5999 µg/g untuk masa panen hari ke-60.
Dari data di atas dapat disimpulkan bahwa kadar nitrit dan nitrat yang terkandung dalam sayur selada yang ditanam dengan menggunakan pupuk kimia
0,0000
H-52 H-54 H-60 H-52 H-54 H-60 H-52 H-54 H-60
lebih tinggi dibandingkan dengan sayur selada tanpa pemupukan maupun sayur selada dengan pupuk organik. Pada penelitian ini, terlihat bahwa penyebab perbedaan kadar nitrit dan nitrat yang terkandung di dalam sayur selada ialah jenis dan jumlah pupuk yang digunakan. Untuk pupuk organik, digunakan pupuk kompos sebanyak 300 g/polibag sementara pupuk kimia menggunakan pupuk urea sebanyak 0,3g/polibag. Jenis pupuk yang berbeda tentu saja memiliki kandungan unsur hara yang berbeda yang dapat mempengaruhi kondisi kesuburan tanah. Tanah mineral dengan kandungan bahan organik yang tinggi mempunyai sifat fisik, sifat kimia dan sifat biologi tanah yang lebih baik untuk mendukung pertumbuhan tanaman yang baik dan produksi yang tinggi. Sebaliknya, bila kandungan bahan organik tanah sedikit, maka sifat fisik, kimia dan biologi tanah juga kurang baik sehingga produktivitas rendah (Manuhuttu, dkk., 2014). Selain itu, seperti yang dikemukakan oleh Maynard, dkk. (1976), komponen lingkungan juga mempengaruhi penyerapan nitrat oleh tanaman, asimilasi nitrat atau pertumbuhan tanaman yang dapat mempengaruhi fluktuasi konsentrasi nitrat pada seluruh bagian tanaman.
panen, konsentrasi karbondioksida serta penggunaan pupuk (Maynard, dkk., 1978).
Pada setiap masa panen, kandungan nitrit yang terkandung dalam selada untuk setiap perlakuan mengalami peningkatan, demikian juga dengan kandungan nitrat. Hal ini menunjukkan bahwa selada lebih baik dipanen pada usia yang masih muda, dikarenakan kandungan nitrit dan nitratnya yang relatif rendah. Di samping itu, pada umumnya selada dipanen pada umur 60-80 hari, tetapi di umur kurang dari 60 hari selada sudah layak dikonsumsi karena lebih dari separuh berat segar tanaman dicapai pada umur dua minggu menjelang panen (Zulkarnain, 2013).
Sebagian besar tumbuhan mengandung 1-25% nitrogen dari berat keringnya. Nitrogen dalam tumbuhan terdapat dalam bentuk antara lain asam amino, protein, amida, klorofil, alkaloida dan basa nitrogen. Tumbuhan menyerap nitrogen dalam bentuk tertentu dari dalam tanah, yaitu nitrat, amonia, nitrogen organik dan molekul nitrogen (Harahap, 2012). Lebih dari 90% nitrogen diserap oleh tanaman dalam bentuk nitrat. Kandungan nitrat di dalam tanaman dipengaruhi oleh jumlah nitrat yang tersedia di dalam tanah dan faktor genetik yang mengontrol pola metabolisme nitrat di dalam tanaman. Penggunaan pupuk juga dapat meningkatkan kapabilitas tanaman untuk mengakumulasikan nitrat (Walters, 2000).
dengan memodifikasi kondisi pertumbuhan seperti sumber air, kondisi tanah, waktu panen serta jumlah, jenis dan waktu pemupukan (Keeton, dkk., 2011). 4.8 Uji Validasi
Pada penelitian ini, parameter validasi yang diuji adalah akurasi (kecermatan) dan presisi (keseksamaan). Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Sedangkan keseksamaan diukur sebagai simpangan baku relatif (Harmita, 2004).
Persen perolehan kembali dilakukan dengan metode penambahan baku, setelah sampel dianalisis lalu sejumlah tertentu larutan baku ditambahkan ke dalam sampel dicampur kemudian dianalisis kembali. Selisih kedua hasil dibandingkan dengan kadar sebenarnya. Persen perolehan kembali kadar nitrit dan nitrat di dalam sampel dengan metode penambahan baku dapat dilihat pada Tabel 4.4 dan Tabel 4.5
Tabel 4.4 Persen Uji Perolehan Kembali Kadar Nitrit pada Selada Sampel Kadar Nitrit (µg/g) Kadar Baku yang
Tabel 4.5 Persen Uji Perolehan Kembali Kadar Nitrat dalam Sayur Selada Sampel Kadar Nitrit (µg/g) Kadar Baku yang
Ditambahkan
Berdasarkan tabel di atas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali kadar nitrit sebesar 101,35 % dan kadar nitrat sebesar 93,29 %. Perhitungan hasil uji perolehan kembali kadar nitrit dan nitrat dapat dilihat pada Lampiran 32 dan 33 halaman 94 dan 95. Persen perolehan kembali untuk kadar nitrit dan nitrat memenuhi syarat akurasi yang telah ditetapkan, yaitu pada rentang 80-120% (Ermer dan McB. Miller, 2005).
4.9 Pengujian Beda Nilai Rata-Rata Kadar Nitrat dan Nitrit di dalam Sampel Pengujian beda nilai rata-rata kadar nitrat dan nitrit di dalam sampel selada bertujuan untuk melihat apakah terdapat perbedaan yang signifikan pada rata-rata kadar nitrat dan nitrit antara ketiga sampel. Dilakukan pengujian One Way ANOVA dengan taraf kepercayaan 99% untuk mengetahui apakah variasi ketiga sampel sama (H0 = H1) atau berbeda (H0≠ H1).
H0 : tidak terdapat perbedaan yang signifikan antara nilai rata-rata kadar nitrat
dan nitrit pada ketiga sampel.
H1 : terdapat perbedaan yang signifikan antara nilai rata-rata kadar nitrat dan
nitrit pada ketiga sampel.
Dari hasil analisis statistik yang dilanjutkan dengan uji Tukey terhadap kadar nitrit, terdapat perbedaan yang signifikan antara nilai rata-rata nitrit pada ketiga sampel untuk masa panen hari ke-54 dan ke-60, sedangkan pada hari ke-52 hanya selada yang ditanam dengan pupuk urea yang memiliki perbedaan signifikan diantara ketiga sampel.
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
1. Pemupukan memberikan pengaruh terhadap kadar nitrat dan nitrit yang terkandung di dalam selada, selada yang ditanam dengan pupuk kimia memiliki kadar nitrat dan nitrit yang paling tinggi dibandingkan dengan selada yang ditanam dengan pupuk organik dan tanpa pemupukan.
2. Kadar nitrit dalam sayur selada untuk masa panen hari ke-52, hari ke-54 dan hari ke-60 untuk selada yang ditanam tanpa pemupukan adalah 22,6209 µg/g; 23,1304 µg/g dan 23,7401 µg/g; selada yang ditanam dengan pupuk organik 22,9765 µg/g; 24,0591 µg/g dan 27, 9530 µg/g; selada yang ditanam dengan pupuk kimia 36,6316 µg/g; 41,6541 µg/g dan 42,9886 µg/g. Kadar nitrat pada selada yang ditanam tanpa pemupukan 28,6386 µg/g; 30,6925 µg/g dan 28,5999 µg/g; selada yang ditanam dengan pupuk organik 29,5394 µg/g; 29,4055 µg/g dan 35,2673 µg/g sedangkan selada yang ditanam dengan pupuk kimia 39,6238 µg/g; 47,4497 µg/g dan 47,2578 µg/g.
5.2Saran
1. Disarankan kepada masyarakat agar mengkonsumsi sayuran yang dipanen pada usia yang masih muda dan ditanam secara organik atau tanpa pemupukan.
`BAB II
TINJAUAN PUSTAKA 2.1 Tanaman Selada (Lactuca sativa L.)
Lactuca sativa adalah satu-satunya genus Lactuca, yang didomestikasi dan
dibudidayakan sebagai tanaman sayuran. Selada diperkirakan berasal dari daerah sekitar Laut Mediterania, yang meliputi Asia Kecil, Transcaucasia, Iran dan Turkistan. Pertama kali, selada dibudidayakan untuk dimanfaatkan sebagai tanaman obat-obatan, seperti obat tidur, dan mulai pada tahun 4.500 SM tanaman ini dimanfaatkan sebagai makanan (Zulkarnain, 2013).
2.1.1 Klasifikasi Selada
Di dalam sistematika botani, tanaman selada menempati kedudukan sebagai berikut (Samadi, 2014):
Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledoneae
Ordo : Asterales
Famili : Asteraceae
Genus : Lactuca
Menurut Pracaya (2006), tanaman selada mempunyai empat varietas sebagai berikut:
a. Selada Kepala (Lactuca sativa var. capitata L.)
Selada yang disebut juga selada kol ini mempunyai daun yang kompak seperti kepala atau kol, hanya lebih kecil dan kurang keras. Daunnya lebar hampir buat, halus dan lembut. Umumnya selada ini hanya membentuk kepala bila ditanam di dataran tinggi.
b. Selada Silindris (Lactuca sativa var. longifolia Lam.)
Selada ini disebut juga selada kerucut, selada romain dan selada cos. Selada ini membentuk krop yang bentuknya silinder atau kerucut. Daunnya memanjang, ujungnya lengkung, tekstur keras, kaku dan agak kasar.
c. Selada daun atau selada keriting (Lactuca sativa var. crispa L.)
Tanaman ini membentuk roset yang longgar (tidak membentuk krop), daunnya menyerupai tekstur selada kepala dengan tepi berumbia.
d. Selada Batang (Lactuca sativa var. asparagina Bailey, sin. L. sativa var. Angustana Irish)
Selada ini mempunyai batang yang berdaging tebal sehingga dapat dikonsumsi. Adapun daunnya tidak dikonsumsi karena kasar dan tidak enak.
2.1.2 Nilai Gizi dan Manfaat Selada
Selada merupakan salah satu tanaman sayuran rendah kalori dan sumber antioksidan serta vitamin K. Selain itu, selada juga memiliki kandungan vitamin A dan C yang tinggi (Zulkarnain, 2013).
yaitu senyawa yang bila dikonsumsi menimbulkan rasa kantuk menyerupai reaksi tubuh setelah mengkonsumsi opium. Oleh karena itu, pada masa lalu, penduduk Romawi dan Mesir memanfaatkan selada sebagai makanan penutup untuk merangsang timbulnya rasa kantuk. Komposisi kimiawi yang terkandung dalam 100 gram tanaman selada dapat dilihat pada Tabel 2.1 (Zulkarnain, 2013).
Tabel 2.1 Komposisi Kimiawi per 100 g Tanaman Selada
Senyawa Kadar Nutrisi Persen dari Kebutuhan Harian
Energi (kalori) 15,00 1,00
Karbohidrat (g) 2,79 2,00
Protein (g) 1,36 2,00
Lemak Total (g) 0,15 0,50
Serat (g) 1,30 3,00
Folat (mikrogram) 38,00 9,50
Vitamin A (IU) 7.405,00 247,00
Vitamin C (mg) 9,20 15,00
Natrium (mg) 28,00 2,00
Kalium (mg) 194,00 4,00
Kalsium (mg) 36,00 3,50
Magnesium (mg) 13,00 3,00
Besi (mg) 0,86 10,00
Fosfor (mg) 29,00 4,00
2.1.3 Syarat Tumbuh Tanaman Selada
Beberapa daerah di Indonesia cocok untuk daerah penanaman selada karena kondisi lingkungannya. Menurut Pracaya (2006), kondisi lingkungan yang berperan dalam pertumbuhan selada yaitu:
a. Iklim
Daerah yang cocok untuk penanaman selada sekitar ketinggian 500-2000 mdpl dan suhu rata-rata 15-20o C. Di dataran rendah, tanaman selada juga bisa tumbuh tetapi krop yang terbentuk kurang baik. Tanaman selada tidak tahan bila terlalu banyak hujan, kelembaban terlalu tinggi dan tergenang air. Dalam kondisi seperti itu tanaman selada akan mudah terserang penyakit. Waktu tanam ang paling cocok pada wkatu musim kemarau dengan penyiraman yang cukup. Selada memerlukan sinar matahari yang cukup dan tempat yang terbuka (Pracaya, 2006).
b. Tanah
Tanaman selada dapat ditanam pada berbagai macam tanah. Namun, pertumbuhan yang baik akan diperoleh bila ditanam pada tanah liat berpasir yang cukup mengandung bahan organik, gembur, remah dan tidak mudah tergenang air (Pracaya, 2006).
2.1.4 Pemeliharaan
a. Pemupukan Susulan
Pemupukan susulan penting untuk dilakukan karena kandungan hara di alam tanah semakin berkurang karena diserap tanaman dan gulma. Pemupukan susulan dilakukan pada saat benih berumur dua minggu. Setelah pemupukan susulan pertama maka pemupukan susulan berikutnya setiap dua minggu sekali (Prasetio, 2013).
b. Penyiraman
Penyiraman dilakukan agar kondisi tanah tetap terjaga kelembabannya. Pada musim hujan, penyiraman dilakukan sekali sehari pada pagi atau sore hari. Pada musim kemarau, lakukan penyiraman dua kali sehari pada pagi dan sore hari. Siram dengan menggunakan air bersih yang bebas dari zat-zat berbahaya (Prasetio, 2013).
c. Penyulaman
Penyulaman perlu dilakukan jika benih lambat tumbuh atau terserang penyakit hingga mati. Penyulaman sebaiknya dilakukan dua minggu setelah tanam (Prasetio, 2013).
d. Penyiangan
2.2 Pemupukan
Pupuk merupakan kunci dari esuburan tanah karena berisi satu atau lebih unsur untuk menggantikan unsur yang habis terisap tanaman (Lingga dan Marsono, 2001). Pemupukan merupakan pemberian atau penambahan bahan-bahan/ zat-zat kepada kompleks tanah – tanaman untuk memperlengkapi keadaan makanan/unsur hara dalam tanah yang tidak cukup terkandung di dalamnya (Sutedjo, 2002).
Menurut Lingga dan Marsono (2001), secara umum pupuk hanya dibagi dalam dua kelompok berdasarkan asalnya, yaitu:
1. Pupuk anorganik seperti urea (pupuk N), TSP atau SP-36 (pupuk P), KCl (pupuk K).
2. Pupuk organik seperti pupuk kandang, kompos, humus dan pupuk hijau.
Pupuk anorganik atau pupuk buatan yang merupakan hasil industri atau hasil dari pabrik-pabrik pembuat pupuk yang mengandung unsur-unsur hara atau zat-zat makanan yang diperlukan tanaman. Sedangkan pupuk organik atau pupuk alam merupakan hasil-hasil akhir dari perubahan atau peruraian bagian-bagian atau sisa-sisa tanaman dan binatang (Sutedjo, 2002).
2.2.1 Pupuk Kompos
Kandungan utama dengan kadar tertinggi dari kompos adalah bahan organik dan terkenal manjur untuk memperbaiki kondisi tanah. Unsur lain dalam kompos yang variasinya cukup banyak walaupun kadarnya rendah adalah nitrogen, fosfor, kalium, kalsium dan magnesium. Kadar hara kompos memang sangat ditentukan oleh bahan yang dikomposkan, cara pengomposan, dan cara penyimpanannya (Lingga dan Marsono, 2001). Menurut Musnamar (2005), kandungan rata-rata hara kompos dapat dilihat pada tabel 2.2
Tabel 2.2 Kandungan Rata-Rata Hara Kompos
Komponen Kandungan (%)
Kadar air 41,00-43,00
C-organik 4,83-8,00
N 0,10-0,51
P2O5 0,35-1,12
K2O 0,32-0,80
Ca 1,00-0,19
Mg 0,10-0,19
Fe 0,50-0,64
Al 0,50-0,92
Menurut Lingga dan Marsono (2001), pupuk organik mempunyai beberapa kelebihan, yaitu:
1. Memperbaiki struktur tanah. Ini dapat terjadi karena organisme tanah saat penguraian bahan organik dalam pupuk bersifat sebagai perekat dan dapat mengikat butir-butir tanah menjadi butiran yang lebih besar.
2. Menaikkan daya serap tanah terhadap air. Bahan organik mempunyai daya serap yang besar terhadap air tanah. Itulah sebabnya pupuk organik sering berpengaruh positif terhadap hasil tanaman, terutama pada musim kering. 3. Menaikkan kondisi kehidupan di dalam tanah. Hal ini terutama disebabkan
oleh organisme dalam tanah yang memanfaatkan bahan organik sebagai makanan. Oleh karena itu, pupuk organik seperti pupuk kandang yang diberikan kepada tanah harus diuraikan terlebih dahulu oleh jasad renik melalui proses pembusukkan atau peragian sebelum dihisap oleh akar tanaman. Dari proses pembusukkan ini, jasad renik memperoleh makanan dan sumber tenaga. Semakin banyak pupuk organik yang diberikan maka semakin banyak pula jasad renik dalam tanah.
4. Sebagai sumber zat makanan bagi tanaman. Pupuk organik mengandung zat makanan yang lengkap meskipun kadarnya tidak setinggi pupuk anorganik.
2.2.2 Pupuk Urea CO (NH2)2
mudah larut dalam air dan mudah diserap oleh tanaman. Kalau diberikan ke tanah, pupuk ini mudah berubah menjadi amoniak dan karbondioksida. Padahal kedua zat ini berupa gas yang mudah menguap. Sifat lainnya ialah mudah tercuci oleh air dan mudah terbakar oleh sinar matahari (Lingga dan Marsono, 2001).
Menurut Lingga dan Marsono (2001), terdapat beberapa keuntungan dari pupuk anorganik yang patut dicatat sehingga tetap diminati sampai sekarang, yaitu sebagai berikut:
1. Pemberiannya dapat terukur dengan tepat karena umumnya pupuk anorganik takaran haranya pas (Lingga dan Marsono, 2001).
2. Kebutuhan tanaman akan hara dapat dipenuhi dengan perbandingan yang tepat. Misalnya, hingga saat panen, singkong menyedot hara nitrogen 200 Kg/ha sehingga bisa diganti dengan takaran pupuk N yang pas (Lingga dan Marsono, 2001).
3. Pupuk anorganik tersedia dalam jumlah cukup. Artinya, kebutuhan akan pupuk ini bisa dipenuhi dengan mudah (Lingga dan Marsono, 2001).
4. Pupuk anorganik mudah diangkut karena jumlahnya relatif sedikit dibanding pupuk organik (Lingga dan Marsono, 2001).
2.2.3 Cara Pemberian Pupuk
Pembuatan rekomendasi pemupukan khusus untuk beraneka jenis tanah dan tanaman tidaklah mudah. Banyak faktor yang harus dipertimbangkan dalam menentukan jenis dan jumlah pupuk yang akan digunakan pada sebidang lahan bagi tanaman tertentu. Pemilihan cara pemupukan yang terbaik, tergantung pada berbagai faktor, diantaranya jenis tanah, kadar lengas, daya semat tanah terhadap berbagai hara, pengolahan, macam tanah, sistem perakaran tanaman, kemampuan tanaman mengekstraksi hara dalam tanah dan macam pupuk yang digunakan (Rosmarkam dan Yuwono, 2006).
2.3 Nitrat dan Nitrit
Nitrit dan nitrat adalah senyawa nitrogen alami yang terdapat di dalam air dalam tanah dan air permukaan. Kalium/natrium nitrit dan kalium/natrium nitrat telah digunakan dalam daging olahan (curing) selama berabad-abad di berbagai negara, termasuk Indonesia, nitrit dizinkan sebagai bahan tambahan makanan Sumber utama nitrit secara umum adalah makanan, terutama sayuran dan air minum. Hal yang perlu diperhatikan adalah pemakaian pupuk pada sayuran. Jika pupuk urea banyak digunakan, akan menyebabkan paparan pada manusia melalui sayuran, terutama sayuran yang berwarna hijau serta sayuran dari umbi dan air minum (Silalahi, 2005).
2.4 Efek Toksik Nitrat dan Nitrit
kemudian dapat mereduksi nitrat menjadi nitrit. Nitrat diabsorbsi dengan cepat pada saluran pencernaan bagian atas, dan sebagian besar dikeluarkan melalui urin. Pengeluaran melalui urin mempunyai waktu paruh sekitar 5 jam. Sebagian nitrat yang diangkut dalam darah dikeluarkan melalui kelenjar ludah. Nitrat yang berada dalam rongga mulut dapat direduksi menjadi nitrit oleh mikroba rongga mulut dan kemudian tertelan. Sebanyak 25% dari asupan nitrat dikeluarkan melalui kelenjar ludah. Sekitar 20% dari nitrat dalam kelenjar ludah direduksi menjadi nitrit, dengan demikian sekitar 5% dari seluruh asupan nitrat akan direduksi menjadi nitrit dalam ludah dan tertelan kembali (Silalahi, 2005).
2.5 Siklus Nitrogen
Nitrogen (N) merupakan bagian dari semua sel hidup. Di dalam tanaman, N berfungsi sebagai komponen utama protein, hormon, klorofil, vitamin dan enzim-enzim esensial untuk kehidupan tanaman. Ia menyusun 40%-50% bobot kering protoplasma. Oleh karena itu, N diperlukan dalam jumlah besar untuk seluruh proses pertumbuhan di dalam tanaman. Metabolisme N merupakn faktor utama pertumbuhan vegetatif, batang dan daun (Munawar, 2011).
Sumber utama nitrogen di dalam tanah berasal dari nitrogen bebas di atmosfir, hasil dekomposisi bahan organik, loncatan listrik di udara (petir) dan pupuk buatan atau pupuk organik. Nitrogen bebas di atmosfir menempati 78% volume atmosfir. Namun demikian dalam bentuk unsur tidak dapat lansung digunakan. Nitrogen harus diubah terlebih dahulu dalam bentuk amonium dan nitrat melalui proses-proses tertentu. Cara utama nitrogen bebas masuk ke dalam tanah melalui kegiatan-kegiatan jasad renik mengikat nitrogen dari udara, baik yang bebas atau yang bersimbiose dengan tanaman seperti bintil akar tanaman leguminosa dengan bakteri rhizobium (Damanik, dkk., 2010). Siklus nitrogen di dalam tanah dapat dilihat pada Gambar 2.1.