PENGARUH KONSENTRASI INDUSER DAN PENAMBAHAN
KOFAKTOR ENZIM TERHADAP PRODUKSI EKSTRAK
KASAR ENZIM LIPASE EKSTRASELULER
OLEH Pseudomonas aeruginosa
SKRIPSI
JIMMY UTAMI
060802052
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGARUH KONSENTRASI INDUSER DAN PENAMBAHAN
KOFAKTOR ENZIM TERHADAP PRODUKSI EKSTRAK
KASAR ENZIM LIPASE EKSTRASELULER
OLEH Pseudomonas aeruginosa
SKRIPSI
Diajukan untuk memenuhi syarat mencapai gelar sarjana
JIMMY UTAMI
060802052
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul
Kategori Nama
Nomor Induk Mahasiswa Pragram Studi
Departemen Fakultas
:
: : : : : :
PENGARUH KONSENTRASI INDUSER DAN PENAMBAHAN KOFAKTOR ENZIM TERHADAP PRODUKSI EKSTRAK KASAR ENZIM LIPASE EKSTRASELULER OLEH Pseudomonas aeruginosa SKRIPSI
JIMMY UTAMI 060802052
SARJANA S-1 KIMIA KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
Disetujui di Medan, 01 Januari 2011
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Dra. Nunuk Priyani, M.Sc. Dr. Yuniarti Yusak, M.S.
NIP.19640428199603 2 001 NIP. 130 809 726
Diketahui/Disetujui oleh :
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENGARUH KONSENTRASI INDUSER DAN PENAMBAHAN KOFAKTOR ENZIM TERHADAP PRODUKSI EKSTRAK KASAR ENZIM LIPASE
EKSTRASELULER OLEH Pseudomonas aeruginosa
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, 01 Januari 2011
PENGHARGAAN
Segala puji bagi Allah, Tuhan pemilik alam semesta yang telah begitu banyak melimpahkan rahmat, nikmat dan karunia-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul PENGARUH KONSENTRASI INDUSER DAN PENAMBAHAN KOFAKTOR ENZIM TERHADAP PRODUKSI EKSTRAK KASAR ENZIM LIPASE EKSTRASELULER OLEH Pseudomonas aeruginosa , yang disusun sebagai salah satu syarat mencapai gelar Sarjana Sains pada Fakultas MIPA USU.
Ucapan terima kasih terbesar pertama sekali penulis sampaikan kepada kedua orang tua penulis, Ayahanda Suherman. R dan Ibunda Sri Astuti, atas pengorbanan, doa, cinta dan kasih sayangnya yang tak terhingga kepada penulis selama ini. Dan juga kepada Bu Dadek yang sangat banyak membantu penulis, serta kepada seluruh keluarga.
Pada kesempatan ini dengan segala kerendahan hati, penulis ingin mengucapkan terima kasih yang tulus kepada:
1. Ibu Dr. Yuniarti Yusak, M.S. dan Ibu Dra. Nunuk Priyani, M.Sc. selaku pembimbing I dan II yang dengan kesabarannya telah memberikan arahan, waktu dan perhatiannya kepada penulis dalam menyelesaikan skripsi ini dari awal hingga akhir.
2. Ibu Dr. Rumondang Bulan Nst, MS selaku Ketua Departement Kimia FMIPA USU.
3. Ibu Dra. Emma Zaidar Nst, MSi selaku Kepala Laboratorium Biokimia / KBM FMIPA USU.
4. Bapak Prof. Dr. H. Erman Munir, M. Sc selaku Kepala Laboratorium Mikrobiologi FMIPA USU.
5. Ibu Sovia Lenny, SSi, MSi selaku dosen wali yang dengan kesabarannya telah memberikan arahan dalam memilih mata kuliah selama menjalani studi
6. Teman-teman selama kuliah, teman angkatan 05, 04, 03, adik-adik stambuk 07, 08, 09, rekan-rekan asisten Lab. Biokimia, rekan-rekan asisten dan teman di Lab. Mikrobiologi.
PENGARUH KONSENTRASI INDUSER DAN PENAMBAHAN
KOFAKTOR ENZIM TERHADAP PRODUKSI EKSTRAK KASAR
ENZIM LIPASE EKSTRASELULER OLEH Pseudomonas
aeruginosa
ABSTRAK
Produksi ekstrak kasar enzim lipase ekstraseluler oleh bakteri Pseudomonas aeruginosa. Dilakukan dengan menumbuhkan bakteri pada variasi konsentrasi induser minyak wijen yang ditambahkan yaitu 2%, 4%, 6%, 8% dan 10% dan dengan pengaruh penambahan koenzim Ca2+ pada masing-masing induser
Parameter yang diamati adalah kadar protein dari ekstrak kasar enzim lipase yang diproduksi dan kadar asam lemak bebas. Kadar protein ditentukan dengan metode pengukuran kuantitatif berdasarkan besar absorbansinya. Uji aktivitas dari ekstrak kasar enzim lipase dilakukan dengan pengukuran kadar asam lemak bebas yang ditentukan dengan metode titrimetri.
THE EFFECT OF CONCENTRATION INDUCER AND COFACTOR ENZYME ADDITION for CRUDE PRODUCTION OF EXTRACELLULAR
LIPASE ENZYME BY Pseudomonas aeruginosa
ABSTRACT
Crude extract production of extracellular lipase by Pseudomonas aeruginosa was performed by growing the bacteria on various inducer concentration of sesame oil which were 2, 4, 6, 8 and 10% and with combined by addition of coenzyme Ca2+ on each inducer
The parameters measured were protein content of the crude extract produced lipase and free fatty acid concentration. Protein content was analyzed by quantitative measurement method based on the absorbance. The activity of lipase crude extract was determined by measuring the free fatty acid concentration which determined by titrimetric method.
DAFTAR ISI
Halaman
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak vi
Abstract vii
Daftar Isi viii
Daftar Tabel xi
Daftar Gambar xii
Daftar Lampiran xiii
Bab 1 Pendahuluan
1.1 Latar Belakang 1
1.2 Permasalahan 3
1.3 Pembatasan Masalah 3
1.4 Tujuan Penelitian 4
1.5 Manfaat Penelitian 4
1.6 Lokasi penelitian 4
1.7 Metodologi Penelitian 4
Bab 2 Tinjauan Pustaka
2.1 Enzim 6
2.1.1 Kerja Enzim pada Substrat 7
2.1.2 Pengaruh Kadar Enzim dan Substrat 7
2.1.3 Enzim Lipase 8
2.1.4 Hipotesis Operon 9
2.1.4 Ion Logam Sebagai koenzim 11
2.2 Minyak 12
2.2.2 Analisa Kuantitatif Asam Lemak Bebas 14
2.3 Bakteri 15
2.3.1 Pseudomonas aeruginosa 16
2.4 Media Fermentasi 17
Bab 3 Metodologi Penelitian
3.1 Alat dan Bahan 19
3.1.1 Alat-Alat 19
3.1.2 Bahan-Bahan 20
3.2 Prosedur Penelitian 21
3.2.1 Pembuatan Larutan Pereaksi 21
3.2.2 Sterilisasi Alat 25
3.2.3 Pembuatan Media 26
3.2.4 Sterilisasi Media dan Bahan 26
3.2.5 Pembuatan starter Pseudomonas Aeruginosa 26
3.2.6 Pembuatan Standard Mac Varlan 27
3.2.7 Pembuatan Mac Varlan Bakteri Pseudomonas Aeruginosa 27
3.2.8 Penanaman bakteri pada media cair 27
3.2.9 Penanaman bakteri pada media cair dengan co-enzim Ca2+- 27
3.2.10 Pembuatan ekstrak Kasar Enzim Lipase 28
3.3 Parameter yang Diamati 28
3.3.1 Penentuan Absorbansi Maksimum Larutan Bovine Serum
Albumin 5000µg/mL 28
3.3.2 Penentuan Absorbansi Maksimum Larutan Bovine Serum
Albumin 5000µg/mL 28
3.3.3 Penentuan Kadar Protein Ekstrak Kasar Enzim Lipase
Ekstraseluler Pseudomonas Aeruginosa 28
3.3.4 Penentuan Kadar Asam Lemak Bebas 29
3.4 Skema Penelitian 30
3.4.1 Skema Pembuatan Media 30
3.4.2 Skema Pembuatan Starter Pseudomonas Aeruginosa 32
3.4.3 Skema Penanaman Media untuk menghasilkan
3.4.4 Skema Parameter yang diamati 35
Bab 4 Hasil dan Pembahasan
4.1 Hasil penelitian 38
4.1.1. Penentuan panjang gelombang maksimum larutan BSA 38
4.1.2. Penentuan kurva standar larutan BSA pada λ 775 nm 40
4.1.3 Penentuan kadar protein enzim lipase dari
Pseudomonas aeruginosa 40
4.1.4 Penentuan kadar protein enzim lipase
dengan penambahan Ca2+ Pseudomonas aeruginosa 41
4.1.5. Uji aktivitas 42
4.2 Pembahasan Hasil Penelitian 44
Bab 5 Kesimpulan dan Saran
5.1 Kesimpulan 50
5.2 Saran 50
Daftar Pustaka 51
DAFTAR TABEL
Halaman
Tabel 2.1
Tabel 2.2
Tabel 2.3
Tabel 4.1
Tabel 4.2
Tabel 4.3
Tabel 4.4
Tabel 4.5
Komposisi Asam Lemak Minyak Wijen
Komposisi Gizi Wijen / 100 gr
Unsur yang ada pada mikrobia
Absorbansi larutan BSA pada λ 775 nm
Kadar protein enzim (μg/mL) pada setiap perlakuan untuk
konsentrasi substrat 2, 4, 6, 8, 10 %.
Kadar protein enzim (μg/mL) pada setiap perlakuan untuk
konsentrasi substrat 2, 4, 6, 8, 10 % dengan penambahan
kofaktor enzim.
Aktivitas ekstrak kasar Enzim Lipase
Aktivits ekstrak kasar Enzim Lipase yang menggunakan
kofaktor enzim Ca2+
13
14
17
40
41
42
43
DAFTAR GAMBAR Halaman Gambar 2.1 Gambar 2.2 Gambar 2.3 Gambar 2.4 Gambar 4.1 Gambar 4.2 Gambar 4.2.2 Gambar 4.2.3 Gambar 4.2.4 Gambar a Gambar b Gambar c Gambar d
Grafik hubungan konsentrasi enzim dan kecepatan
reaksi.
Stereokimianya interaksi ikatan enzim dengan substrat
Struktur Lipid.
Mekanisme Lac_Operon
Grafik Penentuan panjang gelombang maksimum
larutan BSA 5000 µg/mL.
Kadar protein enzim (μg/mL) pada setiap perlakuan
untuk konsentrasi substrat 2, 4, 6, 8, 10 %.
Kadar protein enzim (μg/mL) pada setiap perlakuan
untuk konsentrasi substrat 2, 4, 6, 8, 10 % dengan
penambahan kofaktor enzim.
Kadar Asam Lemak Bebas (%) Pada Ekstrak kasar
Enzim Lipase.
Kadar Asam Lemak Bebas (%) Pada Ekstrak Kasar
Enzim Lipase dengan Penambahan kofaktor enzim
Ca2+ .
Pure culture Pseudomonas aeruginosa.
starter Pseudomonas aeruginosa siap pakai.
Hasil biakan Pseudomonas aeruginos pada media cair.
Hasil biakan Pseudomonas aeruginos pada media cair dengan penambahan kofaktor enzim Ca2+.
DAFTAR LAMPIRAN
Halaman Lampiran 1
Lampiran 2
Lampiran 3
Lampiran 4
Lampiran 5
Lampiran 6
Penentuan kurva standar pada λ 775 nm.
Absorbansi ekstrak kasar enzim lipase pada konsentrasi
minyak wijen 2, 4, 6, 8, 10 %.
Absorbansi ekstrak kasar enzim lipase dengan
penambahan kofaktor enzim Ca2+ pada konsentrasi
minyak wijen 2, 4, 6, 8, 10 %.
Penentuan kadar Asam Lemak Bebas pada ekstrak
kasar enzim lipase pada minyak wijen.
Penentuan kadar Asam Lemak Bebas pada ekstrak
kasar enzim lipase dengan penambahan kofaktor enzim
Ca2+ pada minyak wijen.
Gambar penelitian
55
57
58
60
61
PENGARUH KONSENTRASI INDUSER DAN PENAMBAHAN
KOFAKTOR ENZIM TERHADAP PRODUKSI EKSTRAK KASAR
ENZIM LIPASE EKSTRASELULER OLEH Pseudomonas
aeruginosa
ABSTRAK
Produksi ekstrak kasar enzim lipase ekstraseluler oleh bakteri Pseudomonas aeruginosa. Dilakukan dengan menumbuhkan bakteri pada variasi konsentrasi induser minyak wijen yang ditambahkan yaitu 2%, 4%, 6%, 8% dan 10% dan dengan pengaruh penambahan koenzim Ca2+ pada masing-masing induser
Parameter yang diamati adalah kadar protein dari ekstrak kasar enzim lipase yang diproduksi dan kadar asam lemak bebas. Kadar protein ditentukan dengan metode pengukuran kuantitatif berdasarkan besar absorbansinya. Uji aktivitas dari ekstrak kasar enzim lipase dilakukan dengan pengukuran kadar asam lemak bebas yang ditentukan dengan metode titrimetri.
THE EFFECT OF CONCENTRATION INDUCER AND COFACTOR ENZYME ADDITION for CRUDE PRODUCTION OF EXTRACELLULAR
LIPASE ENZYME BY Pseudomonas aeruginosa
ABSTRACT
Crude extract production of extracellular lipase by Pseudomonas aeruginosa was performed by growing the bacteria on various inducer concentration of sesame oil which were 2, 4, 6, 8 and 10% and with combined by addition of coenzyme Ca2+ on each inducer
The parameters measured were protein content of the crude extract produced lipase and free fatty acid concentration. Protein content was analyzed by quantitative measurement method based on the absorbance. The activity of lipase crude extract was determined by measuring the free fatty acid concentration which determined by titrimetric method.
BAB 1
PENDAHULUAN
1.1Latar Belakang
Proses hidrolisis minyak/lemak menjadi asam lemak dan gliserol secara komersial
yang sampai kini digunakan, beroperasi pada suhu 240-250oC dan tekanan 45-50 bar.
Kondisi proses ini membawa konsekuensi kebutuhan biaya investasi yang tinggi,
karena peralatan proses utama pabrik harus tahan terhadap suhu dan tekanan yang
tinggi, serta tahan terhadap asam (korosif). Proses ini juga mengkonsumsi energi yang
besar untuk mempertahankan kondisi operasinya. Oleh karenanya perlu dicari
alternatif proses yang dapat berlangsung pada suhu dan tekanan rendah. Proses
hidrolisis enzimatik menggunakan enzim lipase memenuhi kriteria tersebut.
(Malcolm, D, 1964)
Penelitian-penelitian produksi enzim lipase terdahulu yang pernah dilakukan
pada umumnya menggunakan limbah minyak kelapa sawit sebagai induser untuk
memacu produksinya (Priyani, Nunuk, 2001). Pada penelitian ini digunakan minyak
wijen sebagai indusernya, karena Wijen (Sesamum indicum L.) merupakan komoditas
pertanian yang sangat potensial sebagai penghasil minyak nabati yang dibutuhkan
dalam industri kosmetik, farmasi, makanan, dan lain-lain. Wijen mendapat julukan
The Queen of Oil Seeds Crops, yang mencerminkan bahwa biji wijen memiliki
kandungan gizi yang tinggi dan berdampak positif bagi konsumennya (Handajani,
2006).
Enzim adalah protein yang diproduksi dari sel hidup dan digunakan oleh
sel-sel untuk mengkatalisis reaksi kimia yang spesifik. (Shahib, 1992). Enzim dikatakan
biologis. Dalam jumlah yang sangat kecil, enzim dapat mengatur reaksi tertentu dan
mempunyai sifat sangat spesifik, karena hanya bekerja pada induser tertentu (Girindra,
1990) yang dalam aktivitasnya enzim kadang-kadang membutuhkan kofaktor yang
bisa berupa senyawa organik atau logam (Soeharsono, 1989).
Enzim lipase atau lengkapnya triasilgliserol lipase adalah enzim yang
menghidrolisis ester karboksilat. Enzim ini mempunyai induser alami berupa
trigliserida dan lipase ekstraseluler berhasil diisolasi dari Pseudomonas aeruginosa
pada tahun 1986. Enzim lipase stabil pada suhu optimumnya yaitu 30o , walaupun
masih aktif pada 51o C. (Nishio, 1987)
Pseudomonas aeruginosa merupakan salah satu spesies dari genus
Pseudomonas. Bakteri ini dapat menggunakan lebih dari 80 macam bahan organik
untuk pertumbuhannya, tetapi Pseudomonas dapat menggunakan arginine dan nitrat
sebagai elektron akseptor sehingga dapat tumbuh pada suasana anaerob. Pseudomonas
aeruginosa tumbuh pada suhu 35-42oC.
Berbagai penelitian telah menunjukkan bahwa Pseudomonas sp merupakan
salah satu anggota bakteri gram negatife yang umumnya menggunakan protein atau
lipid sebagai sumber energi maupun sumber carbon dan juga mampu menguraikan
berbagai jenis induser (Mc Clay, 1996 dan Wischnak, 1998), sedangkan minyak dan
lemak tergolong kepada anggota dari golongan lipid yaitu lipid netral. Minyak dan
lemak yang telah dipisahkan dari jaringan asalnya mengandung sejumlah komponen
selain trigliserida, yaitu: 1. Lipid kompleks (yaitu leshitin, cephalin, fosfatida, lainnya
serta glikolipid), 2. Sterol, berada dalam keadaan bebas atau terikat dengan asam
lemak, 3. Asam lemak bebas, 4. Lilin, 5. Pigmen yang larut dalam lemak, dan 6.
Hidrokarbon. (Ketaren, 1986)
Minyak wijen mengandung kurang lebih 0,3-0,5 % sesameoil, fenol berikatan 1-4
yang dikenal sebagai sesamol, dan sesamine sekitar 0,5-0,1 %.. Minyak wijen juga
mengandung asam-asam lemak, seperti: Palmitat 9,1%, stearat 4,3%, arachidat 0,8%,
oleat 45,4%, dan linoleat 40,4% ( Hilditch, 1947). Dimana menurut penelitian Abigor
baik dan tetap aktif pada pH 7-7,5. Bakteri pada umumnya akan tumbuh dan
berkembang dengan cepat, membentuk suatu koloni bila ditanam pada media
pembenihan yang sesuai. (Tim Mikrobiologi, Fakultas Kedokteran Universitas
Brawijaya,2003), dan dengan penambahkan ion magnesium kedalam media
pertumbuhan dapat menstimulasi pelepasan lipase ektraseluler dari dinding sel
mikroorganisme sehingga dapat meningkatkan pembentukan lipase (Aisaka & Terada,
1979), dimana kofaktor dari ion logam Ca2+ dalam konsentrasi yang rendah akan
mengaktifkan reaksi enzimatik lipase (Malcolm, D, 1964).
1.2 Permasalahan
Berdasarkan penelitian terdahulu dimana kofaktor dapat memantapkan kerja enzim
(Malcolm, D, 1964) maka kami ingin meneliti bagaimana pengaruh konsentrasi
minyak wijen yang digunakan sebagai induser dan penambahan kofaktor enzim Ca2+
terhadap produksi enzim lipase oleh Pseudomonas aeruginosa.
1.3 Pembatasan Masalah
Dalam penelitian ini hanya terbatas pada objek masalah yang berhubungan dengan
penelitian ini saja yaitu :
1. Enzim yang digunakan diperoleh dari bakteri Pseudomonas aeruginosa yang
diperoleh dari Laboratotium Mikrobiologi Departemen Biologi FMIPA USU.
2. Bakteri Pseudomonas aeruginosa yang digunakan adalah yang ber- tipe TJB
01 (Warsito, K. 2009).
3. Induser yang digunakan adalah minyak wijen dengan variasi konsentrasi 2%,
4%, 6%, 8%, dan 10%.
4. Kofaktor enzim yang digunakan adalah Ca2+ (Malcolm, D, 1964) yang berasal
dari Kristal CaCl2
5. Buffer yang digunakan adalah buffer fosfat (Rita, R, et all, 1989) dengan pH
7,0 (Abigor dkk 2002).
6. Waktu inkubasi dalam memproduksi enzim lipase adalah 3x24 jam dengan
7. Parameter yang diamati adalah besar absorbansi dari ekstrak kasar enzim
lipase yang diproduksi dan kadar asam lemak bebas.
8. Untuk mendapatkan ekstrak kasar enzim lipase dilakukan dengan Sentrifuse
dengan kecepatan 6000 rpm.
9. Penentuan kadar enzim lipase kasar yang dilakukan dengan metode
pengukuran kuantitatif menggunakan Spektrofotometri UV-Visible dan
Spektrometri Genecese 20.
10.Penentuan kadar asam lemak bebas dilakukan dengan metode titrasi (Ketaren,
1986).
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah sebagai berikut:
1. Untuk mengetahui pengaruh perbedaan konsentrasi induser yang ditambahkan
ke dalam media terhadap hasil produksi enzim lipase ekstraseluler oleh bakteri
Pseudomonas aeruginosa.
2. Untuk mengetahui pengaruh penambahan kofaktor enzim terhadap jumlah
produksi enzim lipase ekstraseluler yang dihasilkan.
1.5 Manfaat Penelitian
Dari hasil penelitian diharapkan:
1. Dapat diketahui kondisi optimum dari bakteri Pseudomonas aeruginosa
sehingga dapat memproduksi enzim lipase ekstraseluler secara maksimal.
2. Dapat mengetahui pengaruh penambahan kofaktor enzim terhadap enzim
lipase ektraseluler yang diproduksi oleh bakteri Pseudomonas aeruginosa
TJB01.
1.6 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Biokimia FMIPA-USU, Medan,
Laboratorium Mikrobiologi FMIPA-USU, Medan, dan Laboratorium Proteksi Bahan
1.7 Metodologi Penelitian
Penelitian ini adalah eksperimental laboratorium, dengan menggunakan biakan murni
Bakteri Pseudomonas aeruginosa yang diperoleh dari Laboratorium Mikrobiologi
FMIPA USU dan sampel yang digunakan sebagai induser berupa minyak wijen yang
diperoleh dari Supermarket VIGO Medan. Pada penelitian ini untuk mendapatkan
kondisi yang optimum, maka Pseudomonas aeruginosa ditumbuhkan pada media
dengan sumber carbon yang berasal dari minyak wijen dengan konsentrasi yang
divariasikan, sebagai sumber nitrogen yang diujikan adalah 0,3% ammonium nitrat
(NH4NO3) (Chen SY et.al, 2007) dan komposisi senyawa lain yang juga dibuat tetap
yaitu: KH2PO4 dan K2HPO4 (ATCC, 1989) sebagai buffer pada pH 7 (Abigor dkk
(2002) 0,02% MgSO4.7H2O (Koch, et al, 1991) penambahan Co-enzim Ca2+
(Malcolm, D, 1964) yang berasal dari 1,5% CaCL2.2H2O (Gupta, V.K, 2008), dimana
langkah-langkahnya adalah sebagai berikut :
Dalam penelitian ini digunakan tiga variabel yaitu variabel tetap, variabel
bebas dan variabel terikat.
1. Variabel tetap meliputi : Jenis induser, jenis kofaktor enzim, jumlah bakteri yang
dimasukkan, temperatur, pH, tempat produksi, dan lama produksi.
2. Variabel bebas meliputi : Konsentrasi induser, komposisi media.
3. Variabel terikat meliputi : Produksi enzim lipase yang diukur berdasarkan nilai
BAB 2
TINJAUAN PUSTAKA
2.1Enzim
Enzim adalah protein yang diproduksi dari sel hidup dan digunakan oleh sel-sel untuk
mengkatalisis reaksi kimia yang spesifik. Enzim memiliki tenaga katalitik yang luar
biasa dan biasanya lebih besar dari katalisator sintetik. Spesifitas enzim sangat tinggi
terhadap substratnya. Tanpa pembentukan produk samping enzim merupakan unit
fungsional untuk metabolisme dalam sel, bekerja menurut urutan yang teratur. Sistem
enzim terkoordinasi dengan baik menghasilkan suatu hubungan yang harmonis
diantara sejumlah aktivitas metabolic yang berbeda (Shahib, 1992). Enzim dikatakan
sebagai suatu kelompok protein yang berperan sangat penting dalam aktivitas
biologis. Dalam jumlah yang sangat kecil, enzim dapat mengatur reaksi tertentu
sehingga dalam keadaan normal tidak terjadi penyimpangan-penyimpangan hasil akhir
reaksinya. Enzim ini akan kehilangan aktivitasnya akibat panas, asam atau basa kuat,
pelarut organik, atau pengaruh lain yang bisa menyebabkan denaturasi protein. Enzim
dikatakan mempunyai sifat sangat khas, karena hanya bekerja pada substratnya
(Girindra, 1990).
Untuk aktivitasnya kadang-kadang enzim membutuhkan kofaktor yang bisa
berupa senyawa organik atau logam. Senyawa organik itu terikat pada bagian protein
enzim. Bila ikatan itu lemah maka kofaktor tadi disebut co-enzim dan dan jika terikat
erat melalui ikatan kovalen maka dinamakan gugus prostetis. Pada umumnya dua
kofaktor itu tidak dibedakan dan disebut co-enzim saja. Apabila enzim itu terdiri dari
bagian seperti yang diterangkan diatas maka keseluruhan enzim itu dinamakan holo
enzim. Bagian protein dinamakan apo-enzim dan bagian non proteinnya disebut
enzim atau mentransfer electron yang timbul selama proses katalisis (Soeharsono,
1989).
2.1.1 Kerja Enzim Pada Substrat
Enzim meningkatkan kemungkinan molekul-molekul yang bereaksi saling bertemu
dengan permukaan yang saling berorientasi. Hal ini terjadi karena enzim mempunyai
suatu afinitas yang tinggi terhadap substrat dan mempunyai kemampuan untuk
mengikat substrat tersebut walaupun bersifat sementara. Penyatuan antara substrat
dengan enzim sangat spesifik substrat terikat dengan enzim sedemikian rupa, sehingga
setiap substrat terorientasi secara tepat untuk terjadi reaksi.
Pembentukan ikatan yang sementara (biasanya ikatan nonkovalen) antara
substrat dengan enzim menimbulkan penyebaran elektron dalam molekul substrat dan
penyebaran ini menyebabkan suatu regangan pada ikatan kovalen spesifik dalam
molekul substrat, sehingga ikatan kovalen tersebut menjadi mudah terpecah. Para ahli
biokimia menamakan keadaan dimana terjadi regangan ikatan molekul substrat setelah
berinteraksi dengan enzim disebut pengaktifan substrat (Shahib, 1992).
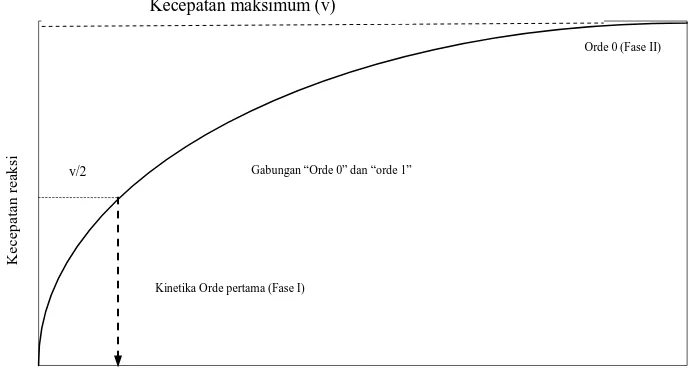
2.1.2 Pengaruh Kadar Enzim dan Substrat
Kecepatan reaksi bergantung pada konsentrasi enzim yang berperan sebagai
katalisator dalam reaksi itu. Pada gambar 2.1.2 terlihat hubungan jika konsentrasi
enzim yang digunakan tetap, sedangkan substrat dinaikkan. Di sini dapat terlihat
bahwa pada penambahan pertama kecepatan reaksi naik dengan cepat. Tetapi jika
penambahan substrat dilanjutkan, dilanjutkan maka tambahan kecepatan mulai
menurun sampai pada suatu ketika tidak ada tambahan kecepatan reaksi lagi (Girindra,
K
e
ce
p
at
an
r
e
ak
si
Gambar. 2.1
Pada Substrat yang spesifik, enzim akan mengkatalisis reaksi sehingga
menghasilkan produk yang spesifik, juga pada penambahan pereaksi kimia tertentu
dapat mengakibatkan enzim menunjukkan bentuk stereokimianya dimana interaksi
enzim dengan substrat terjadi dalam ikatan, dimana kelebihan substrat tidak dapat
diikat seluruhnya oleh enzim (Trevar, 1985).
C
2.1.3 Enzim lipase
Lipase yang berasal dari bakteri pada umumnya adalah protein yang memiliki sifat
asam. Dan mempunyai berat molekul dari 20.000 sampai 60.000. Memiliki aktivitas
Kinetika Orde pertama (Fase I)
Gabungan “Orde 0” dan “orde 1”
Orde 0 (Fase II)
Kecepatan maksimum (v)
Konsentrasi substrat
v/2
Substrat
R’ R’
R’
R
A- A-
A-
Gambar 2.2
Enzim
spesifik protein murni yang berubah-ubah dari 500 sampai 10.000 unit lipase per mg
protein (Fogarty, William, M. 1983).
Gambar 2.3. Lipid (Triasilgliserol)
Enzim lipase atau lengkapnya triasilgliserol lipase adalah enzim yang
menghidrolisis ester karboksilat. Enzim ini mempunyai substrat alami berupa
trigliserida dari asam lemak yang mana reaksinya memerlukan air, dan lipase
ekstraseluler berhasil diisolasi dari Pseudomonas aeruginosa pada tahun 1986. Enzim
lipase memiliki sub unit berupa glikoprotein dan lipoprotein. Sub unit tersebut dapat
sebagai monomer, dimer, oligomer atau polimer. Enzim lipase stabil pada suhu
optimumnya yaitu 30o C, walaupun masih aktif pada 51o C, (Nishio, 1987). Dan
menurut penelitian Abigor dkk (2002) wijen digunakan sebagai katalis enzim lipase
dan dapat bekerja dengan baik dan bertahan hidup pada pH 7-7,5.
Pada banyak mikroorganisme, bagian yang kuat dari lipase ekstraseluler
sebagian masih terikat pada dinding sel. Karena adanya ikatan antara enzim dan
dinding sel mungkin menghambat ekskresi lipase berikutnya dalam media
pertumbuhan dan dengan demikian menurunkan hasil lipase ekstraseluler. Zat yang
dapat menstimulai pelepasan lipase dari dinding sel sehingga dapat meningkatkan
pembentukan lipase yaitu dengan menambahkan ion magnesium kedalam media
pertumbuhan ( Aisaka & Terada, 1979).
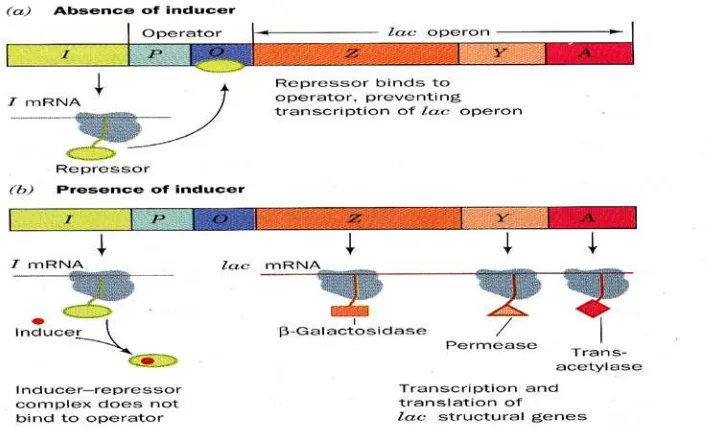
2.1.4 Hipotesis Operon
Dari aktivitas β-galaktosidase dalam sel E. Coli diusulkan hipotesis operon untuk
kontrol genetik dari sintesis protein pada prokariota. Jenis peraturan sintesis protein
kontrol yang diberikan terutama pada transkripsi gen menjadi mRNAs yang sesuai.
Ada cara umum lain dalam sintesis protein, yaitu, dengan kontrol translasi laju sintesis
dari rantai polipeptida dari template mRNA-nya. Kontrol transkripsi tampaknya
menjadi mekanisme utama untuk pengaturan ekspresi gen pada bakteri. Kontrol
Translational, yang tidak dipahami dengan baik, tampaknya merupakan mekanisme
sekunder pada bakteri tetapi sangat penting dalam eukariota.
Dari eksperimen mereka Jacob dan Monod terdapat tiga gen struktural z, y,
dan a coding untuk mensintesis β-galaktosidase, permease dan protein A,
masing-masing, yang semuanya dapat diinduksi oleh laktosa, terletak berdekatan satu sama
lain dalam kromosom E. coli dan DNA mengisi letak lain di dekat gen ini. Bagian i ini
diusulkan menjadi gen regulasi coding untuk sekuens asam amino dari protein yang
disebut represor, ketika gen i ditranskripsi untuk membentuk mRNA yang sesuai,
yang berdifusi terakhir ke ribosom dan ada bertindak sebagai template untuk sintesis
represor. Protein represor mengikat bagian lain pada segmen tertentu pada DNA yang
disebut operator. Pengikatan protein represor ke situs operator dalam DNA
dipostulatkan untuk mencegah atau menekan transkripsi oleh RNA polimerase dari
tiga gen struktural z, y, dan a coding untuk tiga enzim diinduksi oleh 3-galactosides,
Gambar 2.4 Mekanisme Lac_Operon
Untuk menjelaskan tindakan dari inducer, ketika glukosa tidak tersedia, tetapi
pengikatan spesifik yang kedua pada protein represor, letak inducer, untuk
membentuk sebuah kompleks penginduksi-represor. Ikatan dari inducer disebabkan
represor yang akan dibentuk dari operator pada DNA dengan penurunan afinitas untuk
yang kedua. Setelah kompleks represor-inducer dilepaskan, gen struktural untuk β
-galactosiclase dan dua lainnya protein menjadi tersedia untuk transkripsi oleh RNA
polimerase untuk menghasilkan mRNA yang sesuai. Ketiga protein kemudian
disintesis dari template mRNA pada ribosom, memungkinkan sel untuk menggunakan
laktosa sebagai sumber karbon dan energi.sel-sel yang diambil dari media terakhir,
dicuci, dan ditempatkan dalam sebuah medium, sedangkan-laktosa, D-glukosa, yang
sel selalu dapat digunakan. Karena konsentrasi laktosa dalam sel sekarang akan
menjadi rendah. induser terikat pada protein represor akan terpisahkan jauh,
menyebabkan molekul represor untuk kembali ke bentuk aktif, sehingga sekarang
terikat dengan afinitas yang tinggi ke bagian operator. Akibatnya, gen-gen struktural
untuk β-galaktosidase dan dua protein lain tidak bisa lagi ditranskripsikan, dan karena
kekurangan mRNA, protein ini tidak bisa lagi dibuat. Oleh karena itu protein
represor, melalui kapasitasnya untuk mengikat baik induser atau operator reversibel
tapi tidak keduanya secara bersamaan, sehingga dapat dihitung induksi dan represi
keduanya pada sintesis galaktosidase.
Ketiga gen struktural z, - v, dan, a bersama-sama dengan operator o mereka,
yang ditunjuk oleh Jacoob dan Monoc sebagai operon, khususnya, Lac_Operon.
Sebuah operon tetap terdiri dari kelompok gen struktural fungsional terkait, yang
dapat diaktifkan atau dinonaktifkan secara terkoordinasi, bersama dengan operator
mereka.(Lehninger, 1982)
2.1.5 Ion Logam sebagai kofaktor-enzim
Ion logam dapat digunakan sebagai aktivasi enzim dan pembawa elektron dengan
mekanisme variasi yang berbeda dan lingkungan mikro yang berbeda dalam jenis
a) secara tepat menjadi katalis pada enzim, b) Berpartisipasi dalam ikatan substrat
pada sisi aktif, c) menjaga konformasi enzim agar tetap sebagai katalis, dan d)
berpartisipasi dalam reaksi redoks. Beberapa logam seperti Fe2+, Cu2+, Zn2+, Mn2+,
Co2+, Mo2+ berikatan sangat kuat dengan enzim dan membentuk metaloenzim,
sedangkan logam Mg2+, Ca2+, Mn2+ berikatan lemah dengan enzim sehingga
membentuk metal-aktif enzim (Milton, S. H. 1987).
Fakta lain tentang enzim lipase adalah adanya ion logam Ca2+ dalam
konsentrasi yang rendah akan mengaktifkan reaksi enzimatik lipase. Senyawa lain
yang diketahui memiliki fungsi yang sama dengan Ca2+ adalah EDTA. Tetapi kation
divalent lainnya seperti Mg2+, Zn2+, Cu2+, dan Cd2+ pada konsentrasi rendah
menghambat aktivitas enzim ini sampai 70%. Dilain pihak Kalium asetat
mempertinggi aktivitas enzimatik lipase hingga 4 sampai 5 kali dikisaran konsentrasi
1yang lebih tinggi. Natrium Asetat mendorong kenaikan aktivitas enzimatik sampai
dua kali lipat pada konsentrasi rendah dan tidak berpengaruh apa-apa walau dalam
konsentrasi tinggi pada pH 7,0-75. Natrium Klorida hanya sampai batas konsentrasi
rendah yang mempengaruhi aktivitas enzimatik lipase dan pengaruhnya berupa
adanya kenaikan aktivitas enzimatik yang tipis (Schwimmer, S. 1981). Kofaktor akan
terikat pada gugus aktif pada molekul protein enzim, sehingga kerja enzim yang
ditunjukkan oleh aktivitas meningkat.(Lehninger, 1982)
2.2Minyak
Minyak dan lemak tergolong kepada anggota dari golongan lipid yaitu lipid netral.
Lipid itu sendiri dapat diklasifikasikan menjadi 4 kelas yaitu: 1) Lipid netral, 2)
Fosfatida, 3) Spingolipid dan 4) Glikolipid.
Minyak dan lemak yang telah dipisahkan dari jaringan asalnya mengandung
sejumlah komponen selain trigliserida, yaitu: 1) Lipid kompleks (yaitu leshitin,
cephalin, fosfatida, lainnya serta glikolipid), 2) Sterol, berada dalam keadaan bebas
atau terikat dengan asam lemak, 3) Asam lemak bebas, 4) Lilin, 5) Pigmen yang larut
Rata-rata komposisi minyak terdiri dari 58,2% sebagai sampel jenuh, 28,6%
senyawa aromatik dan 14,2% senyawa polar. Berdasarkan klasifikasi minyak,
senyawa aromatik ini adalah senyawa hidrokarbon yang terdiri dari cincin yang
mengandung enam atom karbon. Hampir kebanyakan senyawa aromatik ini bermassa
rendah dan jumlahnya dalam minyak sekitar 10-30% (Syakti, 2005).
2.2.1 Minyak Wijen
Tanaman wijen (Sesamum indicum L) termasuk family Pedaliaceae, varietas
Sesamum indicum sub spesies ialah S. orientale. (Ketaren, 1986) Minyak wijen
mengandung zat tidak tersabunkan dalam jumlah relative tinggi. Tetapi kandungan
tertinggi adalah sterol dan zat-zat yang tidak dapat dipisahkan dengan pemurnian,
sedangkan kadar bahan non minyak lainnya relative rendah (Bailey, 1951).
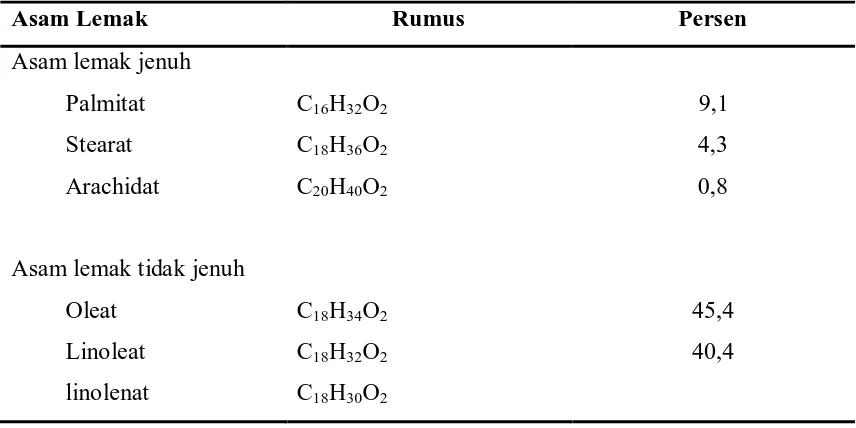
Minyak wijen mengandung kurang lebih 0,3-0,5 % sesameoline, fenol
berikatan 1-4 yang dikenal sebagai sesamol, dan sesamine sekitar 0,5-0,1 %.. Minyak
wijen juga mengandung asam-asam lemak, yaitu:
Asam Lemak Rumus Persen
Asam lemak jenuh
Palmitat
Stearat
Arachidat
Asam lemak tidak jenuh
Oleat
Linoleat
linolenat
C16H32O2
C18H36O2
C20H40O2
C18H34O2
C18H32O2
C18H30O2
9,1
4,3
0,8
45,4
40,4
( Hilditch, 1947)
Komposisi Jumlah (gr) Air
Protein
Lemak
Karbohidrat
Ca
P
Fe
Vitamin B1
Vitamin C
Bagian yang dapat dimakan
6
19,3
57,1
18,1
0,0012
0,614
0,0095
0,00093
0,0058
100
(Ketaren, 1986)
Tabel 2.2. Komposisi Gizi Wijen / 100 gr
2.2.2 Analisis Kuantitatif Asam Lemak Bebas
Kadar Asam lemak bebas dinyatakan sebagai jumlah rata-rata dari bobot asam lemak
yang tidak lagi terikat dengan molekul trigliserida dari setiap gram minyak atau
lemak. Soumano telah meneliti terbentuknya asam lemak yang bebas tersebut pada
saat reaksi interesterifikasi enzimatik minyak nabati dengan biokatalis berbagai jenis
lipase (Soumanou, M.M. 1997).
Untuk menentukan kadar minyak atau lemak dapat digunakan bilangan
penyabunan yaitu jumlah milligram KOH yang diperlukan untuk menyabunkan satu
gram minyak atau lemak. Dalam penetapan bilangan penyabunan biasanya larutan
alkali yang dipergunakan adalah KOH, yang diukur dengan hati-hati dengan
menggunakan buret dan pipet.
Campuran minyak atau lemak dengan larutan KOH didihkan pada pendingin
alir balik sampai terjadi penyabunan yang lengkap, kemudian larutan KOH yang
tersisa ditetapkan dengan jalan titrasi dengan larutan HCl 0,5 N. Bilangan penyabunan
dapat ditetapkan dengan jalan mengurangkan jumlah miliequivalen larutan alkali
tersebut, dibagikan dengan berat contoh dalam gram. Berat molekul untuk larutan
KOH adalah 56,1 : sedangkan berat molekul larutan NaOH adalah 39,9.
contoh gram
HCl N x HCl ml KOH N x KOH ml Penyabunan
Bilangan = 56,1( )( )
(Ketaren, 1986).
Cara lain untuk menentukan kadar asam lemak bebas dalam minyak nabati
yaitu dengan memodifikasi perhitungan menjadi bilangan asam atau acid value (AV).
Bilangan asam dinyatakan sebagai mg KOH yang dibutuhkan untuk mentitrasi asam
lemak bebas yang terkandung dalam 1 g minyak. Karenanya, pada perhitungan
bilangan asam, harus diketahui berat minyak yang bersangkutan (AOCS, 1989).
Terdapat sejumlah metode penentuan kadar asam lemak bebas selain metode
titri metri yaitu seperti metode yang didasarkan pada pengukuran PH atau tingkat
keasaman, dan teknik-teknik spektoskopi dengan atau tanpa pelarut (Velasco Arjona,
A. et al, 1998).
2.3 Bakteri
Bakteri adalah mikroorganisme bersel satu dan berkembang biak dengan membelah
diri. Ukuran bakteri bervariasi baik penampang maupun panjangnya, tetapi pada
umumnya penampang bakteri adalah sekitar 0,7-1,5 µm dan panjangnya sekitar
1-6µ m. Bentuk bakteri dibagi menjadi 3 yaitu :
1. Sferis (kokus)
Bakteri ada yang berbentuk sferis atau bulat, seperti ada yang ditemukan pada
genus Staphylococcus, Streptococcus, Neisseria dan lain-lain
2. Batang (basil)
Bakteri yang berbentuk batang lurus misalnya dapat dijumpai pada famili
Enterobacteriaceae seperti Escheria coli, Salmonella typhi, Klebsiella
Bacillus yaitu Bacillus anthracis penyebab penyakit anthraks. Selain bentuk
batang lurus, dijumpai pula bentuk batang bengkok misalnya pada bakteri
Vibrio cholera penyebab penyakit cholera.
3. Spiral
Bakteri berbentuk spiral dijumpai pada penyebab penyakit sifilis yaitu
Treponema pallidum, bakteri penyebab demam bolak-balik yaitu Borelia
reccurentis (Tim Mikrobiologi, Fakultas Kedokteran Universitas
Brawijaya,2003).
2.3.1 Pseudomonas aeruginosa
Pseudomonas aeruginosa merupakan salah satu spesies dari genus Pseudomonas.
Pseudomonas aeruginosa bergerak aktif dengan flagella polar dan mempunyai ukuran
lebar 0,5-1 µm dan panjang 3-4 µ m dan bersifat aerob. Bakteri ini dapat menggunakan
lebih dari 80 macam bahan organik untuk pertumbuhannya, tetapi Pseudomonas
dapat menggunakan arginine dan nitrat sebagai elektro akseptor sehingga dapat
tumbuh pada suasana anaerob. Pseudomonas aeruginosa tumbuh pada suhu 35-42oC.
P.aeruginosa menghasilkan pigmen piosianin (Tim Mikrobiologi, Fakultas
Kedokteran Universitas Brawijaya,2003).
Menurut Donnel, 1994 klasifikasi bakteri Pseudomonas adalah sebagai
berikut:
Kingdom : Prokaryotae
Divisio : Gracilitutes
Kelas : Protobakteria
Famili : Pseumonadacae
Genus : Pseudomonas
Spesies : Pseudomonas sp.
Berbagai penelitian telah menunjukkan bahwa Pseudomonas sp merupakan
salah satu anggota bakteri gram negative yang umumnya menggunakan protein atau
lipid sebagai sumber energi maupun sumber carbon dan juga mampu menguraikan
2.4Media Fermentasi
Untuk mendapatkan biakan murni bakteri, bahan pemeriksaan klinis tersebut ditanam
pada media pembenihan. Media pembenihan yang digunakan untuk isolasi primer
tergantung dari dugaan kemungkinan bakterinya, namun biasanya digunakan media
pembenihan padat yang mengandung agar-agar untuk mendapatkan koloni bakteri
yang terpisah (isolated colony). Bakteri pada umumnya akan tumbuh dan berkembang
dengan cepat, membentuk suatu koloni bila ditanam pada media pembenihan yang
sesuai setelah diinkubasikan selama 18-24 jam pada suhu yang sesuai pula. (Tim
Mikrobiologi, Fakultas Kedokteran Universitas Brawijaya,2003).
Medium kultur harus mengandung semua elemen yang dibutuhkan untuk
pertumbuhan mikrobia, dalam proporsi yang serupa dengan yang ada pada sel
mikrobia yaitu :
Unsur Fungsi Fisiologi Berat kering
(%) Hidrogen Oksigen Karbon Nitrogen Sulfur Fosfor Magnesium Mangan Kalsium Besi Kobalt Tembaga, seng Molybdenum
Penyusun senyawa organik
Penyusun senyawa organik
Penyusun senyawa organik
Penyusun protein, asam nukleat, dan koenzim
Penyusun protein, dan beberapa koenzim
Penyusun asam nukleat, fosfolipida, dan
koenzim
Kofaktor pada sejumlah reaksi enzim (ATP)
Kofaktor pada beberapa enzim
Kofaktor pada beberapa enzim (Protease)
Penyusun sitokrom, protein, non-heme dan
kofaktor pada beberapa enzim
Penyusun vitamin B12
Penyusun beberapa enzim
[image:32.595.100.531.397.727.2]8 20 50 14 1 3 0.5 0.1 0.5 0.2 0.03 0.03
Umumnya yang disebut makronutrien adalah yang dibutuhkan dalam jumlah besar
seperti C, H, O, N,. Mesonutrien dibutuhkan dalam jumlah lebih sedikit seperti Mg, P,
S, dan mikronutrien dibutuhkan dalam jumlah sangat sedikit seperti Fe, Cu, Zn, dan
Mo. (Hidayat N, dkk. 2006). Salah satu unsur yang sangat penting dalam media adalah
karbon. Secara umum sumber karbon yang optimal digunakan yaitu karbohidrat, hidrokarbon dan
minyak nabati. Beberapa organisme mengkonsumsi beberapa substrat, yang dikombinasi atau secara
BAB 3
METODOLOGI PENELITIAN
3.1Alat dan Bahan
3.1.1 Alat-alat
1. Gelas beaker Pyrex
2. Gelas ukur Pyrex
3. Gelas erlenmeyer Pyrex
4. Neraca analitik Ohaus
5. Indikator universal Merck
6. Autoklaf Yamato SN210
7. Oven Gallenkamp
8. Tabung reaksi Pyrex
9. Inkubator Fisher Cientific
10.Hot plate Thermolyne
11.Termometer
12.Labu takar Pyrex
13.Cawan Petri Pyrex
14.Jarum Ose
15.Pipet serologi Pyrex
16.Pipet Volumetri Pyrex
17.Pipet man Gilson
18.Bunsen
19.Botol akuades
20.Statif dan klem Pyrex
21.Buret Pyrex
22.Vortex Fisons
24.Spektrometric Genesis 20 Simadzu
25.Shaker Kika HS 501
26.Sentrifugasi Hettich EBA 85
3.1.2 Bahan-Bahan 1. Minyak Wijen
2. Akuades
3. Starter Pseudomonas Aeruginosa
4. Tripton Soya Agar p.a.(E.Merck)
5. NH4NO3(s) p.a.(E.Merck)
6. CaCl2.2H2O (s) p.a.(E.Merck)
7. MgSO4.7H2O (s) p.a.(E.Merck)
8. K2HPO4 (p) p.a.(E.Merck)
9. KH2PO4 (s) p.a.(E.Merck)
10.Alkohol 96% Teknis 96% (Bratachem)
11.Alkohol 70% Teknis 70% (Bratachem)
12.Na2CO3 (s) p.a.(E.Merck)
13.NaOH (s) p.a.(E.Merck)
14.Kalium Natrium Tartrat (s) p.a.(E.Merck)
15.CuSO4.5H2O (s) p.a.(E.Merck)
16.Folin Ciocalteu (l) p.a.(E.Merck)
17.Bovine Serum Albumin p.a.(E.Merck)
18.HCl (s) p.a.(E.Merck)
19.KOH (s) p.a.(E.Merck)
20.BaCl2.2H2O (s) p.a.(E.Merck)
21.H2SO4 (l) p.a.(E.Merck)
3.2 Prosedur Penelitian
3.2.1 Pembuatan Larutan Pereaksi 3.2.1.1 Pembuatan HCl 0,1 N
Dimasukkan 2 mL HCl p.a ke dalam labu takar labu takar 1000 mL kemudian
diencerkan dengan akuades hingga tanda batas setelah itu homogenkan.
3.2.1.2 Pembuatan larutan Na2CO3 2 %
Ditimbang 2 g Kristal Na2CO3, kemudian dimasukkan ke dalam labu takar
100 mL; tuangkan akuades ¼ tabung dan homogenkan; tambahkan lagi
dengan akuades sampai tanda batas, homogenkan.
3.2.1.3 Pembuatan Buffer Phosfat 0,05 M untuk pH = 7 Dipakai rumus: 2 , 7 0 , 7 ] [ ] [ log 4 2 4 2 − = − HPO K PO KH ] [ ] [ log 2 , 7 0 , 7 4 2 4 2 HPO K PO KH − = ] [ ] [ log 4 2 4 2 HPO K PO KH pKa
pH = −
Gram garam = % garam x Molaritas x BM
= 38,68 % x 0,05 x 174
= 0,3868 x 0,05 x 174
= 3,3652 g/L
Gram asam = % Asam x Molaritas x BM
= 61,32 % x 0,05 x 136
= 0,6132 x 0,05 x 136
= 4,1698 g/L
3.2.1.4 Pembuatan larutan KOH 0,001 N a. Pembuatan larutan KOH 0,001 N
Ditimbang 0,056 g KOH dan dimasukkan ke dalam labu takar 250 ml,
kemudian dilarutkan dengan akuades hingga tanda batas setelah itu
dihomogenkan
b. Standarisasi larutan KOH 0,001 N dengan Asam Oksalat
Ditimbang dengan teliti 0,001 g asam okslat (BM=126), kemudian
dilarutkan ke dalam 25 mL aquadest dan ditambahkan 3 tetes indikatot
phenolphthalein kemudian dititrasi dengan larutan KOH yang akan
distandarisasi hingga warna merah rose. Hal yang sama dilakuan 3 kali
ulangan.
Perhitungan
(
)
(
0,126xmLKOH)
2 x oksalat asam
g KOH larutan
N = (Sudarmaji, S. 1997)
3.2.1.5 Pembuatan larutan Magnesium Sulfat 0,02 %
Ditimbang 0.05 g MgSO4.7H2O(s), kemudian dimasukkan ke dalam labu takar
250 mL; tuangkan akuades ¼ tabung dan homogenkan; tambahkan lagi
dengan akuades sampai tanda batas, homogenkan kemudian disterilkan.
3.2.1.6 Pembuatan larutan Kalium Natrium Tartrat 1 %
Ditimbang 1 g Kalium Natrium Tartrat, kemudian dimasukkan ke dalam labu
takar 100 mL; tuangkan akuades ¼ tabung dan homogenkan; tambahkan lagi
dengan akuades sampai tanda batas, homogenkan.
3.2.1.7 Pembuatan pereaksi Lowry
a. Pembuatan larutan NaOH 0,1 N
Ditimbang dengan teliti 0,4 g NaOH dan dimasukkan ke dalam labu takar 100
mL, tuangkan akuades ¼ tabung dan homogenkan; tambahkan lagi dengan
akuades sampai tanda batas homogenkan.
b. Pembuatan pereaksi A
Larutan 2% Na2CO3 dan dimasukkan ke dalam labu takar 100 mL, diencerkan
c. Pembuatan pereaksi B
Ditimbang 0,5 g CuSO4.5H2O dan dilarutkan dengan larutan Kalium Natriun
Tartrat 1% dalam labu takar 100 mL hingga tanda batas setelah itu
dihomogenkan.
d. Pembuatan pereaksi C
Dicampurkan pereaksi C dan pereaksi A deengan perbandingan 1:50,
pereaksi ini harus dalam keadaan segar ketika akan digunakan untuk analisa.
e. Folin-Ciocalteu
Diencerkan pereaksi Folin-Ciocalteu dengan akuades dengan perbandingan
1:50 (Apriyantono. A, 1989)
3.2.1.8 Pembuatan larutan Bovine Serum Albumin (BSA) 5 mg/mL
Ditimbang dengan teliti 1,25 g BSA dan dimasukkan ke dalam labu takar 250
mL dan dilarutkan dengan akuades sampai garis tanda setelah itu
dihomogenkan.
3.2.1.9 Pembuatan Larutan standard BSA 1000 µg/mL
Dipipet 20 mL dari larutan induk BSA 5000 µg/mL dimasukkan ke dalam
labu takar 100 mL, dilarutkan dengan akuades sampai garis tanda setelah itu
dihomogenkan.
3.2.1.10 Pembuatan Larutan standard BSA 350 µg/mL
Dipipet 35 mL dari larutan standard BSA 1000 µg/mL dimasukkan ke dalam
labu takar 100 mL, dilarutkan dengan akuades sampai garis tanda setelah itu
dihomogenkan.
3.2.1.11 Pembuatan Larutan standard BSA 300 µg/mL
Dipipet 30 mL dari larutan standard BSA 1000 µg/mL dimasukkan ke dalam
labu takar 100 mL, dilarutkan dengan akuades sampai garis tanda setelah itu
3.2.1.12 Pembuatan Larutan standard BSA 250 µg/mL
Dipipet 25 mL dari larutan standard BSA 1000 µg/mL dimasukkan ke dalam
labu takar 100 mL, dilarutkan dengan akuades sampai garis tanda setelah itu
dihomogenkan.
3.2.1.13 Pembuatan Larutan standard BSA 200 µg/mL
Dipipet 20 mL dari larutan standard BSA 1000 µg/mL dimasukkan ke dalam
labu takar 100 mL, dilarutkan dengan akuades sampai garis tanda setelah itu
dihomogenkan.
3.2.1.14 Pembuatan Larutan standard BSA 150 µg/mL
Dipipet 15 mL dari larutan standard BSA 1000 µg/mL dimasukkan ke dalam
labu takar 100 mL, dilarutkan dengan akuades sampai garis tanda setelah itu
dihomogenkan.
3.2.1.15 Pembuatan Larutan standard BSA 100 µg/mL
Dipipet 10 mL dari larutan standard BSA 1000 µg/mL dimasukkan ke dalam
labu takar 100 mL, dilarutkan dengan akuades sampai garis tanda setelah itu
dihomogenkan.
3.2.1.16 Pembuatan Larutan standard BSA 50 µg/mL
Dipipet 5 mL dari larutan standard BSA 1000 µ g/mL dimasukkan ke dalam
labu takar 100 mL, dilarutkan dengan akuades sampai garis tanda setelah itu
dihomogenkan.
3.2.2 Sterilisasi Alat
Dicuci alat-alat yang akan digunakan sampai bersih, kemudian dikeringkan
dan ditutup rapat dengan kapas setelah itu dibalut dengan kertas. Setelah itu
dimasukkan ke dalam oven. Disterilisasi sampai suhu 221oC dan
3.2.3 Pembuatan Media
3.2.3.1Pembuatan Media Tripton Soya Agar
Ditimbang 4 g tipton Soya Agar setelah itu dimasukkan ke dalam gelas
Erlenmeyer dan dilarutkan dengan 100 mL air laut, kemudian dipanaskan di
atas hot plate hingga larut dan warna larutan berubah menjadi bening, ditutup
dengan kapas dan alumunium foil.
3.2.3.2Pembuatan Media cair
Ditimbang 1,5 g NH4NO3 (s), 4,1698 g KH2PO4 (s) dan 3,3652 g K2HPO4 (s),
dimasukkan ke dalam Botol duran 500 mL, dan dipipet0,1 mL larutan MgSO4
0,02%, dilarutkan dengan akuades sampai garis batas, ditutup rapat, kemudian
distirer hingga larutan menjadi homogen.
3.2.3.3Pembuatan Media cair dengan penambahan Kofaktor enzim Ca2+
Ditimbang 7,5 g CaCl2.2H2O (s), 1,5 g NH4NO3 (s), 4,1698 g KH2PO4 (s) dan
3,3652 g K2HPO4 (s), dimasukkan ke dalam Botol duran 500 mL, dan dipipet
0,1 mL larutan MgSO4 0,02%, dilarutkan dengan akuades sampai garis batas,
ditutup rapat, kemudian di stirer hingga larutan menjadi homogen.
3.2.4 Sterilisasi Media dan Bahan
Dimasukkan +/- 1 L akudes ke dalam autoklaf, kemudian disusun media dan
bahan yang akan diterilkan pada keranjang alat dan dimasukkan ke dalam
autoklaf. Disterilkan pada suhu 121oC pada tekanan 15 Psi selama 15 menit
3.2.5 Pembuatan starter Pseudomonas Aeruginosa
Dimasukkan media tripton yang telah steril ke dalam cawan petri sebanyak ¼
volume cawan lalu diinokulasi biakan murni bakteri Pseudomonas Aeruginosa
ke dalam media tripton, yang dilakukan pada kondisi septik, selanjutnya
ditutup dengan alumunium foil dan klem-bab kemudian dibalut kertas setelah
itu diinkubasi dalam inkobator pada suhu 35oC selama 3-5 hari hingga
3.2.6 Pembuatan Standard Mac Varlan
Diukur 0,05 mL BaCl2 0,048 M dan dimasukkan ke dalam tabung reaksi,
ditambahkan 9,95 mL H2SO4 0,35 N kemudian ditutup dengan alumunium foil
dan divortex. (Larlan,V, 1980)
3.2.7 Pembuatan Mac Varlan Bakteri Pseudomonas Aeruginosa
Dipipet 10 mL air suling steril ke dalam tabung reaksi. Diinokulasi bakteri
Pseudomonas Aeruginosa ke dalam tabung setelah itu divortex dan dilakukan
hal yang sama dalam kondisi septik hingga larutan bakteri sesuai dengan
standar Mac Varlan.
3.2.8 Penanaman bakteri pada media cair
Dipipet sebanyak 20 mL media cair dan dimasukkan ke dalam botol essence
50 mL, kemudian dimasukkan Sebanyak 2 mL larutan Mac Varlan dari bakteri
Pseudomonas Aeruginosa dan ditambahkan induser minyak wijen steril
dengan konsentrasi 2 % dalam kondisi septik, ditutup rapat botol dalam
keadaan terbungkus klem-bab. Dishaker media dengan kecepatan 150 rpm
pada suhu ruang selama 72 jam. Dilakukan prosedur yang sama untuk variasi
konsentrasi induser 4, 6, 8, dan 10%.
3.2.9 Penanaman bakteri pada media cair dengan penambahan kofaktor enzim Ca2+
Dipipet sebanyak 20 mL media cair dengan kofaktor enzim Ca2+ dan
dimasukkan ke dalam botol essence 50 mL, kemudian dimasukkan Sebanyak 2
mL larutan Mac Varlan dari bakteri Pseudomonas Aeruginosa dan
ditambahkan induser minyak wijen steril dengan konsentrasi 2 % dalam
kondisi septik, ditutup rapat botol dalam keadaan terbungkus klem-bab.
Dishaker media dengan kecepatan 150 rpm pada suhu ruang selama 72 jam.
Dilakukan prosedur yang sama untuk variasi konsentrasi induser 4, 6, 8, dan
3.2.10 Pembuatan Ekstrak Kasar Enzim Lipase
Dipipet sebanyak 10 mL media hasil penanaman berdasarkan masing-masing
konsentrasi induser dan dimasukkan ke dalam tabung sentrifuse, kemudian
disentrifuse dengan kecepatan 6000 rpm selama 20 menit; didekantasi
supernatan yang terbentuk. Dan diuji kadar protein dan aktivitasnya.
3.3 Parameter yang Diamati
3.3.1 Penentuan absorbansi maksimum larutan Bovine Serum Albumin 5000µg/mL
Dipipet 1 mL larutan larutan BSA 5000 µg/mL dan dimasukkan ke dalam
tabung reaksi. Ditambahkan 6 mL pereaksi C Lowry dikocok dan dibiarkan
selama 10 menit pada suhu kamar. Selanjutnya ditambahkan 0,5 mL larutan
Folin-Ciocalteu, dikocok dan dibiarkan selama 30 menit. Diukur
absorbansinya pada panjang gelombang 730 – 780 nm untuk menetukan
panjang gelombang dengan absorbansi maksimum. Grafik hasil absorbansi
dapat dilihat pada hasil penelitian (halaman 36-37)
3.3.2 Penentuan Kurva standard larutan Bovine Serum Albumin
Dipipet 1 mL larutan larutan dari masing-masing larutan BSA dengan
konsentrasi 50, 100, 150, 200, 250, 300, 350 µg/mL dan masing-masing
dimasukkan ke dalam tabung reaksi dan dtambahkan 6 mL pereaksi C Lowry
dikocok dan dibiarkan selama 10 menit pada suhu kamar. Selanjutnya
ditambahkan 0,5 mL larutan Folin-Ciocalteu, dikocok dan dibiarkan selama 30
menit. Diukur absorbansinya pada panjang gelombang 775 nm kemudian
dibuat kurva standarnya.
3.3.3 Penentuan Kadar Protein Ekstrak Kasar Enzim Lipase Ekstraseluler
Pseudomonas Aeruginosa
Dipipet 1 mL larutan enzim dari masing-masing supernatant tiap-tiap
perlakuan dan dimasukkan ke dalam tabung reaksi. Ditambahkan 6 mL
pereaksi C Lowry dikocok dan dibiarkan selama 10 menit pada suhu kamar.
Selanjutnya ditambahkan 0,5 mL larutan Folin-Ciocalteu, dikocok dan
775 nm. Dihitung kadar protein dengan menggunakan kurva standar (Boyer,
1993).
3.3.4 Penentuan kadar Asam Lemak Bebas
Ditimbang sampel minyak wijen seberat 2,5 g, dimasukkan ke dalam
Erlenmeyer, ditambahkan 1 mL ekstrak kasar enzim lipase dan ditambahkan
25 mL Alkohol 96%, ditutup dengan plastic dan karet dan dipanaskan hingga
mendidih kemudian didinginkan. Ditambahkan 3 tetes indicator Penolftalein.
Kemudian dititrasi dengan larutan KOH 0,001 N hingga terjadi perubahan
warna dari bening menjadi merah rose dan dicatat volume KOH 0,001 N yang
3.4 Skema Penelitian
3.4.1 Skema Pembuatan Media
3.4.1.1 Skema Pembuatan Media Tripton
Dimasukkan ke dalam gelas Erlenmeyer 250 mL
Ditambahkan 100 mL air laut
Dipanaskan di atas hot plate hingga mendidih
Didinginkan
Ditutup dengan kapas dan alumunium foil
Disterilkan dalam autoklaf pada suhu 121oC dan
tekanan 15 Psi selama 15 menit. 4 g Tripton Soya Agar (s)
3.4.1.2 Skema Pembuatan Media Cair
Dimasukkan ke dalam botol duran 500 mL
Ditambahkan 0,1 g MgSO4.7H2O (s)
Ditambahkan 4,1698 g KH2PO4 (s)
Ditambahkan 3,3652 g K2HPO4 (s)
Ditambahkan 500 mL akuades
Dimasukkan stirrer dan Ditutup rapat
Disterilkan dalam autoklaf pada suhu 121oC dan
tekanan 15 Psi selama 15 menit
3.4.1.3 Skema Pembuatan Media Cair dengan penambahan Kofaktor enzim Ca2+
Dimasukkan ke dalam botol duran 500 mL
Ditambahkan 7,5 g CaCl2.2H2O (s),
Ditambahkan 0,1 g MgSO4.7H2O (s)
Ditambahkan 4,1698 g KH2PO4 (s)
Ditambahkan 3,3652 g K2HPO4 (s)
Ditambahkan 500 mL akuades
Dimasukkan stirrer dan Ditutup rapat
Disterilkan dalam autoklaf pada suhu 121oC dan
tekanan 15 Psi selama 15 menit. 1,5 g NH4NO3 (s)
Hasil 1,5 g NH4NO3 (s)
3.4.2 Skema Pembuatan starter Pseudomonas Aeruginosa
Disterilkan didalam autoklaf
Dimasukkan ke dalam cawan petri sebanyak ¼
volume cawan
Diinokulasi biakan murni bakteri Pseudomonas
Aeruginosa ke dalam media tripton.
Ditutup dengan alumunium foil dan klem-bab
lalu dibalut kertas
Diinkubasi dalam inkobator pada suhu 35oC
selama 4-5 hari Media Triptonl (l)
3.4.3 Skema Penanaman media untuk menghasilkan ekstrak kasar enzim 3.4.3.1 Skema Penanaman bakter pada media cair
Dipipet sebanyak 20 mL Dipipet sebanyak 2 mL
Ditambahkan induser minyak wijen
dengan variasi 2%, 4%, 6%, 8%, 10%.
Ditutup rapat dan dibungkus klem-bab
Dishaker dengan kecepatan 150 rpm
pada suhu 25oC selama 72 jam
Disentrifuse dengan kecepatan 6000 rpm
selama 20 menit
Didekantasi supernatan yang terbentuk.
Dibagi dua
Diukur kadar protein Diuji aktivitasnya dengan
Dengan menggunakan penentuan kadar Asam
Spektrofotomoter UV-Visible Lemak Bebas Media cair (l) Larutan Mac Varlan Bakteri
Pseudomonas Aeruginosa (l)
Ekstrak kasar Enzim Lipase
Campuran Ekstrak dan Media
Hasil 1 mL Ekstrak
kasar enzim
Larutan Media bakteri
1 mL Ekstrak kasar enzim
Endapan sel bakteri
3.4.3.2 Skema Penanaman bakteri pada media cair dengan penambahan kofaktor enzim Ca2+
Dipipet sebanyak 20 mL Dipipet sebanyak 2 mL
Ditambahkan induser minyak wijen
dengan variasi 2%, 4%, 6%, 8%, 10%.
Ditutup rapat dan dibungkus klem-bab
Dishaker dengan kecepatan 150 rpm
pada suhu 25oC selama 72 jam
Disentrifuse dengan kecepatan 6000 rpm
selama 20 menit
Didekantasi supernatan yang terbentuk.
Dibagi dua
Diukur kadar protein Diuji aktivitasnya dengan
Dengan menggunakan penentuan kadar Asam
Spektrofotomoter UV-Visible Lemak Bebas Media cair dengan
kofaktor enzim
2+
Larutan Mac Varlan Bakteri Pseudomonas Aeruginosa (l)
Ekstrak kasar Enzim Lipase
Campuran Ekstrak dan Media
Hasil 1 mL Ekstrak
kasar enzim
Larutan Media bakteri
1 mL Ekstrak kasar enzim
Endapan sel bakteri
3.4.4 Skema Parameter yang diamati
3.4.4.1 Skema Penentuan absorbansi maksimum larutan BSA 5000µg/mL
Diukur sebanyak 1 mL
Dimasukkan ke dalam tabung reaksi
Ditambahkan 6 mL pereaksi C Lowry
Dikocok dan dibiarkan selama 10 menit
pada suhu kamar
Ditambahkan 0,5 mL larutan
Folin-Ciocalteu
Dikocok dan dibiarkan selama 30 menit
Diukur absorbansi maksimumnya pada
panjang gelombang 730 – 780 nm
3.4.4.2 Skema Penentuan Kurva standard larutan Bovine Serum Albumin
Diukur masing-masing sebanyak 1 mL
Dimasukkan ke dalam tabung reaksi
Ditambahkan 6 mL pereaksi C Lowry
Dikocok dan dibiarkan selama 10 menit
pada suhu kamar
Ditambahkan 0,5 mL larutan
Folin-Ciocalteu
Dikocok dan dibiarkan selama 30 menit
Diukur absorbansi pada panjang
gelombang 775 nm Larutan BSA 5000µg/mL
Hasil
Larutan BSA konsentrasi 50, 100, 150, 200, 250, 300, 350 µg/mL
3.4.4.3 Skema Penentuan Kadar Protein Ekstrak Kasar Enzim Lipase Ekstraseluler Pseudomonas Aeruginosa
Diukur masing-masing sebanyak 1 mL
Dimasukkan ke dalam tabung reaksi
Ditambahkan 6 mL pereaksi C Lowry
Dikocok dan dibiarkan selama 10 menit
pada suhu kamar
Ditambahkan 0,5 mL larutan
Folin-Ciocalteu
Dikocok dan dibiarkan selama 30 menit
Diukur absorbansi pada panjang
gelombang 775 nm
Dihitung kadar protein dengan
menggunakan kurva standar Supernatan enzim lipase
3.4.4.4 Skema Penentuan Kadar Asam Lemak Bebas
Dimasukkan ke dalam gelas Erlenmeyer
Ditambahkan 1 mL ekstrak kasar enzim
lipase
Ditambahkan 25 mL Alkohol 96%
Ditutup dengan pelastik dan karet
Dipanaskan hingga mendidih dan
didinginlan
Ditambahkan 3 tetes indicator PP
Dititrasi dengan KOH 0,001 N sampai
terjadi perubahan warna dari bening
menjadi merah rose.
Dihitung volume KOH yang terpakai 2,5 g minyak wijen
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
Dari hasil penelitian tentang produksi enzim lipase oleh Pseudomonas aeruginosa
dalam menghasilkan ekstrak kasar enzim lipase dilakukan beberapa penentuan
4.1.1. Penentuan panjang gelombang maksimum larutan BSA
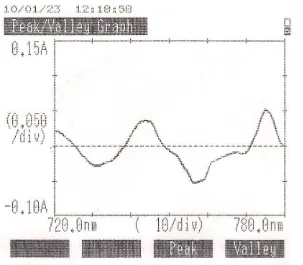
Terhadap 1 mL larutan BSA 5000 µg/mL dengan metode lowry diukur absorbansinya
pada panjang gelombang 720 – 780 nm. Hasilnya menunjukkan bahwa absorbansi
[image:53.595.166.469.506.771.2]maksimum diperoleh pada λ 775 nm. Hasil lengkapnya adalah sebagai berikut :
4.1.2. Penentuan kurva standar larutan BSA pada λ 775 nm
Larutan BSA dengan konsentrasi bertingkat diukur absorbansinya pada panjang
[image:55.595.106.540.231.418.2]gelombang 775 nm. Hasilnya sebagai berikut :
Tabel 4.1.2. Absorbansi larutan BSA pada λ 775 nm
Konsentrasi BSA (μgg/mL) (x)
Absorbansi (y)
50 0,067
100 0,070
150 0,075
200 0,073
250 0,074
300 0,074
350 0,087
Dengan menggunakan rumus persamaan garis regresi y = ax + b diperoleh
nilai
y = 0,00004(x) + 0,065 (Lampiran 1), dimana x adalah kadar ekstrak kasar enzim lipase dengan tetapan a (slope grafik) dan b (intercept) yang diperoleh dari:
( ) ( )( )
( )
2( )
2∑
∑
∑
∑
∑
− − = x x n y x xy n a( )( ) ( )( )
( ) ( )
2 2 2∑
∑
∑
∑
∑
∑
− − = x x n xy x y x b4.1.3 Penentuan kadar protein enzim lipase dari Pseudomonas aeruginosa
Terhadap supernatant dari biakan Pseudomonas aeruginosa yang ditumbuhkan pada
media dengan konsentrasi minyak wijen yang berbeda maka didapat masing – masing
hasil kadar enzim dengan menggunakan persamaan garis regresi y = 0.00004 (x) +
0.065 yaitu sebagai berikut :
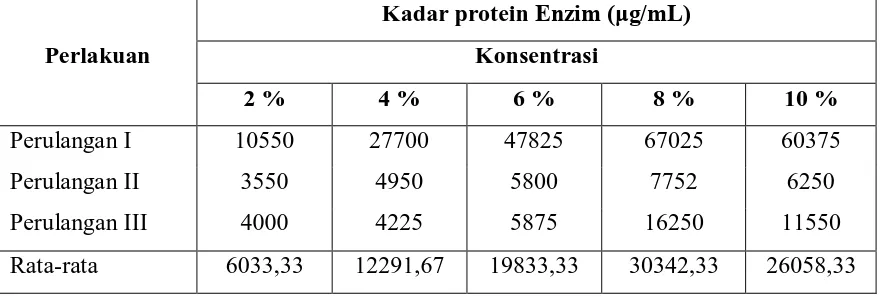
[image:56.595.97.537.210.359.2]
Tabel 4.1.3 Kadar protein enzim (μg/mL) pada setiap perlakuan untuk konsentrasi substrat 2, 4, 6, 8, 10 %.
Perlakuan
Kadar protein Enzim (μg/mL) Konsentrasi
2 % 4 % 6 % 8 % 10 %
Perulangan I 10550 27700 47825 67025 60375
Perulangan II 3550 4950 5800 7752 6250
Perulangan III 4000 4225 5875 16250 11550
Rata-rata 6033,33 12291,67 19833,33 30342,33 26058,33
4.1.4 Penentuan kadar protein enzim lipase dengan penambahan Ca2+
Pada media biakan yang ditumbuhi Pseudomonas aeruginosa ditambahkan ion Ca2+
sebagai Kofaktor enzim dengan konsentrasi 1.5% pada setiap setiap konsentrasi
substrat yang berbeda, yang pengukuran absorbansinya pada setiap konsentrasi dapat
dilihat pada (lampiran III) sehingga diperoleh hasil kadar enzim dengan menggunakan
persamaan garis regresi sebagai berikut :
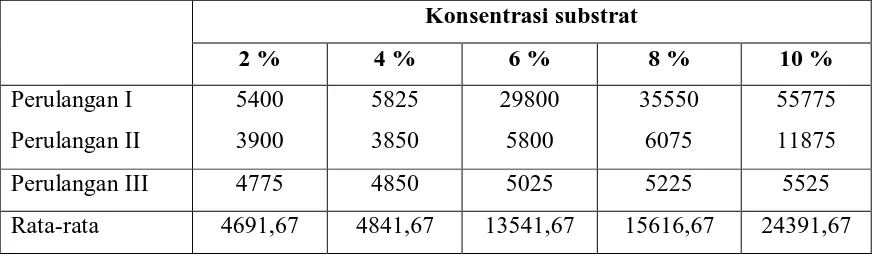
Tabel 4.1.4 Kadar protein enzim (μg/mL) pada setiap perlakuan untuk konsentrasi substrat 2, 4, 6, 8, 10 % dengan penambahan kofaktor enzim Ca2+.
Konsentrasi substrat
2 % 4 % 6 % 8 % 10 %
Perulangan I 5400 5825 29800 35550 55775
Perulangan II 3900 3850 5800 6075 11875
Perulangan III 4775 4850 5025 5225 5525
Rata-rata 4691,67 4841,67 13541,67 15616,67 24391,67
4.1.5. Uji aktivitas
Uji aktivitas terhadap ekstrak kasar enzim lipase dilakukan untuk mengetahui aktivitas
enzim dalam menggunakan asam lemak pada minyak normal. Pengukuran kadar ALB
(%) dilakukan dengan metode titrimetri dengan titran KOH. Uji aktivitas pada ekstrak
kasar enzim lipase tersebut diukur berdasarkan perbedaan kadar asam lemak bebas
dengan menggunakan: % 100 1000 × ×× × = Sampel Berat ALB BM KOH mL KOH N ALB Kadar
N KOH merupakan normalitas KOH yang digunakan ( 0,001 N)
Volume KOH adalah volume hasil titrasi
BM ALB adalah berat molekul ALB yang dihitung sebagai Oleat (Mr = 282)
Berat sampel merupakan berat dari minyak wijen yang diukur kadar ALB-nya, dan
penentuan aktivitas dalam unit dinyatakan dengan,
[image:57.595.98.537.85.215.2]sehingga diperoleh hasil sebagai berikut :
Tabel 4.1.5.1. Aktivitas ekstrak kasar Enzim Lipase
Sampel Ekstrak kasar Enzim (%) Berat Wijen (gram) Volume KOH (mL)
Rata - rata
Kadar ALB
(g ALB/g Minyak)
%
Unit
x 10-4
(µmol/menit)
I II III
Untuk uji aktivitas pada ekstrak kasar enzim lipase yang menggunakan kofaktor
enzim Ca2+ diukur dengan cara yang sama yatu berdasarkan perbedaan kadar asam
lemak bebas pada minyak wijen setelah penambahan enzim lipase yang mengandung
[image:58.595.80.550.84.192.2]kofaktor enzim Ca2+ sehingga diperoleh hasil sebagai berikut :
Tabel 4.1.5.2. Aktivitas ekstrak kasar Enzim Lipase dengan menggunakan kofaktor enzim Ca2+
Ekstrak
kasar Enzim
(%)
Berat Wijen
(gram)
Volume KOH (mL)
Rata -
rata
Kadar ALB
(g ALB/g Minyak)
%
Unit
x 10-4
µmol/menit
I II III
2 2,5 6,8 6,9 6,5 6,73 0,0759 6,23
4 2,5 7,5 7,6 7,5 7,57 0,0854 7,01
6 2,5 7,5 7,6 7,6 7,57 0,0854 7,01
8 2,5 9,6 9,8 9,6 9,67 0,1091 8,96
10 2,5 12,6 12,8 12,2 12,53 0,1413 11,60
4.2. Pembahasan Hasil Penelitian
Grafik berikut memperlihatkan hubungan antara hasil ekskresi enzim oleh
Pseudomonas aeruginosa dengan penambahan substrat dengan konsentrasi yang
berbeda dan perbedaan kadar enzim pada masing – masing perlakuan dapat dilihat
pada grafik dibawah ini.
2 2,5 8,2 8,3 8,9 8,5 0,0959 7,87
4 2,5 9,2 8,7 9,0 8,9 0,1004 8,24
6 2,5 8,8 8,9 9,1 8,9 0,1004 8,24
8 2,5 9,5 9,8 9,0 9,1 0,1026 8,42
10 2,5 8,8 8,7 8,8 8,8 0,0992 8,14
550 950 800 752 250 000 225 875 16250 550 550 700 825 67025 6037560000 70000 80000 12000 14000 16000 18000 ( μ g /m L)
Kadar enzim (
μ
g/mL) pada setiap perlakuan
untuk konsentrasi substrat 2, 4, 6, 8, 10 %.
[image:58.595.95.556.417.580.2]Grafik 4.2.1
Dari hasil di atas secara keseluruhan dapat diketahui bahwa kadar enzim pada
semua perlakuan berbeda – beda, dimana kadar ekstrak kasar enzim tertinggi
diperoleh pada perlakuan konsentrasi substrat minyak wijen 8%, baik pada perlakuan
I, perlakuan II, dan perlakuan III yang masing – masing yaitu 67025 μg/mL, 7752
μg/mL, 16250 μg/mL yang berbeda sangat nyata dibandingkan dengan konsentrasi
awal penambahan substrat. Hal ini menunjukkan bahwa aktivitas metabolisme
Pseudomonas aeruginosa yang tertinggi pada masa inkubasi optimum-nya selama 72
jam (Priyani, N, 2001) dapat dicapai dengan konsentrasi penambahan substrat
sebanyak 8%. Hal ini kemungkinan disebabkan oleh beberapa hal antara lain.
Konsentrasi substrat 8% merupakan konsentrasi optimum bagi Pseudomonas
aeruginosa untuk menghasilkan enzim lipase ekstrasel dimana selama waktu
perulangan tetap menunjukkan bahwa pada konsentrasi substrat 8% bakteri
menghasilkan lipase secara maksimal. Hal ini ditunjukkan oleh kadar enzim yang
mengalami penurunan pada konsentrasi substrat 10%, pada konsentrasi ini
kemungkinan lapisan minyak cukup menghalangi difusi oksigen ke dalam media yang
dapat mengganggu metabolisme bakteri (Wardhana, 1995) mengingat minyak yang
tersedia masih cukup dan Pseudomonas aeruginosa merupakan bakteri aerob yang
sangat membutuhkan oksigen dalam kelangsungan proses metabolismenya (Tim
Mikrobiologi, Fakultas Kedokteran Universitas Brawijaya,2003) sehingga membuat
Grafik berikut memperlihatkan hubungan antara hasil ekskresi enzim oleh
Pseudomonas aeruginosa pada substrat dengan adanya penambahan kofaktor enzim