i
FERMENTASI GLISEROL HASIL SAMPING PABRIK
BIODISEL MENJADI 1,3-PROPANADIOL DENGAN
MENGGUNAKAN BAKTERI KLEBSIELLA
PNEUMONIAE
SKRIPSI
Oleh
100405032
JEKKY BAHAGIA G
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
ii
FERMENTASI GLISEROL HASIL SAMPING PABRIK
BIODISEL MENJADI 1,3-PROPANADIOL DENGAN
MENGGUNAKAN BAKTERI KLEBSIELLA
PNEUMONIAE
SKRIPSI
Oleh
100405032
JEKKY BAHAGIA G
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN M ENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
i
PERNYATAAN KEASLIAN SKRIPSI
Saya menyatakan dengan sesungguhnya bahwa skripsi dengan judul:
FERMENTASI GLISEROL HASIL SAMPING PABRIK BIODISEL
MENJADI 1,3 PROPANADIOL DENGAN MENGGUNAKAN BAKTERI
KLEBSIELLA PNEUMONIA
yang dibuat untuk melengkapi sebagian persyaratan menjadi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara, sejauh yang saya ketahui bukan merupakan tiruan atau duplikasi dari skripsi yang sudah dipublikasikan dan atau pernah dipakai untk mendapatkan gelar kesarjanaan di lingkungan Universitas Sumatera Utara maupun di Perguruan Tinggi atau instansi manapun, kecuali bagian yang sumber informasinya dicantumkan sebagaimana mestinya.
Medan, September 2014
i
PENGESAHAN
Skripsi dengan judul:
FERMENTASI GLISEROL HASIL SAMPING PABRIK BIODISEL
MENJADI 1,3 PROPANADIOL DENGAN MENGGUNAKAN BAKTERI
KLEBSIELLA PNEUMONIA
dibuat sebagai kelengkapan persyaratan untuk mengikuti ujian skripsi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara.
Medan, September 2014
Mengetahui,
Koordinator Skripsi
NIP. 19681214 199702 2 002 Ir. Renita Manurung, MT
Dosen Pembimbing
NIP. 19640617 199403 2 001 Dr. Ir. Dr.Ir. Fatimah, MT
Dosen Penguji I, Dosen Penguji II,
Ir. Bambang Trisakti, MT
ii
PRAKATA
Puji dan syukur kehadirat Tuhan Yang Maha Esa karena atas rahmat-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan skripsi dengan judul “Fermentasi Gliserol Hasil Samping Pabrik Biodiesel Menjadi 1,3-Propanadiol Dengan Menggunakan Bakteri Klebsiella Pneumonia”, berdasarkan hasil penelitian yang penulis lakukan di Laboratorium Bioproses Pusat Penelitian Kelapa Sawit (PPKS) Medan. Skripsi ini merupakan salah satu syarat untuk mendapatkan gelar sarjana teknik.
Selama melakukan penelitian hingga penulisan skripsi ini, penulis banyak mengucapkan terima kasih yang sebesar-besarnya kepada:
Dr. Ir. Fatimah, MT
selaku dosen pembimbing yang telah bersedia meluangkan waktu untuk memberi pengarahan, diskusi dan bimbingan serta persetujuan sehingga skripsi ini dapat selesai dengan baik.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh karena itu penulis mengharapkan saran dan masukan demi kesempurnaan skripsi ini. Semoga skripsi ini memberikan manfaat bagi pengembangan ilmu pengetahuan.
Medan, September 2014 Penulis,
iii
DEDIKASI
Penulis mendedikasikan skripsi ini kepada :
1. Kedua orang tua penulis, S. Ginting dan S. Br. Simangunsong.
2. Dewi Anggraini atas kerjasamanya selama melakukan penelitian dan penulisan skripsi ini.
3. Abangnda Bones dan Fian dan Adik Mendra yang selalu memberikan dukungan dan doanya.
4. Kakak Dila dan Melva yang selalu mendukung dan memberikan doa buat penulis.
5. Keponakan-keponakan tercinta (Nurah, Yosepin, Yohana, Piros, dan Axaria) buat kecerian kalian semua.
6. Bibi, Kila, Paktengah, Maktengah, Bolang, Iting, dan semua keluarga besar penulis, penulis mengucapkan beribu-ribu terima kasih atas cinta, kasih sayang, dukungan dan doa yang telah kalian panjatkan buat penulis.
7. Sahabat-sahabat terbaik di Teknik Kimia stambuk 2010, terkhusus Deril Clinton, Margareth N, Popphy Prawati, Ruben Simanggunsong, Rap Leanon, Rika Silvia dan Jernika Simanggunsong yang telah memberikan banyak dukungan dan semangat kepada penulis.
iv
RIWAYAT HIDUP PENULIS
Nama : Jekky Bahagia G
NIM : 100405032
Tempat, tanggal lahir : Torgamba, 26 November 1991 Nama orang tua : S. Ginting dan
S. Br. Simangunsong Alamat orang tua :
PKS 1 Torgamba, Kec. Torgamba, Kab. Labuhan Batu Selatan, Provinsi Sumatera Utara
Asal Sekolah:
• SD N 116881 Torgamba tahun 1997-2003 • SMP Swasta Torgamba tahun 2003 – 2006 • SMA Santo Yoseph Medan tahun 2006 – 2009
Beasiswa yang diperoleh:
Beasiswa PPA tahun 2011, 2012, 2013 Universitas Sumatera Utara Pengalaman Organisasi:
1. Sekretaris Umum Himpunan Mahasiswa Teknik Kimia (HIMATEK) FT USU periode 2013/2014.
2. Asisten Laboratorium Proses Industri Kimia Departemen Teknik Kimia FT USU tahun 2013-2014 modul Pembuatan Pulp dan Biodiesel.
Artikel yang telah dipublikasikan dalam jurnal:
1. Fermentation of Glycerol from Biodiesel Waste to 1,3-Propanadiol by
Klebsiella Pneumoniaepada seminar “5thSriwijayaInternasionalSeminar On Energy Enviromental Science
and Technology (SISEEST 5th) 2014” yang akanberlangsung di Palembang, pada 10-11 September 2014.
2. Fermentation of Glycerol from Biodiesel Waste to 1,3-Propanadiol by
EnterobacterAerogenespada seminar “5thSriwijayaInternasionalSemonar On Energy Enviromental Science
v ABSTRAK
Salah satu produk fermentasi tertuadarigliserol adalah 1,3-Propanadiol. Pada penelitian ini, 1,3 Propanadiol dihasilkan dari proses fermentasi gliserol dengan bantuan bakteri klebsiella pneumoniae dengan variasi volume bakteri 5, 7, dan 10 %, pada waktu fermentasi 1, 2 dan 3 hari, dengan suhu 25 dan 37 0C. Hasil fermentasi gliserol dianalisa dengan menggunakan kromatografi gas dengan kolom DB 5 HT untuk mengetahui kemurnian 1,3 Propanadiol yang dihasilkan berdasarkan larutan standart 1,3 Propanadiol. Crude gliserol memiliki warna coklat kemerahan, densitas 1,24 gr/ml, FFA 26,22 %, kadar air 2,64 %, kadar abu 11 % dan kemurnian sebesar 29,306 %, sedangkan hasil pemurnian crude gliserol menghasilkan gliserol dengan warna bening, densitas 1,2676 gr/ml, FFA 0,92 %, kadar air 1,265 %, kadar abu 6 % dan kemurnian sebesar 93,1924 %. Berdasarkan analisa kromatografi gas didapat rentang waktu Propanadiol berada pada 4,846 menit. Konsentrasi 1,3-Propanadiol pada 1, 2 dan 3 hari yaitu 14,0963; 14,6330; dan 17,6093mol/ml. Konsentrasi 1,3 Propanadiol pada penambahan volume bakteri 5, 7, dan 10 % (v/v) yaitu 15,0952; 17,3287; dan 17,6093 mol/ml. Sedangkan konsentrasi 1,3-Propanadiol pada suhu 25 dan 37 0C adalah 14,9892 dan 17,6093mol/ml.
vi ABSTRACT
vii
DAFTAR ISI
Halaman
PERNYATAAN KEASLIAN SKRIPSI i
PENGESAHAN ii
PRAKATA iii
DEDIKASI iv
RIWAYAT HIDUP PENULIS v
ABSTRAK vi
ABSTRACT vii
DAFTAR ISI viii
DAFTAR GAMBAR xi
DAFTAR TABEL xiii
DAFTAR LAMPIRAN xiv
DAFTAR SINGKATAN xv
DAFTAR SIMBOL xvi
BAB I PENDAHULUAN 1
1.1 LATAR BELAKANG 1
1.2 PERUMUSAN MASALAH 3
1.3 TUJUAN PENELITIAN 4
1.4 MANFAAT PENELITIAN 4
1.5 RUANG LINGKUP PENELITIAN 4
BAB II TINJAUAN PUSTAKA 6
2.1 GLISEROL 6
2.2 PURIFIKASI GLISEROL 7
2.3FERMENTASI GLISEROL 8
2.4INOKULASI BAKTERI 10
2.5KLEBSIELLA PNEUMONIAE 11
2.6 SINTESIS 1,3 PROPANADIOL 11
2.7 SEPERASI HASIL FERMENTASI 14
2.8GAS KROMATOGRAFI 15
2.9ANALISA EKONOMI 16
viii
3.1 LOKASI PENELITIAN 18
3.2 BAHAN 18
3.2.1 Bahan Baku 18
3.2.2 BahanPurifikasiGliserol 18
3.2.3 BahanPembuatan Media KulturStok 18 3.2.4 Bahan Media PerhitunganJumlahBakteri Yang Tumbuh 18
3.2.5 BahanAnalisa 19
3.2.5.1 BahanAnalisa Kadar Air Gliserol 19 3.2.5.2 BahanAnalisaDensitasGliserol 19
3.2.5.3 BahanAnalisa Kadar Abu 19
3.2.5.4 BahanAnalisaFree Fatty Acid (FFA) Gliserol 19
3.2.5.5 AnalisaKromatografiGas 19
3.3 PERALATAN 20
3.4 PROSEDUR PENELITIAN 21
3.4.1 ProsedurPurifikasiGliserol 21
3.4.2 Prosedur AnalisaGliserol 21
3.4.3 Penentuan Kadar Free Fatty Acid (FFA) Gliserol 21
3.4.4 PenentuanDensitasGliserol 23
3.4.5 Penentuan Kadar Air Gliserol 23
3.4.6 Penentuan Kadar Abu Gliserol 23
3.4.7 Pembuatan Media Pertumbuhan 24
3.4.8 PembuatanKulturStok 24
3.4.9 ProsedurPerhitunganJumlahBakteri 24
3.4.10 ProsedurFermentasi 25
3.4.11 Analisa 1,3 Propanadiol 25
3.5 FLOWCHART PENELITIAN 26
3.5.1 PurifikasiGliserol 26
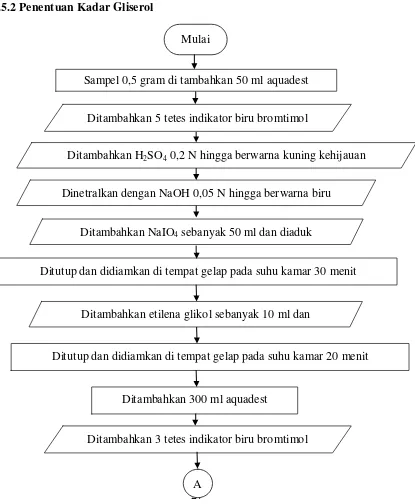
3.5.2 Penentuan Kadar Gliserol 27
3.5.3 Penentuan Kadar Free Fatty Acid (FFA) Gliserol 28
3.5.4 PenentuanDensitasGliserol 29
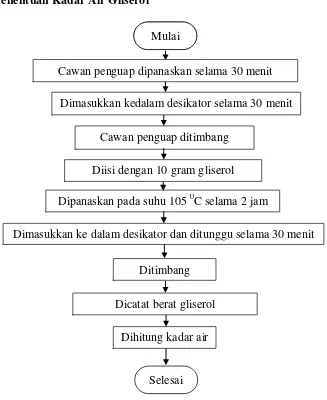
3.5.5 Penentuan Kadar Air Gliserol 30
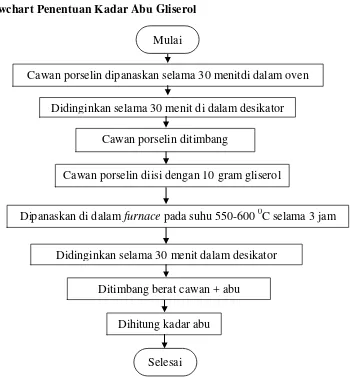
3.5.6 Penentuan Kadar Abu Gliserol 31
3.5.7 Pembuatan Media Pertumbuhan 32
ix
3.5.9 PerhitunganJumlahBakteri 33
3.5.10 FermentasiGliserol 34
BAB IV HASIL DAN PEMBAHASAN 35
4.1 PEMURNIAN GLISEROL 35
4.2 ANALISA GLISEROL 37
4.3 FERMENTASI GLISEROL 38
4.3.1 KonversiGliserol 39
4.3.2 PengaruhWaktuFermentasiTerhadapKonsentrasi
1,3-PropanadiolTerbentuk 41
4.3.3 Pengaruh Volume InokulumBakteriTerhadapKonsentrasi
1,3-PropanadiolTerbentuk 43
4.3.4 PengaruhSuhuFermentasiTerhadapKonsentrasi
1,3-PropanadiolTerbentuk 45
BAB V KESIMPULAN DAN SARAN 47
5.1 KESIMPULAN 47
5.2 SARAN 47
x
DAFTAR GAMBAR
Halaman
Gambar 2.1Skema Proses Fermentasi 9
Gambar 2.2BakteriKlebsiella Pnemonia 11
Gambar 2.3BiokonveksiGliserolmenjadi 1,3-Propandiol 12 Gambar 2.4PerombakanGliserolmenjadi 1,3-Propandiol 13
Gambar 3.1 Flowchart PurifikasiGliserol 26
Gambar 3.2 Flowchart Penentuan Kadar Gliserol 27
Gambar 3.3 Flowchart Penentuan Kadar FFA 28
Gambar 3.4 Flowchart PenentuanDensitasGliserol 29 Gambar 3.5 Flowchart Penentuan Kadar Air Gliserol 30 Gambar 3.6 Flowchart Penentuan Kadar Abu Gliserol 31 Gambar 3.7 Flowchart Pembuatan Media Pertumbuhan 32
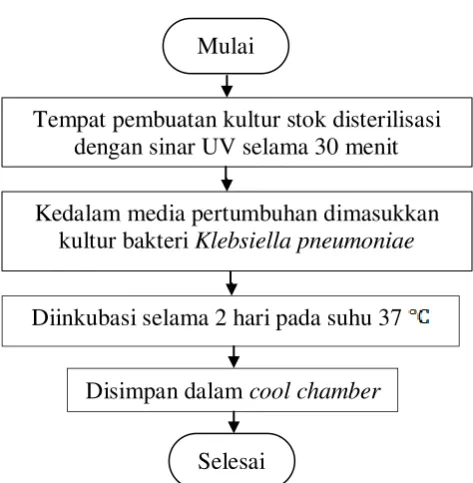
Gambar 3.8 Flowchart PembuatanKulturStok 33
Gambar 3.9 Flowchart PerhitunganJumlahBakteri 33 Gambar 3.10 Flowchart FermentasiGliserol 34 Gambar 4.1 Proses PengasamanCrudeGliseroldenganAsamSulfat 35 Gambar 4.2 Garam yang TerbentukSetelahPemanasan 36
Gambar 4.3 GliserolHasilPemurnian 37
Gambar 4.4 KulturStokSebelumPembiakandanSesudahPembiakan 38 Gambar 4.5 Pengenceran Bakteri Klebsiella Pnemonia 39 Gambar 4.6 Kadar Gliserolpada Proses FermentasiPadaSuhu 25 0C
maupun 370C 40
xi
Gambar L1.3 HasilFermentasiGliserol 1 hari, 37 , 10% 54 Gambar L1.4 HasilFermentasiGliserol 3 hari, 25 , 10% 54 Gambar L1.5 HasilFermentasiGliserol 2 hari, 37 , 10% 55 Gambar L1.6 HasilFermentasiGliserol 3 hari, 37 , 5% 55 Gambar L1.7 HasilFermentasiGliserol 3 hari, 37 , 10% 56 Gambar L1.8 HasilFermentasiGliserol 3 hari, 37 , 7% 56
Gambar L3.1 CrudeGliserol 63
Gambar L3.2 HasilPenambahanAsamPhospat 63
Gambar L3.3 Garam Yang TerbentukPada Proses Pemurnian Crude
Gliserol 63
Gambar L3.4 GliserolMurni 64
Gambar L3.5 Autoclave 64
Gambar L3.6 Proses Sterilisasi Media Pertumbuhan 64
Gambar L3.7 Proses InokulasiBakteri 64
Gambar L3.8 PembiakanBakteriDalamWater Batch 65
Gambar L3.9 Pengenceran 108 65
Gambar L3.10 PerhitunganJumlahKoloniDenganColoni Counter 65 Gambar L3.11 HasilTitrasiPenentuan Kadar Gliserol 65
Gambar L3.12 Proses Distilasi 66
xii
DAFTAR TABEL
Halaman
Tabel 1.1 ProduksidanKonsumsiMinyak Diesel 1
Tabel 1.2 Penelitian Yang Menggunakan Crude Gliserol sebagai Bahan Baku 2 Tabel 1.3 Daftar Penelitian Pembuatan 1,3-Propanadiol Terdahulu 3 Tabel 2.1 Daftar Beberapab Sifat Komponen Yang Terdapat pada
Proses Fermentasi 14
Tabel 3.1 Program Pengatur GC 20
Tabel 4.1 Perbandingan Sifat Fisika Crude Gliserol dengan Gliserol Murni 37
Tabel L1.1 Kadar Gliserol SetelahFermentasi 56
xiii
DAFTAR LAMPIRAN
Halaman
LAMPIRAN 1 HASIL ANALISA 53
L1.1 CRUDE GLISEROL 53
L1.2 GLISEROL MURNI 53
L1.3 HASIL FERMENTASI 54
L1.4 KADAR GLISEROL SETELAH FERMENTASI 57
LAMPIRAN 2 PERHITUNGAN 58
L2.1 CRUDE GLISEROL 58
L2.1.1 Densitas 58
L2.1.2 Kadar Air 58
L2.1.3 Kadar Abu 59
L2.1.4 Kadar Free fatty Acid (FFA) 59
L2.2 GLISEROL MURNI 60
L2.2.1 Densitas 60
L2.2.2 Kadar Air 60
L2.2.3 Kadar Abu 61
L2.2.4 Kadar Free fatty Acid (FFA) 61
L2.3 KADAR GLISEROL SETELAH FERMENTASI 61
xiv
DAFTAR SINGKATAN
BPOM BadanPengawasanObatdanMakanan
FFA Free Fatty Acid
GC Gas Chromatography
PTT Polytrimethylene Terephthalate
PPKS PusatPenelitianKelapaSawit
xv
DAFTAR SIMBOL
Simbol Keterangan Dimensi
T Suhu ºC
T1 Volume titrasi ml
T2 Volume titrasi blanko ml
N Normalitas NaOH N
M Massa gram
W Bobot contoh gram
v ABSTRAK
Salah satu produk fermentasi tertuadarigliserol adalah 1,3-Propanadiol. Pada penelitian ini, 1,3 Propanadiol dihasilkan dari proses fermentasi gliserol dengan bantuan bakteri klebsiella pneumoniae dengan variasi volume bakteri 5, 7, dan 10 %, pada waktu fermentasi 1, 2 dan 3 hari, dengan suhu 25 dan 37 0C. Hasil fermentasi gliserol dianalisa dengan menggunakan kromatografi gas dengan kolom DB 5 HT untuk mengetahui kemurnian 1,3 Propanadiol yang dihasilkan berdasarkan larutan standart 1,3 Propanadiol. Crude gliserol memiliki warna coklat kemerahan, densitas 1,24 gr/ml, FFA 26,22 %, kadar air 2,64 %, kadar abu 11 % dan kemurnian sebesar 29,306 %, sedangkan hasil pemurnian crude gliserol menghasilkan gliserol dengan warna bening, densitas 1,2676 gr/ml, FFA 0,92 %, kadar air 1,265 %, kadar abu 6 % dan kemurnian sebesar 93,1924 %. Berdasarkan analisa kromatografi gas didapat rentang waktu Propanadiol berada pada 4,846 menit. Konsentrasi 1,3-Propanadiol pada 1, 2 dan 3 hari yaitu 14,0963; 14,6330; dan 17,6093mol/ml. Konsentrasi 1,3 Propanadiol pada penambahan volume bakteri 5, 7, dan 10 % (v/v) yaitu 15,0952; 17,3287; dan 17,6093 mol/ml. Sedangkan konsentrasi 1,3-Propanadiol pada suhu 25 dan 37 0C adalah 14,9892 dan 17,6093mol/ml.
vi ABSTRACT
1
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Biodiesel merupakan hasil reaksi transesterifikasi minyak nabati atau hewani dengan metanol dalam suatu kondisi tekanan dan suhu tertentu dengan menggunakan katalis basa. Reaksi transesterifikasi ini menghasilkan senyawa ester metil asam lemak yang merupakan biodiesel itu sendiri dan crude gliserol sebagai produk samping atau limbahnya [1].
Crude gliserol sebagai produk hasil samping pembuatan biodiesel memiliki nilai ekonomis yang rendah karena mengandung impurities seperti metanol, asam lemak (sebagai sabun) dan garam [2]. Nilai ekonomi dari crude gliserol ini dapat ditingkatkan dengan melakukan pretreatment yaitu proses pemurnian. Produksi crude gliserol akan meningkat seiring dengan meningkatnya produksi biodisel. Menurut laporan DitJen Migas (1998) kebutuhan bahan bakar diesel meningkat setiap tahunnya seperti disajikan pada tabel 1.1 di bawah ini.
Tabel 1.1 Produksi dan Konsumsi Minyak Diesel [3] Tahun Minyak Diesel (juta liter)
Produksi Konsumsi
1994/1995 11.866,2 16.342
1995/1996 13.465,1 17.621,5
1996/1997 14.345 19.706,2
1997/1998 15.673,9 22.092,1
1998/1999 16.208,9 22.423,4
2
Tabel 1.2 Penelitian Yang Menggunakan Crude Gliserol sebagai Bahan Baku
Referensi/Judul Proses Hasil
Fan, Xiaohun., dkk. 2010
“Glycerol (Byproduct of Biodiesel Production) as a Source for Fuels and Chemicals – Mini
Review”
Fermentasi
Bahan bakar dan kimia
Drozdzynzka, dkk. 2011
“Biotechnological production of 1,3-propanediol from crude glycerol”
Fermentasi 1,3 Propanadiol Jalansutram, dkk. 2011
“Optimization of 1, 3-Propanediol production by
Klebsiella pneumoniae 141B using Taguchi methodology: Improvement in production by
cofermentation studies”
Fermentasi 1,3
Propanadiol
Saisaard, dkk. 2011
“Micro-aerobic, Anaerobic and two stage condition for Ethanol Production by Enterobacter aerogenes from Biodisel-derived
Crude glycerol”
Fermentasi Ethanol
Salah satu produk nilai tambah tinggi yang dapat dengan mudah dibuat dari gliserol adalah 1,3-propanadiol. Mikroba yang dapat mengkonversi gliserol menjadi 1,3-propanadiol pertama kali diisolasi dan dikarakteristikan oleh Agustus Freund [4]. Sejak itu, banyak mikroorganisme alami yang mampu menghasilkan 1,3-propanadiol. Beberapa peneliti yang telah menggunakan mikroba untuk mengkonversi gliserol yang telah dimurnikan atau crude gliserol menjadi 1,3-propanadiol yaitu dengan bakteri dari kelas Klebsiella (Pakan dan Foster 1982; Menzel et al 1997;. Yang et al 2007), Citrobacter (Homann et al 1990;. Pflugmacher dan Gottschalk 1994 , Daniel et al 1995), Enterobacter (Barbirato et al 1995) dan Clostridia (Forsberg 1987;. Biebl et al 1992). Beberapa Lactobacillus mampu menghasilkan 1,3-propanadiol dari gliserol [4].
3
Pembuatan 1,3 Propanadiol dengan bahan baku gliserol hasil samping proses pembuatan biodisel pernah dilakukan beberapa orang, berikut hasil penelitian yang telah dibuat.
Tabel 1.3 Daftar Penelitian Terdahulu Referensi /Judul Pemurnian
Gliserol
Bakteri Fermentasi Hasil Siregar, 2008
Biosintesis 1,3 Propanadiol dari
Gliserol (hasil samping biodisel)
Asam Sulfat Enterobacter Aerogenes
4 1.3 TUJUAN PENELITIAN
1. Pemurnian crude gliserol hasil samping pabrik biodiesel dengan menggunakan asam sulfat.
2. Membuat senyawa 1,3-Propanadiol melalui proses fermentasi gliserol dengan menggunakan bakteri Klebsiella Pneumoniae.
1.4 MANFAAT PENELITIAN
Hasil penelitian ini diharapkan bermanfaat untuk dapat meningkatkan nilai ekonomis dari crude gliserol hasil samping proses pembuatan biodiesel.
1.5 RUANG LINGKUP PENELITIAN
Ruang lingkup penelitian ini dilakukan di Laboratorium Bioproses Pusat Penelitian Kelapa Sawit (PPKS) yang terletak di Jalan Bridjen Katamso, Medan. Bahan-bahan yang digunakan dalam penelitian ini antara lain gliserol dari hasil samping biodiesel, bakteri Klebsiella Pneumoniae, asam sulfat, NaOH, unsur makro, unsur mikro, etanol, indikator phenolthalen, bromthimol blue, etilen glikol, dan
aquadest. Peralatan yang digunakan adalah fermentor, alat distilasi dan kromatografi gas. Penelitian ini dimulai dengan proses pemurnian crude gliserol dengan menggunakan H2SO4 lalu dinetralkandengan NaOH, dipanaskan untuk memisahkan garam-garam yang terbentuk, kemudian dibleaching dengan karbon aktif dan penguapan air yang terdapat pada gliserol. Gliserol yang sudah murni difermentasi dengan menggunakan bakteri Klebsiella Pneumoniae. Hasil fermentasi gliserol didistilasi untuk memisahkan 1,3-Propanadiol dariproduk samping yang terbentuk. 1,3-Propanadiol yang terbentuk dianalisa menggunakan kromatografi gas untuk mengetahui kemurnian yang terbentuk.
Variabel yang divariasikan dalam penelitian ini meliputi :
1. Jumlah mikroba yang digunakan : 5, 7, dan 10 % dari volume gliserol 2. Lama fermentasi : 24, 48 dan 72 jam
3. Suhu Fermentasi : 25 dan 37 0C
Sedangkan variabel tetapan yang digunakan dalam penelitian ini adalah : 1. Jenis bakteri : Klebsiella Pneumoniae.
5 4. pH
Parameter yang dianalisa adalah:
1.Kemurnian gliserol sebelum dan sesudah purifikasi 2.Kadar air
3.Kadar abu
4.Kadar Free Fatty Acid (FFA) 5.Densitas gliserol
6
BAB II
TINJAUAN PUSTAKA
2.1 GLISEROL
Gliserol pertama kali ditemukan pada tahun 1979 oleh Scheel dari pemanasan minyak zaitun dan litharge yang kemudian mengekstraksinya dengan air [5]. Dalam menguapkan air tersebut, Scheel mendapatkan cairan yang rasanya manis, setelah dipekatkan didapatkan trihidroksi alkohol (gliserol). Gliserol, gliserin, propane-1,2,3-triol, CH2OHCHOHCH2OH atau C3H8O3 adalah trihydroxy alkohol, merupakan senyawa organik berupa cairan kental, tidak berwarna dan tidak berbau namun terasa manis, higroskopik, netral terhadap lakmus [5].
Gliserol adalah produk samping produksi biodisel dari reaksi transesterifikasi dan merupakan senyawa alkohol dengan gugus hidroksil berjumalh tiga buah [6]. Gliserol terdapat secara alami dalam persenyawaaan sebagai gliserida didalam semua jenis minyak dan lemak baik dari tumbuhan maupun hewan, dan gliserol didapatkan dari proses saponifikasi minyak pada pembuatan sabun, atau pemisahan secara langsung dari lemak pada pemroduksian asam lemak.Tetapi biasanya terdapat sebagai trigliserida yang tercampur dengan bermacam-macam asam lemak, misalnya asam stearat, asam palmitat, asam laurat serta sebagian lemak.Beberapa minyak dari kelapa, kelapa sawit, kapok, lobak dan zaitun menghasilkan gliserol dalam jumlah yang lebih besar dari pada beberapa lemak hewan tallow maupun lard.Gliserol juga terdapat secara ilmiah sebagai trigliserida pada semua jenis hewan dan tumbuhan dalam bentuk lipida sebagai lecitin dan chepalins [5]. Sejak 1949 gliserol juga diproduksi secara sintetis dari propilen. Dan proses secara sintetis tercatat kurang lebih sekitar 50% dari total gliserol di pasaran [7].
7 Sifat fisik dari gliserol [9] :
Bobot molekul = 92,09382 g/mol
Sifat kimia dari gliserol [7] : - Larut dalam air
- Merupakan senyawa hidroskopis - Tidak stabil pada suhu kamar - Rumus Kimia Gliserol: C3H8O3
Kegunaan dari gliserol sangatlah banyak tetapi kebutuhan yang paling besar pada pembuatan resin sintetis dan ester gums, obat-obatan, kosmetika, dan pasta gigi. Pemrosesan tembakau dan makanan juga membutuhkan gliserol dalam jumlah yang besar [7].
2.2 PURIFIKASI GLISEROL
Selama ini crude glycerol yang dihasilkan belum dimanfaatkan oleh industri penghasil biodiesel, karena banyaknya zat pengotor yang terdapat dalam crude glycerol tersebut. Oleh sebab itu pemurnian crude glycerol, yang merupakan produk sampingpembuatan biodiesel perlu dilakukan. Crude glycerol yang dihasilkan berwarna coklat kemerahan dan bersifat basa karena menggunakan katalis KOH atau NaOH [10].
8
ini menggunakan corong pemisah. Kemudian lapisan gliserol ditambahkan karbon aktif untuk penghilangan warna dan akhirnya dilakukan distilasi vakum untuk menghilangkan metanol dan air [13, 8].
Penambahan asam pada gliserol kotor tidak terlalu mempengaruhi warna gliserol yang dihasilkan. Hal ini disebabkan masih banyaknya zat pengotor lain yang tidak mampu dipisahkan oleh penambahan asam, sehingga warnanya tetap coklat kemerahan. Untuk menarik zat pengotor lain yang masih terdapat dalam gliserol maka digunakan karbon aktif sebagai adsorben. Pemilihan karbon sebagai adsorben disebabkan karena karbon aktif mempunyai daya adsorbsi yang cukup tinggi. Selain itu dari segi ekonomi harganya juga lebih murah dibandingkan dengan adsorben lain dan mudah di dapat. Penambahan karbon aktif secara langsung kedalam gliserol kotor menyebabkan sebagian besar gliserol menempel pada karbon aktif karena viskositas gliserol cukup tinggi. Untuk itu sebelum karbon aktif ditambahkan, gliserol kotor diencerkan dulu dengan penambahan air sehingga memudahkan proses adsorbsi. Penambahan air ini membawa dampak terhadap kadar gliserol yang dihasilkan, kadarnya menjadi turun. Untuk menarik air dari gliserol maka dilakukan proses penguapan [10].
2.3 FERMENTASI GLISEROL
Fermentasi berasal dari bahasa Latin aitu fervere yang berarti mendidihkan. Seiring perkembangan teknologi, definisi fermentasi meluas, menjadi semua proses yang melibatkan mikroorganisme untuk menghasilkan suatu produk yang disebut metabolit primer dan sekunder dalam suatu lingkungan yang dikendalikan. Pada mulanya istilah fermentasi digunakan untuk menunjukkan proses pengubahan glukosa menjadi alkohol yang berlangsung secara anaerob. Namun, kemudian istilah fermentasi berkembang lagi menjadi seluruh perombakan senyawa organik yang dilakukan mikroorganisme yang melibatkan enzim yang dihasilkannya. Dengan kata lain, fermentasi adalah perubahan struktur kimia dari bahan-bahan organik dengan memanfaatkan agen-agen biologis terutama enzim sebagai biokatalis [14].
9
cara yang telah dikenal dan digunakan sejak lama sejak jaman kuno. Sebagai suatu proses fermentasi memerlukan:
1. Mikroba sebagai inokulum
2. Tempat (wadah) untuk menjamin proses fermentasi berlangsung dengan optimal.
3. Substrat sebagai tempat tumbuh (medium) dan sumber nutrisi bagi mikroba.
Gambar 2.1 Skema Proses Fermentasi [15]
Fermentasi merupakan suatu cara yang telah dikenal dan digunakan sejak lama sejak jaman kuno. Fermentasi merupakan suatu cara untuk mengubah substrat menjadi produk tertentu yang dikehendaki dengan menggunakan bantuan mikroba. Fermentasi dapat dibedakan menjadi:
(1) fermentasi aerob jika memerlukan oksigen mengubah substrat gula menjadi danhasil akhirnya asam piruvat dan karbondioksida (CO2), dan (2) fermentasi anaerob jika tidak memerlukan oksigen, gula akan diubah
menjadiasam piruvat, kemudian asetaldehida dan akhirnya menjadi alkohol, etanol atau metanol dan asam laktat [15].
Pengolahan gliserol dapat dilakukan melalui proses biologis dengan menggunakan bantuan mikroorganisme yang mana gliserol dalam substrat digunakan sebagai sumber energi dan sumber karbon. Beberapa mikroorganisme yang mampu hidup dengan menggunakan substrat gliserol di antaranya adalah Aerobacter Aerogenes, Anaerobiospirillum succiniciproducens, Clostridium butyricum,
10 2.4 INOKULASI BAKTERI
Inokulasi adalah teknik pemindahan mikroba dari satu media ke media lainnya secara subkultur. Bentuk subkultur ada yang menggunakan kaldu sebagai media dan agar miring, tegak, atau lapisan. Inokulasi merupakan teknik yang penting dan banyak digunakan dalam penyiapan dan pemeliharaan kultur stok dan prosedur pengujian mikroba.
Pemindahan mikroba dilakukan dengan menggunakan kawat ose dan jarum. Pemindahan mikroba secara steril juga dilakukan dengan menggunakan pipet. Pipet berperan sebagai sedotan yang mengangkat cairan. Alat ini terbuat dari plastik. Pipet disterilisasi dengan cara memasukkan semuanya ke canister atau masing-masing dibungkus kertas coklat dan disterilisasi dalam otoklaf (autoclave) atau oven pengering panas.
Untuk tumbuh dan berkembang, mikroba membutuhkan suplai nutrisi yang memadai dan lingkungan pertumbuhan yang sesuai. Suplai nutrisi diberikan dalam bentuk media kultur yang mengandung senyawa sederhana. Media kultur dapat berbentuk cair, semi padat, dan padat. Media kultur berwujud cair tidak mengandung agar sebagai pengental dan biasa disebut medium kaldu (broth medium). Penambahan agar menjadikan medium berbentuk semi padat dan padat [16].
Media merupakan tempat yang baik untuk tumbuhnya mikroba, karena media memiliki nutrient yang dibutuhkan oleh mikroba untuk tumbuh dan berkembang. Media ada yang bersifat umum dan ada yang khusus. Media yang bersifat khusus untuk membantu mengisolasi dan mengidentifikasi mikroba spesifik. Media adalah bahan atau campuran bahan yang digunakan untuk menumbuhkan dan mengembangbiakkan mikroba. Media yang akan digunakan harus dalam keadaan steril, artinya sebelum ditanami mikroba yang dimaksud, tidak ditumbuhi oleh mikroba yang lain yang tidak diharapkan. Dalam pembiakan bakteri yang akan digunakan dalam proses fermentasi maka digunakan media cair. Media cair yang dapat digunakan untuk menumbuhkan atau membiakan mikroba Nutrien Broth [17].
11
pembiakan bakteri berupa FeCl3.6H2O, CaCl2.H2O, CuSO4.5H2O, MnSO4.4H2O, ZnSO4.7H2O, (NH4)2SO4, MgSO4.7H2O, Na2SO4, dan KH2PO4 [18]. Persiapan media cair disterilkan terlebih dahulu sebelum kultur bakteri dimasukkan ke dalam media. Kultur bakteri yang berupa agar, diambil dengan kawat ose yang telah disterilkan di atas api. Kultur dimasukkan ke dalam media cair yang kemudian diinkubasi di dalam inkubator pada suhu 37 oC selama 2 hari [18].
2.5 KLEBSIELLA PNEUMONIAE
Klebsiella pneumoniae pertama kali ditemukan oleh Carl Friedlander. Carl Friedlander adalah patologis dan mikrobiologis dari Jerman yang membantu penemuan bakteri penyebab pneumonia pada tahun 1882. Carl Friedlander adalah orang yang pertama kali mengidentifikasi bakteri Klebsiella pneumoniae dari paru-paru orang yang meninggal karena pneumonia. Karena jasanya, Klebsiella pneumoniae sering pula disebut bakteri Friedlander. Klebsiella pneumoniae bersifat gram negatif, berbentuk batang pendek, fakultatif aerob, tidak mampu membuat spora, tidak bergerak dan mempunyai kapsul. Genus bakteri Klebsiella termasuk bakteri famili dari Enterobacteriaceae, terdiri dari tiga spesies yaitu Klebsiella pneumoniae, Klebsiella oaaenae, dan Klebsiella rhinoschleromatis.
Klebsiella pneumonia dapat memfermentasikan laktosa. Pada test dengan indol, Klebsiella pneumonia akan menunjukkan hasil negatif. Klebsiella pneumonia
dapat mereduksi nitrat. Klebsiella pneumonia banyak ditemukan di mulut, kulit, dan sal usus, namun habitat alami dari Klebsiella pneumoniae adalah di tanah [19].
Gambar 2.2 Bakteri Klebsiella
Pneumoniae [19]
2.6 SINTESIS 1,3 PROPANDIOL
Salah satu produk fermentasi tertua dari gliserol adalah Propanadiol. 1,3-Propanadiol pertama kali diidentifikasi oleh Agustus Freund pada tahun 1881 dalam fermentasi gliserol kultur campuran yang mengandung Clostridium pasteurianum
12
yang digunakan dalam sintesis heterosiklik. Karena adanya dua gugus hidroksil pada posisi 1 dan 3, ditemuka nlah aplikasi dari 1,3-Propanadiol dalam produksi polimer, seperti poliester dan poliuretan. Pemanfaatan dari gliserol mentah untuk memproduksi 1,3-propanadiol memberikan kesempatan adanya kemungkinan untuk memanfaatkan nilai gliserol dari limbah [20].
Fermentasi gliserol dengan mikroba menjadi alternatif dalam sintesis 1,3 propanadiol yang selanjutnya dapat disebut sebagai biosintesis. Proses biosintesis ini perlu dikembangkan karena mudah ditangani dan biaya produksinya rendah. Fermentasi ini melibatkan dua reaksi enzimatik. Reaksi enzimatik pertama dikatalisis oleh gliserol dehidratase untuk mengkonversi gliserol menjadi 3 hidroksi propionaldehid dan air. Reaksi enzimatik kedua yaitu 3 hidroksipropionaldehid direduksi menjadi 1,3-propanadiol oleh propanadiol dehidrogenase.
13
Gambar 2.4 Perombakan Gliserol menjadi 1,3 Propandiol [20]
Beberapa peneliti telah menggambarkan proses biologis ramah lingkungan untuk konversi sumber daya terbarukan, seperti gliserol, untuk 1,3-Propanadiol. Mengingat hasil dan pemulihan produk, perlindungan lingkungan dan pembangunan berkelanjutan industri 1,3-Propanadiol, banyak perhatian telah dibayarkan kepada produksi mikroba, baik menggunakan gliserol atau glukosa sebagai sumber karbon. 1,3-Propanadiol telah banyak digunakan sebagai bahan kimia penting dalam polimer, kosmetik, makanan, obat-obatan dan dalam banyak industri berbasis aplikasi lain, namun penggunaannya dibatasi oleh biaya tinggi [21].
2.7 SEPERASI HASIL FERMENTASI
Proses fermentasi gliserol menjadi 1,3-Propanadiol menghasilkan produk yang masih bercampur, sehingga diperlukan metode untuk mengisolasi 1,3-propanadiol dengan produk samping lainnya, antara lain air, asam asetat, metanol dan produk samping lainnya berupa padatan organik. Metode separasi yang dipakai yaitu penambahan basa kemudian dievaporasi, distilasi dan ekstraksi pelarut, sedangkan padatan dan pengotor lainnya diambil dengan metode sentrifugasi.
Perbedaan titik didih yang cukup tinggi dari senyawa-senyawa hasil fermentasi, mengakibatkan pemisahan dapat dilakukan dengan metode distilasi.
Tabel 2.1 Daftar Beberapa Sifat Komponen Yang Terdapat pada Proses Fermentasi [13]
Nama Senyawa Rumus Kimia Berat Molekul
(gr/mol)
Asam Laktat CH3CH(OH)COOH 90,08 122
3-Hidroksi
14
Asam Butirat CH3CH2CHOOH 88,12 165,5
2-3 Butanadiol CH3CHOHCHOHCH3 90,12 178-182,5
1,3 Propanadiol HOCH2CH2CH2OH 76,11 213.5
Asam Suksinat HO2CCH2CH2CO2H 118,09 235
Gliserol HOCH2CH(OH)CH2OH 92,11 290
Secara garis besar, destilasi atau penyulingan adalah suatu metode pemisahan bahan kimia berdasarkan perbedaan kecepatan atau kemudahan menguap (volatilitas) bahan. Dalam penyulingan, campuran zat dididihkan sehingga menguap dan uap ini kemudian di dinginkan kembali dalam bentuk cairan. Zat yang memiliki titik didih lebih rendah akan menguap lebih dulu.
Berdasarkan tekanan operasi yang digunakan, distilasi dibedakan menjadi tiga jenis, yaitu distilasi atmosferik, distilasi vakum, dan distilasi tekanan tinggi (lebih dari 1 atm). Distilasi vakum biasanya digunakan jika senyawa yang ingin didistilasi tidak stabil, dengan pengertian dapat terdekomposisi sebelum atau mendekati titik didihnya atau campuran yang memiliki titik didih di atas 150 0C. Destilasi vakum memisahkan dua kompenen yang titik didihnya sangat tinggi, motode yang digunakan adalah dengan menurunkan tekanan permukaan lebih rendah dari 1atm, sehingga titik didihnya juga menjadi rendah, dalam prosesnya suhu yang digunakan untuk mendestilasinya tidak perlu terlalu tinggi. Destilasi vakum merupakan proses pemisahkan dua kompenen yang titik didihnya sangat tinggi, metode yang digunakan adalah dengan menurunkan tekanan permukaan lebih rendah dari 1 atm dengan tujuan untuk, mengindari terjadinya reaksi oksidasi pada komponen yang akan dipisahkan agar ikatan rangkap pada senyawa tidak putus.Sedangkan destilasi atmosfer adalah proses pemisahan dua komponen berdasarkan perbedaan titik didihnya pada tekanan atmosfer [22].
Distilasi pada tekanan vakum dan atmosfer ini selain dapat menurunkan titik didih bahan dapat juga bertujuan untuk menghindari kerusakan komponen pada proses pemisahan. Oleh karena itu, dalam penyulingan 1,3-Propandiol ini menggunakan cara destilasi vakum dan destilasi atmosferik untuk dapat membandingkan hasil yang diperoleh dari kedua proses destilasi tersebut serta proses mana yang lebih efektif [22].
15
Gas kromatografi merupakan tehnik yang pertama kali diperkenalkan oleh James dan Martin pada tahun 1952, teknik ini merupakan metode analisis kuntitatif dan kualitatif yang cepat untuk menganalisis komponen lipida volatil seperti hidrokarbon, fatty acid, ester, sterol, dan senyawa lainnya. Penggunaan kromatografi dibedakan antara dua metode penggunaan. Pertama, kromatografi gas digunakan sebagai alat untuk melakukan pemisahan. Penggunaan ini memerlukan pengubahan senyawa sampel menjadi senyawa volatil atau senyawa yang dapat di derivatisasi untuk menghasilkan senyawa volatil. Kedua, kromatografi gas sebagai pelengkap untuk hasil analisis yang sempurna, dalam hal ini waktu dan volume retensi digunakan untuk identifikasi senyawa, luas dan bobot peak sebagai informasi kuantitatifnya. Bagian dasar dari suatu kromatografi gas adalah tangki gas pembawa, sistem injeksi sampel, kolom kromatografi, detektor, oven dan rekorder.
Gas pembawa merupakan gas yang inert dan memiliki tingkat kemurnian yang tinggi seperti helium, nitrogen dan hidrogen. Tangki gas pembawa dilengkapi dengan regulator aliran dan tekanan. Oven berfungsi mengontrol temperatur dalam kolom kromatografi. Kolom kromatografi gas dapat berupa packed column atau
capillary column. Detektor yang sering digunakan pada gas kromatografi adalah flame ionization (FID), thermal conductivity (TCD), electron capture (ECD), flame photometric (FPD) dan photoionization (PID). Kromatografi gas adalah alat yang digunakan untuk memisahkan senyawa dengan mengalirkan arus gas melalui fase diam. Bila fase diam berupa zat padat, maka disebut kromatografi gas padat (KGP). Bila fase diam berupa zat cair, maka disebut kromatografi gas cair (KGC).
Kromatografi menyangkut metode pemisahan yang didasarkan atau distribusi diferensial komponen sampel diantara dua sampel. Kromatografi melibatkan dua fase, yaitu fase diam dan fase gerak. Fase diam biasanya berupa cairan yang terikat pada permukaan, sedangkan fase gerak berupa eluen, pelarut atau gas pembawa inert.
Gas chromatography (GC) memiliki prinsip kerja pemisahan antara gas dan lapisan tipis cairan berdasarkan perbedaan jenis bahan [23].
2.9 ANALISA EKONOMI
16
dengan meningkatnya produksi biodisel. Menurut laporan DitJen Migas (1998) kebutuhan bahan bakar diesel meningkat setiap tahunnya.
Crude gliserol tidak dapat langsung dibuang ke lingkungan karena kandungan bahan organiknya yang tinggi. Salah satu solusi untuk menangani jumlah produksi crude gliserol yang terus meningkat adalah menjadikannya ke dalam bentuk produk yang lebih berharga.
Salah satu produk nilai tambah tinggi yang dapat dengan mudah dibuat dari gliserol adalah 1,3-Propanadiol. 1,3-Propanadiol banyak digunakan untuk berbagai produk seperti polimer, kosmetik, makanan, pelumas, dan obat-obatan. Produksi 1,3-Propanadiol dengan bahan baku Crude Gliserol dilakukan dengan tahapan sebagai beikut:
1. Pemurnian Crude Gliserol
2. Pembiakan Bakteri Klebsiella Pneumonia 3. Fermentasi Gliserol
4. Distilasi
5. Analisa Hasil Fermentasi
Berikut merupakan rincian biaya pembuatan 1,3-Propanadiol dengan fermentasi gliserol menggunakan bakteri klebsiella pneumoniae yang telah dilakukan selama penelitian dengan basis bahan baku crude gliserol 5 liter.
1. Biaya pemurnian crude gliserol (5 ltr) Rp 60.000,- 2. Pembiakkan Bakteri (1 L) Rp 25.000,-
3. Fermentasi Rp 10.000,-
4. Distilasi Rp 10.000,-
5. Analisa Rp 250.000,-
Rp 355.000,-
Pada proses pemurnian crude gliserol sebanyak 5 liter akan menghasilkan gliserol murni sebanyak 1,8 L. Setiap fermentasi 50 ml gliserol diperkirakan akan menghasilkan 20 ml 1,3-Propanadiol. Sehingga, diperoleh hasil 1,3-Propanadiol hasil fermentasi gliserol sebanyak 1,8 L diperoleh sekitar 720 ml 1,3-Propanadiol.
17
18
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI PENELITIAN
Penelitian dilakukan di Laboratorium Bioproses Pusat Penelitian Kelapa Sawit (PPKS) di Jalan Bridjen Katamso, Medan.
3.2 BAHAN
3.2.1 Bahan Baku
Bahan baku dalam percobaan ini adalah gliserol dari hasil samping proses pembuatan biodiesel. Crude Gliserol diambil dari salah satu industri pengolahan minyak kelapa sawit menjadi biodiesel yang ada di Dumai dan dibawa ke laboratorium. Bakteri Klebsiella Pneumoniae yang diperoleh dari laboratorium mikrobiologi Badan Pegawasan Obat dan Makanan (BPOM) Medan.
3.2.2 Bahan Purifikasi Gliserol
Bahan purifikasi yang digunakan dalam percobaan ini adalah H2SO4 5 % yang diencerkan sebanyak 50 ml untuk setiap 150 ml gliserol, NaOH, aquadest, dan karbon aktif 2 % dari berat total gliserol.
3.2.3 Bahan Pembuatan Media Kultur Stok
Adapun bahan yang digunakan dalam pembuatan kultur stok adalah Klebsiella Pneumoniae, ekstrak sapi, pepton, margarin, glukosa, NaOH, dan HCl. Unsur makro yaitu: FeCl3.6H2O, CaCl2.H2O, CuSO4.5H2O, MnSO4.4 H2O, ZnSO4.7H2O, aquadest, dan unsur mikro adalah : (NH4)2SO4, MgSO4.7H2O, Na2SO4, KH2PO4.
3.2.4 Bahan Media Perhitungan Jumlah Bakteri Yang Tumbuh
19 3.2.5 Bahan Analisa
3.2.5.1 Bahan Analisa Kadar Air Gliserol 1. Crude Gliserol
Fungsi : Sebagai bahan baku yang akan di analisa kadar airnya. 3.2.5.2 Bahan Analisa Densitas Gliserol
1. Crude Gliserol
Fungsi : Sebagai bahan baku yang akan di analisa densitasnya. 2. Aquadest
Fungsi : Sebagai bahan kalibrasi piknometer. 3.2.5.3 Bahan Analisa Kadar Abu
1. Crude Gliserol
Fungsi : Sebagai bahan baku yang akan diketahui kadar abunya. 3.2.5.4 Bahan Analisa Free Fatty Acid (FFA) Gliserol
1. Crude Gliserol
Fungsi : Sebagai bahan baku yang akan diketahui kadar FFAnya. 2. Etanol 95 %
Fungsi : Sebagai pereaksi dengan gliserol. 3. NaOH 0,1 N
Fungsi : Sebagai bahan pentiter. 4. Phenopthalein
Fungsi : Sebagai indicator
5. Aquadest
Fungsi : Sebagai pelarut universal 3.2.5.5 Analisa Kromatografi Gas
Analisis kromatografi gas dilakukan pada gliserol dan 1,3-Propanadiol. Analisis krmatografi gas juga dilakukan pada hasil fermentasi setelah separasi dengan menggunakan distilasi. Analisis kromatografi gas dilakukan dengan menggunakan GC QP 2010 Shimadzu dengan automatic sampling system yang mampu menganalisis 50 scans perdetik. Kolom yang digunakan DB 5 HT dengan bahan pengisi 100 % dimethyl polysiloxane, yang mampu menganalisis senyawa
20
dengan menggunakan pelarut aquadest dengan gas pembawa helium dengan kondisi pengaturan temperatur pada alat GC (Colom, Injection, Ion Source dan Interface).
Tabel 3.1 Program Pengatur GC
Parameter Nilai Satuan
Temp Oven Kolom 60 0C
Temp Injeksi 370 0C
Tekanan 100 kPa
Kec Aliran 125,1 ml/min
Kecepatan Kolom 2,42 ml/min
Temp Sumber Ion 370 0
Fungsi : Sebagai tempat fermentasi berlangsung 2.Kromatografi gas
Fungsi : Sebagai alat analisa kandungan dari suatu bahan 3. Beaker glass
Fungsi : Sebagai wadah larutan 4. Gelas ukur
Fungsi : Sebagai alat mengukur volume suatu larutan 5. Corong gelas
Fungsi : Sebagai alat letaknya kertas saring untuk memisahkan padatan dari gliserol
6. Oven
Fungsi : Sebagai alat untuk memisahkan gliserol dan air 7. Autoclave
Fungsi : Sebagai alat untuk mensterilkan peralatan yang digunakan dalam fermentasi
8. Counter coloni
21 9. Distilasi
Fungsi : Sebagai alat untuk memisahkan hasil fermentasi
3.4 PROSEDUR PENELITIAN
3.4.1 Prosedur Purifikasi Gliserol
Gliserol disiapkan dalam suatu beaker glass, lalu dipanaskan pada suhu 60 0C selama 1 jam untuk menguapkan kandungan metanol yang masih terdapat pada gliserol, setelah itu ditambahkan H2SO4 5 % sehingga terbentuk 2 lapisan, dimana lapisan bawah adalah gliserol murni dan lapisan atas adalah senyawa yang terdapat pada crude gliserol dan menghasilkan pH 2. Larutan gliserol yang sudah diperoleh dari pemisahan ditambahkan larutan NaOH hingga pH gliserol netral (pH 7). Kemudian dipanaskan supaya terbentuk garam Na2SO4 dan disaring untuk memisahkan garam dengan gliserol. Larutan gliserol kemudian ditambahkan dengan karbon aktif 2 % dari berat total gliserol untuk mengurangi warna pada gliserol tersebut, dipanaskan pada suhu 80 0C dan dibiarkan selama 12 jam dan disaring untuk memisahkan karbon aktif dengan gliserol [8, 9, 13].
1. Crude Gliserol dimasukkan ke wadah dan dipanaskan pada suhu 60 0C untuk menguapkan alkohol yang masih terkandung.
2. Ditambahkan dengan H2SO4 5 % sebanyak 50 ml untuk setiap 150 ml Crude Gliserol sehingga menghasilkan pH 2 dan dibiarkan selama 30 menit.
3. Setelah terbentuk 2 lapisan, dipisahkan, dimana lapisan bawah gliserol dan lapisan atas senyawa yang lain selain gliserol.
4. Gliserol yang didapat ditambahkan NaOH hingga pH netral (pH 7), lalu dipanaskan dan disaring.
5. Gliserol yang didapat ditambahkan karbon aktif 2 % dan dibiarkan selama 12 jam dan dipanaskan, lalu disaring.
3.4.2 Prosedur Analisa Gliserol (Metode SNI)
22
tersebut ditambah NaIO4 sebanyak 50 ml lalu diaduk secara perlahan. Larutan selanjutnya ditutup dan didiamkan dalam ruangan gelap pada suhu kamar selama 30 menit. Larutan kemudian ditambah etilena glikol sebanyak 10 ml lalu ditutup dan didiamkan dalam ruangan gelap pada suhu kamar selama 20 menit. Larutan diencerkan dengan 300 ml air akuades, kemudian ditambah 3 tetes indikator biru bromtimol. Larutan hasil campuran tersebut ditirasi perlahan-lahan dengan NaOH 0,5 N sampai terbentuk warna biru. Proses tersebut juga dilakukan untuk perlakuan blangko. Kadar gliserol dihitung dengan rumus di bawah ini [24].
Dengan;
T1 = volume NaOH untuk titrasi contoh (ml) T2 = volume NaOH untuk titrasi blangko (ml) N = normalitas NaOH
W = bobot contoh (g) Faktor gliserol = 9,209
3.4.3 Penentuan Kadar Free Fatty Acid (FFA) Gliserol
Penentuan kadar asama lemak bebas (FFA) berdasarkan langkah-langkah berikut [25]:
1. sampel sebanyak 20 gram dimasukkan kedalam erlenmeyer dan di larutkan dengan 100 ml etanol 95 %.
2. Dikocok hingga rata, dan diambil 10 ml untuk dianalisa.
3. Campuran larutan ditambahkan 3 tetes indikator phenolphalein.
4. Campuran dititrasi dengan 0,1 N natrium hidroksida sambil diaduk hingga berubah warna menjadi merah muda selama 30 s.
5. Persentase FFA dihitung dengan persamaan :
(3.1)
23 3.4.4 Penentuan Densitas Gliserol
Piknometer terlebih dahulu dikalibrasi dengan air pada suhu 30 0C, dimana piknometer diisi air hingga penuh, lalu dicatat berat air untuk menghitung volume piknometer yang digunakan. Dimasukkan sampel ke dalam piknometer hingga penuh kemudian dilakukan penimbangan piknometer yang telah berisi sampel sampai menunjukkan angka yang konstan. Penentuan densitas dihitung berdasarkan persamaan berikut:
3.4.5 Penentuan Kadar Air Gliserol [25]
Sebanyak 10 gram sampel dimasukkan kedalam cawan penguap. Sampel dalam cawan tersebut dipanaskan di dalam oven pada suhu 105 oC selama ± 3 jam lalu didinginkan di dalam desikator yang berisi silica gel selama 30 menit dan ditimbang beratnya sampai menunjukkan angka timbangan yang konstan. Kadar air dari sampel dihitung dengan persamaan berikut:
3.4.6 Penentuan Kadar Abu Gliserol [25]
Cawan penguap yang telah di panaskan di dalam oven pada suhu 105 oC selama 60 menit dan didinginkan dalam desikator selama 30 menit dan ditimbang berat kosongnya. Sampel sebanyak 10 gram dimasukkan ke dalam cawan penguap lalu di panaskan ke dalam furnace pada suhu 550-650 oC selama 3 jam, lalu didinginkan dan dimasukkan ke dalam desikator selama 30 menit. Ditimbang beratnya sampai menunjukkan angka timbangan yang kostan. Kadar abu dari sampel dapat dihitung dengan persamaan berikut:
24 3.4.7 Pembuatan Media Pertumbuhan
Pembuatan media pertumbuhan bakteri dilakukan dengan cara sebagai berikut. Unsur Makro : 20 gr FeCl3.6 H2O, 10 gr CaCl2 H2O, 0,03 gr CuSO4.5 H2O, 0,05 gr MnSO4.4 H2O, 0,1 ZnSO4.7H2O dilarutkan di dalam 1 liter aquadest. Kedalam larutan, unsur mikro ditambahkan seperti (NH4)2SO4 0,5 gr, MgSO4.7H2O 0,4 gr, Na2SO4 9,65 gr, KH2PO4 2,65 gr. Ditambahkan nutrisi tambahan seperti ekstrak sapi 3 gr, pepton 3 gr, margarin 10 gr, 10 gr glukosa. Larutan pertumbuhan media kemudian diukur pHnya. pH larutan harus antara 6,4-7,4, jika larutan dalam keadaan asam maka diberikan larutan NaOH tetes demi tetes hingga mencapai pH yg telah ditentukan. Jika larutan dalam keadaan basa maka ditambahkan HCl tetes demi tetes hingga mencapai pH yang sesuai. Larutan kemudian dipanaskan sampai medidih dan dibiarkan dingin, kemudian larutan yang terdapat di dalam erlenmeyer ditutup menggunakan kapas dan dibungkus dengan kertas serta diikat menggunakan karet, kemudian disterilkan dengan menggunakan autoklav pada suhu 121 selama 20 menit [18].
3.4.8 Pembuatan Kultur Stok
Tempat pembuatan kultur stok terlebih dahulu disterilisasi dengan sinar UV selama 30 menit. Kultur stok dibuat dengan mengambil kultur mutan Klebsiella Pnemonia kemudian dimasukkan dalam media pertumbuhan, kemudian diinkubasi dalam inkubator statis selama 3 hari pada temperatur 37 0C. Kultur kemudian dapat digunakan dalam fermentasi[13].
3.4.9 Prosedur Perhitungan Jumlah Bakteri
Untuk mengetahui jumlah bakteri yang tumbuh dapat dilakukan dengan cara yaitu sebanyak 10 gr nutrien agar dilarutkan ke dalam 500 ml aquadest. Kemudian dipanaskan hingga mendidih. Larutan nutrien agar yang terdapat didalam erlenmeyer ditutup dengan kapas dan dibungkus dengan kertas serta diikat dengan karet. Larutan yang sudah ditutup disterilkan di dalam autoklav pada suhu 121 0C selama 20 menit. Kemudian larutan didinginkan hingga suhu 35 0C.
25
sebanyak 9 ml aquadest steril lalu ditutup dengan kapas dan tabung reaksi sudah ditandai dengan angka 1-8. Sebanyak 1 ml kultur stok yang sudah dibiakkan selama 2 hari dimasukkan kedalam tabung reaksi no 1, dan dilakukan pengadukkan vorteks, lalu 1 ml diambil dari tabung reaksi no 1 dan dimasukkan kedalam tabung reaksi no 2 dan seterusnya hingga tabung no 8 berisi 1 ml dari tabung no 7.
Perhitunggan jumlah bakteri dikakukan pada pengenceran ke 6,7, dan 8 dengan cara yaitu sebanyak 1 ml dari setiap pengenceran dimasukkan ke dalam cawan petri secara dupplo lalu setiap cawan diisi dengan nutrien agar yang sudah dingin sebanyak ½ dari tinggi cawan petri. Cawan petri yang sudah berisi dibiarkan selama 2 hari. Setelah 2 hari, setiap cawan petri dilihat jumlah bakteri yang ada dengan coloni counter sehingga diperoleh jumlah bakteri yang tumbuh pada media pertumbuhan [26].
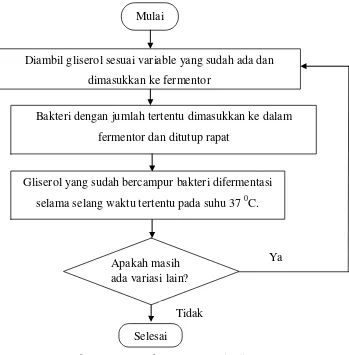
3.4.10 Prosedur Fermentasi
1. Diambil gliserol sesuai variable yang sudah ada dan dimasukkan ke fermentor 2. Kemudian ditambahkan bakteri Klebsiella Pnemonia yang telah diremajakan. 3. Gliserol yang sudah bercampur bakteri Klebsiella Pnemonia difermentasi
selama selang waktu pada suhu 37 oC [13].
3.4.11 Analisa 1,3 Propanadiol
26 3.5 FLOWCHART PENELITIAN
3.5.1 Purifikasi Gliserol
Dipanaskan
A
Ya
Larutan yang didapat ditambahkan dengan karbon aktif 2 % dari massa total gliserol
Dipanaskan pada suhu 60 0C dan dibiarkan selama 12 jam Disaring
Disaring Apakah terbentuk
garam?
Tidak Mulai
Crude Gliserol dimasukkan kedalam wadah dan dipanaskan pada suhu 60 0C selama 1 jam
Didiamkan selama 30 menit
Terbentuk 2 lapisan, lapisan bawah gliserol dan lapisan atas senyawa selain gliserol
Dipisahkan dengan corong pisah Ditambahkan H2SO4
Gliserol ditambahkan larutan NaOH hingga mencapai pH netral
Garam
Diukur volume gliserol
27
Gambar 3.1 Flowchart Purifikasi Gliserol
3.5.2 Penentuan Kadar Gliserol
Selesai A
Air pada gliserol diuapkan
Gliserol dianalisa
Air
Sampel 0,5 gram di tambahkan 50 ml aquadest
Ditutup dan didiamkan di tempat gelap pada suhu kamar 30 menit Ditambahkan 5 tetes indikator biru bromtimol
Mulai
Ditambahkan H2SO4 0,2 N hingga berwarna kuning kehijauan
Dinetralkan dengan NaOH 0,05 N hingga berwarna biru
Ditambahkan NaIO4 sebanyak 50 ml dan diaduk
Ditambahkan etilena glikol sebanyak 10 ml dan
Ditutup dan didiamkan di tempat gelap pada suhu kamar 20 menit
Ditambahkan 300 ml aquadest
Ditambahkan 3 tetes indikator biru bromtimol
28
Gambar 3.2 Flowchart Penentuan Kadar Gliserol 3.5.3 Penentuan Kadar Free Fatty Acid (FFA)
Gliserol sebanyak 20 gram dimasukkan ke dalam erlenmeyer
Ditambahkan 100 mL etanol 95 %
Ditambahkan 3 tetes phenolpthalein
Mulai
Dikocok hingga rata
Diambil 10 ml Ya
Tidak
Hitung kadar gliserol
Selesai Apakah warna
larutan biru?
Ya Dititrassi dengan NaOH 0,5 N
A
29
Gambar 3.3 Flowchart Penentuan Kadar FFA 3.5.4 Penentuan Densitas Gliserol
Dititrasi dengan 0,1 N NaOH
Apakah warna larutan merah muda
?
Ya A
Presentase FFA dihitung
Selesai
Mulai
Piknometer kosong terlebih dahulu ditimbang
Piknometer dikalibrasi dengan air
Piknometer diisi dengan air hingga penuh, lalu ditimbang
Piknometer diisi dengan sampel hingga penuh
Dihitung volume piknometer
30
Gambar 3.4 Flowchart Penentuan Densitas Gliserol
3.5.5 Penentuan Kadar Air Gliserol
Gambar 3.5 Flowchart Penentuan Kadar Air Gliserol Dimasukkan kedalam desikator selama 30 menit
Cawan penguap ditimbang
Dipanaskan pada suhu 105 0C selama 2 jam
Dimasukkan ke dalam desikator dan ditunggu selama 30 menit Ditimbang
Selesai
Diisi dengan 10 gram gliserol Mulai
Dihitung kadar air
Cawan penguap dipanaskan selama 30 menit Mulai
Ditimbang dan dicatat berat sampelnya
Densitas gliserol dihitung
Selesai A
31 3.5.6 Flowchart Penentuan Kadar Abu Gliserol
Gambar 3.6 Flowchart Penentuan Kadar Abu Gliserol Selesai
Dihitung kadar abu
Cawan porselin dipanaskan selama 30 menitdi dalam oven Didinginkan selama 30 menit di dalam desikator
Cawan porselin ditimbang
Dipanaskan di dalam furnace pada suhu 550-600 0C selama 3 jam
Didinginkan selama 30 menit dalam desikator Ditimbang berat cawan + abu
32 3.5.7 Pembuatan Media Pertumbuhan
Gambar 3.7 Flowchart Pembuatan Media Pertumbuhan Mulai
Sebanyak 1 liter aquadest dimasukkan ke dalam erlenmeyer
Dipanaskan hingga mendidih dan didinginkan sampai suhu kamar
Selesai
Disimpan dalam kulkas
Dimasukkan unsur makro (20 gr FeCl3.6 H2O, 10 gr CaCl2 H2O, 0,03 gr CuSO4.5
H2O, 0,05 gr MnSO4.4 H2O, 0,1 ZnSO4.7H2O)
Ditambahkan ekstrak sapi 3 gr, pepton 3 gr, margarine 10 gr, 10 gr glukosa, (NH4)2SO4 0,5 gr, MgSO4.7H2O 0,4, Na2SO3 9,65 gr,
KH2PO4 2,65 gr
33 3.5.8 Prosedur Pembuatan Kultur Stok
Gambar 3.8 Flowchart Pembuatan Kultur Stok
3.5.9 Prosedur Perhitungan Jumlah Bakteri
Kedalam media pertumbuhan dimasukkan kultur bakteri Klebsiella pneumoniae
Diinkubasi selama 2 hari pada suhu 37
Selesai
Disimpan dalam cool chamber Tempat pembuatan kultur stok disterilisasi
dengan sinar UV selama 30 menit Mulai
Mulai
Campuran dipanaskan hingga mendidih dan didinginkan
hingga suhu 35 0C Nutrien agar sebanyak 10 gr larutkan dengan aquadest 500 ml
Sediakan 8 buah tabung reaksi yang berisi dengan 9 ml aquadest steril
Dimasukkan 1 ml kultur stok yang sudah dibiakkan selama 2 hari kedalam tabung reaksi no 1
Diambil 1 ml campuran dari tabung reaksi no 1 dan dimasukkan ke tabung reaksi no 2, dilakukan seterusnya hingga tabung reaksi no 8 yang berisi 1 ml campuran dari tabung reaski no 7.
34
Gambar 3.9 Flowchart Perhitungan Jumlah Bakteri
3.5.10 Fermentasi Gliserol
Gambar 3.10 Flowchart Fermentasi Gliserol Mulai
Diambil gliserol sesuai variable yang sudah ada dan dimasukkan ke fermentor
Bakteri dengan jumlah tertentu dimasukkan ke dalam fermentor dan ditutup rapat
Selesai Apakah masih ada variasi lain?
Ya
Tidak
Gliserol yang sudah bercampur bakteri difermentasi selama selang waktu tertentu pada suhu 37 0C.
Selesai
Diambil 0,1 ml campuran dari tabung reaksi no 6,7,8 dan dimasukkan ke masing-masing
cawan petri secara dupplo Dibiarkan selama 2 hari Dilihat dibawah coloni counter
Dihitung jumlah koloninya
35
BAB IV
HASIL DAN PEMBAHASAN
4.1 PEMURNIAN GLISEROL
Crude gliserol yang digunakan dalam penelitian ini adalah crude gliserol dari pabrik biodiesel yang berasal dari Dumai yang telah dianalisa analisa kandungannya seperti densitas, FFA, kadar air, kadar abu, dan kemurnian gliserol. Dalam pembuatan 1,3-Propanadiol terlebih dahulu dilakukan pemurnian crude gliserol dengan menggunakan asam sulfat (H2SO4). Pada proses pemurnian ini dilakukan 4 tahap untuk menghasilkan gliserol yang memiliki kemurnian yang tinggi, yaitu pengasaman, penetralan, bleaching, dan penguapan air.
Pada tahap pengasaman, dilakukan penambahan asam sulfat ke dalam crude gliserol sehingga terbentuk 2 lapisan yang dapat dilihat pada gambar 4.1 dibawah ini.
Gambar 4.1 Proses Pengasaman Crude Gliserol dengan Asam Sulfat
Lapisan atas merupakan asam lemak bebas yang terdapat pada gliserol dan hasil reaksi antara asam sulfat dengan sabun yang terkandung dalam crude gliserol. Reaksi terbentuknya asam lemak bebas dapat dilihat pada reaksi di bawah ini.
RCOOK + H2SO4 2RCOOH + K2SO4 + H2SO4 sisa (sabun) (asam sulfat) (asam lemak)
36
2KOH + H2SO4 K2SO4 + H2O + H2SO4 (katalis basa) (asam sulfat) (kalium sulfat)
Terdapatnya asam sulfat yang terkandung pada gliserol yang merupakan hasil pengasaman akan dinetralkan dengan penambahan natrium hidroksida. Reaksi penetralan asam sulfat dengan NaOH dapat dilihat pada reaksi di bawah ini.
H2SO4 sisa + K2SO4 + NaOH K2SO4 + Na2SO4 + 2H2O
Pada proses ini diperoleh endapan natrium sulfat dan kalium sulfat yang larut di dalam larutan gliserol yang netral. Pemisahan garam terlarut dalam gliserol dilakukan dengan pemanasan sehingga mempercepat terbentunya garam [8].
Gambar 4.2 Garam Yang Terbentuk setelah Pemanasan
Gliserol yang dihasilkan masih berwarna merah kecoklatan yang belum sesuai dengan sifat gliserol aslinya, oleh karena itu dilakukan proses bleaching dengan penambahan karbon aktif. Warna gliserol yang dihasilkan setelah penambahan karbon aktif adalah bening seperti pada gambar 4.3. Gliserol murni mempunyai warna bening [28]. Gliserol tersebut masih mengandung air, untuk itu perlu dilakukan pemisahan dengan memanaskan gliserol pada oven dengan suhu 105-110 o
C selama 5 jam.
Gliserol
37
Gambar 4.3 Gliserol hasil pemurnian
Gliserol hasil pemurnian yang diperoleh dianalisa warna, densitas, Free Fatty Acid (FFA), kadar air, kadar abu, dan kemurnian gliserol.
4.2 ANALISA GLISEROL
Crude gliserol yang diperoleh dari hasil samping pembuatan biodiesel dianalisa terlebih dahulu sifat fisikanya. Selain itu, gliserol hasil pretreatment juga dilakukan analisa, hasil analisa dapat dilihat pada tabel 4.1 di bawah ini.
Tabel 4.1 Perbandingan sifat fisika Crude Gliserol dan Gliserol hasil pemurnian No Sifat Fisika Crude gliserol Gliserol hasil
pemurnian Satuan
1 Warna Coklat Kemerahan Bening
2 Densitas 1,24 1,27 gr/ml
3 FFA 26,22 0,92 %
4 Kadar Air 2,64 1,26 %
5 Kadar Abu 11,00 6,00 %
6 Kemurnian Gliserol 29,31 93,19 %
Dari sifat fisika di atas diperoleh densitas gliserol murni sebesar 1,27 gr/ml, dimana pada teori bahwa densitas gliserol umumnya sebesar 1,26 gr/ml [10]. Oleh karena itu, bahwa densitas gliserol hasil pemurnian mendekati densitas gliserol sebenarnya.
38 4.3 FERMENTASI GLISEROL
Pada penelitian ini, dilakukan proses fermentasi gliserol dengan bantuan bakteri Klebsiella pneumoniae untuk menghasilkan 1,3-Propanadiol. Proses fermentasi diawali dengan pembuatan media pembiakan, penyiapan kultur stok, perhitungan jumlah bakteri sebelum dilakukan fermentasi. Bakteri Klebsiella pneumoniae dibiakan dalam media yang mengandung unsur makro dan mikro. Indikator terjadinya pembiakan bakteri dilihat secara visual dengan ditandai perubahan warna pada media yaitu hitam kecoklatan menjadi merah kecoklatan yang terlihat pada gambar 4.4.
(a) (b) Gambar 4.4 (a) Kultur stok sebelum pembiakan
(b) Kultur stok sesudah pembiakan
Klebsiella pneumoniae siap diaplikasikan dalam fermentor setelah dilakuakan perhitungan jumlah bakteri yang digunakan dengan teknik pengenceran 108 yang digunakan untuk mengetahui koloni yang tumbuh pada media dengan menggunakan
39
(a) (b) (c)
Gambar 4.5 a) Pengenceran ke 6, b) Pengenceran ke 7, c) Pengenceran ke 8
Dengan proses penggenceran diperoleh jumlah koloni bakteri Klebsiella pneumoniae adalah sekitar 83 x 108/ml.
Proses fermentasi gliserol menjadi 1,3-Propanadiol dilakukan dengan memvariasikan waktu fermentasi yaitu 1, 2, dan 3 hari, volume bakteri yaitu 5,7,dan 10 % dari volume gliserol yang akan difermentasi, dan suhu yaitu 25 dan 37 0C. Tujuannya adalah untuk mengetahui kondisi atau keadaan mana yang paling baik untuk menghasikan 1,3-Propanadiol.
4.3.1 Konversi Gliserol
40
Gambar 4.6 Kadar Gliserol pada Proses Fermentasi Pada Suhu 25 0C maupun 37 0C
Jalansuntram [29] melakukan fermentasi gliserol dengan klebsiella pneumonia menunjukkan bahwa gliserol terkonversi semua setelah 8 jam fermentasi berlangsung.
Gliserol yang telah difermentasi tidah menghasilkan 1,3-Propanadiol saja, akan tetapi beberapa senyawa lainnya seperti etanol, asam suksinat, dan sebagainya. Untuk mengetahui berapa besar kemurnian 1,3-Propanadiol yang dihasilkan perlu dilakukan analisa dengan menggunakan gas kromatografi.
Pada analisa gas kromatografi akan dihasilkan retention time untuk mengetahui senyawa itu berada, untuk mengetahui senyawa 1,3 Propanadiol terbentuk terlebih dahulu perlu dilakukan analisa gas kromatografi pada 1,3 Propanadiol dengan menggunakan alat gas kromatografi dengan kondisi alat yang sama. Analisa terhadap bahan baku disebut sebagai larutan standart. 1,3 Propanadiol dengan kemurnian 98 % dianalisa dengan gas kromatografi, hasil analisa larutan standart 1,3 Propanadiol dapat dilihat pada gambar 4.7 di bawah ini.
0
41
Gambar 4.7 Hasil Analisa Komatografi Standard 1,3 Propanadiol
Gambar 4.7 merupakan hasil analisa terhadap 1,3 Propanadiol murni yang merupakan larutan standart sebagai dasar untuk analisa hasil fermentasi gliserol. Pada gambar 4.7 diatas menunjukkan bahwa 1,3 Propanadiol berada pada rentang waktu 2,885; 4,846; 32,028; dan 32,308 menit. Rentang waktu tersebut merupakan dasar untuk mengetahui 1,3-Propanadiol yang terdapat pada hasil fermentasi gliserol.
4.3.2 Pengaruh Waktu Fermentasi Terhadap Konsentrasi 1,3-Propanadiol
Terbentuk
42
Gambar 4.8 Hubungan Waktu Fermentasi terhadap Kemurnian 1,3-Propanadiol
Dari gambar 4.8 di atas dapat dilihat bahwa terdapat senyawa-senyawa yang tidak diketahui, oleh karena itu senyawa-senyawa itu digolongkan berdasarkan rentang waktu yang terdapat pada hasil gas kromatografi. Siregar [13] melakukan fermentasi gliserol menjadi 1,3 Propanadiol menghasilkan beberapa senyawa kimia seperti etanol, asam formiat, 3-Hidroksi Propinaldehid, asam asetat, asam laktat, asam butirat, 2,3 Butanadiol, dan asam suksinat. Pada gambar 4.8 menunjukkan bahwa konsentrasi 1,3 Propanadiol bertambah seiring dengan bertambahnya waktu fermentasi. Konsentrasi 1,3-Propanadiol yang terbentuk pada hari ke 1 sebesar 14,0963 mol/ml, pada hari ke 2 sebesar 14,6330 mol/ml dan pada hari ke 3 sebesar 17,6093 mol/ml. Meningkatnya 1,3 Propanadiol pada hari ke 2 dan 3 dikarena beberapa senyawa lain yang terbentuk pada hari 1 diubah oleh bakteri Klebsiella menjadi 1,3 Propanadiol, hal ini dapat dilihat dengan menurunnya kemurnian senyawaasam laktat, 3 Hidroksi Propinaldehid, dan 2,3 Butanadiol mengalami penurunan seiring bertambahnya waktu fermentasi.
43
Berdasarkan penelitian Li, dkk [31] beberapa senyawa hasil fermentasi gliserol dengan bakteri Klebsiella diubah menjadi senyawa 1,3 Propanadiol yang dilihat menurunnya kemurnian asam latat, dan asam suksinat.
Hasil gas kromatografi untuk fermentasi gliserol selama 3 hari pada temperatur 37 0C dan volume bakteri yang digunakan 10 % dapat dilihat pada gambar 4.9 di bawah ini.
Gambar 4.9 Hasil GC dari Fermentasi Gliserol 2 hari, 37 0C, 10 %
Pada penelitian ini dapat dilihat bahwa waktu fermentasi 3 hari menghasilkan konsentrasi 1,3 Propanadiol yang tinggi yaitu 17,6093 %.
4.3.3 Pengaruh Volume Inokulum Bakteri Terhadap Konsntrasi
1,3-Propanadiol Terbentuk
44
Gambar 4.10 Hubungan Volume Bakteri terhadap Konsentrasi 1,3 Propanadiol
45
gliserol selama 3 hari pada temperatur 37 0C dan volume bakteri yang digunakan 7 % dapat dilihat pada gambar 4.11.
Gambar 4.11 Hasil GC dari Fermentasi Gliserol 3 hari, 37 0C, 7 %
Pada penelitian Jalasutram [29] variasi volume bakteri (inokulum) yang dilakukan yaitu 1, 2, dan 3 % dari volume gliserol yang digunakan dan Jalansutram [29] memperoleh bahwa dengan penambahan inokulum klebsiella pneumoniae
mutagen yang paling banyak (3 %) menghasilkan konsentrasi 1,3-Propanadiol yang tinggi. Pada penelitian ini 1,3-Propanadiol yang terbentuk diperoleh pada penambahan volume inokulum yang paling besar yaitu 10 % dari volume gliserol.
4.3.4 Pengaruh Suhu Fermentasi Terhadap Konsentrasi 1,3-Propanadiol
Terbentuk
46
Gambar 4.12 Hubungan Suhu Fermentasi terhadap Konsentrasi 1,3-Propanadiol
Dari gambar 4.12 di atas dapat dilihat bahwa konsentrasi 1,3-Propanadiol yang terbentuk pada fermentasi gliserol pada suhu 25 0C sebesar 14,9892 mol/ml sedangkan pada suhu 37 0C sebesar 17,6093 mol/ml. Konsentrasi 1,3-Propanadiol yang tinggi terbentuk pada fermentasi gliserol dengan suhu fermentasi 37 0C. Suhu memegang peranan penting, karena secara langsung dapat mempengaruhi aktivitas mikroorganisme dan secara tidak langsung akan mempengaruhi produk yang dihasilkan [34]. Klebsiella Pneumoniae tumbuh pada medium sederhana dan kompleks, bersifat aerobik dan dapat hidup pada suhu optimum 37 0C [35]. Jalansutram [29] memperoleh kemurnian 1,3 Propanadiol yang tinggi pada suhu 37 0
47
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Hasil penelitian dari fermentasi gliserol hasil samping pabrik biodiesel menjadi 1,3-Propanadiol dengan menggunakan bakteri klebsiella pneumoniae, dapat diambil kesimpulan antara lain :
1. Gliserol yang digunakan pada penelitian ini merupakan Crude Gliserol hasil samping pabrik biodiesel yang telah dimurnikan dengan kadar sebesar 93,1924 %. 2. Fermentasi gliserol selama 3 hari dengan penambahan 10 % inokulum bakteri
klebsiella pneumoniae pada temperatur 37 oC menghasilkan konsentrasi 1,3 Propanadiol yang tinggi yaitu 17,6093 mol/ml.
5.2SARAN
Demi kesempurnaan penelitian ini, maka peneliti menyarankan:
1. Penggunaan bakteri klebsiella pnemonia yang telah dimutagenkan dalam proses fermentasi untuk menghasilkan 1,3-Propanadiol
2. Penambahan nutrisi/makanan pada medium fermentasi seperti glukosa, dan urea dapat dilakukan untuk mengetahui 1,3 Propanadiol yang terbentuk.
![Gambar 2.3 Biokonveksi Gliserol menjadi 1,3 Propandiol [20]](https://thumb-ap.123doks.com/thumbv2/123dok/157448.11813/32.595.145.532.443.827/gambar-biokonveksi-gliserol-menjadi-propandiol.webp)