ABSTRACT
Study Tolerance Level of Three Pineapple Clones [Ananas comosus (L.) Merr.] In the Effect of Lime and Organic Materials for Aluminum Toxicity
in Ultisol Soil of PT Great Giant Pineapple
by
Dudy Arfian
Aluminum (Al) is a metal that is toxic to most plants, inhibits root growth
and led to a series influence of metabolic abnornal. PT Great Giant Pineapple
(GGP) in Terbanggi Besar, Central Lampung is a plantation and canning
pineapple that most of its soil is Ultisol soil types with low soil pH (< 5).
Pineapple mostly grown on acid soils with high Al concentration and often poison
the roots, especially at the root tip.
This study was conducted to : 1) determine the pineapple clones of PT
GGP which tolerant and sensitive to Al toxicity, 2) determine critical limit of Al
saturation in Ultisol soil for 3 pineapple clones of PT GGP, 3) study effect of lime
and organic matter soil against controlling Al toxicity in soil and plants for effort
to improve plant growth and nutrient uptake of pineapple plants.
Study consisted of three experiments, namely: 1) Tolerance test of 3
pineapple clones of PT GGP (GP1, GP3 and F180) in 6 level concentration of
for Factorial 3x6 and 5 replications in the greenhouse environment, 2 ) Evaluation
of Al saturation in the Ultisol soil of 3 pineapple clones (GP1, GP3 and F180) in 7
Al saturation level in soil (0% (sand media), < 30%, 30-40%, 40-50%, 50-60%,
60 -70% and > 70%) with Completely Randomized Design for Factorial 3 x 7 and
3 replications in the greenhouse environment, 3) Effect of organic matter and
liming on Al toxicity with Completely Randomized Design for Factorial 3x4x3
and 3 replications which consisted of 3 factors: Al saturation in the soil (low
< 30%, medium 40-50 % and high > 70%), organic matter dosage (0, 20, 40 and
60 ton / ha), and lime dosage (0, 2 and 4 tons/ha).
Result of the first experiment showed that GP3 and F180 clones have high
levels of Al toxicity tolerance which still can produce good shoot and root growth
in high Al stress condition (500 μM AlCl3 or equivalent of 24,3 ppm Al). GP3
clone showed the best growth in number of leafs, number of seminal roots, total
production of roots sugar, P leaf and root uptake and the lowest Al root uptake
compared to other clones. F180 clone produce the best volume water uptake by
root, fresh roots weight, plants weight, leaf uptake of N, Ca and Mg and the
lowest morphology of Al toxicity in root tips than other clones. While GP1 clone
only produce the best of root length, percentage of vertical root weight and K leaf
uptake. Thus we can said that the best level Al tolerance owned successively by
GP3, F180 and GP1 clones.
Result of the second experiment showed that tolerance limit for controlling
Al saturation in the soil which can produce good root growth in GP3 clone
reached at Al saturation below 70% (with soil pH 4,1), while the GP1 and F180
for optimization of soil pH, C organic level in soil, availability of K, Ca and Mg
nutrients in the soil for good plant growth and suppress leaching of bases K, Ca
and Mg in the soil, the author suggest that Al saturation in soil below 40% is the
optimal limit for controlling Al saturation in the soil to reach good pineapple
growth.
Result of the third experiment showed that using of organic matter in soils
which suffered by Al stress will improve root growth compared to shoot growth in
the early stage of pineapple growth (till 4 months after planting) with decreasing
of shoot root ratio, increase the number of seminal roots and root water content.
While using lime to overcome Al stress in the soil more showed to improve leaf
nutrient uptake and available of soil nutrients compared to improve shoot and
root growth.
For producing good root growth at early stage of pineapple growth (0-4
months after planting), optimization leaf and root nutrient uptake and availability
of soil nutrient, the author suggest for low Al saturation in the soil (< 30%)
require using lime 2 tons/ha and without organic matter, for moderate Al
saturation (40-50%) require lime 4 tons/ha and organic material 20 tons /ha or
without lime and organic matter 40 tons/ha, while for high Al saturation (> 70%)
RINGKASAN
Uji Toleransi Tiga Klon Nanas [Ananas comosus (L.) Merr.] dalam Pengaruh Pemberian Kapur dan Bahan Organik terhadap Toksisitas Aluminium
di Tanah Ultisol PT Great Giant Pineapple
Oleh
Dudy Arfian
Aluminium (Al) adalah logam yang toksik pada kebanyakan tanaman,
menghambat pertumbuhan akar dan menyebabkan serangkaian pengaruh
metabo-lisme yang abnornal. PT Great Giant Pineapple (GGP) di Terbanggi Besar,
Lampung Tengah adalah perkebunan dan pengalengan buah nanas yang sebagian
besar tanahnya tipe Ultisol dengan pH tanah rendah (< 5). Nanas kebanyakan
tumbuh di tanah asam dengan konsentrasi Al tinggi dan sering meracuni
perakarannya, terutama pada bagian ujung akar.
Penelitian ini bertujuan untuk : 1) menentukan klon nanas di PT GGP yang
toleran dan sensitif terhadap toksisitas Al, 2) mempelajari batas kritis kejenuhan
Al terhadap 3 klon nanas di tanah Ultisol PT GGP, 3) mempelajari pengaruh
pemberian kapur dan atau bahan organik tanah terhadap pengendalian toksisitas
Al di tanah dan tanaman dalam upaya meningkatkan pertumbuhan dan serapan
Penelitian ini terdiri dari 3 percobaan yaitu : 1) Uji toleransi 3 klon nanas
(GP1, GP3 dan F180) dalam 6 taraf konsentrasi AlCl3 (0, 100, 200, 300, 400 dan
500 μM) dengan RAK Faktorial 3x6 dan 5 ulangan di lingkungan rumah kaca, 2)
Evaluasi kejenuhan Al di tanah dari 3 klon Nanas (GP1, GP3 dan F180) dalam 7
taraf kejenuhan Al di tanah Ultisol (0% (media pasir), < 30%, 30-40%, 40-50%,
50-60%, 60-70% dan > 70%) dengan RAK Faktorial 3x7 dan 3 ulangan di
lingkungan rumah kaca, 3) Pengaruh bahan organik dan pengapuran terhadap 3
level kejenuhan Al di tanah Ultisol dengan RAK Faktorial 3x4x3 dan 3 ulangan
yang terdiri dari 3 faktor yaitu kejenuhan Al di tanah (rendah < 30%, sedang
40-50% dan tinggi > 70%), dosis bahan organik (0, 20, 40 dan 60 ton/ha), dan dosis
kapur (0, 2 dan 4 ton/ha).
Hasil penelitian pertama memperlihatkan bahwa klon GP3 dan F180
adalah klon-klon yang memiliki tingkat toleransi terhadap toksisitas Al yang
terbaik dengan tetap dapat menghasilkan pertumbuhan tajuk dan akar yang baik
dalam kondisi cekaman Al yang tinggi (500 μM AlCl3 atau setara 24,3 ppm Al) .
Klon GP3 memperlihatkan pertumbuhan jumlah daun, jumlah akar, produksi gula
akar, serapan P daun yang tertinggi dan serapan Al akar terendah dibandingkan
klon lainnya. Klon F180 menghasilkan volume serapan air akar, berat basah akar,
berat tanaman, serapan N, Ca dan Mg daun yang tertinggi dan morfologi toksisitas
Al di ujung akar yang terendah dibandingkan klon lainnya. Sedangkan klon GP1
hanya menghasilkan panjang akar, persen berat akar vertikal, dan serapan K daun
yang terbaik. Dengan demikian dapat dikatakan tingkat toleransi terbaik terhadap
Hasil penelitian kedua memperlihatkan bahwa batas toleransi kejenuhan
Al di tanah yang menghasilkan pertumbuhan akar yang baik pada klon GP3
dicapai pada kejenuhan Al di tanah ≤ 70% (dengan pH tanah 4,1), sedangkan
pada klon GP1 dan F180 pada kejenuhan Al di tanah ≤ 30% (dengan pH tanah
4,3). Namun jika dilihat dari sisi optimalisasi pH tanah, C organik tanah,
ketersediaan hara K, Ca dan Mg di tanah yang optimal bagi tanaman dan menekan
terjadinya pencucian basa-basa K, Ca dan Mg di tanah maka kejenuhan Al di
tanah ≤ 40% adalah batas toleransi Al yang cukup optimal di tanah untuk
pertumbuhan nanas yang baik.
Hasil penelitian ketiga memperlihatkan bahwa penggunaan bahan organik
pada tanah-tanah yang mengalami cekaman Al akan memperbaiki pertumbuhan
akar dibandingkan pertumbuhan tajuk di awal pertumbuhan nanas hingga 4 BST
dengan menurunkan rasio tajuk akar dan meningkatkan jumlah akar seminal dan
kadar air akar. Sedangkan penggunaan kapur untuk mengatasi cekaman Al di
tanah lebih memperlihatkan perbaikan serapan hara daun dan ketersediaan
hara-hara di tanah dibandingkan perbaikan pertumbuhan tajuk dan akar.
Untuk menghasilkan keseimbanganpertumbuhan tajuk dan akar yang baik
pada umur awal pertumbuhan nanas (0-4 bulan setelah tanam), optimalisasi
serapan hara daun, akar dan ketersediaan hara-hara di tanah, maka untuk tanah
dengan kejenuhan Al rendah (< 30%) memerlukan pemberian kapur 2 ton/ha dan
tanpa bahan organik, untuk tanah dengan kejenuhan Al sedang (40-50%) perlu
pemberian kapur 4 ton/ha dan bahan organik 20 ton/ha atau tanpa kapur dan
bahan organik 40 ton/ha, sedangkan untuk tanah dengan kejenuhan Al tinggi
UJI TOLERANSI TIGA KLON NANAS
[
Ananas comosus
(L.) Merr.] DALAM PENGARUH
PEMBERIAN KAPUR DAN BAHAN ORGANIK TERHADAP
TOKSISITAS ALUMINIUM DI TANAH ULTISOL
PT GREAT GIANT PINEAPPLE
Oleh
DUDY ARFIAN
Tesis
Sebagai Salah Satu Syarat untuk Mencapai Gelar
MAGISTER SAINS
Pada
Program Pascasarjana Magister Agronomi Fakultas Pertanian Universitas Lampung
FAKULTAS PERTANIAN UNIVERSITAS LAMPUNG
UJI TOLERANSI TIGA KLON NANAS
[
Ananas comosus
(L.) Merr.] DALAM PENGARUH
PEMBERIAN KAPUR DAN BAHAN ORGANIK TERHADAP
TOKSISITAS ALUMINIUM DI TANAH ULTISOL
PT GREAT GIANT PINEAPPLE
(Tesis)
Oleh
DUDY ARFIAN
PROGRAM PASCASARJANA MAGISTER AGRONOMI FAKULTAS PERTANIAN
UNIVERSITAS LAMPUNG BANDAR LAMPUNG
i DAFTAR GAMBAR
Gambar Halaman 1. Distribusi daun tanaman berdasarkan umur daun... 2 2. Sebaran kejenuhan Al di tanah PT Great Giant Pineapple tahun
2013... 6 3. Penanaman bibit crown dalam kaleng ukuran A2 berlapis kantong
plastik 2 kg yang berisi larutan AlCl3 sesuai jenis perlakuan pada Percobaan 1... 28 4. Penggunaan polibag 15 kg berlapis plastik kresek putih untuk
penanaman bibit crown pada Percobaan 2... 29 5. Penyaringan tanah Percobaan 3 dengan saringan 2 mm dan
inkubasi perlakuan percobaan... 30 6. Penggunaan polibag 15 kg penanaman bibit crown pada
Percobaan 3 di ruang terbuka... 31 7. Pengukuran warna daun dengan Chlorofilmeter SPAD 502... 32 8. Pengaruh jenis klon dan konsentrasi larutan AlCl3 terhadap tinggi
tanaman (TT) umur 16 MST Percobaan 1 ... 37 9. Kurva pertumbuhan tinggi tanaman 3 klon nanas dalam pengaruh
6 konsentrasi AlCl3 umur 1-16 MST... 38 10.Pengaruh jenis klon dan konsentrasi larutan AlCl3 terhadap panjang
daun (PD) umur 16 MST pada Percobaan 1 ... 39 11.Pengaruh interaksi jenis klon dan konsentrasi larutan AlCl3 terhadap
panjang daun-D (PD) umur 6 MST Percobaan 1 ... 40 12.Kurva pertumbuhan panjang daun-D 3 klon nanas dalam pengaruh
6 konsentrasi AlCl3 umur 1-16 MST... 40 13.Pengaruh interaksi jenis klon dan konsentrasi larutan AlCl3 terhadap
jumlah daun (JD) umur 6 MST Percobaan 1 ... 41 14.Kurva pertumbuhan jumlah daun 3 klon nanas dalam pengaruh
6 konsentrasi AlCl3 umur 1-16 MST... 42 15.Pengaruh interaksi jenis klon dan konsentrasi larutan AlCl3 terhadap
panjang akar (PA) umur 6 MST Percobaan 1 ... 44 16.Kurva pertumbuhan panjang akar 3 klon nanas dalam pengaruh
ii
17.Pengaruh interaksi jenis klon dan konsentrasi larutan AlCl3 terhadap jumlah akar (JA) umur 6 MST Percobaan 1 ... 45 18.Kurva pertumbuhan jumlah akar 3 klon nanas dalam pengaruh
6 konsentrasi AlCl3 umur 1-16 MST... 46 19.Pengaruh jenis klon dan konsentrasi larutan AlCl3 terhadap volume
serapan air akar (VSA) umur 14 MST Percobaan 1 ... 47 20.Pengaruh interaksi jenis klon dan konsentrasi larutan AlCl3 terhadap
berat basah akar (BBA) dan persen berat akar vertikal (%BAV)
umur 16 MST Percobaan 1 ... 49 21.Bentuk perakaran 3 klon nanas pada berbagai level toksisitas
AlCl3 pada Percobaan 1... 51 22. Pengaruh interaksi jenis klon dan konsentrasi larutan AlCl3 terhadap
berat tanaman umur 16 MST Percobaan 1 ... 53 23.Kandungan gula akar tiga jenis klon pada enam taraf toksisitas
AlCl3 Percobaan 1... 55
AlCl3 setelah perlakuan staining akar dalam larutan hematoxylin pada Percobaan 1... 59 27.Morfologi tanaman dan akar 3 klon nanas pada 6 taraf konsentrasi
AlCl3 Percobaan 1... 60 28.Pertumbuhan tinggi tanaman dari 3 klon nanas pada 7 taraf
kejenuhan Al di tanah pada umur 1–4 BST di Percobaan 2... 62 29.Pertumbuhan panjang daun-D dari 3 klon nanas pada 7 taraf
kejenuhan Al di tanah pada umur 1–4 BST di Percobaan 2... 64 30.Pertumbuhan lebar daun-D dari 3 klon nanas pada 7 taraf
kejenuhan Al di tanah pada umur 1–4 BST di Percobaan 2... 66 31.Pertumbuhan indeks daun-D dari 3 klon nanas pada 7 taraf
kejenuhan Al di tanah pada umur 1–4 BST di Percobaan 2... 68 32.Pertumbuhan jumlah daun dari 3 klon nanas pada 7 taraf
kejenuhan Al di tanah pada umur 1–4 BST di Percobaan 2... 70 33. Pengaruh interaksi jenis klon dan kejenuhan Al di tanahterhadap
berat kering akar umur 4 BST Percobaan 2 ... 72
pada 7 taraf kejenuhan Al di tanah pada umur 4 BST di
Percobaan 2... 78 37.Kandungan hara kation tercuci di larutan tanah dari 3 klon nanas
pada 7 taraf kejenuhan Al di tanah pada umur 4 BST di
iii
38.Serapan hara N, P, K, Ca, dan Mg di daun pada umur 4 BST pada 3 tingkat kejenuhan Al dalam tanah dalam pengaruh pemberian
kapur dan bahan organik dan pengapuran di Percobaan 3... 91
39.Serapan hara N, P, K, Ca, Mg dan Al di akar nanas pada umur 4 BST pada 3 tingkat kejenuhan Al dalam tanah dalam pengaruh pemberian kapur dan bahan organik dan pengapuran di Percobaan 3 93
40.Analisis hara N, P, K, Ca, Mg dan Al di tanah umur 4 BST pada 3 tingkat kejenuhan Al dalam tanah dalam pengaruh pemberian kapur dan bahan organik dan pengapuran di Percobaan 3... 96
41.Denah percobaan 1... . 123
42.Denah percobaan 2... 124
i DAFTAR ISI
DAFTAR TABEL... vii
DAFTAR GAMBAR... xiii
I. PENDAHULUAN... 1
1.1 Latar Belakang dan Masalah... 1
1.2 Tujuan... 7
1.3 Kerangka Pemikiran... 7
1.4 Hipotesis... 11
II. TINJAUAN PUSTAKA... 13
2.1 Tanah Ultisol... 13
2.2 Toksisitas Aluminium pada Nanas... 14
2.3 Pengaruh Pengapuran dan Bahan Organik terhadap Toksisitas Aluminium... 16
III. METODE PENELITIAN... 22
3.1 Tempat dan Waktu... 22
ii
3.3 Metode... 23
3.4 Pelaksanaan... 28
3.5 Pengamatan... 31
IV. HASIL DAN PEMBAHASAN... 36
4.1 Hasil... 36
4.1.1 Percobaan 1 : Uji Toleransi 3 Klon Nanas terhadap Toksisitas Al dengan Metode Kultur ... 36
4.1.1.1 Tinggi Tanaman ... 36
4.1.1.2 Panjang Daun-D ... 37
4.1.1.3 Jumlah Daun... 41
4.1.1.4 Panjang Akar... 43
4.1.1.5 Jumlah Akar... 45
4.1.1.6 Volume Serapan Air... 47
4.1.1.7 Pertumbuhan Akar... 48
4.1.1.8 Warna Daun dan pH Larutan Kultur Air... 52
4.1.1.9 Pertumbuhan Berat Tanaman... 53
4.1.1.10 Produksi Gula Akar... 54
4.1.1.11 Analisis Hara Daun dan Akar... 55
4.1.1.12 Morfologi toksisitas aluminium di akar dan tanaman nanas... 59
4.1.2 Percobaan 2 : Evaluasi Toksisitas Al dari 3 Klon Nanas dalam Berbagai Kejenuhan Aluminium di Tanah ... 61
4.1.2.1 Tinggi Tanaman ... 61
iii
4.1.2.3 Lebar Daun-D ... 65
4.1.2.4 Indeks Daun-D ... 67
4.1.2.5 Jumlah Daun... 69
4.1.2.6 Pertumbuhan Akar.... ... 71
4.1.2.7 Pertumbuhan Berat Tanaman... 73
4.1.2.8 Analisis Hara Daun, Akar dan Tanah... 74
4.1.2.9 Analisis Hara Tanah Tercuci... 79
4.1.3 Percobaan 3 : Pengaruh Bahan Organik dan Pengapuran terhadap 3 Jenis Kejenuhan Al di Tanah ... 80
4.1.3.1 Tinggi Tanaman ... 80
4.1.3.2 Panjang Daun-D ... 81
4.1.3.3 Lebar Daun-D ... 82
4.1.3.4 Indeks Daun-D ... 83
4.1.3.5 Jumlah Daun... 84
4.1.3.6 Warna Daun... 85
4.1.3.7 Pertumbuhan Akar... 86
4.1.3.8 Pertumbuhan Berat Tanaman... 88
4.1.3.9 Analisis Hara Daun, Akar dan Tanah... 90
4.2 Pembahasan... 97
4.2.1 Percobaan 1 ... 97
4.2.2 Percobaan 2 ... 102
4.2.3 Percobaan 3... 106
V. SIMPULAN DAN SARAN... 112
iv
5.2 Saran... ... 114
DAFTAR PUSTAKA... 115
LAMPIRAN... 122
Gambar 41 – 43... 123-125
i DAFTAR TABEL
Tabel Halaman
1. Deskripsi karakteristik vegetatif dan generatif 3 klon PT GGP... 5
2. Klasifikasi kesesuaian lahan untuk tanaman nanas untuk karakteristik kejenuhan Al... 7
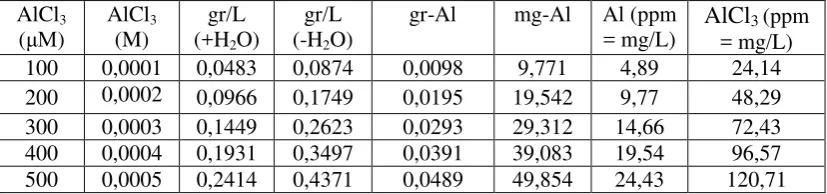
3. Metoda preparasi bahan perlakuan AlCl3 pada Percobaan 1... 24
4. Analisa tanah pendahuluan percobaan 2... 27
5. Analisa tanah pendahuluan percobaan 3... 27
6. Analisa hara kandungan bahan organik yang dipakai dalam Percobaan 3 produksi PT GGP... 30
7. Metoda analisis contoh daun, akar dan tanah Percobaan 1, 2 dan 3 33
8. Hasil uji F pengaruh jenis klon dan konsentrasi AlCl3 terhadap tinggi tanaman umur 1-16 MST Percobaan 1... 37
9. Hasil uji F pengaruh jenis klon dan konsentrasi AlCl3 terhadap panjang daun-D umur 1-16 MST Percobaan 1... 39
10.Hasil uji F pengaruh jenis klon dan konsentrasi AlCl3 terhadap jumlah daun umur 1-16 MST Percobaan 1... 41
11.Hasil uji F pengaruh jenis klon dan konsentrasi AlCl3 terhadap panjang akar umur 1-16 MST Percobaan 1... 43
12.Hasil uji F pengaruh jenis klon dan konsentrasi AlCl3 terhadap jumlah akar umur 1-16 MST Percobaan 1... 45
13.Pengaruh jenis klon dan konsentrasi AlCl3 terhadap volume serapan air oleh akar Percobaan 1... 48
14.Pengaruh jenis klon dan konsentrasi AlCl3 terhadap pertumbuhan akar Percobaan 1 ... 50
15.Pengaruh jenis klon dan konsentrasi AlCl3 terhadap warna daun dan pH larutan kultur air umur 11 MST pada Percobaan 1... 52
16. Pengaruh jenis klon dan konsentrasi AlCl3 terhadap pertumbuhan berat tanaman Percobaan 1... 54
17.Pengaruh jenis klon dan kejenuhan Al di tanah terhadap tinggi tanaman (cm) Percobaan 2... 61
18.Pengaruh jenis klon dan kejenuhan Al di tanah terhadap panjang daun-D (cm) Percobaan 2... 63
ii
20.Pengaruh jenis klon dan kejenuhan Al di tanah terhadap indeks
daun-D (cm) Percobaan 2... 67 21. Pengaruh jenis klon dan kejenuhan Al di tanah terhadap jumlah
daun Percobaan 2 ... 69 22.Pengaruh jenis klon dan kejenuhan Al di tanah terhadap
pertumbuhan perakaran pada umur 4 BST Percobaan 2... 72 23.Pengaruh jenis klon dan kejenuhan Al di tanah terhadap
pertumbuhan berat tanaman Percobaan 2... 73 24.Pengaruh kejenuhan Al dalam tanah, bahan organik dan pengapuran
terhadap tinggi tanaman (cm) Percobaan 3... 80 25.Pengaruh kejenuhan Al dalam tanah , bahan organik dan pengapuran
terhadap panjang daun-D (cm) Percobaan 3... 81 26.Pengaruh kejenuhan Al dalam tanah , bahan organik dan pengapuran
terhadap lebar daun-D (cm) Percobaan 3... 82 27.Pengaruh kejenuhan Al dalam tanah, bahan organik dan pengapuran
terhadap indeks daun-D (cm2) Percobaan 3... 83 28.Pengaruh kejenuhan Al dalam tanah, bahan organik dan pengapuran
terhadap jumlah daun Percobaan 3... 84 29.Pengaruh kejenuhan Al dalam tanah, bahan organik dan pengapuran
terhadap warna daun-D Percobaan 3... 85 30.Pengaruh kejenuhan Al dalam tanah, bahan organik dan pengapuran
terhadap pertumbuhan akar Percobaan 3... 87 31.Pengaruh kejenuhan Al dalam tanah, bahan organik dan pengapuran
terhadap pertumbuhan berat tanaman Percobaan 3... 89 32.Pengaruh jenis klon dan konsentrasi larutan AlCl3 terhadap tinggi
tanaman (cm) Percobaan 1... 126 33.Pengaruh jenis klon dan konsentrasi larutan AlCl3 terhadap panjang
daun-D (cm) Percobaan 1... 127 34.Pengaruh jenis klon dan konsentrasi larutan AlCl3 terhadap jumlah
daun Percobaan 1... 128 35.Pengaruh jenis klon dan konsentrasi larutan AlCl3 terhadap panjang
akar (cm) Percobaan 1... 129 36.Pengaruh jenis klon dan konsentrasi larutan AlCl3 terhadap jumlah
iii
51.Analisis sidik ragam tinggi tanaman (cm) Percobaan 1 pada 15 MST . 135 52. Analisis sidik ragam tinggi tanaman (cm) Percobaan 1 pada 16 MST . 136 53.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 1 MST . 136 54.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 2 MST . 136 55.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 3 MST . 137 56.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 4 MST . 137 57.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 5 MST . 137 58.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 6 MST . 138 59.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 7 MST . 138 60.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 8 MST . 138
61.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 9 MST 139
62. Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 10 MST 139 63.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 11 MST 139 64.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 12 MST 140 65.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 13 MST 140 66.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 14 MST 140 67.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 15 MST 141 68.Analisis sidik ragam panjang daun-D (cm) Percobaan 1 pada 16 MST 141 69.Analisis sidik ragam jumlah daun Percobaan 1 pada 1 MST... 141
70.Analisis sidik ragam jumlah daun Percobaan 1 pada 2 MST... 142
71.Analisis sidik ragam jumlah daun Percobaan 1 pada 3 MST... 142
72. Analisis sidik ragam jumlah daun Percobaan 1 pada 4 MST... 142
73.Analisis sidik ragam jumlah daun Percobaan 1 pada 5 MST... 143
74.Analisis sidik ragam jumlah daun Percobaan 1 pada 6 MST... 143
75.Analisis sidik ragam jumlah daun Percobaan 1 pada 7 MST... 143
76.Analisis sidik ragam jumlah daun Percobaan 1 pada 8 MST... 144
77.Analisis sidik ragam jumlah daun Percobaan 1 pada 9 MST... 144
78.Analisis sidik ragam jumlah daun Percobaan 1 pada 10 MST... 144
79.Analisis sidik ragam jumlah daun Percobaan 1 pada 11 MST... 145
80.Analisis sidik ragam jumlah daun Percobaan 1 pada 12 MST... 145
81.Analisis sidik ragam jumlah daun Percobaan 1 pada 13 MST... 145
82.Analisis sidik ragam jumlah daun Percobaan 1 pada 14 MST... 146
83.Analisis sidik ragam jumlah daun Percobaan 1 pada 15 MST... 146
84.Analisis sidik ragam jumlah daun Percobaan 1 pada 16 MST... 146
85. Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 1 MST... 147
86.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 2 MST... 147
87.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 3 MST... 147
88.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 4 MST... 148
89.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 5 MST... 148
90.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 6 MST... 148
91.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 7 MST... 149
92.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 8 MST... 149
93.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 9 MST... 149
94.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 10 MST... 150
95. Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 11 MST... 150
96.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 12 MST... 150
97.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 13 MST... 151
iv
99.Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 15 MST... 151
100. Analisis sidik ragam panjang akar (cm) Percobaan 1 pada 16 MST... 152
101.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 1 MST... 152
102.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 2 MST... 152
103.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 3 MST... 153
104.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 4 MST... 153
105.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 5 MST... 153
106.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 6 MST... 154
107.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 7 MST... 154
108.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 8 MST... 154
109.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 9 MST... 155
110. Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 10 MST... 155
111.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 11 MST... 155
112.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 12 MST... 156
113.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 13 MST... 156
114.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 14 MST... 156
115.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 15 MST... 157
116.Analisis sidik ragam jumlah akar seminal Percobaan 1 pada 16 MST... 157
117.Analisis sidik ragam volume serapan air (ml/tanaman/minggu) Percobaan 1 pada 11 MST... 157
118.Analisis sidik ragam volume serapan air (ml/tanaman/minggu) Percobaan 1 pada 12 MST... 158
119.Analisis sidik ragam volume serapan air (ml/tanaman/2minggu) Percobaan 1 pada 14 MST... 158
120.Analisis sidik ragam berat basah akar (gr) Percobaan 1 pada 16 MST.. 158
121.Analisis sidik ragam berat kering oven akar (gr) Percobaan 1 pada 16 MST... 159
122.Analisis sidik ragam persen berat akar vertikal Percobaan 1 pada 16 MST... 159
123.Analisis sidik ragam warna daun (klorofilmeter) Percobaan 1 pada 11 MST Percobaan 1 pada 16 MST... 159
124.Analisis sidik ragam pH larutan Percobaan 1 pada 11 MST... 160
125.Analisis sidik ragam berat basah tanaman (gr) Percobaan 1 pada 11 MST Percobaan 1 pada 16 MST... 160
126. Analisis sidik ragam berat kering tanaman (gr) percobaan 1 pada 11 MST Percobaan 1 pada 16 MST... 160
127.Analisis sidik ragam RGR percobaan 1 pada 16 MST... 161
128.Analisis sidik ragam persen kenaikan berat tanaman Percobaan 1 pada 16 MST... 161
129.Analisis sidik ragam rasio tajuk akar tanaman Percobaan 1 pada 16 MST... 161
130.Analisis sidik ragam tinggi tanaman (cm) Percobaan 2 pada 1 BST.... 162
131.Analisis sidik ragam tinggi tanaman (cm) Percobaan 2 pada 2 BST.... 162
132.Analisis sidik ragam tinggi tanaman (cm) Percobaan 2 pada 3 BST.... 162
133. Analisis sidik ragam tinggi tanaman (cm) Percobaan 2 pada 4 BST.... 163
134.Analisis sidik ragam panjang daun-D (cm) Percobaan 2 pada 1 BST... 163
135.Analisis sidik ragam panjang daun-D (cm) Percobaan 2 pada 2 BST... 163
v
137.Analisis sidik ragam panjang daun-D (cm) Percobaan 2 pada 4 BST... 164
138. Analisis sidik ragam lebar daun-D (cm) Percobaan 2 pada 1 BST... 164
139.Analisis sidik ragam lebar daun-D (cm) Percobaan 2 pada 2 BST... 165
140.Analisis sidik ragam lebar daun-D (cm) Percobaan 2 pada 3 BST... 165
141.Analisis sidik ragam lebar daun-D (cm) Percobaan 2 pada 4 BST... 165
142.Analisis sidik ragam indeks daun-D (cm) Percobaan 2 pada 1 BST... 166
143.Analisis sidik ragam indeks daun-D (cm) Percobaan 2 pada 2 BST... 166
144.Analisis sidik ragam indeks daun-D (cm) Percobaan 2 pada 3 BST... 166
145.Analisis sidik ragam indeks daun-D (cm) Percobaan 2 pada 4 BST... 167
146.Analisis sidik ragam jumlah daun Percobaan 2 pada 1 BST... 167
147.Analisis sidik ragam jumlah daun Percobaan 2 pada 2 BST... 167
148. Analisis sidik ragam jumlah daun Percobaan 2 pada 3 BST... 168
149.Analisis sidik ragam jumlah daun percobaan 2 pada 4 BST... 168
150.Analisis sidik ragam panjang akar (cm) Percobaan 2 pada 4 BST... 168
151.Analisis sidik ragam berat basah akar (gr) Percobaan 2 pada 4 BST... 169
152.Analisis sidik ragam berat kering akar (gr) Percobaan 2 pada 4 BST.... 169
153.Analisis sidik ragam jumlah akar seminal Percobaan 2 pada 4 BST.... 169
154.Analisis sidik ragam rerata berat akar (gr) Percobaan 2 pada 4 BST... 170
155.Analisis sidik ragam berat tanaman (gr) Percobaan 2 pada 0 BST... 170
156.Analisis sidik ragam berat tanaman (gr) Percobaan 2 pada 4 BST... 170
157.Analisis sidik ragam rasio tajuk akar Percobaan 2 pada 4 BST... 171
158. Analisis sidik ragam RGR percobaan 2 pada 4 BST... 171
159.Analisis sidik ragam rerata berat akar tajuk akar Percobaan 2 pada 4 BST... 171
160.Analisis sidik ragam tinggi tanaman(cm) Percobaan 3 pada 1 BST... 172
161.Analisis sidik ragam tinggi tanaman(cm) Percobaan 3 pada 2 BST... 172
162.Analisis sidik ragam tinggi tanaman(cm) Percobaan 3 pada 3 BST... 173
163.Analisis sidik ragam tinggi tanaman(cm) Percobaan 3 pada 4 BST... 173
164.Analisis sidik ragam panjang daun-D (cm) Percobaan 3 pada 1 BST... 174
165.Analisis sidik ragam panjang daun-D (cm) Percobaan 3 pada 2 BST... 174
166.Analisis sidik ragam panjang daun-D (cm) Percobaan 3 pada 3 BST... 175
167.Analisis sidik ragam panjang daun-D (cm) Percobaan 3 pada 4 BST... 175
168.Analisis sidik ragam lebar daun-D (cm) Percobaan 3 pada 1 BST... 176
169.Analisis sidik ragam lebar daun-D (cm) Percobaan 3 pada 2 BST... 176
170. Analisis sidik ragam lebar daun-D (cm) Percobaan 3 pada 3 BST... 177
171.Analisis sidik ragam lebar daun-D (cm) Percobaan 3 pada 4 BST... 177
172.Analisis sidik ragam indeks daun-D (cm2) Percobaan 3 pada 1 BST.... 178
173.Analisis sidik ragam indeks daun-D (cm2) Percobaan 3 pada 2 BST.... 178
174.Analisis sidik ragam indeks daun-D (cm2) Percobaan 3 pada 3 BST.... 179
175.Analisis sidik ragam indeks daun-D (cm2) Percobaan 3 pada 4 BST.... 179
176.Analisis sidik ragam jumlah daun Percobaan 3 pada 1 BST... 180
177.Analisis sidik ragam jumlah daun Percobaan 3 pada 2 BST... 180
178.Analisis sidik ragam jumlah daun Percobaan 3 pada 3 BST... 181
179.Analisis sidik ragam jumlah daun Percobaan 3 pada 4 BST... 181
180. Analisis sidik ragam warna daun Percobaan 3 pada 1 BST... 182
181.Analisis sidik ragam warna daun Percobaan 3 pada 2 BST... 182
182.Analisis sidik ragam warna daun Percobaan 3 pada 4 BST... 183
vi
184.Analisis sidik ragam jumlah akar (cm) Percobaan 3 pada 4 BST... 184 185. Analisis sidik ragam berat basah akar (gr) Percobaan 3 pada 4 BST... 184 186.Analisis sidik ragam berat kering akar (gr) Percobaan 3 pada 4 BST.. 185 187.Analisis sidik ragam kadar air akar (%) Percobaan 3 pada 4 BST... 185 188.Analisis sidik ragam berat basah tanaman (gr) Percobaan 3 pada
0 BST... 186 189.Analisis sidik ragam berat basah tanaman (gr) Percobaan 3 pada
4 BST... 186 190.Analisis sidik ragam berat kering tanaman (gr) Percobaan 3 pada
4 BST... 187 191.Analisis sidik ragam kadar air tanaman (%) Percobaan 3 pada
Sesungguhnya dalam penciptaan langit dan bumi,
dan silih bergantinya malam dan siang
terdapat tanda-tanda bagi orang-orang yang berakal,
yaitu orang-orang yang mengingat Allah
sambil berdiri atau duduk atau dalam keadan berbaring dan
mereka memikirkan tentang penciptaan langit dan bumi
(seraya berkata):
"Ya Tuhan kami, tiadalah Engkau menciptakan ini dengan
sia-sia, Maha Suci Engkau, maka peliharalah kami dari
Karya kecil ini kupersembahkan untuk :
Kedua orangtua dan mertuaku,
Istriku tercinta Ir. Suslinda,
Kedua anakku tersayang,
M. Taufiqul Hakim & Alfi Syahriyyah Majidah,
serta seluruh keluarga besar yang telah memberikan doa,
dorongan dan semangat untuk menyelesaikan karya tulis ini.
Dan terkhusus untuk seluruh teman dan sahabat di PT GGP
–
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 20 Juni 1969 di Jakarta
sebagai anak pertama dari enam bersaudara dari Bapak
Ansuruddin Mairun, B.Ac (Alm) dan Ibu Yohanna Rustam,
B.Ac.
Penulis mengawali pendidikannya di Taman Kanak-kanak
Persit Kartika Candra Kirana, Bandar Lampung, yang diselesaikan pada tahun
1975. Setamat dari Sekolah Dasar Persit Kartika Candra Kirana Bandar
Lampung pada tahun 1981, penulis melanjutkan ke Sekolah Menengah Pertama
Persit Kartika Candra Kirana, Bandar Lampung dan tamat pada tahun 1984.
Tahun 1987 penulis tamat dari Sekolah Menengah Atas Negeri 2 Bandar
Lampung, dan diterima sebagai mahasiswa Jurusan Budidaya Pertanian, Fakultas
Pertanian, Institut Pertanian Bogor (IPB) melalui jalur PMDK (Penelusuran Minat
dan Kemampuan).
Selama menjadi mahasiswa penulis pernah aktif di Organisasi Himpunan
Mahasiswa Agronomi (Himagron) Faperta IPB dan Biro Kerohanian Islam (BKI)
IPB. Tahun 1991 penulis melakukan Praktek Kerja Lapang (PKL) pada
Budidaya Tanaman Kedelai di Pasuruan, Jawa Timur. Pada tahun 1992 penulis
Pembumbunan terhadap Pertumbuhan dan Produksi Kacang Bogor (Vigna
subterranea (L.) Verdcourt).
Penulis mulai bekerja sebagai Kepala Kebun Hortikultura di PT Biosonic
Wiramartani di Cugenang, Cianjur, Jawa Barat antara tahun 1993 hingga 1996.
Karir penulis di PT Great Giant Pineapple, Terbanggi Besar, Lampung Tengah,
Lampung dimulai dari Staf Peneliti Agronomi (1996-2003), Staf Evaluasi
Kualitas, Quality Assurance Plantation ( 2003-2008), Kepala Bagian Quality
Assurance Plantation (2008-2011), dan Assistant Manager Project Management
Office - Corporate Planning Departement (2011 hingga kini).
Beberapa riset yang penulis lakukan selama menjadi peneliti di R&D PT GGP di
antaranya adalah Evaluasi penyebab gagal pembungaan di nanas, Evapotranspirasi
di tanaman nanas (ET crop), Evaluasi kebutuhan air di tanaman nanas, Kajian
pengolahan tanah single row, Usaha peningkatan N daun di nanas, Evaluasi jarak
tanam di nanas, Evaluasi dan monitoring kualitas buah nanas, Kurva pertumbuhan
tanaman nanas, Evaluasi tanam dalam di musim kemarau, Evaluasi standar
perawatan nanas, Studi pemangkasan daun saat perkembangan buah di tanaman
Plant Crop nanas, Evaluasi jumlah gulud dan jarak tanam di nanas, Evaluasi
penggunaan bahan organik dosis tinggi di nanas, dan Evaluasi penyebab tingginya
i UCAPAN TERIMA KASIH
Segala pujian hanyalah milik Allah SWT, Yang Maha Suci lagi Maha
Berilmu. Semoga kesejahteraan dan keselamatan dilimpahkan kepada Rasulullah
SAW. Penulis bersyukur kepada-Nya atas selesainya penulisan tesis ini.
Dalam kesempatan ini penulis mengucapkan terima kasih kepada :
1. Bapak Dr. Ir. Paul B. Timotiwu, M.S., selaku Pembimbing Pertama atas
kesediaannya untuk memberikan bimbingan, saran dan kritik dalam proses
penyelesaian tesis ini.
2. Bapak Prof. Dr. Ir. Abdul Kadir Salam, M.Sc., selaku Pembimbing Kedua atas
kesediaannya untuk memberikan bimbingan, saran dan kritik dalam proses
penyelesaian tesis ini.
3. Bapak Dr. Ir. Afandi, M.P., selaku pembahas dan penguji atas saran, arahan,
bantuan dan motivasinya untuk penulisan tesis ini.
4. Bapak Prof. Dr. Ir. Irwan Sukri Banuwa, M.S., selaku Dekan Faperta Unila.
5. Bapak Dr. Ir. Dwi Hapsoro, M.Sc., selaku Ketua Program Studi Magister
Agronomi, Faperta Unila.
6. Ibu Dr. Ir. Tumiar K. B. Manik, M.Sc., selaku Sekretaris Program Studi
ii
7. Bapak Ir. Wayan Ardana, selaku Direktur Produksi PT Great Giant Pineapple
atas izin perkuliahan dan dukungan moril yang telah diberikan selama ini.
8. Bapak Ir. Fauzan, selaku Associate Direktur Plantation PT Great Giant
Pineapple atas saran dan dukungan moril selama proses penelitian.
9. Bapak Ir. Purwito, selaku Manager Research & Development Departement PT
Great Giant Pineapple beserta seluruh kepala bagian dan staf R&D yang telah
banyak membantu selama proses penelitian berlangsung.
10.Bapak Achmad Riyantika, selaku pimpinan di Laboratorium Sentral PT Great
Giant Pineapple Departemen beserta seluruh staf dan laboran yang telah
banyak membantu selama proses analisa percobaan di lab.
11.Para mahasiswa magang dari Universitas Brawijaya – Aris, Ike, Tyas dan
Ikhsan yang telah banyak membantu selama proses penelitian.
12.Rekan-rekan seperjuangan mahasiswa di Magister Agronomi 2013 : Sri
Haryani, Leni Marlina, Sri Nurmayanti, Anisa Ayu Fitri, Reny Mita Sari, Nur
Aflamara, Iskandar Zulkarnain, Heri Hendarto, Endang Sri Ambarwati, dan
Meliya Indriyati atas persahabatan dan kebersamaan selama perkuliahan kita.
13.Semua pihak yang tidak dapat kami sebutkan satu persatu yang telah banyak
membantu dalam proses penelitian ini.
Semoga tesis ini dapat bermanfaat ke depan bagi pengembangan pertanian
khususnya untuk budidaya di lahan asam Ultisol yang tersebar di Indonesia.
Bandar Lampung, 23 Desember 2015
I. PENDAHULUAN
1.1 Latar Belakang dan Masalah
Nanas [Ananas comosus (L.) Merr.] adalah salah satu tanaman komoditas
perkebunan utama di dunia setelah pisang dan jeruk (Bartholomew dkk., 2003).
Umumnya nanas dibudidayakan pada daerah 30 º Lintang Utara hingga 30º
Lintang Selatan, dengan suhu 20-30 º C, dan variasi fotoperiodisme 10-12 jam.
Nanas dilaporkan memiliki daya adaptasi pada kondisi tanah pH rendah dengan
kandungan Al dan Mn yang tinggi (Bartholomew, 2005).
Perakaran nanas umumnya paling banyak tumbuh hingga kedalaman 30
cm dan agak jarang pada kedalaman 30-60 cm. Tinggi tanaman berkisar 0,8
hingga 1,2 meter dan diameter kanopi 1,0 hingga 1,5 meter. Daun nanas
diklasifikasikan berdasarkan bentuk dan posisinya di tanaman sebagai daun A, B,
C, D, E, dan F dari daun tertua di bagian luar dan termuda di bagian tengah
tanaman (Gambar 1). Daun D (‘D’ leaf) merupakan daun termuda di antara daun
dewasa yang paling aktif secara fisiologi dan digunakan untuk mengevaluasi
pertumbuhan dan status nutrisi tanaman. Daun ini mudah diidentifikasi pada
tanaman nanas karena merupakan daun terpanjang dengan sudut daun 45º dari
2
Gambar 1. Distribusi daun tanaman berdasarkan umur daun (A - tertua; F – termuda) (Malavolta, 1982 dalam Souza dan Reinhardt, 2001).
Nanas umumnya ditanam pada lahan asam dengan konsentrasi Aluminium
(Al) yang tinggi dan sering meracuni perakarannya. Kebanyakan jenis nanas
sangat sensitif terhadap toksisitas Al (Lin dan Chen, 2011). Sebagian besar tanah
di PT Great Giant Pineapple merupakan jenis tanah Ultisol, dan sebagian lagi
berjenis tanah Inceptisol (Sudarminto, 2003). Subandi (2007) menyebutkan
bahwa tanah jenis Ultisol tergolong lahan suboptimal karena tanahnya kurang
subur, bereaksi asam, mengandung Al, Fe, dan Mn dalam jumlah tinggi sehingga
dapat meracuni tanaman. Lahan asam pada umumnya miskin bahan organik dan
hara makro N, P, K, Ca, dan Mg. Pemberian bahan ameliorasi kapur, bahan
organik, dan pemupukan N, P, dan K merupakan kunci untuk memperbaiki
kesuburan tanah kering asam.
Al adalah logam yang berlimpah di kulit bumi. Kebanyakan Al menyatu
ke dalam mineral aluminosilikat di dalam tanah dan dalam jumlah yang sangat
kecil dalam bentuk terlarut yang mampu untuk mempengaruhi sistem biologi
3 mineral meningkatkan keasaman tanah. Al yang terlarut dalam tanah asam
diketahui akan menyebabkan toksisitas terhadap pertumbuhan tanaman budidaya
(Bolan dkk. dalam Van dkk., 1994). Al(H2O)63+ atau lebih dikenal dengan Al3+
dominan ketika pH di bawah 5 dan dalam bentuk toksik. Toksisitas Al menjadi
faktor pembatas utama produktivitas tanaman di tanah asam, miskin akan hara Ca
dan Mg (Vitorello dkk., 2005).
Gejala awal dari toksisitas Al adalah penghambatan pertumbuhan.
Absorpsi hara dan fungsi sel akan terganggu setelah terpapar konsentrasi Al
tinggi. Ujung akar adalah daerah tempat Al dan akar berinteraksi, dinding sel
akar memiliki mekanisme untuk melindungi masuknya Al ke dalam akar.
Dinding sel akar terbentuk dari bahan pektin yang bermuatan negatif yang
berfungsi untuk menarik kation-kation. Ketika ujung akar dijenuhi oleh Al,
serapan hara seperti K+, Ca2+, Mg2+ dan NO3- akan menurun untuk memasuki
dinding sel akar. Jika ikatan Al ini berlebihan muncul di antara Al dan dinding sel
akar, pertumbuhan akar akan terhambat (Lin dan Chen, 2011). Hasil penelitian
Yamamoto dkk. (1992) dalamOktavidiati (2002) mendapatkan bahwa toksisitas
Al selain mengakibatkan tanaman kekurangan unsur hara juga mengubah struktur
dan fungsi dari membran plasma dan menghalangi pembelahan sel pada
ujung-ujung akar. Untuk mengatasi toksisitas Al maka tanaman menunjukkan berbagai
respon, di antaranya dengan membangun sistem toleransinya.
Le Van dan Masuda (2004) telah melakukan evaluasi karakteristik
beberapa varietas nanas yang toleran terhadap Al dan menemukan bahwa
penghambatan terjadi ketika diberi perlakuan AlCl3 300 ppm. Setelah terkena
4 lebih tahan daripada klon yang sensitif Al. Klon nanas yang toleran
menyekresikan asam malat lebih banyak dibandingkan klon yang sensitif.
Konsentrasi asam organik lebih tinggi pada daerah apoplast ujung akar daripada
rizosfir. Asam organik berinteraksi dengan komponen dinding sel secara fisiologi
dan biokimia dan meningkatkan toleransi terhadap toksisitas Al .
PT Great Giant Pineapple saat ini membudidayakan nanas varietas Smooth
Cayenne dengan 3 klon utama yang sering digunakan untuk produksi yaitu klon
GP1, GP3 dan F180. Keragaan tiga klon ini di lapangan memiliki karakteristik
yang khas dari sifat vegetatif dan generatifnya seperti disajikan pada Tabel 1 .
Klon GP3 dan F180 umumnya memiliki sifat perakaran yang lebih baik
dibandingkan klon lainnya (Trilaksono, 2012). Hal ini diduga berkaitan dengan
sifat toleransi klon GP3 dan F180 yang lebih baik terhadap kondisi lahan asam di
tanah Ultisol PT Great Giant Pineapple. Informasi mengenai toleransi tiga klon
ini terhadap toksisitas Al di tanah Ultisol belum pernah dipelajari secara
mendalam.
Al dapat dipertukarkan merupakan kation dominan yang berhubungan
dengan keasaman tanah. Ion hidrogen yang dihasilkan dari pelapukan bahan
organik tidak mantap dalam mineral tanah karena bereaksi dengan liat silikat dan
membebaskan Al dapat dipertukarkan dan asam silikat. Al dapat dipertukarkan
sedikit atau tidak ditemukan pada pH yang lebih tinggi dari 5,5. Ukuran
keasaman tanah yang berguna adalah persentase kejenuhan Al. Al dalam larutan
tanah akan meningkat sangat tajam jika kejenuhan Al > 60%. Terdapat < 1 ppm
5 Tabel 1. Deskripsi karakteristik vegetatif dan generatif 3 klon PT GGP.
Klon GP1 Klon GP3 Klon F180
Tanaman
panjang akar : kurang lebih 25 cm
jumlah daun saat forcing: 40 - 60 cm
daun-D : panjang 65 - 79 cm, lebar 4,0 - 5,2 cm
berat/panjang bonggol: 340 - 400 gr, 40 - 60 cm
berat tanaman saat forcing : 2,1 – 2,5 kg
berat/panjang bonggol: 220 - 320 gr, 14 - 20 cm
berat tanaman saat forcing : 4 - 8 kg
berat/panjang bonggol: 240 gr, 14 - 18 cm
mata buah sedikit menonjol, berwarna hijau gelap
warna daging kuning cerah, rasa manis agak masam, kompak dan berserat kasar
jumlah mata : lingkar panjang 12 - 17, pendek 8–10
rasio berat buah / tanaman: 0,38 – 0,50
Buah
bentuk cenderung silindris
mata buah rata berwarna hijau tua
rasio berat buah / tanaman: 0,48 – 0,65
Buah
bentuk buah cenderung kerucut
mata buah sedikit menonjol berwarna hijau muda
warna daging kuning cerah, rasa manis, kompak dan berserat kasar
jumlah mata : lingkar panjang 11 - 14, pendek 7 – 10
rasio berat buah / tanaman: 0,44 – 0,60
Crown
warna hijau keunguan
ukuran : panjang 10 sd 20 cm berat 100 sd 270 gr
daun crown : spiral beraturan
Crown
warna hijau keunguan
ukuran : panjang 13 - 20 cm, berat 100 - 350 gr
daun crown: tidak beraturan
Crown
warna hijau keunguan
ukuran : panjang 19 - 24 cm berat 100 - 400 gr
daun crown : tidak beraturan
Produksi
potensi produksi PC : 55-80 ton/ha & RC 20-45 ton/ha dengan distribusi buah besar (grade buah >2T) : PC 35-50%, RC (30-40%).
perakaran kurang bagus, tidak tahan kekeringan
lebih rentan penyakit virus layu mealybug
hasil seleksi klon lokal (konvensional)
relatip lebih tahan penyakit busuk hati (Phythoptora sp.)
peduncle relatip pendek, buah tidak mudah rebah
Produksi
potensi produksi PC 80 – 125 ton/ha, RC 40-45 ton/ha dengan distribusi buah besar busuk hati (Phythoptora sp.)
brix yang tinggi berpotensi penyakit buah lebih tinggi
Produksi
potensi suckering yang bagus untuk mendukung penyediaan bibit / RC
perakaran bagus, mampu tahan kekeringan
rentan terhadap penyakit busuk hati (Phythoptora sp.)
brix yang tinggi berpotensi penyakit buah lebih tinggi
Rasa kurang disukai konsumen
6 Kendala utama bagi pertumbuhan tanaman di tanah asam adalah
keracunan Al, Fe, dan Mn yang akan menghambat pertumbuhan akar serta
translokasi P dan Ca ke bagian tanaman sehingga tanaman mengalami defisiensi
hara P karena terikat kuat pada partikel tanah seperti mineral liat dan
oksida-oksida besi dan Al membentuk Al dan Fe fosfat sehingga menjadi tidak tersedia
bagi tanaman. Tanah ultisol memiliki produktivitas lahan yang rendah karena
sifat-sifat tanah seperti: pH dan KTK tanah yang rendah, miskin kation basa,
Al-dd tinggi yang dapat meracuni tanaman, fiksasi unsur N, P, K, dan Ca serta mudah
tererosi (BBPPL, 2015).
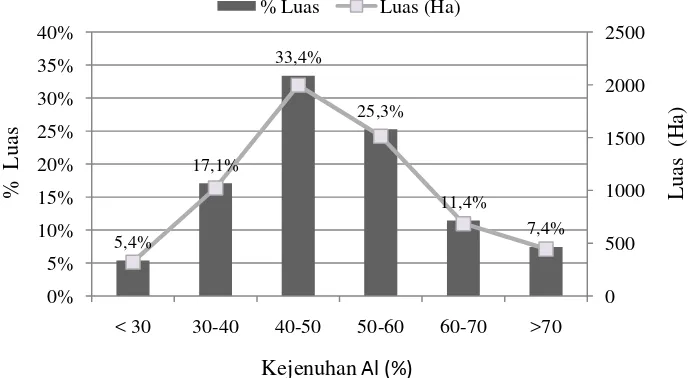
Hasil analisa tanah di lahan produksi nanas aktif PT Great Giant
Pineapple tahun 2013 memperlihatkan bahwa kejenuhan Al > 60% mencapai
luasan 1129,7 Ha atau 18,8% luasan (Gambar 2), yang menurut klasifikasi
kesesuaian lahan untuk nanas (Tabel 2) tanah jenis ini termasuk dalam kelas tanah
tidak sesuai (N1 dan N2) dan sesuai dengan ameliorasi (S3).
Gambar 2. Sebaran kejenuhan Al di lahan produksi nanas aktif PT Great Giant Pineapple tahun 2013.
7 Tabel 2. Klasifikasi kesesuaian lahan untuk tanaman nanas untuk
karakteristik kejenuhan Al.
Berdasarkan identifikasi dan perumusan masalah yang telah disusun maka
ditetapkan tujuan penelitian sebagai berikut :
1. Menentukan klon nanas di PT GGP yang toleran dan sensitif terhadap
toksisitas Al.
2. Mempelajari batas kritis kejenuhan Al terhadap 3 klon nanas di tanah
Ultisol PT GGP.
3. Mempelajari pengaruh pemberian kapur dan atau bahan organik tanah
terhadap pengendalian toksisitas Al di tanah dan tanaman dalam upaya
meningkatkan pertumbuhan dan serapan hara.
1.3Kerangka Pemikiran
Penjelasan teoritis terhadap pertanyaan yang telah dikemukakan di atas
8 Nanas adalah tanaman yang dapat beradaptasi dan tumbuh baik dalam
lingkungan tanah asam dengan pH optimal 4,5 – 5,5. Nanas termasuk tanaman
yang toleran terhadap tanah yang memiliki Al dapat ditukar tinggi dan
mengandung Mn yang umum terjadi pada tanah yang sangat asam (Souza dan
Reinhardt, 2001).
Setiap spesies dan genotip tanaman memperlihatkan variasi toleransi dan
sensitivitas terhadap toksisitas Al. Beberapa studi membuktikan bahwa apoplast
akar berperan penting dalam mekanisme toleransi dengan memproduksi
asam-asam organik seperti asam-asam malat dan asam-asam sitrat. Pada kultivar padi yang sensitif
Al, ion Al dapat menimbulkan terbentuknya formasi calllose yang
mengindikasikan terjadinya pelukaan akibat Al di akar (Alvim dkk., 2012).
Studi Lin dan Chen (2011) menemukan bahwa pada kultivar yang toleran
Al seperti Cayenne ditandai pemanjangan akar yang lebih baik dan dapat menekan
adsorpsi Al ke dalam dinding. Kultivar Cayenne dapat tumbuh baik dalam
lingkungan sangat masam yang mengandung konsentrasi AlCl3 hingga 300 µM.
Karakteristik ketahanan tanaman terhadap Al terlihat dari sifat metabolisme
karbohidrat, produksi asam organik, kemampuan menekan kerusakan akar dan
perubahan fenotip akar (Chen dan Lin, 2010).
Ketika terjadi proses pertumbuhan awal tanaman yang dimulai dengan
munculnya akar maka saat yang bersamaan tanaman akan menghasilkan
menghasilkan senyawa kimia berbentuk gula, asam amino, dan senyawa metabolit
sekunder seperti flavamoid, asam-asam organik, enzim, lektin, dan glikoprotein
yang dieksudasi ke tanah dan dapat dimanfaatkan oleh mikroorganisme tanah
9 dalam, melindungi permukaan akar dari kondisi kering yang ekstrim,
meningkatkan daya adaptasi terhadap tanah masam dan menjadi senyawa sinyal
pada interaksi tanaman-mikroorganisme tanah khususnya untuk mekanisme
pertahanan tanaman (Timotiwu, 2010).
Kejenuhan alumunium di atas 60% merupakan indikasi potensial problem
terhadap toksisitas. Kandungan Al di jaringan dewasa tanaman mencapai di atas
200 ppm (mg/kg). Gejala keracunan Al ditandai pembentukan akar yang
malformasi seperti akar yang mengurus, membelit dengan ujung akar yang
membengkak, warna akar menjadi coklat dan minim perakaran serabut .
Penampakan bagian atas terlihat daun yang menguning dan pertumbuhan yang
terhambat. Gejala ini akan lebih terlihat ketika terjadi cekaman suhu dan
kelembaban di permukaan tanah (Koenig dkk., 2011).
Strategi untuk menjaga produktivitas tanaman di lahan-lahan asam di
antaranya adalah aplikasi kapur untuk meningkatkan pH tanah dan penggunaan
tanaman toleran lahan asam (Ojima, 1989). Walaupun toksisitas Al dapat
dikendalikan dengan aplikasi kapur di permukaan tanah, namun cara ini sering
tidak efisien secara ekonomi sehingga kombinasi pengapuran dan penggunaan
kultivar toleran Al menjadi strategi yang efektif untuk meningkatkan
produktivitas tanaman di lahan asam (Hede dkk., 2001).
Fageria (2008) mengatakan bahwa ketika pH naik maka serapan Ca dan
Mg akan meningkat terutama pada tanah yang kaya akan Fe dan Al oksida.
Kejenuhan Ca di tanah merupakan indikator penting untuk penentuan kebutuhan
kapur di tanah. Di tanah tropis kandungan Ca dd harus lebih dari 2 cmol/kg.
10 berperan dalam perkembangan akar, penggunaan air dan serapan hara. Ideal rasio
kejenuhan kompleks kation dapat ditukar adalah 65% Ca, 10% Mg, 5% K dan
20% H. Tanaman toleran Al dihubungkan dengan lebih besarnya serapan Mg
pada kultivar kentang dan jagung.
Pemberian kapur pada tanah asam bertujuan untuk menurunkan atau
meniadakan pengaruh Al terhadap pertumbuhan tanaman, meniadakan selaput Al
pada akar tanaman, sehingga tanaman dapat mengambil hara dengan optimum.
Pengapuran juga dapat meningkatkan ketersediaan hara P dan K dalam tanah dan
meningkatkan aktivitas biologi tanah. Batas toleransi tanaman jagung dan kedelai
terhadap kejenuhan Al adalah 30 dan 15%, sehingga kapur untuk jagung dan
kedelai sebaiknya diberikan apabila kejenuhan Al lebih dari 30 dan 15%. Dengan
demikian, pada tanah yang sama kebutuhan kapur untuk tanaman kedelai lebih
tinggi dibandingkan jagung. Bahan kapur yang dapat digunakan untuk pertanian
adalah kapur pertanian (CaCO3), kapur tohor (Ca(OH)2), dan dolomit
(Ca Mg(CO3)2) (Anonim, 2005).
Uchida dkk. (2000) mengatakan bahwa tanah asam umumnya terjadi di
daerah tropika basah, di mana curah hujan mencuci profil tanah dan meninggalkan
material yang stabil yang kaya Fe dan Al dan menghasilkan tanah asam dan
miskin hara untuk tanaman. Kehilangan tanah karena pencucian menyebabkan
hara kation mudah terbawa ke bawah lapisan daerah perakaran. Sementara hara
anion seperti P dan Mo akan terikat kuat oleh Al dan Fe dan menjadi tidak
tersedia bagi tanaman.
Salah satu alternatif yang dapat dilakukan untuk mengatasi persoalan
11 penambahan bahan organik (Hairiah dkk., 2000 dalam Isrun, 2010). Aplikasi
bahan organik pada tanah asam akan mengurangi toksisitas Al, menurunkan
kebutuhan kapur dan meningkatkan ketersediaan P. Selama dekomposisi bahan
organik akan meningkatkan pH dan menurunkan Al dapat ditukar dalam larutan
tanah (Haynes dan Mokolobate, 2001).
Sumarsono dkk. (2011) menyebutkan bahwa bahan organik mampu
menetralisir pengaruh racun dari Al sehingga menjadi tidak beracun lagi bagi akar
tanaman. Kualitas bahan organik berkaitan dengan kemampuan dalam
mendetoksifikasi ditentukan dengan tolok ukur total konsentrasi kation K, Ca, Mg
dan Na. Pelepasan kation-kation tersebut dari hasil dekomposisi bahan organik
dapat menekan kelarutan Al melalui peningkatan pH tanah. Bahan organik yang
mempunyai total konsentrasi kation > 60 cmol/kg merupakan bahan organik yang
berpotensi untuk tujuan pengurangan efek beracun Al. Semakin tinggi nilai total
konsentrasi kation suatu bahan organik semakin kuat kemampuannya dalam
mengurangi efek beracun Al.
Kompos secara nyata akan meningkatkan kimia tanah dengan
meningkatkan pH tanah, N total tanah dan serapan N serta menurunkan Al dd
(Isrun, 2010). Namun besar pengaruh kapur dan pemberian kompos sisa tanaman
terhadap ion Al dapat ditukar (Al dd) di dalam tanah dan terhadap produksi
tanaman kedelai masih belum banyak diketahui (Wahyudin, 2006).
1.4 Hipotesis
12 1. Terdapat klon nanas yang toleran terhadap toksisitas Al.
2. Terdapat batas kritis kejenuhan Al di tanah Ultisol PT GGP terhadap 3
klon nanas.
3. Terdapat dosis bahan organik dan kapur optimal yang mampu
II. TINJAUAN PUSTAKA
2.1 Tanah Ultisol
Ultisol merupakan salah satu jenis tanah di Indonesia yang mempunyai
sebaran luas, mencapai 45.794.000 ha atau sekitar 25% dari total luas daratan
Indonesia. Sebaran terluas terdapat di Kalimantan (21.938.000 ha), diikuti di
Sumatera (9.469.000 ha), Maluku dan Papua (8.859.000 ha), Sulawesi (4.303.000
ha), Jawa (1.172.000 ha), dan Nusa Tenggara (53.000 ha) (Subagyo dkk., 2004).
Prasetyo dan Suriadikarta (2006) mengatakan bahwa Ultisol dapat
dijumpai pada berbagai relief, mulai dari datar hingga bergunung. Penampang
tanah yang dalam dan kapasitas tukar kation yang tergolong sedang hingga tinggi
menjadikan tanah ini mempunyai peranan yang penting dalam pengembangan
pertanian lahan kering di Indonesia. Hampir semua jenis tanaman dapat tumbuh
dan dikembangkan pada tanah ini, kecuali terkendala oleh iklim dan relief.
Kesuburan alami Ultisol umumnya terdapat pada Horizon A yang tipis dengan
kandungan bahan organik yang rendah. Unsur hara makro seperti P dan K yang
sering kahat, reaksi tanah asam hingga sangat asam, serta kejenuhan Al yang
tinggi merupakan sifat-sifat tanah Ultisol yang sering menghambat pertumbuhan
tanaman. Selain itu terdapat Horizon Argilik yang mempengaruhi sifat fisika
tanah, seperti: berkurangnya pori mikro dan makro serta bertambahnya aliran
14 Pengapuran, sistem pertanaman lorong, serta pemupukan dengan pupuk
organik maupun anorganik dapat mengatasi kendala pemanfaatan Ultisol.
Pemanfaatan Ultisol untuk pengembangan tanaman perkebunan relatif tidak
menghadapi kendala, tetapi untuk tanaman pangan umumnya terkendala oleh
sifat-sifat kimia tersebut yang dirasakan berat bagi petani untuk mengatasinya,
karena kondisi ekonomi dan pengetahuan yang umumnya lemah (Prasetyo dan
Suriadikarta, 2006).
Usaha pertanian di Ultisol akan menghadapi sejumlah permasalahan
karena Ultisol umumnya mempunyai pH rendah yang menyebabkan kandungan
Al, Fe, dan Mn terlarut tinggi sehingga dapat meracuni tanaman. Jenis tanah ini
biasanya miskin unsur hara makro esensial seperti N, P, K, Ca, dan Mg dan unsur
hara mikro Zn, Mo, Cu, dan B, serta bahan organik. Umumnya tanah Ultisol atau
Podsolik Merah Kuning (PMK) banyak mengandung Al dapat dipertukarkan
kisaran 20-70% (Subandi, 2007).
2.2 Toksisitas Aluminium pada Nanas
Nanas umumnya ditanam pada tanah yang memiliki keasaman kuat,
dengan konsentrasi Al tinggi yang sering meracuni perakaran tanaman. Ujung
akar adalah daerah yang paling sensitif terhadap toksisitas Al. Pengaruh Al
terhadap pertumbuhan akar di 4 klon nanas : Cayenne, Tainung No.6, Tainung
No.13 and Tainung No.17 telah dievaluasi di Taiwan. Perbedaan dalam jumlah
kalus dan malondialdehyde (MDA) di ujung akar (1 cm dari ujung) antara klon
15
Setelah perlakuan 300 μM AlCl3 dalam larutan hidroponik (pH 4,5) selama 72
jam, pemanjangan akar klon Cayenne, Tainung No.6, Tainung No.13 dan Tainung
No. 17 adalah 115, 85, 93 and 73% dibanding kontrol (tanpa perlakuan Al).
Perlakuan AlCl3 tidak meningkatkan kandungan kalus dan MDA pada klon
Cayenne, namun meningkat nyata di klon Tainung No.17. Setelah terpapar Al,
serapan Al di dinding sel ujung akar akan meningkat nyata sejalan waktu dan
konsentrasi AlCl3 untuk klon Cayenne dan Tainung No.17 relatif lebih besar
daripada Tainung No.17. Ini menggambarkan bahwa klon Cayenne adalah klon
yang resistan Al dan Tainung No.17 adalah klon sensitif Al. Ketika ujung akar
diberi perlakuan awal 1 dan 10 mM asam malat, serapan Al di dinding sel ujung
akar klon Cayenne lebih rendah 18 dan 31% dibanding tanpa pemberian
perlakuan asam malat. Ini mengindikasikan bahwa ujung akar klon Cayenne
mampu menyekresikan asam malat yang mampu mengelat Al dan menurunkan
Al terikat pada dinding sel sehingga menjadi lebih toleran terhadap toksisitas Al
(Lin dan Chen, 2011).
Aluminum adalah unsur biotoksik yang sering mempengaruhi penyerapan
hara tanaman pada tanah asam. Lin (2010) telah mengevaluasi pengaruh Al
terhadap pertumbuhan akar, penyerapan hara makro P, K, Ca, Mg dan hara mikro
Fe, Mn, Cu, Zn pada 2 klon nanas, yang resisten Al (Cayenne) dan yang sensitif
Al (Tainung No.17). Empat taraf perlakuan konsentrasi digunakan dalam larutan
hidroponik 0, 100, 200 dan 300 M AlCl3. Setelah umur 4 minggu, pemanjangan
akar klon Cayenne tetap meningkat dengan berbagai konsentrasi Al, sedangkan
klon Tainung No.17 menurun. Berat kering Cayenne meningkat dan Tainung
16 berpengaruh pada klon Al resisten, Cayenne. Sedangkan serapan Ca, Mg dan K
terhambat dengan perlakuan AlCl3 200 M, dan serapan Fe, Mn dan Cu terhambat
secara nyata dengan perlakuan AlCl3 300 M pada klon Al sensitif Tainung No.17.
Dengan kata lain serapan hara Ca, Mg an K meningkat nyata di Cayenne pada
perlakuan AlCl3 200 M. Hal ini mengindikasikan bahwa serapan Ca, Mg dan K
adalah petunjuk penting untuk membedakan klon nanas resisten Al dan sensitif
Al.
2.3 Pengaruh Pengapuran dan Bahan Organik terhadap Toksisitas Aluminium
Pertumbuhan yang tidak baik di tanah asam juga berhubungan dengan
kekahatan Ca dan Mg. Tembakau yang ditanam pada pH 4,2 dan 0,4 meq Ca/100
gr mengalami pertumbuhan akar yang terhambat baik oleh keracunan Al maupun
oleh kekahatan Ca. Jika Al diendapkan melalui pengapuran dengan MgCO3
sampai pH 5,6 dengan mempertahankan Ca pada tingkat yang rendah maka
pertumbuhan akar akan terhenti dalam 60 jam. Apabila Al diendapkan dan
bersamaan dengan itu tingkat Ca dinaikkan menjadi 4,4 meq/100 gr dengan
pengapuran CaCO3 maka pertumbuhan akar akan berlangsung normal. Di
samping itu pada pH < 5,5 unsur mangan akan sangat mudah larut dan
menyebabkan keracunan pada tanaman. Pada pH < 5,5 keracunan Mn dapat
terjadi bersamaan dengan keracunan Al.
Mekanisme pertahanan tanaman terhadap efek toksik Al secara eksternal atau
17 melalui pengkhelatan Al didalam sel dan disimpan dan dikomparmentalisasi
dalam vakuola (Kochian, 1995; Ramgareeb dkk.dalamBlancheteau dkk., 2008).
Al dalam larutan tanah akan menurun apabila kadar bahan organik
meningkat karena bahan organik membentuk kompleks yang sangat kuat dengan
Al. Al di dalam larutan tanah akan meningkat dengan meningkatnya kandungan
garam karena kation-kation lainnya kemudian menggusur Al dapat ditukar dengan
aliran massa (Sanchez, 1992).
Tinggi genangan dan bahan organik nyata meningkatkan P tersedia dan
menurunkan kelarutan Fe dan Al pada tanaman padi. Tanah marginal yang
diberikan bahan organik 20 ton/ha dan penggenangan 10 cm dapat meningkatkan
kesuburan tanah (Cyio, 2008). Penelitian Isrun (2010) juga melaporkan bahwa
aplikasi kompos legume dapat meningkatkan pH tanah, N total tanah, serapan N
dan menurunkan Al dd.
Keasaman tanah merupakan indikator potensial pertumbuhan tanaman dan
indikator kebutuhan kapur bagi tanah (Donahue, 1999). Upjon dkk. (2005)
melaporkan bahwa keasaman tanah akan meningkatkan Al tersedia di tanah (Al3+)
yang menyebabkan pemendekan perkembangan akar di tanaman sehingga
berakibat pada penurunan kemampuan akar dalam mengakses kelembaban tanah
dan menurunkan serapan hara, meningkatkan Mn tersedia di tanah (Mn2+) yang
menyebabkan penurunan pertumbuhan tanaman, menurunkan kelarutan dan
ketersediaan Mo, P, Mg dan Ca di tanah.
Pengapuran berguna untuk menurunkan toksisitas Mn2+ dan Al3+,
meningkatkan aktivitas mikroba tanah, memperbaiki struktur tanah, meningkatkan
18 meningkatkan ketersediaan hara bagi tanaman. (Donahue, 1999). Kapur juga
berguna sebagai bahan pemantap tanah yang baik karena dapat meningkatkan
berbagai sifat tanah seperti KTK tanah, menurunkan indeks plastisitas tanah dan
menurunkan kompaksi tanah (Negi dkk., 2013).
Uchida dkk. (2000) menjelaskan bahwa pemberian kapur akan
mengeliminasi ion Al3+ yang toksik menjadi tidak toksik dan mengikat ion H+
dengan OH- yang dihasilkan dari hasil hidrolisis kapur sehingga pH akan naik
seperti digambarkan pada reaksi berikut ini :
CaCO3 + H2O (dalam tanah) Ca2+ + 2OH- + CO2
Lalu ion Ca2+ akan dipertukarkan dengan Al3+ dan H+ yang ada di tanah asam
Kapur yang menghasilkan ion OH- akan bereaksi dengan Al3+ menjadi bentuk
padat Al (OH)3 yang tidak toksik ke tanaman dan juga bereaksi dengan ion H+
membentuk H2O sehingga pH tanah manjadi naik.
3OH- + Al3+ Al(OH)3 (padat)
OH- + H+ H2O
Mekanisme pengendalian toksisitas Al di tanah dengan pemberian bahan
organik terjadi melalui peningkatan pH tanah, karena asam-asam organik hasil
dekomposisi bahan organik akan mengikat Al dan membentuk senyawa komplek
(khelat), sehingga Al tidak terhidrolisis lagi. Di samping itu muatan negatif pada
humus yang berasal dari gugus karboksil (R-COOH) dan fenolik ( ) nya
19 Penambahan bahan organik pada tanah masam, seperti inseptisol, ultisol dan
andisol akan mampu meningkatkan pH tanah dan mampu menurunkan Al tertukar
tanah (Atmojo, 2003).
Kejenuhan Al didefinisikan sebagai rasio antara Al dapat dipertukarkan
dibagi dengan penjumlahan kation basa-basa ditambah Al (Budianta dan
Vanderdeelen, 1995). Batas toleransi tanaman jagung dan kedelai terhadap
kejenuhan Al adalah 30 dan 15%, sehingga kapur untuk jagung dan kedelai
sebaiknya diberikan apabila kejenuhan Al lebih dari 30% dan 15%. Oleh sebab
itu pada tanah yang sama kebutuhan kapur untuk tanaman kedelai lebih tinggi
dibandingkan jagung. Selain itu pengapuran juga diberikan karena pH tanah
rendah (pH < 5,5) (Anomim, 2005). Ispandi dan Munip (2005) melaporkan
bahwa aplikasi kapur 300 kg/ha meningkatkan serapan hara P, K, dan Ca pada
tanaman ubikayu berturut-turut 68%; 10% and 113% dan meningkatkan produksi
ubikayu sebesar17%.
Di samping aplikasi pengapuran, penggunaan genotipe yang memiliki
toleransi tinggi terhadap cekaman Al untuk lahan asam dengan kejenuhan Al
30-35% dan pH 4,5–5,0, serta didukung oleh umur masak kedelai genjah (75 hari)
telah dilakukan untuk pengembangan kedelai di luar Pulau Jawa. Tanaman yang
memiliki sifat toleran dicirikan memiliki akar yang tetap dapat berkembang lebih
baik pada tanah asam dibandingkan varietas rentan (Sudrajat, 2010).
Tingkat toleransi 3 klon nanas di PT Great Giant Pineapple dan hubungannya
dengan pemberian bahan amelioran kapur serta bahan organik akan menjadi
20 tanaman nanas di tanah Ultisol pada umumnya dan khususnya di lahan PT Great
Giant Pineapple.
Penelitian Cahyono (2012) menyebutkan bahwa tingkat kejenuhan Al di tanah
GGP menentukan jumlah dosis kebutuhan kapur dalam tanah. Dosis yang
direkomendasikan saat ini di PT GGP berada dalam kisaran 1-4 ton per ha.
Bahan organik merupakan komponen penting di tanah yang menentukan
status kesuburan tanah secara biologi, kimia dan fisika. Bahan organik adalah
sumber energi untuk aktivitas biologi tanah. Di tanah marginal status bahan
organik tanah akan menentukan upaya peningkatan produksi dan tingkat
kebutuhan pupuk untuk tanaman (Craswell dan Lefroy, 2001).
Peningkatan nilai pH disebabkan adanya kontribusi bahan organik yang
melepaskan ion OH- karena terjadi proses reduksi. Dalam kondisi demikian, pH
pada tanah asam dapat meningkat hingga 6,5 bila tergenang beberapa minggu
yang disertai dengan pemberian bahan organik. Adanya pelepasan ion OH- yang
dapat meningkatkan pH tanah karena terjadi keseimbangan antara ion H+ dengan
ion OH- baik dari perubahan feri menjadi fero maupun dari nitrat menjadi nitrit,
yang keduanya memberi kontribusi gugus hidroksil ke dalam larutan tanah (Cyio,
2008).
Arfian (2003) melaporkan bahwa aplikasi bahan organik dosis tinggi 200
ton/ha dalam kondisi segar (dari berbagai jenis bahan organik seperti : onggok
segar, extracted cake, kulit singkong segar, pupuk kandang segar ex PT GGL dan
limbah organik cair ex PT UJF) pada saat pengolahan tanah fase finishing harrow
mampu meningkatkan distribusi bibit besar terpetik di pembibitan nursery nanas
21 serta berat batang dan berat tanaman), produksi buah nanas (berat per 100 buah
dan distribusi buah besar ≥2 T) serta meningkatkan C organik dan pH tanah.
Namun kandungan C organik dalam 4 bulan akan kembali turun mendekati nilai
awal karena laju dekomposisi bahan organik yang tinggi. Hal ini juga senada
dengan studi Ziaurrahman (2015) yang menyebutkan bahwa pemberian dosis
kompos mulai 50 hingga 200 ton/ha di nanas klon GP3 dengan cara ditebar di
permukaan tanah nyata meningkatkan berat tanaman umur 6 bulan setelah tanam
(BST) dan saat forcing (9 BST), rata-rata berat buah, distribusi buah besar ≥2 T,
pH tanah, C organik dan kandungan hara P, K, Ca dan Mg tanah. Serangan
penyakit layu mealybug, erwinia dan phythopthora juga dilaporkan tidak berbeda
nyata dengan perlakuan tanpa kompos.
Penggunaan kompos matang 20 ton/ha di tanaman nanas juga dilaporkan
Ziaurrahman (2015) dapat meningkatkan indeks daun-D, berat daun-D,dan berat
tanaman hingga umur 6 bulan serta berpotensi menurunkan penggunaan pupuk
kimia hingga 30%. Studi Pangarso (2014) juga membuktikan penggunaan
vermicompost dari 0, 20, 40, 60, 80 dan 100 ton/ha mampu meningkatkan daya
pegang air di tanah (water holding capacity) hingga 2 kali lipat dibandingkan
kontrol sehingga berpotensi memperpanjang masa interval irigasi pada musim